Optimasi Proses Overproduksi, Pemurnian dan Karakterisasi Protein Mga Sebagai Molekul Target Untuk Pencegahan Infeksi oleh Streptococcus Pyogenes
|
|
|
- Benny Budiaman
- 7 tahun lalu
- Tontonan:
Transkripsi
1 Jurnal Matematika dan Sains Vol. 8 No. 3, September 23, hal Optimasi Proses Overproduksi, Pemurnian dan Karakterisasi Protein Mga Sebagai Molekul Target Untuk Pencegahan Infeksi oleh Streptococcus Pyogenes Muhaimin 1), Oei Ban Liang 2,4), Enny Ratnaningsih 2,4), Endang Purwantini 3,4) dan Debbie Sofie Retnoningrum 3,4) 1) Jurusan Kimia-FKIP Universitas Jambi 2) Departemen Kimia-FMIPA Institut Teknologi Bandung 3) Departemen Farmasi-FMIPA Institut Teknologi Bandung 4) Pusat Penelitian Antar Universitas Bioteknologi ITB Diterima April 23, disetujui untuk dipublikasikan Juli 23 Abstrak Telah dilakukan penelitian tentang optimasi overproduksi, purifikasi dan karakterisasi protein Mga Streptococcus pyogenes dari Escherichia coli pmalmga rekombinan yang mengandung gen mga49. Optimasi overproduksi dilakukan dengan membuat biakan Escherichia coli pmalmga dengan OD 6 =,7 dalam medium LB dengan atau tanpa glukosa, dan diinduksi dengan IPTG,3 mm dalam variasi waktu tertentu. Protein yang dihasilkan berupa protein fusi MBP-Mga dengan massa molekul relatif sekitar 14 kda. Purifikasi dilakukan menggunakan teknik kromatografi afinitas dengan kolom resin amilosa pada kondisi ph 7,4 dilanjutkan dengan SDS PAGE. Terdeteksinya pita tunggal pada 14 kda menunjukkan protein fusi MBP-Mga yang cukup murni. Protein fusi MBP-Mga murni digunakan untuk produksi antibodi poliklonal pada kelinci. Pembentukan antibodi dalam serum kelinci dimonitor dengan teknik dot blot dan Western blot. Antibodi poliklonal yang dihasilkan memberikan reaksi positif terhadap protein fusi MBP-Mga rekombinan. Adsorpsi dan presipitasi terhadap antibodi poliklonal yang bereaksi positif dengan protein MBP dilakukan dengan menambahkan protein MBP murni (56 kda) yang diproduksi oleh Escherichia coli pmalc2 rekombinan dengan konsentrasi tertentu, dan dimurnikan dengan kromatografi afinitas menggunakan ligan amilosa pada kondisi ph 7,4. Antibodi poliklonal yang telah diadsorpsi tersebut, memberikan reaksi positif terhadap protein Mga rekombinan dan reaksi negatif terhadap protein MBP rekombinan. Kata kunci : Streptococcus pyogenes, gen mga49, protein fusi MBP-Mga, protein MBP, antibodi poliklonal Abstract Optimization of overproduction, purification and characterization of Streptococcus pyogenes s Mga recombinant protein from Escherichia coli pmalmga carrying mga49 gene had been carried out. The overproduction optimization was conducted by culturing the Escherichia coli pmalmga of OD 6 =,7 in LB medium with or without glucose, and induced by,3 mm IPTG for a certain period of time. The protein produced was MBP-Mga fusion protein with a molecular weight of about 14 kda. The purification was conducted by affinity chromatography using amylose ligands at ph 7,4 and continued by SDS-PAGE. One band identified at 14 kda showed that the MBP-Mga fusion protein was pure enough for further analysis. The MBP-Mga protein was then injected into rabbit to produce polyclonal antibodies. The antibody development was monitored by dot blot and Western blot. The antibodies produced gave a positive reaction to MBP-Mga fusion protein. Adsorption and precipitation of the polyclonal antibodies which gave a positive reaction to MBP protein was done by adding pure MBP protein (56 kda) produced by Escherichia coli pmalc2, and purified by affinity chromatography using amylose ligands at ph 7,4. The results showed that the antibodies gave a positive reaction to Mga recombinant protein and a negative reaction to MBP recombinant protein. Keywords : Streptococcus pyogenes, mga49 gene, MBP-Mga fusion protein, MBP protein, polyclonal antibodies 1. Pendahuluan Streptococcus pyogenes merupakan salah satu bakteri gram positif yang menyebabkan berbagai penyakit pada manusia, mulai dari infeksi lokal seperti faringitis, impetigo dan pioderma sampai pada infeksi invasif yang membahayakan kehidupan manusia, seperti sepsis, necritizing fascitis, dan toxic shock-like syndrome 1,2). Infeksi ini dapat berkembang menjadi kondisi yang lebih parah, seperti demam 117 rematik dengan karditis dan glomerulonephritis pascastreptococcus akut 2). Di Indonesia dan negaranegara berkembang, faringitis dan pioderma adalah jenis penyakit yang paling banyak dijumpai pada anak-anak usia sekolah. Puncak insiden penyakit ini terdapat pada kelompok usia 5 sampai 15 tahun. Karditis dan glomerulonephritis dilaporkan terjadi pada lebih kurang 5% populasi, terutama jika pengobatan dengan antibiotik tidak dilakukan.
2 118 JMS Vol. 8 No. 3, September 23 Sampai saat ini, kasus infeksi oleh bakteri S. pyogenes masih menjadi masalah kesehatan penting di negara-negara berkembang, termasuk Indonesia 3). Pengobatan terhadap infeksi S. pyogenes yang dilakukan selama ini adalah menggunakan antibiotik ampisilin dan rifampisin 4). Saat ini penggunaan antibiotik menghadapi permasalahan baru dengan ditemukannya galur bakteri yang resisten terhadap antibiotik tersebut. Maka, untuk mengatasi hal ini dilakukan usaha mencari senyawa baru dengan mekanisme kerja yang baru dalam mengatasi infeksi S. pyogenes. Untuk itu, ditelitilah cara kerja dari beberapa faktor virulensi yang terdapat pada S. pyogenes, sehingga diharapkan dapat membantu mencari senyawa baru untuk mengatasi infeksi S. pyogenes. Streptococcus pyogenes memiliki beberapa protein permukaan yaitu protein M, streptococcal C5a peptidase, dan reseptor imunoglobulin 5-7). Protein M dan streptococcal C5a peptidase merupakan faktor virulensi utama dalam S. pyogenes dan sintesisnya dikendalikan oleh suatu protein aktivator Mga 6,8-11). Berdasarkan hipotesa, untuk menghambat sintesis protein M, maka aktivitas protein Mga harus dicegah oleh senyawa bioaktif tertentu sehingga tidak dapat berinteraksi dengan situs aktivator gen emm dan scpa yang letaknya dekat promotor emm dan promotor scpa dari S. pyogenes. Dengan demikian, gen yang terlibat pada faktor virulensi pada S. pyogenes tidak akan terekspresi. Informasi mengenai interaksi antara protein Mga dengan situs aktivator gen emm dan scpa pada tingkat molekul dapat digunakan sebagai dasar untuk mencari suatu senyawa bioaktif yang menghambat ekspresi gen faktor virulensi 1,6). Penemuan senyawa baru yang mampu membunuh bakteri S. pyogenes di dalam tubuh manusia, tetapi tidak membunuh flora normal akan sangat bermanfaat dalam bidang farmasi dan kedokteran. Senyawa tersebut diharapkan pula dapat mengatasi masalah timbulnya resistensi S. pyogenes terhadap berbagai antibiotik. Maka, untuk mengetahui informasi protein Mga pada tingkat molekul diperlukan protein Mga rekombinan murni dalam jumlah yang cukup besar, karena protein Mga rekombinan murni akan digunakan untuk skrining senyawa bioaktif asal Indonesia dan untuk menguji situs aktivator gen emm. Selain itu protein Mga rekombinan murni digunakan untuk produksi antibodi poliklonal pada kelinci, antibodi ini digunakan untuk mendeteksi protein Mga rekombinan dengan cara imunokimia, sehingga berfungsi sebagai kontrol positif untuk protein Mga rekombinan yang diproduksi melalui eksperimen berbeda. Pada penelitian ini, untuk memproduksi protein Mga digunakan teknik DNA rekombinan yang dikombinasi dengan kromatografi afinitas 2,7,11). Fusi protein pengikat maltosa (MBP) dengan Mga dibuat dengan membuat rekombinasi DNA antara gen mga49 dengan male. Hasilnya disisipkan ke vektor pmalc2 dan menghasilkan plasmid pmalmga yang ditransformasi ke Escherichia coli sebagai sel inang 2,6). MBP akan berikatan dengan matriks kolom resin maltosa pada kromatografi afinitas sehingga pemurnian dapat dilakukan dengan mudah. Berdasarkan latar belakang tersebut, maka dalam tulisan ini dilaporkan tentang perlunya dilakukan suatu penelitian untuk menentukan teknik terbaik pada overproduksi protein Mga rekombinan, metode purifikasi yang dapat menghasilkan protein Mga rekombinan dengan kemurnian tinggi, dan teknik terbaik produksi antibodi poliklonal untuk karakterisasi protein Mga rekombinan. Overproduksi protein Mga S. pyogenes dari E. coli pmalmga rekombinan, meliputi tahap deteksi keberadaan gen mga49 pada pmalmga, pembuatan kurva pertumbuhan, optimasi overproduksi, pemurnian protein Mga dengan kromatografi afinitas, dan produksi antibodi poliklonal terhadap protein Mga dalam serum kelinci. Antibodi poliklonal yang dihasilkan dianalisa menggunakan teknik dot blot dan Western blot. 2. Bahan dan Metode Bahan-bahan yang digunakan adalah Escherichia coli pmalmga yang membawa gen mga49, Escherichia coli pmalc2, antibodi terhadap MBP, media cair dan padat Luria Bertani, kelinci jenis Albino dari New Zealand, antibodi primer, antibodi sekunder, dan zat-zat kimia yang digunakan untuk overproduksi, elektroforesis, purifikasi, produksi antibodi, dot blot dan Western blot. Zat-zat kimia yang digunakan dalam penelitian ini memiliki kapasitas p.a (pro analysis) Overekspresi gen mga49 dalam E. coli (pmalmga) Bakteri E. coli yang mengandung plasmid pmalmga ditanam dalam medium LB cair (tripton 1% b/v, ekstrak rag,5% b/v, NaCl 1% b/v dalam akuades) yang mengandung glukosa,2% b/v atau yang tidak mengandung glukosa. Protein Mga rekombinan akan dihasilkan sebagai protein fusi dengan pengikat maltosa. Untuk overproduksi protein fusi MBP-Mga rekombinan, maka dilakukan induksi dengan penambahan,3 mm IPTG (Isopropil-β-Dtiogalaktosida). Lalu untuk menentukan waktu optimal ekspresi, maka dilakukan sampling pada 1 jam, 2 jam, 3 jam, 4 jam, 5 jam dan 6 jam setelah induksi. Sel dipanen dengan cara sentrifugasi, kemudian ditambah buffer sodium-trisetilendiamintetraasetat (NaCl 5 M, EDTA,5 M, Tris-HCl 1 M), diresuspensi dan disentrifugasi kembali sebanyak dua kali. Pelet sel dilisis dengan sonikator, dan protein dipisahkan dari debris sel dengan cara sentrifugasi pada kecepatan tinggi. Protein yang diambil adalah protein yang berada dalam supernatan.
3 JMS Vol. 8 No. 3, September Pemurnian Protein Fusi MBP-Mga. Pemurnian protein fusi MBP-Mga dilakukan dengan kromatografi afinitas menggunakan kolom resin amilosa. Protein Mga yang dihasilkan sebagai protein fusi dengan pengikat maltosa dimasukkan ke dalam kolom amilosa dan diinkubasi selama 1-2 jam. Hal ini bertujuan agar protein fusi dapat menempel pada ligan. Kolom kemudian dicuci dengan buffer (Tris.Cl 2 mm ph 7,4, NaCl,2 M, 2- merkaptoetanol 1 mm, dan EDTA 1 mm) sebanyak 1 X volume kolom, untuk menghilangkan kontaminan. Selanjutnya protein dilepaskan dari ligan dengan mengalirkan buffer elusi (Tris.Cl 2 mm ph 7,4, NaCl,2 M, 2-merkaptoetanol 1 mm, EDTA 1 mm, dan maltosa 1 mm) ke dalam kolom. Setiap 1,5 ml hasil elusi ditampung sebagai fraksifraksi yang diamati dengan spektrofotometer UV-Vis pada panjang gelombang 28 nm. yang menunjukkan absorbansi pada 28 nm adalah fraksi yang mengandung protein fusi yang kita inginkan. Analisa kemudian dilakukan dengan SDS-PAGE pada konsentrasi poliakrilamid 12%. Pita tunggal sekitar 14 kda menunjukkan bahwa protein fusi MBP-Mga yang diperoleh adalah relatif murni Produksi Antibodi untuk Karakterisasi Protein Fusi MBP-Mga Kelinci yang belum diberi perlakuan diambil darah vena marginalisnya sebanyak 3 ml, darah ini digunakan sebagai kontrol negatif. Protein fusi MBP-Mga rekombinan murni dengan konsentrasi 5-2 µg /,75 ml dibuat larutan dengan,75 ml Freund s complete adjuvant. Larutan ini disuntikkan di bawah kulit kelinci dengan volume maksimal,15 ml. Penyuntikan dilakukan di 1 tempat intradermal. Setelah 1 hari dari penyuntikan pertama, serum kelinci diambil untuk dianalisa antibodinya. Pemisahan serum dari sel darah merah dilakukan dengan cara sentrifugasi. Kemudian dilakukan penyuntikan kedua dengan volume maksimal,15 ml. Larutan yang disuntikkan terdiri dari,75 ml incomplete adjuvant dengan 5-2 µg /,75 ml protein fusi MBP-Mga rekombinan. Penyuntikan dilakukan pada 1 tempat intradermal. Sepuluh hari kemudian, serum kelinci diambil lagi untuk dianalisa antibodinya. Penyuntikan antigen pada kelinci dilakukan sampai tidak menginduksi antibodi. Antibodi terhadap protein fusi MBP-Mga diamati dengan dot blot dan Western blot. Pewarnaan dilakukan dengan penambahan nitroblue tetrazolium dan 5-bromo-4-kloro-3-indolil fosfat dalam buffer alkalin fosfatase Absorpsi Terhadap Antibodi MBP Antibodi terhadap protein fusi MBP-Mga yang telah dibuat di kelinci diambil sebanyak 1 ml dengan kadar µg/ml. Protein MBP murni disiapkan dengan kadar 282; 423; 564; 75; 846 µg/ml antibodi. Kemudian 1 ml antibodi dicampurkan terhadap MBP-Mga dengan protein MBP murni tersebut, diinkubasi selama 3 menit pada temperatur 4 o C, setelah itu disentrifugasi dengan kecepatan 12 rpm. Protein MBP murni dan antibodi yang terikat padanya akan membentuk endapan pada tabung. Akhirnya pada supernatan hanya tertinggal antibodi yang hanya mengenali protein Mga, untuk penambahan protein MBP murni dengan kadar tertentu. Jadi untuk menyerap antibodi terhadap protein MBP diperlukan protein MBP murni. 3. Hasil dan Diskusi 3.1. Optimasi overproduksi protein fusi MBP-Mga Sebelum overproduksi, konfirmasi keberadaan gen mga49 dalam plasmid pmalmga dilakukan melalui analisis gel elektroforesis. Plasmid pmalmga rekombinan mempunyai ukuran sekitar 7,2 kb. Dalam analisis ini digunakan enzim restriksi EcoRI dan BamHI, baik untuk single digest maupun double digest. Hasil elektroforesis ditunjukkan dalam Gambar 1. Dapat dilihat bahwa ukuran pmalmga yang diperoleh adalah sesuai dengan yang diharapkan, yaitu sekitar 7,2 kb. Hal ini menunjukkan bahwa gen mga49 memang masih ada dalam pmalmga. 21,226 kb 7,421 kb 5,84 kb 4,878 kb 3,53 kb Gambar 1. Elektroforegram hasil isolasi plasmid. (1) Plasmid pmalmga; (2) pmalmga dipotong dengan EcoRI; (3) pmalmga dipotong dengan BamHI; (4) pmalmga dipotong dengan EcoRI/BamHI; (5) Marker λ EcoRI. Setelah isolasi plasmid, dibuat kurva standar albumin manusia melalui pengukuran A 28 dan kadar protein fusi MBP-Mga ditentukan menggunakan standard albumin tersebut. Kurva pertumbuhan E. coli pmalmga menunjukkan bahwa OD 6 =,7 dicapai rata-rata setelah 3,5 jam dalam medium LB yang mengandung,2% glukosa dan 6 jam dalam medium LB tanpa glukosa. Overproduksi diupayakan dengan penambahan IPTG kedalam medium hingga konsentrasi,3 mm pada saat OD 6 =,7. Hasil analisis dengan SDS-PAGE menunjukkan perbedaan yang jelas antara E. coli pmalmga yang diinduksi
4 12 JMS Vol. 8 No. 3, September 23 dengan yang tidak diinduksi (Gambar 2). Pita protein fusi MBP-Mga paling tebal didapat dari sampel protein kasar E. coli pmalmga yang diinduksi selama 2 jam dalam medium LB yang mengandung,2% glukosa dan 4 jam dalam medium LB yang tidak mengandung glukosa. Hal ini ditunjukkan dalam Gambar 2 jalur 3 dan 4. Hasil perhitungan menunjukkan bahwa protein fusi MBP-Mga mempunyai massa molekul sekitar 14 kda, yang terdiri atas 49 kda protein MBP dan 55 kda protein Mga kda 116,3 kda 97,4 kda 66,3 kda 55,4 kda 36,3 kda 2 kda 116,3 kda 97,4 kda 66,3 kda 55,4 kda 14 kda (a) kda 31, kda 14 kda 36,3 kda 31, kda 21,5 kda 14,4 kda Gambar 2. Elektroforegram protein fusi MBP-Mga yang diproduksi dari E. coli pmalmga. (1) Protein marker; (2) Protein kasar E. coli pmalmga non induksi; (3) Protein kasar E. coli pmalmga yang diinduksi 4 jam dalam medium LB; (4) Protein kasar E. coli pmalmga yang diinduksi 2 jam dalam medium LB +,2 % Glukosa; (5) Protein fusi MBP-Mga hasil purifikasi. Untuk membuktikan bahwa protein yang terekspresi adalah protein MBP-Mga, maka dilakukan uji imunokimia dengan menggunakan antibodi yang bereaksi positif terhadap protein pengikat maltosa. Ternyata setelah dilakukan uji imunokimia protein MBP-Mga memberikan reaksi positif, hal ini terjadi karena protein Mga difusikan dengan protein pengikat maltosa. Reaksi positif yang terjadi sebagai respons protein MBP terhadap antibodinya. Gambar 3 berikut menunjukkan hasil uji imunokimia terhadap protein kasar E. coli pmalmga yang non induksi, protein kasar E. coli pmalmga yang diinduksi, dan protein MBP-Mga murni. (b) Gambar 3. (a) Elektroforegram protein fusi MBP- Mga, (b) Hasil western blot antibodi MBP terhadap protein fusi MBP-Mga. (1) Protein kasar E. coli pmalmga non induksi; (2) Protein kasar E. coli pmalmga yang diinduksi; (3) Protein fusi MBP-Mga hasil purifikasi; (4) Protein marker Purifikasi Protein Fusi MBP-Mga dengan Kromatografi Afinitas Protein fusi MBP-Mga hasil overekspresi dimurnikan dengan kolom amilosa pada ph 7,4, menggunakan wash buffer (2 mm Tris.Cl ph 7,4, NaCl,2 M, 2-merkaptoetanol 1 mm, dan EDTA 1 mm) dan elution buffer (2 mm Tris.Cl ph 7,4, NaCl,2 M, 2-merkaptoetanol 1 mm, EDTA 1 mm, dan maltosa 1 mm). Pemurnian dilakukan 4 kali. yang diambil setiap kali pemurnian adalah 1 fraksi, setiap fraksi 1,5 ml dan dimonitor dengan pengamatan A 28. Gambar 4 menunjukkan pengukuran serapan fraksi-fraksi protein MBP-Mga pada pemurnian pertama sampai ke empat. Elektroforegram sampel protein fusi MBP-Mga hasil pemurnian memberikan satu pita dengan massa molekul sekitar 14 kda (Gambar 2 jalur 5). Hal ini menunjukkan bahwa protein fusi MBP-Mga yang diperoleh adalah relatif murni. Perbandingan kadar protein kasar E. coli pmalmga hasil induksi dengan protein MBP-Mga murni hasil purifikasi menggunakan kolom resin amilosa, dapat dilihat pada Tabel 1.
5 JMS Vol. 8 No. 3, September (a) (b) (c) (d) Gambar 4. Pengukuran serapan fraksi-fraksi protein fusi MBP-Mga Tabel 1. Kadar protein kasar E. coli MALMga dan protein MBP-Mga murni hasil purifikasi dengan kolom resin amilosa. Protein Kasar E. coli pmalmga (µg/ml) Protein MBP-Mga murni (µg/ml) Produksi Antibodi Poliklonal Protein kasar E. coli pmalmga non-induksi, protein kasar E.coli pmalmga yang diinduksi dan protein fusi MBP-Mga hasil pemurnian memberikan reaksi positif terhadap antibodi serum kelinci yang telah disuntik dengan protein MBP-Mga murni yang dicampur Freund s complete adjuvant (penyuntikan primer) dan incomplete adjuvant (penyuntikan sekunder). Antibodi poliklonal yang dihasilkan adalah antibodi yang mengenali protein MBP-Mga. Pada penelitian ini yang akan diperlukan adalah antibodi terhadap protein Mga, maka untuk menghilangkan antibodi terhadap protein MBP yang ada dalam serum dilakukan adsorpsi. Adsorpsi terhadap antibodi MBP dilakukan dengan menambahkan protein MBP murni yang diproduksi dari E. coli pmalc2 dan purifikasi menggunakan kolom resin amilosa. Jumlah protein MBP yang ditambahkan adalah,564 µg/µl serum yang mengandung antibodi poliklonal terhadap MBP-Mga. Gambar 5 menunjukkan reaksi antara antibodi dengan antigen sebelum dan sesudah dilakukan adsorpsi terhadap antibodi MBP. Ternyata setelah antibodi diadsorpsi dengan protein MBP, reaksi positif hanya terjadi dengan protein MBP-Mga sedangkan dengan protein MBP reaksi negatif, sebab yang tertinggal hanya antibodi terhadap protein Mga. Hasil analisis dot blot menunjukkan bahwa
6 122 JMS Vol. 8 No. 3, September 23 pengenceran serum 1:1. (v/v) merupakan pengenceran terendah yang memberikan reaksi positif. 1 2 A B 14 kda 56 kda Gambar 5. Hasil analisis antibodi terhadap protein MBP-Mga dan MBP sebelum dan sesudah dilakukan adsorpsi. (1) Antibodi terhadap MBP-Mga yang tidak diadsorpsi dengan MBP murni; (2) Antibodi terhadap MBP-Mga diadsorpsi dengan MBP murni,564 µg/µl antibodi; (A) Protein MBP-Mga murni dengan kadar 8 ng; (B) Protein MBP murni dengan kadar 8 ng. Berdasarkan data di atas antibodi poliklonal terhadap protein fusi MBP-Mga telah berhasil dibuat pada kelinci. Untuk melihat apakah antibodi yang telah diadsorpsi dengan MBP murni mempunyai reaksi silang dengan protein lain, maka dilakukanlah western blot. Tujuan western blot adalah untuk mendeteksi keberadaan protein MBP-Mga pada protein kasar E. coli pmalmga yang diinduksi dan protein MBP-Mga murni. Western blot dilakukan dengan pengenceran 1 : 1.. Hasil analisis western blot menunjukkan bahwa antibodi yang dibuat hanya bereaksi positif dengan protein MBP- Mga dan bereaksi negatif terhadap protein lain (Gambar 6). 2 kda 116,3 kda 97,4 kda 66,3 kda 55,4 kda 36,3 kda 31, kda (a) (b) Gambar 6. (a) Elektroforegram protein MBP-Mga dan protein MBP, (b) Hasil analisis antibodi terhadap protein MBP-Mga dan protein MBP menggunakan metode western blot. (1) Protein marker; (2) Protein kasar E. coli pmalmga yang diinduksi; (3) Protein MBP-Mga murni; (4) Protein kasar E. coli pmalc2 yang diinduksi; (5) Protein MBP murni. 4. Kesimpulan Produksi protein fusi MBP-Mga Streptococcus pyogenes dari Escherichia coli pmalmga telah berhasil ditingkatkan dengan penambahan IPTG,3 mm, selama 2 jam dalam medium LB yang mengandung,2% glukosa. Protein ini telah berhasil dimurnikan menggunakan kromatografi afinitas dengan kolom resin amilosa. Analisis SDS-PAGE menunjukkan adanya satu pita dengan massa molekul sekitar 14 kda. Antibodi poliklonal terhadap protein fusi MBP-Mga dapat dibuat pada kelinci. Analisis dot blot menunjukkan bahwa pengenceran tertinggi serum kelinci yang masih memberikan hasil positif adalah 1 : 1. (v/v). Adsorpsi terhadap antibodi poliklonal yang bereaksi positif dengan MBP dilakukan dengan menambahkan protein MBP murni yang diproduksi oleh E. coli pmalc2 rekombinan dengan konsentrasi,564 µg/µl serum ke dalam antibodi poliklonal yang bereaksi positif dengan protein fusi MBP-Mga. Hasil dot blot dan western blot menunjukkan bahwa antibodi poliklonal yang dihasilkan memberikan reaksi positif terhadap protein Mga rekombinan dan reaksi negatif dengan protein lain. Hasil penelitian protein Mga rekombinan diharapkan dapat dikembangkan untuk penemuan senyawa bioaktif asal Indonesia yang dapat digunakan sebagai anti mikroba baru terhadap infeksi S. pyogenes. Sedangkan antibodi poliklonal terhadap protein Mga rekombinan akan digunakan untuk karakterisasi protein Mga rekombinan yang dihasilkan dari riset lain.
7 JMS Vol. 8 No. 3, September Ucapan Terimakasih Penelitian ini didanai oleh Hibah Tim (Project URGE Batch IV) dari Departemen Pendidikan dan Kebudayaan Republik Indonesia. Peneliti mengucapkan terimakasih kepada anggota Hibah Tim yang telah memberikan kesempatan untuk turut serta dalam penelitian ini. Terimaksih kepada Prof. Andreas Podbielski, M. D. Ph.D, dari Dept. of Med. Microbiology, University Hospital Ulm, Robert-Koch-Strasse 8, D Ulm, Germany atas pemberian bakteri E. coli pmalmga dan E. coli pmalc2, serta antibodi poliklonal terhadap protein pengikat maltosa (MBP) untuk digunakan dalam penelitian ini. Ucapan terimakasih juga disampaikan kepada PT. Biofarma Indonesia di Bandung yang telah menyediakan fasilitas untuk pembuatan antibodi poliklonal terhadap protein fusi MBP-Mga. Daftar Pustaka 1. Retnoningrum, D.S., & Cleary, P.P., M12 Protein from Streptococcus pyogenes is a Receptor for Immunoglobulin G3 and Human Albumin, Infect. Immun. 61:1, 2387 (1994). 2. Schlievert, P.M., Assimacopoulos, A.P., & Cleary, P.P., Severe Invasive Group A Streptococcal Disease- Clinical Description and Mechanisms of Pathogonesis, J. Labor. Clin. Med. 127:1, 13 (1996). 3. Kisworo, B., Demam Rematik, Cermin Dunia Kedokteran 116:1, 25 (1997). 4. Fischetti, V.A., Jones, K.F., Hollingshead, S.K., & Scott, J.R., Structure, Function, and Genetics of Streptococcal M Protein, Rev. Infect. Dis. 1:S2, S356 (1988). 5. La Penta, D., Zhang, X.P., & Cleary, P.P., Streptococcus pyogenes Type Iia IgG Fc Receptor Expression is co-ordiantely Regulated with M Protein and Streptococcal C5a Peptidase, Mol. Microbiol. 12:6, 873 (1994). 6. Podbielski, A., Woischnik, B.P.M., & Schmidt, K.H., What is the Size of the Group A Streptococcal Vir Regulon? The Mga Regulator Affects Expression of Secreted and Surface Virulence Factors, Med. Microbiol. Immunol. 185:3, 171 (1996). 7. Retnoningrum, D.S., & Cleary, P.P., Group A Streptoccal Class I M Proteins are Functionally and Structurally Similar to Bacterial Ig Receptors in Pathogenic Streptocci : Present and Future, Lancer Publication, 241 (1994). 8. Chen, C., Bormann, N., & Cleary, P.P., VirR and Mry are Homologous Trans-acting Regulators of M Protein and C5a Peptidase Expression in Group A Streptococci, Mol. Gen. Genet. 241:5, 685 (1993). 9. Kihlberg, B.M., Cooney, J., Caparon, M.G., Olsen, A., & Bjorck, L., Biological Properties of A Streptococcus pyogenes Mutant Generated by Tn916 Insertion in mga, Microbiol. Pathol. 19:5, 299 (1995). 1. McIver, K.S., Thurman, A.S., & Scott, J.R., Regulation of mga Transcription in the Group A Streptococcus: Spesific Binding of Mga within Its Own Promoter and Evidence for a Negative Regulator, J. Bacteriol. 181:17, 5373 (1999). 11. McLandsborough, L.A., & Cleary, P.P., Insertional Inactivation of VirR in Streptococcus pyogenes M49 Demonstrates that VirR Function as a Positive Regulator of ScpA, FcRA, OF, and M Protein, FEMS Microbiol. Lett. 128:1, 45 (1995).
Purifikasi Protein Fusi MBP-Mga Streptococcus pyogenes Hasil Ekspresi Heterolog di Escherichia coli
 Jurnal Matematika dan Sains Vol. 1 No. 1, Maret 25, hal 31-36 Purifikasi Protein Fusi MBP-Mga Streptococcus pyogenes Hasil Ekspresi Heterolog di Escherichia coli Muhaimin 1), Oei Ban Liang 2,4), Enny Ratnaningsih
Jurnal Matematika dan Sains Vol. 1 No. 1, Maret 25, hal 31-36 Purifikasi Protein Fusi MBP-Mga Streptococcus pyogenes Hasil Ekspresi Heterolog di Escherichia coli Muhaimin 1), Oei Ban Liang 2,4), Enny Ratnaningsih
Pembuatan Media Kultur Bakteri Pemanenan sel bakteri. Isolasi DNA kromosom bakteri. Kloning DNA
 LAMPIRAN 15 15 Lampiran 1 Tahapan penelitian Pembuatan Media Kultur Bakteri Pemanenan sel bakteri Isolasi DNA kromosom bakteri Pemotongan DNA dengan enzim restriksi Kloning DNA Isolasi DNA plasmid hasil
LAMPIRAN 15 15 Lampiran 1 Tahapan penelitian Pembuatan Media Kultur Bakteri Pemanenan sel bakteri Isolasi DNA kromosom bakteri Pemotongan DNA dengan enzim restriksi Kloning DNA Isolasi DNA plasmid hasil
4 Hasil dan Pembahasan
 4 Hasil dan Pembahasan α-amilase merupakan enzim yang mempunyai peranan penting dalam bioteknologi saat ini. Aplikasi teknis enzim ini sangat luas, seperti pada proses likuifaksi pati pada proses produksi
4 Hasil dan Pembahasan α-amilase merupakan enzim yang mempunyai peranan penting dalam bioteknologi saat ini. Aplikasi teknis enzim ini sangat luas, seperti pada proses likuifaksi pati pada proses produksi
Pengujian Inhibisi RNA Helikase Virus Hepatitis C (Utama et al. 2000) HASIL DAN PEMBAHASAN Hasil Ekspresi dan Purifikasi RNA
 8 kromatografi kemudian diuji aktivitas inhibisinya dengan metode kolorimetri ATPase assay. Beberapa fraksi yang memiliki aktivitas inhibisi yang tinggi digunakan untuk tahapan selanjutnya (Lampiran 3).
8 kromatografi kemudian diuji aktivitas inhibisinya dengan metode kolorimetri ATPase assay. Beberapa fraksi yang memiliki aktivitas inhibisi yang tinggi digunakan untuk tahapan selanjutnya (Lampiran 3).
4 HASIL DAN PEMBAHASAN
 4 HASIL DAN PEMBAHASAN 4.1 Isolasi enzim fibrinolitik Cacing tanah P. excavatus merupakan jenis cacing tanah yang agresif dan tahan akan kondisi pemeliharaan yang ekstrim. Pemeliharaan P. excavatus dilakukan
4 HASIL DAN PEMBAHASAN 4.1 Isolasi enzim fibrinolitik Cacing tanah P. excavatus merupakan jenis cacing tanah yang agresif dan tahan akan kondisi pemeliharaan yang ekstrim. Pemeliharaan P. excavatus dilakukan
FAKULTAS BIOLOGI LABORATORIUM GENETIKA & PEMULIAAN INSTRUKSI KERJA UJI
 Halaman : 1 dari 5 ISOLASI TOTAL DNA HEWAN DENGAN KIT EKSTRAKSI DNA 1. RUANG LINGKUP Metode ini digunakan untuk mengisolasi DNA dari sampel jaringan hewan, dapat dari insang, otot, darah atau jaringan
Halaman : 1 dari 5 ISOLASI TOTAL DNA HEWAN DENGAN KIT EKSTRAKSI DNA 1. RUANG LINGKUP Metode ini digunakan untuk mengisolasi DNA dari sampel jaringan hewan, dapat dari insang, otot, darah atau jaringan
FAKULTAS BIOLOGI LABORATORIUM GENETIKA & PEMULIAAN INSTRUKSI KERJA UJI
 ISOLASI TOTAL DNA TUMBUHAN DENGAN KIT EKSTRAKSI DNA PHYTOPURE Halaman : 1 dari 5 1. RUANG LINGKUP Metode ini digunakan untuk mengisolasi DNA dari sampel jaringan tumbuhan, dapat dari daun, akar, batang,
ISOLASI TOTAL DNA TUMBUHAN DENGAN KIT EKSTRAKSI DNA PHYTOPURE Halaman : 1 dari 5 1. RUANG LINGKUP Metode ini digunakan untuk mengisolasi DNA dari sampel jaringan tumbuhan, dapat dari daun, akar, batang,
3. BAHAN DAN METODE 3.1 Tempat Penelitian 3.2 Metode Penelitian Persiapan dan Pemeliharaan Kelinci sebagai Hewan Coba
 3. BAHAN DAN METODE 3.1 Tempat Penelitian Penelitian dilaksanakan di Laboratorium Terpadu Immunologi, Departemen Ilmu Penyakit Hewan dan Kesehatan Masyarakat Veteriner dan Kandang Terpadu, Fakultas Kedokteran
3. BAHAN DAN METODE 3.1 Tempat Penelitian Penelitian dilaksanakan di Laboratorium Terpadu Immunologi, Departemen Ilmu Penyakit Hewan dan Kesehatan Masyarakat Veteriner dan Kandang Terpadu, Fakultas Kedokteran
RATNA ANNISA UTAMI
 RATNA ANNISA UTAMI 10703022 AMPLIFIKASI DAN KLONING DNA PENGKODE PROTEIN CHAPERONIN 60.1 MYCOBACTERIUM TUBERCULOSIS KE DALAM VEKTOR pgem-t PADA ESCHERICHIA COLI PROGRAM STUDI SAINS DAN TEKNOLOGI FARMASI
RATNA ANNISA UTAMI 10703022 AMPLIFIKASI DAN KLONING DNA PENGKODE PROTEIN CHAPERONIN 60.1 MYCOBACTERIUM TUBERCULOSIS KE DALAM VEKTOR pgem-t PADA ESCHERICHIA COLI PROGRAM STUDI SAINS DAN TEKNOLOGI FARMASI
BAHAN DAN METODE Waktu dan Tempat Penelitian Hewan coba Metode Penelitian 1 Isolasi dan Produksi Antigen E/S Fasciola gigantica
 BAHAN DAN METODE Waktu dan Tempat Penelitian Penelitian dilaksanakan pada bulan September 2009 hingga Februari 2010. Penelitian dilakukan di kandang pemeliharaan hewan coba Fakultas Kedokteran Hewan Institut
BAHAN DAN METODE Waktu dan Tempat Penelitian Penelitian dilaksanakan pada bulan September 2009 hingga Februari 2010. Penelitian dilakukan di kandang pemeliharaan hewan coba Fakultas Kedokteran Hewan Institut
KEMENTERIAN PENDIDIKAN DAN KEBUDAYAAN DIREKTORAT JENDERAL PENDIDIKAN MENENGAH DIREKTORAT PEMBINAAN SEKOLAH MENENGAH ATAS
 KEMENTERIAN PENDIDIKAN DAN KEBUDAYAAN DIREKTORAT JENDERAL PENDIDIKAN MENENGAH DIREKTORAT PEMBINAAN SEKOLAH MENENGAH ATAS Test Seleksi Calon Peserta International Biology Olympiad (IBO) 2014 2 8 September
KEMENTERIAN PENDIDIKAN DAN KEBUDAYAAN DIREKTORAT JENDERAL PENDIDIKAN MENENGAH DIREKTORAT PEMBINAAN SEKOLAH MENENGAH ATAS Test Seleksi Calon Peserta International Biology Olympiad (IBO) 2014 2 8 September
Bab IV Hasil dan Pembahasan
 Bab IV Hasil dan Pembahasan IV.1 Akar Nanas Kering dan Hidroponik Akar nanas kering yang digunakan dalam penelitian ini merupakan akar nanas yang tertanam dalam tanah, berwarna coklat dan berupa suatu
Bab IV Hasil dan Pembahasan IV.1 Akar Nanas Kering dan Hidroponik Akar nanas kering yang digunakan dalam penelitian ini merupakan akar nanas yang tertanam dalam tanah, berwarna coklat dan berupa suatu
Gambar 1. Struktur organisasi promoter pada organisme prokariot [Sumber: University of Miami 2008: 1.]
![Gambar 1. Struktur organisasi promoter pada organisme prokariot [Sumber: University of Miami 2008: 1.] Gambar 1. Struktur organisasi promoter pada organisme prokariot [Sumber: University of Miami 2008: 1.]](/thumbs/63/49770631.jpg) Gambar 1. Struktur organisasi promoter pada organisme prokariot [Sumber: University of Miami 2008: 1.] Gambar 2. Struktur organisasi promoter pada organisme eukariot [Sumber: Gilbert 1997: 1.] Gambar 3.
Gambar 1. Struktur organisasi promoter pada organisme prokariot [Sumber: University of Miami 2008: 1.] Gambar 2. Struktur organisasi promoter pada organisme eukariot [Sumber: Gilbert 1997: 1.] Gambar 3.
3. METODOLOGI 3.1 Waktu dan Tempat Penelitian 3.2 Alat dan Bahan
 3. METODOLOGI 3.1 Waktu dan Tempat Penelitian Penelitian ini dimulai pada bulan Januari 2009 dan selesai pada bulan November 2009. Penelitian dilakukan di Laboratorium Biokimia dan Bioteknologi II, Departemen
3. METODOLOGI 3.1 Waktu dan Tempat Penelitian Penelitian ini dimulai pada bulan Januari 2009 dan selesai pada bulan November 2009. Penelitian dilakukan di Laboratorium Biokimia dan Bioteknologi II, Departemen
III. METODE PENELITIAN. Penelitian dilakukan di Laboratorium Biokimia dan Laboratorium Instrumentasi
 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian dilakukan di Laboratorium Biokimia dan Laboratorium Instrumentasi Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas
III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian dilakukan di Laboratorium Biokimia dan Laboratorium Instrumentasi Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas
4 Hasil dan Pembahasan
 4 Hasil dan Pembahasan α-amilase adalah enzim menghidrolisis ikatan α-1,4-glikosidik pada pati. α-amilase disekresikan oleh mikroorganisme, tanaman, dan organisme tingkat tinggi. α-amilase memiliki peranan
4 Hasil dan Pembahasan α-amilase adalah enzim menghidrolisis ikatan α-1,4-glikosidik pada pati. α-amilase disekresikan oleh mikroorganisme, tanaman, dan organisme tingkat tinggi. α-amilase memiliki peranan
III. METODOLOGI PENELITIAN. Penelitian ini dilakukan pada bulan Juli 2012 sampai bulan Desember 2012 di
 23 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan Juli 2012 sampai bulan Desember 2012 di Laboratorium Biokimia Jurusan Kimia Fakultas Matematika dan Ilmu
23 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan Juli 2012 sampai bulan Desember 2012 di Laboratorium Biokimia Jurusan Kimia Fakultas Matematika dan Ilmu
BAB III BAHAN, ALAT DAN METODA
 15 BAB III BAHAN, ALAT DAN METODA 3.1 BAHAN Lactobacillus acidophilus FNCC116 (kultur koleksi BPPT yang didapatkan dari Universitas Gajah Mada), Bacillus licheniformis F11.4 (kultur koleksi BPPT yang didapatkan
15 BAB III BAHAN, ALAT DAN METODA 3.1 BAHAN Lactobacillus acidophilus FNCC116 (kultur koleksi BPPT yang didapatkan dari Universitas Gajah Mada), Bacillus licheniformis F11.4 (kultur koleksi BPPT yang didapatkan
BAHAN DAN METODE Tempat dan Waktu Bahan Pertumbuhan dan Peremajaan Isolat Pengamatan Morfologi Isolat B. thuringiensis
 13 BAHAN DAN METODE Tempat dan Waktu Penelitian ini dilaksanakan di Laboratorium Mikrobiologi, Departemen Biologi, IPB, dari bulan Oktober 2011 Mei 2012. Bahan Isolasi untuk memperoleh isolat B. thuringiensis
13 BAHAN DAN METODE Tempat dan Waktu Penelitian ini dilaksanakan di Laboratorium Mikrobiologi, Departemen Biologi, IPB, dari bulan Oktober 2011 Mei 2012. Bahan Isolasi untuk memperoleh isolat B. thuringiensis
BAB 3 PERCOBAAN 3.1 Bahan 3.2 Alat
 BAB 3 PERCOBAAN 3.1 Bahan Bahan yang digunakan memiliki kualitas pro analisis atau pro biologi molekular, yaitu : primer M. tuberculosis forward: 5 GGATCCGATGAGCAAGCTGATCGAA3 (Proligo) dan primer M. tuberculosis
BAB 3 PERCOBAAN 3.1 Bahan Bahan yang digunakan memiliki kualitas pro analisis atau pro biologi molekular, yaitu : primer M. tuberculosis forward: 5 GGATCCGATGAGCAAGCTGATCGAA3 (Proligo) dan primer M. tuberculosis
TRANSFORMASI DAN EKSPRESI pet-endo-β-1,4-xilanase DALAM Escherichia coli BL21 SKRIPSI. Oleh : Eka Yuni Kurniawati NIM
 TRANSFORMASI DAN EKSPRESI pet-endo-β-1,4-xilanase DALAM Escherichia coli BL21 SKRIPSI Oleh : Eka Yuni Kurniawati NIM 101810301003 JURUSAN KIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS
TRANSFORMASI DAN EKSPRESI pet-endo-β-1,4-xilanase DALAM Escherichia coli BL21 SKRIPSI Oleh : Eka Yuni Kurniawati NIM 101810301003 JURUSAN KIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS
EKSTRAKSI DNA. 13 Juni 2016
 EKSTRAKSI DNA 13 Juni 2016 Pendahuluan DNA: polimer untai ganda yg tersusun dari deoksiribonukleotida (dari basa purin atau pirimidin, gula pentosa,dan fosfat). Basa purin: A,G Basa pirimidin: C,T DNA
EKSTRAKSI DNA 13 Juni 2016 Pendahuluan DNA: polimer untai ganda yg tersusun dari deoksiribonukleotida (dari basa purin atau pirimidin, gula pentosa,dan fosfat). Basa purin: A,G Basa pirimidin: C,T DNA
HASIL DAN PEMBAHASAN bp bp bp
 HASIL DAN PEBAHASAN Purifikasi dan Pengujian Produk PCR (Stilbena Sintase) Purifikasi ini menggunakan high pure plasmid isolation kit dari Invitrogen. Percobaan dilakukan sesuai dengan prosedur yang terdapat
HASIL DAN PEBAHASAN Purifikasi dan Pengujian Produk PCR (Stilbena Sintase) Purifikasi ini menggunakan high pure plasmid isolation kit dari Invitrogen. Percobaan dilakukan sesuai dengan prosedur yang terdapat
Lampiran 1 Data Rendemen Pelet Kapang Endofit Xylaria psidii KT30. Berat sampel (pelet) setelah sentrifugase: 0,223 gram
 LAMPIRAN 29 30 Lampiran 1 Data Rendemen Pelet Kapang Endofit Xylaria psidii KT30 1) Kultur 1 Volume kultur awal : 350 ml Volume setelah penyaringan : 300 ml ph awal sebelum ekstraksi : 4,31 Berat sampel
LAMPIRAN 29 30 Lampiran 1 Data Rendemen Pelet Kapang Endofit Xylaria psidii KT30 1) Kultur 1 Volume kultur awal : 350 ml Volume setelah penyaringan : 300 ml ph awal sebelum ekstraksi : 4,31 Berat sampel
I. METODOLOGI PENELITIAN. Penelitian ini dilaksanakan pada bulan April - Juli 2012 di Laboratorium. Ilmu Pengetahuan Alam Universitas Lampung.
 1 I. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan April - Juli 2012 di Laboratorium Biokimia, Laboratorium Instrumentasi Jurusan Kimia Fakultas Matematika
1 I. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan April - Juli 2012 di Laboratorium Biokimia, Laboratorium Instrumentasi Jurusan Kimia Fakultas Matematika
LAPORAN PRAKTIKUM 5, 6, 7, 8 ISOLASI DNA, ISOLASI PROTEIN DARAH, SERTA PEMERIKSAAN DENGAN TEKNIK PCR, ELEKTROFORESIS AGAROSE DAN SDS-PAGE
 LAPORAN PRAKTIKUM 5, 6, 7, 8 ISOLASI DNA, ISOLASI PROTEIN DARAH, SERTA PEMERIKSAAN DENGAN TEKNIK PCR, ELEKTROFORESIS AGAROSE DAN SDS-PAGE Nama (NIM) : Debby Mirani Lubis (137008010) dan Melviana (137008011)
LAPORAN PRAKTIKUM 5, 6, 7, 8 ISOLASI DNA, ISOLASI PROTEIN DARAH, SERTA PEMERIKSAAN DENGAN TEKNIK PCR, ELEKTROFORESIS AGAROSE DAN SDS-PAGE Nama (NIM) : Debby Mirani Lubis (137008010) dan Melviana (137008011)
BAHAN DAN METODE. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan dari bulan Juli 2007 sampai bulan Juni 2008 di
 BAHAN DAN METODE : Waktu dan Tempat Penelitian Penelitian ini dilaksanakan dari bulan Juli 2007 sampai bulan Juni 2008 di 1. Laboratorium Bioteknologi Hewan dan Biomedis PPSHB IPB 2. Laboratorium Mikrobiologi
BAHAN DAN METODE : Waktu dan Tempat Penelitian Penelitian ini dilaksanakan dari bulan Juli 2007 sampai bulan Juni 2008 di 1. Laboratorium Bioteknologi Hewan dan Biomedis PPSHB IPB 2. Laboratorium Mikrobiologi
METODOLOGI PENELITIAN. Penelitian ini dilakukan pada bulan April 2012 sampai dengan bulan Juni 2012 di
 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan April 2012 sampai dengan bulan Juni 2012 di Laboratorium Biokimia Jurusan Kimia Fakultas Matematika dan Ilmu
III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan April 2012 sampai dengan bulan Juni 2012 di Laboratorium Biokimia Jurusan Kimia Fakultas Matematika dan Ilmu
BAB III METODE PENELITIAN Bagan Alir Penelitian ini secara umum dapat digambarkan pada skema berikut:
 BAB III METODE PENELITIAN Tahapan-tahapan yang dilakukan dalam penelitian ini adalah: pengumpulan sampel, lisis terhadap sampel mtdna yang telah diperoleh, amplifikasi daerah HVI mtdna sampel dengan menggunakan
BAB III METODE PENELITIAN Tahapan-tahapan yang dilakukan dalam penelitian ini adalah: pengumpulan sampel, lisis terhadap sampel mtdna yang telah diperoleh, amplifikasi daerah HVI mtdna sampel dengan menggunakan
BAHAN DAN METODE. Tempat dan Waktu Penelitian
 BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilakukan di Laboratorium Kerjasama Bioteknologi Indonesia- Belanda (BIORIN) dan Laboratorium Biologi Molekuler dan Seluler Tanaman (BMST), Pusat
BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilakukan di Laboratorium Kerjasama Bioteknologi Indonesia- Belanda (BIORIN) dan Laboratorium Biologi Molekuler dan Seluler Tanaman (BMST), Pusat
PEMURNIAN DAN KARAKTERISAS&I&&NZIM -?G,('" INTRASEL DART Bacillus sp. BAC4
 PEMURNIAN DAN KARAKTERISAS&I&&NZIM -?G,('" INTRASEL DART Bacillus sp. BAC4 TESTS MAGISTER Oien SVAIFUL BAHRI 20598515 BIDANG KHUSUS KIMIA ORGANIK PROGRAM MAGISTER KIMIA INSTITC T TEKNOLOGI BANDUNG 2001
PEMURNIAN DAN KARAKTERISAS&I&&NZIM -?G,('" INTRASEL DART Bacillus sp. BAC4 TESTS MAGISTER Oien SVAIFUL BAHRI 20598515 BIDANG KHUSUS KIMIA ORGANIK PROGRAM MAGISTER KIMIA INSTITC T TEKNOLOGI BANDUNG 2001
BAB III METODE PENELITIAN. Alat dan bahan yang digunakan dalam penelitian ini adalah sebagai
 BAB III METODE PENELITIAN 3.1. Alat dan Bahan Alat dan bahan yang digunakan dalam penelitian ini adalah sebagai berikut: 3.1.1 Alat Alat- alat yang digunakan dalam penelitian ini antara lain : peralatan
BAB III METODE PENELITIAN 3.1. Alat dan Bahan Alat dan bahan yang digunakan dalam penelitian ini adalah sebagai berikut: 3.1.1 Alat Alat- alat yang digunakan dalam penelitian ini antara lain : peralatan
BAB 4 HASIL PERCOBAAN DAN PEMBAHASAN
 BAB 4 HASIL PERCOBAAN DAN PEMBAHASAN Sebelum melakukan PCR, terlebih dahulu dilakukan perancangan primer menggunakan program DNA Star. Pemilihan primer dilakukan dengan mempertimbangkan parameter spesifisitas,
BAB 4 HASIL PERCOBAAN DAN PEMBAHASAN Sebelum melakukan PCR, terlebih dahulu dilakukan perancangan primer menggunakan program DNA Star. Pemilihan primer dilakukan dengan mempertimbangkan parameter spesifisitas,
HASIL DAN PEMBAHASAN
 HASIL DAN PEMBAHASAN Pemotongan Parsial dan Penyisipan Nukleotida pada Ujung Fragmen DNA Konstruksi pustaka genom membutuhkan potongan DNA yang besar. Untuk mendapatkan fragmen-fragmen dengan ukuran relatif
HASIL DAN PEMBAHASAN Pemotongan Parsial dan Penyisipan Nukleotida pada Ujung Fragmen DNA Konstruksi pustaka genom membutuhkan potongan DNA yang besar. Untuk mendapatkan fragmen-fragmen dengan ukuran relatif
YOHANES NOVI KURNIAWAN KONSTRUKSI DAERAH PENGKODE INTERFERON ALFA-2B (IFNα2B) DAN KLONINGNYA PADA Escherichia coli JM109
 YOHANES NOVI KURNIAWAN 10702026 KONSTRUKSI DAERAH PENGKODE INTERFERON ALFA-2B (IFNα2B) DAN KLONINGNYA PADA Escherichia coli JM109 Program Studi Sains dan Teknologi Farmasi INSTITUT TEKNOLOGI BANDUNG 2007
YOHANES NOVI KURNIAWAN 10702026 KONSTRUKSI DAERAH PENGKODE INTERFERON ALFA-2B (IFNα2B) DAN KLONINGNYA PADA Escherichia coli JM109 Program Studi Sains dan Teknologi Farmasi INSTITUT TEKNOLOGI BANDUNG 2007
Hasil dan Pembahasan
 27 Bab IV Hasil dan Pembahasan IV.1 Isolasi Enzim katalase dari kentang Enzim katalase terdapat dalam peroksisom, organel yang ditemukan pada jaringan tumbuhan di luar inti sel kentang sehingga untuk mengekstraknya
27 Bab IV Hasil dan Pembahasan IV.1 Isolasi Enzim katalase dari kentang Enzim katalase terdapat dalam peroksisom, organel yang ditemukan pada jaringan tumbuhan di luar inti sel kentang sehingga untuk mengekstraknya
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN A. Jenis Penelitian Penelitian ini merupakan penelitian murni yang dilakukan dengan metode deskriptif, yaitu suatu metode penelitian untuk membuat deskripsi, gambaran atau lukisan
BAB III METODE PENELITIAN A. Jenis Penelitian Penelitian ini merupakan penelitian murni yang dilakukan dengan metode deskriptif, yaitu suatu metode penelitian untuk membuat deskripsi, gambaran atau lukisan
HASIL DA PEMBAHASA. Kadar Air
 Pemilihan Eluen Terbaik Pelat Kromatografi Lapis Tipis (KLT) yang digunakan adalah pelat aluminium jenis silika gel G 60 F 4. Ekstrak pekat ditotolkan pada pelat KLT. Setelah kering, langsung dielusi dalam
Pemilihan Eluen Terbaik Pelat Kromatografi Lapis Tipis (KLT) yang digunakan adalah pelat aluminium jenis silika gel G 60 F 4. Ekstrak pekat ditotolkan pada pelat KLT. Setelah kering, langsung dielusi dalam
IV. HASIL DAN PEMBAHASAN
 IV. HASIL DAN PEMBAHASAN A. Isolat Actinomycetes Amilolitik Terpilih 1. Isolat Actinomycetes Terpilih Peremajaan isolat actinomycetes dilakukan dengan tujuan sebagai pemeliharaan isolat actinomycetes agar
IV. HASIL DAN PEMBAHASAN A. Isolat Actinomycetes Amilolitik Terpilih 1. Isolat Actinomycetes Terpilih Peremajaan isolat actinomycetes dilakukan dengan tujuan sebagai pemeliharaan isolat actinomycetes agar
PRODUKSI ENZIM AMILASE
 LAPORAN PRAKTIKUM MIKROB DAN POTENSINYA PRODUKSI ENZIM AMILASE KHAIRUL ANAM P051090031/BTK BIOTEKNOLOGI SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR 2010 PRODUKSI ENZIM AMILASE Pendahuluan Amilase merupakan
LAPORAN PRAKTIKUM MIKROB DAN POTENSINYA PRODUKSI ENZIM AMILASE KHAIRUL ANAM P051090031/BTK BIOTEKNOLOGI SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR 2010 PRODUKSI ENZIM AMILASE Pendahuluan Amilase merupakan
MAKALAH. BAKTERI Streptococcus pyogenes. Oleh: Sri Agung Fitri Kusuma, M.Si., Apt
 MAKALAH BAKTERI Streptococcus pyogenes Oleh: Sri Agung Fitri Kusuma, M.Si., Apt UNIVERSITAS PADJADJARAN FAKULTAS FARMASI MARET 2010 LEMBAR PENGESAHAN MAKALAH Streptococcus pyogenes Oleh : Sri Agung Fitri
MAKALAH BAKTERI Streptococcus pyogenes Oleh: Sri Agung Fitri Kusuma, M.Si., Apt UNIVERSITAS PADJADJARAN FAKULTAS FARMASI MARET 2010 LEMBAR PENGESAHAN MAKALAH Streptococcus pyogenes Oleh : Sri Agung Fitri
BAB III METODE PENELITIAN. Penelitian ini merupakan penelitian eksperimental dengan 7 sampel dari 7
 BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian ini merupakan penelitian eksperimental dengan 7 sampel dari 7 individu udang Jari yang diambil dari Segara Anakan Kabupaten Cilacap Jawa Tengah.
BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian ini merupakan penelitian eksperimental dengan 7 sampel dari 7 individu udang Jari yang diambil dari Segara Anakan Kabupaten Cilacap Jawa Tengah.
ADLN- PERPUSTAKAAN UNIVERSITAS AIRLANGGA DAFTAR ISI
 DAFTAR ISI Halaman Sampul Luar... i Sampul Dalam... ii Halaman Prasyarat Gelar... iii Halaman Pengesahan... iv UCAPAN TERIMA KASIH... v ABSTRAK... vi ABSTRACT... vii DAFTAR ISI... viii DAFTAR TABEL...
DAFTAR ISI Halaman Sampul Luar... i Sampul Dalam... ii Halaman Prasyarat Gelar... iii Halaman Pengesahan... iv UCAPAN TERIMA KASIH... v ABSTRAK... vi ABSTRACT... vii DAFTAR ISI... viii DAFTAR TABEL...
HASIL DAN PEMBAHASAN
 HASIL DAN PEMBAHASAN Isolasi DNA Total Tumbuhan Isolasi DNA total merupakan tahap awal dari pembuatan pustaka genom. DNA dipisahkan dari bahan-bahan lain yang ada dalam sel. DNA total yang diperlukan untuk
HASIL DAN PEMBAHASAN Isolasi DNA Total Tumbuhan Isolasi DNA total merupakan tahap awal dari pembuatan pustaka genom. DNA dipisahkan dari bahan-bahan lain yang ada dalam sel. DNA total yang diperlukan untuk
Lampiran 1 Rancangan penelitian
 LAMPIRAN 18 19 Lampiran 1 Rancangan penelitian Cacing tanah E. foetida dewasa Kering oven vakum (Setiawan) Tepung cacing kering Ekstraksi buffer dan sentrifugasi Ekstrak kasar protease Salting-out dengan
LAMPIRAN 18 19 Lampiran 1 Rancangan penelitian Cacing tanah E. foetida dewasa Kering oven vakum (Setiawan) Tepung cacing kering Ekstraksi buffer dan sentrifugasi Ekstrak kasar protease Salting-out dengan
Analisis Bobot Molekul Protein Inhibitor RNA Helikase HCV (Hairany 2010 termodifikasi) HASIL DAN PEMBAHASAN Hasil Isolasi RNA Helikase HCV
 7 diinkubasi pada suhu 37ºC selama 30 menit. Absorbansi diukur menggunakan panjang gelombang 562 nm. Standar protein yang digunakan adalah albumin serum sapi (Bovine Serum Albumin (BSA)) pada kisaran 0.05
7 diinkubasi pada suhu 37ºC selama 30 menit. Absorbansi diukur menggunakan panjang gelombang 562 nm. Standar protein yang digunakan adalah albumin serum sapi (Bovine Serum Albumin (BSA)) pada kisaran 0.05
III. METODOLOGI PENELITIAN. Penelitian ini dilakukan pada bulan Juni-November Penelitian ini
 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan Juni-November 2013. Penelitian ini dilakukan di Laboratorium Biokimia dan Laboratorium Biomassa Jurusan Kimia
III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan Juni-November 2013. Penelitian ini dilakukan di Laboratorium Biokimia dan Laboratorium Biomassa Jurusan Kimia
BAB III METODE PENELITIAN. adalah Bacillus subtilis dan Bacillus cereus yang diperoleh di Laboratorium
 23 BAB III METODE PENELITIAN 3.1 Objek dan Lokasi Penelitian Objek atau bahan penelitian yang digunakan dalam penelitian ini adalah Bacillus subtilis dan Bacillus cereus yang diperoleh di Laboratorium
23 BAB III METODE PENELITIAN 3.1 Objek dan Lokasi Penelitian Objek atau bahan penelitian yang digunakan dalam penelitian ini adalah Bacillus subtilis dan Bacillus cereus yang diperoleh di Laboratorium
KLONING DAN OVEREKSPRESI GEN celd DARI Clostridium thermocellum ATCC DALAM pet-blue VECTOR 1
 PROPOSAL METODOLOGI PENELITIAN (BM-3001) KLONING DAN OVEREKSPRESI GEN celd DARI Clostridium thermocellum ATCC 27405 DALAM pet-blue VECTOR 1 Penyusun: Chandra 10406014 Dosen Narasumber: Dra. Maelita Ramdani
PROPOSAL METODOLOGI PENELITIAN (BM-3001) KLONING DAN OVEREKSPRESI GEN celd DARI Clostridium thermocellum ATCC 27405 DALAM pet-blue VECTOR 1 Penyusun: Chandra 10406014 Dosen Narasumber: Dra. Maelita Ramdani
BAB III METODE PENELITIAN. A. Waktu dan Tempat Penelitian. Penelitian dilaksanakan pada bulan Maret-November 2012 di
 digilib.uns.ac.id BAB III METODE PENELITIAN A. Waktu dan Tempat Penelitian Penelitian dilaksanakan pada bulan Maret-November 2012 di Laboratorium Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas
digilib.uns.ac.id BAB III METODE PENELITIAN A. Waktu dan Tempat Penelitian Penelitian dilaksanakan pada bulan Maret-November 2012 di Laboratorium Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN A. Jenis Penelitian deskriptif. Jenis penelitian yang digunakan adalah penelitian dasar dengan metode B. Objek Penelitian Objek penelitian ini adalah sampel DNA koleksi hasil
BAB III METODE PENELITIAN A. Jenis Penelitian deskriptif. Jenis penelitian yang digunakan adalah penelitian dasar dengan metode B. Objek Penelitian Objek penelitian ini adalah sampel DNA koleksi hasil
BAB 3 PERCOBAAN. Alat elektroforesis agarosa (Biorad), autoklaf, cawan Petri, GeneAid High Speed Plasmid
 BAB 3 PERCOBAAN 3.1 Alat Alat elektroforesis agarosa (Biorad), autoklaf, cawan Petri, GeneAid High Speed Plasmid Mini kit, inkubator goyang (GSL), jarum Ose bundar, kit GFX (GE Healthcare), kompor listrik
BAB 3 PERCOBAAN 3.1 Alat Alat elektroforesis agarosa (Biorad), autoklaf, cawan Petri, GeneAid High Speed Plasmid Mini kit, inkubator goyang (GSL), jarum Ose bundar, kit GFX (GE Healthcare), kompor listrik
II. BAHAN DAN METODE
 II. BAHAN DAN METODE 2.1 Rancangan Perlakuan Penelitian ini terdiri dari enam perlakuan yang masing-masing diberi 3 kali ulangan. Perlakuan yang diberikan berupa perendaman dengan dosis relhp berbeda yaitu
II. BAHAN DAN METODE 2.1 Rancangan Perlakuan Penelitian ini terdiri dari enam perlakuan yang masing-masing diberi 3 kali ulangan. Perlakuan yang diberikan berupa perendaman dengan dosis relhp berbeda yaitu
BAB III METODE A. Jenis Penelitian B. Populasi dan Sampel C. Waktu dan Lokasi Penelitian D. Alat dan Bahan Rizki Indah Permata Sari,2014
 34 BAB III METODE A. Jenis Penelitian Penelitian ini merupakan penelitian murni atau pure research yang dilakukan dengan metode deskriptif, yaitu suatu metode penelitian untuk membuat deskripsi, gambaran
34 BAB III METODE A. Jenis Penelitian Penelitian ini merupakan penelitian murni atau pure research yang dilakukan dengan metode deskriptif, yaitu suatu metode penelitian untuk membuat deskripsi, gambaran
o C 1 menit, penempelan 50 o C 1 menit, polimerisasi 72 o C 1 menit (tiga tahap ini
 13 BAB IV PERCOBAAN IV.1 Bahan Air miliq, deoksinukleotida trifosfat (dntp), MgCl 2, (Promega), enzim Pfu DNA polymerase, dapar Pfu (Stratagene), oligonukleotida SR1, SR2, SR3, SR4, SR5, AR6, AR7, AR8,
13 BAB IV PERCOBAAN IV.1 Bahan Air miliq, deoksinukleotida trifosfat (dntp), MgCl 2, (Promega), enzim Pfu DNA polymerase, dapar Pfu (Stratagene), oligonukleotida SR1, SR2, SR3, SR4, SR5, AR6, AR7, AR8,
BAB 4 HASIL PERCOBAAN DAN BAHASAN. Oligonukleotida sintetis daerah pengkode IFNα2b sintetis dirancang menggunakan
 BAB 4 HASIL PERCOBAAN DAN BAHASAN Oligonukleotida sintetis daerah pengkode IFNα2b sintetis dirancang menggunakan program komputer berdasarkan metode sintesis dua arah TBIO, dimana proses sintesis daerah
BAB 4 HASIL PERCOBAAN DAN BAHASAN Oligonukleotida sintetis daerah pengkode IFNα2b sintetis dirancang menggunakan program komputer berdasarkan metode sintesis dua arah TBIO, dimana proses sintesis daerah
BAB V HASIL DAN PEMBAHASAN
 21 BAB V HASIL DAN PEMBAHASAN Pada penelitian sebelumnya diperoleh kerangka baca terbuka gen IFNα2b yang mengandung tiga mutasi dengan lokasi mutasi yang letaknya berjauhan, sehingga mutagenesis terarah
21 BAB V HASIL DAN PEMBAHASAN Pada penelitian sebelumnya diperoleh kerangka baca terbuka gen IFNα2b yang mengandung tiga mutasi dengan lokasi mutasi yang letaknya berjauhan, sehingga mutagenesis terarah
Kloning Domain KS dan Domain A ke dalam Sel E. coli DH5α. Analisis Bioinformatika. HASIL Penapisan Bakteri Penghasil Senyawa Antibakteri
 3 selama 1 menit, dan elongasi pada suhu 72 0 C selama 1 menit. Tahap terakhir dilakukan pada suhu 72 0 C selama 10 menit. Produk PCR dielektroforesis pada gel agarosa 1 % (b/v) menggunakan tegangan 70
3 selama 1 menit, dan elongasi pada suhu 72 0 C selama 1 menit. Tahap terakhir dilakukan pada suhu 72 0 C selama 10 menit. Produk PCR dielektroforesis pada gel agarosa 1 % (b/v) menggunakan tegangan 70
LAMPIRAN. Lampiran 1. Foto Lokasi Pengambilan Sampel Air Panas Pacet Mojokerto
 LAMPIRAN Lampiran 1. Foto Lokasi Pengambilan Sampel Air Panas Pacet Mojokerto Lampiran 2. Pembuatan Media dan Reagen 2.1 Pembuatan Media Skim Milk Agar (SMA) dalam 1000 ml (Amelia, 2005) a. 20 gram susu
LAMPIRAN Lampiran 1. Foto Lokasi Pengambilan Sampel Air Panas Pacet Mojokerto Lampiran 2. Pembuatan Media dan Reagen 2.1 Pembuatan Media Skim Milk Agar (SMA) dalam 1000 ml (Amelia, 2005) a. 20 gram susu
dimana a = bobot sampel awal (g); dan b = bobot abu (g)
 Lampiran 1. Metode analisis proksimat a. Analisis kadar air (SNI 01-2891-1992) Kadar air sampel tapioka dianalisis dengan menggunakan metode gravimetri. Cawan aluminium dikeringkan dengan oven pada suhu
Lampiran 1. Metode analisis proksimat a. Analisis kadar air (SNI 01-2891-1992) Kadar air sampel tapioka dianalisis dengan menggunakan metode gravimetri. Cawan aluminium dikeringkan dengan oven pada suhu
ABSTRAK. ISOLASI, OPTIMASI AMPLIFIKASI DAN KLONING GEN phoq PADA Salmonella typhi
 ABSTRAK ISOLASI, OPTIMASI AMPLIFIKASI DAN KLONING GEN phoq PADA Salmonella typhi Patrisia Puspapriyanti, 2008. Pembimbing I : Ernawati A.Girirachman, Ph.D. Pembimbing II : Johan Lucianus, dr., M.Si. Salmonella
ABSTRAK ISOLASI, OPTIMASI AMPLIFIKASI DAN KLONING GEN phoq PADA Salmonella typhi Patrisia Puspapriyanti, 2008. Pembimbing I : Ernawati A.Girirachman, Ph.D. Pembimbing II : Johan Lucianus, dr., M.Si. Salmonella
HASIL DAN PEMBAHASAN
 18 HASIL DAN PEMBAHASAN Produksi IgY Anti Salmonella Enteritidis pada Telur Ayam Antibodi spesifik terhadap S. Enteritidis pada serum ayam dan telur dideteksi dengan menggunakan uji agar gel presipitasi
18 HASIL DAN PEMBAHASAN Produksi IgY Anti Salmonella Enteritidis pada Telur Ayam Antibodi spesifik terhadap S. Enteritidis pada serum ayam dan telur dideteksi dengan menggunakan uji agar gel presipitasi
MATERI DAN METODE Lokasi dan Waktu Materi Prosedur Karakterisasi Isolat L. plantarum dan Bakteri Indikator
 MATERI DAN METODE Lokasi dan Waktu Penelitian ini berlangsung selama tujuh bulan, yakni mulai dari bulan Februari sampai dengan bulan Agustus 2011. Penelitian ini dilaksanakan di Laboratorium Terpadu Ilmu
MATERI DAN METODE Lokasi dan Waktu Penelitian ini berlangsung selama tujuh bulan, yakni mulai dari bulan Februari sampai dengan bulan Agustus 2011. Penelitian ini dilaksanakan di Laboratorium Terpadu Ilmu
BAB III METODE PENELITIAN. Penelitian ini dilaksanakan pada bulan Mei sampai September 2014 di Green
 BAB III METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Mei sampai September 2014 di Green House dan Laboratorium Genetika dan Molekuler jurusan Biologi Fakultas Sains dan
BAB III METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Mei sampai September 2014 di Green House dan Laboratorium Genetika dan Molekuler jurusan Biologi Fakultas Sains dan
BAB III METODOLOGI PENELITIAN. Waktu pelaksanaan penelitian pada bulan Juni 2013.
 BAB III METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian 1. Waktu Penelitian Waktu pelaksanaan penelitian pada bulan Juni 2013. 2. Tempat Penelitian Penelitian dilaksanakan di Laboratorium Patologi,
BAB III METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian 1. Waktu Penelitian Waktu pelaksanaan penelitian pada bulan Juni 2013. 2. Tempat Penelitian Penelitian dilaksanakan di Laboratorium Patologi,
III. METODOLOGI PENELITIAN. Penelitian ini dilaksanakan dari bulan Juli sampai bulan September 2010 di
 20 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan dari bulan Juli sampai bulan September 2010 di Laboratorium Instrumentasi dan Laboratorium Biokimia Jurusan Kimia
20 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan dari bulan Juli sampai bulan September 2010 di Laboratorium Instrumentasi dan Laboratorium Biokimia Jurusan Kimia
TUGAS TERSTRUKTUR BIOTEKNOLOGI PERTANIAN VEKTOR DNA
 TUGAS TERSTRUKTUR BIOTEKNOLOGI PERTANIAN VEKTOR DNA Oleh: Gregorius Widodo Adhi Prasetyo A2A015009 KEMENTERIAN RISET TEKNOLOGI DAN PENDIDIKAN TINGGI UNIVERSITAS JENDERAL SOEDIRMAN FAKULTAS PERTANIAN PROGRAM
TUGAS TERSTRUKTUR BIOTEKNOLOGI PERTANIAN VEKTOR DNA Oleh: Gregorius Widodo Adhi Prasetyo A2A015009 KEMENTERIAN RISET TEKNOLOGI DAN PENDIDIKAN TINGGI UNIVERSITAS JENDERAL SOEDIRMAN FAKULTAS PERTANIAN PROGRAM
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian dilakukan pada 4 April 2016 sampai 16 Agustus 2016. Penelitian ini dilaksanakan di Laboratorium Riset Kimia Material dan Hayati Departemen
BAB III METODE PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian dilakukan pada 4 April 2016 sampai 16 Agustus 2016. Penelitian ini dilaksanakan di Laboratorium Riset Kimia Material dan Hayati Departemen
BAB III METODE PENELITIAN. Alat-alat yang digunakan dalam penelitian ini, antara lain: waterbath,
 31 BAB III METODE PENELITIAN 3.1 Alat dan Bahan Alat dan bahan yang digunakan dalam penelitian ini adalah sebagai berikut: 3.1.1 Alat Alat-alat yang digunakan dalam penelitian ini, antara lain: waterbath,
31 BAB III METODE PENELITIAN 3.1 Alat dan Bahan Alat dan bahan yang digunakan dalam penelitian ini adalah sebagai berikut: 3.1.1 Alat Alat-alat yang digunakan dalam penelitian ini, antara lain: waterbath,
METODE PENELITIAN Waktu dan Tempat Penelitian Alat dan Bahan Prosedur Penelitian
 METODE PENELITIAN Waktu dan Tempat Penelitian Penelitian ini dilaksanakan dari bulan Desember 2010 sampai dengan Mei 2011 di Laboratorium Kimia Organik, Departemen Kimia Institut Pertanian Bogor (IPB),
METODE PENELITIAN Waktu dan Tempat Penelitian Penelitian ini dilaksanakan dari bulan Desember 2010 sampai dengan Mei 2011 di Laboratorium Kimia Organik, Departemen Kimia Institut Pertanian Bogor (IPB),
BAB IV HASIL DAN PEMBAHASAN. A. SINTESIS DAN AMPLIFIKASI FRAGMEN GEN tat HIV-1 MELALUI
 BAB IV HASIL DAN PEMBAHASAN A. SINTESIS DAN AMPLIFIKASI FRAGMEN GEN tat HIV-1 MELALUI TEKNIK PCR OVERLAPPING 1. Sintesis dan amplifikasi fragmen ekson 1 dan 2 gen tat HIV-1 Visualisasi gel elektroforesis
BAB IV HASIL DAN PEMBAHASAN A. SINTESIS DAN AMPLIFIKASI FRAGMEN GEN tat HIV-1 MELALUI TEKNIK PCR OVERLAPPING 1. Sintesis dan amplifikasi fragmen ekson 1 dan 2 gen tat HIV-1 Visualisasi gel elektroforesis
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3. 1 Waktu dan Lokasi Penelitian Waktu penelitian dimulai dari bulan Februari sampai Juni 2014. Lokasi penelitian dilakukan di berbagai tempat, antara lain: a. Determinasi sampel
BAB III METODE PENELITIAN 3. 1 Waktu dan Lokasi Penelitian Waktu penelitian dimulai dari bulan Februari sampai Juni 2014. Lokasi penelitian dilakukan di berbagai tempat, antara lain: a. Determinasi sampel
BAHAN DAN METODE. Produksi Protein Rekombinan Hormon Pertumbuhan (rgh)
 11 BAHAN DAN METODE Penelitian ini terdiri atas 2 tahapan utama, yaitu produksi protein rekombinan hormon pertumbuhan (rgh) dari ikan kerapu kertang, ikan gurame, dan ikan mas, dan uji bioaktivitas protein
11 BAHAN DAN METODE Penelitian ini terdiri atas 2 tahapan utama, yaitu produksi protein rekombinan hormon pertumbuhan (rgh) dari ikan kerapu kertang, ikan gurame, dan ikan mas, dan uji bioaktivitas protein
III. METODOLOGI PENELITIAN
 III. METODOLOGI PENELITIAN 3.1. Waktu dan Tempat Penelitian ini dilaksanakan pada bulan November 2006 hingga Agustus 2007. Penangkapan polen dilakukan di kecamatan Pasar Minggu Jakarta Selatan dan analisa
III. METODOLOGI PENELITIAN 3.1. Waktu dan Tempat Penelitian ini dilaksanakan pada bulan November 2006 hingga Agustus 2007. Penangkapan polen dilakukan di kecamatan Pasar Minggu Jakarta Selatan dan analisa
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN A. Jenis Penelitian Jenis penelitian ini adalah penelitian deskriptif yang mengangkat fenomena alam sebagai salah satu masalah dalam penelitian. Penelitian ini dapat menerangkan
BAB III METODE PENELITIAN A. Jenis Penelitian Jenis penelitian ini adalah penelitian deskriptif yang mengangkat fenomena alam sebagai salah satu masalah dalam penelitian. Penelitian ini dapat menerangkan
BAB III METODE PENELITIAN. Dalam penelitian ini dilakukan lima tahap utama yang meliputi tahap
 BAB III METODE PENELITIAN Dalam penelitian ini dilakukan lima tahap utama yang meliputi tahap penyiapan templat mtdna, amplifikasi fragmen mtdna pada daerah D-loop mtdna manusia dengan teknik PCR, deteksi
BAB III METODE PENELITIAN Dalam penelitian ini dilakukan lima tahap utama yang meliputi tahap penyiapan templat mtdna, amplifikasi fragmen mtdna pada daerah D-loop mtdna manusia dengan teknik PCR, deteksi
Analisis kadar protein
 LAMPIRAN Lampiran 1 Bagan alir penelitian Biawak air bagian duodenum, jejenum, ileum, kolon Cuci dengan akuades dan kerok lapisan atasnya (mukosa Ekstraksi enzim protease Analisis kadar protein Pencirian
LAMPIRAN Lampiran 1 Bagan alir penelitian Biawak air bagian duodenum, jejenum, ileum, kolon Cuci dengan akuades dan kerok lapisan atasnya (mukosa Ekstraksi enzim protease Analisis kadar protein Pencirian
3. METODOLOGI PENELITIAN
 3. METODOLOGI PENELITIAN 3.1. Waktu dan tempat Penelitian Penelitian telah dilaksanakan dari bulan Agustus 2006 sampai Juli 2007, bertempat di Laboratorium Bioteknologi Hasil Perairan Departemen Teknologi
3. METODOLOGI PENELITIAN 3.1. Waktu dan tempat Penelitian Penelitian telah dilaksanakan dari bulan Agustus 2006 sampai Juli 2007, bertempat di Laboratorium Bioteknologi Hasil Perairan Departemen Teknologi
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN A. Jenis Penelitian Jenis penelitian yang digunakan adalah penelitian dasar dengan metode deskriptif (Nazir, 1983). B. Populasi dan Sampel Populasi dalam penelitian ini adalah
BAB III METODE PENELITIAN A. Jenis Penelitian Jenis penelitian yang digunakan adalah penelitian dasar dengan metode deskriptif (Nazir, 1983). B. Populasi dan Sampel Populasi dalam penelitian ini adalah
HASIL DAN PEMBAHASAN Isolasi DNA Genomik Sengon
 HASIL DAN PEMBAHASAN Isolasi DNA Genomik Sengon DNA genomik sengon diisolasi dari daun muda pohon sengon. Hasil uji integritas DNA metode 1, metode 2 dan metode 3 pada gel agarose dapat dilihat pada Gambar
HASIL DAN PEMBAHASAN Isolasi DNA Genomik Sengon DNA genomik sengon diisolasi dari daun muda pohon sengon. Hasil uji integritas DNA metode 1, metode 2 dan metode 3 pada gel agarose dapat dilihat pada Gambar
HASIL DAN PEMBAHASAN
 HASIL DAN PEMBAHASAN Pengujian Serum dan Kuning Telur Hasil AGPT memperlihatkan pembentukan garis presipitasi yang berwarna putih pada pengujian serum dan kuning telur tiga dari sepuluh ekor ayam yang
HASIL DAN PEMBAHASAN Pengujian Serum dan Kuning Telur Hasil AGPT memperlihatkan pembentukan garis presipitasi yang berwarna putih pada pengujian serum dan kuning telur tiga dari sepuluh ekor ayam yang
I. PENDAHULUAN. protein dalam jumlah besar (Reece dkk., 2011). kompeten biasanya dibuat dari inokulum awal dengan konsentrasi 2% ( v / v )
 I. PENDAHULUAN A. Latar Belakang Penelitian Plasmid merupakan molekul DNA berukuran relatif kecil, melingkar, dan beruntai ganda. Plasmid membawa gen-gen yang terpisah dari kromosom bakteri. Plasmid digunakan
I. PENDAHULUAN A. Latar Belakang Penelitian Plasmid merupakan molekul DNA berukuran relatif kecil, melingkar, dan beruntai ganda. Plasmid membawa gen-gen yang terpisah dari kromosom bakteri. Plasmid digunakan
1 0,53 0,59 2 0,3 0,2 3 0,02 0,02 4 0,04 0,04 5 0,3 0,3 Ilustrasi rangkaian isolasi DNA tersebut dapat dilihat pada Gambar 1 berikut.
 PERBANDINGAN BEBERAPA METODE ISOLASI DNA UNTUK PENENTUAN KUALITAS LARUTAN DNA TANAMAN SINGKONG (Manihot esculentum L.) Molekul DNA dalam suatu sel dapat diekstraksi atau diisolasi untuk berbagai macam
PERBANDINGAN BEBERAPA METODE ISOLASI DNA UNTUK PENENTUAN KUALITAS LARUTAN DNA TANAMAN SINGKONG (Manihot esculentum L.) Molekul DNA dalam suatu sel dapat diekstraksi atau diisolasi untuk berbagai macam
Lampiran 1 Prosedur uji aktivitas protease (Walter 1984, modifikasi)
 76 Lampiran Prosedur uji aktivitas protease (Walter 984, modifikasi) Pereaksi Blanko (ml) Standard (ml) Contoh ml) Penyangga TrisHCl (.2 M) ph 7. Substrat Kasein % Enzim ekstrak kasar Akuades steril Tirosin
76 Lampiran Prosedur uji aktivitas protease (Walter 984, modifikasi) Pereaksi Blanko (ml) Standard (ml) Contoh ml) Penyangga TrisHCl (.2 M) ph 7. Substrat Kasein % Enzim ekstrak kasar Akuades steril Tirosin
BAB III METODE PENELITIAN. dengan mengadakan manipulasi terhadap objek penelitian serta adanya kontrol
 24 BAB III METODE PENELITIAN A. Jenis Penelitian Penelitian yang dilakukan termasuk penelitian dasar dengan metode penelitian eksperimen. Penelitian eksperimen adalah penelitian yang dilakukan dengan mengadakan
24 BAB III METODE PENELITIAN A. Jenis Penelitian Penelitian yang dilakukan termasuk penelitian dasar dengan metode penelitian eksperimen. Penelitian eksperimen adalah penelitian yang dilakukan dengan mengadakan
III. METODE PENELITIAN. Penelitian ini dilakukan pada bulan Januari 2015 Juli 2015, bertempat di
 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan Januari 2015 Juli 2015, bertempat di Laboratorium Kimia Organik, Jurusan Kimia, Fakultas Matematika dan Ilmu Pengetahuan
III. METODE PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan Januari 2015 Juli 2015, bertempat di Laboratorium Kimia Organik, Jurusan Kimia, Fakultas Matematika dan Ilmu Pengetahuan
DEPARTEMEN BIOLOGI FMIPA USU LAMPIRAN
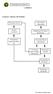 LAMPIRAN Lampiran 1. Diagram Alir Penelitian Peremajaan Bacillus Isolasi Bakteri Oportunistik Produksi Antimikrob Penghitungan Sel Bakteri Oportunistik Pengambilan Supernatan Bebas Sel Pemurnian Bakteri
LAMPIRAN Lampiran 1. Diagram Alir Penelitian Peremajaan Bacillus Isolasi Bakteri Oportunistik Produksi Antimikrob Penghitungan Sel Bakteri Oportunistik Pengambilan Supernatan Bebas Sel Pemurnian Bakteri
Bab IV Hasil dan Pembahasan
 32 Bab IV Hasil dan Pembahasan Penggunaan α-amilase dalam beberapa sektor industri mengalami peningkatan dan sekarang ini banyak diperlukan α-amilase dengan sifat yang khas dan mempunyai kemampuan untuk
32 Bab IV Hasil dan Pembahasan Penggunaan α-amilase dalam beberapa sektor industri mengalami peningkatan dan sekarang ini banyak diperlukan α-amilase dengan sifat yang khas dan mempunyai kemampuan untuk
HASIL DAN PEMBAHASAN
 19 HASIL DAN PEMBAHASAN Vektor Kloning Protein rgh Isolasi Plasmid cdna GH. Plasmid pgem-t Easy yang mengandung cdna; El-mGH, Og-mGH dan Cc-mGH berhasil diisolasi dari bakteri konstruksi E. coli DH5α dengan
19 HASIL DAN PEMBAHASAN Vektor Kloning Protein rgh Isolasi Plasmid cdna GH. Plasmid pgem-t Easy yang mengandung cdna; El-mGH, Og-mGH dan Cc-mGH berhasil diisolasi dari bakteri konstruksi E. coli DH5α dengan
TESIS. Karya tulis sebagai salah satu syarat untuk memperoleh gelar Magister dari Institut Teknologi Bandung RATIH ASMANA NINGRUM
 KLONING DAERAH PENGKODE INTERFERON ALFA-2B (IFNα2b) SINTETIK PADA Escherichia coli, OVERPRODUKSI, PURIFIKASI, DAN KARAKTERISASI PROTEIN REKOMBINAN IFNα2b TESIS Karya tulis sebagai salah satu syarat untuk
KLONING DAERAH PENGKODE INTERFERON ALFA-2B (IFNα2b) SINTETIK PADA Escherichia coli, OVERPRODUKSI, PURIFIKASI, DAN KARAKTERISASI PROTEIN REKOMBINAN IFNα2b TESIS Karya tulis sebagai salah satu syarat untuk
II. MATERI DAN METODE PENELITIAN. 1. Materi Penelitian, Lokasi dan Waktu Penelitian
 II. MATERI DAN METODE PENELITIAN 1. Materi Penelitian, Lokasi dan Waktu Penelitian 1.1. Materi Penelitian 1.1.1. Alat Alat yang digunakan adalah akuarium berukuran 40 X 60 X 60 cm 3 dan ketinggian air
II. MATERI DAN METODE PENELITIAN 1. Materi Penelitian, Lokasi dan Waktu Penelitian 1.1. Materi Penelitian 1.1.1. Alat Alat yang digunakan adalah akuarium berukuran 40 X 60 X 60 cm 3 dan ketinggian air
HASIL DAN PEMBAHASAN. Hasil konfirmasi dicek dengan elektroforesis gel agarosa 1%.
 reaction mix pada tabung mikro, kemudian program PCR dilanjutkan kembali dengan program PCR biasa: 94 o C selama 30 detik, 55 o C selama 1 menit, dan 72 o C selama 2 menit. Hasil konfirmasi dicek dengan
reaction mix pada tabung mikro, kemudian program PCR dilanjutkan kembali dengan program PCR biasa: 94 o C selama 30 detik, 55 o C selama 1 menit, dan 72 o C selama 2 menit. Hasil konfirmasi dicek dengan
Lampiran A : Komposisi Media MS
 Lampiran A : Komposisi Media MS Komposisi Media MS (Murashige & Skoog, 1962) Bahan Kimia Konsentrasi dalam mesia (mg/l) Makro Nutrient NH 4 NO 3 1650,000 KNO 3 1900,000 CaCl 2.H 2 O 440,000 MgSO 4.7H 2
Lampiran A : Komposisi Media MS Komposisi Media MS (Murashige & Skoog, 1962) Bahan Kimia Konsentrasi dalam mesia (mg/l) Makro Nutrient NH 4 NO 3 1650,000 KNO 3 1900,000 CaCl 2.H 2 O 440,000 MgSO 4.7H 2
METODOLOGI PENELITIAN. Tempat dan Waktu Penelitian. Bahan dan Alat Penelitian
 14 METODOLOGI PENELITIAN Tempat dan Waktu Penelitian Tempat penelitian dilakukan di Laboratorium Unit Pelayanan Mikrobiologi Terpadu, Bagian Mikrobiologi Kesehatan, Departemen Ilmu Penyakit Hewan dan Kesehatan
14 METODOLOGI PENELITIAN Tempat dan Waktu Penelitian Tempat penelitian dilakukan di Laboratorium Unit Pelayanan Mikrobiologi Terpadu, Bagian Mikrobiologi Kesehatan, Departemen Ilmu Penyakit Hewan dan Kesehatan
III. METODE PENELITIAN. Penelitian dilaksanakan pada Desember 2014 Mei 2015 di. Laboratorium Mikrobiologi FMIPA Universitas Lampung.
 19 III. METODE PENELITIAN 3.1. Waktu dan Tempat Penelitian Penelitian dilaksanakan pada Desember 2014 Mei 2015 di Laboratorium Mikrobiologi FMIPA Universitas Lampung. 3.2. Alat dan Bahan Alat yang digunakan
19 III. METODE PENELITIAN 3.1. Waktu dan Tempat Penelitian Penelitian dilaksanakan pada Desember 2014 Mei 2015 di Laboratorium Mikrobiologi FMIPA Universitas Lampung. 3.2. Alat dan Bahan Alat yang digunakan
HASIL. Tabel 1 Perbandingan berat abomasum, fundus, dan mukosa fundus dari domba di atas dan di bawah satu tahun
 HASIL Ekstraksi Rennet dari Abomasum Domba di Atas dan di Bawah Satu Tahun Perbandingan antara berat abomasum, fundus, dan mukosa daerah kelejar fundus dapat dilihat seperti disajikan pada Tabel 1. Tabel
HASIL Ekstraksi Rennet dari Abomasum Domba di Atas dan di Bawah Satu Tahun Perbandingan antara berat abomasum, fundus, dan mukosa daerah kelejar fundus dapat dilihat seperti disajikan pada Tabel 1. Tabel
III. Bahan dan Metode
 III. Bahan dan Metode A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan selama 3 bulan dari bulan Mei-Juli 2011 yang dilakukan di LPPT UGM Yogyakarta. B. Bahan Penelitian Sampel yang digunakan
III. Bahan dan Metode A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan selama 3 bulan dari bulan Mei-Juli 2011 yang dilakukan di LPPT UGM Yogyakarta. B. Bahan Penelitian Sampel yang digunakan
METODE PENELITIAN. Metode Penelitian
 METODE PENELITIAN Waktu dan Tempat Penelitian Penelitian ini dilakukan selama 6 bulan, mulai Maret 2010 sampai dengan Agustus 2010 di laboratorium Terpadu Bagian Mikrobiologi Medik dan laboratorium Bakteriologi
METODE PENELITIAN Waktu dan Tempat Penelitian Penelitian ini dilakukan selama 6 bulan, mulai Maret 2010 sampai dengan Agustus 2010 di laboratorium Terpadu Bagian Mikrobiologi Medik dan laboratorium Bakteriologi
BAB III METODE PENELITIAN. Pendidikan Biologi FPMIPA UPI dan protease Bacillus pumilus yang diperoleh
 31 BAB III METODE PENELITIAN 3.1. Objek Dan Lokasi Penelitian Objek atau bahan penelitian yang digunakan dalam penelitian ini adalah proteas Bacillus subtilis diperoleh dari laboratorium Mikrobiologi Jurusan
31 BAB III METODE PENELITIAN 3.1. Objek Dan Lokasi Penelitian Objek atau bahan penelitian yang digunakan dalam penelitian ini adalah proteas Bacillus subtilis diperoleh dari laboratorium Mikrobiologi Jurusan
LAMPIRAN. Lampiran 1. Deskripsi Pembuatan Larutan Stok dan Buffer
 LAMPIRAN Lampiran 1. Deskripsi Pembuatan Larutan Stok dan Buffer 1. Pembuatan Larutan Stok a. CTAB 5 % Larutan dibuat dengan melarutkan : - NaCl : 2.0 gr - CTAB : 5.0 gr - Aquades : 100 ml b. Tris HCl
LAMPIRAN Lampiran 1. Deskripsi Pembuatan Larutan Stok dan Buffer 1. Pembuatan Larutan Stok a. CTAB 5 % Larutan dibuat dengan melarutkan : - NaCl : 2.0 gr - CTAB : 5.0 gr - Aquades : 100 ml b. Tris HCl
