Purifikasi Protein Fusi MBP-Mga Streptococcus pyogenes Hasil Ekspresi Heterolog di Escherichia coli
|
|
|
- Irwan Sumadi
- 7 tahun lalu
- Tontonan:
Transkripsi
1 Jurnal Matematika dan Sains Vol. 1 No. 1, Maret 25, hal Purifikasi Protein Fusi MBP-Mga Streptococcus pyogenes Hasil Ekspresi Heterolog di Escherichia coli Muhaimin 1), Oei Ban Liang 2,4), Enny Ratnaningsih 2,4), Endang Purwantini 3,4) dan Debbie Sofie Retnoningrum 3,4) 1) Staf PengajarJurusan Kimia-FKIP Universitas Jambi 2) Staf PengajarJurusan Kimia-FMIPA Institut Teknologi Bandung 3) Staf PengajarJurusan Farmasi-FMIPA Institut Teknologi Bandung 4) Staf Peneliti Pusat Penelitian Antar Universitas Bioteknologi ITB Abstrak Diterima Nopember 24, disetujui untuk dipublikasikan Pebruari 25 Telah dilakukan optimasi proses pemurnian protein fusi MBP-Mga Streptococcus pyogenes dari Escherichia coli pmalmga rekombinan yang mengandung gen mga49. Pemurnian dilakukan menggunakan kolom kromatografi afinitas dengan ligan amilosa. Analisis SDS-PAGE menghasilkan pita tunggal pada ukuran 14 kda menunjukkan protein fusi MBP-Mga murni. Kata kunci : Streptococcus pyogenes, gen mga49, protein fusi MBP-Mga Abstract Optimization of purification process of Streptococcus pyogenes s MBP-Mga fusion protein from Escherichia coli pmalmga carrying mga49 gene had been carried out. The purification was conducted by using affinity chromatography column with amylose ligands. SDS-PAGE analysis gave a band at 14 kda showing a pure MBP- Mga fusion protein. Key words : Streptococcus pyogenes, mga49 gene, MBP-Mga fusion protein 1. Pendahuluan Pemurnian enzim atau protein menggunakan teknik kromatografi afinitas pada saat ini sangat populer dan menjadi pilihan utama. Pemurnian ini dilakukan berdasarkan afinitas enzim atau protein terhadap biomolekul lain (ligan), misalnya enzim terhadap inhibitor, substrat atau produknya, afinitas antibodi terhadap antigennya, atau afinitas hormon terhadap reseptornya 1,2,3). Pemurnian dengan teknik kromatografi afinitas disebut pemurnian satu tahap (one step purification). Prinsip kromatografi afinitas adalah pengikatan spesifik ligan dengan reseptor. Jadi, dalam kromatografi afinitas minimum harus ada dua senyawa yang berikatan spesifik 2). Dalam proses pemurnian satu tahap menggunakan kromatografi afinitas diperlukan interaksi spesifik antara protein rekombinan dengan suatu ligan. Keterbatasan metode ini adalah protein rekombinan yang akan dimurnikan harus berinteraksi secara spesifik dengan suatu ligan. Jadi, jika tidak diketahui ligan yang dapat berinteraksi secara spesifik maka tidak dapat dilakukan pemurnian satu tahap. Keterbatasan ini sekarang dapat diatasi dengan adanya teknologi fusi protein 3). Idenya adalah membuat suatu protein fusi yang terdiri dari protein yang akan dimurnikan dengan protein yang diketahui dapat berikatan spesifik dengan ligan tertentu. Pemurnian protein Mga yang dilakukan selama ini melalui banyak tahap, sehingga proses 31 pemurnian tidak efisien. Protein Mga merupakan biomolekul yang dapat dimurnikan dengan kromatografi afinitas, sebab teknik ini dapat digunakan untuk secara spesifik memisahkan biomolekul tertentu dari bahan biologis yang merupakan campuran kompleks, yang biasanya tidak mudah untuk dipisahkan dengan menggunakan metode-metode lain 3). Pemurnian protein Mga menggunakan teknik kromatografi afinitas secara langsung tidak dapat dilakukan karena protein Mga ini tidak mempunyai ligan spesifik yang dapat mengikatnya. Dengan teknologi fusi protein dibuat protein fusi MBP-Mga yang terdiri dari protein Mga dan protein MBP yang diketahui dapat berikatan spesifik dengan maltosa 4,5). Pembuatan protein fusi dilakukan pada tingkat DNA, dengan menggabungkan gen mga49 dan male 6,7). Tulisan ini melaporkan tentang cara memurnikan protein fusi MBP-Mga dengan teknik kromatografi afinitas. Tahap-tahap yang dilakukan meliputi tahap overproduksi protein MBP-Mga S. pyogenes dari E. coli pmalmga rekombinan, pemurnian protein fusi MBP-Mga dengan kromatografi afinitas, dan dilanjutkan karakterisasi dengan SDS-PAGE. 2. Metode Penelitian 2.1. Overekspresi gen mga49 dalam E. coli (pmalmga)
2 32 JMS Vol. 1 No. 1, Maret 25 Bakteri E. coli yang mengandung plasmid pmalmga ditanam dalam medium LB (tripton 1% b/v, ekstrak ragi,5% b/v, NaCl 1% b/v dalam aquades) cair yang mengandung glukosa,2% b/v. Untuk overproduksi protein fusi MBP-Mga rekombinan, maka dilakukan induksi dengan penambahan,3 mm IPTG (Isopropil-β-Dtiogalaktosida) selama 2 jam. Sel dipanen dengan cara sentrifugasi, kemudian ditambah bufer sodiumtris-etilendiamintetraasetat (NaCl 5 M, EDTA,5 M, Tris-HCl 1 M), diresuspensi dan disentrifugasi kembali sebanyak dua kali. Pelet sel dilisis dengan sonikator, dan protein dipisahkan dari debris sel dengan cara sentrifugasi pada kecepatan tinggi. Protein yang diambil adalah protein yang berada dalam supernatan Pemurnian Protein Fusi MBP-Mga Pemurnian protein fusi MBP-Mga dilakukan dengan kromatografi afinitas menggunakan kolom resin amilosa. Protein Mga yang dihasilkan sebagai protein fusi dengan pengikat maltosa dimasukkan ke dalam kolom amilosa dan diinkubasi selama 1-2 jam. Hal ini bertujuan agar protein fusi dapat menempel pada ligan. Kolom kemudian dicuci dengan bufer (Tris.Cl 2 mm ph 7,4, NaCl,2 M, 2- merkaptoetanol 1 mm, dan EDTA 1 mm) sebanyak 5 X volume kolom dan 1 X volume kolom, untuk menghilangkan kontaminan. Selanjutnya protein dilepaskan dari ligan dengan mengalirkan bufer elusi (Tris.Cl 2 mm ph 7,4, NaCl,2 M, 2- merkaptoetanol 1 mm, EDTA 1 mm, dan maltosa 1 mm) ke dalam kolom. Setiap 1,5 ml hasil elusi ditampung sebagai fraksi-fraksi yang diamati dengan spektrofotometer UV-Vis pada panjang gelombang 28 nm Karakterisasi protein dengan elektroforesis SDS-PAGE SDS PAGE yang digunakan adalah didasarkan atas sistem Laemmli 3). SDS PAGE sistem Laemmli dilakukan dengan memakai empat komponen utama yaitu bufer elektroforesis, bufer sampel, separating gel dan stacking gel 3). Pada penelitian ini yang digunakan adalah separating gel 12% (b/v), komposisinya adalah 2,5 ml Tris-HCl 1,5 M ph 8,8, 1 µl SDS 1% (b/v), 4 ml larutan akrilamid/bis-akrilamid stock 3% b/v, 5 µl amonium persulfat 1% (b/v), 5 µl TEMED, dan 3,35 ml akuades. Stacking gel 4,% (b/v), komposisinya adalah 2,5 ml Tris-HCl,5 M ph 6,8, 1 µl SDS 1% (b/v), 1,33 ml larutan akrilamid/bis-akrilamid stock 3% b/v, 5 µl amonium persulfat 1% (b/v), 1 µl TEMED, dan 6,1 ml akuades. Separating gel 12% (b/v) sebanyak 1 ml dimasukkan ke dalam alat pencetak lempengan gel dari Mini Protean II Bio Rad pada bagian bawah, setelah separating gel mengeras dimasukkan stacking gel 4,% (b/v) sebanyak 2 ml di atas separating gel, lalu pada stacking gel yang masih cair dimasukkan sisir untuk membuat sumur. Sumur-sumur ini digunakan untuk memasukkan sampel protein yang akan dikarakterisasi pada gel. Gel yang telah dipersiapkan dimasukkan ke dalam alat elektroforesis. Kemudian bufer elektroforesis di masukkan dalam tangki. Larutan sampel dengan jumlah protein MBP-Mga sekitar 2 µg dicampur dengan 1 µl bufer sampel, dididihkan selama 5 menit untuk mendenaturasi protein dan didinginkan pada suhu kamar. Campuran ini dan protein penanda ukuran dimasukkan ke sumur-sumur gel pada alat elektroforesis sebanyak maksimum 2 µl. Elektroforesis dilakukan pada tegangan konstan 2 Volt selama 6 menit. Gel hasil elektroforesis diwarnai dengan larutan pewarna (staining). Gel hasil elektroforesis yang telah diwarnai dimasukkan ke dalam larutan destaining untuk menghilangkan warna pada gel yang tidak mengandung pita protein. Pita pada gel hasil elektroforesis tersebut didokumentasikan. 3. Hasil dan Diskusi Pemurnian protein ekstrak kasar dari E. coli pmalmga yang mengandung protein fusi MBP-Mga dilakukan beberapa kali untuk menentukan kondisi optimum dalam mendapatkan protein murni. Protein fusi MBP-Mga hasil overekspresi dimurnikan menggunakan teknik kromatografi afinitas dengan kolom resin amilosa. Penggunaan amilosa sebagai ligan dimungkinkan karena maltose binding protein (MBP) mampu berikatan secara spesifik dengan maltosa sebagai dimer pada amilosa. Pemurnian ini dilakukan pada kondisi ph 7,4, dengan bufer pencuci (Tris.Cl 2 mm ph 7,4, NaCl,2 M, 2- merkaptoetanol 1 mm, dan EDTA 1 mm) dan bufer pengelusi (Tris.Cl 2 mm ph 7,4, NaCl,2 M, 2- merkaptoetanol 1 mm, EDTA 1 mm, dan maltosa 1 mm). Pemurnian terhadap protein ekstrak kasar E. coli pmalmga hasil overekspresi dilakukan masingmasing 4 kali pengulangan untuk yang dicuci dengan bufer pencuci 1X volume kolom dan 4 kali pengulangan untuk yang dicuci dengan bufer pencuci 5X volume kolom. Dalam setiap proses pemurnian, setelah dicuci dengan bufer pencuci dilanjutkan dengan elusi menggunakan bufer pengelusi untuk mendapatkan protein fusi MBP-Mga murni. Pada penelitian ini bufer pengelusi mengandung maltosa. Maltosa ini berfungsi untuk memutuskan ikatan antara protein fusi MBP-Mga dengan amilosa. Jadi, maltosa ini dapat berkompetisi tempat dengan ligan terikat (amilosa), sehingga protein fusi MBP-Mga lepas dan selanjutnya keluar bersama eluen. Eluen hasil elusi ini ditampung sebagai fraksi-fraksi. yang diambil setiap kali pemurnian adalah 1 fraksi, dengan volume tiap fraksi adalah 1,5 ml. hasil elusi dimonitor dengan pengamatan absorbansi pada panjang gelombang 28 nm 3). Hasil pengukuran serapan fraksi-fraksi protein MBP-Mga hasil pemurnian dengan kolom resin amilosa yang
3 JMS Vol. 1 No. 1, Maret sebelumnya dicuci dengan bufer pencuci 1X volume kolom untuk 4 kali pengulangan ditunjukkan pada Gambar 1. Gambar 1.a adalah serapan fraksifraksi protein MBP-Mga hasil pemurnian dari 3 ml protein ekstrak kasar E. coli pmalmga (1,897 µg/ml); Gambar 1.b adalah serapan fraksi-fraksi protein MBP-Mga hasil pemurnian dari 3 ml protein ekstrak kasar E. coli pmalmga (1,89 µg/ml); Gambar 1.c adalah serapan fraksi-fraksi protein MBP-Mga hasil pemurnian dari 3 ml protein ekstrak kasar E. coli pmalmga (1,91 µg/ml); dan Gambar 1.d adalah serapan fraksi-fraksi protein MBP-Mga hasil pemurnian dari 3 ml protein ekstrak kasar E. coli pmalmga (1,898 µg/ml). Serapan (λ = 28 nm),3,2 5,285,231, Frak s i Serapan (λ = 28 nm),45,4,35,3,2 5,395,231, Frak s i (a) (b) Serapan (λ = 28 nm),45,4,35,3,2 5,381,213, Serapan (λ = 28 nm),45,4,35,3,2 5,385,276, Frak s i (c) (d) Gambar 1. Pengukuran serapan fraksi-fraksi protein fusi MBP-Mga pada panjang gelombang 28 nm, hasil pemurnian dengan kolom resin amilosa (dicuci dengan bufer pencuci 1X volume kolom) (a) Serapan fraksi-fraksi protein MBP-Mga hasil pemurnian dari 3 ml protein ekstrak kasar E. coli pmalmga (1,897 µg/ml); (b) Serapan fraksi-fraksi protein MBP-Mga hasil pemurnian dari 3 ml protein ekstrak kasar E. coli pmalmga (1,89 µg/ml); (c) Serapan fraksi-fraksi protein MBP-Mga hasil pemurnian dari 3 ml protein ekstrak kasar E. coli pmalmga (1,91 µg/ml); dan (d) Serapan fraksi-fraksi protein MBP-Mga hasil pemurnian dari 3 ml protein ekstrak kasar E. coli pmalmga (1,898 µg/ml). Hasil pengukuran serapan fraksi-fraksi protein MBP- Mga hasil pemurnian dengan kolom resin amilosa yang sebelumnya dicuci dengan bufer pencuci 5X volume kolom untuk 4 kali pengulangan ditunjukkan pada Gambar 2. Gambar 2.a adalah serapan fraksifraksi protein MBP-Mga hasil pemurnian dari 3 ml protein ekstrak kasar E. coli pmalmga (1,897 µg/ml); Gambar 2.b adalah serapan fraksi-fraksi protein MBP-Mga hasil pemurnian dari 3 ml protein ekstrak kasar E. coli pmalmga (1,89 µg/ml); Gambar 2.c adalah serapan fraksi-fraksi protein MBP-Mga hasil pemurnian dari 3 ml protein ekstrak kasar E. coli pmalmga (1,91 µg/ml); dan Gambar 2.d adalah serapan fraksi-fraksi protein MBP-Mga hasil pemurnian dari 3 ml protein ekstrak kasar E. coli pmalmga (1,898 µg/ml).
4 34 JMS Vol. 1 No. 1, Maret 25 Serapan (λ = 28 nm),4,35,3,2 5,357,316, Serapan (λ = 28 nm),4,35,3,2 5,376,244, (a) (b),45,4,385,4,35,366 Serapan (λ = 28 nm),35,3,2 5,224, Serapan (λ = 28 nm),3,2 5, (c) (d) Gambar 2. Pengukuran serapan fraksi-fraksi protein fusi MBP-Mga pada panjang gelombang 28 nm, hasil pemurnian dengan kolom resin amilosa (dicuci dengan bufer pencuci 5X volume kolom) (a) Serapan fraksi-fraksi protein MBP-Mga hasil pemurnian dari 3 ml protein ekstrak kasar E. coli pmalmga (1,897 µg/ml); (b) Serapan fraksi-fraksi protein MBP-Mga hasil pemurnian dari 3 ml protein ekstrak kasar E. coli pmalmga (1,89 µg/ml); (c) Serapan fraksi-fraksi protein MBP-Mga hasil pemurnian dari 3 ml protein ekstrak kasar E. coli pmalmga (1,91 µg/ml); dan (d) Serapan fraksi-fraksi protein MBP-Mga hasil pemurnian dari 3 ml protein ekstrak kasar E. coli pmalmga (1,898 µg/ml). Protein fusi MBP-Mga hasil pemurnian yang dicuci dengan bufer pencuci 1X volume kolom terdapat pada fraksi ketiga sampai kelima, sedangkan protein fusi MBP-Mga hasil pemurnian yang dicuci dengan bufer pencuci 5X volume kolom terdapat pada fraksi ketiga sampai ketujuh. Munculnya puncak pada grafik serapan fraksi-fraksi protein fusi MBP-Mga hasil pemurnian tergantung pada bufer pengelusi. Jika bufer pengelusi kurang kuat untuk memutuskan ikatan antara ligan (amilosa) dengan protein fusi MBP-Mga, maka akan terjadi tailing, yaitu puncak yang melebar 5. Selain itu, volume matriks juga mempengaruhi lebarnya puncak, karena ligan yang ada semakin banyak. Jadi, semakin besar volume matriks semakin lebar puncak serapan, sehingga protein MBP-Mga yang dihasilkan lebih banyak. Dari data hasil penelitian, diketahui bahwa pemurnian protein fusi MBP-Mga dengan teknik kromatografi afinitas menggunakan kolom resin amilosa memberikan hasil yang reprodusibel. Analisis SDS-PAGE dilakukan untuk melihat hasil pemurnian dengan kolom resin amilosa. Protein yang digunakan sebagai pembanding terhadap protein MBP-Mga murni hasil pemurnian adalah protein marker, dan protein ekstrak kasar E. coli pmalmga yang diinduksi selama 2 jam dengan IPTG,3 mm dalam medium LB yang mengandung,2% glukosa. Elektroforegram sampel protein fusi MBP-Mga hasil pemurnian memberikan satu pita dengan massa molekul relatif sekitar 14 kda, untuk yang dicuci dengan bufer pencuci 1X volume kolom (Gambar 3.b jalur 3). Sedangkan untuk yang dicuci dengan bufer pencuci 5X volume kolom masih ada sedikit kontaminan (Gambar 3.a jalur 1).
5 JMS Vol. 1 No. 1, Maret Gambar 3.b jalur 3 menunjukkan bahwa protein fusi MBP-Mga yang diperoleh melalui pemurnian dengan teknik kromatografi afinitas cukup murni, karena memberikan satu pita pada 14 kda. 14 kda kda 116,3 kda 97,4 kda 66,3 kda 55,4 kda 14 kda 36,3 kda (a) 31, kda (b) Gambar 3. Elektroforegram protein fusi MBP-Mga yang dicuci dengan bufer pencuci 5X volume kolom (a), Elektro foregram protein fusi MBP-Mga yang dicuci dengan bufer pencuci 1X volume kolom (b). (a) 1 = Protein fusi MBP-Mga hasil pemurnian; 2 = Protein ekstrak kasar E. coli pmalmga yang diinduksi selama 2 jam dengan IPTG dalam medium LB +,2 % Glukosa; 3 = Protein marker, dan (b) 1 = Protein marker; 2 = Protein ekstrak kasar E. coli pmalmga yang diinduksi selama 2 jam dengan IPTG dalam medium LB +,2 % Glukosa; 3 = Protein fusi MBP-Mga hasil pemurnian. Perbandingan kadar protein ekstrak kasar E. coli pmalmga dan protein MBP-Mga murni hasil pemurnian yang menggunakan bufer pencuci 1X dan 5X volume kolom, dapat dilihat pada Tabel 1. Ternyata hasil pemurnian protein fusi MBP-Mga yang dicuci dengan bufer pencuci 1X dan 5X volume kolom memberikan kadar yang hampir sama, tetapi pemurnian protein fusi MBP-Mga yang dicuci dengan bufer pencuci 1X volume kolom memberikan hasil yang lebih murni, karena pada elektroforegram memberikan satu pita dengan massa molekul relatif sekitar 14 kda (Gambar 3.b jalur 3). Protein Mga yang difusikan dengan protein MBP terdiri dari 533 asam amino dan pi 5,88 8). Tabel 1. Protein MBP-Mga hasil pemurnian setelah dicuci dengan bufer pencuci 1X dan 5X volume kolom Protein Kasar E. coli pmalmga (µg/ml) Protein MBP- Mga murni [bufer pencuci 1X volume kolom] (µg/ml) Protein MBP- Mga murni [bufer pencuci 5X volume kolom] (µg/ml) Kesimpulan Protein fusi MBP-Mga telah berhasil dimurnikan menggunakan kromatografi afinitas dengan kolom resin amilosa pada kondisi ph 7,4 dengan bufer pencuci (Tris.Cl 2 mm ph 7,4, NaCl,2 M, 2-merkaptoetanol 1 mm, dan EDTA 1 mm) dan bufer pengelusi (Tris.Cl 2 mm ph 7,4, NaCl,2 M, 2-merkaptoetanol 1 mm, EDTA 1 mm, dan maltosa 1 mm). Proses pemurnian untuk protein fusi MBP-Mga yang dicuci dengan bufer pencuci 1X volume kolom memberikan hasil terbaik, hal ini dibuktikan oleh data analisis SDS-PAGE terhadap protein fusi MBP-Mga menunjukkan adanya pita tunggal dengan massa molekul relatif sekitar 14 kda. Daftar Pustaka 1. Simmonds, R.J., Chemistry of Biomoleculer : An Introduction, Royal Society of Chemistry, Cambridge, (1992). 2. Hermanson, G.T., Mallia, A.K., & Smith, P.K., Immobilized Affinity Ligand Techniques, Academic Press, San Diego, (1992). 3. Deutscher, M.P., Method of Enzymology, Guide to Protein Purification, Academic Press, Inc., San Diego, (199). 4. Kellerman, O.K., & Ferenci, T., Maltose Binding Protein from E. coli, Methods Enzymol., 9:1, 459 (1982). 5. Duplay, P., Bedouelle, H., & Fowler, A., Sequences of The male Gene and of Its Product, The Maltose Binding Protein of
6 36 JMS Vol. 1 No. 1, Maret 25 Escherichia coli, J. Biol. Chem., 259:1, 166 (1984). 6. Guan, C., Vectors that Facilitate the Expression and Purification of Foreign Peptides in E. coli by Fusion to Maltose Binding Protein, Gene, 67:1, 21 (1987), 7. Rhicharme, G., Associative Properties of The Escherichia coli Galactose Binding Protein and Maltose Binding Protein, Biochem. Biophys. Res. Comm., 15:1, 476 (1982). 8. McIver, K.S., Thurman, A.S., & Scott, J.R., Regulation of mga Transcription in the Group A Streptococcus: Spesific Binding of Mga within Its Own Promoter and Evidence for a Negative Regulator, J. Bacteriol., 181:17, 5373 (1999).
Optimasi Proses Overproduksi, Pemurnian dan Karakterisasi Protein Mga Sebagai Molekul Target Untuk Pencegahan Infeksi oleh Streptococcus Pyogenes
 Jurnal Matematika dan Sains Vol. 8 No. 3, September 23, hal 117 123 Optimasi Proses Overproduksi, Pemurnian dan Karakterisasi Protein Mga Sebagai Molekul Target Untuk Pencegahan Infeksi oleh Streptococcus
Jurnal Matematika dan Sains Vol. 8 No. 3, September 23, hal 117 123 Optimasi Proses Overproduksi, Pemurnian dan Karakterisasi Protein Mga Sebagai Molekul Target Untuk Pencegahan Infeksi oleh Streptococcus
4 HASIL DAN PEMBAHASAN
 4 HASIL DAN PEMBAHASAN 4.1 Isolasi enzim fibrinolitik Cacing tanah P. excavatus merupakan jenis cacing tanah yang agresif dan tahan akan kondisi pemeliharaan yang ekstrim. Pemeliharaan P. excavatus dilakukan
4 HASIL DAN PEMBAHASAN 4.1 Isolasi enzim fibrinolitik Cacing tanah P. excavatus merupakan jenis cacing tanah yang agresif dan tahan akan kondisi pemeliharaan yang ekstrim. Pemeliharaan P. excavatus dilakukan
4 Hasil dan Pembahasan
 4 Hasil dan Pembahasan α-amilase merupakan enzim yang mempunyai peranan penting dalam bioteknologi saat ini. Aplikasi teknis enzim ini sangat luas, seperti pada proses likuifaksi pati pada proses produksi
4 Hasil dan Pembahasan α-amilase merupakan enzim yang mempunyai peranan penting dalam bioteknologi saat ini. Aplikasi teknis enzim ini sangat luas, seperti pada proses likuifaksi pati pada proses produksi
Pengujian Inhibisi RNA Helikase Virus Hepatitis C (Utama et al. 2000) HASIL DAN PEMBAHASAN Hasil Ekspresi dan Purifikasi RNA
 8 kromatografi kemudian diuji aktivitas inhibisinya dengan metode kolorimetri ATPase assay. Beberapa fraksi yang memiliki aktivitas inhibisi yang tinggi digunakan untuk tahapan selanjutnya (Lampiran 3).
8 kromatografi kemudian diuji aktivitas inhibisinya dengan metode kolorimetri ATPase assay. Beberapa fraksi yang memiliki aktivitas inhibisi yang tinggi digunakan untuk tahapan selanjutnya (Lampiran 3).
4 Hasil dan Pembahasan
 4 Hasil dan Pembahasan α-amilase adalah enzim menghidrolisis ikatan α-1,4-glikosidik pada pati. α-amilase disekresikan oleh mikroorganisme, tanaman, dan organisme tingkat tinggi. α-amilase memiliki peranan
4 Hasil dan Pembahasan α-amilase adalah enzim menghidrolisis ikatan α-1,4-glikosidik pada pati. α-amilase disekresikan oleh mikroorganisme, tanaman, dan organisme tingkat tinggi. α-amilase memiliki peranan
BAHAN DAN METODE Tempat dan Waktu Bahan Pertumbuhan dan Peremajaan Isolat Pengamatan Morfologi Isolat B. thuringiensis
 13 BAHAN DAN METODE Tempat dan Waktu Penelitian ini dilaksanakan di Laboratorium Mikrobiologi, Departemen Biologi, IPB, dari bulan Oktober 2011 Mei 2012. Bahan Isolasi untuk memperoleh isolat B. thuringiensis
13 BAHAN DAN METODE Tempat dan Waktu Penelitian ini dilaksanakan di Laboratorium Mikrobiologi, Departemen Biologi, IPB, dari bulan Oktober 2011 Mei 2012. Bahan Isolasi untuk memperoleh isolat B. thuringiensis
Pembuatan Media Kultur Bakteri Pemanenan sel bakteri. Isolasi DNA kromosom bakteri. Kloning DNA
 LAMPIRAN 15 15 Lampiran 1 Tahapan penelitian Pembuatan Media Kultur Bakteri Pemanenan sel bakteri Isolasi DNA kromosom bakteri Pemotongan DNA dengan enzim restriksi Kloning DNA Isolasi DNA plasmid hasil
LAMPIRAN 15 15 Lampiran 1 Tahapan penelitian Pembuatan Media Kultur Bakteri Pemanenan sel bakteri Isolasi DNA kromosom bakteri Pemotongan DNA dengan enzim restriksi Kloning DNA Isolasi DNA plasmid hasil
Lampiran 1 Prosedur uji aktivitas protease (Walter 1984, modifikasi)
 76 Lampiran Prosedur uji aktivitas protease (Walter 984, modifikasi) Pereaksi Blanko (ml) Standard (ml) Contoh ml) Penyangga TrisHCl (.2 M) ph 7. Substrat Kasein % Enzim ekstrak kasar Akuades steril Tirosin
76 Lampiran Prosedur uji aktivitas protease (Walter 984, modifikasi) Pereaksi Blanko (ml) Standard (ml) Contoh ml) Penyangga TrisHCl (.2 M) ph 7. Substrat Kasein % Enzim ekstrak kasar Akuades steril Tirosin
Lampiran 1. Pembuatan Larutan Buffer untuk Dialisa Larutan buffer yang digunakan pada proses dialisa adalah larutan buffer Asetat 10 mm ph 5,4 dan
 39 Lampiran 1. Pembuatan Larutan Buffer untuk Dialisa Larutan buffer yang digunakan pada proses dialisa adalah larutan buffer Asetat 10 mm ph 5,4 dan buffer Asetat 20 mm ph 5,4. Larutan buffer asetat 10
39 Lampiran 1. Pembuatan Larutan Buffer untuk Dialisa Larutan buffer yang digunakan pada proses dialisa adalah larutan buffer Asetat 10 mm ph 5,4 dan buffer Asetat 20 mm ph 5,4. Larutan buffer asetat 10
3. METODOLOGI 3.1 Waktu dan Tempat Penelitian 3.2 Alat dan Bahan
 3. METODOLOGI 3.1 Waktu dan Tempat Penelitian Penelitian ini dimulai pada bulan Januari 2009 dan selesai pada bulan November 2009. Penelitian dilakukan di Laboratorium Biokimia dan Bioteknologi II, Departemen
3. METODOLOGI 3.1 Waktu dan Tempat Penelitian Penelitian ini dimulai pada bulan Januari 2009 dan selesai pada bulan November 2009. Penelitian dilakukan di Laboratorium Biokimia dan Bioteknologi II, Departemen
FAKULTAS BIOLOGI LABORATORIUM GENETIKA & PEMULIAAN INSTRUKSI KERJA UJI
 ISOLASI TOTAL DNA TUMBUHAN DENGAN KIT EKSTRAKSI DNA PHYTOPURE Halaman : 1 dari 5 1. RUANG LINGKUP Metode ini digunakan untuk mengisolasi DNA dari sampel jaringan tumbuhan, dapat dari daun, akar, batang,
ISOLASI TOTAL DNA TUMBUHAN DENGAN KIT EKSTRAKSI DNA PHYTOPURE Halaman : 1 dari 5 1. RUANG LINGKUP Metode ini digunakan untuk mengisolasi DNA dari sampel jaringan tumbuhan, dapat dari daun, akar, batang,
Bab IV Hasil dan Pembahasan
 Bab IV Hasil dan Pembahasan IV.1 Akar Nanas Kering dan Hidroponik Akar nanas kering yang digunakan dalam penelitian ini merupakan akar nanas yang tertanam dalam tanah, berwarna coklat dan berupa suatu
Bab IV Hasil dan Pembahasan IV.1 Akar Nanas Kering dan Hidroponik Akar nanas kering yang digunakan dalam penelitian ini merupakan akar nanas yang tertanam dalam tanah, berwarna coklat dan berupa suatu
3 METODE PENELITIAN. 3.1 Bahan Bahan penelitian
 3 METODE PENELITIAN 3.1 Bahan 3.1.1 Bahan penelitian Cacing tanah P. excavatus diperoleh dari peternakan cacing milik Ir. Bambang Sudiarto. Substrat koagulan darah diambil dari darah milik S. Krisnawati
3 METODE PENELITIAN 3.1 Bahan 3.1.1 Bahan penelitian Cacing tanah P. excavatus diperoleh dari peternakan cacing milik Ir. Bambang Sudiarto. Substrat koagulan darah diambil dari darah milik S. Krisnawati
Hasil dan Pembahasan
 27 Bab IV Hasil dan Pembahasan IV.1 Isolasi Enzim katalase dari kentang Enzim katalase terdapat dalam peroksisom, organel yang ditemukan pada jaringan tumbuhan di luar inti sel kentang sehingga untuk mengekstraknya
27 Bab IV Hasil dan Pembahasan IV.1 Isolasi Enzim katalase dari kentang Enzim katalase terdapat dalam peroksisom, organel yang ditemukan pada jaringan tumbuhan di luar inti sel kentang sehingga untuk mengekstraknya
s - soluble fraction i - insoluble fraction p - post-ni 2+ column
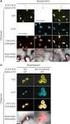 METODE SDS- PAGE Oleh: Susila Kristianingrum susila.k@uny.ac.id SDS-PAGE Trx-STS Trx-CHS s i p s i p 97 66 45 60 K 31 22 14 s - soluble fraction i - insoluble fraction p - post-ni 2+ column Langkah SDS-PAGE
METODE SDS- PAGE Oleh: Susila Kristianingrum susila.k@uny.ac.id SDS-PAGE Trx-STS Trx-CHS s i p s i p 97 66 45 60 K 31 22 14 s - soluble fraction i - insoluble fraction p - post-ni 2+ column Langkah SDS-PAGE
III. METODE PENELITIAN. Penelitian dilakukan di Laboratorium Biokimia dan Laboratorium Instrumentasi
 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian dilakukan di Laboratorium Biokimia dan Laboratorium Instrumentasi Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas
III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian dilakukan di Laboratorium Biokimia dan Laboratorium Instrumentasi Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas
3 METODE 3.1 Waktu dan Tempat 3.2 Bahan dan Alat
 16 3 METODE 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Januari hingga April 2012, dan bertempat di Laboratorium Bakteriologi dan Virologi Molekuler, Laboratorium Biorekayasa Lingkungan,
16 3 METODE 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Januari hingga April 2012, dan bertempat di Laboratorium Bakteriologi dan Virologi Molekuler, Laboratorium Biorekayasa Lingkungan,
FAKULTAS BIOLOGI LABORATORIUM GENETIKA & PEMULIAAN INSTRUKSI KERJA UJI
 Halaman : 1 dari 5 ISOLASI TOTAL DNA HEWAN DENGAN KIT EKSTRAKSI DNA 1. RUANG LINGKUP Metode ini digunakan untuk mengisolasi DNA dari sampel jaringan hewan, dapat dari insang, otot, darah atau jaringan
Halaman : 1 dari 5 ISOLASI TOTAL DNA HEWAN DENGAN KIT EKSTRAKSI DNA 1. RUANG LINGKUP Metode ini digunakan untuk mengisolasi DNA dari sampel jaringan hewan, dapat dari insang, otot, darah atau jaringan
Analisis Bobot Molekul Protein Inhibitor RNA Helikase HCV (Hairany 2010 termodifikasi) HASIL DAN PEMBAHASAN Hasil Isolasi RNA Helikase HCV
 7 diinkubasi pada suhu 37ºC selama 30 menit. Absorbansi diukur menggunakan panjang gelombang 562 nm. Standar protein yang digunakan adalah albumin serum sapi (Bovine Serum Albumin (BSA)) pada kisaran 0.05
7 diinkubasi pada suhu 37ºC selama 30 menit. Absorbansi diukur menggunakan panjang gelombang 562 nm. Standar protein yang digunakan adalah albumin serum sapi (Bovine Serum Albumin (BSA)) pada kisaran 0.05
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN A. Jenis Penelitian Penelitian ini merupakan penelitian murni yang dilakukan dengan metode deskriptif, yaitu suatu metode penelitian untuk membuat deskripsi, gambaran atau lukisan
BAB III METODE PENELITIAN A. Jenis Penelitian Penelitian ini merupakan penelitian murni yang dilakukan dengan metode deskriptif, yaitu suatu metode penelitian untuk membuat deskripsi, gambaran atau lukisan
I. Tujuan Menentukan berat molekul protein dengan fraksinasi (NH 4 ) 2 SO 4 Teori Dasar
 I. Tujuan II. Menentukan berat molekul protein dengan fraksinasi (NH 4 ) 2 SO 4 Teori Dasar Penamabahan garam pada konsentrasi rendah dapat meningkatkan kelarutan protein (salting in). tetapi protein akan
I. Tujuan II. Menentukan berat molekul protein dengan fraksinasi (NH 4 ) 2 SO 4 Teori Dasar Penamabahan garam pada konsentrasi rendah dapat meningkatkan kelarutan protein (salting in). tetapi protein akan
BAB III METODE PENELITIAN. Penelitian ini dilaksanakan pada bulan Mei sampai September 2014 di Green
 BAB III METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Mei sampai September 2014 di Green House dan Laboratorium Genetika dan Molekuler jurusan Biologi Fakultas Sains dan
BAB III METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Mei sampai September 2014 di Green House dan Laboratorium Genetika dan Molekuler jurusan Biologi Fakultas Sains dan
Lampiran 1 Data Rendemen Pelet Kapang Endofit Xylaria psidii KT30. Berat sampel (pelet) setelah sentrifugase: 0,223 gram
 LAMPIRAN 29 30 Lampiran 1 Data Rendemen Pelet Kapang Endofit Xylaria psidii KT30 1) Kultur 1 Volume kultur awal : 350 ml Volume setelah penyaringan : 300 ml ph awal sebelum ekstraksi : 4,31 Berat sampel
LAMPIRAN 29 30 Lampiran 1 Data Rendemen Pelet Kapang Endofit Xylaria psidii KT30 1) Kultur 1 Volume kultur awal : 350 ml Volume setelah penyaringan : 300 ml ph awal sebelum ekstraksi : 4,31 Berat sampel
IV. HASIL DAN PEMBAHASAN
 IV. HASIL DAN PEMBAHASAN A. Isolat Actinomycetes Amilolitik Terpilih 1. Isolat Actinomycetes Terpilih Peremajaan isolat actinomycetes dilakukan dengan tujuan sebagai pemeliharaan isolat actinomycetes agar
IV. HASIL DAN PEMBAHASAN A. Isolat Actinomycetes Amilolitik Terpilih 1. Isolat Actinomycetes Terpilih Peremajaan isolat actinomycetes dilakukan dengan tujuan sebagai pemeliharaan isolat actinomycetes agar
ADLN- PERPUSTAKAAN UNIVERSITAS AIRLANGGA DAFTAR ISI
 DAFTAR ISI Halaman Sampul Luar... i Sampul Dalam... ii Halaman Prasyarat Gelar... iii Halaman Pengesahan... iv UCAPAN TERIMA KASIH... v ABSTRAK... vi ABSTRACT... vii DAFTAR ISI... viii DAFTAR TABEL...
DAFTAR ISI Halaman Sampul Luar... i Sampul Dalam... ii Halaman Prasyarat Gelar... iii Halaman Pengesahan... iv UCAPAN TERIMA KASIH... v ABSTRAK... vi ABSTRACT... vii DAFTAR ISI... viii DAFTAR TABEL...
IV. HASIL DAN PEMBAHASAN. Enzim α-amilase dari Bacillus Subtilis ITBCCB148 diperoleh dengan
 IV. HASIL DAN PEMBAHASAN A. Isolasi Enzim α-amilase Enzim α-amilase dari Bacillus Subtilis ITBCCB148 diperoleh dengan menanam isolat bakteri dalam media inokulum selama 24 jam. Media inokulum tersebut
IV. HASIL DAN PEMBAHASAN A. Isolasi Enzim α-amilase Enzim α-amilase dari Bacillus Subtilis ITBCCB148 diperoleh dengan menanam isolat bakteri dalam media inokulum selama 24 jam. Media inokulum tersebut
Lampiran 1 Rancangan penelitian
 LAMPIRAN 18 19 Lampiran 1 Rancangan penelitian Cacing tanah E. foetida dewasa Kering oven vakum (Setiawan) Tepung cacing kering Ekstraksi buffer dan sentrifugasi Ekstrak kasar protease Salting-out dengan
LAMPIRAN 18 19 Lampiran 1 Rancangan penelitian Cacing tanah E. foetida dewasa Kering oven vakum (Setiawan) Tepung cacing kering Ekstraksi buffer dan sentrifugasi Ekstrak kasar protease Salting-out dengan
Lampiran 1 Prosedur Rotofor
 Lampiran 1 Prosedur Rotofor Kalibrasi Membran Ion Membran ion terdiri dari membran kation yang berkorelasi dengan elektrolit H 3 PO 4 0,1 N terpasang pada elektroda anoda sebagai pembawa ion positif, sedangkan
Lampiran 1 Prosedur Rotofor Kalibrasi Membran Ion Membran ion terdiri dari membran kation yang berkorelasi dengan elektrolit H 3 PO 4 0,1 N terpasang pada elektroda anoda sebagai pembawa ion positif, sedangkan
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN A. Jenis Penelitian deskriptif. Jenis penelitian yang digunakan adalah penelitian dasar dengan metode B. Objek Penelitian Objek penelitian ini adalah sampel DNA koleksi hasil
BAB III METODE PENELITIAN A. Jenis Penelitian deskriptif. Jenis penelitian yang digunakan adalah penelitian dasar dengan metode B. Objek Penelitian Objek penelitian ini adalah sampel DNA koleksi hasil
BAB III METODE PENELITIAN. Dalam penelitian ini dilakukan lima tahap utama yang meliputi tahap
 BAB III METODE PENELITIAN Dalam penelitian ini dilakukan lima tahap utama yang meliputi tahap penyiapan templat mtdna, amplifikasi fragmen mtdna pada daerah D-loop mtdna manusia dengan teknik PCR, deteksi
BAB III METODE PENELITIAN Dalam penelitian ini dilakukan lima tahap utama yang meliputi tahap penyiapan templat mtdna, amplifikasi fragmen mtdna pada daerah D-loop mtdna manusia dengan teknik PCR, deteksi
1 ml enzim + 1 ml larutan pati 1% (dalam bufer) Diinkubasi (suhu optimum, 15 menit) + 2 ml DNS. Dididihkan 5 menit. Didinginkan 5 menit
 LAMPIRAN 10 11 Lampiran 1 Skema metode Bernfeld (1955) 1 ml enzim + 1 ml larutan pati 1% (dalam bufer) Diinkubasi (suhu optimum, 15 menit) + 2 ml DNS Dididihkan 5 menit Didinginkan 5 menit Absorbansi diukur
LAMPIRAN 10 11 Lampiran 1 Skema metode Bernfeld (1955) 1 ml enzim + 1 ml larutan pati 1% (dalam bufer) Diinkubasi (suhu optimum, 15 menit) + 2 ml DNS Dididihkan 5 menit Didinginkan 5 menit Absorbansi diukur
BAB III METODE PENELITIAN. Penelitian ini merupakan penelitian eksperimental dengan 7 sampel dari 7
 BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian ini merupakan penelitian eksperimental dengan 7 sampel dari 7 individu udang Jari yang diambil dari Segara Anakan Kabupaten Cilacap Jawa Tengah.
BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian ini merupakan penelitian eksperimental dengan 7 sampel dari 7 individu udang Jari yang diambil dari Segara Anakan Kabupaten Cilacap Jawa Tengah.
HASIL DAN PEMBAHASAN. Kadar air = Ekstraksi
 2 dikeringkan pada suhu 105 C. Setelah 6 jam, sampel diambil dan didinginkan dalam eksikator, lalu ditimbang. Hal ini dilakukan beberapa kali sampai diperoleh bobot yang konstan (b). Kadar air sampel ditentukan
2 dikeringkan pada suhu 105 C. Setelah 6 jam, sampel diambil dan didinginkan dalam eksikator, lalu ditimbang. Hal ini dilakukan beberapa kali sampai diperoleh bobot yang konstan (b). Kadar air sampel ditentukan
EKSTRAKSI DNA. 13 Juni 2016
 EKSTRAKSI DNA 13 Juni 2016 Pendahuluan DNA: polimer untai ganda yg tersusun dari deoksiribonukleotida (dari basa purin atau pirimidin, gula pentosa,dan fosfat). Basa purin: A,G Basa pirimidin: C,T DNA
EKSTRAKSI DNA 13 Juni 2016 Pendahuluan DNA: polimer untai ganda yg tersusun dari deoksiribonukleotida (dari basa purin atau pirimidin, gula pentosa,dan fosfat). Basa purin: A,G Basa pirimidin: C,T DNA
HASIL DAN PEMBAHASAN
 6 Sampel yang akan diuji kemudian dimasukkan ke dalam sumuran-sumuran cawan ELISA sesuai dengan pola yang telah ditentukan. Setiap sumuran cawan berisi sebanyak 100 μl sampel. Cawan ELISA kemudian diinkubasi
6 Sampel yang akan diuji kemudian dimasukkan ke dalam sumuran-sumuran cawan ELISA sesuai dengan pola yang telah ditentukan. Setiap sumuran cawan berisi sebanyak 100 μl sampel. Cawan ELISA kemudian diinkubasi
LAPORAN PRAKTIKUM BIOKIMIA PERCOBAAN KE 2 PEMISAHAN PROTEIN PUTIH TELUR DENGAN FRAKSINASI (NH 4 ) 2 SO 4
 LAPORAN PRAKTIKUM BIOKIMIA PERCOBAAN KE 2 PEMISAHAN PROTEIN PUTIH TELUR DENGAN FRAKSINASI (NH 4 ) 2 SO 4 Disusun oleh : Ulan Darulan - 10511046 Kelompok 1 Asisten Praktikum : R. Roro Rika Damayanti (10510065)
LAPORAN PRAKTIKUM BIOKIMIA PERCOBAAN KE 2 PEMISAHAN PROTEIN PUTIH TELUR DENGAN FRAKSINASI (NH 4 ) 2 SO 4 Disusun oleh : Ulan Darulan - 10511046 Kelompok 1 Asisten Praktikum : R. Roro Rika Damayanti (10510065)
Dari uji kompetisi, persentase penghambatan dengan rasio inokulum 1:1 sudah cukup bagi Bacillus sp. Lts 40 untuk menghambat pertumbuhan V.
 27 PEMBAHASAN Dari tiga isolat sp. penghasil antimikrob yang diseleksi, isolat sp. Lts 40 memiliki aktivitas penghambatan paling besar terhadap E. coli dan V. harveyi dengan indeks penghambatan masing-masing
27 PEMBAHASAN Dari tiga isolat sp. penghasil antimikrob yang diseleksi, isolat sp. Lts 40 memiliki aktivitas penghambatan paling besar terhadap E. coli dan V. harveyi dengan indeks penghambatan masing-masing
3 Percobaan. 3.1 Tempat dan Bahan Penelitian. 3.2 Peralatan
 3 Percobaan 3.1 Tempat dan Bahan Penelitian Penelitian ini dilakukan di Laboratorium Penelitian Biokimia milik Program Studi Kimia Institut Teknologi Bandung. Ragi Saccharomyces cerevisiae yang mengandung
3 Percobaan 3.1 Tempat dan Bahan Penelitian Penelitian ini dilakukan di Laboratorium Penelitian Biokimia milik Program Studi Kimia Institut Teknologi Bandung. Ragi Saccharomyces cerevisiae yang mengandung
BAB III METODE PENELITIAN. adalah Bacillus subtilis dan Bacillus cereus yang diperoleh di Laboratorium
 23 BAB III METODE PENELITIAN 3.1 Objek dan Lokasi Penelitian Objek atau bahan penelitian yang digunakan dalam penelitian ini adalah Bacillus subtilis dan Bacillus cereus yang diperoleh di Laboratorium
23 BAB III METODE PENELITIAN 3.1 Objek dan Lokasi Penelitian Objek atau bahan penelitian yang digunakan dalam penelitian ini adalah Bacillus subtilis dan Bacillus cereus yang diperoleh di Laboratorium
HASIL DAN PEMBAHASAN
 HASIL DAN PEMBAHASAN Abomasum dan Rennet Ekstrak Kasar Hasil penimbangan menunjukkan berat abomasum, fundus, serta mukosa fundus dari kedua sampel bervariasi (Tabel 1). Salah satu faktor yang berpengaruh
HASIL DAN PEMBAHASAN Abomasum dan Rennet Ekstrak Kasar Hasil penimbangan menunjukkan berat abomasum, fundus, serta mukosa fundus dari kedua sampel bervariasi (Tabel 1). Salah satu faktor yang berpengaruh
I. METODOLOGI PENELITIAN. Penelitian ini dilaksanakan pada bulan April - Juli 2012 di Laboratorium. Ilmu Pengetahuan Alam Universitas Lampung.
 1 I. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan April - Juli 2012 di Laboratorium Biokimia, Laboratorium Instrumentasi Jurusan Kimia Fakultas Matematika
1 I. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan April - Juli 2012 di Laboratorium Biokimia, Laboratorium Instrumentasi Jurusan Kimia Fakultas Matematika
Analisis kadar protein
 LAMPIRAN Lampiran 1 Bagan alir penelitian Biawak air bagian duodenum, jejenum, ileum, kolon Cuci dengan akuades dan kerok lapisan atasnya (mukosa Ekstraksi enzim protease Analisis kadar protein Pencirian
LAMPIRAN Lampiran 1 Bagan alir penelitian Biawak air bagian duodenum, jejenum, ileum, kolon Cuci dengan akuades dan kerok lapisan atasnya (mukosa Ekstraksi enzim protease Analisis kadar protein Pencirian
II. BAHAN DAN METODE
 II. BAHAN DAN METODE 2.1 Rancangan Perlakuan Penelitian ini terdiri dari enam perlakuan yang masing-masing diberi 3 kali ulangan. Perlakuan yang diberikan berupa perendaman dengan dosis relhp berbeda yaitu
II. BAHAN DAN METODE 2.1 Rancangan Perlakuan Penelitian ini terdiri dari enam perlakuan yang masing-masing diberi 3 kali ulangan. Perlakuan yang diberikan berupa perendaman dengan dosis relhp berbeda yaitu
BAB 3 PERCOBAAN. Alat elektroforesis agarosa (Biorad), autoklaf, cawan Petri, GeneAid High Speed Plasmid
 BAB 3 PERCOBAAN 3.1 Alat Alat elektroforesis agarosa (Biorad), autoklaf, cawan Petri, GeneAid High Speed Plasmid Mini kit, inkubator goyang (GSL), jarum Ose bundar, kit GFX (GE Healthcare), kompor listrik
BAB 3 PERCOBAAN 3.1 Alat Alat elektroforesis agarosa (Biorad), autoklaf, cawan Petri, GeneAid High Speed Plasmid Mini kit, inkubator goyang (GSL), jarum Ose bundar, kit GFX (GE Healthcare), kompor listrik
PEMURNIAN DAN KARAKTERISAS&I&&NZIM -?G,('" INTRASEL DART Bacillus sp. BAC4
 PEMURNIAN DAN KARAKTERISAS&I&&NZIM -?G,('" INTRASEL DART Bacillus sp. BAC4 TESTS MAGISTER Oien SVAIFUL BAHRI 20598515 BIDANG KHUSUS KIMIA ORGANIK PROGRAM MAGISTER KIMIA INSTITC T TEKNOLOGI BANDUNG 2001
PEMURNIAN DAN KARAKTERISAS&I&&NZIM -?G,('" INTRASEL DART Bacillus sp. BAC4 TESTS MAGISTER Oien SVAIFUL BAHRI 20598515 BIDANG KHUSUS KIMIA ORGANIK PROGRAM MAGISTER KIMIA INSTITC T TEKNOLOGI BANDUNG 2001
BAB III METODE A. Jenis Penelitian B. Populasi dan Sampel C. Waktu dan Lokasi Penelitian D. Alat dan Bahan Rizki Indah Permata Sari,2014
 34 BAB III METODE A. Jenis Penelitian Penelitian ini merupakan penelitian murni atau pure research yang dilakukan dengan metode deskriptif, yaitu suatu metode penelitian untuk membuat deskripsi, gambaran
34 BAB III METODE A. Jenis Penelitian Penelitian ini merupakan penelitian murni atau pure research yang dilakukan dengan metode deskriptif, yaitu suatu metode penelitian untuk membuat deskripsi, gambaran
BAB III METODOLOGI PENELITIAN. Pada penelitian ini terdapat lima tahapan penelitian yang dilakukan yaitu
 BAB III METODOLOGI PENELITIAN Pada penelitian ini terdapat lima tahapan penelitian yang dilakukan yaitu pengumpulan sampel berupa akar rambut, ekstraksi mtdna melalui proses lisis akar rambut, amplifikasi
BAB III METODOLOGI PENELITIAN Pada penelitian ini terdapat lima tahapan penelitian yang dilakukan yaitu pengumpulan sampel berupa akar rambut, ekstraksi mtdna melalui proses lisis akar rambut, amplifikasi
Asam Asetat Glacial = 5,7 ml EDTA 0,5 M ph 8.0 = 10 ml Aquades ditambahkan hingga volume larutan 100 ml
 36 Lampiran 1. Pembuatan Larutan Stok dan Buffer A. Pembuatan Larutan Stok Tris HCL 1 M ph 8.0 (100 ml) : Timbang Tris sebanyak 12,114 g. Masukkan Tris ke dalam Erlenmeyer dan ditambahkan 80 ml aquades.
36 Lampiran 1. Pembuatan Larutan Stok dan Buffer A. Pembuatan Larutan Stok Tris HCL 1 M ph 8.0 (100 ml) : Timbang Tris sebanyak 12,114 g. Masukkan Tris ke dalam Erlenmeyer dan ditambahkan 80 ml aquades.
Lampiran 1 Pembuatan Medium Kultur DMEM Lampiran 2 Pembuatan Larutan PBS Lampiran 3 Prosedur Pewarnaan HE
 LAMPIRAN Lampiran 1 Pembuatan Medium Kultur DMEM Medium kultur DMEM merupakan medium Dulbecco s Modified Eagle s Medium (DMEM; Sigma) yang telah dimodifikasi dengan penambahan asam amino non-esensial (AANE;
LAMPIRAN Lampiran 1 Pembuatan Medium Kultur DMEM Medium kultur DMEM merupakan medium Dulbecco s Modified Eagle s Medium (DMEM; Sigma) yang telah dimodifikasi dengan penambahan asam amino non-esensial (AANE;
Lampiran 1. Bahan-bahan yang digunakan untuk pengujian aktivitas enzim (Grossowicz et al., 1950) (a). Reagen A 1. 0,2 M bufer Tris-HCl ph 6,0 12,1 gr
 46 47 Lampiran 1. Bahan-bahan yang digunakan untuk pengujian aktivitas enzim (Grossowicz et al., 1950) (a). Reagen A 1. 0,2 M bufer Tris-HCl ph 6,0 12,1 gr Tris base dilarutkan dalam 200 ml akuades, kemudian
46 47 Lampiran 1. Bahan-bahan yang digunakan untuk pengujian aktivitas enzim (Grossowicz et al., 1950) (a). Reagen A 1. 0,2 M bufer Tris-HCl ph 6,0 12,1 gr Tris base dilarutkan dalam 200 ml akuades, kemudian
3. METODOLOGI PENELITIAN
 3. METODOLOGI PENELITIAN 3.1. Waktu dan tempat Penelitian Penelitian telah dilaksanakan dari bulan Agustus 2006 sampai Juli 2007, bertempat di Laboratorium Bioteknologi Hasil Perairan Departemen Teknologi
3. METODOLOGI PENELITIAN 3.1. Waktu dan tempat Penelitian Penelitian telah dilaksanakan dari bulan Agustus 2006 sampai Juli 2007, bertempat di Laboratorium Bioteknologi Hasil Perairan Departemen Teknologi
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN A. Jenis penelitian Jenis penelitian ini adalah penelitian deskriptif yang mengangkat fenomena alam sebagai salah satu masalah dalam penelitian, sehingga dapat menerangkan arti
BAB III METODE PENELITIAN A. Jenis penelitian Jenis penelitian ini adalah penelitian deskriptif yang mengangkat fenomena alam sebagai salah satu masalah dalam penelitian, sehingga dapat menerangkan arti
III. Bahan dan Metode
 III. Bahan dan Metode A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan selama 3 bulan dari bulan Mei-Juli 2011 yang dilakukan di LPPT UGM Yogyakarta. B. Bahan Penelitian Sampel yang digunakan
III. Bahan dan Metode A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan selama 3 bulan dari bulan Mei-Juli 2011 yang dilakukan di LPPT UGM Yogyakarta. B. Bahan Penelitian Sampel yang digunakan
LAPORAN PRAKTIKUM 5, 6, 7, 8 ISOLASI DNA, ISOLASI PROTEIN DARAH, SERTA PEMERIKSAAN DENGAN TEKNIK PCR, ELEKTROFORESIS AGAROSE DAN SDS-PAGE
 LAPORAN PRAKTIKUM 5, 6, 7, 8 ISOLASI DNA, ISOLASI PROTEIN DARAH, SERTA PEMERIKSAAN DENGAN TEKNIK PCR, ELEKTROFORESIS AGAROSE DAN SDS-PAGE Nama (NIM) : Debby Mirani Lubis (137008010) dan Melviana (137008011)
LAPORAN PRAKTIKUM 5, 6, 7, 8 ISOLASI DNA, ISOLASI PROTEIN DARAH, SERTA PEMERIKSAAN DENGAN TEKNIK PCR, ELEKTROFORESIS AGAROSE DAN SDS-PAGE Nama (NIM) : Debby Mirani Lubis (137008010) dan Melviana (137008011)
III BAHAN DAN METODE
 III BAHAN DAN METODE 3.1 Waktu dan Tempat Penelitian ini dilakukan dari bulan Maret 2006 sampai Maret 2007. Penelitian bertempat di laboratorium Mikrobiologi, Departemen Biologi, Fakultas MIPA, Institut
III BAHAN DAN METODE 3.1 Waktu dan Tempat Penelitian ini dilakukan dari bulan Maret 2006 sampai Maret 2007. Penelitian bertempat di laboratorium Mikrobiologi, Departemen Biologi, Fakultas MIPA, Institut
Metode Pengukuran Spektrofotometri (Bergmeyer et al. 1974) Pembuatan Media Heterotrof Media Heterotrof Padat. Pengaruh ph, Suhu, Konsentrasi dan
 4 Metode Penelitian ini dilakukan pada beberapa tahap yaitu, pembuatan media, pengujian aktivitas urikase secara kualitatif, pertumbuhan dan pemanenan bakteri, pengukuran aktivitas urikase, pengaruh ph,
4 Metode Penelitian ini dilakukan pada beberapa tahap yaitu, pembuatan media, pengujian aktivitas urikase secara kualitatif, pertumbuhan dan pemanenan bakteri, pengukuran aktivitas urikase, pengaruh ph,
Laporan Praktikum Isolasi DNA, Teknik PCR dan Elektroforesis Agarose
 Laporan Praktikum Isolasi DNA, Teknik PCR dan Elektroforesis Agarose Hari / Tanggal Praktikum : Kamis / 1 November dan 22 November 2012 Nama Praktikan : Rica Vera Br. Tarigan dan Jekson Martiar Siahaan
Laporan Praktikum Isolasi DNA, Teknik PCR dan Elektroforesis Agarose Hari / Tanggal Praktikum : Kamis / 1 November dan 22 November 2012 Nama Praktikan : Rica Vera Br. Tarigan dan Jekson Martiar Siahaan
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN A. Jenis Penelitian Jenis penelitian ini adalah penelitian deskriptif yang mengangkat fenomena alam sebagai salah satu masalah dalam penelitian. Penelitian ini dapat menerangkan
BAB III METODE PENELITIAN A. Jenis Penelitian Jenis penelitian ini adalah penelitian deskriptif yang mengangkat fenomena alam sebagai salah satu masalah dalam penelitian. Penelitian ini dapat menerangkan
BAB 4 HASIL PERCOBAAN DAN PEMBAHASAN
 BAB 4 HASIL PERCOBAAN DAN PEMBAHASAN Pembuatan homogenat hati tikus dan proses sentrifugasi dilakukan pada suhu 4 o C untuk menghindari kerusakan atau denaturasi enzim karena pengaruh panas. Kebanyakan
BAB 4 HASIL PERCOBAAN DAN PEMBAHASAN Pembuatan homogenat hati tikus dan proses sentrifugasi dilakukan pada suhu 4 o C untuk menghindari kerusakan atau denaturasi enzim karena pengaruh panas. Kebanyakan
III. METODOLOGI PENELITIAN
 III. METODOLOGI PENELITIAN 3.1. Waktu dan Tempat Penelitian ini dilaksanakan pada bulan November 2006 hingga Agustus 2007. Penangkapan polen dilakukan di kecamatan Pasar Minggu Jakarta Selatan dan analisa
III. METODOLOGI PENELITIAN 3.1. Waktu dan Tempat Penelitian ini dilaksanakan pada bulan November 2006 hingga Agustus 2007. Penangkapan polen dilakukan di kecamatan Pasar Minggu Jakarta Selatan dan analisa
3. METODOLOGI 3.1 Waktu dan Tempat Penelitian 3.2. Alat dan Bahan 3.3 Metode Penelitian
 17 3. METODOLOGI 3.1 Waktu dan Tempat Penelitian Penelitian Produksi dan Karakterisasi Enzim Transglutaminase dari Streptoverticillium ladakanum dengan Media yang Disubstitusi Limbah Cair Surimi dilaksanakan
17 3. METODOLOGI 3.1 Waktu dan Tempat Penelitian Penelitian Produksi dan Karakterisasi Enzim Transglutaminase dari Streptoverticillium ladakanum dengan Media yang Disubstitusi Limbah Cair Surimi dilaksanakan
3 METODE. Bahan. Alat
 9 3 METODE Penelitian ini dilaksanakan selama 14 bulan, yaitu dari April 2013 sampai Mei 2014 di Laboratorium Biokimia Departemen Ilmu dan Teknologi Pangan IPB, Seafast Center, Pusat Studi Satwa Primata
9 3 METODE Penelitian ini dilaksanakan selama 14 bulan, yaitu dari April 2013 sampai Mei 2014 di Laboratorium Biokimia Departemen Ilmu dan Teknologi Pangan IPB, Seafast Center, Pusat Studi Satwa Primata
LAMPIRAN. Lampiran 1. Deskripsi Pembuatan Larutan Stok dan Buffer
 LAMPIRAN Lampiran 1. Deskripsi Pembuatan Larutan Stok dan Buffer 1. Pembuatan Larutan Stok a. CTAB 5 % Larutan dibuat dengan melarutkan : - NaCl : 2.0 gr - CTAB : 5.0 gr - Aquades : 100 ml b. Tris HCl
LAMPIRAN Lampiran 1. Deskripsi Pembuatan Larutan Stok dan Buffer 1. Pembuatan Larutan Stok a. CTAB 5 % Larutan dibuat dengan melarutkan : - NaCl : 2.0 gr - CTAB : 5.0 gr - Aquades : 100 ml b. Tris HCl
Metode Penelitian. III.2.1 Sampel
 18 Bab III Metode Penelitian III.1 Alat Alat-alat yang digunakan dalam penelitian ini adalah sentrifuga Beckman JA-14, ph meter digital Beckman, vortex, spektrofotometer Spectronik 20, kuvet plastik, Smartspec
18 Bab III Metode Penelitian III.1 Alat Alat-alat yang digunakan dalam penelitian ini adalah sentrifuga Beckman JA-14, ph meter digital Beckman, vortex, spektrofotometer Spectronik 20, kuvet plastik, Smartspec
BAB III METODE PENELITIAN
 39 BAB III METODE PENELITIAN A. Desain Penelitian Penelitian yang dilakukan merupakan penelitian deskriptif. Penelitian membuat deskripsi secara sistematis, faktual dan akurat mengenai fakta-fakta dan
39 BAB III METODE PENELITIAN A. Desain Penelitian Penelitian yang dilakukan merupakan penelitian deskriptif. Penelitian membuat deskripsi secara sistematis, faktual dan akurat mengenai fakta-fakta dan
Jurnal ILMU DASAR, Vol. 8 No. 1, 2007 :
 Jurnal ILMU DASAR, Vol. 8 No. 1, 2007 : 37-44 37 Purifikasi dan Karakterisasi Protein Antibakteri dari Pheretima javanica (Purification and Characterization of Antibacterial Protein from Pheretima javanica)
Jurnal ILMU DASAR, Vol. 8 No. 1, 2007 : 37-44 37 Purifikasi dan Karakterisasi Protein Antibakteri dari Pheretima javanica (Purification and Characterization of Antibacterial Protein from Pheretima javanica)
RINGKASAN LAPORAN PENELITIAN DOSEN MUDA
 RINGKASAN LAPORAN PENELITIAN DOSEN MUDA OPTIMASI PEMISAHAN DAN UJI AKTIVITAS PROTEIN ANTIBAKTERI DARI CAIRAN SELOM CACING TANAH Perionyx excavatus. Oleh : Yumaihana MSi Jurusan Nutrisi dan Makanan Ternak,
RINGKASAN LAPORAN PENELITIAN DOSEN MUDA OPTIMASI PEMISAHAN DAN UJI AKTIVITAS PROTEIN ANTIBAKTERI DARI CAIRAN SELOM CACING TANAH Perionyx excavatus. Oleh : Yumaihana MSi Jurusan Nutrisi dan Makanan Ternak,
METODOLOGI PENELITIAN. Penelitian ini dilakukan pada bulan April 2012 sampai dengan bulan Juni 2012 di
 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan April 2012 sampai dengan bulan Juni 2012 di Laboratorium Biokimia Jurusan Kimia Fakultas Matematika dan Ilmu
III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan April 2012 sampai dengan bulan Juni 2012 di Laboratorium Biokimia Jurusan Kimia Fakultas Matematika dan Ilmu
Bab IV Hasil dan Pembahasan
 22 Bab IV Hasil dan Pembahasan α-amilase (E.C 3.2.1.1) merupakan salah satu enzim hidrolitik yang memegang peranan penting di dalam industri. Hidrolisis langsung dari pati mentah secara enzimatis dibawah
22 Bab IV Hasil dan Pembahasan α-amilase (E.C 3.2.1.1) merupakan salah satu enzim hidrolitik yang memegang peranan penting di dalam industri. Hidrolisis langsung dari pati mentah secara enzimatis dibawah
BAB III METODE PENELITIAN. dengan mengadakan manipulasi terhadap objek penelitian serta adanya kontrol
 24 BAB III METODE PENELITIAN A. Jenis Penelitian Penelitian yang dilakukan termasuk penelitian dasar dengan metode penelitian eksperimen. Penelitian eksperimen adalah penelitian yang dilakukan dengan mengadakan
24 BAB III METODE PENELITIAN A. Jenis Penelitian Penelitian yang dilakukan termasuk penelitian dasar dengan metode penelitian eksperimen. Penelitian eksperimen adalah penelitian yang dilakukan dengan mengadakan
BAB III METODOLOGI PENELITIAN. Penelitian akan diawali dengan preparasi alat dan bahan untuk sampling
 16 BAB III METODOLOGI PENELITIAN Penelitian akan diawali dengan preparasi alat dan bahan untuk sampling sel folikel akar rambut. Sampel kemudian dilisis, diamplifikasi dan disekuensing dengan metode dideoksi
16 BAB III METODOLOGI PENELITIAN Penelitian akan diawali dengan preparasi alat dan bahan untuk sampling sel folikel akar rambut. Sampel kemudian dilisis, diamplifikasi dan disekuensing dengan metode dideoksi
BAB III METODE PENELITIAN. Alat dan bahan yang digunakan dalam penelitian ini adalah sebagai
 BAB III METODE PENELITIAN 3.1. Alat dan Bahan Alat dan bahan yang digunakan dalam penelitian ini adalah sebagai berikut: 3.1.1 Alat Alat- alat yang digunakan dalam penelitian ini antara lain : peralatan
BAB III METODE PENELITIAN 3.1. Alat dan Bahan Alat dan bahan yang digunakan dalam penelitian ini adalah sebagai berikut: 3.1.1 Alat Alat- alat yang digunakan dalam penelitian ini antara lain : peralatan
PRODUKSI ENZIM AMILASE
 LAPORAN PRAKTIKUM MIKROB DAN POTENSINYA PRODUKSI ENZIM AMILASE KHAIRUL ANAM P051090031/BTK BIOTEKNOLOGI SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR 2010 PRODUKSI ENZIM AMILASE Pendahuluan Amilase merupakan
LAPORAN PRAKTIKUM MIKROB DAN POTENSINYA PRODUKSI ENZIM AMILASE KHAIRUL ANAM P051090031/BTK BIOTEKNOLOGI SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR 2010 PRODUKSI ENZIM AMILASE Pendahuluan Amilase merupakan
HASIL DAN PEMBAHASAN
 18 HASIL DAN PEMBAHASAN Produksi IgY Anti Salmonella Enteritidis pada Telur Ayam Antibodi spesifik terhadap S. Enteritidis pada serum ayam dan telur dideteksi dengan menggunakan uji agar gel presipitasi
18 HASIL DAN PEMBAHASAN Produksi IgY Anti Salmonella Enteritidis pada Telur Ayam Antibodi spesifik terhadap S. Enteritidis pada serum ayam dan telur dideteksi dengan menggunakan uji agar gel presipitasi
BAB III BAHAN DAN CARA KERJA. Penelitian dilakukan di Laboratorium Institute of Human Virology and
 23 BAB III BAHAN DAN CARA KERJA A. LOKASI DAN WAKTU PENELITIAN Penelitian dilakukan di Laboratorium Institute of Human Virology and Cancer Biology of the University of Indonesia (IHVCB-UI), Jl. Salemba
23 BAB III BAHAN DAN CARA KERJA A. LOKASI DAN WAKTU PENELITIAN Penelitian dilakukan di Laboratorium Institute of Human Virology and Cancer Biology of the University of Indonesia (IHVCB-UI), Jl. Salemba
PRODUKSI, ISOLASI DAN KARAKTERISASI ENZIM DEKSTRANASE dari Arthrobacter sp. B7
 Berk. Penel. Hayati: 10 (97 101), 2005 PRODUKSI, ISOLASI DAN KARAKTERISASI ENZIM DEKSTRANASE dari Arthrobacter sp. B7 Afaf Baktir *, Untung Murdiyatmo ** * Jurusan Kimia Fakultas MIPA Universitas Airlangga
Berk. Penel. Hayati: 10 (97 101), 2005 PRODUKSI, ISOLASI DAN KARAKTERISASI ENZIM DEKSTRANASE dari Arthrobacter sp. B7 Afaf Baktir *, Untung Murdiyatmo ** * Jurusan Kimia Fakultas MIPA Universitas Airlangga
III. METODOLOGI PENELITIAN
 III. METODOLOGI PENELITIAN 3.1 WAKTU DAN TEMPAT Penelitian dilaksanakan pada bulan Januari 2012 hingga September 2012. Penelitian dilaksanakan di Laboratorium Pengembangan Teknologi Industri Agro dan Biomedika
III. METODOLOGI PENELITIAN 3.1 WAKTU DAN TEMPAT Penelitian dilaksanakan pada bulan Januari 2012 hingga September 2012. Penelitian dilaksanakan di Laboratorium Pengembangan Teknologi Industri Agro dan Biomedika
BAB III METODE PENELITIAN Bagan Alir Penelitian ini secara umum dapat digambarkan pada skema berikut:
 BAB III METODE PENELITIAN Tahapan-tahapan yang dilakukan dalam penelitian ini adalah: pengumpulan sampel, lisis terhadap sampel mtdna yang telah diperoleh, amplifikasi daerah HVI mtdna sampel dengan menggunakan
BAB III METODE PENELITIAN Tahapan-tahapan yang dilakukan dalam penelitian ini adalah: pengumpulan sampel, lisis terhadap sampel mtdna yang telah diperoleh, amplifikasi daerah HVI mtdna sampel dengan menggunakan
3 Metodologi Percobaan
 3 Metodologi Percobaan 3.1 Waktu dan Tempat Penelitian Penelitian tugas akhir ini dilakukan di Laboratorium Penelitian Kimia Analitik, Program Studi Kimia, FMIPA Institut Teknologi Bandung. Waktu penelitian
3 Metodologi Percobaan 3.1 Waktu dan Tempat Penelitian Penelitian tugas akhir ini dilakukan di Laboratorium Penelitian Kimia Analitik, Program Studi Kimia, FMIPA Institut Teknologi Bandung. Waktu penelitian
BAB III METODE PENELITIAN. Alat-alat yang digunakan dalam penelitian ini, antara lain: waterbath,
 31 BAB III METODE PENELITIAN 3.1 Alat dan Bahan Alat dan bahan yang digunakan dalam penelitian ini adalah sebagai berikut: 3.1.1 Alat Alat-alat yang digunakan dalam penelitian ini, antara lain: waterbath,
31 BAB III METODE PENELITIAN 3.1 Alat dan Bahan Alat dan bahan yang digunakan dalam penelitian ini adalah sebagai berikut: 3.1.1 Alat Alat-alat yang digunakan dalam penelitian ini, antara lain: waterbath,
dimana a = bobot sampel awal (g); dan b = bobot abu (g)
 Lampiran 1. Metode analisis proksimat a. Analisis kadar air (SNI 01-2891-1992) Kadar air sampel tapioka dianalisis dengan menggunakan metode gravimetri. Cawan aluminium dikeringkan dengan oven pada suhu
Lampiran 1. Metode analisis proksimat a. Analisis kadar air (SNI 01-2891-1992) Kadar air sampel tapioka dianalisis dengan menggunakan metode gravimetri. Cawan aluminium dikeringkan dengan oven pada suhu
4 Hasil dan Pembahasan
 4 Hasil dan Pembahasan Danau Kakaban menyimpan berbagai organisme yang langka dan unik. Danau ini terbentuk dari air laut yang terperangkap oleh terumbu karang di sekelilingnya akibat adanya aktivitas
4 Hasil dan Pembahasan Danau Kakaban menyimpan berbagai organisme yang langka dan unik. Danau ini terbentuk dari air laut yang terperangkap oleh terumbu karang di sekelilingnya akibat adanya aktivitas
3 Metode Penelitian Alat
 3 Metode Penelitian 3.1. Alat Penelitian dilakukan di Laboratorium KBK Protein dan Enzim dan Laboratorium Biokimia, Program Studi Kimia ITB. Peralatan gelas yang digunakan terdiri atas labu erlenmeyer,
3 Metode Penelitian 3.1. Alat Penelitian dilakukan di Laboratorium KBK Protein dan Enzim dan Laboratorium Biokimia, Program Studi Kimia ITB. Peralatan gelas yang digunakan terdiri atas labu erlenmeyer,
Y ij = µ + B i + ε ij
 METODE Lokasi dan Waktu Penelitian ini dilaksanakan dari bulan September 2008 sampai bulan September 2009. Penelitian dilakukan di Laboratorium Mikrobiologi Bagian Teknologi Hasil Ternak Perah dan Laboratorium
METODE Lokasi dan Waktu Penelitian ini dilaksanakan dari bulan September 2008 sampai bulan September 2009. Penelitian dilakukan di Laboratorium Mikrobiologi Bagian Teknologi Hasil Ternak Perah dan Laboratorium
BAB III METODE PENELITIAN. Pendidikan Biologi FPMIPA UPI dan protease Bacillus pumilus yang diperoleh
 31 BAB III METODE PENELITIAN 3.1. Objek Dan Lokasi Penelitian Objek atau bahan penelitian yang digunakan dalam penelitian ini adalah proteas Bacillus subtilis diperoleh dari laboratorium Mikrobiologi Jurusan
31 BAB III METODE PENELITIAN 3.1. Objek Dan Lokasi Penelitian Objek atau bahan penelitian yang digunakan dalam penelitian ini adalah proteas Bacillus subtilis diperoleh dari laboratorium Mikrobiologi Jurusan
4 Hasil dan Pembahasan
 4 Hasil dan Pembahasan Dalam bab ini akan dipaparkan hasil dari tahap-tahap penelitian yang telah dilakukan. Melalui tahapan tersebut diperoleh urutan nukleotida sampel yang positif diabetes dan sampel
4 Hasil dan Pembahasan Dalam bab ini akan dipaparkan hasil dari tahap-tahap penelitian yang telah dilakukan. Melalui tahapan tersebut diperoleh urutan nukleotida sampel yang positif diabetes dan sampel
III. METODE PENELITIAN. Penelitian ini dilakukan pada bulan Januari 2015 Juli 2015, bertempat di
 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan Januari 2015 Juli 2015, bertempat di Laboratorium Kimia Organik, Jurusan Kimia, Fakultas Matematika dan Ilmu Pengetahuan
III. METODE PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan Januari 2015 Juli 2015, bertempat di Laboratorium Kimia Organik, Jurusan Kimia, Fakultas Matematika dan Ilmu Pengetahuan
BAHAN DAN METODE Waktu dan Tempat Alat dan Bahan Prosedur Penelitian
 9 BAHAN DAN METODE Waktu dan Tempat Penelitian dilakukan mulai bulan November 2010 sampai dengan bulan Juni 2011 di Laboratorium Kimia Analitik Departemen Kimia FMIPA dan Laboratorium Pusat Studi Biofarmaka
9 BAHAN DAN METODE Waktu dan Tempat Penelitian dilakukan mulai bulan November 2010 sampai dengan bulan Juni 2011 di Laboratorium Kimia Analitik Departemen Kimia FMIPA dan Laboratorium Pusat Studi Biofarmaka
METODE PENELITIAN. Penelitian ini telah dilakukan pada bulan Januari-Mei 2015 di Laboratorium
 15 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian ini telah dilakukan pada bulan Januari-Mei 2015 di Laboratorium Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas
15 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian ini telah dilakukan pada bulan Januari-Mei 2015 di Laboratorium Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas
BAB 4 HASIL PERCOBAAN DAN BAHASAN. Oligonukleotida sintetis daerah pengkode IFNα2b sintetis dirancang menggunakan
 BAB 4 HASIL PERCOBAAN DAN BAHASAN Oligonukleotida sintetis daerah pengkode IFNα2b sintetis dirancang menggunakan program komputer berdasarkan metode sintesis dua arah TBIO, dimana proses sintesis daerah
BAB 4 HASIL PERCOBAAN DAN BAHASAN Oligonukleotida sintetis daerah pengkode IFNα2b sintetis dirancang menggunakan program komputer berdasarkan metode sintesis dua arah TBIO, dimana proses sintesis daerah
PENGARUH LOGAM BERAT PB TERHADAP PROFIL PROTEIN ALGA MERAH ( (Gracillaria
 TUGAS AKHIR SB 1358 PENGARUH LOGAM BERAT PB TERHADAP PROFIL PROTEIN ALGA MERAH ( (Gracillaria sp.) OLEH: HENNY ANDHINI OKTAVIA (1504 100 022) DOSEN PEMBIMBING: 1. KRISTANTI INDAH.P.,S.si.,M.si 2. TUTIK
TUGAS AKHIR SB 1358 PENGARUH LOGAM BERAT PB TERHADAP PROFIL PROTEIN ALGA MERAH ( (Gracillaria sp.) OLEH: HENNY ANDHINI OKTAVIA (1504 100 022) DOSEN PEMBIMBING: 1. KRISTANTI INDAH.P.,S.si.,M.si 2. TUTIK
UJI KUALITATIF ETANOL YANG DIPRODUKSI SECARA ENZAMATIS MENGGUNAKAN Z. MOBILIS PERMEABEL
 UJI KUALITATIF ETANOL YANG DIPRODUKSI SECARA ENZAMATIS MENGGUNAKAN Z. MOBILIS PERMEABEL Dian Pinata NRP. 1406 100 005 DOSEN PEMBIMBING Drs. Refdinal Nawfa, M.S LATAR BELAKANG Krisis Energi Sumber Energi
UJI KUALITATIF ETANOL YANG DIPRODUKSI SECARA ENZAMATIS MENGGUNAKAN Z. MOBILIS PERMEABEL Dian Pinata NRP. 1406 100 005 DOSEN PEMBIMBING Drs. Refdinal Nawfa, M.S LATAR BELAKANG Krisis Energi Sumber Energi
METODE PENELITIAN Waktu dan Tempat Penelitian Alat dan Bahan Prosedur Penelitian
 METODE PENELITIAN Waktu dan Tempat Penelitian Penelitian ini dilaksanakan dari bulan Desember 2010 sampai dengan Mei 2011 di Laboratorium Kimia Organik, Departemen Kimia Institut Pertanian Bogor (IPB),
METODE PENELITIAN Waktu dan Tempat Penelitian Penelitian ini dilaksanakan dari bulan Desember 2010 sampai dengan Mei 2011 di Laboratorium Kimia Organik, Departemen Kimia Institut Pertanian Bogor (IPB),
MATERI DAN METODE Lokasi dan Waktu Materi Prosedur Karakterisasi Isolat L. plantarum dan Bakteri Indikator
 MATERI DAN METODE Lokasi dan Waktu Penelitian ini berlangsung selama tujuh bulan, yakni mulai dari bulan Februari sampai dengan bulan Agustus 2011. Penelitian ini dilaksanakan di Laboratorium Terpadu Ilmu
MATERI DAN METODE Lokasi dan Waktu Penelitian ini berlangsung selama tujuh bulan, yakni mulai dari bulan Februari sampai dengan bulan Agustus 2011. Penelitian ini dilaksanakan di Laboratorium Terpadu Ilmu
DETEKSI MOLEKULER STAPHYLOCOCCUS AUREUS SEBAGAI PENYEBAB MASTITIS PADA PAYUDARA. Oleh:
 Jurnal Sangkareang Mataram 27 DETEKSI MOLEKULER STAPHYLOCOCCUS AUREUS SEBAGAI PENYEBAB MASTITIS PADA PAYUDARA Oleh: I Gst. Ag. Ayu Hari Triandini Dosen Akademi Kebidanan Bhakti Kencana Mataram Abstrak
Jurnal Sangkareang Mataram 27 DETEKSI MOLEKULER STAPHYLOCOCCUS AUREUS SEBAGAI PENYEBAB MASTITIS PADA PAYUDARA Oleh: I Gst. Ag. Ayu Hari Triandini Dosen Akademi Kebidanan Bhakti Kencana Mataram Abstrak
3 Metodologi Penelitian
 3 Metodologi Penelitian 3.1 Alat Penelitian ini dilakukan di Laboratorium Penelitian Biokimia, Program Studi Kimia, Institut Teknologi Bandung. Peralatan yang digunakan pada penelitian ini diantaranya
3 Metodologi Penelitian 3.1 Alat Penelitian ini dilakukan di Laboratorium Penelitian Biokimia, Program Studi Kimia, Institut Teknologi Bandung. Peralatan yang digunakan pada penelitian ini diantaranya
HASIL DA PEMBAHASA. Kadar Air
 Pemilihan Eluen Terbaik Pelat Kromatografi Lapis Tipis (KLT) yang digunakan adalah pelat aluminium jenis silika gel G 60 F 4. Ekstrak pekat ditotolkan pada pelat KLT. Setelah kering, langsung dielusi dalam
Pemilihan Eluen Terbaik Pelat Kromatografi Lapis Tipis (KLT) yang digunakan adalah pelat aluminium jenis silika gel G 60 F 4. Ekstrak pekat ditotolkan pada pelat KLT. Setelah kering, langsung dielusi dalam
BAB 3 PERCOBAAN 3.1 Bahan 3.2 Alat
 BAB 3 PERCOBAAN 3.1 Bahan Bahan yang digunakan memiliki kualitas pro analisis atau pro biologi molekular, yaitu : primer M. tuberculosis forward: 5 GGATCCGATGAGCAAGCTGATCGAA3 (Proligo) dan primer M. tuberculosis
BAB 3 PERCOBAAN 3.1 Bahan Bahan yang digunakan memiliki kualitas pro analisis atau pro biologi molekular, yaitu : primer M. tuberculosis forward: 5 GGATCCGATGAGCAAGCTGATCGAA3 (Proligo) dan primer M. tuberculosis
III. METODOLOGI PENELITIAN. Penelitian ini dilaksanakan dari bulan Juli sampai bulan September 2010 di
 20 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan dari bulan Juli sampai bulan September 2010 di Laboratorium Instrumentasi dan Laboratorium Biokimia Jurusan Kimia
20 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan dari bulan Juli sampai bulan September 2010 di Laboratorium Instrumentasi dan Laboratorium Biokimia Jurusan Kimia
BAB III METODE PENELITIAN. amplifikasi daerah HVI mtdna sampel dengan menggunakan teknik PCR;
 BAB III METODE PENELITIAN Secara garis besar, langkah-langkah yang dilakukan dalam penelitian ini adalah: pengumpulan sampel; lisis terhadap sampel mtdna yang telah diperoleh; amplifikasi daerah HVI mtdna
BAB III METODE PENELITIAN Secara garis besar, langkah-langkah yang dilakukan dalam penelitian ini adalah: pengumpulan sampel; lisis terhadap sampel mtdna yang telah diperoleh; amplifikasi daerah HVI mtdna
