BAB 17 ALKOHOL DAN FENOL
|
|
|
- Vera Cahyadi
- 7 tahun lalu
- Tontonan:
Transkripsi
1 Slaid kuliah Kimia Organik I untuk mhs S1 Kimia semester 3 BAB 17 ALKOHOL DAN FENOL Budi Arifin (dibantu oleh Dumas Flis Tang) Bagian Kimia Organik Departemen Kimia FMIPA-IPB TIU TIK 1
2 Daftar Pustaka: Fessenden RJ, Fessenden JS Organic Chemistry. Ed. ke-6. Boston: Brooks/Cole. Bab 12. McMurry J Organic Chemistry. Ed. ke-7. Belmont: Brooks/Cole. Bab 17. Solomons TWG, Fryhle CB Organic Chemistry. Ed. ke-8. New York: J Wiley. Bab 6, 11, 12, 21. Turunan organik dari air (H O H): Alkohol (R O H): gugus OH terikat pada atom C-sp 3. Fenol (Ar O H): gugus OH terikat pada atom C-sp 2 aril. Enol (C=C O H): gugus OH terikat pada atom C-sp 2 vinilik. Alkohol Fenol Enol Metanol, etanol, dan fenol banyak digunakan dalam industri kimia (baca McMurry hlm ). 2
3 17.1 Pengelompokan dan Tata Nama Alkohol dikelompokkan berdasarkan jumlah gugus organik yang terikat ke karbon-α (karbon yang mengikat OH): α RCH 2 OH: primer (1 o ) R 2 CHOH: sekunder (2 o ) R 3 COH: tersier (3 o ) Tata nama alkohol secara umum: gugus alkil R OH gugus hidroksil Nama IUPAC = alkana, akhiran a diganti -ol Nama trivial: nama gugus alkil + alkohol. Tata nama IUPAC alkohol: Rantai induk rantai terpanjang yang memiliki OH: akhiran a dari nama alkananya diganti ol. Penomoran dimulai dari ujung terdekat dengan OH. Posisi OH dan setiap substituen dinyatakan; nama substituen diurutkan sesuai abjad Inggris. Jika ada >1 OH, akhiran ol diganti diol, triol, dst. Dihindari 2 huruf vokal berurutan pada nama rantai induk. Tata nama cara lama dan baru diperbolehkan. 3
4 CH 3 OH metanol metil alkohol CH 3 CHCH 2 CH 3 OH CH 3 CH 2 OH etanol etil alkohol CH 3 CHCH 2 OH CH 3 2-metil-1-propanol CH 3 CH 2 CH 2 OH 1-propanol n-propil alkohol (1 o ) (1 o ) (1 o ) CH 3 CH 3 C OH CH 3 2-butanol 2-metil-2-propanol sec-butil alkohol isobutil alkohol tert-butil alkohol (2 o ) (1 o ) (3 o ) 3 CH CHCH 2 OH 2-propen-1-ol alil alkohol (alilik) 2 1 ClCH 2 CH 2 OH 2-kloroetanol (1 o ) 5 4 CH 3 C CCH 2 CH 2 OH 3-pentun-1-ol (1 o ) H OH sikloheksanol sikloheksil alkohol (2 o ) CH 2 OH fenilmetanol benzil alkohol (benzilik) HO CH 2 CH 2 OH 1,2-etanadiol etilena glikol 1,2,3-propanatriol gliserol 2-metil-2-pentanol (Baru: 2-metilpentan-2-ol) cis-1,4-sikloheksanadiol (Baru: cis-sikloheksana-1,4-diol) 3-fenil-2-butanol (Baru: 3-fenilbutan-2-ol) 4
5 Untuk tata nama fenol, lihat kembali Bab 15. OH OH CO 2 H OH Br 1 Br 6 2 fenol NO 2 p-nitrofenol OH asam m-hidroksibenzoat 4 Br 2,4,6-tribromofenol m-metilfenol (m-kresol) 2,4-dinitrofenol Problem 17.1, 17.2 Soal-soal Latihan Problem 17.20, 17.25, 17.26, 17.28,
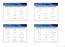
6 17.2 Sifat Fisis dan Keasaman Seperti halnya air, alkohol dan fenol memiliki titik didih yang tinggi karena mampu berikatan hidrogen antarmolekul. Bobot molekul Titik didih ( o C) Bobot molekul Titik didih ( o C) CH 3 (CH 2 ) 2 OH CH 3 (CH 2 ) 2 CH ,5 CH 3 (CH 2 ) 3 OH C 2 H 5 OC 2 H CH 3 CH 2 CH 2 Cl 65 12,5 CH 3 (CH 2 ) 3 CH Alkohol sederhana larut dalam air karena ikatan hidrogen antara air dan alkohol. Semakin panjang rantai alkil, kelarutan alkohol dalam air semakin menurun. Semakin bercabang, alkohol semakin larut dalam air. Semakin banyak gugus OH, kelarutan juga meningkat. Latihan: Jelaskan urutan kenaikan titik didih dan kelarutan dari (a) metanol, 1-butanol, dan 1-heksanol (b) 1-butanol, sec-butil alkohol, dan t-butil alkohol (c) etanol, etilena glikol, dan gliserol 6
7 Alkohol dan fenol bersifat amfiprotik, merupakan asam lemah sekaligus basa lemah menurut Brönsted-Lowry. Alkohol cenderung lebih bersifat basa: alkohol ion oksonium (Pasangan elektron bebas atom O pada alkohol terlokalisasi, maka lebih tersedia untuk mengambil H +.) Sebaliknya, fenol cenderung lebih bersifat asam: fenol ion fenoksida 7
8 Keasaman fenol (pk a = 9,89) >> alkohol (pk a CH 3 OH = 15,54; C 2 H 5 OH = 16,00); bdk juga pk a air (15,74). Ion fenoksida terstabilkan oleh resonans (muatan negatif terdelokalisasi ke dalam cincin aromatik) kesetimbangan pembentukannya lebih disukai daripada ion alkoksida. O O O O O (muatan negatif terdelokalisasi pada posisi cincin orto dan para melalui resonansi) Keasaman tert-butil alkohol (pk a = 18,00) < etanol (pk a = 16,00) < metanol (pk a = 15,54). Substitusi alkil akan menghalangi solvasi ion alkoksida hasil disosiasi sehingga ion tersebut kurang stabil dan kurang disukai pembentukannya. Atom O takterhalangi, mudah diakses, dan mudah disolvasi. Halangan sterik atom O sangat besar, sulit diakses dan disolvasi. ion metoksida, CH 3 O ion tert-butoksida, (CH 3 ) 3 CO 8
9 Keasaman 2,2,2-trifluoroetanol (pk a = 12,43) > etanol. 1. Penjelasan pada reaktan (alkohol): Tarikan-elektron atom F meningkatkan rapat muatan δ+ di atom C-α dan atom H-hidroksil H + kurang terperisai. 2. Penjelasan pada produk (ion alkoksida): Tarikan-elektron atom F mendelokalisasikan muatan negatif sehingga lebih stabil. δ F F C F δ δ δ++ δ++ C O H H 2 H + δ F F C F δ δ δ+ C H 2 O Gugus penarik elektron meningkatkan keasaman: 1. Elektronegativitas (daya tarik elektron): FCH 2 CH 2 OH > ClCH 2 CH 2 OH > BrCH 2 CH 2 OH > ICH 2 CH 2 OH 2. Jumlah gugus: Cl 3 CCH 2 OH > Cl 2 CHCH 2 OH > ClCH 2 CH 2 OH > CH 3 CH 2 OH 3. Jarak gugus dari OH: pk a = 5.4 pk a = 18.0 BrCH 2 OH > BrCH 2 CH 2 OH > BrCH 2 CH 2 CH 2 OH dst. 9
10 Sebaliknya, gugus pendorong elektron (gugus alkil) menurunkan keasaman. Oleh karena itu, Keasaman meningkat p-aminofenol (pk a = 10,46) p-metilfenol (pk a = 10,17) Fenol (pk a = 9,89) p-klorofenol (pk a = 9,38) p-nitrofenol (pk a = 7,15) NH 2 (R+ > I ) CH 3 (R+) sebab Cl (I > R+) NO 2 (I & R ) (baca kembali sifat pengaktif & pendeaktif pada benzena) Dari data di atas, perkirakan pk a p-hidroksibenzaldehida. Alkohol asam lemah: - tidak bereaksi dengan basa lemah (amina, ion bikarbonat), - bereaksi reversibel dengan basa kuat (hidroksida logam), - bereaksi baik dengan basa sangat kuat: (a) logam alkali 2 RO H (l) + 2 Na/K (s) 2 RO Na + /K + (aq) + H 2(g) (b) natrium hidrida RO H (l) + NaH (s) RO Na + (aq) + H 2(g) (c) natrium amida RO H (l) + NaNH 2(aq) RO Na + (aq) + NH 3(g) (d) pereaksi Grignard RO H (l) + R MgX (aq) RO MgX + (aq) + R H (l) 10
11 Contoh: (perhatikan bahwa akhiran at digunakan pada nama IUPAC ion alkoksida) 2-metil-2-propanol (tert-butil alkohol) kalium 2-metil-2-propanolat (kalium tert-butoksida) metanol (metil alkohol) natrium metanolat (natrium metoksida) etanol (etil alkohol) natrium etanolat (natrium etoksida) sikloheksanol bromomagnesium sikloheksanolat Fenol asam lebih kuat daripada alkohol: - tidak bereaksi dengan basa lemah (amina, ion bikarbonat), - bereaksi baik dengan basa kuat (hidroksida logam), maka - tidak perlu basa sangat kuat untuk menggaramkan. RO H + Na + OH O H + Na + OH O Na + + H 2 O Asam karboksilat jauh lebih kuat daripada fenol (KimOrg II): - bereaksi dengan basa lemah, dan - tidak perlu basa kuat atau sangat kuat untuk menggaramkan. 11
12 Perbedaan sifat asam-basa dimanfaatkan dalam ekstraksi dengan pengendalian ph. Campuran asam benzoat, p-klorofenol, dan benzil alkohol Dilarutkan dalam pelarut organik (eter, diklorometana, atau kloroform) + NaHCO 3(aq) Fase air I (Na-benzoat) Fase organik (campuran p-klorofenol & benzil alkohol) + NaOH (aq) Fase air I (Na-p-klorofenolat) Fase organik (benzil alkohol) Fase air I (Na-benzoat) Fase air II (Na-p-klorofenolat) Fase organik (benzil alkohol) + HCl (aq) + HCl (aq) Asam benzoat p-klorofenol Dibebas-airkan dgn Na 2 SO 4(s) & dipekatkan Coba kalian tuliskan persamaanpersamaan reaksi yang terjadi dalam proses pemisahan di atas. Benzil alkohol 12
13 Problem Problem 17.44, Soal-soal Latihan 17.3 Pembuatan Alkohol Alkohol sangat sentral dalam kimia organik. Alkohol dapat disiapkan dari berbagai gugus fungsi, dan sebaliknya aneka gugus fungsi yang sama dapat disiapkan dari alkohol. Asam karboksilat Alkena Keton Ester Aldehida Alkil halida Alkohol Eter 13
14 (1) Sintesis Alkohol dari Alkena (Bab 7) Metode Hidrasi berkataliskan-asam Stereoselektivitas Oksimerkurasidemerkurasi Hidroborasioksidasi Regio-selektivitas Markovnikov Markovnikov Tidak stereoselektif Tidak stereoselektif Penataan ulang Terjadi Tidak terjadi Anti-Markovnikov sin Tidak terjadi Contoh: trans-2-metilsikloheksanol (84%) 1-metilsikloheksena 1-metilsikloheksanol (90%) 14
15 (2) Sintesis Diol dari Alkena (Bab 7) suatu osmat cis-1,2-diol 1-metilsikloheksena 1-metil-1,2-epoksisikloheksana trans-1,2-diol (3) Reduksi Aldehida dan Keton (KimOrg 2) Paling banyak dijumpai di lab maupun di dalam organisme. aldehida alkohol 1º keton alkohol 2º Reduktor NaBH 4 (natrium borohidrida) relatif aman. Padatan putih ini dapat ditimbang di udara terbuka, dan digunakan dalam air atau alkohol dengan rendemen tinggi. Reduktor LiAlH 4 (litium aluminium hidrida, LAH) jauh lebih reaktif dan berbahaya. Wujudnya padatan kelabu, larut dalam eter dan THF, bereaksi hebat dengan air dan terdekomposisi dengan ledakan jika dipanaskan di atas 120 o C. 15
16 Contoh: butanal 1-butanol (85%) (alkohol 1 o ) disikloheksil keton disikloheksilmetanol (88%) (alkohol 2 o ) 2-sikloheksenon 2-sikloheksenol (94%) (4) Reduksi Asam Karboksilat dan Ester (KimOrg 2) Reduksi lazim dilakukan dengan LiAlH 4. Dengan NaBH 4, reduksi ester sangat lambat, sedangkan asam tidak tereduksi. Contoh: asam 9-oktadekenoat (asam oleat) asam 9-oktadeken-1-ol (87%) metil 2-pentenoat 2-penten-1-ol (91%) 16
17 Latihan: Senyawa karbonil apakah yang jika direduksi menghasilkan alkohol berikut: (a) (b) Jawaban: (a) (b) Problem Soal-soal Latihan Problem 17.34, 17.35,
18 (5) Alkohol dari Pereaksi Grignard (a) Pereaksi Grignard + Epoksida/Oksirana Alkohol 1 o Nu: kuat Contoh: serangan pada karbon yang kurang tersubstitusi (b) Pereaksi Grignard + Formaldehida Alkohol 1 o Contoh: fenilmagnesium bromida fenilmetanol (90%) sikloheksilmagnesium bromida sikloheksilmetanol (65%) 18
19 (c) Pereaksi Grignard + Aldehida Lain Alkohol 2 o Contoh: etilmagnesium bromida etanal 2-butanol (90%) fenilmagnesium bromida 3-metilbutanal 3-metil-1-fenil-1-butanol (73%) (d) Pereaksi Grignard + Keton Alkohol 3 o Contoh: butilmagnesium bromida aseton 2-metil-2-heksanol (92%) etilmagnesium bromida sikloheksanon 1-etilsikloheksanol (89%) 19
20 (e) Pereaksi Grignard + Ester Alkohol 3 o Contoh: Ada 2 gugus R sama. Ester format (R = H) alkohol 2 o. etil pentanoat 2-metil-2-heksanol (85%) (f) Merancang Sintesis Alkohol dengan Pereaksi Grignard Misalkan Anda diminta menyintesis 3-fenil-3-pentanol: Alkohol 3 o bahan awal keton atau ester. Diskoneksi retrosintetik dilakukan seperti di bawah ini: diskoneksi retrosintetik 20
21 diskoneksi retrosintetik (Coba Anda tuliskan kemungkinan diskoneksi retrosintetik ketiga.) Latihan: Tuliskan skema retrosintetik dan kemudian reaksi sintetik dengan metode Grignard untuk (a) 2-metil-2-butanol (3 cara) (c) 2-fenil-2-pentanol (3 cara) (b) 3-etil-2-pentanol (2 cara) (d) trifenilmetanol (2 cara) Sifat nukleofili kuat dan basa kuat menyebabkan pereaksi Grignard tidak dapat dibuat dari halida dengan gugus asam/tapak elektrofilik. H-asam akan memprotonasi pereaksi Grignard Tapak elektrofilik akan diadisi oleh pereaksi Grignard Contoh: 21
22 Soal-soal Latihan Problem Problem17.24, 17.33, 17.36, 17.39, 17.47, 17.52, Reaksi Alkohol (1) Substitusi Nukleofilik Berbeda dari alkil halida, reaksi S N berjalan lambat pada alkohol. Kebasaan OH membuatnya bukan gugus pergi yang baik. basa kuat (gugus pergi yang buruk) Protonasi gugus OH (memanfaatkan kebasaan alkohol) mengubah gugus pergi menjadi H 2 O. Sifat basa lemah menjadikan H 2 O gugus pergi yang baik dan reaksi S N berlangsung lebih cepat. R OH + H + R OH 2 R + + H 2 O ion alkiloksonium basa lemah (gugus pergi yang baik) 22
23 (a) Alkohol Alkil Halida (Bab 10) (i) Alkohol + HCl/HBr Reaktivitas alkohol 3 o > 2 o > 1 o < metil: Mekanisme S N 1 pada alkohol 2 o, 3 o, alilik, dan benzilik: alkohol 3º karbokation alkil klorida atau bromida Untuk menekan kompetisi dengan reaksi E1, reaksi dilakukan pada suhu kamar/rendah. Sifat nukleofilik kuat X (kecuali F ) juga meningkatkan rendemen S N 1. Penataan-ulang juga dapat terjadi seperti pada contoh berikut: 23
24 Mekanisme S N 2 pada alkohol 1 o dan metanol: Alkohol 1 o dan 2 o juga lazim disubstitusi dengan menggunakan campuran NaX dalam H 2 SO 4 : Tanpa katalis H 2 SO 4, reaksi tidak berlangsung karena X (dari NaX) tidak dapat mengusir OH, gugus pergi yang buruk. Reaktivitas HI > HBr > HCl (HF umumnya takreaktif): HCl tidak bereaksi dengan alkohol 1 o atau 2 o tanpa ZnCl 2 (reaksi Lucas) atau asam Lewis lainnya yang sejenis 24
25 (ii) Alkohol 1 o /2 o + SOCl 2 /PBr 3 (mekanisme S N 2) Kedua pereaksi ini pada prinsipnya juga mengubah OH menjadi gugus pergi yang lebih baik. Mekanisme: (bereaksi dengan 2 mol alkohol lagi) Mekanisme: (piridina lazim ditambahkan untuk mempercepat reaksi) alkil klorosulfit 25
26 Contoh: Reagen PBr 3 lebih banyak dipilih ketimbang HBr, karena umumnya tidak terjadi penataan-ulang (jika suhu dijaga di bawah 0 o C) Jika atom C-α alkohol kiral, reaksi dengan SOCl 2 terjadi dengan - inversi konfigurasi jika terdapat amina 3 o (seperti piridina), - retensi konfigurasi jika tanpa amina tersebut. Kedua reaksi sama-sama melalui zat antara alkilklorosulfit. 26
27 (b) Alkohol Turunan Ester Sulfonat (Bab 10 & 11) Reaksi ini juga mengubah gugus OH menjadi gugus pergi yang lebih baik. Tiga jenis turunan ester sulfonat yang lazim ialah mesilat, tosilat, dan triflat. alkil mesilat alkil triflat alkil tosilat Ester sulfonat diperoleh dengan mereaksikan alkohol dengan sulfonil klorida yang sesuai (MsCl, TsCl, atau TfCl) atau dengan anhidrida triflat [(CF 3 SO 2 ) 2 O]: metanasulfonil klorida (mesil klorida) etil metanasulfonat (etil mesilat) p-toluenasulfonil klorida (tosil klorida) etil p-toluenasulfonat (etil tosilat) 27
28 Sulfonil klorida tersedia secara komersial atau dapat disiapkan dari asam sulfonat dan PCl 5. asam p-toluenasulfonat p-toluenasulfonil klorida Ion mesilat, tosilat, dan triflat gugus pergi yang baik karena stabilisasi resonans menjadikannya basa sangat lemah. Pengubahan alkohol menjadi ester sulfonat memutus ikatan O H dan bukan C α O, maka kiralitas C α (jika ada) tidak terpengaruh. (Retensi konfigurasi) Reaksi S N 2 pada R OMs/Ts/Tf sesudah itu, baru akan memutus C α -O dan membalik kiralitas C α. (Inversi konfigurasi) Reaksi keseluruhan: 28
29 Rangkaian 2-tahap reaksi ini sangat berguna dalam sintesis senyawa organik untuk pengaturan stereokimia. Contoh: (S)-2-bromooktana etil (R)-1-metilheptil eter (R)-2-oktanol (R)-1-metilheptil tosilat etil (S)-1-metilheptil eter (2) Eliminasi (Dehidrasi) (a) Dehidrasi Berkataliskan-Asam (Bab 7) Kondisi reaksi eliminasi alkohol (dehidrasi) berbeda dari eliminasi alkil halida (dehidrohalogenasi): Dehidrohalogenasi umumnya dilakukan dengan basa kuat dan melalui mekanisme E2. Dehidrasi sebaliknya dilakukan dengan asam kuat dan melalui mekanisme E1. Contoh: 1-metilsikloheksanol 1-metilsikloheksena (91%) 29
30 Asam kuat memprotonasi gugus OH agar karbokation dapat terbentuk, lalu atom H-β dideprotonasi. Lazimnya, reaksi S N 1 berkompetisi dan selalu mendominasi reaksi E1. Bagaimana caranya agar reaksi E1 yang dominan di sini? Reaksi dilakukan dengan asam pekat agar nukleofili H 2 O sedikit. Digunakan asam yang basa konjugasinya adalah nukleofili lemah, misalnya H 2 SO 4 atau H 3 PO 4. Sebagaimana lazimnya reaksi eliminasi, digunakan suhu tinggi. Produk alkena yang atsiri segera disuling begitu terbentuk untuk menggeser kesetimbangan ke pembentukan alkena. 30
31 Urutan reaktivitas reaksi E1 tecermin dalam konsentrasi asam dan suhu yang digunakan: (80%) (84%) Jika ada lebih dari 1 produk alkena, produk dominan ditentukan oleh aturan Zaitsev. H OH H H + H 2 C C CH CH 3 H 2 C C CH 2 CH 3 + H 3 C C CHCH 3 kalor CH 3 H 2 O CH 3 CH 3 2-metil-2-butanol 2-metil-1-butena 2-metil-2-butena produk tambahan (disubstitusi) produk utama (trisubstitusi) Penataan-ulang dimungkinkan karena reaksi melalui karbokation. 31
32 (b) Dehidrasi dengan Fosforus Oksiklorida dalam Piridina POCl 3 dalam basa lemah piridina mengubah gugus OH menjadi diklorofosfat ( OPOCl 2 ) yang mudah dieliminasi secara E2. Cara ini tidak memakai asam kuat (yang dapat merusak senyawa) dan memungkinkan dehidrasi alkohol 2 o atau 3 o pada 0 o C. Contoh: Mekanisme: 1-metilsikloheksanol 1-metilsikloheksena (96%) Soal-soal Latihan Problem Problem17.37, 17.38, 17.45, 17.48, 17.51,
33 (3) Esterifikasi (a) Ester Karboksilat (KimOrg 2) Alkohol bereaksi dengan asam karboksilat atau asil halidanya membentuk ester organik. Reaksinya disebut esterifikasi. asam benzoat (asam karboksilat) metil benzoat (ester) benzoil klorida (asil halida) (b) Ester Sulfat, Nitrit, Nitrat, dan Fosfat Reaksi esterifikasi juga berlangsung dengan H 2 SO 4, HNO 2, HNO 3, atau H 3 PO 4 membentuk ester-ester anorganik. O HO S OH O asam sulfat R OSO 3 H ester sulfat diester sulfat R OH + HO N O asam nitrit O HO N O asam nitrat O HO P OH OH asam fosfat 0 o C R ONO ester nitrit R ONO 2 ester nitrat R OPO 3 H 2 ester fosfat + H 2 O diester fosfat/ triester fosfat 33
34 Cermati perbedaan suhu yang digunakan! 0 o C CH 3 CH 2 OH + H 2 SO 4 CH 3 CH 2 OSO 3 H + H 2 O ESTERIFIKASI etanol etil sulfat 140 o C CH 3 CH 2 2 CH 3 CH 2 OH + H 2 SO 4 O + H 2 O ETERIFIKASI CH 2 CH (Bab 18) 3 dietil eter 180 o C CH 3 CH 2 OH + H 2 SO 4 H 2 C CH 2 + H 2 O ELIMINASI etilena (4) Oksidasi (a) Alkohol 1 o Larutan piridinium klorokromat (PCC) dalam CH 2 Cl 2 mengoksidasi alkohol 1 o aldehida. PCC dibuat dengan melarutkan CrO 3 dalam HCl lalu diolah dengan piridina. 34
35 (b) Alkohol 2 o Oksidator asam kromat (H 2 CrO 4 ) paling lazim digunakan, dibuat dengan menambahkan CrO 3 atau Na 2 Cr 2 O 7 ke dalam H 2 SO 4 pekat. Oksidasi dilakukan dalam aseton atau asam asetat (oksidasi Jones): Perbandingan antara oksidator PCC dan asam kromat: sitronelol (dari minyak bunga mawar) sitronelal (82%) 1-dekanol asam dekanoat (93%) testosteron (hormon seks pria) 4-androstena-3,17-dion (82%) 35
36 (c) Mekanisme Oksidasi Kromat Tahap I: Pembentukan ester kromat dari alkohol. Tahap II: Reaksi E2 eliminasi HCrO 3 membentuk ikatan C=O. Ester kromat dari alkohol 3 o tidak memiliki atom H untuk dieliminasi pada tahap II ini, maka oksidasi tidak terjadi. 36
37 Air dalam oksidator asam kromat akan mengadisi aldehida menjadi hidratnya (KimOrg 2). Ester kromat dari hidrat ini selanjutnya mengalami eliminasi membentuk asam karboksilat. Hidrat tidak terbentuk dalam pelarut diklorometana pada oksidator PCC. Oleh sebab itu, aldehida tidak teroksidasi lebih lanjut menjadi asam karboksilat. Latihan: (a) Tunjukkan bagaimana setiap pengubahan berikut dilakukan: (b) (c) (d) 37
38 Soal-soal Latihan Problem Problem , 17.27, , , 17.49, Pembuatan Fenol dalam Industri Fenol dibuat pertama kali dalam industri sebagai bahan baku asam pikrat (2,4,6-trinitrofenol) untuk bahan peledak. Sekarang ini fenol dibuat terutama untuk produksi resin fenolformaldehida (Bakelit) antara lain untuk perekat kayu lapis. OH OH OH OH CH 2 CH 2 fenol CH 2 O H+, kalor formaldehida H 2 O HO CH 2 OH CH 2 CH 2 CH 2 segmen dari Bakelit OH 38
39 Fenol juga merupakan bahan baku untuk sintesis fenol berklorin serta pengawet makanan BHT dan BHA. pentaklorofenol (pengawet kayu) asam 2,4-diklorofenoksiasetat (herbisida 2,4-D) heksaklorofena (antiseptik) hidroksitoluena berbutil (BHT) hidroksianisol berbutil (BHA) (1) Hidrolisis Klorobenzena (Proses Dow) Klorobenzena dipanaskan dengan NaOH berair pada tekanan tinggi: Reaksi kemungkinan berlangsung dengan mekanisme benzuna. (2) Pelelehan-Basa Natrium Benzenasulfonat Natrium benzenasulfonat dilelehkan dengan NaOH: 39
40 (3) Benzena + Propena Fenol + Aseton Paling banyak digunakan saat ini karena bahan bakunya murah dan mudah didapat. Tahap I: Alkilasi Friedel-Crafts benzena dengan propena. kumena Tahap II: Oksidasi radikal benzilik kumena dengan O 2 dari udara. kumena hidroperoksida Tahap III: Migrasi berkataliskan-asam fenil ke atom oksigen kationik Mekanisme: fenol aseton Migrasi fenil lebih cenderung terjadi daripada migrasi metil. 40
41 17.6 Reaksi Fenol (1) Substitusi Elektrofilik Aromatik Gugus hidroksil pengaktif kuat dan pengarah o-/p-. Reaksi brominasi, nitrasi, dan sulfonasi dapat dijalani. CS 2 dan suhu rendah menurunkan reaktivitas elektrofilik bromin monobrominasi fenol, terutama membentuk isomer para: o-nitrofenol lebih atsiri dan terdistilasi oleh uap. (Rendemen rendah karena bersaing dengan oksidasi cincin.) 41
42 (2) Reaksi Kolbe: Sintesis Asam Salisilat Ion fenoksida lebih rentan terhadap S E Ar daripada fenolnya, dan bereaksi dengan CO 2 menghasilkan asam salisilat: Reaksi asam salisilat dengan anhidrida asetat menghasilkan pereda nyeri yang dikenal luas aspirin: (3) Reaksi Reimer-Tiemann: Sintesis Salisilaldehida 42
43 (4) Oksidasi Hidrokuinon Oksidator lemah mengoksidasi hidrokuinon menjadi p-benzokuinon: Oksidasi-reduksi reversibel ini lazim digunakan di alam untuk transfer sepasang elektron dari satu substrat ke substrat lain. Oksidasi fenol sendiri memerlukan oksidator kuat. Dahulu digunakan Na 2 Cr 2 O 7, sekarang ini lebih lazim dipakai garam Fremy [kalium nitrosodisulfonat, (KSO 3 ) 2 NO]. Reaksi berlangsung pada kondisi lembut melalui mekanisme radikal. Benzokuinon yang dihasilkan mudah direduksi dengan reduktor seperti SnCl 2 atau NaBH 4. 43
44 Problem Problem Soal-soal Latihan 44
45 45
46 46
BAB 17 ALKOHOL DAN FENOL
 Slaid kuliah Kimia Organik I untuk mhs S1 Kimia semester 3 BAB 17 ALKOHOL DAN FENOL Bagian Kimia Organik Departemen Kimia FMIPA-IPB TIU TIK 1 Daftar Pustaka: Fessenden RJ, Fessenden JS. 1998. Organic Chemistry.
Slaid kuliah Kimia Organik I untuk mhs S1 Kimia semester 3 BAB 17 ALKOHOL DAN FENOL Bagian Kimia Organik Departemen Kimia FMIPA-IPB TIU TIK 1 Daftar Pustaka: Fessenden RJ, Fessenden JS. 1998. Organic Chemistry.
Eter dan Epoksida. Budi Arifin. Bagian Kimia Organik Departemen Kimia FMIPA IPB. Tata Nama (dan Penggolongan) R OR'
 Eter dan Epoksida Budi Arifin Bagian Kimia rganik Departemen Kimia FMIPA IPB Tata Nama (dan Penggolongan) ETER rantai induk alkana (atom C lebih banyak) R R' cabang alkoksi (atom C lebih sedikit) Nama
Eter dan Epoksida Budi Arifin Bagian Kimia rganik Departemen Kimia FMIPA IPB Tata Nama (dan Penggolongan) ETER rantai induk alkana (atom C lebih banyak) R R' cabang alkoksi (atom C lebih sedikit) Nama
MAKALAH PRAKTIKUM KIMIA DASAR REAKSI-REAKSI ALKOHOL DAN FENOL
 MAKALAH PRAKTIKUM KIMIA DASAR REAKSI-REAKSI ALKOHOL DAN FENOL Oleh : ZIADUL FAIEZ (133610516) PROGRAM STUDI TEKNIK GEOLOGI FAKULTAS TEKNIK UNIVERSITAS ISLAM RIAU PEKANBARU 2015 BAB I PENDAHULUAN LatarBelakang
MAKALAH PRAKTIKUM KIMIA DASAR REAKSI-REAKSI ALKOHOL DAN FENOL Oleh : ZIADUL FAIEZ (133610516) PROGRAM STUDI TEKNIK GEOLOGI FAKULTAS TEKNIK UNIVERSITAS ISLAM RIAU PEKANBARU 2015 BAB I PENDAHULUAN LatarBelakang
Chapter 20 ASAM KARBOKSILAT
 Chapter 20 ASAM KARBOKSILAT Pengantar Gugus fungsi dari asam karboksilat terdiri atas ikatan C=O dengan OH pada karbon yang sama. Gugus karboksil biasanya ditulis -COOH. Asam alifatik memiliki gugus alkil
Chapter 20 ASAM KARBOKSILAT Pengantar Gugus fungsi dari asam karboksilat terdiri atas ikatan C=O dengan OH pada karbon yang sama. Gugus karboksil biasanya ditulis -COOH. Asam alifatik memiliki gugus alkil
Senyawa Alkohol dan Senyawa Eter. Sulistyani, M.Si
 Senyawa Alkohol dan Senyawa Eter Sulistyani, M.Si sulistyani@uny.ac.id Konsep Dasar Senyawa Organik Senyawa organik adalah senyawa yang sumber utamanya berasal dari tumbuhan, hewan, atau sisa-sisa organisme
Senyawa Alkohol dan Senyawa Eter Sulistyani, M.Si sulistyani@uny.ac.id Konsep Dasar Senyawa Organik Senyawa organik adalah senyawa yang sumber utamanya berasal dari tumbuhan, hewan, atau sisa-sisa organisme
ALKOHOL DAN ETER. Tim Dosen Kimia Dasar II/ Kimia Organik
 ALKOHOL DAN ETER Tim Dosen Kimia Dasar II/ Kimia Organik 1 SUMBER ALKOHOL DAN ETER Alkohol didapatkan dengan berbagai cara yaitu dapat dibuat dengan cara fermentasi terhadap bahan bahan yang mengandung
ALKOHOL DAN ETER Tim Dosen Kimia Dasar II/ Kimia Organik 1 SUMBER ALKOHOL DAN ETER Alkohol didapatkan dengan berbagai cara yaitu dapat dibuat dengan cara fermentasi terhadap bahan bahan yang mengandung
ALKHOHOL-ETER. Putri Anjarsari, S.Si., M.Pd
 ALKOOL-ETER Putri Anjarsari, S.Si., M.Pd putri_anjarsari@uny.ac.id 1 STRUKTUR ALKOOL Alkohol adalah senyawa yang molekulnya memiliki suatu gugus hidroksil, yang terikat pada suatu atom karbon jenuh. C
ALKOOL-ETER Putri Anjarsari, S.Si., M.Pd putri_anjarsari@uny.ac.id 1 STRUKTUR ALKOOL Alkohol adalah senyawa yang molekulnya memiliki suatu gugus hidroksil, yang terikat pada suatu atom karbon jenuh. C
SENYAWA TURUNAN ALKANA. Alkohol - Eter, Aldehid - Keton, Asam Karboksilat - Ester
 SENYAWA TURUNAN ALKANA Alkohol - Eter, Aldehid - Keton, Asam Karboksilat - Ester Tata Nama Senyawa Turunan Alkana Nomor cabang-cabang-nama cabang urut abjad-nomor gugus fungsi-nama induk 1. Mengidentifikasi
SENYAWA TURUNAN ALKANA Alkohol - Eter, Aldehid - Keton, Asam Karboksilat - Ester Tata Nama Senyawa Turunan Alkana Nomor cabang-cabang-nama cabang urut abjad-nomor gugus fungsi-nama induk 1. Mengidentifikasi
ETER dan EPOKSIDA. Oleh : Dr. Yahdiana Harahap, MS
 ETER dan EPOKSIDA Oleh : Dr. Yahdiana Harahap, MS ETER Senyawa yang mempunyai 2 gugus organik melekat pada atom O tunggal R1 O R 2 atau Ar O R Atau Ar O Ar Ket : R : alkil Ar : fenil atau gugus aromatis
ETER dan EPOKSIDA Oleh : Dr. Yahdiana Harahap, MS ETER Senyawa yang mempunyai 2 gugus organik melekat pada atom O tunggal R1 O R 2 atau Ar O R Atau Ar O Ar Ket : R : alkil Ar : fenil atau gugus aromatis
BAB V ALKOHOL, ETER DAN SENYAWA YANG BERHUBUNGAN
 BAB V ALKOHOL, ETER DAN SENYAWA YANG BERHUBUNGAN 1. Pendahuluan etanol suatu alkohol fenol dietil eter suatu eter propilena oksida suatu epoksida 2. Ikatan dalam alcohol dan eter Eter dapat berbentuk rantai
BAB V ALKOHOL, ETER DAN SENYAWA YANG BERHUBUNGAN 1. Pendahuluan etanol suatu alkohol fenol dietil eter suatu eter propilena oksida suatu epoksida 2. Ikatan dalam alcohol dan eter Eter dapat berbentuk rantai
REAKSI-REAKSI ALKOHOL DAN FENOL
 REAKSI-REAKSI ALKHL DAN FENL TUJUAN Tujuan dari Percobaan ini adalah: 1. Membedakan alkohol dengan fenol berdasarkan reaksinya dengan asam karboksilat 2. Membedakan alkohol dan fenol berdasarkan reaksi
REAKSI-REAKSI ALKHL DAN FENL TUJUAN Tujuan dari Percobaan ini adalah: 1. Membedakan alkohol dengan fenol berdasarkan reaksinya dengan asam karboksilat 2. Membedakan alkohol dan fenol berdasarkan reaksi
KIMIA. Sesi HIDROKARBON (BAGIAN II) A. ALKANON (KETON) a. Tata Nama Alkanon
 KIMIA KELAS XII IPA - KURIKULUM GABUNGAN 16 Sesi NGAN HIDROKARBON (BAGIAN II) Gugus fungsional adalah sekelompok atom dalam suatu molekul yang memiliki karakteristik khusus. Gugus fungsional adalah bagian
KIMIA KELAS XII IPA - KURIKULUM GABUNGAN 16 Sesi NGAN HIDROKARBON (BAGIAN II) Gugus fungsional adalah sekelompok atom dalam suatu molekul yang memiliki karakteristik khusus. Gugus fungsional adalah bagian
Gugus Fungsi. Gugus Fungsi. Gugus Fungsi. Gugus Fungsi CH 3 -CH 3 O O H 2 C CH 2 C O C C S C O CH 3 C OCH 2 CH 3 H C NH 2 CH 3 C NH 2. Alkana.
 Gugus Fungsi Struktur Golongan Senyawa ontoh spesifik Gugus Fungsi Struktur Golongan Senyawa ontoh spesifik Alkana - Alkohol Alkena Fenol Alkuna Arena (aromatik) S Tiol (Merkaptan) S Eter X Alkil halida
Gugus Fungsi Struktur Golongan Senyawa ontoh spesifik Gugus Fungsi Struktur Golongan Senyawa ontoh spesifik Alkana - Alkohol Alkena Fenol Alkuna Arena (aromatik) S Tiol (Merkaptan) S Eter X Alkil halida
MODUL SENYAWA KARBON ( Alkohol dan Eter )
 MODUL SENYAWA KARBON ( Alkohol dan Eter ) A. TATANAMA IUPAC ( Internasional Union of Pure and Applied Chemistry )/sistematika Trivial/Lazim/Dagang CONTOH A.1. ALKOHOL IUPAC 1. Tentukan rantai atom C terpanjang
MODUL SENYAWA KARBON ( Alkohol dan Eter ) A. TATANAMA IUPAC ( Internasional Union of Pure and Applied Chemistry )/sistematika Trivial/Lazim/Dagang CONTOH A.1. ALKOHOL IUPAC 1. Tentukan rantai atom C terpanjang
OH (Metil alkohol = Metanol) CH 2. OH (etil alkohol = etanol) OH (1-propanol = n-propanol)
 Rumus umum R-O Gugus fungsional: O (gugus hidroksil) Tata nama Diturunkan dari gugus alkil yang melekat pada O, kemudian ditambah kata alkohol. Dalam sistem IUPAC: akhiran ol menunjukan adanya gugus hidroksil
Rumus umum R-O Gugus fungsional: O (gugus hidroksil) Tata nama Diturunkan dari gugus alkil yang melekat pada O, kemudian ditambah kata alkohol. Dalam sistem IUPAC: akhiran ol menunjukan adanya gugus hidroksil
Kelompok G : Nicolas oerip ( ) Filia irawati ( ) Ayndri Nico P ( )
 Kelompok G : Nicolas oerip (5203011028) Filia irawati (5203011029) Ayndri Nico P (5203011040) Mempelajari reaksi esterifikasi Apa sih reaksi esterifikasi itu? Bagaimana reaksi esterifikasi itu? Reaksi
Kelompok G : Nicolas oerip (5203011028) Filia irawati (5203011029) Ayndri Nico P (5203011040) Mempelajari reaksi esterifikasi Apa sih reaksi esterifikasi itu? Bagaimana reaksi esterifikasi itu? Reaksi
Materi Penunjang Media Pembelajaran Kimia Organik SMA ALKENA
 ALKENA Nama lain alkena adalah olefin atau senyawa vinil. Alkena termasuk senyawa organik tak jenuh. Alkena merupakan senyawa yang relatif stabil, akan tetapi lebih reaktif dari alkana karena terdapatnya
ALKENA Nama lain alkena adalah olefin atau senyawa vinil. Alkena termasuk senyawa organik tak jenuh. Alkena merupakan senyawa yang relatif stabil, akan tetapi lebih reaktif dari alkana karena terdapatnya
Secara umum terdapat 4 tipe reaksi kimia organik: 1. Reaksi substitusi (Penggantian)
 Secara umum terdapat 4 tipe reaksi kimia organik: 1. Reaksi substitusi (Penggantian) Suatu atom/gugus di dalam suatu senyawa diganti oleh suatu atom/gugus lain dari senyawa yang lain. Konsep dasarnya adalah
Secara umum terdapat 4 tipe reaksi kimia organik: 1. Reaksi substitusi (Penggantian) Suatu atom/gugus di dalam suatu senyawa diganti oleh suatu atom/gugus lain dari senyawa yang lain. Konsep dasarnya adalah
Soal-Soal. Bab 14. Latihan. Kimia Karbon II: Gugus Fungsi. Alkohol dan Eter. 1. Rumus struktur alkohol ditunjukkan oleh. (A) C 2
 Bab 14 Kimia Karbon II: Gugus Fungsi Soal-Soal Latihan Alkohol dan Eter 1. Rumus struktur alkohol ditunjukkan oleh. (A) C 2 (B) -CH (C) -CH(H)-C 2 (D) C 3 H 7 -C- (E) -CH 2. Suatu senyawa dengan rumus
Bab 14 Kimia Karbon II: Gugus Fungsi Soal-Soal Latihan Alkohol dan Eter 1. Rumus struktur alkohol ditunjukkan oleh. (A) C 2 (B) -CH (C) -CH(H)-C 2 (D) C 3 H 7 -C- (E) -CH 2. Suatu senyawa dengan rumus
BAB I PENDAHULUAN. Dari uraian latar belakang diatas dirumuskan permasalahan sebagai berikut:
 BAB I PENDAHULUAN 1.1 Latar belakang Dalam kehidupan sehari-hari kita banyak menjumpai senyawa, baik senyawa organik maupun anorganik. Senyawa organik sangat banyak jenisnya, sehingga perlu adanya penggolongan
BAB I PENDAHULUAN 1.1 Latar belakang Dalam kehidupan sehari-hari kita banyak menjumpai senyawa, baik senyawa organik maupun anorganik. Senyawa organik sangat banyak jenisnya, sehingga perlu adanya penggolongan
Struktur Aldehid. Tatanama Aldehida. a. IUPAC Nama aldehida dinerikan dengan mengganti akhiran a pada nama alkana dengan al.
 Kamu tentunya pernah menyaksikan berita tentang penyalah gunaan formalin. Formalin merupakan salah satu contoh senyawa aldehid. Melalui topik ini, kamu tidak hanya akan mempelajari kegunaan aldehid yang
Kamu tentunya pernah menyaksikan berita tentang penyalah gunaan formalin. Formalin merupakan salah satu contoh senyawa aldehid. Melalui topik ini, kamu tidak hanya akan mempelajari kegunaan aldehid yang
(2) kekuatan ikatan yang dibentuk untuk karbon;
 Reaksi Subsitusi Nukleofilik Alifatik Reaksi yang berlangsung karena penggantian satu atau lebih atom atau gugus dari suatu senyawa oleh atom atau gugus lain disebut reaksi substitusi. Bila reaksi substitusi
Reaksi Subsitusi Nukleofilik Alifatik Reaksi yang berlangsung karena penggantian satu atau lebih atom atau gugus dari suatu senyawa oleh atom atau gugus lain disebut reaksi substitusi. Bila reaksi substitusi
1.Pengertian alkohol 2.Klasifikasi alkohol 3.Sifat-sifat fisika dan kimia alkohol 4.Sintesis alkohol 5.Reaksi-reaksi alkohol 6.
 1.Pengertian alkohol 2.Klasifikasi alkohol 3.Sifat-sifat fisika dan kimia alkohol 4.Sintesis alkohol 5.Reaksi-reaksi alkohol 6.Tata nama alkohol 7.Contoh-contoh alkohol dan kegunaannya senyawa organik
1.Pengertian alkohol 2.Klasifikasi alkohol 3.Sifat-sifat fisika dan kimia alkohol 4.Sintesis alkohol 5.Reaksi-reaksi alkohol 6.Tata nama alkohol 7.Contoh-contoh alkohol dan kegunaannya senyawa organik
Gugus Fungsi Senyawa Karbon
 Gugus Fungsi Senyawa Karbon Gugus fungsi merupakan bagian aktif dari senyawa karbon yang menentukan sifat-sifat senyawa karbon. Gugus fungsi tersebut berupa ikatan karbon rangkap dua, ikatan karbon rangkap
Gugus Fungsi Senyawa Karbon Gugus fungsi merupakan bagian aktif dari senyawa karbon yang menentukan sifat-sifat senyawa karbon. Gugus fungsi tersebut berupa ikatan karbon rangkap dua, ikatan karbon rangkap
BAB 8 ALKUNA. Bagian Kimia Organik Departemen Kimia FMIPA IPB. Slaid kuliah Kimia Organik I untuk mhs S1 Kimia semester 3.
 Slaid kuliah Kimia Organik I untuk mhs S1 Kimia semester 3 BAB 8 ALKUNA Budi Arifin (dibantu oleh Dumas Flis Tang) Bagian Kimia Organik Departemen Kimia FMIPA IPB TIU TIK Daftar Pustaka: McMurry J. 2008.
Slaid kuliah Kimia Organik I untuk mhs S1 Kimia semester 3 BAB 8 ALKUNA Budi Arifin (dibantu oleh Dumas Flis Tang) Bagian Kimia Organik Departemen Kimia FMIPA IPB TIU TIK Daftar Pustaka: McMurry J. 2008.
MODUL KIMIA SMA IPA Kelas 12
 A. BENZENA 1. Rumus a. Rumus molekul : C 6H 6 b. Rumus bangun : 2. Hibridisasi Struktur Kekule, setiap atom C dalam benzena membentuk 3 ikatan sigma = ( sp 2 ) 3 dan 1 ikatan phi = ( p-p ) 1. Hal ini dapat
A. BENZENA 1. Rumus a. Rumus molekul : C 6H 6 b. Rumus bangun : 2. Hibridisasi Struktur Kekule, setiap atom C dalam benzena membentuk 3 ikatan sigma = ( sp 2 ) 3 dan 1 ikatan phi = ( p-p ) 1. Hal ini dapat
Eter dan Epoksida. Bagian Kimia Organik Departemen Kimia FMIPA IPB
 Eter dan Epoksida Bagian Kimia Organik Departemen Kimia FMIPA IPB Eter yang paling banyak penggunaan nya ialah dietil eter, anisol, dan THF Apa kegunaan / aplikasi ketiganya? Tiol (R-S-R) dan sulfida (R-S-H)
Eter dan Epoksida Bagian Kimia Organik Departemen Kimia FMIPA IPB Eter yang paling banyak penggunaan nya ialah dietil eter, anisol, dan THF Apa kegunaan / aplikasi ketiganya? Tiol (R-S-R) dan sulfida (R-S-H)
TURUNAN ASAM KARBOKSILAT DAN REAKSI SUBSTITUSI ASIL NUKLEOFILIK
 BAB 4 TURUNAN ASAM KARBOKSILAT DAN REAKSI SUBSTITUSI ASIL NUKLEOFILIK Asam karboksilat hanya merupakan salah satu anggota kelas turunan asil, RCOX, di mana substituen X mungkin oksigen, halogen, nitrogen
BAB 4 TURUNAN ASAM KARBOKSILAT DAN REAKSI SUBSTITUSI ASIL NUKLEOFILIK Asam karboksilat hanya merupakan salah satu anggota kelas turunan asil, RCOX, di mana substituen X mungkin oksigen, halogen, nitrogen
KIMIA. Sesi. Benzena A. STRUKTUR DAN SIFAT BENZENA. Benzena merupakan senyawa hidrokarbon dengan rumus molekul C 6 H 6
 KIMIA KELAS XII IPA - KURIKULUM GABUNGAN 18 Sesi NGAN Benzena Benzena merupakan senyawa hidrokarbon dengan rumus molekul C 6 H 6 dengan struktur berbentuk cincin (siklik) segienam beraturan. Struktur kimia
KIMIA KELAS XII IPA - KURIKULUM GABUNGAN 18 Sesi NGAN Benzena Benzena merupakan senyawa hidrokarbon dengan rumus molekul C 6 H 6 dengan struktur berbentuk cincin (siklik) segienam beraturan. Struktur kimia
SIFAT KIMIA DAN FISIK SENYAWA HIDROKARBON
 SIFAT KIMIA DAN FISIK SENYAWA HIDROKARBON Muhammad Ja far Sodiq (0810920047) 1. ALKANA Pada suhu biasa, metana, etana, propana, dan butana berwujud gas. Pentena sampai heptadekana (C 17 H 36 ) berwujud
SIFAT KIMIA DAN FISIK SENYAWA HIDROKARBON Muhammad Ja far Sodiq (0810920047) 1. ALKANA Pada suhu biasa, metana, etana, propana, dan butana berwujud gas. Pentena sampai heptadekana (C 17 H 36 ) berwujud
LAPORAN PRAKTIKUM KIMIA ORGANIK (KI2051)
 LAPORAN PRAKTIKUM KIMIA ORGANIK (KI2051) PERCOBAAN 5 Alkohol dan Fenol: Sifat Fisik dan Reaksi Kimia DIAH RATNA SARI 11609010 KELOMPOK I Tanggal Percobaan : 27 Oktober 2010 Shift Rabu Siang (13.00 17.00
LAPORAN PRAKTIKUM KIMIA ORGANIK (KI2051) PERCOBAAN 5 Alkohol dan Fenol: Sifat Fisik dan Reaksi Kimia DIAH RATNA SARI 11609010 KELOMPOK I Tanggal Percobaan : 27 Oktober 2010 Shift Rabu Siang (13.00 17.00
REAKSI SUBSTITUSI ALFA KARBONIL
 BAB 5 REAKSI SUBSTITUSI ALFA KARBONIL Dalam bab ini akan dibahas mengenai reaksi substitusi alfa. Ciri utama dari reaksi ini adalah terjadi melalui pembentukan intermediet enol atau ion enolat. 5.1. Keto-enol
BAB 5 REAKSI SUBSTITUSI ALFA KARBONIL Dalam bab ini akan dibahas mengenai reaksi substitusi alfa. Ciri utama dari reaksi ini adalah terjadi melalui pembentukan intermediet enol atau ion enolat. 5.1. Keto-enol
ALKOHOL. Struktur, Tatanama dan Sintesis Alkohol
 ALKL Struktur, Tatanama dan Sintesis Alkohol Struktur, Tatanama dan Sintesis Alkohol Struktur Alkohol Gugus fungsional : Hidroksil (-) Hibridisasi orbital atom ksigen : sp 3 3 Klasifikasi Alkohol Alkohol
ALKL Struktur, Tatanama dan Sintesis Alkohol Struktur, Tatanama dan Sintesis Alkohol Struktur Alkohol Gugus fungsional : Hidroksil (-) Hibridisasi orbital atom ksigen : sp 3 3 Klasifikasi Alkohol Alkohol
Bab 8 Eter dan Epoksida. Robby Noor Cahyono, S.Si., M.Sc.
 Bab 8 Eter dan Epoksida Robby Noor Cahyono, S.Si., M.Sc. Pendahuluan Rumus umum R-O-R dimana R adalah gugus alkil atau aril. Simetris atau asimetris Robby Noor Cahyono, S.Si., M.Sc. 2 Struktur and Polaritas
Bab 8 Eter dan Epoksida Robby Noor Cahyono, S.Si., M.Sc. Pendahuluan Rumus umum R-O-R dimana R adalah gugus alkil atau aril. Simetris atau asimetris Robby Noor Cahyono, S.Si., M.Sc. 2 Struktur and Polaritas
REAKSI PENATAAN ULANG. perpindahan (migrasi) tersebut adalah dari suatu atom ke atom yang lain yang
 EAKSI PENATAAN ULANG eaksi penataan ulang adalah reaksi penataan kembali struktur molekul untuk membentuk struktur molekul yang baru yang berbeda dengan struktur molekul yang semula. eaksi ini dapat terjadi
EAKSI PENATAAN ULANG eaksi penataan ulang adalah reaksi penataan kembali struktur molekul untuk membentuk struktur molekul yang baru yang berbeda dengan struktur molekul yang semula. eaksi ini dapat terjadi
LAPORAN PRAKTIKUM KIMIA ORGANIK (KI2051)
 LAPORAN PRAKTIKUM KIMIA ORGANIK (KI2051) LAPORAN PRAKTIKUM KIMIA ORGANIK (KI2051) PERCOBAAN 5 Alkohol dan Fenol: Sifat Fisik dan Reaksi Kimia PERCOBAAN 6 Aldehid dan Keton: Sifat Fisik dan Reaksi Kimia
LAPORAN PRAKTIKUM KIMIA ORGANIK (KI2051) LAPORAN PRAKTIKUM KIMIA ORGANIK (KI2051) PERCOBAAN 5 Alkohol dan Fenol: Sifat Fisik dan Reaksi Kimia PERCOBAAN 6 Aldehid dan Keton: Sifat Fisik dan Reaksi Kimia
Alkohol, Phenol. Sifat-Sifat alkohol dan Phenol: Ikatan Hydrogen
 Alkohol, Phenol Sifat-Sifat alkohol dan Phenol: Ikatan ydrogen Struktur alkohol dan phenol,menyerupai molekul air, mempunyai hibridisasi, sp 3. Alkohol dan phenol mempunyai ttk didih yg lebih besar dari
Alkohol, Phenol Sifat-Sifat alkohol dan Phenol: Ikatan ydrogen Struktur alkohol dan phenol,menyerupai molekul air, mempunyai hibridisasi, sp 3. Alkohol dan phenol mempunyai ttk didih yg lebih besar dari
OAL TES SEMESTER II. I. Pilihlah huruf a, b, c, d, atau e pada jawaban yang tepat!
 KIMIA XII SMA 249 S AL TES SEMESTER II I. Pilihlah huruf a, b, c, d, atau e pada jawaban yang tepat! 1. Suatu senyawa karbondioksida dengan tembaga pijar dan hasil oksidasinya diuji dengan pereaksi fehling
KIMIA XII SMA 249 S AL TES SEMESTER II I. Pilihlah huruf a, b, c, d, atau e pada jawaban yang tepat! 1. Suatu senyawa karbondioksida dengan tembaga pijar dan hasil oksidasinya diuji dengan pereaksi fehling
Aldehid dan Keton. Sulistyani, M.Si
 Aldehid dan Keton Sulistyani, M.Si sulistyani@uny.ac.id Konsep Dasar Golongan aldehid disebut juga alkanal dan golongan keton disebut juga alkanon. Keduanya berisomer fungsional, karena mempunyai rumus
Aldehid dan Keton Sulistyani, M.Si sulistyani@uny.ac.id Konsep Dasar Golongan aldehid disebut juga alkanal dan golongan keton disebut juga alkanon. Keduanya berisomer fungsional, karena mempunyai rumus
BAB 7 HIDROKARBON DAN MINYAK BUMI
 BAB 7 HIDROKARBON DAN MINYAK BUMI A. Kekhasan / Keunikan Atom Karbon o Terletak pada golongan IVA dengan Z = 6 dan mempunyai 4 elektron valensi. o Untuk mencapai konfigurasi oktet maka atom karbon mempunyai
BAB 7 HIDROKARBON DAN MINYAK BUMI A. Kekhasan / Keunikan Atom Karbon o Terletak pada golongan IVA dengan Z = 6 dan mempunyai 4 elektron valensi. o Untuk mencapai konfigurasi oktet maka atom karbon mempunyai
berupa ikatan tunggal, rangkap dua atau rangkap tiga. o Atom karbon mempunyai kemampuan membentuk rantai (ikatan yang panjang).
 HIDROKARBON Senyawa hidrokarbon merupakan senyawa karbon yang paling sederhana. Dari namanya, senyawa hidrokarbon adalah senyawa karbon yang hanya tersusun dari atom hidrogen dan atom karbon. Dalam kehidupan
HIDROKARBON Senyawa hidrokarbon merupakan senyawa karbon yang paling sederhana. Dari namanya, senyawa hidrokarbon adalah senyawa karbon yang hanya tersusun dari atom hidrogen dan atom karbon. Dalam kehidupan
JURNAL PRAKTIKUM KIMIA ORGANIK : Identifikasi Gugus Fungsional Senyawa Organik
 Paraf Asisten Judul JURNAL PRAKTIKUM KIMIA ORGANIK : Identifikasi Gugus Fungsional Senyawa Organik Tujuan Percobaan : 1. Mempelajari teknik pengukuran fisik untuk mengidentifikasi suatu senyawa organik
Paraf Asisten Judul JURNAL PRAKTIKUM KIMIA ORGANIK : Identifikasi Gugus Fungsional Senyawa Organik Tujuan Percobaan : 1. Mempelajari teknik pengukuran fisik untuk mengidentifikasi suatu senyawa organik
ALDEHID DAN KETON. Putri Anjarsari, S.Si., M.Pd
 ALDEHID DAN KETN Putri Anjarsari, S.Si., M.Pd putri_anjarsari@uny.ac.id ontoh senyawa-senyawa karbonil penting H 3 H Asam asetat (asam cuka) H N H H 3 Asetaminofen (analgesik, antipiretik) H H 3 Asam asetil
ALDEHID DAN KETN Putri Anjarsari, S.Si., M.Pd putri_anjarsari@uny.ac.id ontoh senyawa-senyawa karbonil penting H 3 H Asam asetat (asam cuka) H N H H 3 Asetaminofen (analgesik, antipiretik) H H 3 Asam asetil
1. Senyawa di bawah ini yang memiliki ikatan hidrogen antarmolekulnya adalah. A. CH 3 -CHO D. CH 3 E. CH 3
 KIMIA KELAS XII IPA - KURIKULUM GABUNGAN 20 Sesi NGAN Review III (HIDROKARBON, REAKSI-REAKSI SENYAWA KARBON DAN ISOMER, BENZENA, POLIMER) A. HIDROKARBON 1. Senyawa di bawah ini yang memiliki ikatan hidrogen
KIMIA KELAS XII IPA - KURIKULUM GABUNGAN 20 Sesi NGAN Review III (HIDROKARBON, REAKSI-REAKSI SENYAWA KARBON DAN ISOMER, BENZENA, POLIMER) A. HIDROKARBON 1. Senyawa di bawah ini yang memiliki ikatan hidrogen
OLIMPIADE SAINS NASIONAL CALON PESERTA INTERNATIONAL CHEMISTRY OLYMPIAD (IChO) Yogyakarta Mei Lembar Jawab.
 Hak Cipta Dilindungi Undang-undang OLIMPIADE SAINS NASIONAL 2015 CALON PESERTA INTERNATIONAL CHEMISTRY OLYMPIAD (IChO) 2016 Yogyakarta 18-24 Mei 2015 Lembar Jawab Kimia TEORI Waktu: 240 menit KEMENTERIAN
Hak Cipta Dilindungi Undang-undang OLIMPIADE SAINS NASIONAL 2015 CALON PESERTA INTERNATIONAL CHEMISTRY OLYMPIAD (IChO) 2016 Yogyakarta 18-24 Mei 2015 Lembar Jawab Kimia TEORI Waktu: 240 menit KEMENTERIAN
BAB VIII ALKENA DAN ALKUNA
 BAB VIII ALKENA DAN ALKUNA 1. Ikatan dalam alkena dan alkuna Keasaman : Alkuna> Alkena> Alkana (sp > sp 2 > sp 3 ) Karena untuk sp karakter s = 50% dan p = 50%, sehingga elektron dalam orbital lebih dekat
BAB VIII ALKENA DAN ALKUNA 1. Ikatan dalam alkena dan alkuna Keasaman : Alkuna> Alkena> Alkana (sp > sp 2 > sp 3 ) Karena untuk sp karakter s = 50% dan p = 50%, sehingga elektron dalam orbital lebih dekat
BENZENA. Memahami senyawa organik dan reaksinya, benzena dan turunannya, dan makromolekul.
 Standar Kompetensi: BENZENA Memahami senyawa organik dan reaksinya, benzena dan turunannya, dan makromolekul. Kompetensi Dasar: Mendeskripsikan struktur, cara penulisan, tata nama, sifat, dan kegunaan
Standar Kompetensi: BENZENA Memahami senyawa organik dan reaksinya, benzena dan turunannya, dan makromolekul. Kompetensi Dasar: Mendeskripsikan struktur, cara penulisan, tata nama, sifat, dan kegunaan
LAPORAN PRAKTIKUM KIMIA ORGANIK
 LAPORAN PRAKTIKUM KIMIA ORGANIK ACARA 4 SENYAWA ASAM KARBOKSILAT DAN ESTER Oleh: Kelompok 5 Nova Damayanti A1M013012 Nadhila Benita Prabawati A1M013040 KEMENTRIAN PENDIDIKAN DAN KEBUDAYAAN UNIVERSITAS
LAPORAN PRAKTIKUM KIMIA ORGANIK ACARA 4 SENYAWA ASAM KARBOKSILAT DAN ESTER Oleh: Kelompok 5 Nova Damayanti A1M013012 Nadhila Benita Prabawati A1M013040 KEMENTRIAN PENDIDIKAN DAN KEBUDAYAAN UNIVERSITAS
Pembahasan Soal Multiplechoice OSK Kimia Tahun 2014 Oleh Urip
 Pembahasan Soal Multiplechoice OSK Kimia Tahun 2014 Oleh Urip Kalteng @ http://urip.wordpress.com Dengan senang hati jika ada yang mau mengoreksi pembahasan ini A. Pilih jawaban yang paling tepat ( 25
Pembahasan Soal Multiplechoice OSK Kimia Tahun 2014 Oleh Urip Kalteng @ http://urip.wordpress.com Dengan senang hati jika ada yang mau mengoreksi pembahasan ini A. Pilih jawaban yang paling tepat ( 25
BAB 10. Aromatisitas, Benzena, dan Benzena Tersubstitusi. Tabel Struktur dan nama-nama benzene yang umum
 BAB 10 Aromatisitas, Benzena, dan Benzena Tersubstitusi 10.1 Tata Nama Benzena Tersubstitusi Benzena tersubstitusi diberi nama dengan awalan orto, meta, para dan tidak dengan nomor-nomor posisi. Awalan
BAB 10 Aromatisitas, Benzena, dan Benzena Tersubstitusi 10.1 Tata Nama Benzena Tersubstitusi Benzena tersubstitusi diberi nama dengan awalan orto, meta, para dan tidak dengan nomor-nomor posisi. Awalan
LAPORAN PRAKTIKUM KIMIA ORGANIK (KI2051)
 LAPORAN PRAKTIKUM KIMIA ORGANIK (KI2051) PERCOBAAN 5 Alkohol dan Fenol: Sifat Fisik dan Reaksi Kimia PERCOBAAN 6 Aldehid dan Keton: Sifat Fisik dan Reaksi Kimia DIAH RATNA SARI 11609010 KELOMPOK I Tanggal
LAPORAN PRAKTIKUM KIMIA ORGANIK (KI2051) PERCOBAAN 5 Alkohol dan Fenol: Sifat Fisik dan Reaksi Kimia PERCOBAAN 6 Aldehid dan Keton: Sifat Fisik dan Reaksi Kimia DIAH RATNA SARI 11609010 KELOMPOK I Tanggal
LAPORAN PRAKTIKUM SINTESIS SENYAWA ORGANIK : Reaksi Pembuatan Alkena dengan Dehidrasi Alkohol
 Paraf Asisten Judul LAPORAN PRAKTIKUM SINTESIS SENYAWA ORGANIK : Reaksi Pembuatan Alkena dengan Dehidrasi Alkohol Tujuan Percobaan : 1. Mempelajari reaksi dehidrasi dari suatu alkohol untuk menghasilkan
Paraf Asisten Judul LAPORAN PRAKTIKUM SINTESIS SENYAWA ORGANIK : Reaksi Pembuatan Alkena dengan Dehidrasi Alkohol Tujuan Percobaan : 1. Mempelajari reaksi dehidrasi dari suatu alkohol untuk menghasilkan
Senyawa Halogen Organik (organohalogen) Tim Dosen Kimia FTP - UB
 Senyawa alogen Organik (organohalogen) Tim Dosen Kimia FTP - UB Pendahuluan Organohalogen sebagai pelarut, insektisida, dan bahan sintesis organik. Beberapa organohalogen bersifat racun, sehingga harus
Senyawa alogen Organik (organohalogen) Tim Dosen Kimia FTP - UB Pendahuluan Organohalogen sebagai pelarut, insektisida, dan bahan sintesis organik. Beberapa organohalogen bersifat racun, sehingga harus
2. Substitusi dengan kelompok halogen OH. Halogen gugus-oh diganti dengan menggunakan pereaksi atau PCl5 PCL3:
 Analisa gugus fungsi Reaksi Kimia adalah suatu perubahan dari suatu senyawa atau molekul menjadi senyawa atau molekul lain. Reaksi yang terjadi pada senyawa anorganik biasanya reaksi antar ion, sedangkan
Analisa gugus fungsi Reaksi Kimia adalah suatu perubahan dari suatu senyawa atau molekul menjadi senyawa atau molekul lain. Reaksi yang terjadi pada senyawa anorganik biasanya reaksi antar ion, sedangkan
ASAM KARBOSILAT BAB 3
 BAB 3 ASAM KARBOSILAT 3.1. Tata nama asam karboksilat Asam karbosilat diturunkan dari alkana dengan mengganti a terminal dari alkana yang bersesuaian dengan asam oat. Atom karbon karbosilat selalu diberi
BAB 3 ASAM KARBOSILAT 3.1. Tata nama asam karboksilat Asam karbosilat diturunkan dari alkana dengan mengganti a terminal dari alkana yang bersesuaian dengan asam oat. Atom karbon karbosilat selalu diberi
Keunikan atom C?? Atom karbon primer, sekunder, tersier dan kuartener
 Keunikan atom C?? Atom karbon primer, sekunder, tersier dan kuartener Jenis ikatan karbon edakan : Propena (tak jenuh) Propuna (tak jenuh) Propana (jenuh) Rantai Atom Karbon Bedakan : 2-metil butana siklobutana
Keunikan atom C?? Atom karbon primer, sekunder, tersier dan kuartener Jenis ikatan karbon edakan : Propena (tak jenuh) Propuna (tak jenuh) Propana (jenuh) Rantai Atom Karbon Bedakan : 2-metil butana siklobutana
BENZENA DAN TURUNANNYA
 BENZENA DAN TURUNANNYA 6 benzena dan turunannya A. RUMUS MOLEKUL DAN SIFAT KHAS BENZENA B. TATA NAMA BENZENA C. KEGUNAAN TURUNAN BENZENA Kata aromatik semula digunakan untuk menggambarkan zat-zat berbau
BENZENA DAN TURUNANNYA 6 benzena dan turunannya A. RUMUS MOLEKUL DAN SIFAT KHAS BENZENA B. TATA NAMA BENZENA C. KEGUNAAN TURUNAN BENZENA Kata aromatik semula digunakan untuk menggambarkan zat-zat berbau
GUGUS FUNGSI, ISOMER DAN REAKSI
 GUGUS FUNGSI, ISOMER DAN REAKSI 1. C2H5Cl + C3H7ONa C2H5 - O - C3H7 + NaCl. Reaksi di atas merupakan reaksi. A. penyabunan adisi eliminasi netralisasi subtitusi 2. Dua senyawa yang saling berisomer mempunyai
GUGUS FUNGSI, ISOMER DAN REAKSI 1. C2H5Cl + C3H7ONa C2H5 - O - C3H7 + NaCl. Reaksi di atas merupakan reaksi. A. penyabunan adisi eliminasi netralisasi subtitusi 2. Dua senyawa yang saling berisomer mempunyai
AROMATISITAS, BENZENA DAN BENZENA TERSUBSTITUSI ACHMAD SYAHRANI ORGANIC CHEMISTRY, FESSENDEN DAN FESSENDEN, THIRD EDITION
 AROMATISITAS, BENZENA DAN BENZENA TERSUBSTITUSI ACHMAD SYAHRANI ORGANIC CHEMISTRY, FESSENDEN DAN FESSENDEN, THIRD EDITION 1 BENZENA PERTAMA KALI DIISOLASI OLEH MICHAEL FARADAY, 1825 DARI RESIDU BERMINYAK
AROMATISITAS, BENZENA DAN BENZENA TERSUBSTITUSI ACHMAD SYAHRANI ORGANIC CHEMISTRY, FESSENDEN DAN FESSENDEN, THIRD EDITION 1 BENZENA PERTAMA KALI DIISOLASI OLEH MICHAEL FARADAY, 1825 DARI RESIDU BERMINYAK
KIMIA HIDROKARBON GUGUS FUNGSI
 KMA HDRKARBN GUGUS FUNGS Gugus fungsi adalah bagian suatu molekul (substituen pada rangka hidrokarbon) yang berfungsi secara kimia Dapat bereaksi, tidak lembam Substituen (gugus fungsi) diantaranya mengandung
KMA HDRKARBN GUGUS FUNGS Gugus fungsi adalah bagian suatu molekul (substituen pada rangka hidrokarbon) yang berfungsi secara kimia Dapat bereaksi, tidak lembam Substituen (gugus fungsi) diantaranya mengandung
AMINA dan HETEROSIKLIK
 Slaid kuliah Kimia Organik II AMINA dan HETEROSIKLIK Bagian Kimia Organik Departemen Kimia FMIPA-IPB Amina tersebar luas dalam organisme hidup protein dan asam nukleat. trimetilamina nikotina kokaina Insektisida
Slaid kuliah Kimia Organik II AMINA dan HETEROSIKLIK Bagian Kimia Organik Departemen Kimia FMIPA-IPB Amina tersebar luas dalam organisme hidup protein dan asam nukleat. trimetilamina nikotina kokaina Insektisida
Bab 12 Pengenalan Kimia Organik
 Bab 12 Pengenalan Kimia Organik Sikloalkana Ikhtisar Sumber: hang Bab 11 Alkuna idrokarbon Aromatik Gugus Fungsi Departemen Kimia FMIPA IPB Kimia Organik berfokus pada kimia karbon. Beberapa karakteristik
Bab 12 Pengenalan Kimia Organik Sikloalkana Ikhtisar Sumber: hang Bab 11 Alkuna idrokarbon Aromatik Gugus Fungsi Departemen Kimia FMIPA IPB Kimia Organik berfokus pada kimia karbon. Beberapa karakteristik
kimia K-13 HIDROKARBON II K e l a s A. Alkena Tujuan Pembelajaran
 K-13 kimia K e l a s XI HIDROKARBON II Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut 1 Memahami pengertian, rumus umum, serta tata nama senyawa hidrokarbon
K-13 kimia K e l a s XI HIDROKARBON II Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut 1 Memahami pengertian, rumus umum, serta tata nama senyawa hidrokarbon
Antiremed Kelas 12 Kimia
 Antiremed Kelas 12 Kimia BAb 8 - Senyawa Karbon - Reaksi Identifikasi - Soal Doc. Name: AR12KIM0899 Version : 2013-10 halaman 1 01. Senyawa X mempunyai sifat-sifat sebagai berikut. (1) Titik didih relative
Antiremed Kelas 12 Kimia BAb 8 - Senyawa Karbon - Reaksi Identifikasi - Soal Doc. Name: AR12KIM0899 Version : 2013-10 halaman 1 01. Senyawa X mempunyai sifat-sifat sebagai berikut. (1) Titik didih relative
tanya-tanya.com Soal No.1 Tuliskan nama senyawa alkohol dan eter berikut PEMBAHASAN : Soal No.2
 Soal No.1 Tuliskan nama senyawa alkohol dan eter berikut Soal No.2 Tuliskan nama senyawa berikut dengan benar. a. (CH3)2C(OH)(CH2)2CH3 b. (CH3)3COCH3 c. CH3(CH2)2CH(C2H5)CH2OH LIHAT JUGA : Rangkuman Materi
Soal No.1 Tuliskan nama senyawa alkohol dan eter berikut Soal No.2 Tuliskan nama senyawa berikut dengan benar. a. (CH3)2C(OH)(CH2)2CH3 b. (CH3)3COCH3 c. CH3(CH2)2CH(C2H5)CH2OH LIHAT JUGA : Rangkuman Materi
KIMIAWI SENYAWA KARBONIL
 BAB 1 KIMIAWI SENYAWA KARBONIL Senyawa karbonil adalah kelompok senyawaan organik yang mengandung gugus karbonil, C=O, gugus fungsional yang paling penting dalam kimia organik. Senyawa karbonil ada di
BAB 1 KIMIAWI SENYAWA KARBONIL Senyawa karbonil adalah kelompok senyawaan organik yang mengandung gugus karbonil, C=O, gugus fungsional yang paling penting dalam kimia organik. Senyawa karbonil ada di
Aldehida dan Keton. Robby Noor Cahyono, S.Si., M.Sc.
 Aldehida dan Keton Robby Noor Cahyono, S.Si., M.Sc. Aldehida dan Keton Aldehida dan Keton ditandai dengan gugus fungsi (C=O) Senyawa terbetuk secara luas di alam sebagai perantara dalam metabolisme dan
Aldehida dan Keton Robby Noor Cahyono, S.Si., M.Sc. Aldehida dan Keton Aldehida dan Keton ditandai dengan gugus fungsi (C=O) Senyawa terbetuk secara luas di alam sebagai perantara dalam metabolisme dan
Reaksi Esterifikasi. Oleh : Stefanus Dedy ( ) Soegiarto Adi ( ) Cicilia Setyabudi ( )
 Reaksi Esterifikasi Oleh : Stefanus Dedy (5203011003) Soegiarto Adi (5203011006) Cicilia Setyabudi (5203011014) Macam Reaksi Senyawa Organik Reaksi Substitusi Reaksi penggantian (penukaran) suatu gugus
Reaksi Esterifikasi Oleh : Stefanus Dedy (5203011003) Soegiarto Adi (5203011006) Cicilia Setyabudi (5203011014) Macam Reaksi Senyawa Organik Reaksi Substitusi Reaksi penggantian (penukaran) suatu gugus
OLIMPIADE KIMIA INDONESIA
 OLIMPIADE KIMIA INDONESIA OLIMPIADE SAINS NASIONAL SELEKSI KABUPATEN / KOTA UjianTeori Waktu 2 Jam Departemen Pendidikan Nasional Direktorat Jenderal Managemen Pendidikan Dasar dan Menengah Direktorat
OLIMPIADE KIMIA INDONESIA OLIMPIADE SAINS NASIONAL SELEKSI KABUPATEN / KOTA UjianTeori Waktu 2 Jam Departemen Pendidikan Nasional Direktorat Jenderal Managemen Pendidikan Dasar dan Menengah Direktorat
PENGGOLONGAN SENYAWA ORGANIK DAN DASAR-DASAR REAKSI ORGANIK
 ( Word to PDF Converter - Unregistered ) http://www.word-to-pdf-converter.net PENGGOLONGAN SENYAWA ORGANIK DAN DASAR-DASAR REAKSI ORGANIK PENDAHULUAN Oleh: C. Budimarwanti, M.Si Senyawa organik terlibat
( Word to PDF Converter - Unregistered ) http://www.word-to-pdf-converter.net PENGGOLONGAN SENYAWA ORGANIK DAN DASAR-DASAR REAKSI ORGANIK PENDAHULUAN Oleh: C. Budimarwanti, M.Si Senyawa organik terlibat
LAPORAN PRAKTIKUM KIMIA ORGANIK. Disusun Oleh :
 LAPORAN PRAKTIKUM KIMIA ORGANIK Disusun Oleh : Nama : Veryna Septiany NPM : E1G014054 Kelompok : 3 Hari, Jam : Kamis, 14.00 15.40 WIB Ko-Ass : Jhon Fernanta Sipayung Lestari Nike Situngkir Tanggal Praktikum
LAPORAN PRAKTIKUM KIMIA ORGANIK Disusun Oleh : Nama : Veryna Septiany NPM : E1G014054 Kelompok : 3 Hari, Jam : Kamis, 14.00 15.40 WIB Ko-Ass : Jhon Fernanta Sipayung Lestari Nike Situngkir Tanggal Praktikum
1. Isilah Biodata anda dengan lengkap (di lembar Jawaban) Tulis dengan huruf cetak dan jangan disingkat!
 Petunjuk : 1. Isilah Biodata anda dengan lengkap (di lembar Jawaban) Tulis dengan huruf cetak dan jangan disingkat! 2. Soal Teori ini terdiri dari dua bagian: A. 30 soal pilihan Ganda : 60 poin B. 5 Nomor
Petunjuk : 1. Isilah Biodata anda dengan lengkap (di lembar Jawaban) Tulis dengan huruf cetak dan jangan disingkat! 2. Soal Teori ini terdiri dari dua bagian: A. 30 soal pilihan Ganda : 60 poin B. 5 Nomor
Pengantar KO2 (Kimia Organik Gugus Fungsi)
 Pengantar KO2 (Kimia Organik Gugus Fungsi) Sasaran : pengenalan gugus fungsi. Mengetahui sifat fisika dan kimia suatu bahan yang digunakan sebagai obat, kosmetika, bahan makanan dan minuman. Untuk digunaka
Pengantar KO2 (Kimia Organik Gugus Fungsi) Sasaran : pengenalan gugus fungsi. Mengetahui sifat fisika dan kimia suatu bahan yang digunakan sebagai obat, kosmetika, bahan makanan dan minuman. Untuk digunaka
SENYAWA KARBON. Indriana Lestari
 SENYAWA KARBON Indriana Lestari A. Keunikan Atom Karbon ( C ) Atom Karbon ( C ) memiliki 4 elektron valensi. Dengan nomor atom 6, atom C memiliki 4 elektron valensi, sehingga untuk mencapai kestabilan
SENYAWA KARBON Indriana Lestari A. Keunikan Atom Karbon ( C ) Atom Karbon ( C ) memiliki 4 elektron valensi. Dengan nomor atom 6, atom C memiliki 4 elektron valensi, sehingga untuk mencapai kestabilan
Alkena dan Alkuna. Pertemuan 4
 Alkena dan Alkuna Pertemuan 4 Alkena/Olefin hidrokarbon alifatik tak jenuh yang memiliki satu ikatan rangkap (C = C) Senyawa yang mempunyai dua ikatan rangkap: alkadiena tiga ikatan rangkap: alkatriena,
Alkena dan Alkuna Pertemuan 4 Alkena/Olefin hidrokarbon alifatik tak jenuh yang memiliki satu ikatan rangkap (C = C) Senyawa yang mempunyai dua ikatan rangkap: alkadiena tiga ikatan rangkap: alkatriena,
GUGUS FUNGSI
 ASAM KARBKSILAT GUGUS FUNGSI TATA NAMA SEARA IUPA MENGGUNAKAN NAMA ALKANA INDUKNYA DENGAN IMBUHAN: ASAM.-AT (NAMA LAIN ASAM KARBKSILAT ADALAH ASAM ALKANAT) GUGUS ALKIL ATAU SUBSTITUEN LAIN DILETAKKAN
ASAM KARBKSILAT GUGUS FUNGSI TATA NAMA SEARA IUPA MENGGUNAKAN NAMA ALKANA INDUKNYA DENGAN IMBUHAN: ASAM.-AT (NAMA LAIN ASAM KARBKSILAT ADALAH ASAM ALKANAT) GUGUS ALKIL ATAU SUBSTITUEN LAIN DILETAKKAN
BAB II TINJAUAN PUSTAKA. akan berlangsung selama sintesis, serta alat-alat yang diperlukan untuk sintesis.
 II TINJUN PUSTK 2.1 Rancangan nalisis Dalam sintesis suatu senyawa kimia atau senyawa obat yang baik, diperlukan beberapa persiapan. Persiapan tersebut antara lain berupa bahan dasar sintesis, pereaksi,
II TINJUN PUSTK 2.1 Rancangan nalisis Dalam sintesis suatu senyawa kimia atau senyawa obat yang baik, diperlukan beberapa persiapan. Persiapan tersebut antara lain berupa bahan dasar sintesis, pereaksi,
KIMIA ORGANIK. = Kimia Senyawa Karbon. Kajian Struktur, Sifat, & Reaksi. Ikatan Kovalen : Rumus Kimia : CH 3 C : H = 1 : 3
 KIMIA ORGANIK? = Kimia Senyawa Karbon Kajian Struktur, Sifat, & Reaksi Ikatan Kovalen : Penggunaan sepasang elektron antara dua atom Rumus Kimia : Rumus Empirik : Menggambarkan Jenis atom dan perbandingannya
KIMIA ORGANIK? = Kimia Senyawa Karbon Kajian Struktur, Sifat, & Reaksi Ikatan Kovalen : Penggunaan sepasang elektron antara dua atom Rumus Kimia : Rumus Empirik : Menggambarkan Jenis atom dan perbandingannya
ALDEHID DAN KETON. Tim Dosen Kimia Dasar II/ Kimia Organik
 ALDEHID DAN KETN Tim Dosen Kimia Dasar II/ Kimia rganik TATA NAMA ALDEHID IUPAC Alkana induk dengan huruf akhir a menjadi -al Metanal Etanal Propanal Butanal NTE Aldehid tanpa rantai samping (substituen)
ALDEHID DAN KETN Tim Dosen Kimia Dasar II/ Kimia rganik TATA NAMA ALDEHID IUPAC Alkana induk dengan huruf akhir a menjadi -al Metanal Etanal Propanal Butanal NTE Aldehid tanpa rantai samping (substituen)
SOAL SELEKSI OLIMPIADE SAINS TINGKAT KABUPATEN/KOTA 2004 CALON TIM OLIMPIADE KIMIA INDONESIA
 SOAL SELEKSI OLIMPIADE SAINS TINGKAT KABUPATEN/KOTA 2004 CALON TIM OLIMPIADE KIMIA INDONESIA 2005 Bidang Kimia KEMENTERIAN PENDIDIKAN DAN KEBUDAYAAN DIREKTORAT JENDERAL PENDIDIKAN MENENGAH DIREKTORAT PEMBINAAN
SOAL SELEKSI OLIMPIADE SAINS TINGKAT KABUPATEN/KOTA 2004 CALON TIM OLIMPIADE KIMIA INDONESIA 2005 Bidang Kimia KEMENTERIAN PENDIDIKAN DAN KEBUDAYAAN DIREKTORAT JENDERAL PENDIDIKAN MENENGAH DIREKTORAT PEMBINAAN
RENCANA PROGRAM KEGIATAN PEMBELAJARAN SEMESTER (RPKPS)
 RENCANA PROGRAM KEGIATAN PEMBELAJARAN SEMESTER (RPKPS) I. Nama matakuliah Kimia Organik Dasar I II. Kode / SKS MKS 2401 /2 SKS III. Prasyarat Matakuliah prasyarat adalah Kimia Dasar II IV. Status matakuliah
RENCANA PROGRAM KEGIATAN PEMBELAJARAN SEMESTER (RPKPS) I. Nama matakuliah Kimia Organik Dasar I II. Kode / SKS MKS 2401 /2 SKS III. Prasyarat Matakuliah prasyarat adalah Kimia Dasar II IV. Status matakuliah
BANK SOAL KIMIA ORGANIK I UJIAN MID SEMESTER GANJIL 2002/2003
 BANK SOAL KIMIA ORGANIK I UJIAN MID SEMESTER GANJIL 2002/2003 1. Terangkan dengan jelas bagaimana terjadinya ikatan sigma dan pi antara atom-atom pada periode II yaitu atom boron, karbon, dan nitrogen.
BANK SOAL KIMIA ORGANIK I UJIAN MID SEMESTER GANJIL 2002/2003 1. Terangkan dengan jelas bagaimana terjadinya ikatan sigma dan pi antara atom-atom pada periode II yaitu atom boron, karbon, dan nitrogen.
SENYAWA ALKOHOL DAN FENOL I. TUJUAN Untuk mengetahui sifat fisika alcohol dan fenol Untuk mempelajari beberapa reaksi kimia karakteristik dari
 SENYAWA ALKOHOL DAN FENOL I. TUJUAN Untuk mengetahui sifat fisika alcohol dan fenol Untuk mempelajari beberapa reaksi kimia karakteristik dari alcohol dan fenol Untuk membedakan alcohol primer, sekunder
SENYAWA ALKOHOL DAN FENOL I. TUJUAN Untuk mengetahui sifat fisika alcohol dan fenol Untuk mempelajari beberapa reaksi kimia karakteristik dari alcohol dan fenol Untuk membedakan alcohol primer, sekunder
REAKSI SAPONIFIKASI PADA LEMAK
 REAKSI SAPONIFIKASI PADA LEMAK TUJUAN : Mempelajari proses saponifikasi suatu lemak dengan menggunakan kalium hidroksida dan natrium hidroksida Mempelajari perbedaan sifat sabun dan detergen A. Pre-lab
REAKSI SAPONIFIKASI PADA LEMAK TUJUAN : Mempelajari proses saponifikasi suatu lemak dengan menggunakan kalium hidroksida dan natrium hidroksida Mempelajari perbedaan sifat sabun dan detergen A. Pre-lab
KIMIA. Sesi. Hidrokarbon (Bagian III) A. REAKSI-REAKSI SENYAWA KARBON. a. Adisi
 KIMIA KELAS XII IPA - KURIKULUM GABUNGAN 17 Sesi NGAN Hidrokarbon (Bagian III) A. REAKSI-REAKSI SENYAWA KARBON Reaksi-reaksi kimia yang terjadi pada senyawa hidrokarbon secara umum adalah reaksi adisi,
KIMIA KELAS XII IPA - KURIKULUM GABUNGAN 17 Sesi NGAN Hidrokarbon (Bagian III) A. REAKSI-REAKSI SENYAWA KARBON Reaksi-reaksi kimia yang terjadi pada senyawa hidrokarbon secara umum adalah reaksi adisi,
 TRY OUT SELEKSI OLIMPIADE TINGKAT KABUPATEN/KOTA 2010 TIM OLIMPIADE KIMIA INDONESIA 2011 Waktu: 150 Menit PUSAT KLINIK PENDIDIKAN INDONESIA (PKPI) bekerjasama dengan LEMBAGA BIMBINGAN BELAJAR SSCIntersolusi
TRY OUT SELEKSI OLIMPIADE TINGKAT KABUPATEN/KOTA 2010 TIM OLIMPIADE KIMIA INDONESIA 2011 Waktu: 150 Menit PUSAT KLINIK PENDIDIKAN INDONESIA (PKPI) bekerjasama dengan LEMBAGA BIMBINGAN BELAJAR SSCIntersolusi
ENOLAT DAN KARBANION (REAKSI-REAKSI SUBSTITUSI ALFA)
 ENLAT DAN KABANIN (EAKSIEAKSI SUBSTITUSI ALFA) eagensia nukleofilik bereaksi dengan senyawa yang mengandung atom karbon yg bermuatan positif parsial Nu + X Nu + X eagensia yg mengandung atom nukeofilik
ENLAT DAN KABANIN (EAKSIEAKSI SUBSTITUSI ALFA) eagensia nukleofilik bereaksi dengan senyawa yang mengandung atom karbon yg bermuatan positif parsial Nu + X Nu + X eagensia yg mengandung atom nukeofilik
Senyawa Hidrokarbon. Linda Windia Sundarti
 Senyawa Hidrokarbon Senyawa Hidrokarbon adalah senyawa yang mengandung hanya karbon dan hidrogen C + H Carbon sebagai unsur pokok memiliki keistimewaan sbb : 1. Dengan ev = 4 membentuk 4 ikatan kovalen
Senyawa Hidrokarbon Senyawa Hidrokarbon adalah senyawa yang mengandung hanya karbon dan hidrogen C + H Carbon sebagai unsur pokok memiliki keistimewaan sbb : 1. Dengan ev = 4 membentuk 4 ikatan kovalen
Serangan elektrofil pada posisi orto
 Serangan elektrofil pada posisi orto O Y + O Y O Y O Y I II III O O Y Y Serangan elektrofil pada posisi meta Serangan elektrofil pada posisi para Pada reaksi substitusi elektrofilik fenol ini terlihat
Serangan elektrofil pada posisi orto O Y + O Y O Y O Y I II III O O Y Y Serangan elektrofil pada posisi meta Serangan elektrofil pada posisi para Pada reaksi substitusi elektrofilik fenol ini terlihat
Alkena. KO 1 pertemuan III. Indah Solihah
 Alkena KO 1 pertemuan III Indah Solihah Pengertian Alkena Merupakan senyawa hidrokarbon yang mengandung ikatan rangkap karbon-karbon. Terdapat dalam jumlah berlebih di alam Etena (etilena) merupakan ssalah
Alkena KO 1 pertemuan III Indah Solihah Pengertian Alkena Merupakan senyawa hidrokarbon yang mengandung ikatan rangkap karbon-karbon. Terdapat dalam jumlah berlebih di alam Etena (etilena) merupakan ssalah
Jawaban: b Alasan: Jumlah atom C dan H sama. Siklo alkana berisomer dengan alkena, alkana tidak berisomer dengan alkena.
 1. Senyawa 2-metil 1-pentanol berisomer dengan... a. metil propil eter b. dipropil eter c. isopentanol d. etil propil eter e. 3-pentanol Jawaban: b Alasan: Jumlah atom C pada soal adalah 6. Pada jawaban,
1. Senyawa 2-metil 1-pentanol berisomer dengan... a. metil propil eter b. dipropil eter c. isopentanol d. etil propil eter e. 3-pentanol Jawaban: b Alasan: Jumlah atom C pada soal adalah 6. Pada jawaban,
Sifat fisika: mirip dengan alkana dengan jumlah atom C sama
 SENYAWA ORGANIK HIDROKARBON SENYAWA KARBON DENGAN KARBON NUKLEOFILIK ALKENA Alkena merupakan senyawa hidrokarbon dengan sifat tersendiri karena adanya ikatan rangkap dan reaktivitas senyawa ini senyawa
SENYAWA ORGANIK HIDROKARBON SENYAWA KARBON DENGAN KARBON NUKLEOFILIK ALKENA Alkena merupakan senyawa hidrokarbon dengan sifat tersendiri karena adanya ikatan rangkap dan reaktivitas senyawa ini senyawa
BAB I IDENTIFIKASI GUGUS FUNGSI ALKOHOL
 BAB I IDENTIFIKASI GUGUS FUNGSI ALKOHOL TUJUAN : Mengetahui sifat fisik alkohol dan fenol Membedakan senyawa alkohol primer, sekunder, tersier dan fenol dengan menggunakan tes Lucas dan Ferri Klorida A.
BAB I IDENTIFIKASI GUGUS FUNGSI ALKOHOL TUJUAN : Mengetahui sifat fisik alkohol dan fenol Membedakan senyawa alkohol primer, sekunder, tersier dan fenol dengan menggunakan tes Lucas dan Ferri Klorida A.
bemffums.blogspot.com
 bemffums.blogspot.com Amina Didasarkan pada: McMurry s Organic Chemistry, th edisi 6 24.1 Naming Amines Amina tersubstitusi alkil (alkilamina) atau tersubstitusi aril (arilamina) Klasifikasi: 1 (RNH2),
bemffums.blogspot.com Amina Didasarkan pada: McMurry s Organic Chemistry, th edisi 6 24.1 Naming Amines Amina tersubstitusi alkil (alkilamina) atau tersubstitusi aril (arilamina) Klasifikasi: 1 (RNH2),
Senyawa organik adalah senyawa kimia yang molekulnya mengandung karbon, kecuali karbida, karbonat, dan oksida karbon.
 PENDAULUAN Definisi senyawa organik Kimia organik adalah studi ilmiah mengenai struktur, sifat, komposisi, reaksi, dan sintesis senyawa organik. Senyawa organik dibangun oleh karbon dan hidrogen, dan dapat
PENDAULUAN Definisi senyawa organik Kimia organik adalah studi ilmiah mengenai struktur, sifat, komposisi, reaksi, dan sintesis senyawa organik. Senyawa organik dibangun oleh karbon dan hidrogen, dan dapat
LAPORAN PRAKTIKUM KIMIA ORGANIK (KI2051)
 1 LAPORAN PRAKTIKUM KIMIA ORGANIK (KI2051) PERCOBAAN 6 Aldehid dan Keton: Sifat Fisik dan Reaksi Kimia DIAH RATNA SARI 11609010 KELOMPOK I Tanggal Percobaan : 27 Oktober 2010 Shift Rabu Siang (13.00 17.00
1 LAPORAN PRAKTIKUM KIMIA ORGANIK (KI2051) PERCOBAAN 6 Aldehid dan Keton: Sifat Fisik dan Reaksi Kimia DIAH RATNA SARI 11609010 KELOMPOK I Tanggal Percobaan : 27 Oktober 2010 Shift Rabu Siang (13.00 17.00
Kimia Dasar II / Kimia Organik. Shinta Rosalia D. (SRD) Angga Dheta S. (ADS) Sudarma Dita W. (SDW) Nur Lailatul R. (NLR) Feronika Heppy S (FHS)
 Kimia Dasar II / Kimia Organik Shinta Rosalia D. (SRD) Angga Dheta S. (ADS) Sudarma Dita W. (SDW) Nur Lailatul R. (NLR) Feronika Heppy S (FHS) Kontrak perkuliahan : 1. Ujian : 50% 2. Tugas : 10% 3. Kuis
Kimia Dasar II / Kimia Organik Shinta Rosalia D. (SRD) Angga Dheta S. (ADS) Sudarma Dita W. (SDW) Nur Lailatul R. (NLR) Feronika Heppy S (FHS) Kontrak perkuliahan : 1. Ujian : 50% 2. Tugas : 10% 3. Kuis
OLIMPIADE KIMIA INDONESIA
 OLIMPIADE KIMIA INDONESIA OLIMPIADE SAINS NASIONAL SELEKSI KABUPATEN / KOTA UjianTeori Waktu 2 Jam Departemen Pendidikan Nasional Direktorat Jenderal Managemen Pendidikan Dasar dan Menengah Direktorat
OLIMPIADE KIMIA INDONESIA OLIMPIADE SAINS NASIONAL SELEKSI KABUPATEN / KOTA UjianTeori Waktu 2 Jam Departemen Pendidikan Nasional Direktorat Jenderal Managemen Pendidikan Dasar dan Menengah Direktorat
MKA PROSES KIMIA. Sri Wahyu Murni Prodi Teknik Kimia FTI UPN Veteran Yogyakarta
 MKA PROSES KIMIA Oleh Sri Wahyu Murni Prodi Teknik Kimia FTI UPN Veteran Yogyakarta Alkilasi didefinikan sebagai proses memasukkan gugus alkil atau aril ke dalam suatu senyawa. Gugus alkil : -C n H 2n+1
MKA PROSES KIMIA Oleh Sri Wahyu Murni Prodi Teknik Kimia FTI UPN Veteran Yogyakarta Alkilasi didefinikan sebagai proses memasukkan gugus alkil atau aril ke dalam suatu senyawa. Gugus alkil : -C n H 2n+1
I. DASAR TEORI Struktur benzil alkohol
 JUDUL TUJUAN PERCBAAN IV : BENZIL ALKL : 1. Mempelajari kelarutan benzyl alkohol dalam berbagai pelarut. 2. Mengamati sifat dan reaksi oksidasi pada benzyl alkohol. ari/tanggal : Selasa, 2 November 2010
JUDUL TUJUAN PERCBAAN IV : BENZIL ALKL : 1. Mempelajari kelarutan benzyl alkohol dalam berbagai pelarut. 2. Mengamati sifat dan reaksi oksidasi pada benzyl alkohol. ari/tanggal : Selasa, 2 November 2010
