III BAHAN DAN METODE 3.1 Waktu dan Tempat Penelitian 3.2 Bahan dan Alat 3.3 Metode Ekspresi dan Pemurnian RNA Helikase HCV
|
|
|
- Deddy Kusuma
- 4 tahun lalu
- Tontonan:
Transkripsi
1 27 III BAHAN DAN METODE 3.1 Waktu dan Tempat Penelitian Penelitian ini dilaksanakan mulai bulan Agustus 2009 sampai dengan Desember 2009 di Pusat Penelitian Bioteknologi-LIPI, Cibinong. 3.2 Bahan dan Alat Bahan yang digunakan dalam penelitian ini adalah bakteri Escherichia coli BL21(DE3)pLysS yang membawa gen NS3 RNA helikase HCV dalam plasmid pet 21b (koleksi A. Utama, Puslit Bioteknologi-LIPI), isolat penghasil inhibitor S. chartreusis (koleksi P. Lisdiyanti, Puslit Bioteknologi-LIPI), dan bahan kimia yang terkait. Alat yang digunakan dalam penelitian ini meliputi peralatan kultur bakteri E. coli BL21(DE3)pLysS dan S. chartreusis 5-095, pemurnian RNA helikase HCV, analisa protein SDS PAGE, uji aktivitas enzim dan inhibitor, pemurnian inhibitor dan NMR. 3.3 Metode Ekspresi dan Pemurnian RNA Helikase HCV Ekspresi RNA Helikase HCV Ekspresi RNA helikase protein NS3 HCV dilakukan berdasarkan metode Utama, et al. (2000). Ekspresi dilakukan pada skala 400 ml. Sebanyak 10 L stock gliserol bakteri E. coli BL21(DE3)pLysS yang membawa vektor ekspresi pet-21b/hcv NS3 Helikase diinokulasi ke dalam 10 ml medium LB cair yang mengandung 100 µg/ml ampisilin, kemudian dikultur selama satu malam dalam inkubator berpenggoyang pada suhu 37 o C dengan kecepatan 200 rpm. Hasil kultur diinokulasikan ke dalam 400 ml medium LB yang mengandung ampisilin, selanjutnya dikultur dalam inkubator berpenggoyang pada suhu 37 o C dengan kecepatan 200 rpm, selama 30 menit sampai dengan 1 jam hingga OD 600 mencapai ± 0,3. Apabila OD 600 telah mencapai ± 0,3 maka ditambahkan 410 µl 0,3 M IPTG.
2 28 Kultur E. coli BL21(DE3)pLysS kemudian diinkubasi selama 3 jam dalam inkubator berpenggoyang pada suhu 37 o C dengan kecepatan 200 rpm selama 3 jam atau hingga OD 600 mencapai ± 1. Selanjutnya, kultur disentrifugasi pada suhu 4 o C dengan kecepatan 6000 g, selama 10 menit. Pelet diresuspensi dengan 5 ml medium LB cair, kemudian disentrifugasi kembali. Pelet yang diperoleh disimpan pada suhu -70 o C. Pemurnian RNA Helikase HCV Pemurnian RNA helikase HCV dilakukan berdasarkan metode Utama et al. (2000). Pelet E. coli BL21(DE3)pLysS dilisis dengan metode freeze & thaw sebanyak 3 kali ulangan yaitu dengan membekukan pelet pada suhu -70 o C selama 30 menit, lalu dicairkan pada suhu ruang (25 o C) selama 30 menit. Pelet kemudian diresuspensi dengan 20 ml larutan bufer B (10 mm Tris HCL ph 8,5; 100 mm NaCl; 0,25% Tween 20). Tahap kedua pelisisan sel dilakukan dengan metode sonikasi (Amp 40; cycle 0,5; waktu 3x15 detik; interval waktu 1 menit). Suspensi sel disentrifugasi pada suhu 6 o C dengan kecepatan g selama 20 menit. Supernatan diambil untuk tahapan selanjutnya sedangkan pelet disimpan untuk analisis SDS PAGE. RNA helikase yang berada dalam supernatan dipurifikasi menggunakan metode kromatografi afinitas. Supernatan ditambahkan dengan 300 µl resin Ni- NTA yang sebelumnya telah diequilibrasi dengan larutan bufer B, kemudian diinkubasi dengan menggunakan rotator selama 2-3 jam dalam ruang pendingin (4 o C). Sampel selanjutnya disentrifugasi pada suhu 4 o C dengan kecepatan 6000 g selama 10 menit. Supernatan (inner volume) disimpan pada suhu 4 o C untuk analisis SDS PAGE. Pelet (resin binding) diresuspensi dengan 10 ml larutan bufer B dan disentrifugasi pada suhu 4 o C dengan kecepatan 6000 g selama 7 menit. Tahapan ini dilakukan sebanyak 2 kali sehingga diperoleh 2 larutan supernatan (washing 1 & washing 2) yang disimpan pada suhu 4 o C dan digunakan untuk analisis SDS PAGE. Pelet dari hasil washing 2 kemudian dielusi untuk melepaskan enzim yang terikat pada resin. Elusi dilakukan dengan menambahkan 400 µl larutan bufer
3 29 elusi (400 mm imidazol dalam bufer B), kemudian diinkubasi menggunakan rotator dalam ruangan pendingin (4 o C) selama satu malam. Sampel disentrifugasi pada suhu 4 o C dengan kecepatan 6000 g selama 1 menit. Supernatan yang mengandung enzim dipindahkan dalam eppendorf yang baru (E1), sedangkan pelet ditambahkan kembali dengan 200 µl larutan bufer elusi, kemudian diinkubasi dengan menggunakan rotator selama menit. Sampel kembali disentrifugasi sehingga diperoleh supernatan (E2) dan pelet (RE) Supernatan E1 dan E2 digabungkan dan didialisis dengan bufer dialisis (100 mm NaCL; 10% glycerol; 10 mm Tris HCL ph 8,5) Uji Aktivitas ATPase RNA Helikase HCV Pengujian aktivitas RNA Helikase HCV dilakukan dengan uji ATPase secara kolorimetrik (Chan et al. 1986; Utama et al. 2000), yaitu dengan mengukur jumlah fosfat yang dilepaskan dari hidrolisis senyawa ATP menjadi ADP. Konsentrasi akhir reaksi sebesar 50 µl/sumur mengandung 38,5 µl H 2 O; 5,0 µl 0,1 M MOPS; 0,5 µl 0,1 M MgCl; 1,0 µl 0,1 M ATP dan 5 µl RNA helikase HCV. Campuran reaksi diinkubasi dalam microtiter plate 96-well, pada suhu ruang selama 45 menit. Hasil reaksi divisualisasi dengan penambahan 100 µl/sumur larutan pewarna (H 2 O : 0,081% malachite green : 5,7% ammonium molybdate dalam 6 M HCl : 2,3% polyvinylalcohol = 2:2:1:1). Reaksi diinkubasi selama 5 menit, kemudian ditambahkan sodium sitrat untuk menghentikan reaksi warna. Reaksi diukur pada panjang gelombang 620 nm dengan referensi 405 nm, pada kondisi sebelum dan sesudah penambahan sodium sitrat. Satu unit aktivitas RNA helikase HCV adalah jumlah mol fosfat (Pi) yang terhidrolisis dari ATP per menit per mg protein. Pengukuran aktivitas inhibisi senyawa inhibitor dari S. chartreusis dilakukan dengan penambahan 5 µl/sumur supernatan S. chartreusis dalam campuran reaksi. Konsentrasi akhir reaksi 50 µl/sumur dengan komposisi 45 µl campuran reaksi (38,5 µl H 2 O; 5 µl 0,1 M MOPS; 0,5 µl 0,1 M MgCl; 1 µl 0,1 M ATP dan 5 µl RNA Helikase HCV) dan 5 µl inhibitor.
4 30 Penentuan laju inhibisi dilakukan dengan persamaan: A I % Inhibisi 100% A dengan A : aktivitas RNA helikase HCV tanpa adanya inhibitor I : aktivitas RNA helikase HCV dengan adanya inhibitor Produksi Protein Inhibitor dari S. chartreusis Produksi protein inhibitor dari S. chartreusis dilakukan dengan metode Lisdiyanti et al. (2006). Isolat S. chartreusis diinokulasi sebanyak 3 ose ke dalam erlenmeyer 100 ml yang berisi 10 ml medium cair ISP2, selanjutnya diinkubasi pada suhu ruang (29 o C) selama 4 hari dengan pengocokan. Prekultur ini selanjutnya diinokulasikan ke dalam erlenmeyer 2 L yang berisi 400 ml medium cair ISP2, selanjutnya diinkubasi pada suhu ruang (29 o C) selama 10 hari dengan pengocokan. Kultur selanjutnya disentrifugasi dengan kecepatan g selama 20 menit. Supernatan yang diperoleh dipisahkan dari endapan (miselia) dan digunakan sebagai sumber inhibitor (ekstrak kasar) Pengaruh Pertumbuhan S. chartreusis dengan Aktivitas Inhibitor terhadap RNA Helikase HCV Isolat S. chartreusis diinokulasi sebanyak 3 ose ke dalam erlenmeyer 1000 ml yang berisi 200 ml medium cair ISP2, selanjutnya diinkubasi pada suhu ruang (29 o C) selama 14 hari dengan pengocokan. Biakan selanjutnya disampling setiap hari selama 8 hari dan berikutnya setiap 2 hari. Sampling dilakukan sebanyak 5 ml, selanjutnya disentrifugasi dengan kecepatan g selama 20 menit. Supernatan yang diperoleh dipisahkan dari endapan. Supernatan digunakan sebagai sumber inhibitor dan diuji aktivitas inhibisinya terhadap aktivitas ATPase RNA helikase HCV. Endapan ditimbang dan digunakan sebagai profil pertumbuhan isolat S. chartreusis Pemurnian Protein Inhibitor Pengendapan protein inhibitor menggunakan amonium sulfat Fraksinasi protein dengan menggunakan amonium sulfat atau aseton didasarkan pada metode Scope (1987). Supernatan kultur S. chartreusis 5-095
5 31 ditambahkan sedikit demi sedikit dengan amonium sulfat melalui saturasi bertingkat 50-85% (w/v) (Ratnakomala 2009), menggunakan pengaduk magnetic stirrer dengan kecepatan 20 rpm pada suhu 4 o C. Selanjutnya disentrifugasi dengan kecepatan g selama 20 menit pada suhu 4 o C. Endapan yang diperoleh, kemudian dipisahkan dari supernatan dan dilarutkan ke dalam 5 ml bufer Tris-HCl ph 7,4. Larutan ini selanjutnya didialisis dengan 1 L ddh 2 O selama 60 menit pada suhu 4 o C. Fraksi hasil amonium sulfat dalam berbagai saturasi, diuji aktivitas inhibisinya terhadap RNA helikase HCV dengan uji ATPase, ditentukan kadar protein, dan analisis SDS PAGE. Protein inhibitor kemudian dimurnikan menggunakan kromatografi kolom Pemurnian protein inhibitor menggunakan kromatografi gel filtrasi Protein inhibitor hasil pengendapan amonium sulfat selanjutnya dimurnikan dengan menggunakan kromatografi gel filtrasi (Hatsu et al. 2002; Ratnakomala 2009). Fasa diam yang digunakan adalah Sephadex G-50 yang diberi perlakuan dengan melarutkannya dalam ddh 2 O dan diautoklaf, diekuiliberasi dalam larutan 20 mm bufer Tris-HCl ph 7,4. Kolom kromatografi dicuci dengan etanol 95% sebanyak 1 kali volum kolom (120 ml) dengan laju alir 0,5 ml/menit. Selanjutnya dicuci dengan ddh 2 O sebanyak 1,5 kali volum kolom (180 ml) dengan laju alir 0,5 ml/menit. Sebanyak 1 ml sampel protein inhibitor diinjeksikan ke dalam kolom kromatografi dan dielusi dengan larutan H 2 O:MeOH=3:2 dengan laju alir sebesar 0,2 ml/menit. Hasil elusi ditampung dalam tabung reaksi dengan volum 1 ml tiap tabung. Keseluruhan proses ini dilakukan di suhu 4 o C. Masing-masing fraksi diuji aktivitas penghambatannya dengan uji ATPase, penentuan kadar protein dan analisis SDS PAGE Karakterisasi Protein Inhibitor Analisis bobot molekul protein inhibitor dengan SDS PAGE Analisis bobot molekul protein inhibitor dari berbagai tahap dilakukan dengan SDS-PAGE (Sodium Dedocyl Sulfate Poly Acrilamide Gel Electrophoresis) berdasarkan metode Laemmli (1970). Komposisi gel
6 32 poliakrilamid terdiri atas 2 konsentrasi akrilamid yaitu konsentrasi akrilamid 3,9% untuk stacking gel dan 8% untuk separating gel. SDS-PAGE juga dilakukan dengan gradien konsentrasi separating gel 10-20% untuk menganalisis protein yang memiliki berat molekul kda (Coligan et al. 1995). Elektroforesis di-running pada 30 ma selama 60 menit dalam bufer elektroforesis (24% glycerol, 8% SDS, 100 mm Tris). Setelah elektroforesis, gel kemudian diwarnai dengan Commassie Brilliant Blue R-250 atau pewarnaan perak Pengukuran kadar protein Kadar protein diukur dengan BCA Protein Assay Kit (Pierce). Sebanyak 0,1 ml sampel ditambahkan 2,0 ml working reagent, kemudian diinkubasi pada suhu ruang selama 2 jam. Absorbansi diukur pada panjang gelombang 562 nm Pengujian pengaruh suhu terhadap stabilitas penyimpanan protein inhibitor Pengujian pengaruh suhu terhadap stabilitas protein inhibitor dilakukan dengan menginkubasi protein inhibitor yang telah dimurnikan pada berbagai suhu penyimpanan (-20 o C, 4 o C, dan suhu ruang) selama 30 hari. Setiap 10 hari, diambil untuk diukur aktivitasnya menggunakan uji ATPase Pengujian pengaruh ph terhadap stabilitas protein inhibitor Pengujian pengaruh ph terhadap stabilitas protein inhibitor dilakukan dengan melarutkan protein inhibitor yang telah dimurnikan dalam bufer yang sesuai pada berbagai ph (1,5, 4, 5, 7, 8, dan 9) dan diinkubasi pada suhu 4 o C selama 60 menit, selanjutnya diukur aktivitasnya menggunakan uji ATPase Pengujian stabilitas panas terhadap aktivitas protein inhibitor Pengujian stabilitas panas terhadap aktivitas protein inhibitor dilakukan dengan menginkubasikan larutan protein inhibitor yang telah dimurnikan dalam berbagai suhu (40, 60, 80, dan 100 o C) selama 60 menit. Tiap 10 menit larutan diambil dan diukur aktivitasnya menggunakan uji ATPase.
7 Penentuan konsentrasi 50% penghambatan (IC 50 ) Penentuan konsentrasi 50% penghambatan (IC 50 ) dilakukan dengan menentukan aktivitas inhibisi protein inhibitor melalui uji ATPase terhadap variasi konsentrasi dan waktu. Gambar 11. Bagan alir proses pemurnian dan karakterisasi protein inhibitor RNA helikase HCV dari S. chartreusis 5-095
Pengujian Inhibisi RNA Helikase Virus Hepatitis C (Utama et al. 2000) HASIL DAN PEMBAHASAN Hasil Ekspresi dan Purifikasi RNA
 8 kromatografi kemudian diuji aktivitas inhibisinya dengan metode kolorimetri ATPase assay. Beberapa fraksi yang memiliki aktivitas inhibisi yang tinggi digunakan untuk tahapan selanjutnya (Lampiran 3).
8 kromatografi kemudian diuji aktivitas inhibisinya dengan metode kolorimetri ATPase assay. Beberapa fraksi yang memiliki aktivitas inhibisi yang tinggi digunakan untuk tahapan selanjutnya (Lampiran 3).
Analisis Bobot Molekul Protein Inhibitor RNA Helikase HCV (Hairany 2010 termodifikasi) HASIL DAN PEMBAHASAN Hasil Isolasi RNA Helikase HCV
 7 diinkubasi pada suhu 37ºC selama 30 menit. Absorbansi diukur menggunakan panjang gelombang 562 nm. Standar protein yang digunakan adalah albumin serum sapi (Bovine Serum Albumin (BSA)) pada kisaran 0.05
7 diinkubasi pada suhu 37ºC selama 30 menit. Absorbansi diukur menggunakan panjang gelombang 562 nm. Standar protein yang digunakan adalah albumin serum sapi (Bovine Serum Albumin (BSA)) pada kisaran 0.05
3 METODE 3.1 Waktu dan Tempat 3.2 Bahan dan Alat
 16 3 METODE 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Januari hingga April 2012, dan bertempat di Laboratorium Bakteriologi dan Virologi Molekuler, Laboratorium Biorekayasa Lingkungan,
16 3 METODE 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Januari hingga April 2012, dan bertempat di Laboratorium Bakteriologi dan Virologi Molekuler, Laboratorium Biorekayasa Lingkungan,
Pembuatan Media Kultur Bakteri Pemanenan sel bakteri. Isolasi DNA kromosom bakteri. Kloning DNA
 LAMPIRAN 15 15 Lampiran 1 Tahapan penelitian Pembuatan Media Kultur Bakteri Pemanenan sel bakteri Isolasi DNA kromosom bakteri Pemotongan DNA dengan enzim restriksi Kloning DNA Isolasi DNA plasmid hasil
LAMPIRAN 15 15 Lampiran 1 Tahapan penelitian Pembuatan Media Kultur Bakteri Pemanenan sel bakteri Isolasi DNA kromosom bakteri Pemotongan DNA dengan enzim restriksi Kloning DNA Isolasi DNA plasmid hasil
4 HASIL DAN PEMBAHASAN
 4 HASIL DAN PEMBAHASAN 4.1 Isolasi enzim fibrinolitik Cacing tanah P. excavatus merupakan jenis cacing tanah yang agresif dan tahan akan kondisi pemeliharaan yang ekstrim. Pemeliharaan P. excavatus dilakukan
4 HASIL DAN PEMBAHASAN 4.1 Isolasi enzim fibrinolitik Cacing tanah P. excavatus merupakan jenis cacing tanah yang agresif dan tahan akan kondisi pemeliharaan yang ekstrim. Pemeliharaan P. excavatus dilakukan
BAHAN DAN METODE Tempat dan Waktu Bahan Pertumbuhan dan Peremajaan Isolat Pengamatan Morfologi Isolat B. thuringiensis
 13 BAHAN DAN METODE Tempat dan Waktu Penelitian ini dilaksanakan di Laboratorium Mikrobiologi, Departemen Biologi, IPB, dari bulan Oktober 2011 Mei 2012. Bahan Isolasi untuk memperoleh isolat B. thuringiensis
13 BAHAN DAN METODE Tempat dan Waktu Penelitian ini dilaksanakan di Laboratorium Mikrobiologi, Departemen Biologi, IPB, dari bulan Oktober 2011 Mei 2012. Bahan Isolasi untuk memperoleh isolat B. thuringiensis
4 Hasil dan Pembahasan
 4 Hasil dan Pembahasan α-amilase adalah enzim menghidrolisis ikatan α-1,4-glikosidik pada pati. α-amilase disekresikan oleh mikroorganisme, tanaman, dan organisme tingkat tinggi. α-amilase memiliki peranan
4 Hasil dan Pembahasan α-amilase adalah enzim menghidrolisis ikatan α-1,4-glikosidik pada pati. α-amilase disekresikan oleh mikroorganisme, tanaman, dan organisme tingkat tinggi. α-amilase memiliki peranan
3. METODOLOGI 3.1 Waktu dan Tempat Penelitian 3.2 Alat dan Bahan
 3. METODOLOGI 3.1 Waktu dan Tempat Penelitian Penelitian ini dimulai pada bulan Januari 2009 dan selesai pada bulan November 2009. Penelitian dilakukan di Laboratorium Biokimia dan Bioteknologi II, Departemen
3. METODOLOGI 3.1 Waktu dan Tempat Penelitian Penelitian ini dimulai pada bulan Januari 2009 dan selesai pada bulan November 2009. Penelitian dilakukan di Laboratorium Biokimia dan Bioteknologi II, Departemen
BAB III METODE PENELITIAN. adalah Bacillus subtilis dan Bacillus cereus yang diperoleh di Laboratorium
 23 BAB III METODE PENELITIAN 3.1 Objek dan Lokasi Penelitian Objek atau bahan penelitian yang digunakan dalam penelitian ini adalah Bacillus subtilis dan Bacillus cereus yang diperoleh di Laboratorium
23 BAB III METODE PENELITIAN 3.1 Objek dan Lokasi Penelitian Objek atau bahan penelitian yang digunakan dalam penelitian ini adalah Bacillus subtilis dan Bacillus cereus yang diperoleh di Laboratorium
III. METODE PENELITIAN. Penelitian ini dilakukan di Laboratorium Mikrobiologi Jurusan Biologi
 17 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung pada Januari
17 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung pada Januari
Lampiran 1 Rancangan penelitian
 LAMPIRAN 18 19 Lampiran 1 Rancangan penelitian Cacing tanah E. foetida dewasa Kering oven vakum (Setiawan) Tepung cacing kering Ekstraksi buffer dan sentrifugasi Ekstrak kasar protease Salting-out dengan
LAMPIRAN 18 19 Lampiran 1 Rancangan penelitian Cacing tanah E. foetida dewasa Kering oven vakum (Setiawan) Tepung cacing kering Ekstraksi buffer dan sentrifugasi Ekstrak kasar protease Salting-out dengan
BAB III BAHAN, ALAT DAN METODA
 15 BAB III BAHAN, ALAT DAN METODA 3.1 BAHAN Lactobacillus acidophilus FNCC116 (kultur koleksi BPPT yang didapatkan dari Universitas Gajah Mada), Bacillus licheniformis F11.4 (kultur koleksi BPPT yang didapatkan
15 BAB III BAHAN, ALAT DAN METODA 3.1 BAHAN Lactobacillus acidophilus FNCC116 (kultur koleksi BPPT yang didapatkan dari Universitas Gajah Mada), Bacillus licheniformis F11.4 (kultur koleksi BPPT yang didapatkan
III. METODE PENELITIAN. Penelitian dilakukan di Laboratorium Biokimia dan Laboratorium Instrumentasi
 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian dilakukan di Laboratorium Biokimia dan Laboratorium Instrumentasi Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas
III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian dilakukan di Laboratorium Biokimia dan Laboratorium Instrumentasi Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas
I. METODOLOGI PENELITIAN. Penelitian ini dilaksanakan pada bulan April - Juli 2012 di Laboratorium. Ilmu Pengetahuan Alam Universitas Lampung.
 1 I. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan April - Juli 2012 di Laboratorium Biokimia, Laboratorium Instrumentasi Jurusan Kimia Fakultas Matematika
1 I. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan April - Juli 2012 di Laboratorium Biokimia, Laboratorium Instrumentasi Jurusan Kimia Fakultas Matematika
Purifikasi Protein Fusi MBP-Mga Streptococcus pyogenes Hasil Ekspresi Heterolog di Escherichia coli
 Jurnal Matematika dan Sains Vol. 1 No. 1, Maret 25, hal 31-36 Purifikasi Protein Fusi MBP-Mga Streptococcus pyogenes Hasil Ekspresi Heterolog di Escherichia coli Muhaimin 1), Oei Ban Liang 2,4), Enny Ratnaningsih
Jurnal Matematika dan Sains Vol. 1 No. 1, Maret 25, hal 31-36 Purifikasi Protein Fusi MBP-Mga Streptococcus pyogenes Hasil Ekspresi Heterolog di Escherichia coli Muhaimin 1), Oei Ban Liang 2,4), Enny Ratnaningsih
4 Hasil dan Pembahasan
 4 Hasil dan Pembahasan α-amilase merupakan enzim yang mempunyai peranan penting dalam bioteknologi saat ini. Aplikasi teknis enzim ini sangat luas, seperti pada proses likuifaksi pati pada proses produksi
4 Hasil dan Pembahasan α-amilase merupakan enzim yang mempunyai peranan penting dalam bioteknologi saat ini. Aplikasi teknis enzim ini sangat luas, seperti pada proses likuifaksi pati pada proses produksi
Lampiran 1 Prosedur uji aktivitas protease (Walter 1984, modifikasi)
 76 Lampiran Prosedur uji aktivitas protease (Walter 984, modifikasi) Pereaksi Blanko (ml) Standard (ml) Contoh ml) Penyangga TrisHCl (.2 M) ph 7. Substrat Kasein % Enzim ekstrak kasar Akuades steril Tirosin
76 Lampiran Prosedur uji aktivitas protease (Walter 984, modifikasi) Pereaksi Blanko (ml) Standard (ml) Contoh ml) Penyangga TrisHCl (.2 M) ph 7. Substrat Kasein % Enzim ekstrak kasar Akuades steril Tirosin
BAB III METODE PENELITIAN. Penelitian ini dilaksanakan pada bulan Mei sampai September 2014 di Green
 BAB III METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Mei sampai September 2014 di Green House dan Laboratorium Genetika dan Molekuler jurusan Biologi Fakultas Sains dan
BAB III METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Mei sampai September 2014 di Green House dan Laboratorium Genetika dan Molekuler jurusan Biologi Fakultas Sains dan
3 Metodologi Percobaan
 3 Metodologi Percobaan 3.1 Waktu dan Tempat Penelitian Penelitian tugas akhir ini dilakukan di Laboratorium Penelitian Kimia Analitik, Program Studi Kimia, FMIPA Institut Teknologi Bandung. Waktu penelitian
3 Metodologi Percobaan 3.1 Waktu dan Tempat Penelitian Penelitian tugas akhir ini dilakukan di Laboratorium Penelitian Kimia Analitik, Program Studi Kimia, FMIPA Institut Teknologi Bandung. Waktu penelitian
BAB III BAHAN DAN CARA KERJA. Penelitian dilakukan di Laboratorium Teknologi Bioindustri, Pusat
 BAB III BAHAN DAN CARA KERJA A. LOKASI DAN WAKTU PENELITIAN Penelitian dilakukan di Laboratorium Teknologi Bioindustri, Pusat Teknologi Bioindustri, Badan Pengkajian dan Penerapan Teknologi (LTB- PTB-BPPT)-Serpong.
BAB III BAHAN DAN CARA KERJA A. LOKASI DAN WAKTU PENELITIAN Penelitian dilakukan di Laboratorium Teknologi Bioindustri, Pusat Teknologi Bioindustri, Badan Pengkajian dan Penerapan Teknologi (LTB- PTB-BPPT)-Serpong.
METODE PENELITIAN. Penelitian ini telah dilakukan pada bulan Januari-Mei 2015 di Laboratorium
 15 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian ini telah dilakukan pada bulan Januari-Mei 2015 di Laboratorium Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas
15 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian ini telah dilakukan pada bulan Januari-Mei 2015 di Laboratorium Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas
METODOLOGI PENELITIAN. Penelitian ini dilakukan pada bulan April 2012 sampai dengan bulan Juni 2012 di
 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan April 2012 sampai dengan bulan Juni 2012 di Laboratorium Biokimia Jurusan Kimia Fakultas Matematika dan Ilmu
III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan April 2012 sampai dengan bulan Juni 2012 di Laboratorium Biokimia Jurusan Kimia Fakultas Matematika dan Ilmu
3 Metode Penelitian Alat
 3 Metode Penelitian 3.1. Alat Penelitian dilakukan di Laboratorium KBK Protein dan Enzim dan Laboratorium Biokimia, Program Studi Kimia ITB. Peralatan gelas yang digunakan terdiri atas labu erlenmeyer,
3 Metode Penelitian 3.1. Alat Penelitian dilakukan di Laboratorium KBK Protein dan Enzim dan Laboratorium Biokimia, Program Studi Kimia ITB. Peralatan gelas yang digunakan terdiri atas labu erlenmeyer,
FAKULTAS BIOLOGI LABORATORIUM GENETIKA & PEMULIAAN INSTRUKSI KERJA UJI
 Halaman : 1 dari 5 ISOLASI TOTAL DNA HEWAN DENGAN KIT EKSTRAKSI DNA 1. RUANG LINGKUP Metode ini digunakan untuk mengisolasi DNA dari sampel jaringan hewan, dapat dari insang, otot, darah atau jaringan
Halaman : 1 dari 5 ISOLASI TOTAL DNA HEWAN DENGAN KIT EKSTRAKSI DNA 1. RUANG LINGKUP Metode ini digunakan untuk mengisolasi DNA dari sampel jaringan hewan, dapat dari insang, otot, darah atau jaringan
III. METODOLOGI PENELITIAN. Penelitian ini dilakukan pada bulan Juli 2012 sampai bulan Desember 2012 di
 23 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan Juli 2012 sampai bulan Desember 2012 di Laboratorium Biokimia Jurusan Kimia Fakultas Matematika dan Ilmu
23 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan Juli 2012 sampai bulan Desember 2012 di Laboratorium Biokimia Jurusan Kimia Fakultas Matematika dan Ilmu
EKSTRAKSI DNA. 13 Juni 2016
 EKSTRAKSI DNA 13 Juni 2016 Pendahuluan DNA: polimer untai ganda yg tersusun dari deoksiribonukleotida (dari basa purin atau pirimidin, gula pentosa,dan fosfat). Basa purin: A,G Basa pirimidin: C,T DNA
EKSTRAKSI DNA 13 Juni 2016 Pendahuluan DNA: polimer untai ganda yg tersusun dari deoksiribonukleotida (dari basa purin atau pirimidin, gula pentosa,dan fosfat). Basa purin: A,G Basa pirimidin: C,T DNA
FAKULTAS BIOLOGI LABORATORIUM GENETIKA & PEMULIAAN INSTRUKSI KERJA UJI
 ISOLASI TOTAL DNA TUMBUHAN DENGAN KIT EKSTRAKSI DNA PHYTOPURE Halaman : 1 dari 5 1. RUANG LINGKUP Metode ini digunakan untuk mengisolasi DNA dari sampel jaringan tumbuhan, dapat dari daun, akar, batang,
ISOLASI TOTAL DNA TUMBUHAN DENGAN KIT EKSTRAKSI DNA PHYTOPURE Halaman : 1 dari 5 1. RUANG LINGKUP Metode ini digunakan untuk mengisolasi DNA dari sampel jaringan tumbuhan, dapat dari daun, akar, batang,
MATERI DAN METODE Lokasi dan Waktu Materi Prosedur Karakterisasi Isolat L. plantarum dan Bakteri Indikator
 MATERI DAN METODE Lokasi dan Waktu Penelitian ini berlangsung selama tujuh bulan, yakni mulai dari bulan Februari sampai dengan bulan Agustus 2011. Penelitian ini dilaksanakan di Laboratorium Terpadu Ilmu
MATERI DAN METODE Lokasi dan Waktu Penelitian ini berlangsung selama tujuh bulan, yakni mulai dari bulan Februari sampai dengan bulan Agustus 2011. Penelitian ini dilaksanakan di Laboratorium Terpadu Ilmu
3. METODOLOGI 3.1 Waktu dan Tempat Penelitian 3.2. Alat dan Bahan 3.3 Metode Penelitian
 17 3. METODOLOGI 3.1 Waktu dan Tempat Penelitian Penelitian Produksi dan Karakterisasi Enzim Transglutaminase dari Streptoverticillium ladakanum dengan Media yang Disubstitusi Limbah Cair Surimi dilaksanakan
17 3. METODOLOGI 3.1 Waktu dan Tempat Penelitian Penelitian Produksi dan Karakterisasi Enzim Transglutaminase dari Streptoverticillium ladakanum dengan Media yang Disubstitusi Limbah Cair Surimi dilaksanakan
BAHAN DAN METODE. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan dari bulan Juli 2007 sampai bulan Juni 2008 di
 BAHAN DAN METODE : Waktu dan Tempat Penelitian Penelitian ini dilaksanakan dari bulan Juli 2007 sampai bulan Juni 2008 di 1. Laboratorium Bioteknologi Hewan dan Biomedis PPSHB IPB 2. Laboratorium Mikrobiologi
BAHAN DAN METODE : Waktu dan Tempat Penelitian Penelitian ini dilaksanakan dari bulan Juli 2007 sampai bulan Juni 2008 di 1. Laboratorium Bioteknologi Hewan dan Biomedis PPSHB IPB 2. Laboratorium Mikrobiologi
III. BAHAN DAN METODE
 III. BAHAN DAN METODE 3.1. Waktu dan Tempat Penelitian Penelitian ini dilakukan dari bulan November 2006 sampai dengan Januari 2008. Penelitian bertempat di Laboratorium Mikrobiologi, Departemen Biologi,
III. BAHAN DAN METODE 3.1. Waktu dan Tempat Penelitian Penelitian ini dilakukan dari bulan November 2006 sampai dengan Januari 2008. Penelitian bertempat di Laboratorium Mikrobiologi, Departemen Biologi,
Lampiran 1 Pembuatan Medium Kultur DMEM Lampiran 2 Pembuatan Larutan PBS Lampiran 3 Prosedur Pewarnaan HE
 LAMPIRAN Lampiran 1 Pembuatan Medium Kultur DMEM Medium kultur DMEM merupakan medium Dulbecco s Modified Eagle s Medium (DMEM; Sigma) yang telah dimodifikasi dengan penambahan asam amino non-esensial (AANE;
LAMPIRAN Lampiran 1 Pembuatan Medium Kultur DMEM Medium kultur DMEM merupakan medium Dulbecco s Modified Eagle s Medium (DMEM; Sigma) yang telah dimodifikasi dengan penambahan asam amino non-esensial (AANE;
Analisis kadar protein
 LAMPIRAN Lampiran 1 Bagan alir penelitian Biawak air bagian duodenum, jejenum, ileum, kolon Cuci dengan akuades dan kerok lapisan atasnya (mukosa Ekstraksi enzim protease Analisis kadar protein Pencirian
LAMPIRAN Lampiran 1 Bagan alir penelitian Biawak air bagian duodenum, jejenum, ileum, kolon Cuci dengan akuades dan kerok lapisan atasnya (mukosa Ekstraksi enzim protease Analisis kadar protein Pencirian
Lampiran 1. Pembuatan Larutan Buffer untuk Dialisa Larutan buffer yang digunakan pada proses dialisa adalah larutan buffer Asetat 10 mm ph 5,4 dan
 39 Lampiran 1. Pembuatan Larutan Buffer untuk Dialisa Larutan buffer yang digunakan pada proses dialisa adalah larutan buffer Asetat 10 mm ph 5,4 dan buffer Asetat 20 mm ph 5,4. Larutan buffer asetat 10
39 Lampiran 1. Pembuatan Larutan Buffer untuk Dialisa Larutan buffer yang digunakan pada proses dialisa adalah larutan buffer Asetat 10 mm ph 5,4 dan buffer Asetat 20 mm ph 5,4. Larutan buffer asetat 10
IV. HASIL DAN PEMBAHASAN. Enzim α-amilase dari Bacillus Subtilis ITBCCB148 diperoleh dengan
 IV. HASIL DAN PEMBAHASAN A. Isolasi Enzim α-amilase Enzim α-amilase dari Bacillus Subtilis ITBCCB148 diperoleh dengan menanam isolat bakteri dalam media inokulum selama 24 jam. Media inokulum tersebut
IV. HASIL DAN PEMBAHASAN A. Isolasi Enzim α-amilase Enzim α-amilase dari Bacillus Subtilis ITBCCB148 diperoleh dengan menanam isolat bakteri dalam media inokulum selama 24 jam. Media inokulum tersebut
BAB III METODE PENELITIAN. A. Waktu dan Tempat Penelitian. Penelitian dilaksanakan pada bulan Maret-November 2012 di
 digilib.uns.ac.id BAB III METODE PENELITIAN A. Waktu dan Tempat Penelitian Penelitian dilaksanakan pada bulan Maret-November 2012 di Laboratorium Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas
digilib.uns.ac.id BAB III METODE PENELITIAN A. Waktu dan Tempat Penelitian Penelitian dilaksanakan pada bulan Maret-November 2012 di Laboratorium Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas
III. METODOLOGI PENELITIAN. Penelitian ini dilakukan pada bulan Juni-November Penelitian ini
 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan Juni-November 2013. Penelitian ini dilakukan di Laboratorium Biokimia dan Laboratorium Biomassa Jurusan Kimia
III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan Juni-November 2013. Penelitian ini dilakukan di Laboratorium Biokimia dan Laboratorium Biomassa Jurusan Kimia
III. METODE PENELITIAN. Penelitian dilaksanakan pada Desember 2014 Mei 2015 di. Laboratorium Mikrobiologi FMIPA Universitas Lampung.
 19 III. METODE PENELITIAN 3.1. Waktu dan Tempat Penelitian Penelitian dilaksanakan pada Desember 2014 Mei 2015 di Laboratorium Mikrobiologi FMIPA Universitas Lampung. 3.2. Alat dan Bahan Alat yang digunakan
19 III. METODE PENELITIAN 3.1. Waktu dan Tempat Penelitian Penelitian dilaksanakan pada Desember 2014 Mei 2015 di Laboratorium Mikrobiologi FMIPA Universitas Lampung. 3.2. Alat dan Bahan Alat yang digunakan
ADLN- PERPUSTAKAAN UNIVERSITAS AIRLANGGA DAFTAR ISI
 DAFTAR ISI Halaman Sampul Luar... i Sampul Dalam... ii Halaman Prasyarat Gelar... iii Halaman Pengesahan... iv UCAPAN TERIMA KASIH... v ABSTRAK... vi ABSTRACT... vii DAFTAR ISI... viii DAFTAR TABEL...
DAFTAR ISI Halaman Sampul Luar... i Sampul Dalam... ii Halaman Prasyarat Gelar... iii Halaman Pengesahan... iv UCAPAN TERIMA KASIH... v ABSTRAK... vi ABSTRACT... vii DAFTAR ISI... viii DAFTAR TABEL...
IV. HASIL DAN PEMBAHASAN
 IV. HASIL DAN PEMBAHASAN A. Isolat Actinomycetes Amilolitik Terpilih 1. Isolat Actinomycetes Terpilih Peremajaan isolat actinomycetes dilakukan dengan tujuan sebagai pemeliharaan isolat actinomycetes agar
IV. HASIL DAN PEMBAHASAN A. Isolat Actinomycetes Amilolitik Terpilih 1. Isolat Actinomycetes Terpilih Peremajaan isolat actinomycetes dilakukan dengan tujuan sebagai pemeliharaan isolat actinomycetes agar
MATERI DAN METODE. Prosedur
 MATERI DAN METODE Lokasi dan Waktu Penelitian ini dilaksanakan di Laboratorium Mikrobiologi dan Laboratorium Terpadu, Departemen Ilmu Produksi dan Teknologi Peternakan, Fakultas Peternakan, Institut Pertanian
MATERI DAN METODE Lokasi dan Waktu Penelitian ini dilaksanakan di Laboratorium Mikrobiologi dan Laboratorium Terpadu, Departemen Ilmu Produksi dan Teknologi Peternakan, Fakultas Peternakan, Institut Pertanian
BAB III METODE PENELITIAN. Penelitian ini merupakan penelitian eksperimental dengan 7 sampel dari 7
 BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian ini merupakan penelitian eksperimental dengan 7 sampel dari 7 individu udang Jari yang diambil dari Segara Anakan Kabupaten Cilacap Jawa Tengah.
BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian ini merupakan penelitian eksperimental dengan 7 sampel dari 7 individu udang Jari yang diambil dari Segara Anakan Kabupaten Cilacap Jawa Tengah.
III BAHAN DAN METODE
 III BAHAN DAN METODE 3.1 Waktu dan Tempat Penelitian ini dilakukan dari bulan Maret 2006 sampai Maret 2007. Penelitian bertempat di laboratorium Mikrobiologi, Departemen Biologi, Fakultas MIPA, Institut
III BAHAN DAN METODE 3.1 Waktu dan Tempat Penelitian ini dilakukan dari bulan Maret 2006 sampai Maret 2007. Penelitian bertempat di laboratorium Mikrobiologi, Departemen Biologi, Fakultas MIPA, Institut
III. METODOLOGI PENELITIAN. Penelitian ini dilaksanakan dari bulan Juli sampai bulan September 2010 di
 20 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan dari bulan Juli sampai bulan September 2010 di Laboratorium Instrumentasi dan Laboratorium Biokimia Jurusan Kimia
20 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan dari bulan Juli sampai bulan September 2010 di Laboratorium Instrumentasi dan Laboratorium Biokimia Jurusan Kimia
II. METODELOGI PENELITIAN
 II. METODELOGI PENELITIAN 2.1 Metode Pengumpulan Data 2.1.1 Waktu dan Tempat Penelitian Penelitian ini dilakukan di UPT Laboratorium Biosain dan Bioteknologi Universitas Udayana. Penelitian ini berlangsung
II. METODELOGI PENELITIAN 2.1 Metode Pengumpulan Data 2.1.1 Waktu dan Tempat Penelitian Penelitian ini dilakukan di UPT Laboratorium Biosain dan Bioteknologi Universitas Udayana. Penelitian ini berlangsung
BAB III METODOLOGI PENELITIAN. Percobaan yang dilakukan pada penelitian ini yaitu penggunaan amonium
 24 BAB III METODOLOGI PENELITIAN Percobaan yang dilakukan pada penelitian ini yaitu penggunaan amonium sulfat dalam menghasilkan enzim bromelin dan aplikasinya sebagai koagulan pada produksi keju. 3.1
24 BAB III METODOLOGI PENELITIAN Percobaan yang dilakukan pada penelitian ini yaitu penggunaan amonium sulfat dalam menghasilkan enzim bromelin dan aplikasinya sebagai koagulan pada produksi keju. 3.1
Lampiran 1 Prosedur Rotofor
 Lampiran 1 Prosedur Rotofor Kalibrasi Membran Ion Membran ion terdiri dari membran kation yang berkorelasi dengan elektrolit H 3 PO 4 0,1 N terpasang pada elektroda anoda sebagai pembawa ion positif, sedangkan
Lampiran 1 Prosedur Rotofor Kalibrasi Membran Ion Membran ion terdiri dari membran kation yang berkorelasi dengan elektrolit H 3 PO 4 0,1 N terpasang pada elektroda anoda sebagai pembawa ion positif, sedangkan
III. METODE KERJA. Penelitian ini telah dilakukan di Laboratorium Mikrobiologi Fakultas
 14 III. METODE KERJA A. Tempat dan Waktu Penelitian Penelitian ini telah dilakukan di Laboratorium Mikrobiologi Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Lampung dari bulan Januari 2015
14 III. METODE KERJA A. Tempat dan Waktu Penelitian Penelitian ini telah dilakukan di Laboratorium Mikrobiologi Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Lampung dari bulan Januari 2015
Lampiran 1 Data Rendemen Pelet Kapang Endofit Xylaria psidii KT30. Berat sampel (pelet) setelah sentrifugase: 0,223 gram
 LAMPIRAN 29 30 Lampiran 1 Data Rendemen Pelet Kapang Endofit Xylaria psidii KT30 1) Kultur 1 Volume kultur awal : 350 ml Volume setelah penyaringan : 300 ml ph awal sebelum ekstraksi : 4,31 Berat sampel
LAMPIRAN 29 30 Lampiran 1 Data Rendemen Pelet Kapang Endofit Xylaria psidii KT30 1) Kultur 1 Volume kultur awal : 350 ml Volume setelah penyaringan : 300 ml ph awal sebelum ekstraksi : 4,31 Berat sampel
3. METODOLOGI PENELITIAN
 3. METODOLOGI PENELITIAN 3.1. Waktu dan tempat Penelitian Penelitian telah dilaksanakan dari bulan Agustus 2006 sampai Juli 2007, bertempat di Laboratorium Bioteknologi Hasil Perairan Departemen Teknologi
3. METODOLOGI PENELITIAN 3.1. Waktu dan tempat Penelitian Penelitian telah dilaksanakan dari bulan Agustus 2006 sampai Juli 2007, bertempat di Laboratorium Bioteknologi Hasil Perairan Departemen Teknologi
BAB III METODE PENELITIAN. dengan mengadakan manipulasi terhadap objek penelitian serta adanya kontrol
 24 BAB III METODE PENELITIAN A. Jenis Penelitian Penelitian yang dilakukan termasuk penelitian dasar dengan metode penelitian eksperimen. Penelitian eksperimen adalah penelitian yang dilakukan dengan mengadakan
24 BAB III METODE PENELITIAN A. Jenis Penelitian Penelitian yang dilakukan termasuk penelitian dasar dengan metode penelitian eksperimen. Penelitian eksperimen adalah penelitian yang dilakukan dengan mengadakan
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN A. Jenis Penelitian Penelitian ini merupakan penelitian murni yang dilakukan dengan metode deskriptif, yaitu suatu metode penelitian untuk membuat deskripsi, gambaran atau lukisan
BAB III METODE PENELITIAN A. Jenis Penelitian Penelitian ini merupakan penelitian murni yang dilakukan dengan metode deskriptif, yaitu suatu metode penelitian untuk membuat deskripsi, gambaran atau lukisan
DEPARTEMEN BIOLOGI FMIPA USU LAMPIRAN
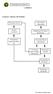 LAMPIRAN Lampiran 1. Diagram Alir Penelitian Peremajaan Bacillus Isolasi Bakteri Oportunistik Produksi Antimikrob Penghitungan Sel Bakteri Oportunistik Pengambilan Supernatan Bebas Sel Pemurnian Bakteri
LAMPIRAN Lampiran 1. Diagram Alir Penelitian Peremajaan Bacillus Isolasi Bakteri Oportunistik Produksi Antimikrob Penghitungan Sel Bakteri Oportunistik Pengambilan Supernatan Bebas Sel Pemurnian Bakteri
3 Percobaan. 3.1 Tempat dan Bahan Penelitian. 3.2 Peralatan
 3 Percobaan 3.1 Tempat dan Bahan Penelitian Penelitian ini dilakukan di Laboratorium Penelitian Biokimia milik Program Studi Kimia Institut Teknologi Bandung. Ragi Saccharomyces cerevisiae yang mengandung
3 Percobaan 3.1 Tempat dan Bahan Penelitian Penelitian ini dilakukan di Laboratorium Penelitian Biokimia milik Program Studi Kimia Institut Teknologi Bandung. Ragi Saccharomyces cerevisiae yang mengandung
7. LAMPIRAN. Gambar 19. Kurva Standar Protein
 7. LAMPIRAN Lampiran 1. Kurva Standar Protein Larutan Bardfrod Commasive blue ditimbang sebanyak 0,01 gram kemudian dilarutkan ke dalam 5 ml etanol 95% dan ditambah dengan 10 ml asam fosfor. Larutan selanjutnya
7. LAMPIRAN Lampiran 1. Kurva Standar Protein Larutan Bardfrod Commasive blue ditimbang sebanyak 0,01 gram kemudian dilarutkan ke dalam 5 ml etanol 95% dan ditambah dengan 10 ml asam fosfor. Larutan selanjutnya
Sampel air panas. Pengenceran 10-1
 Lampiran 1. Metode kerja Sampel air panas Diambil 10 ml Dicampur dengan media selektif 90ml Di inkubasi 24 jam, suhu 50 C Pengenceran 10-1 Di encerkan sampai 10-10 Tiap pengenceran di tanam di cawan petri
Lampiran 1. Metode kerja Sampel air panas Diambil 10 ml Dicampur dengan media selektif 90ml Di inkubasi 24 jam, suhu 50 C Pengenceran 10-1 Di encerkan sampai 10-10 Tiap pengenceran di tanam di cawan petri
III. METODE. Penelitian ini dilaksanakan pada bulan Januari - April 2015 di Laboratorium
 28 III. METODE A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan Januari - April 2015 di Laboratorium Biokimia Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas
28 III. METODE A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan Januari - April 2015 di Laboratorium Biokimia Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas
Air Panas. Isolat Murni Bakteri. Isolat Bakteri Selulolitik. Isolat Terpilih Bakteri Selulolitik. Kuantitatif
 75 Lampiran 1. Metode Kerja L.1.1 Bagan kerja Air Panas - Isolasi dan Seleksi Bakteri Pemurnian Bakteri Isolat Murni Bakteri Uji Bakteri Penghasil Selulase Secara Kualitatif Isolat Bakteri Selulolitik
75 Lampiran 1. Metode Kerja L.1.1 Bagan kerja Air Panas - Isolasi dan Seleksi Bakteri Pemurnian Bakteri Isolat Murni Bakteri Uji Bakteri Penghasil Selulase Secara Kualitatif Isolat Bakteri Selulolitik
LAPORAN PRAKTIKUM BIOKIMIA PERCOBAAN KE 2 PEMISAHAN PROTEIN PUTIH TELUR DENGAN FRAKSINASI (NH 4 ) 2 SO 4
 LAPORAN PRAKTIKUM BIOKIMIA PERCOBAAN KE 2 PEMISAHAN PROTEIN PUTIH TELUR DENGAN FRAKSINASI (NH 4 ) 2 SO 4 Disusun oleh : Ulan Darulan - 10511046 Kelompok 1 Asisten Praktikum : R. Roro Rika Damayanti (10510065)
LAPORAN PRAKTIKUM BIOKIMIA PERCOBAAN KE 2 PEMISAHAN PROTEIN PUTIH TELUR DENGAN FRAKSINASI (NH 4 ) 2 SO 4 Disusun oleh : Ulan Darulan - 10511046 Kelompok 1 Asisten Praktikum : R. Roro Rika Damayanti (10510065)
III. METODE PENELITIAN
 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan April - September 2015. Penelitian ini dilakukan di Laboratorium Biokimia Jurusan Kimia Fakultas Matematika dan
III. METODE PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan April - September 2015. Penelitian ini dilakukan di Laboratorium Biokimia Jurusan Kimia Fakultas Matematika dan
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian dilakukan pada 4 April 2016 sampai 16 Agustus 2016. Penelitian ini dilaksanakan di Laboratorium Riset Kimia Material dan Hayati Departemen
BAB III METODE PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian dilakukan pada 4 April 2016 sampai 16 Agustus 2016. Penelitian ini dilaksanakan di Laboratorium Riset Kimia Material dan Hayati Departemen
Lampiran 1. Bahan-bahan yang digunakan untuk pengujian aktivitas enzim (Grossowicz et al., 1950) (a). Reagen A 1. 0,2 M bufer Tris-HCl ph 6,0 12,1 gr
 46 47 Lampiran 1. Bahan-bahan yang digunakan untuk pengujian aktivitas enzim (Grossowicz et al., 1950) (a). Reagen A 1. 0,2 M bufer Tris-HCl ph 6,0 12,1 gr Tris base dilarutkan dalam 200 ml akuades, kemudian
46 47 Lampiran 1. Bahan-bahan yang digunakan untuk pengujian aktivitas enzim (Grossowicz et al., 1950) (a). Reagen A 1. 0,2 M bufer Tris-HCl ph 6,0 12,1 gr Tris base dilarutkan dalam 200 ml akuades, kemudian
III. METODOLOGI PENELITIAN. Penelitian ini dilaksanakan dari bulan Maret 2011 sampai dengan bulan
 26 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian ini dilaksanakan dari bulan Maret 2011 sampai dengan bulan November 2011 di Laboratorium Mikrobiologi Balai Riset dan Standarisasi Industri
26 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian ini dilaksanakan dari bulan Maret 2011 sampai dengan bulan November 2011 di Laboratorium Mikrobiologi Balai Riset dan Standarisasi Industri
3 METODE. Bahan. Alat
 9 3 METODE Penelitian ini dilaksanakan selama 14 bulan, yaitu dari April 2013 sampai Mei 2014 di Laboratorium Biokimia Departemen Ilmu dan Teknologi Pangan IPB, Seafast Center, Pusat Studi Satwa Primata
9 3 METODE Penelitian ini dilaksanakan selama 14 bulan, yaitu dari April 2013 sampai Mei 2014 di Laboratorium Biokimia Departemen Ilmu dan Teknologi Pangan IPB, Seafast Center, Pusat Studi Satwa Primata
Asam Asetat Glacial = 5,7 ml EDTA 0,5 M ph 8.0 = 10 ml Aquades ditambahkan hingga volume larutan 100 ml
 36 Lampiran 1. Pembuatan Larutan Stok dan Buffer A. Pembuatan Larutan Stok Tris HCL 1 M ph 8.0 (100 ml) : Timbang Tris sebanyak 12,114 g. Masukkan Tris ke dalam Erlenmeyer dan ditambahkan 80 ml aquades.
36 Lampiran 1. Pembuatan Larutan Stok dan Buffer A. Pembuatan Larutan Stok Tris HCL 1 M ph 8.0 (100 ml) : Timbang Tris sebanyak 12,114 g. Masukkan Tris ke dalam Erlenmeyer dan ditambahkan 80 ml aquades.
BAHAN DAN METODE Waktu dan Tempat Penelitian Alat dan Bahan Alat Bahan
 BAHAN DAN METODE Waktu dan Tempat Penelitian Penelitian dilakukan di Laboratorium Mikrobiologi dan Laboratorium Rekayasa Genetika Puslit Limnologi LIPI Cibinong, Laboratorium Bioremediasi Puslit Bioteknologi
BAHAN DAN METODE Waktu dan Tempat Penelitian Penelitian dilakukan di Laboratorium Mikrobiologi dan Laboratorium Rekayasa Genetika Puslit Limnologi LIPI Cibinong, Laboratorium Bioremediasi Puslit Bioteknologi
Sampel air kolam, usus ikan nila dan endapan air kolam ikan. Seleksi BAL potensial (uji antagonis)
 Lampiran 1. Diagram Alir Penelitian Sampel air kolam, usus ikan nila dan endapan air kolam ikan. Seleksi BAL potensial (uji antagonis) Str Isolasi dan Karakteristik Bakteri Asam Laktat Isolat Bakteri Asam
Lampiran 1. Diagram Alir Penelitian Sampel air kolam, usus ikan nila dan endapan air kolam ikan. Seleksi BAL potensial (uji antagonis) Str Isolasi dan Karakteristik Bakteri Asam Laktat Isolat Bakteri Asam
III. METODOLOGI PENELITIAN
 III. METODOLOGI PENELITIAN 3.1 WAKTU DAN TEMPAT Penelitian dilaksanakan pada bulan Januari 2012 hingga September 2012. Penelitian dilaksanakan di Laboratorium Pengembangan Teknologi Industri Agro dan Biomedika
III. METODOLOGI PENELITIAN 3.1 WAKTU DAN TEMPAT Penelitian dilaksanakan pada bulan Januari 2012 hingga September 2012. Penelitian dilaksanakan di Laboratorium Pengembangan Teknologi Industri Agro dan Biomedika
LAMPIRAN. Lampiran 1. Foto Lokasi Pengambilan Sampel Air Panas Pacet Mojokerto
 LAMPIRAN Lampiran 1. Foto Lokasi Pengambilan Sampel Air Panas Pacet Mojokerto Lampiran 2. Pembuatan Media dan Reagen 2.1 Pembuatan Media Skim Milk Agar (SMA) dalam 1000 ml (Amelia, 2005) a. 20 gram susu
LAMPIRAN Lampiran 1. Foto Lokasi Pengambilan Sampel Air Panas Pacet Mojokerto Lampiran 2. Pembuatan Media dan Reagen 2.1 Pembuatan Media Skim Milk Agar (SMA) dalam 1000 ml (Amelia, 2005) a. 20 gram susu
Dari uji kompetisi, persentase penghambatan dengan rasio inokulum 1:1 sudah cukup bagi Bacillus sp. Lts 40 untuk menghambat pertumbuhan V.
 27 PEMBAHASAN Dari tiga isolat sp. penghasil antimikrob yang diseleksi, isolat sp. Lts 40 memiliki aktivitas penghambatan paling besar terhadap E. coli dan V. harveyi dengan indeks penghambatan masing-masing
27 PEMBAHASAN Dari tiga isolat sp. penghasil antimikrob yang diseleksi, isolat sp. Lts 40 memiliki aktivitas penghambatan paling besar terhadap E. coli dan V. harveyi dengan indeks penghambatan masing-masing
III. METODE PENELITIAN. Penelitian ini dilakukan pada bulan Februari sampai dengan Desember di Laboratorium Biomasa Universitas Lampung.
 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan Februari sampai dengan Desember 2011 di Laboratorium Biomasa Universitas Lampung. B. Alat dan Bahan Alat-alat yang
III. METODE PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan Februari sampai dengan Desember 2011 di Laboratorium Biomasa Universitas Lampung. B. Alat dan Bahan Alat-alat yang
3 Metode Penelitian. 3.1 Alat
 3 Metode Penelitian 3.1 Alat Peralatan yang digunakan pada penelitian ini adalah peralatan gelas standar meliputi: labu erlenmeyer, cawan petri, gelas ukur, gelas kimia, botol reagen, tabung reaksi, batang
3 Metode Penelitian 3.1 Alat Peralatan yang digunakan pada penelitian ini adalah peralatan gelas standar meliputi: labu erlenmeyer, cawan petri, gelas ukur, gelas kimia, botol reagen, tabung reaksi, batang
III. METODELOGI PENELITIAN. Penelitian ini dilaksanakan pada bulan Mei-November 2013 di Laboratorium
 24 III. METODELOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan Mei-November 2013 di Laboratorium Biokimia dan Laboratorium Instrumentasi Jurusan Kimia Fakultas Matematika
24 III. METODELOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan Mei-November 2013 di Laboratorium Biokimia dan Laboratorium Instrumentasi Jurusan Kimia Fakultas Matematika
METODE. A. Peremajaan Salmonella sp. B. Verifikasi Salmonella sp.
 METODE Alur Penelitian Alur penelitian dan metode yang digunakan dalam penelitian ini terdiri dari 6 tahapan, yaitu: peremajaan bakteri Salmonella sp., verifikasi bakteri Salmonella sp., isolasi fage,
METODE Alur Penelitian Alur penelitian dan metode yang digunakan dalam penelitian ini terdiri dari 6 tahapan, yaitu: peremajaan bakteri Salmonella sp., verifikasi bakteri Salmonella sp., isolasi fage,
PEMURNIAN DAN KARAKTERISASI PROTEIN INHIBITOR RNA HELIKASE VIRUS HEPATITIS C DARI Streptomyces chartreusis AINUN HAIRANY
 PEMURNIAN DAN KARAKTERISASI PROTEIN INHIBITOR RNA HELIKASE VIRUS HEPATITIS C DARI Streptomyces chartreusis 5-095 AINUN HAIRANY SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR BOGOR 2010 PERNYATAAN MENGENAI
PEMURNIAN DAN KARAKTERISASI PROTEIN INHIBITOR RNA HELIKASE VIRUS HEPATITIS C DARI Streptomyces chartreusis 5-095 AINUN HAIRANY SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR BOGOR 2010 PERNYATAAN MENGENAI
BAHAN DAN METODE. Penelitian ini dilaksanakan di Laboratorium Analisis Hasil Pertanian dan
 III. BAHAN DAN METODE 3.1. Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Analisis Hasil Pertanian dan Laboratorium Mikrobiologi Hasil Pertanian, Jurusan Teknologi Hasil Pertanian,
III. BAHAN DAN METODE 3.1. Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Analisis Hasil Pertanian dan Laboratorium Mikrobiologi Hasil Pertanian, Jurusan Teknologi Hasil Pertanian,
BAB III METODE PENELITIAN. lengkap (RAL) pola faktorial yang terdiri dari 2 faktor. Faktor pertama adalah variasi
 BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Rancangan yang digunakan dalam penelitian ini adalah rancangan acak lengkap (RAL) pola faktorial yang terdiri dari 2 faktor. Faktor pertama adalah variasi
BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Rancangan yang digunakan dalam penelitian ini adalah rancangan acak lengkap (RAL) pola faktorial yang terdiri dari 2 faktor. Faktor pertama adalah variasi
3 METODE PENELITIAN. 3.1 Bahan Bahan penelitian
 3 METODE PENELITIAN 3.1 Bahan 3.1.1 Bahan penelitian Cacing tanah P. excavatus diperoleh dari peternakan cacing milik Ir. Bambang Sudiarto. Substrat koagulan darah diambil dari darah milik S. Krisnawati
3 METODE PENELITIAN 3.1 Bahan 3.1.1 Bahan penelitian Cacing tanah P. excavatus diperoleh dari peternakan cacing milik Ir. Bambang Sudiarto. Substrat koagulan darah diambil dari darah milik S. Krisnawati
III. METODE PENELITIAN. Penelitian ini dilakukan pada bulan Januari 2015 Juli 2015, bertempat di
 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan Januari 2015 Juli 2015, bertempat di Laboratorium Kimia Organik, Jurusan Kimia, Fakultas Matematika dan Ilmu Pengetahuan
III. METODE PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan Januari 2015 Juli 2015, bertempat di Laboratorium Kimia Organik, Jurusan Kimia, Fakultas Matematika dan Ilmu Pengetahuan
BAB III METODE PENELITIAN. Alat-alat yang digunakan dalam penelitian ini, antara lain: waterbath,
 31 BAB III METODE PENELITIAN 3.1 Alat dan Bahan Alat dan bahan yang digunakan dalam penelitian ini adalah sebagai berikut: 3.1.1 Alat Alat-alat yang digunakan dalam penelitian ini, antara lain: waterbath,
31 BAB III METODE PENELITIAN 3.1 Alat dan Bahan Alat dan bahan yang digunakan dalam penelitian ini adalah sebagai berikut: 3.1.1 Alat Alat-alat yang digunakan dalam penelitian ini, antara lain: waterbath,
III. METODOLOGI PENELITIAN. Penelitian ini dilaksanakan dari bulan Maret sampai bulan Agustus 2013 di
 25 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan dari bulan Maret sampai bulan Agustus 2013 di Laboratorium Instrumentasi dan Laboratorium Biokimia Jurusan Kimia
25 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan dari bulan Maret sampai bulan Agustus 2013 di Laboratorium Instrumentasi dan Laboratorium Biokimia Jurusan Kimia
BAB 3 PERCOBAAN. Alat elektroforesis agarosa (Biorad), autoklaf, cawan Petri, GeneAid High Speed Plasmid
 BAB 3 PERCOBAAN 3.1 Alat Alat elektroforesis agarosa (Biorad), autoklaf, cawan Petri, GeneAid High Speed Plasmid Mini kit, inkubator goyang (GSL), jarum Ose bundar, kit GFX (GE Healthcare), kompor listrik
BAB 3 PERCOBAAN 3.1 Alat Alat elektroforesis agarosa (Biorad), autoklaf, cawan Petri, GeneAid High Speed Plasmid Mini kit, inkubator goyang (GSL), jarum Ose bundar, kit GFX (GE Healthcare), kompor listrik
II. BAHAN DAN METODE
 II. BAHAN DAN METODE 2.1 Rancangan Perlakuan Penelitian ini terdiri dari enam perlakuan yang masing-masing diberi 3 kali ulangan. Perlakuan yang diberikan berupa perendaman dengan dosis relhp berbeda yaitu
II. BAHAN DAN METODE 2.1 Rancangan Perlakuan Penelitian ini terdiri dari enam perlakuan yang masing-masing diberi 3 kali ulangan. Perlakuan yang diberikan berupa perendaman dengan dosis relhp berbeda yaitu
ISOLASI DAN PEMURNIAN PROTEIN INHIBITOR RNA HELIKASE VIRUS HEPATITIS C DARI KAPANG ENDOFIT CgKTm 5 F ERVIAN HADI RAMDANI
 ISOLASI DAN PEMURNIAN PROTEIN INHIBITOR RNA HELIKASE VIRUS HEPATITIS C DARI KAPANG ENDOFIT CgKTm 5 F ERVIAN HADI RAMDANI DEPARTEMEN BIOKIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN
ISOLASI DAN PEMURNIAN PROTEIN INHIBITOR RNA HELIKASE VIRUS HEPATITIS C DARI KAPANG ENDOFIT CgKTm 5 F ERVIAN HADI RAMDANI DEPARTEMEN BIOKIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN
BAB III BAHAN DAN CARA KERJA. Penelitian dilakukan di Laboratorium Institute of Human Virology and
 23 BAB III BAHAN DAN CARA KERJA A. LOKASI DAN WAKTU PENELITIAN Penelitian dilakukan di Laboratorium Institute of Human Virology and Cancer Biology of the University of Indonesia (IHVCB-UI), Jl. Salemba
23 BAB III BAHAN DAN CARA KERJA A. LOKASI DAN WAKTU PENELITIAN Penelitian dilakukan di Laboratorium Institute of Human Virology and Cancer Biology of the University of Indonesia (IHVCB-UI), Jl. Salemba
BAB III METODE PENELITIAN Bagan Alir Penelitian ini secara umum dapat digambarkan pada skema berikut:
 BAB III METODE PENELITIAN Tahapan-tahapan yang dilakukan dalam penelitian ini adalah: pengumpulan sampel, lisis terhadap sampel mtdna yang telah diperoleh, amplifikasi daerah HVI mtdna sampel dengan menggunakan
BAB III METODE PENELITIAN Tahapan-tahapan yang dilakukan dalam penelitian ini adalah: pengumpulan sampel, lisis terhadap sampel mtdna yang telah diperoleh, amplifikasi daerah HVI mtdna sampel dengan menggunakan
Metode Pengukuran Spektrofotometri (Bergmeyer et al. 1974) Pembuatan Media Heterotrof Media Heterotrof Padat. Pengaruh ph, Suhu, Konsentrasi dan
 4 Metode Penelitian ini dilakukan pada beberapa tahap yaitu, pembuatan media, pengujian aktivitas urikase secara kualitatif, pertumbuhan dan pemanenan bakteri, pengukuran aktivitas urikase, pengaruh ph,
4 Metode Penelitian ini dilakukan pada beberapa tahap yaitu, pembuatan media, pengujian aktivitas urikase secara kualitatif, pertumbuhan dan pemanenan bakteri, pengukuran aktivitas urikase, pengaruh ph,
BAB III METODOLOGI PENELITIAN. Penelitian akan diawali dengan preparasi alat dan bahan untuk sampling
 16 BAB III METODOLOGI PENELITIAN Penelitian akan diawali dengan preparasi alat dan bahan untuk sampling sel folikel akar rambut. Sampel kemudian dilisis, diamplifikasi dan disekuensing dengan metode dideoksi
16 BAB III METODOLOGI PENELITIAN Penelitian akan diawali dengan preparasi alat dan bahan untuk sampling sel folikel akar rambut. Sampel kemudian dilisis, diamplifikasi dan disekuensing dengan metode dideoksi
III. METODOLOGI PENELITIAN. Penelitian ini dilakukan pada bulan Agustus-Desember 2015 di Laboratorium
 23 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan Agustus-Desember 2015 di Laboratorium Biokimia Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam
23 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan Agustus-Desember 2015 di Laboratorium Biokimia Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam
s - soluble fraction i - insoluble fraction p - post-ni 2+ column
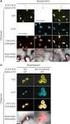 METODE SDS- PAGE Oleh: Susila Kristianingrum susila.k@uny.ac.id SDS-PAGE Trx-STS Trx-CHS s i p s i p 97 66 45 60 K 31 22 14 s - soluble fraction i - insoluble fraction p - post-ni 2+ column Langkah SDS-PAGE
METODE SDS- PAGE Oleh: Susila Kristianingrum susila.k@uny.ac.id SDS-PAGE Trx-STS Trx-CHS s i p s i p 97 66 45 60 K 31 22 14 s - soluble fraction i - insoluble fraction p - post-ni 2+ column Langkah SDS-PAGE
BAB III METODE PENELITIAN. yang digunakan adalah Rancangan Acak Lengkap (RAL) dengan 4 perlakuan dan
 BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian ini merupakan penelitian eksperimental. Rancangan penelitian yang digunakan adalah Rancangan Acak Lengkap (RAL) dengan 4 perlakuan dan 6 ulangan,
BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian ini merupakan penelitian eksperimental. Rancangan penelitian yang digunakan adalah Rancangan Acak Lengkap (RAL) dengan 4 perlakuan dan 6 ulangan,
III. METODE PERCOBAAN. Penelitian ini dilaksanakan pada bulan Februari sampai April 2014 di
 18 III. METODE PERCOBAAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan Februari sampai April 2014 di Laboratorium Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan
18 III. METODE PERCOBAAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan Februari sampai April 2014 di Laboratorium Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan
Metode Penelitian. III.2.1 Sampel
 18 Bab III Metode Penelitian III.1 Alat Alat-alat yang digunakan dalam penelitian ini adalah sentrifuga Beckman JA-14, ph meter digital Beckman, vortex, spektrofotometer Spectronik 20, kuvet plastik, Smartspec
18 Bab III Metode Penelitian III.1 Alat Alat-alat yang digunakan dalam penelitian ini adalah sentrifuga Beckman JA-14, ph meter digital Beckman, vortex, spektrofotometer Spectronik 20, kuvet plastik, Smartspec
Hasil dan Pembahasan
 27 Bab IV Hasil dan Pembahasan IV.1 Isolasi Enzim katalase dari kentang Enzim katalase terdapat dalam peroksisom, organel yang ditemukan pada jaringan tumbuhan di luar inti sel kentang sehingga untuk mengekstraknya
27 Bab IV Hasil dan Pembahasan IV.1 Isolasi Enzim katalase dari kentang Enzim katalase terdapat dalam peroksisom, organel yang ditemukan pada jaringan tumbuhan di luar inti sel kentang sehingga untuk mengekstraknya
KEMENTERIAN PENDIDIKAN DAN KEBUDAYAAN DIREKTORAT JENDERAL PENDIDIKAN MENENGAH DIREKTORAT PEMBINAAN SEKOLAH MENENGAH ATAS
 KEMENTERIAN PENDIDIKAN DAN KEBUDAYAAN DIREKTORAT JENDERAL PENDIDIKAN MENENGAH DIREKTORAT PEMBINAAN SEKOLAH MENENGAH ATAS Test Seleksi Calon Peserta International Biology Olympiad (IBO) 2014 2 8 September
KEMENTERIAN PENDIDIKAN DAN KEBUDAYAAN DIREKTORAT JENDERAL PENDIDIKAN MENENGAH DIREKTORAT PEMBINAAN SEKOLAH MENENGAH ATAS Test Seleksi Calon Peserta International Biology Olympiad (IBO) 2014 2 8 September
o C 1 menit, penempelan 50 o C 1 menit, polimerisasi 72 o C 1 menit (tiga tahap ini
 13 BAB IV PERCOBAAN IV.1 Bahan Air miliq, deoksinukleotida trifosfat (dntp), MgCl 2, (Promega), enzim Pfu DNA polymerase, dapar Pfu (Stratagene), oligonukleotida SR1, SR2, SR3, SR4, SR5, AR6, AR7, AR8,
13 BAB IV PERCOBAAN IV.1 Bahan Air miliq, deoksinukleotida trifosfat (dntp), MgCl 2, (Promega), enzim Pfu DNA polymerase, dapar Pfu (Stratagene), oligonukleotida SR1, SR2, SR3, SR4, SR5, AR6, AR7, AR8,
ANALISIS PROTEIN SPESIFIK TEMBAKAU SRINTHIL. Disusun oleh : Nama : Slamet Haryono NIM :
 ANALISIS PROTEIN SPESIFIK TEMBAKAU SRINTHIL Disusun oleh : Nama : Slamet Haryono NIM : 412000011 FAKULTAS BIOLOGI UNIVERSITAS KRISTEN SATYA WACANA SALATIGA 2004 1. PENDAHULUAN Tembakau srinthil merupakan
ANALISIS PROTEIN SPESIFIK TEMBAKAU SRINTHIL Disusun oleh : Nama : Slamet Haryono NIM : 412000011 FAKULTAS BIOLOGI UNIVERSITAS KRISTEN SATYA WACANA SALATIGA 2004 1. PENDAHULUAN Tembakau srinthil merupakan
1 atm selama 15 menit
 85 Lampiran 1. Prosedur Kerja L.1.1 Pembuatan Media Nutrient Agar Media Nutrient Agar - ditimbang sebanyak 20 gram dan dimasukkan dalam erlenmeyer 1000 ml - dilarutkandengan aquades 1000 ml - dipanaskan
85 Lampiran 1. Prosedur Kerja L.1.1 Pembuatan Media Nutrient Agar Media Nutrient Agar - ditimbang sebanyak 20 gram dan dimasukkan dalam erlenmeyer 1000 ml - dilarutkandengan aquades 1000 ml - dipanaskan
III. METODE. Penelitian ini dilaksanakan pada bulan Januari-April 2015 di Laboratorium
 23 III. METODE A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan Januari-April 2015 di Laboratorium Biokimia Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas
23 III. METODE A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan Januari-April 2015 di Laboratorium Biokimia Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas
Kadar protein (%) = (ml H 2 SO 4 ml blanko) x N x x 6.25 x 100 % bobot awal sampel (g) Keterangan : N = Normalitas H 2 SO 4
 LAMPIRAN Lampiran 1. Prosedur Analisis. 1. Kadar Air (AOAC, 1999) Sebanyak 3 gram sampel ditimbang dalam cawan alumunium yang telah diketahui bobot keringnya. tersebut selanjutnya dikeringkan dalam oven
LAMPIRAN Lampiran 1. Prosedur Analisis. 1. Kadar Air (AOAC, 1999) Sebanyak 3 gram sampel ditimbang dalam cawan alumunium yang telah diketahui bobot keringnya. tersebut selanjutnya dikeringkan dalam oven
