Disarikan dari berbagai sumber oleh : Dr. Sri Handayani Jurdik Kimia FMIPA Disampaikan Oleh : Dr. Kun Sri Budiasih
|
|
|
- Leony Indradjaja
- 7 tahun lalu
- Tontonan:
Transkripsi
1 Disarikan dari berbagai sumber oleh : Dr. Sri Handayani Jurdik Kimia FMIP Disampaikan Oleh : Dr. Kun Sri Budiasih
2 Yang dipelajari : Pengertian Persamaan Laju Orde reaksi Pengaruh Temperatur terhadap laju reaksi Pengaruh Konsentrasi terhadap laju reaksi Katalis
3 5 Reaksi Orde Nol 6 Reaksi Orde Satu 7 Reaksi Orde Dua 8 Waktu Paruh
4 POKOK BHSN (#7) 9 Model Teoritis Kinetika Kimia 0 Pengaruh Temperatur Mekanisme Reaksi Katalisis
5 pakah laju reaksi itu...? Laju reaksi B
6 KONSEP LJU REKSI Laju reaksi kimia adalah perubahan konsentrasi pereaksi atau produk dalam suatu satuan waktu. Laju reaksi dapat dinyatakan sebagai laju berkurangnya konsentrasi suatu pereaksi atau laju bertambahnya konsentrasi suatu produk persatuan waktu. B Laju reaksi d d t d B d t
7 Perhatikan reaksi berikut : 3 B Laju reaksi Persamaan di atas dapat diartikan tiga mol berkurang untuk setiap mol B yang terbentuk. tau laju berkurangnya adalah tiga kali lebih cepat d dibandingkan d B d terbentuknya C dd B. Sehingga laju reaksi tersebut : a d t b d t c d t d d t Laju reaksi 3 d d t d B d t Secara umum, untuk reaksi : a + bb cc + dd
8 PENENTUN PERSMN LJU Mempelajari laju reaksi berarti : - menentukan pers. Laju - menentukan tetapan laju - menentukan orde reaksi Pers. laju, tetapan laju dan orde reaksi merupakan hasil eksperimen. Data kinetika pada umumnya berupa informasi tentang konsentrasi pereaksi atau hasil reaksi pada berbagai waktu
9 CR PENENTUN PERSMN LJU. Cara Laju wal Laju diukur pada saat awal reaksi untuk berbagai konsentrasi awal pereaksi Misal : + B Produk Laju reaksi V k a B b Konsentrasi awal : [] o Konsentrasi awal B : [B] o Maka laju awal adalah : Vo k Logaritma persamaan di atas menghasilkan : log V o log k alog o a b o B o blog B o
10 o log V o log k alog o blog B Untuk [B] tetap dibuat grafik log V 0 terhadap log [] 0 log V 0 Slope = tg α = a Intersep = log k log [] 0
11 . Cara Integrasi atau Grafik Untuk membuktikan orde reaksi REKSI ORDE Reaksi orde adalah reaksi-reaksi yang lajunya berbanding langsung hanya dengan konsentrasi satu senyawa ln 0 B d Laju reaksi k d t Hasil eksperimen memberikan harga konsentrasi pada berbagai waktu. Jika konsentrasi pada t = 0 adalah 0 dan pada t tertentu konsentrasi adalah, maka integrasinya : k. t 0 k. t ln ln d k t 0 d t 0
12 Grafik reaksi orde lurus. ln [] ln ln t plot ln [] thd t membentuk garis ln t 0 0 Intersep : [ 0 ] Slope : -k k. t 0 k. t ln k k. t 0,693 k Waktu paruh (t / ) Pada saat t = t / maka =/ 0
13 REKSI ORDE Reaksi dikatakan memiliki orde, jika laju reaksi sebanding dengan kuadrat konsentrasi salah satu pereaksi atau dengan hasil kali konsentrasi dua pereaksi yang masing-masing dipangkatkan satu Laju reaksi 0 d 0 + B 0 d d t k t 0 d t k. t k. t k produk. Jika konsentrasi awal kedua pereaksi sama /[] Intersep : /[ 0 ] Slope : k t
14 k t t k t k Pada saat t = t / maka [] = ½ [ o ] Waktu paruh orde
15 . Jka konsentrasi awal kedua reaktan tidak sama + B C a b (a-x) (b-x) x V = = k [ ] [B] = k ( a-x )( b-x) = k dt
16 = k Gunakan aturan integral parsial = + = (b - x) + B( a-x) = ( b - x ) + B ( a - x ) Misal : x = b = B ( a - b ) B =
17 x = a = ( b a ) = = = ( b - x ) + B ( a - x ) = = k dt = k dt
18 = k x 0 = k t = k t = k t = k t = k t
19 . Jika konsentrasi awal pereksi sama t k C C t k C C dt k C C d t C C REKSI ORDE 3
20 + B C W L : [ ] 0 [B]0 B E R E K S I : X X X [ ] 0 - X [B]0 - X [B] 0 = [] 0. Jika konsentrasi awal pereksi tidak sama x k x x k B k dt d kt ] [ ] [ 0 8 ] [ ] [ ] [ ] [ ] 4[ ] [ kdt d kt 0 ] [ ] [ 8
21 ] [ ] [ ] [ ] [ ] 4[ ] [ kdt d kt ] [ ] [ 0 8 kt 0 ] [ ] [ 8 kt 8 ] [ ] [ 0
22 [B] = []0 X [B] = {[]0 X } d[ ] dt k[ ][ B] k [ ] x [ x 0 ] 0 k [ ] x 4 [ x 0 ] 0 3 k [ 4 x ] 0 k4[ ] 3
23 PENGRUH TEMPERTUR TERHDP LJU REKSI
24 PERSMN RRHENIUS / ln ln ln ln ln ln ln T T R Ea k k T R Ea k T R Ea k T R Ea k e k RT Ea
25 PENGRUH KONSENTRSI DN TEMPERTUR
26 CONTOH SOL. Dari hasil pengamatan reaksi antara NO dengan Br : NO(g) + Br (g) NOBr(g) menghasilkan data sebagai berikut : Percobaan ke : Konsentrasi awal Mol/dm 3 NO Br Kecepatan awal pembentukan NOBr mol/dm 3.dt ,0 0,0 0,0 0,0 0,30 0,0 0,0 0,30 0,0 0, Tentukan orde reaksi dan konstanta reaksi!
27 Jawab : V = k [NO] x [Br ] y Pada percobaan s/d 3, konsentrasi NO konstan, sedangkan Br bervariasi. Jadi laju reaksi yang bervariasi akibat perubahan konsentrasi Brom, Br 0,0 0,0 3 0,0 V 3 Jadi V [Br ] berarti reaksi orde terhadap Brom Pada percobaan, 4 dan 5 konsentrasi Brom tetap, konsentrasi NO bervariasi, jadi variasi laju reaksi akibat dari variasi konsentrasi NO. NO 0,0 0,0 3 0,0 V 4 atau 9 atau 3 3 Jadi V [NO] berarti reaksi orde terhadap NO
28 V total = k [NO] [Br ] Orde reaksi = ( +) = 3 Dari percobaan didapatkan data : mol/dm 3 dt = k (0,0 mol/dm 3 ) ( 0,0 mol/ dm 3 ) = k ( 0,000 mol 3 /dm 9 3 mol / dm dt k = 3 0,000 mol / dm =,.0 4 dm 9 mol - dt
29 . Suatu wadah berisi hidrogen iodida dengan konsentrasi sebesar 0,040 M, Laju penguraian HI ditentukan sebesar 8,0 x 0-6 mol L- S-. Berapakah laju reaksi pada temperatur yang sama, bila konsentrasi HI dikurangi menjadi 0,00 M, diketahui orde reaksi sama dengan? Jawab: Reaksi : HI H + I Persamaan lajun = k [HI] Untuk laju pertama 8,0 0-6 mol L - S - = k (0,04 M) Untuk laju kedua laju = k (0,00 M) dari persamaan di atas diperoleh, k Laju = 8,0 0 6 mol L 0,040 M S Laju 0,00 M 6 8,0 0 mol L S 0,00 M 0,040 M = = 5,0 x 0-7 mol L - S -
30 3. Reaksi dekomposisi termal pada suhu 98 0 C adalah sbb : H 3 CN = NCH 3 (g) C H 6 (g) + N (g) Data : t (menit) 0,0,0 35,0 ~ P (torr) 49,9 548,0 609,0 86,6 a. Buktikan bahwa reaksi mengikuti persamaan laju orde b. Hitung harga tetapan laju pada suhu 30,6 0 C, jika t / = 9,5 menit c. Berapakah harga Ea Data diatas menunjukkan adanya t ~, yang berarti reaktan pada saat itu habis kondisi reaktan pada saat t = 0 adl P = 86,6 torr Dibuat data baru antara t dengan reaktan t (menit) 0 0,0,0 35,0 P (torr) 86,6 369,7 33,6 5,6 ln P reaktan 6,8 5,9 5,7 5,5
31 a. Pembuktian reaksi orde dp k P dt 0 dp P k. dt - (ln P ln P 0 ) = kt ln P = ln P 0 - kt Ln P t b. slope k k 5,7 5,9 0 0,08 0,08 k 0,03 T = 30,6 o C = 593,6 K t / = 9,5 menit k =,693 9,5menit 0 0,073menit T = 98 o C = 57 K t / = 0,693 0,03,66 menit
32 ,6 57 0,073 0,03 / 0,87 0 6,67 0,85.8,34 0 6,67 0, ,6 0,03 0,073 ln ln ln ln. kj mol K x K mol J Ea K x R Ea K R Ea dt RT Ea k d diturunkanterhadap T RT Ea k e k RT Ea
33 SOL LTIHN. Salah satu reaksi gas yang terjadi dalam kendaraan adalah: NO (g) + CO(g) NO(g) + CO (g) Laju = k[no ] m [CO] n Jika diketahui data sebagai berikut, tentukan orde reaksi keseluruhan Eksperimen Laju awal (mol/l.s) [NO ] awal (mol/l) [CO] awal (mol/l) 0,0050 0,0 0,0 0,080 0,40 0,0 3 0,0050 0,0 0,0
34 . Penggabungan kembali atom-atom iodium dalam fasa gas dan yang mengandung argon mempunyai laju awal sbb : [I] 0 /0-5 M,0,0 4,0 6,0 Laju awal (M/det) a. 8,7X0-4 3,48X0-3,39X0-3,3X0 - b. 4,35X0-3,74X0-6,96X0 -,57X0 - c. 8,69X0-3 3,47X0 -,38X0-3,3X0 - Konsentrasi r pada keadaan : a.,0 x 0-3 M b. 5,0 x 0-3 M c.,0 x 0 - M Tentukan orde reaksi dan tetapan laju penggabungan tsb dengan Menggunakan cara laju awal, dimanareaksinya dapat ditulis sbb : I + r I + r
35 3. The initial rate of formation of a sobstance J depended on concentration as follows : [J] 0 /0-3 M 5,0 8, 7 30 V j,0 /0-7 Ms - 3,6 9, Find the order of reaction and the rate constant 4. Siklobutana (C 4 H 8 ) terdekomposisi pada 000 o C menjadi dua molekul etilen (C H 4 ) dengan konstanta laju reaksi orde satu 87 s - a. Jika konsentrasi awal siklobutana,00 M berapa konsentrasinya setelah 0,00 s? b. Berapa fraksi siklobutana terdekomposisi pada waktu tersebut
36 5. Harga tetapan laju k dari suatu reaksi pada berbagai suhu diamati sbb: T (K) k 0,04 0,40 0,894,356 5,039 9,3 Bila data tersebut diinterpretasikan berdasarkan hubungan rrhenius, k =. e -Ea/RT Tentukan harga dan energi pengaktifan Ea
37 ln k Jawab : k. e Ea / RT ln k ln Ea RT /T 0,004 0,0033 0,009 0,005 0,00 0,00 ln k -3,7 -,43-0, 0,86,6,3 Grafik ln k vs /T Ea R Ea,43 ( 3,7) ,74 x 0,08 485,74, /T
38 6. Laju reaksi : OH - (aq) + NH 4+ (aq) H O(l) + NH 3 (aq) adalah orde pertama bagi konsentrasi OH - maupun NH 4+, dan tetapan laju k pada 0 o C adalah 3,4 x 00 L.mol -.s -. ndaikan,00 L larutan NaOH 0,000 M dengan cepat dicampurkan dengan larutan 0,000 M NH 4 Cl dengan volume yang sama, hitunglah waktu (dalam detik) yang diperlukan agar konsentrasi OH - turun menjadi,0 x 0-5 M.
39 Jawab : Reaksi: OH - (aq) + NH 4 + (aq) H O (l) + NH 3(aq) 0,00M L 0,00M L OH k. OH NH k. OH d dt OH t OH o OH d OH 0 5 L 5 0 mol L. mol Jadi: OH OH t mol /L t 0 3 k. dt o 0 3 L mol k. t mol / L L. mol 0 3,4.0 L. mol. s, s 4 3,4.0 3, L. mol L. mol 3,4.0. s 0. t L. mol. s. t s. t
40 7. Reaksi P mempunyai hukum laju orde kedua dengan k = 3,50 x 0-4 M - s -. Hitunglah waktu yang diperlukan agar konsentrasi berubah dari,60 M menjadi 0,0 M Buktikan bahwa t / /[ 0 ] n- untuk reaksi yang mempunyai orde ke-n terhadap Suatu zat terdekomposisi menurut reaksi P dengan hukum laju orde kedua dan k =,6 x 0-3 M - s -. Berapakah waktu paruh jika [] 0 =,70M?
41 TUGS KELOMPOK. Tekanan parsial azometana sbg fungsi waktu pada 600K ditunjukkan sbb: t/detik P/0 - mmhg 8,0 5,7 3,99,78,94 Tunjukkan reaksi penguraian azometana CH 3 N CH 3 CH 3 CH 3 + N merupakan orde satu dan tentukan tetapan lajunya.. Reaksi fase gas B diikuti metode spekofotometri memberikan hasil sbb: t/detik ~ [B] / M 0 0,089 0,53 0,00 0,30 0,3 Tentukan orde dan tetapan laju reaksi
42 3. Buktikan bahwa penguraian azometana merupakan orde satu dan carilah konstanta lajunya. Data konsentrasi dari azometana sebagai fungsi waktu adalah sebagai berikut : t / [zo] / 0 - M,,53,07 0,75 0,5 4. Suatu reaksi NO NO + O adalah orde satu dengan harga tetapan laju = 3,06 x0-5 menit - a. Tentukan waktu pada saat konsentrasi oksigen yang terbentuk sama dengan konsentrasi NO sisa b. Berapa konsentrasi NO yang terbentuk 5. Hubungan laju awal dengan konsentrasi awal J pada pembentukan senyawanya adalah sebagai berikut : [J] 0 / 0-3 M 5,0 8, 7 30 V j,0 / 0-7 MS - 3,6 9, Tentukan orde dan harga tetapan laju rekasi
43 6. Berlangsungnya reaksi antara atom Bromium dan Cl O diikuti dengan mengukur konsentrasi radikal ClO, jika konsentrasi awal atom Bromium dan Cl O adalah, x 0-6 M dan 4,4 x 0-6 M. Hitung tetapan laju reaksi. Br + Cl O Br + ClO t/µs ClO/0-6 M,68,74 3,66 4,7 5,6 6,9 6,55 7,40 7,84 7. Tetapan laju dekomposisi N O 5 dalam reaksi N O 5 4 NO + O adalah 388 x0-5 s -. Tentukan : a. Orde untuk reaksi tersebut b. Waktu paruh N O 5 c. Tekanan parsial N O 5 pada t = 00s, jika diketahui P 0 = 500 Torr 8. Tetapan laju suatu reaksi berubah oleh suhu dinyatakan sebagai persamaan : ln k 067 T 3,33 Tentukan besarnya energi aktivasi dan harga tetapan pra-eksponensial
44 EFFECT OF CTLYST ON RECTION Enhances reaction rate by reducing the activation energy EOS
45 DEFINISI KTLIS Definisi Katalis oleh Bell : Suatu zat yg muncul dlm ungkapan laju dg pangkat lebih tinggi dr yg ada dlm pers stoikiometri Contoh : + B produk r = k [] [B] 3/ maka menurut Bell, B tdk hanya sbg pereaksi ttp jg berfungsi sbg katalis Definisi praktis : Katalis adl suatu zat yg mempercepat suatu reaksi kimia, dg tanpa memperhatikan apa yg terj pada zat tsb Contoh : lcl 3 pada reaksi alkilasi (Friedel Kraft) R Cl + R H R R + HCl lcl 3
46 HOMOGENEOUS CTLYSIS Reaction profile for the uncatalyzed and catalyzed decomposition of ozone EOS
47 KTLISIS HOMOGEN FS GS SO + O = SO 3 (lambat) Dapat dipercepat oleh adanya NO, dengan mekanisme : NO + O NO NO + SO SO 3 + NO
48 MEKNISME KTLISIS Secara umum, mekanisme katalisis adl sbb: + B k hasil (lambat tanpa katalis) + kat X (cepat) X + B hasil + kat (lebih cepat) d[hasil] = k [] [B] dt dapat diselesaikan berdasarkan pendekatan steady state atau kesetimbangan
49 Contoh Katalisis dlm Fasa Cair : Penguraian H O H O = H O + ½ O Merupakan bahan bakar roket shg Utk menyimpan mol O lebih praktis dlm bentuk H O Penguraian tsb dikatalisis oleh HBr -d[h O ] dt = k [H + ] [Br - ] [H O ] Mekanisme : H O + H + + Br - HBrO + H O lambat HBrO + Br - + H + Br + H O cepat H O + HBrO O + Br - + H + + H O lambat
50 Contoh : Ce 4+ + Tl + Ce 3+ + Tl 3+ Secara termodinamika : sangat mungkin Secara kinetik : sangat lambat Dipercepat oleh adanya Mn + Ce 4+ + Mn + Ce 3+ + Mn 3+ Mn 3+ + Ce 4+ Ce 3+ + Mn 4+ Mn 4+ + Tl 4+ Mn + + Tl 3+ Unsur transisi dpt berperan dg baik sebagai katalis, krn adanya tingkattingkat energi yg berdekatan satu sama lain (adanya tingkat-tingkat oksidasi)
51 HETEROGENEOUS CTLYSIS Many reactions are catalyzed by the surfaces of appropriate solids EOS
52 END PRESENTTION TERIM KSIH
53 Pengertian & Cakupan Kinetika Kimia Pengertian & Pengukuran Laju Reaksi 3 Pengaruh Konsentrasi Hukum Laju 4 Penurunan Persamaan Laju Reaksi
54 5 Reaksi Orde Nol 6 Reaksi Orde Satu 7 Reaksi Orde Dua 8 Waktu Paruh
55 POKOK BHSN (#7) 9 Model Teoritis Kinetika Kimia 0 Pengaruh Temperatur Mekanisme Reaksi Katalisis
56 KINETIK KIMI Bagian dari kimia yang fokus kajiannya laju reaksi kimia, baik aspek: Teoritis: pengembangan model/teori yang menjelaskan laju reaksi (dan mekanisme reaksi) Eksperimental: Metode penentuan orde reaksi & konstanta laju Kondisi agar reaksi dapat berlangsung dalam laju yang bermakna (T, p, katalis, reaktor yang sesuai)
57 KINETIK KIMI Sangat penting karena: Umumnya suatu reaksi kimia hanya akan bermakna jika berlangsung dalam laju yang bermakna. Contoh: Jika kita mengetahui laju (dan mekanisme reaksi), kita dapat mengendalikannya! Contoh:
58 KINETIK VS TERMODINMIK KIMI + B ¾ C + D Termodinamika Ž [C] [D] [] [B] (pada kesetimbangan) Termodinamika ŽDapatkah reaksi terjadi? Kinetika ŽSeberapa cepat reaksi terjadi?. Laju reaksi sebelum kesetimbangan tercapai. Mekanisme reaksi
59 KINETIK VS TERMODINMIK: E VS DH E a DH
60 KINETIK VS TERMODINMIK: E VS DH E a Spontanitas reaksi: DG = DH TDS Laju reaksi terkait dengan energi aktivasi (E a ). Menurunkan E a menaikkan laju; tetapi DH tetap. DH
61 KINETIK TERMODINMIK Fe (s) + 3/ O (g) Fe O 3 (s) DG o = -740 kj/mol Tapi laju reaksi sangat rendah! CH 4 (g) + 3 O (g) CO (g) + H O (g) DG o = -80 kj/mol Laju reaksi jauh lebih tinggi!
62 LJU REKSI SNGT BERVRISI Satuan waktu berjalannya reaksi: milidetik, detik,..., trilyun tahun
63 LEDKN; STUN WKTU: MS - S
64 PEMTNGN BUH; HRI/BULN
65 PEMTNGN BUH; HRI/BULN
66 PENNMN PNEN TOMT; BULN Tanaman muda; wal Januari Bakal Bunga; Februari Buah Pertama; Februari
67 PENNMN PNEN TOMT; BULN Buah hijau; wal Maret Buah kuning; Tengah Maret Buah Dipanen; khir Maret
68 PERKRTN BESI; MINGGU/BULN/THN
69 PENUN MNUSI; THUN
70 PELURUHN RDIOKTIF: MS TRILYUN THN
71 LJU REKSI SNGT BERVRISI Proses Ledakan Pematangan buah Tanam panen buah Perkaratan besi Penuaan (manusia) Peluruhan radioaktif < s Waktu hari/bulan bulan minggu/bulan/thn tahun ms trilyun tahun
72 LJU REKSI (R) Perubahan konsentrasi reaktan atau produk terhadap waktu Pengurangan konsentrasi reaktan Penambahan konsentrasi produk Secara matematis, untuk reaksi: B Laju reaksi = r = -d[]/dt = d[b]/dt Dengan berjalannya waktu
73 LJU REKSI DPT DIPENGRUHI OLEH Konsentrasi reaktan Luas permukaan Temperatur da tidaknya katalis Faktor paling dominan, tergantung jenis reaksi
74 MEMPELJRI FKTOR-FKTOR LJU REKSI Prinsip desain eksperimen: variasi faktor; jaga agar faktor lain tetap. Mg (s) + HCl (aq) MgCl + H (g) Luas muka: Sejumlah tertentu pita Mg (misal cm) divariasi ukuran potongannya ( cm; 0,75 cm; 0,5 cm; 0,5 cm; 0, cm) Direaksikan dengan HCl konsentrasi tertentu (misalnya M) Pada suhu tertentu (misalnya 30 0 C) & tanpa katalis
75 MEMPELJRI FKTOR-FKTOR LJU REKSI Mg (s) + HCl (aq) MgCl + H (g) Bagaimana desain eksperimen untuk mempelajari pengaruh: Konsentrasi HCl: Suhu:
76 Laju Reaksi Laju Rata-rata Laju Sesaat Laju pada selang waktu Laju pada t tertentu
77 LJU RT-RT Rerata perubahan konsentrasi reaktan atau produk dalam selang waktu tertentu Secara matematis, untuk reaksi: B Laju rata-rata laju = - D[] Dt laju = D[B] Dt D[] = perubahan konsentrasi dalam selang waktu Dt D[B] = perubahan konsentrasi B dalam selang waktu Dt Karena [] menurun terhadap waktu, D[] bernilai negatif.
78 B waktu laju = - D[] Dt laju = D[B] Dt
79 Secara kasat mata Br (aq) + HCOOH (aq) Br - (aq) + H + (aq) + CO (g) waktu Perubahan warna dengan berjalannya waktu [Br ] a Intensitas warna coklat-kuning
80 393 nm Br (aq) + HCOOH (aq) Br - (aq) + H + (aq) + CO (g) nalisis Instrumen waktu Br (aq) 393 nm cahaya Detektor [Br ] a bsorbansi
81 Br (aq) + HCOOH (aq) Br - (aq) + H + (aq) + CO (g) Hitunglah laju rata-rata pada: a) 00 s pertama b) dari 300 s hingga 350 s Laju rata-rata = - D[Br ] Dt = - [Br ] akhir [Br ] awal t akhir - t awal
82 LJU SEST kemiringan garis singgung Laju sesaat = laju pada saat tertentu
83 LJU REKSI & STOIKIOMETRI a + b B c C + d D Laju reaksi = laju hilangnya reaktan = - a Δ[] Δt = - b Δ[B] Δt = laju munculnya produk = c Δ[C] Δt = d Δ[D] Δt
84 Tulislah persamaan laju untuk reaksi di bawah ini: CH 4 (g) + O (g) CO (g) + H O (g) laju = - D[CH 4] Dt = - D[O ] Dt = D[CO ] Dt = D[H O] Dt Jika konsentrasi O menurun dengan laju 0,0 M/s, berapakah laju reaksinya? Berapakah laju terbentuknya CO?
85 PENGRUH KONSENTRSI TERHDP LJU: HUKUM LJU a + b B. g G + h H. Laju reaksi = k [] m [B] n. Tetapan laju reaksi = k Orde/tingkat reaksi terhadap = m Orde/tingkat reaksi terhadap B = n Orde/tingkat reaksi total = m + n +.
86 Laju reaksi = k [] m [B] n. k m & n semakin besar k; laju reaksi makin besar k tergantung pada: jenis reaksi konsentrasi katalis temperatur m & n dapat berupa: bil bulat (-, 0, +) pecahan m & n umumnya tidak terkait dengan koefisien reaksi
87 pa pengaruh konsentrasi terhadap laju? laju = k [Br ] k = laju [Br ] = konstanta laju = 3,50 x 0-3 s -
88 PENURUNN PERSMN LJU REKSI [ ] kdt m [ ] d[ ] r k[ ] dt m Bentuk Integral Bentuk Diferensial
89 JIK M =, BGIMN PERS. LJU? d[ ] dt k [ ] Bentuk Integral Bentuk Diferensial d [ ] k dt
90 JIK M =, BGIMN PERS. LJU? d [ ] k ln[ ] t C dt ln[ ] k t C [ ] ln k ( t t ) [ ] [ ] ln k ( t t ) [ ]
91 ORDE : LN [] VS T; GRIS LURUS
92 TURUNKN PERS. LJU REKSI GRDIPEROLEH PERS. GRIS LURUS Untuk reaksi orde 0 Untuk reaksi orde Untuk reaksi orde
93 SEE YOU NEXT WEEK!
Perubahan kimia secara sederhana ditulis dalam persamaan reaksi dengan kondisi kesetimbangan
 KINETIKA Pendahuluan Perubahan kimia secara sederhana ditulis dalam persamaan reaksi dengan kondisi kesetimbangan Namun persamaan reaksi tidak dapat menjawab :. Seberapa cepat reaksi berlangsung 2. Bagaimana
KINETIKA Pendahuluan Perubahan kimia secara sederhana ditulis dalam persamaan reaksi dengan kondisi kesetimbangan Namun persamaan reaksi tidak dapat menjawab :. Seberapa cepat reaksi berlangsung 2. Bagaimana
BAB 9. KINETIKA KIMIA
 BAB 9 BAB 9. KINETIKA KIMIA 9.1 TEORI TUMBUKAN DARI LAJU REAKSI 9.2 TEORI KEADAAN TRANSISI DARI LAJU REAKSI 9.3 HUKUM LAJU REAKSI 9.4 FAKTOR-FAKTOR LAJU REAKSI 9.5 MEKANISME REAKSI 9.6 ENZIM SEBAGAI KATALIS
BAB 9 BAB 9. KINETIKA KIMIA 9.1 TEORI TUMBUKAN DARI LAJU REAKSI 9.2 TEORI KEADAAN TRANSISI DARI LAJU REAKSI 9.3 HUKUM LAJU REAKSI 9.4 FAKTOR-FAKTOR LAJU REAKSI 9.5 MEKANISME REAKSI 9.6 ENZIM SEBAGAI KATALIS
Bab 10 Kinetika Kimia
 D e p a r t e m e n K i m i a F M I P A I P B Bab 0 Kinetika Kimia http://chem.fmipa.ipb.ac.id Ikhtisar 2 3 Laju Reaksi Teori dalam Kinetika Kimia 4 Mekanisme Reaksi 5 46 Faktor Penentu Laju Reaksi Enzim
D e p a r t e m e n K i m i a F M I P A I P B Bab 0 Kinetika Kimia http://chem.fmipa.ipb.ac.id Ikhtisar 2 3 Laju Reaksi Teori dalam Kinetika Kimia 4 Mekanisme Reaksi 5 46 Faktor Penentu Laju Reaksi Enzim
Termodinamika apakah suatu reaksi dapat terjadi? Kinetika Seberapa cepat suatu reaksi berlangsung?
 Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi Chapter 8 Kinetika Kimia Termodinamika apakah suatu reaksi dapat terjadi? Kinetika Seberapa cepat suatu reaksi berlangsung?
Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi Chapter 8 Kinetika Kimia Termodinamika apakah suatu reaksi dapat terjadi? Kinetika Seberapa cepat suatu reaksi berlangsung?
KINETIKA KIMIA LAJU DAN MEKANISME DALAM REAKSI KIMIA
 KINETIKA KIMIA LAJU DAN MEKANISME DALAM REAKSI KIMIA Pendahuluan Perubahan kimia secara sederhana ditulis dalam persamaan reaksi dengan koefisien seimbang Namun persamaan reaksi tidak dapat menjawab 3
KINETIKA KIMIA LAJU DAN MEKANISME DALAM REAKSI KIMIA Pendahuluan Perubahan kimia secara sederhana ditulis dalam persamaan reaksi dengan koefisien seimbang Namun persamaan reaksi tidak dapat menjawab 3
BAB VI KINETIKA REAKSI KIMIA
 BANK SOAL SELEKSI MASUK PERGURUAN TINGGI BIDANG KIMIA 1 BAB VI 1. Padatan NH 4 NO 3 diaduk hingga larut selama 77 detik dalam akuades 100 ml sesuai persamaan reaksi berikut: NH 4 NO 2 (s) + H 2 O (l) NH
BANK SOAL SELEKSI MASUK PERGURUAN TINGGI BIDANG KIMIA 1 BAB VI 1. Padatan NH 4 NO 3 diaduk hingga larut selama 77 detik dalam akuades 100 ml sesuai persamaan reaksi berikut: NH 4 NO 2 (s) + H 2 O (l) NH
Perubahan konsentrasi reaktan atau produk terhadap waktu. Secara matematis, untuk reaksi: A B Laju reaksi = r = -d[a]/dt = d[b]/dt
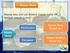
![Perubahan konsentrasi reaktan atau produk terhadap waktu. Secara matematis, untuk reaksi: A B Laju reaksi = r = -d[a]/dt = d[b]/dt Perubahan konsentrasi reaktan atau produk terhadap waktu. Secara matematis, untuk reaksi: A B Laju reaksi = r = -d[a]/dt = d[b]/dt](/thumbs/52/30298935.jpg) 1 Laju reaksi (r) Perubahan konsentrasi reaktan atau produk terhadap waktu Pengurangan konsentrasi reaktan Penambahan konsentrasi produk Dengan berjalannya waktu Secara matematis, untuk reaksi: A B Laju
1 Laju reaksi (r) Perubahan konsentrasi reaktan atau produk terhadap waktu Pengurangan konsentrasi reaktan Penambahan konsentrasi produk Dengan berjalannya waktu Secara matematis, untuk reaksi: A B Laju
Kinetika kimia. Shinta Rosalia Dewi
 Kinetika kimia Shinta Rosalia Dewi Pendahuluan Termodinamika Kinetika Reaksi Mekanika fluida Pindah panas neraca massa ekonomi mendesain reaktor kimia Pendahuluan (cont ) Kinetika reaksi adalah studi tentang
Kinetika kimia Shinta Rosalia Dewi Pendahuluan Termodinamika Kinetika Reaksi Mekanika fluida Pindah panas neraca massa ekonomi mendesain reaktor kimia Pendahuluan (cont ) Kinetika reaksi adalah studi tentang
Kinetika Kimia. Abdul Wahid Surhim
 Kinetika Kimia bdul Wahid Surhim 2014 Kerangka Pembelajaran Laju Reaksi Hukum Laju dan Orde Reaksi Hukum Laju Terintegrasi untuk Reaksi Orde Pertama Setengah Reaksi Orde Pertama Reaksi Orde Kedua Laju
Kinetika Kimia bdul Wahid Surhim 2014 Kerangka Pembelajaran Laju Reaksi Hukum Laju dan Orde Reaksi Hukum Laju Terintegrasi untuk Reaksi Orde Pertama Setengah Reaksi Orde Pertama Reaksi Orde Kedua Laju
KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI
 KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI 1. Untuk membuat 500 ml larutan H 2 SO 4 0.05 M dibutuhkan larutan H 2 SO 4 5 M sebanyak ml a. 5 ml b. 10 ml c. 2.5 ml d. 15 ml e. 5.5 ml 2. Konsentrasi larutan yang
KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI 1. Untuk membuat 500 ml larutan H 2 SO 4 0.05 M dibutuhkan larutan H 2 SO 4 5 M sebanyak ml a. 5 ml b. 10 ml c. 2.5 ml d. 15 ml e. 5.5 ml 2. Konsentrasi larutan yang
Waktu (t) Gambar 3.1 Grafik hubungan perubahan konsentrasi terhadap waktu
 3 LAJU REAKSI Setelah mempelajari bab ini, kamu diharapkan mampu: Menghitung konsentrasi larutan (molaritas larutan). Menganalisis faktor-faktor yang mempengaruhi laju reaksi (konsentrasi, luas permukaan,
3 LAJU REAKSI Setelah mempelajari bab ini, kamu diharapkan mampu: Menghitung konsentrasi larutan (molaritas larutan). Menganalisis faktor-faktor yang mempengaruhi laju reaksi (konsentrasi, luas permukaan,
KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI
 KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI 1. Untuk membuat 500 ml larutan H2SO4 0.05 M dibutuhkan larutan H2SO4 5 M sebanyak ml a. 5 ml b. 10 ml c. 2.5 ml d. 15 ml e. 5.5
KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI 1. Untuk membuat 500 ml larutan H2SO4 0.05 M dibutuhkan larutan H2SO4 5 M sebanyak ml a. 5 ml b. 10 ml c. 2.5 ml d. 15 ml e. 5.5
Purwanti Widhy H, M.Pd. Laju Reaksi
 Purwanti Widhy H, M.Pd Laju Reaksi SK, KD dan Indikator Kemolaran Konsep Laju Reaksi Faktor-faktor yang mempengaruhi laju reaksi Evaluasi Referensi Selesai Standar Kompetensi, Kompetensi Dasar & Indikator
Purwanti Widhy H, M.Pd Laju Reaksi SK, KD dan Indikator Kemolaran Konsep Laju Reaksi Faktor-faktor yang mempengaruhi laju reaksi Evaluasi Referensi Selesai Standar Kompetensi, Kompetensi Dasar & Indikator
SOAL LAJU REAKSI. Mol CaCO 3 = = 0.25 mol = 25. m Mr
 SOAL LAJU REAKSI 1. Untuk membuat 500 ml larutan H 2 SO 4 0.05 M dibutuhkan larutan H 2 SO 4 5 M sebanyak ml A. 5 ml B. 10 ml C. 2.5 ml D. 15 ml E. 5.5 ml : A Mencari volume yang dibutuhkan pada proses
SOAL LAJU REAKSI 1. Untuk membuat 500 ml larutan H 2 SO 4 0.05 M dibutuhkan larutan H 2 SO 4 5 M sebanyak ml A. 5 ml B. 10 ml C. 2.5 ml D. 15 ml E. 5.5 ml : A Mencari volume yang dibutuhkan pada proses
KINETIKA KIMIA. SHINTA ROSALIA DEWI
 KINETIKA KIMIA. SHINTA ROSALIA DEWI Kinetika kimia Shinta Rosalia Dewi Pendahuluan Kinetika Reaksi Mekanika fluida mendesain reaktor kimia Pindah panas neraca massa ekonomi Termodinamika Pendahuluan (cont
KINETIKA KIMIA. SHINTA ROSALIA DEWI Kinetika kimia Shinta Rosalia Dewi Pendahuluan Kinetika Reaksi Mekanika fluida mendesain reaktor kimia Pindah panas neraca massa ekonomi Termodinamika Pendahuluan (cont
Bahasan: Mempelajari kecepatan/laju reaksi suatu proses/perubahan kimia. reaksi berlangsung mekanisme reaksi
 Mempelajari kecepatan/laju reaksi suatu proses/perubahan kimia. Kinetika juga mempelajari bagaimana reaksi berlangsung mekanisme reaksi Referensi: Brown et.al; Chemistry, The Central Science, 11th edition
Mempelajari kecepatan/laju reaksi suatu proses/perubahan kimia. Kinetika juga mempelajari bagaimana reaksi berlangsung mekanisme reaksi Referensi: Brown et.al; Chemistry, The Central Science, 11th edition
Sulistyani, M.Si.
 Sulistyani, M.Si. Email: sulistyani@uny.ac.id Laju reaksi adalah laju pengurangan reaktan tiap satuan waktu atau laju pembentukan produk tiap satuan waktu. Laju reaksi dipengaruhi oleh: sifat dan keadan
Sulistyani, M.Si. Email: sulistyani@uny.ac.id Laju reaksi adalah laju pengurangan reaktan tiap satuan waktu atau laju pembentukan produk tiap satuan waktu. Laju reaksi dipengaruhi oleh: sifat dan keadan
Kinetika Kimia dan Mekanisme Reaksi
 Kinetika Kimia dan Mekanisme Reaksi Kinetika Kimia Kinetika kimia adalah ilmu yang mempelajari laju reaksi, atau seberapa cepat proses reaksi berlangsung dalam waktu tertentu. Kinetika kimia menjelaskan
Kinetika Kimia dan Mekanisme Reaksi Kinetika Kimia Kinetika kimia adalah ilmu yang mempelajari laju reaksi, atau seberapa cepat proses reaksi berlangsung dalam waktu tertentu. Kinetika kimia menjelaskan
LAJU REAKSI MEKANISME REAKSI
 KINETIKA KIMIA LAJU REAKSI BAGAIMANA PERUB. KIMIA TSB BERLANGSUNG - BESI MUDAH BERKARAT PD UDARA YANG LEMBAB - MAKANAN LEBIH CEPAT BUSUK BILA TIDAK DIINGINKAN MEKANISME REAKSI - PENJUMLAHAN TAHAP TAHAP
KINETIKA KIMIA LAJU REAKSI BAGAIMANA PERUB. KIMIA TSB BERLANGSUNG - BESI MUDAH BERKARAT PD UDARA YANG LEMBAB - MAKANAN LEBIH CEPAT BUSUK BILA TIDAK DIINGINKAN MEKANISME REAKSI - PENJUMLAHAN TAHAP TAHAP
Kunci jawaban dan pembahasan soal laju reaksi
 Kunci jawaban dan pembahasan soal laju reaksi Soal nomor 1 Mencari volume yang dibutuhkan pada proses pengenceran. Rumus pengenceran V 1. M 1 = V 2. M 2 Misal volume yang dibutuhkan sebanyak x ml, maka
Kunci jawaban dan pembahasan soal laju reaksi Soal nomor 1 Mencari volume yang dibutuhkan pada proses pengenceran. Rumus pengenceran V 1. M 1 = V 2. M 2 Misal volume yang dibutuhkan sebanyak x ml, maka
OAL TES SEMESTER I. I. Pilihlah jawaban yang paling tepat! a. 2d d. 3p b. 2p e. 3s c. 3d 6. Unsur X dengan nomor atom
 KIMIA XI SMA 3 S OAL TES SEMESTER I I. Pilihlah jawaban yang paling tepat!. Elektron dengan bilangan kuantum yang tidak diizinkan n = 3, l = 0, m = 0, s = - / n = 3, l =, m =, s = / c. n = 3, l =, m =
KIMIA XI SMA 3 S OAL TES SEMESTER I I. Pilihlah jawaban yang paling tepat!. Elektron dengan bilangan kuantum yang tidak diizinkan n = 3, l = 0, m = 0, s = - / n = 3, l =, m =, s = / c. n = 3, l =, m =
A. MOLARITAS (M) B. KONSEP LAJU REAKSI C. PERSAMAAN LAJU REAKSI D. TEORI TUMBUKAN E. FAKTOR-FAKTOR YANG MEMPENGARUHI LAJU REAKSI
 3 LAJU REAKSI A. MOLARITAS (M) B. KONSEP LAJU REAKSI C. PERSAMAAN LAJU REAKSI D. TEORI TUMBUKAN E. FAKTOR-FAKTOR YANG MEMPENGARUHI LAJU REAKSI Materi dapat berubah dari bentuk yang satu ke bentuk yang
3 LAJU REAKSI A. MOLARITAS (M) B. KONSEP LAJU REAKSI C. PERSAMAAN LAJU REAKSI D. TEORI TUMBUKAN E. FAKTOR-FAKTOR YANG MEMPENGARUHI LAJU REAKSI Materi dapat berubah dari bentuk yang satu ke bentuk yang
KINETIKA KIMIA LAJU DAN MEKANISME DALAM REAKSI KIMIA. Disampaikan oleh : Dr. Sri Handayani 2013
 KINETIK KIMI LJU DN MEKNISME DLM REKSI KIMI Disampaikan oleh : Dr. Sri Handayani 03 Pendahuluan Perubahan kimia secara sederhana diulis dalam persamaan reaksi dengan koefisien seimbang Namun persamaan
KINETIK KIMI LJU DN MEKNISME DLM REKSI KIMI Disampaikan oleh : Dr. Sri Handayani 03 Pendahuluan Perubahan kimia secara sederhana diulis dalam persamaan reaksi dengan koefisien seimbang Namun persamaan
KESETIMBANGAN KIMIA SOAL DAN PEMBAHASAN
 KESETIMBANGAN KIMIA SOAL DAN PEMBAHASAN 1. Suatu reaksi dikatakan mencapai kesetimbangan apabila. A. laju reaksi ke kiri sama dengan ke kanan B. jumlah koefisien reaksi ruas kiri sama dengan ruas kanan
KESETIMBANGAN KIMIA SOAL DAN PEMBAHASAN 1. Suatu reaksi dikatakan mencapai kesetimbangan apabila. A. laju reaksi ke kiri sama dengan ke kanan B. jumlah koefisien reaksi ruas kiri sama dengan ruas kanan
MODUL LAJU REAKSI. Laju reaksi _ 2013 Page 1
 MODUL LAJU REAKSI Standar Kompetensi ( SK ) : Memahami kinetika reaksi, kesetimbangan kimia dan faktor-faktor yang mempengaruhinya, serta penerapannya dalam kehidupan sehari-hari dan industri. Kompetensi
MODUL LAJU REAKSI Standar Kompetensi ( SK ) : Memahami kinetika reaksi, kesetimbangan kimia dan faktor-faktor yang mempengaruhinya, serta penerapannya dalam kehidupan sehari-hari dan industri. Kompetensi
Soal Soal Kesetimbangan Kimia. Proses Haber-Bosch merupakan proses pembentukan atau produksi ammonia berdasarkan reaksi:
 Nama : Fitria Puspita NIM : 1201760 Kelas : Pendidikan Kimia A Soal Soal Kesetimbangan Kimia SBMPTN 2014 Untuk soal no 1-3, bacalah narasi berikut. Proses Haber-Bosch merupakan proses pembentukan atau
Nama : Fitria Puspita NIM : 1201760 Kelas : Pendidikan Kimia A Soal Soal Kesetimbangan Kimia SBMPTN 2014 Untuk soal no 1-3, bacalah narasi berikut. Proses Haber-Bosch merupakan proses pembentukan atau
kimia KTSP & K-13 KESETIMBANGAN KIMIA 1 K e l a s A. Reaksi Kimia Reversible dan Irreversible Tujuan Pembelajaran
 KTSP & K-13 kimia K e l a s XI KESETIMBANGAN KIMIA 1 Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami definisi reaksi kimia reversible dan irreversible..
KTSP & K-13 kimia K e l a s XI KESETIMBANGAN KIMIA 1 Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami definisi reaksi kimia reversible dan irreversible..
Kode KIM.10. Laju Reaksi
 Kode KIM.10 Laju Reaksi BAGIAN PROYEK PENGEMBANGAN KURIKULUM DIREKTORAT PENDIDIKAN MENENGAH KEJURUAN DIREKTORAT JENDERAL PENDIDIKAN DASAR DAN MENENGAH DEPARTEMEN PENDIDIKAN NASIONAL 2004 BAB I. PENDAHULUAN
Kode KIM.10 Laju Reaksi BAGIAN PROYEK PENGEMBANGAN KURIKULUM DIREKTORAT PENDIDIKAN MENENGAH KEJURUAN DIREKTORAT JENDERAL PENDIDIKAN DASAR DAN MENENGAH DEPARTEMEN PENDIDIKAN NASIONAL 2004 BAB I. PENDAHULUAN
H 2 O (l) H 2 O (g) Kesetimbangan kimia. N 2 O 4 (g) 2NO 2 (g)
 Purwanti Widhy H Kesetimbangan adalah suatu keadaan di mana tidak ada perubahan yang terlihat seiring berjalannya waktu. Kesetimbangan kimia tercapai jika: Laju reaksi maju dan laju reaksi balik sama besar
Purwanti Widhy H Kesetimbangan adalah suatu keadaan di mana tidak ada perubahan yang terlihat seiring berjalannya waktu. Kesetimbangan kimia tercapai jika: Laju reaksi maju dan laju reaksi balik sama besar
Laju Reaksi KIM 2 A. KEMOLARAN B. LAJU REAKSI C. UNGKAPAN LAJU REAKSI LAJU REAKSI. materi78.co.nr
 Laju eaksi A. KEMOLAAN Dalam laju reaksi, besaran yang digunakan adalah kemolaran benda. Kemolaran menyatakan jumlah mol zat terlarut dari tiap liter larutan atau gas, menunjukkan kekentalan atau kepekatan.
Laju eaksi A. KEMOLAAN Dalam laju reaksi, besaran yang digunakan adalah kemolaran benda. Kemolaran menyatakan jumlah mol zat terlarut dari tiap liter larutan atau gas, menunjukkan kekentalan atau kepekatan.
SOAL KIMIA 2 KELAS : XI IPA
 SOAL KIMIA KELAS : XI IPA PETUNJUK UMUM. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan. Periksa dan bacalah soal dengan teliti sebelum Anda bekerja. Kerjakanlah soal anda pada lembar jawaban
SOAL KIMIA KELAS : XI IPA PETUNJUK UMUM. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan. Periksa dan bacalah soal dengan teliti sebelum Anda bekerja. Kerjakanlah soal anda pada lembar jawaban
tanya-tanya.com Soal No.2 Apabila anda diminta untuk mengukur laju reaksi terhadap reaksi : Zn(s) + 2HCI(aq)
 Soal No.1 Apa yang di maksud dengan laju reaksi dan satuan dari laju reaksi? Laju reaksi dinyatakan sebagai berkurangnya jumlah pereaksi untuk setiap satuan waktu atau bertambahnya jumlah hasil reaksi
Soal No.1 Apa yang di maksud dengan laju reaksi dan satuan dari laju reaksi? Laju reaksi dinyatakan sebagai berkurangnya jumlah pereaksi untuk setiap satuan waktu atau bertambahnya jumlah hasil reaksi
Gambar 2.1 Reaksi Saponifikasi tripalmitin
 I. JUDUL : Kinetika Reaksi Saponifikasi Etil Asetat II. TANGGAL PERCOBAAN : Rabu, 16 November 2011 III. TUJUAN : 1. Untuk memberikan gambaran bahwa reaksi penyabunan etil asetat oleh ion hidroksida adalah
I. JUDUL : Kinetika Reaksi Saponifikasi Etil Asetat II. TANGGAL PERCOBAAN : Rabu, 16 November 2011 III. TUJUAN : 1. Untuk memberikan gambaran bahwa reaksi penyabunan etil asetat oleh ion hidroksida adalah
PRAKTIKUM KIMIA DASAR I KECEPATAN REAKSI. Kelompok V : Amir Hamzah Umi Kulsum
 PRAKTIKUM KIMIA DASAR I KECEPATAN REAKSI Kelompok V : Amir Hamzah 1415005 Umi Kulsum 1415018 AKADEMI KIMIA ANALISIS CARAKA NUSANTARA CIMANGGIS, KELAPA DUA DEPOK, 2015 BAB 1 PENDAHULUAN 1.1 Latar Belakang
PRAKTIKUM KIMIA DASAR I KECEPATAN REAKSI Kelompok V : Amir Hamzah 1415005 Umi Kulsum 1415018 AKADEMI KIMIA ANALISIS CARAKA NUSANTARA CIMANGGIS, KELAPA DUA DEPOK, 2015 BAB 1 PENDAHULUAN 1.1 Latar Belakang
PETA KONSEP LAJU REAKSI. Percobaan. Waktu perubahan. Hasil reaksi. Pereaksi. Katalis. Suhu pereaksi. Konsentrasi. Luas. permukaan.
 PETA KONSEP LAJU REAKSI Berkaitan dengan ditentukan melalui Waktu perubahan Dipengaruhi oleh Percobaan dari Pereaksi Hasil reaksi Konsentrasi Luas Katalis Suhu pereaksi permukaan menentukan membentuk mengadakan
PETA KONSEP LAJU REAKSI Berkaitan dengan ditentukan melalui Waktu perubahan Dipengaruhi oleh Percobaan dari Pereaksi Hasil reaksi Konsentrasi Luas Katalis Suhu pereaksi permukaan menentukan membentuk mengadakan
Kesetimbangan Kimia. A b d u l W a h i d S u r h i m
 Kesetimbangan Kimia A b d u l W a h i d S u r h i m 2 0 1 4 Rujukan Chapter 12 dan 14: Masterton, William L. and Hurley, Cecile N. 2009. Chemistry: Principles and Reactions. Sixth Edition. Books/Cole.
Kesetimbangan Kimia A b d u l W a h i d S u r h i m 2 0 1 4 Rujukan Chapter 12 dan 14: Masterton, William L. and Hurley, Cecile N. 2009. Chemistry: Principles and Reactions. Sixth Edition. Books/Cole.
HUBUNGAN ENERGI DALAM REAKSI KIMIA
 HUBUNGAN ENERGI DALAM REAKSI KIMIA _KIMIA INDUSTRI_ DEWI HARDININGTYAS, ST, MT, MBA WIDHA KUSUMA NINGDYAH, ST, MT AGUSTINA EUNIKE, ST, MT, MBA ENERGI & KERJA Energi adalah kemampuan untuk melakukan kerja.
HUBUNGAN ENERGI DALAM REAKSI KIMIA _KIMIA INDUSTRI_ DEWI HARDININGTYAS, ST, MT, MBA WIDHA KUSUMA NINGDYAH, ST, MT AGUSTINA EUNIKE, ST, MT, MBA ENERGI & KERJA Energi adalah kemampuan untuk melakukan kerja.
MODUL 1 TERMOKIMIA. A. Hukum Pertama Termodinamika. B. Kalor Reaksi
 MODUL 1 TERMOKIMIA Termokimia adalah ilmu yang mempelajari hubungan antara energi panas dan energi kimia. Sebagai prasyarat untuk mempelajari termokimia, kita harus mengetahui tentang perbedaan kalor (Q)
MODUL 1 TERMOKIMIA Termokimia adalah ilmu yang mempelajari hubungan antara energi panas dan energi kimia. Sebagai prasyarat untuk mempelajari termokimia, kita harus mengetahui tentang perbedaan kalor (Q)
Laporan Kimia Fisik KI-3141
 Laporan Kimia Fisik KI-3141 PERCOBN M-1 KINETIK HLOGENSI SETON DENGN KTLISTOR SM Nama : Kartika Trianita NIM : 1517 Kelompok : 2 Tanggal Percobaan : 22 Oktober 212 Tanggal Laporan : 2 November 212 sisten
Laporan Kimia Fisik KI-3141 PERCOBN M-1 KINETIK HLOGENSI SETON DENGN KTLISTOR SM Nama : Kartika Trianita NIM : 1517 Kelompok : 2 Tanggal Percobaan : 22 Oktober 212 Tanggal Laporan : 2 November 212 sisten
BY SMAN 16 SURABAYA : Sri Utami, S. P LAJU REAKSI KESIMPULAN
 BY SMAN 16 SURABAYA : Sri Utami, S. P LAJU REAKSI KESIMPULAN STANDAR KOMPETENSI 3. Memahami kinetika reaksi, kesetimbangan kimia, dan faktor-faktor yang mempengaruhinya, serta penerapannya dalam kehidupan
BY SMAN 16 SURABAYA : Sri Utami, S. P LAJU REAKSI KESIMPULAN STANDAR KOMPETENSI 3. Memahami kinetika reaksi, kesetimbangan kimia, dan faktor-faktor yang mempengaruhinya, serta penerapannya dalam kehidupan
Dari Neraca Massa A di Reaktor
 Kinetika dan Katalisis Semester Genap Tahun kademik 010-011 NLISIS & INTERPRETSI DT KINETIK - SISTEM REKTOR BTCH - siti diyar kholisoh PROGRM STUDI TEKNIK KIMI FTI UPN VETERN YOGYKRT Thursday, 19 th May
Kinetika dan Katalisis Semester Genap Tahun kademik 010-011 NLISIS & INTERPRETSI DT KINETIK - SISTEM REKTOR BTCH - siti diyar kholisoh PROGRM STUDI TEKNIK KIMI FTI UPN VETERN YOGYKRT Thursday, 19 th May
Wardaya College IKATAN KIMIA STOIKIOMETRI TERMOKIMIA CHEMISTRY. Part III. Summer Olympiad Camp Kimia SMA
 Part I IKATAN KIMIA CHEMISTRY Summer Olympiad Camp 2017 - Kimia SMA 1. Untuk menggambarkan ikatan yang terjadi dalam suatu molekul kita menggunakan struktur Lewis atau 'dot and cross' (a) Tuliskan formula
Part I IKATAN KIMIA CHEMISTRY Summer Olympiad Camp 2017 - Kimia SMA 1. Untuk menggambarkan ikatan yang terjadi dalam suatu molekul kita menggunakan struktur Lewis atau 'dot and cross' (a) Tuliskan formula
2. Konfigurasi elektron dua buah unsur tidak sebenarnya:
 . Atom X memiliki elektron valensi dengan bilangan kuantum: n =, l =, m = 0, dan s =. Periode dan golongan yang mungkin untuk atom X adalah A. dan IIIB B. dan VA C. 4 dan III B D. 4 dan V B E. 5 dan III
. Atom X memiliki elektron valensi dengan bilangan kuantum: n =, l =, m = 0, dan s =. Periode dan golongan yang mungkin untuk atom X adalah A. dan IIIB B. dan VA C. 4 dan III B D. 4 dan V B E. 5 dan III
Kesetimbangan Kimia. Chapter 9 P N2 O 4. Kesetimbangan akan. Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi
 Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi Kesetimbangan adalah suatu keadaan di mana tidak ada perubahan yang terlihat seiring berjalannya waktu. Kesetimbangan kimia
Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi Kesetimbangan adalah suatu keadaan di mana tidak ada perubahan yang terlihat seiring berjalannya waktu. Kesetimbangan kimia
wanibesak.wordpress.com
 1. Diberikan beberapa pernyataan 1) katalis dapat mempercepat laju reaksi dengan cara menaikan energi aktivasi 2) tahap penentu laju reaksi adalah tahap reaksi yang berlangsung paling lambat 3) laju reaksi
1. Diberikan beberapa pernyataan 1) katalis dapat mempercepat laju reaksi dengan cara menaikan energi aktivasi 2) tahap penentu laju reaksi adalah tahap reaksi yang berlangsung paling lambat 3) laju reaksi
TEORI TUMBUKAN PADA LAJU REAKSI KIMIA
 PENGEMBANGAN BAHAN AJAR TEORI TUMBUKAN PADA LAJU REAKSI KIMIA OLEH : Drs. I Wayan Suarsa, M.Si JURUSAN KIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS UDAYANA 2017 Kata Pengantar Puji dan
PENGEMBANGAN BAHAN AJAR TEORI TUMBUKAN PADA LAJU REAKSI KIMIA OLEH : Drs. I Wayan Suarsa, M.Si JURUSAN KIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS UDAYANA 2017 Kata Pengantar Puji dan
PENGARUH KATALISIS TERHADAP TETAPAN LAJU
 PENGARUH KATALISIS TERHADAP TETAPAN LAJU Laju reaksi sering dipengaruhi oleh adanya katalis Contoh : Hidrolisis sukrosa dalam air Suhu kamar lama (bisa beberapa bulan) Namun jika hidrolisis dilakukan dalam
PENGARUH KATALISIS TERHADAP TETAPAN LAJU Laju reaksi sering dipengaruhi oleh adanya katalis Contoh : Hidrolisis sukrosa dalam air Suhu kamar lama (bisa beberapa bulan) Namun jika hidrolisis dilakukan dalam
H 2 O (L) H 2 O (G) KESETIMBANGAN KIMIA. N 2 O 4 (G) 2NO 2 (G)
 H 2 O (L) H 2 O (G) KESETIMBANGAN KIMIA. N 2 O 4 (G) 2NO 2 (G) Purwanti Widhy H Kesetimbangan adalah suatu keadaan di mana tidak ada perubahan yang terlihat seiring berjalannya waktu. Kesetimbangan kimia
H 2 O (L) H 2 O (G) KESETIMBANGAN KIMIA. N 2 O 4 (G) 2NO 2 (G) Purwanti Widhy H Kesetimbangan adalah suatu keadaan di mana tidak ada perubahan yang terlihat seiring berjalannya waktu. Kesetimbangan kimia
Disampaikan oleh : Dr. Sri Handayani 2013
 Disampaikan oleh : Dr. Sri Handayani 2013 PENGERTIAN Termokimia adalah cabang dari ilmu kimia yang mempelajari hubungan antara reaksi dengan panas. HAL-HAL YANG DIPELAJARI Perubahan energi yang menyertai
Disampaikan oleh : Dr. Sri Handayani 2013 PENGERTIAN Termokimia adalah cabang dari ilmu kimia yang mempelajari hubungan antara reaksi dengan panas. HAL-HAL YANG DIPELAJARI Perubahan energi yang menyertai
LEMBAR KERJA SISWA 4
 88 LEMBAR KERJA SISWA 4 Mata Pelajaran Kelas/Semester Materi Pokok Submateri Pokok Alokasi Waktu : Kimia : I/ganjil : Laju Reaksi : Teori Tumbukan : 2 x 45 menit Standar Kompetensi Memahami Kinetika Reaksi,
88 LEMBAR KERJA SISWA 4 Mata Pelajaran Kelas/Semester Materi Pokok Submateri Pokok Alokasi Waktu : Kimia : I/ganjil : Laju Reaksi : Teori Tumbukan : 2 x 45 menit Standar Kompetensi Memahami Kinetika Reaksi,
BAB II LANDASAN TEORI
 digilib.uns.ac.id BAB II LANDASAN TEORI A. Tinjauan Pustaka 1. Mekanisme reaksi hidrogen peroksida dengan iodida a. Hidrogen peroksida Hidrogen peroksida merupakan agen pengoksidasi yang kuat. Senyawa
digilib.uns.ac.id BAB II LANDASAN TEORI A. Tinjauan Pustaka 1. Mekanisme reaksi hidrogen peroksida dengan iodida a. Hidrogen peroksida Hidrogen peroksida merupakan agen pengoksidasi yang kuat. Senyawa
BAB IV HASIL DAN PEMBAHASAN. A. Hasil
 digilib.uns.ac.id BAB IV HASIL DAN PEMBAHASAN A. Hasil 1. Penentuan Panjang Gelombang Maksimum dan Absorbtivitas Molar I 3 Penentuan Panjang Gelombang Maksimum Penentuan dilakukan dengan mereaksikan KI
digilib.uns.ac.id BAB IV HASIL DAN PEMBAHASAN A. Hasil 1. Penentuan Panjang Gelombang Maksimum dan Absorbtivitas Molar I 3 Penentuan Panjang Gelombang Maksimum Penentuan dilakukan dengan mereaksikan KI
Kesetimbangan Kimia. Bab 4
 Kesetimbangan Kimia Bab 4 Standar Kompetensi 3. Memahami kinetika reaksi, kesetimbangan kimia, dan faktor-faktor yang memengaruhinya, serta penerapannya dalam kehidupan sehari-hari dan industri Kompetensi
Kesetimbangan Kimia Bab 4 Standar Kompetensi 3. Memahami kinetika reaksi, kesetimbangan kimia, dan faktor-faktor yang memengaruhinya, serta penerapannya dalam kehidupan sehari-hari dan industri Kompetensi
Kinetika Reaksi Homogen Sistem Reaktor Alir (Kontinyu)
 KINETIKA DAN KATALISIS / SEMESTER PENDEK 2009-2010 PRODI TEKNIK KIMIA FTI UPN VETERAN YOGYAKARTA Kinetika Reaksi Homogen Sistem Reaktor Alir (Kontinyu) Senin, 19 Juli 2010 / Siti Diyar Kholisoh, ST, MT
KINETIKA DAN KATALISIS / SEMESTER PENDEK 2009-2010 PRODI TEKNIK KIMIA FTI UPN VETERAN YOGYAKARTA Kinetika Reaksi Homogen Sistem Reaktor Alir (Kontinyu) Senin, 19 Juli 2010 / Siti Diyar Kholisoh, ST, MT
Kesetimbangan dinamis adalah keadaan dimana dua proses yang berlawanan terjadi dengan laju yang sama, akibatnya tidak terjadi perubahan bersih dalam
 Kesetimbangan dinamis adalah keadaan dimana dua proses yang berlawanan terjadi dengan laju yang sama, akibatnya tidak terjadi perubahan bersih dalam sistem pada kesetimbangan Uap mengembun dengan laju
Kesetimbangan dinamis adalah keadaan dimana dua proses yang berlawanan terjadi dengan laju yang sama, akibatnya tidak terjadi perubahan bersih dalam sistem pada kesetimbangan Uap mengembun dengan laju
BAB II DASAR TEORI. FeO. CO Fe CO 2. Fe 3 O 4. Fe 2 O 3. Gambar 2.1. Skema arah pergerakan gas CO dan reduksi
 BAB II DASAR TEORI Pengujian reduksi langsung ini didasari oleh beberapa teori yang mendukungnya. Berikut ini adalah dasar-dasar teori mengenai reduksi langsung yang mendasari penelitian ini. 2.1. ADSORPSI
BAB II DASAR TEORI Pengujian reduksi langsung ini didasari oleh beberapa teori yang mendukungnya. Berikut ini adalah dasar-dasar teori mengenai reduksi langsung yang mendasari penelitian ini. 2.1. ADSORPSI
Soal-Soal. Bab 4. Latihan. Laju Reaksi. 1. Madu dengan massa jenis 1,4 gram/ cm 3 mengandung glukosa (M r. 5. Diketahui reaksi:
 Bab Laju Reaksi Soal-Soal Latihan. Madu dengan massa jenis, gram/ cm 3 mengandung glukosa (M r = 80) sebanyak 35 % b/b. Kemolaran glukosa dalam madu adalah... 0,8 M (D),7 M,8 M (E) 3,0 M, M. Untuk membuat
Bab Laju Reaksi Soal-Soal Latihan. Madu dengan massa jenis, gram/ cm 3 mengandung glukosa (M r = 80) sebanyak 35 % b/b. Kemolaran glukosa dalam madu adalah... 0,8 M (D),7 M,8 M (E) 3,0 M, M. Untuk membuat
LAPORAN PRAKTIKUM KIMIA DASAR
 LAPORAN PRAKTIKUM KIMIA DASAR KECEPATAN REAKSI Disusun Oleh : 1. Achmad Zaimul Khaqqi (132500030) 2. Dinda Kharisma Asmara (132500014) 3. Icha Restu Maulidiah (132500033) 4. Jauharatul Lailiyah (132500053)
LAPORAN PRAKTIKUM KIMIA DASAR KECEPATAN REAKSI Disusun Oleh : 1. Achmad Zaimul Khaqqi (132500030) 2. Dinda Kharisma Asmara (132500014) 3. Icha Restu Maulidiah (132500033) 4. Jauharatul Lailiyah (132500053)
SOAL-SOAL KESETIMBANGAN KIMIA
 H=+380 kj/mol SOAL-SOAL KESETIMBANGAN KIMIA 1. Ebtanas 99 Suatu reaksi berada dalam keadaan setimbang apabila A. Reaksi ke kanan dan kiri telah berhenti B. Mol pereaksi selalu sama dengan mol hasil reaksi
H=+380 kj/mol SOAL-SOAL KESETIMBANGAN KIMIA 1. Ebtanas 99 Suatu reaksi berada dalam keadaan setimbang apabila A. Reaksi ke kanan dan kiri telah berhenti B. Mol pereaksi selalu sama dengan mol hasil reaksi
BAB II KAJIAN PUSTAKA. kemampuan adalah karakteristik yang menonjol dari seorang individu yang
 BAB II KAJIAN PUSTAKA 2.1 Defenisi Kemampuan Kemampuan sama dengan kata kesanggupan atau kecakapan. Dengan bahasa yang lebih terperinci, kemampuan dapat diartikan sebagai kesanggupan individu untuk melakukan
BAB II KAJIAN PUSTAKA 2.1 Defenisi Kemampuan Kemampuan sama dengan kata kesanggupan atau kecakapan. Dengan bahasa yang lebih terperinci, kemampuan dapat diartikan sebagai kesanggupan individu untuk melakukan
Laporan Kimia Fisik KI-3141
 Laporan Kimia Fisik KI-3141 PERCOBAAN M-2 PENENTUAN LAJU REAKSI DAN TETAPAN LAJU REAKSI Nama : Kartika Trianita NIM : 10510007 Kelompok : 2 Tanggal Percobaan : 2 November 2012 Tanggal Laporan : 9 November
Laporan Kimia Fisik KI-3141 PERCOBAAN M-2 PENENTUAN LAJU REAKSI DAN TETAPAN LAJU REAKSI Nama : Kartika Trianita NIM : 10510007 Kelompok : 2 Tanggal Percobaan : 2 November 2012 Tanggal Laporan : 9 November
Chapter 6. Gas. Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display.
 Chapter 6 Gas Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. Beberapa zat yang berwujud gas pada suhu 25 0 C dan tekanan 1 Atm 5.1 1 5.1 Sifat-sifat fisis yang
Chapter 6 Gas Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. Beberapa zat yang berwujud gas pada suhu 25 0 C dan tekanan 1 Atm 5.1 1 5.1 Sifat-sifat fisis yang
Stoikiometri. Bab 3. Massa atom merupakan massa dari atom dalam satuan massa atom (sma). Secara Mikro atom & molekul.
 Bab 3 Stoikiometri Secara Mikro atom & molekul Secara Makro gram Massa atom merupakan massa dari atom dalam satuan massa atom (sma). Perjanjian internasional: 1 atom 12 C beratnya 12 sma Jika ditimbang
Bab 3 Stoikiometri Secara Mikro atom & molekul Secara Makro gram Massa atom merupakan massa dari atom dalam satuan massa atom (sma). Perjanjian internasional: 1 atom 12 C beratnya 12 sma Jika ditimbang
Kesetimbangan Kimia KIM 2 A. PENDAHULUAN B. REAKSI KESETIMBANGAN. α = KESETIMBANGAN KIMIA. materi78.co.nr. setimbang
 konsentrasi laju reaksi materi78.co.nr Kesetimbangan Kimia A. PENDAHULUAN Reaksi satu arah (irreversible) atau reaksi tidak dapat balik adalah reaksi yang terjadi pada satu arah, dan produknya tidak dapat
konsentrasi laju reaksi materi78.co.nr Kesetimbangan Kimia A. PENDAHULUAN Reaksi satu arah (irreversible) atau reaksi tidak dapat balik adalah reaksi yang terjadi pada satu arah, dan produknya tidak dapat
c. Suhu atau Temperatur
 Pada laju reaksi terdapat faktor-faktor yang dapat mempengaruhi laju reaksi. Selain bergantung pada jenis zat yang beraksi laju reaksi dipengaruhi oleh : a. Konsentrasi Pereaksi Pada umumnya jika konsentrasi
Pada laju reaksi terdapat faktor-faktor yang dapat mempengaruhi laju reaksi. Selain bergantung pada jenis zat yang beraksi laju reaksi dipengaruhi oleh : a. Konsentrasi Pereaksi Pada umumnya jika konsentrasi
BAB IV TERMOKIMIA A. PENGERTIAN KALOR REAKSI
 BAB IV TERMOKIMIA A. Standar Kompetensi: Memahami tentang ilmu kimia dan dasar-dasarnya serta mampu menerapkannya dalam kehidupan se-hari-hari terutama yang berhubungan langsung dengan kehidupan. B. Kompetensi
BAB IV TERMOKIMIA A. Standar Kompetensi: Memahami tentang ilmu kimia dan dasar-dasarnya serta mampu menerapkannya dalam kehidupan se-hari-hari terutama yang berhubungan langsung dengan kehidupan. B. Kompetensi
Kinetika Reaksi Homogen Sistem Reaktor Alir (Kontinyu)
 KINETIKA DAN KATALISIS / SEMESTER GENAP 2010-2011 PRODI TEKNIK KIMIA FTI UPN VETERAN YOGYAKARTA Kinetika Reaksi Homogen Sistem Reaktor Alir (Kontinyu) Siti Diyar Kholisoh & I Gusti S. Budiaman / Juni 2011
KINETIKA DAN KATALISIS / SEMESTER GENAP 2010-2011 PRODI TEKNIK KIMIA FTI UPN VETERAN YOGYAKARTA Kinetika Reaksi Homogen Sistem Reaktor Alir (Kontinyu) Siti Diyar Kholisoh & I Gusti S. Budiaman / Juni 2011
OLIMPIADE SAINS NASIONAL 2012 SELEKSI KABUPATEN / KOTA SOAL. UjianTeori. Waktu: 100 menit
 OLIMPIADE SAINS NASIONAL 2012 SELEKSI KABUPATEN / KOTA SOAL UjianTeori Waktu: 100 menit Kementerian Pendidikan dan Kebudayaan Direktorat Jenderal Pendidikan Menengah Direktorat Pembinaan Sekolah Menengah
OLIMPIADE SAINS NASIONAL 2012 SELEKSI KABUPATEN / KOTA SOAL UjianTeori Waktu: 100 menit Kementerian Pendidikan dan Kebudayaan Direktorat Jenderal Pendidikan Menengah Direktorat Pembinaan Sekolah Menengah
KIMIa ASAM-BASA II. K e l a s. A. Kesetimbangan Air. Kurikulum 2006/2013
 Kurikulum 2006/2013 KIMIa K e l a s XI ASAM-BASA II Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami kesetimbangan air. 2. Memahami pengaruh asam
Kurikulum 2006/2013 KIMIa K e l a s XI ASAM-BASA II Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami kesetimbangan air. 2. Memahami pengaruh asam
kecuali . kecuali . kecuali
 1. Berikut ini adalah ciri-ciri terjadinya reaksi kesetimbangan, kecuali. A. reaksi reversibel B. terjadi dalam ruang tertutup C. laju reaksi ke kiri sama dengan laju reaksi ke kanan D. reaksinya tidak
1. Berikut ini adalah ciri-ciri terjadinya reaksi kesetimbangan, kecuali. A. reaksi reversibel B. terjadi dalam ruang tertutup C. laju reaksi ke kiri sama dengan laju reaksi ke kanan D. reaksinya tidak
AMALDO FIRJARAHADI TANE
 DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN UTUL UGM KIMIA 2015 Page 1 1. MATERI: STOIKIOMETRI Persen massa adalah persentase massa zat terlarut dalam 100 gram massa larutan (massa pelarut + massa
DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN UTUL UGM KIMIA 2015 Page 1 1. MATERI: STOIKIOMETRI Persen massa adalah persentase massa zat terlarut dalam 100 gram massa larutan (massa pelarut + massa
Laju reaksi menunjukkan perubahan konsentrasi pereaksi atau hasil reaksi persatuan waktu.
 Bab IV Laju Reaksi Sumber: Ebbing, General Chemistry Laju reaksi menunjukkan perubahan konsentrasi pereaksi atau hasil reaksi persatuan waktu. TUJUAN PEMBELAJARAN Setelah mengikuti pembelajaran siswa dapat
Bab IV Laju Reaksi Sumber: Ebbing, General Chemistry Laju reaksi menunjukkan perubahan konsentrasi pereaksi atau hasil reaksi persatuan waktu. TUJUAN PEMBELAJARAN Setelah mengikuti pembelajaran siswa dapat
Hubungan entalpi dengan energi yang dipindahkan sebagai kalor pada tekanan tetap kepada sistem yang tidak dapat melakukan kerja lain
 Hubungan entalpi dengan energi yang dipindahkan sebagai kalor pada tekanan tetap kepada sistem yang tidak dapat melakukan kerja lain Jika sistem mengalami perubahan, maka : ΔH = H 2 H 1 ΔH = ( U 2 + p
Hubungan entalpi dengan energi yang dipindahkan sebagai kalor pada tekanan tetap kepada sistem yang tidak dapat melakukan kerja lain Jika sistem mengalami perubahan, maka : ΔH = H 2 H 1 ΔH = ( U 2 + p
Gas. Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display.
 Bab 5 Gas Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. Beberapa zat yang berwujud gas pada suhu 25 0 C dan tekanan 1At Atm 5.1 5.1 Sifat-sifat fisis yang khas
Bab 5 Gas Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. Beberapa zat yang berwujud gas pada suhu 25 0 C dan tekanan 1At Atm 5.1 5.1 Sifat-sifat fisis yang khas
PERCOBAAN 3 PERSAMAAN ARRHENIUS DAN ENERGI AKTIVASI
 LAPORAN PRAKTIKUM KIMIA FISIKA Nama : Any Kurniawati Kelompok : 6 NIM : 4301410009 Prodi/Jurusan : Pend. Kimia/Kimia Dosen : Ir. Sri Wahyuni, M.Si Tanggal Praktikum : 19 September 2012 Teman kerja : Fitriya
LAPORAN PRAKTIKUM KIMIA FISIKA Nama : Any Kurniawati Kelompok : 6 NIM : 4301410009 Prodi/Jurusan : Pend. Kimia/Kimia Dosen : Ir. Sri Wahyuni, M.Si Tanggal Praktikum : 19 September 2012 Teman kerja : Fitriya
Massa atom merupakan massa dari atom dalam satuan massa atom (sma).
 Bab 3 Stoikiometri Secara Mikro atom & molekul Secara Makro gram Massa atom merupakan massa dari atom dalam satuan massa atom (sma). Perjanjian internasional: 1 atom 12 C beratnya 12 sma Jika ditimbang
Bab 3 Stoikiometri Secara Mikro atom & molekul Secara Makro gram Massa atom merupakan massa dari atom dalam satuan massa atom (sma). Perjanjian internasional: 1 atom 12 C beratnya 12 sma Jika ditimbang
D. 8 mol S E. 4 mol Fe(OH) 3 C. 6 mol S Kunci : B Penyelesaian : Reaksi :
 1. Perhatikan reaksi, 2 Fe 2 S 3 + 3O 2 + 6 H 2 O 4 Fe(OH) 3 + 6S Jika 2 mol Fe 2 S 3, 2 mol O 2 dan 3 mol H 2 O bereaksi dengan sempurna, akan dihasilkan : A. 3 mol Fe(OH) 3 B. 2 mol Fe(OH) 3 D. 8 mol
1. Perhatikan reaksi, 2 Fe 2 S 3 + 3O 2 + 6 H 2 O 4 Fe(OH) 3 + 6S Jika 2 mol Fe 2 S 3, 2 mol O 2 dan 3 mol H 2 O bereaksi dengan sempurna, akan dihasilkan : A. 3 mol Fe(OH) 3 B. 2 mol Fe(OH) 3 D. 8 mol
RENCANA PELAKSANAAN PEMBELAJARAN (RPP) KELAS EKSPERIMEN PERTEMUAN KE-1
 RENCANA PELAKSANAAN PEMBELAJARAN (RPP) KELAS EKSPERIMEN PERTEMUAN KE-1 Sekolah : SMAN 3 Tangerang Selatan Mata Pelajaran : Kimia Kelas/ Semester : XI/ I Tahun Pelajaran : 010/011 Pokok Bahasan : Laju Reaksi
RENCANA PELAKSANAAN PEMBELAJARAN (RPP) KELAS EKSPERIMEN PERTEMUAN KE-1 Sekolah : SMAN 3 Tangerang Selatan Mata Pelajaran : Kimia Kelas/ Semester : XI/ I Tahun Pelajaran : 010/011 Pokok Bahasan : Laju Reaksi
BAB II KESETIMBANGAN KIMIA
 BAB II KESETIMBANGAN KIMIA TIU : 1. Memahami definisi kimia dan mengidentifikasi keadaan kimia. Memahami faktor-faktor yang mempengaruhi kimia: Prinsip Le Chatelier. Memahami aplikasi kimia dalam perolehan
BAB II KESETIMBANGAN KIMIA TIU : 1. Memahami definisi kimia dan mengidentifikasi keadaan kimia. Memahami faktor-faktor yang mempengaruhi kimia: Prinsip Le Chatelier. Memahami aplikasi kimia dalam perolehan
LEMBAR KERJA SISWA 2
 76 LEMBAR KERJA SISWA 2 Mata Pelajaran Kelas / Semester Materi pokok Submateri pokok Alokasi Waktu : Kimia : XI/ganjil : Laju Reaksi : Konsep Laju Reaksi : 2 x 45 menit Standar Kompetensi 3. Memahami Kinetika
76 LEMBAR KERJA SISWA 2 Mata Pelajaran Kelas / Semester Materi pokok Submateri pokok Alokasi Waktu : Kimia : XI/ganjil : Laju Reaksi : Konsep Laju Reaksi : 2 x 45 menit Standar Kompetensi 3. Memahami Kinetika
Stoikhiometri : dan metron = mengukur. Membahas tentang : senyawa) senyawa (stoikhiometri. (stoikhiometri. reaksi)
 STOIKHIOMETRI Stoikhiometri : Dari kata Stoicheion = unsur dan metron = mengukur Membahas tentang : hub massa antar unsur dalam suatu senyawa (stoikhiometri senyawa) dan antar zat dalam suatu reaksi (stoikhiometri
STOIKHIOMETRI Stoikhiometri : Dari kata Stoicheion = unsur dan metron = mengukur Membahas tentang : hub massa antar unsur dalam suatu senyawa (stoikhiometri senyawa) dan antar zat dalam suatu reaksi (stoikhiometri
TES AWAL II KIMIA DASAR II (KI-112)
 TES AWAL II KIMIA DASAR II (KI112) NAMA : Tanda Tangan N I M : JURUSAN :... BERBAGAI DATA. Tetapan gas R = 0,082 L atm mol 1 K 1 = 1,987 kal mol 1 K 1 = 8,314 J mol 1 K 1 Tetapan Avogadro = 6,023 x 10
TES AWAL II KIMIA DASAR II (KI112) NAMA : Tanda Tangan N I M : JURUSAN :... BERBAGAI DATA. Tetapan gas R = 0,082 L atm mol 1 K 1 = 1,987 kal mol 1 K 1 = 8,314 J mol 1 K 1 Tetapan Avogadro = 6,023 x 10
No Indikator Soal Valid
 107 Lampiran 3 Rekapitulasi asi Instrumen TDM-TWO-TIER No Indikator Soal 1 Memahami kesetimbangan Reaksi kesetimbangan antara N 2 O 4 dengan NO 2 mengikuti persamaan kimia berikut ini : ator 1 :- dinamis
107 Lampiran 3 Rekapitulasi asi Instrumen TDM-TWO-TIER No Indikator Soal 1 Memahami kesetimbangan Reaksi kesetimbangan antara N 2 O 4 dengan NO 2 mengikuti persamaan kimia berikut ini : ator 1 :- dinamis
kimia LAJU REAKSI 1 TUJUAN PEMBELAJARAN
 KTSP & K-13 kimia K e l a s XI LAJU REAKSI 1 TUJUAN PEMBELAJARAN Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami konsep molaritas. 2. Memahami definisi dan faktor-faktor
KTSP & K-13 kimia K e l a s XI LAJU REAKSI 1 TUJUAN PEMBELAJARAN Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami konsep molaritas. 2. Memahami definisi dan faktor-faktor
Tabel Periodik. Bab 3a. Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi 2010 dimodifikasi oleh Dr.
 Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi 2010 dimodifikasi oleh Dr. Indriana Kartini Bab 3a Tabel Periodik Kapan unsur-unsur ditemukan? 8.1 1 ns 1 Konfigurasi elektron
Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi 2010 dimodifikasi oleh Dr. Indriana Kartini Bab 3a Tabel Periodik Kapan unsur-unsur ditemukan? 8.1 1 ns 1 Konfigurasi elektron
Soal ini terdiri dari 10 soal Essay (153 poin)
 Bidang Studi Kode Berkas : Kimia : KI-L01 (soal) Soal ini terdiri dari 10 soal Essay (153 poin) Tetapan Avogadro N A = 6,022 10 23 partikel.mol 1 Tetapan Gas Universal R = 8,3145 J.mol -1.K -1 = 0,08206
Bidang Studi Kode Berkas : Kimia : KI-L01 (soal) Soal ini terdiri dari 10 soal Essay (153 poin) Tetapan Avogadro N A = 6,022 10 23 partikel.mol 1 Tetapan Gas Universal R = 8,3145 J.mol -1.K -1 = 0,08206
Siswa diingatkan tentang struktur atom, bilangan kuantum, bentuk-bentuk orbital, dan konfigurasi elektron
 RENCANA PELAKSANAAN PEMBELAJARAN NO: 1 Mata Pelajaran : Kimia Kelas/Semester : XI/1 Materi Pokok : Stuktur atom dan sistem periodik unsur Pertemuan Ke- : 1 dan 2 Alokasi Waktu : 2 x pertemuan (4 x 45 menit)
RENCANA PELAKSANAAN PEMBELAJARAN NO: 1 Mata Pelajaran : Kimia Kelas/Semester : XI/1 Materi Pokok : Stuktur atom dan sistem periodik unsur Pertemuan Ke- : 1 dan 2 Alokasi Waktu : 2 x pertemuan (4 x 45 menit)
TERMOKIMIA. STANDART KOMPETENSI; 2. Memahami perubahan energi dalam kimia dan cara pengukuran. ENTALPI DAN PERUBAHANNYA
 TERMOKIMIA STANDART KOMPETENSI; 2. Memahami perubahan energi dalam kimia dan cara pengukuran. ENTALPI DAN PERUBAHANNYA KOMPETENSI DASAR; 2.1. Mendeskripsikan perubahan entalpi suatu reaksi, reaksi eksoterm
TERMOKIMIA STANDART KOMPETENSI; 2. Memahami perubahan energi dalam kimia dan cara pengukuran. ENTALPI DAN PERUBAHANNYA KOMPETENSI DASAR; 2.1. Mendeskripsikan perubahan entalpi suatu reaksi, reaksi eksoterm
yang berkaitan dengan Laju Reaksi, diberikan pada tabel berikut ini.
 BAB IV HASIL PENELITIAN DAN PEMBAHASAN 4.1 Hasil Penelitian Berdasarkan hasil pengumpulan data, persentase siswa SMA Negeri 1 Paguyaman, Kabupaten Boalemo yang memberikan jawaban untuk tiap item tes yang
BAB IV HASIL PENELITIAN DAN PEMBAHASAN 4.1 Hasil Penelitian Berdasarkan hasil pengumpulan data, persentase siswa SMA Negeri 1 Paguyaman, Kabupaten Boalemo yang memberikan jawaban untuk tiap item tes yang
AMALDO FIRJARAHADI TANE
 DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN UTUL UGM KIMIA 2013 Page 1 1. 2. MATERI: HUKUM-HUKUM DASAR KIMIA Di soal diketahui dan ditanya: m (NH 2 ) 2 CO = 12.000 ton/tahun (pabrik) m N 2 = ton/tahun?
DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN UTUL UGM KIMIA 2013 Page 1 1. 2. MATERI: HUKUM-HUKUM DASAR KIMIA Di soal diketahui dan ditanya: m (NH 2 ) 2 CO = 12.000 ton/tahun (pabrik) m N 2 = ton/tahun?
AMALDO FIRJARAHADI TANE
 DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN UTUL UGM KIMIA 2013 Page 1 1. 2. MATERI: TERMOKIMIA Pada soal diketahui dan ditanya: ΔH c C 2 H 5 OH = -1380 kj/mol ΔH d C 6 H 12 O 6 = -60 kj/mol ΔH c C
DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN UTUL UGM KIMIA 2013 Page 1 1. 2. MATERI: TERMOKIMIA Pada soal diketahui dan ditanya: ΔH c C 2 H 5 OH = -1380 kj/mol ΔH d C 6 H 12 O 6 = -60 kj/mol ΔH c C
Kekekalan Energi energi tidak dapat diciptakan maupun dimusnahkan
 Termokimia XI IPA CO 2, mineral, panas, cahaya Kekekalan Energi energi tidak dapat diciptakan maupun dimusnahkan Manusia Fotosintesis Sayuran dan Buah Entalpi energi / kalor yang terdapat dalam suatu materi.
Termokimia XI IPA CO 2, mineral, panas, cahaya Kekekalan Energi energi tidak dapat diciptakan maupun dimusnahkan Manusia Fotosintesis Sayuran dan Buah Entalpi energi / kalor yang terdapat dalam suatu materi.
TERMOKIMIA. Sistem terbagi atas: 1. Sistem tersekat: Antara sistem dan lingkungan tidak dapat terjadi pertukaran energi maupun materi
 TERMOKIMIA almair amrulloh 12:04:00 AM 11 IPAKimia 11 IPA Asas kekekalan energi menyatakan bahwa energi tidak dapat diciptakan atau dimusnahkan, tetapi energi dapat diubah dari satu bentuk kebentuk lain
TERMOKIMIA almair amrulloh 12:04:00 AM 11 IPAKimia 11 IPA Asas kekekalan energi menyatakan bahwa energi tidak dapat diciptakan atau dimusnahkan, tetapi energi dapat diubah dari satu bentuk kebentuk lain
OLIMPIADE SAINS NASIONAL 2012 SELEKSI KABUPATEN / KOTA SOAL. UjianTeori. Waktu: 100 menit
 OLIMPIADE SAINS NASIONAL 2012 SELEKSI KABUPATEN / KOTA SOAL UjianTeori Waktu: 100 menit Kementerian Pendidikan dan Kebudayaan Direktorat Jenderal Pendidikan Menengah Direktorat Pembinaan Sekolah Menengah
OLIMPIADE SAINS NASIONAL 2012 SELEKSI KABUPATEN / KOTA SOAL UjianTeori Waktu: 100 menit Kementerian Pendidikan dan Kebudayaan Direktorat Jenderal Pendidikan Menengah Direktorat Pembinaan Sekolah Menengah
SOAL SELEKSI NASIONAL TAHUN 2006
 SOAL SELEKSI NASIONAL TAHUN 2006 Soal 1 ( 13 poin ) KOEFISIEN REAKSI DAN LARUTAN ELEKTROLIT Koefisien reaksi merupakan langkah penting untuk mengamati proses berlangsungnya reaksi. Lengkapi koefisien reaksi-reaksi
SOAL SELEKSI NASIONAL TAHUN 2006 Soal 1 ( 13 poin ) KOEFISIEN REAKSI DAN LARUTAN ELEKTROLIT Koefisien reaksi merupakan langkah penting untuk mengamati proses berlangsungnya reaksi. Lengkapi koefisien reaksi-reaksi
Laju Reaksi. Kode KIM.10
 Kode KIM.10 Laju Reaksi BAGIAN PROYEK PENGEMBANGAN KURIKULUM DIREKTORAT PENDIDIKAN MENENGAH KEJURUAN DIREKTORAT JENDERAL PENDIDIKAN DASAR DAN MENENGAH DEPARTEMEN PENDIDIKAN NASIONAL 004 Kim. 10. Laju Reaksi
Kode KIM.10 Laju Reaksi BAGIAN PROYEK PENGEMBANGAN KURIKULUM DIREKTORAT PENDIDIKAN MENENGAH KEJURUAN DIREKTORAT JENDERAL PENDIDIKAN DASAR DAN MENENGAH DEPARTEMEN PENDIDIKAN NASIONAL 004 Kim. 10. Laju Reaksi
A. ARTI KESETIMBANGAN B. FAKTOR-FAKTOR YANG MEMPENGARUHI PERGESERAN KESETIMBANGAN C. TETAPAN KESETIMBANGAN D. KESETIMBANGAN KIMIA DALAM INDUSTRI
 4 KESETIMBANGAN KIMIA A. ARTI KESETIMBANGAN B. FAKTOR-FAKTOR YANG MEMPENGARUHI PERGESERAN KESETIMBANGAN C. TETAPAN KESETIMBANGAN D. KESETIMBANGAN KIMIA DALAM INDUSTRI Dalam kehidupan sehari-hari, sering
4 KESETIMBANGAN KIMIA A. ARTI KESETIMBANGAN B. FAKTOR-FAKTOR YANG MEMPENGARUHI PERGESERAN KESETIMBANGAN C. TETAPAN KESETIMBANGAN D. KESETIMBANGAN KIMIA DALAM INDUSTRI Dalam kehidupan sehari-hari, sering
OLIMPIADE SAINS NASIONAL 2012 SELEKSI KABUPATEN / KOTA JAWABAN (DOKUMEN NEGARA) UjianTeori. Waktu: 100 menit
 OLIMPIADE SAINS NASIONAL 2012 SELEKSI KABUPATEN / KOTA JAWABAN (DOKUMEN NEGARA) UjianTeori Waktu: 100 menit Kementerian Pendidikan Nasional Dan Kebudayaan Direktorat Jenderal Managemen Pendidikan Dasar
OLIMPIADE SAINS NASIONAL 2012 SELEKSI KABUPATEN / KOTA JAWABAN (DOKUMEN NEGARA) UjianTeori Waktu: 100 menit Kementerian Pendidikan Nasional Dan Kebudayaan Direktorat Jenderal Managemen Pendidikan Dasar
Faktor-Faktor yang Mempengaruhi Pergeseran Kesetimbangan
 Standar Kometensi Kometensi Dasar Menjelaskan kinetika dan kesetimbangan reaksi kimia serta faktor-faktor yang memengaruhinya. Menjelaskan engertian reaksi kesetimbangan. Menyelidiki faktor-faktor yang
Standar Kometensi Kometensi Dasar Menjelaskan kinetika dan kesetimbangan reaksi kimia serta faktor-faktor yang memengaruhinya. Menjelaskan engertian reaksi kesetimbangan. Menyelidiki faktor-faktor yang
Laju Reaksi. Bahan Ajar Mata Pelajaran Kimia Kelas XI Semester I
 Laju Reaksi Bahan Ajar Mata Pelajaran Kimia Kelas XI Semester I SK, KD dan Indikator Kemolaran Konsep Laju Reaksi Faktor-faktor yang mempengaruhi laju reaksi Evaluasi Referensi Selesai Standar Kompetensi,
Laju Reaksi Bahan Ajar Mata Pelajaran Kimia Kelas XI Semester I SK, KD dan Indikator Kemolaran Konsep Laju Reaksi Faktor-faktor yang mempengaruhi laju reaksi Evaluasi Referensi Selesai Standar Kompetensi,
