UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MIPA
|
|
|
- Hendri Sanjaya
- 6 tahun lalu
- Tontonan:
Transkripsi
1 UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MIPA SILABI SIL/BIC291 / 01 1 Februari Fakultas : Matematika dan Ilmu Pengetahuan Alam (MIPA) 2. Program Studi : Biologi dan Pendidikan Biologi 3. Mata kuliah & Kode : Kimia Dasar / BIC Jumlah sks : Teori 2 sks. 5. Semester : 1 6. Mata kuliah Prasyarat & Kode:Tidak ada 7. Dosen : Susila K, M.Si, Annisa F, M.Si I. DESKRIPSI MATA KULIAH Pendahuluan (Materi dan Perubahannya), Stoikiometri, Larutan, Kinetika Kimia, Termokimia, Kimia Inti & Radiokimia, Kimia Organik & Biokimia (Karbohidrat, Lemak, Protein) II. STANDAR KOMPETENSI MATA KULIAH Setelah menyelesaikan mata kuliah ini mahasiswa dapat memahami dan menjelaskan perubahan materi, memahami dan menyelesaikan soal-soal Stoikiometri, memahami dan menyelesaikan soal-soal Larutan dan dapat mengaplikasikannya, memahami dan menyelesaikan soal-soal Kinetika Kimia, memahami dan menyelesaikan soal-soa Termokimia, memahami dan menjelaskan tentang Kimia Inti & Radiokimia, memahami dan menjelaskan tentang Kimia Organik & Biokimia III. RENCANA KEGIATAN Tatap Muka ke Kompetensi Dasar 1 Mahasiswa dapat memahami & menjelaskan perubahan materi 2 Mahasiswa dapat memahami dan menyelesaikan soal-soal Materi Pokok Materi dan Perubahannya Stoikiometri bag. 1 Strategi Perkuliahan Perkuliahan tatap muka, diskusi Perkuliahan tatap muka, diskusi informasi Sumber Bahan/ Referensi 1, (a-e) 1, (a-e)
2 Stoikiometri 3 Mahasiswa dapat Stoikiometri bag. 2 Perkuliahan tatap memahami dan muka, diskusi menyelesaikan soal-soal Stoikiometri informasi 4 Mahasiswa dapat Larutan bag. 1 Perkuliahan tatap memahami dan muka, diskusi menyelesaikan informasi soal-soal Larutan 5 Mahasiswa dapat Larutan bag. 2 Perkuliahan tatap mengaplikasikan muka, diskusi prinsip larutan informasi 6 Mahasiswa dapat Kinetika Kimia bag. Perkuliahan tatap memahami dan 1 muka, diskusi menyelesaikan informasi soal-soal Kinetika Kimia 7 Mahasiswa dapat Kinetika Kimia bag. Perkuliahan tatap memahami dan 1 muka, diskusi menyelesaikan informasi soal-soal Kinetika Kimia 8 UJIAN TENGAH SEMESTER ke-1 9 Mahasiswa dapat Termokimia bag.1 Perkuliahan tatap memahami dan muka, diskusi menyelesaikan informasi soal-soal Termokimia 10 Mahasiswa dapat Termokimia bag.2 Perkuliahan tatap memahami dan muka, diskusi menyelesaikan informasi soal-soal Termokimia 11 Mahasiswa dapat Kimia Inti & Perkuliahan tatap memahami dan Radiokimia, muka, diskusi menjelaskan informasi, tugas tentang Kimia Inti & Radiokimia, 12 Mahasiswa dapat Kimia Organik Perkuliahan tatap memahami dan muka, diskusi menjelaskan reaksi informasi dalam Kimia Organik 13 Mahasiswa dapat Karbohidrat Perkuliahan tatap memahami dan muka, diskusi 1 (a,b,d,e) 1 (a,b,d,e) 1 (a,b,d,e) 1 (a,b,d,e) 1 (a,b,d,e) 1 (a,b,d, e) 1, (a,b,d, e) 1, (b,c,d,e) 1, (b,e) 1, (b,e)
3 menjelaskan, mengklasifikasikan karbohidrat 14 Mahasiswa dapat memahami dan menjelaskan, mengklasifikasikan lemak 15 Mahasiswa dapat memahami dan menjelaskan, mengklasifikasikan protein Lemak Protein informasi Perkuliahan tatap muka, diskusi informasi, tugas Perkuliahan tatap muka, diskusi informasi, tugas 16 UJIAN TENGAH SEMESTER ke-2 1, (b,e) 1, (b,e) IV. REFERENSI/SUMBER BAHAN A. Wajib : 1. Retno Arianingrum, Siti Sulastri, dan Susila Kristianingrum, dkk (2006). Diktat Kuliah Kimia Dasar untuk Biologi,,Yogyakarta: Universitas Negeri Yogyakarta. B. Anjuran : a. Atkins, P.W. (1997), Kimia Fisika, Edisi ke-4. Jakarta : Penerbit Erlangga.. b. Brady, J.E., (1990), General Chemistry, 5 th Ed. New York : John Wiley & Sons. c. Hiskia Ahmad, (1992), Kimia Unsur dan Radiokimia, Bandung: Penerbit PT. CAB. d. Keenan, C.W., Kleinfelter, D.C., and Wood., J.H. (1980). General College Chemistry, Harper & Row Publisher, Inc. e. Petrucci, R.H. (1992), Kimia Dasar Prinsip dan Terapan Modern. terjemahan oleh Suminar Achmadi, Jakarta: Penerbit Erlangga. V. EVALUASI No Komponen Evaluasi Bobot (%) 1 Partisipasi Kuliah 20 2 Tugas-tugas 10 3 Ujian Tengah Semester 30 4 Ujian Semester 40 Jumlah 100 Yogyakarta, Februari 2013 Mengetahui, Ketua Jurusan Pendidikan Kimia FMIPA UNY Dosen Dr. Hari Sutrisno Susila Kristianingrum, M.Si NIP NIP
4 UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MIPA RENCANA PELAKSANAAN PEMBELAJARAN RPP/BIC291 / Februari Fakultas/Progran Studi : MIPA/ Biologi & Pendidikan Biologi 2. Mata kuliah & Kode : Kimia Dasar /BIC Jumlah sks : Teori 2 sks. 4. Semester dan Waktu : 1,Waktu 2 x 50 menit 5. Kompetensi Dasar : Memahami berbagai proses perubahan materi 6. Indikator Ketercapaian :Dapat menjelaskan perubahan fisika dan kimia 7. Materi Pokok/Penggalan Materi: Pendahuluan 8. Kegiatan Perkuliahan : Komponen Langkah Uraian Kegiatan Pendahuluan Memberi salam, memotivasi peserta didik, dan memberikan apersepsi tentang materi dan perubahannya Penyajian -Menjelaskan (Inti) sifat intensif dan ekstensif dari suatu materi dan contohnya -Menjelaskan materi dan perubahannya, proses-proses fisika dan kimia Estimasi Waktu Metode Media Sumber Bahan/ Referensi 10 menit Ceramah 70 menit Ceramah, diskusi informasi, Tanya LCD 1, a, b, c 1, a, b, c -Memberikan contoh proses perubahan fisika
5 Penutup Tindak Lanjut -Memberikan contoh proses perubahan kimia dalamkehidupan sehari-hari Memberikan rangkuman materi, memberikan salam Memerintahkan peserta didik untuk membaca diktat Kimia Dasar Untuk Biologi 15 menit Diskusi, tanya 5 menit Tanya 1,a,b,c,d 1 9. Evaluasi Untuk memperdalam pemahaman anda mengenai materi di atas, kerjakanlah latihan berikut: 1. Jelaskan perbedaan antara sifat intensif dan ekstensif dari suatu materi serta berikan contohnya. 2. Jelaskan apa yang dimaksud dengan: a. proses fisika b. proses kimia 3. Jelaskan perbedaan antara perubahan fisika dan kimia 4. Berikan contoh perubahan fisika dalam kehidupan sehari-hari 5. Berikan contoh perubahan kimia dalam kehidupan sehari-hari Mengetahui, Ketua Jurusan Pendidikan Kimia FMIPA UNY Yogyakarta, Februari 2011 Dosen Dr. Hari Sutrisno Susila Kristianingrum, M.Si NIP NIP
6 UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MIPA RENCANA PELAKSANAAN PEMBELAJARAN RPP/BIC291 / Februari Fakultas/Progran Studi : MIPA/ Biologi & Pendidikan Biologi 2. Mata kuliah & Kode : Kimia Dasar /BIC Jumlah sks : Teori 2 sks. 4. Semester dan Waktu : 1,Waktu 2 x 50 menit 5. Kompetensi Dasar : Memahami perhitungan dalam stoikiometri 6. Indikator Ketercapaian : Dapat menerapkan hukum-hukum dasar kimia dalam menyelesaikan perhitungan kimia 7. Materi Pokok/Penggalan Materi: Stoikiometri bag Kegiatan Perkuliahan : Komponen Langkah Uraian Kegiatan Pendahuluan Memberi salam, memotivasi peserta didik, dan memberikan apersepsi tentang stoikiometri Penyajian -Menjelaskan (Inti) perkembangan teori atom -Menjelaskan hukum-hukum dasar reaksi kimia (hk. Kekekalan massa, hk perbandingan tetap, hk perbandingan berganda, hk. Perbandingan Estimasi Waktu Metode Media Sumber Bahan/ Referensi 10 menit Ceramah 70 menit Ceramah, diskusi informasi, Tanya LCD 1, a, b 1, a, b, c,d,e
7 Penutup Tindak Lanjut setara, hk.perbandingan volume dan hk. Avogadro). Memberikan rangkuman materi, memberikan soal untuk tugas di rumah Memerintahkan peserta didik untuk membaca diktat Kimia Dasar Untuk Biologi dan mengerjakan tugas di rumah 15 menit Diskusi, tanya 5 menit Tanya 1,a,b,c,d,e 1 9. Evaluasi Untuk memperdalam pemahaman anda mengenai materi di atas, kerjakanlah latihan berikut: 1. Jelaskan bagaimanakah teori atom Dalton 2. Ungkapkan dengan kata-kata sendiri mengenai: a. hukum perbandingan tetap (Proust) b. hukum perbandingan berganda (Dalton) c. hukum perbandingan setara d. hukum perbandingan volumen e. hukum Avogadro 3. Tiga macam oksida dari suatu logam masing-masing mengandung 7,20; 9,39; dan 13,44% oksigen. Tunjukkan dengan perhitungan bahwa data tersebut sesuai dengan hukum perbandingan berganda. 4. Tiga buah senyawa yang mengandung atom X dan Y. Senyawa pertama mengandung 4,31 g X dan 7,69 g Y; senyawa kedua terdiri dari 35,9% X dan 64,1% Y. Bila 0,718 g X direaksikan dengan Y maka terbentuk 2 g senyawa baru. Buktikan hukum Perbandingan Tetap pada senyawa tersebut. Mengetahui, Ketua Jurusan Pendidikan Kimia FMIPA UNY Yogyakarta, Februari 2013 Dosen Dr. Hari Sutrisno Susila Kristianingrum, M.Si NIP NIP
8 UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MIPA ENCANA PELAKSANAAN PEMBELAJARAN RPP/BIC291 / Februari Fakultas/Progran Studi : MIPA/ Biologi & Pendidikan Biologi 2. Mata kuliah & Kode : Kimia Dasar /BIC Jumlah sks : Teori 2 sks. 4. Semester dan Waktu : 1,Waktu 2 x 50 menit 5. Kompetensi Dasar : Memahami perhitungan dalam stoikiometri 6. Indikator Ketercapaian : Dapat menerapkan hukum-hukum dasar kimia dalam menyelesaikan perhitungan kimia 7. Materi Pokok/Penggalan Materi: Stoikiometri bag Kegiatan Perkuliahan : Komponen Langkah Uraian Kegiatan Pendahuluan Memberi salam, memotivasi peserta didik, dan memberikan apersepsi tentang stoikiometri Penyajian -Menjelaskan (Inti) pengertian massa atom relatif, massa rumus relatif dan massa molekul relatif -Menjelaskan konsep mol dan penerapannya dalam soal -Menjelaskan rumus empirik dan rumus molekul dan contoh soalnya. Estimasi Waktu Metode Media Sumber Bahan/ Referensi 10 menit Ceramah 70 menit Ceramah, diskusi informasi, Tanya LCD 1, a, b 1, a, b, c,d,e
9 Penutup Tindak Lanjut -Menjelaskan reaksi-reaksi kimia Memberikan rangkuman materi, memberikan soal untuk tugas di rumah Memerintahkan peserta didik untuk membaca diktat Kimia Dasar Untuk Biologi dan mengerjakan tugas di rumah 15 menit Diskusi, tanya 5 menit Tanya 1,a,b,c,d,e 1 9. Evaluasi Untuk memperdalam pemahaman anda mengenai materi di atas, kerjakanlah latihan berikut: 1. Hitunglah: a. Berapa mol 242 g NaHCO 3? (Ar Na=23, H=1, C=12, dan O=16) b. Berapa mol S yang ada dalam 632 g FeS 2? (Ar S=32, Fe=56) 2. Pembakaran 0,200 g sampel senyawa C,H,O dalam vitamin C menghasilkan 0,2998 g CO 2 dan 0,0819 g H 2 O a. Bagaimanakah rumus empiris vitamin C? b. Tentukan % susunan unsur dalam vitamin C tersebut. (Diketahui Ar C=12, H=1, O=16). 3. Sebanyak 0,537 g senyawa yang mengandung C, H, dan O dibakar menghasilkan 1,030 g CO 2 dan 0,632 g H 2 O. Tentukan rumus empiris senyawa tersebut (Diketahui Ar C=12, H=1, O=16). Mengetahui, Ketua Jurusan Pendidikan Kimia FMIPA UNY Yogyakarta, Februari 2013 Dosen Dr. Hari Sutrisno Susila Kristianingrum, M.Si NIP NIP
10 UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MIPA RENCANA PELAKSANAAN PEMBELAJARAN RPP/BIC291 / Februari Fakultas/Progran Studi : MIPA/ Biologi & Pendidikan Biologi 2. Mata kuliah & Kode : Kimia Dasar /BIC Jumlah sks : Teori 2 sks. 4. Semester dan Waktu : 1,Waktu 2 x 50 menit 5. Kompetensi Dasar : Memahami konsep dasar larutan dan menginterpretasikan serta menerapkannya dalam berbagai perhitungan kimia 6. Indikator Ketercapaian : Dapat menyelesaikan soal-soal yang terkait dengan konsentrasi larutan & sifat koligatif larutan 7. Materi Pokok/Penggalan Materi: Larutan bag.1 8. Kegiatan Perkuliahan : Komponen Langkah Uraian Kegiatan Pendahuluan Memberi salam, memotivasi peserta didik, dan memberikan apersepsi tentang larutan Penyajian -Menjelaskan (Inti) pengertian larutan,berbagai satuankonsentrasi larutan(%,bpj/ppm, molaritas, molalitas, fraksi mol, normalitas -Menjelaskan sifat koligatif larutan -Menjelaskan proses asosiasi dan disosiasi zat dalam larutan -Memberikan contoh-contoh soal Estimasi Waktu Metode Media Sumber Bahan/ Referensi 10 menit Ceramah 70 menit Ceramah, diskusi informasi, Tanya LCD 1, a, b 1, a, b, c,d,e
11 Penutup Tindak Lanjut Memberikan rangkuman materi, memberikan soal untuk tugas di rumah Memerintahkan peserta didik untuk membaca diktat Kimia Dasar Untuk Biologi dan mengerjakan tugas di rumah 15 menit Diskusi, tanya 5 menit Tanya 1,a,b,c,d,e 1 9. Evaluasi Untuk memperdalam pemahaman anda mengenai materi di atas, kerjakanlah latihan berikut: 1. Hitunglah: a.molaritas 26 gram CH 3 COOH dalam 750 ml larutan b.molalitas 14,4 gram glukosa (C 6 H 12 O 6 ) dalam 750 gram air. (Diket: Ar C=12, O=16, H=1). c. Tentukan fraksi mol etanol dalam larutan etanol 46%. 2. Hitunglah kemolalan larutan yang dibuat dari 8 gram NaOH dalam 750 gram air? Diketahui. Ar Na=23, H=1, O= Jelaskan mengenai sifat koligatif larutan. 4. Berapa gram sukrosa(c 12 H 22 O 11 ) yang harus dilarutkan ke dalam 200 ml air supaya tekanannya 0,25 atm pada 20 o C? (Diketahui Ar C=12, H=1, O=16); R=0,082 L.atm/mol.K 5. Hitunglah Mr dari zat apabila 5 gram zat tersebut dimasukkan dalam 200mL larutan dan menyebabkan tekanan osmosis 0,0237 atm pada 27 o C? Diketahui R=0,082 L.atm/mol.K Mengetahui, Ketua Jurusan Pendidikan Kimia FMIPA UNY Yogyakarta, Februari 2013 Dosen Dr. Hari Sutrisno Susila Kristianingrum, M.Si NIP NIP
12 UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MIPA RENCANA PELAKSANAAN PEMBELAJARAN RPP/BIC291 / Februari Fakultas/Progran Studi : MIPA/ Biologi & Pendidikan Biologi 2. Mata kuliah & Kode : Kimia Dasar /BIC Jumlah sks : Teori 2 sks. 4. Semester dan Waktu : 1,Waktu 2 x 50 menit 5. Kompetensi Dasar : Memahami sifat larutan asam dan basa 6. Indikator Ketercapaian : Dapat menyelesaikan soal-soal yang terkait dengan larutan asam dan basa 7. Materi Pokok/Penggalan Materi: Larutan bag.2 8. Kegiatan Perkuliahan : Komponen Langkah Uraian Kegiatan Pendahuluan Memberi salam, memotivasi peserta didik, dan memberikan apersepsi tentang larutan asam basa Penyajian -Menjelaskan (Inti) pengertian asam basa menurut Arrhenius, Bronsted-Lowry, dan Lewis dan contoh-contohnya. -Menentukan ph suatu larutan asam basa lemah, ph buffer dan ph hidrolisis garam -Memberikan contoh-contoh soal Estimasi Waktu Metode Media Sumber Bahan/ Referensi 10 menit Ceramah 70 menit Ceramah, diskusi informasi, Tanya LCD 1, a, b 1, a, b, c,d,e Penutup Memberikan rangkuman materi, 15 menit Diskusi, tanya 1,a,b,c,d,e
13 Tindak Lanjut memberikan soal untuk tugas di rumah Memerintahkan peserta didik untuk membaca diktat Kimia Dasar Untuk Biologi dan mengerjakan tugas di rumah 5 menit Tanya 1 9. Evaluasi Untuk memperdalam pemahaman anda mengenai materi di atas, kerjakanlah latihan berikut: 1. a. Apa yang dimaksud dengan asam-basa menurut Arrhenius? b. Berikan contoh asam-basa yang ada dalam kehidupan sehari-hari! c. Berikan ciri-ciri sifat asam dan basa! 2. a. Berapa daerah ph larutan yang bersifat asam, basa, dan netral? b. Jelaskan apa yang dimaksud dengan asam monoprotik, diprotik, dan triprotik? 3. Hitunglah ph larutan jika 50 cm 3 NH 3 (aq) 0,03 M (K b =10-5 ) dicampurkan dengan 100 cm 3 HCl 0,01 M. 4. Hitung ph larutan apabila 8,2 gram natrium asetat dilarutkan dalam air menjadi 100 ml larutan, jika K a asam asetat= 1,8 x Mengetahui, Ketua Jurusan Pendidikan Kimia FMIPA UNY Yogyakarta, Februari 2013 Dosen Dr. Hari Sutrisno Susila Kristianingrum, M.Si NIP NIP
14 UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MIPA RENCANA PELAKSANAAN PEMBELAJARAN RPP/BIC291 / Februari Fakultas/Progran Studi : MIPA/ Biologi & Pendidikan Biologi 2. Mata kuliah & Kode : Kimia Dasar /BIC Jumlah sks : Teori 2 sks. 4. Semester dan Waktu : 1,Waktu 2 x 50 menit 5. Kompetensi Dasar : Memahami konsep laju reaksi dan faktor-faktor yang mempengaruhinya 6. Indikator Ketercapaian : Dapat menjelaskan pengertian laju reaksi, menyebutkan faktor-faktor yang mempengaruhinya, serta perbedaan pengaruh konsentrasi, suhu, dan katalisator terhadap laju reaksi. 7. Materi Pokok/Penggalan Materi: Kinetika Kimia bag Kegiatan Perkuliahan : Komponen Langkah Uraian Kegiatan Pendahuluan Memberi salam, memotivasi peserta didik, dan memberikan apersepsi tentang laju reaksi Penyajian -Menjelaskan (Inti) pengertian laju reaksi, faktorfaktor yang mempengaruhinya, serta perbedaan pengaruh konsentrasi, suhu, dan katalisator terhadap laju reaksi, -Menjelaskan hukum laju -Memberikan Estimasi Waktu Metode Media Sumber Bahan/ Referensi 10 menit Ceramah 70 menit Ceramah, diskusi informasi, Tanya LCD 1, a, b 1, a, b, c,d,e
15 contoh soal-soal terkait dengan laju reaksi Penutup Tindak Lanjut Memberikan rangkuman materi, memberikan soal untuk tugas di rumah Memerintahkan peserta didik untuk membaca diktat Kimia Dasar Untuk Biologi dan mengerjakan tugas di rumah 15 menit Diskusi, tanya 5 menit Tanya 1,a,b,c,d,e 1 9. Evaluasi Untuk memperdalam pemahaman anda mengenai materi di atas, kerjakanlah latihan berikut: 1. Jelaskan pengertian laju reaksi, dan persamaan matematisnya secara umum. 2. Jelaskan perbedaan pengaruh konsentrasi, suhu, dan katalisator terhadap laju reaksi. 3. Jelaskan maksud katalisator dapat mempercepat reaksi tetapi tidak ikut bereaksi. Mengetahui, Ketua Jurusan Pendidikan Kimia FMIPA UNY Yogyakarta, Februari 2013 Dosen Dr. Hari Sutrisno Susila Kristianingrum, M.Si NIP NIP
16 UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MIPA RENCANA PELAKSANAAN PEMBELAJARAN RPP/BIC291 / Februari Fakultas/Progran Studi : MIPA/ Biologi & Pendidikan Biologi 2. Mata kuliah & Kode : Kimia Dasar /BIC Jumlah sks : Teori 2 sks. 4. Semester dan Waktu : 1,Waktu 2 x 50 menit 5. Kompetensi Dasar : Memahami konsep laju reaksi dan menentukan orde reaksi serta konstanta laju reaksi 6. Indikator Ketercapaian : Dapat menentukan orde reaksi dan konstanta laju reaksi. 7. Materi Pokok/Penggalan Materi: Kinetika Kimia bag Kegiatan Perkuliahan : Komponen Langkah Uraian Kegiatan Pendahuluan Memberi salam, memotivasi peserta didik, dan memberikan apersepsi tentang laju reaksi Penyajian -Menjelaskan (Inti) hubungan laju reaksi dg konsentrasi reaktan, harga orde reaksi dan tahap penentu laju reaksi. -Memberikan contoh soal-soal terkait dengan laju reaksi -Menjelaskan tentang energi aktivasi dan teori laju reaksi. Estimasi Waktu Metode Media Sumber Bahan/ Referensi 10 menit Ceramah 70 menit Ceramah, diskusi informasi, Tanya LCD 1, a, b 1, a, b, c,d,e
17 Penutup Tindak Lanjut Memberikan rangkuman materi, memberikan soal untuk tugas di rumah Memerintahkan peserta didik untuk membaca diktat Kimia Dasar Untuk Biologi dan mengerjakan tugas di rumah 15 menit Diskusi, tanya 5 menit Tanya 1,a,b,c,d,e 1 9. Evaluasi Untuk memperdalam pemahaman anda mengenai materi di atas, kerjakanlah latihan berikut: 1.Tentukan persamaan laju reaksi orde dua! 2. Di bawah ini tertera data kinetika: A + B hasil reaksi Eksperimen Konsentrasi awal (mol/l) Laju awal (mol/l.menit) [A] [B] 1 4x x x10-2 5x10-3 1,5x x x10-6 a. Tulis definisi orde reaksi b. Tulis definisi tetapan laju reaksi c. Hitung orde reaksi terhadap A d. Hitung orde reaksi terhadap B e. Hitung tetapan laju reaksinya f. Tuliskan satuan tetapan laju Mengetahui, Ketua Jurusan Pendidikan Kimia FMIPA UNY Yogyakarta, Februari 2013 Dosen Dr. Hari Sutrisno Susila Kristianingrum, M.Si NIP NIP
18 UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MIPA RENCANA PELAKSANAAN PEMBELAJARAN RPP/BIC291 / Februari Fakultas/Progran Studi : MIPA/ Biologi & Pendidikan Biologi 2. Mata kuliah & Kode : Kimia Dasar /BIC Jumlah sks : Teori 2 sks. 4. Semester dan Waktu : 1,Waktu 2 x 50 menit 5. Kompetensi Dasar : Memahami konsep termokimia 6. Indikator Ketercapaian : Dapat menyelesaikan soal-soal terkait dengan termokimia 7. Materi Pokok/Penggalan Materi: Termokimia bag Kegiatan Perkuliahan : Komponen Langkah Uraian Kegiatan Pendahuluan Memberi salam, memotivasi peserta didik, dan memberikan apersepsi tentang termokimia Penyajian -Menjelaskan (Inti) tentang entalpi reaksi, entropi -Memberikan contoh soal-soal terkait dengan entalpi reaksi Estimasi Waktu Metode Media Sumber Bahan/ Referensi 10 menit Ceramah 70 menit Ceramah, diskusi informasi, Tanya LCD 1, a, b 1, a, b, c,d,e Penutup Memberikan rangkuman materi, 15 menit Diskusi, tanya 1,a,b,c,d,e memberikan soal untuk tugas di rumah Tindak Memerintahkan 5 menit Tanya 1
19 Lanjut peserta didik untuk membaca diktat Kimia Dasar Untuk Biologi dan mengerjakan tugas di rumah 9. Evaluasi Untuk memperdalam pemahaman anda mengenai materi di atas, kerjakanlah latihan berikut: 1. Jelaskan pengertian tentang entalpi reaksi 2. Jelaskan pengertian tentang entropi reaksi 3. Apa yang dimaksud dengan entalpi pembentukan stándar Mengetahui, Ketua Jurusan Pendidikan Kimia FMIPA UNY Yogyakarta, Februari 2013 Dosen Dr. Hari Sutrisno Susila Kristianingrum, M.Si NIP NIP
20 UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MIPA RENCANA PELAKSANAAN PEMBELAJARAN RPP/BIC291 / Februari Fakultas/Progran Studi : MIPA/ Biologi & Pendidikan Biologi 2. Mata kuliah & Kode : Kimia Dasar /BIC Jumlah sks : Teori 2 sks. 4. Semester dan Waktu : 1,Waktu 2 x 50 menit 5. Kompetensi Dasar : Memahami konsep termokimia 6. Indikator Ketercapaian : Dapat menyelesaikan soal-soal terkait dengan termokimia 7. Materi Pokok/Penggalan Materi: Termokimia bag Kegiatan Perkuliahan : Komponen Langkah Uraian Kegiatan Pendahuluan Memberi salam, memotivasi peserta didik, dan memberikan apersepsi tentang termokimia Penyajian -Menjelaskan (Inti) tentang entalpi reaksi, entropi, energy bebas Gibbs -Memberikan contoh soal-soal terkait dengan entalpi reaksi Estimasi Waktu Metode Media Sumber Bahan/ Referensi 10 menit Ceramah 70 menit Ceramah, diskusi informasi, Tanya LCD 1, a, b 1, a, b, c,d,e Penutup Memberikan rangkuman materi, 15 menit Diskusi, tanya 1,a,b,c,d,e memberikan soal untuk tugas di rumah Tindak Memerintahkan 5 menit Tanya 1
21 Lanjut peserta didik untuk membaca diktat Kimia Dasar Untuk Biologi dan mengerjakan tugas di rumah 9. Evaluasi Untuk memperdalam pemahaman anda mengenai materi di atas, kerjakanlah latihan berikut: 1.CCl 4 adalah pelarut komersialpenting, dibuat dari reaksi Cl 2 (g) dengan senyawa karbon. Tentukan H o untuk reaksi CS 2 (l) + 3Cl 2 (g) CCl 4 (l) + S 2 Cl 2 (l) jika diberikan data berikut: a. CS 2 (l) + 3O 2 (g) CO 2 (g) + 2 SO 2 (g) H o =-1077 kj/mol b. 2S (s) + Cl 2 (g) S 2 Cl 2 (l) H o =-60,2 kj/mol c. C(s) + 2 Cl 2 (g) CCl 4 (l) H o =-135,4kJ/mol d. S(s) + O 2 (g) SO 2 (g) H o =-269,9kJ/mol e. C(s) + O 2 (g) CO 2 (g) H o =-393,5kJ/mol 2. Gunakan hukum Hess untuk menentukan H o reaksi C 3 H 4 (g) + 2H 2 (g) C 3 H 8 (g) Diketahui bahwa: a. H 2 (g) + 1/2 O 2 (g) H 2 O (l) H o =-285,85 kj/mol b. C 3 H 4 (g) +4 O 2 (g) 3 CO 2 (g)+ 2 H 2 O (l) H o =-1.941kJ/mol c. C 3 H 8 (g) + 5O 2 (g) 3 CO 2 (g) + 4 H 2 O (l) H o =-2.220kJ/mol Mengetahui, Ketua Jurusan Pendidikan Kimia FMIPA UNY Yogyakarta, Februari 2013 Dosen Dr. Hari Sutrisno Susila Kristianingrum, M.Si NIP NIP
22 UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MIPA RENCANA PELAKSANAAN PEMBELAJARAN RPP/BIC291 / Februari Fakultas/Progran Studi : MIPA/ Biologi & Pendidikan Biologi 2. Mata kuliah & Kode : Kimia Dasar /BIC Jumlah sks : Teori 2 sks. 4. Semester dan Waktu : 1,Waktu 2 x 50 menit 5. Kompetensi Dasar : Memahami konsep kimia inti dan radiokimia 6. Indikator Ketercapaian : Dapat menjelaskan perbedaan isotop, isobar, isoton dan isomer; kriteria kestabilan inti, peluruhan radioaktif. 7. Materi Pokok/Penggalan Materi: Kimia Inti dan Radiokimia bag.1 8. Kegiatan Perkuliahan : Komponen Langkah Uraian Kegiatan Pendahuluan Memberi salam, memotivasi peserta didik, dan memberikan apersepsi tentang kimia inti dan radiokimia Penyajian -Menjelaskan (Inti) pengertian kimia inti & radiokimia, isotop, isobar, isoton, isomer, kriteria kestabilan inti -Memberikan contoh tentang isotop, isobar, isoton, dan isomer. -Menjelaskan tentang peluruhan radioaktif yang terjadi dari suatu Estimasi Waktu Metode Media Sumber Bahan/ Referensi 10 menit Ceramah 70 menit Ceramah, diskusi informasi, Tanya LCD 1, a, b 1, a, b, c,d,e
23 nuklida -Menjelaskan kegunaan unsur radioaktif Penutup Tindak Lanjut Memberikan rangkuman materi, memberikan soal untuk tugas di rumah Memerintahkan peserta didik untuk membaca diktat Kimia Dasar Untuk Biologi dan mengerjakan tugas di rumah 15 menit Diskusi, tanya 5 menit Tanya 1,a,b,c,d,e 1 9. Evaluasi Untuk memperdalam pemahaman anda mengenai materi di atas, kerjakanlah latihan berikut: 1. Jelaskan perbedaan antara isotop, isobar, isoton dan isomer. 2. Berikan contoh isotop, isobar, isoton dan isomer. 3. Berikan contoh kegunaan unsur radioaktif sebagai perunut. 4. Jelaskan kriteria kestabilan inti yang anda ketahui secara ringkas. Mengetahui, Ketua Jurusan Pendidikan Kimia FMIPA UNY Yogyakarta, Februari 2013 Dosen Dr. Hari Sutrisno Susila Kristianingrum, M.Si NIP NIP
24 UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MIPA RENCANA PELAKSANAAN PEMBELAJARAN RPP/BIC291 / Februari Fakultas/Progran Studi : MIPA/ Biologi & Pendidikan Biologi 2. Mata kuliah & Kode : Kimia Dasar /BIC Jumlah sks : Teori 2 sks. 4. Semester dan Waktu : 1,Waktu 2 x 50 menit 5. Kompetensi Dasar : Memahami konsep kimia inti dan radiokimia 6. Indikator Ketercapaian : Dapat menghitung energi pengikat inti dari suatu nuklida, menjelaskan jenis-jenis reaksi inti, dan aspek kinetikanya 7. Materi Pokok/Penggalan Materi:Kimia Inti dan Radiokimia bag.2 8. Kegiatan Perkuliahan : Komponen Langkah Uraian Kegiatan Pendahuluan Memberi salam, memotivasi peserta didik, dan memberikan apersepsi tentang kimia inti dan radiokimia Penyajian -Menjelaskan (Inti) tentang energi pengikat inti dari suatu nuklida -Menjelaskan jenis-jenis reaksi inti dan aspek kinetikanya. -Memberikan contoh soal-soal terkait energi pengikat inti Estimasi Waktu Metode Media Sumber Bahan/ Referensi 10 menit Ceramah 70 menit Ceramah, diskusi informasi, Tanya LCD 1, a, b 1, a, b, c,d,e Penutup Memberikan 15 menit Diskusi, 1,a,b,c,d,e
25 Tindak Lanjut rangkuman materi, memberikan soal untuk tugas di rumah Memerintahkan peserta didik untuk membaca diktat Kimia Dasar Untuk Biologi dan mengerjakan tugas di rumah tanya 5 menit Tanya 1 9. Evaluasi Untuk memperdalam pemahaman anda mengenai materi di atas, kerjakanlah latihan berikut: 1. Hitung energi pengikat inti per nukleon dari isotop 40 K dalam Joule, bila massa 1 proton dan 1 netron berturut-turut sebesar dan 1,00866 sma, serta massa 1 atom K sebesar 39,10 sma. 19 1,0078 sma 2. Suatu cuplikan 90 Sr mula-mula mempunyai keaktifan 0,600 mci. 38 Hitung keaktifannya setelah cuplikan tersebut disimpan mulai dari tanggal 20 Mei sampai 31 Mei 1999 pada jam yang sama, bila waktu paruhnya 20 jam. Mengetahui, Ketua Jurusan Pendidikan Kimia FMIPA UNY Yogyakarta, Februari 2013 Dosen Dr. Hari Sutrisno Susila Kristianingrum, M.Si NIP NIP
26 UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MIPA RENCANA PELAKSANAAN PEMBELAJARAN RPP/BIC291 / Februari Fakultas/Progran Studi : MIPA/ Biologi & Pendidikan Biologi 2. Mata kuliah & Kode : Kimia Dasar /BIC Jumlah sks : Teori 2 sks. 4. Semester dan Waktu : 1,Waktu 2 x 50 menit 5. Kompetensi Dasar : Memahami konsep kimia organik & biokimia 6. Indikator Ketercapaian : Dapat menjelaskan gugus fungsional, tata nama senyawa karbon, jenis isomer dan jenis reaksi senyawa karbon 7. Materi Pokok/Penggalan Materi:Kimia Organik & Biokimia bag.1 8. Kegiatan Perkuliahan : Komponen Langkah Uraian Kegiatan Pendahuluan Memberi salam, memotivasi peserta didik, dan memberikan apersepsi tentang Kimia Organik & Biokimia Penyajian -Menjelaskan (Inti) tentang klasifikasi senyawa karbon -Menjelaskan jenis-jenis gugus fungsional, tata nama senyawa karbon, jenis isomer senyawa karbon. -Memberikan contoh reaksi senyawa karbon Estimasi Waktu Metode Media Sumber Bahan/ Referensi 10 menit Ceramah 70 menit Ceramah, diskusi informasi, Tanya LCD 1, a, b 1, a, b, c,d,e Penutup Memberikan 15 menit Diskusi, 1,a,b,c,d,e
27 Tindak Lanjut rangkuman materi, memberikan soal untuk tugas di rumah Memerintahkan peserta didik untuk membaca diktat Kimia Dasar Untuk Biologi dan mengerjakan tugas di rumah tanya 5 menit Tanya 1 9. Evaluasi Untuk memperdalam pemahaman anda mengenai materi di atas, kerjakanlah latihan berikut: 1. Apa yang dimaksud dengan gugus fungsional? 2. Tunjukkan gugus fungsional untuk eter, ester, alkohol, aldehida, dan asam karboksilat. 3. Sebutkan nama yang tepat untuk senyawa berikut: CH 3 CH 3 --CH---CH-CH 2 --C-CH 2 -CH 3 C 2 H 5 CH 3 C 2 H 5 4. Tunjukkan jenis isomer antara pasangan senyawa berikut ini: a. C-C-C=C dengan C-C=C-C b. C-C-C-OH dengan C-C-O-C Mengetahui, Ketua Jurusan Pendidikan Kimia FMIPA UNY Yogyakarta, Februari 2013 Dosen Dr. Hari Sutrisno Susila Kristianingrum, M.Si NIP NIP
28 UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MIPA RENCANA PELAKSANAAN PEMBELAJARAN RPP/BIC291 / Februari Fakultas/Progran Studi : MIPA/ Biologi & Pendidikan Biologi 2. Mata kuliah & Kode : Kimia Dasar /BIC Jumlah sks : Teori 2 sks. 4. Semester dan Waktu : 1,Waktu 2 x 50 menit 5. Kompetensi Dasar : Memahami konsep kimia organik & biokimia 6. Indikator Ketercapaian : Dapat menjelaskan Pengertian karbohidrat, lemak, protein dan klasifikasinya serta ujinya 7. Materi Pokok/Penggalan Materi:Kimia Organik & Biokimia bag.2 8. Kegiatan Perkuliahan : Komponen Langkah Uraian Kegiatan Pendahuluan Memberi salam, memotivasi peserta didik, dan memberikan apersepsi tentang Kimia Organik & Biokimia Penyajian -Menjelaskan (Inti) pengertian dari karbohidrat, lemak, dan protein. -Menjelaskan tentang klasifikasi karbohidrat, lemak, dan protein -Memberikan contoh karbohidrat, lemak dan protein. -Menjelaskan uji/test adanya karbohidrat, lemak, dan protein Estimasi Waktu Metode Media Sumber Bahan/ Referensi 10 menit Ceramah 70 menit Ceramah, diskusi informasi, Tanya LCD 1, a, b 1, a, b, c,d,e
29 Penutup Tindak Lanjut Memberikan rangkuman materi, memberikan soal untuk tugas di rumah Memerintahkan peserta didik untuk membaca diktat Kimia Dasar Untuk Biologi dan mengerjakan tugas di rumah 15 menit Diskusi, tanya 5 menit Tanya 1,a,b,c,d,e 1 9. Evaluasi Untuk memperdalam pemahaman anda mengenai materi di atas, kerjakanlah latihan berikut: 1. Jelaskan apa yang dimaksud dengan: a. Karbohidrat b. Lemak c. Protein 2. Jelaskan apa yang dimaksud dengan: a. Monosakarida b. Disakarida c. Polisakarida 3. Berikan contohnya masing-masing 3 buah. 4. Jelaskan bagaimana uji untuk membedakan antara monosakarida dan disakarida. 5. Sebutkan ciri utama dari molekul protein Mengetahui, Ketua Jurusan Pendidikan Kimia FMIPA UNY Yogyakarta, Februari 2013 Dosen Dr. Hari Sutrisno Susila Kristianingrum, M.Si NIP NIP
UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM SILABUS
 UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM SILABUS I. Fakultas : Matematika dan Ilmu Pengetahuan Alam Program Studi : Kimia Mata Kuliah : Kimia Umum Semester : 1 Dosen
UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM SILABUS I. Fakultas : Matematika dan Ilmu Pengetahuan Alam Program Studi : Kimia Mata Kuliah : Kimia Umum Semester : 1 Dosen
UNIVERSITAS NEGERI YOGYAKARTA F A K U L T A S M I P A
 RPP/KIC202/01 2. Mata Kuliah & Kode : Kimia Dasar 2 Kode : KIC 202 5 Kompetensi Dasar : Mahasiswa mampu menjelaskan sifat-sifat larutan mencakup derajat keasaman, terjadinya hidrolisis dan larutan buffer,
RPP/KIC202/01 2. Mata Kuliah & Kode : Kimia Dasar 2 Kode : KIC 202 5 Kompetensi Dasar : Mahasiswa mampu menjelaskan sifat-sifat larutan mencakup derajat keasaman, terjadinya hidrolisis dan larutan buffer,
UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM SILABUS
 UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM SILABUS I. Fakultas : Matematika Ilmu Pengetahuan Alam Program Studi : Kimia Mata Kuliah : Kimia I Semester : 1 Dosen : Dini
UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM SILABUS I. Fakultas : Matematika Ilmu Pengetahuan Alam Program Studi : Kimia Mata Kuliah : Kimia I Semester : 1 Dosen : Dini
 TRY OUT SELEKSI OLIMPIADE TINGKAT KABUPATEN/KOTA 2010 TIM OLIMPIADE KIMIA INDONESIA 2011 Waktu: 150 Menit PUSAT KLINIK PENDIDIKAN INDONESIA (PKPI) bekerjasama dengan LEMBAGA BIMBINGAN BELAJAR SSCIntersolusi
TRY OUT SELEKSI OLIMPIADE TINGKAT KABUPATEN/KOTA 2010 TIM OLIMPIADE KIMIA INDONESIA 2011 Waktu: 150 Menit PUSAT KLINIK PENDIDIKAN INDONESIA (PKPI) bekerjasama dengan LEMBAGA BIMBINGAN BELAJAR SSCIntersolusi
kimia ASAM-BASA III Tujuan Pembelajaran
 KTSP K-13 kimia K e l a s XI ASAM-BASA III Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami mekanisme reaksi asam-basa. 2. Memahami stoikiometri
KTSP K-13 kimia K e l a s XI ASAM-BASA III Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami mekanisme reaksi asam-basa. 2. Memahami stoikiometri
Hukum Dasar Ilmu Kimia Sumber :
 A Hukum Kekekalan Massa (Hukum Lavoisier) Hukum Dasar Ilmu Kimia Sumber : wwwe-dukasinet Pernahkah Anda memperhatikan sepotong besi yang dibiarkan di udara terbuka, dan pada suatu waktu kita akan menemukan,
A Hukum Kekekalan Massa (Hukum Lavoisier) Hukum Dasar Ilmu Kimia Sumber : wwwe-dukasinet Pernahkah Anda memperhatikan sepotong besi yang dibiarkan di udara terbuka, dan pada suatu waktu kita akan menemukan,
AMALDO FIRJARAHADI TANE
 DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN UTUL UGM KIMIA 2015 Page 1 1. MATERI: STOIKIOMETRI Persen massa adalah persentase massa zat terlarut dalam 100 gram massa larutan (massa pelarut + massa
DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN UTUL UGM KIMIA 2015 Page 1 1. MATERI: STOIKIOMETRI Persen massa adalah persentase massa zat terlarut dalam 100 gram massa larutan (massa pelarut + massa
PEMBAHASAN SBMPTN KIMIA 2016
 PEMBAHASAN SBMPTN KIMIA 2016 DISUSUN OLEH Amaldo Firjarahadi Tane 1 31. 32. MATERI: SISTEM PERIODIK UNSUR Energi pengionan disebut juga energi ionisasi. Setiap unsur bisa mengalami energi ionisasi berkali-kali,
PEMBAHASAN SBMPTN KIMIA 2016 DISUSUN OLEH Amaldo Firjarahadi Tane 1 31. 32. MATERI: SISTEM PERIODIK UNSUR Energi pengionan disebut juga energi ionisasi. Setiap unsur bisa mengalami energi ionisasi berkali-kali,
Stoikhiometri : dan metron = mengukur. Membahas tentang : senyawa) senyawa (stoikhiometri. (stoikhiometri. reaksi)
 STOIKHIOMETRI Stoikhiometri : Dari kata Stoicheion = unsur dan metron = mengukur Membahas tentang : hub massa antar unsur dalam suatu senyawa (stoikhiometri senyawa) dan antar zat dalam suatu reaksi (stoikhiometri
STOIKHIOMETRI Stoikhiometri : Dari kata Stoicheion = unsur dan metron = mengukur Membahas tentang : hub massa antar unsur dalam suatu senyawa (stoikhiometri senyawa) dan antar zat dalam suatu reaksi (stoikhiometri
LEMBAR SOAL. Mata pelajaran : Kimia. Kelas/Program : XI/IPA Hari, tanggal : Selasa, 8 April 2008 Alokasi waktu : 90 Menit
 DEPARTEMEN PENDIDIKAN NASIONAL UNIVERSITAS NEGERI SEMARANG FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM JURUSAN KIMIA Gedung D6. Kampus Sekaran Gunungpati Semarang 50229 Telp. 8508035 LEMBAR SOAL Mata
DEPARTEMEN PENDIDIKAN NASIONAL UNIVERSITAS NEGERI SEMARANG FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM JURUSAN KIMIA Gedung D6. Kampus Sekaran Gunungpati Semarang 50229 Telp. 8508035 LEMBAR SOAL Mata
Wardaya College IKATAN KIMIA STOIKIOMETRI TERMOKIMIA CHEMISTRY. Part III. Summer Olympiad Camp Kimia SMA
 Part I IKATAN KIMIA CHEMISTRY Summer Olympiad Camp 2017 - Kimia SMA 1. Untuk menggambarkan ikatan yang terjadi dalam suatu molekul kita menggunakan struktur Lewis atau 'dot and cross' (a) Tuliskan formula
Part I IKATAN KIMIA CHEMISTRY Summer Olympiad Camp 2017 - Kimia SMA 1. Untuk menggambarkan ikatan yang terjadi dalam suatu molekul kita menggunakan struktur Lewis atau 'dot and cross' (a) Tuliskan formula
TERMOKIMIA. Hukum Hess Perubahan entalpi reaksi tetap sama, baik berlangsung dalam satu tahap maupun beberapa tahap.
 TERMOKIMIA (Teori) Entalpi adalah jumlah total energi kalor yang terkandung dalam suatu materi Reaksi Eksoterm Menghasilkan kalor Melepas energi Perubahan entalpi negatif Reaksi Endoterm Menyerap kalor
TERMOKIMIA (Teori) Entalpi adalah jumlah total energi kalor yang terkandung dalam suatu materi Reaksi Eksoterm Menghasilkan kalor Melepas energi Perubahan entalpi negatif Reaksi Endoterm Menyerap kalor
UNIVERSITAS NEGERI YOGYAKARTA F A K U L T A S M I P A
 UNIVERSITAS NEGERI YOGYAKARTA F A K U L T A S M I P A SILABI SIL/KIC104/01 18 Februari 2011 Fakultas : Matematika dan Ilmu Pengetahuan Alam Program Studi : Kimia Mata kuliah : Kode : KIC104 SKS : 1 SKS
UNIVERSITAS NEGERI YOGYAKARTA F A K U L T A S M I P A SILABI SIL/KIC104/01 18 Februari 2011 Fakultas : Matematika dan Ilmu Pengetahuan Alam Program Studi : Kimia Mata kuliah : Kode : KIC104 SKS : 1 SKS
PEMBAHASAN SBMPTN KIMIA 2016
 PEMBAHASAN SBMPTN KIMIA 2016 DISUSUN OLEH Amaldo Firjarahadi Tane 1 31. 32. MATERI: SISTEM PERIODIK UNSUR Energi pengionan disebut juga energi ionisasi. Setiap unsur bisa mengalami energi ionisasi berkali-kali,
PEMBAHASAN SBMPTN KIMIA 2016 DISUSUN OLEH Amaldo Firjarahadi Tane 1 31. 32. MATERI: SISTEM PERIODIK UNSUR Energi pengionan disebut juga energi ionisasi. Setiap unsur bisa mengalami energi ionisasi berkali-kali,
OLIMPIADE KIMIA INDONESIA
 OLIMPIADE KIMIA INDONESIA OLIMPIADE SAINS NASIONAL SELEKSI KABUPATEN / KOTA UjianTeori Waktu 2 Jam Departemen Pendidikan Nasional Direktorat Jenderal Managemen Pendidikan Dasar dan Menengah Direktorat
OLIMPIADE KIMIA INDONESIA OLIMPIADE SAINS NASIONAL SELEKSI KABUPATEN / KOTA UjianTeori Waktu 2 Jam Departemen Pendidikan Nasional Direktorat Jenderal Managemen Pendidikan Dasar dan Menengah Direktorat
1. Isilah Biodata anda dengan lengkap (di lembar Jawaban) Tulis dengan huruf cetak dan jangan disingkat!
 Petunjuk : 1. Isilah Biodata anda dengan lengkap (di lembar Jawaban) Tulis dengan huruf cetak dan jangan disingkat! 2. Soal Teori ini terdiri dari dua bagian: A. 30 soal pilihan Ganda : 60 poin B. 5 Nomor
Petunjuk : 1. Isilah Biodata anda dengan lengkap (di lembar Jawaban) Tulis dengan huruf cetak dan jangan disingkat! 2. Soal Teori ini terdiri dari dua bagian: A. 30 soal pilihan Ganda : 60 poin B. 5 Nomor
SATUAN ACARA PERKULIAHAN UNIVERSITAS GUNADARMA KIMIA DASAR JURUSAN D3 TEKNIK KOMPUTER
 SATUAN ACARA PERKULIAHAN UNIVERSITAS GUNADARMA KIMIA DASAR JURUSAN D3 TEKNIK KOMPUTER Minggu Ke- Pokok Bahasan dan TIU Sub Pokok Bahasan dan Tujuan Intruksional Khusus Teknik Pembelajaran Media Pembelajaran
SATUAN ACARA PERKULIAHAN UNIVERSITAS GUNADARMA KIMIA DASAR JURUSAN D3 TEKNIK KOMPUTER Minggu Ke- Pokok Bahasan dan TIU Sub Pokok Bahasan dan Tujuan Intruksional Khusus Teknik Pembelajaran Media Pembelajaran
SOAL SELEKSI NASIONAL TAHUN 2006
 SOAL SELEKSI NASIONAL TAHUN 2006 Soal 1 ( 13 poin ) KOEFISIEN REAKSI DAN LARUTAN ELEKTROLIT Koefisien reaksi merupakan langkah penting untuk mengamati proses berlangsungnya reaksi. Lengkapi koefisien reaksi-reaksi
SOAL SELEKSI NASIONAL TAHUN 2006 Soal 1 ( 13 poin ) KOEFISIEN REAKSI DAN LARUTAN ELEKTROLIT Koefisien reaksi merupakan langkah penting untuk mengamati proses berlangsungnya reaksi. Lengkapi koefisien reaksi-reaksi
OAL TES SEMESTER I. I. Pilihlah jawaban yang paling tepat! a. 2d d. 3p b. 2p e. 3s c. 3d 6. Unsur X dengan nomor atom
 KIMIA XI SMA 3 S OAL TES SEMESTER I I. Pilihlah jawaban yang paling tepat!. Elektron dengan bilangan kuantum yang tidak diizinkan n = 3, l = 0, m = 0, s = - / n = 3, l =, m =, s = / c. n = 3, l =, m =
KIMIA XI SMA 3 S OAL TES SEMESTER I I. Pilihlah jawaban yang paling tepat!. Elektron dengan bilangan kuantum yang tidak diizinkan n = 3, l = 0, m = 0, s = - / n = 3, l =, m =, s = / c. n = 3, l =, m =
Hukum Dasar Kimia Dan Konsep Mol
 A. PENDAHULUAN Hukum Dasar Kimia Dan Konsep Mol Hukum dasar kimia merupakan hukum dasar yang digunakan dalam stoikiometri (perhitungan kimia), antara lain: 1) Hukum Lavoisier atau hukum kekekalan massa.
A. PENDAHULUAN Hukum Dasar Kimia Dan Konsep Mol Hukum dasar kimia merupakan hukum dasar yang digunakan dalam stoikiometri (perhitungan kimia), antara lain: 1) Hukum Lavoisier atau hukum kekekalan massa.
SAP-GARIS-GARIS BESAR PROGRAM PENGAJARAN
 SAP-GARIS-GARIS BESAR PROGRAM PENGAJARAN Mata kuliah : Kimia Kode : Kim 101/3(2-3) Deskripsi : Mata kuliah ini membahas konsep-konsep dasar kimia yang disampaikan secara sederhana, meliputi pengertian
SAP-GARIS-GARIS BESAR PROGRAM PENGAJARAN Mata kuliah : Kimia Kode : Kim 101/3(2-3) Deskripsi : Mata kuliah ini membahas konsep-konsep dasar kimia yang disampaikan secara sederhana, meliputi pengertian
Massa atom merupakan massa dari atom dalam satuan massa atom (sma).
 Bab 3 1. Apakah yang dimaksud dengan Ar dan Mr? 2. Apakah yang dimaksud dengan mol? 3. Bagaimana cara mencari mol jika diketahui massa zat, volume (dalam STP), dan jumah molekul/partikelnya? 4. Berapa
Bab 3 1. Apakah yang dimaksud dengan Ar dan Mr? 2. Apakah yang dimaksud dengan mol? 3. Bagaimana cara mencari mol jika diketahui massa zat, volume (dalam STP), dan jumah molekul/partikelnya? 4. Berapa
UNIVERSITAS NEGERI YOGYAKARTA
 RPP 1 KIMIA DASAR 1 1. Fakultas/Program Studi 2. Mata Kuliah/Kode 3. Jumlah SKS 4. Semester dan waktu 5. Kompetensi Dasar 6. Indikator Ketercapaian 7. Materi Pokok/Penggalan Materi MIPA/ Pendidikan IPA
RPP 1 KIMIA DASAR 1 1. Fakultas/Program Studi 2. Mata Kuliah/Kode 3. Jumlah SKS 4. Semester dan waktu 5. Kompetensi Dasar 6. Indikator Ketercapaian 7. Materi Pokok/Penggalan Materi MIPA/ Pendidikan IPA
AMALDO FIRJARAHADI TANE
 DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN UTUL UGM KIMIA 2014 Page 1 1. MATERI: STOIKIOMETRI Reaksi kondensasi berkaitan dengan reaksi pembentukan polimer, di samping ada juga yang mengalami reaksi
DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN UTUL UGM KIMIA 2014 Page 1 1. MATERI: STOIKIOMETRI Reaksi kondensasi berkaitan dengan reaksi pembentukan polimer, di samping ada juga yang mengalami reaksi
D. 2 dan 3 E. 2 dan 5
 1. Pada suhu dan tekanan sama, 40 ml P 2 tepat habis bereaksi dengan 100 ml, Q 2 menghasilkan 40 ml gas PxOy. Harga x dan y adalah... A. 1 dan 2 B. 1 dan 3 C. 1 dan 5 Kunci : E D. 2 dan 3 E. 2 dan 5 Persamaan
1. Pada suhu dan tekanan sama, 40 ml P 2 tepat habis bereaksi dengan 100 ml, Q 2 menghasilkan 40 ml gas PxOy. Harga x dan y adalah... A. 1 dan 2 B. 1 dan 3 C. 1 dan 5 Kunci : E D. 2 dan 3 E. 2 dan 5 Persamaan
Amin Fatoni, M.Si 2008
 Amin Fatoni, M.Si 2008 Massa rumus (Mr) = massa molekul = bobot molekul (BM) merupakan penjumlahan dari massa atom penyusun-penyusunnya Contoh: Air - H 2 O 1 atom Oksigen 2(1.0079 u) + 15.9994 u = 18.0152
Amin Fatoni, M.Si 2008 Massa rumus (Mr) = massa molekul = bobot molekul (BM) merupakan penjumlahan dari massa atom penyusun-penyusunnya Contoh: Air - H 2 O 1 atom Oksigen 2(1.0079 u) + 15.9994 u = 18.0152
OLIMPIADE KIMIA INDONESIA
 OLIMPIADE KIMIA INDONESIA OLIMPIADE SAINS NASIONAL SELEKSI KABUPATEN / KOTA UjianTeori Waktu 2 Jam Departemen Pendidikan Nasional Direktorat Jenderal Managemen Pendidikan Dasar dan Menengah Direktorat
OLIMPIADE KIMIA INDONESIA OLIMPIADE SAINS NASIONAL SELEKSI KABUPATEN / KOTA UjianTeori Waktu 2 Jam Departemen Pendidikan Nasional Direktorat Jenderal Managemen Pendidikan Dasar dan Menengah Direktorat
TERMOKIMIA. STANDART KOMPETENSI; 2. Memahami perubahan energi dalam kimia dan cara pengukuran. ENTALPI DAN PERUBAHANNYA
 TERMOKIMIA STANDART KOMPETENSI; 2. Memahami perubahan energi dalam kimia dan cara pengukuran. ENTALPI DAN PERUBAHANNYA KOMPETENSI DASAR; 2.1. Mendeskripsikan perubahan entalpi suatu reaksi, reaksi eksoterm
TERMOKIMIA STANDART KOMPETENSI; 2. Memahami perubahan energi dalam kimia dan cara pengukuran. ENTALPI DAN PERUBAHANNYA KOMPETENSI DASAR; 2.1. Mendeskripsikan perubahan entalpi suatu reaksi, reaksi eksoterm
Pilihan Ganda Soal dan Jawaban Sifat Koligatif Larutan 20 butir. 5 uraian Soal dan Jawaban Sifat Koligatif Larutan.
 1 Pilihan Ganda Soal dan Jawaban Sifat Koligatif Larutan 20 butir. 5 uraian Soal dan Jawaban Sifat Koligatif Larutan. Berilah tanda silang (X) pada huruf A, B, C, D atau E di depan jawaban yang benar!
1 Pilihan Ganda Soal dan Jawaban Sifat Koligatif Larutan 20 butir. 5 uraian Soal dan Jawaban Sifat Koligatif Larutan. Berilah tanda silang (X) pada huruf A, B, C, D atau E di depan jawaban yang benar!
KIMIA TERAPAN STOIKIOMETRI DAN HUKUM-HUKUM KIMIA Haris Puspito Buwono
 KIMIA TERAPAN STOIKIOMETRI DAN HUKUM-HUKUM KIMIA Haris Puspito Buwono Semester Gasal 2012/2013 STOIKIOMETRI 2 STOIKIOMETRI adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif dari komposisi
KIMIA TERAPAN STOIKIOMETRI DAN HUKUM-HUKUM KIMIA Haris Puspito Buwono Semester Gasal 2012/2013 STOIKIOMETRI 2 STOIKIOMETRI adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif dari komposisi
Struktur atom, dan Tabel periodik unsur,
 KISI-KISI PENULISAN USBN Jenis Sekolah : SMA/MA Mata Pelajaran : KIMIA Kurikulum : 2006 Alokasi Waktu : 120 menit Jumlah : Pilihan Ganda : 35 Essay : 5 1 2 3 1.1. Memahami struktur atom berdasarkan teori
KISI-KISI PENULISAN USBN Jenis Sekolah : SMA/MA Mata Pelajaran : KIMIA Kurikulum : 2006 Alokasi Waktu : 120 menit Jumlah : Pilihan Ganda : 35 Essay : 5 1 2 3 1.1. Memahami struktur atom berdasarkan teori
Siswa diingatkan tentang struktur atom, bilangan kuantum, bentuk-bentuk orbital, dan konfigurasi elektron
 RENCANA PELAKSANAAN PEMBELAJARAN NO: 1 Mata Pelajaran : Kimia Kelas/Semester : XI/1 Materi Pokok : Stuktur atom dan sistem periodik unsur Pertemuan Ke- : 1 dan 2 Alokasi Waktu : 2 x pertemuan (4 x 45 menit)
RENCANA PELAKSANAAN PEMBELAJARAN NO: 1 Mata Pelajaran : Kimia Kelas/Semester : XI/1 Materi Pokok : Stuktur atom dan sistem periodik unsur Pertemuan Ke- : 1 dan 2 Alokasi Waktu : 2 x pertemuan (4 x 45 menit)
Ujian Akhir Semester Mata Pelajaran Kimia Kelas X Wacana berikut digunakan untuk menjawab soal no 1 dan 2. Ditentukan 5 unsur dengan konfigurasi
 Ujian Akhir Semester Mata Pelajaran Kimia Kelas X Wacana berikut digunakan untuk menjawab soal no 1 dan 2. Ditentukan 5 unsur dengan konfigurasi elektron sebagai berikut: P : 2 8 7 S : 2 8 8 Q : 2 8 8
Ujian Akhir Semester Mata Pelajaran Kimia Kelas X Wacana berikut digunakan untuk menjawab soal no 1 dan 2. Ditentukan 5 unsur dengan konfigurasi elektron sebagai berikut: P : 2 8 7 S : 2 8 8 Q : 2 8 8
Stoikiometri. Berasal dari kata Stoicheion (partikel) dan metron (pengukuran). Cara perhitungan dan pengukuran zat serta campuran kimia.
 Stoikiometri Berasal dari kata Stoicheion (partikel) dan metron (pengukuran). Cara perhitungan dan pengukuran zat serta campuran kimia. Bilangan Avogadro Stoikometri: pengukuran kuantitatif sehingga perlu
Stoikiometri Berasal dari kata Stoicheion (partikel) dan metron (pengukuran). Cara perhitungan dan pengukuran zat serta campuran kimia. Bilangan Avogadro Stoikometri: pengukuran kuantitatif sehingga perlu
AMALDO FIRJARAHADI TANE
 DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN UTUL UGM KIMIA 2013 Page 1 1. 2. MATERI: HUKUM-HUKUM DASAR KIMIA Di soal diketahui dan ditanya: m (NH 2 ) 2 CO = 12.000 ton/tahun (pabrik) m N 2 = ton/tahun?
DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN UTUL UGM KIMIA 2013 Page 1 1. 2. MATERI: HUKUM-HUKUM DASAR KIMIA Di soal diketahui dan ditanya: m (NH 2 ) 2 CO = 12.000 ton/tahun (pabrik) m N 2 = ton/tahun?
AMALDO FIRJARAHADI TANE
 DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN UTUL UGM KIMIA 2013 Page 1 1. 2. MATERI: TERMOKIMIA Pada soal diketahui dan ditanya: ΔH c C 2 H 5 OH = -1380 kj/mol ΔH d C 6 H 12 O 6 = -60 kj/mol ΔH c C
DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN UTUL UGM KIMIA 2013 Page 1 1. 2. MATERI: TERMOKIMIA Pada soal diketahui dan ditanya: ΔH c C 2 H 5 OH = -1380 kj/mol ΔH d C 6 H 12 O 6 = -60 kj/mol ΔH c C
PEMBAHASAN SBMPTN KIMIA 2016
 PEMBAHASAN SBMPTN KIMIA 2016 DISUSUN OLEH Amaldo Firjarahadi Tane 1 31. 32. MATERI: SISTEM PERIODIK UNSUR Energi pengionan disebut juga energi ionisasi. Setiap unsur bisa mengalami energi ionisasi berkali-kali,
PEMBAHASAN SBMPTN KIMIA 2016 DISUSUN OLEH Amaldo Firjarahadi Tane 1 31. 32. MATERI: SISTEM PERIODIK UNSUR Energi pengionan disebut juga energi ionisasi. Setiap unsur bisa mengalami energi ionisasi berkali-kali,
KEMENTERIAN RISET, TEKNOLOGI DAN PENDIDIKAN TINGGI UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
 KEMENTERIAN RISET, TEKNOLOGI DAN PENDIDIKAN TINGGI UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM RENCANA PEMBELAJARAN SEMESTER Program Studi : Pendidikan IPA Nama Mata Kuliah
KEMENTERIAN RISET, TEKNOLOGI DAN PENDIDIKAN TINGGI UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM RENCANA PEMBELAJARAN SEMESTER Program Studi : Pendidikan IPA Nama Mata Kuliah
KONSEP MOL DAN STOIKIOMETRI
 KONSEP MOL DAN STOIKIOMETRI HUKUM-HUKUM DASAR KIMIA 1. Asas Lavoiser atau kekekalan massa jumlah sebelum dan setelah reaksi kimia adalah tetap 2. Hukum Gas Ideal P V = nrt Dengan P adalah tekanan (atm),
KONSEP MOL DAN STOIKIOMETRI HUKUM-HUKUM DASAR KIMIA 1. Asas Lavoiser atau kekekalan massa jumlah sebelum dan setelah reaksi kimia adalah tetap 2. Hukum Gas Ideal P V = nrt Dengan P adalah tekanan (atm),
KISI-KISI UN KIMIA SMA/MA
 KISI-KISI UN KIMIA SMA/MA 2015-2016 Siswa mampu memahami, menguasai pengetahuan/ mengaplikasikan pengetahuan/ menggunakan nalar dalam hal: Struktur Atom Sistem Periodik Unsur Ikatan Kimia (Jenis Ikatan)
KISI-KISI UN KIMIA SMA/MA 2015-2016 Siswa mampu memahami, menguasai pengetahuan/ mengaplikasikan pengetahuan/ menggunakan nalar dalam hal: Struktur Atom Sistem Periodik Unsur Ikatan Kimia (Jenis Ikatan)
KISI KISI SOAL UJIAN SEKOLAH SMK SE-KABUPATEN CIAMIS TP. 2013/2014
 Mata Pelajaran : KIMIA KISI KISI UJIAN SEKOLAH SMK SE-KABUPATEN CIAMIS TP. 2013/2014 TINGKAT 1 Memahami konsep materi dan perubahannya Pengertian perubahan Kimia dan Fisika dijelaskan melalui contoh-contoh
Mata Pelajaran : KIMIA KISI KISI UJIAN SEKOLAH SMK SE-KABUPATEN CIAMIS TP. 2013/2014 TINGKAT 1 Memahami konsep materi dan perubahannya Pengertian perubahan Kimia dan Fisika dijelaskan melalui contoh-contoh
PAKET UJIAN NASIONAL 17 Pelajaran : KIMIA Waktu : 120 Menit
 PAKET UJIAN NASIONAL 17 Pelajaran : KIMIA Waktu : 120 Menit Pilihlah salah satu jawaban yang tepat! Jangan lupa Berdoa dan memulai dari yang mudah. 01. Diketahui ion X 3+ mempunyai 10 elektron dan 14 neutron.
PAKET UJIAN NASIONAL 17 Pelajaran : KIMIA Waktu : 120 Menit Pilihlah salah satu jawaban yang tepat! Jangan lupa Berdoa dan memulai dari yang mudah. 01. Diketahui ion X 3+ mempunyai 10 elektron dan 14 neutron.
Wardaya College. Tes Simulasi Ujian Nasional SMA Berbasis Komputer. Mata Pelajaran Kimia Tahun Ajaran 2017/2018. Departemen Kimia - Wardaya College
 Tes Simulasi Ujian Nasional SMA Berbasis Komputer Mata Pelajaran Kimia Tahun Ajaran 2017/2018-1. Sebuah unsur X memiliki no massa 52 dan jumlah neutron sebesar 28. Kongurasi elektron dari ion X + adalah...
Tes Simulasi Ujian Nasional SMA Berbasis Komputer Mata Pelajaran Kimia Tahun Ajaran 2017/2018-1. Sebuah unsur X memiliki no massa 52 dan jumlah neutron sebesar 28. Kongurasi elektron dari ion X + adalah...
KISI-KISI PENULISAN SOAL USBN
 KISI-KISI PENULISAN USBN Jenis Sekolah : SMA/MA Mata Pelajaran : KIMIA Kurikulum : 2013 Alokasi Waktu : 120 menit Jumlah : Pilihan Ganda : 35 Essay : 5 1 2 3 4 3.4 Menganalisis hubungan konfigurasi elektron
KISI-KISI PENULISAN USBN Jenis Sekolah : SMA/MA Mata Pelajaran : KIMIA Kurikulum : 2013 Alokasi Waktu : 120 menit Jumlah : Pilihan Ganda : 35 Essay : 5 1 2 3 4 3.4 Menganalisis hubungan konfigurasi elektron
SATUAN ACARA PERKULIAHAN MATA KULIAH KIMIA DASAR (KD) KODE / SKS : KD / 3 SKS
 1 1 Pada akhir pokok bahasan ini mahasiswa diharapkan dapat : 1 Memahami pengertian materi, penggolongannya dan hal-hal yang menyangkut materi dan perubahannya sebagai dasar dalam mempelajari kimia Setelah
1 1 Pada akhir pokok bahasan ini mahasiswa diharapkan dapat : 1 Memahami pengertian materi, penggolongannya dan hal-hal yang menyangkut materi dan perubahannya sebagai dasar dalam mempelajari kimia Setelah
OLIMPIADE SAINS NASIONAL 2012 SELEKSI KABUPATEN / KOTA SOAL. UjianTeori. Waktu: 100 menit
 OLIMPIADE SAINS NASIONAL 2012 SELEKSI KABUPATEN / KOTA SOAL UjianTeori Waktu: 100 menit Kementerian Pendidikan dan Kebudayaan Direktorat Jenderal Pendidikan Menengah Direktorat Pembinaan Sekolah Menengah
OLIMPIADE SAINS NASIONAL 2012 SELEKSI KABUPATEN / KOTA SOAL UjianTeori Waktu: 100 menit Kementerian Pendidikan dan Kebudayaan Direktorat Jenderal Pendidikan Menengah Direktorat Pembinaan Sekolah Menengah
Materi Pokok Bahasan :
 STOIKIOMETRI Kompetensi : Memiliki kemampuan untuk menginterpretasikan serta menerapkan dalam perhitungan kimia. Memiliki kemampuan untuk mengaplikasikan pengetahuan yang dimilikinya dan terbiasa menggunakan
STOIKIOMETRI Kompetensi : Memiliki kemampuan untuk menginterpretasikan serta menerapkan dalam perhitungan kimia. Memiliki kemampuan untuk mengaplikasikan pengetahuan yang dimilikinya dan terbiasa menggunakan
1s 2 2s 2 2p 6 3s 2 2p 6 3d 4s 1 4p 4d 4f 5s 5p 5d 5f
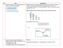 NO SOAL PEMBAHASAN 1 Konfigurasi elekttron ion X - yang memiliki nomor massa 39 dan 21 neutron adalah.. A. 1s2 2s2 2p6 3s2 3p6 4s2 3d1 B. 1s2 2s2 2p6 3s2 3p6 4s1 C. 1s2 2s2 2p6 3s2 3p6 3d1 D. 1s2 2s2 2p6
NO SOAL PEMBAHASAN 1 Konfigurasi elekttron ion X - yang memiliki nomor massa 39 dan 21 neutron adalah.. A. 1s2 2s2 2p6 3s2 3p6 4s2 3d1 B. 1s2 2s2 2p6 3s2 3p6 4s1 C. 1s2 2s2 2p6 3s2 3p6 3d1 D. 1s2 2s2 2p6
D kj/mol E kj/mol
 1. Dari data : 2H 2 (g) + O 2 (g) 2H 2 O (l) H = -571 kj 2Ca (s) + O 2 (g) 2CaO(s) H = -1269 kj CaO (s) + H 2 O (l) Ca(OH)2(s) H = -64 kj Dapat dihitung entalpi pembentukan Ca(OH) 2 (s) sebesar... A. -984
1. Dari data : 2H 2 (g) + O 2 (g) 2H 2 O (l) H = -571 kj 2Ca (s) + O 2 (g) 2CaO(s) H = -1269 kj CaO (s) + H 2 O (l) Ca(OH)2(s) H = -64 kj Dapat dihitung entalpi pembentukan Ca(OH) 2 (s) sebesar... A. -984
STOIKIOMETRI. Massa molekul relatif suatu zat sama dengan jumlah massa atom relatif atomatom penyusun molekul zat tersebut.
 STOIKIOMETRI Istilah STOIKIOMETRI berasal dari kata-kata Yunani yaitu Stoicheion (partikel) dan metron (pengukuran). STOIKIOMETRI akhirnya mengacu kepada cara perhitungan dan pengukuran zat serta campuran
STOIKIOMETRI Istilah STOIKIOMETRI berasal dari kata-kata Yunani yaitu Stoicheion (partikel) dan metron (pengukuran). STOIKIOMETRI akhirnya mengacu kepada cara perhitungan dan pengukuran zat serta campuran
TERMOKIMIA. Kalor reaksi pada pembakaran 1 mol metanol menurut reaksi adalah... CH 3 OH + O 2 CO H 2 O. Penyelesaian : H
 1. Diketahui energi ikatan rata-rata : H - O : 111 kkal.mol -1 C - H : 99 kkal.mol -1 C - O : 85 kkal.mol -1 C = O : 173 kkal.mol -1 O = O : 119 Kkal.mol -1 TERMOKIMIA Kalor reaksi pada pembakaran 1 mol
1. Diketahui energi ikatan rata-rata : H - O : 111 kkal.mol -1 C - H : 99 kkal.mol -1 C - O : 85 kkal.mol -1 C = O : 173 kkal.mol -1 O = O : 119 Kkal.mol -1 TERMOKIMIA Kalor reaksi pada pembakaran 1 mol
UN SMA IPA Kimia. Kode Soal 305
 UN SMA IPA Kimia Kode Soal 305 Doc.name : UNSMAIPAKIM305 Version : 2012-12 halaman 1 1. Di antara hal-hal di bawah ini : 1. besi berpilar 2. pagar di cat 3. belerang meleleh 4. nasi jadi basi 5. bel berdering
UN SMA IPA Kimia Kode Soal 305 Doc.name : UNSMAIPAKIM305 Version : 2012-12 halaman 1 1. Di antara hal-hal di bawah ini : 1. besi berpilar 2. pagar di cat 3. belerang meleleh 4. nasi jadi basi 5. bel berdering
2. Konfigurasi elektron dua buah unsur tidak sebenarnya:
 . Atom X memiliki elektron valensi dengan bilangan kuantum: n =, l =, m = 0, dan s =. Periode dan golongan yang mungkin untuk atom X adalah A. dan IIIB B. dan VA C. 4 dan III B D. 4 dan V B E. 5 dan III
. Atom X memiliki elektron valensi dengan bilangan kuantum: n =, l =, m = 0, dan s =. Periode dan golongan yang mungkin untuk atom X adalah A. dan IIIB B. dan VA C. 4 dan III B D. 4 dan V B E. 5 dan III
SATUAN ACARA PERKULIAHAN MATA KULIAH KIMIA DASAR 1 (ID) KODE / SKS : KD / 2 SKS. Sub Pokok Bahasan Khusus
 1 1. Materi 1.1. Pengertian materi 1.2. Sifat dan perubahan materi 1.3. Klasifikasi materi 1.4. Hukum-hukum yang berhubungan dengan materi Memahami pengertian materi, massa dan gunaan ilmu kimia Memahami
1 1. Materi 1.1. Pengertian materi 1.2. Sifat dan perubahan materi 1.3. Klasifikasi materi 1.4. Hukum-hukum yang berhubungan dengan materi Memahami pengertian materi, massa dan gunaan ilmu kimia Memahami
UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM SILABUS. : 1 : Dini Rohmawati, M.Sc.
 UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM SILABUS Mata Kuliah : Praktikum Kimia Umum Kode/SKS : BIO6104/ 1 Pra-syarat : - Co-syarat : Kimia Umum Semester Pengampu : 1
UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM SILABUS Mata Kuliah : Praktikum Kimia Umum Kode/SKS : BIO6104/ 1 Pra-syarat : - Co-syarat : Kimia Umum Semester Pengampu : 1
Mata Pelajaran : KIMIA Tanggal : - Waktu : 120 MENIT
 PAKET PREDIKSI UJIAN NASINAL SA/A ata Pelajaran : KIIA Tanggal : - Waktu : 0 ENIT PETUNJUK UU Isikan identitas Anda ke dalam Lembar Jawaban Ujian Nasional (LJUN) menggunakan pensil B sesuai petunjuk di
PAKET PREDIKSI UJIAN NASINAL SA/A ata Pelajaran : KIIA Tanggal : - Waktu : 0 ENIT PETUNJUK UU Isikan identitas Anda ke dalam Lembar Jawaban Ujian Nasional (LJUN) menggunakan pensil B sesuai petunjuk di
RENCANA PROGRAM KEGIATAN PERKULIAHAN SEMESTER (RPKPS)
 RENCANA PROGRAM KEGIATAN PERKULIAHAN SEMESTER (RPKPS) Kode / Nama Mata Kuliah : E124106 / Kimia Industri Revisi 4 Satuan Kredit Semester : 2 SKS Tgl revisi : 16 Juli 2015 Jml Jam kuliah dalam seminggu
RENCANA PROGRAM KEGIATAN PERKULIAHAN SEMESTER (RPKPS) Kode / Nama Mata Kuliah : E124106 / Kimia Industri Revisi 4 Satuan Kredit Semester : 2 SKS Tgl revisi : 16 Juli 2015 Jml Jam kuliah dalam seminggu
CH 3 COONa 0,1 M K a CH 3 COOH = 10 5
 Soal No. 1 Dari beberapa larutan berikut ini yang tidak mengalami hidrolisis adalah... A. NH 4 Cl C. K 2 SO 4 D. CH 3 COONa E. CH 3 COOK Yang tidak mengalami peristiwa hidrolisis adalah garam yang berasal
Soal No. 1 Dari beberapa larutan berikut ini yang tidak mengalami hidrolisis adalah... A. NH 4 Cl C. K 2 SO 4 D. CH 3 COONa E. CH 3 COOK Yang tidak mengalami peristiwa hidrolisis adalah garam yang berasal
BAB IV HASIL PENELITIAN DAN PEMBAHASAN. Data-data yang telah dikumpulkan dapat dikaji lebih lanjut untuk dilihat
 32 BAB IV HASIL PENELITIAN DAN PEMBAHASAN 4.1. Hasil Penelitian Data-data yang telah dikumpulkan dapat dikaji lebih lanjut untuk dilihat bagaimana komposisi soal berdasarkan domain kognitif Taksonomi Bloom
32 BAB IV HASIL PENELITIAN DAN PEMBAHASAN 4.1. Hasil Penelitian Data-data yang telah dikumpulkan dapat dikaji lebih lanjut untuk dilihat bagaimana komposisi soal berdasarkan domain kognitif Taksonomi Bloom
Stoikiometri. OLEH Lie Miah
 Stoikiometri OLEH Lie Miah 1 STANDAR KOMPETENSI KOMPETENSI DASAR INDIKATOR KARAKTERISTIK MATERI KESULITAN BELAJAR SISWA STANDAR KOMPETENSI Memahami hukum-hukum dasar Kimia dan penerapannya dalam perhitungan
Stoikiometri OLEH Lie Miah 1 STANDAR KOMPETENSI KOMPETENSI DASAR INDIKATOR KARAKTERISTIK MATERI KESULITAN BELAJAR SISWA STANDAR KOMPETENSI Memahami hukum-hukum dasar Kimia dan penerapannya dalam perhitungan
LAMPIRAN 1. LEMBAR INSTRUMEN WAWANCARA UNTUK GURU KIMIA, DAN GURU KEPERAWATAN TENTANG RELEVANSI MATERI KIMIA TERHADAP MATERI KEPERAWATAN
 LAMPIRAN 1. LEMBAR INSTRUMEN WAWANCARA UNTUK GURU KIMIA, DAN GURU KEPERAWATAN TENTANG RELEVANSI MATERI KIMIA TERHADAP MATERI KEPERAWATAN Pertanyaan 1. Bagaimana pendapat Anda tentang relevansi (kesesuaian)
LAMPIRAN 1. LEMBAR INSTRUMEN WAWANCARA UNTUK GURU KIMIA, DAN GURU KEPERAWATAN TENTANG RELEVANSI MATERI KIMIA TERHADAP MATERI KEPERAWATAN Pertanyaan 1. Bagaimana pendapat Anda tentang relevansi (kesesuaian)
BAB I STOIKHIOMETRI I - 1
 BAB I STOIKHIOMETRI 1.1 PENDAHULUAN Setiap zat, unsur, senyawa dalam kimia mempunyai nama dan rumus uniknya sendiri. Cara tersingkat untuk memerikan suatu reaksi kimia adalah dengan menuliskan rumus untuk
BAB I STOIKHIOMETRI 1.1 PENDAHULUAN Setiap zat, unsur, senyawa dalam kimia mempunyai nama dan rumus uniknya sendiri. Cara tersingkat untuk memerikan suatu reaksi kimia adalah dengan menuliskan rumus untuk
PEMBAHASAN SBMPTN KIMIA 2016
 PEMBAHASAN SBMPTN KIMIA 2016 DISUSUN OLEH Amaldo Firjarahadi Tane 1 31. 32. MATERI: SISTEM PERIODIK UNSUR Energi pengionan disebut juga energi ionisasi. Setiap unsur bisa mengalami energi ionisasi berkali-kali,
PEMBAHASAN SBMPTN KIMIA 2016 DISUSUN OLEH Amaldo Firjarahadi Tane 1 31. 32. MATERI: SISTEM PERIODIK UNSUR Energi pengionan disebut juga energi ionisasi. Setiap unsur bisa mengalami energi ionisasi berkali-kali,
AMALDO FIRJARAHADI TANE
 DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN SBMPTN KIMIA 2017 Page 1 1. 2. MATERI: STRUKTUR ATOM DAN SISTEM PERIODIK UNSUR Ingat, bahwa jumlah neutron suatu unsur dan ionnya bernilai sama, yang membedakannya
DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN SBMPTN KIMIA 2017 Page 1 1. 2. MATERI: STRUKTUR ATOM DAN SISTEM PERIODIK UNSUR Ingat, bahwa jumlah neutron suatu unsur dan ionnya bernilai sama, yang membedakannya
SILABUS MATAKULIAH. Revisi : 4 Tanggal Berlaku : 4 September 2015
 SILABUS MATAKULIAH Revisi : 4 Tanggal Berlaku : 4 September 2015 A. Identitas 1. Nama Matakuliah : Kimia Industri 2. Program Studi : Teknik Industri 3. Fakultas : Teknik 4. Bobot sks : 2 SKS 5. Elemen
SILABUS MATAKULIAH Revisi : 4 Tanggal Berlaku : 4 September 2015 A. Identitas 1. Nama Matakuliah : Kimia Industri 2. Program Studi : Teknik Industri 3. Fakultas : Teknik 4. Bobot sks : 2 SKS 5. Elemen
Kimia Study Center - Contoh soal dan pembahasan tentang hidrolisis larutan garam dan menentukan ph atau poh larutan garam, kimia SMA kelas 11 IPA.
 Kimia Study Center - Contoh soal dan pembahasan tentang hidrolisis larutan garam dan menentukan ph atau poh larutan garam, kimia SMA kelas 11 IPA. Soal No. 1 Dari beberapa larutan berikut ini yang tidak
Kimia Study Center - Contoh soal dan pembahasan tentang hidrolisis larutan garam dan menentukan ph atau poh larutan garam, kimia SMA kelas 11 IPA. Soal No. 1 Dari beberapa larutan berikut ini yang tidak
Bab IV Hukum Dasar Kimia
 Bab IV Hukum Dasar Kimia Sumber: Silberberg, Chemistry :The Molecular Nature of Matter and Change Kalsium karbonat ditemukan pada beberapa bentuk seperti pualam, batu koral, dan kapur. Persen massa unsur-unsur
Bab IV Hukum Dasar Kimia Sumber: Silberberg, Chemistry :The Molecular Nature of Matter and Change Kalsium karbonat ditemukan pada beberapa bentuk seperti pualam, batu koral, dan kapur. Persen massa unsur-unsur
STOKIOMETRI. Kimia Kelas X
 STOKIOMETRI Kimia Kelas X SEKOLAH MENENGAH ATAS NEGERI 12 SURABAYA 2015 STOKIOMETRI STOKIOMETRI Pada materi stokiometri, kita akan mempelajari beberapa hal seperti persamaan reaksi, hukum-hukum dasar kimia,
STOKIOMETRI Kimia Kelas X SEKOLAH MENENGAH ATAS NEGERI 12 SURABAYA 2015 STOKIOMETRI STOKIOMETRI Pada materi stokiometri, kita akan mempelajari beberapa hal seperti persamaan reaksi, hukum-hukum dasar kimia,
KONSEP MOL DAN STOIKIOMETRI
 BAB V KONSEP MOL DAN STOIKIOMETRI Dalam ilmu fisika, dikenal satuan mol untuk besaran jumlah zat. Dalam bab ini, akan dibahas mengenai konsep mol yang mendasari perhitungan kimia (stoikiometri). A. KONSEP
BAB V KONSEP MOL DAN STOIKIOMETRI Dalam ilmu fisika, dikenal satuan mol untuk besaran jumlah zat. Dalam bab ini, akan dibahas mengenai konsep mol yang mendasari perhitungan kimia (stoikiometri). A. KONSEP
Hubungan koefisien dalam persamaan reaksi dengan hitungan
 STOIKIOMETRI Pengertian Stoikiometri adalah ilmu yang mempelajari dan menghitung hubungan kuantitatif dari reaktan dan produk dalam reaksi kimia (persamaan kimia) Stoikiometri adalah hitungan kimia Hubungan
STOIKIOMETRI Pengertian Stoikiometri adalah ilmu yang mempelajari dan menghitung hubungan kuantitatif dari reaktan dan produk dalam reaksi kimia (persamaan kimia) Stoikiometri adalah hitungan kimia Hubungan
SILABUS. Agustien Zulaidah,ST,MT. Kompetensi Dasar Indikator Materi Pokok & Sub Materi pokok. Alokasi Waktu pengalaman belajar
 SILABUS Mata Kuliah : Azas Rekayasa Proses Kode mata Kuliah / SKS : MTK 113 / 2 ( Dua ) Semester : II ( Dua ) Deskripsi Mata Kuliah : Mata kuliah Azas Rekayasa Proses ini mata kuliah yang membahas tentang
SILABUS Mata Kuliah : Azas Rekayasa Proses Kode mata Kuliah / SKS : MTK 113 / 2 ( Dua ) Semester : II ( Dua ) Deskripsi Mata Kuliah : Mata kuliah Azas Rekayasa Proses ini mata kuliah yang membahas tentang
AMALDO FIRJARAHADI TANE
 DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN SBMPTN KIMIA 2017 Page 1 1. 2. MATERI: STRUKTUR ATOM DAN SISTEM PERIODIK UNSUR Ingat, bahwa jumlah neutron suatu unsur dan ionnya bernilai sama, yang membedakannya
DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN SBMPTN KIMIA 2017 Page 1 1. 2. MATERI: STRUKTUR ATOM DAN SISTEM PERIODIK UNSUR Ingat, bahwa jumlah neutron suatu unsur dan ionnya bernilai sama, yang membedakannya
BAB V PERHITUNGAN KIMIA
 BAB V PERHITUNGAN KIMIA KOMPETENSI DASAR 2.3 : Menerapkan hukum Gay Lussac dan hukum Avogadro serta konsep mol dalam menyelesaikan perhitungan kimia (stoikiometri ) Indikator : 1. Siswa dapat menghitung
BAB V PERHITUNGAN KIMIA KOMPETENSI DASAR 2.3 : Menerapkan hukum Gay Lussac dan hukum Avogadro serta konsep mol dalam menyelesaikan perhitungan kimia (stoikiometri ) Indikator : 1. Siswa dapat menghitung
Sifat Koligatif Larutan (Bagian I)
 KIMIA KELAS XII IPA - KURIKULUM GABUNGAN 01 Sesi NGAN Sifat Koligatif Larutan (Bagian I) Sebelum mempelajari sifat koligatif larutan, terlebih dahulu kita akan meninjau kembali sedikit pengetahuan mengenai
KIMIA KELAS XII IPA - KURIKULUM GABUNGAN 01 Sesi NGAN Sifat Koligatif Larutan (Bagian I) Sebelum mempelajari sifat koligatif larutan, terlebih dahulu kita akan meninjau kembali sedikit pengetahuan mengenai
UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MIPA
 UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MIPA SILABUS SIL/KIM313 / 01 5 September 2008 1. Fakultas : Matematika dan Ilmu Pengetahuan Alam (MIPA) 2. Program Studi : Pendidikan Kimia 3. Mata kuliah & Kode
UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MIPA SILABUS SIL/KIM313 / 01 5 September 2008 1. Fakultas : Matematika dan Ilmu Pengetahuan Alam (MIPA) 2. Program Studi : Pendidikan Kimia 3. Mata kuliah & Kode
11. Mata Pelajaran Kimia Untuk Paket C Program IPA
 11. Mata Pelajaran Kimia Untuk Paket C Program IPA A. Latar Belakang Ilmu Pengetahuan Alam (IPA) berkaitan dengan cara mencari tahu tentang gejala alam secara sistematis, sehingga pendidikan IPA bukan
11. Mata Pelajaran Kimia Untuk Paket C Program IPA A. Latar Belakang Ilmu Pengetahuan Alam (IPA) berkaitan dengan cara mencari tahu tentang gejala alam secara sistematis, sehingga pendidikan IPA bukan
Pelatihan Online I OSN Bidang Kimia Page 1 PETUNJUK PENGERJAAN SOAL
 PETUNJUK PENGERJAAN SOAL 1. Periksalah terlebih dahulu soal yang Anda terima, apakah dalam keadaan baik, terbaca, lengkap, dan jelas, sebelum Anda mengerjakan. 2. Jawaban dikerjakan pada lembar jawaban
PETUNJUK PENGERJAAN SOAL 1. Periksalah terlebih dahulu soal yang Anda terima, apakah dalam keadaan baik, terbaca, lengkap, dan jelas, sebelum Anda mengerjakan. 2. Jawaban dikerjakan pada lembar jawaban
LOGO STOIKIOMETRI. Marselinus Laga Nur
 LOGO STOIKIOMETRI Marselinus Laga Nur Materi Pokok Bahasan : A. Konsep Mol B. Penentuan Rumus Kimia C. Koefisien Reaksi D. Hukum-hukum Gas A. Konsep Mol Pengertian konsep mol Hubungan mol dengan jumlah
LOGO STOIKIOMETRI Marselinus Laga Nur Materi Pokok Bahasan : A. Konsep Mol B. Penentuan Rumus Kimia C. Koefisien Reaksi D. Hukum-hukum Gas A. Konsep Mol Pengertian konsep mol Hubungan mol dengan jumlah
UJIAN NASIONAL TAHUN PELAJARAN 2007/2008
 UJIAN NASIONAL TAHUN PELAJARAN 2007/2008 PANDUAN MATERI SMA DAN MA K I M I A PROGRAM STUDI IPA PUSAT PENILAIAN PENDIDIKAN BALITBANG DEPDIKNAS KATA PENGANTAR Dalam rangka sosialisasi kebijakan dan persiapan
UJIAN NASIONAL TAHUN PELAJARAN 2007/2008 PANDUAN MATERI SMA DAN MA K I M I A PROGRAM STUDI IPA PUSAT PENILAIAN PENDIDIKAN BALITBANG DEPDIKNAS KATA PENGANTAR Dalam rangka sosialisasi kebijakan dan persiapan
SIMULASI UJIAN NASIONAL 1
 SIMULASI UJIAN NASIONAL 1 1. Bilangan-bilangan kuantum yang mungkin dimiliki oleh suatu elektron (A) n = 2, l = 2, m = 0, s = - 1 2 (B) n = 3, l = 0, m = +1, s = + 1 2 (C) n = 4, l = 2, m = - 3, s = -
SIMULASI UJIAN NASIONAL 1 1. Bilangan-bilangan kuantum yang mungkin dimiliki oleh suatu elektron (A) n = 2, l = 2, m = 0, s = - 1 2 (B) n = 3, l = 0, m = +1, s = + 1 2 (C) n = 4, l = 2, m = - 3, s = -
PREDIKSI UJIAN NASIONAL 2011 KIMIA
 Soal PREDIKSI Latihan UJIAN NASIONAL 2011 2013 KIMIA 1 LATIHAN UJIAN AKHIR NASIONAL TAHUN AJARAN 2012/2013 KIMIA 1. Jika unsur 19 X berikatan dengan unsur 35 Z maka, rumus senyawa dan jenis ikatan yang
Soal PREDIKSI Latihan UJIAN NASIONAL 2011 2013 KIMIA 1 LATIHAN UJIAN AKHIR NASIONAL TAHUN AJARAN 2012/2013 KIMIA 1. Jika unsur 19 X berikatan dengan unsur 35 Z maka, rumus senyawa dan jenis ikatan yang
YAYASAN BINA SEJAHTERA SMK BINA SEJAHTERA 2 BOGOR Jl. Ledeng Sindangsari No. 05 Bogor Jl. Radar baru no. 08 Bogor ULANGAN SEMESTER GANJIL
 : XI (Semua Jurusan) Jawablah pertanyaan-pertanyaan di bawah ini dengan benar! 1. Apa yang dimaksud dengan pengertian istilah-istilah berikut : a. ikatan ionik b. reaksi basa c. reaksi reduksi d. reaksi
: XI (Semua Jurusan) Jawablah pertanyaan-pertanyaan di bawah ini dengan benar! 1. Apa yang dimaksud dengan pengertian istilah-istilah berikut : a. ikatan ionik b. reaksi basa c. reaksi reduksi d. reaksi
SOAL KIMIA 2 KELAS : XI IPA
 SOAL KIMIA KELAS : XI IPA PETUNJUK UMUM. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan. Periksa dan bacalah soal dengan teliti sebelum Anda bekerja. Kerjakanlah soal anda pada lembar jawaban
SOAL KIMIA KELAS : XI IPA PETUNJUK UMUM. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan. Periksa dan bacalah soal dengan teliti sebelum Anda bekerja. Kerjakanlah soal anda pada lembar jawaban
OLIMPIADE SAINS NASIONAL CALON PESERTA INTERNATIONAL CHEMISTRY OLYMPIAD (IChO) Yogyakarta Mei Lembar Jawab.
 Hak Cipta Dilindungi Undang-undang OLIMPIADE SAINS NASIONAL 2015 CALON PESERTA INTERNATIONAL CHEMISTRY OLYMPIAD (IChO) 2016 Yogyakarta 18-24 Mei 2015 Lembar Jawab Kimia TEORI Waktu: 240 menit KEMENTERIAN
Hak Cipta Dilindungi Undang-undang OLIMPIADE SAINS NASIONAL 2015 CALON PESERTA INTERNATIONAL CHEMISTRY OLYMPIAD (IChO) 2016 Yogyakarta 18-24 Mei 2015 Lembar Jawab Kimia TEORI Waktu: 240 menit KEMENTERIAN
LOGO. Stoikiometri. Tim Dosen Pengampu MK. Kimia Dasar
 LOGO Stoikiometri Tim Dosen Pengampu MK. Kimia Dasar Konsep Mol Satuan jumlah zat dalam ilmu kimia disebut mol. 1 mol zat mengandung jumlah partikel yang sama dengan jumlah partikel dalam 12 gram C 12,
LOGO Stoikiometri Tim Dosen Pengampu MK. Kimia Dasar Konsep Mol Satuan jumlah zat dalam ilmu kimia disebut mol. 1 mol zat mengandung jumlah partikel yang sama dengan jumlah partikel dalam 12 gram C 12,
LATIHAN ULANGAN TENGAH SEMESTER 2
 Pilihlah jawaban yang paling benar LATIHAN ULANGAN TENGAH SEMESTER 2 TATANAMA 1. Nama senyawa berikut ini sesuai dengan rumus kimianya, kecuali. A. NO = nitrogen oksida B. CO 2 = karbon dioksida C. PCl
Pilihlah jawaban yang paling benar LATIHAN ULANGAN TENGAH SEMESTER 2 TATANAMA 1. Nama senyawa berikut ini sesuai dengan rumus kimianya, kecuali. A. NO = nitrogen oksida B. CO 2 = karbon dioksida C. PCl
6.1 HUKUM-HUKUM DASAR KIMIA
 6.1 HUKUM-HUKUM DASAR KIMIA 1. Hukum kekekalan massa oleh Antoine Laurent Lavoiser (1789). Lavoiser mengemukakan pernyataan yang disebut hukum kekekalan massa, yang berbunyi : Pada reaksi kimia, massa
6.1 HUKUM-HUKUM DASAR KIMIA 1. Hukum kekekalan massa oleh Antoine Laurent Lavoiser (1789). Lavoiser mengemukakan pernyataan yang disebut hukum kekekalan massa, yang berbunyi : Pada reaksi kimia, massa
AMALDO FIRJARAHADI TANE
 DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN SBMPTN KIMIA 2017 Page 1 1. 2. MATERI: STRUKTUR ATOM DAN SISTEM PERIODIK UNSUR Di soal diketahui bahwa unsur X memiliki nomor atom 19. Ingat, bahwa jumlah
DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN SBMPTN KIMIA 2017 Page 1 1. 2. MATERI: STRUKTUR ATOM DAN SISTEM PERIODIK UNSUR Di soal diketahui bahwa unsur X memiliki nomor atom 19. Ingat, bahwa jumlah
Kekekalan Energi energi tidak dapat diciptakan maupun dimusnahkan
 Termokimia XI IPA CO 2, mineral, panas, cahaya Kekekalan Energi energi tidak dapat diciptakan maupun dimusnahkan Manusia Fotosintesis Sayuran dan Buah Entalpi energi / kalor yang terdapat dalam suatu materi.
Termokimia XI IPA CO 2, mineral, panas, cahaya Kekekalan Energi energi tidak dapat diciptakan maupun dimusnahkan Manusia Fotosintesis Sayuran dan Buah Entalpi energi / kalor yang terdapat dalam suatu materi.
STOIKIOMETRI. Purwanti Widhy H, M.Pd
 STOIKIOMETRI Purwanti Widhy H, M.Pd widhy_ipauny@yahoo.com Menentukan jumlah partikel dan jumlah mol Jumlah molx(n) = jumlah partikelx L 1 mol = L partikel L= bilangan avogadro (6.02 x 10 23 /mol)
STOIKIOMETRI Purwanti Widhy H, M.Pd widhy_ipauny@yahoo.com Menentukan jumlah partikel dan jumlah mol Jumlah molx(n) = jumlah partikelx L 1 mol = L partikel L= bilangan avogadro (6.02 x 10 23 /mol)
TRY OUT UJIAN NASIONAL TAHUN AJARAN 2008 / 2009
 TRY UT UJIAN NASINAL TAHUN AJARAN 2008 / 2009 LEMBAR SAL B Bidang Studi : KIMIA Kelas/Program : XII (Dua Belas)/IPA PETUNJUK UMUM 1. Berdo alah sebelum mengerjakan soal 2. Tulislah dahulu nama dan kelas
TRY UT UJIAN NASINAL TAHUN AJARAN 2008 / 2009 LEMBAR SAL B Bidang Studi : KIMIA Kelas/Program : XII (Dua Belas)/IPA PETUNJUK UMUM 1. Berdo alah sebelum mengerjakan soal 2. Tulislah dahulu nama dan kelas
KONTRAK PEMBELAJARAN KIMIA DASAR
 SELAMAT DATANG DI KAMPUS MERAH UNIVERSITAS HASANUDDIN MAKASSAR INDONESIA KONTRAK PEMBELAJARAN KIMIA DASAR KOORDINATOR MATA KULIAH Dr. Sci. MUHAMMAD ZAKIR KIMIA DASAR UPT MKU UNIVERSITAS HASANUDDIN 2012
SELAMAT DATANG DI KAMPUS MERAH UNIVERSITAS HASANUDDIN MAKASSAR INDONESIA KONTRAK PEMBELAJARAN KIMIA DASAR KOORDINATOR MATA KULIAH Dr. Sci. MUHAMMAD ZAKIR KIMIA DASAR UPT MKU UNIVERSITAS HASANUDDIN 2012
K13 Revisi Antiremed Kelas 11 Kimia
 K13 Revisi Antiremed Kelas 11 Kimia Persiapan UTS Semester Ganjil Doc. Name: RK13AR11KIM01UTS Doc. Version: 2016-10 halaman 1 01. Sebenarnya kimia organik dan anorganik tidaklah perlu dipisah-pisahkan,
K13 Revisi Antiremed Kelas 11 Kimia Persiapan UTS Semester Ganjil Doc. Name: RK13AR11KIM01UTS Doc. Version: 2016-10 halaman 1 01. Sebenarnya kimia organik dan anorganik tidaklah perlu dipisah-pisahkan,
KIMIa ASAM-BASA II. K e l a s. A. Kesetimbangan Air. Kurikulum 2006/2013
 Kurikulum 2006/2013 KIMIa K e l a s XI ASAM-BASA II Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami kesetimbangan air. 2. Memahami pengaruh asam
Kurikulum 2006/2013 KIMIa K e l a s XI ASAM-BASA II Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami kesetimbangan air. 2. Memahami pengaruh asam
UNIVERSITAS ANDALAS FAKULTAS MIPA JURUSAN KIMIA Mata Kuliah Service Untuk Jurusan Biologi
 KEMENTERIAN PENDIDIKAN DAN KEBUDAYAAN UNIVERSITAS ANDALAS FAKULTAS MIPA JURUSAN KIMIA Mata Kuliah Service Untuk Jurusan Biologi RENCANA PROGRAM DAN KEGIATAN PEMBELAJARAN SEMESETER (RPKPS) Mata Kuliah Kimia
KEMENTERIAN PENDIDIKAN DAN KEBUDAYAAN UNIVERSITAS ANDALAS FAKULTAS MIPA JURUSAN KIMIA Mata Kuliah Service Untuk Jurusan Biologi RENCANA PROGRAM DAN KEGIATAN PEMBELAJARAN SEMESETER (RPKPS) Mata Kuliah Kimia
BAB VI KINETIKA REAKSI KIMIA
 BANK SOAL SELEKSI MASUK PERGURUAN TINGGI BIDANG KIMIA 1 BAB VI 1. Padatan NH 4 NO 3 diaduk hingga larut selama 77 detik dalam akuades 100 ml sesuai persamaan reaksi berikut: NH 4 NO 2 (s) + H 2 O (l) NH
BANK SOAL SELEKSI MASUK PERGURUAN TINGGI BIDANG KIMIA 1 BAB VI 1. Padatan NH 4 NO 3 diaduk hingga larut selama 77 detik dalam akuades 100 ml sesuai persamaan reaksi berikut: NH 4 NO 2 (s) + H 2 O (l) NH
AMALDO FIRJARAHADI TANE
 DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN SBMPTN KIMIA 2015 Page 1 1. MATERI: IKATAN KIMIA DAN GEOMETRI MOLEKUL Pada soal diketahui bahwa nomor atom nitrogen adalah 7 (ditulis 7 N) dan nomor atom
DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN SBMPTN KIMIA 2015 Page 1 1. MATERI: IKATAN KIMIA DAN GEOMETRI MOLEKUL Pada soal diketahui bahwa nomor atom nitrogen adalah 7 (ditulis 7 N) dan nomor atom
KIMIA UMUM 1. PUTRI ANJARSARI, S.SI.,M.Pd 2015
 KIMIA UMUM 1 PUTRI ANJARSARI, S.SI.,M.Pd putri_anjarsari@uny.ac.id 2015 PENDAHULUAN KULIAH KIMIA UMUM 1 3 sks mata kuliah wajib Tujuan Pembelajaran Mata kuliah ini untuk mengembangkan kompetensi dalam
KIMIA UMUM 1 PUTRI ANJARSARI, S.SI.,M.Pd putri_anjarsari@uny.ac.id 2015 PENDAHULUAN KULIAH KIMIA UMUM 1 3 sks mata kuliah wajib Tujuan Pembelajaran Mata kuliah ini untuk mengembangkan kompetensi dalam
STOKIOMETRI BAB. B. Konsep Mol 1. Hubungan Mol dengan Jumlah Partikel. Contoh: Jika Ar Ca = 40, Ar O = 16, Ar H = 1, tentukan Mr Ca(OH) 2!
 BAB 7 STOKIOMETRI A. Massa Molekul Relatif Massa Molekul Relatif (Mr) biasanya dihitung menggunakan data Ar masing-masing atom yang ada dalam molekul tersebut. Mr senyawa = (indeks atom x Ar atom) Contoh:
BAB 7 STOKIOMETRI A. Massa Molekul Relatif Massa Molekul Relatif (Mr) biasanya dihitung menggunakan data Ar masing-masing atom yang ada dalam molekul tersebut. Mr senyawa = (indeks atom x Ar atom) Contoh:
RENCANA PELAKSANAAN PEMBELAJARAN (Tatap Muka Ke-9) 1. Identitas : Matematika dan Ilmu Pengetahuan Alam Jurusan/Program Studi : Pendidikan Kimia/Kimia
 (Tatap Muka Ke-9) Semester dan Pertemuan : 2 (Kimia) 100 menit Dosen : Annisa Fillaeli, M.Si Isti Yunita, M.Sc (isti_yunita@uny.ac.id) percobaan Penentuan Kadar Asam cuka perdagangan pada NaOH dan menerapkan
(Tatap Muka Ke-9) Semester dan Pertemuan : 2 (Kimia) 100 menit Dosen : Annisa Fillaeli, M.Si Isti Yunita, M.Sc (isti_yunita@uny.ac.id) percobaan Penentuan Kadar Asam cuka perdagangan pada NaOH dan menerapkan
