BUKU PEGANGAN MAHASISWA KIMIA ORGANIK SINTESIS
|
|
|
- Hengki Kusuma
- 7 tahun lalu
- Tontonan:
Transkripsi
1 BUKU PEGANGAN MAHASISWA KIMIA RGANIK SINTESIS leh: Dr. Amanatie M.Pd., M.Si uny.ac.id FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS NEGERI YGYAKATA
2 Prinsip Dasar Pendekatan Diskoneksi A. Pendahuluan LaatrBelakang ranik sintesis merupakan ilmu yang memudahkan kimiawan melakukan peniltian dalam sintesis senyawa organik. Perkembangan ilmu ini disebabkan pengetahuan struktur suatu senyawa menjadi terbuka setelah diperkenalkan cara-cara mengidentifikan sisenyawa organic dan berkembangnya bahan lama yang sangat pesat.teori yang menunjang semakin berkembangnya organic sintesisa dalam pendekatan diskoneksi. Pendekatan diskoneksi adalah metode yang dapat memudahkan para kimiawan alam merekayasa dan menentukan bahan dasar apa saja yang dapat digunakan pada penelitian. Dalam makalah ini akan dibahas tentang metode sintesis pendekatan deskoneksi dalam merancang proses sintesis dari suatu senyawa organik. Tujuan penyusunan makalah ini dapat membantu para kimiawan pemula dalam memahami proses sintesis pendekatan diskoneksi. B. Isi 1. Diskoneksi Diskoneksi adalah pemotongan ikatan secara imaginer pemecah molekul yang diharapkan lebih sederhana. Diskoneksi bias disebut kebalikan dari sintesis, jika sintesis mereaksikan senyawa starting material menjadi suatu produk senyawa baru. Proses dikoneksi dapat dilakukan beberapa tahap hingga mendapat senyawa yang diinginkan.apabila suatu senyawa kimia memiliki ikatan lebih dari satu yang harus diputus, maka harus dipilih salah satu pertimbangan: a. Sedapat mungkin di sekitar bagian tengah molekul sehingga didapatkan dua molekul yang seimbang. b. Sebaiknya pada titik cabang yang lebih memberikan fragmen berantai lurus untuk meminimalkan gangguan sterik dalam reaksi. c. Diskoneksi untuk senyawa-senyawa aromatic secara umum dilakukan pada gugus/ subtituennya.
3 d. Memilihr untutan reaksi juga harus didasarkan pada factor efisiensi dan kelayan reaksi serat bahan baku yang digunakan. e. Jika pada suatu senyawa aromatic terdapat dua gugus yang berbeda, maka pemotongan ikatan berdasarkan pada reaktivitas relatifnya. Gugus penarik elektron (deaktivasi) mendapat prioritas pertama dalam pemutusan ikatan dan seterusnya. (Budimarwati: 2012) 2. InterkonversiGugusFungsi Tahapan analisis dilakukan pengenalan gugus fungsional yang dada pada molekul target terkait dengan keelektronegatifannya, pengaruh pada sintesis dan penentuan diskoneksi secara langsung atau harus diubah terlebih dahulu memalui interkonversi gugus fungsi atau IGF. Diskoneksi dilakukan dengan cara demikan supaya senyawa dapat direaksikan kembali esuaidenganmetodereaksi-reaksikimiaorganik yang dipercaya. Untukmendapatkanhasil yang selektifkadangkadangmemerlukansenyapelindunggugus.berikutmerupakancontohinterkonverensigugusfun gsional (Stuart: 1995). Gambar 1. Proses Interkonversi Fungsional (Stuart: 1995). 3. Sinton Diskoneksi aromatik yang berguna lainnya adalah sinton. Sinton merupakan fragmen ideal yang dapat atau tidak dapat terlibat dalam reaksi, tetapi yang membantu untuk menentukan reagen-reagen yang sesuai untuk digunakan. Reagen inilah yang disebut sebagai material pemula, yaitu senyawa yang digunakan dalam reaksi sintesis sebagai pengganti sinton (Stuart: 1995). Berikut merupakan mechanism ediskoneksi.
4 Gambar 2. Mekanismediskoneksi(Stuart: 1995). Bila analisis lengkap, maka sinton harus digantikan oleh reagen untuk kegunaan praktis.untuk sinton an ionic, reagen yang sering digunakan adalah hidrokarbon yang bersangkutan, untuk sinton kationik reagen yang umum digunakan merupakan halide yang bersangkutan (Stuart: 1995).
5 PRINSIP-PRINSIP DASAR SINTESIS SENYAWA ARMATIK Dalam sintesis senyawa aromatik digunakan term-term teknik diskoneksi, interkonversi gugus fungsional (IGF), dan sinton. A. Diskoneksi dan IGF dalam sintesis senyawa aromatik Diskoneksi merupakan kebalikan dari langkah sintesis atau reaksi. Diskoneksi dilakukan bila dihasilkan reaksi kimia yang sesuai dan lazim (reliable reaction) untuk senyawa aromatik. Terdapat 4 macam reaksi substitusi elektrofilik terhadap senyawa aromatik. 1. Reaksi halogenasi X + X 2 FeX 3 panas + HX Sebagai elektrofil adalah X +, dihasilkan dari reaksi antara X 2 + FeX Reaksi nitrasi N 2 + HN 3 H 2 S 4 pekat panas + H 2 Sebagai elektrofil adalah N + 2 (ion nitronium), dihasilkan dari reaksi antara HN 3 dan H 2 S 4. HN 3 + H 2 S - 4 H-H-N 2 + HS 4 H H-H-N 2 H H N 2 ion nitronium 3. Reaksi sulfonasi Benzena bereaksi lambat dengan H 2 S 4 pada suhu tinggi menghasilkan asam benzena sufonat.
6 N 2 + HN 3 H 2 S 4 pekat panas + H 2 Sebagai elektrofil adalah S 3 yang merupakan elektrofil relatif kuat karena atom S yang kekurangan elektron, atau + S 3 H yang dihasilkan dari reaksi: 2 H 2 S 4 S 3 + H HS 4 atau H 2 S - 4 HS 4 + H + H 2 S 4 + H + H--S--H H H- - S--H H S 3 H H 4. Reaksi Friedel-Crafts Reaksi Friedel-Crafts meliputi reaksi alkilasi dan reaksi asilasi. Reaksi alkilasi: R + RX FeX 3 + HX Sebagai elektrofil dalam reaksi alkilasi Friedel-Crafts adalah ion karbonium (R + ). Karena melibatkan ion karbonium, maka seringkali terjadi reaksi pnyusunan ulang (rearrangement) membentuk karbonium yang lebih stabil. Reaksi asilasi: + R-C-X FeX 3 C R Sebagai elektrofil dalam reaksi asilasi Friedel-Crafts adalah ion asilium, terbentuk dari hasil reaksi: R-C-X + FeX 3 R-C FeX 4 ion asilium Pada reaksi asilasi Friedel-Crafts tidak erjadi reaksi penataan ulang.
7 Dengan memahami keempat reaksi substitusi elektrofilik terhadap senyawa aromatik tersebut kita dapat menentukan dimana dilakukan diskoneksi pada tahap analisis, sehingga pada tahap sintesis akan didapatkan reaksi yang lazim terhadap senyawa aromatik. Senyawa benzokaina (1) yang merupakan senyawa patirasa lokal adalah senyawa ester, ester dapat dibuat dari reaksi antara: alkohol dengan asam karboksilat menggunakan katalis asam, alkohol dengan anhidrida asam karboksilat, atau reaksi antara alkohol dengan asilhalida. Pada tahap analisis dilakukan diskoneksi pada ikatan C-, diskoneksi diberi label untuk memperlihatkan reaksi pebuatannya. Analisis : C 2 H Et C - + EtH ester NH NH 2 2 Benzokaina (1) Pada tahap analisis 1 didapatkan senyawa asam p-aminobenzoat, dimana terdapat gugus CH dan NH 2 yang terikat pada cincin aromatik. Bila dilakukan diskoneksi baik pada CH atau NH 2, maka tidak dikenal reaksi yang bersangkutan dengan diskoneksi ini. leh sebab itu yang dapat dilakukan adalah melakukan interkonversi gugus fungsional untuk mengubah gugus fungsional CH dan NH 2 ke gugus fungsional yang lain, sehingga dapat dilakukan diskoneksi. Asam aromatik dapat dibuat dari reaksi oksidasi gugus metal, dan gugus amino dapat dibuat dengan reaksi reduksi gugus amino. Sehingga pada tahap analisis 2 dapat dilakukan IGF sebagai berikut: Analisis 2: C 2 H IGF C 2 H IGF CH 3 NH 2 N 2 N 2 Pada tahap analisis 2, yaitu dengan IGF akan didapatkan senyawa dengan gugus N 2 dan CH 3 terikat pada cincin aromatik. Sekarang diskoneksi gugus nitro dapat dilakukan dan rasional, karena diketahui bahwa nitrasi toluena secara mudah dapat dilakukan di laboratoium, dan toluena mudah didapatkan. Analisis 3:
8 CH 3 C-N nitrasi CH 3 N 2 Pada tahap analisis 3 didapatkan toluena sebagai bahan awal. Dari tahap analisis sekarang dapat ditulis tahap sintesis dengan reagen yang sesuai. Sangat penting untuk mengetahui tipe reagen dan kondisi reaksi yang dibutuhkan, agar diperoleh hasil senyawa seperti yang diharapkan. Sintesis senyawa benzokaina dapat dituliskan sebagai berikut: Sintesis: H CH 3 HN 3 CH 3 KMn 4 C 2 H H 2 S 4 N2 N 2 H Pd, C NH 2 C 2 H EtH H + Benzokaina Pada tahap sintesis dimungkinkan melaksanakan tahap-tahap reaksi dalam urutan yang berbeda, misalnya penggantian urutan dari dua langkah terakhir. Pada tahap sintesis di atas dilakukan reaksi reduksi gugus nitro terlebih dahulu, baru kemudian dilakukan reaksi esterifikasi. Bila urutan reaksi dibalik, dilakukan reaksi esterifikasi terlebih dahulu, baru kemudian dilakukan reaksi redukdi gugus nitro. B. Sinton dalam sintesis senyawa aromatik Diskoneksi aromatik lainnya adalah yang berhubungan dengan reaksi Friedel-Crafts, yang akan digunakan dalam sintesis senyawa hawthorn blossom perfume (2). Sintesis ini merupakan sintesis satu langkah yang berawal dari suatu eter yang tersedia. Analisis: Sintesis: H C-C + Friedel-Crafts Cl Me Me hawthorn blossom (2)
9 Me MeCCl AlCl 3 hawthorn blossom Dalam reaksi Friedel-Crafts, dan dalam reaksi nirasi yang melakukan penyerangan terhadap cincin benzena adalah kation MeC + untuk reaksi Friedel-Crafts, dan N2 + untuk reaksi nitrasi. Bila dilakukan diskoneksi suatu ikatan pada cincin aromatik, maka secara normal diharapkan tipe reaksi ini, yaitu reaksi antara cincin aromatik yang kaya elektron dengan suatu elektrofil. Dengan demikian dalam diskoneksi suatu ikatan pada cincin aromatik selain dapat ditentukan ikatan mana yang terpotong, juga dapat ditentukan dengan cara apa, yaitu secara elektronik untuk memotongnya. Dengan demikian hasil pemotongan akan ditulis (a) dan bukan (b), disebabkan cincin aromatik berkelakuan sebagai nukleofil, dan asam asil klorida sebagai elektrofil. a Me (i) + (ii) Me b + Me (iii) (iv) Fragmen (i), (ii), (iii), dan (iv) merupakan sinton, yaitu merupakan fragmen ideal yang dapat atau tidak dapat terlibat dalam reaksi, dan dapat membantu kita untuk menentukan reagen-reagen mana yang dapat digunakan. Fragmen (i) merupakan zat antara intermediet dalam sintesis, sedangkan fragmen (ii) bukan merupakan zat antara. Dalam analisis lengkap, sinton haru digantikan oleh reagen untuk kegunaan praktis. Untuk sinton anionik, reagen sering merupakan hidrokarbon yang bersangkutan, untuk sinton kationik reagen sering merupakan halida yang bersangkutan.
10 Cl H Me Me Me sinton reagen Reaksi alkilasi Friedel-Crafts juga merupakan reaksi yang berhasil guna, terutama dengan halida tersier. Sebagai contoh diskoneksi terhadap senyawa BHT (3) (butylated hydroxytoluene = hidroksitoluena terbutilasi, suatu antioksidan yang digunakan dalam makanan), akan dihasilkan kation tersier butil. Analisis: H H BHT (3) C-C Friedel- Crafts H H + kation tersier butil Sebagai reagen untuk kation t-butil dapat digunakan t-butil klorida dan AlCl 3, isobutena dan asam protik, atau t-butil alkohol dan asam protik. Sintesis: H + H + BHT Pada reaksi asilasi Friedel-Crafts seringkali terjadi reaksi polialkilasi. Di samping itu karena melibatkan karbokation sebagai zat antara intermediet, seringkali terjadi reaksi penataan ulang (rearrangement reaction). Sehingga reaksi alkilasi Friedel-Craft terhadap benzena menggunakan senyawa 1-kloro-2-metil propana dan AlCl 3 memberikan hasil campuran senyawa (4) dan (5).
11 AlCl 3 Cl + (4) (5) Apabila ingin membuat senyawa (6) dapat ditempuh dengan menggunakan reaksi asilasi Friedel-Crafts, kemudian mereduksi gugus karbonil. AlCl 3 CCl Zn, Hg HCl pekat (6) Apabila diinginkan menambah tepat satu atom karbon, seperti dalam sintesis aldehida aromatik, dalam hal ini tidak dapat dilakukan dengan menambah reagen HCCl karena memang tidak terdapat reagen HCCl. Salah satu metode yang dapat dilakukan adalah dengan klorometilasi menggunakan CH 2 + HCl + ZnCl 2 memberikan gugus CH 2 Cl yang dengan mudah dapat dioksidasi menjadi CH (IGF). Metode lain menambah satu atom karbon dengan satu gugus fungsional diberikan pada tabel 1. Tabel 1. Elektrofil satu atom karbon untuk sintesis senyawa aromatik H X X + R R CH 2 Cl CH X Reagen Reaksi CH 2 + HCl + ZnCl 2 Klorometilasi CHCl 2 + H - Reimer-Tiemenn Me 2 N=CH-PCl 2 Formilasi Vilsmeir Haack (Me 2 NCH + PCl 3 ) C + HCl + AlCl 3 Zn(CN) 2 + HCl Senyawa piperonal (7) yang merupakan senyawa parfum dapat dibuat dengan metode menambahkan satu atom karbon ke cincin aromatik. Analisis:
12 CH CH 2 Cl H IGF C-C Sintesis: (7) CH 2 Cl klorometilasi CH 2 oksidasi piperonal ZnCl 2 heksamin HCl Reaksi substitusi elektrofilik aromatik yang lain, misalnya reaksi nitrasi memasukkan gugus N 2, reaksi halogenasi memasukkan Cl atau Br secara langsung ke cincin aromatik. Reagen untuk reaksi substitusi elektrofilik aromatik diberikan pada tabel 2. Tabel 2. Reagen untuk reaksi substitusi elektrofilik aromatik H X X + R R R + RC + N2 + Cl + Br + + S 2 H + S 2 Cl ArN 2 + Sinton Reagen Reaksi RBr + AlCl 3 Alkilasi Friedel-Crafts RH + H + Alkena + H + RCCl + AlCl 3 Alkilasi Friedel-Crafts HN 3 + H 2 S 4 Nitrasi Cl 2 + FeCl 3 Klorinasi Br 2 + Fe Brominasi H 2 S 4 Sulfonasi ClS 2 H Klorosulfonasi + ArN 2 Koplingdiazo Reaksi samping senyawa aromatik yang lain dapat ditambahkan dengan baik oleh IGF. IGF rantai samping senyawa aromatik dapat dilakukan dengan reaksi oksidasi, reduksi, dan substitusi. Beberapa contoh perubahan rantai samping senyawa aromatik oleh IGF disajikan pada tabel 3.
13 Tabel 3. Perubahan rantai samping senyawa aromatik dengan IGF Y X R R Reduksi -N 2 -CR -CR Y X Reagen -NH 2 -CH(H)R -CH 2 Cl H 2, Pd, C Sn, HCl pekat NaBH 4 Misalnya Zn/Hg, HCl pekat ksidasi -CH 2 Cl -CH 2 R -CH 3 -CR Substitusi -CH 3 -CCl 3 -CN -CH -C 2 H -CR -CCl 3 -CF 3 -C 2 H Heksamin KMn 4 RC 3 H Cl 2, PCl 5 SbF 5 H -, H 2 C. Substitusi nukleofilik terhadap senyawa aromatik Apabila dikehendaki penambahan atom oksigen pada cincin aromatik diperlukan pendekatan alternatif lain, yaitu dengan menambahkan sinton R - pada senyawa aromatik dengan suatu gugus pergi (a leaving group). Reaksi ini dikenal dengan nama reaksi substitusi nukleofilik terhadap senyawa aromatik. Reaksi akan berjalan dengan baik apabila gugus pergi adalah N 2 (garam diazonium). Urutan sintesis adalah nitrasi, diazotasi, dan substitusi.
14 R HN 3 H 2 S 4 R N 2 H 2 Pd, C R NH 2 NaN 3 HCl, 5 o C R N 2 H2 R H Sintesis senyawa fenol (8) dapat dianalisis dengan cara ini, H diubah menjadi N 2. Brom dapat ditambahkan pada tingkat amino atau tingkat fenol, tetapi tingkat amino memberikan kontrol yang lebih baik. Analisis: H subst + via N 2 NH 2 C-Br brominasi Me Br Me Br (8) NH 2 IGF N 2 C-N nitrasi Me Me Me toluen Dalam praktek di laboratorium, gugus amino dilindungi sebagai amida untuk mencegah brom juga terikat pada posisi orto yang lain. Sintesis: Me HN 3 H 2 S 4 Me N 2 Sn HCl pekat Me NH 2 HAc Me NHAc 1. Br 2, HAc 2. NaH Me NH 2 Br 1. NaN 3 HCl 2. H 2 senyawa (8) Beberapa nukleofil seperti CN -, Cl -, Br -, paling baik ditambahkan sebagai derivat Cu(I). Daftar nukleofil lain yang dapat digunakan dalam reaksi pemindahan (displacement) nukleofilik dari garam diazonium disajikan pada tabel 4.
15 Tabel 4. Senyawa aromatik yang dibuat dengan pemindahan nukleofilik dari garam diazonium ArNH 2 HN 2 + ArN 2 Z + ArZ Z Reagen H R H 2 RH CN Cl Br I Ar H Cu(I)CN Cu(I)Cl Cu(I)Br KI ArH H 3 P 2 atau EtH/H + Salah satu contoh sintesis senyawa aromatik dengan cara pemindahan nukleofilik dari garam diazonium adalah sintesis senyawa sianida aromatik (9). Analisis: (9) Me CN subst via N 2 + Me NH 2 IGF Me N 2 C-N nitrasi Me Sintesis: Me HN 3 H 2 S 4 Me N 2 H 2 Pd, C Me NH 2 1. NaN 3 HCl 2. Cu(I)CN senyawa (9) D. Substitusi nukleofilik dari halida Reaksi pemindahan langsung gugus halida dari cincin aromatik dengan suatu nukleofil hanya dimungkinkan apabila terdapat gugus nitro pada posisi orto dan para terhadap halida, atau gugus penarik elektron sejenis. Senyawa ini mudah dibuat dengan reaksi nitrasi. Cl Cl Nu HN 3 H 2 S 4 N 2 Nu - N 2 N 2 N 2
16 Herbisida buatan Liley Company, seperti trifluralin B (10) merupakan contoh yang baik bagi pendekatan ini. Gugus amino dapat ditambahkan dengan cara ini, dan dua gugus nitro dimasukkan dengan reaksi nitrasi secara langsung. Analisis: NR 2 Cl Cl N 2 N 2 C-N N 2 N 2 C-N nitrasi Sintesis: Cl CF 3 (10) R= n-propil Cl CF 3 CF 3 HN 3 H 2 S 4 N 2 N 2 basa senyawa (10) n-pr 2 NH CF 3 CF 3 E. Campuran produk orto dan para Reaksi nitrasi terhadap toluena akan menghasilkan produk orto nitro toluena dan para nitro toluena. Dalam praktek, suatu campuran akan terbentuk dan harus dipisahkan agar memberikan isomer yang diinginkan. Seringkali dalam suatu reaksi dihindari terjadinya produk campuran, tetapi reaksi substitusi aromatik sangat mudah dikerjakan sehingga produk campuran tidak dapat dihindari, dan langkah pemisahan dapat diterima, terutama bila dilakukan pada urutan pertama. Reaksi kemudian dikerjakan pada skala besar untuk mendapatkan isomer yang dikehendaki. Senyawa sakarina (11) dapat dibuat dengan cara pemisahan produk orto dan para. Diskoneksi imida akan menghasilkan senyawa diasid (12) yang dapat dibuat dengan IGF dari senyawa asam toluena-orto-sulfonat (13).
17 S 2 NH S-N C-N amida (11) (12) C 2 H S 2 H IGF oksidasi (13) Me S 2 H C-S Me sulfonasi Dalam praktek, lebih cepat untuk membuat senyawa sulfonil klorida (14) secara langsung dan memisahkan dari produk para (15). Me ClS 2 H (14) Me S 2 Cl + Cl 2 S Me = TsCl Me KMn 4 C 2 H S 2 NH 2 S 2 NH 2 Sakarina dibuat dalam skala besar, sehingga terdapat banyak toluena-p-sulfonil klorida (15) sebagai hasil samping dan murah. Hal ini merupakan salah satu alasan mengapa gugus tosil merupakan gugus tinggal yang populer bagi ahli kimia organik. F. Term teknik pendekatan diskoneksi 1. Molekul Target (MT): molekul yang disintesis 2. Analisis atau analisis retrosintetik: proses pemotongan MT menjadi bahan awal (material start) yang tersedia, dilakukan dengan interkonversi gugus fungsional (IGF) dan diskoneksi. 3. Interkonversi Gugus Fungsional (IGF): proses pengubahan suatu gugus fungsional satu menjadi gugus fungsional yang lain dengan reaksi substitusi, adisi, eliminasi, oksidasi, dan reduksi serta operasi balik yang digunakan dalam langkah analisis. 4. Diskoneksi: operasi balik suatu reaksi. Proses pemotongan yang dibayangkan dari suatu ikatan untuk memutus molekul menjadi material start yang mungkin. 5. : simbol untuk diskoneksi atau IGF.
18 6. Sinton: fragmen ideal, biasanya suatu kation atau anion hasil dari diskoneksi.sinton tersebut mungkin atau tidak mungkin merupakan zat antara dalam reaksi bersangkutan 7. Reagen: senyawa yang digunakan dalam praktek untuk suatu sinton. Misalnya MeI merupakan reagen untuk sinton Me +. Diskoneksi satu Gugus C-X Diskoneksi satu gugus C-X telah dimulai dengan senyawa aromatic, karena memang pada senyawa aromatic posisi diskoneksi dengan mudah dapat diputuskan. Kemudian dilanjutkan dengan senyawa eter, amida, dan silfida. Pada senyawa-senyawa tersebut sekali lagi posisi diskoneksi mudah ditentukan, diskoneksi dilakukan pada ikatan yang menghubungkan antara karbon dengan heteroatom (X) diskoneksi ini diberi nama diskoneksi satu gugus karena hanya diperlukan pengenalan satu gugus fungsional sebelum dilakukan diskoneksi. Label C-X atau C-N, dan sebagainya dapat digunakan. Dalam diskoneksi akan menghasilkan sinton karbon kationik (R+). Reagen untuk sinton ini biasanya mempunyai gugus pergi yang baik (good leaving group) yang terikat pada R. dalam reaksi bersangkutan hamper semua bersifat ionic, dan melibatkan heteroatom nukleofilik seperti alcohol (RH), amina (RNH2) atau tiol (RSH). Reaksi yang terjadi adalah reaksi substitusi, reagen yang terlibat dapat suatu alkil halide, aril klorida, atau senyawa sejenis. Reagen yang paling baik adalah reagen yang paling mudah mengalami reaksi substitusi. Hasil pemotongan menghasilkan sinton R+, reagen untuk sinton ini adalah RY, dimana Y dapar Br, ts (para toluene sulfonil), atau gugus pergi yang baik lainnya. Senyawa Turunan Karbonil RC-X Senyawa-senyawa turunan asam mudah untuk didiskoneksi, pertama kali didiskoneksi dilakukan pada ikatan antara gugus karbonil dan heteroatom.
19 Senyawa ester (1) merupakan senyawa pengusir serangga, atau sebagai pelarut dalam parfum dapat didiskoneksi dengan cara ini, yaitu pertamakali diskoneksi dilakukan pada ikatan antara gugus karbonil dan heteroatom. Analisis : Sintesis ini dapat dilakukan dengan beberapa cara, untuk pembentukan ester dapat dilakukan dengan mereaksikan alcohol dengan asam karboksilat, alcohol dengan anhidrida asam karboksilat, atau alcohol dengan asil halide. Untuk sintesi senyawa ester (1) diatas paling mudah adalah dengan rute asil klorida (Y=Cl), menggunakan piridin sebagai katalis dan pelarut. Sintesis : Senyawa asil klorida sering digunakan dalam sintesis senyawa ester, karena senyawa ini merupakan turunan asam yang paling reaktif. Asil klorida dapat dibuat dari asamnya sendiri dengan PCl5 atau SCl2. Reaktivitas turunan asam dari yang paling reaktif adalah klorida asam anhidrida asam, ester, dan paling tidak reaktif adalah amida. Senyawa propanil (2) digunakan sebagi pembunuh rumput-rumputan/semak, merupakan senyawa amida, apabila didiskoneksi akan menghasilkan suatu amina dan klorida asam. Analisis :
20 Pada langkah reaksi orientasi untuk nitrasi benar, hambatan sterik akan mencegah pembentuka senyawa 1,2,3-trisubstitusi dalam jumlah yang banyak. Sintesis : Senyawa (3) merupakan contoh yang lebih sukar, tetapi dari struktur senyawa tersebut dengan mudah dapat dikenali bahwa senyawa tersebut adalah suatu ester, dan dapat dilakukan diskoneksi dengan cara biasa. Dari hasil diskoneksi diperoleh senyawa anhidrida ftalat sebagai bahan awal. Analisis :
21 Sintesis : Alkohol, Eter, Alkil Halida dan Sulfida Diskoneksi C-X suatu senyawa alifatik RX akan menghasilkan nukleofilik XH dan suatu spesies karbon elektrofilik. Spesies karbon elektrofilik dapat diperoleh dari senyawa alkil halide, tosilat = RTs (toluene-p-sulfonat), atau mesilat = RMs (metana sulfonat). Senyawa-senyawa tersebut semuanya dapat dibuat dari alcohol.
22 Senyawa-senyawa alifatik turunan alcohol diatas dapat diperoleh dengan reaksi substitusi. Kondisi reaksi harus dipilih sedemikian rupa, disesuaikan dengan struktur molekul. Turunan metil dan alkil primer breaksi dengan mekanisme SN2, mekanisme ini akan efektif apabila digunakan nukleofil kuat dan pelarut non polar. Misalnya senyawa nitro (4) dan azida (5) yang meruapakan contoh dari senyawa turunan lain yang sesuai dengan mekanisme reaksi SN2, karena keduanya adalah senyawa alkil halide primer. Senyawa-senyawa tersiserbereaksi lebih mudah dengan mekanisme reaksi SN1 via karbonium (6), karbonium ini stabil dan dihasilkan secara langsung dari alcohol, alkil halide, atau bahkan alkena. Dalam reaksi ini tidak dibutuhkan nukleofil kuat karena apabila digunakan nukleofil kuat akan terjadi reaksi eliminasi. Reaksi SN1 akan efektif apabila digunakan pelarut polar dan katalis (dapat berupa asam atau basa Lewis). Katalis disini berfungsi utuk membuat H menjadi gugus pergi yang lebih baik. Senyawa (7) dapat dibuat dengan reaksi alkilasi Friedel-Craft dari senyawa alkil klorida tersier (8) yang dapat dibuat dari alcohol (9). Satu-satunya reagen yang dapat dipakai untuk membuat senyaw alkil klorida tersier (8) menjadi alcohol (9) adalah HCl pekat.
23 Analisis : Sintesis : Senyawa turunan alilik (10) dan benzilik (11) mudah bereaksi baik dengan mekanisme SN1 Maupun SN2, sehingga kondisi secara relative tidak diperlukan disini. Sebaliknya untuk senyawa turunan alkil halide sekunder memerlukan kondisi sedikit ketat untuk menentukan jejak mekanistik yang diikuti. Eter dan Sulfida Dalam sintesis senyawa eter, pada langkah analisis dengan mudah dapat dipilih diskoneksi yang pertama, karena reaktivitas (atau tidak ada reaktivitas) dari satu sisi aktif yaitu Me (dengan SN2) dan sisi tidak reaktif yaitu Ar sehingga diskoneksi dengan mudah dapat ditentukan. Analisis :
24 Dimetil sulfat dapat digunakan untuk metilasi fenol dalam larutan alkali, dimana dalam larutan alkali fenol diionisasikan. Karena mekanisme reaksi adalah SN2, maka akan menguntungkan apabila digunakan nukleofil kuat. Sintesis : Senyawa parfum gardenia (13) dapat didiskoneksikan pada kedua sisi, karena keduanya melibatkan alkil halide primer. Analisis : Diskoneksi (b) akan menghasilakn benzyl halide yang lebih reaktif, sehingga rute (b) ini dipilih, disamping itu apabila dipilih rute (a) dapat menuju proses eliminasi. Sintesis : Dalam sintesis reaksi mengikuti mekanisme reaksi SN2, sehingga katalis basa akan sangat membantu. Apabila dalam menetukan diskoneksi tidak ada pilihan yang jelas, akan sangat menolong untuk menuliskan kedua fragmen sebagai alcohol, kemudian baru ditentukan mana yang akan diubah menjadi elektrofil. Sebagai contoh dalam sintesis senyawa eter (14) yang dibutuhkan oleh Baldwin untuk mempelajari penataan ulang karbanion. Kedua sisi semuanya reaktif, sehingga untuk pertama kali
25 dituliskan kedua fragmen dalam bentuk alcohol. Baldwin tidak mengumumkan bagaimana secara actual ia membuat eter, kedua rute kelihatan baik. Analisis : Sintesis : Prinsip yang sama juga diterapkan pada sintesis senyawa sulfide (R1SR2). Reaksi dengan mekanisme SN2 bahkan lebih mudah, karena tiol terionisasi pada pka lebih rendah daripada alcohol. Anion (15) lebih lunak diabnding R- sehingga lebih nukleofilik terhadap atom karbon sp3. Senyawa akarisida Klorbensida (16) yang dipakai sebagai pembunuh kuman dan semacam kuman, pertama kali lebih disukai didiskoneksi pada sisi alkil daripada sisi aril. Analisis : Sintesis :
26 Urutan Langkah dalam Sintesis Senyawa Aromatik Garis Penuntun Garis penuntun 5 Salah satu kiat untuk memecahkan masalah yang sulit, yaitu dengan suatu tipuan, seperti menambah dua gugus pengarah orto dan para yang terletak meta satu sama lain. Suatu gugus amino sebagai dummy ditambahkan, digunakan untuk mengatur hubungan yang dibutuhkan, kemudian dihilangkan dengan diazotasi dan reduksi. Senyawa asam (8) digunakan dalam sintesis senyawa anestetika lokal seperti propoksikaina (9). Gugus amino tidak dapat dimasukkan dengan nitrasi dari asam salisilat (10), karena atom oksigen akan mengarahkan pada posisi orto dan para, dan akan memberikan isomer yang salah. Problema ini dapat dipecahkan dengan sengaja membuat isomer yang salah, kemudian dilakukan reaksi nitrasi.
27 Analisis: Dalam praktek, sangat baik jika menambahkan gugus alkik pada tahap awal untuk melindungi gugus hidroksil. Sintesis :
28 2. Garis penuntun 6 Cari substituen yang sukar ditambahkan. Strategi yang baik tidak usah memotong substituen ini, gunakan bahan awal yang mengandung substituen ini, sebagai contoh H dan R. Contohnya : 3. Garis penuntun 7 Garis penuntun ini merupakan perluasan dari garis penuntun 6. Cari kombinasi substituen yang telah ada dalam bahan awal yang telah tersedia, terutama bila ugus-gugus tersebut merupakankombinasi yang sukar. Contoh:
29 Garis penuntun ini telah digunakan dalam sintesis senyawa musk ambrette (3) dengan menggunakan bahan awal n-kresol dan sintesis senyawa (7) dari bahan awal bifenil. Contoh lain adalah dalam sintesis senyawa (11), senyawa tersebut diperlukan untuk sintesis obat anti asma Salbutamol (12), dapat dibuat dengan reaksi Friedel-Craft terhadap asam salisilat. Analisis : Sintesis ternyata lebih mudah dari yang diperkirakan, karena asilasi Friedel-Craft dari fenol paling baik dikerjakan dengan perama-tam membuat ester fenolat dan menata ulangnya dengan AlCl3. Ester fenolat yang terbentuk adalah senyawa (13) yang sudah dikenal dengan nama aspirin. Sintesis :
30 4. Garis penuntun 8 Hindarkan urutan yang dapat menuju ke reaksi yang tidak dikehendaki. Contohnya reaksi nitrasi terhadap benzaldehida hanya memberikan produk 50% m-nitro benzaldehida, karena asam nitrat dapat mengoksidasi CH menjadi C2H. untuk mengatasi hal ini adalah dengan menitrai asam benzoat, kemudian mereduksi gugus C2H menjadi CH. Suatu contoh adalah sintesis senyawa (14) yang dibutuhkan untuk membuat senyawa amina (15). Gugus et dibiarkan tinggal pada bahan awal (garis penuntun 6) sehingga ada dua strategi yang hanya berbeda dalam urutan langkah. Analisis : Kedua strategi sesuai dengan pola substitusi, gugus Et merupakan gugus pemberi elektron yang lebih kuat dibandingkan CH2Cl, dan strategi (a) juga sesuai
31 dengan garis penuntun 2. Tetapi CH2Cl dapat dioksidasi dengan mudah sehingga kondisi situasi dapat merusaknya. Strategi (b) memberikan hasil yang baik. Analisis : 5. Garis penuntun 9 Bila posisi orto dan para terlibat, satu strategi dapat diambil yaitu dengan menghalangi salah satu posisi sehingga tidak perlu dilakukan pemisahan isomer. Sebagai contoh adalah sintesis senyawa ester dari fenol (15) yang digunakan sebagai fungisida kebun seperti senyawa dinokap (16). Analisis 1 :
32 Pada analisis 1 di atas pertama kali dilakukan pemotongan gugus nitro, baru diikuti pemotongan gugus alkil, sehingga pada langkah sintesis pertama kali dilakukan reaksi alkilasi Friedel-Craft terhadap fenol. Gugus H fenol merupakan pengarah orto dan para sehingga gugus alkil akan terikat baik pada posisi orto maupun para, maka akan didapatkan senyawa campuran. Apabila urutan pemotongan diganti, yaitu pertama kali dilakukan pemotongan gugus alkil, baru diikuti pemotongan gugus nitro adalah langkah yang tidak biasa. Pada langkah sintesis pertama kali dilakukan reaksi nitrasi terhadap senyawa fenol, sehingga gugus nitro akan terikat pada posisi orto dan para. Pada reaksi selanjutnya dalah reaksi alkilasi terhadap produk nitrasi, gugus alkil hanya akan terikat pada posisi orto terhadap gugus H karena posisi para sudah terhalangi. Secara industrial senyawa dinokap dibuat melalui rute kedua ini. Analisis 2: Sintesis : Terdapat dua reaksi yang dapat memberikan sejumlah besar produksi orto, yaitu penataan ulang Fries(i) dan reaksi Reimer-Tiemann (ii). Reaksi ini dapat digunakan untuk menghailkan senyawa dengan substituen orto saa, tetapi gugus H diperlukan dalam molekul.
33 Tidak semua sembilan garis penuntun ini dapat diterapkan pada setiap peristiwa, memang beberapa terdapat kontradiksi antara satu dengan lain. Untuk itu diperlukan kebijaksanaan, seperti halnya kerja di laboratorium harus trial and error untuk memilih rute reaksi yang baik. Sebagai upaya agar strategi yang kita pilih dapat menghasilkan rute reaksi yang baik, dengan keberhasilan yang tinggi diperlukan pengetahuan tentang arah dan aktivasi dari substituen pada cincin aromatik dalam substitusi elektrofilik aromatik. Pada tabel 1.1 berikut disajikan arah dan aktivasi beberapa gugus/substituen dalam substitusi elektrofilik aromatik. Gugus disusun berdasarkan kemampuan mengaktivasi cincin, gugus yang berada di urutan paling atas merupakan gugus paling mengaktivasi/paling efektif. Umumnya gugus pengaktivasi yang lebih kuat mendominasi yang kurang mengaktivai, dan selektivitas akan lebih besar apabial perbedaan diantaranya lebih besar. Tabel 1.1. Arah dan aktivasi Substituen dalam Substitusi Elektrofilik Aromatik Arah Gugus Aktivasi rto, para R2N, NH2 R, H Alkenil Aril Alkil C2-, H Aktivasi (pemberi elektron) Secara elektronik netral
34 Halida Meta CX3 (X = F, Cl, dst) C2H CR, CH S3H N2 Deaktivasi (penarik elektron) URUTAN LANGKAH SINTESIS SENYAWA ARMATIK GARIS PENUNTUN 1-4 Urutan langkah sintesis senyawa aromatik membahas tentang langkah mana yang harus dikerjakan terlebih dahulu supaya hasil yang diinginkan dapat diperoleh. Garis Penuntun I : Teliti hubungan antara gugus-gugus, cari gugus yang mengarahkan ke posisi yang benar. Cara yang sempurna untuk melaksanakannya adalah mendiskoneksi semua gugus bergantian dan dilihat reaksi balik, apakah akan memberikan orientasi yang benar. Analisis senyawa keton (2) yang berbau rris berikut dapat dilakukan dengan dua didiskoneksi. Analisis :
35 Sintesis : Apabila pemotongan dilakukan di a akan didapatkan reaksi balik dengan orientasi salah, karena gugus keton merupakan pengarah meta. Sedangkan bila pemotongan dilakukan di b akan didapatkan reaksi balik dengan orientasi benar, karena gugus alkil merupakan orto dan para. Garis Penuntun 2 : Apabila ada pilihan, pertama kali potonglah gugus yang paling menarik elektron (dalam langkah sintesis dilakukan pada langkah paling akhir). Gugus penarik elektron (electron withdrawing) akan mendeaktivasi cincin, sehingga sukar untuk menambahkan apapun pada cincin. Senyawa musk ambrette (3), suatu musk sintetik, adalah senyawa esensial dalam parfum yang dipakai untuk mempercepat dan mempertahankan bau, merupakan senyawa aromatik dengan lima substituen pada cincin benzena. Gugus nitro merupakan penarik elektron yang paling kuat, sehinggat dapat dipotong pertama kali. Analisis 1 :
36 Hasil analisis pertama menghasilkann senyawa (4) yang memiliki 3 substituen pada cincin benzena, satu gugus metoksi dan dua gugus alkali. Pemotongan berikutnya dapat dilakukan untuk gugus alkali, terdapat dua kemungkinan pemotongan, yaitu : Analisis 2 : Hasil analisis kedua menghasilkan senyawa m-metoksi toulene, pemotongan berikutnya dapat dilakukan pada ikatan -CH 3.
37 Hasil analisis ketiga menghasilkan senyawa meta kresol sebagai bahan awal, dan sebagai reagen untuk sinton + CH 3 dapat dipergunakan dimetil sulfat (DMS = Me 2 S 4 ). Sintesis : Garis Penuntun 3 : Apabila IGF diperlukan pada waktu sintesis, maka harus diingat bahwa perubahan gugus fungsional akan mengubah arah orientasi. Beberapa contoh adalah : - Gugus Me ( pengarah orto dan para ) oksidasi - CH (pengarah meta) - Gugus Me (pengarah orto dan para ) substitusi - CCl 3 / CF 3 (pengarah meta) - Gugus N 2 (pengarah meta) reduksi - NH 2 (pengarah orto dan para) Sintesis senyawa (5) jelas melibatkan klorinasi baik pada cincin maupun pada gugus metil (IGF). Gugus Cl 3 merupakan gugus pengarah meta, sehingga diperlukan langkah IGF untuk mengubah gugus CCl 3 menjadi CH 3. Gugus CH 3 merupakan pengarah orto dan para sehingga reaksi klorinasi akan menghasilkan orientasi yang benar. Analisis:
38 Langkah sintesis menghasilkan hasil yang memuaskan, dan bila dilanjutkan akann menghasilkan senyawa (6). Sintesis : Garis Penuntun 4 : Banyak gugus dapat ditambahkan melalui reaksi substitusi nukleofilik pada garam diazonium yang dapat dibuat dari amina. Penambahan gugus-gugus lain pada tingkatan amina dianjurkan, oleh karena gugus amino adalah gugus pengarah orto dan para yang kuat. Senyawa asam (7) dipakai di Universitas Hull untuk mempelajari kelakuan kristal cairnya. Cincin benzena yang lain akan mengarahkan ke posisi orto dan para, sehingga untuk mendapatkan klor di posisi tersebut gugus CH harus diganti dengan gugus pengarah orto dan para yang lebih kuat daripada gugus fenil. Gugus yang dapat dipilih adalah gugus amino. Analisis :
39 Dalam langkah sintesis diperlukan pengasilan ( penambahan gugus asil ) gugus amino membentuk amida untuk mencegah klorinasi yang berlebihan. Sintesis :
40 Kemoselektivitas Garis Penuntun 1 sampai 4 Kemoselektivitas adalah memilih untuk dapat mereaksikan salah satu gugus fungsional dari dua gugus yang berada pada satu molekul. Dalam sintesis, masalah kemoselektivitas seringkali ditemukan, misalnya molekul yang akan direaksikan mengandung dua (2) gugus fungsi yang reaktif padahal kita hanya menginginkan salah satu dari kedua gugus fungsi tersebut yang bereaksi, maka kemoselektivitas adalah faktor penting yang harus dipertimbangkan. Beberapa penuntun dalam kemoselektivitas: Garis Penuntun 1 Jika sebuah molekul terdiri dari dua gugus fungsi yang berbeda kereaktifannya, maka gugus yang lebih reaktif selalu dapat direaksikan Misalnya, pada reaksi Parasetamol. Apabila terdapat 2 gugus yang berbeda reaktivitasnya, maka gugus yang lebih reaktif yang akan bereaksi terlebih dahulu. Contoh: CH Y +? H Pertanyaan yang muncul adalah, gugus mana yang teralkilasi? Apakah gugus CCH saja, apakah gugus H saja, ataukah kedua gugus akan teralkilasi? Pada larutan alkilasi (PH > 10) kedua gugus akan terionisasi, tetapi ion fenolat jauh lebih reaktif dibandingkan ion karboksilat, sehingga hanya ion fenol yang teralkilasi. Senyawa asam (1) yang dibutuhkan untuk sintesis anestetik Siklometikaina (2) dapat dianalisis sebagai eter menuju bahan awal yang sederhana. Analisis :
41 NR 2 CH C ester C eter CH H + Y (2) (1) Sintesis yang telah dipblikasikan menggunakan alkil iodida yang merupakan senyawa alkil halida sekunder, sehingga kurang reaktif. Iodida sendiri merupakan gugus pergi yang lebih baik dibandingkan klorida atau bromida. Sintesis: CH C - I alkali + senyawa (1) H - Analgesik parasetamol (3) merupakan senyawa amida sederhana, sudah seharusnya senyawa ini mudah diperoleh dengan reaksi asetilasi p-aminofenol. Dalam reaksi ini dipertahakan fenol tidak terionisasi, sehingga NH 2 akan menjadi lebih reaktif dibandingkan H (NH 3 lebih nukleofilik dibandingkan air, tetapi kurang nukleofilik dibandingkan H - ). Analisa : H H N C N amida H NH 2 IGF N 2 C N H nitrasi H
42 Sintesis: HN 3 N 2 H2, Pd, C H H H Garis Penuntun 2 NH 2 Ac 2 senyawa (3) 79% Apabila terdapat suatu gugus fungsional yang dapat bereaksi dua kali, maka bahan awal dan produk pertama akan berkompetisi untuk menyerang reagen. Reaksi ini akan berhasil baik apabila produk pertama kurang reaktif bila dibanding bahan awal. Senyawa klorida asam (4) dapat digunakan untuk melindungi gugus amino dalam sintesis peptida. Diskoneksi ikatan ester memberikan bahan awal yang sederhana, tetapi dalam sintesis senyawa CCl 2 (fosgene) dimana hanya berekasi sekali dengan PhCH 2 H. Hal ini dapat berhasil karena separuh senyawa ester (4) kurang reaktif karena dapat mengalami konjugasi (5). Analisis : C Ph Cl ester Ph H + CCl 2 R Cl (5) Sintesis :
43 PhCH 2 H CCl 2 Ph Cl Garis Penuntun 3 Apabila diinginkan yang berekasi adalah gugus yang kurang reaktif dari dua gugus fungsional yang berbeda, atau apabila produk pertama dari suatu reaksi mempunyai satu gugus fungsional yang sama atau lebih reaktif dibandingkan bahan awal, maka gugus yang lebih reaktif harus dilindungi dengan gugus pelindung. Asam amini (6) merupakan konstituen protein, mempunyai dua gugus fungsi yaitu CH dan gugus NH 2, dimana gugus NH 2 lebih reaktif dibandingkan gugus CH. Apabila menginginkan gugus CH yang bereaksi maka gugus NH 2 harus dilindungi. Senyawa (4) dapat digunakan sebagai gugus pelindung untuk gugus NH 2. Perlu dicatat bahwa senyawa (4) dapat berekasi dua kali dengan gugus amino, tetapi produk pertama (7) kurang reaktif karena lebih terkonjugasi dibanding senyawa (4). R R NH 2 C 2 H + Ph N C Ph Cl 2 H (6) (4) H (7) Dalam sintesis senyawa tiol, RSH, dengan reaksi alkilasi langsung terhadap H 2 S merupakan reaksi yang tidak baik, hal ini disebabkan karena produk yang terbentuk mempunyai reaktivitas yang relatif sama dengan bahan awal, sehingga reaksi akan berlanjut dan menghasilkan senyawa sulfida, RSH. basa H 2 S H S- RBr basa RSH RS - RBr RSR Untuk membuat senyawa tiol dapat digunakan senyawa tiourea (8) sebagai aktivitas H 2 S yang terlindungi, garam tiouronium (9) tidak mampu bereaksi lebih lanjut dan musah terhidrolisi menjadi tiol.
44 H 2 N S RBr H 2 N + SR H - H 2 H 2 N + HSR Tiol H 2 N H 2 N (8) (9) NH 2 Senyawa Kaptodiamina (10), suatu senyawa sedatif dan trankulaser, dapat dipakai sebagai ilustrasi untuk menerangkan peristiwa sintesis senyawa tiol (11). BuS Ph Ph NMe 2 S SH C S + Cl BuS (10) (11) (12) NMe 2 Senyawa tiol (11) dapat dibuat dengan metode tiourea dari halida (13), dan senyawa ini jelas dapat diperoleh dari produk Friedel-Crafts (14). Diskoneksi selanjutnya akan diperoleh senyawa benzena tiol sebagai bahan awal, senyawa benzena tiol ini tersedia. Analisis 2: Dlam sintesis orientasi reaksi Friedel-Crafts adalah benar, karea pasangan elektron menyendiri pada atom sulfur bivalen akan mengarahkan pada posisi orto, para.
45 Garis Penuntun 4 Apabila terdapat dua gugus yang identik, maka salah satu dari dua gugus yang identik dapat bereaksi apabila produknya kurang reaktif dibanding bahan awal. Sebagai contoj reduksi parsial dari m-dinitrobenena. Reduksi melibatkan penerimaan elektron dari reagen pereduksi. Produk hanya mempunyai satu gugus nitro sebagai penarik elektron, dengan demikian akan tereduksi lebih lambat dibanding bahan awal. Reagen pereduksi yang paling baik untuk tujuan ini adalah natrium hidrogem sulfida, NaHS. HN 3 H 2 S 4 N 2 N 2 N 2 NaHS NH 2 MeH N 2 (15) 90 % Senyawa m-nitroanilina (15) sebagai produk mempunyai kegunaan di dalam sintesis karena gugus amino dapat digunakan untuk mengarahkan reaksi substitusi elektrofilik, dan dia sendiri dapat digunkan oleh nukleofil lain setelah diazotasi. KEMSELEKTIVITAS GARIS PENUNTUN 5 : Satu dari dua gugus fungsional yang identik dapat bereaksi dengan satu ekivalen reagen dengan menggunakan efek statistik. Ini merupakan metode yang tidak dapat
46 dipercaya, tetapi apabila sukses dapat mencegah gugus pelindung atau strategi yang panjang lebur. Kedua gugus harus identik dan harus terpisah satu dengan lainnya. Senyawa diol (20) dapat termonoalkilasi dengan hasil yang cukup dengan menggunakan satu ekivalen natrium dalam silena untuk memproduksi hampir seluruhnya monoanion (21). Walaupun ini akan berada dalam keseimbangan dengan dianion dari (20), dengan menambah alkil halida akan menghasilkan hidroksi eter (22) dalam jumlah cukup dan senyawa ini digunakan dalam sintesis vitamin E. GARIS PENUNTUN 6 : Suatu metode yang lebih dapat dipercaya untuk reaksi dua gugus fungsional yang identik adalah dengan menggunakan derivatnya yang hanya bereaksi satu kali. Sebagai contoh adalah suatu anhidrida siklik, bila anhidrida siklik, bila anhidrida telah terkombinasi satu kali dengan nukleofilik sehingga menghasilkan senyawa (23), maka produk tidak lagi reaktif. Reaksi lebih lanjut dapat tetap mempertahankan perbedaan, yaitu memberikan setengah ester dan setengah asil klorida (24), (23) (24) Reaksi Friedel-Crafts juga efektif terhadap anhidrida, dan hanya bereaksi sekali dengan anhidrida siklik. Senyawa (25) digunakan dalam sintesis senyawa fungisida.
47 + (25) GARIS PENUNTUN 7 : Apabila terdapat dua gugus hampir identik tetapi tidak sempurna identiknya, seperti dalam (26) dan (27), maka jangan merencanakan gugus mana yang akan bereaksi. (26) (27) Pemutusan 2 Gugus C-X Senyawa Karbonil & Senyawa 1,3 Disfungsional Senyawa Karbonil Senyawa Karbonil adalah senyawa yang memiliki tingkat oksidasi lebih tinggi dibanding alkohol. Pada diskoneksi senyawa seperti (31) akan menghasilkan sinton elektrofilik yang berupa kation karbonil (32) suatu spesies yang tidak stabil. Reagen yang paling baik untuk sinton ini adalah senyawa α-halo karbonil (mudah dibuat dan dapat diserang oleh nukleofil) + = Nu Nu - 1,2- dix Hal R + R R (31) (32)
48 Senyawa herbisida 2,4 D (33) merupakan salah satu pestisida yang bayak digunakan, mempunyai diskoneksi yang jelas, dan dengan pendekatan ini akan diperoleh bahan awal senyawa fenol. Analisis : C 2 H Cl Cl (33) 1,2- dix Cl C 2 H + H H C-Cl Cl Cl Pada langkah sintesis, pada tahap klorinasi fenol reaksi dikontrol sehingga akan di dapatkan paling banyak senyawa 2,4-diklorofenol, karena setiap atom klor dapat menurunkan reaktivitas molekul terhadap klorinasi lebih lanjut. Kemudian ditambahkan basa NaH untuk membentuk anion fenol, dan selanjutnya terjadi reaksi substitusi. Sintesis : H H C 2 H 1. NaH 2. ClCH Cl 2C 2H 2,Fe Cl Cl Cl Cl Senyawa ester (34) dengan pendekatan diskoneksi ini akan memberikan senyawa α- halokarbonil (35) yang cukup reaktif. Analisis : R Br - R 1,2- dix + Br Br (34) (35) Reaksi pembentukan ester di atas adalah sederhana untuk dilakukan, dan merupakan cara membuat derivat kristal dari asam karboksilat cari. Sintesis : Br RC 2H R Br NaHC 3
49 Senyawa 1,3-disfungsional Senyawa 1,3-disfungsional hanya dapat didiskoneksikan pada tingkat oksidasi karbonil. Diskoneksi senyawa 1,3-diX senyawa (36) akan menghasilkan sinton (37), reagennya adalah senyawa tidak jenuh (38). Reaksinya dikenal sebagai reaksi Michael, reaksi ini efektif untuk semua senyawa karbonil, sianida, senyawa nitro, dan sebagainya (hampir semua nukleofil). Nu R R R - Nu + + = (37) (38) (36) Senyawa amina (39) dapat dibuat dengan reduksi senyawa sianida (40), reaksinya disebut juga reaksi Michael. Dalam reaksi sintesis ini dipersyaratkan katalis basa, karena R - merupakan nukleofil yang lebih baik daripada RH. IGF R NH R 2 reduksi (39) (40) CN - R + CN Contoh lain sebagai berikut : H NaMe CN CN H 2 Rh, Al 2 3 NH 2 Senyawa asetal (41) dengan diskoneksi 1,1-diX akan didapatkan senyawa β-bromo aldehida, dan senyawa β-bromo aldehida ini dapat diperoleh dengan reaksi adisi Michael dari Br - pada akrolein (42). 1,1-diX + Br H asetal Br H H (41) (42) Br - Semua derivat akrilat yang sederhana CH 2 =CH.CR (R=H, R, H, Me) tersedia secara komersial, karena mereka merupakan monomer dariaman polimer akrilik diperoleh. Dalam sintesis senyawa asetal (41) diperlukan katalis asam, sebab Br - merupakan nukleofil yag sangat lemah.
50 H H HBr (41) Br H H + Dalam diskoneksi senyawa 1,3-diX tidak pada tingkat oksidasi karbonil, pertama-tama yang harus dilakukan adalah mengubah tingkat oksidasi dengan IGIF. Apabila molekul target tidak mengandung substituen oksigen, maka harus diadakan atom oksigen dengan reaksi subtitusi. PEMUTUSAN DUA GUGUS C X DALAM SINTESIS SENYAWA RGANIK A. Senyawa 1,1-difungsional Mengenal asetat merupakan problem bagi ahli kimia dalam praktik. Molekul (1) jelas suatu asetat dan diskoneksi pertama adalah sebagi berikut : Analisis (1) Kedua material start tersedia, glikol (2) merupakan reagen pembentuk asetal yang efisien dan murah. Sintesis Mengenal kembali asetal dalam frontalin (3), suatu feromon dari kumbang cemara tidaklah mudah, namun senyawa tersebut penting untuk dicari dua atom oksigen yang diikat pada atom karbo yang sama ( dalam 3a) dan asetal didiskoneksikan sebelum mempertimbangkan tiap langkah lain. Analisis
51 Pembentukan asetal intramolekular sedemikian menguntungkan sehinhha setiap usaha untuk membuat (4) segera menuntun ke frontalin. Problema Mengenal asetal dalam MTs berikut dan melakukan diskoneksi pertama. Jawab : Atom karbon asetal ditandai
52 Problema Mensugestikan sintesis bagi konstituen parfum Jawab : disini terdapat dua asetal, yang masing-masing dapat pertama didiskoneksikan, walaupun tidak keduanya, karena problema khemoselektivitas akan timbul. Dan piperonal (9) akan digunakan sebagai intermediate. Analisis
53 Asetol (10) tersedia walu mahal dan dibuat dari katekhol serta CH 2 X 2 (X = Cl, Br, I) dalam basa 52 sebagai ganti metoda yang biasa digunakan. Asetal final dibuat dengn metode terkatalisa-asam yang biasa dengann menggunakan orto-format HC (Et) 3 sebagai agen pendehidrasi. B. Senyawa 1,2-difungsional Banyak antiseptik merupakan garam ammonium kuarterner dengan aksi seperti detergen dan Benzetonium klorida (11) adalah sangat efisien. Gugus benzil dapat ditambahkan dengan alkilasi dari (12) yang mengandung dua set hubungan 1,2-diX. Analisis 1
54 Diskoneksi pada setiap posisi ini dimungkinkan (12a). Kemungkinan lebih disukai apabila didiskoneksi pertama di pusat (b atau c) tetapi akan berakhir dengan Me 2 NH, dua molekul etilena oksioda, dan fenol (13) sebagai material start. Analisis 2 Fenol adalah produk Friedel-Crefts dan katiion yang dikehendaki (14), paling memuaskan diperoleh dari diiso-butilena suatu campuran dari (15) dan (16) yang tersedia secara industri dari dimerisasi Me 2 C=CH 2. Analisis 3 Sintesis 54 yang dipatenkan mengkombinasikan reagen-reagen dalam urutan yang berbeda dan mempercayakan pada kontrol statistik khemoselektivitas dalam reaksi (17) dengan (13). Keuntungannya adalah bahwa (17) yang simetris dapat dibuat dari etilena klorohidrin. Sintesis 54,55
55 Problema Dua problema dalam seksi ini mengunakan nukleofil sulfur karena mereka tidak begitu tuntas ditampilkan dalam buku utama. 1. Alkohol (18) digunakan dalam industri demetron, suatu keluarga insektisida sistemik. Bagaimana dapa dibuat Jawab : Analisis Sintesis Etilena klorohidrin dalam basa dapat digunakakn sebagai ganti etilena oksida.
56 Penolak coro (18A) dibuat dari tiol dengan etlena oksida 2. Intermediate (19) dibutuhkan untuk sintesis tianaftalena 57 (20). Bagaimana membuat (19) Jawab : Diskoneksi Friedel-Crafts menampakkan senyawa 1,2-diX (21) yang dibuat secara mudah dari tiol (22) dan asam kloroasetat. Tiol (22) dapat dibuat dengan rute tio urea. Analisis Sintesis 59 C. Senyawa 1,3-difungsional
57 Senyawa (29) diperlukan untuk siklisasi secara fotokimia menjadi (30). Diskoneksi eter yang jelas kelihatannya sangat memberi harapan tetapi eksperimen telah memperlihatkan bahwa sukar untuk mengalkilasi (31) tanpa polimerisasi. Analisis 1 Diskoneksi 1,3-diX sebagai pengganti (29b) memerlukan adisi allil alkohol pada enona (32) dan berlangsung dengan baik oleh katalis BF 3. Analisis 2 Sintesis 61 DAFTAR PUSTAKA Anonim. Diakses dari pada 29 September 2014 pukul WIB. Budimarwati., (2012). Diktat Kuliah Kimia rganiksintesis.yogyajarta: FMIPA UNY.
58 Firdaus Alkil Halida. Makassar : UNHAS Press. Sobry Khairus. Diaskes dari pada 15 September 2014 pukul WIB. Stuart Warren Buku Kerja untuk Sintesis rganik Pendekatan Diskoneksi. Yogyakarta : UGM Press. Warren, Stuart., (1995). Sintesisrganik: PendekatanDiskoneksi. (diterjemahkanolehsamhoedi R). Yogyakarta: Gajah Mada University Press.
BASIC PRINCIPLES: SYNTHESIS OF AROMATIC COMPOUNDS
 BASIC PRINCIPLES: SYNTHESIS F ARMATIC CMPUNDS Pada senyawa aromatik diskoneksi biasanya sering dilakukan pada ikatan yang menghubungkan antara cincin aromatik dengan bagian lain dari molekul X Review Retrosynthesis
BASIC PRINCIPLES: SYNTHESIS F ARMATIC CMPUNDS Pada senyawa aromatik diskoneksi biasanya sering dilakukan pada ikatan yang menghubungkan antara cincin aromatik dengan bagian lain dari molekul X Review Retrosynthesis
KIMIA. Sesi. Benzena A. STRUKTUR DAN SIFAT BENZENA. Benzena merupakan senyawa hidrokarbon dengan rumus molekul C 6 H 6
 KIMIA KELAS XII IPA - KURIKULUM GABUNGAN 18 Sesi NGAN Benzena Benzena merupakan senyawa hidrokarbon dengan rumus molekul C 6 H 6 dengan struktur berbentuk cincin (siklik) segienam beraturan. Struktur kimia
KIMIA KELAS XII IPA - KURIKULUM GABUNGAN 18 Sesi NGAN Benzena Benzena merupakan senyawa hidrokarbon dengan rumus molekul C 6 H 6 dengan struktur berbentuk cincin (siklik) segienam beraturan. Struktur kimia
Serangan elektrofil pada posisi orto
 Serangan elektrofil pada posisi orto O Y + O Y O Y O Y I II III O O Y Y Serangan elektrofil pada posisi meta Serangan elektrofil pada posisi para Pada reaksi substitusi elektrofilik fenol ini terlihat
Serangan elektrofil pada posisi orto O Y + O Y O Y O Y I II III O O Y Y Serangan elektrofil pada posisi meta Serangan elektrofil pada posisi para Pada reaksi substitusi elektrofilik fenol ini terlihat
Secara umum terdapat 4 tipe reaksi kimia organik: 1. Reaksi substitusi (Penggantian)
 Secara umum terdapat 4 tipe reaksi kimia organik: 1. Reaksi substitusi (Penggantian) Suatu atom/gugus di dalam suatu senyawa diganti oleh suatu atom/gugus lain dari senyawa yang lain. Konsep dasarnya adalah
Secara umum terdapat 4 tipe reaksi kimia organik: 1. Reaksi substitusi (Penggantian) Suatu atom/gugus di dalam suatu senyawa diganti oleh suatu atom/gugus lain dari senyawa yang lain. Konsep dasarnya adalah
BAB II TINJAUAN PUSTAKA. akan berlangsung selama sintesis, serta alat-alat yang diperlukan untuk sintesis.
 II TINJUN PUSTK 2.1 Rancangan nalisis Dalam sintesis suatu senyawa kimia atau senyawa obat yang baik, diperlukan beberapa persiapan. Persiapan tersebut antara lain berupa bahan dasar sintesis, pereaksi,
II TINJUN PUSTK 2.1 Rancangan nalisis Dalam sintesis suatu senyawa kimia atau senyawa obat yang baik, diperlukan beberapa persiapan. Persiapan tersebut antara lain berupa bahan dasar sintesis, pereaksi,
bemffums.blogspot.com
 bemffums.blogspot.com Amina Didasarkan pada: McMurry s Organic Chemistry, th edisi 6 24.1 Naming Amines Amina tersubstitusi alkil (alkilamina) atau tersubstitusi aril (arilamina) Klasifikasi: 1 (RNH2),
bemffums.blogspot.com Amina Didasarkan pada: McMurry s Organic Chemistry, th edisi 6 24.1 Naming Amines Amina tersubstitusi alkil (alkilamina) atau tersubstitusi aril (arilamina) Klasifikasi: 1 (RNH2),
BAB 10. Aromatisitas, Benzena, dan Benzena Tersubstitusi. Tabel Struktur dan nama-nama benzene yang umum
 BAB 10 Aromatisitas, Benzena, dan Benzena Tersubstitusi 10.1 Tata Nama Benzena Tersubstitusi Benzena tersubstitusi diberi nama dengan awalan orto, meta, para dan tidak dengan nomor-nomor posisi. Awalan
BAB 10 Aromatisitas, Benzena, dan Benzena Tersubstitusi 10.1 Tata Nama Benzena Tersubstitusi Benzena tersubstitusi diberi nama dengan awalan orto, meta, para dan tidak dengan nomor-nomor posisi. Awalan
TURUNAN ASAM KARBOKSILAT DAN REAKSI SUBSTITUSI ASIL NUKLEOFILIK
 BAB 4 TURUNAN ASAM KARBOKSILAT DAN REAKSI SUBSTITUSI ASIL NUKLEOFILIK Asam karboksilat hanya merupakan salah satu anggota kelas turunan asil, RCOX, di mana substituen X mungkin oksigen, halogen, nitrogen
BAB 4 TURUNAN ASAM KARBOKSILAT DAN REAKSI SUBSTITUSI ASIL NUKLEOFILIK Asam karboksilat hanya merupakan salah satu anggota kelas turunan asil, RCOX, di mana substituen X mungkin oksigen, halogen, nitrogen
RANCANGAN PEMBELAJARAN KBK
 RANCANGAN PEMBELAJARAN KBK Nama / Kode Matakuliah : Kimia Organik Sintesis II / 305H3102 Komptensi Sasaran : 1. Kompetensi Utama : Kemampuan dalam menerapkan pengetahuan dasar Kimia. Kemampuan dan keterampilan
RANCANGAN PEMBELAJARAN KBK Nama / Kode Matakuliah : Kimia Organik Sintesis II / 305H3102 Komptensi Sasaran : 1. Kompetensi Utama : Kemampuan dalam menerapkan pengetahuan dasar Kimia. Kemampuan dan keterampilan
BAB I PENDAHULUAN. Dari uraian latar belakang diatas dirumuskan permasalahan sebagai berikut:
 BAB I PENDAHULUAN 1.1 Latar belakang Dalam kehidupan sehari-hari kita banyak menjumpai senyawa, baik senyawa organik maupun anorganik. Senyawa organik sangat banyak jenisnya, sehingga perlu adanya penggolongan
BAB I PENDAHULUAN 1.1 Latar belakang Dalam kehidupan sehari-hari kita banyak menjumpai senyawa, baik senyawa organik maupun anorganik. Senyawa organik sangat banyak jenisnya, sehingga perlu adanya penggolongan
REAKSI SUBSTITUSI ALFA KARBONIL
 BAB 5 REAKSI SUBSTITUSI ALFA KARBONIL Dalam bab ini akan dibahas mengenai reaksi substitusi alfa. Ciri utama dari reaksi ini adalah terjadi melalui pembentukan intermediet enol atau ion enolat. 5.1. Keto-enol
BAB 5 REAKSI SUBSTITUSI ALFA KARBONIL Dalam bab ini akan dibahas mengenai reaksi substitusi alfa. Ciri utama dari reaksi ini adalah terjadi melalui pembentukan intermediet enol atau ion enolat. 5.1. Keto-enol
BENZENA. Memahami senyawa organik dan reaksinya, benzena dan turunannya, dan makromolekul.
 Standar Kompetensi: BENZENA Memahami senyawa organik dan reaksinya, benzena dan turunannya, dan makromolekul. Kompetensi Dasar: Mendeskripsikan struktur, cara penulisan, tata nama, sifat, dan kegunaan
Standar Kompetensi: BENZENA Memahami senyawa organik dan reaksinya, benzena dan turunannya, dan makromolekul. Kompetensi Dasar: Mendeskripsikan struktur, cara penulisan, tata nama, sifat, dan kegunaan
REAKSI PENATAAN ULANG. perpindahan (migrasi) tersebut adalah dari suatu atom ke atom yang lain yang
 EAKSI PENATAAN ULANG eaksi penataan ulang adalah reaksi penataan kembali struktur molekul untuk membentuk struktur molekul yang baru yang berbeda dengan struktur molekul yang semula. eaksi ini dapat terjadi
EAKSI PENATAAN ULANG eaksi penataan ulang adalah reaksi penataan kembali struktur molekul untuk membentuk struktur molekul yang baru yang berbeda dengan struktur molekul yang semula. eaksi ini dapat terjadi
ETER dan EPOKSIDA. Oleh : Dr. Yahdiana Harahap, MS
 ETER dan EPOKSIDA Oleh : Dr. Yahdiana Harahap, MS ETER Senyawa yang mempunyai 2 gugus organik melekat pada atom O tunggal R1 O R 2 atau Ar O R Atau Ar O Ar Ket : R : alkil Ar : fenil atau gugus aromatis
ETER dan EPOKSIDA Oleh : Dr. Yahdiana Harahap, MS ETER Senyawa yang mempunyai 2 gugus organik melekat pada atom O tunggal R1 O R 2 atau Ar O R Atau Ar O Ar Ket : R : alkil Ar : fenil atau gugus aromatis
BAB IX AROMATISITAS, BENZENA, DAN BENZENA TERSUBSTITUSI
 BAB IX AROMATISITAS, BENZENA, DAN BENZENA TERSUBSTITUSI Benzena diisolasi tahun 1825 oleh Michael Faraday dan residu berminyak yang terimbun dalam pipa induk gas di London. Sampai 1940 ter batubara sebagai
BAB IX AROMATISITAS, BENZENA, DAN BENZENA TERSUBSTITUSI Benzena diisolasi tahun 1825 oleh Michael Faraday dan residu berminyak yang terimbun dalam pipa induk gas di London. Sampai 1940 ter batubara sebagai
AROMATISITAS, BENZENA DAN BENZENA TERSUBSTITUSI ACHMAD SYAHRANI ORGANIC CHEMISTRY, FESSENDEN DAN FESSENDEN, THIRD EDITION
 AROMATISITAS, BENZENA DAN BENZENA TERSUBSTITUSI ACHMAD SYAHRANI ORGANIC CHEMISTRY, FESSENDEN DAN FESSENDEN, THIRD EDITION 1 BENZENA PERTAMA KALI DIISOLASI OLEH MICHAEL FARADAY, 1825 DARI RESIDU BERMINYAK
AROMATISITAS, BENZENA DAN BENZENA TERSUBSTITUSI ACHMAD SYAHRANI ORGANIC CHEMISTRY, FESSENDEN DAN FESSENDEN, THIRD EDITION 1 BENZENA PERTAMA KALI DIISOLASI OLEH MICHAEL FARADAY, 1825 DARI RESIDU BERMINYAK
REAKTIVITAS SENYAWA AROMATIK. DR. Bambang Cahyono
 REAKTIVITAS SENYAWA AROMATIK DR. Bambang Cahyono PERBEDAAN IKATAN RANGKAP BENZENA DAN ALKENA AKIBAT LAIN AKIBAT ADANYA STABILITAS PADA AROMATIK Senyawa aromatik distabilkan oleh stabilitas aromatik Mengingat
REAKTIVITAS SENYAWA AROMATIK DR. Bambang Cahyono PERBEDAAN IKATAN RANGKAP BENZENA DAN ALKENA AKIBAT LAIN AKIBAT ADANYA STABILITAS PADA AROMATIK Senyawa aromatik distabilkan oleh stabilitas aromatik Mengingat
KIMIAWI SENYAWA KARBONIL
 BAB 1 KIMIAWI SENYAWA KARBONIL Senyawa karbonil adalah kelompok senyawaan organik yang mengandung gugus karbonil, C=O, gugus fungsional yang paling penting dalam kimia organik. Senyawa karbonil ada di
BAB 1 KIMIAWI SENYAWA KARBONIL Senyawa karbonil adalah kelompok senyawaan organik yang mengandung gugus karbonil, C=O, gugus fungsional yang paling penting dalam kimia organik. Senyawa karbonil ada di
MODUL KIMIA SMA IPA Kelas 12
 A. BENZENA 1. Rumus a. Rumus molekul : C 6H 6 b. Rumus bangun : 2. Hibridisasi Struktur Kekule, setiap atom C dalam benzena membentuk 3 ikatan sigma = ( sp 2 ) 3 dan 1 ikatan phi = ( p-p ) 1. Hal ini dapat
A. BENZENA 1. Rumus a. Rumus molekul : C 6H 6 b. Rumus bangun : 2. Hibridisasi Struktur Kekule, setiap atom C dalam benzena membentuk 3 ikatan sigma = ( sp 2 ) 3 dan 1 ikatan phi = ( p-p ) 1. Hal ini dapat
SENYAWA AROMATIK. Tim dosen kimia dasar FTP
 SENYAWA AROMATIK Tim dosen kimia dasar FTP SENYAWA AROMATIK SIFAT-SIFAT Senyawa dengan aroma tertentu Senyawa siklik yang mengandung ikatan rangkap berselang seling (konjugasi) Bersifat non polar Banyak
SENYAWA AROMATIK Tim dosen kimia dasar FTP SENYAWA AROMATIK SIFAT-SIFAT Senyawa dengan aroma tertentu Senyawa siklik yang mengandung ikatan rangkap berselang seling (konjugasi) Bersifat non polar Banyak
PENGGOLONGAN SENYAWA ORGANIK DAN DASAR-DASAR REAKSI ORGANIK
 ( Word to PDF Converter - Unregistered ) http://www.word-to-pdf-converter.net PENGGOLONGAN SENYAWA ORGANIK DAN DASAR-DASAR REAKSI ORGANIK PENDAHULUAN Oleh: C. Budimarwanti, M.Si Senyawa organik terlibat
( Word to PDF Converter - Unregistered ) http://www.word-to-pdf-converter.net PENGGOLONGAN SENYAWA ORGANIK DAN DASAR-DASAR REAKSI ORGANIK PENDAHULUAN Oleh: C. Budimarwanti, M.Si Senyawa organik terlibat
SENYAWA ORGANIK HIDROKARBON DENGAN KARBON ELEKTROFILIK
 SENYAWA ORGANIK HIDROKARBON DENGAN KARBON ELEKTROFILIK Aromatisitas Seperti yang dibicarakan pada kimia organik I., senyawa hidrokarbon adalah kelompok zat organik yang hanya terdiri dari unsur karbon
SENYAWA ORGANIK HIDROKARBON DENGAN KARBON ELEKTROFILIK Aromatisitas Seperti yang dibicarakan pada kimia organik I., senyawa hidrokarbon adalah kelompok zat organik yang hanya terdiri dari unsur karbon
berupa ikatan tunggal, rangkap dua atau rangkap tiga. o Atom karbon mempunyai kemampuan membentuk rantai (ikatan yang panjang).
 HIDROKARBON Senyawa hidrokarbon merupakan senyawa karbon yang paling sederhana. Dari namanya, senyawa hidrokarbon adalah senyawa karbon yang hanya tersusun dari atom hidrogen dan atom karbon. Dalam kehidupan
HIDROKARBON Senyawa hidrokarbon merupakan senyawa karbon yang paling sederhana. Dari namanya, senyawa hidrokarbon adalah senyawa karbon yang hanya tersusun dari atom hidrogen dan atom karbon. Dalam kehidupan
MAKALAH PRAKTIKUM KIMIA DASAR REAKSI-REAKSI ALKOHOL DAN FENOL
 MAKALAH PRAKTIKUM KIMIA DASAR REAKSI-REAKSI ALKOHOL DAN FENOL Oleh : ZIADUL FAIEZ (133610516) PROGRAM STUDI TEKNIK GEOLOGI FAKULTAS TEKNIK UNIVERSITAS ISLAM RIAU PEKANBARU 2015 BAB I PENDAHULUAN LatarBelakang
MAKALAH PRAKTIKUM KIMIA DASAR REAKSI-REAKSI ALKOHOL DAN FENOL Oleh : ZIADUL FAIEZ (133610516) PROGRAM STUDI TEKNIK GEOLOGI FAKULTAS TEKNIK UNIVERSITAS ISLAM RIAU PEKANBARU 2015 BAB I PENDAHULUAN LatarBelakang
Chapter 20 ASAM KARBOKSILAT
 Chapter 20 ASAM KARBOKSILAT Pengantar Gugus fungsi dari asam karboksilat terdiri atas ikatan C=O dengan OH pada karbon yang sama. Gugus karboksil biasanya ditulis -COOH. Asam alifatik memiliki gugus alkil
Chapter 20 ASAM KARBOKSILAT Pengantar Gugus fungsi dari asam karboksilat terdiri atas ikatan C=O dengan OH pada karbon yang sama. Gugus karboksil biasanya ditulis -COOH. Asam alifatik memiliki gugus alkil
BENZENA DAN TURUNANNYA
 BENZENA DAN TURUNANNYA 6 benzena dan turunannya A. RUMUS MOLEKUL DAN SIFAT KHAS BENZENA B. TATA NAMA BENZENA C. KEGUNAAN TURUNAN BENZENA Kata aromatik semula digunakan untuk menggambarkan zat-zat berbau
BENZENA DAN TURUNANNYA 6 benzena dan turunannya A. RUMUS MOLEKUL DAN SIFAT KHAS BENZENA B. TATA NAMA BENZENA C. KEGUNAAN TURUNAN BENZENA Kata aromatik semula digunakan untuk menggambarkan zat-zat berbau
BENZEN DAN AROMATISITAS. Oleh : Dr. Yahdiana Harahap, MS
 BENZEN DAN AROMATISITAS Oleh : Dr. Yahdiana Harahap, MS BENZEN DAN AROMATISITAS BENZENA DAN AROMATISITAS C6H6 Hidrokarbon tidak jenuh ikatan rangkap beresonisasi Senyawa aromatis benzena & senyawa-senyawa
BENZEN DAN AROMATISITAS Oleh : Dr. Yahdiana Harahap, MS BENZEN DAN AROMATISITAS BENZENA DAN AROMATISITAS C6H6 Hidrokarbon tidak jenuh ikatan rangkap beresonisasi Senyawa aromatis benzena & senyawa-senyawa
OAL TES SEMESTER II. I. Pilihlah huruf a, b, c, d, atau e pada jawaban yang tepat!
 KIMIA XII SMA 249 S AL TES SEMESTER II I. Pilihlah huruf a, b, c, d, atau e pada jawaban yang tepat! 1. Suatu senyawa karbondioksida dengan tembaga pijar dan hasil oksidasinya diuji dengan pereaksi fehling
KIMIA XII SMA 249 S AL TES SEMESTER II I. Pilihlah huruf a, b, c, d, atau e pada jawaban yang tepat! 1. Suatu senyawa karbondioksida dengan tembaga pijar dan hasil oksidasinya diuji dengan pereaksi fehling
REAKSI-REAKSI ALKOHOL DAN FENOL
 REAKSI-REAKSI ALKHL DAN FENL TUJUAN Tujuan dari Percobaan ini adalah: 1. Membedakan alkohol dengan fenol berdasarkan reaksinya dengan asam karboksilat 2. Membedakan alkohol dan fenol berdasarkan reaksi
REAKSI-REAKSI ALKHL DAN FENL TUJUAN Tujuan dari Percobaan ini adalah: 1. Membedakan alkohol dengan fenol berdasarkan reaksinya dengan asam karboksilat 2. Membedakan alkohol dan fenol berdasarkan reaksi
ALKOHOL DAN ETER. Tim Dosen Kimia Dasar II/ Kimia Organik
 ALKOHOL DAN ETER Tim Dosen Kimia Dasar II/ Kimia Organik 1 SUMBER ALKOHOL DAN ETER Alkohol didapatkan dengan berbagai cara yaitu dapat dibuat dengan cara fermentasi terhadap bahan bahan yang mengandung
ALKOHOL DAN ETER Tim Dosen Kimia Dasar II/ Kimia Organik 1 SUMBER ALKOHOL DAN ETER Alkohol didapatkan dengan berbagai cara yaitu dapat dibuat dengan cara fermentasi terhadap bahan bahan yang mengandung
(2) kekuatan ikatan yang dibentuk untuk karbon;
 Reaksi Subsitusi Nukleofilik Alifatik Reaksi yang berlangsung karena penggantian satu atau lebih atom atau gugus dari suatu senyawa oleh atom atau gugus lain disebut reaksi substitusi. Bila reaksi substitusi
Reaksi Subsitusi Nukleofilik Alifatik Reaksi yang berlangsung karena penggantian satu atau lebih atom atau gugus dari suatu senyawa oleh atom atau gugus lain disebut reaksi substitusi. Bila reaksi substitusi
Senyawa Alkohol dan Senyawa Eter. Sulistyani, M.Si
 Senyawa Alkohol dan Senyawa Eter Sulistyani, M.Si sulistyani@uny.ac.id Konsep Dasar Senyawa Organik Senyawa organik adalah senyawa yang sumber utamanya berasal dari tumbuhan, hewan, atau sisa-sisa organisme
Senyawa Alkohol dan Senyawa Eter Sulistyani, M.Si sulistyani@uny.ac.id Konsep Dasar Senyawa Organik Senyawa organik adalah senyawa yang sumber utamanya berasal dari tumbuhan, hewan, atau sisa-sisa organisme
2. Substitusi dengan kelompok halogen OH. Halogen gugus-oh diganti dengan menggunakan pereaksi atau PCl5 PCL3:
 Analisa gugus fungsi Reaksi Kimia adalah suatu perubahan dari suatu senyawa atau molekul menjadi senyawa atau molekul lain. Reaksi yang terjadi pada senyawa anorganik biasanya reaksi antar ion, sedangkan
Analisa gugus fungsi Reaksi Kimia adalah suatu perubahan dari suatu senyawa atau molekul menjadi senyawa atau molekul lain. Reaksi yang terjadi pada senyawa anorganik biasanya reaksi antar ion, sedangkan
BAB 17 ALKOHOL DAN FENOL
 Slaid kuliah Kimia Organik I untuk mhs S1 Kimia semester 3 BAB 17 ALKOHOL DAN FENOL Bagian Kimia Organik Departemen Kimia FMIPA-IPB TIU TIK 1 Daftar Pustaka: Fessenden RJ, Fessenden JS. 1998. Organic Chemistry.
Slaid kuliah Kimia Organik I untuk mhs S1 Kimia semester 3 BAB 17 ALKOHOL DAN FENOL Bagian Kimia Organik Departemen Kimia FMIPA-IPB TIU TIK 1 Daftar Pustaka: Fessenden RJ, Fessenden JS. 1998. Organic Chemistry.
Pengantar KO2 (Kimia Organik Gugus Fungsi)
 Pengantar KO2 (Kimia Organik Gugus Fungsi) Sasaran : pengenalan gugus fungsi. Mengetahui sifat fisika dan kimia suatu bahan yang digunakan sebagai obat, kosmetika, bahan makanan dan minuman. Untuk digunaka
Pengantar KO2 (Kimia Organik Gugus Fungsi) Sasaran : pengenalan gugus fungsi. Mengetahui sifat fisika dan kimia suatu bahan yang digunakan sebagai obat, kosmetika, bahan makanan dan minuman. Untuk digunaka
Materi Penunjang Media Pembelajaran Kimia Organik SMA ALKENA
 ALKENA Nama lain alkena adalah olefin atau senyawa vinil. Alkena termasuk senyawa organik tak jenuh. Alkena merupakan senyawa yang relatif stabil, akan tetapi lebih reaktif dari alkana karena terdapatnya
ALKENA Nama lain alkena adalah olefin atau senyawa vinil. Alkena termasuk senyawa organik tak jenuh. Alkena merupakan senyawa yang relatif stabil, akan tetapi lebih reaktif dari alkana karena terdapatnya
LAPORAN PRAKTIKUM KIMIA ORGANIK (KI2051)
 LAPORAN PRAKTIKUM KIMIA ORGANIK (KI2051) PERCOBAAN 5 Alkohol dan Fenol: Sifat Fisik dan Reaksi Kimia DIAH RATNA SARI 11609010 KELOMPOK I Tanggal Percobaan : 27 Oktober 2010 Shift Rabu Siang (13.00 17.00
LAPORAN PRAKTIKUM KIMIA ORGANIK (KI2051) PERCOBAAN 5 Alkohol dan Fenol: Sifat Fisik dan Reaksi Kimia DIAH RATNA SARI 11609010 KELOMPOK I Tanggal Percobaan : 27 Oktober 2010 Shift Rabu Siang (13.00 17.00
Senyawa Halogen Organik (organohalogen) Tim Dosen Kimia FTP - UB
 Senyawa alogen Organik (organohalogen) Tim Dosen Kimia FTP - UB Pendahuluan Organohalogen sebagai pelarut, insektisida, dan bahan sintesis organik. Beberapa organohalogen bersifat racun, sehingga harus
Senyawa alogen Organik (organohalogen) Tim Dosen Kimia FTP - UB Pendahuluan Organohalogen sebagai pelarut, insektisida, dan bahan sintesis organik. Beberapa organohalogen bersifat racun, sehingga harus
BAB 7 HIDROKARBON DAN MINYAK BUMI
 BAB 7 HIDROKARBON DAN MINYAK BUMI A. Kekhasan / Keunikan Atom Karbon o Terletak pada golongan IVA dengan Z = 6 dan mempunyai 4 elektron valensi. o Untuk mencapai konfigurasi oktet maka atom karbon mempunyai
BAB 7 HIDROKARBON DAN MINYAK BUMI A. Kekhasan / Keunikan Atom Karbon o Terletak pada golongan IVA dengan Z = 6 dan mempunyai 4 elektron valensi. o Untuk mencapai konfigurasi oktet maka atom karbon mempunyai
VI Benzena dan Turunannya
 Bab VI Benzena dan Turunannya Tujuan Pembelajaran Setelah mempelajari bab ini Anda dapat memahami tentang struktur, tata nama, sifat, dan kegunaan benzena dan turunannya. Benzena dan turunannya (benzena
Bab VI Benzena dan Turunannya Tujuan Pembelajaran Setelah mempelajari bab ini Anda dapat memahami tentang struktur, tata nama, sifat, dan kegunaan benzena dan turunannya. Benzena dan turunannya (benzena
SINTESIS SENYAWA BIBENZIL DARI BAHAN AWAL VANILIN MELALUI REAKSI WITTIG DAN HIDROGENASI KATALITIK
 Sintesis Senyawa Bibenzil.. (. Budimarwanti) SINTESIS SENYAWA BIBENZIL DAI BAHAN AWAL VANILIN MELALUI EAKSI WITTIG DAN HIDGENASI KATALITIK. Budimarwanti Jurdik Kimia FMIPA Universitas Negeri Yogyakarta
Sintesis Senyawa Bibenzil.. (. Budimarwanti) SINTESIS SENYAWA BIBENZIL DAI BAHAN AWAL VANILIN MELALUI EAKSI WITTIG DAN HIDGENASI KATALITIK. Budimarwanti Jurdik Kimia FMIPA Universitas Negeri Yogyakarta
benzena dan turunannya
 6 benzena dan turunannya A. RUMUS MOLEKUL DAN SIFAT KAS BENZENA B. TATA NAMA BENZENA. KEGUNAAN TURUNAN BENZENA Kata aromatik semula digunakan untuk menggambarkan zat-zat berbau harum dari buah-buahan,
6 benzena dan turunannya A. RUMUS MOLEKUL DAN SIFAT KAS BENZENA B. TATA NAMA BENZENA. KEGUNAAN TURUNAN BENZENA Kata aromatik semula digunakan untuk menggambarkan zat-zat berbau harum dari buah-buahan,
KIMIA. Sesi HIDROKARBON (BAGIAN II) A. ALKANON (KETON) a. Tata Nama Alkanon
 KIMIA KELAS XII IPA - KURIKULUM GABUNGAN 16 Sesi NGAN HIDROKARBON (BAGIAN II) Gugus fungsional adalah sekelompok atom dalam suatu molekul yang memiliki karakteristik khusus. Gugus fungsional adalah bagian
KIMIA KELAS XII IPA - KURIKULUM GABUNGAN 16 Sesi NGAN HIDROKARBON (BAGIAN II) Gugus fungsional adalah sekelompok atom dalam suatu molekul yang memiliki karakteristik khusus. Gugus fungsional adalah bagian
AMINA dan HETEROSIKLIK
 Slaid kuliah Kimia Organik II AMINA dan HETEROSIKLIK Bagian Kimia Organik Departemen Kimia FMIPA-IPB Amina tersebar luas dalam organisme hidup protein dan asam nukleat. trimetilamina nikotina kokaina Insektisida
Slaid kuliah Kimia Organik II AMINA dan HETEROSIKLIK Bagian Kimia Organik Departemen Kimia FMIPA-IPB Amina tersebar luas dalam organisme hidup protein dan asam nukleat. trimetilamina nikotina kokaina Insektisida
LAPORAN PRAKTIKUM KIMIA ORGANIK I PERCOBAAN III SIFAT-SIFAT KIMIA HIDROKARBON
 LAPORAN PRAKTIKUM KIMIA ORGANIK I PERCOBAAN III SIFAT-SIFAT KIMIA HIDROKARBON OLEH NAMA : HABRIN KIFLI HS. STAMBUK : F1C1 15 034 KELOMPOK ASISTEN : VI (ENAM) : HERIKISWANTO LABORATORIUM KIMIA FAKULTAS
LAPORAN PRAKTIKUM KIMIA ORGANIK I PERCOBAAN III SIFAT-SIFAT KIMIA HIDROKARBON OLEH NAMA : HABRIN KIFLI HS. STAMBUK : F1C1 15 034 KELOMPOK ASISTEN : VI (ENAM) : HERIKISWANTO LABORATORIUM KIMIA FAKULTAS
Kelompok G : Nicolas oerip ( ) Filia irawati ( ) Ayndri Nico P ( )
 Kelompok G : Nicolas oerip (5203011028) Filia irawati (5203011029) Ayndri Nico P (5203011040) Mempelajari reaksi esterifikasi Apa sih reaksi esterifikasi itu? Bagaimana reaksi esterifikasi itu? Reaksi
Kelompok G : Nicolas oerip (5203011028) Filia irawati (5203011029) Ayndri Nico P (5203011040) Mempelajari reaksi esterifikasi Apa sih reaksi esterifikasi itu? Bagaimana reaksi esterifikasi itu? Reaksi
SIFAT KIMIA DAN FISIK SENYAWA HIDROKARBON
 SIFAT KIMIA DAN FISIK SENYAWA HIDROKARBON Muhammad Ja far Sodiq (0810920047) 1. ALKANA Pada suhu biasa, metana, etana, propana, dan butana berwujud gas. Pentena sampai heptadekana (C 17 H 36 ) berwujud
SIFAT KIMIA DAN FISIK SENYAWA HIDROKARBON Muhammad Ja far Sodiq (0810920047) 1. ALKANA Pada suhu biasa, metana, etana, propana, dan butana berwujud gas. Pentena sampai heptadekana (C 17 H 36 ) berwujud
Pendahuluan Bab.6. Mekanisme reaksi substitusi elektrofilik. H H
 Pendahuluan Bab.6 Telah diketahui benzena merupakan senyawa yang kaya akan elektron, sehingga sifat yang menonjol dari benzena adalah mudah melakukan reaksi substitusi elektrofilik. Pereaksi semacam apa
Pendahuluan Bab.6 Telah diketahui benzena merupakan senyawa yang kaya akan elektron, sehingga sifat yang menonjol dari benzena adalah mudah melakukan reaksi substitusi elektrofilik. Pereaksi semacam apa
KONSEP DASAR KIMIA ORGANIK YANG MENUNJANG PEMBELAJARAN KIMIA SMA GEBI DWIYANTI
 KNSEP DASAR KIMIA RGANIK YANG MENUNJANG PEMBELAJARAN KIMIA SMA GEBI DWIYANTI 1. Kekhasan Atom Karbon Atom karbon adalah atom yang memiliki enam elektron dengan dengan konfigurasi 1s 2 2s 2 2p 2. Empat
KNSEP DASAR KIMIA RGANIK YANG MENUNJANG PEMBELAJARAN KIMIA SMA GEBI DWIYANTI 1. Kekhasan Atom Karbon Atom karbon adalah atom yang memiliki enam elektron dengan dengan konfigurasi 1s 2 2s 2 2p 2. Empat
Eter dan Epoksida. Budi Arifin. Bagian Kimia Organik Departemen Kimia FMIPA IPB. Tata Nama (dan Penggolongan) R OR'
 Eter dan Epoksida Budi Arifin Bagian Kimia rganik Departemen Kimia FMIPA IPB Tata Nama (dan Penggolongan) ETER rantai induk alkana (atom C lebih banyak) R R' cabang alkoksi (atom C lebih sedikit) Nama
Eter dan Epoksida Budi Arifin Bagian Kimia rganik Departemen Kimia FMIPA IPB Tata Nama (dan Penggolongan) ETER rantai induk alkana (atom C lebih banyak) R R' cabang alkoksi (atom C lebih sedikit) Nama
BAB V ALKOHOL, ETER DAN SENYAWA YANG BERHUBUNGAN
 BAB V ALKOHOL, ETER DAN SENYAWA YANG BERHUBUNGAN 1. Pendahuluan etanol suatu alkohol fenol dietil eter suatu eter propilena oksida suatu epoksida 2. Ikatan dalam alcohol dan eter Eter dapat berbentuk rantai
BAB V ALKOHOL, ETER DAN SENYAWA YANG BERHUBUNGAN 1. Pendahuluan etanol suatu alkohol fenol dietil eter suatu eter propilena oksida suatu epoksida 2. Ikatan dalam alcohol dan eter Eter dapat berbentuk rantai
1. Pendahuluan 2. Intermediate reaktif 3. Nukleofil and elektrofil 4. Tipe reaksi 5. Ions versus radicals
 1. Pendahuluan 2. Intermediate reaktif 3. Nukleofil and elektrofil 4. Tipe reaksi 5. Ions versus radicals TUJUAN INSTRUKSIONAL KHUSUS Setelah mengikuti kuliah pokok bahasan Reaktivitas dan Mekanisme, mahasiswa
1. Pendahuluan 2. Intermediate reaktif 3. Nukleofil and elektrofil 4. Tipe reaksi 5. Ions versus radicals TUJUAN INSTRUKSIONAL KHUSUS Setelah mengikuti kuliah pokok bahasan Reaktivitas dan Mekanisme, mahasiswa
μ =1,18 D 1,8D 1,78D 1,64D BAB IV ALKIL HALIDA Reaksi Substitusi dan Eliminasi Ikatannya:
 BAB IV ALKIL HALIDA Reaksi Substitusi dan Eliminasi Ikatannya: F, C1, Br bersifat elektronegatif terhadap C, elektroneg. 1 dekat C alkil halide bersifat polar. 2. Sifat fisis alkana terhalogenasikan Momen
BAB IV ALKIL HALIDA Reaksi Substitusi dan Eliminasi Ikatannya: F, C1, Br bersifat elektronegatif terhadap C, elektroneg. 1 dekat C alkil halide bersifat polar. 2. Sifat fisis alkana terhalogenasikan Momen
Alkena. KO 1 pertemuan III. Indah Solihah
 Alkena KO 1 pertemuan III Indah Solihah Pengertian Alkena Merupakan senyawa hidrokarbon yang mengandung ikatan rangkap karbon-karbon. Terdapat dalam jumlah berlebih di alam Etena (etilena) merupakan ssalah
Alkena KO 1 pertemuan III Indah Solihah Pengertian Alkena Merupakan senyawa hidrokarbon yang mengandung ikatan rangkap karbon-karbon. Terdapat dalam jumlah berlebih di alam Etena (etilena) merupakan ssalah
Eter dan Epoksida. Bagian Kimia Organik Departemen Kimia FMIPA IPB
 Eter dan Epoksida Bagian Kimia Organik Departemen Kimia FMIPA IPB Eter yang paling banyak penggunaan nya ialah dietil eter, anisol, dan THF Apa kegunaan / aplikasi ketiganya? Tiol (R-S-R) dan sulfida (R-S-H)
Eter dan Epoksida Bagian Kimia Organik Departemen Kimia FMIPA IPB Eter yang paling banyak penggunaan nya ialah dietil eter, anisol, dan THF Apa kegunaan / aplikasi ketiganya? Tiol (R-S-R) dan sulfida (R-S-H)
MKA PROSES KIMIA. Sri Wahyu Murni Prodi Teknik Kimia FTI UPN Veteran Yogyakarta
 MKA PROSES KIMIA Oleh Sri Wahyu Murni Prodi Teknik Kimia FTI UPN Veteran Yogyakarta Alkilasi didefinikan sebagai proses memasukkan gugus alkil atau aril ke dalam suatu senyawa. Gugus alkil : -C n H 2n+1
MKA PROSES KIMIA Oleh Sri Wahyu Murni Prodi Teknik Kimia FTI UPN Veteran Yogyakarta Alkilasi didefinikan sebagai proses memasukkan gugus alkil atau aril ke dalam suatu senyawa. Gugus alkil : -C n H 2n+1
Keunikan atom C?? Atom karbon primer, sekunder, tersier dan kuartener
 Keunikan atom C?? Atom karbon primer, sekunder, tersier dan kuartener Jenis ikatan karbon edakan : Propena (tak jenuh) Propuna (tak jenuh) Propana (jenuh) Rantai Atom Karbon Bedakan : 2-metil butana siklobutana
Keunikan atom C?? Atom karbon primer, sekunder, tersier dan kuartener Jenis ikatan karbon edakan : Propena (tak jenuh) Propuna (tak jenuh) Propana (jenuh) Rantai Atom Karbon Bedakan : 2-metil butana siklobutana
JURNAL PRAKTIKUM KIMIA ORGANIK : Identifikasi Gugus Fungsional Senyawa Organik
 Paraf Asisten Judul JURNAL PRAKTIKUM KIMIA ORGANIK : Identifikasi Gugus Fungsional Senyawa Organik Tujuan Percobaan : 1. Mempelajari teknik pengukuran fisik untuk mengidentifikasi suatu senyawa organik
Paraf Asisten Judul JURNAL PRAKTIKUM KIMIA ORGANIK : Identifikasi Gugus Fungsional Senyawa Organik Tujuan Percobaan : 1. Mempelajari teknik pengukuran fisik untuk mengidentifikasi suatu senyawa organik
Gugus Fungsi Senyawa Karbon
 Gugus Fungsi Senyawa Karbon Gugus fungsi merupakan bagian aktif dari senyawa karbon yang menentukan sifat-sifat senyawa karbon. Gugus fungsi tersebut berupa ikatan karbon rangkap dua, ikatan karbon rangkap
Gugus Fungsi Senyawa Karbon Gugus fungsi merupakan bagian aktif dari senyawa karbon yang menentukan sifat-sifat senyawa karbon. Gugus fungsi tersebut berupa ikatan karbon rangkap dua, ikatan karbon rangkap
BANK SOAL KIMIA ORGANIK I UJIAN MID SEMESTER GANJIL 2002/2003
 BANK SOAL KIMIA ORGANIK I UJIAN MID SEMESTER GANJIL 2002/2003 1. Terangkan dengan jelas bagaimana terjadinya ikatan sigma dan pi antara atom-atom pada periode II yaitu atom boron, karbon, dan nitrogen.
BANK SOAL KIMIA ORGANIK I UJIAN MID SEMESTER GANJIL 2002/2003 1. Terangkan dengan jelas bagaimana terjadinya ikatan sigma dan pi antara atom-atom pada periode II yaitu atom boron, karbon, dan nitrogen.
BAB VIII ALKENA DAN ALKUNA
 BAB VIII ALKENA DAN ALKUNA 1. Ikatan dalam alkena dan alkuna Keasaman : Alkuna> Alkena> Alkana (sp > sp 2 > sp 3 ) Karena untuk sp karakter s = 50% dan p = 50%, sehingga elektron dalam orbital lebih dekat
BAB VIII ALKENA DAN ALKUNA 1. Ikatan dalam alkena dan alkuna Keasaman : Alkuna> Alkena> Alkana (sp > sp 2 > sp 3 ) Karena untuk sp karakter s = 50% dan p = 50%, sehingga elektron dalam orbital lebih dekat
OH (Metil alkohol = Metanol) CH 2. OH (etil alkohol = etanol) OH (1-propanol = n-propanol)
 Rumus umum R-O Gugus fungsional: O (gugus hidroksil) Tata nama Diturunkan dari gugus alkil yang melekat pada O, kemudian ditambah kata alkohol. Dalam sistem IUPAC: akhiran ol menunjukan adanya gugus hidroksil
Rumus umum R-O Gugus fungsional: O (gugus hidroksil) Tata nama Diturunkan dari gugus alkil yang melekat pada O, kemudian ditambah kata alkohol. Dalam sistem IUPAC: akhiran ol menunjukan adanya gugus hidroksil
KIMIA HIDROKARBON GUGUS FUNGSI
 KMA HDRKARBN GUGUS FUNGS Gugus fungsi adalah bagian suatu molekul (substituen pada rangka hidrokarbon) yang berfungsi secara kimia Dapat bereaksi, tidak lembam Substituen (gugus fungsi) diantaranya mengandung
KMA HDRKARBN GUGUS FUNGS Gugus fungsi adalah bagian suatu molekul (substituen pada rangka hidrokarbon) yang berfungsi secara kimia Dapat bereaksi, tidak lembam Substituen (gugus fungsi) diantaranya mengandung
SENYAWA AROMATIK POLISIKLIK DAN HETEROSIKLIK
 SEYAWA ARMATIK PLISIKLIK DA ETERSIKLIK A. PEDAULUA Beberapa senyawa aromatik yang lain dapat dikelompokkan dalam dua kelas, yaitu senyawa polisiklik dan senyawa heterosiklik. Senyawa aromatik polisiklik
SEYAWA ARMATIK PLISIKLIK DA ETERSIKLIK A. PEDAULUA Beberapa senyawa aromatik yang lain dapat dikelompokkan dalam dua kelas, yaitu senyawa polisiklik dan senyawa heterosiklik. Senyawa aromatik polisiklik
BAB I IDENTIFIKASI GUGUS FUNGSI ALKOHOL
 BAB I IDENTIFIKASI GUGUS FUNGSI ALKOHOL TUJUAN : Mengetahui sifat fisik alkohol dan fenol Membedakan senyawa alkohol primer, sekunder, tersier dan fenol dengan menggunakan tes Lucas dan Ferri Klorida A.
BAB I IDENTIFIKASI GUGUS FUNGSI ALKOHOL TUJUAN : Mengetahui sifat fisik alkohol dan fenol Membedakan senyawa alkohol primer, sekunder, tersier dan fenol dengan menggunakan tes Lucas dan Ferri Klorida A.
Bahan Bacaan 5 BENZENA DAN TURUNANNYA
 Bahan Bacaan 5 BENZENA DAN TURUNANNYA Benzena mempunyai struktur dan sifat khas sehingga sering disebut senyawa aromatik dan dikelompokkan pada senyawa karbosiklik. Benzena mempunyai rumus molekul C 6
Bahan Bacaan 5 BENZENA DAN TURUNANNYA Benzena mempunyai struktur dan sifat khas sehingga sering disebut senyawa aromatik dan dikelompokkan pada senyawa karbosiklik. Benzena mempunyai rumus molekul C 6
1.Pengertian alkohol 2.Klasifikasi alkohol 3.Sifat-sifat fisika dan kimia alkohol 4.Sintesis alkohol 5.Reaksi-reaksi alkohol 6.
 1.Pengertian alkohol 2.Klasifikasi alkohol 3.Sifat-sifat fisika dan kimia alkohol 4.Sintesis alkohol 5.Reaksi-reaksi alkohol 6.Tata nama alkohol 7.Contoh-contoh alkohol dan kegunaannya senyawa organik
1.Pengertian alkohol 2.Klasifikasi alkohol 3.Sifat-sifat fisika dan kimia alkohol 4.Sintesis alkohol 5.Reaksi-reaksi alkohol 6.Tata nama alkohol 7.Contoh-contoh alkohol dan kegunaannya senyawa organik
LAPORAN PRAKTIKUM KIMIA ORGANIK. Disusun Oleh :
 LAPORAN PRAKTIKUM KIMIA ORGANIK Disusun Oleh : Nama : Veryna Septiany NPM : E1G014054 Kelompok : 3 Hari, Jam : Kamis, 14.00 15.40 WIB Ko-Ass : Jhon Fernanta Sipayung Lestari Nike Situngkir Tanggal Praktikum
LAPORAN PRAKTIKUM KIMIA ORGANIK Disusun Oleh : Nama : Veryna Septiany NPM : E1G014054 Kelompok : 3 Hari, Jam : Kamis, 14.00 15.40 WIB Ko-Ass : Jhon Fernanta Sipayung Lestari Nike Situngkir Tanggal Praktikum
GUGUS FUNGSI, TATA NAMA, SIFAT, DAN SINTESIS SEDERHANA SENYAWA HIDROKARBON
 GUGUS FUNGSI, TATA NAMA, SIFAT, DAN SINTESIS SEDERHANA SENYAWA HIDROKARBON Kelompok VII: 1. Anggi Cahaya Nirwana (F1C116012) 2. Eko Prastyo (F1C116022) 3. Mardiana (F1C116023) 4. Mutiara Sarah H. (F1C116029)
GUGUS FUNGSI, TATA NAMA, SIFAT, DAN SINTESIS SEDERHANA SENYAWA HIDROKARBON Kelompok VII: 1. Anggi Cahaya Nirwana (F1C116012) 2. Eko Prastyo (F1C116022) 3. Mardiana (F1C116023) 4. Mutiara Sarah H. (F1C116029)
LAPORAN PRAKTIKUM KIMIA ORGANIK (KI2051)
 LAPORAN PRAKTIKUM KIMIA ORGANIK (KI2051) LAPORAN PRAKTIKUM KIMIA ORGANIK (KI2051) PERCOBAAN 5 Alkohol dan Fenol: Sifat Fisik dan Reaksi Kimia PERCOBAAN 6 Aldehid dan Keton: Sifat Fisik dan Reaksi Kimia
LAPORAN PRAKTIKUM KIMIA ORGANIK (KI2051) LAPORAN PRAKTIKUM KIMIA ORGANIK (KI2051) PERCOBAAN 5 Alkohol dan Fenol: Sifat Fisik dan Reaksi Kimia PERCOBAAN 6 Aldehid dan Keton: Sifat Fisik dan Reaksi Kimia
ALDEHID DAN KETON. Putri Anjarsari, S.Si., M.Pd
 ALDEHID DAN KETN Putri Anjarsari, S.Si., M.Pd putri_anjarsari@uny.ac.id ontoh senyawa-senyawa karbonil penting H 3 H Asam asetat (asam cuka) H N H H 3 Asetaminofen (analgesik, antipiretik) H H 3 Asam asetil
ALDEHID DAN KETN Putri Anjarsari, S.Si., M.Pd putri_anjarsari@uny.ac.id ontoh senyawa-senyawa karbonil penting H 3 H Asam asetat (asam cuka) H N H H 3 Asetaminofen (analgesik, antipiretik) H H 3 Asam asetil
Gambar IV 1 Serbuk Gergaji kayu sebelum ekstraksi
 Bab IV Pembahasan IV.1 Ekstraksi selulosa Kayu berdasarkan struktur kimianya tersusun atas selulosa, lignin dan hemiselulosa. Selulosa sebagai kerangka, hemiselulosa sebagai matrik, dan lignin sebagai
Bab IV Pembahasan IV.1 Ekstraksi selulosa Kayu berdasarkan struktur kimianya tersusun atas selulosa, lignin dan hemiselulosa. Selulosa sebagai kerangka, hemiselulosa sebagai matrik, dan lignin sebagai
ALKHOHOL-ETER. Putri Anjarsari, S.Si., M.Pd
 ALKOOL-ETER Putri Anjarsari, S.Si., M.Pd putri_anjarsari@uny.ac.id 1 STRUKTUR ALKOOL Alkohol adalah senyawa yang molekulnya memiliki suatu gugus hidroksil, yang terikat pada suatu atom karbon jenuh. C
ALKOOL-ETER Putri Anjarsari, S.Si., M.Pd putri_anjarsari@uny.ac.id 1 STRUKTUR ALKOOL Alkohol adalah senyawa yang molekulnya memiliki suatu gugus hidroksil, yang terikat pada suatu atom karbon jenuh. C
Kimia Organik 1. Pertemuan ke 4 Indah Solihah
 Kimia Organik 1 Pertemuan ke 4 Indah Solihah Klasifikasi Senyawa Organik 1. Senyawa Alifatik a. Senyawa alifatik rantai lurus (non siklis) b. Senyawa alifatik siklis (alisiklis) 2. Senyawa Aromatis Senyawa
Kimia Organik 1 Pertemuan ke 4 Indah Solihah Klasifikasi Senyawa Organik 1. Senyawa Alifatik a. Senyawa alifatik rantai lurus (non siklis) b. Senyawa alifatik siklis (alisiklis) 2. Senyawa Aromatis Senyawa
ALDEHID DAN KETON. Tim Dosen Kimia Dasar II/ Kimia Organik
 ALDEHID DAN KETN Tim Dosen Kimia Dasar II/ Kimia rganik TATA NAMA ALDEHID IUPAC Alkana induk dengan huruf akhir a menjadi -al Metanal Etanal Propanal Butanal NTE Aldehid tanpa rantai samping (substituen)
ALDEHID DAN KETN Tim Dosen Kimia Dasar II/ Kimia rganik TATA NAMA ALDEHID IUPAC Alkana induk dengan huruf akhir a menjadi -al Metanal Etanal Propanal Butanal NTE Aldehid tanpa rantai samping (substituen)
GUGUS FUNGSI
 ASAM KARBKSILAT GUGUS FUNGSI TATA NAMA SEARA IUPA MENGGUNAKAN NAMA ALKANA INDUKNYA DENGAN IMBUHAN: ASAM.-AT (NAMA LAIN ASAM KARBKSILAT ADALAH ASAM ALKANAT) GUGUS ALKIL ATAU SUBSTITUEN LAIN DILETAKKAN
ASAM KARBKSILAT GUGUS FUNGSI TATA NAMA SEARA IUPA MENGGUNAKAN NAMA ALKANA INDUKNYA DENGAN IMBUHAN: ASAM.-AT (NAMA LAIN ASAM KARBKSILAT ADALAH ASAM ALKANAT) GUGUS ALKIL ATAU SUBSTITUEN LAIN DILETAKKAN
Rencana Pelaksanaan Pembelajaran
 Rencana Pelaksanaan Pembelajaran Mata Pelajaran : KIMIA Kelas/Prog/Semester : XII / IPA / 2 Alokasi Waktu : 2x45 menit Standar Kompetensi : 4. Memahami senyawa organik dan reaksinya, benzena dan turunannya,
Rencana Pelaksanaan Pembelajaran Mata Pelajaran : KIMIA Kelas/Prog/Semester : XII / IPA / 2 Alokasi Waktu : 2x45 menit Standar Kompetensi : 4. Memahami senyawa organik dan reaksinya, benzena dan turunannya,
OLIMPIADE KIMIA INDONESIA
 OLIMPIADE KIMIA INDONESIA OLIMPIADE SAINS NASIONAL SELEKSI KABUPATEN / KOTA UjianTeori Waktu 2 Jam Departemen Pendidikan Nasional Direktorat Jenderal Managemen Pendidikan Dasar dan Menengah Direktorat
OLIMPIADE KIMIA INDONESIA OLIMPIADE SAINS NASIONAL SELEKSI KABUPATEN / KOTA UjianTeori Waktu 2 Jam Departemen Pendidikan Nasional Direktorat Jenderal Managemen Pendidikan Dasar dan Menengah Direktorat
Gugus Fungsi. Gugus Fungsi. Gugus Fungsi. Gugus Fungsi CH 3 -CH 3 O O H 2 C CH 2 C O C C S C O CH 3 C OCH 2 CH 3 H C NH 2 CH 3 C NH 2. Alkana.
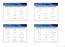 Gugus Fungsi Struktur Golongan Senyawa ontoh spesifik Gugus Fungsi Struktur Golongan Senyawa ontoh spesifik Alkana - Alkohol Alkena Fenol Alkuna Arena (aromatik) S Tiol (Merkaptan) S Eter X Alkil halida
Gugus Fungsi Struktur Golongan Senyawa ontoh spesifik Gugus Fungsi Struktur Golongan Senyawa ontoh spesifik Alkana - Alkohol Alkena Fenol Alkuna Arena (aromatik) S Tiol (Merkaptan) S Eter X Alkil halida
Gambar 1.1 Struktur khalkon
 BAB 1 PENDAHULUAN 1.1 Latar Belakang Penelitian Senyawa khalkon (C 15 H 12 O) atau benziliena asetofenon atau E-1,3- difenilprop-2-en-1-on, merupakan senyawa golongan flavonoid yang ditemukan dalam tanaman
BAB 1 PENDAHULUAN 1.1 Latar Belakang Penelitian Senyawa khalkon (C 15 H 12 O) atau benziliena asetofenon atau E-1,3- difenilprop-2-en-1-on, merupakan senyawa golongan flavonoid yang ditemukan dalam tanaman
LAPORAN PRAKTIKUM KIMIA ORGANIK
 Paraf Asisten LAPRAN PRAKTIKUM KIMIA RGANIK Judul : Identifikasi Gugus Fungsional Senyawa rganik Tujuan Percobaan : - Mempelajari teknik pengukuran fisik untuk mengidentifikasi suatu senyawa organik -
Paraf Asisten LAPRAN PRAKTIKUM KIMIA RGANIK Judul : Identifikasi Gugus Fungsional Senyawa rganik Tujuan Percobaan : - Mempelajari teknik pengukuran fisik untuk mengidentifikasi suatu senyawa organik -
OKSIDASI OLEH SRI WAHYU MURNI PRODI TEKNIK KIMIA FTI UPN VETERAN YOGYAKARTA
 KSIDASI MKA PRSES KIMIA LEH SRI WAHYU MURNI PRDI TEKNIK KIMIA FTI UPN VETERAN YGYAKARTA Tipe-tipe proses oksidasi: 1. Dehidrogenasi C 2 H 5 H + ½ 2 etanol CH 3 2. Pemasukan Atom ksigen CH 3 C H + ½ 2 C
KSIDASI MKA PRSES KIMIA LEH SRI WAHYU MURNI PRDI TEKNIK KIMIA FTI UPN VETERAN YGYAKARTA Tipe-tipe proses oksidasi: 1. Dehidrogenasi C 2 H 5 H + ½ 2 etanol CH 3 2. Pemasukan Atom ksigen CH 3 C H + ½ 2 C
Soal-Soal. Bab 14. Latihan. Kimia Karbon II: Gugus Fungsi. Alkohol dan Eter. 1. Rumus struktur alkohol ditunjukkan oleh. (A) C 2
 Bab 14 Kimia Karbon II: Gugus Fungsi Soal-Soal Latihan Alkohol dan Eter 1. Rumus struktur alkohol ditunjukkan oleh. (A) C 2 (B) -CH (C) -CH(H)-C 2 (D) C 3 H 7 -C- (E) -CH 2. Suatu senyawa dengan rumus
Bab 14 Kimia Karbon II: Gugus Fungsi Soal-Soal Latihan Alkohol dan Eter 1. Rumus struktur alkohol ditunjukkan oleh. (A) C 2 (B) -CH (C) -CH(H)-C 2 (D) C 3 H 7 -C- (E) -CH 2. Suatu senyawa dengan rumus
Aromatisitas, Benzena, dan Benzena Tersubstitusi
 Aromatisitas, Benzena, dan Benzena Tersubstitusi Bagian Kimia Organik Departemen Kimia FMIPA IPB Senyawa Aromatik Aromatik dahulu diartikan senyawa beraroma. Kini, aromatik merujuk sekelompok senyawa dengan
Aromatisitas, Benzena, dan Benzena Tersubstitusi Bagian Kimia Organik Departemen Kimia FMIPA IPB Senyawa Aromatik Aromatik dahulu diartikan senyawa beraroma. Kini, aromatik merujuk sekelompok senyawa dengan
SENYAWA TURUNAN ALKANA. Alkohol - Eter, Aldehid - Keton, Asam Karboksilat - Ester
 SENYAWA TURUNAN ALKANA Alkohol - Eter, Aldehid - Keton, Asam Karboksilat - Ester Tata Nama Senyawa Turunan Alkana Nomor cabang-cabang-nama cabang urut abjad-nomor gugus fungsi-nama induk 1. Mengidentifikasi
SENYAWA TURUNAN ALKANA Alkohol - Eter, Aldehid - Keton, Asam Karboksilat - Ester Tata Nama Senyawa Turunan Alkana Nomor cabang-cabang-nama cabang urut abjad-nomor gugus fungsi-nama induk 1. Mengidentifikasi
Penggolongan hidrokarbon
 Penggolongan hidrokarbon idrokarbon Alifatik Alisiklik Aromatik Jenuh Tidak jenuh Jenuh Tidak jenuh Alkana Sikloalkana Sikloalkena Alkena Alkuna Sifat Fisika Alkana yang memiliki massa molekul rendah yaitu
Penggolongan hidrokarbon idrokarbon Alifatik Alisiklik Aromatik Jenuh Tidak jenuh Jenuh Tidak jenuh Alkana Sikloalkana Sikloalkena Alkena Alkuna Sifat Fisika Alkana yang memiliki massa molekul rendah yaitu
GUGUS AMINA, AMIDA DAN SULFONAT
 GUGUS AMINA, AMIDA DAN SULFONAT AMINA Senyawa yang mengandung gugus NH 2 Strukrur : RNH 2 Jenis : Amina primer (1 o ) Amina sekunder (2 o ) Amina tersier (3 o ) R N H R N H R N R'' H R' R' amina 1 amina
GUGUS AMINA, AMIDA DAN SULFONAT AMINA Senyawa yang mengandung gugus NH 2 Strukrur : RNH 2 Jenis : Amina primer (1 o ) Amina sekunder (2 o ) Amina tersier (3 o ) R N H R N H R N R'' H R' R' amina 1 amina
Setelah mengikuti kuliah pokok bahasan Alkuna, mahasiswa memahami dan menjelaskan struktur, sifat fisis, kegunaan, dan reaksi-reaksi yang dapat
 Setelah mengikuti kuliah pokok bahasan Alkuna, mahasiswa memahami dan menjelaskan struktur, sifat fisis, kegunaan, dan reaksi-reaksi yang dapat terjadi pada senyawa alkuna. Senyawa alkuna memiliki ikatan
Setelah mengikuti kuliah pokok bahasan Alkuna, mahasiswa memahami dan menjelaskan struktur, sifat fisis, kegunaan, dan reaksi-reaksi yang dapat terjadi pada senyawa alkuna. Senyawa alkuna memiliki ikatan
LAPORAN PRAKTIKUM KIMIA ORGANIK
 LAPORAN PRAKTIKUM KIMIA ORGANIK ACARA 4 SENYAWA ASAM KARBOKSILAT DAN ESTER Oleh: Kelompok 5 Nova Damayanti A1M013012 Nadhila Benita Prabawati A1M013040 KEMENTRIAN PENDIDIKAN DAN KEBUDAYAAN UNIVERSITAS
LAPORAN PRAKTIKUM KIMIA ORGANIK ACARA 4 SENYAWA ASAM KARBOKSILAT DAN ESTER Oleh: Kelompok 5 Nova Damayanti A1M013012 Nadhila Benita Prabawati A1M013040 KEMENTRIAN PENDIDIKAN DAN KEBUDAYAAN UNIVERSITAS
ORTO DAN PARA NITROFENOL
 ORTO DAN PARA NITROFENOL Tujuan 1. Mensintesis o-nitrofenol dan p-nitrofenol dari fenol dan asam nitrat melalui nitrasi 2. Memisahkan o-nitrofenol dan p-nitrofenol dengan metode distilasi uap 3. Memurnikan
ORTO DAN PARA NITROFENOL Tujuan 1. Mensintesis o-nitrofenol dan p-nitrofenol dari fenol dan asam nitrat melalui nitrasi 2. Memisahkan o-nitrofenol dan p-nitrofenol dengan metode distilasi uap 3. Memurnikan
Struktur Aldehid. Tatanama Aldehida. a. IUPAC Nama aldehida dinerikan dengan mengganti akhiran a pada nama alkana dengan al.
 Kamu tentunya pernah menyaksikan berita tentang penyalah gunaan formalin. Formalin merupakan salah satu contoh senyawa aldehid. Melalui topik ini, kamu tidak hanya akan mempelajari kegunaan aldehid yang
Kamu tentunya pernah menyaksikan berita tentang penyalah gunaan formalin. Formalin merupakan salah satu contoh senyawa aldehid. Melalui topik ini, kamu tidak hanya akan mempelajari kegunaan aldehid yang
LAPORAN PENDAHULUAN PRAKTIKUM KIMIA ORGANIK II
 LAPORAN PENDAHULUAN PRAKTIKUM KIMIA ORGANIK II I. Nomor Percobaan : VI II. Nama Percobaan : Reaksi Asetilasi Anilin III. Tujuan Percobaan : Agar mahasiswa dapat mengetahui salah satu cara mensintesa senyawa
LAPORAN PENDAHULUAN PRAKTIKUM KIMIA ORGANIK II I. Nomor Percobaan : VI II. Nama Percobaan : Reaksi Asetilasi Anilin III. Tujuan Percobaan : Agar mahasiswa dapat mengetahui salah satu cara mensintesa senyawa
LAPORAN PRAKTIKUM SINTESIS SENYAWA ORGANIK
 Paraf Asisten LAPRAN PRAKTIKUM SINTESIS SENYAWA RGANIK Judul : Sintesis Para Nitroasetanilida Tujuan Percobaan : Memperlajari reaksi nitrasi senyawa aromatis Pendahuluan Asetanilida adalah senyawa turunan
Paraf Asisten LAPRAN PRAKTIKUM SINTESIS SENYAWA RGANIK Judul : Sintesis Para Nitroasetanilida Tujuan Percobaan : Memperlajari reaksi nitrasi senyawa aromatis Pendahuluan Asetanilida adalah senyawa turunan
Sifat fisika: mirip dengan alkana dengan jumlah atom C sama
 SENYAWA ORGANIK HIDROKARBON SENYAWA KARBON DENGAN KARBON NUKLEOFILIK ALKENA Alkena merupakan senyawa hidrokarbon dengan sifat tersendiri karena adanya ikatan rangkap dan reaktivitas senyawa ini senyawa
SENYAWA ORGANIK HIDROKARBON SENYAWA KARBON DENGAN KARBON NUKLEOFILIK ALKENA Alkena merupakan senyawa hidrokarbon dengan sifat tersendiri karena adanya ikatan rangkap dan reaktivitas senyawa ini senyawa
I. DASAR TEORI Struktur benzil alkohol
 JUDUL TUJUAN PERCBAAN IV : BENZIL ALKL : 1. Mempelajari kelarutan benzyl alkohol dalam berbagai pelarut. 2. Mengamati sifat dan reaksi oksidasi pada benzyl alkohol. ari/tanggal : Selasa, 2 November 2010
JUDUL TUJUAN PERCBAAN IV : BENZIL ALKL : 1. Mempelajari kelarutan benzyl alkohol dalam berbagai pelarut. 2. Mengamati sifat dan reaksi oksidasi pada benzyl alkohol. ari/tanggal : Selasa, 2 November 2010
kimia K-13 HIDROKARBON II K e l a s A. Alkena Tujuan Pembelajaran
 K-13 kimia K e l a s XI HIDROKARBON II Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut 1 Memahami pengertian, rumus umum, serta tata nama senyawa hidrokarbon
K-13 kimia K e l a s XI HIDROKARBON II Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut 1 Memahami pengertian, rumus umum, serta tata nama senyawa hidrokarbon
LKS HIDROKARBON. Nama : Kelas/No.Abs :
 Nama : Kelas/No.Abs : LKS HIDROKARBON 1. Kekhasan / Keunikan Atom Karbon 1. Terletak pada golongan IVA dengan Z = 6 dan mempunyai 4 elektron valensi. 2. Untuk mencapai konfigurasi oktet maka atom karbon
Nama : Kelas/No.Abs : LKS HIDROKARBON 1. Kekhasan / Keunikan Atom Karbon 1. Terletak pada golongan IVA dengan Z = 6 dan mempunyai 4 elektron valensi. 2. Untuk mencapai konfigurasi oktet maka atom karbon
Kondensasi Benzoin Benzaldehid: Rute Menujuu Sintesis Obat Antiepileptik Dilantin
 Laporan Praktikum Senyawa Organik Polifungsi KI2251 1 Kondensasi Benzoin Benzaldehid: Rute Menujuu Sintesis Obat Antiepileptik Dilantin Antika Anggraeni Kelas 01; Subkelas I; Kelompok C; Nurrahmi Handayani
Laporan Praktikum Senyawa Organik Polifungsi KI2251 1 Kondensasi Benzoin Benzaldehid: Rute Menujuu Sintesis Obat Antiepileptik Dilantin Antika Anggraeni Kelas 01; Subkelas I; Kelompok C; Nurrahmi Handayani
Senyawa Halogen Organik; Reaksi Substitusi dan Eliminasi
 Senyawa Halogen Organik; Reaksi Substitusi dan Eliminasi Prof. Jumina, Ph.D. Robby Noor Cahyono, S.Si., M.Sc. Chemistry Dept.,FMIPA, Universitas Gadjah Mada Rumus Umum Tipe Struktur Alkil Halida Primer
Senyawa Halogen Organik; Reaksi Substitusi dan Eliminasi Prof. Jumina, Ph.D. Robby Noor Cahyono, S.Si., M.Sc. Chemistry Dept.,FMIPA, Universitas Gadjah Mada Rumus Umum Tipe Struktur Alkil Halida Primer
Senyawa organik adalah senyawa kimia yang molekulnya mengandung karbon, kecuali karbida, karbonat, dan oksida karbon.
 PENDAULUAN Definisi senyawa organik Kimia organik adalah studi ilmiah mengenai struktur, sifat, komposisi, reaksi, dan sintesis senyawa organik. Senyawa organik dibangun oleh karbon dan hidrogen, dan dapat
PENDAULUAN Definisi senyawa organik Kimia organik adalah studi ilmiah mengenai struktur, sifat, komposisi, reaksi, dan sintesis senyawa organik. Senyawa organik dibangun oleh karbon dan hidrogen, dan dapat
