DAFTAR PUSTAKA. X dari Tawas NaOH dan Water Glass dengan Response Surface Methodology,
|
|
|
- Yenny Wibowo
- 6 tahun lalu
- Tontonan:
Transkripsi
1 DAFTAR PUSTAKA 1. Snavely, F.A., Yoder, C.H., (1971), The preparation and analysis of some double salt. An introductory experiment, Journal Chemical Education, V.48, hal Knaggs, V. H., (1963) Potatos as Food and Medicine-Epsom Salt: Its value and use the Cleansing Saline Fast, Linda Edenfield Fantasy Tan & Float, San Bernardino. 3 Jordanvska, V.B.,(1989) Synthesis and Thermal Decomposition of Double Salt Dimethilammonium Sulfat Hexahydrate of Aluminium and Chromium Journal of Thermal Analysis and Calorimetry, Volume 35, 4 William, B, (2003) Zinc Ammonium Chlorida: Double Salt, the limited England. 5 Young, Jay A. (2004). Potasium Aluminum Sulfate 12 Hydrate, Journal Chemical Education.V.81 hal Holden, A., Morisson, P.,(1960) Crystals and Crystal Growing, Doubleday, Anchor, NewYork, p Langs, D., A., Curtis., R, (1967). H., The Crystal Structure of Calcium Copper Acetate Hexahidrate and its Isomorph Calcium Cadmium Acetate Hexahidrate, Departement of Chemistry, State University of New York, New York 8 Canham, R., Geoffrey, (2000) Descriptive Inorganic Chemistry, Freeman and Compeny, New York, p Ulfah, E., M., Yasnur, F., A., Istadi( 2006) Optimasi Pembuatan Katalis Zeolit X dari Tawas NaOH dan Water Glass dengan Response Surface Methodology, 10 Sukasediati, N., (1989) Tawas Penawar Bau Badan Tradisional, Pusat Penelitian dan Pengembangan Farmasi, Badan Penelitian dan Pengembangan Kesehatan, Departemen Kesehatan RI, Jakarta,. 11 Jordi, F., (1996), Paceite Mineral Data, ck.php?oparams=2_bannerid=11_2oneid, 12/18/
2 12 Klop, E., A., Duisenberg, A., J., M., Spek., A.,L., (1983) Reinvestigation of the Structure of Calcium Copper Acetate Hexahydrate, CaCu(CH 3 COO) 4.6H 2 O, Acta Crystaloghrafica, C39, p Georgiev, M., Stoilova, D., (2007) Metal-water Interactions and Hydrogen Bond Strength, Journal of the University of Chemical Technology and Metallurgy, 42, 2,, p Saito, T., (1996) Buku Teks Kimia Anorganik Online, diterjemahkan oleh Ismunandar, Iwanami Shoten Publishers, Tokyo. 15 Musumeci, A., Frost, R., L., Waclawik, E.,( 2007) A Spectroscopic Study of the Mineral Paceite ( calcium acetate ), Inorganic Materials Program, School of Physical and Chemical Sciences, Queensland, Australia.. 16 Bellini, J.V., Machado, R., Morelli, M.R., Kiminami, R.H.G.A., (2002) Thermal Structural and Morphologicalharacterisation of Freezi-dried Copper (II) Acetate Monohydrate and its Solid Decomposition Product, Journal of Material Research. V.5.n.4. hal Nugroho, P., Indrarti, L., (1989) Pelatihan Alat-Alat Karakterisasi Polimer, Puslitbang Fisika Terapan, LIPI-Japan International Coorporation Agency, Bandung, 18 Basset, J., Denny, R. C., Jeffrey. G. H., Medham. J, (1994) Buku ajar Vogel Kimia Analisis Kuantitatif Anorganik, edisi keempat, diterjemahkan oleh Hadyana Pudjaatmaka, Penerbit IKAPI Jakarta,. hal Skoog, D. H., Nieman, T. A., Holler, F. J,(1998) Principles of Instrumental Analysis fifth edition, Saunders College Publishing, San Francisco,p
3 Lampiran A Data dan perhitungan jumlah air kristal secara gravimetric Untuk kristal biru cerah yang dipanaskan di dalam oven suhu 120 o C: massa cawan kosong (sudah konstan) = 51,0698 gram massa cawan dan kristal sebelum dioven = 51,5452 gram massa kristal sebelum dioven adalah = 0,4754 gram massa cawan dan kristal sesudah dioven = 51,4293 gram massa kristal sesudah dioven = 0,3595 gram massa H 2 O yang diuapkan (0,4754-0,3595) = gram Perhitungan : CaCu(CH 3 COO) 4.xH 2 O CaCu(CH 3 COO) 4 + x H 2 O Mol H 2 O = 0,1159/18 = 0,0064 mol Mol CaCu(CH 3 COO) 4 = 0,3595/339,89 = 0,00106 mol (dibulatkan 0,0011) Berdasarkan persamaan reaksi maka mol air yang diuapkan setara dengan 0,0011 mol dikali x mol air maka didapat persamaan : 0,0064 mol = 0,0011 x atau x = 0,0064/0,0011 Maka diperoleh nilai x adalah = 5,90 dibulatkan menjadi 6 Sehingga rumus kimia menjadi CaCu(CH 3 COO) 4.6H 2 O 37
4 Lampiran B Penentuan dan pembakuan larutan Na 2 S 2 O 3 Pertama : Penentuan Konsentrasi Larutan Standard K 2 Cr 2 O 7. Konsentrasi K2Cr2O7 = (1,2274 g/294,2 g.mol -1 ) / 0,250 L = 0,0167 M Kedua : Pembakuan Konsentrasi Larutan Standard Na 2 S 2 O 3 (Mr=248,17) Reaksi : Cr2O7 (aq) + 14H + (aq) + 6I - (aq) 2Cr 3+ (aq) + 3I2(aq) + 7H2O(l) 3( I 2(aq) + 2S 2 O 3 (aq) 2I - (aq) + S 4 O 6 (aq) ) Cr 2 O 7 (aq) + 14H + (aq) + 6S 2 O 3 (aq) 2Cr 3+ (aq) + 3S 4 O 6 (aq) Data Titrasi larutan Na 2 S 2 O 3 dengan larutan K 2 Cr 2 O 7 0,0167 M No. Volum larutan K 2 Cr 2 O 7 0,0167M Volum larutan Na 2 S 2 O 3 (ml) , ,55 Rata-rata 24,57 Konsentrasi larutan S 2 O 3 = ( 6 x 25 ml x 0,0167)/ 24,57 = 0,1018 M Setelah dipipet seukuran 10 ml dan diencerkan di dalam ukur diperoleh larutan standar dengan konsentrasi = 0,0102 M Penentuan kadar Cu dalam CaCu(CH 3 COO) 4.6H 2 O secara titrasi iodometri Titrasi larutan garam rangkap dengan larutan Na 2 S 2 O 3 0,0102 M No. Volum larutan garam rangkap, Volum larutan Na 2 S 2 O 3 (ml) Cu 2+ (ml) , ,85 Rata-rata 9,85 38
5 10 ml larutan Cu 2+ diambil dari 100 ml larutan yang mengadung 0,4472 gram sampel garam rangkap. Reaksi yang terjadi pada titrasi iodometri : 2 Cu 2+ (aq) + 4I - (aq) 2 CuI (s) + I 2 (aq) I 2(aq) + 2 S 2 O 3 (aq) 2I - (aq) + S 2 O 4 (aq) Jumlah mmol S 2 O 3 setara dengan jumlah mmol Cu 2+ Maka dapat ditentukan [ Cu 2+ ] = (V.S 2 O 3 x M.S 2 O 3 ) / V.Cu 2+ Massa Cu yang diperoleh dinyatakan dalam persen (%). Berdasarkan data titrasi tersebut dapat dihitung: [Cu 2+ ] = (9,85 ml x 0,01018M) / 10 ml = 0,01002 M Dalam 100 ml larutan terdapat Cu sebanyak = 1,002 mmol Massa Cu dalam = 1,002 x 63,55 = 63,67 mg Kadar Cu dalam 0,4475 gram sampel = (63,67 mg / 447,2 mg)/100% = 14,20 % 39
6 Lampiran C Data titrasi kompleksometri EDTA untuk penentuan kadar Ca 2+ dalam sampel garam rangkap CaCu(CH 3 COO) 4.6H 2 O : Larutan yang dititrasi berupa filtrat I dan Filtrat II masing-masing berasal dari 10 ml larutan yang diambil dari 100 ml. Larutan mengandung 0,4472 gram garam rangkap. Titrasi dilakukan duplo: 1.Filtrat I, volume EDTA yang terpakai = 8,55 ml 2.Filatrat II, volume EDTA yang terpakai = 8.50 ml Volume rata-rata EDTA yang terpakai = 8,52 ml Konsentrasi EDTA standar = 0,0114 M Reaksi yang terjadi : Ca 2+ (aq) + H 2 Y CAH 2 Y Jumlah mmol H 2 Y yang terpakai = 8,52 ml x 0,0114 M = 0,0971 mmol Sesuai persamaan reaksi di atas maka jumlah mol H 2 Y yang bereaksi setara dengan jumlah Ca 2+ yang ada, jadi banyaknya Ca 2+ adalah 0,0971 mmol / 10 ml Dalam 100 ml larutan yang mengandung 0,4472 gram garam rangkap, jumlah Ca 2+ = 0,0971 mmol /10 ml x 100 ml = 0,971 mmol Massa Ca (Ar=40,08) adalah = 0,971 mmol x 40,08 gram /mol = 38,90 mg Kadar Ca dalam 0,4472 gram garam rangkap, dinyatakan dalam % adalah: = ( 38,90mg/0,4472 g) x (1 g/1000 mg) x 100 % = 8,62 % 40
7 Lampiran D Data-data pada penentuan momen magnet CaCu(CH 3 COO) 4.6H 2 O dengan MSB Rumus Kimia R o R s m o (gram) m s (gram) l (cm) m s -m o (gram) m obs CaCu(CH 3 COO) 4.6H 2 O , ,50 0,1275 1,75 Perhitungan : χ q = { c x l ( Rs Ro ) }/ (m s m o ).10 9 cgs unit = { 1,1 x 2,5 ( 84-(-32))}/(0,1275) cgs = { 319} / 0, cgs = 2,63 x 10-6 cgs χ M = χ q x Mr = 2,63 x 10-6 x 447,89 = 1175,9 x 10-6 cgs Faktor koreksi untuk CaCu(CH3COO) 4.6H 2 O χ D = { Ca 2+ + Cu ( CH3COO - ) + 6(H 2 O)} = { (-8) + (-11) + 4(-28,79) + 6(-13)}.10-6 cgs = - 211,96 x 10-6 cgs χ 1 M = χ M - χ D = { 1175,9 - ( - 211,96) } x 10-6 = 1387,9 x 10-6 cgs Momen magnet hasil observasi pada suhu 26,5 o C adalah: 1 μ obs = 8 x χ M x T = (8 x 1387,9 x 10-6 x 299,5 ) = 3,325 = 1,75 BM 41
8 Lampiran E Data gravimetri kadar air kristal garam sederhana Cu 2 (CH 3 COO) 4.2H 2 O massa cawan kosong (sudah konstan) = 44,0772 gram massa cawan dan kristal sebelum dioven = 44,4254 gram massa kristal sebelum dioven adalah = 0,3482 gram massa cawan dan kristal sesudah dioven = 44,3916 gram massa kristal sesudah dioven = 0,3144 gram massa H 2 O yang diuapkan (44, ,0772) = 0,0338 gram Persamaan reaksi: Cu 2 (CH 3 COO) 4.xH 2 O Cu 2 (CH 3 COO) 4 + x H 2 O Dengan cara yang sama seperti pada lampiran A diperoleh x = 1,02 yang dibulatkan menjadi 1 sehingga rumus kimia garam sederhana tembaga(ii) asetat untuk bentuk dimernya adalah Cu 2 (CH 3 COO) 4.2H 2 O. 42
9 Lampiran F Penentuan kadar Cu dalam Cu(CH 3 COO) 2.H 2 O secara titrasi iodometri Data titrasi larutan tembaga asetat dengan larutan Na 2 S 2 O 3 0,0102 M No. Volum larutan tembaga (II) asetat Volum larutan Na 2 S 2 O 3 (ml) Cu 2+ (ml) , ,80 Rata-rata 9,82 10 ml larutan Cu 2+ dari sampel 0,2003 gram dalam 100 ml. Reaksi yang terjadi pada titrasi iodometri : 2 Cu 2+ (aq) + 4I - (aq) 2 CuI (s) + I 2 (aq) I 2(aq) + 2 S 2 O 3 (aq) 2I - (aq) + S 2 O 4 (aq) Jumlah mmol S 2 O 3 setara dengan jumlah mmol Cu 2+ Maka dapat ditentukan [ Cu 2+ ] = (V.S 2 O 3 x M.S 2 O 3 ) / V.Cu 2+ = ( 9,82 ml x 0,0102 M) / 10 ml = 0,0101 M Dalam 100 ml larutan Cu 2+ = 100 ml x 0,0101 M = 1,007 mmol Massa Cu sama dengan = 1,007 mmol x 63,55 g/mol = 63,60 mg Kadar Cu dalam 0,2003 gram sampel = (63,60mg/200,3mg) x 100 %= 31,87 % 43
10 Lampiran G Data-data pada penentuan momen magnet Cu 2 (CH 3 COO) 4.2H 2 O dengan MSB m o m s Rumus Kimia R o R s (gram) l m s -m o (gram) (cm) (gram) m obs Cu 2 (CH 3 COO) 4.2H 2 O , ,50 0,1229 1,86 Perhitungan : χ q = { c x l ( Rs Ro ) }/ (m s m o ).10 9 cgs unit = { 1,1 x 2,50 (115-(-32))}/(0,1229) cgs = { 404,25} / 0, cgs = 3,23 x 10-6 cgs χ M = χ q x Mr = 3,23 x 10-6 x 399,30 = 1289,7 x 10-6 cgs Faktor koreksi untuk Cu 2 (CH 3 COO) 4.2H 2 O χ D = { 2Cu ( CH3COO - ) + 2(H 2 O)} = { 2(-11) + 4(-28,79) + 2(-13)}.10-6 cgs = ( ,16 26 )x 10-6 cgs = -163,16 x 10-6 cgs χ 1 M = χ M - χ D = { 1289,7 - ( -163,16) } x 10-6 = 1453 x 10-6 cgs Momen magnet hasil observasi pada suhu 26,5 o C adalah: 1 μ obs = 8 x χ M x T = (8 x 1453 x 10-6 x 299,5 ) 44
11 = 3,48 = 1,86 BM Lampiran H Perhitungan Randemen untuk hasil sintesis dari perbandingan Ca 2+ : Cu 2+ = 4:1 Massa CaO(Mr=56,08) = 0,5 gram Massa Cu(CH 3 COO) 2 H 2 O(199,65) = 0,5 gram Ca 2+ (aq) + Cu 2+ (aq) + 4 CH 3 COO - (aq) CaCu(CH 3 COO) 4.6H 2 O 0,008 mol 0,002 mol 0,002 mol Massa CaCu(CH 3 COO) 4.6H 2 O (Mr=447,89) secara teoritis berdasarkan persamaan reaksi tersebut adalah = 0,002 mol X 447,89 gram/mol = 0,8958 gram Massa yang dihasilkan dari sintesis = 0,3578 gram 0,3578 gr Randemen = x 100 % 0,8958 gr = 39,94 % dibilatkan menjadi 40 % 45
12 Perhitungan Randemen untuk hasil sintesis dari perbandingan Ca 2+ : Cu 2+ = 6:1 Massa CaO(Mr=56,08) = 0,84 gram Massa Cu(CH 3 COO) 2 H 2 O(199,65) = 0,49 gram Reaksi : Ca 2+ (aq) + Cu 2+ (aq) + 4 CH 3 COO - (aq) CaCu(CH 3 COO) 4.6H 2 O 0,0150 mol 0,0025 mol 0,0025 mol Massa CaCu(CH 3 COO) 4.6H 2 O (Mr=447,89) secara teoritis berdasarkan persamaan reaksi tersebut adalah = 0,0025 mol X 447,89 gram/mol = 1,1196 gram Massa yang dihasilkan dari sintesis = 0,6833 gram Randemen = 0,6833 gr x 100 % 1,1196 gr = 61,03 % dibulatkan menjadi 61 % Perhitungan Randemen untuk hasil sintesis dari perbandingan Ca 2+ : Cu 2+ = 2:1 Massa CaO(Mr=56,08) = 0,48 gram Massa Cu(CH 3 COO) 2 H 2 O(199,65) = 0,89 gram Ca 2+ (aq) + Cu 2+ (aq) + 2 CH 3 COO - (aq) Cu(CH 3 COO) 2.H 2 O 0,008 mol 0,004 mol 0,004 mol Massa Cu(CH 3 COO) 2.H 2 O (Mr=199,65) secara teoritis berdasarkan persamaan reaksi tersebut adalah=0,004 mol X 199,65 gram/mol = gram Massa yang dihasilkan dari sintesis = 0,3697 gram 0,3697 gr Randemen = x 100% 0,7986 gr = 46,30 % dibulatkan menjadi 46 % 46
13 Lampiran I Data kristal Cu 2 (CH 3 COO) 4.2H 2 O Data sistem kristal dan struktur hasil refinement 47
14 Rumus empiris Berat molekul Temperatur(K) Panjang gelombang Ǻ Sistem kristal/ group ruang Parameter sel satuan C 8 H 16 Cu 2 O , ,71073 I 4/m a = 13,153(4) α = 90 o b = 8,558(2) β = 116,969(4) o c = 13,832(4) γ = 90 o Volume Ǻ 3 Jumlah molekul dalam sel satuan(z) Massa jenis terhitung(gcm -3 ) Ukuran kristal Nilai 2 theta untuk pengumpulan data Indek-indek pembatas 1387,5(7) 4 1,282 0,39 x 0,36 x 0,13 mm 2,95 25,50-14<h<15, -7<k<10, -16<l<13 Reflections collected/unique Completenes to theta Data/restraints/parameter Goodness-of-fit on F 2 Final R indices [I>2sigma(I)] R indices (all data) 3550/1298 [R(Int) = 0,0134 ] 99,9% 1298/0/99 1,103 R1 = 0,0264 wr2 = 0,0733 R1 = 0,0280 wr2 = 0,0744 Lampiran J Data Panjang dan sudut ikatan terseleksi dalam Cu 2 (CH 3 COO) 4 2H 2 O Ikatan Panjang (Ǻ) Ikatan Sudut ( o ) 48
15 Cu(1)-O(5) 1,9423(18) O(5)-Cu(1)-O(2) 168,70(8) Cu(1)-O(2) 1,9535(19) O(5)-Cu(1)-O(1) 87,52(8) Cu(1)-O(1) 1,9802(19) O(2)-Cu(1)-O(1) 90.90(8) Cu(1)-O(4) 1,9920(19) O(5)-Cu(1)-O(4) 90,12(8) Cu(1)-Cu(1)#1 2,6114(70) O(2)-Cu(1)-O(4) 89,27(8) Cu(1)-O(3) 2,1520(20) O(1)-Cu(1)-O(4) 168,78(8) O(1)-C(2) 1,259(30) O(5)-Cu(1)-O(3) 97,80(8) O(2)-C(3)#1 1,254(30) O(2)-Cu(1)-O(3) 93,50(9) O(4)-C(2)#1 1,2620(3) O(1)-Cu(1)-O(3) 98,04(9) O(5)-C(3) 1,249(3) O(5)-Cu(1)-Cu(1)#1 86,04(6) O(3)-H(3A) 0,7800(4) O(2)-Cu(1)-Cu(1)#1 82,69(6) O(3)-H(3B) 0,7300(3) O(1)-Cu(1)-Cu(1)#1 86,27(6) O(4)-C(2)#1 1,262(30) O(4)-Cu(1)-Cu(1)#1 82,63(6) C(1)-H(1A) 0,9600 O(3)-Cu(1)-Cu(1)#1 174,32(6) C(1)-H(1A) 0,9600 C(2)-O(1)-CU(1) 121,63(16) C(1)-H(1B) 0,9600 C(3)#1-O(2)-(1) 124,27(17) C(4)-H(4B) 0,9600 Cu(1)-O(3)-H(3A) 114(3) C(4)-H(4C) 0,9600 Cu(1)-O(3)-H(3B) 131(3) C(4)-H(4D) 0,9600 H(3A)-O(3)-H(3B) 111(4) C(2)-O(4)#1 1,2620(3) C(2)#1-O(4)-Cu(1) 125,13(17) C(3)-C(4)#1 1,2540(3) C(3)-O(5)-Cu(1) 121,04(17) C(1)-C(2) 1,4950(4) C(2)-C(1)-H(1A) 109,5 C(3)-C(4) 1,5040(4) C(2)-C(1)-H(1B) 109,5 49
16 Data panjang ikatan (Ǻ) sudut ikatan ( o ) terseleksi pada struktur molekul Cu 2 (CH 3 COO) 4.2H 2 O CU(1)-O(5) (18) CU(1)-O(2) (19) CU(1)-O(1) (19) CU(1)-O(4) (19) CU(1)-O(3) 2.152(2) CU(1)-CU(1)# (7) 50
17 O(1)-C(2) 1.259(3) O(2)-C(3)# (3) O(3)-H(3A) 0.78(4) O(3)-H(3B) 0.73(3) O(4)-C(2)# (3) O(5)-C(3) 1.249(3) C(1)-C(2) 1.495(4) C(1)-H(1A) C(1)-H(1B) C(1)-H(1C) C(2)-O(4)# (3) C(3)-O(2)# (3) C(3)-C(4) 1.504(4) C(4)-H(4B) C(4)-H(4C) C(4)-H(4D) O(5)-CU(1)-O(2) (8) O(5)-CU(1)-O(1) 87.52(8) O(2)-CU(1)-O(1) 90.90(8) O(5)-CU(1)-O(4) 90.12(8) O(2)-CU(1)-O(4) 89.27(8) O(1)-CU(1)-O(4) (8) O(5)-CU(1)-O(3) 97.80(8) O(2)-CU(1)-O(3) 93.50(9) O(1)-CU(1)-O(3) 98.04(9) O(4)-CU(1)-O(3) 93.15(9) O(5)-CU(1)-CU(1)# (6) O(2)-CU(1)-CU(1)# (6) O(1)-CU(1)-CU(1)# (6) O(4)-CU(1)-CU(1)# (6) O(3)-CU(1)-CU(1)# (6) C(2)-O(1)-CU(1) (16) C(3)#1-O(2)-CU(1) (17) CU(1)-O(3)-H(3A) 114(3) CU(1)-O(3)-H(3B) 131(3) H(3A)-O(3)-H(3B) 111(4) C(2)#1-O(4)-CU(1) (17) 51
18 1 Snavely, F.A., Yoder, C.H., (1971), The preparation and analysis of some double salt. An introductory experiment, Journal Chemical Education, V.48, hal H. Valentine Knaggs, Potatos as Food and Medicine-Epsom Salt: Its value and use the Cleansing Saline Fast, Linda Edenfield Fantasy Tan & Float, San Bernardino, V.B. Jordanvska, Synthesis and Thermal Decomposition of Double Salt Dimethilammonium sulfat Hexahydrate of Aluminium and Chromium Journal of Thermal Analysis and Calorimetry, Volume 35, William Bly, Zinc Ammonium Chlorida: Double Salt, the limited England, Young, Jay A. (2004). Potasium Aluminum Sulfate 12 Hydrate, Journal Chemical Education.V.81 hal Holden, Morisson, Crystals and Crystal Growing, Doubleday, Anchor, New York, 1960, p David A. Langs, Curtis R. Hare, The Crystal Structure of Calcium Copper Acetate Hexahidrate and its Isomorph Calcium Cadmium Acetate Hexahidrate, Departement of Chemistry, State University of New York, New York,
19 8 Canham,.Geoff Rayner, Descriptive Inorganic Chemistry, Freeman and Compeny, New York, 2000 p Eli Maria Ulfah, Fani alifia Yasnur, Istadi, 2006, Optimasi pembuatan katalis Zeolit X dari Tawas, NaOH dan Water Glass dengan Response Surface Methodology 10 Nani Sukasediati, Tawas Penawar Bau Badan Tradisional, Pusat Penelitian dan Pengembangan Farmasi, Badan Penelitian dan Pengembangan Kesehatan, Departemen Kesehatan RI, Jakarta, Jordi, F., (1996), Paceite Mineral Data, ck.php?oparams=2_bannerid=11_2oneid, 12/18/ E.A.Klop,A.J.M.Duisenberg and A.L.Spek, Reinvestigation of the Structure of Calcium Copper Acetate Hexahydrate, CaCu(CH 3 COO) 4.6H 2 O, Acta Crystaloghrafica, C39, 1983, p , 13 M.Georgiev,D.Stoilova, Metal-water Interactions and Hydrogen Bond Strength, Journal of the University of Chemical Technology and Metallurgy, 42,2, 2007,p Anthony Musumeci, Ray.L.Frost, Eric Waclawik, A spectroscopic study of the mineral paceite ( calcium acetate ) Inorganic Materials Program, School of Physical and Chemical Sciences, Queensland, Australia J.V.Bellini, R.Machado, M.R.Morelli,R.H.G.A.Kiminami, Thermal Structural and Morphological Characterisation of Freezi-dried Copper (II) Acetate Monohydrate and its Solid Decomposition Product.Journal of Material Research. V.5.n Vogel, Kimia Analisis Kuantitatif Anorganik, edisi ke- 4 diterjemahkan oleh Hadyana Pudjaatmaka,Penerbit IKAPI Jakarta, hal
Bab IV Hasil Penelitian dan Pembahasan. IV.1 Sintesis dan karaktrisasi garam rangkap CaCu(CH 3 COO) 4.6H 2 O
 Bab IV Hasil Penelitian dan Pembahasan IV.1 Sintesis dan karaktrisasi garam rangkap CaCu(CH 3 COO) 4.6H 2 O Garam rangkap CaCu(CH 3 COO) 4.6H 2 O telah diperoleh dari reaksi larutan kalsium asetat dengan
Bab IV Hasil Penelitian dan Pembahasan IV.1 Sintesis dan karaktrisasi garam rangkap CaCu(CH 3 COO) 4.6H 2 O Garam rangkap CaCu(CH 3 COO) 4.6H 2 O telah diperoleh dari reaksi larutan kalsium asetat dengan
Bab III Metodologi Penelitian. Sintesis CaCu(CH 3 COO) 4.xH 2 O. Karakterisasi. Penentuan Rumus kimia
 Bab III Metodologi Penelitian Penelitian ini terdiri dari dua bagian yaitu sintesis dan karakterisasi garam rangkap CaCu(CH 3 COO) 4.6H 2 O. Pada sintesis garam rangkap tersebut dilakukan variasi perbandingan
Bab III Metodologi Penelitian Penelitian ini terdiri dari dua bagian yaitu sintesis dan karakterisasi garam rangkap CaCu(CH 3 COO) 4.6H 2 O. Pada sintesis garam rangkap tersebut dilakukan variasi perbandingan
Modul 3 Ujian Praktikum. KI2121 Dasar Dasar Kimia Analitik PENENTUAN KADAR TEMBAGA DALAM KAWAT TEMBAGA
 Modul 3 Ujian Praktikum KI2121 Dasar Dasar Kimia Analitik PENENTUAN KADAR TEMBAGA DALAM KAWAT TEMBAGA Disusun Oleh: Siwi Aji Widhi Astuti (10515026) Irin Safitri (10515029) Yasmine Sophi Damayanti (10515031)
Modul 3 Ujian Praktikum KI2121 Dasar Dasar Kimia Analitik PENENTUAN KADAR TEMBAGA DALAM KAWAT TEMBAGA Disusun Oleh: Siwi Aji Widhi Astuti (10515026) Irin Safitri (10515029) Yasmine Sophi Damayanti (10515031)
Bab II Tinjauan Pustaka
 Bab II Tinjauan Pustaka II.1 Garam rangkap Garam rangkap adalah garam yang terdiri dari dua kation yang berbeda dengan sebuah anion yang sama dalam satu kisi kristalnya. Garam rangkap biasanya lebih mudah
Bab II Tinjauan Pustaka II.1 Garam rangkap Garam rangkap adalah garam yang terdiri dari dua kation yang berbeda dengan sebuah anion yang sama dalam satu kisi kristalnya. Garam rangkap biasanya lebih mudah
SINTESIS DAN KARAKTERISASI GARAM RANGKAP KALSIUM TEMBAGA(II) ASETAT HEKSAHIDRAT CaCu(CH 3 COO) 4.6H 2 O
 SINTESIS DAN KARAKTERISASI GARAM RANGKAP KALSIUM TEMBAGA(II) ASETAT HEKSAHIDRAT CaCu(CH 3 COO) 4.6H 2 O TESIS Karya tulis ini sebagai salah satu syarat Untuk memperoleh gelar Magister dari Institut Teknologi
SINTESIS DAN KARAKTERISASI GARAM RANGKAP KALSIUM TEMBAGA(II) ASETAT HEKSAHIDRAT CaCu(CH 3 COO) 4.6H 2 O TESIS Karya tulis ini sebagai salah satu syarat Untuk memperoleh gelar Magister dari Institut Teknologi
Modul 3 Ujian Praktikum. KI2121 Dasar Dasar Kimia Analitik PENENTUAN KADAR TEMBAGA DALAM KAWAT TEMBAGA
 Modul 3 Ujian Praktikum KI2121 Dasar Dasar Kimia Analitik PENENTUAN KADAR TEMBAGA DALAM KAWAT TEMBAGA Disusun oleh: Sandya Yustitia 10515050 Fritz Ferdinand 10515059 Maulinda Kusumawardani 10515061 Muhammad
Modul 3 Ujian Praktikum KI2121 Dasar Dasar Kimia Analitik PENENTUAN KADAR TEMBAGA DALAM KAWAT TEMBAGA Disusun oleh: Sandya Yustitia 10515050 Fritz Ferdinand 10515059 Maulinda Kusumawardani 10515061 Muhammad
Hubungan koefisien dalam persamaan reaksi dengan hitungan
 STOIKIOMETRI Pengertian Stoikiometri adalah ilmu yang mempelajari dan menghitung hubungan kuantitatif dari reaktan dan produk dalam reaksi kimia (persamaan kimia) Stoikiometri adalah hitungan kimia Hubungan
STOIKIOMETRI Pengertian Stoikiometri adalah ilmu yang mempelajari dan menghitung hubungan kuantitatif dari reaktan dan produk dalam reaksi kimia (persamaan kimia) Stoikiometri adalah hitungan kimia Hubungan
LOGO. Stoikiometri. Tim Dosen Pengampu MK. Kimia Dasar
 LOGO Stoikiometri Tim Dosen Pengampu MK. Kimia Dasar Konsep Mol Satuan jumlah zat dalam ilmu kimia disebut mol. 1 mol zat mengandung jumlah partikel yang sama dengan jumlah partikel dalam 12 gram C 12,
LOGO Stoikiometri Tim Dosen Pengampu MK. Kimia Dasar Konsep Mol Satuan jumlah zat dalam ilmu kimia disebut mol. 1 mol zat mengandung jumlah partikel yang sama dengan jumlah partikel dalam 12 gram C 12,
HUKUM DASAR KIMIA. 2CUO. 28GRAM NITROGEN 52 GRAM MAGNESIUM NITRIDA 3 MG + N 2 MG 3 N 2
 HUKUM DASAR KIMIA. 2CUO. 28GRAM NITROGEN 52 GRAM MAGNESIUM NITRIDA 3 MG + N 2 MG 3 N 2 HUKUM DASAR KIMIA 1) Hukum Kekekalan Massa ( Hukum Lavoisier ). Yaitu : Dalam sistem tertutup, massa zat sebelum
HUKUM DASAR KIMIA. 2CUO. 28GRAM NITROGEN 52 GRAM MAGNESIUM NITRIDA 3 MG + N 2 MG 3 N 2 HUKUM DASAR KIMIA 1) Hukum Kekekalan Massa ( Hukum Lavoisier ). Yaitu : Dalam sistem tertutup, massa zat sebelum
UJIAN PRAKTIKUM KI2121 DASAR-DASAR KIMIA ANALITIK PENENTUAN KADAR KALSIUM DALAM KAPUR TULIS
 UJIAN PRAKTIKUM KI2121 DASAR-DASAR KIMIA ANALITIK PENENTUAN KADAR KALSIUM DALAM KAPUR TULIS Kelompok : Kelompok 1 Tanggal Persentasi : 14 November 2016 Tanggal Percobaan : 21 November 2016 Alfontius Linata
UJIAN PRAKTIKUM KI2121 DASAR-DASAR KIMIA ANALITIK PENENTUAN KADAR KALSIUM DALAM KAPUR TULIS Kelompok : Kelompok 1 Tanggal Persentasi : 14 November 2016 Tanggal Percobaan : 21 November 2016 Alfontius Linata
13. Gilbert, G. L., (1976), A Buffer solution and its action, J.Chem.Ed, 53, Wiger, G. R., de la Comp, U., (1978), Conjugate acid base
 DAFTAR PUSTAKA 1. Whitten, K. W., Davis, R. E., Peck, M. L., Stanley, G. G., (200), General chemistry, Seventh edition, Thomson Brooks/Cole, USA 2. Harris, D. C., (1991), Quantitative chemical analysis,
DAFTAR PUSTAKA 1. Whitten, K. W., Davis, R. E., Peck, M. L., Stanley, G. G., (200), General chemistry, Seventh edition, Thomson Brooks/Cole, USA 2. Harris, D. C., (1991), Quantitative chemical analysis,
MODUL Dasar-Dasar Kimia Analitik. Kelompok 2 :
 MODUL Dasar-Dasar Kimia Analitik Percobaan P02 Penentuan Kandungan Asam Askorbat dalam YOU C-1000 secara Iodometri Kelompok 2 : 1. Ryan Permana - 10515014 2. Ghumaydha Adha T - 10515024 3. Syafiqa Ulfa
MODUL Dasar-Dasar Kimia Analitik Percobaan P02 Penentuan Kandungan Asam Askorbat dalam YOU C-1000 secara Iodometri Kelompok 2 : 1. Ryan Permana - 10515014 2. Ghumaydha Adha T - 10515024 3. Syafiqa Ulfa
STOKIOMETRI BAB. B. Konsep Mol 1. Hubungan Mol dengan Jumlah Partikel. Contoh: Jika Ar Ca = 40, Ar O = 16, Ar H = 1, tentukan Mr Ca(OH) 2!
 BAB 7 STOKIOMETRI A. Massa Molekul Relatif Massa Molekul Relatif (Mr) biasanya dihitung menggunakan data Ar masing-masing atom yang ada dalam molekul tersebut. Mr senyawa = (indeks atom x Ar atom) Contoh:
BAB 7 STOKIOMETRI A. Massa Molekul Relatif Massa Molekul Relatif (Mr) biasanya dihitung menggunakan data Ar masing-masing atom yang ada dalam molekul tersebut. Mr senyawa = (indeks atom x Ar atom) Contoh:
LARUTAN PENYANGGA DAN HIDROLISIS
 6 LARUTAN PENYANGGA DAN HIDROLISIS A. LARUTAN PENYANGGA B. HIDROLISIS Pada bab sebelumnya, kita sudah mempelajari tentang reaksi asam-basa dan titrasi. Jika asam direaksikan dengan basa akan menghasilkan
6 LARUTAN PENYANGGA DAN HIDROLISIS A. LARUTAN PENYANGGA B. HIDROLISIS Pada bab sebelumnya, kita sudah mempelajari tentang reaksi asam-basa dan titrasi. Jika asam direaksikan dengan basa akan menghasilkan
PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA
 PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA 1 Tujuan Percobaan Tujuan dari percobaan ini adalah menentukan kadar natrium karbonat dan natrium hidrogen karbonat dengan titrasi
PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA 1 Tujuan Percobaan Tujuan dari percobaan ini adalah menentukan kadar natrium karbonat dan natrium hidrogen karbonat dengan titrasi
Laporan Praktikum KI1212. Dasar Dasar Kimia Analitik PENENTUAN KADAR KALSIUM DALAM KAPUR TULIS DENGAN METODE KOMPLEKSOMETRI
 Laporan Praktikum KI1212 Dasar Dasar Kimia Analitik PENENTUAN KADAR KALSIUM DALAM KAPUR TULIS DENGAN METODE KOMPLEKSOMETRI Disusun oleh: Alexander Leslie (10515007) Sharhan Hasabi (10515018) Devina Thasia
Laporan Praktikum KI1212 Dasar Dasar Kimia Analitik PENENTUAN KADAR KALSIUM DALAM KAPUR TULIS DENGAN METODE KOMPLEKSOMETRI Disusun oleh: Alexander Leslie (10515007) Sharhan Hasabi (10515018) Devina Thasia
Rumus Kimia. Mol unsur =
 Rumus Kimia Menentukan Rumus Kimia Zat Rumus kimia zat dapat dibedakan menjadi rumus empiris dan rumus molekul. Rumus empiris dapat ditentukan dengan menghitung mol komponen penyusun zat dengan menggunakan
Rumus Kimia Menentukan Rumus Kimia Zat Rumus kimia zat dapat dibedakan menjadi rumus empiris dan rumus molekul. Rumus empiris dapat ditentukan dengan menghitung mol komponen penyusun zat dengan menggunakan
Lampiran 1 Bahan baku dan hasil percobaan
 LAMPIRAN 13 14 Lampiran 1 Bahan baku dan hasil percobaan a a. Sampel Bijih Besi Laterit dan b. Batu bara b a b a. Briket Bijih Besi Laterit dan b. Bentuk Pelet yang akan direduksi Hasil Titrasi Analisis
LAMPIRAN 13 14 Lampiran 1 Bahan baku dan hasil percobaan a a. Sampel Bijih Besi Laterit dan b. Batu bara b a b a. Briket Bijih Besi Laterit dan b. Bentuk Pelet yang akan direduksi Hasil Titrasi Analisis
Penentuan Kesadahan Dalam Air
 Penentuan Kesadahan Dalam Air I. Tujuan 1. Dapat menentukan secara kualitatif dan kuantitatif kation (Ca²+,Mg²+) 2. Dapat membuat larutan an melakukan pengenceran II. Latar Belakang Teori Semua makhluk
Penentuan Kesadahan Dalam Air I. Tujuan 1. Dapat menentukan secara kualitatif dan kuantitatif kation (Ca²+,Mg²+) 2. Dapat membuat larutan an melakukan pengenceran II. Latar Belakang Teori Semua makhluk
I. LARUTAN BUFFER. 1. Membuat Larutan Buffer 2. Mempelajari Daya Sanggah Larutan Buffer TINJAUAN PUSTAKA
 I. LARUTAN BUFFER II. TUJUAN 1. Membuat Larutan Buffer 2. Mempelajari Daya Sanggah Larutan Buffer III. TINJAUAN PUSTAKA Larutan penyangga atau larutan buffer atau larutan dapar merupakan suatu larutan
I. LARUTAN BUFFER II. TUJUAN 1. Membuat Larutan Buffer 2. Mempelajari Daya Sanggah Larutan Buffer III. TINJAUAN PUSTAKA Larutan penyangga atau larutan buffer atau larutan dapar merupakan suatu larutan
STOIKIOMETRI. STOIKIOMETRI adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif dari komposisi zat-zat kimia dan reaksi-reaksinya.
 STOIKIOMETRI STOIKIOMETRI adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif dari komposisi zat-zat kimia dan reaksi-reaksinya. 1.HUKUM KEKEKALAN MASSA = HUKUM LAVOISIER "Massa zat-zat sebelum
STOIKIOMETRI STOIKIOMETRI adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif dari komposisi zat-zat kimia dan reaksi-reaksinya. 1.HUKUM KEKEKALAN MASSA = HUKUM LAVOISIER "Massa zat-zat sebelum
PENENTUAN KADAR CuSO 4. Dengan Titrasi Iodometri
 PENENTUAN KADAR CuSO 4 Dengan Titrasi Iodometri 22 April 2014 NURUL MU NISAH AWALIYAH 1112016200008 Kelompok 2 : 1. Widya Kusumaningrum (111201620000) 2. Ipa Ida Rosita (1112016200007) 3. Ummu Kalsum A.L
PENENTUAN KADAR CuSO 4 Dengan Titrasi Iodometri 22 April 2014 NURUL MU NISAH AWALIYAH 1112016200008 Kelompok 2 : 1. Widya Kusumaningrum (111201620000) 2. Ipa Ida Rosita (1112016200007) 3. Ummu Kalsum A.L
Stoikiometri. OLEH Lie Miah
 Stoikiometri OLEH Lie Miah 1 STANDAR KOMPETENSI KOMPETENSI DASAR INDIKATOR KARAKTERISTIK MATERI KESULITAN BELAJAR SISWA STANDAR KOMPETENSI Memahami hukum-hukum dasar Kimia dan penerapannya dalam perhitungan
Stoikiometri OLEH Lie Miah 1 STANDAR KOMPETENSI KOMPETENSI DASAR INDIKATOR KARAKTERISTIK MATERI KESULITAN BELAJAR SISWA STANDAR KOMPETENSI Memahami hukum-hukum dasar Kimia dan penerapannya dalam perhitungan
wanibesak.wordpress.com 1
 Ringkasan, contoh soal dan pembahasan mengenai asam, basa dan larutan penyangga atau larutan buffer Persamaan ionisasi air H 2O H + + OH Dari reaksi di atas sesuai hukum kesetimbangan, tetapan kesetimbangan
Ringkasan, contoh soal dan pembahasan mengenai asam, basa dan larutan penyangga atau larutan buffer Persamaan ionisasi air H 2O H + + OH Dari reaksi di atas sesuai hukum kesetimbangan, tetapan kesetimbangan
LEMBARAN SOAL 4. Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA )
 LEMBARAN SOAL 4 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah
LEMBARAN SOAL 4 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah
Bab VIII Reaksi Penetralan dan Titrasi Asam-Basa
 Bab VIII Reaksi Penetralan dan Titrasi Asam-Basa Sumber: James Mapple, Chemistry an Enquiry-Based Approach Pengukuran ph selama titrasi akan lebih akurat dengan menggunakan alat ph-meter. TUJUAN PEMBELAJARAN
Bab VIII Reaksi Penetralan dan Titrasi Asam-Basa Sumber: James Mapple, Chemistry an Enquiry-Based Approach Pengukuran ph selama titrasi akan lebih akurat dengan menggunakan alat ph-meter. TUJUAN PEMBELAJARAN
LAPORAN LENGKAP PRAKTIKUM ANORGANIK PERCOBAAN 1 TOPIK : SINTESIS DAN KARAKTERISTIK NATRIUM TIOSULFAT
 LAPORAN LENGKAP PRAKTIKUM ANORGANIK PERCOBAAN 1 TOPIK : SINTESIS DAN KARAKTERISTIK NATRIUM TIOSULFAT DI SUSUN OLEH : NAMA : IMENG NIM : ACC 109 011 KELOMPOK : 2 ( DUA ) HARI / TANGGAL : SABTU, 28 MEI 2011
LAPORAN LENGKAP PRAKTIKUM ANORGANIK PERCOBAAN 1 TOPIK : SINTESIS DAN KARAKTERISTIK NATRIUM TIOSULFAT DI SUSUN OLEH : NAMA : IMENG NIM : ACC 109 011 KELOMPOK : 2 ( DUA ) HARI / TANGGAL : SABTU, 28 MEI 2011
Soal 5 Jumlah mol dari 29,8 gram amonium fosfat ((NH4)3PO4) (Ar N = 14, H = 1, dan P = 31) adalah. A. 0,05 mol
 Bank Soal Stoikiometri Kimia Bagian 2 Soal 1 Satu liter campuran gas terdiri dari 60% volume metana (CH4) dan sisanya gas etana (C2H6) dibakar sempurna sesuai reaksi: CH4 + 3 O2 2 CO2 + 2 H2O 2 C2H6 +
Bank Soal Stoikiometri Kimia Bagian 2 Soal 1 Satu liter campuran gas terdiri dari 60% volume metana (CH4) dan sisanya gas etana (C2H6) dibakar sempurna sesuai reaksi: CH4 + 3 O2 2 CO2 + 2 H2O 2 C2H6 +
KONSEP MOL DAN STOIKIOMETRI
 BAB V KONSEP MOL DAN STOIKIOMETRI Dalam ilmu fisika, dikenal satuan mol untuk besaran jumlah zat. Dalam bab ini, akan dibahas mengenai konsep mol yang mendasari perhitungan kimia (stoikiometri). A. KONSEP
BAB V KONSEP MOL DAN STOIKIOMETRI Dalam ilmu fisika, dikenal satuan mol untuk besaran jumlah zat. Dalam bab ini, akan dibahas mengenai konsep mol yang mendasari perhitungan kimia (stoikiometri). A. KONSEP
Bab III Metodologi. III.1 Alat dan Bahan. III.1.1 Alat-alat
 Bab III Metodologi Penelitian ini dibagi menjadi 2 bagian yaitu isolasi selulosa dari serbuk gergaji kayu dan asetilasi selulosa hasil isolasi dengan variasi waktu. Kemudian selulosa hasil isolasi dan
Bab III Metodologi Penelitian ini dibagi menjadi 2 bagian yaitu isolasi selulosa dari serbuk gergaji kayu dan asetilasi selulosa hasil isolasi dengan variasi waktu. Kemudian selulosa hasil isolasi dan
STOIKIOMETRI. Purwanti Widhy H, M.Pd
 STOIKIOMETRI Purwanti Widhy H, M.Pd widhy_ipauny@yahoo.com Menentukan jumlah partikel dan jumlah mol Jumlah molx(n) = jumlah partikelx L 1 mol = L partikel L= bilangan avogadro (6.02 x 10 23 /mol)
STOIKIOMETRI Purwanti Widhy H, M.Pd widhy_ipauny@yahoo.com Menentukan jumlah partikel dan jumlah mol Jumlah molx(n) = jumlah partikelx L 1 mol = L partikel L= bilangan avogadro (6.02 x 10 23 /mol)
STUDI SPEKTROSKOPI UV-VIS DAN INFRAMERAH SENYAWA KOMPLEKS INTI GANDA Cu-EDTA
 PENULIS : 1. Sus Indrayanah, S.Si 2. Dr. rer. nat. Irmina Kris Murwani ALAMAT : JURUSAN KIMIA ITS SURABAYA JUDUL : STUDI SPEKTROSKOPI UV-VIS DAN INFRAMERAH SENYAWA KOMPLEKS INTI GANDA Cu-EDTA Abstrak :
PENULIS : 1. Sus Indrayanah, S.Si 2. Dr. rer. nat. Irmina Kris Murwani ALAMAT : JURUSAN KIMIA ITS SURABAYA JUDUL : STUDI SPEKTROSKOPI UV-VIS DAN INFRAMERAH SENYAWA KOMPLEKS INTI GANDA Cu-EDTA Abstrak :
Nova Nurfauziawati Kelompok 11A V. PEMBAHASAN
 V. PEMBAHASAN Praktikum yang dilaksanakan tanggal 3 Oktober 2011 mengenai pembuatan larutan buffer dan pengujian kestabilannya. Larutan buffer adalah campuran asam/basa lemah dan basa/asam konjugasinya
V. PEMBAHASAN Praktikum yang dilaksanakan tanggal 3 Oktober 2011 mengenai pembuatan larutan buffer dan pengujian kestabilannya. Larutan buffer adalah campuran asam/basa lemah dan basa/asam konjugasinya
Hukum Dasar Kimia Dan Konsep Mol
 A. PENDAHULUAN Hukum Dasar Kimia Dan Konsep Mol Hukum dasar kimia merupakan hukum dasar yang digunakan dalam stoikiometri (perhitungan kimia), antara lain: 1) Hukum Lavoisier atau hukum kekekalan massa.
A. PENDAHULUAN Hukum Dasar Kimia Dan Konsep Mol Hukum dasar kimia merupakan hukum dasar yang digunakan dalam stoikiometri (perhitungan kimia), antara lain: 1) Hukum Lavoisier atau hukum kekekalan massa.
BAB V PERHITUNGAN KIMIA
 BAB V PERHITUNGAN KIMIA KOMPETENSI DASAR 2.3 : Menerapkan hukum Gay Lussac dan hukum Avogadro serta konsep mol dalam menyelesaikan perhitungan kimia (stoikiometri ) Indikator : 1. Siswa dapat menghitung
BAB V PERHITUNGAN KIMIA KOMPETENSI DASAR 2.3 : Menerapkan hukum Gay Lussac dan hukum Avogadro serta konsep mol dalam menyelesaikan perhitungan kimia (stoikiometri ) Indikator : 1. Siswa dapat menghitung
SKL 2 RINGKASAN MATERI. 1. Konsep mol dan Bagan Stoikiometri ( kelas X )
 SKL 2 Menerapkan hukum-hukum dasar kimia untuk memecahkan masalah dalam perhitungan kimia. o Menganalisis persamaan reaksi kimia o Menyelesaikan perhitungan kimia yang berkaitan dengan hukum dasar kimia
SKL 2 Menerapkan hukum-hukum dasar kimia untuk memecahkan masalah dalam perhitungan kimia. o Menganalisis persamaan reaksi kimia o Menyelesaikan perhitungan kimia yang berkaitan dengan hukum dasar kimia
3.5 Karakterisasi Sampel Hasil Sintesis
 7 konsentrasi larutan Ca, dan H 3 PO 4 yang digunakan ada 2 yaitu: 1) Larutan Ca 1 M (massa 7,6889 gram) dan H 3 PO 4 0,6 M (volume 3,4386 ml) 2) Larutan Ca 0,5 M (massa 3,8449) dan H 3 PO 4 0,3 M (volume
7 konsentrasi larutan Ca, dan H 3 PO 4 yang digunakan ada 2 yaitu: 1) Larutan Ca 1 M (massa 7,6889 gram) dan H 3 PO 4 0,6 M (volume 3,4386 ml) 2) Larutan Ca 0,5 M (massa 3,8449) dan H 3 PO 4 0,3 M (volume
TITRASI REDUKSI OKSIDASI OXIDATION- REDUCTION TITRATION
 TITRASI REDUKSI OKSIDASI OXIDATION- REDUCTION TITRATION HERMAN, S.Pd., M.Si FARMASI UNMUL TITRASI REDUKSI OKSIDASI TITRASI REDUKSI OKSIDASI DEFINISI analisis titrimetri yang didasarkan pada reaksi reduksi
TITRASI REDUKSI OKSIDASI OXIDATION- REDUCTION TITRATION HERMAN, S.Pd., M.Si FARMASI UNMUL TITRASI REDUKSI OKSIDASI TITRASI REDUKSI OKSIDASI DEFINISI analisis titrimetri yang didasarkan pada reaksi reduksi
STOIKIOMETRI. Massa molekul relatif suatu zat sama dengan jumlah massa atom relatif atomatom penyusun molekul zat tersebut.
 STOIKIOMETRI Istilah STOIKIOMETRI berasal dari kata-kata Yunani yaitu Stoicheion (partikel) dan metron (pengukuran). STOIKIOMETRI akhirnya mengacu kepada cara perhitungan dan pengukuran zat serta campuran
STOIKIOMETRI Istilah STOIKIOMETRI berasal dari kata-kata Yunani yaitu Stoicheion (partikel) dan metron (pengukuran). STOIKIOMETRI akhirnya mengacu kepada cara perhitungan dan pengukuran zat serta campuran
Sintesis Zeolit 4A dari Fly Ash Sawit Dengan Variasi Waktu Pengadukan dan Waktu Pemanasan Gel
 Sintesis Zeolit 4A dari Fly Ash Sawit Dengan Variasi Pengadukan dan Pemanasan Gel Yelmida, Ida Zahrina, Fajril Akbar, Adelia Suchi Laboratorium Teknik Reaksi Kimia Jurusan Teknik Kimia Universitas Riau
Sintesis Zeolit 4A dari Fly Ash Sawit Dengan Variasi Pengadukan dan Pemanasan Gel Yelmida, Ida Zahrina, Fajril Akbar, Adelia Suchi Laboratorium Teknik Reaksi Kimia Jurusan Teknik Kimia Universitas Riau
BAB III METODOLOGI PENELITIAN. Jenis penelitian ini adalah termasuk penelitian deskriptif.
 BAB III METODOLOGI PENELITIAN A. Jenis Penelitian Jenis penelitian ini adalah termasuk penelitian deskriptif. B. Tempat dan Waktu Penelitian Tempat penelitian di laboratorium kimia Analis Kesehatan Muhammadiyah
BAB III METODOLOGI PENELITIAN A. Jenis Penelitian Jenis penelitian ini adalah termasuk penelitian deskriptif. B. Tempat dan Waktu Penelitian Tempat penelitian di laboratorium kimia Analis Kesehatan Muhammadiyah
ASIDI-ALKALIMETRI PENETAPAN KADAR ASAM SALISILAT
 ASIDI-ALKALIMETRI PENETAPAN KADAR ASAM SALISILAT I. DASAR TEORI I.1 Asidi-Alkalimetri Asidi-alkalimetri merupakan salah satu metode analisis titrimetri. Analisis titrimetri mengacu pada analisis kimia
ASIDI-ALKALIMETRI PENETAPAN KADAR ASAM SALISILAT I. DASAR TEORI I.1 Asidi-Alkalimetri Asidi-alkalimetri merupakan salah satu metode analisis titrimetri. Analisis titrimetri mengacu pada analisis kimia
KONSEP MOL DAN STOIKIOMETRI
 KONSEP MOL DAN STOIKIOMETRI HUKUM-HUKUM DASAR KIMIA 1. Asas Lavoiser atau kekekalan massa jumlah sebelum dan setelah reaksi kimia adalah tetap 2. Hukum Gas Ideal P V = nrt Dengan P adalah tekanan (atm),
KONSEP MOL DAN STOIKIOMETRI HUKUM-HUKUM DASAR KIMIA 1. Asas Lavoiser atau kekekalan massa jumlah sebelum dan setelah reaksi kimia adalah tetap 2. Hukum Gas Ideal P V = nrt Dengan P adalah tekanan (atm),
LARUTAN. Zat terlarut merupakan komponen yang jumlahnya sedikit, sedangkan pelarut adalah komponen yang terdapat dalam jumlah banyak.
 LARUTAN Larutan merupakan campuran yang homogen,yaitu campuran yang memiliki komposisi merata atau serba sama di seluruh bagian volumenya. Suatu larutan mengandung dua komponen atau lebih yang disebut
LARUTAN Larutan merupakan campuran yang homogen,yaitu campuran yang memiliki komposisi merata atau serba sama di seluruh bagian volumenya. Suatu larutan mengandung dua komponen atau lebih yang disebut
PENENTUAN KADAR KLORIDA DALAM MgCl 2 DENGAN ANALISIS GRAVIMETRI
 PENENTUAN KADAR KLORIDA DALAM MgCl 2 DENGAN ANALISIS GRAVIMETRI Tujuan: Menerapkan analisis gravimetric dalam penentuan kadar klorida Menentukan kadar klorida dalam MgCl 2 Widya Kusumaningrum (1112016200005),
PENENTUAN KADAR KLORIDA DALAM MgCl 2 DENGAN ANALISIS GRAVIMETRI Tujuan: Menerapkan analisis gravimetric dalam penentuan kadar klorida Menentukan kadar klorida dalam MgCl 2 Widya Kusumaningrum (1112016200005),
TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN
 TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN I. JUDUL PERCOBAAN : TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN II. TUJUAN PERCOBAAN : 1. Membuat dan
TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN I. JUDUL PERCOBAAN : TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN II. TUJUAN PERCOBAAN : 1. Membuat dan
LAMPIRAN B DATA HASIL PENGINDEKSAN DAN PENGHALUSAN PUNCAK DIFRAKSI SINAR-X SERBUK
 LAMPIRAN B DATA HASIL PENGINDEKSAN DAN PENGHALUSAN PUNCAK DIFRAKSI SINAR-X SERBUK 1. Kompleks [Fe(NH 2 trz) 3 ]Cl 2.3H 2 O Tabel B.1 Data input (puncak difraksi) dan out put hasil dari program CELL-A Data
LAMPIRAN B DATA HASIL PENGINDEKSAN DAN PENGHALUSAN PUNCAK DIFRAKSI SINAR-X SERBUK 1. Kompleks [Fe(NH 2 trz) 3 ]Cl 2.3H 2 O Tabel B.1 Data input (puncak difraksi) dan out put hasil dari program CELL-A Data
SOAL SELEKSI NASIONAL TAHUN 2006
 SOAL SELEKSI NASIONAL TAHUN 2006 Soal 1 ( 13 poin ) KOEFISIEN REAKSI DAN LARUTAN ELEKTROLIT Koefisien reaksi merupakan langkah penting untuk mengamati proses berlangsungnya reaksi. Lengkapi koefisien reaksi-reaksi
SOAL SELEKSI NASIONAL TAHUN 2006 Soal 1 ( 13 poin ) KOEFISIEN REAKSI DAN LARUTAN ELEKTROLIT Koefisien reaksi merupakan langkah penting untuk mengamati proses berlangsungnya reaksi. Lengkapi koefisien reaksi-reaksi
Fraksi mol adalah perbandingan antara jumiah mol suatu komponen dengan jumlah mol seluruh komponen yang terdapat dalam larutan.
 Konsentrasi Larutan Ditulis oleh Redaksi chem-is-try.org pada 02-05-2009 Konsentrasi merupakan cara untuk menyatakan hubungan kuantitatif antara zat terlarut dan pelarut. Menyatakan konsentrasi larutan
Konsentrasi Larutan Ditulis oleh Redaksi chem-is-try.org pada 02-05-2009 Konsentrasi merupakan cara untuk menyatakan hubungan kuantitatif antara zat terlarut dan pelarut. Menyatakan konsentrasi larutan
OAL TES SEMESTER II. I. Pilihlah jawaban yang paling tepat!
 KIMIA XI SMA 217 S OAL TES SEMESTER II I. Pilihlah jawaban yang paling tepat! 1. Basa menurut Arhenius adalah senyawa yang bila dilarutkan dalam air akan menghasilkan a. proton d. ion H b. elektron e.
KIMIA XI SMA 217 S OAL TES SEMESTER II I. Pilihlah jawaban yang paling tepat! 1. Basa menurut Arhenius adalah senyawa yang bila dilarutkan dalam air akan menghasilkan a. proton d. ion H b. elektron e.
Stoikiometri. Berasal dari kata Stoicheion (partikel) dan metron (pengukuran). Cara perhitungan dan pengukuran zat serta campuran kimia.
 Stoikiometri Berasal dari kata Stoicheion (partikel) dan metron (pengukuran). Cara perhitungan dan pengukuran zat serta campuran kimia. Bilangan Avogadro Stoikometri: pengukuran kuantitatif sehingga perlu
Stoikiometri Berasal dari kata Stoicheion (partikel) dan metron (pengukuran). Cara perhitungan dan pengukuran zat serta campuran kimia. Bilangan Avogadro Stoikometri: pengukuran kuantitatif sehingga perlu
STOIKIOMETRI. Oleh. Sitti Rahmawati S.Pd.
 STOIKIOMETRI Oleh Sitti Rahmawati S.Pd Copyright oke.or.id Artikel ini boleh dicopy,diubah, dikutip, di cetak dalam media kertas atau yang lain, dipublikasikan kembali dalam berbagai bentuk dengan tetap
STOIKIOMETRI Oleh Sitti Rahmawati S.Pd Copyright oke.or.id Artikel ini boleh dicopy,diubah, dikutip, di cetak dalam media kertas atau yang lain, dipublikasikan kembali dalam berbagai bentuk dengan tetap
OLIMPIADE KIMIA INDONESIA
 OLIMPIADE KIMIA INDONESIA OLIMPIADE SAINS NASIONAL SELEKSI KABUPATEN / KOTA UjianTeori Waktu 2 Jam Departemen Pendidikan Nasional Direktorat Jenderal Managemen Pendidikan Dasar dan Menengah Direktorat
OLIMPIADE KIMIA INDONESIA OLIMPIADE SAINS NASIONAL SELEKSI KABUPATEN / KOTA UjianTeori Waktu 2 Jam Departemen Pendidikan Nasional Direktorat Jenderal Managemen Pendidikan Dasar dan Menengah Direktorat
BAB I STOIKHIOMETRI I - 1
 BAB I STOIKHIOMETRI 1.1 PENDAHULUAN Setiap zat, unsur, senyawa dalam kimia mempunyai nama dan rumus uniknya sendiri. Cara tersingkat untuk memerikan suatu reaksi kimia adalah dengan menuliskan rumus untuk
BAB I STOIKHIOMETRI 1.1 PENDAHULUAN Setiap zat, unsur, senyawa dalam kimia mempunyai nama dan rumus uniknya sendiri. Cara tersingkat untuk memerikan suatu reaksi kimia adalah dengan menuliskan rumus untuk
MODUL PRAKTIKUM KIMIA ANALITIK ( KI-2121) PENENTUAN KADAR IOD DALAM BETADINE SECARA TITRIMETRI
 MODUL PRAKTIKUM KIMIA ANALITIK ( KI-2121) PENENTUAN KADAR IOD DALAM BETADINE SECARA TITRIMETRI Disusun oleh: 1. SISCA ERICA (10515001) 2. DYAH AYU R. (10515003) 3. WANDA HIMAWAN (10515008) 4. VIORANTY
MODUL PRAKTIKUM KIMIA ANALITIK ( KI-2121) PENENTUAN KADAR IOD DALAM BETADINE SECARA TITRIMETRI Disusun oleh: 1. SISCA ERICA (10515001) 2. DYAH AYU R. (10515003) 3. WANDA HIMAWAN (10515008) 4. VIORANTY
Soal dan Jawaban Titrasi Asam Basa
 Soal dan Jawaban Titrasi Asam Basa Rabu, 16 Januari 20130 komentar Inilah beberapa contoh soal dan jawaban tentang titrasi asam basa. Bacalah benarbenar setiap latihan soal asam basa berikut. Kalau perlu,
Soal dan Jawaban Titrasi Asam Basa Rabu, 16 Januari 20130 komentar Inilah beberapa contoh soal dan jawaban tentang titrasi asam basa. Bacalah benarbenar setiap latihan soal asam basa berikut. Kalau perlu,
Penentuan Kadar Vitamin C dengan Titrasi Iodometri Langsung
 Laporan Praktikum Nama : Linda Trivana Kimia Analitik 1 NRP : G44080075 Kelompok : B-Siang Asisten : Yuyun Yunita Hari, tanggal : Selasa, 11 Mei 2010 PJP : Zulhan A, S.Si Penentuan Kadar Vitamin C dengan
Laporan Praktikum Nama : Linda Trivana Kimia Analitik 1 NRP : G44080075 Kelompok : B-Siang Asisten : Yuyun Yunita Hari, tanggal : Selasa, 11 Mei 2010 PJP : Zulhan A, S.Si Penentuan Kadar Vitamin C dengan
3. Metodologi Penelitian
 3. Metodologi Penelitian 3.1 Alat dan bahan 3.1.1 Alat Peralatan gelas yang digunakan dalam penelitian ini adalah gelas kimia, gelas ukur, labu Erlenmeyer, cawan petri, corong dan labu Buchner, corong
3. Metodologi Penelitian 3.1 Alat dan bahan 3.1.1 Alat Peralatan gelas yang digunakan dalam penelitian ini adalah gelas kimia, gelas ukur, labu Erlenmeyer, cawan petri, corong dan labu Buchner, corong
PERCOBAAN VII PEMBUATAN KALIUM NITRAT
 I. Tujuan Percobaan ini yaitu: PERCOBAAN VII PEMBUATAN KALIUM NITRAT Adapun tujuan yang ingin dicapai praktikan setelah melakukan percobaan 1. Memisahkan dua garam berdasarkan kelarutannya pada suhu tertentu
I. Tujuan Percobaan ini yaitu: PERCOBAAN VII PEMBUATAN KALIUM NITRAT Adapun tujuan yang ingin dicapai praktikan setelah melakukan percobaan 1. Memisahkan dua garam berdasarkan kelarutannya pada suhu tertentu
III. METODE PENELITIAN. Gambar 3.1 Peta Lokasi Jalur Hijau Jalan Gerilya Kota Purwokerto. bio.unsoed.ac.id
 III. METODE PENELITIAN A. Bahan dan Alat Bahan yang digunakan pada penelitian ini adalah HCl 0,7 %, NaOH1 N, ZnSO4 5%, Ba(OH)2 0,3 N, Akuades, Pereaksi Cu, Alkohol 70%. Sedangkan alat yang digunakan adalah
III. METODE PENELITIAN A. Bahan dan Alat Bahan yang digunakan pada penelitian ini adalah HCl 0,7 %, NaOH1 N, ZnSO4 5%, Ba(OH)2 0,3 N, Akuades, Pereaksi Cu, Alkohol 70%. Sedangkan alat yang digunakan adalah
BAB III METODOLOGI PENELITIAN. Jenis penelitian yang digunakan dalam penelitian ini adalah ekperimental.
 BAB III METODOLOGI PENELITIAN A. Jenis Penelitian Jenis penelitian yang digunakan dalam penelitian ini adalah ekperimental. B. Tempat dan Waktu Pengerjaan sampel dilakukan di laboratorium Teknik Kimia
BAB III METODOLOGI PENELITIAN A. Jenis Penelitian Jenis penelitian yang digunakan dalam penelitian ini adalah ekperimental. B. Tempat dan Waktu Pengerjaan sampel dilakukan di laboratorium Teknik Kimia
STOIKIOMETRI STOIKIOMETRI
 BAB V STOIKIOMETRI Standar Kompetensi Memahami hukum-hukum dasar kimia dan penerapannya dalam perhitungan kimia (stoikiometri) Kompetensi Dasar Mendeskripsikan tata nama senyawa anorganik dan organik sederhana
BAB V STOIKIOMETRI Standar Kompetensi Memahami hukum-hukum dasar kimia dan penerapannya dalam perhitungan kimia (stoikiometri) Kompetensi Dasar Mendeskripsikan tata nama senyawa anorganik dan organik sederhana
Soal-Soal. Bab 7. Latihan Larutan Penyangga, Hidrolisis Garam, serta Kelarutan dan Hasil Kali Kelarutan. Larutan Penyangga
 Bab 7 Soal-Soal Latihan Larutan Penyangga, Hidrolisis Garam, serta Kelarutan dan Hasil Kali Kelarutan Larutan Penyangga 1. Berikut ini yang merupakan pasangan asam basa terkonjugasi (A) H 3 O + dan OH
Bab 7 Soal-Soal Latihan Larutan Penyangga, Hidrolisis Garam, serta Kelarutan dan Hasil Kali Kelarutan Larutan Penyangga 1. Berikut ini yang merupakan pasangan asam basa terkonjugasi (A) H 3 O + dan OH
MODUL STOIKIOMETRI 1
 MODUL STOIKIOMETRI 1 1. Pengertian Mol Mol merupakan suatu satuan jumlah, yang berasal dari kata moles yang artinya sejumlah massa / sejumlah kecil massa, hampir sama dengan lusin. 1 mol = 6,02 X 10 23
MODUL STOIKIOMETRI 1 1. Pengertian Mol Mol merupakan suatu satuan jumlah, yang berasal dari kata moles yang artinya sejumlah massa / sejumlah kecil massa, hampir sama dengan lusin. 1 mol = 6,02 X 10 23
Penentuan Kadar Klorida Menggunakan Metode Gravimetri
 Penentuan Kadar Klorida Menggunakan Metode Gravimetri Kamis, 3 Apri 2014 Raisa Soraya, Naryanto, Melinda Indana Nasution, Septiwi Tri Pusparini Jurusan Pendidikan Imu Pengetahuan Alam Program Studi Pendidikan
Penentuan Kadar Klorida Menggunakan Metode Gravimetri Kamis, 3 Apri 2014 Raisa Soraya, Naryanto, Melinda Indana Nasution, Septiwi Tri Pusparini Jurusan Pendidikan Imu Pengetahuan Alam Program Studi Pendidikan
Lampiran 1. Lokasi Pengambilan Sampel. Mata air yang terletak di Gunung Sitember. Tempat penampungan air minum sebelum dialirkan ke masyarakat
 Lampiran 1. Lokasi Pengambilan Sampel Mata air yang terletak di Gunung Sitember Tempat penampungan air minum sebelum dialirkan ke masyarakat 48 Air minum yang dialirkan menggunakan pipa besi Lokasi pengambilan
Lampiran 1. Lokasi Pengambilan Sampel Mata air yang terletak di Gunung Sitember Tempat penampungan air minum sebelum dialirkan ke masyarakat 48 Air minum yang dialirkan menggunakan pipa besi Lokasi pengambilan
Pembuatan Kristal Tembaga Sulfat Pentahidrat (CuSO 4.5H 2 O) dari Tembaga Bekas Kumparan
 JURNAL TEKNIK POMITS Vol. 2, No. 1, (2013) ISSN: 2337-3539 (2301-9271 Print) F-121 Pembuatan Kristal Tembaga Sulfat Pentahidrat (CuSO 4.5H 2 O) dari Tembaga Bekas Kumparan Fitrony, Rizqy Fauzi, Lailatul
JURNAL TEKNIK POMITS Vol. 2, No. 1, (2013) ISSN: 2337-3539 (2301-9271 Print) F-121 Pembuatan Kristal Tembaga Sulfat Pentahidrat (CuSO 4.5H 2 O) dari Tembaga Bekas Kumparan Fitrony, Rizqy Fauzi, Lailatul
kimia ASAM-BASA III Tujuan Pembelajaran
 KTSP K-13 kimia K e l a s XI ASAM-BASA III Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami mekanisme reaksi asam-basa. 2. Memahami stoikiometri
KTSP K-13 kimia K e l a s XI ASAM-BASA III Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami mekanisme reaksi asam-basa. 2. Memahami stoikiometri
LAPORAN PRAKTIKUM 3 ph METER, BUFFER, dan PENGENCERAN DISUSUN OLEH : MARIA LESTARI DAN YULIA FITRI GHAZALI Kamis 04 Oktober s/d 16.
 LAPORAN PRAKTIKUM 3 ph METER, BUFFER, dan PENGENCERAN DISUSUN OLEH : MARIA LESTARI DAN YULIA FITRI GHAZALI Kamis 04 Oktober 2012 14.00 s/d 16.00 wib TUJUAN : 1. Agar mahasiswa dapat memahami prinsip-prinsip
LAPORAN PRAKTIKUM 3 ph METER, BUFFER, dan PENGENCERAN DISUSUN OLEH : MARIA LESTARI DAN YULIA FITRI GHAZALI Kamis 04 Oktober 2012 14.00 s/d 16.00 wib TUJUAN : 1. Agar mahasiswa dapat memahami prinsip-prinsip
BAB IV ANALISIS HASIL PENELITIAN
 BAB IV ANALISIS HASIL PENELITIAN Bab ini peneliti menganalisis hasil penelitian, yaitu isi buku Teks Kimia SMA Kelas X jilid 1 Materi Pokok Stoikiometri karangan Unggul Sudarmo yang diterbitkan oleh Erlangga
BAB IV ANALISIS HASIL PENELITIAN Bab ini peneliti menganalisis hasil penelitian, yaitu isi buku Teks Kimia SMA Kelas X jilid 1 Materi Pokok Stoikiometri karangan Unggul Sudarmo yang diterbitkan oleh Erlangga
BAB III METODOLOGI PENELITIAN. Penelitian ini dilakukan di Laboratorium Penelitian Jurusan Pendidikan
 BAB III METODOLOGI PENELITIAN 3.1 Lokasi dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Penelitian Jurusan Pendidikan Kimia FPMIPA UPI. Sementara analisis dengan menggunakan instrumen dilakukan
BAB III METODOLOGI PENELITIAN 3.1 Lokasi dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Penelitian Jurusan Pendidikan Kimia FPMIPA UPI. Sementara analisis dengan menggunakan instrumen dilakukan
METODE PENELITIAN. Penelitian ini telah dilaksanakan pada bulan April sampai September 2015 dengan
 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini telah dilaksanakan pada bulan April sampai September 2015 dengan tahapan isolasi selulosa dan sintesis CMC di Laboratorium Kimia Organik
III. METODE PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini telah dilaksanakan pada bulan April sampai September 2015 dengan tahapan isolasi selulosa dan sintesis CMC di Laboratorium Kimia Organik
Praktikum Kimia Fisika II Hidrolisis Etil Asetat dalam Suasana Asam Lemah & Asam Kuat
 I. Judul Percobaan Hidrolisis Etil Asetat dalam Suasana Asam Lemah & dalam Suasana Asam Kuat II. Tanggal Percobaan Senin, 8 April 2013 pukul 11.00 14.00 WIB III. Tujuan Percobaan Menentukan orde reaksi
I. Judul Percobaan Hidrolisis Etil Asetat dalam Suasana Asam Lemah & dalam Suasana Asam Kuat II. Tanggal Percobaan Senin, 8 April 2013 pukul 11.00 14.00 WIB III. Tujuan Percobaan Menentukan orde reaksi
KIMIA TERAPAN STOIKIOMETRI DAN HUKUM-HUKUM KIMIA Haris Puspito Buwono
 KIMIA TERAPAN STOIKIOMETRI DAN HUKUM-HUKUM KIMIA Haris Puspito Buwono Semester Gasal 2012/2013 STOIKIOMETRI 2 STOIKIOMETRI adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif dari komposisi
KIMIA TERAPAN STOIKIOMETRI DAN HUKUM-HUKUM KIMIA Haris Puspito Buwono Semester Gasal 2012/2013 STOIKIOMETRI 2 STOIKIOMETRI adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif dari komposisi
Larutan penyangga dapat terbentuk dari campuran asam lemah dan basa
 Larutan penyangga dapat terbentuk dari campuran asam lemah dan basa konjugasinya atau campuran basa lemah dan asam konjugasinya. Larutan penyangga disebut juga larutan penahan atau larutan dapar atau buffer.
Larutan penyangga dapat terbentuk dari campuran asam lemah dan basa konjugasinya atau campuran basa lemah dan asam konjugasinya. Larutan penyangga disebut juga larutan penahan atau larutan dapar atau buffer.
Tentukan ph dari suatu larutan yang memiliki konsentrasi ion H + sebesar 10 4 M dengan tanpa bantuan alat hitung kalkulator!
 Kimia Study Center - Contoh soal dan pembahasan tentang cara menghitung ph dan poh larutan asam basa berdasarkan konsentrasi ion [H + ] dan [OH ] SMA kelas 11 IPA. Berikut contoh-contoh soal yang bisa
Kimia Study Center - Contoh soal dan pembahasan tentang cara menghitung ph dan poh larutan asam basa berdasarkan konsentrasi ion [H + ] dan [OH ] SMA kelas 11 IPA. Berikut contoh-contoh soal yang bisa
Analisa Klorida Analisa Kesadahan
 Analisa Klorida Analisa Kesadahan Latar Belakang Tropis basah Air bersih Air kotor limbah Pencegahan yang serius Agar tidak berdampak buruk bagi kelangsungan hidup semua makhluk hidup Air tercemar 1 Prinsip
Analisa Klorida Analisa Kesadahan Latar Belakang Tropis basah Air bersih Air kotor limbah Pencegahan yang serius Agar tidak berdampak buruk bagi kelangsungan hidup semua makhluk hidup Air tercemar 1 Prinsip
PERCOBAAN I PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA
 LAPORAN PRAKTIKUM KIMIA ANALITIK KI-2122 PERCOBAAN I PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA Nama Praktikan : Anggi Febrina NIM : 13010107 Kelompok : 5 (Shift Pagi) Tanggal
LAPORAN PRAKTIKUM KIMIA ANALITIK KI-2122 PERCOBAAN I PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA Nama Praktikan : Anggi Febrina NIM : 13010107 Kelompok : 5 (Shift Pagi) Tanggal
Larutan penyangga adalah larutan yang dapat mempertahankan harga ph terhadap pengaruh penambahan sedikit asam atau basa, atau terhadap pengenceran.
 Standar Kompetensi Kompetensi Dasar Memahami sifatsifat larutan asambasa, metode pengukuran, dan terapannya. Mendeskripsikan sifat larutan penyangga dan peranan larutan penyangga dalam tubuh makhluk hidup.
Standar Kompetensi Kompetensi Dasar Memahami sifatsifat larutan asambasa, metode pengukuran, dan terapannya. Mendeskripsikan sifat larutan penyangga dan peranan larutan penyangga dalam tubuh makhluk hidup.
Laporan Praktikum Kimia Analitik II. Koefisien Distribusi Iod
 Laporan Praktikum Kimia Analitik II Koefisien Distribusi Iod Oleh : 1. Fitri Aprilia 093194205 2. Wilda Ulin Nuha 093194211 3. Endah Rohmawati 093194216 Universitas Negeri Surabaya Fakultas Matematika
Laporan Praktikum Kimia Analitik II Koefisien Distribusi Iod Oleh : 1. Fitri Aprilia 093194205 2. Wilda Ulin Nuha 093194211 3. Endah Rohmawati 093194216 Universitas Negeri Surabaya Fakultas Matematika
1. Dari pengujian larutan dengan kertas lakmus diperoleh data berikut:
 SOAL-SOAL BAB 5 LARUTAN ASAM BASA/ Kimia Erlangga 2B 1. Dari pengujian larutan dengan kertas lakmus diperoleh data berikut: No Larutan yang diuji Warna lakmus Merah Biru 1 X Merah Biru 2 Y Merah Merah
SOAL-SOAL BAB 5 LARUTAN ASAM BASA/ Kimia Erlangga 2B 1. Dari pengujian larutan dengan kertas lakmus diperoleh data berikut: No Larutan yang diuji Warna lakmus Merah Biru 1 X Merah Biru 2 Y Merah Merah
BAB III. METODE PENELITIAN. Penelitian ini dilaksanakan dari Bulan Januari sampai dengan bulan Juni 2015
 BAB III. METODE PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan dari Bulan Januari sampai dengan bulan Juni 2015 yang meliputi kegiatan di lapangan dan di laboratorium. Lokasi pengambilan
BAB III. METODE PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan dari Bulan Januari sampai dengan bulan Juni 2015 yang meliputi kegiatan di lapangan dan di laboratorium. Lokasi pengambilan
Lampiran 1. Skema pembuatan biodiesel. CPO H2S04 Metanol. Reaksi Esterifikasi. (^ao ( Metanol. Pencampuran. Reaksi Transesterifikasi
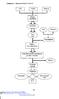 Lampiran 1. Skema pembuatan biodiesel CPO H2S04 Metanol Reaksi Esterifikasi (^ao ( Metanol Pencampuran Reaksi Transesterifikasi Pemisahan melalui penanganan gravitasi semalam Gliserol Biodiesel mentah
Lampiran 1. Skema pembuatan biodiesel CPO H2S04 Metanol Reaksi Esterifikasi (^ao ( Metanol Pencampuran Reaksi Transesterifikasi Pemisahan melalui penanganan gravitasi semalam Gliserol Biodiesel mentah
PAKET UJIAN NASIONAL 7 Pelajaran : KIMIA Waktu : 120 Menit
 PAKET UJIAN NASIONAL 7 Pelajaran : KIMIA Waktu : 120 Menit Pilihlah salah satu jawaban yang tepat! Jangan lupa Berdoa dan memulai dari yang mudah. 1. Dari beberapa unsur berikut yang mengandung : 1. 20
PAKET UJIAN NASIONAL 7 Pelajaran : KIMIA Waktu : 120 Menit Pilihlah salah satu jawaban yang tepat! Jangan lupa Berdoa dan memulai dari yang mudah. 1. Dari beberapa unsur berikut yang mengandung : 1. 20
PRAKTIKUM KIMIA ANALITIK
 PRAKTIKUM KIMIA ANALITIK Percobaan 6 PENENTUAN KADAR IOD DALAM BETADINE Disusun Oleh: Fachra Nur Arifa (10514054) Ahmad Kushay (10515053) Ikhlas Khairil Imam (10515063) Suci Jami atul M (10515083) Reneva
PRAKTIKUM KIMIA ANALITIK Percobaan 6 PENENTUAN KADAR IOD DALAM BETADINE Disusun Oleh: Fachra Nur Arifa (10514054) Ahmad Kushay (10515053) Ikhlas Khairil Imam (10515063) Suci Jami atul M (10515083) Reneva
dimana hasilnya dalam bentuk jumlah atau bilangan kadar.
 VOLUMETRI I Drs Kusumo Hariyadi Apt MS. Analisa Kimia dibagi 2 bagian : 1. Analisa Kualitatif ( analisa jenis) bertujuan mencari adanya unsur / senyawa dalam suatu sampel 2. Analisa Kuantitatif (analisa
VOLUMETRI I Drs Kusumo Hariyadi Apt MS. Analisa Kimia dibagi 2 bagian : 1. Analisa Kualitatif ( analisa jenis) bertujuan mencari adanya unsur / senyawa dalam suatu sampel 2. Analisa Kuantitatif (analisa
Lampiran 1. Prosedur kerja analisa bahan organik total (TOM) (SNI )
 41 Lampiran 1. Prosedur kerja analisa bahan organik total (TOM) (SNI 06-6989.22-2004) 1. Pipet 100 ml contoh uji masukkan ke dalam Erlenmeyer 300 ml dan tambahkan 3 butir batu didih. 2. Tambahkan KMnO
41 Lampiran 1. Prosedur kerja analisa bahan organik total (TOM) (SNI 06-6989.22-2004) 1. Pipet 100 ml contoh uji masukkan ke dalam Erlenmeyer 300 ml dan tambahkan 3 butir batu didih. 2. Tambahkan KMnO
STOKIOMETRI. Kimia Kelas X
 STOKIOMETRI Kimia Kelas X SEKOLAH MENENGAH ATAS NEGERI 12 SURABAYA 2015 STOKIOMETRI STOKIOMETRI Pada materi stokiometri, kita akan mempelajari beberapa hal seperti persamaan reaksi, hukum-hukum dasar kimia,
STOKIOMETRI Kimia Kelas X SEKOLAH MENENGAH ATAS NEGERI 12 SURABAYA 2015 STOKIOMETRI STOKIOMETRI Pada materi stokiometri, kita akan mempelajari beberapa hal seperti persamaan reaksi, hukum-hukum dasar kimia,
OLIMPIADE KIMIA INDONESIA
 OLIMPIADE KIMIA INDONESIA OLIMPIADE SAINS NASIONAL SELEKSI KABUPATEN / KOTA UjianTeori Waktu 2 Jam Departemen Pendidikan Nasional Direktorat Jenderal Managemen Pendidikan Dasar dan Menengah Direktorat
OLIMPIADE KIMIA INDONESIA OLIMPIADE SAINS NASIONAL SELEKSI KABUPATEN / KOTA UjianTeori Waktu 2 Jam Departemen Pendidikan Nasional Direktorat Jenderal Managemen Pendidikan Dasar dan Menengah Direktorat
BAB 6. Jika ke dalam air murni ditambahkan asam atau basa meskipun dalam jumlah. Larutan Penyangga. Kata Kunci. Pengantar
 Kimia XI SMA 179 BAB 6 Larutan Penyangga Tujuan Pembelajaran: Setelah mempelajari bab ini, Anda diharapkan mampu: 1. Menjelaskan pengertian larutan penyangga dan komponen penyusunnya. 2. Merumuskan persamaan
Kimia XI SMA 179 BAB 6 Larutan Penyangga Tujuan Pembelajaran: Setelah mempelajari bab ini, Anda diharapkan mampu: 1. Menjelaskan pengertian larutan penyangga dan komponen penyusunnya. 2. Merumuskan persamaan
MODUL 2 PENENTUAN KADAR ASAM ASKORBAT DALAM YOU C Kurnia Sandwika Henry Liyanto Ignatio Glory
 MODUL 2 PENENTUAN KADAR ASAM ASKORBAT DALAM YOU C-1000 Kurnia Sandwika 10515048 Henry Liyanto 10515049 Ignatio Glory 10515062 Christopher Chandra 10515071 Dita Nurkhusis 10515073 Bayu Andi Saputra 10515074
MODUL 2 PENENTUAN KADAR ASAM ASKORBAT DALAM YOU C-1000 Kurnia Sandwika 10515048 Henry Liyanto 10515049 Ignatio Glory 10515062 Christopher Chandra 10515071 Dita Nurkhusis 10515073 Bayu Andi Saputra 10515074
Reaksi Dehidrasi: Pembuatan Sikloheksena. Oleh : Kelompok 3
 Reaksi Dehidrasi: Pembuatan Sikloheksena Oleh : Kelompok 3 Outline Tujuan Prinsip Sifat fisik dan kimia bahan Cara kerja Hasil pengamatan Pembahasan Kesimpulan Tujuan Mensintesis Sikloheksena Menentukan
Reaksi Dehidrasi: Pembuatan Sikloheksena Oleh : Kelompok 3 Outline Tujuan Prinsip Sifat fisik dan kimia bahan Cara kerja Hasil pengamatan Pembahasan Kesimpulan Tujuan Mensintesis Sikloheksena Menentukan
Larutan dan Konsentrasi
 Larutan dan Konsentrasi Tujuan Pembelajaran Mahasiswa memahami konsep larutan Mahasiswa memahami konsep perhitungan konsentrasi Pentingnya perhitungan konsentrasi Pentingnya memahami sifat larutan dan
Larutan dan Konsentrasi Tujuan Pembelajaran Mahasiswa memahami konsep larutan Mahasiswa memahami konsep perhitungan konsentrasi Pentingnya perhitungan konsentrasi Pentingnya memahami sifat larutan dan
MODUL KIMIA SMA IPA Kelas 10
 SMA IPA Kelas 0 A. Massa Atom. Massa Atom Relatif (Ar) Massa atom relatif (Ar) merupakan perbandingan massa atom dengan massa satu atom yang tetap. Secara matematis dapat dirumuskan sebagai berikut. sma
SMA IPA Kelas 0 A. Massa Atom. Massa Atom Relatif (Ar) Massa atom relatif (Ar) merupakan perbandingan massa atom dengan massa satu atom yang tetap. Secara matematis dapat dirumuskan sebagai berikut. sma
SIFAT KOLIGATIF LARUTAN
 SIFAT KOLIGATIF LARUTAN STANDAR KOMPETENSI 1. Mendeskripsikan sifat-sifat Larutan, metode pengukuran dan terapannya. KOMPETENSI DASAR 1.1 Mendeskripsikan sifat-sifat Larutan, metode pengukuran dan terapannya.
SIFAT KOLIGATIF LARUTAN STANDAR KOMPETENSI 1. Mendeskripsikan sifat-sifat Larutan, metode pengukuran dan terapannya. KOMPETENSI DASAR 1.1 Mendeskripsikan sifat-sifat Larutan, metode pengukuran dan terapannya.
STOIKIOMETRI LARUTAN. Andian Ari Anggraeni, M.Sc
 STOIKIOMETRI LARUTAN Andian Ari Anggraeni, M.Sc A.1. MASSA ATOM RELATIF (A r ) DAN MASSA MOLEKUL RELATIF (M r ) Dari percobaan diketahui bahwa perbandingan massa hidrogen dan oksigen dalam air adalah 1
STOIKIOMETRI LARUTAN Andian Ari Anggraeni, M.Sc A.1. MASSA ATOM RELATIF (A r ) DAN MASSA MOLEKUL RELATIF (M r ) Dari percobaan diketahui bahwa perbandingan massa hidrogen dan oksigen dalam air adalah 1
FAKULTAS TEKNIK UNIVERSITAS NEGERI YOGYAKARTA BAHAN AJAR KIMIA DASAR BAB IV STOIKIOMETRI
 No. BAK/TBB/SBG201 Revisi : 00 Tgl. 01 Mei 2008 Hal 1 dari 6 BAB IV STOIKIOMETRI A. HUKUM GAY LUSSAC Bila diukur pada suhu dan tekanan yang sama, volum gas yang bereaksi dan volum gas hasil reaksi berbanding
No. BAK/TBB/SBG201 Revisi : 00 Tgl. 01 Mei 2008 Hal 1 dari 6 BAB IV STOIKIOMETRI A. HUKUM GAY LUSSAC Bila diukur pada suhu dan tekanan yang sama, volum gas yang bereaksi dan volum gas hasil reaksi berbanding
LAMPIRAN 0,5 M 0,75 M 1 M 30 0,6120 % 1,4688 % 5,0490 % 45 2,2185 % 4,7838 % 2,9197 % 60 1,1016 % 0,7344 % 3,3666 %
 LAMPIRAN LAMPIRAN 1. DATA PERCOBAAN L.1.1 Data Percobaan Kadar Gula Reduksi Sebelum Inversi Tabel L.1 Data Percobaan Kadar Gula Reduksi Sebelum Inversi Waktu Hidrolisis (Menit) Konsentrai HCl 0,5 M 0,75
LAMPIRAN LAMPIRAN 1. DATA PERCOBAAN L.1.1 Data Percobaan Kadar Gula Reduksi Sebelum Inversi Tabel L.1 Data Percobaan Kadar Gula Reduksi Sebelum Inversi Waktu Hidrolisis (Menit) Konsentrai HCl 0,5 M 0,75
BAB IV HASIL PENGAMATAN DAN PERHITUNGAN
 BAB IV HASIL PENGAMATAN DAN PERHITUNGAN A. HASIL PENGAMATAN 1. Standarisasi Na 2 S 2 O 3 terhadap K 2 Cr 2 O 7 0.1 N Kelompok Vol. K 2 Cr 2 O 7 Vol. Na 2 S 2 O 3 7 10 ml 11 ml 8 10 ml 12.7 ml 9 10 ml 11.6
BAB IV HASIL PENGAMATAN DAN PERHITUNGAN A. HASIL PENGAMATAN 1. Standarisasi Na 2 S 2 O 3 terhadap K 2 Cr 2 O 7 0.1 N Kelompok Vol. K 2 Cr 2 O 7 Vol. Na 2 S 2 O 3 7 10 ml 11 ml 8 10 ml 12.7 ml 9 10 ml 11.6
LATIHAN ULANGAN TENGAH SEMESTER 2
 Pilihlah jawaban yang paling benar LATIHAN ULANGAN TENGAH SEMESTER 2 TATANAMA 1. Nama senyawa berikut ini sesuai dengan rumus kimianya, kecuali. A. NO = nitrogen oksida B. CO 2 = karbon dioksida C. PCl
Pilihlah jawaban yang paling benar LATIHAN ULANGAN TENGAH SEMESTER 2 TATANAMA 1. Nama senyawa berikut ini sesuai dengan rumus kimianya, kecuali. A. NO = nitrogen oksida B. CO 2 = karbon dioksida C. PCl
