13. Gilbert, G. L., (1976), A Buffer solution and its action, J.Chem.Ed, 53, Wiger, G. R., de la Comp, U., (1978), Conjugate acid base
|
|
|
- Yenny Susanto
- 7 tahun lalu
- Tontonan:
Transkripsi
1 DAFTAR PUSTAKA 1. Whitten, K. W., Davis, R. E., Peck, M. L., Stanley, G. G., (200), General chemistry, Seventh edition, Thomson Brooks/Cole, USA 2. Harris, D. C., (1991), Quantitative chemical analysis, Third edition, W.H. Freeman and Company, New York 3. Buckley, P. T., (2001), Preparation of buffers: An Experiment for quantitative analysis laboratory, J.Chem.Ed, 78, 138. Fessenden & Fessenden, (Terjemahan: Pudjaatmaka, A.H), (1997), Kimia Organic, Edisi ketiga, Jilid 1, Penerbit Erlangga, Jakarta, Day, R. A & Underwood, A. L., (1992), Analisis kimia kuantitatif, Edisi kelima, Penerbit Erlangga, Jakarta 6. Brown, T. L., Lemay, H. E., Bursten, B. E., (1993), Chemistry: The central science, Sixth edition, Prentice Hall, Christian, D. G., (200), Analytical chemistry, Sixth edition, John Wiley and Sons, USA, 220, Perrin, D. D., Dempsey, B., (197), Buffers for ph and metal ion control, First Published, Chapman and Hall, London 9. Basset, J., Denny, R. C., Jeffrey, G. H., Mendham, J., (Terjemahan: Pudjaatmaka, A.H), (199), Buku ajar Vogel: Kimia analisis kuantitatif anorganik, Edisi keempat, Penerbit: Buku Kedokteran, EGC, Jakarta,16 18, 6 50, 27, Vogel, A. I, (Terjemahan: Pudjaatmaka, A.H), (1985), Buku teks analisis anorganik kualitatif makro dan semi mikro, Edisi kelima, PT. Kalman Media Pusaka, Jakarta, 61 68, Petrucci, R. H., (Penerjemah: Suminar A), (1987), Kimia dasar: Prinsip dan terapan modern, Edisi keempat, Penerbit Erlangga, Jakarta 12. Bishop, C. B., Bishop, M. B., Whitten, K. W., (2000), Standard and microscale experiment in general chemistry, Fourth edition, Saunders College Publishing, USA,
2 13. Gilbert, G. L., (1976), A Buffer solution and its action, J.Chem.Ed, 53, Wiger, G. R., de la Comp, U., (1978), Conjugate acid base mixtures in the general chemistry laboratory: a comprehensive buffer experiment, J.Chem.Ed, 55, Gold, M., Slotnick, H., (1982), Buffers, J.Chem.Ed, 59, Sudarmadji, S., Haryono, B., Suhardi, (198), Prosedur analisa untuk bahan makanan dan pertanian, Edisi ketiga, Penerbit: Liberty, Yogyakarta, Russo, S. O., Hanannia, G. I. H., (2001), Buffer capacity: An Undergraduate laboratory experiment, J.Chem.Ed, 6, Tim Kimia Dasar, (2006), Petunjuk Praktikum Kimia Dasar II, Departemen Kimia, FMIPA, ITB, Bandung 30
3 LAMPIRAN LAMPIRAN 31
4 Lampiran A Massa Atom Relatif (Ar), Massa Molekul Relatif (Mr), dan Tetapan Disosiasi Asam Lemah Pada 25 o C Berikut ini tercantum beberapa data massa atom relatif, massa molekul relatif, dan tetapan disosiasi asam lemah (Day, R. A & Underwood, A. L, 1992): A.1 Massa atom relatif (Ar) dari beberapa unsur Tabel A.1 Massa atom relatif (Ar) beberapa unsur No. Nama Unsur Lambang Unsur Ar 1. Hidrogen H 1, Karbon C 12, Oksigen O 15,999. Natrium Na 22,99 5. Fosfor P 30,97 6. Klor Cl 35,53 7. Kalium K 39,098 A.2 Massa molekul relatif (Mr) dari beberapa unsur Tabel A.2 Massa molekul relatif (Mr) beberapa senyawa No. Nama Senyawa Rumus Kimia Mr 1. Asam sitrat dihidrat H 3 C 6 H 5 O 7.2H 2 O 228, Natrium sitrat dihidrat Na 3 C 6 H 5 O 7.2H 2 O 29, Natrium dihidrogen fosfat NaH 2 PO 119,9758. Dinatrium monohidrogen fosfat Na 2 HPO 11, Kalium dihidrogen fosfat KH 2 PO 136, Natrium hidroksida NaOH 39, Asam klorida HCl 36, Asam oksalat dihidrat H 2 C 2 O.2H 2 O 126,063 A.3 Tetapan disosiasi asam lemah pada 25 o C Tabel A.3 Tetapan disosiasi asam lemah pada 25 o C No. Nama Asam Rumus Kimia Ka pka 1. Asam sitrat H 3 C 6 H 5 O 7 8, x 10 3,08 2. Ion dihidrogen sitrat H 2 C 6 H 5 O 7 1,8 x 10 5,7 3. Ion monohidrogen sitrat HC 6 H 5 O 7,0 x ,0. Ion sitrat 3 C 6 H 5 O 7 2,5 x ,60 5. Asam fosfat H 3 PO 7,5 x ,12 6. Ion dihidrogen fosfat H 2 PO 6,2 x ,21 7. Ion monohidrogen fosfat HPO,8 x ,32 8. Ion fosfat 3 PO 2,1 x ,68 32
5 Lampiran B Perhitungan Pembuatan Bahan Larutan Buffer ml asam sitrat dihidrat 1 M = 0,1 x 1 x 228,1518 g = 22,8152 g Asam sitrat: H 3 C 6 H 5 O 7 (Ka 1 >Ka 2 >Ka 3 ), maka yang digunakan adalah persamaan Ka 1. H 3 C 6 H 5 O 7 H 2 C 6 H 5 O 7 Ka 1= [ HCHO ] [ HCHO ] H + + H + Ka 1 = 8, x 10 [H + ] = [H 2 C 6 H 5 O 7 ] [H + ] 2 = Ka 1. [H 3 C 6 H 5 O 7 ] + [H ]= Ka1x[H3C6H5O 7] a. 1 M + 2 [H ]= 8,x10 x1=2,9x10 M maka ph = 1,5 b. 0,1 M + 3 [H ]= 8,x10 x0,1=9,2x10 M maka ph = 2, ml natrium sitrat dihidrat 1 M = 0,1 x 1 x 29,0981 g = 29,098 g Natrium sitrat: Na 3 C 6 H 5 O 7 Na 3 C 6 H 5 O 7 3Na C 6 H 5 O 7 3 C 6 H 5 O 7 + H 2 O HC 6 H 5 O 7 + OH [HC H O ][ OH] [H ] Kh=. [C H O ] [H ] Kw 1x10 Kh= = =2,5x10 6 Ka x [HC H O ][ OH] Kh= [C H O ] [ OH] 2 = Kh x [C 6 H 5 O 7 3 ] [ OH] = [HC 6 H 5 O 7 ] 3 [ OH]= Khx[C6H5O 7 ] a. 1 M 9 5 [ OH]= 2,5x10 x1=5x10 M maka poh =,30 dan ph = 9,70 33
6 b. 0,1 M 9 5 [ OH]= 2,5x10 x0,1=1,6x10 M maka poh =,80 dan ph = 9, ml natrium dihidrogen fosfat 1 M = 0,1 x 1 x 119,9758 g = 11,9976 g 100 ml kalium dihidrogen fosfat 1 M = 0,1 x 1 x 136,0838 g = 13,608 g a. Natrium dihidrogen fosfat: NaH 2 PO NaH 2 PO Na + + H 2 PO H 2 PO H + + HPO Ka 2 = 6,2 x 10 8 H 2 PO + H 2 O H 3 PO + OH Kh [H PO ][ OH] [H ] Kw Kh=. = = =1,3x [H2PO ] [H ] Ka1 7,5x10 Ka 2 >Kh, maka yang digunakan adalah persamaan Ka 2. [HPO ][H ] Ka= [H + ] = [HPO ] [H PO ] + 2 [H + ] 2 = Ka 2. [H 2 PO ] + [H ]= Ka 2x[H2PO ] 1) 1 M 2) 0,1 M + 8 [H ]= 6,2x10 x1=2,5x10 M maka ph = 3, [H ]= 6,2x10 x0,1=7,9x10 M maka ph =,10 b. Kalium dihidrogen fosfat: KH 2 PO KH 2 PO K + + H 2 PO H 2 PO H + + HPO Ka 2 = 6,2 x 10 8 H 2 PO + H 2 O H 3 PO + OH Kh [H PO ][ OH] [H ] Kw Kh=. = = =1,3x [H2PO ] [H ] Ka1 7,5x10 Ka 2 >Kh, maka yang digunakan adalah persamaan Ka 2. [HPO ][H ] Ka= [H + ] = [HPO ] [H PO ] + 2 [H + ] 2 = Ka 2. [H 2 PO ] 3
7 + [H ]= Ka 2x[H2PO ] 1) 1 M 2) 0,1 M + 8 [H ]= 6,2x10 x1=2,5x10 M maka ph = 3, [H ]= 6,2x10 x0,1=7,9x10 M maka ph =, ml dinatrium monohidrogen fosfat 1 M = 0,1x1x11,9579 g = 1,1958 g Dinatrium monohidrogen fosfat: Na 2 HPO Na 2 HPO Na + + HPO HPO HPO H PO Ka 3 =,8 x H 2 O H 2 PO + OH Kh [H PO ][ OH] [H ] Kw 10 Kh=. = = =1,6x [HPO ] [H ] Ka 2 6,2x10 Ka 3 <Kh, maka yang digunakan adaah persamaan Kh. 7 [H PO ][ OH] Kh= [HPO ] 2 [H 2 PO ] = [ OH] [ OH]= Khx[HPO ] a. 1 M 7 [ OH]= 1,6x10 x1=x10 M maka poh = 3,0 dan ph = 10,60 b. 0,1 M 7 [ OH]= 1,6x10 x1=x10 M maka poh = 3,89 dan ph = 10, ml natrium hidroksida 1 M = 0,1 x 1 x 39,9969 g = 3,9997 g ph larutan natrium hidroksida 0,1 M dan 1 M adalah 13 dan ml asam oksalat dihidrat 0,0500 M = 0,1x0,0500x126,063 g = 0,6303 g 35
8 Lampiran C Prosedur Kerja dan Perhitungan Konsentrasi Larutan HCl dan NaOH C.1 Prosedur kerja standarisasi dan titrasi Larutan NaOH yang digunakan distandarisasi dahulu dengan larutan standar primer asam oksalat dihidrat 0,0500 M dan HCl melalui titrasi dengan NaOH yang sudah distandarisasi. Berikut ini langkah langkah yang dilakukan: a. Membuat larutan standar primer asam oksalat dihidrat 0,0500 M Sebanyak 0,6303gram H 2 C 2 O.2H 2 O (Mr = 126,063) dilarutkan dengan akuades dalam labu ukur 100 ml dan diencerkan sampai tanda batas. b. Penentuan konsentrasi NaOH dengan larutan standar primer asam oksalat dihidrat 0,0500 M. Cara kerjanya : Buret bersih dibilas dengan larutan NaOH lalu diisi dengan larutan NaOH. Keadaan awal buret (volume NaOH awal) dicatat. 25 ml larutan asam oksalat dihidrat 0,0500 M dipipet dari labu ukur, lalu dimasukkan ke dalam labu erlenmeyer 100 ml dan ditambah tetes indikator fenolftalein. Selanjutnya dilakukan titrasi dengan larutan NaOH secara hati hati sampai terjadi perubahan warna dari tak berwarna menjadi merah muda. Pemakaian NaOH dapat diketahui dari selisih pembacaan akhir dan awal buret. 18 c. Penentuan konsentrasi HCl 0,1 M melalui titrasi dengan larutan NaOH 0,1 M. Dengan prosedur yang sama seperti NaOH, dilakukan juga untuk penentuan konsentrasi HCl di mana larutan asam oksalat dihidrat diganti dengan HCl dan indikator fenolftalein dengan metil merah (merah muda menjadi kuning). 36
9 C.2 Hasil Penentuan konsentrasi NaOH dan HCl Berikut ini tabel data volume NaOH yang tertera dalam Tabel C.2.1 dan perhitungan konsentrasinya: Tabel C.2.1 Volume NaOH hasil standarisasi No. Volume H 2 C 2 O.2H 2 O 0,0500 M Volume NaOH (ml) ml 22, ml 22,60 Rata rata 22,58 Perhitungan Konsentrasi NaOH: 25x0,0500x2 Z= =0,1107M 22,58 Konsentrasi NaOH yang diperoleh dari hasil standarisasi dengan larutan standar primer asam oksalat 0,0500 M adalah 0,1107 M. Berikut ini tabel data volume NaOH untuk pengukuran konsentrasi HCl yang tertera dalam Tabel C.2.2 dan perhitungan konsentrasinya: Tabel C.2.2 Volume NaOH untuk pengukuran konsentrasi HCl No. Volume HCl 0,1 M (ml) Volume NaOH (ml) , ,80 Rata rata 20,78 Perhitungan Konsentrasi HCl: 25x0,1107 Y= =0,0920M 20,78 Konsentrasi HCl yang diperoleh dari titrasi dengan NaOH yaitu sebesar 0,0920M. 37
10 Lampiran D Petunjuk Penggunaan ph Meter ORION model 20 A Sebelum dan sesudah pengukuran ph, ph meter harus selalu dikalibrasi dahulu. Biasanya dikalibrasi oleh ph,00 dengan 7,00; ph,00 dengan 10,01 atau ph 7,00 dengan ph 10,01; Berikut ini terdapat beberapa langkah kalibrasi ph yaitu: 1. ph meter dihidupkan dan dipanaskan dahulu ±15 menit; 2. Elektrodanya dicelupkan ke dalam akuades kemudian dicelupkan ke dalam larutan buffer standar (harga ph terbaca pada angka digital ph meter); 3. Setelah dikalibrasi baru digunakan untuk pengukuran ph setiap larutan buffer yang diinginkan. 38
11 Lampiran E Perhitungan ph Larutan Buffer 1. Larutan buffer ph 12,50 ml asam sitrat dihidrat 0,1 M + 12,50 ml natrium sitrat dihidrat 0,1M 1,25 [Nasitrat] 25,00 ph=pka 2 +Log =,7+Log =,7 [Assitrat] 1,25 25,00 12,50 ml asam sitrat dihidrat 1 M + 12,50 ml natrium sitrat dihidrat 1 M 12,50 [Nasitrat] 25,00 ph=pka 2+Log =,7+Log =,7 [Assitrat] 12,50 25,00 2. Larutan buffer ph 6 12,50 ml asam sitrat dihidrat 0,1 M + 12,50 ml natrium sitrat dihidrat 1 M 12,50 [Nasitrat] 25,00 ph=pka 2+Log =,7+Log =5,7 [Assitrat] 1,25 25,00 20,00 ml kalium dihidrogen fosfat 1 M + 5,00 ml natrium hidroksida 1 M 5,00 [HPO ] 25,00 ph=pka 2+Log =7,21+Log =6,73 [H 15,00 2PO ] 25,00 12,50 ml natrium dihidrogen fosfat 1 M + 12,50 ml dinatrium monohidrogen fosfat 1 M [HPO ] 0,5 ph=pka +Log =7,21+Log =7,21 [H PO ] 0,
12 3. Larutan buffer ph 8 20,00 ml kalium dihidrogen fosfat 1 M + 15,00 ml natrium hidroksida 1 M 15,00 [HPO ] 35,00 ph=pka 2+Log =7,21+Log =7,69 [H 5,00 2PO ] 35,00 3,80 ml natrium dihidrogen fosfat 1 M + 26,20 ml dinatrium monohidrogen fosfat 1 M 3,80 [HPO ] 30,00 ph=pka 2+Log =7,21+Log =8,05 [H 26,20 2PO ] 30,00. Larutan buffer ph 10 12,50 ml kalium dihidrogen fosfat 1 M + 12,50 ml natrium hidroksida 1 M H 2 PO + OH H 2 O + HPO 12,5 mmol 12,5 mmol 12,5 mmol HPO + H 2 O H 3 O + + PO 3 Ka 3 =,8 x HPO + H 2 O OH + H 2 PO Kh [H PO ][ OH] [H ] Kw 10 Kh=. = = =1,6x [HPO ] [H ] Ka 2 6,2x10 7 Karena Kh > Ka 2, maka yang digunakan adalah persamaan Kh. [H2PO ][ OH] Kh= [H 2 PO ] = [ OH] [HPO ] 7 12,5 [ OH]= Khx[HPO ]= 1,6x10 x =2,83x10 M 25 maka poh = 3,55 dan ph = 10,5 0
13 Lampiran F Data Pengukuran ph Larutan Buffer ph 6, 8, dan 10 Komposisi Volume (ml) Buffer HCl/ NaOH Tabel F.1 Pengukuran ph larutan buffer ph 6 ph Buffer HCl 0,0920 M NaOH 0,1107 M I II Rataratrata I II Rata 5 5 6,08 6,07 6,08 6,55 6,55 6, ,53 5,53 5,53 7,01 7,00 7, ,36 2,35 2,36 11,51 11,51 11, ,02 1,33 1,33 1,33 12,0 12,05 12, ,87 0,87 0,87 12,25 12,25 12, ,77 0,77 0,77 12,90 12,90 12, ,61 0,61 0,61 13,07 13,08 13,08 Komposisi Volume (ml) Buffer HCl/ NaOH ph Tabel F.2 Pengukuran ph larutan buffer ph 8 ph Buffer HCl 0,0920 M NaOH 0,1107 M I II Rataratrata I II Rata 5 5 7,19 7,18 7,19 8,65 8,65 8, ,97 6,96 6,97 10,32 10,32 10, ,09 6,08 6,09 11,86 11,8 11, ,52 2,65 2,6 2,65 12,66 12,65 12, ,31 1,30 1,31 13,00 13,00 13, ,95 0,93 0,9 13,10 13,08 13, ,76 0,7 0,75 13,20 13,19 13,20 Komposisi Volume (ml) Buffer HCl/ NaOH ph Tabel F.3 Pengukuran ph larutan buffer ph 10 ph Buffer HCl 0,0920 M NaOH 0,1107 M I II Rataratrata I II Rata 5 5 8,72 8,73 8,73 10,27 10,28 10, ,99 7,98 7,99 11,31 11,32 11, ,62 1,61 1,62 12,50 12,50 12, ,62 0,79 0,78 0,79 12,70 12,71 12, , ,77 12,79 12,80 12, ,58 0,58 0,58 12,99 13,01 13, ,52 0,51 0,52 13,07 13,08 13,08 ph 1
14 2
Metodologi Penelitian
 Bab III Metodologi Penelitian Pembuatan larutan buffer menggunakan metode pencampuran antara asam lemah dengan basa konjugasinya. Selanjutnya larutan buffer yang sudah dibuat diuji kemampuannya dalam mempertahankan
Bab III Metodologi Penelitian Pembuatan larutan buffer menggunakan metode pencampuran antara asam lemah dengan basa konjugasinya. Selanjutnya larutan buffer yang sudah dibuat diuji kemampuannya dalam mempertahankan
Bab IV Hasil dan Pembahasan
 Bab IV Hasil dan Pembahasan IV.1 Pembuatan Larutan Buffer Semua zat yang digunakan untuk membuat larutan buffer dapat larut dengan sempurna. Larutan yang diperoleh jernih, homogen, dan tidak berbau. Data
Bab IV Hasil dan Pembahasan IV.1 Pembuatan Larutan Buffer Semua zat yang digunakan untuk membuat larutan buffer dapat larut dengan sempurna. Larutan yang diperoleh jernih, homogen, dan tidak berbau. Data
TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN
 TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN I. JUDUL PERCOBAAN : TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN II. TUJUAN PERCOBAAN : 1. Membuat dan
TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN I. JUDUL PERCOBAAN : TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN II. TUJUAN PERCOBAAN : 1. Membuat dan
ASIDI-ALKALIMETRI PENETAPAN KADAR ASAM SALISILAT
 ASIDI-ALKALIMETRI PENETAPAN KADAR ASAM SALISILAT I. DASAR TEORI I.1 Asidi-Alkalimetri Asidi-alkalimetri merupakan salah satu metode analisis titrimetri. Analisis titrimetri mengacu pada analisis kimia
ASIDI-ALKALIMETRI PENETAPAN KADAR ASAM SALISILAT I. DASAR TEORI I.1 Asidi-Alkalimetri Asidi-alkalimetri merupakan salah satu metode analisis titrimetri. Analisis titrimetri mengacu pada analisis kimia
Nova Nurfauziawati Kelompok 11A V. PEMBAHASAN
 V. PEMBAHASAN Praktikum yang dilaksanakan tanggal 3 Oktober 2011 mengenai pembuatan larutan buffer dan pengujian kestabilannya. Larutan buffer adalah campuran asam/basa lemah dan basa/asam konjugasinya
V. PEMBAHASAN Praktikum yang dilaksanakan tanggal 3 Oktober 2011 mengenai pembuatan larutan buffer dan pengujian kestabilannya. Larutan buffer adalah campuran asam/basa lemah dan basa/asam konjugasinya
TITRASI DENGAN INDIKATOR GABUNGAN DAN DUA INDIKATOR
 TITRASI DENGAN INDIKATOR GABUNGAN DAN DUA INDIKATOR I. TUJUAN 1. Memahami prinsip kerja dari percobaan. 2. Menentukan konsentrasi dari NaOH dan Na 2 CO 3. 3. Mengetahui kegunaan dari titrasi dengan indikator
TITRASI DENGAN INDIKATOR GABUNGAN DAN DUA INDIKATOR I. TUJUAN 1. Memahami prinsip kerja dari percobaan. 2. Menentukan konsentrasi dari NaOH dan Na 2 CO 3. 3. Mengetahui kegunaan dari titrasi dengan indikator
PERCOBAAN I PEMBUATAN DAN PENENTUAN KONSENTRASI LARUTAN
 PERCOBAAN I PEMBUATAN DAN PENENTUAN KONSENTRASI LARUTAN I. TUJUAN PERCOBAAN Tujuan percobaan praktikum ini adalah agar praktikan dapat membuat larutan dengan konsentrasi tertentu, mengencerkan larutan,
PERCOBAAN I PEMBUATAN DAN PENENTUAN KONSENTRASI LARUTAN I. TUJUAN PERCOBAAN Tujuan percobaan praktikum ini adalah agar praktikan dapat membuat larutan dengan konsentrasi tertentu, mengencerkan larutan,
LARUTAN PENYANGGA DAN HIDROLISIS
 6 LARUTAN PENYANGGA DAN HIDROLISIS A. LARUTAN PENYANGGA B. HIDROLISIS Pada bab sebelumnya, kita sudah mempelajari tentang reaksi asam-basa dan titrasi. Jika asam direaksikan dengan basa akan menghasilkan
6 LARUTAN PENYANGGA DAN HIDROLISIS A. LARUTAN PENYANGGA B. HIDROLISIS Pada bab sebelumnya, kita sudah mempelajari tentang reaksi asam-basa dan titrasi. Jika asam direaksikan dengan basa akan menghasilkan
Laporan Praktikum KI1212. Dasar Dasar Kimia Analitik PENENTUAN KADAR KALSIUM DALAM KAPUR TULIS DENGAN METODE KOMPLEKSOMETRI
 Laporan Praktikum KI1212 Dasar Dasar Kimia Analitik PENENTUAN KADAR KALSIUM DALAM KAPUR TULIS DENGAN METODE KOMPLEKSOMETRI Disusun oleh: Alexander Leslie (10515007) Sharhan Hasabi (10515018) Devina Thasia
Laporan Praktikum KI1212 Dasar Dasar Kimia Analitik PENENTUAN KADAR KALSIUM DALAM KAPUR TULIS DENGAN METODE KOMPLEKSOMETRI Disusun oleh: Alexander Leslie (10515007) Sharhan Hasabi (10515018) Devina Thasia
I. LARUTAN BUFFER. 1. Membuat Larutan Buffer 2. Mempelajari Daya Sanggah Larutan Buffer TINJAUAN PUSTAKA
 I. LARUTAN BUFFER II. TUJUAN 1. Membuat Larutan Buffer 2. Mempelajari Daya Sanggah Larutan Buffer III. TINJAUAN PUSTAKA Larutan penyangga atau larutan buffer atau larutan dapar merupakan suatu larutan
I. LARUTAN BUFFER II. TUJUAN 1. Membuat Larutan Buffer 2. Mempelajari Daya Sanggah Larutan Buffer III. TINJAUAN PUSTAKA Larutan penyangga atau larutan buffer atau larutan dapar merupakan suatu larutan
BAB I PENDAHULUAN A. Judul Percobaan B. Tujuan Percobaan
 BAB I PENDAHULUAN A. Judul Percobaan Penentuan kadar karbonat dan bikarbonat dalam larutan. B. Tujuan Percobaan Menyelidiki kadar karbonat dan bikarbonat dalam larutan secara asidimetri dengan menggunakan
BAB I PENDAHULUAN A. Judul Percobaan Penentuan kadar karbonat dan bikarbonat dalam larutan. B. Tujuan Percobaan Menyelidiki kadar karbonat dan bikarbonat dalam larutan secara asidimetri dengan menggunakan
BERKAS SOAL BIDANG STUDI: KIMIA PRAKTIKUM MODUL I KOMPETISI SAINS MADRASAH NASIONAL 2012
 BERKAS SOAL BIDANG STUDI: KIMIA PRAKTIKUM MODUL I KOMPETISI SAINS MADRASAH NASIONAL 2012 Hal-0 Instruksi Pastikan bahwa nama dan kode peserta Anda sudah tertulis pada halaman pertama lembar soal dan lembar
BERKAS SOAL BIDANG STUDI: KIMIA PRAKTIKUM MODUL I KOMPETISI SAINS MADRASAH NASIONAL 2012 Hal-0 Instruksi Pastikan bahwa nama dan kode peserta Anda sudah tertulis pada halaman pertama lembar soal dan lembar
Bab III Metodologi. Penelitian ini dirancang untuk menjawab beberapa permasalahan yang sudah penulis kemukakan pada Bab I. Waktu dan Tempat Penelitian
 Bab III Metodologi Penelitian ini dirancang untuk menjawab beberapa permasalahan yang sudah penulis kemukakan pada Bab I. III.1 Waktu dan Tempat Penelitian Penelitian ini dilakukan dalam rentang waktu
Bab III Metodologi Penelitian ini dirancang untuk menjawab beberapa permasalahan yang sudah penulis kemukakan pada Bab I. III.1 Waktu dan Tempat Penelitian Penelitian ini dilakukan dalam rentang waktu
Bab VIII Reaksi Penetralan dan Titrasi Asam-Basa
 Bab VIII Reaksi Penetralan dan Titrasi Asam-Basa Sumber: James Mapple, Chemistry an Enquiry-Based Approach Pengukuran ph selama titrasi akan lebih akurat dengan menggunakan alat ph-meter. TUJUAN PEMBELAJARAN
Bab VIII Reaksi Penetralan dan Titrasi Asam-Basa Sumber: James Mapple, Chemistry an Enquiry-Based Approach Pengukuran ph selama titrasi akan lebih akurat dengan menggunakan alat ph-meter. TUJUAN PEMBELAJARAN
LAPORAN PRAKTIKUM 3 ph METER, BUFFER, dan PENGENCERAN DISUSUN OLEH : MARIA LESTARI DAN YULIA FITRI GHAZALI Kamis 04 Oktober s/d 16.
 LAPORAN PRAKTIKUM 3 ph METER, BUFFER, dan PENGENCERAN DISUSUN OLEH : MARIA LESTARI DAN YULIA FITRI GHAZALI Kamis 04 Oktober 2012 14.00 s/d 16.00 wib TUJUAN : 1. Agar mahasiswa dapat memahami prinsip-prinsip
LAPORAN PRAKTIKUM 3 ph METER, BUFFER, dan PENGENCERAN DISUSUN OLEH : MARIA LESTARI DAN YULIA FITRI GHAZALI Kamis 04 Oktober 2012 14.00 s/d 16.00 wib TUJUAN : 1. Agar mahasiswa dapat memahami prinsip-prinsip
KESEIMBANGAN ASAM BASA
 LAPORAN PRAKTIKUM PRAKTIKUM PH METER, PERSIAPAN LARUTAN PENYANGGA NAMA PRAKTIKAN : Fani Nuryana Manihuruk (NIM 147008013) Mesrida Simarmata (NIM 147008011) HARI/TGL. PRAKTIKUM : Selasa, 10 Maret 2015 TUJUAN
LAPORAN PRAKTIKUM PRAKTIKUM PH METER, PERSIAPAN LARUTAN PENYANGGA NAMA PRAKTIKAN : Fani Nuryana Manihuruk (NIM 147008013) Mesrida Simarmata (NIM 147008011) HARI/TGL. PRAKTIKUM : Selasa, 10 Maret 2015 TUJUAN
PERCOBAAN I PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA
 LAPORAN PRAKTIKUM KIMIA ANALITIK KI-2122 PERCOBAAN I PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA Nama Praktikan : Anggi Febrina NIM : 13010107 Kelompok : 5 (Shift Pagi) Tanggal
LAPORAN PRAKTIKUM KIMIA ANALITIK KI-2122 PERCOBAAN I PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA Nama Praktikan : Anggi Febrina NIM : 13010107 Kelompok : 5 (Shift Pagi) Tanggal
LAPORAN LENGKAP PRAKTIKUM KIMIA ANORGANIK PERCOBAAN 3 PENENTUAN BILANGAN KOORDINAI KOMPLEKS TEMBAGA (II)
 LAPORAN LENGKAP PRAKTIKUM KIMIA ANORGANIK PERCOBAAN 3 PENENTUAN BILANGAN KOORDINAI KOMPLEKS TEMBAGA (II) OLEH : NAMA : IMENG NIM: ACC 109 011 KELOMPOK : 2 ( DUA ) HARI, TANGGAL : RABU, 8 JUNI 2011 ASISTEN
LAPORAN LENGKAP PRAKTIKUM KIMIA ANORGANIK PERCOBAAN 3 PENENTUAN BILANGAN KOORDINAI KOMPLEKS TEMBAGA (II) OLEH : NAMA : IMENG NIM: ACC 109 011 KELOMPOK : 2 ( DUA ) HARI, TANGGAL : RABU, 8 JUNI 2011 ASISTEN
II. HARI DAN TANGGAL PERCOBAAN
 I. JUDUL PERCOBAAN Titrasi Penetralan dan Aplikasinya II. HARI DAN TANGGAL PERCOBAAN Jum at, 4 Desember 2015 III. SELESAI PERCOBAAN Jum at, 4 Desember 2015 IV. TUJUAN PERCOBAAN 1. Membuat dan menentukan
I. JUDUL PERCOBAAN Titrasi Penetralan dan Aplikasinya II. HARI DAN TANGGAL PERCOBAAN Jum at, 4 Desember 2015 III. SELESAI PERCOBAAN Jum at, 4 Desember 2015 IV. TUJUAN PERCOBAAN 1. Membuat dan menentukan
STUDI ELEKTROLISIS LARUTAN KALIUM IODIDA. Oleh : Aceng Haetami ABSTRAK
 STUDI ELEKTROLISIS LARUTAN KALIUM IODIDA Oleh : Aceng Haetami ABSTRAK Telah dilakukan penelitian dengan judul : Studi Elektrolisis Larutan Kalium Iodida. Penelitian ini bertujuan untuk mengetahui : waktu
STUDI ELEKTROLISIS LARUTAN KALIUM IODIDA Oleh : Aceng Haetami ABSTRAK Telah dilakukan penelitian dengan judul : Studi Elektrolisis Larutan Kalium Iodida. Penelitian ini bertujuan untuk mengetahui : waktu
KIMIA DASAR PRINSIP TITRASI TITRASI (VOLUMETRI)
 KIMIA DASAR TITRASI (VOLUMETRI) Drs. Saeful Amin, M.Si., Apt. PRINSIP TITRASI Titrasi (volumetri) merupakan metode analisis kimia yang cepat, akurat dan sering digunakan untuk menentukan kadar suatu unsur
KIMIA DASAR TITRASI (VOLUMETRI) Drs. Saeful Amin, M.Si., Apt. PRINSIP TITRASI Titrasi (volumetri) merupakan metode analisis kimia yang cepat, akurat dan sering digunakan untuk menentukan kadar suatu unsur
LEMBARAN SOAL 4. Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA )
 LEMBARAN SOAL 4 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah
LEMBARAN SOAL 4 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah
LAPORAN PRAKTIKUM KIMIA DASAR I
 LAPORAN PRAKTIKUM KIMIA DASAR I NAMA KELOMPOK : MELVIA PERMATASARI (08121006013) MELANY AMDIRA (08121006027) ANIS ALAFIFAH (08121006029) PUTRI WULANDARI (08121006071) MUTIARA BELLA (08121006073) JURUSAN
LAPORAN PRAKTIKUM KIMIA DASAR I NAMA KELOMPOK : MELVIA PERMATASARI (08121006013) MELANY AMDIRA (08121006027) ANIS ALAFIFAH (08121006029) PUTRI WULANDARI (08121006071) MUTIARA BELLA (08121006073) JURUSAN
PENUNTUN PRAKTIKUM KIMIA DASAR II KI1201
 PENUNTUN PRAKTIKUM KIMIA DASAR II KI1201 Disusun Ulang Oleh: Dr. Deana Wahyuningrum Dr. Ihsanawati Dr. Irma Mulyani Dr. Mia Ledyastuti Dr. Rusnadi LABORATORIUM KIMIA DASAR PROGRAM TAHAP PERSIAPAN BERSAMA
PENUNTUN PRAKTIKUM KIMIA DASAR II KI1201 Disusun Ulang Oleh: Dr. Deana Wahyuningrum Dr. Ihsanawati Dr. Irma Mulyani Dr. Mia Ledyastuti Dr. Rusnadi LABORATORIUM KIMIA DASAR PROGRAM TAHAP PERSIAPAN BERSAMA
KONTROL KEASAMAN LARUTAN PENYANGGA (BUFFER)
 KONTROL KEASAMAN LARUTAN PENYANGGA (BUFFER) TUJUAN: 1. Memahami manfaat mengontrol ph, terutama dalam sistem fisiologi. 2. Mempelajari tehnik mempertahankan nilai ph larutan dalam berbagai aplikasi. 3.
KONTROL KEASAMAN LARUTAN PENYANGGA (BUFFER) TUJUAN: 1. Memahami manfaat mengontrol ph, terutama dalam sistem fisiologi. 2. Mempelajari tehnik mempertahankan nilai ph larutan dalam berbagai aplikasi. 3.
PENENTUAN TETAPAN PENGIONAN INDIKATOR METIL MERAH SECARA SPEKTROFOTOMETRI
 PENENTUAN TETAPAN PENGIONAN INDIKATOR METIL MERAH SECARA SPEKTROFOTOMETRI A. Tujuan Percobaan Percobaan. Menentukan tetapan pengionan indikator metil merah secara spektrofotometri. B. Dasar Teori Dalam
PENENTUAN TETAPAN PENGIONAN INDIKATOR METIL MERAH SECARA SPEKTROFOTOMETRI A. Tujuan Percobaan Percobaan. Menentukan tetapan pengionan indikator metil merah secara spektrofotometri. B. Dasar Teori Dalam
M 0,4 0,1 0,2 B 0,1 0,1 0,1 0,1 S 0,3-0,3 0,1 POH = -
 1. Campuran di bawah ini yang dapat membentuk larutan penyangga adalah.... A. Asam nitrat dengan natrium asetat B. Asam fosfat dengan natrium asetat C. Asam nitrat dengan kalium nitrat D.Asam asetat dengan
1. Campuran di bawah ini yang dapat membentuk larutan penyangga adalah.... A. Asam nitrat dengan natrium asetat B. Asam fosfat dengan natrium asetat C. Asam nitrat dengan kalium nitrat D.Asam asetat dengan
LAPORAN PRAKTIKUM STANDARISASI LARUTAN NaOH
 LAPORAN PRAKTIKUM STANDARISASI LARUTAN NaOH I. Tujuan Praktikan dapat memahami dan menstandarisasi larutan baku sekunder NaOH dengan larutan baku primer H 2 C 2 O 4 2H 2 O II. Dasar Teori Reaksi asam basa
LAPORAN PRAKTIKUM STANDARISASI LARUTAN NaOH I. Tujuan Praktikan dapat memahami dan menstandarisasi larutan baku sekunder NaOH dengan larutan baku primer H 2 C 2 O 4 2H 2 O II. Dasar Teori Reaksi asam basa
BAB IV. HASIL PENGAMATAN dan PERHITUNGAN
 BAB IV HASIL PENGAMATAN dan PERHITUNGAN A. HASIL PENGAMATAN 1. Standarisasi KMnO 4 terhadap H 2 C 2 O 4 0.1 N Kelompok Vol. H 2 C 2 O 4 Vol. KMnO 4 7 10 ml 10.3 ml 8 10 ml 10.8 ml 9 10 ml 10.4 ml 10 10
BAB IV HASIL PENGAMATAN dan PERHITUNGAN A. HASIL PENGAMATAN 1. Standarisasi KMnO 4 terhadap H 2 C 2 O 4 0.1 N Kelompok Vol. H 2 C 2 O 4 Vol. KMnO 4 7 10 ml 10.3 ml 8 10 ml 10.8 ml 9 10 ml 10.4 ml 10 10
Metodologi Penelitian
 16 Bab III Metodologi Penelitian Penelitian dilakukan dengan menggunakan metode titrasi redoks dengan menggunakan beberapa oksidator (K 2 Cr 2 O 7, KMnO 4 dan KBrO 3 ) dengan konsentrasi masing-masing
16 Bab III Metodologi Penelitian Penelitian dilakukan dengan menggunakan metode titrasi redoks dengan menggunakan beberapa oksidator (K 2 Cr 2 O 7, KMnO 4 dan KBrO 3 ) dengan konsentrasi masing-masing
Laporan Praktikum 3. Praktikum 3 : ph meter, Persiapan larutan penyangga, Pengenceran stok glukosa. Oleh : Rebecca Rumesty L dan Jimmy
 Laporan Praktikum 3 Praktikum 3 : ph meter, Persiapan larutan penyangga, Pengenceran stok glukosa Oleh : Rebecca Rumesty L dan Jimmy Hari/Tanggal Praktikum : Kamis / 4 Oktober 2012 Jam : 12.00 15.00 WIB
Laporan Praktikum 3 Praktikum 3 : ph meter, Persiapan larutan penyangga, Pengenceran stok glukosa Oleh : Rebecca Rumesty L dan Jimmy Hari/Tanggal Praktikum : Kamis / 4 Oktober 2012 Jam : 12.00 15.00 WIB
BAB 6. Jika ke dalam air murni ditambahkan asam atau basa meskipun dalam jumlah. Larutan Penyangga. Kata Kunci. Pengantar
 Kimia XI SMA 179 BAB 6 Larutan Penyangga Tujuan Pembelajaran: Setelah mempelajari bab ini, Anda diharapkan mampu: 1. Menjelaskan pengertian larutan penyangga dan komponen penyusunnya. 2. Merumuskan persamaan
Kimia XI SMA 179 BAB 6 Larutan Penyangga Tujuan Pembelajaran: Setelah mempelajari bab ini, Anda diharapkan mampu: 1. Menjelaskan pengertian larutan penyangga dan komponen penyusunnya. 2. Merumuskan persamaan
LAPORAN PRAKTIKUM KIMIA FARMASI ASIDIMETRI DAN ALKALIMETRI. Senin, 9 November 2015 KELOMPOK IV Senin, Pukul WIB
 LAPORAN PRAKTIKUM KIMIA FARMASI ASIDIMETRI DAN ALKALIMETRI Senin, 9 November 2015 KELOMPOK IV Senin, Pukul 10.00 13.00 WIB Nama NPM Muhammad Naufal Mu tashim 260110150016 Puty Prianti Novira 260110150017
LAPORAN PRAKTIKUM KIMIA FARMASI ASIDIMETRI DAN ALKALIMETRI Senin, 9 November 2015 KELOMPOK IV Senin, Pukul 10.00 13.00 WIB Nama NPM Muhammad Naufal Mu tashim 260110150016 Puty Prianti Novira 260110150017
LAPORAN PRAKTIKUM 2 PH METER, PERSIAPAN LARUTAN PENYANGGA
 LAPORAN PRAKTIKUM 2 PH METER, PERSIAPAN LARUTAN PENYANGGA Nama : T.M. Reza Syahputra Dinno Rilando Hari / Tgl: Kamis / 24 Maret 2016 Tujuan Praktikum: 1. Mahasiswa/i dapat memahami pengertian dan fungsi
LAPORAN PRAKTIKUM 2 PH METER, PERSIAPAN LARUTAN PENYANGGA Nama : T.M. Reza Syahputra Dinno Rilando Hari / Tgl: Kamis / 24 Maret 2016 Tujuan Praktikum: 1. Mahasiswa/i dapat memahami pengertian dan fungsi
LAPORAN PRAKTIKUM KIMIA FISIK BASA
 LAPORAN PRAKTIKUM KIMIA FISIK MODUL PRAKTIKUM NAMA PEMBIMBING NAMA MAHASISWA : STANDARISASI LARUTAN ASAM DAN BASA : Drs. AGUSTINUS NGATIN, MT. : SIFA FUZI ALLAWIYAH TANGGAL PRAKTEK : 9 Oktober 2013 TANGGAL
LAPORAN PRAKTIKUM KIMIA FISIK MODUL PRAKTIKUM NAMA PEMBIMBING NAMA MAHASISWA : STANDARISASI LARUTAN ASAM DAN BASA : Drs. AGUSTINUS NGATIN, MT. : SIFA FUZI ALLAWIYAH TANGGAL PRAKTEK : 9 Oktober 2013 TANGGAL
LAPORAN PRAKTIKUM KIMIA ANALITIK 2 PENENTUAN KADAR KLORIDA. Senin, 21 April Disusun Oleh: MA WAH SHOFWAH KELOMPOK 1
 LAPORAN PRAKTIKUM KIMIA ANALITIK 2 PENENTUAN KADAR KLORIDA Senin, 21 April 2014 Disusun Oleh: MA WAH SHOFWAH 1112016200040 KELOMPOK 1 MILLAH HANIFAH (1112016200073) YASA ESA YASINTA (1112016200062) WIDYA
LAPORAN PRAKTIKUM KIMIA ANALITIK 2 PENENTUAN KADAR KLORIDA Senin, 21 April 2014 Disusun Oleh: MA WAH SHOFWAH 1112016200040 KELOMPOK 1 MILLAH HANIFAH (1112016200073) YASA ESA YASINTA (1112016200062) WIDYA
DEAMINASI TEMPE (TMP)
 MODUL PRAKTIKUM LABORATORIUM INSTRUKSIONAL TEKNIK KIMIA DEAMINASI TEMPE (TMP) Disusun oleh: Hertiara Ratu Anindya Dr. Ukan Sukandar Dr. Ardiyan Harimawan PROGRAM STUDI TEKNIK KIMIA FAKULTAS TEKNOLOGI INDUSTRI
MODUL PRAKTIKUM LABORATORIUM INSTRUKSIONAL TEKNIK KIMIA DEAMINASI TEMPE (TMP) Disusun oleh: Hertiara Ratu Anindya Dr. Ukan Sukandar Dr. Ardiyan Harimawan PROGRAM STUDI TEKNIK KIMIA FAKULTAS TEKNOLOGI INDUSTRI
TITRASI IODOMETRI Oleh: Regina Tutik Padmaningrum Jurusan Pendidikan Kimia, FMIPA, Universitas Negeri Yogyakarta
 TITRASI IODOMETRI Oleh: Regina Tutik Padmaningrum Jurusan Pendidikan Kimia, FMIPA, Universitas Negeri Yogyakarta regina_tutikp@uny.ac.id Pendahuluan Titrasi merupakan suatu proses analisis dimana suatu
TITRASI IODOMETRI Oleh: Regina Tutik Padmaningrum Jurusan Pendidikan Kimia, FMIPA, Universitas Negeri Yogyakarta regina_tutikp@uny.ac.id Pendahuluan Titrasi merupakan suatu proses analisis dimana suatu
8. ASIDI-ALKALINITAS
 Asidialkalinitas 8. ASIDIALKALINITAS 8.1. Umum Pengertian asiditas adalah kemampuan air untuk menetralkan larutan basa, sedangkan alkalinitas adalah kemampuan air untuk menetralkan larutan asam. Asidialkalinitas
Asidialkalinitas 8. ASIDIALKALINITAS 8.1. Umum Pengertian asiditas adalah kemampuan air untuk menetralkan larutan basa, sedangkan alkalinitas adalah kemampuan air untuk menetralkan larutan asam. Asidialkalinitas
Regina Tutik Padmaningrum, UNY
 TITRASI ASAM LEMAH DENGAN BASA KUAT Oleh: Regina Tutik Padmaningrum, M.Si Jurusan Pendidikan Kimia, FMIPA, Universitas Negeri Yogyakarta regina_tutikp@uny.ac.id Pada titrasi asam lemah dengan basa kuat,
TITRASI ASAM LEMAH DENGAN BASA KUAT Oleh: Regina Tutik Padmaningrum, M.Si Jurusan Pendidikan Kimia, FMIPA, Universitas Negeri Yogyakarta regina_tutikp@uny.ac.id Pada titrasi asam lemah dengan basa kuat,
Laporan Praktikum Kimia Dasar II. Standarisasi Larutan NaOH 0,1 M dan Penggunaannya Dalam Penentuan Kadar Asam Cuka Perdagangan.
 Laporan Praktikum Kimia Dasar II Standarisasi Larutan NaOH 0,1 M dan Penggunaannya Dalam Penentuan Kadar Asam Cuka Perdagangan Oleh: Kelompok : I (satu) Nama Nim Prodi : Ardinal : F1D113002 : Teknik Pertambangan
Laporan Praktikum Kimia Dasar II Standarisasi Larutan NaOH 0,1 M dan Penggunaannya Dalam Penentuan Kadar Asam Cuka Perdagangan Oleh: Kelompok : I (satu) Nama Nim Prodi : Ardinal : F1D113002 : Teknik Pertambangan
KAJIAN MATERI LARUTAN BUFFER ASAM BASA TESIS. SUSI HERAWATI NIM : Program Studi Kimia
 KAJIAN MATERI LARUTAN BUFFER ASAM BASA TESIS Oleh SUSI HERAWATI NIM : 20506033 Program Studi Kimia INSTITUT TEKNOLOGI BANDUNG 2008 KAJIAN MATERI LARUTAN BUFFER ASAM BASA TESIS Karya tulis ini sebagai salah
KAJIAN MATERI LARUTAN BUFFER ASAM BASA TESIS Oleh SUSI HERAWATI NIM : 20506033 Program Studi Kimia INSTITUT TEKNOLOGI BANDUNG 2008 KAJIAN MATERI LARUTAN BUFFER ASAM BASA TESIS Karya tulis ini sebagai salah
LAPORAN PRAKTIKUM KIMIA ANALITIK 2. Titrasi Permanganometri. Selasa, 6 Mei Disusun Oleh: Yeni Setiartini. Kelompok 3: Fahmi Herdiansyah
 LAPORAN PRAKTIKUM KIMIA ANALITIK 2 Titrasi Permanganometri Selasa, 6 Mei 2014 Disusun Oleh: Yeni Setiartini 1112016200050 Kelompok 3: Fahmi Herdiansyah Huda Rahmawati Aida Nadia Rizky Harry Setiawan. PROGRAM
LAPORAN PRAKTIKUM KIMIA ANALITIK 2 Titrasi Permanganometri Selasa, 6 Mei 2014 Disusun Oleh: Yeni Setiartini 1112016200050 Kelompok 3: Fahmi Herdiansyah Huda Rahmawati Aida Nadia Rizky Harry Setiawan. PROGRAM
PRAKTIKUM 3 : PH METER, PERSIAPAN LARUTAN PENYANGGA, PENGENCERAN STOK GLUKOSA. Oleh : Henny Erina Saurmauli Ompusunggu. Jekson Martiar Siahaan
 PRAKTIKUM 3 : PH METER, PERSIAPAN LARUTAN PENYANGGA, PENGENCERAN STOK GLUKOSA Oleh : Henny Erina Saurmauli Ompusunggu Jekson Martiar Siahaan I. Tujuan Praktikum 1. Memahami prinsip-prinsip dasar larutan
PRAKTIKUM 3 : PH METER, PERSIAPAN LARUTAN PENYANGGA, PENGENCERAN STOK GLUKOSA Oleh : Henny Erina Saurmauli Ompusunggu Jekson Martiar Siahaan I. Tujuan Praktikum 1. Memahami prinsip-prinsip dasar larutan
Haris Dianto Darwindra BAB V PEMBAHASAN
 BAB V PEMBAHASAN Titrasi merupakan suatu metoda untuk menentukan kadar suatu zat dengan menggunakan zat lain yang sudah diketahui konsentrasinya. Titrasi biasanya dibedakan berdasarkan jenis reaksi yang
BAB V PEMBAHASAN Titrasi merupakan suatu metoda untuk menentukan kadar suatu zat dengan menggunakan zat lain yang sudah diketahui konsentrasinya. Titrasi biasanya dibedakan berdasarkan jenis reaksi yang
PENENTUAN KADAR ASAM ASETAT DALAM ASAM CUKA DENGAN ALKALIMETRI
 PENENTUAN KADAR ASAM ASETAT DALAM ASAM CUKA DENGAN ALKALIMETRI I. CAPAIAN PEMBELAJARAN Praktikan mampu menetapkan kadar CH3COOH (asam asetat) dan asam cuka (HCl) menggunakan prinsip reaksi asam-basa. II.
PENENTUAN KADAR ASAM ASETAT DALAM ASAM CUKA DENGAN ALKALIMETRI I. CAPAIAN PEMBELAJARAN Praktikan mampu menetapkan kadar CH3COOH (asam asetat) dan asam cuka (HCl) menggunakan prinsip reaksi asam-basa. II.
PENENTUAN KOMPOSISI MAGNESIUM HIDROKSIDA DAN ALUMINIUM HIDROKSIDA DALAM OBAT MAAG
 PENENTUAN KOMPOSISI MAGNESIUM HIDROKSIDA DAN ALUMINIUM HIDROKSIDA DALAM OBAT MAAG PENDAHULUAN Obat maag atau antasida adalah obat yang mengandung bahan-bahan yang efektif yang menetralkan asam dilambung.
PENENTUAN KOMPOSISI MAGNESIUM HIDROKSIDA DAN ALUMINIUM HIDROKSIDA DALAM OBAT MAAG PENDAHULUAN Obat maag atau antasida adalah obat yang mengandung bahan-bahan yang efektif yang menetralkan asam dilambung.
Titrasi Volumetri. Modul 1 PENDAHULUAN
 Modul 1 Titrasi Volumetri Dr. Anna Permanasari, M.Si. K PENDAHULUAN egiatan praktikum ini dimaksudkan untuk melatih keterampilan dasar Anda dalam melakukan pekerjaan laboratorium, melatih Anda dalam bekerja
Modul 1 Titrasi Volumetri Dr. Anna Permanasari, M.Si. K PENDAHULUAN egiatan praktikum ini dimaksudkan untuk melatih keterampilan dasar Anda dalam melakukan pekerjaan laboratorium, melatih Anda dalam bekerja
LARUTAN PENYANGGA Bahan Ajar Kelas XI IPA Semester Gasal 2012/2013
 LARUTAN PENYANGGA [Yea r] LARUTAN PENYANGGA Bahan Ajar Kelas XI IPA Semester Gasal 2012/2013 MARI BELAJAR Indikator Produk Menjelaskan komponen pembentuk larutan penyangga dengan berpikir kritis. Menjelaskan
LARUTAN PENYANGGA [Yea r] LARUTAN PENYANGGA Bahan Ajar Kelas XI IPA Semester Gasal 2012/2013 MARI BELAJAR Indikator Produk Menjelaskan komponen pembentuk larutan penyangga dengan berpikir kritis. Menjelaskan
LOGO TEORI ASAM BASA
 LOGO TEORI ASAM BASA TIM DOSEN KIMIA DASAR FTP 2012 Beberapa ilmuan telah memberikan definisi tentang konsep asam basa Meskipun beberapa definisi terlihat kurang jelas dan berbeda satu sama lain, tetapi
LOGO TEORI ASAM BASA TIM DOSEN KIMIA DASAR FTP 2012 Beberapa ilmuan telah memberikan definisi tentang konsep asam basa Meskipun beberapa definisi terlihat kurang jelas dan berbeda satu sama lain, tetapi
LAPORAN PRAKTIKUM. ph METER DAN PERSIAPAN LARUTAN PENYANGGA
 LAPORAN PRAKTIKUM ph METER DAN PERSIAPAN LARUTAN PENYANGGA Hari/Tanggal Praktikum : Kamis/ 17 Oktober 2013 Nama Mahasiswa : 1. Nita Andriani Lubis 2. Ade Sinaga Tujuan Praktikum : Teori 1. Mengetahui pembuatan
LAPORAN PRAKTIKUM ph METER DAN PERSIAPAN LARUTAN PENYANGGA Hari/Tanggal Praktikum : Kamis/ 17 Oktober 2013 Nama Mahasiswa : 1. Nita Andriani Lubis 2. Ade Sinaga Tujuan Praktikum : Teori 1. Mengetahui pembuatan
I. KEASAMAN ION LOGAM TERHIDRAT
 I. KEASAMAN ION LOGAM TERHIDRAT Tujuan Berdasarkan metode ph-metri akan ditunjukkan bahwa ion metalik terhidrat memiliki perilaku seperti suatu mono asam dengan konstanta keasaman yang tergantung pada
I. KEASAMAN ION LOGAM TERHIDRAT Tujuan Berdasarkan metode ph-metri akan ditunjukkan bahwa ion metalik terhidrat memiliki perilaku seperti suatu mono asam dengan konstanta keasaman yang tergantung pada
1. Dari pengujian larutan dengan kertas lakmus diperoleh data berikut:
 SOAL-SOAL BAB 5 LARUTAN ASAM BASA/ Kimia Erlangga 2B 1. Dari pengujian larutan dengan kertas lakmus diperoleh data berikut: No Larutan yang diuji Warna lakmus Merah Biru 1 X Merah Biru 2 Y Merah Merah
SOAL-SOAL BAB 5 LARUTAN ASAM BASA/ Kimia Erlangga 2B 1. Dari pengujian larutan dengan kertas lakmus diperoleh data berikut: No Larutan yang diuji Warna lakmus Merah Biru 1 X Merah Biru 2 Y Merah Merah
HASIL KALI KELARUTAN (Ksp)
 LAPORAN PRAKTIKUM KIMIA FISIKA HASIL KALI KELARUTAN (Ksp) NAMA : YUSI ANDA RIZKY NIM : H311 08 003 KELOMPOK : II (DUA) HARI/TGL PERC. : SENIN/08 MARET 2010 ASISTEN : FITRI JUNIANTI LABORATORIUM KIMIA FISIKA
LAPORAN PRAKTIKUM KIMIA FISIKA HASIL KALI KELARUTAN (Ksp) NAMA : YUSI ANDA RIZKY NIM : H311 08 003 KELOMPOK : II (DUA) HARI/TGL PERC. : SENIN/08 MARET 2010 ASISTEN : FITRI JUNIANTI LABORATORIUM KIMIA FISIKA
LAPORAN PRAKTIKUM KIMIA FISIKA II PENENTUAN LAJU REAKSI DAN TETAPAN LAJU
 LAPORAN PRAKTIKUM KIMIA FISIKA II PENENTUAN LAJU REAKSI DAN TETAPAN LAJU Nama NIM Prodi Anggota kelompok Disusun oleh: : Edi Siswanto : H13112071 : Kimia : 1. Alpius Suriadi 2. Gloria Sindora 3. Indri
LAPORAN PRAKTIKUM KIMIA FISIKA II PENENTUAN LAJU REAKSI DAN TETAPAN LAJU Nama NIM Prodi Anggota kelompok Disusun oleh: : Edi Siswanto : H13112071 : Kimia : 1. Alpius Suriadi 2. Gloria Sindora 3. Indri
Penambahan oleh sedikit asam-kuat (H + ) menyebabkan kesetimbangan. CH 3 COOH(aq) CH 3 COO - (aq) + H + (aq) (9.1) asam lemah
 Larutan bufer* merupakan sistem larutan yang dapat mempertahankan lingkungannya dari pengaruh seperti oleh penambahan sedikit asam/basa kuat, atau oleh pengenceran. Sistem bufer terdiri atas dua komponen,
Larutan bufer* merupakan sistem larutan yang dapat mempertahankan lingkungannya dari pengaruh seperti oleh penambahan sedikit asam/basa kuat, atau oleh pengenceran. Sistem bufer terdiri atas dua komponen,
PENENTUAN KADAR CuSO 4. Dengan Titrasi Iodometri
 PENENTUAN KADAR CuSO 4 Dengan Titrasi Iodometri 22 April 2014 NURUL MU NISAH AWALIYAH 1112016200008 Kelompok 2 : 1. Widya Kusumaningrum (111201620000) 2. Ipa Ida Rosita (1112016200007) 3. Ummu Kalsum A.L
PENENTUAN KADAR CuSO 4 Dengan Titrasi Iodometri 22 April 2014 NURUL MU NISAH AWALIYAH 1112016200008 Kelompok 2 : 1. Widya Kusumaningrum (111201620000) 2. Ipa Ida Rosita (1112016200007) 3. Ummu Kalsum A.L
Titrasi asam kuat-basa kuat
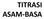 TITRASI ASAM-BASA KURVA TITRASI plot atau kurva antara ph atau poh terhadap volume titran untuk menguji apakah suatu reaksi dapat digunakan untuk analisa titrimetri ataukah tidak memilih indikator Titrasi
TITRASI ASAM-BASA KURVA TITRASI plot atau kurva antara ph atau poh terhadap volume titran untuk menguji apakah suatu reaksi dapat digunakan untuk analisa titrimetri ataukah tidak memilih indikator Titrasi
 VISIT MY WEBSITE : KLIK AJA LINKNYA SOB http://dionlegionis.blogspot.com/search/label/education%20mipa http://dionlegionis.blogspot.com/2015/03/klasifikasi-kodok-beranak-darisulawesi.html http://dionlegionis.blogspot.com/2015/03/download-pdf-statistika-datatunggal.html
VISIT MY WEBSITE : KLIK AJA LINKNYA SOB http://dionlegionis.blogspot.com/search/label/education%20mipa http://dionlegionis.blogspot.com/2015/03/klasifikasi-kodok-beranak-darisulawesi.html http://dionlegionis.blogspot.com/2015/03/download-pdf-statistika-datatunggal.html
PERCOBAAN IV PEMBUATAN BUFFER Tujuan Menghitung dan pembuat larutan buffer atau dapar untuk aplikasi dalam bidang farmasi.
 A B PERCOBAAN IV PEMBUATAN BUFFER Tujuan Menghitung dan pembuat larutan buffer atau dapar untuk aplikasi dalam bidang farmasi. Dasar Teori Larutan penyangga atau larutan buffer atau larutan dapar merupakan
A B PERCOBAAN IV PEMBUATAN BUFFER Tujuan Menghitung dan pembuat larutan buffer atau dapar untuk aplikasi dalam bidang farmasi. Dasar Teori Larutan penyangga atau larutan buffer atau larutan dapar merupakan
BAB I PRAKTIKUM ASIDI AL-KALIMETRI
 BAB I PRAKTIKUM ASIDI AL-KALIMETRI I. TUJUAN a. Mahasiswa dapat menjelaskan proses titrasi asidi alkalimetri. b. Mahasiswa mampu menghitung konsentrasi sampel dengan metode asidi alkalimetri. II. DASAR
BAB I PRAKTIKUM ASIDI AL-KALIMETRI I. TUJUAN a. Mahasiswa dapat menjelaskan proses titrasi asidi alkalimetri. b. Mahasiswa mampu menghitung konsentrasi sampel dengan metode asidi alkalimetri. II. DASAR
LAPORAN PRAKTIKUM KIMIA FISIKA II PENENTUAN KADAR KOEFISIEN DISTRIBUSI SELASA, 22 MEI 2014
 LAPORAN PRAKTIKUM KIMIA FISIKA II PENENTUAN KADAR KOEFISIEN DISTRIBUSI SELASA, 22 MEI 2014 Disusun oleh : Fika Rakhmalinda (1112016200003) Fikri Sholihah (1112016200028 ) Naryanto (1112016200018 ) PROGRAM
LAPORAN PRAKTIKUM KIMIA FISIKA II PENENTUAN KADAR KOEFISIEN DISTRIBUSI SELASA, 22 MEI 2014 Disusun oleh : Fika Rakhmalinda (1112016200003) Fikri Sholihah (1112016200028 ) Naryanto (1112016200018 ) PROGRAM
LARUTAN. Zat terlarut merupakan komponen yang jumlahnya sedikit, sedangkan pelarut adalah komponen yang terdapat dalam jumlah banyak.
 LARUTAN Larutan merupakan campuran yang homogen,yaitu campuran yang memiliki komposisi merata atau serba sama di seluruh bagian volumenya. Suatu larutan mengandung dua komponen atau lebih yang disebut
LARUTAN Larutan merupakan campuran yang homogen,yaitu campuran yang memiliki komposisi merata atau serba sama di seluruh bagian volumenya. Suatu larutan mengandung dua komponen atau lebih yang disebut
LAPORAN PRAKTIKUM 2 PH METER, PERSIAPAN LARUTAN PENYANGGA, DAN PENGENCERAN
 LAPORAN PRAKTIKUM 2 PH METER, PERSIAPAN LARUTAN PENYANGGA, DAN PENGENCERAN Nama : Atri Gustiana Gultom Dewi Maya Sarah Hari/ Tgl Praktikum : Selasa/ 10 Maret 2015 TUJUAN PRAKTIKUM : 1. Mahasiswa/i dapat
LAPORAN PRAKTIKUM 2 PH METER, PERSIAPAN LARUTAN PENYANGGA, DAN PENGENCERAN Nama : Atri Gustiana Gultom Dewi Maya Sarah Hari/ Tgl Praktikum : Selasa/ 10 Maret 2015 TUJUAN PRAKTIKUM : 1. Mahasiswa/i dapat
Laporan Praktikum ph Meter, Persiapan Larutan Penyangga
 Laporan Praktikum ph Meter, Persiapan Larutan Penyangga Hari / Tanggal Praktikum : Kamis / 4 Oktober 2012 Nama Praktikan : Rica Vera Br. Tarigan dan Nunung Sri Mulyani Tujuan Praktikum: Agar Mahasiswa/i
Laporan Praktikum ph Meter, Persiapan Larutan Penyangga Hari / Tanggal Praktikum : Kamis / 4 Oktober 2012 Nama Praktikan : Rica Vera Br. Tarigan dan Nunung Sri Mulyani Tujuan Praktikum: Agar Mahasiswa/i
Larutan penyangga dapat terbentuk dari campuran asam lemah dan basa
 Larutan penyangga dapat terbentuk dari campuran asam lemah dan basa konjugasinya atau campuran basa lemah dan asam konjugasinya. Larutan penyangga disebut juga larutan penahan atau larutan dapar atau buffer.
Larutan penyangga dapat terbentuk dari campuran asam lemah dan basa konjugasinya atau campuran basa lemah dan asam konjugasinya. Larutan penyangga disebut juga larutan penahan atau larutan dapar atau buffer.
KIMIA ANALITIK TITRASI ASAM-BASA
 KIMIA ANALITIK TITRASI ASAM-BASA KIMIA ANALITIK 02 REGULER KELOMPOK 6 Disusun oleh: 1. Jang Jin Joo 1306399071 (11) 2. Robby Samuel 1306402204 (12) TEKNIK METALURGI DAN MATERIAL 2014 Pengertian Titrasi
KIMIA ANALITIK TITRASI ASAM-BASA KIMIA ANALITIK 02 REGULER KELOMPOK 6 Disusun oleh: 1. Jang Jin Joo 1306399071 (11) 2. Robby Samuel 1306402204 (12) TEKNIK METALURGI DAN MATERIAL 2014 Pengertian Titrasi
TITRASI IODOMETRI. Siti Masitoh. M. Ikhwan Fillah, Indah Desi Permana, Ira Nurpialawati PROGRAM STUDI PENDIDIKAN KIMIA
 TITRASI IODOMETRI Siti Masitoh 1112016200006 M. Ikhwan Fillah, Indah Desi Permana, Ira Nurpialawati PROGRAM STUDI PENDIDIKAN KIMIA JURUSAN ILMU PENDIDIKAN ILMU PENGETAHUAN ALAM FAKULTAS ILMU TARBIYAH DAN
TITRASI IODOMETRI Siti Masitoh 1112016200006 M. Ikhwan Fillah, Indah Desi Permana, Ira Nurpialawati PROGRAM STUDI PENDIDIKAN KIMIA JURUSAN ILMU PENDIDIKAN ILMU PENGETAHUAN ALAM FAKULTAS ILMU TARBIYAH DAN
LAPORAN PRAKTIKUM 2:
 LAPORAN PRAKTIKUM 2: PH METER, PERSIAPAN LARUTAN PENYANGGA, PENGENCERAN STOK GLUKOSA Oleh : AMIRUL HADI (137008015) SERI RAYANI BANGUN (137008003) Waktu praktikum : Kamis, 17 OKtober 2013 I. TUJUAN PRAKTIKUM
LAPORAN PRAKTIKUM 2: PH METER, PERSIAPAN LARUTAN PENYANGGA, PENGENCERAN STOK GLUKOSA Oleh : AMIRUL HADI (137008015) SERI RAYANI BANGUN (137008003) Waktu praktikum : Kamis, 17 OKtober 2013 I. TUJUAN PRAKTIKUM
Lampiran 1. Prosedur analisis karakteristik kompos
 LAMPIRA 30 Lampiran 1. Prosedur analisis karakteristik kompos A. Kadar Air Bahan (AOAC 1984) Cawan alumunium kosong dimasukkan ke dalam oven selama 15 menit pada temperatur 100 o C. Cawan porselen kemudian
LAMPIRA 30 Lampiran 1. Prosedur analisis karakteristik kompos A. Kadar Air Bahan (AOAC 1984) Cawan alumunium kosong dimasukkan ke dalam oven selama 15 menit pada temperatur 100 o C. Cawan porselen kemudian
LAPORAN PRAKTIKUM KIMIA DASAR. Percobaan 3 INDIKATOR DAN LARUTAN
 LAPORAN PRAKTIKUM KIMIA DASAR Percobaan 3 INDIKATOR DAN LARUTAN Disusun oleh Nama : Cinderi Maura Restu NPM : 10060312009 Shift / kelompok : 1 / 2 Tanggal Praktikum : 29 Oktober 2012 Tanggal Laporan :
LAPORAN PRAKTIKUM KIMIA DASAR Percobaan 3 INDIKATOR DAN LARUTAN Disusun oleh Nama : Cinderi Maura Restu NPM : 10060312009 Shift / kelompok : 1 / 2 Tanggal Praktikum : 29 Oktober 2012 Tanggal Laporan :
LAPORAN PRAKTIKUM KIMIA DASAR II PERCOBAAN II REAKSI ASAM BASA : OSU OHEOPUTRA. H STAMBUK : A1C : PENDIDIKAN MIPA
 LAPORAN PRAKTIKUM KIMIA DASAR II PERCOBAAN II REAKSI ASAM BASA NAMA : OSU OHEOPUTRA. H STAMBUK : A1C4 07 017 KELOMPOK PROGRAM STUDI JURUSAN : II : PENDIDIKAN KIMIA : PENDIDIKAN MIPA ASISTEN PEMBIMBING
LAPORAN PRAKTIKUM KIMIA DASAR II PERCOBAAN II REAKSI ASAM BASA NAMA : OSU OHEOPUTRA. H STAMBUK : A1C4 07 017 KELOMPOK PROGRAM STUDI JURUSAN : II : PENDIDIKAN KIMIA : PENDIDIKAN MIPA ASISTEN PEMBIMBING
Praktikum Kimia Fisika II Hidrolisis Etil Asetat dalam Suasana Asam Lemah & Asam Kuat
 I. Judul Percobaan Hidrolisis Etil Asetat dalam Suasana Asam Lemah & dalam Suasana Asam Kuat II. Tanggal Percobaan Senin, 8 April 2013 pukul 11.00 14.00 WIB III. Tujuan Percobaan Menentukan orde reaksi
I. Judul Percobaan Hidrolisis Etil Asetat dalam Suasana Asam Lemah & dalam Suasana Asam Kuat II. Tanggal Percobaan Senin, 8 April 2013 pukul 11.00 14.00 WIB III. Tujuan Percobaan Menentukan orde reaksi
PETA KONSEP. Larutan Penyangga. Larutan Penyangga Basa. Larutan Penyangga Asam. Asam konjugasi. Basa lemah. Asam lemah. Basa konjugasi.
 PETA KONSEP Larutan Penyangga mempertahankan berupa ph Larutan Penyangga Asam mengandung Larutan Penyangga Basa mengandung Asam lemah Basa konjugasi Asam konjugasi Basa lemah contoh contoh contoh contoh
PETA KONSEP Larutan Penyangga mempertahankan berupa ph Larutan Penyangga Asam mengandung Larutan Penyangga Basa mengandung Asam lemah Basa konjugasi Asam konjugasi Basa lemah contoh contoh contoh contoh
SMA NEGERI 6 SURABAYA LARUTAN ASAM & BASA. K a = 2.M a. 2. H 2 SO 4 (asam kuat) α = 1 H 2 SO 4 2H + 2
 SMA NEGERI 6 SURABAYA LARUTAN ASAM & BASA K I M I A 1). TEORI ARCHENIUS Asam adalah zat yang jika di dalam air melepaskan ion H +, dengan kata lain pembawa sifat asam adalah ion H +. jumlah ion H+ yang
SMA NEGERI 6 SURABAYA LARUTAN ASAM & BASA K I M I A 1). TEORI ARCHENIUS Asam adalah zat yang jika di dalam air melepaskan ion H +, dengan kata lain pembawa sifat asam adalah ion H +. jumlah ion H+ yang
kimia ASAM-BASA III Tujuan Pembelajaran
 KTSP K-13 kimia K e l a s XI ASAM-BASA III Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami mekanisme reaksi asam-basa. 2. Memahami stoikiometri
KTSP K-13 kimia K e l a s XI ASAM-BASA III Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami mekanisme reaksi asam-basa. 2. Memahami stoikiometri
Desikator Neraca analitik 4 desimal
 Lampiran 1. Prosedur Uji Kadar Air A. Prosedur Uji Kadar Air Bahan Anorganik (Horwitz, 2000) Haluskan sejumlah bahan sebanyak yang diperlukan agar cukup untuk analisis, atau giling sebanyak lebih dari
Lampiran 1. Prosedur Uji Kadar Air A. Prosedur Uji Kadar Air Bahan Anorganik (Horwitz, 2000) Haluskan sejumlah bahan sebanyak yang diperlukan agar cukup untuk analisis, atau giling sebanyak lebih dari
LAPORAN PRAKTIKUM ph METER DAN PERSIAPAN LARUTAN PENYANGGA
 LAPORAN PRAKTIKUM ph METER DAN PERSIAPAN LARUTAN PENYANGGA Nama : 1. Irmayanti (157008011) 2. Binayanti Nainggolan (157008008) 3. Henny Gusvina Batubara (157008010) Tanggal Praktikum : 31 Maret 2016 Tujuan
LAPORAN PRAKTIKUM ph METER DAN PERSIAPAN LARUTAN PENYANGGA Nama : 1. Irmayanti (157008011) 2. Binayanti Nainggolan (157008008) 3. Henny Gusvina Batubara (157008010) Tanggal Praktikum : 31 Maret 2016 Tujuan
DERAJAT KEASAMAN (ph)
 LAPORAN PRAKTIKUM KIMIA DASAR DERAJAT KEASAMAN (ph) DISUSUN OLEH FAISAL ARSYAD (13513128) NURUL FIKRI (13513136) JURUSAN TEKNIK LINGKUNGAN FAKULTAS TEKNIK SIPIL DAN PERENCANAAN UNIVERSITAS ISLAM INDONESIA
LAPORAN PRAKTIKUM KIMIA DASAR DERAJAT KEASAMAN (ph) DISUSUN OLEH FAISAL ARSYAD (13513128) NURUL FIKRI (13513136) JURUSAN TEKNIK LINGKUNGAN FAKULTAS TEKNIK SIPIL DAN PERENCANAAN UNIVERSITAS ISLAM INDONESIA
UJIAN PRAKTIKUM KI2121 DASAR-DASAR KIMIA ANALITIK PENENTUAN KADAR BIKARBONAT DALAM SODA KUE
 UJIAN PRAKTIKUM KI2121 DASAR-DASAR KIMIA ANALITIK PENENTUAN KADAR BIKARBONAT DALAM SODA KUE Kelompok : Kelompok 5 Tanggal Persentasi : 14 November 2016 Tanggal Percobaan : 21 November 2016 Sahlillah Dwi
UJIAN PRAKTIKUM KI2121 DASAR-DASAR KIMIA ANALITIK PENENTUAN KADAR BIKARBONAT DALAM SODA KUE Kelompok : Kelompok 5 Tanggal Persentasi : 14 November 2016 Tanggal Percobaan : 21 November 2016 Sahlillah Dwi
PRAKTIKUM PH METER, PERSIAPAN LARUTAN PENYANGGA
 LAPORAN PRAKTIKUM : 2 PRAKTIKUM PH METER, PERSIAPAN LARUTAN PENYANGGA Nama : Sunarti NIM :147008015 Hari/ tgl: Selasa, 3 Maret 2015 Tujuan Praktikum: 1. Mengerti prnsip dasar tentang larutan buffer (penyangga)
LAPORAN PRAKTIKUM : 2 PRAKTIKUM PH METER, PERSIAPAN LARUTAN PENYANGGA Nama : Sunarti NIM :147008015 Hari/ tgl: Selasa, 3 Maret 2015 Tujuan Praktikum: 1. Mengerti prnsip dasar tentang larutan buffer (penyangga)
LAPORAN PRAKTIKUM 03 ph METER DAN PERSIAPAN LARUTAN PENYANGGA
 LAPORAN PRAKTIKUM 03 ph METER DAN PERSIAPAN LARUTAN PENYANGGA Nama : Juwita (127008003) Herviani Sari (127008008) Tanggal Praktikum: 4 Oktober 2012 Tujuan Praktikum: 1. Memahami prinsip dasar larutan buffer
LAPORAN PRAKTIKUM 03 ph METER DAN PERSIAPAN LARUTAN PENYANGGA Nama : Juwita (127008003) Herviani Sari (127008008) Tanggal Praktikum: 4 Oktober 2012 Tujuan Praktikum: 1. Memahami prinsip dasar larutan buffer
LAPORAN PRAKTIKUM ph METER DAN PERSIAPAN LARUTAN PENYANGGA
 LAPORAN PRAKTIKUM ph METER DAN PERSIAPAN LARUTAN PENYANGGA Nama : Meutia Atika Faradilla (147008014) Sri Wulandari (147008005) Tanggal Praktikum : 10 Maret 2015 Tujuan Praktikum : 1. Memahami prinsip dasar
LAPORAN PRAKTIKUM ph METER DAN PERSIAPAN LARUTAN PENYANGGA Nama : Meutia Atika Faradilla (147008014) Sri Wulandari (147008005) Tanggal Praktikum : 10 Maret 2015 Tujuan Praktikum : 1. Memahami prinsip dasar
Laporan Praktikum ph Meter dan Persiapan Larutan Penyangga
 Tujuan Praktikum : Laporan Praktikum ph Meter dan Persiapan Larutan Penyangga Oleh : Ferry Prawira Gurusinga; Maya Anjelir Antika; Winda Kharunnisa Harahap Hari/Tanggal : Kamis / 10 Oktober 2013 1. Untuk
Tujuan Praktikum : Laporan Praktikum ph Meter dan Persiapan Larutan Penyangga Oleh : Ferry Prawira Gurusinga; Maya Anjelir Antika; Winda Kharunnisa Harahap Hari/Tanggal : Kamis / 10 Oktober 2013 1. Untuk
FAKULTAS TEKNIK UNIVERSITAS NEGERI YOGYAKARTA BAHAN AJAR KIMIA DASAR
 No. BAK/TBB/SBG201 Revisi : 00 Tgl. 01 Mei 2008 Hal 1 dari 11 BAB VIII LARUTAN ASAM DAN BASA Asam dan basa sudah dikenal sejak dahulu. Istilah asam (acid) berasal dari bahasa Latin acetum yang berarti
No. BAK/TBB/SBG201 Revisi : 00 Tgl. 01 Mei 2008 Hal 1 dari 11 BAB VIII LARUTAN ASAM DAN BASA Asam dan basa sudah dikenal sejak dahulu. Istilah asam (acid) berasal dari bahasa Latin acetum yang berarti
Tentukan ph dari suatu larutan yang memiliki konsentrasi ion H + sebesar 10 4 M dengan tanpa bantuan alat hitung kalkulator!
 Kimia Study Center - Contoh soal dan pembahasan tentang cara menghitung ph dan poh larutan asam basa berdasarkan konsentrasi ion [H + ] dan [OH ] SMA kelas 11 IPA. Berikut contoh-contoh soal yang bisa
Kimia Study Center - Contoh soal dan pembahasan tentang cara menghitung ph dan poh larutan asam basa berdasarkan konsentrasi ion [H + ] dan [OH ] SMA kelas 11 IPA. Berikut contoh-contoh soal yang bisa
BAB IV PROSEDUR PENELITIAN
 BAB IV PROSEDUR PENELITIAN 4.1. Penentuan Trayek ph Indikator Alami Dalam penentuan trayek ph, dilakukan beberapa persiapan seperti pembuatan ekstrak buah naga merah dan buah murbei. Selain itu, juga diakukan
BAB IV PROSEDUR PENELITIAN 4.1. Penentuan Trayek ph Indikator Alami Dalam penentuan trayek ph, dilakukan beberapa persiapan seperti pembuatan ekstrak buah naga merah dan buah murbei. Selain itu, juga diakukan
TITRASI KOMPLEKSOMETRI
 TITRASI KOMPLEKSOMETRI I. TUJUAN a. Menstandarisasi EDTA dengan larutan ZnSO 4 b. Menentukan konsentrasi larutan Ni 2+ c. Memahami prinsip titrasi kompleksometri II. TEORI Titrasi kompleksometri adalah
TITRASI KOMPLEKSOMETRI I. TUJUAN a. Menstandarisasi EDTA dengan larutan ZnSO 4 b. Menentukan konsentrasi larutan Ni 2+ c. Memahami prinsip titrasi kompleksometri II. TEORI Titrasi kompleksometri adalah
SOAL SELEKSI NASIONAL TAHUN 2006
 SOAL SELEKSI NASIONAL TAHUN 2006 Soal 1 ( 13 poin ) KOEFISIEN REAKSI DAN LARUTAN ELEKTROLIT Koefisien reaksi merupakan langkah penting untuk mengamati proses berlangsungnya reaksi. Lengkapi koefisien reaksi-reaksi
SOAL SELEKSI NASIONAL TAHUN 2006 Soal 1 ( 13 poin ) KOEFISIEN REAKSI DAN LARUTAN ELEKTROLIT Koefisien reaksi merupakan langkah penting untuk mengamati proses berlangsungnya reaksi. Lengkapi koefisien reaksi-reaksi
LAPORAN PRATIKUM II PRATIKUM PH METER DAN PERSIAPAN LARUTAN PENYANGGA
 LAPORAN PRATIKUM II PRATIKUM PH METER DAN PERSIAPAN LARUTAN PENYANGGA NAMA : ASTRID SISKA PRATIWI (147008007) IKA WARAZTUTY (147008019) PRODI : MAGISTER ILMU BIOMEDIK TGL PRATIKUM : 10 MARET 2015 TUJUAN
LAPORAN PRATIKUM II PRATIKUM PH METER DAN PERSIAPAN LARUTAN PENYANGGA NAMA : ASTRID SISKA PRATIWI (147008007) IKA WARAZTUTY (147008019) PRODI : MAGISTER ILMU BIOMEDIK TGL PRATIKUM : 10 MARET 2015 TUJUAN
LAPORAN PRAKTIKUM SINTESIS SENYAWA ORGANIK : Reaksi Pembuatan Alkena dengan Dehidrasi Alkohol
 Paraf Asisten Judul LAPORAN PRAKTIKUM SINTESIS SENYAWA ORGANIK : Reaksi Pembuatan Alkena dengan Dehidrasi Alkohol Tujuan Percobaan : 1. Mempelajari reaksi dehidrasi dari suatu alkohol untuk menghasilkan
Paraf Asisten Judul LAPORAN PRAKTIKUM SINTESIS SENYAWA ORGANIK : Reaksi Pembuatan Alkena dengan Dehidrasi Alkohol Tujuan Percobaan : 1. Mempelajari reaksi dehidrasi dari suatu alkohol untuk menghasilkan
Lampiran Sumber Belajar : Purba, Michael Kimia SMA. Erlangga. Jakarta
 Lampiran 3 95 INTRUKSI 1. Setiap siswa harus membaca penuntun praktikum ini dengan seksama. 2. Setelah alat dan bahan siap tersedia, laksanakanlah percobaan menurut prosedur percobaan. 3. Setelah melakukan
Lampiran 3 95 INTRUKSI 1. Setiap siswa harus membaca penuntun praktikum ini dengan seksama. 2. Setelah alat dan bahan siap tersedia, laksanakanlah percobaan menurut prosedur percobaan. 3. Setelah melakukan
Larutan Asam-Basa. Sifat Larutan Asam dan Basa. Penentuan ph Larutan Asam Kuat dan Basa Kuat. Penentuan ph Larutan Asam Lemah dan Basa Lemah
 Setelah mempelajari bab ini, peserta didik dapat: 1. menjelaskan konsep asam-basa serta sifat larutan asam dan basa; 2. menentukan ph larutan asam kuat, asam lemah, basa kuat, dan basa lemah; 3. terampil
Setelah mempelajari bab ini, peserta didik dapat: 1. menjelaskan konsep asam-basa serta sifat larutan asam dan basa; 2. menentukan ph larutan asam kuat, asam lemah, basa kuat, dan basa lemah; 3. terampil
kimia TITRASI ASAM BASA
 Kurikulum 2006/2013 2013 kimia K e l a s XI TITRASI ASAM BASA Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami definisi dan macam-macam titrasi.
Kurikulum 2006/2013 2013 kimia K e l a s XI TITRASI ASAM BASA Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami definisi dan macam-macam titrasi.
Titrasi Potensiometri
 Modul 1 Titrasi Potensiometri Dr. Anna Permanasari, M.Si. K egiatan praktikum ini dimaksudkan untuk melatih mahasiswa agar terampil dalam melakukan praktikum yang berhubungan dengan titrasi potensiometri.
Modul 1 Titrasi Potensiometri Dr. Anna Permanasari, M.Si. K egiatan praktikum ini dimaksudkan untuk melatih mahasiswa agar terampil dalam melakukan praktikum yang berhubungan dengan titrasi potensiometri.
LOGO. Stoikiometri. Tim Dosen Pengampu MK. Kimia Dasar
 LOGO Stoikiometri Tim Dosen Pengampu MK. Kimia Dasar Konsep Mol Satuan jumlah zat dalam ilmu kimia disebut mol. 1 mol zat mengandung jumlah partikel yang sama dengan jumlah partikel dalam 12 gram C 12,
LOGO Stoikiometri Tim Dosen Pengampu MK. Kimia Dasar Konsep Mol Satuan jumlah zat dalam ilmu kimia disebut mol. 1 mol zat mengandung jumlah partikel yang sama dengan jumlah partikel dalam 12 gram C 12,
LARUTAN ASAM-BASA DAN LARUTAN PENYANGGA
 LARUTAN ASAM-BASA DAN LARUTAN PENYANGGA A. Pengertian Larutan Penyangga Larutan penyangga biasa disebut juga dengan larutan Buffer atau larutan Dapar. Dimana larutan penyangga merupakan larutan yang mampu
LARUTAN ASAM-BASA DAN LARUTAN PENYANGGA A. Pengertian Larutan Penyangga Larutan penyangga biasa disebut juga dengan larutan Buffer atau larutan Dapar. Dimana larutan penyangga merupakan larutan yang mampu
Kimia Study Center - Contoh soal dan pembahasan tentang hidrolisis larutan garam dan menentukan ph atau poh larutan garam, kimia SMA kelas 11 IPA.
 Kimia Study Center - Contoh soal dan pembahasan tentang hidrolisis larutan garam dan menentukan ph atau poh larutan garam, kimia SMA kelas 11 IPA. Soal No. 1 Dari beberapa larutan berikut ini yang tidak
Kimia Study Center - Contoh soal dan pembahasan tentang hidrolisis larutan garam dan menentukan ph atau poh larutan garam, kimia SMA kelas 11 IPA. Soal No. 1 Dari beberapa larutan berikut ini yang tidak
III. METODOLOGI PENELITIAN. Penelitian ini dilaksanakan pada bulan Agustus sampai dengan bulan Oktober
 24 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan Agustus sampai dengan bulan Oktober 2011 di Laboratorium Biomassa Jurusan Kimia Fakultas Matematika dan
24 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan Agustus sampai dengan bulan Oktober 2011 di Laboratorium Biomassa Jurusan Kimia Fakultas Matematika dan
LAPORAN PRAKTIKUM 2. : Magister Ilmu Biolmedik : ph meter, persiapan larutan penyangga Tanggal pelaksanaan : 10 Maret 2015
 LAPORAN PRAKTIKUM NAMA PRAKTIKAN : Nini Chairani (14700801) Zakirullah Syafei (1470080) PRODI : Magister Ilmu Biolmedik JUDUL : ph meter, persiapan larutan penyangga Tanggal pelaksanaan : 10 Maret 015
LAPORAN PRAKTIKUM NAMA PRAKTIKAN : Nini Chairani (14700801) Zakirullah Syafei (1470080) PRODI : Magister Ilmu Biolmedik JUDUL : ph meter, persiapan larutan penyangga Tanggal pelaksanaan : 10 Maret 015
