Uji Stabilitas Obat Tradisional sesuai CPOTB dan GMP ASEAN TM/HS
|
|
|
- Sudomo Tanuwidjaja
- 6 tahun lalu
- Tontonan:
Transkripsi
1 Uji Stabilitas Obat Tradisional sesuai CPOTB dan GMP ASEAN TM/HS Disajikan pada Rakernas dan PIT IAI 2017 Jakarta, 6 8 September Mei 2016 Widiastuti Adiputra 2 REGULASI TERKAIT UJI STABILITAS OBAT TRADISIONAL 1
2 INDONESIA Peraturan Menteri Kesehatan Republik Indonesia Nomor 007 tahun 2012 tentang Registrasi Obat Tradisional Peraturan Ka BPOM No. HK tahun 2005; Kriteria dan Tata laksana pendaftaran obat tradisional,oht dan fitofarmaka CPOTB 2011 LAIN-LAIN Asean Guideline on Stability Study and Shelf Life of TM and HS pre-marketing Guidelines on Good Manufacturing Practice for TM and HS post-marketing WHO TRS 937 Annex 3 Supplementary Guidelines on Good Manufacturing Practices for The Manufacture of Herbal Medicines 3 PRE-MARKETING Peraturan Ka BPOM No. HK ; Kriteria dan Tata laksana pendaftaran Obat Tradisional,OHT dan Fitofarmaka Check list kelengkapan berkas (POM-02.SOP.07.IK.02(41)/F.01 POST MARKETING PERMEN Bab VI pasal 22 Kewajiban Pemegang Nomor Izin Edar CPOTB 2011 BAB 7 Pengawasan Mutu Program Stabiltas Pascapemasaran 4 2
3 Sesuai dengan ketentuan Peraturan Ka BPOM No. HK ; Kriteria dan Tata laksana pendaftaran obat tradisional,oht dan fitofarmaka Pendaftaran Baru Variasi :... perubahan stabilitas CHECKLIST PEMERIKSAAN BERKAS PENDAFTARAN Metode dan hasil uji stabilitas jangka panjang minimal 2 bets, suhu 30±2ºC RH 75±5% sampai dengan batas daluwarsa ATAU Metode dan hasil uji stabilitas minimal 2batch,suhu 30±2ºC RH 75±5% min 6 bln, disertai dengan accelerated stability 6 bln disertai komitmen stabilitas 5 WHO TRS 937 Annex 3 Jika mencantumkan tanggal daluwarsa maka data stabilitas yang mendukung shelf life dlm kondisi penyimpanan yang ditentukan harus tersedia 6 3
4 PRE MARKETING POST MARKETING/ PASCAPEMASARAN Pendaftaran PRODUK untuk mendapatkan Izin Edar Memberikan bukti kualitas produk jadi : Jangka waktu tertentu MASA EDAR Penentuan kondisi penyimpanan Pemenuhan aspek CPOTB Penjaminan Mutu Produk dengan memantau : Mutu produk selama masa edar Menjamin bahwa produk tetap memenuhi spesifikasi pada kondisi penyimpanan sesuai yang tercantum pada label 7 8 STUDI STABILITAS 4
5 OBAT TRADISIONAL 20/08/2017 Tujuan pengujian stabilitas adalah memberikan bukti tentang mutu zat aktif atau produk obat yang bervariasi seiring waktu di bawah pengaruh berbagai faktor lingkungan seperti suhu, kelembaban, dan cahaya, dan menetapkan masa uji ulang untuk zat aktif atau umur simpan untuk produk obat dan kondisi penyimpanan yang direkomendasikan ICH Q1A : STABILITY TESTING OF NEW DRUG SUBSTANCES AND PRODUCTS 9 WAJIB melaksnanakan UJI Stabilitas Premarket Pascapemasaran 10 5
6 KELENGKAPAN 20/08/2017 DESAIN PROGRAM SARANA TERKUALIFIKASI DAN DIMONITOR PENGELOLAAN PROTAP 11 1 CAKUPAN Pemilihan bets dan jumlah sampel Sistem wadah (dan tutup) Kondisi penyimpanan Frekwensi pengujian Spesifikasi/ testing parameter 12 6
7 CAKUPAN DESKRIPSI Pemilihan bets Minimal 2 bets. Jumlah sampel disesuaikan dengan kebutuhan seluruh pengujian Sistem wadah (dan tutup) Dikemas dengan jenis kemasan yang sama dengan yang akan dipasarkan ( kemasan primer dan sekunder ) Kondisi penyimpanan 30 0 ±2 0 C/ RH 75% ± 5% & 40 0 ±2 0 C/ RH 75% ± 5% Frekwensi pengujian Spesifikasi/ testing parameter PREMARKET Periode pemeriksaan: sesuai dengan stabilitas jangka panjang : 0, 3, 6, 12, 18, 24, 36 atau sampai masa daluarsanya tercapai. Parameter pengujian sesuai spesifikasi produk jadi (sesuai dokumen izin edar) 13 CAKUPAN DESKRIPSI Pemilihan bets Minimal 1 bets dalam 1 tahun, asalkan didukung data Pengkajian Mutu Produk. Jumlah sampel disesuaikan dengan kebutuhan seluruh pengujian Sistem wadah (dan tutup) Dikemas dengan jenis kemasan yang sama dengan yang akan dipasarkan ( kemasan primer dan sekunder ) Kondisi penyimpanan 30 0 ±2 0 C/ RH 75% ± 5% & 40 0 ±2 0 C/ RH 75% ± 5% Frekwensi pengujian Spesifikasi/ testing parameter POSTMARKET Periode pemeriksaan: sesuai dengan stabilitas jangka panjang : 0, 3, 6, 12, 18, 24, 36 atau sampai masa daluarsanya tercapai. Parameter pengujian sesuai spesifikasi produk 14 jadi (sesuai dokumen izin edar) 7
8 PEMILIHAN BETS (PREMARKETING) Minimal 2 bets yg berasal dari bets pilot ( lk 10% dari skala produksi ), bets primer ( % skala produksi), bets komersial atau kombinasinya, pemakaian bets dg skala lab tidak dapat diterima Proses pembuatan bets-bets yang digunakan dalam uji stabilitas hendaklah identik dengan bets skala komersial, mempunyai kualitas yang sama dalam hal spesifikasi dengan bets yang dipasarkan Dikemas dengan jenis kemasan yang sama dengan yang akan dipasarkan ( kemasan primer dan sekunder ) Studi dilakukan untuk tiap kekuatan dan jenis wadah / kemasan produk jadi, kecuali desain bracketing / matrixing diaplikasikan. Justifikasi pemakaian reduced design harus disertakan. 15 PEMILIHAN BETS (PRE & POSTMARKETING) Prinsip desain bracketing dan matrixing dapat diberlakukan Bracketing Rancangan studi stabilitas dari sampel yang hanya menelaah halhal yang ekstrim pada seluruh pengamatan, misalnya kekuatan, volume / isi Matrixing Rancangan studi stabilitas terhadap sebagian dari sampel yang tersedia yang mewakili kombinasi faktor diperiksa pada waktu yang ditentukan. Kemudian pada waktu yang lain, sekelompok sampel lain yang mewakili faktor kombinasi diperiksa. 16 8
9 Strength 20/08/2017 Kekuatan 50 mg 75 mg 100 mg Bets Wadah 15 ml T T T T T T 100 ml 500 ml T T T T T T 17 One half reduction Time point (months) Sl Batch1 T T T T T T Batch2 T T T T T S2 Batch1 T T T T T Batch2 T T T T T T Min 6 dari 12 titik Min 4 dari 8 titik 18 9
10 Strength 20/08/2017 One third reduction Time point (months) Sl S2 Batch1 T T T T T T T Batch2 T T T T T T Batch1 T T T T T T T Batch2 T T T T T T Min 8 dari 12 titik Min 6 dari 8 titik 19 ASEAN GL 20 10
11 KONDISI PERCOBAAN Tipe wadah Produk dalam kemasan primer permeable terhadap uap air Produk dalam kemasan primer impermeable terhadap uap air Accelerated study Kondisi Pengujian 30 o C± 2 0 C/75%± 5%RH 30 o C± 2 0 C 40 o C± 2 0 C/75%± 5%RH 21 SPESIFIKASI (1) Meliputi pemeriksaan fisik, kimia dan mikrobiologi obat jadi yang bisa berubah selama penyimpanan dan perubahan tersebut memengaruhi kualitas Tidak semua parameter pengujian pada spesifikasi produk dimasukkan dlm protokol uji stabilitas dari produk terkait mis. logam berat 22 11
12 SPESIFIKASI (2) Produk yang berisi komponen tanpa marker yang diketahui, maka parameter fisik dapat dipakai sebagai indikator yang diamati selama penyimpanan. Parameter fisik yang dipilih harus disertai justifikasi. Parameter fisik dapat diperiksa dengan cara sebagai berikut : Pengujian organoleptis : berdasarkan pancaindera Uji makroskopis : berdasarkan penglihatan / visual Uji mikroskopis : pemeriksaan dengan mikroskop 23 SPESIFIKASI (3) Produk kombinasi yang terdiri dari beberapa zat berkhasiat, meski tidak harus melakukan penetapan kadar untuk semua bahan aktif, maka dapat dilakukan penetapan untuk 1( satu ) atau lebih bahan aktif, atau marker yang diketahui dapat mengalami perubahan selama penyimpanan dan perubahan ini akan memengaruhi kualitas produk jadi. Justifikasi yang memadai harus disertakan 24 12
13 SPESIFIKASI (4) Untuk pemastian batas daluwarsa dari obat herbal, parameter seperti moisture content, AKK, dan spesifikasi umum dari setiap bentuk sediaan seperti waktu hancur, kekerasan, harus dipantau Stabilitas dari bahan pengawet juga diperiksa Spesifikasi dan persyaratan merujuk kepada : Dokumen Izizn Edar yang disetujui PerKaBPOM 12/2014 Tentang Persyaratan Mutu Obat Tradisional 25 Dosage Forms Organoleptic characteristics Assay Hardness/ friability TESTING PARAMETER Disintegrati on or Water Microbial Viscosity ph dissolution content content rate Granules/ Particle size variatioon Resuspen ability Adhesive ness Oral powder Hard capsule Soft capsule Coated and Uncoated tablet Coated and Uncoated Pill/Pellet Suspension Solution Emulsion Semi Solid Preparation (Oint/Cream/G el/lotion/paste Plaster Granules Herbal Tea Bag Pastilles 26 13
14 CAKUPAN Pemilihan bets dan jumlah sampel Sistem wadah (dan tutup) Kondisi penyimpanan Frekwensi pengujian Spesifikasi/ testing parameter Dituangkan dalam PROTOKOL 27 2 Climatic Chamber atau Ruangan Syarat Terkualifikasi RH dan Suhu terkalibrasi Dimonitor terus menerus 28 14
15 3 Penjadwalan sampling produk dan pengujian Dikelola oleh QC/QA Manual atau alat bantu (MS Office : Excell/Access) 29 4 PROTAP Desain program stabilitas Sarana Pengelolaan Pengujian Evaluasi hasil Format protokol Format laporan 30 15
16 KELENGKAPAN PELAKSANAAN 20/08/2017 Protokol Desain program SARANA terkualifikasi dan dimonitor Pengelolaan Protap Produk terpilih Pengujian sesuai jadwal Laporan 31 PROTOKOL: memberikan instruksi untuk melakukan dan mencatat pelaksanaan kegiatan tertentu. Studi Stabilitas hendaklah dilengkapi dengan PROTOKOL yang sah dan tersedia untuk regulator Pemilihan bets berdasarkan ketentuan yang merujuk kepada regulasi mutahir Pengujian/analisis dilakukan sesuai program yang dibuat Hasil dari pelaksanaan dituangkan dalam laporan Ad Interim final 32 16
17 BERISI a.l jumlah bets dan ukuran bets yang berbeda, jika ada; metode uji fisika, kimia, dan mikrobiologi; kriteria penerimaan; referensi ke metode pengujian; sistem tutup-wadah kemasan primer ; interval waktu pengujian; uraian kondisi penyimpanan; parameter lain yang spesifik untuk obat tradisional 33 LAPORAN Bila perlu dibuat laporan ad interim Tersedia untuk Regulator Berisi Informasi produk dan studi (sesuai protokol) Hasil pengujian Evaluasi Kesimpulan Disahkan 34 17
18 PROGRAM STABILITA PASCA PEMASARAN memantau produk selama masa edar dan menjamin bahwa produk tetap memenuhi spesifikasi pada kondisi penyimpanan sesuai yang tercantum pada label (butir 7.28 CPOTB 2011) Stabilitas produk OT hendaklah dipantau sesuai program yang berkesinambungan agar dapat mendeteksi setiap masalah stabilitas (mis: perubahan tingkat kontaminasi) yang berkaitan dengan formulasi dalam kemasan yang dipasarkan (butir 7.27 CPOTB 2011) 35 Dalam kemasan yang dipasarkan Bentuk produk ruahan, bila disimpan untuk waktu lama sebelum dikemas dan/atau dikirimkan ke pabrik lain untuk dikemas, pada kondisi ambient. Produk antara yang disimpan dan digunakan untuk waktu lama waktu tunggu (butir 7.29 CPOTB 2011) 36 18
19 Pendekatan sistematis digunakan dalam penyajian dan evaluasi dari hasil uji stabilitas, hal ini termasuk, hasil uji fisis, kimia dan mikrobiologi Evaluasi hasil uji stabilitas tidak hanya mempertimbangkan penetapan kadar, tetapi juga parameter lain yang sesuai Evaluasi (referensi ICH Q1) Perubahan yang signifikan, misal > 5% dari initial Produk degradasi yang t.m.s. Pemerian dan sifat fisik 37 HULS yang terkonfirmasi, atau tren negatif yang signifikan Dilaporkan ke Badan POM. Kemungkinan dampak terhadap bets yang dipasarkan hendaklah dipertimbangkan Perbaikan internal terhadap mutu dan tipe/bahan pengemas primer 38 19
20 WAKTU TUNGGU PRODUK (HOLDING TIME) -2 PROSEDUR Wadah produk : sesuai untuk penyimpanan atau yang setara Kondisi penyimpanan : sesuai dengan suhu (&RH) produk akan disimpan Waktu : disesuaikan dengan kebutuhan Dokumen : Protokol dan Laporan Hasil merupakan informasi yang tertera di Catatan Bets (sebagai persyaratan) 39 PRODUK BERISIKO -1 Hasil PENGOLAHAN ULANG dengan keputusan dapat diproses lanjut Pelulusan akhir harus mempertimbangkan stabilita dipercepat (3-6 bulan) Pemastian dengan stabilita hingga waktu daluwarsa pada kondisi 30 o C± 2 0 C/75%± 5%RH 40 20
21 PRODUK BERISIKO -2 Adanya PERUBAHAN Berkaitan dengan data pendukung VARIASI Sebagai jaminan kualitas setelah proses atau material divalidasi 41 Studi yang dilakukan oleh pihak ketiga KONTRAK 42 21
Oleh : Bambang Priyambodo
 Oleh : Bambang Priyambodo SISTEMATIKA CPOB: 2012 merupakan penyempurnaan dari CPOB: 2006, mencakup revisi terhadap : Pedoman CPOB: 2006 Suplemen I Pedoman CPOB: 2006 tahun 2009 Aneks 8 : Cara Pembuatan
Oleh : Bambang Priyambodo SISTEMATIKA CPOB: 2012 merupakan penyempurnaan dari CPOB: 2006, mencakup revisi terhadap : Pedoman CPOB: 2006 Suplemen I Pedoman CPOB: 2006 tahun 2009 Aneks 8 : Cara Pembuatan
BAB II TINJAUAN PUSTAKA. Obat Jadi dan Industri Bahan Baku Obat. Definisi dari obat jadi yaitu
 BAB II TINJAUAN PUSTAKA A. Industri Farmasi 1. Pengertian Industri Farmasi Berdasarkan Surat Keputusan Menteri Kesehatan No. 245/MenKes/SK/V/1990 tentang Ketentuan dan Tata Cara Pelaksanaan Pemberian Izin
BAB II TINJAUAN PUSTAKA A. Industri Farmasi 1. Pengertian Industri Farmasi Berdasarkan Surat Keputusan Menteri Kesehatan No. 245/MenKes/SK/V/1990 tentang Ketentuan dan Tata Cara Pelaksanaan Pemberian Izin
Tugas dan tanggungjawab Quality Assurance (QA) / Jaminan Mutu
 Tugas dan tanggungjawab Quality Assurance (QA) / Jaminan Mutu Departemen QA merupakan departemen yang bertanggung jawab antara lain : a) Audit internal QA melakukan evaluasi kerja kesemua bagian/departemen
Tugas dan tanggungjawab Quality Assurance (QA) / Jaminan Mutu Departemen QA merupakan departemen yang bertanggung jawab antara lain : a) Audit internal QA melakukan evaluasi kerja kesemua bagian/departemen
BAB II TINJAUAN PUSTAKA. Indonesia Nomor 245/Menkes/SK/V/1990 terdiri dari industri obat jadi dan
 BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi 2.1.1 Pengertian Industri Farmasi Industri farmasi menurut Surat Keputusan Menteri Kesehatan Republik Indonesia Nomor 245/Menkes/SK/V/1990 terdiri dari industri
BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi 2.1.1 Pengertian Industri Farmasi Industri farmasi menurut Surat Keputusan Menteri Kesehatan Republik Indonesia Nomor 245/Menkes/SK/V/1990 terdiri dari industri
BAB I PENDAHULUAN. Kesehatan merupakan kebutuhan terpenting bagi manusia sehingga
 BAB I PENDAHULUAN A. Latar Belakang Kesehatan merupakan kebutuhan terpenting bagi manusia sehingga berbagai usaha dilakukan untuk memperoleh tubuh yang sehat. Mulai dari melakukan olah raga, hidup secara
BAB I PENDAHULUAN A. Latar Belakang Kesehatan merupakan kebutuhan terpenting bagi manusia sehingga berbagai usaha dilakukan untuk memperoleh tubuh yang sehat. Mulai dari melakukan olah raga, hidup secara
KATA PENGANTAR QUALITY CONTROL
 KATA PENGANTAR Assalamu alaikum, wr, wb, Segala Puji senantiasa kami panjatkan kehadirat Allah SWT beserta junjungan kita Nabi Besar Muhammad Rasulullah S.A.W yang telah melimpahkan rahmat, berkah, dan
KATA PENGANTAR Assalamu alaikum, wr, wb, Segala Puji senantiasa kami panjatkan kehadirat Allah SWT beserta junjungan kita Nabi Besar Muhammad Rasulullah S.A.W yang telah melimpahkan rahmat, berkah, dan
Penggunaan terbesar herbal. Fitofarmaka. supplement. kosmetik
 Penggunaan terbesar herbal Fitofarmaka supplement kosmetik Pasar herbal Pasar dunia 10 M USD Nilai export indonesia 100 Triliun Kualitas Produksi herbal GAP GMP GDP GAP ON FARM Iklim Tanah Ketinggian bibit
Penggunaan terbesar herbal Fitofarmaka supplement kosmetik Pasar herbal Pasar dunia 10 M USD Nilai export indonesia 100 Triliun Kualitas Produksi herbal GAP GMP GDP GAP ON FARM Iklim Tanah Ketinggian bibit
CPOB. (Cara Pembuatan Obat yang Baik)
 CPOB { (Cara Pembuatan Obat yang Baik) CPOB (Cara Pembuatan Obat Yang Baik) 2006 atau GMP (Good Manufacturing Practices) 2006 adalah suatu pedoman pembuatan obat berdasarkan berbagai ketentuan dalam CPOB
CPOB { (Cara Pembuatan Obat yang Baik) CPOB (Cara Pembuatan Obat Yang Baik) 2006 atau GMP (Good Manufacturing Practices) 2006 adalah suatu pedoman pembuatan obat berdasarkan berbagai ketentuan dalam CPOB
CHECKLIST DOKUMEN REGISTRASI OBAT COPY
 CHECKLIST DOKUMEN REGISTRASI OBAT COPY I. INFORMASI PRODUK Nama Obat : Bentuk sediaan & Kekuatan : Zat aktif : Kemasan : Pendaftar : Produsen : Kategori registrasi : II. DOKUMEN YANG DISERAHKAN No. Parameter
CHECKLIST DOKUMEN REGISTRASI OBAT COPY I. INFORMASI PRODUK Nama Obat : Bentuk sediaan & Kekuatan : Zat aktif : Kemasan : Pendaftar : Produsen : Kategori registrasi : II. DOKUMEN YANG DISERAHKAN No. Parameter
Tugas Individu Farmasi Industri. Uraian Tugas Kepala Bagian Produksi, Pengawasan Mutu dan Pemastian Mutu
 Tugas Individu Farmasi Industri Uraian Tugas Kepala Bagian Produksi, Pengawasan Mutu dan Pemastian Mutu Disusun Oleh : Eka Wahyu Lestari 14340004 Dosen : Drs. Kosasih, M.Sc., Apt. Program Profesi Apoteker
Tugas Individu Farmasi Industri Uraian Tugas Kepala Bagian Produksi, Pengawasan Mutu dan Pemastian Mutu Disusun Oleh : Eka Wahyu Lestari 14340004 Dosen : Drs. Kosasih, M.Sc., Apt. Program Profesi Apoteker
METODE PENGUJIAN STABILITAS Stabilitas didefinisikan sebagai kemampuan zat obat atau produk obat untuk tetap di dalam spesifikasi yang dibentuk untuk
 METODE PENGUJIAN STABILITAS Stabilitas didefinisikan sebagai kemampuan zat obat atau produk obat untuk tetap di dalam spesifikasi yang dibentuk untuk menjaga identitas, kekuatan, kualitas dan kemurnian.
METODE PENGUJIAN STABILITAS Stabilitas didefinisikan sebagai kemampuan zat obat atau produk obat untuk tetap di dalam spesifikasi yang dibentuk untuk menjaga identitas, kekuatan, kualitas dan kemurnian.
Aspek CPOTB/CPKB Pengawasan Mutu
 Aspek CPOTB/CPKB Pengawasan Mutu Better Ridder, S.Si., Apt., M.Buss. Direktorat Inspeksi dan Sertifikasi Obat Tradisional, Kosmetik dan Produk Komplemen AGENDA 1. Tujuan dan Indikator BPOM 2015-2019 2.
Aspek CPOTB/CPKB Pengawasan Mutu Better Ridder, S.Si., Apt., M.Buss. Direktorat Inspeksi dan Sertifikasi Obat Tradisional, Kosmetik dan Produk Komplemen AGENDA 1. Tujuan dan Indikator BPOM 2015-2019 2.
BAB II TINJAUAN PUSTAKA. menurut Peraturan Menteri Kesehatan RI No. 1799/Menkes/Per/XII/2010 tentang Industri Farmasi adalah badan usaha yang
 BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi 2.1.1 Pengertian Industri Farmasi Industri farmasi menurut Peraturan Menteri Kesehatan RI No. 1799/Menkes/Per/XII/2010 tentang Industri Farmasi adalah badan
BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi 2.1.1 Pengertian Industri Farmasi Industri farmasi menurut Peraturan Menteri Kesehatan RI No. 1799/Menkes/Per/XII/2010 tentang Industri Farmasi adalah badan
BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA
 PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.04.1.33.12.11.09938 TAHUN 2011 TENTANG KRITERIA DAN TATA CARA PENARIKAN OBAT YANG TIDAK MEMENUHI STANDAR DAN/ATAU PERSYARATAN DENGAN RAHMAT TUHAN
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.04.1.33.12.11.09938 TAHUN 2011 TENTANG KRITERIA DAN TATA CARA PENARIKAN OBAT YANG TIDAK MEMENUHI STANDAR DAN/ATAU PERSYARATAN DENGAN RAHMAT TUHAN
BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA
 PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.04.1.33.12.11.09938 TAHUN 2011 TENTANG KRITERIA DAN TATA CARA PENARIKAN OBAT YANG TIDAK MEMENUHI STANDAR DAN/ATAU PERSYARATAN DENGAN RAHMAT TUHAN
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.04.1.33.12.11.09938 TAHUN 2011 TENTANG KRITERIA DAN TATA CARA PENARIKAN OBAT YANG TIDAK MEMENUHI STANDAR DAN/ATAU PERSYARATAN DENGAN RAHMAT TUHAN
BAB II TINJAUAN PUSTAKA. Industri farmasi menurut SK Menkes No. 245/Menkes/SK/V/1990
 BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi 2.1.1 Pengertian Industri Farmasi Industri farmasi menurut SK Menkes No. 245/Menkes/SK/V/1990 adalah industri obat jadi dan industri bahan baku obat. Industri
BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi 2.1.1 Pengertian Industri Farmasi Industri farmasi menurut SK Menkes No. 245/Menkes/SK/V/1990 adalah industri obat jadi dan industri bahan baku obat. Industri
BAB II TINJAUAN PUSTAKA. Indonesia Nomor 245/Menkes/SK/V/1990 terdiri dari industri obat jadi dan
 BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi 2.1.1 Pengertian Industri Farmasi Industri farmasi menurut Surat Keputusan Menteri Kesehatan Republik Indonesia Nomor 245/Menkes/SK/V/1990 terdiri dari industri
BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi 2.1.1 Pengertian Industri Farmasi Industri farmasi menurut Surat Keputusan Menteri Kesehatan Republik Indonesia Nomor 245/Menkes/SK/V/1990 terdiri dari industri
Quality Control (QC) dan Quality Assurance (QA) Mata Kuliah : Rancangan Produk Industri (2 SKS) Dosen : Kuni Zu aimah B.,S.Farm., M.Farm., Apt.
 Quality Control (QC) dan Quality Assurance (QA) Mata Kuliah : Rancangan Produk Industri (2 SKS) Dosen : Kuni Zu aimah B.,S.Farm., M.Farm., Apt. Industri farmasi harus membuat obat sedemikian rupa agar
Quality Control (QC) dan Quality Assurance (QA) Mata Kuliah : Rancangan Produk Industri (2 SKS) Dosen : Kuni Zu aimah B.,S.Farm., M.Farm., Apt. Industri farmasi harus membuat obat sedemikian rupa agar
DALAM PENGAWASAN DAN PENINGKATAN DAYA SAING
 DALAM PENGAWASAN DAN PENINGKATAN DAYA SAING Obat Tradisional Drs. Ondri Dwi Sampurno, M.Si, Apt Deputi Bidang Pengawasan Obat Tradisional, Kosmetik dan Produk Komplemen RAPAT KERJA NASIONAL GP JAMU Jakarta,
DALAM PENGAWASAN DAN PENINGKATAN DAYA SAING Obat Tradisional Drs. Ondri Dwi Sampurno, M.Si, Apt Deputi Bidang Pengawasan Obat Tradisional, Kosmetik dan Produk Komplemen RAPAT KERJA NASIONAL GP JAMU Jakarta,
OUTLINE. Drs. Hary Wahyu T., Apt. Direktur Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen A. PENDAHULUAN
 Drs. Hary Wahyu T., Apt Direktur Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen BADAN POM RI OUTLINE A. PENDAHULUAN B. KONSEP PENGAWASAN OT/OBAT HERBAL C. KEAMANAN, KHASIAT/MANFAAT, MUTU
Drs. Hary Wahyu T., Apt Direktur Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen BADAN POM RI OUTLINE A. PENDAHULUAN B. KONSEP PENGAWASAN OT/OBAT HERBAL C. KEAMANAN, KHASIAT/MANFAAT, MUTU
1 Pendaftaran Akun Perusahaan. 2 Pendaftaran OT Low Risk. 3 Pendaftaran Ulang OT & SK 4 E-Trecking System Pendaftaran Baru dan Variasi OT & SK
 1 2 Aplikasi sistem E-Registrasi yang telah berlaku di Subdit Penilaian Obat Tradisional dan Suplemen Kesehatan yaitu: 1 Pendaftaran Akun Perusahaan 2 Pendaftaran OT Low Risk 3 Pendaftaran Ulang OT & SK
1 2 Aplikasi sistem E-Registrasi yang telah berlaku di Subdit Penilaian Obat Tradisional dan Suplemen Kesehatan yaitu: 1 Pendaftaran Akun Perusahaan 2 Pendaftaran OT Low Risk 3 Pendaftaran Ulang OT & SK
BAB II TINJAUAN PUSTAKA. Industri farmasi menurut Peraturan Menteri Kesehatan RI No.
 BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi 2.1.1 Pengertian Industri Farmasi Industri farmasi menurut Peraturan Menteri Kesehatan RI No. 1799/Menkes/Per/XII/2010 tentang Industri Farmasi adalah badan
BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi 2.1.1 Pengertian Industri Farmasi Industri farmasi menurut Peraturan Menteri Kesehatan RI No. 1799/Menkes/Per/XII/2010 tentang Industri Farmasi adalah badan
BAB II TINJAUAN PUSTAKA
 BAB II TINJAUAN PUSTAKA 2.1 Pengertian Industri Farmasi. Industri farmasi menurut Surat Keputusan Menteri Kesehatan Nomor. 245/Menkes/V/1990 adalah industri obat jadi dan industri bahan baku obat. Industri
BAB II TINJAUAN PUSTAKA 2.1 Pengertian Industri Farmasi. Industri farmasi menurut Surat Keputusan Menteri Kesehatan Nomor. 245/Menkes/V/1990 adalah industri obat jadi dan industri bahan baku obat. Industri
BAB II TINJAUAN UMUM. Universitas Sumatera Utara
 BAB II TINJAUAN UMUM 2.1 Industri Farmasi Industri farmasi adalah industri obat jadi dan industri bahan baku obat. Industri farmasi sebagai industri penghasil obat, dituntut untuk dapat menghasilkan obat
BAB II TINJAUAN UMUM 2.1 Industri Farmasi Industri farmasi adalah industri obat jadi dan industri bahan baku obat. Industri farmasi sebagai industri penghasil obat, dituntut untuk dapat menghasilkan obat
BAB II TINJAUAN PUSTAKA
 BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi Berdasarkan Surat Keputusan Menteri Kesehatan Republik Indonesia Nomor 245/Menkes/SK/V/1990 tentang Ketentuan dan Tata cara Pelaksanaan Pemberian Izin Usaha
BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi Berdasarkan Surat Keputusan Menteri Kesehatan Republik Indonesia Nomor 245/Menkes/SK/V/1990 tentang Ketentuan dan Tata cara Pelaksanaan Pemberian Izin Usaha
REGULASI PENGELOLAAN DISTRIBUSI OBAT DAN URGENCY SERTIFIKASI CDOB
 REGULASI PENGELOLAAN DISTRIBUSI OBAT DAN URGENCY SERTIFIKASI CDOB Disampaikan oleh: Direktur Pengawasan Distribusi Produk Terapetik & PKRT Pertemuan Ilmiah Tahunan (PIT) IKATAN APOTEKER INDONESIA Tangerang
REGULASI PENGELOLAAN DISTRIBUSI OBAT DAN URGENCY SERTIFIKASI CDOB Disampaikan oleh: Direktur Pengawasan Distribusi Produk Terapetik & PKRT Pertemuan Ilmiah Tahunan (PIT) IKATAN APOTEKER INDONESIA Tangerang
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR : HK TENTANG
 PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR : HK.00.05.41.1384 TENTANG KRITERIA DAN TATA LAKSANA PENDAFTARAN OBAT TRADISIONAL, OBAT HERBAL TERSTANDAR DAN FITOFARMAKA DENGAN RAHMAT TUHAN YANG
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR : HK.00.05.41.1384 TENTANG KRITERIA DAN TATA LAKSANA PENDAFTARAN OBAT TRADISIONAL, OBAT HERBAL TERSTANDAR DAN FITOFARMAKA DENGAN RAHMAT TUHAN YANG
Cara Distribusi Obat yang Baik (CDOB)
 Cara Distribusi Obat yang Baik (CDOB) BPOM dalam mengawal obat Visi : Obat dan makanan terjamin aman,bermutu dan berkhasiat. Misi: Melindungi masyarakat dari obat dan makanan yang beresiko terhadap kesehatan.
Cara Distribusi Obat yang Baik (CDOB) BPOM dalam mengawal obat Visi : Obat dan makanan terjamin aman,bermutu dan berkhasiat. Misi: Melindungi masyarakat dari obat dan makanan yang beresiko terhadap kesehatan.
BAB II TINJAUAN PUSTAKA. Indonesia Nomor 245/Menkes/SK/V/1990 terdiri dari industri obat jadi dan
 BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi 2.1.1 Pengertian Industri Farmasi Industri farmasi menurut Surat Keputusan Menteri Kesehatan Republik Indonesia Nomor 245/Menkes/SK/V/1990 terdiri dari industri
BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi 2.1.1 Pengertian Industri Farmasi Industri farmasi menurut Surat Keputusan Menteri Kesehatan Republik Indonesia Nomor 245/Menkes/SK/V/1990 terdiri dari industri
UJI STABILITAS DIPERCEPAT TENGAH SEMESTER KE II PTA 2007-2008 PROGRAM S2 ILMU KEFARMASIAN
 UJI STABILITAS DIPERCEPAT TENGAH SEMESTER KE II PTA 2007-2008 PROGRAM S2 ILMU KEFARMASIAN SASARAN UTAMA Mengembangkan formulasi obat Menentukan jangka waktu stabilitas obat Memenuhi persyaratan registrasi
UJI STABILITAS DIPERCEPAT TENGAH SEMESTER KE II PTA 2007-2008 PROGRAM S2 ILMU KEFARMASIAN SASARAN UTAMA Mengembangkan formulasi obat Menentukan jangka waktu stabilitas obat Memenuhi persyaratan registrasi
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA
 PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.03.1.23.02.12.1248 TAHUN 2012 TENTANG KRITERIA DAN TATA CARA PENARIKAN OBAT TRADISIONAL YANG TIDAK MEMENUHI PERSYARATAN DENGAN RAHMAT TUHAN YANG
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.03.1.23.02.12.1248 TAHUN 2012 TENTANG KRITERIA DAN TATA CARA PENARIKAN OBAT TRADISIONAL YANG TIDAK MEMENUHI PERSYARATAN DENGAN RAHMAT TUHAN YANG
BAB II TINJAUAN PUSTAKA. Obat Jadi dan Industri Bahan Baku Obat. Definisi dari obat jadi yaitu
 BAB II TINJAUAN PUSTAKA A. Industri Farmasi 1. Pengertian Industri Farmasi Berdasarkan Surat Keputusan Menteri Kesehatan No. 245/MenKes/SK/V/1990 tentang Ketentuan dan Tata Cara Pelaksanaan Pemberian Izin
BAB II TINJAUAN PUSTAKA A. Industri Farmasi 1. Pengertian Industri Farmasi Berdasarkan Surat Keputusan Menteri Kesehatan No. 245/MenKes/SK/V/1990 tentang Ketentuan dan Tata Cara Pelaksanaan Pemberian Izin
BAB II TINJAUAN PUSTAKA. (CPOB). Hal ini didasarkan oleh Keputusan Menteri Kesehatan RI.
 BAB II TINJAUAN PUSTAKA Industri farmasi diwajibkan menerapkan Cara Pembuatan Obat yang Baik (CPOB). Hal ini didasarkan oleh Keputusan Menteri Kesehatan RI. No.43/MENKES/SK/II/1988 tentang CPOB dan Keputusan
BAB II TINJAUAN PUSTAKA Industri farmasi diwajibkan menerapkan Cara Pembuatan Obat yang Baik (CPOB). Hal ini didasarkan oleh Keputusan Menteri Kesehatan RI. No.43/MENKES/SK/II/1988 tentang CPOB dan Keputusan
 Pengawasan mutu:. Proses Pembuatan OT Pembuatan Produksi Pengadaan bahan awal/penyiapan BB Penimbangan BB Produk antara Produk ruahan Pengemasan Pengawasan Mutu Distribusi Pengolahan http://farmasibahanalam.com
Pengawasan mutu:. Proses Pembuatan OT Pembuatan Produksi Pengadaan bahan awal/penyiapan BB Penimbangan BB Produk antara Produk ruahan Pengemasan Pengawasan Mutu Distribusi Pengolahan http://farmasibahanalam.com
Menimbang : Mengingat :
 KEPUTUSAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR HK.00.5.1.2569 TENTANG KRITERIA DAN TATA LAKSANA PENILAIAN PRODUK PANGAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN, Menimbang : Mengingat
KEPUTUSAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR HK.00.5.1.2569 TENTANG KRITERIA DAN TATA LAKSANA PENILAIAN PRODUK PANGAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN, Menimbang : Mengingat
1 Pendaftaran Akun Perusahaan. 2 Pendaftaran OT Low Risk. 3 Pendaftaran Ulang OT & SK 4 E-Trecking System Pendaftaran Baru dan Variasi OT & SK
 1 2 Aplikasi sistem E-Registrasi yang telah berlaku di Subdit Penilaian Obat Tradisional dan Suplemen Kesehatan yaitu: 1 Pendaftaran Akun Perusahaan 2 Pendaftaran OT Low Risk 3 Pendaftaran Ulang OT & SK
1 2 Aplikasi sistem E-Registrasi yang telah berlaku di Subdit Penilaian Obat Tradisional dan Suplemen Kesehatan yaitu: 1 Pendaftaran Akun Perusahaan 2 Pendaftaran OT Low Risk 3 Pendaftaran Ulang OT & SK
B. Tujuan Tujuan Qualiy Assurance adalah untuk memastikan bahwa obat dihasilkan dengan mutu yang sesuai dengan tujuan pemakaiannya.
 PEMASTIAN MUTU (QUALITY ASSURANCE/QA) A. Pendahuluan Industri farmasi bertujuan untuk menghasilkan obat yang harus memenuhi persyaratan khasiat (efficacy), keamanan (safety) dan mutu (quality). Berdasarkan
PEMASTIAN MUTU (QUALITY ASSURANCE/QA) A. Pendahuluan Industri farmasi bertujuan untuk menghasilkan obat yang harus memenuhi persyaratan khasiat (efficacy), keamanan (safety) dan mutu (quality). Berdasarkan
BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA
 BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 17 TAHUN 2016 TENTANG PERUBAHAN KEDUA ATAS PERATURAN KEPALA BADAN PENGAWAS OBAT
BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 17 TAHUN 2016 TENTANG PERUBAHAN KEDUA ATAS PERATURAN KEPALA BADAN PENGAWAS OBAT
BAB II TINJAUAN PUSTAKA. Industri farmasi menurut SK Menkes No. 245/Menkes/SK/V/1990 adalah
 BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi Industri farmasi menurut SK Menkes No. 245/Menkes/SK/V/1990 adalah industri obat jadi dan industri bahan baku obat. Industri obat jadi adalah industri yang
BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi Industri farmasi menurut SK Menkes No. 245/Menkes/SK/V/1990 adalah industri obat jadi dan industri bahan baku obat. Industri obat jadi adalah industri yang
No Kode DAR2/Profesional/582/010/2018 PENDALAMAN MATERI FARMASI MODUL 010: CARA DISTRIBUSI OBAT YANG BAIK. Dr. NURKHASANAH, M.Si., Apt.
 No Kode DAR2/Profesional/582/010/2018 PENDALAMAN MATERI FARMASI MODUL 010: CARA DISTRIBUSI OBAT YANG BAIK Dr. NURKHASANAH, M.Si., Apt. Kementerian Pendidikan dan Kebudayaan Kementerian Riset, Teknologi
No Kode DAR2/Profesional/582/010/2018 PENDALAMAN MATERI FARMASI MODUL 010: CARA DISTRIBUSI OBAT YANG BAIK Dr. NURKHASANAH, M.Si., Apt. Kementerian Pendidikan dan Kebudayaan Kementerian Riset, Teknologi
JAKARTA, 24 NOVEMBER 2017
 JAKARTA, 24 NOVEMBER 2017 Dra. Togi J. Hutadjulu, Apt. MHA. BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA www.pom.go.id 1. PENDAHULUAN 2. REVISI KRITERIA DAN TATA LAKSANA REGISTRASI OBAT 3. PENUTUP
JAKARTA, 24 NOVEMBER 2017 Dra. Togi J. Hutadjulu, Apt. MHA. BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA www.pom.go.id 1. PENDAHULUAN 2. REVISI KRITERIA DAN TATA LAKSANA REGISTRASI OBAT 3. PENUTUP
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 14 TAHUN 2017 TENTANG PEDOMAN DOKUMEN INFORMASI PRODUK
 BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 14 TAHUN 2017 TENTANG PEDOMAN DOKUMEN INFORMASI PRODUK DENGAN RAHMAT TUHAN YANG
BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 14 TAHUN 2017 TENTANG PEDOMAN DOKUMEN INFORMASI PRODUK DENGAN RAHMAT TUHAN YANG
2016, No Mengingat : 1. Undang-undang Nomor 8 Tahun 1999 tentang Perlindungan Konsumen (Lembaran Negara Republik Indonesia Tahun 1999 Nomor 42,
 BERITA NEGARA REPUBLIK INDONESIA No.498, 2016 BPOM. Obat Tradisional Tidak Memenuhi Persyaratan. Penarikan dan Pemusnahan. Pencabutan. PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA
BERITA NEGARA REPUBLIK INDONESIA No.498, 2016 BPOM. Obat Tradisional Tidak Memenuhi Persyaratan. Penarikan dan Pemusnahan. Pencabutan. PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA
PEDOMAN PENYIAPAN DOKUMEN INDUK INDUSTRI FARMASI DAN INDUSTRI OBAT TRADISIONAL PENDAHULUAN
 7 2012, No.294 LAMPIRAN PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR HK.04.1.33.02.12.0883 TAHUN 2012 TENTANG DOKUMEN INDUK INDUSTRI FARMASI DAN INDUSTRI OBAT TRADISIONAL PEDOMAN
7 2012, No.294 LAMPIRAN PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR HK.04.1.33.02.12.0883 TAHUN 2012 TENTANG DOKUMEN INDUK INDUSTRI FARMASI DAN INDUSTRI OBAT TRADISIONAL PEDOMAN
DOKUMENTASI
 DOKUMENTASI PENDAHULUAN Dokumentasi adalah suatu bukti yang dapat dipercaya pada penerapan/pemenuhan CPOTB. Mutu yang direncanakan adalah satu-satunya solusi untuk mengatasi keluhan yang terkait dengan
DOKUMENTASI PENDAHULUAN Dokumentasi adalah suatu bukti yang dapat dipercaya pada penerapan/pemenuhan CPOTB. Mutu yang direncanakan adalah satu-satunya solusi untuk mengatasi keluhan yang terkait dengan
DOKUMENTASI DIREKTORAT INSPEKSI DAN SERTIFIKASI OBAT TRADISIONAL, KOSMETIK DAN PRODUK KOMPLEMEN BADAN PENGAWAS OBAT DAN MAKANAN 2017
 DOKUMENTASI DIREKTORAT INSPEKSI DAN SERTIFIKASI OBAT TRADISIONAL, KOSMETIK DAN PRODUK KOMPLEMEN BADAN PENGAWAS OBAT DAN MAKANAN 2017 SUBSISTEM MUTU Corrective And Preventive Actions (CAPA) Management Review
DOKUMENTASI DIREKTORAT INSPEKSI DAN SERTIFIKASI OBAT TRADISIONAL, KOSMETIK DAN PRODUK KOMPLEMEN BADAN PENGAWAS OBAT DAN MAKANAN 2017 SUBSISTEM MUTU Corrective And Preventive Actions (CAPA) Management Review
BAB I PENDAHULUAN. A. Latar Belakang. pilihan alternatif solusi kesehatan masyarakat. Oleh karena harga obat tradisional
 BAB I PENDAHULUAN A. Latar Belakang Dewasa ini, penggunaan obat tradisional dan obat yang berasal dari bahan alami semakin marak di masyarakat. Obat tradisional dan obat bahan alam menjadi pilihan alternatif
BAB I PENDAHULUAN A. Latar Belakang Dewasa ini, penggunaan obat tradisional dan obat yang berasal dari bahan alami semakin marak di masyarakat. Obat tradisional dan obat bahan alam menjadi pilihan alternatif
b. Sertifikat CPOB sesuai dengan bentuk sediaan yang diajukan
 CHECKLIST DOKUMEN PRA REGISTRASI OBAT BARU I. INFORMASI PRODUK Nama obat : Bentuk sediaan & kekuatan : Zat aktif : Kemasan : Pendaftar : Produsen : Kategori registrasi : II. DOKUMEN YANG DISERAHKAN A.
CHECKLIST DOKUMEN PRA REGISTRASI OBAT BARU I. INFORMASI PRODUK Nama obat : Bentuk sediaan & kekuatan : Zat aktif : Kemasan : Pendaftar : Produsen : Kategori registrasi : II. DOKUMEN YANG DISERAHKAN A.
BAB II TINJAUAN UMUM INDUSTRI FARMASI. (BUMN) dibentuk sebagai Perusahaan Perseroan pada tanggal 16 Agustus
 BAB II TINJAUAN UMUM INDUSTRI FARMASI 2.1 Tinjauan PT. Kimia Farma (Persero) Tbk. 2.1.1 Sejarah Perusahaan. PT. Kimia Farma (Persero) Tbk. sebagai Badan Usaha Milik Negara (BUMN) dibentuk sebagai Perusahaan
BAB II TINJAUAN UMUM INDUSTRI FARMASI 2.1 Tinjauan PT. Kimia Farma (Persero) Tbk. 2.1.1 Sejarah Perusahaan. PT. Kimia Farma (Persero) Tbk. sebagai Badan Usaha Milik Negara (BUMN) dibentuk sebagai Perusahaan
5.1.1 Kesimpulan Tugas Khusus Pengawasan Mutu - Kualitas air dan menjaga air dari kontaminasi mikrobiologi merupakan bagian penting untuk memastikan
 BAB V KESIMPULAN 5.1. Kesimpulan Kesimpulan yang dapat diambil dari hasil kegiatan Praktek Kerja Profesi Apoteker (PKPA) pada tanggal 03 April 2017 sampai 19 Mei 2017 di PT. OTTO Pharmaceutical Industries
BAB V KESIMPULAN 5.1. Kesimpulan Kesimpulan yang dapat diambil dari hasil kegiatan Praktek Kerja Profesi Apoteker (PKPA) pada tanggal 03 April 2017 sampai 19 Mei 2017 di PT. OTTO Pharmaceutical Industries
Produksi di Industri Farmasi
 Produksi di Industri Farmasi PRODUKSI istilah terkait Pembuatan Seluruh rangkaian kegiatan dalam menghasilkan suatu obat, meliputi produksi dan pengawasan mutu, mulai dari pengadaan bahan awal dan bahan
Produksi di Industri Farmasi PRODUKSI istilah terkait Pembuatan Seluruh rangkaian kegiatan dalam menghasilkan suatu obat, meliputi produksi dan pengawasan mutu, mulai dari pengadaan bahan awal dan bahan
BAB II TINJAUAN UMUM PT. COMBIPHAR. bawah pengelolaan Drs. Handoko Prayogo, Apt. Berawal dari industri rumah
 BAB II TINJAUAN UMUM PT. COMBIPHAR 2.1 Sejarah Perkembangan PT. Combiphar PT. Combiphar didirikan pada tahun 1971 di Jl. Sukabumi 61 Bandung, di bawah pengelolaan Drs. Handoko Prayogo, Apt. Berawal dari
BAB II TINJAUAN UMUM PT. COMBIPHAR 2.1 Sejarah Perkembangan PT. Combiphar PT. Combiphar didirikan pada tahun 1971 di Jl. Sukabumi 61 Bandung, di bawah pengelolaan Drs. Handoko Prayogo, Apt. Berawal dari
BAB II TINJAUAN UMUM INDUSTRI FARMASI. Belanda, pada tahun 1958 pemerintah melebur sejumlah perusahaan farmasi
 BAB II TINJAUAN UMUM INDUSTRI FARMASI 2.1 Sejarah PT. Kimia Farma (Persero) Tbk. Sejalan dengan kebijakan nasionalisasi bekas perusahaan-perusahaan Belanda, pada tahun 1958 pemerintah melebur sejumlah
BAB II TINJAUAN UMUM INDUSTRI FARMASI 2.1 Sejarah PT. Kimia Farma (Persero) Tbk. Sejalan dengan kebijakan nasionalisasi bekas perusahaan-perusahaan Belanda, pada tahun 1958 pemerintah melebur sejumlah
BAB II TINJAUAN PUSTAKA. Indonesia Nomor 245/Menkes/SK/V/1990 adalah industri obat jadi dan industri
 BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi Industri farmasi menurut Surat Keputusan Menteri Kesehatan Republik Indonesia Nomor 245/Menkes/SK/V/1990 adalah industri obat jadi dan industri bahan baku obat.
BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi Industri farmasi menurut Surat Keputusan Menteri Kesehatan Republik Indonesia Nomor 245/Menkes/SK/V/1990 adalah industri obat jadi dan industri bahan baku obat.
The Hazard Analysis and Critical Control Point System
 The Hazard Analysis and Critical Control Point System HACCP merupakan metode yang rasional & alamiah untuk penjaminan mutu makanan. Sistem ini terdiri atas identifikasi serta pengkajian yang sistematis
The Hazard Analysis and Critical Control Point System HACCP merupakan metode yang rasional & alamiah untuk penjaminan mutu makanan. Sistem ini terdiri atas identifikasi serta pengkajian yang sistematis
BAB III KEGIATAN DI INDUSTRI FARMASI P.T. KIMIA FARMA (PERSERO) TBK. PLANT MEDAN
 BAB III KEGIATAN DI INDUSTRI FARMASI P.T. KIMIA FARMA (PERSERO) TBK. PLANT MEDAN 3.1 Keterlibatan Dalam Produksi Praktek Kerja Profesi Apoteker di P.T. Kimia Farma (Persero) Tbk. Plant Medan, dilaksanakan
BAB III KEGIATAN DI INDUSTRI FARMASI P.T. KIMIA FARMA (PERSERO) TBK. PLANT MEDAN 3.1 Keterlibatan Dalam Produksi Praktek Kerja Profesi Apoteker di P.T. Kimia Farma (Persero) Tbk. Plant Medan, dilaksanakan
RANCANGAN PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR... TAHUN 2016 TENTANG PENGAWASAN SUPLEMEN KESEHATAN
 FILE EDIT 16 November 2016 Masukan dapat disampaikan kepada Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen melalui email mmi_stand_ot@yahoo.com, telp/fax 021-4241038 paling lambat
FILE EDIT 16 November 2016 Masukan dapat disampaikan kepada Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen melalui email mmi_stand_ot@yahoo.com, telp/fax 021-4241038 paling lambat
BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA
 BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 15 TAHUN 2016 TENTANG PERUBAHAN ATAS PERATURAN KEPALA BADAN PENGAWAS OBAT DAN
BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 15 TAHUN 2016 TENTANG PERUBAHAN ATAS PERATURAN KEPALA BADAN PENGAWAS OBAT DAN
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR HK TAHUN 2011 TENTANG PENDAFTARAN PANGAN OLAHAN
 PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.03.1.5.12.11.09955 TAHUN 2011 TENTANG PENDAFTARAN PANGAN OLAHAN DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN PENGAWAS OBAT DAN MAKANAN, Menimbang
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.03.1.5.12.11.09955 TAHUN 2011 TENTANG PENDAFTARAN PANGAN OLAHAN DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN PENGAWAS OBAT DAN MAKANAN, Menimbang
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR : HK TENTANG TATA LAKSANA PENDAFTARAN SUPLEMEN MAKANAN
 PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR : HK.00.05.41.1381 TENTANG TATA LAKSANA PENDAFTARAN SUPLEMEN MAKANAN DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN PENGAWAS OBAT DAN MAKANAN, Menimbang
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR : HK.00.05.41.1381 TENTANG TATA LAKSANA PENDAFTARAN SUPLEMEN MAKANAN DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN PENGAWAS OBAT DAN MAKANAN, Menimbang
Silakan tulis nama dan nim pada kertas satu lembar
 Silakan tulis nama dan nim pada kertas satu lembar Apa yg dimaksud dengan produk jadi, produk ½ jadi, produk ruahan, dan produk antara? Buatlah bagan produksi suatu obat secara umum! Produksi PRODUKSI
Silakan tulis nama dan nim pada kertas satu lembar Apa yg dimaksud dengan produk jadi, produk ½ jadi, produk ruahan, dan produk antara? Buatlah bagan produksi suatu obat secara umum! Produksi PRODUKSI
KEBIJAKAN PEMERINTAH DALAM MENDUKUNG PENGEMBANGAN PRODUK HERBAL BERBASIS RISET
 KEBIJAKAN PEMERINTAH DALAM MENDUKUNG PENGEMBANGAN PRODUK HERBAL BERBASIS RISET oleh : Dra. Kustantinah, Apt., M.App.Sc Kepala Badan POM RI Disampaikan Pada : Kuliah Umum Program Magister Herbal Universitas
KEBIJAKAN PEMERINTAH DALAM MENDUKUNG PENGEMBANGAN PRODUK HERBAL BERBASIS RISET oleh : Dra. Kustantinah, Apt., M.App.Sc Kepala Badan POM RI Disampaikan Pada : Kuliah Umum Program Magister Herbal Universitas
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR HK TAHUN 2011 TENTANG PENGAWASAN PEMASUKAN OBAT IMPOR
 PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.03.1.3.12.11.10692 TAHUN 2011 TENTANG PENGAWASAN PEMASUKAN OBAT IMPOR DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN PENGAWAS OBAT DAN MAKANAN,
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.03.1.3.12.11.10692 TAHUN 2011 TENTANG PENGAWASAN PEMASUKAN OBAT IMPOR DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN PENGAWAS OBAT DAN MAKANAN,
Pengawasan Mutu Obat di Instalasi Farmasi
 Pengawasan Mutu Obat di Instalasi Farmasi B a d a n P e n g a w a s Obat dan Makanan R a p a t K o o r d i n a s i N a s i o n a l, P r o g r a m K e f a r m a s i a n d a n A l a t K e s e h a t a n D
Pengawasan Mutu Obat di Instalasi Farmasi B a d a n P e n g a w a s Obat dan Makanan R a p a t K o o r d i n a s i N a s i o n a l, P r o g r a m K e f a r m a s i a n d a n A l a t K e s e h a t a n D
Lampiran 1. Bagan proses Pembuatan Krim / Salep
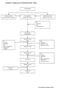 Lampiran 1. Bagan proses Pembuatan Krim / Salep Penimbangan Peleburan bahan Dasar krim (Fase minyak) Pencampuran Dengan ultra turrax Pelarutan zat aktif, Pengawet (Fase cair) -ph -Stabilitas krim Pencampuran
Lampiran 1. Bagan proses Pembuatan Krim / Salep Penimbangan Peleburan bahan Dasar krim (Fase minyak) Pencampuran Dengan ultra turrax Pelarutan zat aktif, Pengawet (Fase cair) -ph -Stabilitas krim Pencampuran
2. KETENTUAN UMUM Obat tradisional Bahan awal Bahan baku Simplisia
 1. PNGERTIAN CPOTB Cara Pembuatan Obat Tradisional yang Baik (CPOTB) meliputi seluruh aspek yang menyangkut pembuatan obat tradisional, Tujuan untuk menjamin agar produk yang dihasilkan senantiasa memenuhi
1. PNGERTIAN CPOTB Cara Pembuatan Obat Tradisional yang Baik (CPOTB) meliputi seluruh aspek yang menyangkut pembuatan obat tradisional, Tujuan untuk menjamin agar produk yang dihasilkan senantiasa memenuhi
KEPUTUSAN MENTERI KESEHATAN REPUBLIK INDONESIA NOMOR : 965/MENKES/SK/XI/1992 TENTANG
 KEPUTUSAN MENTERI KESEHATAN NOMOR : 965/MENKES/SK/XI/1992 TENTANG CARA PRODUKSI KOSMETIKA YANG BAIK MENTERI KESEHATAN, Menimbang : a. bahwa langkah utama untuk menjamin keamanan kosmetika adalah penerapan
KEPUTUSAN MENTERI KESEHATAN NOMOR : 965/MENKES/SK/XI/1992 TENTANG CARA PRODUKSI KOSMETIKA YANG BAIK MENTERI KESEHATAN, Menimbang : a. bahwa langkah utama untuk menjamin keamanan kosmetika adalah penerapan
LAPORAN PENGKAJIAN MUTU PRODUK (PMP) Halaman 1 dari 28
 Halaman 1 dari 28 Nama Sediaan :Amoxicillin 500 mg Bentuk Sediaan : Kaplet Jumlah Batch : 12 Jumlah Batch Disetujui : 12 Jumlah Batch Ditolak : - Ukuran Batch : 350,000 kaplet Kemasan : 10 strip @ 10 kaplet
Halaman 1 dari 28 Nama Sediaan :Amoxicillin 500 mg Bentuk Sediaan : Kaplet Jumlah Batch : 12 Jumlah Batch Disetujui : 12 Jumlah Batch Ditolak : - Ukuran Batch : 350,000 kaplet Kemasan : 10 strip @ 10 kaplet
DITOLAK BAGIAN PENGAWASAN MUTU PHARMACEUTICAL INDUSTRIES MEDAN
 Lampiran 15. Etiket PT. UNIVERSAL PHARMACEUTICAL INDUSTRIES MEDAN Nama Produk/Bahan No. Batch/Lot Pabrik Pemasok No. Penerimaan Barang Jumlah No. Sertifikat Analisis Tanda Tangan DITOLAK BAGIAN PENGAWASAN
Lampiran 15. Etiket PT. UNIVERSAL PHARMACEUTICAL INDUSTRIES MEDAN Nama Produk/Bahan No. Batch/Lot Pabrik Pemasok No. Penerimaan Barang Jumlah No. Sertifikat Analisis Tanda Tangan DITOLAK BAGIAN PENGAWASAN
BAB II TINJAUAN PUSTAKA. Industri Farmasi menurut Peraturan Menteri Kesehatan RI Nomor
 BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi 2.1.1 Pengertian Industri Farmasi Industri Farmasi menurut Peraturan Menteri Kesehatan RI Nomor 1799/Menkes/Per/XII/2010 adalah badan usaha yang memiliki izin
BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi 2.1.1 Pengertian Industri Farmasi Industri Farmasi menurut Peraturan Menteri Kesehatan RI Nomor 1799/Menkes/Per/XII/2010 adalah badan usaha yang memiliki izin
BAB II TINJAUAN PUSTAKA. Gudang merupakan sarana pendukung kegiatan produksi industri farmasi
 BAB II TINJAUAN PUSTAKA 2.1 Definisi Gudang merupakan sarana pendukung kegiatan produksi industri farmasi yang berfungsi untuk menyimpan bahan baku, bahan kemas dan obat jadi yang belum didistribusikan.
BAB II TINJAUAN PUSTAKA 2.1 Definisi Gudang merupakan sarana pendukung kegiatan produksi industri farmasi yang berfungsi untuk menyimpan bahan baku, bahan kemas dan obat jadi yang belum didistribusikan.
Lampiran 1. Bagan Proses Pembuatan Tablet
 Lampiran 1. Bagan Proses Pembuatan Tablet Penimbangan Pencampuran Granulasi Basah Oven, suhu 60 o C LOD Granulasi Kering Lubrikasi Kadar Zat Berkhasiat LOD Pemerian Pemerian Friabilitas Keseragaman Bobot
Lampiran 1. Bagan Proses Pembuatan Tablet Penimbangan Pencampuran Granulasi Basah Oven, suhu 60 o C LOD Granulasi Kering Lubrikasi Kadar Zat Berkhasiat LOD Pemerian Pemerian Friabilitas Keseragaman Bobot
BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA
 BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 5 TAHUN 2016 TENTANG PENARIKAN DAN PEMUSNAHAN OBAT TRADISIONAL YANG TIDAK MEMENUHI
BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 5 TAHUN 2016 TENTANG PENARIKAN DAN PEMUSNAHAN OBAT TRADISIONAL YANG TIDAK MEMENUHI
Setelah proses Login berhasil, pendaftar akan masuk pada halaman awal Aplikasi e-registrasi Obat.
 PETUNJUK TEKNIS REGISTRASI ULANG APLIKASI e REGISTRASI OBAT (AeRO) aero.pom.go.id Alur Pengajuan Registrasi Ulang Obat Copy =============================== Memulai Proses Registrasi Ulang Obat Copy Pengajuan
PETUNJUK TEKNIS REGISTRASI ULANG APLIKASI e REGISTRASI OBAT (AeRO) aero.pom.go.id Alur Pengajuan Registrasi Ulang Obat Copy =============================== Memulai Proses Registrasi Ulang Obat Copy Pengajuan
IOT adalah industri yang memproduksi obat traditional dengan total asset diatas Rp ,- (enam ratus juta rupiah), tidak termasuk harga tanah
 CPOTB CPOB vs CPOTB Ruang Lingkup CPOB : Industri farmasi yang memproduksi Obat dan Bahan Baku Obat; lembaga lain yg memproduksi sediaan radiofarmaka; Instalasi farmasi RS yang melakukan proses pembuatan
CPOTB CPOB vs CPOTB Ruang Lingkup CPOB : Industri farmasi yang memproduksi Obat dan Bahan Baku Obat; lembaga lain yg memproduksi sediaan radiofarmaka; Instalasi farmasi RS yang melakukan proses pembuatan
UMUR SIMPAN. 31 October
 UMUR SIMPAN 31 October 2014 1 Outline 1. Pendahuluan 2. Umur Simpan 3. Penentuan Umur Simpan 4. Penutup 31 October 2014 2 Pendahuluan Makanan dan minuman disimpan, holding time mutu menurun. Produk minuman
UMUR SIMPAN 31 October 2014 1 Outline 1. Pendahuluan 2. Umur Simpan 3. Penentuan Umur Simpan 4. Penutup 31 October 2014 2 Pendahuluan Makanan dan minuman disimpan, holding time mutu menurun. Produk minuman
PERSONALIA
 PERSONALIA 1. Persyaratan Umum Jumlah dan Pengetahuan: Memiliki pengetahuan, keterampilan dan kemampuan sesuai dengan tugasnya. Mempunyai sikap dan kesadaran yang tinggi untuk melaksanakan Cara Pembuatan
PERSONALIA 1. Persyaratan Umum Jumlah dan Pengetahuan: Memiliki pengetahuan, keterampilan dan kemampuan sesuai dengan tugasnya. Mempunyai sikap dan kesadaran yang tinggi untuk melaksanakan Cara Pembuatan
GOOD LABORATORY PRACTICE (PRAKTEK LABORATORIUM YANG BENAR) Hasil pemeriksaan laboratorium digunakan untuk :
 GOOD LABORATORY PRACTICE (PRAKTEK LABORATORIUM YANG BENAR) Pelayanan laboratorium merupakan bagian integral dari pelayanan kesehatan yang diperlukan untuk menunjang upaya peningkatan kesehatan, pencegahan
GOOD LABORATORY PRACTICE (PRAKTEK LABORATORIUM YANG BENAR) Pelayanan laboratorium merupakan bagian integral dari pelayanan kesehatan yang diperlukan untuk menunjang upaya peningkatan kesehatan, pencegahan
BAB II TINJAUAN PUSTAKA. Industri farmasi adalah industri obat jadi dan industri bahan baku obat.
 BAB II TINJAUAN PUSTAKA A. Industri Farmasi Industri farmasi adalah industri obat jadi dan industri bahan baku obat. Industri farmasi sebagai industri penghasil obat, dituntut untuk dapat menghasilkan
BAB II TINJAUAN PUSTAKA A. Industri Farmasi Industri farmasi adalah industri obat jadi dan industri bahan baku obat. Industri farmasi sebagai industri penghasil obat, dituntut untuk dapat menghasilkan
BAB II TINJAUAN UMUM INDUSTRI. 1799/Menkes/Per/XII/2010 adalah badan usaha yang memiliki izin dari menteri
 BAB II TINJAUAN UMUM INDUSTRI 2.1 Industri Farmasi 2.1.1 Pengertian Industri Farmasi Industri Farmasi menurut Peraturan Menteri Kesehatan RI Nomor 1799/Menkes/Per/XII/2010 adalah badan usaha yang memiliki
BAB II TINJAUAN UMUM INDUSTRI 2.1 Industri Farmasi 2.1.1 Pengertian Industri Farmasi Industri Farmasi menurut Peraturan Menteri Kesehatan RI Nomor 1799/Menkes/Per/XII/2010 adalah badan usaha yang memiliki
BAB II TINJAUAN PUSTAKA. Berdasarkan Surat Keputusan Menteri Kesehatan Republik Indonesia No.
 BAB II TINJAUAN PUSTAKA 2.1 Pengertian Industri Farmasi Berdasarkan Surat Keputusan Menteri Kesehatan Republik Indonesia No. 245/Menkes/SK/V/1990, yang dimaksud dengan industri farmasi adalah industri
BAB II TINJAUAN PUSTAKA 2.1 Pengertian Industri Farmasi Berdasarkan Surat Keputusan Menteri Kesehatan Republik Indonesia No. 245/Menkes/SK/V/1990, yang dimaksud dengan industri farmasi adalah industri
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 12 TAHUN 2016 TENTANG PENDAFTARAN PANGAN OLAHAN
 BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 12 TAHUN 2016 TENTANG PENDAFTARAN PANGAN OLAHAN DENGAN RAHMAT TUHAN YANG MAHA
BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 12 TAHUN 2016 TENTANG PENDAFTARAN PANGAN OLAHAN DENGAN RAHMAT TUHAN YANG MAHA
BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA
 PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR 14 TAHUN 2015 TENTANG PENERAPAN PROGRAM MANAJEMEN RISIKO KEAMANAN PANGAN DI INDUSTRI FORMULA BAYI, FORMULA LANJUTAN, DAN FORMULA PERTUMBUHAN DENGAN
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR 14 TAHUN 2015 TENTANG PENERAPAN PROGRAM MANAJEMEN RISIKO KEAMANAN PANGAN DI INDUSTRI FORMULA BAYI, FORMULA LANJUTAN, DAN FORMULA PERTUMBUHAN DENGAN
PERSYARATAN ISO 9001 REVISI 2008 HANYA DIGUNAKAN UNTUK PELATIHAN
 PERSYARATAN ISO 9001 REVISI 2008 HANYA DIGUNAKAN UNTUK PELATIHAN 4. Sistem Manajemen Mutu (=SMM) 4.1 Persyaratan Umum Organisasi harus menetapkan, mendokumentasikan, menerapkan dan memelihara suatu SMM
PERSYARATAN ISO 9001 REVISI 2008 HANYA DIGUNAKAN UNTUK PELATIHAN 4. Sistem Manajemen Mutu (=SMM) 4.1 Persyaratan Umum Organisasi harus menetapkan, mendokumentasikan, menerapkan dan memelihara suatu SMM
BAB II TINJAUAN UMUM. Industri farmasi menurut Surat Keputusan Menteri Kesehatan Republik
 BAB II TINJAUAN UMUM 2.1 Industri Farmasi Industri farmasi menurut Surat Keputusan Menteri Kesehatan Republik Indonesia Nomor 245/Menkes/SK/V/1990 adalah industri obat jadi dan industri bahan baku obat.
BAB II TINJAUAN UMUM 2.1 Industri Farmasi Industri farmasi menurut Surat Keputusan Menteri Kesehatan Republik Indonesia Nomor 245/Menkes/SK/V/1990 adalah industri obat jadi dan industri bahan baku obat.
ABSTRAK. Keywords: pemastian mutu, CPOB produksi, in-process control
 ABSTRAK Pemastian Mutu adalah totalitas semua pengaturan yang dibuat dengan tujuan untuk memastikan bahwa obat dihasilkan dengan mutu yang sesuai dengan tujuan pemakaiannya. Pemastian Mutu mencakup Cara
ABSTRAK Pemastian Mutu adalah totalitas semua pengaturan yang dibuat dengan tujuan untuk memastikan bahwa obat dihasilkan dengan mutu yang sesuai dengan tujuan pemakaiannya. Pemastian Mutu mencakup Cara
Dra. Togi J. Hutadjulu, Apt., MHA Direktur Penilaian Obat dan Produk Biologi Badan Pengawas Obat dan Makanan
 Kriteria dan Tata Laksana Registrasi Obat & Implementasi Sistem Registrasi Online dalam Mendukung Akses & Ketersediaan Obat yang Aman, Berkhasiat dan Bermutu Dra. Togi J. Hutadjulu, Apt., MHA Direktur
Kriteria dan Tata Laksana Registrasi Obat & Implementasi Sistem Registrasi Online dalam Mendukung Akses & Ketersediaan Obat yang Aman, Berkhasiat dan Bermutu Dra. Togi J. Hutadjulu, Apt., MHA Direktur
Wimbuh Dumadi,S.Si.M.H.,Apt Ketua Pengurus Daerah IAI DIY. Yogyakarta, 14 April 2018
 Wimbuh Dumadi,S.Si.M.H.,Apt Ketua Pengurus Daerah IAI DIY Yogyakarta, 14 April 2018 1 2 Pendahuluan Sistem Regulasi 3 Peran Apoteker Dalam menjamin kualitas Obat 4 Peran Apoteker Dalam Keamanan Obat 5
Wimbuh Dumadi,S.Si.M.H.,Apt Ketua Pengurus Daerah IAI DIY Yogyakarta, 14 April 2018 1 2 Pendahuluan Sistem Regulasi 3 Peran Apoteker Dalam menjamin kualitas Obat 4 Peran Apoteker Dalam Keamanan Obat 5
Quality Management System
 Quality Management System Mutu (Quality)? The degree to which a set of inherent properties of a product, system or process fulfils requirements. (ICH Q9) Industri farmasi harus membuat obat sedemikian
Quality Management System Mutu (Quality)? The degree to which a set of inherent properties of a product, system or process fulfils requirements. (ICH Q9) Industri farmasi harus membuat obat sedemikian
BAB II GAMBARAN UMUM PERUSAHAAN
 BAB II GAMBARAN UMUM PERUSAHAAN 1.1. Sejarah dan Perkembangan Perusahaan. Bintang Toedjoe didirikan pada tanggal 29 April 1946 bertempat di Garut, Jawa Barat oleh seorang sinshe yang bernama Tan Jun Sie.
BAB II GAMBARAN UMUM PERUSAHAAN 1.1. Sejarah dan Perkembangan Perusahaan. Bintang Toedjoe didirikan pada tanggal 29 April 1946 bertempat di Garut, Jawa Barat oleh seorang sinshe yang bernama Tan Jun Sie.
Industri farmasi menurut Surat Keputusan Menteri Kesehatan Nomor. 245/Menkes/V/1990 adalah industri obat jadi dan industri bahan baku obat.
 BAB II TINJAUAN PUSTAKA 2.1. Pengertian Industri Farmasi. Industri farmasi menurut Surat Keputusan Menteri Kesehatan Nomor. 245/Menkes/V/1990 adalah industri obat jadi dan industri bahan baku obat. Industri
BAB II TINJAUAN PUSTAKA 2.1. Pengertian Industri Farmasi. Industri farmasi menurut Surat Keputusan Menteri Kesehatan Nomor. 245/Menkes/V/1990 adalah industri obat jadi dan industri bahan baku obat. Industri
BAB 1 PENDAHULUAN 1.1. Latar belakang penelitian
 BAB 1 PENDAHULUAN 1.1. Latar belakang penelitian Indonesia merupakan salah satu negara tropis yang kaya akan sumber daya alamnya, sehingga menjadi negara yang sangat potensial dalam bahan baku obat, karena
BAB 1 PENDAHULUAN 1.1. Latar belakang penelitian Indonesia merupakan salah satu negara tropis yang kaya akan sumber daya alamnya, sehingga menjadi negara yang sangat potensial dalam bahan baku obat, karena
MODUL MATERI UJIAN PERPINDAHAN JABATAN FUNGSIONAL PENGAWAS FARMASI DAN MAKANAN TERAMPIL KE AHLI PEGAWAI NEGERI SIPIL (PNS) BADAN POM RI
 MODUL MATERI UJIAN PERPINDAHAN JABATAN FUNGSIONAL PENGAWAS FARMASI DAN MAKANAN TERAMPIL KE AHLI PEGAWAI NEGERI SIPIL (PNS) BADAN POM RI MATA PELAJARAN : KONSEP DASAR PENGAWASAN BADAN PENGAWAS OBAT DAN
MODUL MATERI UJIAN PERPINDAHAN JABATAN FUNGSIONAL PENGAWAS FARMASI DAN MAKANAN TERAMPIL KE AHLI PEGAWAI NEGERI SIPIL (PNS) BADAN POM RI MATA PELAJARAN : KONSEP DASAR PENGAWASAN BADAN PENGAWAS OBAT DAN
Perizinan BPOM (Badan Pengawasan Obat dan Makanan)
 Perizinan BPOM (Badan Pengawasan Obat dan Makanan) Sistem Pengawasan Obat dan Makanan (SisPOM) yang efektif dan efisien yang mampu mendeteksi, mencegah dan mengawasi produk-produk dengan tujuan melindungi
Perizinan BPOM (Badan Pengawasan Obat dan Makanan) Sistem Pengawasan Obat dan Makanan (SisPOM) yang efektif dan efisien yang mampu mendeteksi, mencegah dan mengawasi produk-produk dengan tujuan melindungi
MENTERI KESEHATAN REPUBLIK INDONESIA
 KEPUTUSAN MENTERI KESEHATAN NOMOR: 659/MENKES/SK/X/1991 TENTANG CARA PEMBUATAN OBAT TRADISIONAL YANG BAIK MENTERI KESEHATAN Menimbang : a. bahwa untuk membuat obat tradisional yang memenuhi persyaratan
KEPUTUSAN MENTERI KESEHATAN NOMOR: 659/MENKES/SK/X/1991 TENTANG CARA PEMBUATAN OBAT TRADISIONAL YANG BAIK MENTERI KESEHATAN Menimbang : a. bahwa untuk membuat obat tradisional yang memenuhi persyaratan
BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA
 BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA KEPUTUSAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR HK.04.1.23.09.10.9269 TAHUN 2010 TENTANG PEDOMAN TINDAK LANJUT HASIL PENGAWASAN
BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA KEPUTUSAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR HK.04.1.23.09.10.9269 TAHUN 2010 TENTANG PEDOMAN TINDAK LANJUT HASIL PENGAWASAN
BAB II TINJAUAN PUSTAKA
 BAB II TINJAUAN PUSTAKA 2.1. Pengertian Industri Farmasi Berdasarkan Surat Keputusan Menteri Kesehatan Republik Indonesia No.245 /Menkes/VI/1990, industri farmasi adalah industri obat jadi dan industri
BAB II TINJAUAN PUSTAKA 2.1. Pengertian Industri Farmasi Berdasarkan Surat Keputusan Menteri Kesehatan Republik Indonesia No.245 /Menkes/VI/1990, industri farmasi adalah industri obat jadi dan industri
BAB I PENDAHULUAN Latar Belakang Masalah. Saat ini sektor industri mempunyai peran yang sangat penting di dalam
 BAB I PENDAHULUAN 1.1 Latar Belakang Masalah Saat ini sektor industri mempunyai peran yang sangat penting di dalam pembangunan perekonomian Indonesia di mana sektor industri ini merupakan prioritas untuk
BAB I PENDAHULUAN 1.1 Latar Belakang Masalah Saat ini sektor industri mempunyai peran yang sangat penting di dalam pembangunan perekonomian Indonesia di mana sektor industri ini merupakan prioritas untuk
PERATURAN OBAT ASLI INDONESIA
 PERATURAN OBAT ASLI INDONESIA A. Obat Asli Indonesia Obat tradisional adalah obat yang berasal dari bahan baku alam yang dikeringkan yang dibuat secara turun temurun yang biasanya dikemas dalam wadah yang
PERATURAN OBAT ASLI INDONESIA A. Obat Asli Indonesia Obat tradisional adalah obat yang berasal dari bahan baku alam yang dikeringkan yang dibuat secara turun temurun yang biasanya dikemas dalam wadah yang
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR HK.03.1.23.12.10.12123 TAHUN 2010 TENTANG PEDOMAN DOKUMEN INFORMASI PRODUK
 PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.03.1.23.12.10.12123 TAHUN 2010 TENTANG PEDOMAN DOKUMEN INFORMASI PRODUK DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN PENGAWAS OBAT DAN MAKANAN,
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.03.1.23.12.10.12123 TAHUN 2010 TENTANG PEDOMAN DOKUMEN INFORMASI PRODUK DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN PENGAWAS OBAT DAN MAKANAN,
