CHECKLIST DOKUMEN REGISTRASI OBAT COPY
|
|
|
- Susanti Oesman
- 6 tahun lalu
- Tontonan:
Transkripsi
1 CHECKLIST DOKUMEN REGISTRASI OBAT COPY I. INFORMASI PRODUK Nama Obat : Bentuk sediaan & Kekuatan : Zat aktif : Kemasan : Pendaftar : Produsen : Kategori registrasi : II. DOKUMEN YANG DISERAHKAN No. Parameter A. KELENGKAPAN DOKUMEN ADMINISTRATIF 1. Surat pengantar 2. Formulir registrasi 3. Surat penyataan pendaftar 4. Sertifikat dan dokumen administratif (sesuai dengan status produksi: obat produksi lokal, kontrak, lisensi, khusus ekspor atau impor) Obat produksi lokal a. Ijin industri farmasi pendaftar b. Sertifikat CPOB sesuai dengan bentuk sediaan yang diajukan Obat kontrak a. Ijin industri farmasi pendaftar/pemberi kontrak b. Ijin industri farmasi penerima kontrak c. Perjanjian kontrak d. Sertifikat CPOB industri farmasi pendaftar/pemberi kontrak e. Sertifikat CPOB industri farmasi penerima kontrak sesuai dengan bentuk sediaan yang diajukan f. Untuk obat kontrak dengan sumber bahan baku, spesifikasi, formula, proses dan tempat produksi obat serta jenis dan spesifikasi kemasan sama dengan obat yang dimiliki oleh penerima kontrak harus dilengkapi dengan surat pernyataan bermaterai yang ditandatangani pemberi dan penerima kontrak Obat lisensi a. Ijin industri farmasi penerima lisensi b. Sertifikat CPOB industri farmasi penerima lisensi sesuai dengan bentuk sediaan yang diajukan Check List Registrasi Obat Copy Pebruari dari 8
2 No. Parameter c. Perjanjian lisensi Obat khusus ekspor a. Ijin industri farmasi pendaftar b. Sertifikat CPOB sesuai dengan bentuk sediaan yang diajukan c. Persetujuan tertulis dari negara tujuan yang disahkan oleh institusi berwenang di negara tujuan ekspor untuk obat yang tidak diijinkan beredar di Indonesia d. Proforma invoice untuk obat yang tidak beredar di Indonesia Obat impor a. Ijin industri farmasi pendaftar b. Surat penunjukan dari industri farmasi atau pemilik obat di luar negeri (LoA) c. Certificate of Pharmaceutical Product terbaru dari negara produsen dan/atau negara dimana diterbitkan sertifikat pelulusan bets d. Site master file industri farmasi di luar negeri, untuk produsen yang belum mempunyai obat dengan persyaratan sama yang disetujui beredar di Indonesia e. Sertifikat CPOB dari produsen di luar negeri (kecuali sudah tercakup dalam dokumen lain) f. Inspeksi terakhir oleh institusi yang berwenang terhadap industri farmasi yang terlibat dalam produksi obat jadi 5. Salinan Hasil Pra Registrasi (HPR) 6. Bukti pembayaran 7. Dokumen Terkait Paten a. Surat Pernyataan Terkait Paten b. Hasil Penelusuran Paten dari Ditjen HKI c. Pengkajian terkait Paten (Self Assessment) 8. Dokumen Lain B. KELENGKAPAN INFORMASI OBAT DAN DESAIN 1 Informasi Obat a. Ringkasan karakteristik obat 2. b. Brosur c. Informasi obat untuk pasien Penandaan pada kemasan a. Penandaan bungkus luar b. Etiket c. Blister/ strips d. Ampul / vial FORM CLR02 Check List Registrasi Obat Copy Pebruari dari 8
3 No. Parameter e. Catch cover/ amplop f. Mock up C. KELENGKAPAN DOKUMEN MUTU S. Zat Aktif S1 Informasi Umum S1.1 Tata Nama - International non proprietary name (INN) - Nama farmakope - Nomor registrasi dari Chemical Abstract Service (CAS) - Kode laboratorium (jika ada) - Nama kimia S1.3 Sifat-sifat umum - Sifat-sifat fisikokimia atau sifat-sifat lain yang relevan dari zat aktif termasuk aktifitas biologik untuk Bioteknologi S2 S4 Proses Produksi dan Sumber Zat Aktif S2.1 Produsen Nama dan alamat lengkap termasuk kota dan negara produsen zat aktif Kontrol terhadap Zat Aktif S4.1 Spesifikasi Informasi rinci spesifikasi, pengujian, dan kriteria penerimaan zat aktif (sesuai Farmakope). S4.2 Prosedur analisa Prosedur analisa yang digunakan untuk pengujian zat aktif harus rinci. S5 Baku Pembanding Informasi baku pembanding atau bahan baku yang digunakan untuk pengujian zat aktif. CoA/Informasi baku pembanding primer (USPRS, EPCRS, BPFI, ASEANRS, BPCRS, Sigma Aldrich, EDQOM) CoA baku kerja untuk anallisa obat rutin dan trial dengan mencantumkan informasi baku pembanding primer yang digunakan untuk membakukan baku kerja tersebut. Prosedur penetapan dan penanganan baku kerja Dokumen Mutu Lain 1. Certificate of Suitability (Ph.Eur) jika diperlukan 2. Untuk zat aktif bentuk liofilisasi (bulk) : - komposisi zat aktif 3. Untuk zat aktif berupa pellet : - formula Check List Registrasi Obat Copy Pebruari dari 8
4 No. Parameter 4. Hasil pemeriksaan zat aktif - spesifikasi kemasan primer P. Obat P1 Deskripsi dan Komposisi Uraian dan komposisi obat jadi harus dicantumkan, seperti: - Bentuk sediaan; - Komposisi lengkap, jumlah masing-masing zat dalam satu bets produksi (termasuk overage, bila ada), fungsi masingmasing zat dan acuan yang digunakan (contoh : monografi farmakope atau spesifikasi dari produsen); - Uraian cara rekonstitusi; dan - Tipe kemasan yang digunakan dan pelarut rekonstitusi (jika ada). P2 P3 Pengembangan farmasetika P2.2 Komponen Obat Jadi P2.4 Pengembangan Proses Pembuatan Pemilihan dan optimalisasi proses pembuatan yang tercantum dalam butir P 3.2 terutama pada tahap kritis harus dijelaskan. Metoda sterilisasi yang relevan harus dijelaskan. P2.7 Kompatibilitas Kompatibilitas antara zat aktif dan zat tambahan atau dengan pelarut untuk rekonstitusi atau dengan kemasan atau dengan alat bantu khusus, harus dicantumkan untuk menunjang informasi yang sesuai pada penandaan. Proses Produksi P3.1 Formula Bets Formula harus mencantumkan nama dan jumlah semua zat aktif dan zat tambahan yang digunakan termasuk zat yang hilang selama proses pembuatan P3.2 Proses Produksi dan Kontrol Proses - Diagram alur proses pembuatan harus dicantumkan tahap demi tahap. - Tahapan kritis pada proses control, uji intermediate atau control obat jadi harus diidentifikasi (dari tahap penimbangan sampai dengan pengemasan akhir termasuk IPC lengkap dengan parameter uji) Check List Registrasi Obat Copy Pebruari dari 8
5 No. Parameter P3.3 Kontrol terhadap Tahapan Kritis dan Produk Antara - Tahapan kritis Pengujian dan kriteria penerimaan (dengan justifikasi termasuk data percobaan) yang dilakukan pada tahapan kritis proses pembuatan seperti pada bagian P3.3, untuk meyakinkan bahwa proses tersebut terkontrol. - Produk Antara Informasi mutu dan control intermediates yang diperoleh selama proses P3.4 Validasi Proses dan/atau Laporan Uraian, dokumentasi, dan hasil studi validasi dari tahapan kritis atau assays kritis yang dilakukan pada proses pembuatan harus diserahkan (Contoh : validasi proses sterilisasi atau proses aseptik atau pengisian). Protokol dan Laporan Validasi Proses (3 bets pertama skala produksi), lengkap dengan informasi : - No bets - besar bets + skala produksi/skala pilot - kualifikasi ruangan - kualifikasi + kapasitas alat (gambar jika ada) - kecepatan dan lama pengadukan - titik sampling Komitmen Validasi Proses Jika laporan validasi proses 3 bets pertama skala produksi belum tersedia : - Laporan validasi proses minimum 1 skala pilot - Komitmen Validasi proses : Surat pernyataan sebagai komitmen menyerahkan laporan validasi proses 3 bets pertama skala produksi beserta prediksi waktu penyerahan laporan validasi tersebut dengan tembusan kepada Direktorat Pengawasan Produksi PT dan PKRT - Obat impor : Laporan validasi proses harus menggunakan 3 bets skala produksi Obat Steril Metode Sterilisasi Akhir dengan Autoklaf Suhu & Waktu Jika suhu & waktu sterilisasi selain kondisi 121ºC, menit : - Perhitungan Fo - Alasan & justifikasi Validasi autoklaf Check List Registrasi Obat Copy Pebruari dari 8
6 No. Parameter Metoda Aseptis Jumlah dan ukuran filter Uji ketegaran membran filter Laporan validasi media fill 3 bets (minimal 3000 vial/bets) P4 Kontrol terhadap Zat Tambahan P4.1 Spesifikasi - Spesifikasi zat tambahan yang digunakan. - CoA (sumber, tgl produksi, tgl kadaluarsa) P4.2 Prosedur analisa Prosedur analisa yang digunakan pada pengujian zat tambahan. P5 1. Zat tambahan bersumber hewan : - Sertifikat Halal (jika ada) - Sertifikat Bebas BSE/TSE 2. Untuk bentuk sediaan kapsul : - CoA Kapsul - Sertifikat Halal (jika ada) - Sertifikat Bebas BSE/TSE 3. Zat warna (Colour Index), jika ada Kontrol terhadap Obat P5.1 Spesifikasi Spesifikasi obat P5.2 Prosedur analisa Prosedur analisa yang digunakan untuk pengujian obat dan pustaka acuan (sesuai spesifikasi obat), misal : - identifikasi - pemerian - kadar - disolusi (bila dipersyaratkan) - waktu hancur, - kerenyahan, - kekerasan - berat jenis, - viskositas, dll Check List Registrasi Obat Copy Pebruari dari 8
7 No. Parameter P5.3 Validasi Prosedur Analisa Informasi validasi metode analisa untuk prosedur analisa yang digunakan pada pengujian obat a. Metoda Analisa (MA) : - obat jadi - pustaka acuan b. Metode kompendial : Protokol dan laporan verifikasi MA (akurasi, presisi, linearitas) c. Metode non kompendial Protokol dan laporan validasi MA (selektivitas/spesifisitas, akurasi, presisi, LOD, LOQ, linearitas, sistem suitabilitas, ruggedness, robustness) d. Laporan validasi kesesuaian metoda analisa dengan metoda kompendial (jika perlu) e. Rekaman hasil analisa (untuk tiap parameter) P5.4 Analisis Bets Uraian analisa dan hasil analisa bets (termasuk Certificate of Analysis obat) CoA obat jadi (no bets sesuai bets untuk uji stabilitas) Bentuk konvensional min 2 bets; Bentuk non konvensional 3 bets (misal : tablet lepas lambat, liofilisasi) Mencantumkan informasi : - no bets. - besar bets & skala pilot/ produksi - nama produsen (jika toll manufacturing), - kemasan primer - tgl produksi - tgl kadaluarsa - tgl dan tandatangan Penanggung Jawab Mutu P6 Baku pembanding Informasi baku pembanding atau bahan baku yang digunakan untuk pengujian obat. CoA/Informasi baku pembanding primer (USPRS, EPCRS, BPFI, ASEANRS, BPCRS, Sigma Aldrich, EDQOM) P7 Kemasan (blister, strip, ampul/vial, tube, botol plastik/gelas, dus, etiket, brosur, catch cover, amplop, sendok takar/dropper) 1. Spesifikasi (bahan/tipe gelas/lapisan dan ketebalan, ukuran, warna, gambar (jika ada) sesuai kemasan obat jadi) 2. Metoda Pemeriksaan Kemasan primer & sekunder 3. Uji Kebocoran kemasan primer 4. Kalibrasi dropper / spray / inhaler Check List Registrasi Obat Copy Pebruari dari 8
8 No. Parameter P8 Uji Stabilitas (nomor bets sama dengan nomor bets CoA Obat, kecuali obat impor) 1. Bentuk konvensional min 2 bets; 2. Bentuk non konvensional 3 bets (misal : tablet lepas lambat, liofilisasi) 3. Format Laporan mengacu pada ASEAN GUIDELINE ON STABILITY STUDY OF DRUG PRODUCT 4. Protokol & Laporan Stabilitas dengan informasi : - nama obat - formula obat - besar bets - kondisi penyimpanan Dipercepat/SuhuRH/bulan ke Jangka panjang/suhu/rh/bulan ke 0,3,6,9,12,18,24 dst - jadwal pengujian - jumlah sampel yang digunakan - spesifikasi obat - jenis kemasan primer - tempat produksi obat P9 5. Jika data uji stabilitas jangka panjang yang tersedia belum sesuai dengan shelf life yang diajukan : Surat Penyataan bermaterai untuk menyerahkan data Uji Stabilitas jangka panjang sampai shelf life yang diajukan. Catatan : hanya untuk obat lokal 6. Shelf life yg diajukan 7. Laporan In Use Stability (setelah rekonstitusi, setelah kemasan dibuka), 8. Jika kondisi pengujian stabilitas tidak sesuai dengan kondisi yang dipersyaratkan untuk Indonesia : Surat Pernyataan bermaterai untuk melakukan dan melaporkan data uji stabilitas paska pemasaran Bukti Ekivalensi (jika dipersyaratkan) 1. In vitro Studi disolusi terbanding - Protokol dan laporan uji disolusi terbanding pada 3 ph dibandingkan terhadap innovator - Perhitungan f2 - Profil Disolusi - Kesimpulan 2. In vivo Studi Bioekivalensi : - Laporan Uji BE - Informasi obat pembanding yang digunakan Check List Registrasi Obat Copy Pebruari dari 8
b. Sertifikat CPOB sesuai dengan bentuk sediaan yang diajukan
 CHECKLIST DOKUMEN PRA REGISTRASI OBAT BARU I. INFORMASI PRODUK Nama obat : Bentuk sediaan & kekuatan : Zat aktif : Kemasan : Pendaftar : Produsen : Kategori registrasi : II. DOKUMEN YANG DISERAHKAN A.
CHECKLIST DOKUMEN PRA REGISTRASI OBAT BARU I. INFORMASI PRODUK Nama obat : Bentuk sediaan & kekuatan : Zat aktif : Kemasan : Pendaftar : Produsen : Kategori registrasi : II. DOKUMEN YANG DISERAHKAN A.
CHECK LIST DOKUMEN REGISTRASI OBAT BARU
 CHECK LIST DOKUMEN REGISTRASI OBAT BARU I. INFORMASI PRODUK Nama Obat : Bentuk sediaan & Kekuatan : Zat aktif : Kemasan : Pendaftar : Produsen : Kategori registrasi : II. DOKUMEN YANG DISERAHKAN No. Parameter
CHECK LIST DOKUMEN REGISTRASI OBAT BARU I. INFORMASI PRODUK Nama Obat : Bentuk sediaan & Kekuatan : Zat aktif : Kemasan : Pendaftar : Produsen : Kategori registrasi : II. DOKUMEN YANG DISERAHKAN No. Parameter
PETUNJUK TEKNIS PRA-REGISTRASI APLIKASI e REGISTRASI OBAT (AeRO) aero.pom.go.id. Login. Alur Pengajuan Pra Registrasi Obat Copy
 PETUNJUK TEKNIS PRA-REGISTRASI APLIKASI e REGISTRASI OBAT (AeRO) aero.pom.go.id 2 Alur Pengajuan Pra Registrasi Obat Copy Login Mengisi form pengajuan pra registrasi baru obat copy Mendapat SPB + pembayaran
PETUNJUK TEKNIS PRA-REGISTRASI APLIKASI e REGISTRASI OBAT (AeRO) aero.pom.go.id 2 Alur Pengajuan Pra Registrasi Obat Copy Login Mengisi form pengajuan pra registrasi baru obat copy Mendapat SPB + pembayaran
BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA
 BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 17 TAHUN 2016 TENTANG PERUBAHAN KEDUA ATAS PERATURAN KEPALA BADAN PENGAWAS OBAT
BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 17 TAHUN 2016 TENTANG PERUBAHAN KEDUA ATAS PERATURAN KEPALA BADAN PENGAWAS OBAT
User Manual. Badan Pengawas Obat dan Makanan Republik Indonesia
 User Manual Badan Pengawas Obat dan Makanan Republik Indonesia Copyright @2016 DAFTAR ISI Login Aplikasi... 5 Melakukan Login... 5 Pra Registrasi... 7 Membuat Permohonan... 7 Isian Data Bentuk Sediaan,
User Manual Badan Pengawas Obat dan Makanan Republik Indonesia Copyright @2016 DAFTAR ISI Login Aplikasi... 5 Melakukan Login... 5 Pra Registrasi... 7 Membuat Permohonan... 7 Isian Data Bentuk Sediaan,
Setelah proses Login berhasil, pendaftar akan masuk pada halaman awal Aplikasi e-registrasi Obat.
 PETUNJUK TEKNIS REGISTRASI ULANG APLIKASI e REGISTRASI OBAT (AeRO) aero.pom.go.id Alur Pengajuan Registrasi Ulang Obat Copy =============================== Memulai Proses Registrasi Ulang Obat Copy Pengajuan
PETUNJUK TEKNIS REGISTRASI ULANG APLIKASI e REGISTRASI OBAT (AeRO) aero.pom.go.id Alur Pengajuan Registrasi Ulang Obat Copy =============================== Memulai Proses Registrasi Ulang Obat Copy Pengajuan
PETUNJUK TEKNIS PRA-REGISTRASI APLIKASI e REGISTRASI OBAT (AeRO) aero.pom.go.id
 PETUNJUK TEKNIS PRA-REGISTRASI APLIKASI e REGISTRASI OBAT (AeRO) aero.pom.go.id 2 Alur Pengajuan Pra Registrasi Obat Copy Verifikasi BPOM Verifikasi BPOM Aplikasi e Registrasi Obat (AeRO) versi 1 1 Memulai
PETUNJUK TEKNIS PRA-REGISTRASI APLIKASI e REGISTRASI OBAT (AeRO) aero.pom.go.id 2 Alur Pengajuan Pra Registrasi Obat Copy Verifikasi BPOM Verifikasi BPOM Aplikasi e Registrasi Obat (AeRO) versi 1 1 Memulai
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR : HK TENTANG TATA LAKSANA PENDAFTARAN SUPLEMEN MAKANAN
 PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR : HK.00.05.41.1381 TENTANG TATA LAKSANA PENDAFTARAN SUPLEMEN MAKANAN DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN PENGAWAS OBAT DAN MAKANAN, Menimbang
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR : HK.00.05.41.1381 TENTANG TATA LAKSANA PENDAFTARAN SUPLEMEN MAKANAN DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN PENGAWAS OBAT DAN MAKANAN, Menimbang
MATERI KONSULTASI PUBLIK KETIGA 27 JULI 2017
 MATERI KONSULTASI PUBLIK KETIGA 27 JULI 2017 RANCANGAN PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR TAHUN 2017 TENTANG KRITERIA DAN TATA LAKSANA REGISTRASI SUPLEMEN KESEHATAN
MATERI KONSULTASI PUBLIK KETIGA 27 JULI 2017 RANCANGAN PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR TAHUN 2017 TENTANG KRITERIA DAN TATA LAKSANA REGISTRASI SUPLEMEN KESEHATAN
RANCANGAN PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR TAHUN
 Masukan dapat disampaikan kepada Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen melalui email mmi_stand_ot@yahoo.com, telp/fax 021-4241038 paling lambat tanggal 31 November 2016.
Masukan dapat disampaikan kepada Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen melalui email mmi_stand_ot@yahoo.com, telp/fax 021-4241038 paling lambat tanggal 31 November 2016.
2011, No Tentang Registrasi Obat dan Pasal 36 ayat (4) Undang-Undang Nomor 35 Tahun 2009 tentang Narkotika perlu menetapkan Peraturan Kepal
 No.634, 2011 BERITA NEGARA REPUBLIK INDONESIA BADAN PENGAWAS OBAT DAN MAKANAN/ Obat. Registrasi. Tata Laksana. PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR HK.03.1.23.10.11.08481
No.634, 2011 BERITA NEGARA REPUBLIK INDONESIA BADAN PENGAWAS OBAT DAN MAKANAN/ Obat. Registrasi. Tata Laksana. PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR HK.03.1.23.10.11.08481
DIREKTORAT JENDERAL BINA KEFARMASIAN DAN ALAT KESEHATAN DIREKTORAT BINA PRODUKSI DAN DISTRIBUSI ALAT KESEHATAN
 Formulir 1 Formulir Pendaftaran Alat Kesehatan DIREKTORAT JENDERAL BINA KEFARMASIAN DAN ALAT KESEHATAN DIREKTORAT BINA PRODUKSI DAN DISTRIBUSI ALAT KESEHATAN PERMOHONAN PENDAFTARAN ALAT KESEHATAN PERATURAN
Formulir 1 Formulir Pendaftaran Alat Kesehatan DIREKTORAT JENDERAL BINA KEFARMASIAN DAN ALAT KESEHATAN DIREKTORAT BINA PRODUKSI DAN DISTRIBUSI ALAT KESEHATAN PERMOHONAN PENDAFTARAN ALAT KESEHATAN PERATURAN
1 Pendaftaran Akun Perusahaan. 2 Pendaftaran OT Low Risk. 3 Pendaftaran Ulang OT & SK 4 E-Trecking System Pendaftaran Baru dan Variasi OT & SK
 1 2 Aplikasi sistem E-Registrasi yang telah berlaku di Subdit Penilaian Obat Tradisional dan Suplemen Kesehatan yaitu: 1 Pendaftaran Akun Perusahaan 2 Pendaftaran OT Low Risk 3 Pendaftaran Ulang OT & SK
1 2 Aplikasi sistem E-Registrasi yang telah berlaku di Subdit Penilaian Obat Tradisional dan Suplemen Kesehatan yaitu: 1 Pendaftaran Akun Perusahaan 2 Pendaftaran OT Low Risk 3 Pendaftaran Ulang OT & SK
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR : HK TENTANG
 PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR : HK.00.05.41.1384 TENTANG KRITERIA DAN TATA LAKSANA PENDAFTARAN OBAT TRADISIONAL, OBAT HERBAL TERSTANDAR DAN FITOFARMAKA DENGAN RAHMAT TUHAN YANG
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR : HK.00.05.41.1384 TENTANG KRITERIA DAN TATA LAKSANA PENDAFTARAN OBAT TRADISIONAL, OBAT HERBAL TERSTANDAR DAN FITOFARMAKA DENGAN RAHMAT TUHAN YANG
RANCANGAN PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR TAHUN
 Masukan dapat disampaikan kepada Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen melalui email mmi_stand_ot@yahoo.com, telp/fax 021-4241038 paling lambat tanggal 07 Oktober 2016.
Masukan dapat disampaikan kepada Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen melalui email mmi_stand_ot@yahoo.com, telp/fax 021-4241038 paling lambat tanggal 07 Oktober 2016.
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR HK.03.1.23.12.10.12123 TAHUN 2010 TENTANG PEDOMAN DOKUMEN INFORMASI PRODUK
 PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.03.1.23.12.10.12123 TAHUN 2010 TENTANG PEDOMAN DOKUMEN INFORMASI PRODUK DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN PENGAWAS OBAT DAN MAKANAN,
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.03.1.23.12.10.12123 TAHUN 2010 TENTANG PEDOMAN DOKUMEN INFORMASI PRODUK DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN PENGAWAS OBAT DAN MAKANAN,
KEPUTUSAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR : HK TENTANG KRITERIA DAN TATA LAKSANA REGISTRASI OBAT
 KEPUTUSAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR : HK.00.05.3.1950 TENTANG KRITERIA DAN TATA LAKSANA REGISTRASI OBAT KEPALA BADAN PENGAWAS OBAT DAN MAKANAN, Menimbang : a. bahwa untuk melindungi
KEPUTUSAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR : HK.00.05.3.1950 TENTANG KRITERIA DAN TATA LAKSANA REGISTRASI OBAT KEPALA BADAN PENGAWAS OBAT DAN MAKANAN, Menimbang : a. bahwa untuk melindungi
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR HK.03.1.23.10.11.08481 TAHUN 2011
 PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.03.1.23.10.11.08481 TAHUN 2011 TENTANG KRITERIA DAN TATA LAKSANA REGISTRASI OBAT DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN PENGAWAS OBAT DAN
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.03.1.23.10.11.08481 TAHUN 2011 TENTANG KRITERIA DAN TATA LAKSANA REGISTRASI OBAT DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN PENGAWAS OBAT DAN
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 24 TAHUN 2017 TENTANG KRITERIA DAN TATA LAKSANA REGISTRASI OBAT
 BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 24 TAHUN 2017 TENTANG KRITERIA DAN TATA LAKSANA REGISTRASI OBAT DENGAN RAHMAT
BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 24 TAHUN 2017 TENTANG KRITERIA DAN TATA LAKSANA REGISTRASI OBAT DENGAN RAHMAT
BADAN PENGAWAS OBAT DAN MAKANAN PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR HK
 BADAN PENGAWAS OBAT DAN MAKANAN PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR HK.00.05.41.1381 TENTANG TATA LAKSANA PENDAFTARAN SUPLEMEN MAKANAN DENGAN RAHMAT TUHAN YANG MAHA
BADAN PENGAWAS OBAT DAN MAKANAN PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR HK.00.05.41.1381 TENTANG TATA LAKSANA PENDAFTARAN SUPLEMEN MAKANAN DENGAN RAHMAT TUHAN YANG MAHA
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 14 TAHUN 2017 TENTANG PEDOMAN DOKUMEN INFORMASI PRODUK
 BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 14 TAHUN 2017 TENTANG PEDOMAN DOKUMEN INFORMASI PRODUK DENGAN RAHMAT TUHAN YANG
BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 14 TAHUN 2017 TENTANG PEDOMAN DOKUMEN INFORMASI PRODUK DENGAN RAHMAT TUHAN YANG
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK TAHUN 2011 TENTANG KRITERIA DAN TATA LAKSANA REGISTRASI OBAT
 www.hukumonline.com PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.03.1.23.10.11.08481 TAHUN 2011 TENTANG KRITERIA DAN TATA LAKSANA REGISTRASI OBAT DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN
www.hukumonline.com PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.03.1.23.10.11.08481 TAHUN 2011 TENTANG KRITERIA DAN TATA LAKSANA REGISTRASI OBAT DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 16 TAHUN 2015 TENTANG TATA LAKSANA DAN PENILAIAN OBAT PENGEMBANGAN BARU
 BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 16 TAHUN 2015 TENTANG TATA LAKSANA DAN PENILAIAN OBAT PENGEMBANGAN BARU DENGAN
BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 16 TAHUN 2015 TENTANG TATA LAKSANA DAN PENILAIAN OBAT PENGEMBANGAN BARU DENGAN
1 Pendaftaran Akun Perusahaan. 2 Pendaftaran OT Low Risk. 3 Pendaftaran Ulang OT & SK 4 E-Trecking System Pendaftaran Baru dan Variasi OT & SK
 1 2 Aplikasi sistem E-Registrasi yang telah berlaku di Subdit Penilaian Obat Tradisional dan Suplemen Kesehatan yaitu: 1 Pendaftaran Akun Perusahaan 2 Pendaftaran OT Low Risk 3 Pendaftaran Ulang OT & SK
1 2 Aplikasi sistem E-Registrasi yang telah berlaku di Subdit Penilaian Obat Tradisional dan Suplemen Kesehatan yaitu: 1 Pendaftaran Akun Perusahaan 2 Pendaftaran OT Low Risk 3 Pendaftaran Ulang OT & SK
BAB II TINJAUAN PUSTAKA. menurut Peraturan Menteri Kesehatan RI No. 1799/Menkes/Per/XII/2010 tentang Industri Farmasi adalah badan usaha yang
 BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi 2.1.1 Pengertian Industri Farmasi Industri farmasi menurut Peraturan Menteri Kesehatan RI No. 1799/Menkes/Per/XII/2010 tentang Industri Farmasi adalah badan
BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi 2.1.1 Pengertian Industri Farmasi Industri farmasi menurut Peraturan Menteri Kesehatan RI No. 1799/Menkes/Per/XII/2010 tentang Industri Farmasi adalah badan
Quality Control (QC) dan Quality Assurance (QA) Mata Kuliah : Rancangan Produk Industri (2 SKS) Dosen : Kuni Zu aimah B.,S.Farm., M.Farm., Apt.
 Quality Control (QC) dan Quality Assurance (QA) Mata Kuliah : Rancangan Produk Industri (2 SKS) Dosen : Kuni Zu aimah B.,S.Farm., M.Farm., Apt. Industri farmasi harus membuat obat sedemikian rupa agar
Quality Control (QC) dan Quality Assurance (QA) Mata Kuliah : Rancangan Produk Industri (2 SKS) Dosen : Kuni Zu aimah B.,S.Farm., M.Farm., Apt. Industri farmasi harus membuat obat sedemikian rupa agar
BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA
 PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR : HK.00.05.1.3460 TENTANG PENGAWASAN PEMASUKAN BAHAN BAKU OBAT DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN PENGAWAS OBAT DAN MAKANAN, Menimbang
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR : HK.00.05.1.3460 TENTANG PENGAWASAN PEMASUKAN BAHAN BAKU OBAT DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN PENGAWAS OBAT DAN MAKANAN, Menimbang
JAKARTA, 24 NOVEMBER 2017
 JAKARTA, 24 NOVEMBER 2017 Dra. Togi J. Hutadjulu, Apt. MHA. BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA www.pom.go.id 1. PENDAHULUAN 2. REVISI KRITERIA DAN TATA LAKSANA REGISTRASI OBAT 3. PENUTUP
JAKARTA, 24 NOVEMBER 2017 Dra. Togi J. Hutadjulu, Apt. MHA. BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA www.pom.go.id 1. PENDAHULUAN 2. REVISI KRITERIA DAN TATA LAKSANA REGISTRASI OBAT 3. PENUTUP
MODUL MATERI UJIAN PERPINDAHAN JABATAN FUNGSIONAL PENGAWAS FARMASI DAN MAKANAN TERAMPIL KE AHLI PEGAWAI NEGERI SIPIL (PNS) BADAN POM RI
 MODUL MATERI UJIAN PERPINDAHAN JABATAN FUNGSIONAL PENGAWAS FARMASI DAN MAKANAN TERAMPIL KE AHLI PEGAWAI NEGERI SIPIL (PNS) BADAN POM RI MATA PELAJARAN : KONSEP DASAR PENILAIAN BADAN PENGAWAS OBAT DAN MAKANAN
MODUL MATERI UJIAN PERPINDAHAN JABATAN FUNGSIONAL PENGAWAS FARMASI DAN MAKANAN TERAMPIL KE AHLI PEGAWAI NEGERI SIPIL (PNS) BADAN POM RI MATA PELAJARAN : KONSEP DASAR PENILAIAN BADAN PENGAWAS OBAT DAN MAKANAN
MODUL MATERI UJIAN PERPINDAHAN JABATAN FUNGSIONAL PENGAWAS FARMASI DAN MAKANAN TERAMPIL KE AHLI PEGAWAI NEGERI SIPIL (PNS) BADAN POM RI
 MODUL MATERI UJIAN PERPINDAHAN JABATAN FUNGSIONAL PENGAWAS FARMASI DAN MAKANAN TERAMPIL KE AHLI PEGAWAI NEGERI SIPIL (PNS) BADAN POM RI MATA PELAJARAN : KONSEP DASAR PENILAIAN BADAN PENGAWAS OBAT DAN MAKANAN
MODUL MATERI UJIAN PERPINDAHAN JABATAN FUNGSIONAL PENGAWAS FARMASI DAN MAKANAN TERAMPIL KE AHLI PEGAWAI NEGERI SIPIL (PNS) BADAN POM RI MATA PELAJARAN : KONSEP DASAR PENILAIAN BADAN PENGAWAS OBAT DAN MAKANAN
DOKUMENTASI
 DOKUMENTASI PENDAHULUAN Dokumentasi adalah suatu bukti yang dapat dipercaya pada penerapan/pemenuhan CPOTB. Mutu yang direncanakan adalah satu-satunya solusi untuk mengatasi keluhan yang terkait dengan
DOKUMENTASI PENDAHULUAN Dokumentasi adalah suatu bukti yang dapat dipercaya pada penerapan/pemenuhan CPOTB. Mutu yang direncanakan adalah satu-satunya solusi untuk mengatasi keluhan yang terkait dengan
PEDOMAN PENYIAPAN DOKUMEN INDUK INDUSTRI FARMASI DAN INDUSTRI OBAT TRADISIONAL PENDAHULUAN
 7 2012, No.294 LAMPIRAN PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR HK.04.1.33.02.12.0883 TAHUN 2012 TENTANG DOKUMEN INDUK INDUSTRI FARMASI DAN INDUSTRI OBAT TRADISIONAL PEDOMAN
7 2012, No.294 LAMPIRAN PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR HK.04.1.33.02.12.0883 TAHUN 2012 TENTANG DOKUMEN INDUK INDUSTRI FARMASI DAN INDUSTRI OBAT TRADISIONAL PEDOMAN
BAB II TINJAUAN PUSTAKA. Obat Jadi dan Industri Bahan Baku Obat. Definisi dari obat jadi yaitu
 BAB II TINJAUAN PUSTAKA A. Industri Farmasi 1. Pengertian Industri Farmasi Berdasarkan Surat Keputusan Menteri Kesehatan No. 245/MenKes/SK/V/1990 tentang Ketentuan dan Tata Cara Pelaksanaan Pemberian Izin
BAB II TINJAUAN PUSTAKA A. Industri Farmasi 1. Pengertian Industri Farmasi Berdasarkan Surat Keputusan Menteri Kesehatan No. 245/MenKes/SK/V/1990 tentang Ketentuan dan Tata Cara Pelaksanaan Pemberian Izin
5. Undang-Undang Nomor 32 Tahun 2004 tentang Pemerintahan Daerah (Lembaran Negara Republik Indonesia Tahun 2004 Nomor 125, Tambahan Lembaran Negara
 1999 Nomor 42, Tambahan Lembaran Negara Republik Indonesia Nomor 3821); 5. Undang-Undang Nomor 32 Tahun 2004 tentang Pemerintahan Daerah (Lembaran Negara Republik Indonesia Tahun 2004 Nomor 125, Tambahan
1999 Nomor 42, Tambahan Lembaran Negara Republik Indonesia Nomor 3821); 5. Undang-Undang Nomor 32 Tahun 2004 tentang Pemerintahan Daerah (Lembaran Negara Republik Indonesia Tahun 2004 Nomor 125, Tambahan
CHECK LIST DOKUMEN REGISTRASI VARIASI PRODUK BIOLOGI
 CHECK LIST DOKUMEN REGISTRASI VARIASI PRODUK BIOLOGI I. INFORMASI PRODUK Nama Obat : Bentuk Sediaan & Kekuatan : Zat aktif : Kemasan : Pendaftar : Produsen : Kategori Registrasi : II. DOKUMEN YANG DISERAHKAN
CHECK LIST DOKUMEN REGISTRASI VARIASI PRODUK BIOLOGI I. INFORMASI PRODUK Nama Obat : Bentuk Sediaan & Kekuatan : Zat aktif : Kemasan : Pendaftar : Produsen : Kategori Registrasi : II. DOKUMEN YANG DISERAHKAN
BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA
 PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.04.1.33.12.11.09938 TAHUN 2011 TENTANG KRITERIA DAN TATA CARA PENARIKAN OBAT YANG TIDAK MEMENUHI STANDAR DAN/ATAU PERSYARATAN DENGAN RAHMAT TUHAN
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.04.1.33.12.11.09938 TAHUN 2011 TENTANG KRITERIA DAN TATA CARA PENARIKAN OBAT YANG TIDAK MEMENUHI STANDAR DAN/ATAU PERSYARATAN DENGAN RAHMAT TUHAN
BADAN PENGAWAS OBAT DAN MAKANAN RI
 PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR HK.00.05.1.3459 TENTANG PENGAWASAN PEMASUKAN OBAT IMPOR DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN PENGAWAS OBAT DAN MAKANAN
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR HK.00.05.1.3459 TENTANG PENGAWASAN PEMASUKAN OBAT IMPOR DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN PENGAWAS OBAT DAN MAKANAN
Sejak Februari 2018, seluruh sistem registrasi obat tradisional dan suplemen kesehatan menggunakan website asrot yang sudah dimutakhirkan
 Sejak Februari 2018, seluruh sistem registrasi obat tradisional dan suplemen kesehatan menggunakan website asrot yang sudah dimutakhirkan Website : asrot.pom.go.id/asrot Untuk produk yang telah didaftarkan
Sejak Februari 2018, seluruh sistem registrasi obat tradisional dan suplemen kesehatan menggunakan website asrot yang sudah dimutakhirkan Website : asrot.pom.go.id/asrot Untuk produk yang telah didaftarkan
Oleh : Bambang Priyambodo
 Oleh : Bambang Priyambodo SISTEMATIKA CPOB: 2012 merupakan penyempurnaan dari CPOB: 2006, mencakup revisi terhadap : Pedoman CPOB: 2006 Suplemen I Pedoman CPOB: 2006 tahun 2009 Aneks 8 : Cara Pembuatan
Oleh : Bambang Priyambodo SISTEMATIKA CPOB: 2012 merupakan penyempurnaan dari CPOB: 2006, mencakup revisi terhadap : Pedoman CPOB: 2006 Suplemen I Pedoman CPOB: 2006 tahun 2009 Aneks 8 : Cara Pembuatan
KISI-KISI MATERI PLPG MATA PELAJARAN FARMASI INDUSTRI
 KISI-KISI MATERI PLPG MATA PELAJARAN FARMASI INDUSTRI Standar Guru (SKG) Inti Guru (KI) Guru Mata Pelajaran 1 Menguasai karakteristik Mengidentifikasi karakteristik peserta didik yang berkaitan dengan
KISI-KISI MATERI PLPG MATA PELAJARAN FARMASI INDUSTRI Standar Guru (SKG) Inti Guru (KI) Guru Mata Pelajaran 1 Menguasai karakteristik Mengidentifikasi karakteristik peserta didik yang berkaitan dengan
B. Tujuan Tujuan Qualiy Assurance adalah untuk memastikan bahwa obat dihasilkan dengan mutu yang sesuai dengan tujuan pemakaiannya.
 PEMASTIAN MUTU (QUALITY ASSURANCE/QA) A. Pendahuluan Industri farmasi bertujuan untuk menghasilkan obat yang harus memenuhi persyaratan khasiat (efficacy), keamanan (safety) dan mutu (quality). Berdasarkan
PEMASTIAN MUTU (QUALITY ASSURANCE/QA) A. Pendahuluan Industri farmasi bertujuan untuk menghasilkan obat yang harus memenuhi persyaratan khasiat (efficacy), keamanan (safety) dan mutu (quality). Berdasarkan
BAB II TINJAUAN UMUM INDUSTRI FARMASI. Lembaga Farmasi Direktorat Kesehatan Angkatan Darat (Lafi Ditkesad)
 BAB II TINJAUAN UMUM INDUSTRI FARMASI 2.1 Perkembangan Lafi Ditkesad Lembaga Farmasi Direktorat Kesehatan Angkatan Darat (Lafi Ditkesad) merupakan lembaga yang telah ada sejak zaman penjajahan Belanda.
BAB II TINJAUAN UMUM INDUSTRI FARMASI 2.1 Perkembangan Lafi Ditkesad Lembaga Farmasi Direktorat Kesehatan Angkatan Darat (Lafi Ditkesad) merupakan lembaga yang telah ada sejak zaman penjajahan Belanda.
DASAR KOMPETENSI KEJURUAN DAN KOMPETENSI KEJURUAN SEKOLAH MENENGAH KEJURUAN
 DASAR KOMPETENSI KEJURUAN DAN KOMPETENSI KEJURUAN SEKOLAH MENENGAH KEJURUAN BIDANG STUDI KEAHLIAN : KESEHATAN PROGRAM STUDI KEAHLIAN : KESEHATAN KOMPETENSI KEAHLIAN : 1. FARMASI (079) 2. FARMASI INDUSTRI
DASAR KOMPETENSI KEJURUAN DAN KOMPETENSI KEJURUAN SEKOLAH MENENGAH KEJURUAN BIDANG STUDI KEAHLIAN : KESEHATAN PROGRAM STUDI KEAHLIAN : KESEHATAN KOMPETENSI KEAHLIAN : 1. FARMASI (079) 2. FARMASI INDUSTRI
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR HK TAHUN 2011 TENTANG PENGAWASAN PEMASUKAN OBAT IMPOR
 PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.03.1.3.12.11.10692 TAHUN 2011 TENTANG PENGAWASAN PEMASUKAN OBAT IMPOR DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN PENGAWAS OBAT DAN MAKANAN,
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.03.1.3.12.11.10692 TAHUN 2011 TENTANG PENGAWASAN PEMASUKAN OBAT IMPOR DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN PENGAWAS OBAT DAN MAKANAN,
BAB I PENDAHULUAN. menghambat enzim HMG-CoA reduktase. HMG-CoA merupakan pembentuk
 BAB I PENDAHULUAN 1.1 Latar Belakang Simvastatin merupakan obat antihiperlidemia yang bekerja dengan cara menghambat enzim HMG-CoA reduktase. HMG-CoA merupakan pembentuk kolesterol dengan bantuan katalis
BAB I PENDAHULUAN 1.1 Latar Belakang Simvastatin merupakan obat antihiperlidemia yang bekerja dengan cara menghambat enzim HMG-CoA reduktase. HMG-CoA merupakan pembentuk kolesterol dengan bantuan katalis
CPOB. (Cara Pembuatan Obat yang Baik)
 CPOB { (Cara Pembuatan Obat yang Baik) CPOB (Cara Pembuatan Obat Yang Baik) 2006 atau GMP (Good Manufacturing Practices) 2006 adalah suatu pedoman pembuatan obat berdasarkan berbagai ketentuan dalam CPOB
CPOB { (Cara Pembuatan Obat yang Baik) CPOB (Cara Pembuatan Obat Yang Baik) 2006 atau GMP (Good Manufacturing Practices) 2006 adalah suatu pedoman pembuatan obat berdasarkan berbagai ketentuan dalam CPOB
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR HK TAHUN 2010 TENTANG PERSYARATAN TEKNIS KOSMETIKA
 PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR HK.03.1.23.12.10.12459 TAHUN 2010 TENTANG PERSYARATAN TEKNIS KOSMETIKA DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN PENGAWAS
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR HK.03.1.23.12.10.12459 TAHUN 2010 TENTANG PERSYARATAN TEKNIS KOSMETIKA DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN PENGAWAS
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR HK TAHUN 2011 TENTANG PENDAFTARAN PANGAN OLAHAN
 PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.03.1.5.12.11.09955 TAHUN 2011 TENTANG PENDAFTARAN PANGAN OLAHAN DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN PENGAWAS OBAT DAN MAKANAN, Menimbang
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.03.1.5.12.11.09955 TAHUN 2011 TENTANG PENDAFTARAN PANGAN OLAHAN DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN PENGAWAS OBAT DAN MAKANAN, Menimbang
BAB II TINJAUAN PUSTAKA. Indonesia Nomor 245/Menkes/SK/V/1990 adalah industri obat jadi dan industri
 BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi Industri farmasi menurut Surat Keputusan Menteri Kesehatan Republik Indonesia Nomor 245/Menkes/SK/V/1990 adalah industri obat jadi dan industri bahan baku obat.
BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi Industri farmasi menurut Surat Keputusan Menteri Kesehatan Republik Indonesia Nomor 245/Menkes/SK/V/1990 adalah industri obat jadi dan industri bahan baku obat.
PEDOMAN PENILAIAN REGISTRASI
 PEDOMAN PENILAIAN REGISTRASI LAMPIRAN A DATA ADMINISTRASI 1 Berikan Foto copy sertifikat Produksi alat kesehatan yang dikeluarkan oleh Menteri Kesehatan Cq Direktorat Jenderal Bina Kefarmasian dan Alat
PEDOMAN PENILAIAN REGISTRASI LAMPIRAN A DATA ADMINISTRASI 1 Berikan Foto copy sertifikat Produksi alat kesehatan yang dikeluarkan oleh Menteri Kesehatan Cq Direktorat Jenderal Bina Kefarmasian dan Alat
2016, No terakhir dengan Peraturan Presiden Nomor 3 Tahun 2013 tentang Perubahan Ketujuh Atas Keputusan Presiden Nomor 103 Tahun 2001 tentang
 No. 1510, 2016 BERITA NEGARA REPUBLIK INDONESIA BSN. Alat Konversi BBG. Skema Sertifikasi. PERATURAN KEPALA BADAN STANDARDISASI NASIONAL NOMOR 7 TAHUN 2016 TENTANG SKEMA SERTIFIKASI ALAT KONVERSI BAHAN
No. 1510, 2016 BERITA NEGARA REPUBLIK INDONESIA BSN. Alat Konversi BBG. Skema Sertifikasi. PERATURAN KEPALA BADAN STANDARDISASI NASIONAL NOMOR 7 TAHUN 2016 TENTANG SKEMA SERTIFIKASI ALAT KONVERSI BAHAN
BADAN PENGAWAS OBAT DAN MAKANAN KEPUTUSAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 02002/SK/KBPOM
 BADAN PENGAWAS OBAT DAN MAKANAN KEPUTUSAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 02002/SK/KBPOM TENTANG TATA LAKSANA UJI KLINIK KEPALA BADAN PENGAWAS OBAT DAN MAKANAN Menimbang
BADAN PENGAWAS OBAT DAN MAKANAN KEPUTUSAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 02002/SK/KBPOM TENTANG TATA LAKSANA UJI KLINIK KEPALA BADAN PENGAWAS OBAT DAN MAKANAN Menimbang
BAB II TINJAUAN PUSTAKA. Indonesia Nomor 245/Menkes/SK/V/1990 terdiri dari industri obat jadi dan
 BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi 2.1.1 Pengertian Industri Farmasi Industri farmasi menurut Surat Keputusan Menteri Kesehatan Republik Indonesia Nomor 245/Menkes/SK/V/1990 terdiri dari industri
BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi 2.1.1 Pengertian Industri Farmasi Industri farmasi menurut Surat Keputusan Menteri Kesehatan Republik Indonesia Nomor 245/Menkes/SK/V/1990 terdiri dari industri
BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA
 BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 15 TAHUN 2016 TENTANG PERUBAHAN ATAS PERATURAN KEPALA BADAN PENGAWAS OBAT DAN
BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 15 TAHUN 2016 TENTANG PERUBAHAN ATAS PERATURAN KEPALA BADAN PENGAWAS OBAT DAN
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 12 TAHUN 2016 TENTANG PENDAFTARAN PANGAN OLAHAN
 BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 12 TAHUN 2016 TENTANG PENDAFTARAN PANGAN OLAHAN DENGAN RAHMAT TUHAN YANG MAHA
BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR 12 TAHUN 2016 TENTANG PENDAFTARAN PANGAN OLAHAN DENGAN RAHMAT TUHAN YANG MAHA
BAB II TINJAUAN UMUM. Industri farmasi menurut Surat Keputusan Menteri Kesehatan Republik
 BAB II TINJAUAN UMUM 2.1 Industri Farmasi Industri farmasi menurut Surat Keputusan Menteri Kesehatan Republik Indonesia Nomor 245/Menkes/SK/V/1990 adalah industri obat jadi dan industri bahan baku obat.
BAB II TINJAUAN UMUM 2.1 Industri Farmasi Industri farmasi menurut Surat Keputusan Menteri Kesehatan Republik Indonesia Nomor 245/Menkes/SK/V/1990 adalah industri obat jadi dan industri bahan baku obat.
BAB V ANALISA DATA. Sampel uji diterima oleh Manajer Teknis. Kaji ulang terhadap permintaan pemeriksaan Permintaan Ditolak NOT OK
 BAB V ANALISA DATA 5.1 Perbaikan Alur Kerja Penanganan Sampel Uji Sesudah Proses Akreditasi ISO 17025:2008 5.1.1 Alur Kerja Penanganan Sampel Uji Sebelum Proses Akreditasi Sampel uji diterima oleh Manajer
BAB V ANALISA DATA 5.1 Perbaikan Alur Kerja Penanganan Sampel Uji Sesudah Proses Akreditasi ISO 17025:2008 5.1.1 Alur Kerja Penanganan Sampel Uji Sebelum Proses Akreditasi Sampel uji diterima oleh Manajer
- 3 - PERBEKALAN KESEHATAN RUMAH TANGGA PEDOMAN PELAYANAN IZIN EDAR BAB I PENDAHULUAN
 -2- - 3 - LAMPIRAN DIREKTUR JENDERAL BINA KEFARMASIAN DAN ALAT KESEHATAN NOMOR HK.02.03/I/769/2014 TENTANG PEDOMAN PELAYANAN IZIN EDAR PERBEKALAN KESEHATAN RUMAH TANGGA A. Latar Belakang PEDOMAN PELAYANAN
-2- - 3 - LAMPIRAN DIREKTUR JENDERAL BINA KEFARMASIAN DAN ALAT KESEHATAN NOMOR HK.02.03/I/769/2014 TENTANG PEDOMAN PELAYANAN IZIN EDAR PERBEKALAN KESEHATAN RUMAH TANGGA A. Latar Belakang PEDOMAN PELAYANAN
RANCANGAN PERATURAN BADAN PENGAWAS OBAT DAN MAKANAN NOMOR... TAHUN 2018 TENTANG STANDAR PELAYANAN PUBLIK DI LINGKUNGAN BADAN PENGAWAS OBAT DAN MAKANAN
 RANCANGAN PERATURAN BADAN PENGAWAS OBAT DAN MAKANAN NOMOR... TAHUN 2018 TENTANG STANDAR PELAYANAN PUBLIK DI LINGKUNGAN BADAN PENGAWAS OBAT DAN MAKANAN DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN PENGAWAS
RANCANGAN PERATURAN BADAN PENGAWAS OBAT DAN MAKANAN NOMOR... TAHUN 2018 TENTANG STANDAR PELAYANAN PUBLIK DI LINGKUNGAN BADAN PENGAWAS OBAT DAN MAKANAN DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN PENGAWAS
PRODUKSI FARMASI di RUMAH SAKIT
 PRODUKSI FARMASI di RUMAH SAKIT Kuliah : FARMASI RUMAH SAKIT Heru Sasongko, M.Sc,.,Apt. Pustaka : IFRS RSUP DR SARDJITO YOGYAKARTA PRODUKSI FARMASI : Merupakan kegiatan membuat, merubah bentuk dan me-ngemas
PRODUKSI FARMASI di RUMAH SAKIT Kuliah : FARMASI RUMAH SAKIT Heru Sasongko, M.Sc,.,Apt. Pustaka : IFRS RSUP DR SARDJITO YOGYAKARTA PRODUKSI FARMASI : Merupakan kegiatan membuat, merubah bentuk dan me-ngemas
BERITA NEGARA REPUBLIK INDONESIA
 No.1249, 2012 BERITA NEGARA REPUBLIK INDONESIA KEMENTERIAN KESEHATAN. Sel Punca. Klinis. Laboratorium. Penyelenggaraan. PERATURAN MENTERI KESEHATAN REPUBLIK INDONESIA NOMOR 50 TAHUN 2012 TENTANG PENYELENGGARAAN
No.1249, 2012 BERITA NEGARA REPUBLIK INDONESIA KEMENTERIAN KESEHATAN. Sel Punca. Klinis. Laboratorium. Penyelenggaraan. PERATURAN MENTERI KESEHATAN REPUBLIK INDONESIA NOMOR 50 TAHUN 2012 TENTANG PENYELENGGARAAN
PERSYARATAN REGISTRASI ALAT KESEHATAN
 PERSYARATAN REGISTRASI ALAT KESEHATAN NO. PERSYARATAN FORMULIR A DATA ADMINISTRASI 1 Mengisi formulir permohonan sesuai Permenkes 1190/MENKES/PER/VIII/2010 Formulir 1 (mencantumkan nomor surat & tanggal,
PERSYARATAN REGISTRASI ALAT KESEHATAN NO. PERSYARATAN FORMULIR A DATA ADMINISTRASI 1 Mengisi formulir permohonan sesuai Permenkes 1190/MENKES/PER/VIII/2010 Formulir 1 (mencantumkan nomor surat & tanggal,
Perizinan BPOM (Badan Pengawasan Obat dan Makanan)
 Perizinan BPOM (Badan Pengawasan Obat dan Makanan) Sistem Pengawasan Obat dan Makanan (SisPOM) yang efektif dan efisien yang mampu mendeteksi, mencegah dan mengawasi produk-produk dengan tujuan melindungi
Perizinan BPOM (Badan Pengawasan Obat dan Makanan) Sistem Pengawasan Obat dan Makanan (SisPOM) yang efektif dan efisien yang mampu mendeteksi, mencegah dan mengawasi produk-produk dengan tujuan melindungi
PERATURAN MENTERI KELAUTAN DAN PERIKANAN REPUBLIK INDONESIA NOMOR PER.04/MEN/2012 TENTANG OBAT IKAN DENGAN RAHMAT TUHAN YANG MAHA ESA
 PERATURAN MENTERI KELAUTAN DAN PERIKANAN REPUBLIK INDONESIA NOMOR PER.04/MEN/2012 TENTANG OBAT IKAN DENGAN RAHMAT TUHAN YANG MAHA ESA MENTERI KELAUTAN DAN PERIKANAN REPUBLIK INDONESIA, Menimbang : a. bahwa
PERATURAN MENTERI KELAUTAN DAN PERIKANAN REPUBLIK INDONESIA NOMOR PER.04/MEN/2012 TENTANG OBAT IKAN DENGAN RAHMAT TUHAN YANG MAHA ESA MENTERI KELAUTAN DAN PERIKANAN REPUBLIK INDONESIA, Menimbang : a. bahwa
SEDIAAN INJEKSI (PARENTERAL)
 BAB II SEDIAAN INJEKSI (PARENTERAL) PENDAHULUAN Setelah mahasiswa mengikuti kuliah bab II yang diberikan pada pertemuan kedua dan ketiga, diharapkan mahasiswa mampu menjelaskan komponen, prinsip pembuatan,
BAB II SEDIAAN INJEKSI (PARENTERAL) PENDAHULUAN Setelah mahasiswa mengikuti kuliah bab II yang diberikan pada pertemuan kedua dan ketiga, diharapkan mahasiswa mampu menjelaskan komponen, prinsip pembuatan,
BERITA NEGARA REPUBLIK INDONESIA KEMENTERIAN KESEHATAN. Industri Farmasi. Perizinan. Penyelenggaraan.
 No.721, 2010 BERITA NEGARA REPUBLIK INDONESIA KEMENTERIAN KESEHATAN. Industri Farmasi. Perizinan. Penyelenggaraan. PERATURAN MENTERI KESEHATAN REPUBLIK INDONESIA NOMOR 1799/MENKES/PER/XII/2010 TENTANG
No.721, 2010 BERITA NEGARA REPUBLIK INDONESIA KEMENTERIAN KESEHATAN. Industri Farmasi. Perizinan. Penyelenggaraan. PERATURAN MENTERI KESEHATAN REPUBLIK INDONESIA NOMOR 1799/MENKES/PER/XII/2010 TENTANG
Lampiran 1. Bagan proses Pembuatan Krim / Salep
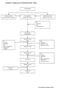 Lampiran 1. Bagan proses Pembuatan Krim / Salep Penimbangan Peleburan bahan Dasar krim (Fase minyak) Pencampuran Dengan ultra turrax Pelarutan zat aktif, Pengawet (Fase cair) -ph -Stabilitas krim Pencampuran
Lampiran 1. Bagan proses Pembuatan Krim / Salep Penimbangan Peleburan bahan Dasar krim (Fase minyak) Pencampuran Dengan ultra turrax Pelarutan zat aktif, Pengawet (Fase cair) -ph -Stabilitas krim Pencampuran
BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA
 PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.04.1.33.12.11.09938 TAHUN 2011 TENTANG KRITERIA DAN TATA CARA PENARIKAN OBAT YANG TIDAK MEMENUHI STANDAR DAN/ATAU PERSYARATAN DENGAN RAHMAT TUHAN
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.04.1.33.12.11.09938 TAHUN 2011 TENTANG KRITERIA DAN TATA CARA PENARIKAN OBAT YANG TIDAK MEMENUHI STANDAR DAN/ATAU PERSYARATAN DENGAN RAHMAT TUHAN
R A N C A N G A N PERATURAN MENTERI KELAUTAN DAN PERIKANAN NOMOR / /2017 T E N T A N G O B A T I K A N
 R A N C A N G A N PERATURAN MENTERI KELAUTAN DAN PERIKANAN NOMOR / /2017 T E N T A N G O B A T I K A N DENGAN RAHMAT TUHAN YANG MAHA ESA MENTERI KELAUTAN DAN PERIKANAN, Menimbang : a. bahwa dalam rangka
R A N C A N G A N PERATURAN MENTERI KELAUTAN DAN PERIKANAN NOMOR / /2017 T E N T A N G O B A T I K A N DENGAN RAHMAT TUHAN YANG MAHA ESA MENTERI KELAUTAN DAN PERIKANAN, Menimbang : a. bahwa dalam rangka
BAB II TINJAUAN PUSTAKA. Industri farmasi menurut SK Menkes No. 245/Menkes/SK/V/1990 adalah
 BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi Industri farmasi menurut SK Menkes No. 245/Menkes/SK/V/1990 adalah industri obat jadi dan industri bahan baku obat. Industri obat jadi adalah industri yang
BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi Industri farmasi menurut SK Menkes No. 245/Menkes/SK/V/1990 adalah industri obat jadi dan industri bahan baku obat. Industri obat jadi adalah industri yang
PERATURAN MENTERI KESEHATAN REPUBLIK INDONESIA NOMOR 1190/MENKES/PER/VIII/2010 TENTANG IZIN EDAR ALAT KESEHATAN DAN PERBEKALAN KESEHATAN RUMAH TANGGA
 PERATURAN MENTERI KESEHATAN REPUBLIK INDONESIA NOMOR 1190/MENKES/PER/VIII/2010 TENTANG IZIN EDAR ALAT KESEHATAN DAN PERBEKALAN KESEHATAN RUMAH TANGGA DENGAN RAHMAT TUHAN YANG MAHA ESA MENTERI KESEHATAN
PERATURAN MENTERI KESEHATAN REPUBLIK INDONESIA NOMOR 1190/MENKES/PER/VIII/2010 TENTANG IZIN EDAR ALAT KESEHATAN DAN PERBEKALAN KESEHATAN RUMAH TANGGA DENGAN RAHMAT TUHAN YANG MAHA ESA MENTERI KESEHATAN
KEPUTUSAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR HK
 KEPUTUSAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR HK.00.05.23.3644 TE N TA N G KETENTUAN POKOK PENGAWASAN SUPLEMEN MAKANAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA,
KEPUTUSAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR HK.00.05.23.3644 TE N TA N G KETENTUAN POKOK PENGAWASAN SUPLEMEN MAKANAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA,
BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA
 KEPUTUSAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.00.05.23.4416 TAHUN 2008 TENTANG PENETAPAN TINGKAT LAYANAN (SERVICE LEVEL ARRANGEMENT) DI LINGKUNGAN BADAN PENGAWAS OBAT DAN MAKANAN DALAM KERANGKA
KEPUTUSAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.00.05.23.4416 TAHUN 2008 TENTANG PENETAPAN TINGKAT LAYANAN (SERVICE LEVEL ARRANGEMENT) DI LINGKUNGAN BADAN PENGAWAS OBAT DAN MAKANAN DALAM KERANGKA
Produksi di Industri Farmasi
 Produksi di Industri Farmasi PRODUKSI istilah terkait Pembuatan Seluruh rangkaian kegiatan dalam menghasilkan suatu obat, meliputi produksi dan pengawasan mutu, mulai dari pengadaan bahan awal dan bahan
Produksi di Industri Farmasi PRODUKSI istilah terkait Pembuatan Seluruh rangkaian kegiatan dalam menghasilkan suatu obat, meliputi produksi dan pengawasan mutu, mulai dari pengadaan bahan awal dan bahan
BERITA NEGARA REPUBLIK INDONESIA
 No.139,2012 BERITA NEGARA REPUBLIK INDONESIA KEMENTERIAN KELAUTAN DAN PERIKANAN. Obat Ikan. Peredaran. Mekanisme. PERATURAN MENTERI KELAUTAN DAN PERIKANAN REPUBLIK INDONESIA NOMOR PER.04/MEN/2012 TENTANG
No.139,2012 BERITA NEGARA REPUBLIK INDONESIA KEMENTERIAN KELAUTAN DAN PERIKANAN. Obat Ikan. Peredaran. Mekanisme. PERATURAN MENTERI KELAUTAN DAN PERIKANAN REPUBLIK INDONESIA NOMOR PER.04/MEN/2012 TENTANG
BAB II TINJAUAN PUSTAKA. Industri farmasi menurut Peraturan Menteri Kesehatan RI No.
 BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi 2.1.1 Pengertian Industri Farmasi Industri farmasi menurut Peraturan Menteri Kesehatan RI No. 1799/Menkes/Per/XII/2010 tentang Industri Farmasi adalah badan
BAB II TINJAUAN PUSTAKA 2.1 Industri Farmasi 2.1.1 Pengertian Industri Farmasi Industri farmasi menurut Peraturan Menteri Kesehatan RI No. 1799/Menkes/Per/XII/2010 tentang Industri Farmasi adalah badan
DITOLAK BAGIAN PENGAWASAN MUTU PHARMACEUTICAL INDUSTRIES MEDAN
 Lampiran 15. Etiket PT. UNIVERSAL PHARMACEUTICAL INDUSTRIES MEDAN Nama Produk/Bahan No. Batch/Lot Pabrik Pemasok No. Penerimaan Barang Jumlah No. Sertifikat Analisis Tanda Tangan DITOLAK BAGIAN PENGAWASAN
Lampiran 15. Etiket PT. UNIVERSAL PHARMACEUTICAL INDUSTRIES MEDAN Nama Produk/Bahan No. Batch/Lot Pabrik Pemasok No. Penerimaan Barang Jumlah No. Sertifikat Analisis Tanda Tangan DITOLAK BAGIAN PENGAWASAN
RANCANGAN PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA NOMOR... TAHUN 2016 TENTANG PENGAWASAN SUPLEMEN KESEHATAN
 FILE EDIT 16 November 2016 Masukan dapat disampaikan kepada Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen melalui email mmi_stand_ot@yahoo.com, telp/fax 021-4241038 paling lambat
FILE EDIT 16 November 2016 Masukan dapat disampaikan kepada Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen melalui email mmi_stand_ot@yahoo.com, telp/fax 021-4241038 paling lambat
BAB II TINJAUAN UMUM INDUSTRI FARMASI. mendapatkan sertifikat Cara Pembuatan Obat yang Baik pada tahun Saat ini
 BAB II TINJAUAN UMUM INDUSTRI FARMASI 2.1. Sejarah PT. Universal Pharmaceutical Industries didirikan pada tahun 1975 dan mendapatkan sertifikat Cara Pembuatan Obat yang Baik pada tahun 1995. Saat ini dalam
BAB II TINJAUAN UMUM INDUSTRI FARMASI 2.1. Sejarah PT. Universal Pharmaceutical Industries didirikan pada tahun 1975 dan mendapatkan sertifikat Cara Pembuatan Obat yang Baik pada tahun 1995. Saat ini dalam
BAB II TINJAUAN PUSTAKA. (CPOB). Hal ini didasarkan oleh Keputusan Menteri Kesehatan RI.
 BAB II TINJAUAN PUSTAKA Industri farmasi diwajibkan menerapkan Cara Pembuatan Obat yang Baik (CPOB). Hal ini didasarkan oleh Keputusan Menteri Kesehatan RI. No.43/MENKES/SK/II/1988 tentang CPOB dan Keputusan
BAB II TINJAUAN PUSTAKA Industri farmasi diwajibkan menerapkan Cara Pembuatan Obat yang Baik (CPOB). Hal ini didasarkan oleh Keputusan Menteri Kesehatan RI. No.43/MENKES/SK/II/1988 tentang CPOB dan Keputusan
PERATURAN MENTERI KESEHATAN REPUBLIK INDONESIA NOMOR 1010/MENKES/PER/XI/2008 TENTANG REGISTRASI OBAT
 PERATURAN MENTERI KESEHATAN REPUBLIK INDONESIA NOMOR 1010/MENKES/PER/XI/2008 TENTANG REGISTRASI OBAT Menimbang : a. bahwa dalam rangka melindungi masyarakat dari peredaran obat yang tidak memenuhi persyaratan,
PERATURAN MENTERI KESEHATAN REPUBLIK INDONESIA NOMOR 1010/MENKES/PER/XI/2008 TENTANG REGISTRASI OBAT Menimbang : a. bahwa dalam rangka melindungi masyarakat dari peredaran obat yang tidak memenuhi persyaratan,
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA
 PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.04.1.33.02.12.0883 TAHUN 2012 TENTANG DOKUMEN INDUK INDUSTRI FARMASI DAN INDUSTRI OBAT TRADISIONAL DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN
PERATURAN KEPALA BADAN PENGAWAS OBAT DAN MAKANAN NOMOR HK.04.1.33.02.12.0883 TAHUN 2012 TENTANG DOKUMEN INDUK INDUSTRI FARMASI DAN INDUSTRI OBAT TRADISIONAL DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN
M E M U T U S K A N : Menetapkan : PERATURAN MENTERI KESEHATAN TENTANG PEREDARAN OBAT TRADISIONAL IMPOR BAB I KETENTUAN UMUM.
 PERATURAN MENTERI KESEHATAN REPUBLIK INDONESIA NOMOR 1297/MENKES/PER/XI/1998 TENTANG PEREDARAN OBAT TRADISIONAL IMPOR MENTERI KESEHATAN REBUBLIK INDONESIA Menimbang : a. bahwa dalam rangka melindungi masyarakat
PERATURAN MENTERI KESEHATAN REPUBLIK INDONESIA NOMOR 1297/MENKES/PER/XI/1998 TENTANG PEREDARAN OBAT TRADISIONAL IMPOR MENTERI KESEHATAN REBUBLIK INDONESIA Menimbang : a. bahwa dalam rangka melindungi masyarakat
Tugas Individu Farmasi Industri. Uraian Tugas Kepala Bagian Produksi, Pengawasan Mutu dan Pemastian Mutu
 Tugas Individu Farmasi Industri Uraian Tugas Kepala Bagian Produksi, Pengawasan Mutu dan Pemastian Mutu Disusun Oleh : Eka Wahyu Lestari 14340004 Dosen : Drs. Kosasih, M.Sc., Apt. Program Profesi Apoteker
Tugas Individu Farmasi Industri Uraian Tugas Kepala Bagian Produksi, Pengawasan Mutu dan Pemastian Mutu Disusun Oleh : Eka Wahyu Lestari 14340004 Dosen : Drs. Kosasih, M.Sc., Apt. Program Profesi Apoteker
PERATURAN MENTERI KESEHATAN REPUBLIK INDONESIA NOMOR 1189/MENKES/PER/VIII/2010 TENTANG PRODUKSI ALAT KESEHATAN DAN PERBEKALAN KESEHATAN RUMAH TANGGA
 PERATURAN MENTERI KESEHATAN REPUBLIK INDONESIA NOMOR 1189/MENKES/PER/VIII/2010 TENTANG PRODUKSI ALAT KESEHATAN DAN PERBEKALAN KESEHATAN RUMAH TANGGA DENGAN RAHMAT TUHAN YANG MAHA ESA MENTERI KESEHATAN
PERATURAN MENTERI KESEHATAN REPUBLIK INDONESIA NOMOR 1189/MENKES/PER/VIII/2010 TENTANG PRODUKSI ALAT KESEHATAN DAN PERBEKALAN KESEHATAN RUMAH TANGGA DENGAN RAHMAT TUHAN YANG MAHA ESA MENTERI KESEHATAN
BAB III TINJAUAN TEORITIS PENDAFTARAN PANGAN OLAHAN. digunakan dalam proses penyiapan, pengolahan dan atau pembuatan makanan atau
 1 BAB III TINJAUAN TEORITIS PENDAFTARAN PANGAN OLAHAN A. TINJAUAN PANGAN OLAHAN 1. Pengertian Pangan Olahan Menurut Peraturan Pemerintah RI nomor 28 tahun 2004 pangan adalah segala sesuatu yang berasal
1 BAB III TINJAUAN TEORITIS PENDAFTARAN PANGAN OLAHAN A. TINJAUAN PANGAN OLAHAN 1. Pengertian Pangan Olahan Menurut Peraturan Pemerintah RI nomor 28 tahun 2004 pangan adalah segala sesuatu yang berasal
UJI STABILITAS FISIK DAN KIMIA SEDIAAN SIRUP RACIKAN
 Prosiding SNaPP2012 : Sains, Teknologi, dan Kesehatan ISSN 2089-3582 UJI STABILITAS FISIK DAN KIMIA SEDIAAN SIRUP RACIKAN YANG MENGANDUNG ERDOSTEIN 1 Fetri Lestari, 2 Hilda Aprilia 1,2 Program Studi Farmasi,
Prosiding SNaPP2012 : Sains, Teknologi, dan Kesehatan ISSN 2089-3582 UJI STABILITAS FISIK DAN KIMIA SEDIAAN SIRUP RACIKAN YANG MENGANDUNG ERDOSTEIN 1 Fetri Lestari, 2 Hilda Aprilia 1,2 Program Studi Farmasi,
Cara Distribusi Obat yang Baik (CDOB)
 Cara Distribusi Obat yang Baik (CDOB) BPOM dalam mengawal obat Visi : Obat dan makanan terjamin aman,bermutu dan berkhasiat. Misi: Melindungi masyarakat dari obat dan makanan yang beresiko terhadap kesehatan.
Cara Distribusi Obat yang Baik (CDOB) BPOM dalam mengawal obat Visi : Obat dan makanan terjamin aman,bermutu dan berkhasiat. Misi: Melindungi masyarakat dari obat dan makanan yang beresiko terhadap kesehatan.
Lampiran 1. Blanko Laporan Hasil Pengujian Laboratorium LEMBAGA FARMASI DIREKTORAT KESEHATAN ANGKATAN DARAT INSTALASI PENGAWASAN MUTU
 Lampiran 1. Blanko Laporan Hasil Pengujian Laboratorium LEMBAGA FARMASI DIREKTORAT KESEHATAN ANGKATAN DARAT INSTALASI PENGAWASAN MUTU LAPORAN HASIL PENGUJIAN NOMOR : / /201 1. NAMA CONTOH 2. NAMA PABRIK
Lampiran 1. Blanko Laporan Hasil Pengujian Laboratorium LEMBAGA FARMASI DIREKTORAT KESEHATAN ANGKATAN DARAT INSTALASI PENGAWASAN MUTU LAPORAN HASIL PENGUJIAN NOMOR : / /201 1. NAMA CONTOH 2. NAMA PABRIK
PERATURAN BADAN PENGAWAS OBAT DAN MAKANAN NOMOR 27 TAHUN 2017 TENTANG PENDAFTARAN PANGAN OLAHAN DENGAN RAHMAT TUHAN YANG MAHA ESA
 BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA PERATURAN BADAN PENGAWAS OBAT DAN MAKANAN NOMOR 27 TAHUN 2017 TENTANG PENDAFTARAN PANGAN OLAHAN DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN PENGAWAS
BADAN PENGAWAS OBAT DAN MAKANAN REPUBLIK INDONESIA PERATURAN BADAN PENGAWAS OBAT DAN MAKANAN NOMOR 27 TAHUN 2017 TENTANG PENDAFTARAN PANGAN OLAHAN DENGAN RAHMAT TUHAN YANG MAHA ESA KEPALA BADAN PENGAWAS
Lampiran 1. Struktur Organisasi Direktorat Kesehatan Angkatan Darat
 Lampiran 1. Struktur Organisasi Direktorat Kesehatan Angkatan Darat DITKESAD POKPIM ITDIT SESDITKESAD INFOLAHTA SUBDIT BINCAB SUBDIT BINYANKES SUBDIT BINMATKES SUBDIT BINDUKKES RSPAD LAFI AD LAKESMIL LABIOMED
Lampiran 1. Struktur Organisasi Direktorat Kesehatan Angkatan Darat DITKESAD POKPIM ITDIT SESDITKESAD INFOLAHTA SUBDIT BINCAB SUBDIT BINYANKES SUBDIT BINMATKES SUBDIT BINDUKKES RSPAD LAFI AD LAKESMIL LABIOMED
BERITA NEGARA REPUBLIK INDONESIA
 No.739, 2013 BERITA NEGARA REPUBLIK INDONESIA BADAN PENGAWAS OBAT DAN MAKANAN. Pengawasan. Bahan Obat. Obat Tradisional. Suplemen Kesehatan. Pangan. Pemasukan. PERATURAN KEPALA BADAN PENGAWAS OBAT DAN
No.739, 2013 BERITA NEGARA REPUBLIK INDONESIA BADAN PENGAWAS OBAT DAN MAKANAN. Pengawasan. Bahan Obat. Obat Tradisional. Suplemen Kesehatan. Pangan. Pemasukan. PERATURAN KEPALA BADAN PENGAWAS OBAT DAN
Lampiran 1. Bagan proses Pembuatan Krim / Salep
 Lampiran 1. Bagan proses Pembuatan Krim / Salep Penimbangan Peleburan bahan D ki (F i k) Pencampuran D lt t Pelarutan zat aktif, P t(f i) ph Pencampuran Identifikasi ph Kadar zat berkhasiat Homogenitas
Lampiran 1. Bagan proses Pembuatan Krim / Salep Penimbangan Peleburan bahan D ki (F i k) Pencampuran D lt t Pelarutan zat aktif, P t(f i) ph Pencampuran Identifikasi ph Kadar zat berkhasiat Homogenitas
PERATURAN MENTERI KELAUTAN DAN PERIKANAN REPUBLIK INDONESIA, NOMOR PER. 02/MEN/2010 TENTANG PENGADAAN DAN PEREDARAN PAKAN IKAN
 PERATURAN MENTERI KELAUTAN DAN PERIKANAN REPUBLIK INDONESIA NOMOR PER. 02/MEN/2010 TENTANG PENGADAAN DAN PEREDARAN PAKAN IKAN MENTERI KELAUTAN DAN PERIKANAN REPUBLIK INDONESIA, Menimbang : a. bahwa dalam
PERATURAN MENTERI KELAUTAN DAN PERIKANAN REPUBLIK INDONESIA NOMOR PER. 02/MEN/2010 TENTANG PENGADAAN DAN PEREDARAN PAKAN IKAN MENTERI KELAUTAN DAN PERIKANAN REPUBLIK INDONESIA, Menimbang : a. bahwa dalam
BAB II TINJAUAN PUSTAKA
 BAB II TINJAUAN PUSTAKA 2.1 Pengertian Industri Farmasi. Industri farmasi menurut Surat Keputusan Menteri Kesehatan Nomor. 245/Menkes/V/1990 adalah industri obat jadi dan industri bahan baku obat. Industri
BAB II TINJAUAN PUSTAKA 2.1 Pengertian Industri Farmasi. Industri farmasi menurut Surat Keputusan Menteri Kesehatan Nomor. 245/Menkes/V/1990 adalah industri obat jadi dan industri bahan baku obat. Industri
PERSYARATAN TAMBAHAN LABORATORIUM LINGKUNGAN
 PERSYARATAN TAMBAHAN LABORATORIUM LINGKUNGAN Lampiran I Peraturan Menteri Negara Lingkungan Hidup Nomor : 06 Tahun 2009 Tanggal : 6 April 2009 PERSYARATAN TAMBAHAN LABORATORIUM LINGKUNGAN Persyaratan
PERSYARATAN TAMBAHAN LABORATORIUM LINGKUNGAN Lampiran I Peraturan Menteri Negara Lingkungan Hidup Nomor : 06 Tahun 2009 Tanggal : 6 April 2009 PERSYARATAN TAMBAHAN LABORATORIUM LINGKUNGAN Persyaratan
KEMENTERIAN KELAUTAN DAN PERIKANAN BADAN KARANTINA IKAN, PENGENDALIAN MUTU DAN KEAMANAN HASIL PERIKANAN
 KEMENTERIAN KELAUTAN DAN PERIKANAN BADAN KARANTINA IKAN, PENGENDALIAN MUTU DAN KEAMANAN HASIL PERIKANAN PERATURAN KEPALA BADAN KARANTINA IKAN, PENGENDALIAN MUTU DAN KEAMANAN HASIL PERIKANAN SELAKU OTORITAS
KEMENTERIAN KELAUTAN DAN PERIKANAN BADAN KARANTINA IKAN, PENGENDALIAN MUTU DAN KEAMANAN HASIL PERIKANAN PERATURAN KEPALA BADAN KARANTINA IKAN, PENGENDALIAN MUTU DAN KEAMANAN HASIL PERIKANAN SELAKU OTORITAS
BAB I PENDAHULUAN. A. Latar Belakang Masalah. Furosemid merupakan obat golongan loop diuretik yang banyak digunakan
 BAB I PENDAHULUAN A. Latar Belakang Masalah Furosemid merupakan obat golongan loop diuretik yang banyak digunakan untuk berbagai macam indikasi, diantaranya: antihipertensi, asites, sindrom kekurangan
BAB I PENDAHULUAN A. Latar Belakang Masalah Furosemid merupakan obat golongan loop diuretik yang banyak digunakan untuk berbagai macam indikasi, diantaranya: antihipertensi, asites, sindrom kekurangan
PERATURAN BADAN PENGAWAS OBAT DAN MAKANAN NOMOR... TAHUN... TENTANG PEDOMAN PENGELOLAAN OBAT-OBAT TERTENTU YANG SERING DISALAHGUNAKAN
 Masukan dapat kami terima selambat-lambatnya tanggal 12 Februari 2018 dan diperpanjang sampai dengan 19 Februari 2018 melalui email: 1. wasnapza@yahoo.co.id 2. wasnapza@gmail.com PERATURAN BADAN PENGAWAS
Masukan dapat kami terima selambat-lambatnya tanggal 12 Februari 2018 dan diperpanjang sampai dengan 19 Februari 2018 melalui email: 1. wasnapza@yahoo.co.id 2. wasnapza@gmail.com PERATURAN BADAN PENGAWAS
KEPUTUSAN MENTERI PERTANIAN NOMOR: 695/Kpts/TN.260/8/96 TENTANG SYARAT DAN TATA CARA PENDAFTARAN DAN PENGUJIAN MUTU OBAT HEWAN MENTERI PERTANIAN,
 KEPUTUSAN MENTERI PERTANIAN NOMOR: 695/Kpts/TN.260/8/96 TENTANG SYARAT DAN TATA CARA PENDAFTARAN DAN PENGUJIAN MUTU OBAT HEWAN MENTERI PERTANIAN, Menimbang : a. bahwa untuk menjamin mutu obat hewan yang
KEPUTUSAN MENTERI PERTANIAN NOMOR: 695/Kpts/TN.260/8/96 TENTANG SYARAT DAN TATA CARA PENDAFTARAN DAN PENGUJIAN MUTU OBAT HEWAN MENTERI PERTANIAN, Menimbang : a. bahwa untuk menjamin mutu obat hewan yang
