BAB III HASIL PENELITIAN
|
|
|
- Johan Kusuma
- 8 tahun lalu
- Tontonan:
Transkripsi
1 BAB III HASIL PENELITIAN A. Gambaran Umum Buku Teks Kimia SMA Kelas X 1. Identitas Buku Teks Kimia SMA Kelas X Buku yang menjadi obyek penelitian peneliti adalah buku teks kimia SMA kelas X jilid 1 materi pokok Stoikiometri karangan Unggul Sudarmo yang telah diterbitkan bulan September 2013 oleh Erlangga. Buku ini diterbitkan menyesuaikan kurikulum Peneliti memilih buku teks kimia SMA kelas X karangan Unggul Sudarmo sebagai obyek penelitian karena dari Kementerian Pendidikan dan Kebudayaan belum mengeluarkan atau menerbitkan buku teks kimia SMA kelas X yang sesuai dengan perubahan Kurikulum yaitu Kurikulum Buku tersebut banyak dipakai di Sekolah Menengah Atas wilayah Semarang. Sebagai pembanding peneliti memilih buku teks Kimia SMA kelas X jilid 1 karangan Unggul Sudarmo yang diterbitkan bulan Mei Deskripsi Umum Isi Buku Teks Kimia SMA Kelas X Isi buku teks kimia SMA kelas X jilid 1 karangan Unggul Sudarmo yang diterbitkan oleh Erlangga Bulan September 2013 terdapat 5 bab antara lain : a. Struktur atom dan sistem periodik unsur b. Ikatan kimia c. Larutan elektrolit, non-elektrolit dan reaksi redoks, d. Rumus kimia tata nama persamaan reaksi dan hukum dasar kimia e. Stoikiometri Sedangkan buku teks kimia SMA kelas X jilid 1 karangan Unggul Sudarmo yang diterbitkan oleh Erlangga bulan Mei 2013 terdapat 6 bab yaitu : a. Struktur atom dan sistem periodik unsur b. Ikatan kimia c. Rumus kimia tata nama persamaan reaksi dan hukum dasar kimia d. Stoikiometri e. Larutan elektrolit non-elektrolit dan reaksi redoks 37
2 f. Hidrokarbon dan minyak bumi Setelah peneliti memaparkan gambaran umum isi buku teks kimia kelas X, peneliti memfokuskan pada Materi Stoikiometri yang akan di analisis kesesuaiannya dengan KI dan KD Kurikulum a. Kesesuaian Materi Pokok Stoikiometri dengan KI dan KD Kurikulum 2013 Kesesuaian materi pokok stoikiometri dengan Kompetensi Inti dan Kompetensi Dasar yaitu seperti yang tercantum pada tabel 3.1 berikut : Tabel 3.1 Kesesuaian Materi Pokok Stoikiometri dengan KI 3 : Memahami, menerapkan, menganalisis pengetahuan faktual, konseptual, prosedural berdasarkan rasa ingin tahunya tentang ilmu pengetahuan, teknologi, seni, budaya, dan humaniora dengan wawasan kemanusiaan, kebangsaan, kenegaraan, dan peradaban terkait penyebab fenomena dan kejadian, serta menerapkan pengetahuan prosedural pada bidang kajian yang spesifik sesuai dengan bakat dan minatnya untuk memecahkan masalah. KI 4 : Mengolah, menalar, dan menyaji dalam ranah konkret dan ranah abstrak terkait dengan pengembangan dari yang dipelajarinya di sekolah secara mandiri, dan mampu menggunakan metoda sesuai kaidah keilmuan KD 3.11 : (1) Menerapkan konsep massa atom relatif (2) Massa molekul relatif (3) Persamaan reaksi (4) Hukum-hukum dasar kimia (5) Konsep mol untuk menyelesaikan perhitungan kimia KD 4.11 : (1) Mengolah dan menganalisis data terkait massa atom relatif (2) Massa molekul relatif (3) Persamaan reaksi (4) Hukum-hukum dasar kimia 38
3 (5) Konsep mol untuk menyelesaikan perhitungan kimia. Materi Perbutir Kesesuaian dengan Poin Kompetensi Dasar 3.11 Massa atom rata-rata (1) & (2) Massa atom relatif (1) & (2) Kesesuaian dengan Poin Kompetensi Dasar 4.11 (1) & (2) (1) & (2) Massa molekul relatif & massa rumus relatif (Mr) (2) (2) Massa molar (5) (5) Volume molar (5) (5) Hipotesis Avogadro (4) (4) Hukum gas ideal (4) (4) Interkonversi Mol- Gram-Volume Penentuan rumus empiris & rumus molekul (5) (5) (5) (5) Persentase unsur dalam senyawa Persen massa (5) (5) Persen volume (5) (5) Molaritas (M) (5) (5) Molalitas (m) (5) (5) Fraksi mol (X) (5) (5) Pengenceran Membuat larutan dengan konsentrasi tertantu Membuat larutan dengan zat padat (air kristal) Stoikiometri dalam (3) & (5) (3) & (5) 39
4 persamaan reaksi Air Kristal Pereaksi pembatas (3) (3) b. Kesesuaian Materi Pokok Stoikiometri dalam Buku Teks Kimia SMA Kelas X Jilid 1 Karangan Unggul Sudarmo Terbitan Erlangga September 2013 dengan Tujuan Pembelajaran Pada materi pokok stoikiometri mencakup tujuh pembahasan yaitu seperti yang tercantum pada tabel 3.2 berikut : Tabel 3.2 Materi Pokok & Tujuan Pembelajaran dalam Bab Stoikiometri Materi Pokok 1. Massa Atom : a. Massa atom rata-rata b. Massa atom relatif (Ar) c. Massa molekul relatif & massa rumus relatif (Mr) 2. Mol : a. Massa molar b. Volume molar 3. Hukum-hukum Tentang Gas a. Hipotesis Avogadro b. Hukum gas ideal 4. Interkonversi Mol-Gram- Volume 5. Perhitungan Kimia a. Penentuan rumus empiris & rumus molekul b. Persentase unsur dalam senyawa 6. Kadar Zat Dalam Campuran a. Persen (%) 1) Persen massa 2) Persen volume b. Bagian Per Juta (bpj) Tujuan Pembelajaran Setelah mempelajari ini, siswa diharapkan mampu: 1. Menghitung jumlah mol, jumlah partikel, massa dan volume gas. (sesuai dengan KD 3.11 & KD 4.11 poin 5) 2. Menentukan rumus empiris, rumus molekul, dan air Kristal. (sesuai dengan KD 3.11 dan KD 4.11 poin 5) 3. Menghitung kadar zat dalam senyawa. 4. Menentukan pereaksi pembatas. (sesuai dengan KD 3.11 & KD 4.11 poin 3) 40
5 atau Part Permillion (ppm) 1) Molaritas (M) 2) Molalitas (m) 3) Fraksi mol (X) c. Pengenceran d. Pencampuran larutan dengan konsentrasi berbeda : Membuat larutan dengan konsentrasi tertentu Membuat larutan dari zat padat (air kristal) 7. Perhitungan Kimia dalam Persamaan Reaksi a. Stoikiometri Persamaan Reaksi b. Air Kristal c. Pereaksi Pembatas c. Kesesuaian Materi Pokok Stoikiometri dalam Buku Teks Kimia SMA Kelas X Jilid 1 Karangan Unggul Sudarmo Terbitan Erlangga Mei 2013 dengan Tujuan Pembelajaran Pada materi pokok stoikiometri mencakup yaitu seperti yang tercantum pada tabel berikut : Tabel 3.3 Materi Pokok & Tujuan Pembelajaran dalam Bab Stoikiometri Materi Pokok 1. Massa Atom a. Massa atom rata-rata b. Massa atom relatif (Ar) c. Massa molekul relatif & massa rumus relatif (Mr) 2. Mol a. Massa molar b. Massa volum 3. Hukum-hukum Tentang Gas a. Hipotesis Avogadro b. Hukum gas ideal 4. Interkonversi Mol-Gram- Volume 5. Perhitungan Kimia enam pembahasan Tujuan Pembelajaran Setelah mempelajari materi ini, siswa diharapkan mampu: 1. Menghitung jumlah mol, jumlah partikel, massa dan volume gas (sesuai dengan KD 3.11 & KD 4.11 poin 5) 2. Menentukan rumus empiris, rumus molekul, dan air Kristal (sesuai dengan KD 3.11 & KD 4.11 poin 41
6 a. Penentuan rumus empiris dan rumus molekul b. Persentase unsur dalam senyawa 6. Perhitungan Kimia dalam Persamaan Reaksi a. Stoikiometri persamaan reaksi b. Air Kristal c. Pereaksi pembatas 3) 3. Menghitung kadar zat dalam senyawa 4. Menentukan pereaksi pembatas (sesuai dengan KD 3.11 & KD 4.11 poin 3) B. Hasil Telaah Konsep-konsep Kimia dalam Buku Teks Kimia SMA Kelas X Jilid 1 Karangan Unggul Sudarmo terbitan Erlangga Bulan September dan Mei Hasil pembahasan atau deskripsi umum Materi Pokok Stoikiometri di atas dari buku teks Kimia Kelas X Materi Pokok Stoikiometri yang diterbitkan bulan September mencakup tujuh pembahasan, sedangkan buku yang diterbitkan bulan Mei mencakup enam pembahasan materi tidak mencantumkan materi kadar zat dalam campuran. Hasil telaah Konsep-konsep Kimia dalam Buku Teks Kimia tersebut seperti pada tabel 3.4. Tabel 3.4 Hasil Telaah Konsep-konsep Kimia Konsep yang Diajarkan (Sumber Buku Kimia Universitas) Metode paling akurat untuk menentukan Massa Atom dan massa molekul adalah spektrometri massa. Massa atom rata-rata: dalam Buku Teks Kimia Kelas X Buku Teks Kimia Kelas X Karangan Unggul Sudarmo terbitan Erlangga bulan September Massa Atom dapat ditentukan menggunakan spektrometer massa. Massa atom ratarata: Buku Teks Kimia Kelas X Karangan Unggul Sudarmo terbitan Erlangga bulan Mei Massa atom dapat ditentukan menggunakan spektrometer massa. Massa atom ratarata: 42
7 Massa atom relatif merupakan massa atom rata-rata terhadap atom C-12 Massa relatif: ArX atom Massa atom relatif : ArX massa molekul adalah jumlah dari massamassa atom (dalam sma) dalam suatu molekul. Massa molekul relatif & massa rumus relatif (Mr): A x B y Massa molekul relatif & massa rumus relatif (Mr) : A x B y Massa molar adalah massa (dalam gram atau kilogram) dari 1 mol entitas seperti atom atau molekul zat. Massa molar Satuan massa molar gram mol - 1 (gram/mol). Massa molar (M)= massa 1 mol zat A x B y = (Mr A x B y ) gram. Satuan massa molar gram mol - 1 (gram/mol). Massa molar (M)= massa 1 mol zat A x B y = (Mr A x B y ) gram. Volume molar gas V n jumlah mol gas hukum gas ideal Volum molar adalah volume 1 mol gas pada suhu dan tekanan tertentu. V = n mol 22,4 L/mol Volum molar adalah volume 1 mol gas pada suhu dan tekanan tertentu. V = n mol 22,4 L/mol V volume gas pada 0 P T, K R m mol -1 K -1 at Hukum avogadro Hipotesis Avogadro Hipotesis Avogadro 43
8 bahwa pada tekanan dan suhu konstan, volume suatu gas berbanding langsung dengan jumlah mol gas yang ada Persamaan gas ideal : PV = nrt Persen komposisi senyawa Persen komposisi adalah persentase massa dari tiap unsur yang terkandung dalam suatu senyawa. Persen komposisi suatu unsur bahwa pada suhu dan tekanan yang sama, sejumlah volume yang sama suatu gas (sembarang gas) mengandung sejumlah molekul yang sama. Berarti apabila jumlah molekulnya sama maka jumlah mol gas akan sama pula. Perbandingan volume gas akan sama dengan perbandingan mol gas. V 1 : V 2 = n 1 : n 2 Persamaan gas ideal : PV = nrt Interkonversi Mol-Gram- Volume Persentase unsur dalam senyawa : bahwa pada suhu dan tekanan yang sama, sejumlah volume yang sama suatu gas (sembarang gas) mengandung sejumlah molekul yang sama. Berarti apabila jumlah molekulnya sama maka jumlah mol gas akan sama pula. Perbandingan volume gas akan sama dengan perbandingan mol gas. V 1 : V 2 = n 1 : n 2 Persamaan gas ideal : PV = nrt Interkonversi Mol- Gram-Volume Persentase unsur dalam senyawa : Persen massa massa suatu zat (dalam gram) yang terdapat dalam setiap
9 gram campuran. Persen volume volume zat yang terdapat dalam setiap 100 bagian volume campuran. ppm Bagian per juta, 10 6 yaitu kadar zat yang banyaknya bagian zat yang terdapat dalam setiap satu juta bagian campuran Ppm Molaritas atau konsentrasi molar adalah jumlah mol zat terlarut dalam 1 liter larutan. Persamaan : M Molaritas atau kemolaran suatu larutan banyaknya mol zat terlarut yang terlarut di dalam satu liter larutan. Molalitas sebagai jumlah mol zat dengan : M= molaritas (mol/l atau mol dm -3 ) n = mol zat terlarut (mol) V = volume larutan (liter atau dm 3 ) Molalitas atau kemolalan 45
10 terlarut per kilogram pelarut, M banyaknya mol zat terlarut di dalam setiap 1000 gram pelarut. dengan : m = molalitas larutan n = jumlah mol zat terlarut P = massa pelarut (gram) Fraksi mol suatu zat dalam campuran adalah jumlah mol zat itu dibagi jumlah keseluruhan mol yang ada. X 1 X 2 Fraksi mol suatu zat di dalam suatu larutan perbandingan banyaknya mol dari zat tersebut terhadap jumlah mol seluruh komponen dalam larutan. X A X B Proses pengenceran adalah mencampur larutan pekat (konsentrasi tinggi) dengan cara menambahkan pelarut agar diperoleh volume akhir yang Dengan : n A = mol zat A n B = mol zat B X A = fraksi mol zat A X B = fraksi mol zat B Pengenceran larutan adalah penambahan zat pelarut ke dalam suatu larutan. Dari rumus Molaritas : 46
11 lebih besar. M awal V awal = M akhir V akhir Pereaksi pembatas adalah reaktan yang pertama kali habis digunakan pada reaksi kimia V 1 M 1 = V 2 M 2 Pencampuran larutan dengan konsentrasi berbeda, n 1 + n 2 = n campuran maka, (M 1 V 1 ) +(M 2 V 2 ) = (M V ) campuran Air Kristal adalah air yang terjebak di dalam kristal. Kristal merupakan zat padat yang bentuknya teratur Pereaksi pembatas adalah pereaksi yang membatasi hasil reaksi karena habis bereaksi Air Kristal adalah air yang terjebak di dalam kristal. Kristal merupakan zat padat yang bentuknya teratur Pereaksi pembatas adalah pereaksi yang membatasi hasil reaksi karena habis bereaksi 47
BAB IV ANALISIS HASIL PENELITIAN
 BAB IV ANALISIS HASIL PENELITIAN Bab ini peneliti menganalisis hasil penelitian, yaitu isi buku Teks Kimia SMA Kelas X jilid 1 Materi Pokok Stoikiometri karangan Unggul Sudarmo yang diterbitkan oleh Erlangga
BAB IV ANALISIS HASIL PENELITIAN Bab ini peneliti menganalisis hasil penelitian, yaitu isi buku Teks Kimia SMA Kelas X jilid 1 Materi Pokok Stoikiometri karangan Unggul Sudarmo yang diterbitkan oleh Erlangga
RENCANA PELAKSANAAN PEMBELAJARAN (RPP)
 RENCANA PELAKSANAAN PEMBELAJARAN (RPP) Satuan Pendidikan Kelas/Semester Mata Pelajaran Materi Pokok Waktu : SMA Muhammadiyah I Metro : X/Genap : Kimia - peminatan : - Massa atom relative (Ar) dan massa
RENCANA PELAKSANAAN PEMBELAJARAN (RPP) Satuan Pendidikan Kelas/Semester Mata Pelajaran Materi Pokok Waktu : SMA Muhammadiyah I Metro : X/Genap : Kimia - peminatan : - Massa atom relative (Ar) dan massa
Tugas Kimia STOIKIOMETRI
 Tugas Kimia STOIKIOMETRI NAMA ANGGOTA : 1. Nyoman Dharma Triyasa (10) 2. Komang Jnana Shindu Putra (17) 3. I.G.A Dharsasasmitha Yani (19) 4. Ni Putu Riska Valentini (25) 5. Putu Ayu Rosita Octaviani (26)
Tugas Kimia STOIKIOMETRI NAMA ANGGOTA : 1. Nyoman Dharma Triyasa (10) 2. Komang Jnana Shindu Putra (17) 3. I.G.A Dharsasasmitha Yani (19) 4. Ni Putu Riska Valentini (25) 5. Putu Ayu Rosita Octaviani (26)
Massa atom merupakan massa dari atom dalam satuan massa atom (sma).
 Bab 3 1. Apakah yang dimaksud dengan Ar dan Mr? 2. Apakah yang dimaksud dengan mol? 3. Bagaimana cara mencari mol jika diketahui massa zat, volume (dalam STP), dan jumah molekul/partikelnya? 4. Berapa
Bab 3 1. Apakah yang dimaksud dengan Ar dan Mr? 2. Apakah yang dimaksud dengan mol? 3. Bagaimana cara mencari mol jika diketahui massa zat, volume (dalam STP), dan jumah molekul/partikelnya? 4. Berapa
KIMIA TERAPAN STOIKIOMETRI DAN HUKUM-HUKUM KIMIA Haris Puspito Buwono
 KIMIA TERAPAN STOIKIOMETRI DAN HUKUM-HUKUM KIMIA Haris Puspito Buwono Semester Gasal 2012/2013 STOIKIOMETRI 2 STOIKIOMETRI adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif dari komposisi
KIMIA TERAPAN STOIKIOMETRI DAN HUKUM-HUKUM KIMIA Haris Puspito Buwono Semester Gasal 2012/2013 STOIKIOMETRI 2 STOIKIOMETRI adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif dari komposisi
KRITERIA KETUNTASAN MINIMUM KIMIA KELAS X TAHUN PELAJARAN 2013/2014
 PEMERINTAH KABUPATEN BANTUL DINAS PENDIDIKAN SEKOLAH MENENGAH ATAS (SMA) NEGERI 1 KASIHAN Jalan Bugisan Selatan, Yogyakarta Telepon (0274) 376067, Faksimile 376067, Kasihan 55181 e-mail : [email protected]
PEMERINTAH KABUPATEN BANTUL DINAS PENDIDIKAN SEKOLAH MENENGAH ATAS (SMA) NEGERI 1 KASIHAN Jalan Bugisan Selatan, Yogyakarta Telepon (0274) 376067, Faksimile 376067, Kasihan 55181 e-mail : [email protected]
Konsep Mol. 1. Jumlah Partikel Dalam 1 Mol Zat
 Konsep Mol Setiap zat yang ada di alam tersusun atas partikel-partikel bentuk atom, molekul, dan ion. Ukuran dan massa partikel-partikel zat tersebut sangat kecil sehingga kita kesulitan untuk mengukurnya.
Konsep Mol Setiap zat yang ada di alam tersusun atas partikel-partikel bentuk atom, molekul, dan ion. Ukuran dan massa partikel-partikel zat tersebut sangat kecil sehingga kita kesulitan untuk mengukurnya.
Hukum Dasar Kimia Dan Konsep Mol
 A. PENDAHULUAN Hukum Dasar Kimia Dan Konsep Mol Hukum dasar kimia merupakan hukum dasar yang digunakan dalam stoikiometri (perhitungan kimia), antara lain: 1) Hukum Lavoisier atau hukum kekekalan massa.
A. PENDAHULUAN Hukum Dasar Kimia Dan Konsep Mol Hukum dasar kimia merupakan hukum dasar yang digunakan dalam stoikiometri (perhitungan kimia), antara lain: 1) Hukum Lavoisier atau hukum kekekalan massa.
STOIKIOMETRI. Massa molekul relatif suatu zat sama dengan jumlah massa atom relatif atomatom penyusun molekul zat tersebut.
 STOIKIOMETRI Istilah STOIKIOMETRI berasal dari kata-kata Yunani yaitu Stoicheion (partikel) dan metron (pengukuran). STOIKIOMETRI akhirnya mengacu kepada cara perhitungan dan pengukuran zat serta campuran
STOIKIOMETRI Istilah STOIKIOMETRI berasal dari kata-kata Yunani yaitu Stoicheion (partikel) dan metron (pengukuran). STOIKIOMETRI akhirnya mengacu kepada cara perhitungan dan pengukuran zat serta campuran
Tabel Hasil Analisis Kebenaran Konsep pada Objek Penelitian
 202 Lampiran B Label Pengertian stoikiometri Pengertian massa atom Perhitungan massa atom Tabel Hasil Analisis pada Objek Penelitian Penjelasan pada Stoikiometri berasal dari bahasa Yunani (stoicheion,
202 Lampiran B Label Pengertian stoikiometri Pengertian massa atom Perhitungan massa atom Tabel Hasil Analisis pada Objek Penelitian Penjelasan pada Stoikiometri berasal dari bahasa Yunani (stoicheion,
BAB V PERHITUNGAN KIMIA
 BAB V PERHITUNGAN KIMIA KOMPETENSI DASAR 2.3 : Menerapkan hukum Gay Lussac dan hukum Avogadro serta konsep mol dalam menyelesaikan perhitungan kimia (stoikiometri ) Indikator : 1. Siswa dapat menghitung
BAB V PERHITUNGAN KIMIA KOMPETENSI DASAR 2.3 : Menerapkan hukum Gay Lussac dan hukum Avogadro serta konsep mol dalam menyelesaikan perhitungan kimia (stoikiometri ) Indikator : 1. Siswa dapat menghitung
Stoikiometri. Berasal dari kata Stoicheion (partikel) dan metron (pengukuran). Cara perhitungan dan pengukuran zat serta campuran kimia.
 Stoikiometri Berasal dari kata Stoicheion (partikel) dan metron (pengukuran). Cara perhitungan dan pengukuran zat serta campuran kimia. Bilangan Avogadro Stoikometri: pengukuran kuantitatif sehingga perlu
Stoikiometri Berasal dari kata Stoicheion (partikel) dan metron (pengukuran). Cara perhitungan dan pengukuran zat serta campuran kimia. Bilangan Avogadro Stoikometri: pengukuran kuantitatif sehingga perlu
LOGO. Stoikiometri. Tim Dosen Pengampu MK. Kimia Dasar
 LOGO Stoikiometri Tim Dosen Pengampu MK. Kimia Dasar Konsep Mol Satuan jumlah zat dalam ilmu kimia disebut mol. 1 mol zat mengandung jumlah partikel yang sama dengan jumlah partikel dalam 12 gram C 12,
LOGO Stoikiometri Tim Dosen Pengampu MK. Kimia Dasar Konsep Mol Satuan jumlah zat dalam ilmu kimia disebut mol. 1 mol zat mengandung jumlah partikel yang sama dengan jumlah partikel dalam 12 gram C 12,
LARUTAN. Zat terlarut merupakan komponen yang jumlahnya sedikit, sedangkan pelarut adalah komponen yang terdapat dalam jumlah banyak.
 LARUTAN Larutan merupakan campuran yang homogen,yaitu campuran yang memiliki komposisi merata atau serba sama di seluruh bagian volumenya. Suatu larutan mengandung dua komponen atau lebih yang disebut
LARUTAN Larutan merupakan campuran yang homogen,yaitu campuran yang memiliki komposisi merata atau serba sama di seluruh bagian volumenya. Suatu larutan mengandung dua komponen atau lebih yang disebut
STOIKIOMETRI LARUTAN. Andian Ari Anggraeni, M.Sc
 STOIKIOMETRI LARUTAN Andian Ari Anggraeni, M.Sc A.1. MASSA ATOM RELATIF (A r ) DAN MASSA MOLEKUL RELATIF (M r ) Dari percobaan diketahui bahwa perbandingan massa hidrogen dan oksigen dalam air adalah 1
STOIKIOMETRI LARUTAN Andian Ari Anggraeni, M.Sc A.1. MASSA ATOM RELATIF (A r ) DAN MASSA MOLEKUL RELATIF (M r ) Dari percobaan diketahui bahwa perbandingan massa hidrogen dan oksigen dalam air adalah 1
STOIKIOMETRI. Purwanti Widhy H, M.Pd
 STOIKIOMETRI Purwanti Widhy H, M.Pd [email protected] Menentukan jumlah partikel dan jumlah mol Jumlah molx(n) = jumlah partikelx L 1 mol = L partikel L= bilangan avogadro (6.02 x 10 23 /mol)
STOIKIOMETRI Purwanti Widhy H, M.Pd [email protected] Menentukan jumlah partikel dan jumlah mol Jumlah molx(n) = jumlah partikelx L 1 mol = L partikel L= bilangan avogadro (6.02 x 10 23 /mol)
STOIKIOMETRI Konsep mol
 STOIKIOMETRI Konsep mol Dalam hukum-hukum dasar materi ditegaskan bahwa senyawa terbentuk dari unsur bukan dengan perbandingan sembarang tetapi dalam jumlah yang spesifik, demikian juga reaksi kimia antara
STOIKIOMETRI Konsep mol Dalam hukum-hukum dasar materi ditegaskan bahwa senyawa terbentuk dari unsur bukan dengan perbandingan sembarang tetapi dalam jumlah yang spesifik, demikian juga reaksi kimia antara
Hubungan koefisien dalam persamaan reaksi dengan hitungan
 STOIKIOMETRI Pengertian Stoikiometri adalah ilmu yang mempelajari dan menghitung hubungan kuantitatif dari reaktan dan produk dalam reaksi kimia (persamaan kimia) Stoikiometri adalah hitungan kimia Hubungan
STOIKIOMETRI Pengertian Stoikiometri adalah ilmu yang mempelajari dan menghitung hubungan kuantitatif dari reaktan dan produk dalam reaksi kimia (persamaan kimia) Stoikiometri adalah hitungan kimia Hubungan
Fraksi mol adalah perbandingan antara jumiah mol suatu komponen dengan jumlah mol seluruh komponen yang terdapat dalam larutan.
 Konsentrasi Larutan Ditulis oleh Redaksi chem-is-try.org pada 02-05-2009 Konsentrasi merupakan cara untuk menyatakan hubungan kuantitatif antara zat terlarut dan pelarut. Menyatakan konsentrasi larutan
Konsentrasi Larutan Ditulis oleh Redaksi chem-is-try.org pada 02-05-2009 Konsentrasi merupakan cara untuk menyatakan hubungan kuantitatif antara zat terlarut dan pelarut. Menyatakan konsentrasi larutan
Sulistyani M.Si
 Sulistyani M.Si Email:[email protected] + Larutan terdiri dari pelarut (solvent) dan zat terlarut (solute). Jumlah zat terlarut dalam suatu larutan dinyatakan dengan konsentrasi larutan. Secara kuantitatif,
Sulistyani M.Si Email:[email protected] + Larutan terdiri dari pelarut (solvent) dan zat terlarut (solute). Jumlah zat terlarut dalam suatu larutan dinyatakan dengan konsentrasi larutan. Secara kuantitatif,
Stoikhiometri : dan metron = mengukur. Membahas tentang : senyawa) senyawa (stoikhiometri. (stoikhiometri. reaksi)
 STOIKHIOMETRI Stoikhiometri : Dari kata Stoicheion = unsur dan metron = mengukur Membahas tentang : hub massa antar unsur dalam suatu senyawa (stoikhiometri senyawa) dan antar zat dalam suatu reaksi (stoikhiometri
STOIKHIOMETRI Stoikhiometri : Dari kata Stoicheion = unsur dan metron = mengukur Membahas tentang : hub massa antar unsur dalam suatu senyawa (stoikhiometri senyawa) dan antar zat dalam suatu reaksi (stoikhiometri
Amin Fatoni, M.Si 2008
 Amin Fatoni, M.Si 2008 Massa rumus (Mr) = massa molekul = bobot molekul (BM) merupakan penjumlahan dari massa atom penyusun-penyusunnya Contoh: Air - H 2 O 1 atom Oksigen 2(1.0079 u) + 15.9994 u = 18.0152
Amin Fatoni, M.Si 2008 Massa rumus (Mr) = massa molekul = bobot molekul (BM) merupakan penjumlahan dari massa atom penyusun-penyusunnya Contoh: Air - H 2 O 1 atom Oksigen 2(1.0079 u) + 15.9994 u = 18.0152
Sifat Koligatif Larutan (Bagian I)
 KIMIA KELAS XII IPA - KURIKULUM GABUNGAN 01 Sesi NGAN Sifat Koligatif Larutan (Bagian I) Sebelum mempelajari sifat koligatif larutan, terlebih dahulu kita akan meninjau kembali sedikit pengetahuan mengenai
KIMIA KELAS XII IPA - KURIKULUM GABUNGAN 01 Sesi NGAN Sifat Koligatif Larutan (Bagian I) Sebelum mempelajari sifat koligatif larutan, terlebih dahulu kita akan meninjau kembali sedikit pengetahuan mengenai
STOKIOMETRI. Kimia Kelas X
 STOKIOMETRI Kimia Kelas X SEKOLAH MENENGAH ATAS NEGERI 12 SURABAYA 2015 STOKIOMETRI STOKIOMETRI Pada materi stokiometri, kita akan mempelajari beberapa hal seperti persamaan reaksi, hukum-hukum dasar kimia,
STOKIOMETRI Kimia Kelas X SEKOLAH MENENGAH ATAS NEGERI 12 SURABAYA 2015 STOKIOMETRI STOKIOMETRI Pada materi stokiometri, kita akan mempelajari beberapa hal seperti persamaan reaksi, hukum-hukum dasar kimia,
STOIKIOMETRI. STOIKIOMETRI adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif dari komposisi zat-zat kimia dan reaksi-reaksinya.
 STOIKIOMETRI STOIKIOMETRI adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif dari komposisi zat-zat kimia dan reaksi-reaksinya. 1.HUKUM KEKEKALAN MASSA = HUKUM LAVOISIER "Massa zat-zat sebelum
STOIKIOMETRI STOIKIOMETRI adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif dari komposisi zat-zat kimia dan reaksi-reaksinya. 1.HUKUM KEKEKALAN MASSA = HUKUM LAVOISIER "Massa zat-zat sebelum
SILABUS. Agustien Zulaidah,ST,MT. Kompetensi Dasar Indikator Materi Pokok & Sub Materi pokok. Alokasi Waktu pengalaman belajar
 SILABUS Mata Kuliah : Azas Rekayasa Proses Kode mata Kuliah / SKS : MTK 113 / 2 ( Dua ) Semester : II ( Dua ) Deskripsi Mata Kuliah : Mata kuliah Azas Rekayasa Proses ini mata kuliah yang membahas tentang
SILABUS Mata Kuliah : Azas Rekayasa Proses Kode mata Kuliah / SKS : MTK 113 / 2 ( Dua ) Semester : II ( Dua ) Deskripsi Mata Kuliah : Mata kuliah Azas Rekayasa Proses ini mata kuliah yang membahas tentang
BAB 1 SIFAT KOLIGATIF LARUTAN. STANDART KOMPETENSI Mendeskripsikan sifat-sifat larutan, metode pengukuran serta terapannya.
 BAB 1 SIFAT KOLIGATIF LARUTAN STANDART KOMPETENSI Mendeskripsikan sifat-sifat larutan, metode pengukuran serta terapannya. KOMPETENSI DASAR Mendeskripsikan penurunan tekanan uap, kenaikan titik didih,
BAB 1 SIFAT KOLIGATIF LARUTAN STANDART KOMPETENSI Mendeskripsikan sifat-sifat larutan, metode pengukuran serta terapannya. KOMPETENSI DASAR Mendeskripsikan penurunan tekanan uap, kenaikan titik didih,
STOKIOMETRI BAB. B. Konsep Mol 1. Hubungan Mol dengan Jumlah Partikel. Contoh: Jika Ar Ca = 40, Ar O = 16, Ar H = 1, tentukan Mr Ca(OH) 2!
 BAB 7 STOKIOMETRI A. Massa Molekul Relatif Massa Molekul Relatif (Mr) biasanya dihitung menggunakan data Ar masing-masing atom yang ada dalam molekul tersebut. Mr senyawa = (indeks atom x Ar atom) Contoh:
BAB 7 STOKIOMETRI A. Massa Molekul Relatif Massa Molekul Relatif (Mr) biasanya dihitung menggunakan data Ar masing-masing atom yang ada dalam molekul tersebut. Mr senyawa = (indeks atom x Ar atom) Contoh:
KONSEP MOL DAN STOIKIOMETRI
 BAB V KONSEP MOL DAN STOIKIOMETRI Dalam ilmu fisika, dikenal satuan mol untuk besaran jumlah zat. Dalam bab ini, akan dibahas mengenai konsep mol yang mendasari perhitungan kimia (stoikiometri). A. KONSEP
BAB V KONSEP MOL DAN STOIKIOMETRI Dalam ilmu fisika, dikenal satuan mol untuk besaran jumlah zat. Dalam bab ini, akan dibahas mengenai konsep mol yang mendasari perhitungan kimia (stoikiometri). A. KONSEP
Kompetensi Pengetahuan dan Kompetensi Keterampilan dirumuskan sebagai berikut, yaitu siswa mampu:
 No. Dokumen : F/751/WKS1/P/6 No. Revisi : 1 Tanggal Berlaku : 1 Juli 2016 KOMPETENSI INTI DAN KOMPTENSI DASAR KIMIA SMA/MA KELAS: XI Tujuan kurikulum mencakup empat kompetensi, yaitu (1) kompetensi sikap
No. Dokumen : F/751/WKS1/P/6 No. Revisi : 1 Tanggal Berlaku : 1 Juli 2016 KOMPETENSI INTI DAN KOMPTENSI DASAR KIMIA SMA/MA KELAS: XI Tujuan kurikulum mencakup empat kompetensi, yaitu (1) kompetensi sikap
HUKUM DASAR KIMIA. 2CUO. 28GRAM NITROGEN 52 GRAM MAGNESIUM NITRIDA 3 MG + N 2 MG 3 N 2
 HUKUM DASAR KIMIA. 2CUO. 28GRAM NITROGEN 52 GRAM MAGNESIUM NITRIDA 3 MG + N 2 MG 3 N 2 HUKUM DASAR KIMIA 1) Hukum Kekekalan Massa ( Hukum Lavoisier ). Yaitu : Dalam sistem tertutup, massa zat sebelum
HUKUM DASAR KIMIA. 2CUO. 28GRAM NITROGEN 52 GRAM MAGNESIUM NITRIDA 3 MG + N 2 MG 3 N 2 HUKUM DASAR KIMIA 1) Hukum Kekekalan Massa ( Hukum Lavoisier ). Yaitu : Dalam sistem tertutup, massa zat sebelum
PERCOBAAN I PEMBUATAN DAN PENENTUAN KONSENTRASI LARUTAN
 PERCOBAAN I PEMBUATAN DAN PENENTUAN KONSENTRASI LARUTAN I. TUJUAN PERCOBAAN Tujuan percobaan praktikum ini adalah agar praktikan dapat membuat larutan dengan konsentrasi tertentu, mengencerkan larutan,
PERCOBAAN I PEMBUATAN DAN PENENTUAN KONSENTRASI LARUTAN I. TUJUAN PERCOBAAN Tujuan percobaan praktikum ini adalah agar praktikan dapat membuat larutan dengan konsentrasi tertentu, mengencerkan larutan,
SILABUS MATA PELAJARAN KIMIA (BIDANG KEAHLIAN AGRIBISNIS DAN AGROTEKNOLOGI)
 SILABUS MATA PELAJARAN KIMIA (BIDANG KEAHLIAN AGRIBISNIS DAN AGROTEKNOLOGI) Satuan Pendidikan : SMK Kelas : X Kompetensi Inti KI 1 : Menghayati dan mengamalkan ajaran agama yang dianutnya KI 2 : Menghayati
SILABUS MATA PELAJARAN KIMIA (BIDANG KEAHLIAN AGRIBISNIS DAN AGROTEKNOLOGI) Satuan Pendidikan : SMK Kelas : X Kompetensi Inti KI 1 : Menghayati dan mengamalkan ajaran agama yang dianutnya KI 2 : Menghayati
MODUL STOIKIOMETRI 1
 MODUL STOIKIOMETRI 1 1. Pengertian Mol Mol merupakan suatu satuan jumlah, yang berasal dari kata moles yang artinya sejumlah massa / sejumlah kecil massa, hampir sama dengan lusin. 1 mol = 6,02 X 10 23
MODUL STOIKIOMETRI 1 1. Pengertian Mol Mol merupakan suatu satuan jumlah, yang berasal dari kata moles yang artinya sejumlah massa / sejumlah kecil massa, hampir sama dengan lusin. 1 mol = 6,02 X 10 23
Larutan dan Konsentrasi
 Larutan dan Konsentrasi Tujuan Pembelajaran Mahasiswa memahami konsep larutan Mahasiswa memahami konsep perhitungan konsentrasi Pentingnya perhitungan konsentrasi Pentingnya memahami sifat larutan dan
Larutan dan Konsentrasi Tujuan Pembelajaran Mahasiswa memahami konsep larutan Mahasiswa memahami konsep perhitungan konsentrasi Pentingnya perhitungan konsentrasi Pentingnya memahami sifat larutan dan
SILABUS MATA PELAJARAN KIMIA (Peminatan Bidang MIPA) Satuan Pendidikan : SMA
 SILABUS MATA PELAJARAN KIMIA (Peminatan Bidang MIPA) Satuan Pendidikan : SMA Kelas : X Kompetensi Inti : KI 1 : Menghayati dan mengamalkan ajaran agama yang dianutnya KI 2 : Menghayati dan mengamalkan
SILABUS MATA PELAJARAN KIMIA (Peminatan Bidang MIPA) Satuan Pendidikan : SMA Kelas : X Kompetensi Inti : KI 1 : Menghayati dan mengamalkan ajaran agama yang dianutnya KI 2 : Menghayati dan mengamalkan
STOIKIOMETRI. Oleh. Sitti Rahmawati S.Pd.
 STOIKIOMETRI Oleh Sitti Rahmawati S.Pd Copyright oke.or.id Artikel ini boleh dicopy,diubah, dikutip, di cetak dalam media kertas atau yang lain, dipublikasikan kembali dalam berbagai bentuk dengan tetap
STOIKIOMETRI Oleh Sitti Rahmawati S.Pd Copyright oke.or.id Artikel ini boleh dicopy,diubah, dikutip, di cetak dalam media kertas atau yang lain, dipublikasikan kembali dalam berbagai bentuk dengan tetap
Konsentrasi Larutan. a. Persen Berat (%W/W) Dalam pph : % w/w = Dalam ppm : % w/w = Dalam ppb :
 Konsentrasi Larutan Konsentrasi larutan adalah banyaknya zat terlarut di dalam sejumlah pelarut. Konsentrasi larutan dapat dinyatakan baik secara kualitatif atau kuantitatif. Istilah encer (dilute) dan
Konsentrasi Larutan Konsentrasi larutan adalah banyaknya zat terlarut di dalam sejumlah pelarut. Konsentrasi larutan dapat dinyatakan baik secara kualitatif atau kuantitatif. Istilah encer (dilute) dan
BAB I STOIKHIOMETRI I - 1
 BAB I STOIKHIOMETRI 1.1 PENDAHULUAN Setiap zat, unsur, senyawa dalam kimia mempunyai nama dan rumus uniknya sendiri. Cara tersingkat untuk memerikan suatu reaksi kimia adalah dengan menuliskan rumus untuk
BAB I STOIKHIOMETRI 1.1 PENDAHULUAN Setiap zat, unsur, senyawa dalam kimia mempunyai nama dan rumus uniknya sendiri. Cara tersingkat untuk memerikan suatu reaksi kimia adalah dengan menuliskan rumus untuk
Materi Pokok Bahasan :
 STOIKIOMETRI Kompetensi : Memiliki kemampuan untuk menginterpretasikan serta menerapkan dalam perhitungan kimia. Memiliki kemampuan untuk mengaplikasikan pengetahuan yang dimilikinya dan terbiasa menggunakan
STOIKIOMETRI Kompetensi : Memiliki kemampuan untuk menginterpretasikan serta menerapkan dalam perhitungan kimia. Memiliki kemampuan untuk mengaplikasikan pengetahuan yang dimilikinya dan terbiasa menggunakan
LOGO STOIKIOMETRI. Marselinus Laga Nur
 LOGO STOIKIOMETRI Marselinus Laga Nur Materi Pokok Bahasan : A. Konsep Mol B. Penentuan Rumus Kimia C. Koefisien Reaksi D. Hukum-hukum Gas A. Konsep Mol Pengertian konsep mol Hubungan mol dengan jumlah
LOGO STOIKIOMETRI Marselinus Laga Nur Materi Pokok Bahasan : A. Konsep Mol B. Penentuan Rumus Kimia C. Koefisien Reaksi D. Hukum-hukum Gas A. Konsep Mol Pengertian konsep mol Hubungan mol dengan jumlah
Pilihan Ganda Soal dan Jawaban Sifat Koligatif Larutan 20 butir. 5 uraian Soal dan Jawaban Sifat Koligatif Larutan.
 1 Pilihan Ganda Soal dan Jawaban Sifat Koligatif Larutan 20 butir. 5 uraian Soal dan Jawaban Sifat Koligatif Larutan. Berilah tanda silang (X) pada huruf A, B, C, D atau E di depan jawaban yang benar!
1 Pilihan Ganda Soal dan Jawaban Sifat Koligatif Larutan 20 butir. 5 uraian Soal dan Jawaban Sifat Koligatif Larutan. Berilah tanda silang (X) pada huruf A, B, C, D atau E di depan jawaban yang benar!
A. Pengertian larutan B. Jenis-jenis larutan C. Sifat larutan
 A. Pengertian larutan Larutan didefinisikan sebagai campuran homogen antara dua atau lebih zat yang terdispersi baik sebagai molekul, atom maupun ion yang komposisinya dapat bervariasi. Larutan dapat berupa
A. Pengertian larutan Larutan didefinisikan sebagai campuran homogen antara dua atau lebih zat yang terdispersi baik sebagai molekul, atom maupun ion yang komposisinya dapat bervariasi. Larutan dapat berupa
9. KOMPETENSI INTI DAN KOMPTENSI DASAR KIMIA SMA/MA KELAS: X
 9. KOMPETENSI INTI DAN KOMPTENSI DASAR KIMIA SMA/MA KELAS: X Tujuan kurikulum mencakup empat kompetensi, yaitu (1) kompetensi sikap spiritual, (2) sikap sosial, (3) pengetahuan, dan (4) keterampilan. Kompetensi
9. KOMPETENSI INTI DAN KOMPTENSI DASAR KIMIA SMA/MA KELAS: X Tujuan kurikulum mencakup empat kompetensi, yaitu (1) kompetensi sikap spiritual, (2) sikap sosial, (3) pengetahuan, dan (4) keterampilan. Kompetensi
kimia LAJU REAKSI 1 TUJUAN PEMBELAJARAN
 KTSP & K-13 kimia K e l a s XI LAJU REAKSI 1 TUJUAN PEMBELAJARAN Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami konsep molaritas. 2. Memahami definisi dan faktor-faktor
KTSP & K-13 kimia K e l a s XI LAJU REAKSI 1 TUJUAN PEMBELAJARAN Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami konsep molaritas. 2. Memahami definisi dan faktor-faktor
KIMIA TERAPAN LARUTAN
 KIMIA TERAPAN LARUTAN Pokok Bahasan A. Konsentrasi Larutan B. Masalah Konsentrasi C. Sifat Elektrolit Larutan D. Sifat Koligatif Larutan E. Larutan Ideal Pengantar Larutan adalah campuran homogen atau
KIMIA TERAPAN LARUTAN Pokok Bahasan A. Konsentrasi Larutan B. Masalah Konsentrasi C. Sifat Elektrolit Larutan D. Sifat Koligatif Larutan E. Larutan Ideal Pengantar Larutan adalah campuran homogen atau
FAKULTAS TEKNIK UNIVERSITAS NEGERI YOGYAKARTA BAHAN AJAR KIMIA DASAR BAB IV STOIKIOMETRI
 No. BAK/TBB/SBG201 Revisi : 00 Tgl. 01 Mei 2008 Hal 1 dari 6 BAB IV STOIKIOMETRI A. HUKUM GAY LUSSAC Bila diukur pada suhu dan tekanan yang sama, volum gas yang bereaksi dan volum gas hasil reaksi berbanding
No. BAK/TBB/SBG201 Revisi : 00 Tgl. 01 Mei 2008 Hal 1 dari 6 BAB IV STOIKIOMETRI A. HUKUM GAY LUSSAC Bila diukur pada suhu dan tekanan yang sama, volum gas yang bereaksi dan volum gas hasil reaksi berbanding
Rumus Kimia. Mol unsur =
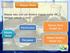 Rumus Kimia Menentukan Rumus Kimia Zat Rumus kimia zat dapat dibedakan menjadi rumus empiris dan rumus molekul. Rumus empiris dapat ditentukan dengan menghitung mol komponen penyusun zat dengan menggunakan
Rumus Kimia Menentukan Rumus Kimia Zat Rumus kimia zat dapat dibedakan menjadi rumus empiris dan rumus molekul. Rumus empiris dapat ditentukan dengan menghitung mol komponen penyusun zat dengan menggunakan
RENCANA PELAKSANAAN PEMBELAJARAN (RPP)
 RENCANA PELAKSANAAN PEMBELAJARAN (RPP) Nama Sekolah : SMAN Mata Pelajaran : Kimia Kelas / Semester : X / 2 Materi Pokok : STOIKIOMETRI (Persamaan Reaksi) Alokasi Waktu : 2 x 45 menit A. KOMPETENSI INTI
RENCANA PELAKSANAAN PEMBELAJARAN (RPP) Nama Sekolah : SMAN Mata Pelajaran : Kimia Kelas / Semester : X / 2 Materi Pokok : STOIKIOMETRI (Persamaan Reaksi) Alokasi Waktu : 2 x 45 menit A. KOMPETENSI INTI
KATA PENGANTAR. Bangko, sepetember Penyusun
 KATA PENGANTAR Puji syukur kami ucapkan ke hadirat Tuhan Yang Maha Esa karena atas rahmat-nya lah sehingga kami dapat menyelesaikan makalah ini sebagai salah satu tugas dari mata kuliah Kimia Dasar. Makalah
KATA PENGANTAR Puji syukur kami ucapkan ke hadirat Tuhan Yang Maha Esa karena atas rahmat-nya lah sehingga kami dapat menyelesaikan makalah ini sebagai salah satu tugas dari mata kuliah Kimia Dasar. Makalah
KONSEP MOL DAN STOIKIOMETRI
 KONSEP MOL DAN STOIKIOMETRI HUKUM-HUKUM DASAR KIMIA 1. Asas Lavoiser atau kekekalan massa jumlah sebelum dan setelah reaksi kimia adalah tetap 2. Hukum Gas Ideal P V = nrt Dengan P adalah tekanan (atm),
KONSEP MOL DAN STOIKIOMETRI HUKUM-HUKUM DASAR KIMIA 1. Asas Lavoiser atau kekekalan massa jumlah sebelum dan setelah reaksi kimia adalah tetap 2. Hukum Gas Ideal P V = nrt Dengan P adalah tekanan (atm),
Laporan Praktikum Kimia
 Laporan Praktikum Kimia Membuat Larutan Na2S2O3( Natriumthiosulfat) disusun oleh: Natasya Octavia Indrawan ( 20 ) Kelas: XI IPA 1 SMA MARDI YUANA BOGOR Jl Siliwangi No. 50 Sukasari 2012-2013 KATA PENGANTAR
Laporan Praktikum Kimia Membuat Larutan Na2S2O3( Natriumthiosulfat) disusun oleh: Natasya Octavia Indrawan ( 20 ) Kelas: XI IPA 1 SMA MARDI YUANA BOGOR Jl Siliwangi No. 50 Sukasari 2012-2013 KATA PENGANTAR
KIMIA DASAR. Ashfar Kurnia, M.Farm., Apt.
 KIMIA DASAR Ashfar Kurnia, M.Farm., Apt. ILMU KIMIA Kimia Ilmu pengetahuan alam yang mempelajari tentang MATERIyang meliputi: Struktur materi Susunan materi Sifat materi Perubahan materi Energi yang menyertai
KIMIA DASAR Ashfar Kurnia, M.Farm., Apt. ILMU KIMIA Kimia Ilmu pengetahuan alam yang mempelajari tentang MATERIyang meliputi: Struktur materi Susunan materi Sifat materi Perubahan materi Energi yang menyertai
Kadar Zat dalam Campuran
 55 Kadar Zat dalam Campuran 1. Persen Massa (% massa) Persen massa menyatakan bagian massa komponen dalam 100 bagian massa campuran. Atau Massa (gram) zat terlarut dalam 100 gram larutan. Menentukan rumus
55 Kadar Zat dalam Campuran 1. Persen Massa (% massa) Persen massa menyatakan bagian massa komponen dalam 100 bagian massa campuran. Atau Massa (gram) zat terlarut dalam 100 gram larutan. Menentukan rumus
6.1 HUKUM-HUKUM DASAR KIMIA
 6.1 HUKUM-HUKUM DASAR KIMIA 1. Hukum kekekalan massa oleh Antoine Laurent Lavoiser (1789). Lavoiser mengemukakan pernyataan yang disebut hukum kekekalan massa, yang berbunyi : Pada reaksi kimia, massa
6.1 HUKUM-HUKUM DASAR KIMIA 1. Hukum kekekalan massa oleh Antoine Laurent Lavoiser (1789). Lavoiser mengemukakan pernyataan yang disebut hukum kekekalan massa, yang berbunyi : Pada reaksi kimia, massa
BAB II TINJAUAN PUSTAKA
 BAB II TINJAUAN PUSTAKA A. Karakteristik Ilmu Kimia Kimia merupakan ilmu yang termasuk rumpun IPA, oleh karenanya kimia mempunyai karakteristik sama dengan IPA. Karakteristik tersebut adalah objek ilmu
BAB II TINJAUAN PUSTAKA A. Karakteristik Ilmu Kimia Kimia merupakan ilmu yang termasuk rumpun IPA, oleh karenanya kimia mempunyai karakteristik sama dengan IPA. Karakteristik tersebut adalah objek ilmu
d. Kompetensi Inti dan Kompetensi Dasar Kimia
 d. Kompetensi Inti dan Kompetensi Dasar Kimia KELAS: X KOMPETENSI INTI 1. Menghayati dan mengamalkan ajaran agama yang dianutnya 2. Mengembangkan perilaku (jujur, disiplin, tanggung jawab, peduli, santun,
d. Kompetensi Inti dan Kompetensi Dasar Kimia KELAS: X KOMPETENSI INTI 1. Menghayati dan mengamalkan ajaran agama yang dianutnya 2. Mengembangkan perilaku (jujur, disiplin, tanggung jawab, peduli, santun,
Sifat Dasar Larutan Kelarutan Pengaruh Jenis Zat pada Kelarutan
 2. LARUTAN 1. Sifat Dasar Larutan Larutan adalah campuran yang bersifat homogen antara molekul, atom ataupun ion dari dua zat atau lebih. Disebut campuran karena susunannya atau komposisinya dapat berubah.
2. LARUTAN 1. Sifat Dasar Larutan Larutan adalah campuran yang bersifat homogen antara molekul, atom ataupun ion dari dua zat atau lebih. Disebut campuran karena susunannya atau komposisinya dapat berubah.
BAB 5 KONSEP LARUTAN 1. KOMPOSISI LARUTAN 2. SIFAT-SIFAT ZAT TERLARUT 3. KESETIMBANGAN LARUTAN 4. SIFAT KOLIGATIF LARUTAN
 BAB 5 KONSEP LARUTAN 1. KOMPOSISI LARUTAN 2. SIFAT-SIFAT ZAT TERLARUT 3. KESETIMBANGAN LARUTAN 4. SIFAT KOLIGATIF LARUTAN ZAT TERLARUT + PELARUT LARUTAN Komponen minor Komponen utama Sistem homogen PELARUTAN
BAB 5 KONSEP LARUTAN 1. KOMPOSISI LARUTAN 2. SIFAT-SIFAT ZAT TERLARUT 3. KESETIMBANGAN LARUTAN 4. SIFAT KOLIGATIF LARUTAN ZAT TERLARUT + PELARUT LARUTAN Komponen minor Komponen utama Sistem homogen PELARUTAN
No. Dokumen : FTK-FR-AKD-001 FAKULTAS TARBIYAH DAN KEGURUAN Tgl. Terbit : 02 September SUNAN GUNUNG DJATI BANDUNG Hal : 1/2 SILABUS
 SUNAN GUNUNG DJATI BANDUNG Hal : 1/2 SILABUS Jurusan/Program Studi : MIPA/Pendidikan Mata Kuliah/Kode : Stoikiometri Mata Kuliah Prasyarat : Dasar I dan II Tahun Akademik/Semester : 2013-2014/III Jenjang/Bobot
SUNAN GUNUNG DJATI BANDUNG Hal : 1/2 SILABUS Jurusan/Program Studi : MIPA/Pendidikan Mata Kuliah/Kode : Stoikiometri Mata Kuliah Prasyarat : Dasar I dan II Tahun Akademik/Semester : 2013-2014/III Jenjang/Bobot
KOMPETENSI INTI KOMPETENSI DASAR
 Program Tahunan Lampiran E-4 Mata Pelajaran : Kimia Kelas / Smt. : X / I Tahun Pelajaran : 2013-2014 smt 1. Menghayati dan mengamalkan ajaran agama yang dianutnya 2. Menghayati dan mengamalkan perilaku
Program Tahunan Lampiran E-4 Mata Pelajaran : Kimia Kelas / Smt. : X / I Tahun Pelajaran : 2013-2014 smt 1. Menghayati dan mengamalkan ajaran agama yang dianutnya 2. Menghayati dan mengamalkan perilaku
Analisis Keterkaitan KI - KD dengan IPK dan Materi Pembelajaran. Kompetensi Inti Kompetensi Dasar Indikator Pencapaian Kompetensi
 No. Dokumen : F/751/WKS1/P/6 No. Revisi : 1 Tanggal Berlaku : 1 Juli 2016 Analisis Keterkaitan KI - KD dengan IPK dan Sekolah : SMA NEGERI 1 GODEAN Mata Pelajaran : Kimia Kelas / Program : XI/MIPA Semester
No. Dokumen : F/751/WKS1/P/6 No. Revisi : 1 Tanggal Berlaku : 1 Juli 2016 Analisis Keterkaitan KI - KD dengan IPK dan Sekolah : SMA NEGERI 1 GODEAN Mata Pelajaran : Kimia Kelas / Program : XI/MIPA Semester
Massa atom merupakan massa dari atom dalam satuan massa atom (sma).
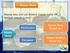 Bab 3 Stoikiometri Secara Mikro atom & molekul Secara Makro gram Massa atom merupakan massa dari atom dalam satuan massa atom (sma). Perjanjian internasional: 1 atom 12 C beratnya 12 sma Jika ditimbang
Bab 3 Stoikiometri Secara Mikro atom & molekul Secara Makro gram Massa atom merupakan massa dari atom dalam satuan massa atom (sma). Perjanjian internasional: 1 atom 12 C beratnya 12 sma Jika ditimbang
BAB II PEMBUATAN DAN PENGENCERAN LARUTAN
 ELAS ELOMPO 4 TUJUAN: BAB II PEMBUATAN DAN PENGENCERAN LARUTAN Membuat larutan dengan konsentrasi tertentu Mengencerkan larutan dengan konsentrasi tertentu A. PRE-LAB 1. Jelaskan perbedaan molaritas, molalitas
ELAS ELOMPO 4 TUJUAN: BAB II PEMBUATAN DAN PENGENCERAN LARUTAN Membuat larutan dengan konsentrasi tertentu Mengencerkan larutan dengan konsentrasi tertentu A. PRE-LAB 1. Jelaskan perbedaan molaritas, molalitas
larutan yang lebih pekat, hukum konservasi massa, hukum perbandingan tetap, hukum perbandingan berganda, hukum perbandingan volume dan teori
 i M Tinjauan Mata Kuliah ata kuliah Kimia Dasar 1 yang diberi kode PEKI 4101 mempunyai bobot 3 SKS yang terdiri dari 9 modul. Dalam mata kuliah ini dibahas tentang dasar-dasar ilmu kimia, atom, molekul
i M Tinjauan Mata Kuliah ata kuliah Kimia Dasar 1 yang diberi kode PEKI 4101 mempunyai bobot 3 SKS yang terdiri dari 9 modul. Dalam mata kuliah ini dibahas tentang dasar-dasar ilmu kimia, atom, molekul
Stoikiometri. Bab 3. Massa atom merupakan massa dari atom dalam satuan massa atom (sma). Secara Mikro atom & molekul.
 Bab 3 Stoikiometri Secara Mikro atom & molekul Secara Makro gram Massa atom merupakan massa dari atom dalam satuan massa atom (sma). Perjanjian internasional: 1 atom 12 C beratnya 12 sma Jika ditimbang
Bab 3 Stoikiometri Secara Mikro atom & molekul Secara Makro gram Massa atom merupakan massa dari atom dalam satuan massa atom (sma). Perjanjian internasional: 1 atom 12 C beratnya 12 sma Jika ditimbang
Soal dan Pembahasan. Soal dan Pembahasan Fraksi Mol. 1.Tentukan kemolalan larutan dari 0,01 mol NaOH dalam 200 gram air!
 Soal dan Pembahasan Fraksi Mol Soal dan Pembahasan 1.Tentukan kemolalan larutan dari 0,01 mol NaOH dalam 200 gram air! Menentukan kemolalan Dimana m = kemolalan larutan p = massa pelarut n = jumlah mol
Soal dan Pembahasan Fraksi Mol Soal dan Pembahasan 1.Tentukan kemolalan larutan dari 0,01 mol NaOH dalam 200 gram air! Menentukan kemolalan Dimana m = kemolalan larutan p = massa pelarut n = jumlah mol
Sifat-sifat Fisis Larutan
 Chapter 7a Sifat-sifat Fisis Larutan Larutan adalah campuran homogen dari dua atau lebih zat Zat yang jumlahnya lebih sedikit disebut zat terlarut Zat yang jumlahnya lebih banyak disebut zat pelarut. 13.1
Chapter 7a Sifat-sifat Fisis Larutan Larutan adalah campuran homogen dari dua atau lebih zat Zat yang jumlahnya lebih sedikit disebut zat terlarut Zat yang jumlahnya lebih banyak disebut zat pelarut. 13.1
kimia Kelas X KONSEP MOL I K-13 A. Persamaan Reaksi
 K-13 Kelas X kimia KNSEP ML I Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami persamaan reaksi kimia dan komponen-komponennya. 2. Memahami cara
K-13 Kelas X kimia KNSEP ML I Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami persamaan reaksi kimia dan komponen-komponennya. 2. Memahami cara
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN A. Lokasi dan Subjek Penelitian Penelitian ini dilakukan di salah satu SMA Negeri di kabupaten Garut. Subjek dalam penelitian ini adalah siswa SMA yang telah mempelajari materi
BAB III METODE PENELITIAN A. Lokasi dan Subjek Penelitian Penelitian ini dilakukan di salah satu SMA Negeri di kabupaten Garut. Subjek dalam penelitian ini adalah siswa SMA yang telah mempelajari materi
RENCANA PELAKSANAAN PEMBELAJARAN (RPP)
 RENCANA PELAKSANAAN PEMBELAJARAN (RPP) Satuan Pendidikan : SMA MARI AYU KELAPA Kelas / Semester : XI / 1 Materi Pembelajaran : Senyawa Hidrokarbon dan Minyak Bumi Alokasi Waktu : 12 45 menit Jumlah Pertemuan
RENCANA PELAKSANAAN PEMBELAJARAN (RPP) Satuan Pendidikan : SMA MARI AYU KELAPA Kelas / Semester : XI / 1 Materi Pembelajaran : Senyawa Hidrokarbon dan Minyak Bumi Alokasi Waktu : 12 45 menit Jumlah Pertemuan
BAB IV HASIL PENELITIAN DAN PEMBAHASAN. kelompok mahasiswa dalam menyelesaikan soal-soal stoikiometri.
 4.1 Deskripsi Hasil Penelitian BAB IV HASIL PENELITIAN DAN PEMBAHASAN 4.1.1 Cara Mahasiswa Menyelesaikan Soal-Soal Stoikiometri Cara mahasiswa menyelesaikan soal stoikiometri dianalisis berdasarkan respon
4.1 Deskripsi Hasil Penelitian BAB IV HASIL PENELITIAN DAN PEMBAHASAN 4.1.1 Cara Mahasiswa Menyelesaikan Soal-Soal Stoikiometri Cara mahasiswa menyelesaikan soal stoikiometri dianalisis berdasarkan respon
I. PENDAHULUAN. melalui proses kerja praktikum di laboratorium untuk menghasilkan sikap
 1 I. PENDAHULUAN 1.1. Latar Belakang Masalah Kegiatan praktikum di laboratorium merupakan kegiatan yang sangat penting dalam pembelajaran Ilmu Pengetahuan Alam (IPA) khususnya mata pelajaran kimia. Kimia
1 I. PENDAHULUAN 1.1. Latar Belakang Masalah Kegiatan praktikum di laboratorium merupakan kegiatan yang sangat penting dalam pembelajaran Ilmu Pengetahuan Alam (IPA) khususnya mata pelajaran kimia. Kimia
BAB 1 PENDAHULUAN 1.1 Latar Belakang
 BAB 1 PENDAHULUAN 1.1 Latar Belakang Reaksi-reaksi kimia berlangsung antara dua campuran zat, bukannya antara dua zat murni. Salah satu bentuk yang umum dari campuran ialah larutan. Larutan memainkan peran
BAB 1 PENDAHULUAN 1.1 Latar Belakang Reaksi-reaksi kimia berlangsung antara dua campuran zat, bukannya antara dua zat murni. Salah satu bentuk yang umum dari campuran ialah larutan. Larutan memainkan peran
BAB IV HASIL DAN PEMBAHASAN
 BAB IV HASIL DAN PEMBAHASAN Stoikiometri kimia merupakan suatu materi pelajaran kimia yang menekankan pada segi kuantitatif analisis kimia. Materi stoikiometri kimia di SMA berdasarkan silabus kimia KTSP
BAB IV HASIL DAN PEMBAHASAN Stoikiometri kimia merupakan suatu materi pelajaran kimia yang menekankan pada segi kuantitatif analisis kimia. Materi stoikiometri kimia di SMA berdasarkan silabus kimia KTSP
RENCANA PELAKSANAAN PEMBELAJARAN (RPP)
 RENCANA PELAKSANAAN PEMBELAJARAN (RPP) A. IDENTITAS 1. Sekolah : SMKN 2 Pekanbaru 2. Mata Pelajaran : Kimia 3. Kelas/Semester : XI/Ganjil 4. Materi Pokok : Laju Reaksi 5. AlokasiWaktu : 2 JP (1 x pertemuan)
RENCANA PELAKSANAAN PEMBELAJARAN (RPP) A. IDENTITAS 1. Sekolah : SMKN 2 Pekanbaru 2. Mata Pelajaran : Kimia 3. Kelas/Semester : XI/Ganjil 4. Materi Pokok : Laju Reaksi 5. AlokasiWaktu : 2 JP (1 x pertemuan)
SIFAT KOLIGATIF LARUTAN
 SIFAT KOLIGATIF LARUTAN PENURUNAN TEKANAN UAP Penurunan Tekanan Uap adalah selisih antara tekanan uap jenuh pelarut murni dengan tekanan uap jenuh larutan. P = P - P P = Penurunan Tekanan Uap P = Tekanan
SIFAT KOLIGATIF LARUTAN PENURUNAN TEKANAN UAP Penurunan Tekanan Uap adalah selisih antara tekanan uap jenuh pelarut murni dengan tekanan uap jenuh larutan. P = P - P P = Penurunan Tekanan Uap P = Tekanan
Hasil dan Pembahasan
 Bab IV Hasil dan Pembahasan IV.1 Hasil Analisis Pustaka Stoikiometri Analisis (kajian) kesesuaian antara ketiga pustaka stoikiometri dilakukan untuk mendapatkan kerangka struktur hiperteks yang memuat
Bab IV Hasil dan Pembahasan IV.1 Hasil Analisis Pustaka Stoikiometri Analisis (kajian) kesesuaian antara ketiga pustaka stoikiometri dilakukan untuk mendapatkan kerangka struktur hiperteks yang memuat
SIFAT KOLIGATIF LARUTAN
 SIFAT KOLIGATIF LARUTAN STANDAR KOMPETENSI 1. Mendeskripsikan sifat-sifat Larutan, metode pengukuran dan terapannya. KOMPETENSI DASAR 1.1 Mendeskripsikan sifat-sifat Larutan, metode pengukuran dan terapannya.
SIFAT KOLIGATIF LARUTAN STANDAR KOMPETENSI 1. Mendeskripsikan sifat-sifat Larutan, metode pengukuran dan terapannya. KOMPETENSI DASAR 1.1 Mendeskripsikan sifat-sifat Larutan, metode pengukuran dan terapannya.
LAPORAN PRAKTIKUM KIMIA FISIK VOLUM MOLAL PARSIAL. Nama : Ardian Lubis NIM : Kelompok : 6 Asisten : Yuda Anggi
 LAPORAN PRAKTIKUM KIMIA FISIK VOLUM MOLAL PARSIAL Nama : Ardian Lubis NIM : 121810301028 Kelompok : 6 Asisten : Yuda Anggi LABORATORIUM KIMIA FISIK JURUSAN KIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN
LAPORAN PRAKTIKUM KIMIA FISIK VOLUM MOLAL PARSIAL Nama : Ardian Lubis NIM : 121810301028 Kelompok : 6 Asisten : Yuda Anggi LABORATORIUM KIMIA FISIK JURUSAN KIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN
BAB III METODOLOGI PENELITIAN
 BAB III METODOLOGI PENELITIAN A. Lokasi dan Subjek Penelitian Penelitian ini dilaksanakan di SMA Negeri 2 Bandung. Subyek penelitian dalam penelitian ini adalah siswa SMA kelas X dan XI yang telah mempelajari
BAB III METODOLOGI PENELITIAN A. Lokasi dan Subjek Penelitian Penelitian ini dilaksanakan di SMA Negeri 2 Bandung. Subyek penelitian dalam penelitian ini adalah siswa SMA kelas X dan XI yang telah mempelajari
STOIKIOMETRI _KIMIA INDUSTRI_ DEWI HARDININGTYAS, ST, MT, MBA WIDHA KUSUMA NINGDYAH, ST, MT AGUSTINA EUNIKE, ST, MT, MBA
 STOIKIOMETRI _KIMIA INDUSTRI_ DEWI HARDININGTYAS, ST, MT, MBA WIDHA KUSUMA NINGDYAH, ST, MT AGUSTINA EUNIKE, ST, MT, MBA 1. Hukum-Hukum Dasar 2. Persamaan Gas Ideal 3. Persamaan Kimia 4. Yield STOIKIOMETRI
STOIKIOMETRI _KIMIA INDUSTRI_ DEWI HARDININGTYAS, ST, MT, MBA WIDHA KUSUMA NINGDYAH, ST, MT AGUSTINA EUNIKE, ST, MT, MBA 1. Hukum-Hukum Dasar 2. Persamaan Gas Ideal 3. Persamaan Kimia 4. Yield STOIKIOMETRI
A. HUKUM PERBANDINGAN VOLUM DAN HIPOTESIS AVOGADRO*
 Di muka kita telah membahas tentang jenis perubahan materi. Bagian dari Kimia yang membahas hubungan kuantitatif (jumlah) antara zat-zat yang terlibat dalam suatu perubahan kimia atau reaksi kimia dikenal
Di muka kita telah membahas tentang jenis perubahan materi. Bagian dari Kimia yang membahas hubungan kuantitatif (jumlah) antara zat-zat yang terlibat dalam suatu perubahan kimia atau reaksi kimia dikenal
MODUL KIMIA SMA IPA Kelas 10
 SMA IPA Kelas 0 A. Massa Atom. Massa Atom Relatif (Ar) Massa atom relatif (Ar) merupakan perbandingan massa atom dengan massa satu atom yang tetap. Secara matematis dapat dirumuskan sebagai berikut. sma
SMA IPA Kelas 0 A. Massa Atom. Massa Atom Relatif (Ar) Massa atom relatif (Ar) merupakan perbandingan massa atom dengan massa satu atom yang tetap. Secara matematis dapat dirumuskan sebagai berikut. sma
Rencana Pelaksanaan Pembelajaran (RPP) : SMA N 1 Mertoyudan
 Sekolah Mata Pelajaran Kelas/Semester Materi Pokok Alokasi Waktu Rencana Pelaksanaan Pembelajaran (RPP) : SMA N 1 Mertoyudan : Kimia : XI/1 : Sistem dan Lingkungan : 90 menit A. Kompetensi Inti 1. Menghayati
Sekolah Mata Pelajaran Kelas/Semester Materi Pokok Alokasi Waktu Rencana Pelaksanaan Pembelajaran (RPP) : SMA N 1 Mertoyudan : Kimia : XI/1 : Sistem dan Lingkungan : 90 menit A. Kompetensi Inti 1. Menghayati
BAB IV HASIL PENELITIAN DAN PEMBAHASAN. Data-data yang telah dikumpulkan dapat dikaji lebih lanjut untuk dilihat
 32 BAB IV HASIL PENELITIAN DAN PEMBAHASAN 4.1. Hasil Penelitian Data-data yang telah dikumpulkan dapat dikaji lebih lanjut untuk dilihat bagaimana komposisi soal berdasarkan domain kognitif Taksonomi Bloom
32 BAB IV HASIL PENELITIAN DAN PEMBAHASAN 4.1. Hasil Penelitian Data-data yang telah dikumpulkan dapat dikaji lebih lanjut untuk dilihat bagaimana komposisi soal berdasarkan domain kognitif Taksonomi Bloom
RENCANA PELAKSANAAN PEMBELAJARAN (RPP)
 RENCANA PELAKSANAAN PEMBELAJARAN (RPP) Sekolah Mata Pelajaran Kelas/ Semester Materi Pokok Alokasi Waktu : SMAN 1 SANDEN : Kimia : X / Ganjil : Struktur Atom : 3 x 45 menit A. Kompetensi Inti KI 1 : Menghayati
RENCANA PELAKSANAAN PEMBELAJARAN (RPP) Sekolah Mata Pelajaran Kelas/ Semester Materi Pokok Alokasi Waktu : SMAN 1 SANDEN : Kimia : X / Ganjil : Struktur Atom : 3 x 45 menit A. Kompetensi Inti KI 1 : Menghayati
RENCANA PELAKSANAAN PEMBELAJARAN (RPP)
 RENCANA PELAKSANAAN PEMBELAJARAN (RPP) Sekolah Mata Pelajaran Kelas / Semester Materi Pokok Alokasi Waktu : SMAN. : Kimia : X MIA/ Ganjil : Struktur Atom Bohr : 3 x 45 Menit (1 x Pertemuan) I. Kompetensi
RENCANA PELAKSANAAN PEMBELAJARAN (RPP) Sekolah Mata Pelajaran Kelas / Semester Materi Pokok Alokasi Waktu : SMAN. : Kimia : X MIA/ Ganjil : Struktur Atom Bohr : 3 x 45 Menit (1 x Pertemuan) I. Kompetensi
SILABUS. Alokasi Sumber/ Kompetensi Dasar Materi Pembelajaran Kegiatan Pembelajaran Indikator Penilaian
 SILABUS Nama Sekolah : SMA Mata Pelajaran : KIMIA Kelas/Semester : X/1 Standar Kompetensi : 1. Memahami struktur atom, sifat-sifat periodik unsur, dan ikatan kimia Alokasi Waktu : 18 jam pelajaran (untuk
SILABUS Nama Sekolah : SMA Mata Pelajaran : KIMIA Kelas/Semester : X/1 Standar Kompetensi : 1. Memahami struktur atom, sifat-sifat periodik unsur, dan ikatan kimia Alokasi Waktu : 18 jam pelajaran (untuk
4. Menentukan Himpunan Penyelesaian untuk Sistem Persamaan Linear Dua Variabel
 BAHAN AJAR A. Kompetensi Inti KI 1 : Menghayati dan mengamalkan ajaran agama yang dianutnya. KI 2 : Menghayati dan mengamalkan perilaku jujur, disiplin, tanggungjawab, peduli (gotong royong, kerjasama,
BAHAN AJAR A. Kompetensi Inti KI 1 : Menghayati dan mengamalkan ajaran agama yang dianutnya. KI 2 : Menghayati dan mengamalkan perilaku jujur, disiplin, tanggungjawab, peduli (gotong royong, kerjasama,
RENCANA PELAKSANAAN PEMBELAJARAN
 RENCANA PELAKSANAAN PEMBELAJARAN Nama Sekolah Mata Pelajaran Kelas / Semester Topik Materi Alokasi Waktu : SMA N 1 Mertoyudan : Kimia : XI / Satu : Eksoterm dan Endoterm : 2 x 45 menit A. Kompetensi Inti
RENCANA PELAKSANAAN PEMBELAJARAN Nama Sekolah Mata Pelajaran Kelas / Semester Topik Materi Alokasi Waktu : SMA N 1 Mertoyudan : Kimia : XI / Satu : Eksoterm dan Endoterm : 2 x 45 menit A. Kompetensi Inti
MATA PELAJARAN/PAKET KEAHLIAN ILMU KIMIA
 SUMBER BELAJAR PENUNJANG PLPG 2016 MATA PELAJARAN/PAKET KEAHLIAN ILMU KIMIA BAB II HUKUM-HUKUM DASAR KIMIA, STOIKIOMETRI Prof. Dr. Sudarmin, M.Si Dra. Woro Sumarni, M.Si Cepi Kurniawan, M.Si, Ph.D KEMENTERIAN
SUMBER BELAJAR PENUNJANG PLPG 2016 MATA PELAJARAN/PAKET KEAHLIAN ILMU KIMIA BAB II HUKUM-HUKUM DASAR KIMIA, STOIKIOMETRI Prof. Dr. Sudarmin, M.Si Dra. Woro Sumarni, M.Si Cepi Kurniawan, M.Si, Ph.D KEMENTERIAN
STOIKIOMETRI STOIKIOMETRI
 BAB V STOIKIOMETRI Standar Kompetensi Memahami hukum-hukum dasar kimia dan penerapannya dalam perhitungan kimia (stoikiometri) Kompetensi Dasar Mendeskripsikan tata nama senyawa anorganik dan organik sederhana
BAB V STOIKIOMETRI Standar Kompetensi Memahami hukum-hukum dasar kimia dan penerapannya dalam perhitungan kimia (stoikiometri) Kompetensi Dasar Mendeskripsikan tata nama senyawa anorganik dan organik sederhana
Rencana Pelaksanaan Pembelajaran (RPP) : SMA N Yogyakarta
 Sekolah Mata Pelajaran Kelas/Semester Materi Pokok Alokasi Waktu Rencana Pelaksanaan Pembelajaran (RPP) : SMA N Yogyakarta : Kimia : XI/1 : Isomer Senyawa Hidrokarbon : 90 menit A. Kompetensi Inti 1. Menghayati
Sekolah Mata Pelajaran Kelas/Semester Materi Pokok Alokasi Waktu Rencana Pelaksanaan Pembelajaran (RPP) : SMA N Yogyakarta : Kimia : XI/1 : Isomer Senyawa Hidrokarbon : 90 menit A. Kompetensi Inti 1. Menghayati
1. Penyelesaian persamaan linier tiga variabel dengan metode eliminasi
 Bahan ajar A. Kompetensi Inti KI 1: Menghayati dan mengamalkan ajaran agama yang dianutnya. KI 2: Menghayati dan mengamalkan perilaku jujur, disiplin, tanggungjawab, peduli (gotong royong, kerjasama, toleran,
Bahan ajar A. Kompetensi Inti KI 1: Menghayati dan mengamalkan ajaran agama yang dianutnya. KI 2: Menghayati dan mengamalkan perilaku jujur, disiplin, tanggungjawab, peduli (gotong royong, kerjasama, toleran,
Lampiran 1.4 Rencana Pelaksanaan Pembelajaran
 113 Lampiran 1.4 Rencana Pelaksanaan Pembelajaran RENCANA PELAKSANAAN PEMBELAJARAN Identitas sekolah Mata pelajaran Kelas/Semester Materi Pokok Sub Materi Alokasi Waktu Jumlah Pertemuan : SMA : Kimia :
113 Lampiran 1.4 Rencana Pelaksanaan Pembelajaran RENCANA PELAKSANAAN PEMBELAJARAN Identitas sekolah Mata pelajaran Kelas/Semester Materi Pokok Sub Materi Alokasi Waktu Jumlah Pertemuan : SMA : Kimia :
Konsep Mol : Menghubungkan Dunia Makroskopik dan Dunia Molekular
 Konsep Mol : Menghubungkan Dunia Makroskopik dan Dunia Molekular 1 Secara Mikro atom & molekul Secara Makro gram Massa atom merupakan massa dari atom dalam satuan massa atom (sma). Perjanjian internasional:
Konsep Mol : Menghubungkan Dunia Makroskopik dan Dunia Molekular 1 Secara Mikro atom & molekul Secara Makro gram Massa atom merupakan massa dari atom dalam satuan massa atom (sma). Perjanjian internasional:
Belajar Kimia dengan Aplikasi ChemMobile
 Belajar Kimia dengan Aplikasi ChemMobile Belajar Kimia dengan Aplikasi ChemMobile Pada kesempatan kali ini, saya ingin berbagi tentang sebuah aplikasi kimia berbasisis android. Dengan aplikasi kimia ini,
Belajar Kimia dengan Aplikasi ChemMobile Belajar Kimia dengan Aplikasi ChemMobile Pada kesempatan kali ini, saya ingin berbagi tentang sebuah aplikasi kimia berbasisis android. Dengan aplikasi kimia ini,
RENCANA PELAKSANAAN PEMBELAJARAN. Satuan Pendidikan. Kelas/ Semester
 RENCANA PELAKSANAAN PEMBELAJARAN Satuan Pendidikan Mata Pelajaran Kelas/ Semester Materi Pokok Alokasi Waktu : SMA : Fisika : XI/2 : Gas Isotermik : (1 x 45 menit) A. KOMPETENSI INTI (KI) 1. Menghayati
RENCANA PELAKSANAAN PEMBELAJARAN Satuan Pendidikan Mata Pelajaran Kelas/ Semester Materi Pokok Alokasi Waktu : SMA : Fisika : XI/2 : Gas Isotermik : (1 x 45 menit) A. KOMPETENSI INTI (KI) 1. Menghayati
RENCANA PELAKSANAAN PEMBELAJARAN
 RENCANA PELAKSANAAN PEMBELAJARAN Satuan Pendidikan : SMA Dwiwarna Mata Pelajaran : Fisika Kelas/Semester : XI / IV Peminatan : MIA Materi Pokok : Teori Kinetik Gas Alokasi Waktu : 8 x 2 JP A. Kompetensi
RENCANA PELAKSANAAN PEMBELAJARAN Satuan Pendidikan : SMA Dwiwarna Mata Pelajaran : Fisika Kelas/Semester : XI / IV Peminatan : MIA Materi Pokok : Teori Kinetik Gas Alokasi Waktu : 8 x 2 JP A. Kompetensi
