BAB III KESETIMBANGAN KIMIA. AH = 92 kj
|
|
|
- Lanny Susman
- 6 tahun lalu
- Tontonan:
Transkripsi
1 BAB III KESETIMBANGAN KIMIA Amonia (NH 3 ) merupakan salah satu zat kimia yang paling banyak diproduksi. Amonia digunakan terutama untuk membuat pupuk, yaitu urea dan ZA. Penggunaan amonia yang lain, yaitu untuk membuat resin, bahan mesiu, dan berbagai senyawa nitrogen lainnya. Di bidang industri, amonia dibuat dari gas nitrogen dan gas hidrogen. Gas nitrogen diperoleh dan udara, sedangkan gas hidrogen dan gas alam. Persamaan termokimia reaksi pembuatan amonia dinyatakan sebagai berikut. N 2 (g) + 3H 2 (g) ---> 2NH 3 (g) AH = 92 kj Stoikiometri reaksi menunjukkan bahwa 1 mol nitrogen bereaksi dengan 3 mol hidrogen membentuk 2 mol amonia. Akan tetapi, dari percobaan diketahui bahwa hasil seperti itu tidak pernah dicapai. Artinya, jika direaksikan 1 mol nitrogen dengan 3 mol hidrogen ternyata tidak dapat menghasilkan 2 mol amonia, tetapi selalu kurang dan 2 mol. Mengapa hal itu terjadi? Ternyata, reaksi berlangsung tidak tuntas. Reaksi "seperti berhenti" setelah sebagian nitrogen dan hidrogen bereaksi. Reaksi berakhir dengansuatu campuran yang mengandung NH 3, N 2, dan H 2. Keadaan seperti itulah yang disebut keadaan setimbang. Jadi, keadaan setimbang adalah suatu keadaan di mana zat-zat pereaksi dan hasil reaksi terdapat bersama-sama, tetapi tidak ada lagi perubahan yang dapat diamati. Dengan kata lain, campuran masih mengandung zat-zat pereaksi, tetapi reaksi seolah-olah sudah berhenti. Dikatakan seolah-olah berhenti karena ternyata reaksi tetap berlangsung pada tingkat mikroskopis. Hal itulah yang akan diuraikan pada bagian berikut. Pembahasan dalam bab ini akan dimulai dengan mengenali bahwa reaksi kimia ada yang dapat balik, artinya produk reaksi dapat bereaksi kembali membentuk zat-zat pereaksi. Reaksi-reaksi yang dapat balik ini, jika berlangsung dalam sistem tertutup akan berakhir dengan suatu keadaan setimbang. Kita akan melihat bahwa kesetimbangan kimia bersifat dinamis, artinya reaksi tetap berlangsung tetapi tidak ada perubahan yang dapat diamati. Pada bagian kedua akan dibahas tetapan 45
2 kesetimbangan, yaitu besaran yang menyatakan seberapa tuntas suatu reaksi. Selanjutnya akan dibahas pengaruh konsentrasi, suhu, tekanan, dan katalis terhadap kesetimbangan Kesetimbangan Dinas 4.1.a. Reaksi Reversible dan Irreversible Perhatikanlah kertas yang terbakar. Apakah abu hasil pembakaran kertas dapat diubah kembali menjadi kertas seperti semula? Pengalaman menunjukkan bahwa proses itu tidak dapat dilakukan, bukan? Reaksi seperti itu kita golongkan sebagai reaksi yang berlangsung searah atau reaksi yang tidak dapat balik (irreversible). Apakah ada reaksi kimia yang dapat balik? Dalam kehidupan sehari-hari sulit menemukan reaksi yang dapat balik. Proses-proses alami umumnya berlangsung searah, tidak dapat balik. Namun, di laboratorium maupun dalam proses industri, banyak reaksi yang dapat balik. Reaksi yang dapat balik kita sebut reaksi reversible. Salah satu di antaranya adalah reaksi antara nitrogen dengan hidrogen membentuk amonia. Jika campuran gas nitrogen dan hidrogen dipanaskan akan menghasilkan ammonia. N 2 (g) + 3H 2 ---> 2NH 3 (g) (4.1) Sebaliknya, jika amonia (NH 3 ) dipanaskan akan terurai membentuk nitrogen dan hidrogen. 2NH 3 (g) ---> N 2 ( g ) + 3 H, ( g ) ( 4. 2 ) Apabila diperhatikan, ternyata Reaksi (4.2) merupakan kebalikan dari Reaksi (4.1). Kedua reaksi itu dapat digabung.ebagai berikut. N 2 (g) + 3H 2 (g) 2 N H 3 ( g ) ( 4. 3 ) Tanda dimaksudkan untuk menyatakan reaksi dapat balik. Reaksi ke kanan disebut reaksi maju; reaksi ke kiri disebut reaksi balik. 3.1.b. Keadaan Setimbang Pada awal bab telah disebutkan bahwa pada keadaan setimbang reaksi tetap berlangsung. Tetapi tidak ada perubahan yang dapat diamati. Bagaimanakah kita memahami keadaan ini? 46
3 Bayangkanlah suatu ruangan tertutup di mana 1 mol gas nitrogen dipanaskan bersama 3 mol gas hidrogen. Pada awalnya, hanya terjadi satu reaksi yaitu pembentukan amonia. N 2 (g) + 3H 2 (g) -->2NH 3 (g)... (4.4) Seperti telah disebutkan di atas, amonia dapat pula terurai membentuk nitrogen dan hidrogen. Oleh karena itu, segera setelah terbentuk, sebagian amonia akan terurai kembali membentuk gas nitrogen dan gas hidrogen. 2NH 3 (g) --> N 2 (g) + 3H 2 (g)... (4.5) Selanjutnya, kedua reaksi tersebut akan berlangsung secara simultan (bersama-sama) menurut reaksi dapat balik berikut. N 2 (g) + 3H 2 (g) 2NH 3 (g)... (4.6) Misalkan laju reaksi maju v 1 dan laju reaksi balik v 2. Sebagaimana telah dipelajari dalam Bab 3, nilai v 1 bergantung pada konsentrasi N 2 dan H 2, sedangkan nilai v 2 bergantung pada konsentrasi NH 3. Pada awal reaksi, v 1 mempunyai nilai maksimum, sedangkan v 2 = 0 (karena NH 3 belum ada). Selanjutnya, seiring dengan berkurangnya konsentrasi N 2 dan H 2, nilai v 1 semakin lama semakin kecil. Sebaliknya, dengan bertambahnya konsentrasi NH 3, nilai v 2 semakin lama semakin besar. Pada suatu saat, laju reaksi maju (v 1 ) menjadi sama dengan laju reaksi balik (v 2 ). Hal itu berarti bahwa laju menghilangnya suatu komponen sama dengan laju pembentukan komponen itu. Berarti, H 2 Waktu --> Gambar 3.b. 1 Perubahan konsentrasi pereaksi dan hasil reaksi menuju keadaan setimbang untuk reaksi: N 2 (g) + 3H 2 (g) 2NH 3 (g) Konsentrasi N 2 dan H 2 (pereaksi) turun, konsentrasi NH 3 (hasil reaksi) naik. Pada keadaan setimbang, konsentrasi masingmasing zat tetap. Gambar 3.b.2 Grafik perubahan laju reaksi terhadap waktu pada reaksi bolak-batik: N2(g) + 3H2(g) = 2NH3(g) v i = laju reaksi dari kin ke kanan 1/ 2 = laju reaksi dari kanan ke kiri Kesetimbangan tercapai pada saat = v 2. 47
4 sejak v 1 = v 2, jumlah masing-masing komponen tidak berubah terhadap waktu. Oleh karena itu, tidak ada perubahan yang dapat diamati atau diukur (sifat makroskopis tidak berubah), reaksi seolah-olah telah berhenti. Kita katakan bahwa campuran telah mencapai keadaan setimbang (kesetimbangan). Akan tetapi, melalui percobaan dapat ditunjukkan bahwa dalam keadaan setimbang tersebut reaksi tetap berlangsung pada tingkat molekul (tingkat mikroskopis). Artinya, reaksi antara nitrogen dengan hidrogen membentuk amonia tetap berlangsung, demikian pula penguraian amonia membentuk nitrogen dan hidrogen. Oleh karena itu, kesetimbangan kimia disebut kesetimbangan dinamis. Perubahan konsentrasi N 2, H 2, dan NH 3 terhadap waktu Tetapan Kesetimabangan 3.2.a. Hukum Kesetimbangan Suatu hasil percobaan terhadap reaksi kesetimbangan antara gas karbon monoksida dengan gas hidrogen membentuk gas metana dan uap air dapat dilihat pada Tabel 4.1. Tabel 4.1 Susunan Kesetimbangan Reaksi antara Gas Karbon Monoksida dengan Gas Hidrogen Membentuk Metana pada Suhu 1200 K CO(g) +3H.,(g) CH,(g) + H 2 O(a) Konsentrasi Awal Konsentrasi pada Keadaan Setimbang (M) (M) [CH 4 ] [H 2 O] [CO] [H 2 ] [CO] [H 2 ] [CH 4 ] [ [CO] [H 2 ] 3 0,1000 0,3000 0,0613 0,1839 0,0387 0,0387 3,93 0,2000 0,3000 0,1522 0,1566 0,0478 0,0478 3,91 0,1000 0,4000 0,0479 0,2437 0,0521 0,0521 3,92 0,1000 0,1000 0,0894 0,0683 0,0106 0,0106 3,94 Data dalam tabel tersebut menunjukkan bahwa komposisi kesetimbangan bergantung pada perbandingan mol pereaksinya. Namun demikian, terdapat suatu hubungan yang tetap antara konsentrasi kesetimbangan, yaitu nisbah hasil kali konsentrasi setimbang zat-zat produk terhadap hasil konsentrasi setimbang zat-zat pereaksi, masingmasing dipangkatkan dengan koefisien reaksinya. Hubungan ini ditemukan oleh Cato 48
5 Maximillian Gulberg dan Peter Wage pada tahun 1864, dan selanjutnya disebut hukum kesetimbangan. Nilai dan hukum kesetimbangan disebut tetapan kesetimbangan dan dinyatakan dengan lambang Ungkapan hukum kesetimbangan untuk reaksi kesetimbangan di atas dapat dinyatakan sebagai berikut. K c = CH 4 H 2 O CO (H) 2 3 Nilai tetapan kesetimbangan bergantung pada suhu. Untuk contoh di atas, nilai tetapan kesetimbangan yaitu 3,92 pada suhu 1200 K. Perubahan suhu akan mengubah komposisi kesetimbangan, sehingga nilai tetapan kesetimbangannya berubah. 3.2.b. Hubungan Nilai Tetapan Kesetimbangan antara Reaksi-reaksi yang Berkaitan Reaksi dapat balik yang melibatkan S0 2 (g), 0 2 (g), dan S0 3 (g) dapat dinyatakan dengan tiga cara berikut. (1) 2S0 2 (g) (g) 2S0 3 (g) K = K 1 (2) 2S0 3 (g) 2S0 2 (g) (g) K = K 2 (3) S0 2 (g) + ½ 0 2 (g) S0 3 (g) K = K 3 Bagaimanakah hubungan antara nilai tetapan kesetimbangan reaksi-reaksi itu? Dalam hal ini, berlaku aturan-aturan sebagai berikut. (1) Jika persamaan reaksi kesetimbangan dibalik, maka harga K juga dibalik. (2) Jika koefisien reaksi kesetimbangan dibagi dengan faktor n, maka harga tetapan kesetimbangan yang barn adalah akar pangkat n dari harga tetapan kesetimbangan yang lama. (3) Jika koefisien reaksi kesetimbangan dikalikan dengan faktor n, maka harga tetapan kesetimbangan yang barn adalah harga tetapan kesetimbangan yang lama dipangkatkan dengan n. Jika diterapkan pada contoh di atas, maka: 49
6 Reaksi (2) adalah kebalikan dari reaksi (1). Jadi, K 2 = 1 K 1 Reaksi (3) sama dengan reaksi (1), tetapi koefisiennya dibagi dua, sehingga K 1 = K 1 1/2 atau K 3 = K 1 Latihan. 1. Tulislah persamaan tetapan kesetimbangan (K dan K p ) untuk sistem kesetimbangan berikut. a. CaCO 3 CaO(s) + CO 2 (g) b. Ca 3 (PO 4 ) 2 (s) 3Ca 2+ (aq) + 2PO 4 3- (aq) 2. Sebanyak 4 mol gas HI dipanaskan dalam suatu ruangan 5 liter pada 458 C sehingga sebagian terurai dan membentuk kesetimbangan 2HI(g) H 2 (g) (g). Apabila pada keadaan setimbang terdapat 0,5 mol I 2, tentukanlah harga tetapan kesetimbangan K dan K reaksi itu pada 458 C. 3. Dalam suatu ruangan 2 liter dipanaskan kristal La 2 (C ) 3 sehingga sebagian terurai membentuk sistem kesetimbangan heterogen: La 2 (C ) 3 (s) La (s) + 3C0(g) + 3CO 2 (g) Pada suatu suhu T terdapat kesetimbangan di mana tekanan total gas dalam ruangan itu = 0,2 atm. Tentukan harga tetapan kesetimbangan K p pada suhu tersebut. 4. Reaksi N (g) 2NO 2 (g) mempunyai harga K = 0,25 pada T C. Pada suhu yang sama tentukanlah harga K reaksi: a. 2NO 2 (g) N (g) b. NO 2 (g) ½ N (g) 3.3. Pergeseran Kesetimbangan 50
7 Telah disebutkan bahwa reaksi dapat balik (reversible) berlangsung tidak tuntas. Apakah tingkat ketuntasan dapat dipengaruhi oleh faktor luar? Untuk menjawab pertanyaan ini, marilah kita perhatikan Tabel 4.2 berikut. Tabel tersebut memuat data tentang pengaruh suhu dan tekanan pada reaksi kesetimbangan antara gas nitrogen dengan gas hidrogen membentuk amonia. Tabel 4.2 Rendemen Amonia Hasil Reaksi Nitrogen dengan Hidrogen pada Berbagai Suhu dan Tekanan. N 2 (g) + 3H 2 (g) 2NH 3 (g) AH = - 92,2 kj [Suhu C Hasil NH3, A 10,0 atm 30,0 atm 50,0 atm 100 atm 300 atm 600 atm atm ,7 67,6 74,4 81,5 90,0 95,4 98, ,7 30,3 39,4 52,0 71,0 84,2 92, ,9 10,2 15,3 25,1 47,0 65,2 79, ,2 3,5 5, ,4 42,2 57, ,5 1,4 2,3 4,5 13,8 23,1 31, ,2 0,7 1,1 2,2 7,3 12,6 12,9 Perhatikanlah lajur pertama pada tabel itu, yaitu percobaan pada suhu tetap 200 C dengan variasi tekanan. Data tersebut menunjukkan bahwa semakin besar tekanan, semakin besar pula persentase amonia. Jadi, dapat dikatakan bahwa penambahan tekanan menggeser kesetimbangan ke kekanan. Kemudian, perhatikanlah data pada kolom pertama, yaitu percobaan pada tekanan tetap sebesar 10 atm dengan suhu yang bervariasi. Data tersebut menunjukkan bahwa semakin tinggi suhu, semakin kecil persentase amonia. Dengan demikian dapat dikatakan bahwa penambahan suhu menggeser kesetimbangan itu ke kiri. Kesetimbangan dikatakan bergeser ke kanan, jika produk bertambah atau pereaksi berkurang. Kesetimbangan dikatakan bergeser ke kiri, jika produk berkurang atau pereaksi bertambah. 3.3.a.. Azas Le Chatelier 51
8 Mengapa kesetimbangan di atas bergeser ke kanan ketika tekanan diperbesar? Mengapa pula bergeser ke kiri ketika suhu dinaikkan? Bagimana kita mengetahui arah pergeseran kesetimbangan? Pada tahun 1884, Henri Louis Le Chatelier ( ) berhasil menyimpulkan pengaruh faktor luar terhadap kesetimbangan. Kesimpulan Le Chatelier tersebut kini kita kenal sebagai azas Le Chatelier sebagai berikut: Bila terhadap suatu kesetimbangan dilakukan suatu tindakan (aksi), maka sistem itu akan mengadakan reaksi yang cenderung mengurangi pengaruh aksi tersebut. Secara singkat, azas Le Chatelier dapat disimpulkan sebagai berikut: Reaksi = Aksi Cara sistem bereaksi adalah dengan melakukan pergeseran ke kiri atau ke kanan. Marilah kita bahas penerapan azas Le Chatelier untuk meramalkan arah pergeseran kesetimbangan. 3.3.b. Pengaruh Konsentrasi Sesuai dengan azas Le Chatelier (reaksi = aksi), jika konsentrasi salah satu komponen diperbesar maka reaksi sistem adalah mengurangi komponen tersebut. Sebaliknya, jika konsentrasi salah satu komponen diperkecil, maka reaksi sistem adalah menambah komponen itu. Jika konsentrasi preaksi diperbesar, kesetimbangan akan bergeser ke kanan. Jika konsentrasi pereaksi diperkecil, kesetimbangan akan bergeser ke kiri. 3.3.c. Pengaruh Tekanan Penambahan tekanan dengan cara memperkecil volum akan memperbesar konsentrasi semua komponen. Sesuai dengan azas Le Chatelier, maka sistem akan bereaksi dengan mengurangi tekanan. Sebagaimana Anda ketahui, tekanan gas bergantung pada jumlah molekul dan tidak bergantung pada jenis gas. Oleh karena itu, untuk mengurangi tekanan maka reaksi kesetimbangan kesetimbangan akan bergeser ke arah yang jumlah koefisiennya lebih kecil. Sebaliknya, jika tekanan dikurangi dengan cara memperbesar volum, maka sistem akan bereaksi dengan menambah tekanan dengan cara menambah jumlah molekul. Reaksi akan bergeser ke arah yang jumlah koefisiennya lebih besar. Jika tekanan diperbesar (volum diperkecil), kesetimbangan akan bergeser ke arah yang jumlah koefisiennya terkecil. 52
9 Jika tekanan diperkecil (volum diperbesar), kesetimbangan akan bergeser ke arah yang jumlah koefisiennya terbesar. (a) (b) (c) Gambar 3.3.c. Pengaruh volum dan tekanan pada kesetimbangan N 2 (g) + 3H 2 (g) 2NH 3 (g). (a) Campuran gas N 2, H 2, dan NH 3 pada kesetimbangan. (b) Ketika tekanan ditingkatkan dengan memperkecil volum, campuran tidak lagi setimbang<k c ). (c) Reaksi bergeser ke arah kanan, jumlah total molekul gas menurun sampai terbentuk kestabilan kembali (Q c = K s ). Contoh Soal 4.5 Menerapkan Azas Le Chatelier Ditentukan kesetimbangan: (1) N 2 (g) + 3H 2 (g) 2NH 3 (g) (2) 2HI(g) H 2 (g) + 1 2(g) Ke arah mana kesetimbangan bergeser, jika tekanan diperbesar? Jawab: Jika tekanan diperbesar, maka kesetimbangan akan bergeser ke arah yang jumlah koefisiennya terkecil. (1) N 2 (g) + 3H 2 (g) 2NH 3 (g) Jumlah koefisien di ruas kiri = 3; sedangkan di ruas kanan = 2. Kesetimbangan akan bergeser ke kanan. (2) 2HI(g) H 2 (g) + I 2 (g) Jumlah koefisien di ruas kiri = 2; sedangkan di ruas kanan = 2. Kesetimbangan tidak bergeser. 3.3.d. Pengaruh Komponen Padat dan Cair 53
10 Penambahan atau pengurangan komponen yang berupa padatan atau cairan murni tidak mempengaruhi kesetimbangan. Hal ini dapat dipahami sebagai berikut. Penambahan komponen yang berupa larutan atau gas akan berpengaruh pada kerapatan antarpartikel dalam campuran. Jika suatu komponen gas atau terlarut ditambahkan, maka konsentrasi meningkat, sehingga sistem bereaksi untuk mengurangi konsentrasi. Jika yang ditambahkan berupa padatan atau cairan murni, hal itu tidak mengubah konsentrasi karena jarak antarpatikel dalam padatan dan cairan adalah tetap. Demikian juga halnya pada perubahan tekanan atau volum. Perubahan tekanan atau volum tidak mempengaruhi konsentrasi padatan atau cairan murni. Jadi, ketika mempertimbangkan pengaruh tekanan dan volum, koefisien komponen padat tidak diperhitungkan. Tekanan hanya berpengaruh pada sistem kesetimbangan gas. Komponen padat atau cair tidak menggeser kesetimbangan. Catatan: Dalam sistem larutan (pelarut air), penambahan air dalam jumlah yang signifikan dapat juga berarti memperbesar volum, sehingga kesetimbangan akan bergeser ke ruas yang jumlah koefisiennya terbesar. Contoh Soal 4.6 Menerapkan Azas Le Chatelier Diketahui reaksi kesetimbangan BiC1 3 (aq) + H 2 0(/) BiOC1(s) + 2HC1(aq) Ke arah mana kesetimbangan bergeser jika pada suhu tetap: a. ditambahkan BiC1 3? b. ditambahkan air? Jawab: a. Penambahan BiC1 3, salah satu pereaksi, menggeser kesetimbangan ke kanan. b. Penambahan air merupakan penggeseran (memperbesar volum), maka kesetimbangan akanbergeser ke kanan, yaitu ke arah koefisien yang lebih besar (jumlah koefisien di ruas kiri = 1, yaitu koefisien dari BiC1 3 ; sedangkan jumlah koefisien di ruas kanan = 2, yaitu koefisien dari HC1. Koefisien dari H 2 O dan BiOC1 tidak diperhitungkan). 3.3.e. Pengaruh Suhu 54
11 Sesuai dengan azas Le Chatelier, jika suhu sistem kesetimbangan dinaikkan, maka reaksi sistem adalah menurunkan suhu, kesetimbangan akan bergeser ke pihak reaksi yang menyerap kalor (ke pihak reaksi endoterm). Sebaliknya jika suhu diturunkan, maka kesetimbangan akan bergeser ke pihak reaksi eksoterm. ika suhu dinaikkan, kesetimbangan akan bergeser ke arah reaksi endoterm. Jika suhu diturunkan, kesetimbangan akan bergeser ke arah reaksi eksoterm. Perhatikanlah contoh soal berikut. Contoh Soal 4.7 Menganalisis pengaruh suhu pada kesetimbangan Ditentukan reaksi kesetimbangan: (1) N 2 (g) + 3H 2 (g)---> 2NH 3 (g) H= -92,2 kj (2) H20(g) > (g) (g) H = +242 kj Ke arah mana kesetimbangan bergeser jika suhu dinaikkan? Jawab: Pada kenaikan suhu, kesetimbangan bergeser ke pihak reaksi endoterm. Pada kesetimbangan (1), reaksi bergeser ke kiri. Pada kesetimbangan (2), reaksi bergeser ke kanan Kesetimbanagn Dalam Industri Kondisi reaksi menentukan hasil reaksi kesetimbangan dalam industri. Banyak pembuatan zat kimia yang didasarkan pada reaksi kesetimbangan. Agar efisien, kondisi reaksi haruslah diusahakan sedemikian sehingga menggeser kesetimbangan ke arah produk dan meminimalkan reaksi balik. Pada bagian berikut kita akan membahas bagaimana prinsip kesetimbangan diterapkan pada pembuatan amonia dan asam sulfat. 3.4.a. Pembuatan Amonia menurut Proses Haber-Bosch Nitrogen terdapat melimpah di udara, yaitu sekitar 78% volum. Walaupun demikian, senyawa nitrogen tidak terdapat banyak di alam. Satu-satunya sumber alam yang penting ialah NaNO 3 yang disebut sendawa chili. Sementara itu, kebutuhan senyawa nitrogen semakin banyak, misalnya, untuk industri pupuk, mesiu, dan bahan peledak. Oleh karena itu, proses sintesis 55
12 senyawa nitrogen, disebut fiksasi nitrogen buatan, merupakan proses industri yang sangat penting. Metode yang utama adalah mereaksikan nitrogen dengan hidrogen membentuk amonia. Selanjutnya, amonia dapat diubah menjadi senyawa nitrogen lain seperti asam nitrat dan pram nitrat. Dasar teori pembuatan amonia dan nitrogen dan hidrogen ditemukan oleh Fritz Haber (1908), seorang ahli kimia dari Jerman. Sedangkan proses industri pembuatan amonia, untuk produksi secara besar-besaran ditemukan oleh Carl Bosch, seorang insinyur kimia, juga dan Jerman. Persamaan termokimia reaksi sintesis amonia adalah: N 2 (g) + 3H 2 (g) > 2NH 3 (g) H= 92,4 kj erdasarkan prinsip kesetimbangan, kondisi yang menguntungkan untuk ketuntasan reaksi ke kanan (pembentukan NH 3 ) adalah suhu rendah dan tekanan tinggi. Akan tetapi, reaksi tersebut berlangsung sangat lambat pada suhu rendah, bahkan pada suhu 500 C. Di pihak lain, karena reaksi ke kanan eksoterm, penambahan temperatur akanmengurangi rendemen. Pada awalnya proses Haber-Bosch dilangsungkan pada suhu sekitar 500 C dan tekanan sekitar atm dengan katalis, yaitu serbuk besi dicampur dengan Al 2 0 3, MgO, CaO, dan K 2 0. Dewasa ini, dengan kemajuan teknologi, digunakan tekanan yang jauh lebih besar, bahkan mencapai 700 atm. Untuk mengurangi reaksi balik, maka amonia yang terbentuk segera dipisahkan. Diagram alur dari proses Haber-Bosch untuk sintesis amonia diberikan pada Gambar 4.5. Mula-mula campuran gas nitrogen dan hidrogen dikompresi hingga mencapai tekanan yang diinginkan. Campuran gas kemudian dipanaskan dalam suatu ruangan bersama katalisator sehingga terbentuk amonia. Campuran gas kemudian didinginkan sehingga amonia mencair. Gas nitrogen dan gas hidrogen yang belum bereaksi (dan juga amonia yang tidak mencair) diresirkulasi, sehingga pada akhimya semua diubah menjadi amonia. 3.4.b. Pembuatan Asam Su!fat menurut Proses Kontak 56
13 Satu lagi contoh industri yang berdasarkan reaksi kesetimbangan ialah pembuatan asam sulfat yang dikenal dengan proses kontak. Reaksi yang terjadi dapat diringkaskan sebagai berikut. 1. Belerang dibakar dengan udara membentuk belerang dioksida. S(s) (g) -->S0 2 (g) 2. Belerang dioksida dioksidasi lebih lanjut menjadi belerang trioksida. 2S0 2 (g) (g) 2S0 3 (g) 3. Belerang trioksida dilarutkan dalam asam sulfat pekat membentuk asam pirosulfat. H 2 SO 4 (aq) + S0 3 (g) ---> H 2 S (/) 4. Asam pirosulfat direaksikan dengan air membentuk asam sulfat pekat. H 2 S (l) + H 2 0(l) H 2 SO 4 (aq) Tahap penting dalam proses ini adalah reaksi (2). Reaksi ini merupakan reaksi kesetimbangan dan eksoterm. Sama seperti pada sintesis amonia, reaksi ini hanya berlangsung baik pada suhu tinggi. Akan tetapi, pada suhu tinggi justru kesetimbangan bergeser ke kiri. Pada proses kontak digunakan suhu sekitar 500 C dan katalis V Sebenarnya tekanan besar akan menguntungkan produksi SO 3, tetapi penambahan tekanan temyata tidak diimbangi penambahan hasil yang memadai. Oleh karena itu, pada proses kontak tidak digunakan tekanan besar melainkan tekanan normal, 1 atm Rangkuman Materi 1. Reaksi kimia ada yang berlangsung searah ada pula yang dapat balik. Reaksi dapat balik yang berlangsung dalam sistem tertutup akan berakhir dengan kesetimbangan. 2. Kesetimbangan tercapai pada saat laju reaksi maju sama dengan laju reaksi balik. 3. Pada keadaan setimbang tidak terjadi perubahan makroskopis, tetapi pada tingkat mikroskopis reaksi tetap berlangsung. Oleh karena itu, kesetimbangan kimia disebut juga kesetimbangan dinamis. 4. Kesetimbangan kimia hanya dapat terjadi dalam sistem tertutup. 57
14 5. Tetapan kesetimbangan (K) adalah nisbah konsentrasi produk terhadap pereaksi, masingmasing dipangkatkan dengan koefisien reaksinya, dan merupakan bilangan konstan. 6. Sistem kesetimbangan gas juga mempunyai tetapan kesetimbangan tekanan (K r ). Nilai tetapan kesetimbangan tekanan adalah nisbah tekanan dari produk terhadap pereaksi, masingmasing dipangkatkan dengan koefisien reaksinya. 7. Hubungan K p dengan K p K ( R T? ' 8. Posisi kesetimbangan dapat dipengaruhi oleh faktor-faktor luar seperti suhu, tekanan, dan konsentrasi. 9. Pengaruh konsentrasi, tekanan, dan suhu terhadap letak kesetimbangan dapat diramalkan dengan azas La Chatelier. 10. Prinsip-prinsip kesetimbangan diterapkan dalam industri untuk mencapai hasil yang optimum. "Hari ini, Anda adalah orang yang sama dengan Anda di lima tahun endatang, kecuali dua hal: orang-orang di sekeliling Anda dan buku-buku yang Anda baca." Charles Jones 3.6. Latihan I. PILIHAN GANDA 1. Suatu kesetimbangan dikatakan dinamis, apabila dalam keadaan setimbang. A. reaksi berjalan ke dua arah dan bersifat mikroskopis B. ada perubahan dari kin ke kanan tetapi jumlahnya setimbang C. reaksi dari kiri selalu sama dengan reaksi dari kanan D. perubahan kesetimbangan dari kiri dan kanan yang berlangsung terusmenerus E. reaksi berlangsung terus-menerus bersifat makroskopis 58
15 2. Larutan FeC1 3 bereaksi dengan larutan KSCN membentuk ion (FeSCN) 2+ yang berwarna merah menurut persamaan: Fe 3+ (aq) + SCN - (aq) Fe(SCN) 2+ (aq) Apabila pada suhu tetap pada sistem itu ditambah air, maka.... A. kesetimbangan akan bergeser ke kanan, warna makin merah dan harga K bertambah B. kesetimbangan bergeser ke kiri, warna makin merah, dan harga K berkurang C. kesetimbangan bergeser ke kiri, warna luntur, dan harga K berkurang D. kesetimbangan bergeser ke kiri, warna luntur tetapi harga K tetap E. kesetimbangan tidak bergeser 3. Di antara persamaan reaksi kesetimbangan di bawah ini, kesetimbangan yang bergeser ke kanan jika tekanan diperbesar adalah.... A. 2HI(g) H 2 (g) + I 2 (g) D. 2N0(g) (g) 2NO 2 (g) B. N (g) 2NO 2 (g) E. S(s) (g) S0 2 (g) C. CaCO 3 (s) CaO(s) + CO 2 (g) 4. Pada reaksi kesetimbangan berikut, N 2 (g) + 3H 2 (g) 2NH 3 (g) MI = -92 kj jika suhu diturunkan, maka.... A. NH 3 akan bertambah D. H 2 akan bertambah B. NH 3 akan berkurang E. N 2 dan H 2 akan bertambah C. N 2 akan bertambah 5. Untuk reaksi kesetimbangan berikut, CO(g) + 3H 2 (g)ch 4 (g) + H 2 0(g) bila pada suhu tetap volum sistem diperkecil maka.... A. kesetimbangan bergeser ke kanan dan harga K semakin besar B. kesetimbangan bergeser ke kiri dan harga K semakin kecil C. kesetimbangan bergeser ke kanan dan harga K semakin kecil D. kesetimbangan bergeser ke kiri dan harga K semakin besar E. kesetimbangan bergeser ke kanan dan harga K tetap 6. Pada reaksi kesetimbangan: 3Fe(s) + 4H 2 0(g) Fe (s) + 4H 2 (g) OH = positi kesetimbangan akan bergeser ke kanan apabila.... A. pada suhu tetap ditambah serbuk besi B. pada suhu tetap ditambah suatu katalis C. pada suhu tetap tekanan diperbesar dengan memperkecil volum D. pada volum tetap suhu dinaikkan E. pada volum tetap suhu diturunkan 7. Perhatikan kesetimbangan 2X(g) + Y(g)3P(g) + Q(g). Jika ke dalam suatu ruang 59
16 hampa dimasukkan zat X dan Y dengan jumlah mol yang sama, dan bila tercapai kesetimbangan akan selalu berlaku.... A. [Y] = [Q] D. [Y] < [X] [X] < [Y] E. [X] + [Y] > [P] + [Q] 8. Pada reaksi kesetimbangan A + BC + D, kesetimbangan akan lebih cepat tercapai apabila.... A. zat A ditambah D. digunakan katalis B. tekanan diperbesar E. suhu dinaikkan C. volum diperbesar 9. Reaksi penting pada pembuatan asam sulfat menurut proses kontak ialah 2S0 2 (g) (g) 2S0 3 (g) All = -.188,2 kj Agar diperoleh hasil optimum, maka faktor yang dapat diubah adalah.. A. menambah katalis dan menurunkan suhu B. C. menaikkan suhu dan tekanan reaksi menurunkan tekanan dan menambah suhu D. menaikkan tekanan dan menurunkan suhu E. memperbesar volum dan menambah suhu 10. Ke dalam ruangan tertutup dimasukkan 1 mol gas A dan 1 mol gas B. Setelah bereaksi menurut persamaan 2A + 3B A 2 B 3 dan dicapai kesetimbangan, masih terdapat 0,25 mol gas B. Kalau volum ruang 1 dm 3, maka tetapan kesetimbangan reaksi tersebut ialah.... A. 16 D. 72 B. 32 E. 80 C Pada reaksi kesetimbangan dari CO + H 2 OCO 2 + H 2 harga K = 0,80. Untuk menghasilkan 4 mol H 2 per liter dan 6 mol H 2 O per liter, jumlah gas CO yang hares ditambahkan adalah.... A. 20 mol L -1 D. 12 mol L -1 B. 16 mol L -1 E. 10 mol C. 14 mol L Sebanyak 20 ml oksigen dan 40 ml belerang dioksida direaksikan pada suhu dan tekanan tetap membentuk belerang trioksida menurut reaksi setimbang: 2S0 2 (g) (g) 2S0 3 (g) Bila volum akhir sistem adalah 45 ml, maka belerang trioksida yang terbentuk adalah.... A. 15 ml D. 30 ml B. 20 ml E. 45 ml C. 25 ml 60
17 I. HUBUNGAN ANTARHAL 13. Jika suatu reaksi mencapai kesetimbangan, maka komposisi campuran reaksinya tidak akandapat berubah selama suhu tidak berubah SEBAB tetapan kesetimbangan reaksi kimia bergantung pada suhu. 14. Katalis mempengaruhi kesetimbangan reaksi katalis mempengaruhi laju reaksi. SEBAB III. ASOSIASI PILIHAN GANDA 15. Pada 298 K, reaksi N (g)2no 2 (g) AH = 57,2 kj diketahui dapat mencapai kesetimbangan dengan K p = 0,14. Dapat disimpulkan bahwa.... (1) reaksi tersebut bersifat endoterm (2) jika dua mol NO 2 bereaksi pada 298 K hingga mencapai kesetimbangan, maka akan diserap kalor sebanyak 57,2 kj (3) jika reaksi dimulai dengan N 2 O 4, maka dalam kesetimbangan konsentrasi NO 2 lebih rendah dan konsentrasi N 2 O 4 peningkatan suhu akan meningkatkan kadar N 2 O 4 dalam campuran reaksi dalam kesetimbanga 61
Kesetimbangan Kimia. Bab 4
 Kesetimbangan Kimia Bab 4 Standar Kompetensi 3. Memahami kinetika reaksi, kesetimbangan kimia, dan faktor-faktor yang memengaruhinya, serta penerapannya dalam kehidupan sehari-hari dan industri Kompetensi
Kesetimbangan Kimia Bab 4 Standar Kompetensi 3. Memahami kinetika reaksi, kesetimbangan kimia, dan faktor-faktor yang memengaruhinya, serta penerapannya dalam kehidupan sehari-hari dan industri Kompetensi
KESETIMBANGAN KIMIA SOAL DAN PEMBAHASAN
 KESETIMBANGAN KIMIA SOAL DAN PEMBAHASAN 1. Suatu reaksi dikatakan mencapai kesetimbangan apabila. A. laju reaksi ke kiri sama dengan ke kanan B. jumlah koefisien reaksi ruas kiri sama dengan ruas kanan
KESETIMBANGAN KIMIA SOAL DAN PEMBAHASAN 1. Suatu reaksi dikatakan mencapai kesetimbangan apabila. A. laju reaksi ke kiri sama dengan ke kanan B. jumlah koefisien reaksi ruas kiri sama dengan ruas kanan
kimia KESETIMBANGAN KIMIA 2 Tujuan Pembelajaran
 KTSP & K-13 kimia K e l a s XI KESETIMBANGAN KIMIA 2 Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami faktor-faktor yang memengaruhi kesetimbangan.
KTSP & K-13 kimia K e l a s XI KESETIMBANGAN KIMIA 2 Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami faktor-faktor yang memengaruhi kesetimbangan.
Kesetimbangan Kimia KIM 2 A. PENDAHULUAN B. REAKSI KESETIMBANGAN. α = KESETIMBANGAN KIMIA. materi78.co.nr. setimbang
 konsentrasi laju reaksi materi78.co.nr Kesetimbangan Kimia A. PENDAHULUAN Reaksi satu arah (irreversible) atau reaksi tidak dapat balik adalah reaksi yang terjadi pada satu arah, dan produknya tidak dapat
konsentrasi laju reaksi materi78.co.nr Kesetimbangan Kimia A. PENDAHULUAN Reaksi satu arah (irreversible) atau reaksi tidak dapat balik adalah reaksi yang terjadi pada satu arah, dan produknya tidak dapat
MODUL III KESETIMBANGAN KIMIA
 MODUL III KESETIMBANGAN KIMIA I. Petunjuk Umum 1. Kompetensi Dasar 1) Mahasiswa memahami Asas Le Chatelier 2) Mahasiswa mampu menjelaskan aplikasi reaksi kesetimbangan dalam dunia industry 3) Mahasiswa
MODUL III KESETIMBANGAN KIMIA I. Petunjuk Umum 1. Kompetensi Dasar 1) Mahasiswa memahami Asas Le Chatelier 2) Mahasiswa mampu menjelaskan aplikasi reaksi kesetimbangan dalam dunia industry 3) Mahasiswa
A. ARTI KESETIMBANGAN B. FAKTOR-FAKTOR YANG MEMPENGARUHI PERGESERAN KESETIMBANGAN C. TETAPAN KESETIMBANGAN D. KESETIMBANGAN KIMIA DALAM INDUSTRI
 4 KESETIMBANGAN KIMIA A. ARTI KESETIMBANGAN B. FAKTOR-FAKTOR YANG MEMPENGARUHI PERGESERAN KESETIMBANGAN C. TETAPAN KESETIMBANGAN D. KESETIMBANGAN KIMIA DALAM INDUSTRI Dalam kehidupan sehari-hari, sering
4 KESETIMBANGAN KIMIA A. ARTI KESETIMBANGAN B. FAKTOR-FAKTOR YANG MEMPENGARUHI PERGESERAN KESETIMBANGAN C. TETAPAN KESETIMBANGAN D. KESETIMBANGAN KIMIA DALAM INDUSTRI Dalam kehidupan sehari-hari, sering
MODUL KIMIA SMA IPA Kelas 11
 SMA IPA Kelas Di sekitar kita banyak dijumpai peristiwa reaksi kimia, misalnya reaksi pembakaran kayu, pembakaran bensin, fotosintesis, perkaratan besi dan lain sebagainya. Dalam reaksi kimia, ada reaksi
SMA IPA Kelas Di sekitar kita banyak dijumpai peristiwa reaksi kimia, misalnya reaksi pembakaran kayu, pembakaran bensin, fotosintesis, perkaratan besi dan lain sebagainya. Dalam reaksi kimia, ada reaksi
HAND OUT KIMIA XI IPA BAB IV KESETIMBANGAN KIMIA
 HAND OUT KIMIA XI IPA BAB IV KESETIMBANGAN KIMIA 1 BAB IV KESETIMBANGAN KIMIA I. Standar Kompetensi 3. Memahami kinetika reaksi, kesetimbangan kimia, dan faktor-faktor yang mempengaruhinya, serta penerapannya
HAND OUT KIMIA XI IPA BAB IV KESETIMBANGAN KIMIA 1 BAB IV KESETIMBANGAN KIMIA I. Standar Kompetensi 3. Memahami kinetika reaksi, kesetimbangan kimia, dan faktor-faktor yang mempengaruhinya, serta penerapannya
SOAL-SOAL KESETIMBANGAN KIMIA
 H=+380 kj/mol SOAL-SOAL KESETIMBANGAN KIMIA 1. Ebtanas 99 Suatu reaksi berada dalam keadaan setimbang apabila A. Reaksi ke kanan dan kiri telah berhenti B. Mol pereaksi selalu sama dengan mol hasil reaksi
H=+380 kj/mol SOAL-SOAL KESETIMBANGAN KIMIA 1. Ebtanas 99 Suatu reaksi berada dalam keadaan setimbang apabila A. Reaksi ke kanan dan kiri telah berhenti B. Mol pereaksi selalu sama dengan mol hasil reaksi
Soal Pilihan Ganda Berilah tanda silang pada huruf A, B, C, D atau E di depan jawaban yang benar!
 Soal Pilihan Ganda Berilah tanda silang pada huruf A, B, C, D atau E di depan jawaban yang benar!. Berikut ini adalah ciri-ciri terjadinya reaksi kesetimbangan, kecuali. reaksi reversibel B. terjadi dalam
Soal Pilihan Ganda Berilah tanda silang pada huruf A, B, C, D atau E di depan jawaban yang benar!. Berikut ini adalah ciri-ciri terjadinya reaksi kesetimbangan, kecuali. reaksi reversibel B. terjadi dalam
REAKSI KESETIMBANGAN Reaksi dua arah
 REAKSI KIMIA REAKSI HABIS Reaksi satu arah REAKSI KESETIMBANGAN Reaksi dua arah REAKSI KIMIA REAKSI Irreversible / reaksi habis / Reaksi tidak dapat balik Reaksi satu arah REAKSI Reversible/ reaksi dapat
REAKSI KIMIA REAKSI HABIS Reaksi satu arah REAKSI KESETIMBANGAN Reaksi dua arah REAKSI KIMIA REAKSI Irreversible / reaksi habis / Reaksi tidak dapat balik Reaksi satu arah REAKSI Reversible/ reaksi dapat
Termodinamika dan Kesetimbangan Kimia
 Termodinamika dan Kesetimbangan Kimia Dalam kesetimbangan kimia terdapat 2 reaksi yaitu reaksi irreversible dan reaksi reversible. Reaksi irreversible (reaksi searah) adalah reaksi yang berlangsung searah.
Termodinamika dan Kesetimbangan Kimia Dalam kesetimbangan kimia terdapat 2 reaksi yaitu reaksi irreversible dan reaksi reversible. Reaksi irreversible (reaksi searah) adalah reaksi yang berlangsung searah.
A. KESEIMBANGAN DINAMIS
 1 Tugas Kimia IV Prakerin KESEIMBANGAN KIMIA Coba kamu perhatikan proses pendidihan air dengan panci tertutup. Pada waktu air menguap, uap air akan tertahan dalam tutup panci. Selanjutnya, uap air akan
1 Tugas Kimia IV Prakerin KESEIMBANGAN KIMIA Coba kamu perhatikan proses pendidihan air dengan panci tertutup. Pada waktu air menguap, uap air akan tertahan dalam tutup panci. Selanjutnya, uap air akan
kecuali . kecuali . kecuali
 1. Berikut ini adalah ciri-ciri terjadinya reaksi kesetimbangan, kecuali. A. reaksi reversibel B. terjadi dalam ruang tertutup C. laju reaksi ke kiri sama dengan laju reaksi ke kanan D. reaksinya tidak
1. Berikut ini adalah ciri-ciri terjadinya reaksi kesetimbangan, kecuali. A. reaksi reversibel B. terjadi dalam ruang tertutup C. laju reaksi ke kiri sama dengan laju reaksi ke kanan D. reaksinya tidak
H 2 O (l) H 2 O (g) Kesetimbangan kimia. N 2 O 4 (g) 2NO 2 (g)
 Purwanti Widhy H Kesetimbangan adalah suatu keadaan di mana tidak ada perubahan yang terlihat seiring berjalannya waktu. Kesetimbangan kimia tercapai jika: Laju reaksi maju dan laju reaksi balik sama besar
Purwanti Widhy H Kesetimbangan adalah suatu keadaan di mana tidak ada perubahan yang terlihat seiring berjalannya waktu. Kesetimbangan kimia tercapai jika: Laju reaksi maju dan laju reaksi balik sama besar
kimia KTSP & K-13 KESETIMBANGAN KIMIA 1 K e l a s A. Reaksi Kimia Reversible dan Irreversible Tujuan Pembelajaran
 KTSP & K-13 kimia K e l a s XI KESETIMBANGAN KIMIA 1 Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami definisi reaksi kimia reversible dan irreversible..
KTSP & K-13 kimia K e l a s XI KESETIMBANGAN KIMIA 1 Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami definisi reaksi kimia reversible dan irreversible..
H 2 O (L) H 2 O (G) KESETIMBANGAN KIMIA. N 2 O 4 (G) 2NO 2 (G)
 H 2 O (L) H 2 O (G) KESETIMBANGAN KIMIA. N 2 O 4 (G) 2NO 2 (G) Purwanti Widhy H Kesetimbangan adalah suatu keadaan di mana tidak ada perubahan yang terlihat seiring berjalannya waktu. Kesetimbangan kimia
H 2 O (L) H 2 O (G) KESETIMBANGAN KIMIA. N 2 O 4 (G) 2NO 2 (G) Purwanti Widhy H Kesetimbangan adalah suatu keadaan di mana tidak ada perubahan yang terlihat seiring berjalannya waktu. Kesetimbangan kimia
Soal Soal Kesetimbangan Kimia. Proses Haber-Bosch merupakan proses pembentukan atau produksi ammonia berdasarkan reaksi:
 Nama : Fitria Puspita NIM : 1201760 Kelas : Pendidikan Kimia A Soal Soal Kesetimbangan Kimia SBMPTN 2014 Untuk soal no 1-3, bacalah narasi berikut. Proses Haber-Bosch merupakan proses pembentukan atau
Nama : Fitria Puspita NIM : 1201760 Kelas : Pendidikan Kimia A Soal Soal Kesetimbangan Kimia SBMPTN 2014 Untuk soal no 1-3, bacalah narasi berikut. Proses Haber-Bosch merupakan proses pembentukan atau
Contoh Soal & Pembahasan Reaksi Kesetimbangan
 Soal No.1 Contoh Soal & Pembahasan Reaksi Kesetimbangan Reaksi kimia ada yang berlangsung searah (berkesudahan) dan ada yang dapat balik (bolak-balik). Jelaskan perbedaanya disertai dengan contoh-contohnya.
Soal No.1 Contoh Soal & Pembahasan Reaksi Kesetimbangan Reaksi kimia ada yang berlangsung searah (berkesudahan) dan ada yang dapat balik (bolak-balik). Jelaskan perbedaanya disertai dengan contoh-contohnya.
KESETIMBANGAN. titik setimbang
 KESETIMBANGAN STANDART KOMPETENSI;. Memahami kinetika reaksi, kesetimbangan kimia, dan faktor-faktor yang berpengaruh, serta penerapannya dalam kehidupan sehari-hari. KOMPETENSI DASAR;.. Menjelaskan kestimbangan
KESETIMBANGAN STANDART KOMPETENSI;. Memahami kinetika reaksi, kesetimbangan kimia, dan faktor-faktor yang berpengaruh, serta penerapannya dalam kehidupan sehari-hari. KOMPETENSI DASAR;.. Menjelaskan kestimbangan
Kesetimbangan dinamis adalah keadaan dimana dua proses yang berlawanan terjadi dengan laju yang sama, akibatnya tidak terjadi perubahan bersih dalam
 Kesetimbangan dinamis adalah keadaan dimana dua proses yang berlawanan terjadi dengan laju yang sama, akibatnya tidak terjadi perubahan bersih dalam sistem pada kesetimbangan Uap mengembun dengan laju
Kesetimbangan dinamis adalah keadaan dimana dua proses yang berlawanan terjadi dengan laju yang sama, akibatnya tidak terjadi perubahan bersih dalam sistem pada kesetimbangan Uap mengembun dengan laju
MODUL 1 TERMOKIMIA. A. Hukum Pertama Termodinamika. B. Kalor Reaksi
 MODUL 1 TERMOKIMIA Termokimia adalah ilmu yang mempelajari hubungan antara energi panas dan energi kimia. Sebagai prasyarat untuk mempelajari termokimia, kita harus mengetahui tentang perbedaan kalor (Q)
MODUL 1 TERMOKIMIA Termokimia adalah ilmu yang mempelajari hubungan antara energi panas dan energi kimia. Sebagai prasyarat untuk mempelajari termokimia, kita harus mengetahui tentang perbedaan kalor (Q)
SKL 2 RINGKASAN MATERI. 1. Konsep mol dan Bagan Stoikiometri ( kelas X )
 SKL 2 Menerapkan hukum-hukum dasar kimia untuk memecahkan masalah dalam perhitungan kimia. o Menganalisis persamaan reaksi kimia o Menyelesaikan perhitungan kimia yang berkaitan dengan hukum dasar kimia
SKL 2 Menerapkan hukum-hukum dasar kimia untuk memecahkan masalah dalam perhitungan kimia. o Menganalisis persamaan reaksi kimia o Menyelesaikan perhitungan kimia yang berkaitan dengan hukum dasar kimia
[C] dan [D] [A] dan [B] Waktu KIM/ IND - II
![[C] dan [D] [A] dan [B] Waktu KIM/ IND - II [C] dan [D] [A] dan [B] Waktu KIM/ IND - II](/thumbs/52/30085144.jpg) Konsentrasi [C] dan [D] [A] dan [B] Waktu t KIM/ IND - II BAGIAN PROYEK PENGEMBANGAN KURIKULUM DIREKTORAT PENDIDIKAN MENENGAH KEJURUAN DIREKTORAT JENDERAL PENDIDIKAN DASAR DAN MENENGAH DEPARTEMEN PENDIDIKAN
Konsentrasi [C] dan [D] [A] dan [B] Waktu t KIM/ IND - II BAGIAN PROYEK PENGEMBANGAN KURIKULUM DIREKTORAT PENDIDIKAN MENENGAH KEJURUAN DIREKTORAT JENDERAL PENDIDIKAN DASAR DAN MENENGAH DEPARTEMEN PENDIDIKAN
BAB V PERHITUNGAN KIMIA
 BAB V PERHITUNGAN KIMIA KOMPETENSI DASAR 2.3 : Menerapkan hukum Gay Lussac dan hukum Avogadro serta konsep mol dalam menyelesaikan perhitungan kimia (stoikiometri ) Indikator : 1. Siswa dapat menghitung
BAB V PERHITUNGAN KIMIA KOMPETENSI DASAR 2.3 : Menerapkan hukum Gay Lussac dan hukum Avogadro serta konsep mol dalam menyelesaikan perhitungan kimia (stoikiometri ) Indikator : 1. Siswa dapat menghitung
Sumber: Silberberg, Chemistry: The Molecular Nature of Matter and Change
 Bab V Kesetimbangan Kimia Sumber: Silberberg, Chemistry: The Molecular Nature of Matter and Change Amonia cair digunakan sebagai pupuk. Pembuatan gas amonia menggunakan prinsip-prinsip reaksi kesetimbangan,
Bab V Kesetimbangan Kimia Sumber: Silberberg, Chemistry: The Molecular Nature of Matter and Change Amonia cair digunakan sebagai pupuk. Pembuatan gas amonia menggunakan prinsip-prinsip reaksi kesetimbangan,
KELOMPOK 6 ( ENAM ) ADHI PERMANA ANASTASIA EVIRA EVANPHILO IBIE NORISA JUMALA RHOPI KLAWA
 LAPORAN PRAKTIKUM KIMIA DISUSUN OLEH : KELOMPOK 6 ( ENAM ) ADHI PERMANA ANASTASIA EVIRA EVANPHILO IBIE NORISA JUMALA RHOPI KLAWA JANUARI 2009 SMA NEGERI 2 PALANGKARAYA I. TUJUAN PERCOBAAN : Tujuan percobaan
LAPORAN PRAKTIKUM KIMIA DISUSUN OLEH : KELOMPOK 6 ( ENAM ) ADHI PERMANA ANASTASIA EVIRA EVANPHILO IBIE NORISA JUMALA RHOPI KLAWA JANUARI 2009 SMA NEGERI 2 PALANGKARAYA I. TUJUAN PERCOBAAN : Tujuan percobaan
Faktor-Faktor yang Mempengaruhi Pergeseran Kesetimbangan
 Standar Kometensi Kometensi Dasar Menjelaskan kinetika dan kesetimbangan reaksi kimia serta faktor-faktor yang memengaruhinya. Menjelaskan engertian reaksi kesetimbangan. Menyelidiki faktor-faktor yang
Standar Kometensi Kometensi Dasar Menjelaskan kinetika dan kesetimbangan reaksi kimia serta faktor-faktor yang memengaruhinya. Menjelaskan engertian reaksi kesetimbangan. Menyelidiki faktor-faktor yang
Ria Fitriani BAHAN AJAR KESETIMBANGAN KIMIA. Kesetimbangan Kimia 0
 Ria Fitriani BAHAN AJAR KESETIMBANGAN KIMIA Kesetimbangan Kimia 0 KESETIMBANGAN KIMIA Air yang ada di permukaan bumi akan menguap ketika terkena panas matahari. Uap air di zat cair (air laut) berada dalam
Ria Fitriani BAHAN AJAR KESETIMBANGAN KIMIA Kesetimbangan Kimia 0 KESETIMBANGAN KIMIA Air yang ada di permukaan bumi akan menguap ketika terkena panas matahari. Uap air di zat cair (air laut) berada dalam
MODUL II KESETIMBANGAN KIMIA
 MODUL II KESETIMBANGAN KIMIA I. Petunjuk Umum 1. Kompetensi Dasar Mahasiswa memahami konsep kesetimbangan kimia dan mampu menyelesaikan soal/masalah yang berhubungan dengan reaksi kesetimbangan. 2. Materi
MODUL II KESETIMBANGAN KIMIA I. Petunjuk Umum 1. Kompetensi Dasar Mahasiswa memahami konsep kesetimbangan kimia dan mampu menyelesaikan soal/masalah yang berhubungan dengan reaksi kesetimbangan. 2. Materi
OAL TES SEMESTER I. I. Pilihlah jawaban yang paling tepat! a. 2d d. 3p b. 2p e. 3s c. 3d 6. Unsur X dengan nomor atom
 KIMIA XI SMA 3 S OAL TES SEMESTER I I. Pilihlah jawaban yang paling tepat!. Elektron dengan bilangan kuantum yang tidak diizinkan n = 3, l = 0, m = 0, s = - / n = 3, l =, m =, s = / c. n = 3, l =, m =
KIMIA XI SMA 3 S OAL TES SEMESTER I I. Pilihlah jawaban yang paling tepat!. Elektron dengan bilangan kuantum yang tidak diizinkan n = 3, l = 0, m = 0, s = - / n = 3, l =, m =, s = / c. n = 3, l =, m =
SOAL KIMIA 2 KELAS : XI IPA
 SOAL KIMIA KELAS : XI IPA PETUNJUK UMUM. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan. Periksa dan bacalah soal dengan teliti sebelum Anda bekerja. Kerjakanlah soal anda pada lembar jawaban
SOAL KIMIA KELAS : XI IPA PETUNJUK UMUM. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan. Periksa dan bacalah soal dengan teliti sebelum Anda bekerja. Kerjakanlah soal anda pada lembar jawaban
KONSEP MOL DAN STOIKIOMETRI
 BAB V KONSEP MOL DAN STOIKIOMETRI Dalam ilmu fisika, dikenal satuan mol untuk besaran jumlah zat. Dalam bab ini, akan dibahas mengenai konsep mol yang mendasari perhitungan kimia (stoikiometri). A. KONSEP
BAB V KONSEP MOL DAN STOIKIOMETRI Dalam ilmu fisika, dikenal satuan mol untuk besaran jumlah zat. Dalam bab ini, akan dibahas mengenai konsep mol yang mendasari perhitungan kimia (stoikiometri). A. KONSEP
BAGIAN PROYEK PENGEMBANGAN KURIKULUM
 Kode KIM.11 Kesetimbangan Kimia BAGIAN PROYEK PENGEMBANGAN KURIKULUM DIREKTORAT PENDIDIKAN MENENGAH KEJURUAN DIREKTORAT JENDERAL PENDIDIKAN DASAR DAN MENENGAH DEPARTEMEN PENDIDIKAN NASIONAL 004 Modul Kim.11.Kesetimbangan
Kode KIM.11 Kesetimbangan Kimia BAGIAN PROYEK PENGEMBANGAN KURIKULUM DIREKTORAT PENDIDIKAN MENENGAH KEJURUAN DIREKTORAT JENDERAL PENDIDIKAN DASAR DAN MENENGAH DEPARTEMEN PENDIDIKAN NASIONAL 004 Modul Kim.11.Kesetimbangan
BAB II KESETIMBANGAN KIMIA
 BAB II KESETIMBANGAN KIMIA TIU : 1. Memahami definisi kimia dan mengidentifikasi keadaan kimia. Memahami faktor-faktor yang mempengaruhi kimia: Prinsip Le Chatelier. Memahami aplikasi kimia dalam perolehan
BAB II KESETIMBANGAN KIMIA TIU : 1. Memahami definisi kimia dan mengidentifikasi keadaan kimia. Memahami faktor-faktor yang mempengaruhi kimia: Prinsip Le Chatelier. Memahami aplikasi kimia dalam perolehan
1. Perhatikan struktur senyawa berikut!
 . Perhatikan struktur senyawa berikut! CH CH CH CH CH CH CH Jumlah atom C primer, atom C sekunder, dan atom C tersier dari senyawa di atas adalah...,, dan D.,, dan,, dan E.,, dan,, dan. Di bawah ini merupakan
. Perhatikan struktur senyawa berikut! CH CH CH CH CH CH CH Jumlah atom C primer, atom C sekunder, dan atom C tersier dari senyawa di atas adalah...,, dan D.,, dan,, dan E.,, dan,, dan. Di bawah ini merupakan
HUKUM DASAR KIMIA. 2CUO. 28GRAM NITROGEN 52 GRAM MAGNESIUM NITRIDA 3 MG + N 2 MG 3 N 2
 HUKUM DASAR KIMIA. 2CUO. 28GRAM NITROGEN 52 GRAM MAGNESIUM NITRIDA 3 MG + N 2 MG 3 N 2 HUKUM DASAR KIMIA 1) Hukum Kekekalan Massa ( Hukum Lavoisier ). Yaitu : Dalam sistem tertutup, massa zat sebelum
HUKUM DASAR KIMIA. 2CUO. 28GRAM NITROGEN 52 GRAM MAGNESIUM NITRIDA 3 MG + N 2 MG 3 N 2 HUKUM DASAR KIMIA 1) Hukum Kekekalan Massa ( Hukum Lavoisier ). Yaitu : Dalam sistem tertutup, massa zat sebelum
K13 Revisi Antiremed Kelas 10 Kimia
 K13 Revisi Antiremed Kelas 10 Kimia Hukum Dasar Perhitungan Kimia - Latihan Soal Doc. Name: RK13AR10KIM0801 Version : 2016-11 halaman 1 01. Pernyataan yang paling sesuai tentang hukum Lavoisier (A) Jumlah
K13 Revisi Antiremed Kelas 10 Kimia Hukum Dasar Perhitungan Kimia - Latihan Soal Doc. Name: RK13AR10KIM0801 Version : 2016-11 halaman 1 01. Pernyataan yang paling sesuai tentang hukum Lavoisier (A) Jumlah
LEMBAR AKTIVITAS SISWA ( LAS )_ 1
 LEMBAR AKTIVITAS SISWA ( LAS )_ 1 1. Perhatikan reaksi berikut: CaCO 2 (s) CaO (s) + CO 2 (g) H = 178 KJ/mol. Jelaskan! a. Arah kesetimbangan ditambahkan CaCO 2 (s) b. Tiga kemungkinan yang dapat dilakukan
LEMBAR AKTIVITAS SISWA ( LAS )_ 1 1. Perhatikan reaksi berikut: CaCO 2 (s) CaO (s) + CO 2 (g) H = 178 KJ/mol. Jelaskan! a. Arah kesetimbangan ditambahkan CaCO 2 (s) b. Tiga kemungkinan yang dapat dilakukan
Secara umum tahapan-tahapan proses pembuatan Amoniak dapat diuraikan sebagai berikut :
 PROSES PEMBUATAN AMONIAK ( NH3 ) Amoniak diproduksi dengan mereaksikan gas Hydrogen (H 2) dan Nitrogen (N 2) dengan rasio H 2/N 2 = 3 : 1. Disamping dua komponen tersebut campuran juga berisi inlet dan
PROSES PEMBUATAN AMONIAK ( NH3 ) Amoniak diproduksi dengan mereaksikan gas Hydrogen (H 2) dan Nitrogen (N 2) dengan rasio H 2/N 2 = 3 : 1. Disamping dua komponen tersebut campuran juga berisi inlet dan
LATIHAN ULANGAN TENGAH SEMESTER 2
 Pilihlah jawaban yang paling benar LATIHAN ULANGAN TENGAH SEMESTER 2 TATANAMA 1. Nama senyawa berikut ini sesuai dengan rumus kimianya, kecuali. A. NO = nitrogen oksida B. CO 2 = karbon dioksida C. PCl
Pilihlah jawaban yang paling benar LATIHAN ULANGAN TENGAH SEMESTER 2 TATANAMA 1. Nama senyawa berikut ini sesuai dengan rumus kimianya, kecuali. A. NO = nitrogen oksida B. CO 2 = karbon dioksida C. PCl
Oleh. Dewi Candrawati
 126 Lampiran 4 Oleh Dewi Candrawati 2014 127 Petunjuk Pengerjaan: 1. Tes diagnostik ini terdiri dari delapan soal pilihan ganda dua tingkat. 2. Setiap soal memiliki 4 pilihan jawaban dan 5 pilihan alasan.
126 Lampiran 4 Oleh Dewi Candrawati 2014 127 Petunjuk Pengerjaan: 1. Tes diagnostik ini terdiri dari delapan soal pilihan ganda dua tingkat. 2. Setiap soal memiliki 4 pilihan jawaban dan 5 pilihan alasan.
Hubungan koefisien dalam persamaan reaksi dengan hitungan
 STOIKIOMETRI Pengertian Stoikiometri adalah ilmu yang mempelajari dan menghitung hubungan kuantitatif dari reaktan dan produk dalam reaksi kimia (persamaan kimia) Stoikiometri adalah hitungan kimia Hubungan
STOIKIOMETRI Pengertian Stoikiometri adalah ilmu yang mempelajari dan menghitung hubungan kuantitatif dari reaktan dan produk dalam reaksi kimia (persamaan kimia) Stoikiometri adalah hitungan kimia Hubungan
KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI
 KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI 1. Untuk membuat 500 ml larutan H2SO4 0.05 M dibutuhkan larutan H2SO4 5 M sebanyak ml a. 5 ml b. 10 ml c. 2.5 ml d. 15 ml e. 5.5
KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI 1. Untuk membuat 500 ml larutan H2SO4 0.05 M dibutuhkan larutan H2SO4 5 M sebanyak ml a. 5 ml b. 10 ml c. 2.5 ml d. 15 ml e. 5.5
: Mempelajari kesetimbangan ion-ion dalam larutan D. Tinjauan Pustaka
 A. Judul Praktikum : Kesetimbangan Kimia B. Hari/Tanggal Percobaan : Senin, 19 Maret 2012 jam 10.00-12.30 C. Tujuan Percobaan : Mempelajari kesetimbangan ion-ion dalam larutan D. Tinjauan Pustaka : Kesetimbangan
A. Judul Praktikum : Kesetimbangan Kimia B. Hari/Tanggal Percobaan : Senin, 19 Maret 2012 jam 10.00-12.30 C. Tujuan Percobaan : Mempelajari kesetimbangan ion-ion dalam larutan D. Tinjauan Pustaka : Kesetimbangan
LOGO. Stoikiometri. Tim Dosen Pengampu MK. Kimia Dasar
 LOGO Stoikiometri Tim Dosen Pengampu MK. Kimia Dasar Konsep Mol Satuan jumlah zat dalam ilmu kimia disebut mol. 1 mol zat mengandung jumlah partikel yang sama dengan jumlah partikel dalam 12 gram C 12,
LOGO Stoikiometri Tim Dosen Pengampu MK. Kimia Dasar Konsep Mol Satuan jumlah zat dalam ilmu kimia disebut mol. 1 mol zat mengandung jumlah partikel yang sama dengan jumlah partikel dalam 12 gram C 12,
D. H 2 S 2 O E. H 2 S 2 O 7
 1. Jika gas belerang dioksida dialirkan ke dalam larutan hidrogen sulfida, maka zat terakhir ini akan teroksidasi menjadi... A. S B. H 2 SO 3 C. H 2 SO 4 D. H 2 S 2 O E. H 2 S 2 O 7 Reaksi yang terjadi
1. Jika gas belerang dioksida dialirkan ke dalam larutan hidrogen sulfida, maka zat terakhir ini akan teroksidasi menjadi... A. S B. H 2 SO 3 C. H 2 SO 4 D. H 2 S 2 O E. H 2 S 2 O 7 Reaksi yang terjadi
STOIKIOMETRI I. HUKUM DASAR ILMU KIMIA
 STOIKIOMETRI I. HUKUM DASAR ILMU KIMIA a. Hukum Kekekalan Massa (Hukum Lavoisier) Massa zat sebelum dan sesudah reaksi adalah sama. Contoh: S + O 2 SO 2 2 gr 32 gr 64 gr b. Hukum Perbandingan Tetap (Hukum
STOIKIOMETRI I. HUKUM DASAR ILMU KIMIA a. Hukum Kekekalan Massa (Hukum Lavoisier) Massa zat sebelum dan sesudah reaksi adalah sama. Contoh: S + O 2 SO 2 2 gr 32 gr 64 gr b. Hukum Perbandingan Tetap (Hukum
Siswa diingatkan tentang struktur atom, bilangan kuantum, bentuk-bentuk orbital, dan konfigurasi elektron
 RENCANA PELAKSANAAN PEMBELAJARAN NO: 1 Mata Pelajaran : Kimia Kelas/Semester : XI/1 Materi Pokok : Stuktur atom dan sistem periodik unsur Pertemuan Ke- : 1 dan 2 Alokasi Waktu : 2 x pertemuan (4 x 45 menit)
RENCANA PELAKSANAAN PEMBELAJARAN NO: 1 Mata Pelajaran : Kimia Kelas/Semester : XI/1 Materi Pokok : Stuktur atom dan sistem periodik unsur Pertemuan Ke- : 1 dan 2 Alokasi Waktu : 2 x pertemuan (4 x 45 menit)
BAB VI KINETIKA REAKSI KIMIA
 BANK SOAL SELEKSI MASUK PERGURUAN TINGGI BIDANG KIMIA 1 BAB VI 1. Padatan NH 4 NO 3 diaduk hingga larut selama 77 detik dalam akuades 100 ml sesuai persamaan reaksi berikut: NH 4 NO 2 (s) + H 2 O (l) NH
BANK SOAL SELEKSI MASUK PERGURUAN TINGGI BIDANG KIMIA 1 BAB VI 1. Padatan NH 4 NO 3 diaduk hingga larut selama 77 detik dalam akuades 100 ml sesuai persamaan reaksi berikut: NH 4 NO 2 (s) + H 2 O (l) NH
Materi Pokok Bahasan :
 STOIKIOMETRI Kompetensi : Memiliki kemampuan untuk menginterpretasikan serta menerapkan dalam perhitungan kimia. Memiliki kemampuan untuk mengaplikasikan pengetahuan yang dimilikinya dan terbiasa menggunakan
STOIKIOMETRI Kompetensi : Memiliki kemampuan untuk menginterpretasikan serta menerapkan dalam perhitungan kimia. Memiliki kemampuan untuk mengaplikasikan pengetahuan yang dimilikinya dan terbiasa menggunakan
No Indikator Soal Valid
 107 Lampiran 3 Rekapitulasi asi Instrumen TDM-TWO-TIER No Indikator Soal 1 Memahami kesetimbangan Reaksi kesetimbangan antara N 2 O 4 dengan NO 2 mengikuti persamaan kimia berikut ini : ator 1 :- dinamis
107 Lampiran 3 Rekapitulasi asi Instrumen TDM-TWO-TIER No Indikator Soal 1 Memahami kesetimbangan Reaksi kesetimbangan antara N 2 O 4 dengan NO 2 mengikuti persamaan kimia berikut ini : ator 1 :- dinamis
UJIAN NASIONAL TAHUN PELAJARAN 2007/2008
 UJIAN NASIONAL TAHUN PELAJARAN 2007/2008 PANDUAN MATERI SMA DAN MA K I M I A PROGRAM STUDI IPA PUSAT PENILAIAN PENDIDIKAN BALITBANG DEPDIKNAS KATA PENGANTAR Dalam rangka sosialisasi kebijakan dan persiapan
UJIAN NASIONAL TAHUN PELAJARAN 2007/2008 PANDUAN MATERI SMA DAN MA K I M I A PROGRAM STUDI IPA PUSAT PENILAIAN PENDIDIKAN BALITBANG DEPDIKNAS KATA PENGANTAR Dalam rangka sosialisasi kebijakan dan persiapan
Kelarutan (s) dan Hasil Kali Kelarutan (Ksp)
 Kelarutan (s) dan Hasil Kali Kelarutan (Ksp) Tim Dosen Kimia Dasar FTP UNIVERSITAS BRAWIJAYA Kelarutan (s) Kelarutan (solubility) adalah jumlah maksimum suatu zat yang dapat larut dalam suatu pelarut.
Kelarutan (s) dan Hasil Kali Kelarutan (Ksp) Tim Dosen Kimia Dasar FTP UNIVERSITAS BRAWIJAYA Kelarutan (s) Kelarutan (solubility) adalah jumlah maksimum suatu zat yang dapat larut dalam suatu pelarut.
Stoikiometri. OLEH Lie Miah
 Stoikiometri OLEH Lie Miah 1 STANDAR KOMPETENSI KOMPETENSI DASAR INDIKATOR KARAKTERISTIK MATERI KESULITAN BELAJAR SISWA STANDAR KOMPETENSI Memahami hukum-hukum dasar Kimia dan penerapannya dalam perhitungan
Stoikiometri OLEH Lie Miah 1 STANDAR KOMPETENSI KOMPETENSI DASAR INDIKATOR KARAKTERISTIK MATERI KESULITAN BELAJAR SISWA STANDAR KOMPETENSI Memahami hukum-hukum dasar Kimia dan penerapannya dalam perhitungan
BAB IV TEMUAN DAN PEMBAHASAN. Dalam pengembangan strategi pembelajaran intertekstual pada materi
 BAB IV TEMUAN DAN PEMBAHASAN Dalam pengembangan strategi pembelajaran intertekstual pada materi pokok kesetimbangan kimia secara garis besar penelitian terbagi dalam beberapa tahapan yaitu: Tahap pertama
BAB IV TEMUAN DAN PEMBAHASAN Dalam pengembangan strategi pembelajaran intertekstual pada materi pokok kesetimbangan kimia secara garis besar penelitian terbagi dalam beberapa tahapan yaitu: Tahap pertama
KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI
 KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI 1. Untuk membuat 500 ml larutan H 2 SO 4 0.05 M dibutuhkan larutan H 2 SO 4 5 M sebanyak ml a. 5 ml b. 10 ml c. 2.5 ml d. 15 ml e. 5.5 ml 2. Konsentrasi larutan yang
KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI 1. Untuk membuat 500 ml larutan H 2 SO 4 0.05 M dibutuhkan larutan H 2 SO 4 5 M sebanyak ml a. 5 ml b. 10 ml c. 2.5 ml d. 15 ml e. 5.5 ml 2. Konsentrasi larutan yang
LOGO STOIKIOMETRI. Marselinus Laga Nur
 LOGO STOIKIOMETRI Marselinus Laga Nur Materi Pokok Bahasan : A. Konsep Mol B. Penentuan Rumus Kimia C. Koefisien Reaksi D. Hukum-hukum Gas A. Konsep Mol Pengertian konsep mol Hubungan mol dengan jumlah
LOGO STOIKIOMETRI Marselinus Laga Nur Materi Pokok Bahasan : A. Konsep Mol B. Penentuan Rumus Kimia C. Koefisien Reaksi D. Hukum-hukum Gas A. Konsep Mol Pengertian konsep mol Hubungan mol dengan jumlah
MODUL KESETIMBANGAN. Perhatikan reaksi berikut
 MODUL KESETIMBANGAN Perhatikan reaksi berikut a.n 2 (g) + 3H 2 (g) 2NH 3 (g), di sebut juga reaksi... b. N 2 (g) + 3H 2 (g) 2NH 3 (g), di sebut juga reaksi... Perhatikan reaksi: Maka persamaan laju reaksi
MODUL KESETIMBANGAN Perhatikan reaksi berikut a.n 2 (g) + 3H 2 (g) 2NH 3 (g), di sebut juga reaksi... b. N 2 (g) + 3H 2 (g) 2NH 3 (g), di sebut juga reaksi... Perhatikan reaksi: Maka persamaan laju reaksi
KESETIMBANGAN KIMIA. Bahan Ajar Mata Pelajaran Kimia Kelas XI Semester I. SK+KD+Indikator Materi Evaluasi Referensi
 KESETIMBANGAN KIMIA Bahan Ajar Mata Pelajaran Kimia Kelas XI Semester I SK+KD+Indikator Materi Evaluasi Referensi Standar Kompetensi dan Kompetensi Dasar Standar Kompetensi Kompetensi Dasar Standar Kompetensi
KESETIMBANGAN KIMIA Bahan Ajar Mata Pelajaran Kimia Kelas XI Semester I SK+KD+Indikator Materi Evaluasi Referensi Standar Kompetensi dan Kompetensi Dasar Standar Kompetensi Kompetensi Dasar Standar Kompetensi
PERGESERAN KESETIMBANGAN KIMIA BERBASIS MATERIAL LOKAL
 144 LEMBAR KERJA SISWA PRAKTIKUM PERGESERAN KESETIMBANGAN KIMIA BERBASIS MATERIAL LOKAL KELAS/KELOMPOK : KETUA KELOMPOK : ANGGOTA : UPI #PENDIDIKAN KIMIA AULIA WAHYUNINGTYAS #0706475 TUJUAN PERCOBAAN 1.
144 LEMBAR KERJA SISWA PRAKTIKUM PERGESERAN KESETIMBANGAN KIMIA BERBASIS MATERIAL LOKAL KELAS/KELOMPOK : KETUA KELOMPOK : ANGGOTA : UPI #PENDIDIKAN KIMIA AULIA WAHYUNINGTYAS #0706475 TUJUAN PERCOBAAN 1.
KESETIMBANGAN KIMIA A. Pendahuluan 1. Latar Belakang Keadaan setimbang adalah suatu keadaaan dimana konsentrasi seluruh zat tidak lagi mengalami
 KESETIMBANGAN KIMIA A. Pendahuluan 1. Latar Belakang Keadaan setimbang adalah suatu keadaaan dimana konsentrasi seluruh zat tidak lagi mengalami perubahan, sebab zat-zat diruas kanan terbentuk dan terurai
KESETIMBANGAN KIMIA A. Pendahuluan 1. Latar Belakang Keadaan setimbang adalah suatu keadaaan dimana konsentrasi seluruh zat tidak lagi mengalami perubahan, sebab zat-zat diruas kanan terbentuk dan terurai
STOKIOMETRI BAB. B. Konsep Mol 1. Hubungan Mol dengan Jumlah Partikel. Contoh: Jika Ar Ca = 40, Ar O = 16, Ar H = 1, tentukan Mr Ca(OH) 2!
 BAB 7 STOKIOMETRI A. Massa Molekul Relatif Massa Molekul Relatif (Mr) biasanya dihitung menggunakan data Ar masing-masing atom yang ada dalam molekul tersebut. Mr senyawa = (indeks atom x Ar atom) Contoh:
BAB 7 STOKIOMETRI A. Massa Molekul Relatif Massa Molekul Relatif (Mr) biasanya dihitung menggunakan data Ar masing-masing atom yang ada dalam molekul tersebut. Mr senyawa = (indeks atom x Ar atom) Contoh:
Kesetimbangan Kimia. Chapter 9 P N2 O 4. Kesetimbangan akan. Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi
 Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi Kesetimbangan adalah suatu keadaan di mana tidak ada perubahan yang terlihat seiring berjalannya waktu. Kesetimbangan kimia
Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi Kesetimbangan adalah suatu keadaan di mana tidak ada perubahan yang terlihat seiring berjalannya waktu. Kesetimbangan kimia
KIMIA TERAPAN STOIKIOMETRI DAN HUKUM-HUKUM KIMIA Haris Puspito Buwono
 KIMIA TERAPAN STOIKIOMETRI DAN HUKUM-HUKUM KIMIA Haris Puspito Buwono Semester Gasal 2012/2013 STOIKIOMETRI 2 STOIKIOMETRI adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif dari komposisi
KIMIA TERAPAN STOIKIOMETRI DAN HUKUM-HUKUM KIMIA Haris Puspito Buwono Semester Gasal 2012/2013 STOIKIOMETRI 2 STOIKIOMETRI adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif dari komposisi
Kesetimbangan Kimia. Tim Dosen Kimia Dasar FTP
 Kesetimbangan Kimia Tim Dosen Kimia Dasar FTP Pengertian kesetimbangan kimia Suatu sistem dikatakan setimbang jika dua proses yang berlawanan terjadi dengan laju yang sama atau dengan kata lain tidak terjadi
Kesetimbangan Kimia Tim Dosen Kimia Dasar FTP Pengertian kesetimbangan kimia Suatu sistem dikatakan setimbang jika dua proses yang berlawanan terjadi dengan laju yang sama atau dengan kata lain tidak terjadi
Waktu (t) Gambar 3.1 Grafik hubungan perubahan konsentrasi terhadap waktu
 3 LAJU REAKSI Setelah mempelajari bab ini, kamu diharapkan mampu: Menghitung konsentrasi larutan (molaritas larutan). Menganalisis faktor-faktor yang mempengaruhi laju reaksi (konsentrasi, luas permukaan,
3 LAJU REAKSI Setelah mempelajari bab ini, kamu diharapkan mampu: Menghitung konsentrasi larutan (molaritas larutan). Menganalisis faktor-faktor yang mempengaruhi laju reaksi (konsentrasi, luas permukaan,
A. MOLARITAS (M) B. KONSEP LAJU REAKSI C. PERSAMAAN LAJU REAKSI D. TEORI TUMBUKAN E. FAKTOR-FAKTOR YANG MEMPENGARUHI LAJU REAKSI
 3 LAJU REAKSI A. MOLARITAS (M) B. KONSEP LAJU REAKSI C. PERSAMAAN LAJU REAKSI D. TEORI TUMBUKAN E. FAKTOR-FAKTOR YANG MEMPENGARUHI LAJU REAKSI Materi dapat berubah dari bentuk yang satu ke bentuk yang
3 LAJU REAKSI A. MOLARITAS (M) B. KONSEP LAJU REAKSI C. PERSAMAAN LAJU REAKSI D. TEORI TUMBUKAN E. FAKTOR-FAKTOR YANG MEMPENGARUHI LAJU REAKSI Materi dapat berubah dari bentuk yang satu ke bentuk yang
RIA FITRIANI BAHAN AJAR KESETIMBANGAN KIMIA. KESETIMBANGAN KIMIA 0
 RIA FITRIANI BAHAN AJAR KESETIMBANGAN KIMIA. KESETIMBANGAN KIMIA 0 Ria Fitriani BAHAN AJAR KESETIMBANGAN KIMIA Kesetimbangan Kimia 0 KESETIMBANGAN KIMIA Air yang ada di permukaan bumi akan menguap ketika
RIA FITRIANI BAHAN AJAR KESETIMBANGAN KIMIA. KESETIMBANGAN KIMIA 0 Ria Fitriani BAHAN AJAR KESETIMBANGAN KIMIA Kesetimbangan Kimia 0 KESETIMBANGAN KIMIA Air yang ada di permukaan bumi akan menguap ketika
SOAL LAJU REAKSI. Mol CaCO 3 = = 0.25 mol = 25. m Mr
 SOAL LAJU REAKSI 1. Untuk membuat 500 ml larutan H 2 SO 4 0.05 M dibutuhkan larutan H 2 SO 4 5 M sebanyak ml A. 5 ml B. 10 ml C. 2.5 ml D. 15 ml E. 5.5 ml : A Mencari volume yang dibutuhkan pada proses
SOAL LAJU REAKSI 1. Untuk membuat 500 ml larutan H 2 SO 4 0.05 M dibutuhkan larutan H 2 SO 4 5 M sebanyak ml A. 5 ml B. 10 ml C. 2.5 ml D. 15 ml E. 5.5 ml : A Mencari volume yang dibutuhkan pada proses
Wardaya College IKATAN KIMIA STOIKIOMETRI TERMOKIMIA CHEMISTRY. Part III. Summer Olympiad Camp Kimia SMA
 Part I IKATAN KIMIA CHEMISTRY Summer Olympiad Camp 2017 - Kimia SMA 1. Untuk menggambarkan ikatan yang terjadi dalam suatu molekul kita menggunakan struktur Lewis atau 'dot and cross' (a) Tuliskan formula
Part I IKATAN KIMIA CHEMISTRY Summer Olympiad Camp 2017 - Kimia SMA 1. Untuk menggambarkan ikatan yang terjadi dalam suatu molekul kita menggunakan struktur Lewis atau 'dot and cross' (a) Tuliskan formula
PETA KONSEP LAJU REAKSI. Percobaan. Waktu perubahan. Hasil reaksi. Pereaksi. Katalis. Suhu pereaksi. Konsentrasi. Luas. permukaan.
 PETA KONSEP LAJU REAKSI Berkaitan dengan ditentukan melalui Waktu perubahan Dipengaruhi oleh Percobaan dari Pereaksi Hasil reaksi Konsentrasi Luas Katalis Suhu pereaksi permukaan menentukan membentuk mengadakan
PETA KONSEP LAJU REAKSI Berkaitan dengan ditentukan melalui Waktu perubahan Dipengaruhi oleh Percobaan dari Pereaksi Hasil reaksi Konsentrasi Luas Katalis Suhu pereaksi permukaan menentukan membentuk mengadakan
Soal 5 Jumlah mol dari 29,8 gram amonium fosfat ((NH4)3PO4) (Ar N = 14, H = 1, dan P = 31) adalah. A. 0,05 mol
 Bank Soal Stoikiometri Kimia Bagian 2 Soal 1 Satu liter campuran gas terdiri dari 60% volume metana (CH4) dan sisanya gas etana (C2H6) dibakar sempurna sesuai reaksi: CH4 + 3 O2 2 CO2 + 2 H2O 2 C2H6 +
Bank Soal Stoikiometri Kimia Bagian 2 Soal 1 Satu liter campuran gas terdiri dari 60% volume metana (CH4) dan sisanya gas etana (C2H6) dibakar sempurna sesuai reaksi: CH4 + 3 O2 2 CO2 + 2 H2O 2 C2H6 +
H = H hasil reaksi H pereaksi. Larutan HCl
 Standar Kompetensi Kompetensi Dasar Memahami perubahan energi dalam kimia, cara pengukuran dan sifat ketidakteraturan dalam alam semesta. Menjelaskan pengertian tentang entalpi suatu zat dan perubahannya.
Standar Kompetensi Kompetensi Dasar Memahami perubahan energi dalam kimia, cara pengukuran dan sifat ketidakteraturan dalam alam semesta. Menjelaskan pengertian tentang entalpi suatu zat dan perubahannya.
LEMBARAN SOAL 5. Pilih satu jawaban yang benar!
 LEMBARAN SOAL 5 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah
LEMBARAN SOAL 5 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah
1. Ciri-Ciri Reaksi Kimia
 Apakah yang dimaksud dengan reaksi kimia? Reaksi kimia adalah peristiwa perubahan kimia dari zat-zat yang bereaksi (reaktan) menjadi zat-zat hasil reaksi (produk). Pada reaksi kimia selalu dihasilkan zat-zat
Apakah yang dimaksud dengan reaksi kimia? Reaksi kimia adalah peristiwa perubahan kimia dari zat-zat yang bereaksi (reaktan) menjadi zat-zat hasil reaksi (produk). Pada reaksi kimia selalu dihasilkan zat-zat
Antiremed Kelas 10 KIMIA
 Antiremed Kelas 10 KIMIA Persiapan UAS 1 Kimia Doc Name: AR10KIM01UAS Version : 2016-07 halaman 1 01. Partikel berikut yang muatannya sebesar 19 1,6 10 C dan bermassa 1 sma (A) elektron (B) proton (C)
Antiremed Kelas 10 KIMIA Persiapan UAS 1 Kimia Doc Name: AR10KIM01UAS Version : 2016-07 halaman 1 01. Partikel berikut yang muatannya sebesar 19 1,6 10 C dan bermassa 1 sma (A) elektron (B) proton (C)
 TRY OUT SELEKSI OLIMPIADE TINGKAT KABUPATEN/KOTA 2010 TIM OLIMPIADE KIMIA INDONESIA 2011 Waktu: 150 Menit PUSAT KLINIK PENDIDIKAN INDONESIA (PKPI) bekerjasama dengan LEMBAGA BIMBINGAN BELAJAR SSCIntersolusi
TRY OUT SELEKSI OLIMPIADE TINGKAT KABUPATEN/KOTA 2010 TIM OLIMPIADE KIMIA INDONESIA 2011 Waktu: 150 Menit PUSAT KLINIK PENDIDIKAN INDONESIA (PKPI) bekerjasama dengan LEMBAGA BIMBINGAN BELAJAR SSCIntersolusi
Stoikiometri. Bab 3. Massa atom merupakan massa dari atom dalam satuan massa atom (sma). Secara Mikro atom & molekul.
 Bab 3 Stoikiometri Secara Mikro atom & molekul Secara Makro gram Massa atom merupakan massa dari atom dalam satuan massa atom (sma). Perjanjian internasional: 1 atom 12 C beratnya 12 sma Jika ditimbang
Bab 3 Stoikiometri Secara Mikro atom & molekul Secara Makro gram Massa atom merupakan massa dari atom dalam satuan massa atom (sma). Perjanjian internasional: 1 atom 12 C beratnya 12 sma Jika ditimbang
STOKIOMETRI. Kimia Kelas X
 STOKIOMETRI Kimia Kelas X SEKOLAH MENENGAH ATAS NEGERI 12 SURABAYA 2015 STOKIOMETRI STOKIOMETRI Pada materi stokiometri, kita akan mempelajari beberapa hal seperti persamaan reaksi, hukum-hukum dasar kimia,
STOKIOMETRI Kimia Kelas X SEKOLAH MENENGAH ATAS NEGERI 12 SURABAYA 2015 STOKIOMETRI STOKIOMETRI Pada materi stokiometri, kita akan mempelajari beberapa hal seperti persamaan reaksi, hukum-hukum dasar kimia,
SMAN 1 MATAULI PANDAN
 LAPORAN PRAKTIKUM KIMIA D I S U S U N OLEH KELOMPOK IV Chaidi Reza Depari Firdanta Ginting Hadi Mulki Siregar Lazuardyas Ligardi Zulhanggari Dwitama XI IPA 1 SMAN 1 MATAULI PANDAN 2013 Percobaan II Reaksi
LAPORAN PRAKTIKUM KIMIA D I S U S U N OLEH KELOMPOK IV Chaidi Reza Depari Firdanta Ginting Hadi Mulki Siregar Lazuardyas Ligardi Zulhanggari Dwitama XI IPA 1 SMAN 1 MATAULI PANDAN 2013 Percobaan II Reaksi
2. Konfigurasi elektron dua buah unsur tidak sebenarnya:
 . Atom X memiliki elektron valensi dengan bilangan kuantum: n =, l =, m = 0, dan s =. Periode dan golongan yang mungkin untuk atom X adalah A. dan IIIB B. dan VA C. 4 dan III B D. 4 dan V B E. 5 dan III
. Atom X memiliki elektron valensi dengan bilangan kuantum: n =, l =, m = 0, dan s =. Periode dan golongan yang mungkin untuk atom X adalah A. dan IIIB B. dan VA C. 4 dan III B D. 4 dan V B E. 5 dan III
BAB 2. PERSAMAAN KIMIA DAN HASIL REAKSI
 BAB 2. PERSAMAAN KIMIA DAN HASIL REAKSI 1. RUMUS KIMIA 2. MENULISKAN PERSAMAAN KIMIA YANG BALANS 3. HUBUNGAN MASSA DALAM REAKSI KIMIA 4. REAKTAN PEMBATAS 5. HASIL PERSENTASE Reaktan (Pereaksi) Produk (Hasil
BAB 2. PERSAMAAN KIMIA DAN HASIL REAKSI 1. RUMUS KIMIA 2. MENULISKAN PERSAMAAN KIMIA YANG BALANS 3. HUBUNGAN MASSA DALAM REAKSI KIMIA 4. REAKTAN PEMBATAS 5. HASIL PERSENTASE Reaktan (Pereaksi) Produk (Hasil
BAB IV TERMOKIMIA A. PENGERTIAN KALOR REAKSI
 BAB IV TERMOKIMIA A. Standar Kompetensi: Memahami tentang ilmu kimia dan dasar-dasarnya serta mampu menerapkannya dalam kehidupan se-hari-hari terutama yang berhubungan langsung dengan kehidupan. B. Kompetensi
BAB IV TERMOKIMIA A. Standar Kompetensi: Memahami tentang ilmu kimia dan dasar-dasarnya serta mampu menerapkannya dalam kehidupan se-hari-hari terutama yang berhubungan langsung dengan kehidupan. B. Kompetensi
TERMOKIMIA. Sistem terbagi atas: 1. Sistem tersekat: Antara sistem dan lingkungan tidak dapat terjadi pertukaran energi maupun materi
 TERMOKIMIA almair amrulloh 12:04:00 AM 11 IPAKimia 11 IPA Asas kekekalan energi menyatakan bahwa energi tidak dapat diciptakan atau dimusnahkan, tetapi energi dapat diubah dari satu bentuk kebentuk lain
TERMOKIMIA almair amrulloh 12:04:00 AM 11 IPAKimia 11 IPA Asas kekekalan energi menyatakan bahwa energi tidak dapat diciptakan atau dimusnahkan, tetapi energi dapat diubah dari satu bentuk kebentuk lain
1. Isilah Biodata anda dengan lengkap (di lembar Jawaban) Tulis dengan huruf cetak dan jangan disingkat!
 Petunjuk : 1. Isilah Biodata anda dengan lengkap (di lembar Jawaban) Tulis dengan huruf cetak dan jangan disingkat! 2. Soal Teori ini terdiri dari dua bagian: A. 30 soal pilihan Ganda : 60 poin B. 5 Nomor
Petunjuk : 1. Isilah Biodata anda dengan lengkap (di lembar Jawaban) Tulis dengan huruf cetak dan jangan disingkat! 2. Soal Teori ini terdiri dari dua bagian: A. 30 soal pilihan Ganda : 60 poin B. 5 Nomor
Tujuh4reaksi - - REAKSI KIMIA - - 2H 2 (g) + O 2(g) 2H 2 O ( l ) Reaksi Kimia 7206 Kimia. Reaksi Kimia
 - - REAKSI KIMIA - - Modul ini singkron dengan Aplikasi Android, Download melalui Play Store di HP Kamu, ketik di pencarian Tujuh4reaksi Jika Kamu kesulitan, Tanyakan ke tentor bagaimana cara downloadnya.
- - REAKSI KIMIA - - Modul ini singkron dengan Aplikasi Android, Download melalui Play Store di HP Kamu, ketik di pencarian Tujuh4reaksi Jika Kamu kesulitan, Tanyakan ke tentor bagaimana cara downloadnya.
Sebutkan data pada kalor yang diserap atau dikeluarkan pada sistem reaksi!
 contoh soal termokimia dan pembahasannya 1. Apa yang dimaksud dengan energi kinetik dan energi potensial? Jawab : Energi kinetik adalah energi yang terkandung di dalam materi yang bergerak, sedangkan energi
contoh soal termokimia dan pembahasannya 1. Apa yang dimaksud dengan energi kinetik dan energi potensial? Jawab : Energi kinetik adalah energi yang terkandung di dalam materi yang bergerak, sedangkan energi
MODUL KIMIA SMA IPA Kelas 10
 SMA IPA Kelas 0 A. Massa Atom. Massa Atom Relatif (Ar) Massa atom relatif (Ar) merupakan perbandingan massa atom dengan massa satu atom yang tetap. Secara matematis dapat dirumuskan sebagai berikut. sma
SMA IPA Kelas 0 A. Massa Atom. Massa Atom Relatif (Ar) Massa atom relatif (Ar) merupakan perbandingan massa atom dengan massa satu atom yang tetap. Secara matematis dapat dirumuskan sebagai berikut. sma
1. Hukum Lavoisier 2. Hukum Proust 3. Hukum Dalton 4. Hukum Gay Lussac & Hipotesis Avogadro
 - - 1. Hukum Lavoisier 2. Hukum Proust 3. Hukum Dalton 4. Hukum Gay Lussac & Hipotesis Avogadro 1. Hukum Lavoisier (Hukum Kekekalan Massa) : Dalam sistem tertutup, massa zat sebelum dan sesudah reaksi
- - 1. Hukum Lavoisier 2. Hukum Proust 3. Hukum Dalton 4. Hukum Gay Lussac & Hipotesis Avogadro 1. Hukum Lavoisier (Hukum Kekekalan Massa) : Dalam sistem tertutup, massa zat sebelum dan sesudah reaksi
Massa atom merupakan massa dari atom dalam satuan massa atom (sma).
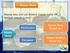 Bab 3 Stoikiometri Secara Mikro atom & molekul Secara Makro gram Massa atom merupakan massa dari atom dalam satuan massa atom (sma). Perjanjian internasional: 1 atom 12 C beratnya 12 sma Jika ditimbang
Bab 3 Stoikiometri Secara Mikro atom & molekul Secara Makro gram Massa atom merupakan massa dari atom dalam satuan massa atom (sma). Perjanjian internasional: 1 atom 12 C beratnya 12 sma Jika ditimbang
TERMOKIMIA. Hukum Hess Perubahan entalpi reaksi tetap sama, baik berlangsung dalam satu tahap maupun beberapa tahap.
 TERMOKIMIA (Teori) Entalpi adalah jumlah total energi kalor yang terkandung dalam suatu materi Reaksi Eksoterm Menghasilkan kalor Melepas energi Perubahan entalpi negatif Reaksi Endoterm Menyerap kalor
TERMOKIMIA (Teori) Entalpi adalah jumlah total energi kalor yang terkandung dalam suatu materi Reaksi Eksoterm Menghasilkan kalor Melepas energi Perubahan entalpi negatif Reaksi Endoterm Menyerap kalor
AMALDO FIRJARAHADI TANE
 DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN UTUL UGM KIMIA 2013 Page 1 1. 2. MATERI: HUKUM-HUKUM DASAR KIMIA Di soal diketahui dan ditanya: m (NH 2 ) 2 CO = 12.000 ton/tahun (pabrik) m N 2 = ton/tahun?
DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN UTUL UGM KIMIA 2013 Page 1 1. 2. MATERI: HUKUM-HUKUM DASAR KIMIA Di soal diketahui dan ditanya: m (NH 2 ) 2 CO = 12.000 ton/tahun (pabrik) m N 2 = ton/tahun?
AMALDO FIRJARAHADI TANE
 DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN UTUL UGM KIMIA 2013 Page 1 1. 2. MATERI: TERMOKIMIA Pada soal diketahui dan ditanya: ΔH c C 2 H 5 OH = -1380 kj/mol ΔH d C 6 H 12 O 6 = -60 kj/mol ΔH c C
DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN UTUL UGM KIMIA 2013 Page 1 1. 2. MATERI: TERMOKIMIA Pada soal diketahui dan ditanya: ΔH c C 2 H 5 OH = -1380 kj/mol ΔH d C 6 H 12 O 6 = -60 kj/mol ΔH c C
Bab IV Hukum Dasar Kimia
 Bab IV Hukum Dasar Kimia Sumber: Silberberg, Chemistry :The Molecular Nature of Matter and Change Kalsium karbonat ditemukan pada beberapa bentuk seperti pualam, batu koral, dan kapur. Persen massa unsur-unsur
Bab IV Hukum Dasar Kimia Sumber: Silberberg, Chemistry :The Molecular Nature of Matter and Change Kalsium karbonat ditemukan pada beberapa bentuk seperti pualam, batu koral, dan kapur. Persen massa unsur-unsur
BAB IV HASIL PENELITIAN DAN PEMBAHASAN. Pemahaman siswa yang dimaksud adalah pemahaman konseptual dan pemahaman
 36 BAB IV HASIL PENELITIAN DAN PEMBAHASAN 4. 1 Hasil Penelitian Tujuan utama penelitian ini adalah mendeskripsikan tingkat pemahaman siswa XI IPA SMA Negeri 2 Limboto pada materi kesetimbangan kimia. Pemahaman
36 BAB IV HASIL PENELITIAN DAN PEMBAHASAN 4. 1 Hasil Penelitian Tujuan utama penelitian ini adalah mendeskripsikan tingkat pemahaman siswa XI IPA SMA Negeri 2 Limboto pada materi kesetimbangan kimia. Pemahaman
BAB 5 HUKUM DASAR KIMIA
 BAB 5 HUKUM DASAR KIMIA Dalam ilmu kimia perlu dipelajari massa dan volume zat-zat yang bereaksi dan zat yang dihasilkan dalam suatu reaksi kimia. Studi tentang hubungan-hubungan kuantitatif dalam suatu
BAB 5 HUKUM DASAR KIMIA Dalam ilmu kimia perlu dipelajari massa dan volume zat-zat yang bereaksi dan zat yang dihasilkan dalam suatu reaksi kimia. Studi tentang hubungan-hubungan kuantitatif dalam suatu
STOIKIOMETRI. STOIKIOMETRI adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif dari komposisi zat-zat kimia dan reaksi-reaksinya.
 STOIKIOMETRI STOIKIOMETRI adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif dari komposisi zat-zat kimia dan reaksi-reaksinya. 1.HUKUM KEKEKALAN MASSA = HUKUM LAVOISIER "Massa zat-zat sebelum
STOIKIOMETRI STOIKIOMETRI adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif dari komposisi zat-zat kimia dan reaksi-reaksinya. 1.HUKUM KEKEKALAN MASSA = HUKUM LAVOISIER "Massa zat-zat sebelum
MODUL STOIKIOMETRI 1
 MODUL STOIKIOMETRI 1 1. Pengertian Mol Mol merupakan suatu satuan jumlah, yang berasal dari kata moles yang artinya sejumlah massa / sejumlah kecil massa, hampir sama dengan lusin. 1 mol = 6,02 X 10 23
MODUL STOIKIOMETRI 1 1. Pengertian Mol Mol merupakan suatu satuan jumlah, yang berasal dari kata moles yang artinya sejumlah massa / sejumlah kecil massa, hampir sama dengan lusin. 1 mol = 6,02 X 10 23
K13 Revisi Antiremed Kelas 10 Kimia
 K1 Revisi Antiremed Kelas 10 Kimia Stoikiometri - Soal Doc. Name:RK1AR10KIM0901 Version : 2016-10 halaman 1 1. Jika diketahui massa atom C-12= p gram dan massa 1 atom unsur X adalah a gram. Massa atom
K1 Revisi Antiremed Kelas 10 Kimia Stoikiometri - Soal Doc. Name:RK1AR10KIM0901 Version : 2016-10 halaman 1 1. Jika diketahui massa atom C-12= p gram dan massa 1 atom unsur X adalah a gram. Massa atom
