ADSORPSI Pb(II) MENGGUNAKAN ZEOLIT ALAM TERMODIFIKASI ASAM FOSFAT IIS SUBARIYAH
|
|
|
- Widya Dharmawijaya
- 6 tahun lalu
- Tontonan:
Transkripsi
1 ADSORPSI Pb(II) MENGGUNAKAN ZEOLIT ALAM TERMODIFIKASI ASAM FOSFAT IIS SUBARIYAH SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR BOGOR 2011
2
3 PERNYATAAN MENGENAI TESIS DAN SUMBER INFORMASI Dengan ini saya menyatakan bahwa tesis Adsorpsi Pb(II) Menggunakan Zeolit Alam Termodifikasi Asam Fosfat adalah karya saya dengan arahan dari Komisi Pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam daftar pustaka di bagian akhir tesis ini. Bogor, Agustus 2011 Iis Subariyah NRP G
4
5 ABSTRACT IIS SUBARIYAH. Adsorption of Pb(II) Using Natural Zeolite Modified Phosphoric Acid. Under direction of ETI ROHAETI and SRI SUGIARTI. In this study, both of natural zeolite, which were obtained from Sukabumi and Lampung have been modified, using H 3 PO 4 and NaHCO 3 solution. Analysis of the zeolites using XRD, BET, SEM-EDS and Cation Exchange Capacity (CEC) showed that there are differences between zeolite before modified and the one after modification. Application of the modified zeolites as an adsorbent for Pb(II) in solution showed; the optimum adsorption capacity reached at ph of 5 and 0.2 g of adsorbent. Based on the dynamic study, both type of adsorbents for Pb(II) sorption were following pseudo second order kinetic and Langmuir equation as chemosorption. Additionally, the thermodynamic determination revealed that the adsorption were exothermic. Keywords: adsorption, H 3 PO 4, modified, NaHCO 3, natural zeolite, and Pb(II)
6
7 RINGKASAN IIS SUBARIYAH. Adsorpsi Pb(II) Menggunakan Zeolit Alam Termodifikasi Asam Fosfat. Dibimbing oleh ETI ROHAETI dan SRI SUGIARTI. Timbal (Pb) merupakan salah satu logam berat yang biasa menjadi salah satu kontaminan dalam limbah cair kegiatan industri, misalnya pada industri: pengecoran dan pemurnian, baterai, bahan bakar, kabel, serta bahan kimia yang menggunakan bahan pewarna. Keracunan Pb dapat menyebabkan gangnguan kesehatan seperti gangguan fungsi hati, ginjal, keterlambatan perkembangan mental, kemandulan dan gangguan sistem syaraf. Oleh karena itu perlu ada upaya untuk mengurangi keberadaan kontaminan ini dalam limbah atau lingkungan. Berbagai metode telah dikembangkan untuk upaya penanganan hal tersebut, salah satunya adalah adsorpsi dengan zeolit. Meskipun telah banyak dilakukan penelitian tentang adsorpsi Pb(II) dari larutan air menggunakan zeolit alam, tetapi setiap zeolit yang berbeda asalnya memerlukan penelitian tersendiri. Adsorpsi Pb(II) dengan klinoptilolit yang dimodifikasi dengan HCl dan Na-klinoptilolit menunjukkan bahwa adsorpsi Pb(II) terjadi secara spontan. Stabilitas dan kapasitas tukar kation (KTK) zeolit alam jenis klinoptilolit asal Meksiko yang dimodifikasi dengan larutan asam fosfat telah dilaporkan. Hasil penelitian menunjukkan bahwa ph larutan fosfat mempengaruhi stabilitas dan KTK dari klinoptilolit. Pada ph 4-6, perubahan kristalinitas ini tidak teramati dan jumlah aluminium mirip dengan klinoptilolit tanpa modifikasi, serta adanya kenaikan KTK dari 1.10 menjadi 1.26 mek/g. Zeolit-Y termodifikasi asam fosfat mampu menjerap ion Cu 2+ dari larutan dan kapasitas adsorpsinya meningkat 67% dibanding dengan zeolit tanpa modifikasi. Penelitain ini terdiri atas tiga tahap, yaitu perlakuan adsorben zeolit, karakterisasi adsorben dan percobaan adsorpsi. Pembuatan adsorben zeolit diawali dengan preparasi zeolit alam asal Sukabumi dan Lampung, dilanjutkan dengan aktivasi dan memodifikasinya dengan H 3 PO 4 serta mengubahnya dalam bentuk Na-zeolit dengan menambahkan NaHCO 3 jenuh. Tahap selanjutnya adalah karakterisasi adsorben yang dilakukan dengan XRD (X-Ray Diffraction), SEM- EDS (Scanning Electron Microscopy-Electron Dispersive Spectroscopy), metode BET (Brunauer-Emmett-Teller) dan penentuan KTK (Kapasitas Tukar Kation) dengan metode ammonium asetat. Tahap ketiga adalah percobaan adsorpsi Pb(II) dengan adsorben hasil modifikasi. Zeolit alam asal Sukabumi dan Lampung hasil preparasi awal dianalisis dengan XRD yang menunjukkan bahwa zeolit Sukabumi merupakan jenis mordenit dan zeolit Lampung merupakan jenis klinoptilolit. Hasil pengukuran dengan SEM menunjukkan ukuran butir berkisar antara mm. Zeolit hasil preparasi kemudian diaktivasi untuk memperoleh bentuk H-zeolit kemudian dimodifikasi dengan H 3 PO 4 dan diubah dalam bentuk Na-zeolit dengan menambahkan larutan NaHCO 3. Zeolit hasil modifikasi selanjutnya disebut Z-PNa 2 -S untuk zeolit Sukabumi dan Z-PNa 2 -L untuk zeolit Lampung. Keberhasilan dari modifikasi dapat dilihat dari kapasitas adsorpsi zeolit terhadap asam fosfat yang digunakan. Hasil perhitungan menunjukkan kapasitas adsorpsi zeolit Sukabumi dan Lampung terhadap asam fosfat berturut-turut adalah
8 iii mg/g dan mg/g. Hasil analisis unsur dengan EDS juga menunjukkan adanya unsur P pada zeolit termodifikasi, yaitu 0.07% dalam Z-PNa 2 -S dan 0.02% dalam Z-PNa 2 -L. Karakterisasi adsorben dengan metode BET, menghasilkan adanya kenaikan luas permukaan dan volume total pori setelah dilakukan modifikasi, sedangkan rata-rata diameter pori mengalami penurunan. Hal ini diduga bahwa gugus fosfat terjerap dalam rongga zeolit sehingga ukuran pori menjadi lebih kecil dari sebelum modifikasi. Hasil analisis XRD menunjukkan adanya perubahan kristalinitas zeolit sebelum dan sesudah modifikasi, yang diduga karena pengaruh dari pengotor. Difraktogram hasil analisis XRD juga masih menunjukkan puncakpuncak utama penciri klinoptilolit dan mordenit. Analisis morfologi permukaan zeolit sebelum dan sesudah modifikasi dilakukan SEM yang menunjukkan bahwa setelah modifikasi bentuk struktur kristal zeolit tampak lebih jelas. Hasil pengukuran KTK dengan metode ammonium asetat menunjukkan bahwa modifikasi dengan asam asetat dapat menaikkan KTK. Zeolit Sukabumi mengalami kenaikan KTK dari menjadi mek/100g dan zeolit Lampung dari menjadi mek/100g. Pada modifikasi zeolit dengan asam fosfat, setiap mol asam fosfat yang teradsorpsi dalam zeolit menyediakan dua mol proton yang dapat dipertukarkan dengan Na + dengan basa lemah seperti NaHCO 3. Bentuk Na-zeolit mempunyai dua Na + yang dapat dipertukarkan dengan ion NH 4 + pada penentuan KTK dengan metode ammonium asetat dibandingkan zeolit tanpa modifikasi, dan semakin banyak ion Na + yang dipertukarkan maka makin besar nilai KTKnya Zeolit Z-PNa 2 -S dan Z-PNa 2 -L hasil modifikasi digunakan unruk percobaan adsorpsi Pb(II) dengan mempelajari pengaruh dari bobot adsorben, ph, waktu kontak, konsentrasi awal dan suhu. Pada bobot adsorben 0.2 g diperoleh kapasitas adsorpsi sebesar mg/g (%adsorpsi = 99.67%) untuk Z-PNa 2 -S dan mg/g (%adsorpsi = 99.29%) untuk Z-PNa 2 -L. Faktor ph, waktu kontak dan suhu tidak memberikan pengaruh yang signifikan terhadap kenaikan kapasitas adsorpsi untuk konsentrasi awal 50 mg/l. Adsorpsi Pb(II) dengan Z-PNa 2 -S maupun Z-PNa 2 -L mengikuti persamaan kinetika orde kedua semu dan model isoterm Langmuir. Hasil perhitungan parameter termodinamika menunjukkan bahwa adsorpsi Pb(II) dengan Z-PNa 2 -S maupun Z-PNa 2 -L adalah adsorpsi kimia, spontan di lingkungan dan eksotermis. Kata kunci: adsorpsi, H 3 PO 4, modifikasi, NaHCO 3, Pb(II) dan zeolit alam.
9 Hak Cipta Milik IPB, tahun 2011 Hak Cipta dilindungi Undang-undang 1. Dilarang mengutip sebagian atau seluruhnya karya tulis ini tanpa mencantumkan atau menyebutkan sumber. a. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu masalah. b. Pengutipan tersebut tidak merugikan kepentingan yang wajar IPB 2. Dilarang mengumumkan dan memperbanyak sebagian atau seluruh karya tulis dalam bentuk laporan apapun tanpa izin IPB
10
11 ADSORPSI Pb(II) MENGGUNAKAN ZEOLIT ALAM TERMODIFIKASI ASAM FOSFAT IIS SUBARIYAH Tesis sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada Program Studi Kimia SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR BOGOR 2011
12 Penguji Luar Komisi pada Ujian Tesis: Dr. Iskandar
13 HALAMAN PENGESAHAN Judul Tesis Nama NRP Program Studi : Adsorpsi Pb(II) Menggunakan Zeolit Alam Termodifikasi Asam Fosfat : Iis Subariyah : G : Kimia Disetujui Komisi Pembimbing Dr. Eti Rohaeti Ketua Sri Sugiarti, Ph.D Anggota Diketahui Ketua Program Studi Kimia Dekan Sekolah Pascasarjana Prof. Dr. Purwantiningsih Sugita, MS Dr. Ir. Dahrul Syah, M.Sc.Agr. Tanggal Ujian: Tanggal Lulus:
14
15 PRAKATA Puji dan syukur saya panjatkan kehadirat Allah SWT atas rahmat dan karunia-nya sehingga karya ilmiah ini dapat diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan Januari sampai bulai Mei 2011 ini ialah Adsorpsi Pb(II) Menggunakan Zeolit Alam Termodifikasi Asam Fosfat. Ucapan terima kasih yang tulus kepada Dr. Eti Rohaeti selaku Ketua Komisi Pembimbing dan Sri Sugiarti, Ph.D selaku Anggota Komisi Pembimbing, atas segala curahan waktu, bimbingan, arahan, serta dorongan moral kepada saya. Ucapan terima kasih juga saya sampaikan kepada Dr. Iskandar sebagai dosen penguji luar komisi dan Dr. Dyah Iswantini Pradono, M.Agr selaku wakil dari departemen yang telah memberikan saran pada penulisan karya ilmiah ini. Ungkapan terima kasih juga disampaikan kepada suami saya serta seluruh keluarga, atas segala doa dan kasih sayangnya dan kepada Kementerian Agama Republik Indonesia yang telah mendanai pendidikan penulis selama menjalani program pascasarjna Kimia. Semoga karya ilmiah ini bermanfaat Bogor, Agustus 2011 Iis Subariyah
16
17 RIWAYAT HIDUP Penulis dilahirkan di Cilacap pada tanggal 12 Nopember 1977 dari pasangan Bapak H.Pardjan Sayuti dan Ibu Hj. Gunarti. Penulis merupakan anak kedua dari tiga bersaudara. Pendidikan sarjana ditempuh di Program Studi Kimia Universitas Gadjah Mada, lulus pada tahun Bekerja sebagai staf pengajar MTs-Al Mujtahidin Bojonggede Bogor. Pada tahun 2009 penulis mengikuti seleksi Beasiswa Utusan Daerah (BUD) yang diselenggarakan oleh Kementerian Agama Republik Indonesia dan diterima di Program Studi Kimia pada Program Pascasarjana IPB.
18
19 DAFTAR ISI DAFTAR GAMBAR DAFTAR TABEL DAFTAR LAMPIRAN. PENDAHULUAN Halaman Latar Belakang 1 Perumusan Masalah 3 Tujuan.. 3 Manfaat... 4 Hipotesis. 4 TINJAUAN PUSTAKA Zeolit... 5 Timbal. 10 Isoterm Adsorpsi. 11 Kinetika Adsorpsi Parameter Termodinamika.. 13 BAHAN DAN METODE Waktu dan Tempat Penelitian. 15 Bahan dan Alat Metode Penelitian HASIL DAN PEMBAHASAN Adsorben Zeolit.. 19 Karakterisasi Adsorben.. 21 Percobaan Adsorpsi 28 SIMPULAN DAN SARAN Simpulan 39 Saran.. 39 DAFTAR PUSTAKA 41 LAMPIRAN xi xii xiii
20
21 DAFTAR GAMBAR Halaman 1 Kerangka struktur zeolit 5 2 Struktur kristal klinoptilolit 8 3 Struktur kristal mordenit 9 4 Skema reaksi modifikasi zeolit-pna Difraktogram XRD zeolit Sukabumi 22 6 Difraktogram XRD zeolit Lampung 22 7 Difraktogram XRD zeolit Sukabumi A. tanpa perlakuan; B. setelah aktivasi; C. setelah modifikasi 25 8 Difraktogram XRD zeolit Lampung A. tanpa perlakuan; B. setelah aktivasi; C. setelah modifikasi 25 9 SEM zeolit Sukabumi perbesaran 1000x: a. tanpa perlakuan; b. setelah aktivasi; c. setelah modifikasi SEM zeolit Lampung perbesaran 1000x: a. tanpa perlakuan; b. setelah aktivasi; c. setelah modifikasi Kapasitas adsorpsi Z-PNa 2 -S dan Z-PNa 2 -L pada variasi bobot.. 12 Kapasitas adsorpsi Z-PNa 2 -S dan Z-PNa 2 -L pada variasi ph Kapasitas adsorpsi Z-PNa 2 -S dan Z-PNa 2 -L pada variasi waktu. 14 Plot kinetika orde pertama semu adsorpsi Pb(II) oleh Z-PNa 2 - S dan Z-PNa 2 -L Plot kinetika orde kedua semu adsorpsi Pb(II) oleh Z-PNa 2 -S dan Z-PNa 2 -L Isoterm adsorpsi Pb(II) oleh Z-PNa 2 -S dan Z-PNa 2 -L Isoterm Langmuir adsorpsi Pb(II) oleh Z-PNa 2 -S dan Z-PNa 2 -L Isoterm Freundlich adsorpsi Pb(II) oleh Z-PNa 2 -S dan Z-PNa 2 -L. 19 Efek variasi suhu pada adsorpsi Pb(II) oleh Z-PNa 2 -S dan Z-PNa 2 -L Hubungan antara 1/T dan ln Kd untuk Z-PNa 2 -S dan Z-PNa 2 -L
22
23 DAFTAR TABEL Halaman 1 Hasil karakterisasi zeolit Lmpung dan Sukabumi 7 2 Komponen kimia zeolit Lampung dan Sukabumi 8 3 Hasil pengukuran luas permukaan, volume pori dan diameter pori sebelum dan sesudah modifikasi zeolit Sukabumi dan Lampung.. 4 Hasil pengukuran KTK 27 5 Perbandingan konstanta laju orde pertama dan kedua semu 32 6 Parameter isoterm Langmuir dan Freunlich 34 7 Data parameter termodinamika adsorpsi Pb(II) dengan Z-PNa 2 -S dan Z-PNa 2 -L 37 23
24
25 DAFTAR LAMPIRAN Halaman 1 Bagan alir penelitian Preparasi zeolit alam Aktivasi zeolit alam Modifikasi zeolit alam dengan asam fosfat Penentuan KTK Percobaan adsorpsi 50 7 Penentuan kadar fosfat Data hasil pengukuran KTK Data hasil adsorpsi Pb(II) oleh Z-PNa 2 -S pada variasi bobot adsorben Data hasil adsorpsi Pb(II) oleh Z-PNa 2 -L pada variasi bobot adsorben Data hasil adsorpsi Pb(II) oleh Z-PNa 2 -S pada variasi ph Data hasil adsorpsi Pb(II) oleh Z-PNa 2 -L pada variasi ph Data hasil adsorpsi Pb(II) oleh Z-PNa 2 -S pada variasi waktu Data hasil adsorpsi Pb(II) oleh Z-PNa 2 -L pada variasi waktu Persamaan linear laju reaksi adsorpsi Pb(II) Data hasil adsorpsi Pb(II) oleh Z-PNa 2 -S pada variasi konsentrasi Data hasil adsorpsi Pb(II) oleh Z-PNa 2 -L pada variasi konsentrasi Data hasil analisis isoterm Langmuir dan Freundlich adsorpsi Pb(II) oleh Z-PNa 2 -S Data hasil analisis isoterm Langmuir dan Freundlich adsorpsi Pb(II) oleh Z-PNa 2 -L Data hasil adsorpsi Pb(II) oleh Z-PNa 2 -S pada variasi suhu Data hasil adsorpsi Pb(II) oleh Z-PNa 2 -L pada variasi suhu Data perhitungan parameter termodinamika
26
27 PENDAHULUAN Latar Belakang Kondisi lingkungan dapat tercemar akibat terbuangnya sejumlah polutan berbahaya. Logam berat adalah salah satu polutan yang merupakan ancaman potensial untuk kualitas air, tanah, tanaman, hewan dan kesehatan manusia. Sebagai unsur, logam berat tidak dapat dihancurkan secara kimia. Adanya unsur logam seperti timbal (Pb), kadmium (Cd), arsen (As), merkuri (Hg), dan kromium (Cr), bahkan pada konsentrasi sangat rendah (<2 ppb) tidak diinginkan karena toksisitasnya (Senthilkumar & Saraswathi, 2009). Menurut Hamidpour (2010) timbal (Pb) bersama-sama dengan kadmium (Cd) dan merkuri (Hg) merupakan kelompok tiga besar logam berat yang mempunyai potensial berbahaya bagi manusia dan lingkungan. Timbal (Pb) merupakan salah satu logam berat yang biasa menjadi salah satu kontaminan dalam limbah cair dari industri. Industri yang berpotensi sebagai sumber pencemaran Pb adalah semua industri yang memakai Pb sebagai bahan baku maupun bahan tambahan, misalnya: industri pengecoran, industri baterai, industri bahan bakar, industri kabel, dan industri kimia yang menggunakan bahan pewarna. Keracunan Pb dapat menyebabkan gangnguan kesehatan seperti gangguan fungsi hati, ginjal, keterlambatan perkembangan mental, kemandulan dan gangguan sistem syaraf (Gunay et al. 2007). Menurut Keputusan Menteri Kesehatan RI No. 907 tahun 2002 tentang syarat-syarat dan pengawasan air minum, bahwa persyaratan kualitas air minum, kadar ion Pb maksimum yang diperbolehkan adalah 0.01 mg/l. Keputusan Menteri Negara Lingkungan Hidup No. 51 tahun 1995 tentang baku mutu limbah cair bagi kegiatan industri, kadar maksimum ion Pb dalam limbah cair adalah 0.1 mg/l dan beban pencemaran maksimum g/ton. WHO (2004) mensyaratkan batas maksimum ion Pb dalam air minun mg/l. Berbagai metode telah dikembangkan untuk mengurangi keberadaan polutan logam berat, misalnya dengan pengendapan, ekstraksi padat, pertukaran ion, penguapan, proses membran, osmosis balik dan adsorpsi. Di antara teknikteknik tersebut, adsorpsi merupakan teknik yang sederhana dan efektif
28 2 (Wingenfelder et al. 2005; Wang et al. 2008). Proses adsorpsi melibatkan adanya adsorben yang mengikat molekul oleh gaya tarik-menarik antarmolekul, pertukaran ion, dan ikatan kimia. Menurut Wang & Peng (2010) keberhasilan teknik ini sebagian besar tergantung pada pengembangan adsorben yang efisien. Adsorben yang digunakan harus memenuhi kriteria yang dibutuhkan, diantaranya mempunyai daya serap yang besar terhadap solut, zat padat yang mempunyai luas permukaan yang besar, tidak larut dalam zat cair yang akan diadsorpsi, tidak beracun dan mudah didapat serta, memiliki harga yang relatif murah. Karbon aktif, mineral lempung, zeolit, biomaterial, dan beberapa limbah padat industri telah banyak digunakan sebagai adsorben untuk adsorpsi ion dan nonionik dalam pengolahan air limbah. Zeolit alam merupakan mineral aluminosilikat terhidrasi dengan struktur berpori dengan sifat fisiko kimia yang penting, misalnya tukar kation, penyaring molekul, katalisis, dan adsorpsi. Zeolit alam tanpa modifikasi dan termodifikasi telah dilaporkan untuk adsorpsi senyawa anion dan organik dari sistem air (Wang & Peng, 2010). Meskipun telah banyak dilakukan penelitian tentang adsorpsi Pb(II) dari larutan air menggunakan zeolit alam, tetapi setiap zeolit yang berbeda asalnya memerlukan penelitian tersendiri (Buasri et al. 2008). Buasri et al. (2008) melaporkan penggunaan zeolit jenis klinoptilolit untuk penghilangan Pb(II) dengan percobaan adsorpsi secara tumpak. Kapasitas adsorpsi yang didapatkan sebesar mg/g pada suhu 70 C dan isoterm adsorpsi mengikuti model isoterm Langmuir. Wang & Ariyanto (2007) juga melaporkan penggunaan zeolit alam jenis klinoptilolit sebagai adsorben Pb(II). Untuk sistem tunggal, adsorpsi ion Pb mengikuti model isoterm Freundlich, kinetika orde pertama semu dan kapasitas adsorpsi sebesar mg/g. Adsorpsi Pb(II) dengan klinoptilolit yang dimodifikasi dengan HCl telah dilakukan oleh Sprynskyy et al. (2006) dengan hasil kapasitas adsorpsi mg/g. Isoterm adsorpsi mengikuti model Freundlich dan kinetika orde kedua semu. Pengubahan klinoptilolit alam ke dalam bentuk Na-klinoptilolit dapat meningkatkan kapasitas adsorpsi terhadap Pb(II) telah dilakukan oleh Gunay et al. (2007) dan Bektas & Kara (2004). Kapasitas adsorpsi dilaporkan berturut-turut sebesar mg/g dan mg/g. Model isoterm adsorpsi dilaporkan mengikuti model Langmuir, sedangkan untuk kinetika adsorpsi berturut-turut
29 3 mengikuti orde pertama semu dan kedua semu. Gunay et al. (2007) juga melaporkan parameter termodinamika ΔG 0 = kj/mol yang menunjukkan bahwa adsorpsi Pb(II) terjadi secara spontan. Hernandez-Beltran et al. (2008) melaporkan stabilitas dan kapasitas tukar kation (KTK) dari klinoptilolit asal Meksiko yang dimodifikasi dengan larutan asam fosfat. Hasil penelitian menunjukkan bahwa ph larutan fosfat mempengaruhi stabilitas dan KTK dari klinoptilolit. Pada ph 4-6, perubahan kristalinitas tidak teramati dan terjadi kenaikan KTK dari 1.10 menjadi 1.26 mek/g. Panneerselvam et al. (2008) memodifikasi zeolit-y dengan asam fosfat untuk menjerap ion Cu 2+ dari larutan air, dan diperoleh bahwa kapasitas adsorpsinya meningkat 67% dibanding dengan zeolit tanpa modifikasi. Efek ph, waktu kontak, model kinetika, isoterm adsorpsi dan parameter termodinamika juga dilaporkan. Penyerapan Cu 2+ mengikuti model kinetika orde dua semu, isoterm Langmuir dan dari parameter termodinamika diketahui bahwa proses berjalan secara spontan. Pada penelitian ini, zeolit alam asal Sukabumi dan Lampung dimodifikasi dengan asam fosfat dan diubah dalam bentuk Na-zeolit dengan larutan NaHCO 3. Karakterisasi zeolit termodifikasi dilakukan dengan XRD (X-ray Diffraction), SEM-EDS (Scanning Electron Microscopy-Energy Dispersive Spectroscopy), metode BET (Brunauer-Emmett-Teller) untuk menentukan luas permukaan dan penentuan KTK (kapasitas tukar kation) dengan metode ammonium asetat. Hasil penelitian menunjukkan bahwa modifikasi asam fosfat dapat meningkatkan KTK zeolit alam asal Sukabumi dan Lampung. Zeolit alam hasil modifikasi diaplikasikan untuk adsorpsi Pb(II) dalam larutan berair. Adsorpi Pb(II) dengan zeolit termodifikasi tidak terlalu dipengaruhi oleh faktor ph, waktu dan suhu yang ditunjukkan oleh kapasitas adsorpsinya yang tidak berubah secara signifikan dengan adanya faktor tersebut. Proses adsorpsi Pb(II) dengan zeolit termodifikasi mengikuti model kinetika orde kedua semu, isoterm Langmuir sehingga proses adsorpsi cenderung terjadi secara kimia, spontan di lingkungan dan bersifat eksotermis.
30 4 Perumusan Masalah Zeolit alam termodifikasi asam fosfat berpotensi sebagai adsorben Pb(II) dalam media berair. Hal ini diduga disebabkan adanya gugus fosfat yang mampu mengikat Pb(II) melalui proses adsorpsi dalam media berair. Hingga saat ini studi dinamika yang meliputi kinetika dan ekuilibrium adsorpsi Pb(II) dalam media berair dengan zeolit termodifikasi asam fosfat belum pernah dilakukan. Oleh karena itu, pada penelitian ini telah dilakukan modifikasi zeolit alam asal Sukabumi dan Lampung dengan asam fosfat. Zeolit hasil modifikasi diaplikasikan untuk adsorpsi Pb(II) dalam media air serta dipelajari karakteristik adsorpsimya. Tujuan Penelitian ini bertujuan memodifikasi zeolit asal Lampung dan Sukabumi dengan asam fosfat untuk meningkatkan kapasitas tukar kation. Selain itu, untuk mempelajari karakteristik adsorpsi kedua zeolit tersebut terhadap ion Pb(II). Manfaat Dari penelitian ini diharapkan dapat diketahui seberapa besar potensi zeolit alam asal Lampung dan Sukabumi termodifikasi asam fosfat dalam menjerap ion logam Pb (II) sehingga dapat mengurangi potensi pencemaran lingkungan akibat limbah logam berat. Hipotesis 1. Zeolit alam termodifikasi asam fosfat mempunyai kapasitas tukar kation tinggi dibandingkan yang tanpa dimodifikasi. 2. Zeolit asal Lampung merupakan jenis klinoptilolit dan asal Sukabumi merupakan jenis mordenit yang masing-masing mempunyai struktur dan komposisi kimia yang berbeda sehingga karakteristik adsorpsi terhadap Pb(II) akan berbeda.
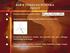
31 TINJAUAN PUSTAKA Zeolit Zeolit merupakan aluminasilikat hidrat yang mengandung logam alkali dan alkali tanah dengan rumus empiris (M + 2,M 2+ )O.Al 2 O 3. xsio 2.yH 2 O, (M + adalah Na atau K, dan M 2+ adalah Mg, Ca, atau Fe) termasuk dalam kelompok tektosilikat, memiliki bentuk tetrahedral SiO 4 tiga dimensi supercages. Di dalam struktur tektosilikat (Gambar 1), beberapa atom Si digantikan oleh atom Al melalui substitusi isomorfik, menghasilkan struktur bermuatan negatif yang berasal dari perbedaan muatan antara tetrahedral (AlO 4 ) 5- dan (SiO 4 ) 4-. Sisi negatif ini diseimbangkan oleh kation yang dapat dipetukarkan, biasanya oleh alkali dan alkali tanah, dapat digantikan oleh kation lain dalam larutan seperti Pb, Cd, Cu, Zn, dan Mn, sehingga memungkinkan zeolit bersifat sebagai penukar ion (Valdes et al. 2006, Panneerselvam et al. 2008, Jamil et al. 2010). Gambar 1 Kerangka struktur zeolit (Valdes et al. 2006) Penggunaan zeolit alam untuk remediasi lingkungan (senyawa organik dan ion logam berat) telah banyak dilaporkan. Aplikasi zeolit alam yang paling awal adalah untuk menghilangkan dan memurnikan radioisotop cesium (Cs) dan stronsium (Sr). Zeolit alam diklasifikasikan sebagai adsorben murah karena keberadaannya yang luas dan ekstraksi serta persiapannya yang murah. Zeolit
32 6 alam juga memberikan ketertarikan yang tersendiri bagi kalangan ilmuwan, terutama karena sifatnya seperti kemampuan pertukaran ion dan luas permukaan yang tinggi. Zeolit menawarkan potensi untuk berbagai kegunaan seperti penyaring molekul, penukar ion, adsorben, katalis, bahan pengisi deterjen, penghilang kation dari sumber pembuangan asam dan air limbah industri. Zeolit memiliki afinitas yang kuat untuk ion logam berat (Jamil et al. 2010). Menurut Wang & Peng (2010) zeolit mempunyai kemampuan penukar ion dengan medium eksternal, yang merupakan karakteristik zeolit. Pada umumnya reaksi pertukaran ion antara larutan yang mengandung kation A za+ dan bentuk B zeolit (B merupakan kation dengan valensi z B ) dituliskan dalam persamaan reaksi berikut: L adalah bagian dari unit kerangka zeolit yang bermuatan negatif. Sifat pertukaran ion zeolit alam tergantung pada beberapa faktor, termasuk struktur rangka, ukuran dan bentuk ion, kerapatan muatan dari kerangka anionik, muatan ion dan konsentrasi larutan elektolit luar. Karena kondisi pembentukannya zeolit alam mempunyai komposisi kimia dan kapasitas tukar kation yang berbeda-beda. Dalam penelitian ini digunakan zeolit alam asal Lampung dan asal Cikembar, Sukabumi. Menurut Las (2005) zeolit Lampung kemurnian dan sifat penukar ionnya lebih baik dari zeolit Tasikmalaya dan Sukabumi. Rohaeti (2007) telah melakukan karakterisasi zeolit Lampung dan Sukabumi dengan hasil tertera pada Tabel 1 dan Tabel 2. Klinoptilolit dan mordenit adalah aluminium silikat dengan kandungan silika tinggi. Struktur kristal klinoptilolit memiliki rongga 2-dimensi, yang dibentuk oleh lapisan tetrahedral. Rongga A (tersusun dari 10-unit cincin, diameter 0,44 x 0,72 nm) dan rongga B (tersusun dari 8-unit cincin, diameter 0,41 x 0,47 nm) yang sejajar satu sama lain, sementara rongga C (tersusun dari 8-unit cincin, diameter 0,40 x 0,55 nm) merupakan perpotongan rongga A dan B. Pengutuban dari 8 dan 10-unit cincin membentuk sistem saluran non polar (Korkuna et al. 2006). Menurut Ghiara et al. (1999), secara konvensional, komposisi batas klinoptilolit adalah Si/A1> 4.0 dan (Na + K)> (Ca + Sr + Ba).
33 7 Struktur Klinoptilolit tidak hancur setelah pemanasan selama 12 jam pada suhu 750 C. Namun, struktur Klinoptilolit yang mengandung kapur akan hancur antara suhu C. Tabel 1 Hasil Karakterisasi zeolit Lampung dan Sukabumi Parameter Asal zeolit Lampung Sukabumi Jenis zeolit Kadar zeolit (%) Mineral lain (%) Warna KTK (me/100g) Volume pori (ml/g) Luas pori (m 2 /g) Klinoptilolit Kuarsa α (5.76) Putih Mordenit Fledspar (12.91) Kuarsa α (3.25) Hijau Sumber: Rohaeti (2007) Struktur kristal mordenit lebih rumit dibandingkan klinoptilolit. Mordenit terdiri dari dua jenis rongga pori yang berbeda jenisnya dan sistem kosong. Rongga A dibentuk oleh himpunan 12-unit cincin, yang masing-masing memiliki 12 atom oksigen. Rongga B terbentuk dari 8-unit cincin di mana masing-masing memiliki 8 atom oksigen. Rongga A berbentuk elips, dengan diameter 0,65 x 0,70 nm, sedangkan diameter 8-unit cincin adalah 0,26 x 0,57 nm. Rongga A dan B saling berhubungan tegak lurus melalui rongga tabung B, dalam bentuk kantong kecil (Korkuna et al. 2006). Mordenit sering bersamaan dengan klinoptilolit, menunjukkan kondisi yang sama dalam pembentukan. Mordenit menunjukkan rasio Si/A1 berkisar , memiliki Ca , Na , dan K atom per satuan sel. Rasio Si/A1 sangat tinggi dalam mordenit menghasilkan stabilitas termal yang tinggi. Struktur rangka menunjukkan sedikit perubahan akibat dari dehidrasi, dan mineral yang stabil sampai 900 C (Ghiara et al. 1999). Gambar 2 dan 3, berturut-turut menunjukkan struktur kristal klinoptilolit dan mordenit.
34 8 Tabel 2 Komponen kimia zeolit Lampung dan Sukabumi Komponen Kadar dalam % berat Lampung SiO Al 2 O Fe 2 O TiO CaO 4.85 MgO - Na 2 O 1.61 K 2 O 1.81 Hilang pijar 7.36 Sumber: Rohaeti (2007) Sukabumi Gambar 2 Struktur kristal klinoptilolit ( 2010)
35 9 Gambar 3 Struktur kristal mordenit ( 2010) Berbagai metode dikembangkan untuk meningkatkan selektivitas dan daya adsorpsi zeolit alam maupun sintetik. Salah satu cara yang sedang berkembang adalah dengan modifikasi permukaan zeolit. Modifikasi dapat dilakukan dengan memberikan perlakuan kimia seperti direaksikan dengan asam. Memodifikasi adsorben dengan asam paling umum dan terbukti efektif dalam meningkatkan kapasitas dan efisiensi adsorben. Selama proses perlakuan dengan asam, ion H + akan menggantikan kation-kation yang tidak terikat secara kuat di dalam kerangka zeolit dan mengatur kembali letak atom yang dapat dipertukarkan. Modifikasi asam menyebabkan terjadinya dekationisasi yang menyebabkan bertambahnya luas permukaan zeolit karena berkurangnya pengotor yang menutupi pori-pori zeolit. Luas permukaan yang bertambah diharapkan meningkatkan kemampuan zeolit dalam proses adsorpsi (Tarlan-Yel & Onen 2010; Wang et al. 2010; Pentrak et al. 2009). Tarlan-Yel & Onen (2010) memodifikasi zeolit alam dengan asam nitrat untuk menghilangkan sianida bebas dan kompleks Cu-sianida dengan kapasitas adsorpsi mencapai 96%. Zeolit P termodifikasi asam hidroksamik digunakan oleh Haron et al. (2009) untuk menjerap Cu dalam larutan. Penjerapan Cu(II) mengikuti model isoterm Langmuir dengan kapasitas maksimum mg/g pada suhu 25 C dan meningkat mg/g pada suhu 70 C. Modifikasi zeolit alam
36 10 jenis klinoptilolit dengan HCl untuk menyerap ion logam berat (Pb 2+, Cu 2+, Ni 2+, dan Cd 2+ ) dalam larutan telah diteliti oleh Sprynskyy et al. (2006). Panneerselvam et al memodifikasi zeolit Y dengan asam fosfat sebagai adsorben Cu dalam larutan, dan kapasitas adsorpsi meningkat sekitar 67% dibandingkan zeolit alam tanpa modifikasi. Timbal Logam timbal (Pb) merupakan logam yang sangat populer dan banyak dikenal oleh masyarakat awam. Hal ini disebabkan oleh banyaknya Pb yang digunakan di industri nonpangan dan paling banyak menimbulkan keracunan pada makhluk hidup. Pb adalah sejenis logam yang lunak dan berwarna cokelat kehitaman, serta mudah dimurnikan dari pertambangan. Dalam pertambangan, logam ini berbentuk sulfida logam (PbS), yang sering disebut galena. Senyawa ini banyak ditemukan dalam pertambangan di seluruh dunia. Bahaya yang ditimbulkan oleh penggunaan Pb ini adalah sering menyebabkan keracunan (Astawan 2008). Kadar Pb yang secara alami dapat ditemukan dalam bebatuan sekitar 13 mg/kg. Khusus Pb yang tercampur dengan batu fosfat dan terdapat didalam batu pasir kadarnya lebih besar yaitu 100 mg/kg. Pb yang terdapat di tanah berkadar sekitar 5-25 mg/kg dan di air bawah tanah berkisar antara 1-60 µg/l. Secara alami Pb juga ditemukan di air permukaan. Kadar Pb pada air telaga dan air sungai adalah sebesar 1-10 µg/liter. Dalam air laut kadar Pb lebih rendah dari dalam air tawar. Laut yang dikatakan terbebas dari pencemaran mengandung Pb sekitar 0,07 µg/l. Secara alami Pb juga ditemukan di udara yang kadarnya berkisar antara µg/m 3 (Sudarmaji 2006). Logam Pb dapat masuk ke dalam tubuh melalui pernapasan, makanan, dan minuman (Astawan 2008). Logam Pb tidak dibutuhkan oleh manusia, sehingga bila makanan tercemar oleh logam tersebut, tubuh akan mengeluarkannya sebagian. Sisanya akan terakumulasi pada bagian tubuh tertentu seperti ginjal, hati, kuku, jaringan lemak, dan rambut. Pb dapat mempengaruhi sistem saraf, inteligensia, dan pertumbuhan. Pb di dalam tubuh terikat pada gugus SH dalam molekul protein dan hal ini menyebabkan hambatan pada aktivitas kerja sistem
37 11 enzim. Efek logam Pb pada kesehatan manusia adalah menimbulkan kerusakan otak, kejang-kejang, gangguan tingkah laku, dan bahkan kematian. Timbal merupakan logam penting dari sudut pandang toksikologi lingkungan, logam ini sampai ke udara dan air dari banyak sumber seperti peleburan timah, produsen baterai, industri kertas dan pulp, bahan bakar perahu dan kapal, amunisi industri, dan lain-lain. Efek toksisitas timbal seperti pada sistem saraf, sistem sirkulasi darah, sistem kardiovaskular, organ vital seperti otak dan ginjal, serta mengganggu pengembangan IQ dan lain-lain telah banyak dilaporkan (Gupta & Bhattacharyya, 2008). Konsentrasi ion Pb mencapai mg/l dalam limbah cair industri, nilai tersebut sangat tinggi untuk standar kualitas air dan harus dikurangi sampai mg/l (Ghassabzadeh et al. 2010). Isoterm adsorpsi Isoterm adsorpsi menyatakan hubungan spesifik antara konsentrasi sorbent (fasa teradsorpsi) dan terdistribusinya pada permukaan adsorben pada suhu konstan. Kesetimbangan adsorpsi biasanya digambarkan dengan persamaan isoterm, di mana parameter-parameternya menunjukkan sifat permukaan dan afinitas dari adsorben. Beberapa penelitian dilakukan untuk menyelidiki isoterm adsorpsi antara ion logam pada ph optimum, jumlah adsorben dan waktu kontak dengan mengubah konsentrasi ion awal dalam larutan dalam rentang 5-50 mg/l (Gupta & Bhattacharyya, 2008; Ghassabzadeh et al. 2010). Terdapat beberapa jenis persamaan isoterm adsorpsi. Tipe isoterm adsorpsi yang sering digunakan secara luas adalah (Subramanyam & Das, 2009): (a) Isoterm Langmuir Isoterm adsorpsi Langmuir didasarkan atas asumsi, (1) adsorpsi hanya terjadi pada lapisan tunggal (monolayer), (2) panas adsorpsi tidak tergantung pada penutupan permukaan, (3) semua bagian dan permukaannya bersifat homogen, dan (4) sejumlah tertentu tapak aktif adsorben yang membentuk ikatan kovalen atau ion. Persamaan isoterm adsorpsi Langmuir dapat diturunkan secara teoritis dengan menganggap terjadinya kesetimbangan antara molekul-molekul yang diadsorpsi pada permukaan adsorben dangan molekul-molekul yang tidak
38 12 teradsorpsi. Persamaan isoterm adsorpsi Langmuir dapat dituliskan sebagai berikut (Gupta & Bhattacharyya, 2008; Ghassabzadeh et al. 2010): = (1) dengan q e = jumlah adsorbat yang teradsorpsi per unit bobot adsorben pada kesetimbangan (mg/g), q m = kapasitas adsorpsi maksimum (mg/g), C e = konsentrasi kesetimbangan adsorbat dalam larutan (mg/l), b = konstanta yang berhubungan dengan energi bebas adsorpsi (L/mg). (b) Isoterm Freundlich Persamaan isoterm adsorpsi Freundlich didasarkan pada asumsi, (1) terbentuknya adsorpsi beberapa lapisan (multilayer) dari molekul-molekul adsorbat pada adsorben, (2) bagian tapak aktif pada permukaan adsorben bersifat heterogen, dan (3) hanya melibatkan gaya Van der Waals sehingga adsorbat dapat bergerak dari satu bagian permukaan ke bagian permukaan lain dari adsorben. Persamaan isoterm adsorpsi Freundlich dapat dituliskan sebagai berikut (Gupta & Bhattacharyya, 2008; Ghassabzadeh et al. 2010): = dengan K F = konstanta, yang menggambarkan kapasitas adsorpsi relatif dari adsorben ((mgg -1 )(mgl -1 ) n ), n = konstanta yang menggambarkan intensitas adsorpsi. Gambar persamaan linear Langmuir dan Freundlich diperoleh dengan memplot berturut-turut C e /q e vs C e dan log q e vs log C e, dan dengan persamaan tersebut koefisien dapat dicari. Persamaan Langmuir juga digunakan untuk memperoleh nilai R L, yang menggambarkan dimensi parameter kesetimbangan atau faktor pemisahan dengan persamaan (Ghassabzadeh et al. 2010): = (2) (3) berdasarkan nilai R, bentuk isoterm dapat ditafsirkan sebagai R>1 menggambarkan adsorpsi yang kurang baik, R = 1 adsorpsi linear, 0<R<1 adsorpsi yang baik, R = 0 adsorpsi irreversible. Dalam persamaan Freudlich, nilai n dalam rentang 1-10 menggambarkan adsorpsi yang baik (Fan et al. 2008)
39 13 Kinetika Adsorpsi Untuk menentukan orde kinetika adsorpsi biasanya digunakan persamaan model kinetika orde pertama semu dan orde kedua semu. Persamaan Lagergren, pertama diterapkan dengan asumsi kinetika orde pertama semu, di mana jumlah ion logam melebihi jumlah tempat adsorpsi di permukaan adsorben. Nilai konstanta rata-rata orde pertama, k 1, diperoleh dari persamaan berikut (Mohan et al. 2006; Fan et al. 2008; Gupta & Bhattacharyya, 2011) : = ( ) (4) Integrasi persamaan (4) dari q t = 0 pada t = 0 adalah: = (5) atau ( ) = (bentuk linear) (6) = (1 ) (bentuk non linear) (7) di mana nilai k 1 dapat ditentukan dari slope grafik log (q e q t ) versus t. Jika validitasnya rendah, kinetika adsorpsi dapat dicoba untuk mekanisme orde dua semu dengan persamaan (Mohan et al. 2006; Fan et al. 2008; Gupta & Bhattacharyya, 2008): = ( ) (8) dengan k 2 adalah konstanta rata-rata orde kedua. Bentuk integrasi dari persamaan (8) adalah: = nilai k 2 dapat ditentukan dengan memplot grafik t/q t versus t. + (9) Parameter termodinamika Dalam praktek teknik faktor entropi dan energi bebas Gibbs harus dipertimbangkan untuk menentukan apakah proses akan terjadi secara spontan. Parameter termodinamika seperti perubahan entalpi (ΔH ), energi bebas Gibbs (ΔG ) dan perubahan entropi (ΔS ) dapat diperkirakan dengan menggunakan konstanta kesetimbangan dengan perubahan suhu. Nilai-nilai perubahan energi bebas Gibbs standar untuk proses adsorpsi dievaluasi dengan menggunakan nilai yang diperoleh dari K d model Langmuir pada suhu yang berbeda. Konstanta kesetimbangan dapat diekspresikan dalam perubahan entalpi adsorpsi dan suhu
40 14 sebagai berikut (Fan et al. 2008; Gupta & Bhattacharyya, 2008; Ghassabzadeh et al. 2010): = ln (10) = (11) = (12) dengan K d adalah konstanta kesetimbangan (= q e /C e ), T = suhu absolut (K), R = konstanta gas = x 10-3 kj/k mol. Dengan memplot grafik ln K d versus 1/T maka nilai ΔH, ΔS dan ΔG dapat ditentukan.
41 BAHAN DAN METODE Waktu dan Tempat Penelitian Penelitian dilaksanakan mulai dari bulan Januari sampai Mei 2011 yang dilakukan di Laboratorium Kimia Analitik IPB, Laboratorium Kimia Fisik IPB, Laboratorium Kimia Organik IPB, Laboratorium Bersama IPB, Balitbang Kehutanan Bogor, Lemigas Jakarta dan Laboratorium Geologi Quarterner PPGL (Pusat Penelitian Geologi Kelautan) Bandung. Bahan dan Alat Bahan yang digunakan pada penelitian ini di antaranya adalah zeolit alam asal Sukabumi dan Lampung, Pb(NO 3 ) 2, HCl, H 3 PO 4, NaHCO 3, CH 3 COONa, NH 4 COOH, NaOH. Larutan stok terdiri dari 1000 mg Pb(II) per liter dibuat dengan melarutkan g Pb(NO 3 ) 2 dalam 1 L air bebas ion dan digunakan sebagai larutan adsorbat (Sprynskyy et al. 2006). Alat yang digunakan di antaranya ph meter Toa HM-20S, sentrifuse Kokusan H-107, shaker Titramax 101, SSA (Spektroskopi Serapan Atom) Shimadzu AA-7000, SEM-EDS (Scanning Electron Microscopy-Electron Dispersive Spektroscopy) JEOLJSM-6360 LA, dan XRD (X-ray Diffraction) Shimadzu 7000, alat BET (Brunauer-Emmett-Teller) Quantachrome. Metode Penelitian Penelitian ini terdiri tiga tahap, yaitu pembuatan adsorben zeolit, karakterisasi adsorben sebelum dan sesudah modifikasi dan percobaan adsorpsi Pb(II) dengan adsorben tersebut (Lampiran 1). Adsorben zeolit Preparasi zeolit alam: zeolit alam dihaluskan, diayak sehingga diperoleh zeolit dengan ukuran butir lolos ayakan 40 mesh, dicuci dengan akuades berulang-ulang, kemudian dikeringkan dalam oven pada suhu 110 C selama 24 jam dan disimpan dalam eksikator untuk pemakaian selanjutnya, (Amri et al. 2004; Berber-Mendoza et al. 2006; Can et al. 2010; Jamil et al. 2010) (Lampiran 2).
42 16 Aktivasi zeolit alam: 100 gram sampel dilarutkan dalam 2000 ml HCl 1 M. Campuran diaduk dengan pengaduk magnet selama 3 jam, kemudian dibilas dengan akuades sampai ph netral dan dikeringkan dalam oven pada suhu 130 C selama 3 jam (Cakicioglu-Ozkan & Ulku 2005; Trisunaryati et al 2005; Sastiono 1993) (Lampiran 3). Zeolit modifikasi asam fosfat: 100 g zeolit alam dalam 2000 ml akuabides dicampur dengan g asam fosfat. Campuran diaduk dengan magnetik stirer pada suhu 60 C selama 3 jam kemudian dikeringkan dalam oven pada suhu 120 C selama 3 jam. Zeolit modifikasi asam fosfat dicampur dengan 1500 ml larutan NaHCO 3 jenuh dan diaduk dengan magnetik stirer pada suhu 60 C selama 3 jam untuk mendapatkan bentuk dinatrium, disaring, dicuci dengan akuades dan dikeringkan dalam oven pada suhu 120 C selama 3 jam. Zeolit hasil modifikasi selanjutnya disebut zeolit-pna 2 (Panneerselvam et al. 2008). Di mana untuk zeolit asal Sukabumi disebut Z-PNa 2 -S dan Z-PNa 2 -L untuk zeolit asal Lampung (Lampiran 4). Karakterisasi adsorben Analisis XRD dilakukan untuk mengetahui kristalinitas, SEM untuk mengetahui morfologi, EDS untuk mengetahui kandungan unsur P dalam zeolit setelah modifikasi metode BET untuk mengukur luas permukaan, volume total pori dan rata-rata diameter pori dan uji KTK menggunakan metode ammonium asetat (Olu-Owolabi & Unuabonah 2010): 2 gram sampel ditambahkan 50 ml larutan CH 3 COONa 1 M dikocok dengan shaker selama 60 menit pada kecepatan 200 rpm. Filtrat disaring, residu dicuci beberapa kali dengan air bebas ion untuk menghilangkan sisa natrium asetat, kemudian dikering-udarakan. Sampel ditambakan 50 ml larutan CH 3 COONH 4 1 M (ph 7), dikocok dengan shaker, filtrat disaring dan ditampung. Langkah ini diulang tiga kali. Kadar Na dalam filtrat diukur dengan SSA (Spektroskopi Serapan Atom) (Lampiran 5). Percobaan adsorpsi Percobaan adsorpsi dilakukan secara tumpak (batch) dengan mencampurkan 50 ml larutan ion logam dengan 0.05 g zeolit-pna 2 dalam erlenmeyer 100 ml.
43 17 Campuran digoyangkan dengan shaker pada kecepatan 150 rpm, suhu dijaga agar konstan selama interval waktu yang ditentukan. Setelah tercapai kesetimbangan campuran disentrifugasi dan ion logam yang tertinggal dalam filtrat dianalisis dengan SSA. Percobaan diulang dengan variasi bobot adsorben ( g), konsentrasi adsorbat ( mg/l), ph larutan (2-6), waktu kontak ( menit) dan suhu ( K). Untuk menjaga ph larutan, ditambahkan NaOH 0,01N atau HNO 3 0,01N sebelum adsorpsi, dan ph dikontrol sebelum dan sesudah adsorpsi (Gupta & Bhattacharyya 2008; Panneerselvam et al. 2008; Gunay et al. 2007) (Lampiran 6). Efisiensi adsorpsi dihitung dengan persamaan: % = ( ) 100 (13) Jumlah logam yang teradsorpsi dari larutan air pada saat kesetimbangan ditentukan dengan persamaan: = ( ) (14) dengan q e = jumlah ion logam yang teradsorpsi (mg/g), C o = konsentrasi awal ion logam dalam larutan (mg/l), C e = konsentrasi ion logam dalam larutan pada saat kesetimbangan (mg/l), V = volume larutan (L), m = massa adsorben (g).
44
45 HASIL DAN PEMBAHASAN Adsorben Zeolit Preparasi zeolit alam Penelitian ini diawali dengan preparasi adsorben zeolit. Preparasi awal dilakukan dengan menghaluskan zeolit asal Sukabumi dan Lampung sehingga lolos ayakan 40 mesh, yang diukur dengan SEM mempunyai kisaran ukuran butir mm baik untuk zeolit asal Sukabumi maupun Lampung. Pencucian dilakukan dengan akuades untuk menghilangkan kotoran pada permukaan zeolit. Untuk menghilangkan air dilakukan pemanasan dalam oven pada suhu 110 C selama 24 jam. Pemanasan pada suhu 105 C sampai kurang lebih 250 C akan menyebabkan air yang terkandung di dalam rongga kristal zeolit menguap. Fungsi dari dehidrasi tersebut adalah untuk mempertinggi keaktifan zeolit, yang disebabkan terbukanya pori-pori atau saluran pada kristal. Sedikit banyaknya air yang dapat dikeluarkan tergantung dari tingkat suhu dan lamanya waktu pemanasan (Sastiono 1993). Zeolit hasil preparasi awal kemudian disimpan dalam eksikator sebelum pemakaian selanjutnya, hal ini untuk menghindari penyerapan air kembali oleh zeolit. Aktivasi zeolit alam Zeolit alam umumnya masih mempunyai kemampuan rendah baik sebagai penjerap maupun penukar ion. Untuk meningkatkan mutu zeolit alam diperlukan proses aktivasi. Aktivasi kimia dapat dilakukan dengan penambahan asam. Pada penelitian ini untuk proses aktivasi digunakan HCl 1N. Penggunaan konsentrasi ini sesuai hasil yang dilaporkan Sastiono (1993), yang melakukan aktivasi zeolit jenis mordenit dan klinoptilolit dan diperoleh hasil KTK dari zeolit tersebut meningkat. Tapi penggunaan HCl lebih dari 1N telah menurunkan nilai KTK. Perlakuan pengasaman terhadap zeolit bertujuan untuk menghilangkan senyawa pengotor yang menutupi rongga dan permukaan pori-pori, sehingga lebih porous dan permukaan pertukaran menjadi lebih luas. Luas permukaan yang bertambah diharapkan meningkatkan kemampuan zeolit dalam proses penjerapan. Selama proses perlakuan dengan asam, ion H + akan menggantikan kation-kation
46 20 yang tidak terikat secara kuat di dalam kerangka zeolit dan mengatur kembali letak atom yang dapat dipertukarkan (Tarlan-Yel & Onen 2010; Wang et al. 2010; Pentrak et al. 2009). Zeolit modifikasi asam fosfat Zeolit yang telah diaktivasi, menjadi bentuk H-zeolit kemudian dimodifikasi dengan asam fosfat (Pannerselvam et al. 2008). Pada modifikasi ini gugus fosfat yang memiliki empat atom oksigen diharapkan mampu meningkatkan muatan negatif total pada zeolit sehingga mampu meningkatkan kapasitas adsorpsinya terhadap ion logam. Selain itu, penggunaan asam fosfat ini mempunyai beberapa alasan, yaitu (1) fosfat merupakan pengelat yang paling banyak di alam, (2) bisa bersifat asam keras maupun asam lunak tergantung kondisi reaksi, (3) pada adsorben yang dimodifikasi dengan asam fosfat, anion-anion fosfat pada permukaan adsorben menjadi bersifat basa lunak dibandingkan dengan anion sulfat dan flourida, sehingga anion fosfat memiliki afinitas yang tinggi terhadap kation-kation lunak (Wang et al. 2010). Beberapa penelitian modifikasi adsorben dengan asam fosfat dalam suasana asam mampu mengikat kation-kation lunak. Hal ini diduga adanya media asam mampu mengubah sifat basa keras pada asam fosfat menjadi basa lunak. Olu- Owolabi & Unuabonah (2010) memodifikasi bentonit dengan asam fosfat untuk mengadsorpsi Zn(II) dan Cu(II). Unuabonah et al. (2007) memodifikasi kaolinit untuk mengadsorpsi Pb(II). Menurut teori HSAB (Hard and Soft Acid Bases) bahwa Zn(II), Cu(II) dan Pb(II) merupakan kelompok asam lunak (Lippard & Berg 1994). Oleh karena itu, modifikasi zeolit dengan asam fosfat diharapkan akan mempunyai afinitas yang tinggi terhadap ion Pb(II). Modifikasi montmorillonit dengan asam fosfat juga dapat meningkatkan afinitasnya terhadap unsur radioaktif cesium (Cs) (Wang et al. 2010). Penambahan NaHCO 3 juga untuk menghindari terjadinya ikatan hidrogen pada zeolit termodifikasi. Adanya ikatan hidrogen akan membuat atom H terikat kuat sehingga akan sulit untuk dipertukarkan dengan ion logam. Mekanisme reaksi diilustrasikan pada Gambar 4.
47 21 Gambar 4 Skema reaksi modifikasi zeolit PNa 2 (Panneerselvam et al. 2008) Keberhasilan dari modifikasi dapat dilihat dari kapasitas adsorpsi zeolit terhadap asam fosfat yang digunakan. Hasil perhitungan menunjukkan kapasitas adsorpsi zeolit Sukabumi dan Lampung terhadap asam fosfat berturut-turut adalah mg/g dan mg/g. (Lampiran 7). Hasil analisis unsur dengan EDS menunjukkan adanya unsur P pada zeolit termodifikasi yaitu kadar unsur P dalam Z-PNa 2 -S dan Z-PNa 2 -L berturut-turut 0.07% dan 0.02%. Karakterisasi adsorben Hasil analisis XRD yang dilakukan terhadap zeolit alam Sukabumi maupun Lampung sebelum modifikasi diperoleh hasil bahwa zeolit asal Sukabumi merupakan jenis mordenit dan zeolit asal Lampung merupakan jenis klinoptilolit. Hasil ini sesuai dengan yang telah dilaporkan Rohaeti (2007). Mordenit dicirikan oleh puncak 6.55, 6.02, 5.78, 4.49, 4.03, 3.44, 3.39, 3.19, 2.88, 2.53 dan 2.52 Å, sedangkan klinoptilolit mempunyai puncak pada 5.20, 4.63, 4.31, 4.11, 3.97, 3.94, 3.89, 3.40, 3.16, 3.11, 2.96, 2.72, dan 2.42 Å. Hasil difraktogram menunjukkan
48 22 bahwa sampel zeolit tersebut tidak hanya mengandung mineral zeolit, akan tetapi juga diikuti oleh mineral silikat lainnya yaitu kuarsa, plagioklas, mika serta mineral liat montmorillonit. Gambar 5 dan Gambar 6, berturut-turut menunjukkan difraktogram zeolit Sukabumi dan Lampung. Identifikasi mineral kuarsa pada difraktogram sinar-x dicirikan oleh puncak 4.23 dan 3.31 Å, sedangkan plagioklas pada puncak 3.79, 3.72 dan 2.79Å. Golongan mineral liat montmorillonit dapat dikenali pada puncak 5.15, 5.08, 3.06, 2.58, dan 2.56 Å, sedangkan mika memiliki puncak pada 4.23 dan 3.31 Å. Keterangan: M: mordenit; K: klinoptilolit; Mn: montmorillonit; Mk: mika; P: plagioklas Gambar 5 Difraktogram XRD zeolit Sukabumi Keterangan: K: klinoptilolit; M: mordenit; Mn: montmorillonit; Ku:Kuarsa; P: plagioklas Gambar 6 Difraktogram XRD zeolit Lampung Hasil analisis BET dengan menggunakan gas nitrogen menghasilkan luas permukaan, volume pori total dan rata-rata diameter pori yang disajikan dalam
49 23 Tabel 3. Luas permukaan dan volume pori total mengalami kenaikan, hal ini menunjukkan bahwa dengan adanya aktivasi dan modifikasi telah menghilangkan pengotor yang ada pada zeolit. Sedangkan untuk rata-rata diameter pori mengalami penurunan, hal ini diduga bahwa gugus fosfat terjerap dalam rongga zeolit sehingga ukuran pori menjadi lebih kecil dari sebelum modifikasi. Tabel 3 Hasil pengukuran luas permukaan, volume pori dan diameter pori sebelum dan sesudah modifikasi zeolit Sukabumi dan Lampung Zeolit Sukabumi Zeolit Lampung Parameter Sebelum modifikasi Sesudah modifikasi Sebelum modifikasi Sesudah modifikasi Luas permukaan (m 2 /g) Volume pori total (L/g) Rata-rata diameter pori (Å) Kristalinitas XRD digunakan untuk menganalisis kristalinitas zeolit sebelum dan sesudah perlakuan. Hal ini dapat membantu mengidentifikasi kerusakan struktur zeolit setelah diaktivasi dengan HCl 1N dan dimodifikasi dengan asam fosfat serta mengubahnya dalam bentuk Na-zeolit. Difraktogram zeolit Sukabumi dan Lampung sebelum dan sesudah perlakuan ditunjukkan pada Gambar 7 dan Gambar 8, berturut-turut. Hasil difraktogram yang diperoleh pada zeolit Sukabumi terlihat tidak terjadi perubahan puncak-puncak difaktogram yang signifikan, hanya terjadi perubahan intensitas. Perhitungan kristalinitas menunjukkan bahwa zeolit Sukabumi tanpa perlakuan mempunyai kristalinitas sebesar 90.77%, setelah perlakuan aktivasi nilai tersebut turun menjadi 63.42%. Hal tersebut diduga karena hilangnya senyawa-senyawa pengotor yang mempengaruhi kristalinitas zeolit tersebut dan rusaknya struktur zeolit. Turunnya nilai kristalinitas tersebut juga diduga karena ada beberapa puncak utama penciri mordenit yang mengalami perubahan intensitas dan pergeseran sudut 2θ, bahkan puncak pada 2θ = (d = 6.02Å) dan 2θ = (d = 2.52Å) menjadi hilang. Setelah dilakukan modifikasi menjadi Z-PNa 2 -S kristalinitas meningkat kembali menjadi 74.51%. Hal ini
50 24 menunjukkan bahwa perlakuan dengan asam fosfat pada zeolit jenis mordenit dapat meningkatkan struktur kristalin dibandingkan yang amorf. Mordenit tergolong sangat tahan terhadap asam, dengan terjerapnya fosfat dalam zeolit yang membentuk ikatan baru Si-O-P-O-Al (Gambar 4) sehingga jarak Si-Al menjadi lebih jauh yang memungkinkan struktur zeolit menjadi fleksibel dan bentuk kristalnya menjadi lebih teratur. Perlakuan dengan basa NaHCO 3 setelah modifikasi asam fosfat beberapa puncak mordenit intensitasnya meningkat sesuai yang dilaporkan oleh Sastiono (1993) yang memberikan perlakuan terhadap mordenit dengan basa. Gambar 7 yang menunjukkan difraktogram zeolit Lampung terlihat ada perubahan intensitas untuk puncak-puncak penciri klinoptilolit. Kristalinitas zeolit Lampung tanpa perlakuan adalah 84.70% dan meningkat setelah dilakukan aktivasi dengan HCl 1N menjadi 90.42%. Hal ini diduga karena jumlah beberapa senyawa pengotor yang mengalami penurunan intensitas dan bahkan ada yang hilang. Senyawa pengotor seperti kuarsa (2θ = 20.95, d = 4.23Å) dan montmorillonit (2θ = 20.10, d = 3.06Å dan 2θ = 34.69, d = 2.58Å) menjadi hilang. Senyawa pengotor lain seperti plagioklas (2θ = 32.02, d = 2.79Å; (2θ = 23.85, d = 3.72Å) mengalami penurunan intensitas. Tetapi salah satu puncak penciri utama klinoptilolit (2θ = 28.19, d = 3.16Å) mengalami kenaikan intensitas yang signifikan yaitu dari 39% menjadi 100%. Perlakuaan dengan asam fosfat pada zeolit Lampung menghasilkan nilai kristalinitasnya turun dari 90.42% menjadi 81.00%. Hal ini diduga klinoptilolit yang kurang tahan terhadap asam, mengakibatkan sejumlah Al dalam struktur zeolit menjadi hilang, sehingga ikatan Si-O-P-O-Al- yang terbentuk tidak sebanyak pada mordenit. Selain itu, adanya asam fosfat dapat menyebabkan kerusakan struktur pada pengotor montmorillonit (Wang et al. 2010). Penambahan NaHCO 3 juga mengakibatkan turunnya intensitas puncak klinoptilolit, seperti yang telah dilaporkan Sastiono (1993) bahwa dengan perlakuan basa mengakibatkan beberapa puncak klinoptilolit mengalami penurunan intensitas.
51 25 Gambar 7 Difraktogram XRD zeolit Sukabumi A. tanpa perlakuan; B. setelah aktivasi; C. setelah modifikasi. Gambar 8 Difraktogram XRD zeolit Lampung A. tanpa perlakuan; B. setelah aktivasi; C. setelah modifikasi. Morfologi Gambar hasil SEM untuk zeolit Sukabumi dan Lampung sebelum dan sesudah modifikasi ditunjukkan pada Gambar 9 dan Gambar 10, berturut-turut. Berdasarkan kedua gambar tersebut, baik zeolit Sukabumi maupun Lampung sebelum perlakuan terlihat lebih kasar dan terdapat banyak serpihan kecil-kecil yang diduga adalah pengotor. Setelah dilakukan aktivasi dengan HCl, kedua zeolit tampak lebih bersih dari serpihan dan bentuk kristalnya lebih nyata. Setelah dilakukan modifikasi dengan asam fosfat dan mengubahnya dalam bentuk Nazeolit, terlihat bahwa permukaannya lebih bersih dan bentuk morfologi kristalnya lebih tampak. Berdasarkan pengamatan perlakuan aktivasi dan modifikasi tidak menghasilkan perubahan bentuk stuktur. Hal serupa juga dilaporkan oleh
52 26 Pannnerselvam (2008) ( yangg melakukaan modifikaasi zeolit sintetik s Na--Y dengan mengggunakan asam fosfat. a b c Gam mbar 9 SEM M zeolit Sukaabumi perbesaran x: a. tanpaa perlakuan;; b. setelah aktivasi; c. setelahh modifikasii. a b c Gam mbar 10 SEM M zeolit Lam mpung perbbesaran 1000x: a. tanpaa perlakuan; b. setelah aktivasi; c. setelahh modifikasii. Peneentuan kap pasitas tukaar kation Zeolit berppotensi dalaam menukaarkan kation n yang param meternya daapat dilihat dari besaran b kappasits tukar kation (KT TK). Kation-kation yanng dapat dippertukarkan dari zeolit terikaat secara tiddak kuat di dalam keraangka tetrahhedral zeolitt, sehingga denggan mudah akan a dilepaaskan ataupuun dipertuk karkan melaalui pencuciian dengan larutan kation-kkation yang lain. Kemaampuan perrtukaran zeoolit merupaakan fungsi t subttitusi Al terrhadap Si pada strukturr bangun zeeolit. Semakkin banyak dari tingkat pengggantian akkan semakkin besar pula keku urangan muatan m possitif yang menggakibatkan semakin baanyak pula jumlah j kation-kation alkali a atau aalkali tanah yangg diperlukann untuk mennetralkannyaa (Sastiono 1993).
TINJAUAN PUSTAKA Zeolit
 TINJAUAN PUSTAKA Zeolit Zeolit merupakan aluminasilikat hidrat yang mengandung logam alkali dan alkali tanah dengan rumus empiris (M + 2,M 2+ )O.Al 2 O 3. xsio 2.yH 2 O, (M + adalah Na atau K, dan M 2+
TINJAUAN PUSTAKA Zeolit Zeolit merupakan aluminasilikat hidrat yang mengandung logam alkali dan alkali tanah dengan rumus empiris (M + 2,M 2+ )O.Al 2 O 3. xsio 2.yH 2 O, (M + adalah Na atau K, dan M 2+
HASIL DAN PEMBAHASAN Hasil analisis proses preparasi, aktivasi dan modifikasi terhadap zeolit
 HASIL DAN PEMBAHASAN Hasil analisis proses preparasi, aktivasi dan modifikasi terhadap zeolit Penelitian ini menggunakan zeolit alam yang berasal dari Lampung dan Cikalong, Jawa Barat. Zeolit alam Lampung
HASIL DAN PEMBAHASAN Hasil analisis proses preparasi, aktivasi dan modifikasi terhadap zeolit Penelitian ini menggunakan zeolit alam yang berasal dari Lampung dan Cikalong, Jawa Barat. Zeolit alam Lampung
TINJAUAN PUSTAKA Kadmium (Cd) Stuktur Kimia Zeolit
 TINJAUAN PUSTAKA Kadmium (Cd) Unsur kadmium dengan nomor atom 48, bobot atom 112,4 g/mol, dan densitas 8.65 g/cm 3 merupakan salah satu jenis logam berat yang berbahaya, karena dalam jangka waktu panjang
TINJAUAN PUSTAKA Kadmium (Cd) Unsur kadmium dengan nomor atom 48, bobot atom 112,4 g/mol, dan densitas 8.65 g/cm 3 merupakan salah satu jenis logam berat yang berbahaya, karena dalam jangka waktu panjang
HASIL DAN PEMBAHASAN Adsorben Zeolit Preparasi zeolit alam Aktivasi zeolit alam
 HASIL DAN PEMBAHASAN Adsorben Zeolit Preparasi zeolit alam Penelitian ini diawali dengan preparasi adsorben zeolit. Preparasi awal dilakukan dengan menghaluskan zeolit asal Sukabumi dan Lampung sehingga
HASIL DAN PEMBAHASAN Adsorben Zeolit Preparasi zeolit alam Penelitian ini diawali dengan preparasi adsorben zeolit. Preparasi awal dilakukan dengan menghaluskan zeolit asal Sukabumi dan Lampung sehingga
HASIL DAN PEMBAHASAN. nm. Setelah itu, dihitung nilai efisiensi adsorpsi dan kapasitas adsorpsinya.
 5 E. ampas sagu teraktivasi basa-bentonit teraktivasi asam (25 : 75), F. ampas sagu teraktivasi basa-bentonit teraktivasi asam (50 : 50), G. ampas sagu teraktivasi basa-bentonit teraktivasi asam (75 :
5 E. ampas sagu teraktivasi basa-bentonit teraktivasi asam (25 : 75), F. ampas sagu teraktivasi basa-bentonit teraktivasi asam (50 : 50), G. ampas sagu teraktivasi basa-bentonit teraktivasi asam (75 :
BAHAN DAN METODE Alat dan Bahan Metode Penelitian Pembuatan zeolit dari abu terbang batu bara (Musyoka et a l 2009).
 BAHAN DAN METODE Alat dan Bahan Pada penelitian ini alat yang digunakan adalah timbangan analitik dengan ketelitian 0,1 mg, shaker, termometer, spektrofotometer serapan atom (FAAS GBC), Oven Memmert, X-Ray
BAHAN DAN METODE Alat dan Bahan Pada penelitian ini alat yang digunakan adalah timbangan analitik dengan ketelitian 0,1 mg, shaker, termometer, spektrofotometer serapan atom (FAAS GBC), Oven Memmert, X-Ray
HASIL DAN PEMBAHASAN. Lanjutan Nilai parameter. Baku mutu. sebelum perlakuan
 dan kemudian ditimbang. Penimbangan dilakukan sampai diperoleh bobot konstan. Rumus untuk perhitungan TSS adalah sebagai berikut: TSS = bobot residu pada kertas saring volume contoh Pengukuran absorbans
dan kemudian ditimbang. Penimbangan dilakukan sampai diperoleh bobot konstan. Rumus untuk perhitungan TSS adalah sebagai berikut: TSS = bobot residu pada kertas saring volume contoh Pengukuran absorbans
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1 Deskripsi Penelitian Penelitian ini dilakukan dari bulan Maret sampai Agustus 2013 di Laboratorium Riset dan Kimia Instrumen Jurusan Pendidikan Kimia Universitas Pendidikan
BAB III METODE PENELITIAN 3.1 Deskripsi Penelitian Penelitian ini dilakukan dari bulan Maret sampai Agustus 2013 di Laboratorium Riset dan Kimia Instrumen Jurusan Pendidikan Kimia Universitas Pendidikan
HASIL DAN PEMBAHASAN. kedua, dan 14 jam untuk Erlenmeyer ketiga. Setelah itu larutan disaring kembali, dan filtrat dianalisis kadar kromium(vi)-nya.
 8 kedua, dan 14 jam untuk Erlenmeyer ketiga. Setelah itu larutan disaring kembali, dan filtrat dianalisis kadar kromium(vi)-nya. HASIL DAN PEMBAHASAN Penentuan Kapasitas Tukar Kation Kapasitas tukar kation
8 kedua, dan 14 jam untuk Erlenmeyer ketiga. Setelah itu larutan disaring kembali, dan filtrat dianalisis kadar kromium(vi)-nya. HASIL DAN PEMBAHASAN Penentuan Kapasitas Tukar Kation Kapasitas tukar kation
BAB I PENDAHULUAN A. Latar Belakang Masalah Perindustrian di Indonesia semakin berkembang. Seiring dengan perkembangan industri yang telah memberikan
 BAB I PENDAHULUAN A. Latar Belakang Masalah Perindustrian di Indonesia semakin berkembang. Seiring dengan perkembangan industri yang telah memberikan kontribusi dalam peningkatan kualitas hidup manusia,
BAB I PENDAHULUAN A. Latar Belakang Masalah Perindustrian di Indonesia semakin berkembang. Seiring dengan perkembangan industri yang telah memberikan kontribusi dalam peningkatan kualitas hidup manusia,
Gambar 3.1 Diagram Alir Penelitian Secara Keseluruhan
 25 BAB III METODE PENELITIAN 3.1 Diagram Alir Penelitian Secara umum penelitian akan dilakukan dengan pemanfaatan limbah media Bambu yang akan digunakan sebagai adsorben dengan diagram alir keseluruhan
25 BAB III METODE PENELITIAN 3.1 Diagram Alir Penelitian Secara umum penelitian akan dilakukan dengan pemanfaatan limbah media Bambu yang akan digunakan sebagai adsorben dengan diagram alir keseluruhan
PENGEMBANGAN METODE SINTESIS UNTUK MENINGKATKAN KUALITAS ZEOLIT ALAMI DI INDONESIA
 Laporan Akhir Tesis LOGO PENGEMBANGAN METODE SINTESIS UNTUK MENINGKATKAN KUALITAS ZEOLIT ALAMI DI INDONESIA Disusun Oleh: M. Furoiddun Nais 2309201016 Dosen Pembimbing: Prof. Dr. Ir. Gede Wibawa, M.Eng
Laporan Akhir Tesis LOGO PENGEMBANGAN METODE SINTESIS UNTUK MENINGKATKAN KUALITAS ZEOLIT ALAMI DI INDONESIA Disusun Oleh: M. Furoiddun Nais 2309201016 Dosen Pembimbing: Prof. Dr. Ir. Gede Wibawa, M.Eng
HASIL DAN PEMBAHASAN. Preparasi Adsorben
 4 HASIL DAN PEMBAHASAN Preparasi Adsorben Perlakuan awal kaolin dan limbah padat tapioka yang dicuci dengan akuades, bertujuan untuk membersihkan pengotorpengotor yang bersifat larut dalam air. Selanjutnya
4 HASIL DAN PEMBAHASAN Preparasi Adsorben Perlakuan awal kaolin dan limbah padat tapioka yang dicuci dengan akuades, bertujuan untuk membersihkan pengotorpengotor yang bersifat larut dalam air. Selanjutnya
HASIL DAN PEMBAHASAN. Skema interaksi proton dengan struktur kaolin (Dudkin et al. 2004).
 4 HASIL DAN PEMBAHASAN Preparasi Adsorben Penelitian ini menggunakan campuran kaolin dan limbah padat tapioka yang kemudian dimodifikasi menggunakan surfaktan kationik dan nonionik. Mula-mula kaolin dan
4 HASIL DAN PEMBAHASAN Preparasi Adsorben Penelitian ini menggunakan campuran kaolin dan limbah padat tapioka yang kemudian dimodifikasi menggunakan surfaktan kationik dan nonionik. Mula-mula kaolin dan
BAB IV HASIL DAN PEMBAHASAN. Sebelum melakukan uji kapasitas adsorben kitosan-bentonit terhadap
 BAB IV HASIL DAN PEMBAHASAN Sebelum melakukan uji kapasitas adsorben kitosan-bentonit terhadap diazinon, terlebih dahulu disintesis adsorben kitosan-bentonit mengikuti prosedur yang telah teruji (Dimas,
BAB IV HASIL DAN PEMBAHASAN Sebelum melakukan uji kapasitas adsorben kitosan-bentonit terhadap diazinon, terlebih dahulu disintesis adsorben kitosan-bentonit mengikuti prosedur yang telah teruji (Dimas,
ZEOLIT CIKALONG DAN LAMPUNG TERMODIFIKASI ASAM FOSFAT SEBAGAI ADSORBEN LOGAM Cd(II) NOPRIYANI
 ZEOLIT CIKALONG DAN LAMPUNG TERMODIFIKASI ASAM FOSFAT SEBAGAI ADSORBEN LOGAM Cd(II) NOPRIYANI SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR BOGOR 2011 PERNYATAAN MENGENAI TESIS DAN SUMBER INFORMASI Dengan
ZEOLIT CIKALONG DAN LAMPUNG TERMODIFIKASI ASAM FOSFAT SEBAGAI ADSORBEN LOGAM Cd(II) NOPRIYANI SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR BOGOR 2011 PERNYATAAN MENGENAI TESIS DAN SUMBER INFORMASI Dengan
HASIL DAN PEMBAHASAN. Adsorpsi Zat Warna
 Adsorpsi Zat Warna Pembuatan Larutan Zat Warna Larutan stok zat warna mg/l dibuat dengan melarutkan mg serbuk Cibacron Red dalam air suling dan diencerkan hingga liter. Kemudian dibuat kurva standar dari
Adsorpsi Zat Warna Pembuatan Larutan Zat Warna Larutan stok zat warna mg/l dibuat dengan melarutkan mg serbuk Cibacron Red dalam air suling dan diencerkan hingga liter. Kemudian dibuat kurva standar dari
Kata kunci: surfaktan HDTMA, zeolit terdealuminasi, adsorpsi fenol
 PENGARUH PENAMBAHAN SURFAKTAN hexadecyltrimethylammonium (HDTMA) PADA ZEOLIT ALAM TERDEALUMINASI TERHADAP KEMAMPUAN MENGADSORPSI FENOL Sriatun, Dimas Buntarto dan Adi Darmawan Laboratorium Kimia Anorganik
PENGARUH PENAMBAHAN SURFAKTAN hexadecyltrimethylammonium (HDTMA) PADA ZEOLIT ALAM TERDEALUMINASI TERHADAP KEMAMPUAN MENGADSORPSI FENOL Sriatun, Dimas Buntarto dan Adi Darmawan Laboratorium Kimia Anorganik
HASIL DAN PEMBAHASAN Preparasi Contoh
 15 HASIL DAN PEMBAHASAN Preparasi Contoh Contoh yang diambil dari alam merupakan contoh zeolit dengan bentuk bongkahan batuan yang berukuran besar, sehingga untuk dapat dimanfaatkan harus diubah ukurannya
15 HASIL DAN PEMBAHASAN Preparasi Contoh Contoh yang diambil dari alam merupakan contoh zeolit dengan bentuk bongkahan batuan yang berukuran besar, sehingga untuk dapat dimanfaatkan harus diubah ukurannya
ION EXCHANGE DASAR TEORI
 ION EXCHANGE I. TUJUAN PERCOBAAN Setelah melakukan praktikum ini diharapkan mahasiswa dapat : 1. Menentukan konsentrasi ion-ion H+, Na+, Mg2+, Zn2+ dengan menggunakan resin penukar kation. 2. Pengurangan
ION EXCHANGE I. TUJUAN PERCOBAAN Setelah melakukan praktikum ini diharapkan mahasiswa dapat : 1. Menentukan konsentrasi ion-ion H+, Na+, Mg2+, Zn2+ dengan menggunakan resin penukar kation. 2. Pengurangan
BAB II TINJAUAN PUSTAKA
 BAB II TINJAUAN PUSTAKA 2.1 Logam Berat Istilah "logam berat" didefinisikan secara umum bagi logam yang memiliki berat spesifik lebih dari 5g/cm 3. Logam berat dimasukkan dalam kategori pencemar lingkungan
BAB II TINJAUAN PUSTAKA 2.1 Logam Berat Istilah "logam berat" didefinisikan secara umum bagi logam yang memiliki berat spesifik lebih dari 5g/cm 3. Logam berat dimasukkan dalam kategori pencemar lingkungan
BAB III METODE PENELITIAN. Ide Penelitian. Studi Literatur. Persiapan Alat dan Bahan Penelitian. Pelaksanaan Penelitian.
 BAB III METODE PENELITIAN 3.1 Diagram Alir Penelitian Tahapan penelitian secara umum mengenai pemanfaatan tulang sapi sebagai adsorben ion logam Cu (II) dijelaskan dalam diagram pada Gambar 3.1 berikut
BAB III METODE PENELITIAN 3.1 Diagram Alir Penelitian Tahapan penelitian secara umum mengenai pemanfaatan tulang sapi sebagai adsorben ion logam Cu (II) dijelaskan dalam diagram pada Gambar 3.1 berikut
BAB I PENDAHULUAN 1.1 Latar Belakang
 BAB I PENDAHULUAN 1.1 Latar Belakang Air merupakan salah satu sumber daya alam yang terpenting bagi semua makhluk hidup di bumi. Air digunakan hampir di setiap aktivitas makhluk hidup. Bagi manusia, air
BAB I PENDAHULUAN 1.1 Latar Belakang Air merupakan salah satu sumber daya alam yang terpenting bagi semua makhluk hidup di bumi. Air digunakan hampir di setiap aktivitas makhluk hidup. Bagi manusia, air
BAB III METODE PENELITIAN. Pengujian dilakukan di Laboratorium Kimia Analitik Instrumen Jurusan
 27 BAB III METODE PENELITIAN 3.1 Deskripsi Penelitian Penelitian ini dilakukan dari bulan Januari sampai September 2012 di Laboratorium Riset Jurusan Pendidikan Kimia Universitas Pendidikan Indonesia.
27 BAB III METODE PENELITIAN 3.1 Deskripsi Penelitian Penelitian ini dilakukan dari bulan Januari sampai September 2012 di Laboratorium Riset Jurusan Pendidikan Kimia Universitas Pendidikan Indonesia.
HASIL DAN PEMBAHASAN y = x R 2 = Absorban
 5 Kulit kacang tanah yang telah dihaluskan ditambahkan asam sulfat pekat 97%, lalu dipanaskan pada suhu 16 C selama 36 jam. Setelah itu, dibilas dengan air destilata untuk menghilangkan kelebihan asam.
5 Kulit kacang tanah yang telah dihaluskan ditambahkan asam sulfat pekat 97%, lalu dipanaskan pada suhu 16 C selama 36 jam. Setelah itu, dibilas dengan air destilata untuk menghilangkan kelebihan asam.
BAB I PENDAHULUAN Latar Belakang
 BAB I PENDAHULUAN 1.1. Latar Belakang Pencemaran lingkungan oleh logam berat menjadi masalah yang cukup serius seiring dengan penggunaan logam berat dalam bidang industri yang semakin meningkat. Keberadaan
BAB I PENDAHULUAN 1.1. Latar Belakang Pencemaran lingkungan oleh logam berat menjadi masalah yang cukup serius seiring dengan penggunaan logam berat dalam bidang industri yang semakin meningkat. Keberadaan
HASIL DAN PEMBAHASAN
 HASIL DAN PEMBAHASAN Uji Pendahuluan dan Karakterisasi Uji pendahuluan zeolit sintetis dan abu terbang batu bara sebagai bahan dasar dilakukan untuk parameter kadar air dan daya serap terhadap iodin. (Tabel
HASIL DAN PEMBAHASAN Uji Pendahuluan dan Karakterisasi Uji pendahuluan zeolit sintetis dan abu terbang batu bara sebagai bahan dasar dilakukan untuk parameter kadar air dan daya serap terhadap iodin. (Tabel
III. METODOLOGI PENELITIAN. Penelitian ini dilakukan selama 4 bulan yaitu pada bulan Februari hingga Mei
 III. METODOLOGI PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilakukan selama 4 bulan yaitu pada bulan Februari hingga Mei 2014, bertempat di Laboratorium Biomassa Jurusan Kimia Fakultas MIPA
III. METODOLOGI PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilakukan selama 4 bulan yaitu pada bulan Februari hingga Mei 2014, bertempat di Laboratorium Biomassa Jurusan Kimia Fakultas MIPA
ISOTERMA DAN TERMODINAMIKA ADSORPSI KATION PLUMBUM(II) PADA LEMPUNG CENGAR TERAKTIVASI ASAM SULFAT
 ISOTERMA DAN TERMODINAMIKA ADSORPSI KATION PLUMBUM(II) PADA LEMPUNG CENGAR TERAKTIVASI ASAM SULFAT A. Johan 1, Muhdarina 2, T. A. Amri 2 1 Mahasiswa Program Studi S1 Kimia 2 Bidang Kimia Fisika Jurusan
ISOTERMA DAN TERMODINAMIKA ADSORPSI KATION PLUMBUM(II) PADA LEMPUNG CENGAR TERAKTIVASI ASAM SULFAT A. Johan 1, Muhdarina 2, T. A. Amri 2 1 Mahasiswa Program Studi S1 Kimia 2 Bidang Kimia Fisika Jurusan
MAKALAH PENDAMPING : PARALEL A. PEMANFAATAN SERBUK GERGAJI KAYU SENGON SEBAGAI ADSORBEN ION LOGAM Pb 2+
 MAKALAH PENDAMPING : PARALEL A SEMINAR NASIONAL KIMIA DAN PENDIDIKAN KIMIA IV Peran Riset dan Pembelajaran Kimia dalam Peningkatan Kompetensi Profesional Program Studi Pendidikan Kimia Jurusan PMIPA FKIP
MAKALAH PENDAMPING : PARALEL A SEMINAR NASIONAL KIMIA DAN PENDIDIKAN KIMIA IV Peran Riset dan Pembelajaran Kimia dalam Peningkatan Kompetensi Profesional Program Studi Pendidikan Kimia Jurusan PMIPA FKIP
ADSORPSI ION Cr 3+ OLEH SERBUK GERGAJI KAYU ALBIZIA (Albizzia falcata): Studi Pengembangan Bahan Alternatif Penjerap Limbah Logam Berat
 ADSORPSI ION Cr 3+ OLEH SERBUK GERGAJI KAYU ALBIZIA (Albizzia falcata): Studi Pengembangan Bahan Alternatif Penjerap Limbah Logam Berat I NYOMAN SUKARTA SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR BOGOR
ADSORPSI ION Cr 3+ OLEH SERBUK GERGAJI KAYU ALBIZIA (Albizzia falcata): Studi Pengembangan Bahan Alternatif Penjerap Limbah Logam Berat I NYOMAN SUKARTA SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR BOGOR
et al., 2005). Menurut Wan Ngah et al (2005), sambung silang menggunakan glutaraldehida, epiklorohidrin, etilen glikol diglisidil eter, atau agen
 PENDAHULUAN A. Latar Belakang Masalah Kitosan merupakan senyawa dengan rumus kimia poli(2-amino-2-dioksi-β-d-glukosa) yang dapat diperoleh dari deasetilasi kitin. Kitosan serta turunannya sangat bermanfaat
PENDAHULUAN A. Latar Belakang Masalah Kitosan merupakan senyawa dengan rumus kimia poli(2-amino-2-dioksi-β-d-glukosa) yang dapat diperoleh dari deasetilasi kitin. Kitosan serta turunannya sangat bermanfaat
BAB III METODE PENELITIAN
 16 BAB III METODE PENELITIAN 3.1 Kerangka Penelitian Kerangka penelitian secara umum dijelaskan dalam diagram pada Gambar 3.1 berikut ini; Latar Belakang: Sebelum air limbah domestik maupun non domestik
16 BAB III METODE PENELITIAN 3.1 Kerangka Penelitian Kerangka penelitian secara umum dijelaskan dalam diagram pada Gambar 3.1 berikut ini; Latar Belakang: Sebelum air limbah domestik maupun non domestik
adsorpsi dan katalisator. Zeolit memiliki bentuk kristal yang sangat teratur dengan rongga yang saling berhubungan ke segala arah yang menyebabkan
 BAB I PENDAHULUAN 1.1 Latar Belakang Kemajuan dalam bidang industri sampai saat ini masih menjadi tolak ukur perkembangan pembangunan dan kemajuan suatu negara. Kemajuan dalam bidang industri ini ternyata
BAB I PENDAHULUAN 1.1 Latar Belakang Kemajuan dalam bidang industri sampai saat ini masih menjadi tolak ukur perkembangan pembangunan dan kemajuan suatu negara. Kemajuan dalam bidang industri ini ternyata
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1. Diagram Alir Penelitian Tahapan penelitian secara umum tentang pemanfaatan daun matoa sebagai adsorben untuk menyerap logam Pb dijelaskan dalam diagram pada Gambar 3.1. Preparasi
BAB III METODE PENELITIAN 3.1. Diagram Alir Penelitian Tahapan penelitian secara umum tentang pemanfaatan daun matoa sebagai adsorben untuk menyerap logam Pb dijelaskan dalam diagram pada Gambar 3.1. Preparasi
III. METODE PENELITIAN. Penelitian ini dilaksanakan pada bulan Mei sampai Juli 2015 di Laboratorium
 23 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Mei sampai Juli 2015 di Laboratorium Kimia Anorganik/Fisik FMIPA Universitas Lampung. Penyiapan alga Tetraselmis sp
23 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Mei sampai Juli 2015 di Laboratorium Kimia Anorganik/Fisik FMIPA Universitas Lampung. Penyiapan alga Tetraselmis sp
BAB I PENDAHULUAN. 1.1 Latar Belakang
 BAB I PENDAHULUAN 1.1 Latar Belakang Air merupakan salah satu sumber daya alam yang sangat dibutuhkan oleh makhluk hidup. Sebagian besar bumi terdiri atas air karena luas daratan lebih kecil dibandingkan
BAB I PENDAHULUAN 1.1 Latar Belakang Air merupakan salah satu sumber daya alam yang sangat dibutuhkan oleh makhluk hidup. Sebagian besar bumi terdiri atas air karena luas daratan lebih kecil dibandingkan
BAB IV HASIL DAN PEMBAHASAN
 BAB IV HASIL DAN PEMBAHASAN 4.1 Perlakuan Awal dan Karakteristik Abu Batubara Abu batubara yang digunakan untuk penelitian ini terdiri dari 2 jenis, yaitu abu batubara hasil pembakaran di boiler tungku
BAB IV HASIL DAN PEMBAHASAN 4.1 Perlakuan Awal dan Karakteristik Abu Batubara Abu batubara yang digunakan untuk penelitian ini terdiri dari 2 jenis, yaitu abu batubara hasil pembakaran di boiler tungku
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1 Lokasi Penelitian Penelitian ini dilakukan di laboratorium Teknik Kimia FT Unnes yang meliputi pembuatan adsorben dari Abu sekam padi (rice husk), penentuan kondisi optimum
BAB III METODE PENELITIAN 3.1 Lokasi Penelitian Penelitian ini dilakukan di laboratorium Teknik Kimia FT Unnes yang meliputi pembuatan adsorben dari Abu sekam padi (rice husk), penentuan kondisi optimum
BAB IV HASIL DAN PEMBAHASAN. Modifikasi Ca-Bentonit menjadi kitosan-bentonit bertujuan untuk
 BAB IV HASIL DAN PEMBAHASAN Modifikasi Ca-Bentonit menjadi kitosan-bentonit bertujuan untuk merubah karakter permukaan bentonit dari hidrofilik menjadi hidrofobik, sehingga dapat meningkatkan kinerja kitosan-bentonit
BAB IV HASIL DAN PEMBAHASAN Modifikasi Ca-Bentonit menjadi kitosan-bentonit bertujuan untuk merubah karakter permukaan bentonit dari hidrofilik menjadi hidrofobik, sehingga dapat meningkatkan kinerja kitosan-bentonit
BAB 3 METODE PENELITIAN. Neraca Digital AS 220/C/2 Radwag Furnace Control Indicator Universal
 BAB 3 METODE PENELITIAN 3.1 Alat Neraca Digital AS 220/C/2 Radwag Furnace Control Fisher Indicator Universal Hotplate Stirrer Thermilyte Difraktometer Sinar-X Rigaku 600 Miniflex Peralatan Gelas Pyrex
BAB 3 METODE PENELITIAN 3.1 Alat Neraca Digital AS 220/C/2 Radwag Furnace Control Fisher Indicator Universal Hotplate Stirrer Thermilyte Difraktometer Sinar-X Rigaku 600 Miniflex Peralatan Gelas Pyrex
METODA AKTIVASI ZEOLIT ALAM DAN APLIKASINYA SEBAGAI MEDIA AMOBILISASI ENZIM α-amilase. Skripsi Sarjana Kimia. Oleh WENI ASTUTI
 METODA AKTIVASI ZEOLIT ALAM DAN APLIKASINYA SEBAGAI MEDIA AMOBILISASI ENZIM α-amilase Skripsi Sarjana Kimia Oleh WENI ASTUTI 07132011 JURUSAN KIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS
METODA AKTIVASI ZEOLIT ALAM DAN APLIKASINYA SEBAGAI MEDIA AMOBILISASI ENZIM α-amilase Skripsi Sarjana Kimia Oleh WENI ASTUTI 07132011 JURUSAN KIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS
AKTIVASI ABU LAYANG BATUBARA DAN APLIKASINYA SEBAGAI ADSORBEN TIMBAL DALAM PENGOLAHAN LIMBAH ELEKTROPLATING
 AKTIVASI ABU LAYANG BATUBARA DAN APLIKASINYA SEBAGAI ADSORBEN TIMBAL DALAM PENGOLAHAN LIMBAH ELEKTROPLATING Widi Astuti 1, F. Widhi Mahatmanti 2 1 Fakultas Teknik, 2 Fakultas Matematika dan Ilmu Pengetahuan
AKTIVASI ABU LAYANG BATUBARA DAN APLIKASINYA SEBAGAI ADSORBEN TIMBAL DALAM PENGOLAHAN LIMBAH ELEKTROPLATING Widi Astuti 1, F. Widhi Mahatmanti 2 1 Fakultas Teknik, 2 Fakultas Matematika dan Ilmu Pengetahuan
BAB I PENDAHULUAN. lingkungan adalah kromium (Cr). Krom adalah kontaminan yang banyak ditemukan
 BAB I PENDAHULUAN 1.1. LATAR BELAKANG Logam berat merupakan salah satu pencemar yang sangat berbahaya bagi manusia dan lingkungannya, sebab toksisitasnya dapat mengancam kehidupan mahluk hidup. Salah satu
BAB I PENDAHULUAN 1.1. LATAR BELAKANG Logam berat merupakan salah satu pencemar yang sangat berbahaya bagi manusia dan lingkungannya, sebab toksisitasnya dapat mengancam kehidupan mahluk hidup. Salah satu
PASI NA R SI NO L SI IK LI A KA
 NANOSILIKA PASIR Anggriz Bani Rizka (1110 100 014) Dosen Pembimbing : Dr.rer.nat Triwikantoro M.Si JURUSAN FISIKA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT TEKNOLOGI SEPULUH NOPEMBER SURABAYA
NANOSILIKA PASIR Anggriz Bani Rizka (1110 100 014) Dosen Pembimbing : Dr.rer.nat Triwikantoro M.Si JURUSAN FISIKA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT TEKNOLOGI SEPULUH NOPEMBER SURABAYA
ADSORPSI ION LOGAM PB 2+ PADA LIMBAH ACCU ZUUR PT MUHTOMAS MENGGUNAKAN ZEOLIT ALAM TERAKTIVASI ASAM SULFAT
 SEMINA NASIONAL KIMIA DAN PENDIDIKAN KIMIA VI Pemantapan iset Kimia dan Asesmen Dalam Pembelajaran Berbasis Pendekatan Saintifik Program Studi Pendidikan Kimia Jurusan PMIPA FKIP UNS Surakarta, 21 Juni
SEMINA NASIONAL KIMIA DAN PENDIDIKAN KIMIA VI Pemantapan iset Kimia dan Asesmen Dalam Pembelajaran Berbasis Pendekatan Saintifik Program Studi Pendidikan Kimia Jurusan PMIPA FKIP UNS Surakarta, 21 Juni
Oleh: ARUM KARTIKA SARI
 Efek Suhu Kalsinasi pada Penggunaan Lumpur Alum IPA sebagai Adsorben untuk Menurunkan Konsentrasi Seng (Zn 2+ ) pada Limbah Cair Industri Elektroplating Oleh: ARUM KARTIKA SARI 3307 100 043 Pembimbing:
Efek Suhu Kalsinasi pada Penggunaan Lumpur Alum IPA sebagai Adsorben untuk Menurunkan Konsentrasi Seng (Zn 2+ ) pada Limbah Cair Industri Elektroplating Oleh: ARUM KARTIKA SARI 3307 100 043 Pembimbing:
PENGARUH PENGASAMAN TERHADAP PENJERAPAN KROMIUM TRIVALEN OLEH ZEOLIT ASAL CIKEMBAR NURUL HASANAH
 PENGARUH PENGASAMAN TERHADAP PENJERAPAN KROMIUM TRIVALEN OLEH ZEOLIT ASAL CIKEMBAR NURUL HASANAH DEPARTEMEN KIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN INSTITUT PERTANIAN BOGOR BOGOR 2008 PENGARUH PENGASAMAN
PENGARUH PENGASAMAN TERHADAP PENJERAPAN KROMIUM TRIVALEN OLEH ZEOLIT ASAL CIKEMBAR NURUL HASANAH DEPARTEMEN KIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN INSTITUT PERTANIAN BOGOR BOGOR 2008 PENGARUH PENGASAMAN
BAB II TINJAUAN PUSTAKA
 BAB II TINJAUAN PUSTAKA 2.1 POLUTAN LOGAM BERAT Pencemaran lingkungan dengan zat beracun telah meningkat dalam beberapa tahun terakhir sebagai akibat dari pesatnya pertumbuhan industri [8]. Aktivitas berbagai
BAB II TINJAUAN PUSTAKA 2.1 POLUTAN LOGAM BERAT Pencemaran lingkungan dengan zat beracun telah meningkat dalam beberapa tahun terakhir sebagai akibat dari pesatnya pertumbuhan industri [8]. Aktivitas berbagai
4 Hasil dan Pembahasan
 4 Hasil dan Pembahasan Secara garis besar, penelitian ini terdiri dari tiga tahap. Tahap pertama yaitu penentuan spektrum absorpsi dan pembuatan kurva kalibrasi dari larutan zat warna RB red F3B. Tahap
4 Hasil dan Pembahasan Secara garis besar, penelitian ini terdiri dari tiga tahap. Tahap pertama yaitu penentuan spektrum absorpsi dan pembuatan kurva kalibrasi dari larutan zat warna RB red F3B. Tahap
besarnya polaritas zeolit alam agar dapat (CO) dan hidrokarbon (HC)?
 OPTIMALISASI SUHU AKTIVASI DAN POLARITAS ZEOLIT ALAM UNTUK MENGURANGI EMISI GAS BUANG SEPEDA MOTOR Drs. Noto Widodo, M.Pd. Bambang Sulistyo, S.Pd., M.Eng Amir Fatah, MPd M.Pd. JURUSAN PENDIDIKAN TEKNIK
OPTIMALISASI SUHU AKTIVASI DAN POLARITAS ZEOLIT ALAM UNTUK MENGURANGI EMISI GAS BUANG SEPEDA MOTOR Drs. Noto Widodo, M.Pd. Bambang Sulistyo, S.Pd., M.Eng Amir Fatah, MPd M.Pd. JURUSAN PENDIDIKAN TEKNIK
BAB I PENDAHULUAN. Banyak sekali logam-logam berat yang dilepaskan ke lingkungan sebagai
 BAB I PENDAHULUAN 1.1 Latar Belakang Masalah Penelitian Banyak sekali logam-logam berat yang dilepaskan ke lingkungan sebagai limbah yang menyebabkan terjadinya polusi air ataupun tanah. Ion logam tembaga
BAB I PENDAHULUAN 1.1 Latar Belakang Masalah Penelitian Banyak sekali logam-logam berat yang dilepaskan ke lingkungan sebagai limbah yang menyebabkan terjadinya polusi air ataupun tanah. Ion logam tembaga
LAMPIRAN I. LANGKAH KERJA PENELITIAN ADSORPSI Cu (II)
 LAMPIRAN I LANGKAH KERJA PENELITIAN ADSORPSI Cu (II) 1. Persiapan Bahan Adsorben Murni Mengumpulkan tulang sapi bagian kaki di RPH Grosok Menghilangkan sisa daging dan lemak lalu mencucinya dengan air
LAMPIRAN I LANGKAH KERJA PENELITIAN ADSORPSI Cu (II) 1. Persiapan Bahan Adsorben Murni Mengumpulkan tulang sapi bagian kaki di RPH Grosok Menghilangkan sisa daging dan lemak lalu mencucinya dengan air
HASIL DAN PEMBAHASAN. standar, dilanjutkan pengukuran kadar Pb dalam contoh sebelum dan setelah koagulasi (SNI ).
 0.45 µm, ph meter HM-20S, spektrofotometer serapan atom (AAS) Analytic Jena Nova 300, spektrofotometer DR 2000 Hach, SEM-EDS EVO 50, oven, neraca analitik, corong, pompa vakum, dan peralatan kaca yang
0.45 µm, ph meter HM-20S, spektrofotometer serapan atom (AAS) Analytic Jena Nova 300, spektrofotometer DR 2000 Hach, SEM-EDS EVO 50, oven, neraca analitik, corong, pompa vakum, dan peralatan kaca yang
I. PENDAHULUAN. akumulatif dalam sistem biologis (Quek dkk., 1998). Menurut Sutrisno dkk. (1996), konsentrasi Cu 2,5 3,0 ppm dalam badan
 I. PENDAHULUAN A. Latar Belakang Logam berat merupakan komponen alami yang terdapat di kulit bumi yang tidak dapat didegradasi atau dihancurkan (Agustina, 2010). Logam dapat membahayakan bagi kehidupan
I. PENDAHULUAN A. Latar Belakang Logam berat merupakan komponen alami yang terdapat di kulit bumi yang tidak dapat didegradasi atau dihancurkan (Agustina, 2010). Logam dapat membahayakan bagi kehidupan
MODIFIKASI ZEOLIT MELALUI INTERAKSI DENGAN Fe(OH) 3 UNTUK MENINGKATKAN KAPASITAS TUKAR ANION. Syafii, F; Sugiarti, S; Charlena.
 MODIFIKASI ZEOLIT MELALUI INTERAKSI DENGAN Fe(OH) 3 UNTUK MENINGKATKAN KAPASITAS TUKAR ANION Syafii, F; Sugiarti, S; Charlena Departemen Kimia, FMIPA Institut Pertanian Bogor Abstrak Aktivasi zeolit pada
MODIFIKASI ZEOLIT MELALUI INTERAKSI DENGAN Fe(OH) 3 UNTUK MENINGKATKAN KAPASITAS TUKAR ANION Syafii, F; Sugiarti, S; Charlena Departemen Kimia, FMIPA Institut Pertanian Bogor Abstrak Aktivasi zeolit pada
IV. HASIL DAN PEMBAHASAN. Tabel 7. Hasil Analisis Karakterisasi Arang Aktif
 IV. HASIL DAN PEMBAHASAN 4. 1 Hasil Analisis Karakterisasi Arang Aktif Hasil analisis karakterisasi arang dan arang aktif berdasarkan SNI 06-3730-1995 dapat dilihat pada Tabel 7. Contoh Tabel 7. Hasil
IV. HASIL DAN PEMBAHASAN 4. 1 Hasil Analisis Karakterisasi Arang Aktif Hasil analisis karakterisasi arang dan arang aktif berdasarkan SNI 06-3730-1995 dapat dilihat pada Tabel 7. Contoh Tabel 7. Hasil
BABrV HASIL DAN PEMBAHASAN
 BABrV HASIL DAN PEMBAHASAN 4.1. HasU Penelitian 4.1.1. Sintesis Zeolit mo 3«00 3200 2aiW 2400 2000 IMO l«m l«m I2«) 1000 100 600 430.0 Putri H_ kaolin 200 m_zeolit Gambar 11. Spektogram Zeolit A Sintesis
BABrV HASIL DAN PEMBAHASAN 4.1. HasU Penelitian 4.1.1. Sintesis Zeolit mo 3«00 3200 2aiW 2400 2000 IMO l«m l«m I2«) 1000 100 600 430.0 Putri H_ kaolin 200 m_zeolit Gambar 11. Spektogram Zeolit A Sintesis
BAB III METODE PENELITIAN. 3.1 Kerangka Penelitian Kerangka penelitian secara umum dijelaskan dalam diagram pada Gambar 3.
 12 BAB III METODE PENELITIAN 3.1 Kerangka Penelitian Kerangka penelitian secara umum dijelaskan dalam diagram pada Gambar 3.1 berikut ini : Latar belakang penelitian Rumusan masalah penelitian Tujuan penelitian
12 BAB III METODE PENELITIAN 3.1 Kerangka Penelitian Kerangka penelitian secara umum dijelaskan dalam diagram pada Gambar 3.1 berikut ini : Latar belakang penelitian Rumusan masalah penelitian Tujuan penelitian
BAB IV HASIL PENELITIAN DAN ANALISIS DATA
 BAB IV HASIL PENELITIAN DAN ANALISIS DATA 4.1 Persiapan Adsorben Cangkang Gonggong Cangkang gonggong yang telah dikumpulkan dicuci bersih dan dikeringkan dengan matahari. Selanjutnya cangkang gonggong
BAB IV HASIL PENELITIAN DAN ANALISIS DATA 4.1 Persiapan Adsorben Cangkang Gonggong Cangkang gonggong yang telah dikumpulkan dicuci bersih dan dikeringkan dengan matahari. Selanjutnya cangkang gonggong
Efek Suhu Kalsinasi Pada Penggunaan Lumpur Alum IPA sebagai Adsorben Untuk Menurunkan Konsentrasi Limbah Fosfat
 Company LOGO Efek Suhu Kalsinasi Pada Penggunaan Lumpur Alum IPA sebagai Adsorben Untuk Menurunkan Konsentrasi Limbah Fosfat Oleh : Frida Novia Handini (3307.100.071) Dosen Pembimbing : Welly Herumurti,
Company LOGO Efek Suhu Kalsinasi Pada Penggunaan Lumpur Alum IPA sebagai Adsorben Untuk Menurunkan Konsentrasi Limbah Fosfat Oleh : Frida Novia Handini (3307.100.071) Dosen Pembimbing : Welly Herumurti,
BAB IV HASIL DAN PEMBAHASAN
 BAB IV HASIL DAN PEMBAHASAN 4.1 Penjelasan Umum Penelitian ini menggunakan lumpur hasil pengolahan air di PDAM Tirta Binangun untuk menurunkan ion kadmium (Cd 2+ ) yang terdapat pada limbah sintetis. Pengujian
BAB IV HASIL DAN PEMBAHASAN 4.1 Penjelasan Umum Penelitian ini menggunakan lumpur hasil pengolahan air di PDAM Tirta Binangun untuk menurunkan ion kadmium (Cd 2+ ) yang terdapat pada limbah sintetis. Pengujian
STUDI KEMAMPUAN LUMPUR ALUM UNTUK MENURUNKAN KONSENTRASI ION LOGAM Zn (II) PADA LIMBAH CAIR INDUSTRI ELEKTROPLATING
 STUDI KEMAMPUAN LUMPUR ALUM UNTUK MENURUNKAN KONSENTRASI ION LOGAM Zn (II) PADA LIMBAH CAIR INDUSTRI ELEKTROPLATING Oleh : Eka Masrifatus Anifah (3306 100 016) Dosen Pembimbing : Welly Herumurti, ST.,
STUDI KEMAMPUAN LUMPUR ALUM UNTUK MENURUNKAN KONSENTRASI ION LOGAM Zn (II) PADA LIMBAH CAIR INDUSTRI ELEKTROPLATING Oleh : Eka Masrifatus Anifah (3306 100 016) Dosen Pembimbing : Welly Herumurti, ST.,
BAB I PENDAHULUAN. Perkembangan industri di Indonesia saat ini berlangsung sangat pesat seiring
 BAB I PENDAHULUAN 1.1. Latar belakang Perkembangan industri di Indonesia saat ini berlangsung sangat pesat seiring dengan kemajuan ilmu pengetahuan dan teknologi, hal ini ditandai dengan semakin banyaknya
BAB I PENDAHULUAN 1.1. Latar belakang Perkembangan industri di Indonesia saat ini berlangsung sangat pesat seiring dengan kemajuan ilmu pengetahuan dan teknologi, hal ini ditandai dengan semakin banyaknya
BAB I PENDAHULUAN I.1 Latar Belakang
 BAB I PENDAHULUAN I.1 Latar Belakang Industri mempunyai pengaruh besar terhadap lingkungan, karena dalam prosesnya akan dihasilkan produk utama dan juga produk samping berupa limbah produksi, baik limbah
BAB I PENDAHULUAN I.1 Latar Belakang Industri mempunyai pengaruh besar terhadap lingkungan, karena dalam prosesnya akan dihasilkan produk utama dan juga produk samping berupa limbah produksi, baik limbah
BAB V HASIL DAN PEMBAHASAN
 BAB V HASIL DAN PEMBAHASAN Bentonit diperoleh dari bentonit alam komersiil. Aktivasi bentonit kimia. Aktivasi secara kimia dilakukan dengan merendam bentonit dengan menggunakan larutan HCl 0,5 M yang bertujuan
BAB V HASIL DAN PEMBAHASAN Bentonit diperoleh dari bentonit alam komersiil. Aktivasi bentonit kimia. Aktivasi secara kimia dilakukan dengan merendam bentonit dengan menggunakan larutan HCl 0,5 M yang bertujuan
BAB V HASIL DAN PEMBAHASAN. Pada penelitian ini akan dibahas tentang sintesis katalis Pt/Zr-MMT dan
 BAB V HASIL DAN PEMBAHASAN Pada penelitian ini akan dibahas tentang sintesis katalis Pt/Zr-MMT dan uji aktivitas katalis Pt/Zr-MMT serta aplikasinya sebagai katalis dalam konversi sitronelal menjadi mentol
BAB V HASIL DAN PEMBAHASAN Pada penelitian ini akan dibahas tentang sintesis katalis Pt/Zr-MMT dan uji aktivitas katalis Pt/Zr-MMT serta aplikasinya sebagai katalis dalam konversi sitronelal menjadi mentol
BAHAN DAN METODE. Prosedur Penelitian
 10 BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilaksanakan dari bulan Mei 2010 sampai Maret 2011 di Laboratorium Bagian Kimia Analitik Departemen Kimia FMIPA IPB dan di Laboratory of Applied
10 BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilaksanakan dari bulan Mei 2010 sampai Maret 2011 di Laboratorium Bagian Kimia Analitik Departemen Kimia FMIPA IPB dan di Laboratory of Applied
BAB IV HASIL PENELITIAN DAN PEMBAHASAN. A. Hasil Penelitian Penelitian yang telah dilakukan bertujuan untuk menentukan waktu aging
 BAB IV HASIL PENELITIAN DAN PEMBAHASAN A. Hasil Penelitian Penelitian yang telah dilakukan bertujuan untuk menentukan waktu aging optimal pada sintesis zeolit dari abu sekam padi pada temperatur kamar
BAB IV HASIL PENELITIAN DAN PEMBAHASAN A. Hasil Penelitian Penelitian yang telah dilakukan bertujuan untuk menentukan waktu aging optimal pada sintesis zeolit dari abu sekam padi pada temperatur kamar
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1. Diagram Alir Penelitian Metode penelitian secara umum tentang pemanfaatan cangkang kerang darah (AnadaraGranosa) sebagai adsorben penyerap logam Tembaga (Cu) dijelaskan melalui
BAB III METODE PENELITIAN 3.1. Diagram Alir Penelitian Metode penelitian secara umum tentang pemanfaatan cangkang kerang darah (AnadaraGranosa) sebagai adsorben penyerap logam Tembaga (Cu) dijelaskan melalui
DAYA ADSORPSI METANIL YELLOW DENGAN MENGGUNAKAN ZEOLIT ALAM TERAKTIVASI HCl
 DAYA ADSORPSI METANIL YELLOW DENGAN MENGGUNAKAN ZEOLIT ALAM TERAKTIVASI HCl Johan Unduk Manatap 1, Akmal Mukhtar 2, Emrizal Mahidin Tamboesai 2 1 Mahasiswa Program Studi S1 Kimia 2 Bidang Anorganik Jurusan
DAYA ADSORPSI METANIL YELLOW DENGAN MENGGUNAKAN ZEOLIT ALAM TERAKTIVASI HCl Johan Unduk Manatap 1, Akmal Mukhtar 2, Emrizal Mahidin Tamboesai 2 1 Mahasiswa Program Studi S1 Kimia 2 Bidang Anorganik Jurusan
LAPORAN PRAKTIKUM KIMIA FISIKA
 LAPORAN PRAKTIKUM KIMIA FISIKA ISOTHERM ADSORPSI Oleh : Kelompok 2 Kelas C Ewith Riska Rachma 1307113269 Masroah Tuljannah 1307113580 Michael Hutapea 1307114141 PROGRAM SARJANA STUDI TEKNIK KIMIA UNIVERSITAS
LAPORAN PRAKTIKUM KIMIA FISIKA ISOTHERM ADSORPSI Oleh : Kelompok 2 Kelas C Ewith Riska Rachma 1307113269 Masroah Tuljannah 1307113580 Michael Hutapea 1307114141 PROGRAM SARJANA STUDI TEKNIK KIMIA UNIVERSITAS
4 Hasil dan Pembahasan
 4 Hasil dan Pembahasan 4.1 Aktivasi Zeolit Sebelum digunakan, zeolit sebaiknya diaktivasi terlebih dahulu untuk meningkatkan kinerjanya. Dalam penelitian ini, zeolit diaktivasi melalui perendaman dengan
4 Hasil dan Pembahasan 4.1 Aktivasi Zeolit Sebelum digunakan, zeolit sebaiknya diaktivasi terlebih dahulu untuk meningkatkan kinerjanya. Dalam penelitian ini, zeolit diaktivasi melalui perendaman dengan
I. PENDAHULUAN. serius, ini karena penggunaan logam berat yang semakin meningkat seiring
 I. PENDAHULUAN A. Latar Belakang Pencemaran lingkungan karena logam berat merupakan masalah yang sangat serius, ini karena penggunaan logam berat yang semakin meningkat seiring dengan perkembangan di bidang
I. PENDAHULUAN A. Latar Belakang Pencemaran lingkungan karena logam berat merupakan masalah yang sangat serius, ini karena penggunaan logam berat yang semakin meningkat seiring dengan perkembangan di bidang
III. METODOLOGI PENELITIAN. Penelitian ini telah dilakukan pada bulan Mei sampai Juli 2013 di Laboratorium
 25 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian ini telah dilakukan pada bulan Mei sampai Juli 2013 di Laboratorium Kimia Anorganik dan Laboratorium Biokimia FMIPA Universitas Lampung, serta
25 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian ini telah dilakukan pada bulan Mei sampai Juli 2013 di Laboratorium Kimia Anorganik dan Laboratorium Biokimia FMIPA Universitas Lampung, serta
BAB III METODE PENELITIAN. Matematika dan Ilmu Pengetahuan Alam Universitas Udayana. Untuk sampel
 BAB III METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian dilakukan di laboratorium penelitian jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Udayana. Untuk sampel kulit
BAB III METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian dilakukan di laboratorium penelitian jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Udayana. Untuk sampel kulit
BAB 1 PENDAHULUAN Latar Belakang
 13 BAB 1 PENDAHULUAN 1.1. Latar Belakang Molekul-molekul pada permukaan zat padat atau zat cair mempunyai gaya tarik kearah dalam, karena tidak ada gaya-gaya lain yang mengimbangi. Adanya gayagaya ini
13 BAB 1 PENDAHULUAN 1.1. Latar Belakang Molekul-molekul pada permukaan zat padat atau zat cair mempunyai gaya tarik kearah dalam, karena tidak ada gaya-gaya lain yang mengimbangi. Adanya gayagaya ini
DAFTAR ISI HALAMAN JUDUL HALAMAN PENGESAHAN HALAMAN PERNYATAAN HALAMAN MOTTO DAN PERSEMBAHAN KATA PENGANTAR DAFTAR GAMBAR DAFTAR TABEL DAFTAR LAMPIRAN
 DAFTAR ISI HALAMAN JUDUL HALAMAN PENGESAHAN HALAMAN PERNYATAAN HALAMAN MOTTO DAN PERSEMBAHAN KATA PENGANTAR DAFTAR ISI DAFTAR GAMBAR DAFTAR TABEL DAFTAR LAMPIRAN INTISARI ABSTRACT ii iii iv v vi x xi xii
DAFTAR ISI HALAMAN JUDUL HALAMAN PENGESAHAN HALAMAN PERNYATAAN HALAMAN MOTTO DAN PERSEMBAHAN KATA PENGANTAR DAFTAR ISI DAFTAR GAMBAR DAFTAR TABEL DAFTAR LAMPIRAN INTISARI ABSTRACT ii iii iv v vi x xi xii
4 Hasil dan Pembahasan
 4 Hasil dan Pembahasan 4.1 Sintesis Padatan TiO 2 Amorf Proses sintesis padatan TiO 2 amorf ini dimulai dengan melarutkan titanium isopropoksida (TTIP) ke dalam pelarut etanol. Pelarut etanol yang digunakan
4 Hasil dan Pembahasan 4.1 Sintesis Padatan TiO 2 Amorf Proses sintesis padatan TiO 2 amorf ini dimulai dengan melarutkan titanium isopropoksida (TTIP) ke dalam pelarut etanol. Pelarut etanol yang digunakan
DAFTAR ISI. Halaman Judul... ii. Halaman Pengesahan... iii. Halaman Pernyataan... iv. Prakata... v. Daftar Isi... vii. Daftar Tabel...
 vii DAFTAR ISI Cover Halaman Judul... ii Halaman Pengesahan... iii Halaman Pernyataan... iv Prakata... v Daftar Isi... vii Daftar Tabel... xi Daftar Gambar... xiii Daftar Grafik... xv Daftar Lampiran...
vii DAFTAR ISI Cover Halaman Judul... ii Halaman Pengesahan... iii Halaman Pernyataan... iv Prakata... v Daftar Isi... vii Daftar Tabel... xi Daftar Gambar... xiii Daftar Grafik... xv Daftar Lampiran...
PENENTUAN MASSA DAN WAKTU KONTAK OPTIMUM ADSORPSI KARBON GRANULAR SEBAGAI ADSORBEN LOGAM BERAT Pb(II) DENGAN PESAING ION Na +
 PENENTUAN MASSA DAN WAKTU KONTAK OPTIMUM ADSORPSI KARBON GRANULAR SEBAGAI ADSORBEN LOGAM BERAT Pb(II) DENGAN PESAING ION Na + DETERMINATION OF OPTIMUM MASS AND THE TIME CONTACT OF THE GRANULAR ACTIVATED
PENENTUAN MASSA DAN WAKTU KONTAK OPTIMUM ADSORPSI KARBON GRANULAR SEBAGAI ADSORBEN LOGAM BERAT Pb(II) DENGAN PESAING ION Na + DETERMINATION OF OPTIMUM MASS AND THE TIME CONTACT OF THE GRANULAR ACTIVATED
BAB I PENDAHULUAN A. Latar Belakang
 BAB I PENDAHULUAN A. Latar Belakang Lingkungan hidup dikatakan tercemar apabila telah terjadi perubahanperubahan dalam tatanan lingkungan itu sehingga tidak sama lagi dengan bentuk asalnya, sebagai akibat
BAB I PENDAHULUAN A. Latar Belakang Lingkungan hidup dikatakan tercemar apabila telah terjadi perubahanperubahan dalam tatanan lingkungan itu sehingga tidak sama lagi dengan bentuk asalnya, sebagai akibat
BAB I PENDAHULUAN 1.1 Latar Belakang
 BAB I PENDAHULUAN 1.1 Latar Belakang Meningkatnya perkembangan industri, semakin menimbulkan masalah. Karena limbah yang dihasilkan di sekitar lingkungan hidup menyebabkan timbulnya pencemaran udara, air
BAB I PENDAHULUAN 1.1 Latar Belakang Meningkatnya perkembangan industri, semakin menimbulkan masalah. Karena limbah yang dihasilkan di sekitar lingkungan hidup menyebabkan timbulnya pencemaran udara, air
KIMIA FISIKA (Kode : C-15) MODIFIKASI ZEOLIT ALAM MENJADI MATERIAL KATALIS PERENGKAHAN
 MAKALAH PENDAMPING KIMIA FISIKA (Kode : C-5) ISBN : 978-979-533-85- MODIFIKASI ZEOLIT ALAM MENJADI MATERIAL KATALIS PERENGKAHAN Imelda H. Silalahi, * Aladin Sianipar, Endah Sayekti Jurusan Kimia, Fakultas
MAKALAH PENDAMPING KIMIA FISIKA (Kode : C-5) ISBN : 978-979-533-85- MODIFIKASI ZEOLIT ALAM MENJADI MATERIAL KATALIS PERENGKAHAN Imelda H. Silalahi, * Aladin Sianipar, Endah Sayekti Jurusan Kimia, Fakultas
BAB I PENDAHULUAN A. Latar Belakang
 BAB I PENDAHULUAN A. Latar Belakang Air merupakan kebutuhan hidup pokok karena tidak satupun kehidupan yang ada di dunia ini dapat berlangsung tanpa tersedianya air yang cukup baik kualitas maupun kuantitasnya.
BAB I PENDAHULUAN A. Latar Belakang Air merupakan kebutuhan hidup pokok karena tidak satupun kehidupan yang ada di dunia ini dapat berlangsung tanpa tersedianya air yang cukup baik kualitas maupun kuantitasnya.
BAB I PENDAHULUAN 1.1 Latar Belakang
 BAB I PENDAHULUAN 1.1 Latar Belakang Pencemaran lingkungan baik udara, tanah, ataupun air banyak terjadi akibat dari aktivitas manusia. Menurut UU No.32 tahun 2009, yang dimaksud dengan pencemaran adalah
BAB I PENDAHULUAN 1.1 Latar Belakang Pencemaran lingkungan baik udara, tanah, ataupun air banyak terjadi akibat dari aktivitas manusia. Menurut UU No.32 tahun 2009, yang dimaksud dengan pencemaran adalah
BAB I. PENDAHULUAN A. Latar Belakang Masalah
 BAB I. PENDAHULUAN A. Latar Belakang Masalah Air merupakan sumber daya alam yang penting bagi semua mahluk hidup. Manusia dalam kehidupan sehari-hari memerlukan air untuk berbagai keperluan mulai dari
BAB I. PENDAHULUAN A. Latar Belakang Masalah Air merupakan sumber daya alam yang penting bagi semua mahluk hidup. Manusia dalam kehidupan sehari-hari memerlukan air untuk berbagai keperluan mulai dari
BAB III METODOLOGI PENELITIAN. Penelitian ini dilaksanakan pada bulan Februari - Juni 2015 di Balai Besar
 30 BAB III METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Februari - Juni 2015 di Balai Besar Pengembangan Budidaya Laut Lampung untuk pengambilan biomassa alga porphyridium
30 BAB III METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Februari - Juni 2015 di Balai Besar Pengembangan Budidaya Laut Lampung untuk pengambilan biomassa alga porphyridium
BAB IV HASIL DAN PEMBAHASAN
 BAB IV HASIL DAN PEMBAHASAN Dalam bab ini, hasil uji kemampuan adsorpsi adsorben hasil pirolisis lumpur bio terhadap fenol akan dibahas. Kondisi operasi pirolisis yang digunakan untuk menghasilkan adsorben
BAB IV HASIL DAN PEMBAHASAN Dalam bab ini, hasil uji kemampuan adsorpsi adsorben hasil pirolisis lumpur bio terhadap fenol akan dibahas. Kondisi operasi pirolisis yang digunakan untuk menghasilkan adsorben
BAB II TINJAUAN PUSTAKA
 BAB II TINJAUAN PUSTAKA 2.1. Zeolit 2.1.1 Pengertian Zeolit Zeolit adalah polimir anorganik unit kerangka tetrahedral AlO4 dan SiO4 yang mempunyai struktur berongga dari Natrium silikat dan berkemampuan
BAB II TINJAUAN PUSTAKA 2.1. Zeolit 2.1.1 Pengertian Zeolit Zeolit adalah polimir anorganik unit kerangka tetrahedral AlO4 dan SiO4 yang mempunyai struktur berongga dari Natrium silikat dan berkemampuan
4 Hasil dan Pembahasan
 4 Hasil dan Pembahasan 4.1 Penyiapan Zeolit Zeolit yang digunakan dalam penelitian ini berasal dari Tasikmalaya. Warna zeolit awal adalah putih kehijauan. Ukuran partikel yang digunakan adalah +48 65 mesh,
4 Hasil dan Pembahasan 4.1 Penyiapan Zeolit Zeolit yang digunakan dalam penelitian ini berasal dari Tasikmalaya. Warna zeolit awal adalah putih kehijauan. Ukuran partikel yang digunakan adalah +48 65 mesh,
BAB I PENDAHULUAN. Universitas Sumatera Utara
 BAB I PENDAHULUAN 1.1 Latar Belakang Pada masa sekarang kecenderungan pemakaian bahan bakar sangat tinggi sedangkan sumber bahan bakar minyak bumi yang di pakai saat ini semakin menipis. Oleh karena itu,
BAB I PENDAHULUAN 1.1 Latar Belakang Pada masa sekarang kecenderungan pemakaian bahan bakar sangat tinggi sedangkan sumber bahan bakar minyak bumi yang di pakai saat ini semakin menipis. Oleh karena itu,
BAB IV HASIL DAN PEMBAHASAN
 BAB IV HASIL DAN PEMBAHASAN 4.1. Hasil Penelitian 4.1.1. Hasil penentuan kandungan oksida logam dalam abu boiler PKS Penentuan kandungan oksida logam dari abu boiler PKS dilakukan dengan menggvmakan XRF
BAB IV HASIL DAN PEMBAHASAN 4.1. Hasil Penelitian 4.1.1. Hasil penentuan kandungan oksida logam dalam abu boiler PKS Penentuan kandungan oksida logam dari abu boiler PKS dilakukan dengan menggvmakan XRF
SKRIPSI KOMPOSIT BENTONIT-KITOSAN UNTUK PENYERAPAN LOGAM BERAT. Diajukan Oleh: Stephen Utomo NRP:
 SKRIPSI KOMPOSIT BENTONIT-KITOSAN UNTUK PENYERAPAN LOGAM BERAT Diajukan Oleh: Stephen Utomo NRP: 5203013017 JURUSAN TEKNIK KIMIA FAKULTAS TEKNIK UNIVERSITAS KATOLIK WIDYA MANDALA SURABAYA 2016 iii iv
SKRIPSI KOMPOSIT BENTONIT-KITOSAN UNTUK PENYERAPAN LOGAM BERAT Diajukan Oleh: Stephen Utomo NRP: 5203013017 JURUSAN TEKNIK KIMIA FAKULTAS TEKNIK UNIVERSITAS KATOLIK WIDYA MANDALA SURABAYA 2016 iii iv
TINJAUAN PUSTAKA Abu Terbang Batu Bara
 TINJAUAN PUSTAKA Abu Terbang Batu Bara Abu terbang batu bara merupakan limbah padat yang dihasilkan pembangkit listrik yang menggunakan batu bara sebagai bahan bakar dan dihasilkan dalam jumlah besar.
TINJAUAN PUSTAKA Abu Terbang Batu Bara Abu terbang batu bara merupakan limbah padat yang dihasilkan pembangkit listrik yang menggunakan batu bara sebagai bahan bakar dan dihasilkan dalam jumlah besar.
BAB IV HASIL DAN PEMBAHASAN. coba untuk penentuan daya serap dari arang aktif. Sampel buatan adalah larutan
 BAB IV HASIL DAN PEMBAHASAN 4.1 Pembuatan Sampel Buatan Pada prosedur awal membuat sampel buatan yang digunakan sebagai uji coba untuk penentuan daya serap dari arang aktif. Sampel buatan adalah larutan
BAB IV HASIL DAN PEMBAHASAN 4.1 Pembuatan Sampel Buatan Pada prosedur awal membuat sampel buatan yang digunakan sebagai uji coba untuk penentuan daya serap dari arang aktif. Sampel buatan adalah larutan
PENYEHATAN MAKANAN MINUMAN A
 PETUNJUK PRAKTIKUM PENYEHATAN MAKANAN MINUMAN A Cemaran Logam Berat dalam Makanan Cemaran Kimia non logam dalam Makanan Dosen CHOIRUL AMRI JURUSAN KESEHATAN LINGKUNGAN POLTEKKES KEMENKES YOGYAKARTA 2016
PETUNJUK PRAKTIKUM PENYEHATAN MAKANAN MINUMAN A Cemaran Logam Berat dalam Makanan Cemaran Kimia non logam dalam Makanan Dosen CHOIRUL AMRI JURUSAN KESEHATAN LINGKUNGAN POLTEKKES KEMENKES YOGYAKARTA 2016
BAB III METODE PENELITIAN. Laboratorium Kimia Analitik Instrumen Jurusan Pendidikan Kimia FPMIPA UPI.
 21 BAB III METODE PENELITIAN 3.1 Lokasi Penelitian Adapun lokasi penelitian dilakukan di Laboratorium Riset dan Laboratorium Kimia Analitik Instrumen Jurusan Pendidikan Kimia FPMIPA UPI. 3.2 Alat dan Bahan
21 BAB III METODE PENELITIAN 3.1 Lokasi Penelitian Adapun lokasi penelitian dilakukan di Laboratorium Riset dan Laboratorium Kimia Analitik Instrumen Jurusan Pendidikan Kimia FPMIPA UPI. 3.2 Alat dan Bahan
Pengaruh Kadar Logam Ni dan Al Terhadap Karakteristik Katalis Ni-Al- MCM-41 Serta Aktivitasnya Pada Reaksi Siklisasi Sitronelal
 Pengaruh Kadar Logam Ni dan Al Terhadap Karakteristik Katalis Ni-Al- MCM-41 Serta Aktivitasnya Pada Reaksi Siklisasi Sitronelal K Oleh Said Mihdar Said Hady Nrp. 1407201729 Dosen Pembimbing Dra. Ratna
Pengaruh Kadar Logam Ni dan Al Terhadap Karakteristik Katalis Ni-Al- MCM-41 Serta Aktivitasnya Pada Reaksi Siklisasi Sitronelal K Oleh Said Mihdar Said Hady Nrp. 1407201729 Dosen Pembimbing Dra. Ratna
BAB IV HASIL DAN PEMBAHASAN. 4.1 Isolasi sinamaldehida dari minyak kayu manis. Minyak kayu manis yang digunakan dalam penelitian ini diperoleh dari
 37 BAB IV HASIL DAN PEMBAHASAN 4.1 Isolasi sinamaldehida dari minyak kayu manis Minyak kayu manis yang digunakan dalam penelitian ini diperoleh dari hasil penyulingan atau destilasi dari tanaman Cinnamomum
37 BAB IV HASIL DAN PEMBAHASAN 4.1 Isolasi sinamaldehida dari minyak kayu manis Minyak kayu manis yang digunakan dalam penelitian ini diperoleh dari hasil penyulingan atau destilasi dari tanaman Cinnamomum
