BERBAGAI MIKROORGANISME RIZOSFER PADA TANAMAN PEPAYA
|
|
|
- Ade Agus Atmadja
- 7 tahun lalu
- Tontonan:
Transkripsi
1 BERBAGAI MIKROORGANISME RIZOSFER PADA TANAMAN PEPAYA (Carica papaya L.) DI PUSAT KAJIAN BUAH-BUAHAN TROPIKA (PKBT) IPB DESA CIOMAS, KECAMATAN PASIRKUDA, KABUPATEN BOGOR, JAWA BARAT DODY SUSENO SIMATUPANG A DEPARTEMEN PROTEKSI TANAMAN FAKULTAS PERTANIAN INSTITUT PERTANIAN BOGOR 2008
2 ABSTRAK DODY SUSENO S. Berbagai Mikroorganisme Rizosfer pada Tanaman Pepaya (Carica papaya L.) di Pusat Kajian Buah-buahan Tropika (PKBT) IPB Desa Ciomas, Kecamatan Pasirkuda, Kabupaten Bogor, Jawa Barat. Dibimbing oleh IVONNE OLEY SUMARAUW. Pepaya (Carica papaya L) merupakan tanaman yang sudah lama dikenal di Indonesia. Dalam budidaya tanaman ini dipengaruhi oleh keberadaan mikroorganisme rizosfer seperti bakteri, cendawan, dan protozoa. Populasi mikroorganisme rizosfer biasanya lebih banyak dan beragam dibandingkan pada tanah bukan rizosfer. Mikroorganisme rizosfer dapat mempengaruhi pertumbuhan tanaman, bermanfaat atau menjadi patogen tanaman. Penelitian mengenai keragaman organisme yang ada pada rizosfer perlu dilakukan sebagai sumber informasi awal yang dapat digunakan sebagai acuan dalam pengembangan pengendalian hama terpadu. Pengamatan dilakukan pada lahan pertanaman pepaya sebanyak 3 petak yang masing-masing berukuran 500 m 2 dengan varietas IPB 1, IPB 2, dan IPB 6. Tanaman contoh kemudian ditetapkan dengan metode acak diagonal. Tanah dari tanaman contoh diambil dengan mengebor tanah sekitar akar dengan kedalaman 5 sampai 25 cm. Tanah yang telah diambil dimasukan kedalam kantong terpisah dan diuji di laboratorium. Tanah sebanyak 10 g dari masing-masing titik dicampur dan dibuat suspensi yaitu mencampurkannya dengan 90 ml air steril kemudian dikocok selama 15 menit. Suspensi tersebut diambil sebanyak 1 ml kemudian dimasukkan kedalam tabung berisi 9 ml air steril lalu dilakukan pengenceran berseri sampai pengenceran Sebanyak 0,1 ml hasil pengenceran masingmasing 10-4, 10-5, dan 10-6 dituangkan kedalam cawan petri yang berisi media Potato Dextrose Agar (PDA) dan Martin Agar (MA) untuk isolasi cendawan. Isolasi bakteri pada media Nutrient Agar (NA), Yeast Dextrose Agar (YDC) dan King s B. Pengamatan dilakukan setelah masa inkubasi dengan mengamati dan mengidentifikasi koloni cendawan dan bakteri yang muncul. Hasil penelitian menunjukkan ditemukan beberapa mikroorganisme rizosfer yang terdiri dari bakteri dan cendawan. Pada pertanaman pepaya IPB 1 ditemukan 8 koloni bakteri yang terdiri dari Pseudomonas fluorescens, Xanthomonas sp, Erwinia sp., Pantoea sp., Agrobacterium sp., bakteri Grampositif dan 4 isolat cendawan yaitu Aspergillus fumigatus, Aspergillus flavus, Penicillium sp., Trichoderma sp. Pada pertanaman IPB 2 ditemukan 7 koloni bakteri yang terdiri dari Pseudomonas fluorescens, Xanthomonas sp., Erwinia sp., Pantoea sp., bakteri Gram-positif dan 3 isolat cendawan Aspergillus flavus., Aspergillus fumigatus., Aspergillus sp. Pada pertanaman IPB 6 ditemukan 6 koloni bakteri yang terdiri dari Pseudomonas fluorescens, Xanthomonas sp., Erwinia sp., Pantoea sp., Agrobacterium sp., bakteri Gram-positif dan 4 isolat cendawan yaitu Aspergillus fumigatus, Aspergillus sp., Penicillium sp., Trichoderma sp.
3 BERBAGAI MIKROORGANISME RIZOSFER PADA TANAMAN PEPAYA (Carica papaya L.) DI PUSAT KAJIAN BUAH-BUAHAN TROPIKA (PKBT) IPB DESA CIOMAS, KECAMATAN PASIRKUDA, KABUPATEN BOGOR, JAWA BARAT Skripsi Sebagai salah satu syarat untuk memperoleh gelar Sarjana Pertanian pada Fakultas Pertanian, Institut Pertanian Bogor DODY SUSENO SIMATUPANG A DEPARTEMEN PROTEKSI TANAMAN FAKULTAS PERTANIAN INSTITUT PERTANIAN BOGOR 2008
4 Judul Skripsi : Berbagai Mikroorganisme Rizosfer pada Tanaman Pepaya (Carica papaya L.) di Pusat Kajian Buah-buahan Tropika (PKBT) IPB Desa Ciomas, Kecamatan Pasirkuda, Kabupaten Bogor, Jawa Barat. Nama : Dody Suseno Simatupang NRP : A Disetujui, Dosen Pembimbing Ir. Ivonne Oley Sumarauw, MSi. NIP Diketahui, Dekan Fakultas Pertanian Prof.Dr. Ir. Didy Soepandie, M.Agr NIP Tanggal lulus :
5 RIWAYAT HIDUP Penulis dilahirkan di Jakarta pada tanggal 12 Juli 1984 sebagai anak kedua dari tiga bersaudara dari pasangan bapak Sorie Mula Simatupang dan ibu Sukarsih Nasution. Tahun 2002, penulis lulus dari Sekolah Menengah Umum PGRI 22 Serpong. Pada tahun yang sama penulis diterima di Institut Pertanian Bogor, Fakultas Pertanian, Departemen Proteksi Tanaman, melalui jalur USMI. Selama kuliah penulis pernah menjadi pengurus Himpunan Mahasiswa Proteksi Tanaman (HIMASITA) periode 2003 sampai 2004, penulis juga pernah menjadi asisten praktikum mata kuliah Proteksi Tanaman periode , dan Hama Penyakit Benih dan Pascapanen untuk program Diploma Bogor, Mei 2008 Dody Suseno S
6 PRAKATA Puji dan syukur penulis panjatkan kepada Allah SWT berkat rahmat dan hidayah-nya penulis dapat menyelesaikan penulisan skripsi yang berjudul Berbagai Mikroorganisme Rizosfer pada Tanaman Pepaya (Carica papaya L.) di Pusat Kajian Buah-buahan Tropika (PKBT) IPB Desa Ciomas, Kecamatan Pasirkuda, Kabupaten Bogor, Jawa Barat Penulisan skripsi ini ditujukan sebagai salah satu syarat untuk menyelesaikan tugas akhir di Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor. Selama penulisan skripsi ini, penulis banyak mendapatkan bantuan. Pada kesempatan ini penulis mengucapkan banyak terima kasih kepada : 1. Ir. Ivonne Oley Sumarauw, MSi yang telah menjadi pembimbing pembuatan proposal, penelitian, dan penyelesaian skripsi ini. 2. Prof. Dr. Ir Utomo Kartosuwondo MS. selaku pembimbing akademik dan dosen penguji tamu. 3. Pusat Kajian Buah-buahan Tropika (PKBT) IPB yang telah memberi dukungan untuk kelancaran berjalannya penelitian ini. 4. Bapak Baisuni yang telah membantu penulis dalam survei lahan dan metode di lapangan. 5. Bapak Yusuf Irawan yang telah membantu dalam penyediaan alat dan bahan penelitian. 6. Sorie Mula Simatupang dan Sukarsih Nasution selaku orang tua yang telah memberi dukungan, do a, nasihat, dan membiayai penulis hingga menyelesaikan pendidikan di IPB. 7. Ade ku Meidy tercinta terima kasih atas kesabaran, cinta, dukungan dan semangat yang diberikan. Semoga Allah SWT, membalas kebaikanmu. 8. Semua pihak yang telah membantu baik moril maupun materil yang tidak dapat disebutkan satu persatu Penulis menyadari bahwa penulisan skripsi ini masih banyak kekurangan, namun penulis berharap semoga skripsi ini bermanfaat bagi kita semua. Amiin. Bogor, Mei 2008 Dody Suseno S
7 DAFTAR ISI Halaman DAFTAR TABEL... vii DAFTAR GAMBAR... viii PENDAHULUAN... 1 Latar Belakang... 1 Tujuan... 1 Manfaat... 2 TINJAUAN PUSTAKA... 3 Karakteristik Tanaman... 3 Budidaya Pepaya... 3 Manfaat Tanaman Pepaya... 4 Hama dan Penyakit Tanaman Pepaya... 4 Rizosfer... 5 BAHAN DAN METODE Tempat dan Waktu... 7 Metode... 7 Pra Pengamatan/ Survei Penentuan Tanaman Contoh dan Pengambilan Tanah... 7 Isolasi Mikroba Tanah... 7 Identifikasi... 8 Cendawan... 8 Bakteri... 8 Uji Gram (KOH 3%)... 8 Uji Oksidatif/fermentatif... 8 Uji fluorescent... 9 Uji Levan... 9 Uji oksidase... 9 Uji pembusukkan pada kentang... 9 Uji arginine dihydrolase Pertumbuhan pada media YDC (33 ºC) Pertumbuhan pada media D1M agar Reaksi hipersensitif... 10
8 HASIL DAN PEMBAHASAN Isolasi Mikroorganisme Rizosfer Cendawan Bakteri Hasil uji Gram (KOH 3%) Hasil uji Oksidatif/fermentatif Hasil uji fluorescent Hasil uji Levan Hasil uji oksidase Hasil uji pembusukkan pada kentang Hasil uji arginine dihydrolase Hasil pertumbuhan pada media YDC (33 ºC) Hasil pertumbuhan media D1M agar Hasil reaksi hipersensitif Keragaman Mikroorganisme Rizosfer KESIMPULAN DAN SARAN Kesimpulan Saran DAFTAR PUSTAKA LAMPIRAN Komposisi bahan untuk isolasi dan identifikasi bakteri Kunci identifikasi (Schaad et al. 2001)... 26
9 DAFTAR TABEL Halaman 1. Hasil identifikasi cendawan pada rizosfer tanaman pepaya IPB 1, IPB 2, dan IPB Hasil identifikasi bakteri dan cendawan pada eksplorasi rizosfer tanaman IPB 1, IPB 2, dan IPB
10 DAFTAR GAMBAR Halaman 1. Cendawan (a) Trichoderma sp., (b) Aspergillus flavus, (c) Aspergillus fumigatus, (d) Penicilium sp, hasil eksplorasi rizosfer tanaman pepaya IPB 1, IPB 2, dan IPB 6 ) Mikroskopis Penicilium sp. (a), mikroskopis Aspergillus sp. (b) hasil eksplorasi rizosfer tanaman pepaya IPB 1, IPB 2, dan IPB Hasil uji uji oksidatif/fermentatif. Bakteri bersifat fermentatif (a), bakteri bersifat oksidatif (b) Reaksi positif (a) dan reaksi negatif (b) uji fluorescent Reaksi positif (a) dan reaksi negatif (b) pada uji Levan Reaksi positif (a) dan reaksi negatif (b) pada uji oksidase Reaksi positif pembusukkan kentang isolat Erwinia sp.(a) dan reaksi negatif (b) hasil eksplorasi rizosfer tanaman pepaya IPB 1, IPB 2, dan IPB Reaksi positif bakteri uji (b) pada uji arginine dihydrolase dibandingkan kontrol (a) Reaksi positif pada media YDC berupa koloni berwarna kuning Reaksi positif uji hipersensitif pada daun tembakau berupa gejala nekrosis... 18
11 PENDAHULUAN Latar Belakang Pepaya (Carica papaya L) merupakan tanaman yang sudah lama dikenal di Indonesia. Tanaman ini mudah ditanam dan tidak memerlukan lahan yang luas sehingga memberi peluang untuk dibudidayakan lebih banyak dan intensif. Luas daerah pertanaman pepaya di Indonesia dengan orientasi bisnis mencapai ha, yang produksinya ton per tahun (Warisno 2003), dengan pusat penanaman diantaranya daerah Jawa Barat, Jawa Timur, DKI Jakarta, Yogyakarta, Lampung Tengah, Sulawesi Selatan, dan Sulawesi Utara (BAPPENAS 2006). Tanaman yang berasal dari Amerika Tengah dan Hindia Barat ini memiliki batang bulat, agak lunak, dengan diameter antara 10 sampai 30 cm. Daunnya berbentuk bintang, menyebar pada bagian ujung batang (BAPPENAS 2006), daging buahnya berwarna kuning sampai jingga. Karakteristik bunga, daun, batang, dan biji berbeda-beda. Hampir semua bagian tanaman pepaya dapat dimanfaatkan baik buah, batang, daun maupun akarnya. Buah pepaya merupakan buah bermutu dan bergizi tinggi, sebagai sumber nutrisi terutama vitamin A dan C. Daunnya berkhasiat sebagai obat dari berbagai penyakit. Akar tanamannya dapat digunakan untuk mengobati cacingan pada anak-anak yaitu dengan cara direbus untuk diminum airnya (Warisno 2003). Dalam budidayanya tanaman ini dipengaruhi oleh keberadaan mikroorganisme rizosfer seperti bakteri, cendawan, dan protozoa. Menurut Lynch (1990) dan Carlile et al. (2001), populasi mikroorganisme di rizosfer biasanya lebih banyak dan beragam dibandingkan pada tanah bukan rizosfer. Mikroorganisme rizosfer dapat mempengaruhi pertumbuhan tanaman, baik menguntungkan atau menjadi patogen tanaman (Curl & Truelove 1986 dalam Hornbyn 1990). Tujuan Penelitian bertujuan untuk mengetahui keragaman mikroorganisme (cendawan dan bakteri) rizosfer pada tanaman pepaya (Carica papaya L.).
12 2 Manfaat Penelitian ini memberikan informasi mengenai jenis mikroorganisme rizosfer tanaman pepaya (Carica papaya L.) yang selanjutnya dapat digunakan sebagai sumber acuan program pengendalian organisme pengganggu tanaman (OPT) secara terpadu.
13 3 TINJAUAN PUSTAKA Karakteristik Tanaman Pepaya merupakan tanaman anggota famili Caricaceae. Tinggi tanaman pepaya antara 2 sampai 10 m, berbatang bulat, agak lunak, berongga dengan diameter antara 10 sampai 30 cm. Daun berbentuk bintang, menyebar dan berdesakan pada bagian ujung batang (BAPPENAS 2006). Di Indonesia terdapat banyak jenis pepaya, baik yang berdaging buah kuning maupun jingga dengan karakteristik bunga, daun, batang, dan biji yang berbeda-beda. Bunga sempurna muncul setelah bunga keempat yaitu ketika tanaman berumur tiga bulan. Budidaya Pepaya Tanaman pepaya tumbuh subur pada daerah yang memilki curah hujan 1000 hingga 2000 mm/tahun. Suhu udara optimum 22 o C sampai 26 o C dengan kelembaban udara 40%. Tanah yang subur dan banyak mengandung humus baik untuk pertumbuhan tanaman pepaya, selain itu tanah juga harus banyak menahan air dan gembur. Derajat keasaman tanah (ph) antara 6 sampai 7 (Warisno 2003). Di Indonesia tanaman pepaya dapat tumbuh di daerah dataran rendah sampai pegunungan yang memiliki ketinggian 1000 m di atas permukaan laut. Luas daerah pertanaman pepaya dengan orientasi bisnis mencapai ha, dengan produksi ton per tahun. Buah pepaya belum merupakan komoditi ekspor yang dapat diandalkan karena masih terbatas untuk mencapai kebutuhan dalam negeri (Warisno 2003). Penanaman dilakukan dengan cara menyemai biji di polibag kemudian ditanam di kebun atau biji ditanam langsung pada lubang tanam. Lubang tanam dibuat berukuran 60 cm x 60 cm x 40 cm, kemudian diisi pupuk kandang sebanyak 20 kg/lubang. Jarak tanam dibuat 3 m x 3 m atau 13,5 m x 2 m. Setiap lubang ditanam 3 hingga 5 biji. Setelah tumbuh, bibit yang tidak terpilih dibuang sehingga satu lubang hanya diisi satu bibit yang tumbuh kekar, sehat, dan berbunga sempurna (BAPPENAS 2006).
14 4 Pemeliharaan tanaman meliputi pemupukan, pengairan dan penyiangan. Pupuk buatan yang diberikan berupa NPK dengan dosis 25 sampai 200 g per tanaman, tergantung umurnya. Pengairan dilakukan sekurang-kurangnya 1 minggu sekali bila musim kemarau. Pemeliharaan selanjutnya yaitu penyiangan yang meliputi pembersihan gulma atau alang-alang dengan menggunakan cangkul. Tanaman pepaya dapat dipanen setelah berumur 9 sampai 12 bulan. Buah pepaya dipanen pada stadium mendekati matang pohon, yakni setelah buah menunjukkan garis-garis menguning. Panen dilakukan setiap 10 hari sekali. Manfaat Tanaman Pepaya Hampir semua bagian tanaman pepaya dapat dimanfaatkan, mulai dari buah, daun, biji, getah, batang, dan akar. Buah pepaya merupakan buah bermutu dan bergizi tinggi. Pepaya yang masih muda dimanfaatkan untuk dibuat sayur, sedangkan buah yang sudah matang disajikan sebagai buah meja. Selain itu buah pepaya sebagai sumber nutrisi terutama vitamin A dan C serta dapat dijadikan bahan baku pembuatan saus tomat yakni untuk penambah cita rasa, warna dan kadar vitamin. Daun tanaman pepaya berkhasiat sebagai obat malaria, kejang perut, sakit panas, dan dapat menyembuhkan penyakit beri-beri. Menurut penelitian, biji pepaya dapat menghasilkan minyak yang mengandung 71,60% asam oleat, 15,13% asam palmat 7,68% asam linoleat, 3,60% asam stearat, dan asam-asam lemak lain dalam jumlah relatif sedikit. Getah pepaya yang banyak mengandung papain dapat digunakan untuk berbagai keperluan, antara lain: penjernihan bir, pengempuk daging, bahan baku industri penyamak kulit, serta digunakan dalam industri farmasi dan kosmetik (kecantikan). Papain merupakan enzim proteolitik yaitu enzim yang dapat mengurai dan memecah protein. Akar tanaman ini dapat digunakan untuk mengobati cacingan pada anak-anak yaitu dengan cara direbus untuk diminum airnya (Warisno 2003). Hama dan Penyakit Tanaman Pepaya Hama yang menjadi masalah pada pertanaman pepaya adalah jenis serangga seperti kutu daun spesies Myzus persicae Sulz, Aphis gossypii Glov, lalat buah Bactrocera dorsalis Hend, kepik Nezara viridula L., Thrips tabaci
15 5 Lind., dan tungau yang menjadi hama pada pertanaman ini. Jenis tungau yang sering menyerang tanaman pepaya sebagian besar merupakan tungau dari famili Tetranychidae. Penyakit yang sering menyerang tanaman pepaya antara lain: hawar daun bakteri yang disebabkan oleh Erwinia papayae (Rant), virus bercak cincin pepaya, virus mosaik pepaya, busuk akar yang disebabkan oleh Pythium sp. dan penyakit antraknosa yang disebabkan oleh Colletotrichum gloeosporioides (Sriyanti 2004). Rizosfer Rizosfer merupakan bagian tanah yang berada di sekitar perakaran tanaman dan berperan sebagai pertahanan luar bagi tanaman terhadap serangan patogen akar. Konsep rizosfer pertama kali dikemukakan oleh Hiltner (1904) dalam Lynch (1990). Populasi mikroorganisme di rizosfer biasanya lebih banyak dan beragam dibandingkan pada tanah bukan rizosfer (Lynch 1990; Carlile et al. 2001). Menurut Foster (1985), Curl & True love (1986) dalam Hornby (1990), beberapa mikroorganisme rizosfer berperan penting dalam siklus hara dan proses pembentukan tanah, pertumbuhan tanaman, mempengaruhi aktivitas mikroorganisme serta sebagai pengendali hayati terhadap patogen akar. Menurut Jeger (2001), kehadiran sejumlah populasi organisme baik yang bersifat antagonis, patogen, maupun saprofit dapat menambah keragaman spesies di dalam komunitas alami tanaman. Berdasarkan bibliografinya, rizosfer dicirikan dengan aktivitas biologinya yang paling tinggi pada tanah (Patkowska 2002). Lingkungan rizosfer total ditentukan oleh interaksi dari tanah, tanaman, dan organisme yang berasosiasi dengan akar (Lynch 1990). Hubungan antara organisme dan akar dapat menguntungkan, merusak, atau netral tetapi seiring pengaruhya tergantung pada kondisi tanah. Secara alami tanah memiliki potensi mikroorganisme yang mampu menekan perkembangan patogen dalam tanah. Sebagian besar mikroorganisme antagonis tersebut hidup sebagai saprofit. Kemampuan organisme dalam beradaptasi terhadap berbagai keadaan lingkungan merupakan potensi besar untuk digunakan sebagai agen pengendali hayati (Baker & Cook 1974).
16 6 Mikroorganisme yang hidup pada daerah rizosfer biasanya digunakan sebagai agen pengendalian hayati. Keberadaan mikroorganisme antagonis pada daerah rizosfer dapat menghambat persebaran dan infeksi akar oleh patogen, keadaan ini disebut hambatan alamiah mikroba Mikroba antagonis sangat potensial dikembangkan sebagai agen pengendalian hayati. Selain sebagai agen antagonis, mikroorganisme tanah juga dapat mempengaruhi pertumbuhan tanaman dengan memproduksi senyawa-senyawa stimulat pertumbuhan seperti auksin dan fitohormon (Waksman 1952).
17 7 BAHAN DAN METODE Tempat dan Waktu Penelitian dilaksanakan di pertanaman pepaya Pusat Kajian Buah-buahan Tropika (PKBT) IPB di desa Ciomas, Kelurahan Pasirkuda, Kabupaten Bogor, Jawa Barat. Penelitian dilanjutkan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanain Bogor, dari Juli 2007 sampai Desember Metode Pra pengamatan/ survei Sebelum pengamatan terlebih dahulu dilakukan survei pada lahan yang akan digunakan. Kegiatan survei bertujuan untuk mengetahui kondisi lahan, kondisi tanaman pepaya yang akan diamati, dan untuk memudahkan dalam menentukan tanaman contoh yang akan dijadikan sampel. Penentuan tanaman contoh dan pengambilan tanah Lahan yang digunakan sebanyak 3 petak yang masing-masing berukuran 500 m 2 dan ditanami pepaya varietas IPB 1, IPB 2, dan IPB 6. Tanaman contoh kemudian ditetapkan dengan metode acak diagonal. Tanah dari tanaman contoh diambil dengan mengebor tanah sekitar akar dengan kedalaman 5 sampai 25 cm. Tanah dari masing-masing titik tersebut dimasukan ke dalam plastik terpisah dan diuji di laboratorium. Isolasi mikroba tanah Tanah yang telah diambil dari 5 titik contoh selanjutnya diisolasi dengan metode pengenceran berseri. Tanah sebanyak 10 g dari masing-masing titik dicampur dan dibuat suspensi yaitu mencampurkannya dengan 90 ml air steril kemudian dikocok selama 15 menit. Suspensi tersebut diambil sebanyak 1 ml kemudian dimasukkan ke dalam tabung berisi 9 ml air steril dan dibuat pengenceran berseri sampai pengenceran 10-6.
18 8 Isolasi cendawan dilakukan secara tidak langsung dengan metode pengenceran kemudian penggoresan pada media, dan secara langsung dengan meletakan tanah langsung pada permukaan media. Media yang digunakan adalah Potato Dextrose Agar (PDA) dan Martin Agar (MA). Isolasi bakteri dilakukan dengan metode penggoresan pada beberapa media yaitu Nutrient Agar (NA), Kings' B, Yeast Dextrose Agar (YDC), Identifikasi A. Cendawan Cendawan yang diperoleh dari hasil isolasi dibuat preparat slide kemudian diidentifikasi dibawah mikroskop compound. Identifikasi dilakukan berdasarkan kunci identifikasi yang dikemukakan oleh Watanabe T (1993) dan Domsch KH et al. (1993). B. Bakteri Identifikasi bakteri berdasarkan kunci identifikasi yang dikemukakan Schaad NW et al. (2001) (lampiran 1) dan Brown JF et al (1980). Beberapa uji yang dilakukan untuk mengetahui genus maupun spesies bakteri hasil isolasi rizosfer tanaman pepaya IPB 1, IPB 2, dan IPB 6, sebagai berikut: 1. Uji Gram (KOH 3%) Uji ini dilakukan dengan mencampurkan satu loop suspensi bakteri uji pada preparat yang telah ditetesi KOH 3%, kemudian diamati terbentuk tidaknya lendir. Apabila terbentuk lendir saat lup ditarik ke atas maka dikelompokan sebagai Gram-negatif dan apabila tidak terbentuk lendir maka bakteri Gram- positif. 2. Uji oksidatif/fermentatif Uji oksidatif/fermentatif dilakukan dengan menumbuhkan bakteri uji pada media oksidatif/fermentatif dengan ph 7.1 dalam tabung reaksi. Bakteri uji diinokulasikan dengan cara menusukkannya sedalam 0.5 cm, kemudian ditutup dengan vaselin steril pada salah satu tabung. Pada pengujian ini digunakan kontrol berupa media uji tanpa bakteri. Pada pengujian ini digunakan kontrol berupa media uji tanpa bakteri. Bakteri bersifat oksidatif apabila terjadi perubahan warna menjadi
19 9 kuning pada media uji tanpa vaselin, tetapi tidak mengalami perubahan warna pada media yang diberi vaselin. Bakteri bersifat fermentatif apabila mengalami perubahan warna menjadi kuning, baik pada media bervaselin maupun tidak bervaselin. 3. Uji fluorescent Uji ini dilakukan untuk membedakan kelompok bakteri Pseudomonas sp. dengan kelompok bakteri lainnya, yaitu dengan menggoreskan bakteri uji pada media King's B. Reaksi positif berupa kelompok bakteri Pseudomonas sp. ditunjukkan oleh warna kuning-hijau kebiruan pada koloni bakteri apabila diamati di bawah sinar ultraviolet setelah 48 jam inkubasi. 4. Uji Levan Pengujian dilakukan dengan menggoreskan bakteri uji pada media NA yang ditambahkan dengan 5% ( b / v ) sukrosa. Reaksi positif ditunjukkan dengan terbentuknya koloni berwarna putih, cembung, dan berlendir setelah diinokulasi selama 3 hari. 5. Uji oksidase Pengujian ini dilakukan dengan menggoreskan koloni bakteri berumur 24 jam pada kertas saring steril yang telah ditetesi dengan media berupa 1% larutan tetramethylparaphenylenediamine dihydrochloride. Reaksi positif ditunjukkan dengan adanya perubahan warna bakteri pada kertas saring yang menjadi warna ungu gelap setelah 10 hingga 15 detik. 6. Uji pembusukkan pada kentang Uji ini dilakukan dengan menggoreskan koloni bakteri yang berumur 24 sampai 48 jam pada irisan kentang (ketebalan 7 hingga 8 mm) yang telah disterilisasi permukaannya dengan natrium hipoklorit (NaOCl) 1% selama 1 menit kemudian dibilas dengan aquades steril. Selanjutnya irisan kentang tersebut diinkubasi dalam cawan petri pada kondisi lembab. Reaksi positif ditunjukkan dengan terjadinya pembusukkan setelah penggoresan inokulum bakteri pada irisan kentang. Permukaan kentang yang di inokulasi menjadi berlendir dan terdapat lubang kecil setelah 24 jam perlakuan. Uji pembusukkan kentang dilakukan untuk mengetahui
20 10 apakah kelompok bakteri yang diuji bersifat patogen atau bukan patogen khususnya kelompok Pseudomonas sp. Pada bakteri Pseudomonas sp. yang bukan patogen lubang yang terbentuk lebih dangkal dan tidak terdapat lendir pada kentang yang diinokulasi (Lelliot et al dalam Schaad et al. 2001). 7. Uji arginine dihydrolase Pengujian ini dilakukan dengan memasukkan inokulum bakteri pada tabung reaksi yang telah berisi media arginine dengan cara menusukkannya dengan kedalaman 0,5 cm, kemudian ditutup dengan menggunakan vaselin steril. Reaksi positif ditunjukkan dengan adanya perubahan warna media dari orange menjadi merah muda. 8. Pertumbuhan pada media YDC (33 ºC) Yeast Dextrose Carbonat (YDC) merupakan media semi selektif untuk pertumbuhan bakteri Xanthomonas sp. dan menjadi uji untuk membedakan antara bakteri Xanthomonas sp. dengan Xylophilus sp. Bakteri uji digoreskan pada media YDC yang kemudian diinkubasi selama 48 jam pada suhu 33 ºC. Reaksi positif ditunjukkan dengan munculnya koloni bakteri berwarna kuning pada media. 9. Pertumbuhan pada media D1M agar D1M merupakan media semiselektif untuk pertumbuhan bakteri Agrobacterium sp. Uji ini dilakukan dengan menumbuhkan bakteri uji pada media D1M agar. 10. Reaksi hipersensitif Reaksi hipersensitif merupakan uji yang dilakukan untuk mengetahui sifat patogenik bakteri uji. Reaksi ini dilakukan dengan mencampurkan 1 hingga 2 loop koloni bakteri, lalu dikocok selama 24 jam dengan kecepatan 100 rpm. Selanjutnya suspensi tersebut di inokulasi pada daun tembakau dengan menyuntikkannya pada lamina daun. Reaksi hipersensitif positif ditunjukkan dengan terbentuknya gejala nekrosis pada bagian daun yang diinokulasi setelah 24 sampai 48 jam.
21 11 HASIL DAN PEMBAHASAN Isolasi Mikroorganisme Rizosfer A. Cendawan Hasil identifikasi isolasi cendawan dari lahan pertanaman pepaya IPB 1, IPB 2, dan IPB 6 pada preparat slide mikroorganisme diperoleh 5 isolat cendawan yaitu Aspergillus fumigatus, Aspergillus flavus, Penicillium sp., Trichoderma sp., dan Aspergillus sp. (Tabel 1). Tabel 1 Hasil identifikasi cendawan pada rizosfer tanaman pepaya IPB 1, IPB 2, dan IPB 6 Warna miselium Nama cendawan Pepaya IPB 1 Hijau tua A. fumigatus Hijau muda A. flavus Hijau abu-abu Penicillium sp. Hijau gelap Trichoderma sp. Pepaya IPB 2 Hijau tua A. fumigatus Putih Aspergillus sp. Hijau muda A. flavus Pepaya IPB 6 Hijau tua A. fumigatus Putih Aspergillus sp. Hijau abu-abu Penicillium sp. Hijau gelap Trichoderma sp. (a) (b) (c) (d) (e) Gambar 1 Cendawan (a) Trichoderma sp., (b) A. flavus, (c) A. fumigatus, (d) Penicillium sp, dan (e) Aspergillus sp. hasil eksplorasi rizosfer tanaman pepaya IPB 1, IPB 2, dan IPB 6.
22 12 (a) (b) Gambar 2 Mikroskopis Penicillium sp. (a), mikroskopis Aspergillus sp. (b) hasil eksplorasi rizosfer tanaman pepaya IPB 1, IPB 2, dan IPB 6. B. Bakteri Berdasarkan hasil isolasi mikroorganisme pada rizosfer tanaman pepaya IPB 1, IPB 2, dan IPB 6 diperoleh 21 koloni bakteri yang dindentifikasi sebagai P. fluorescens, Xanthomonas sp., Erwinia sp., Pantoea sp., Agrobacterium sp., dan 5 koloni bakteri Gram-positif. Untuk mengetahui genus maupun spesies bakteri hasil isolasi tersebut dilakukan beberapa uji sebagai berikut: 1. Hasil uji Gram (KOH 3%) Hasil isolasi bakteri pertanaman pepaya IPB 1, IPB 2 dan IPB 6 diperoleh 21 isolat uji. Hasil pengujian Gram dengan KOH 3% diperoleh 16 isolat Gram-negatif dan 5 isolat Gram-positif yang didasarkan pada terbentuk tidaknya lendir. Menurut Stainer et al. (1984), bakteri akan selalu menjaga osmolaritasnya jauh melebihi medium. Apabila tekanan osmotik internal sel turun sampai di bawah tekanan osmotik eksternal, maka air akan keluar dari sel, menyebabkan volume sitoplasma berkurang dan terjadi kerusakan pada membran. Penambahan KOH 3% yang memiliki viskositas lebih tinggi dibandingkan sel bakteri akan menyebabkan cairan sel keluar dan terjadi osmosis. Hal ini yang terjadi pada bakteri Gram-negatif. 2. Hasil uji oksidatif/fermentatif Pada pertanaman pepaya IPB 1 yang terdiri dari 8 isolat, 6 isolat menunjukkan perubahan warna menjadi kuning pada media yang tidak diberi vaselin (kondisi aerob), dan 2 isolat lainnya menunjukkan perubahan warna pada media yang diberi vaselin (kondisi anaerob), sedangkan pertanaman pepaya IPB 2 yang terdiri dari 7 isolat, 5 isolat menujukkan perubahan warna
23 13 menjadi kuning pada media yang tidak diberi vaselin (kondisi aerob), dan 2 isolat menunjukkan perubahan warna pada media yang diberi vaselin (kondisi anaerob). Pada pertanaman pepaya IPB 6 yang terdiri dari 6 isolat, 4 isolat menunjukkan perubahan warna menjadi kuning pada media yang tidak diberi vaselin (kondisi aerob) dan 2 isolat lainnya tidak menunjukkan perubahan warna pada media diberi vaselin (anaerob). a a b b Gambar 3 Hasil uji uji oksidatif/fermentatif. Bakteri bersifat fermentatif (a), bakteri bersifat oksidatif (b). 3. Hasil uji fluorescent Uji fluorescent adalah uji yang dilakukan pada media King s B. Dari 21 isolat yang di uji hanya 3 isolat yang mengeluarkan pigmen fluorescent di bawah sinar ultraviolet (Gambar 5). Berdasarkan uji ini diketahui bahwa isolat tersebut adalah bakteri Pseudomonas sp. Selanjutnya untuk mengetahui apakah bakteri bersifat patogen atau bukan patogen maka diperlukan uji lanjutan yaitu uji Levan, uji oksidase, uji pembusukkan kentang, arginine dihydrolase dan uji hipersensitif pada tembakau (LOPAT) (Brown JF et al. 1980). Uji fluorescent merupakan salah satu uji yang memberikan kemudahan untuk dapat membedakan bakteri Pseudomonas sp. kelompok fluorescent dengan kelompok bakteri lainnya. Ciri khas P. fluorescens adalah berpendar di bawah sinar ultraviolet. Fluoresensi ini dihasilkan oleh pigmen fluorescent berupa senyawa fluoresein atau pioverdin yang akan terbentuk apabila bakteri tumbuh pada media yang kurang unsur besi seperti media King s B.
24 14 (a) (b) Gambar 4 Reaksi positif (a) dan reaksi negatif (b) uji fluorescent 4. Hasil uji Levan Dari 21 isolat yang diuji pada media Levan, 8 isolat menunjukkan reaksi positif yang ditunjukkan dengan tumbuhnya isolat bakteri yang cembung dan berlendir pada media Levan serta 13 isolat menunjukkan reaksi negatif yaitu tumbuhnya isolat bakteri tidak melebar dan berlendir. Pada 3 isolat bakteri Pseudomonas sp. yang diuji menunjukkan hasil negatif pada media levan. Uji Levan merupakan uji karakterisasi sifat bakteri kelompok Pseudomonas sp., untuk membuktikan apakah bakteri termasuk kelompok patogen atau bukan patogen terhadap tanaman. Berdasarkan uji ini diketahui bahwa Pseudomonas sp. yang ditemukan tidak bersifat patogen bagi tanaman. (a) (b) Gambar 5 Reaksi positif (a) dan reaksi negatif (b) pada uji levan 5. Hasil uji oksidase Reaksi positif pada hasil uji oksidase ditunjukkan dengan adanya perubahan warna pada kertas saring menjadi warna ungu gelap setelah 10 sampai 15 detik. Dari 21 isolat bakteri yang diuji, 18 isolat menunjukkan reaksi positif termasuk bakteri Pseudomonas sp. termasuk 3 isolat lainnya menunjukkan reaksi negatif.
25 15 (a) (b) Gambar 6 Reaksi positif (a) dan reaksi negatif (b) isolat bakteri pada uji oksidase. 6. Hasil uji pembusukkan pada kentang Hasil uji pembusukkan pada kentang menunjukkan dari 21 isolat, 18 isolat termasuk 3 isolat Pseudomonas sp. masing-masing dari pertanaman pepaya IPB 1, IPB 2, dan IPB 6 menunjukkan reaksi negatif yaitu tidak terjadi pembusukkan, tidak berlendir dan tidak terdapat lubang pada irisan kentang. Hal ini menunjukkan bahwa semua isolat tersebut termasuk bakteri Pseudomonas sp yang diuji merupakan bakteri bukan patogen dan 4 isolat lainnya menunjukkan reaksi positif. Tiga isolat bakteri masing-masing dari lahan pertanaman pepaya IPB 1, IPB 2, IPB 6 yang menunjukkan reaksi positif yaitu terdapat lubang pada irisan kentang kemudian diindentifikasi dengan uji lanjutan seperti uji oksidatif /fermentatif, uji pertumbuhan pada media YDC yang diinkubasi pada suhu 33 0 C. Dari hasil uji maka diduga bakteri tersebut adalah Erwinia sp (lampiran 1). Terjadinya pembusukkan pada kentang merupakan akibat dari adanya aktivitas pektat pada 24 jam perlakuan, sehingga terbentuk lubang-lubang kecil yang cukup dalam pada permukaan yang diinokulasikan serta menyebabkan kentang menjadi berlendir.
26 16 (a) (b) Gambar 7 Reaksi positif pembusukkan kentang isolat Erwinia sp.(a) dan reaksi negatif (b) hasil eksplorasi rizosfer tanaman pepaya IPB 1, IPB 2, dan IPB Hasil uji arginine dihydrolase Hasil uji arginine dihydrolase menunjukkan adanya reaksi positif pada semua isolat yang di uji yakni terjadi perubahan warna media dari orange menjadi merah muda, termasuk bakteri Pseudomonas sp.. Perubahan warna media terjadi akibat adanya aktivitas dua enzim yang dihasilkan bakteri yaitu enzim desmidase yang berperan mendegradasi arginine menjadi citrulline dan NH 3 serta enzim citrulline ureidase yang dapat mengubah citrulline menjadi ornithine, CO 2 dan NH 3. Reaksi yang terjadi adalah reaksi alkalin dari produksi NH 3 yang terlihat melalui uji ini (Thornley 1960). a b Gambar 8 Reaksi positif bakteri uji (b) pada uji arginine dihydrolase dibandingkan kontrol (a). Berdasarkan uji LOPAT yang dilakukan pada bakteri Pseudomonas sp. maka dapat diketahui bahwa spesies bakteri rizosfer pada tanaman pepaya IPB 1, IPB 2, dan IPB 6 tersebut adalah P. fluorescens bukan patogen (Brown JF et al 1980).
27 17 8. Hasil uji pertumbuhan pada media YDC (33 0 C) Hasil isolasi pada 21 isolat bakteri, 5 isolat yang masing-masing menunjukkan koloni berwarna kuning pada media NA. Dari 5 isolat tersebut hanya 3 isolat yang dapat tumbuh pada media YDC yang diinkubasi pada suhu 33 0 C. Media YDC merupakan media semiselektif untuk pertumbuhan bakteri Xanthomonas sp. Dari pengujian ini dapat disimpulkan bahwa ketiga bakteri yang di uji adalah Xanthomonas sp (lampiran 1). Berdasarkan pengujian ini 3 isolat bakteri masing-masing dari pertanaman pepaya IPB 1, IPB 2 dan IPB 6 yang bersifat fermentatif dengan koloni warna kuning tumbuh pada media YDC diidentifikasi sebagai bakteri Pantoea sp (lampiran 1). Gambar 9 Reaksi positif pada media YDC berupa koloni berwarna kuning 9. Hasil uji pertumbuhan pada media D1M agar Berdasarkan hasil pengujian pada semua isolat bakteri, 2 isolat bakteri masing-masing dari pertanaman IPB 1 dan IPB 6 dapat tumbuh pada media D1M agar. Reaksi positif yaitu tumbuhnya bakteri pada media ini menunjukkan bahwa bakteri tersebut adalalah Agrobacterium sp. Media D1M ialah media semiselektif bagi bakteri tersebut (lampiran 1). 10. Hasil uji reaksi hipersensitif Berdasarkan hasil pengamatan dan pengujian 21 isolat bakteri, 3 isolat masing-masing dari pertanaman pepaya IPB 1, IPB 2, dan IPB 6 menujukkan reaksi positif yaitu munculnya gejala nekrosis. Hal ini menunjukkan bahwa bakteri tersebut bersifat patogen. Salah satu reaksi tanaman terhadap serangan patogen adalah berupa
28 18 reaksi kematian yang cepat pada jaringan yang diserang. Reaksi ini dapat dilihat dari gejala berupa nekrosis pada jaringan tanaman yang diserang, dalam hal ini daun tembakau yang diinokulasikan. Gejala muncul pada 24 sampai 48 jam setelah inokulasi. Gambar 10 Reaksi positif uji hipersensitif pada daun tembakau berupa gejala nekrosis. Keragaman Mikroorganisme Rizosfer Berdasarkan hasil identifikasi pertanaman pepaya IPB 1, IPB 2, dan IPB 6 diperoleh mikroorganisme rizosfer berupa bakteri dan cendawan. Bakteri yang berhasil diidentifikasi yaitu P. fluorescens, Xanthomonas sp, Erwinia sp, Pantoea sp. Agrobacterium sp dan lima isolat bakteri Gram-positif. P. fluorescens. berbentuk batang lurus atau lengkung, selnya berukuran µm x µm, tidak membentuk spora dan bereaksi negatif terhadap pewarnaan Gram. Bakteri ini ada yang dapat dimanfaatkan sebagai agen pengendali hayati karena mempunyai sifat antagonisme terhadap patogen tular tanah. Xanthomonas sp. merupakan bakteri berbentuk batang, pendek, berukuran 1-2 x 0.3-0,5 µm, tidak membentuk rantai, tidak berspora, dan tidak berkapsul. Bakteri ini dapat bergerak menggunakan flagellumnya yang tunggal dan polar. Pada media NA koloni bakteri ini bundar, cembung, halus mengkilat dan berwarna kuning, bersifat aerobik, Gram-negatif, dan dapat mengoksidasi glukosa sehingga pada media Levan koloninya berlendir. Selain itu Xanthomonas sp. hasil isolasi pada pertanaman pepaya IPB 1, IPB 2, dan IPB 6 tidak bersifat patogen. Hal ini diketahui dari reaksi negatif pada daun tembakau yang diinokulasi tidak menunjukkan gejala nekrosis saat uji hipersensitif.
29 19 Bakteri Erwinia sp. berbentuk batang, mempunyai bulu cambuk, tidak membentuk spora dan kapsul, Gram-negatif, serta bersifat fermentatif. Erwinia sp. dapat tumbuh pada kisaran suhu yang luas yaitu antara 22 0 C dan 37 0 C. Bakteri tersebut menghasilkan enzim pektinase yang dapat menguraikan pektin (fungsi pektin adalah untuk merekatkan dinding sel tumbuhan), dengan terurainya pektin sel akan terlepas satu sama lain (Agrios 1988). Pantoea sp termasuk bakteri Gram-negatif, bersifat fermentatif dengan koloni warna kuning tumbuh pada media YDC. Agrobacterium sp. merupakan bakteri Gram-negatif, bakteri ini bersifat bukan patogen yang terlihat dari reaksi negatif pada uji hipersensitif. Berdasarkan uji dalam penelitian ini diketahui bahwa keberadaan bakteri Agrobacterium sp. tidak memberikan dampak negatif pada pertanaman pepaya. Tabel 2 Hasil identifikasi bakteri dan cendawan pada eksplorasi rizosfer tanaman pepaya IPB 1, IPB 2, dan IPB 6. Jenis Mikroorganisme Tanah Pepaya IPB 1 Tanah pepaya IPB 2 Tanah pepaya IPB 6 Bakteri P. fluorescens. P. fluorescens P. fluorescens. Xanthomonas sp. Xanthomonas sp. Xanthomonas sp. Erwinia sp. Erwinia sp. Erwinia sp. Pantoea sp. Pantoea sp. Pantoea sp. Agrobacterium sp - Agrobacterium sp. Bakteri Gram-positif Bakteri Gram-positif Bakteri Gram-positif Cendawan A. fumigatus A. fumigatus A. fumigatus A. flavus A. flavus Aspergillus sp. Penicillium sp. Aspergillus sp. Penicillium sp. Trichoderma sp. Trichoderma sp. Cendawan yang berhasil diindentifikasi dari pertanaman pepaya IPB 1, IPB 2, dan IPB 6 adalah Aspergillus sp, A. fumigatus, A. flavus, Penicillium sp., dan Trichoderma sp. Aspergillus sp. merupakan cendawan yang termasuk dalam kelas Deuteromycetes. Cendawan tersebut memiliki hifa septat (bersekat) dengan konidium berbentuk bulat, dan memiliki sel kaki (sel hifa bercabang) yang menyangga sel konidiofornya. Penicillium sp. merupakan cendawan yang termasuk dalam kelas
30 20 Deuteromycetes, memiliki konidium bulat dan konidiofor bertangkai tunggal yang berakhir pada rangkaian fialid yang membentuk struktur seperti sikat atau sapu lidi. Cendawan Trichoderma sp. memiliki hifa septat, dengan ciri khas fialid yang bercabang tiga, ujung fialidnya menghasilkan konidium bergerombol dan termasuk dalam kelas Deuteromycetes. Berdasarkan hasil penelitian ini cendawan dan bakteri yang ditemukan dari masing-masing lahan pertanaman pepaya hampir sama. Hal ini disebabkan pertanaman pepaya ditanam dengan jarak berdekatan yaitu pada satu lokasi perkebunan dengan perlakuan yang diberikan petani sama misalnya aplikasi pupuk dan pestisida.
31 21 KESIMPULAN DAN SARAN Kesimpulan Pada lahan pertanaman pepaya IPB 1, IPB 2, dan IPB 6 terdapat keragaman mikroorganisme bakteri dan cendawan. Bakteri yang berhasil diidentifikasi adalah P. fluorescens, Xanthomonas sp., Erwinia sp., Pantoea sp., Agrobacterium sp. dan lima isolat bakteri Gram-positif. Cendawan yang berhasil diindentifikasi dari pertanaman pepaya IPB 1, IPB 2, dan IPB 6 adalah Aspergillus fumigatus, Aspergillus flavus, Penicillium sp., Trichoderma sp., dan Aspergillus sp. Saran Perlu dilakukan penelitian lanjutan untuk mengetahui peranan masingmasing mikroorganisme rizosfer yang diperoleh. Informasi ini penting untuk mengetahui mikroorganisme yang dapat bersifat antagonis, pemacu pertumbuhan, maupun sifat lainnya yang akan membantu dalam pengendalian penyakit.
32 22 DAFTAR PUSTAKA Agrios GN Plant Pathology. 5 th ed. Academic Press Inc. San Diego. 803p. BAPPENAS Budidaya Pertanian [5 Maret 2007]. Baker SK. Cook JR Biological Control of Plant Pathogens. San Fransisco: WH Freeman and Company. Brown JF, Kerr A, Morgan FD, Parbey IH Plant Protection. Australia: Australian Vice-Chancelors Committee. Carlile MJ, Watkinson SC, Goodday GW The Fungi. 2 nd. NewYork, London: Academic Press. Domsch KH, Gams W, Anderson TH Compendium of Soil Fungi. Vol I. IHW-Velag. Evayani L Siklus hidup tungau Tetranychus cinnabarinus (boisd.) (Acarina: Tetranychidae) pada daun muda dan daun tua tanaman pepaya [skripsi]. Bogor: Institut Pertanian Bogor, Fakultas Pertanian. Foster RC The Biology of the rhizosphere. In: Parker CA, Rovira AD, More KJ, Wong PTW, Kollmorgen JF, editors. Ecology And Management of Soilborne Plant Pathogens, Prosiding 1 st and 5 st International Congress of Plant Pathology, Australia, and August 1983.Minnesota (USA): The American Phytopathologycal Society. Gunawan AW, Dharmaputra OS, Rahayu G Cendawan Dalam Praktik Laboratorium. Bogor: IPB Press. Hornbyn D Root diseases. In Lynch JM, editor. The Rhizosphere. New York: John Willey & Sons. Jeger MJ Biotic interaction and plant-pathogen association. In: Jeger MJ, Spence NJ. Biotic Interaction in Plant. Pathogen Association. New York (USA): CABL publishing. Lynch JM Introduction: Some consequences of microbial rhizosphere competence for plant and soil. In : Lynch JM, editors. The Rhizosphere New York: John Willey & Sons. P Ou SH Rice Diseases. Commonwealth Mycologycal Institute. Kew Surrey, England. p
33 23 Patkowska E The Role of Rhizosphere Antagonistic Microorganism in Limiting the Infection of Underground Part of Spring Wheat. www. ejpau. media. Pl /series/ volume/ 5/ issue 2/ horticultura/ art-04. html.[16 Februari 2008]. Schaad NW, Jones JB, Chun W Laboratory Guide for Identification of Plant Pathogenic Bacteria. 3 nd. Minnesota: APS Press. Semangun H Penyakit-penyakit Tanaman Hortikultura di Indonesia. Gadjah Mada. Univ. Press. Yogyakarta. 85 hal. Stainer RY, Adelberg EA, Ingraham J Dunia Mikroba 2. Jakarta: Bharata Karya Aksara. Senior Getah Pepaya Atasi Kanker. =cybermed%7c1%7c0%7c3%7c96. [09 November 2006]. Sriyanti W Pengamatan Hama dan Penyakit Pepaya (Carica papaya L.) di Kebun Pusat Kajian Buah-Buahan Tropika (PKBT) IPB, Bogor [skripsi]. Bogor: Institut Pertanian Bogor, Fakultas Pertanian. Thornley MJ The differentiation of Pseudomonas from other Gramnegative bacteria on the basis arginine metabolism. Journal Appl. Bacteriology 1: Waksman SA Soil Microbiology. New York : John Willey & Sons. 237p. Warisno Budidaya Pepaya. Yogyakarta: Kanisius. Watanabe T Pictorial Atlas of Soil and Seed Fungi Morphological of Cultured Fungi and Key to Species. Lewis Publisher Domsch KH et al. (1993).
34 24 Lampiran 1 Komposisi bahan untuk isolasi dan identifikasi bakteri. Tabel 1 Komposisi bahan media NA (Nutrient Agar) No. Bahan Jumlah 1. Beef ekstact 3.0 g 2. Pepton 5.0 g 3. Glukosa 2.5 g 4. Agar 15 g 5. Aquades 1.0 liter Tabel 2 Komposisi bahan media Potato Dextrose Agar (PDA) No. Bahan Jumlah 1. Kentang 200 g 2. Dextrose 20 g 3. Agar 15 g 4. Aquades 1.0 liter Tabel 3 Komposisi bahan media Martin Agar (MA) No. Bahan Jumlah 1. Pepton 20.0 g 2. Dextrose 10.0 g 3. KH 2 PO 4.7H 2 O 1.0 g 4. MgSO 4.7H 2 O 0.5 g 5. Rose bengal 1% 3,3 ml 6. Agar 20.0 g 7. Aquades 1.0 liter 8. Streptomycin 50 mg/liter Tabel 4 Komposisi bahan media Oksidase No. Bahan Jumlah 1. Tetramethylparaphenylenediamine dihydrochloride 1%
35 25 Tabel 5 Komposisi bahan media Uji Gram No. Bahan Jumlah 1. KOH 3% Tabel 6 Komposisi bahan media King s B No. Bahan Jumlah 1. Protease pepton no g 2. Glycerol 10.0 ml 3. K 2 HPO g 4. MgSO 4.7H 2 O 1.5 g 5. Agar 15.0 g 6. Aquades 1.0 liter Tabel 7 Komposisi bahan media Yeast Dextrose Agar (Lelliot & Stead 1978) No. Bahan Jumlah 1. Yeast Extract 10.0 g 2. D-glucose 20.0 g 3. CaCO g 4. Aquades 1.0 liter Tabel 8 Komposisi bahan media Oksidatif/fermentatif No. Bahan Jumlah 1. Pepton 1.0 g 2. NH 4 H 2 PO g 3. KCl 0.2 g 4. MgSO 4.7H 2 O 0.2 g 5. Bromtimol biru 40.0 g 6. Agar 1.5 g 7. Aquades 1.0 liter
36 26 Tabel 9 Komposisi bahan media Levan No. Bahan Jumlah 1. Nutrient Broth 8.0 g 2. Sucrose 50 g 3. Agar 20 g 4. Aquades 1 liter Tabel 10 Komposisi bahan media Arginine Dihydrolase (Lelliot & Stead 1978) No. Bahan Jumlah 1. Pepton 1.0 g 2. NaCl 5.0 g 3. K 2 HPO g 4. L (+) arginin HCl 10.0 g 5. Phenol red 0.01 g 6. Agar 3.0 g 7. Aquades 1.0 g Tabel 11 Komposisi bahan media D1M Agar No. Bahan Jumlah 1. Cellobiose 5.0 g 2. NH 4 Cl 1.0 g 3. NH 4 H 2 PO g 4. K 2 HPO g 5. MgSO 4.7H 2 O 3.0 g 6. Malachite green 10.0 mg 7. Agar 15.0 g 8. Aquades 1.0 liter
37 Lampiran 2 Kunci identifikasi bakteri (Schaad et al. 2001) - Erwinia, Pantoea, Xylophilus, Acidovorax, Burkholderia, Ralstonia, Pseudomonas, Xanthomonas, Agrobacterium. Gram Reaction Corynebacterium, Bacillus, Clostridium + + Erwinia Pantoea Anaerobic Growth - Xylophilus, Acidovorax, Burkholderia, Ralstonia, Pseudomonas, Xanthomonas,,Agrobacterium. + Bacillus, Clostridium Endospored Formed - Coryneform, Streptomyces Colonies Yellow + on YDC - Pantoea Erwinia Fluorescent Pigment on KB + Pseudomonas Xylophilus, Acidovorax, Burkholderia, Ralstonia, Pseudomonas, Xanthomonas, Agrobacterium. - Anaerobic Growth Aerial Mycellium Clostridium Bacillus Streptomyces + Colonies Yellow on YDC/NA - Corynebacterium 27
38 Kunci Identifikasi bakteri (lanjutan) Collonies Yellow on YDC/NA Xanthomonas, Xylophilus Agrobacterium, Acidovorax, Burkholderia, Ralstonia + Urease Growth at 33 ºC on YDC Growth on D1M Agar Xylophilus Xanthomonas Xanthomonas Xylophilus Agrobacterium Acidovorax, Burkholderia,Ralstonia + Utilizes Arginine and Betaine - Burkholderia Ralstonia, Acidovorax + Growth at 40 ºC - Acidovorax Ralstonia 28
39 - Gram Reaction + - Gram Reaction + Anaerobic Growth - Flourescent Pigment on KB + Pseudomonas Anaerobic Growth - Flourescent Pigment on KB - + Colonies Yellow on YDC/NA Levan Oksidase (-) (+) Potat o (-) Arginine (+) + Growth at 33 ºC on YDC Pseudomonas flourescens Xantomonas sp. 29
40 - Gram Reaction + - Gram Reaction + Anaerobic Growth + - Flourescent Pigment on KB + - Collonies Yellow on YDC/NA - Growth on D1M Agar + Corynebacterium, Bacillus, Clostridium Endospored Formed + - Anaerobic Growth + - Bacillus sp. Agrobacterium 30
BAHAN DAN METODE Tempat dan Waktu Penelitian Bahan dan Alat Metode Penelitian Pra-pengamatan atau survei
 BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilaksanakan di Kebun Percobaan Pusat Kajian Buah-Buahan Tropika IPB (PKBT-IPB) Pasir Kuda, Desa Ciomas, Bogor, dan Laboratorium Bakteriologi Tumbuhan,
BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilaksanakan di Kebun Percobaan Pusat Kajian Buah-Buahan Tropika IPB (PKBT-IPB) Pasir Kuda, Desa Ciomas, Bogor, dan Laboratorium Bakteriologi Tumbuhan,
HASIL DAN PEMBAHASAN
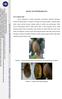 10 HASIL DAN PEMBAHASAN Survei Buah Sakit Survei dilakukan di kebun percobaan Leuwikopo, Fakultas Pertanian, Institut Pertanian Bogor, di lahan ini terdapat 69 tanaman pepaya. Kondisi lahan tidak terawat
10 HASIL DAN PEMBAHASAN Survei Buah Sakit Survei dilakukan di kebun percobaan Leuwikopo, Fakultas Pertanian, Institut Pertanian Bogor, di lahan ini terdapat 69 tanaman pepaya. Kondisi lahan tidak terawat
BAHAN DAN METODE Tempat dan Waktu . Bahan dan Alat Metode Penelitian Survei Buah Pepaya Sakit
 5 BAHAN DAN METODE Tempat dan Waktu Penelitian dilaksanakan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman dan Kebun Percobaan Leuwikopo, Fakultas Pertanian, Institut Pertanian Bogor.
5 BAHAN DAN METODE Tempat dan Waktu Penelitian dilaksanakan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman dan Kebun Percobaan Leuwikopo, Fakultas Pertanian, Institut Pertanian Bogor.
EKSPLORASI BAKTERI DAN CENDAWAN RIZOSFER YANG BERASOSIASI DENGAN PENYAKIT BUSUK BASAH PADA BATANG PEPAYA
 EKSPLORASI BAKTERI DAN CENDAWAN RIZOSFER YANG BERASOSIASI DENGAN PENYAKIT BUSUK BASAH PADA BATANG PEPAYA (Carica papaya L.) DI PASIR KUDA, DESA CIOMAS, BOGOR ANGGIE FERFINIA DEPARTEMEN PROTEKSI TANAMAN
EKSPLORASI BAKTERI DAN CENDAWAN RIZOSFER YANG BERASOSIASI DENGAN PENYAKIT BUSUK BASAH PADA BATANG PEPAYA (Carica papaya L.) DI PASIR KUDA, DESA CIOMAS, BOGOR ANGGIE FERFINIA DEPARTEMEN PROTEKSI TANAMAN
Gambar 1 Tanaman uji hasil meriklon (A) anggrek Phalaenopsis, (B) bunga Phalaenopsis yang berwarna putih
 BAHAN DAN METODE Tempat dan Waktu Penelitian Isolasi dan perbanyakan sumber inokulum E. carotovora dilakukan di Laboratorium Bakteriologi Departemen Proteksi Tanaman Fakultas Pertanian, Institut Pertanian
BAHAN DAN METODE Tempat dan Waktu Penelitian Isolasi dan perbanyakan sumber inokulum E. carotovora dilakukan di Laboratorium Bakteriologi Departemen Proteksi Tanaman Fakultas Pertanian, Institut Pertanian
KARAKTERISTIK PENYEBAB PENYAKIT LAYU BAKTERI PADA TANAMAN TEMBAKAU DI PROBOLINGGO
 KARAKTERISTIK PENYEBAB PENYAKIT LAYU BAKTERI PADA TANAMAN TEMBAKAU DI PROBOLINGGO Pendahuluan Tembakau merupakan salah satu komoditas perkebunan yang strategis dan memiliki nilai ekonomi cukup tinggi.
KARAKTERISTIK PENYEBAB PENYAKIT LAYU BAKTERI PADA TANAMAN TEMBAKAU DI PROBOLINGGO Pendahuluan Tembakau merupakan salah satu komoditas perkebunan yang strategis dan memiliki nilai ekonomi cukup tinggi.
POTENSI CENDAWAN RHIZOSFER DALAM MENGINDUKSI KETAHANAN TANAMAN
 POTENSI CENDAWAN RHIZOSFER DALAM MENGINDUKSI KETAHANAN TANAMAN Jumriani Rusli & Hafsan Jurusan Biologi, Fakultas Sains dan Teknologi Universitas Islam Negeri Alauddin Makassar PENDAHULUAN A. Latar Belakang
POTENSI CENDAWAN RHIZOSFER DALAM MENGINDUKSI KETAHANAN TANAMAN Jumriani Rusli & Hafsan Jurusan Biologi, Fakultas Sains dan Teknologi Universitas Islam Negeri Alauddin Makassar PENDAHULUAN A. Latar Belakang
BAHAN DAN METODE. Pembiakan P. fluorescens dari Kultur Penyimpanan
 BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilaksanakan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor mulai bulan Februari
BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilaksanakan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor mulai bulan Februari
BAHAN DAN METODE. Tempat dan Waktu
 15 BAHAN DAN METODE Tempat dan Waktu Penelitian dilaksanakan di laboratorium dan rumah kaca Hama dan Penyakit dan rumah kaca Balai penelitian Tanaman Obat dan Aromatik (BALITTRO), Bogor; pada bulan Oktober
15 BAHAN DAN METODE Tempat dan Waktu Penelitian dilaksanakan di laboratorium dan rumah kaca Hama dan Penyakit dan rumah kaca Balai penelitian Tanaman Obat dan Aromatik (BALITTRO), Bogor; pada bulan Oktober
III. BAHAN DAN METODE. Penelitian ini dilaksanakan pada bulan Juli sampai dengan Desember 2014.
 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan pada bulan Juli sampai dengan Desember 2014. Isolasi dan karakterisasi penyebab penyakit dilakukan di Laboratorium Penyakit
III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan pada bulan Juli sampai dengan Desember 2014. Isolasi dan karakterisasi penyebab penyakit dilakukan di Laboratorium Penyakit
EKSPLORASI BAKTERI DAN CENDAWAN RIZOSFER YANG BERASOSIASI DENGAN PENYAKIT BUSUK BASAH PADA BATANG PEPAYA
 EKSPLORASI BAKTERI DAN CENDAWAN RIZOSFER YANG BERASOSIASI DENGAN PENYAKIT BUSUK BASAH PADA BATANG PEPAYA (Carica papaya L.) DI PASIR KUDA, DESA CIOMAS, BOGOR ANGGIE FERFINIA DEPARTEMEN PROTEKSI TANAMAN
EKSPLORASI BAKTERI DAN CENDAWAN RIZOSFER YANG BERASOSIASI DENGAN PENYAKIT BUSUK BASAH PADA BATANG PEPAYA (Carica papaya L.) DI PASIR KUDA, DESA CIOMAS, BOGOR ANGGIE FERFINIA DEPARTEMEN PROTEKSI TANAMAN
III BAHAN DAN METODE
 meliputi daerah Jawa, Kalimantan dan Sumatera. Tanaman Kilemo di daerah Jawa banyak ditemui pada daerah dengan ketinggian 230 700 meter di atas permukaan laut (mdpl). Tanaman ini terutama banyak ditemui
meliputi daerah Jawa, Kalimantan dan Sumatera. Tanaman Kilemo di daerah Jawa banyak ditemui pada daerah dengan ketinggian 230 700 meter di atas permukaan laut (mdpl). Tanaman ini terutama banyak ditemui
BAHAN DAN METODE. Tabel 1 Kombinasi perlakuan yang dilakukan di lapangan
 13 BAHAN DAN METODE Tempat dan waktu Penelitian ini dilaksanakan di Desa Ciburuy, Kecamatan Cigombong, Kabupaten Bogor serta di Laboratorium Bakteriologi, Departemen Proteksi Tanaman, Fakultas Pertanian,
13 BAHAN DAN METODE Tempat dan waktu Penelitian ini dilaksanakan di Desa Ciburuy, Kecamatan Cigombong, Kabupaten Bogor serta di Laboratorium Bakteriologi, Departemen Proteksi Tanaman, Fakultas Pertanian,
BAHAN DAN METODE Tempat dan waktu penelitian Bahan dan Alat Isolasi dan Uji Reaksi Hipersensitif Bakteri Penghasil Siderofor
 BAHAN DAN METODE Tempat dan waktu penelitian Penelitian dilaksanakan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor, dari Oktober 2010
BAHAN DAN METODE Tempat dan waktu penelitian Penelitian dilaksanakan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor, dari Oktober 2010
BAHAN DAN METODE. Metode Penelitian
 BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilakukan di Laboratorium Bakteriologi Tumbuhan dan Rumah Kaca University Farm, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian
BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilakukan di Laboratorium Bakteriologi Tumbuhan dan Rumah Kaca University Farm, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian
HASIL DAN PEMBAHASAN Isolasi dan Inokulasi Penyebab Busuk Lunak Karakterisasi Bakteri Penyebab Busuk Lunak Uji Gram
 HASIL DAN PEMBAHASAN Isolasi dan Inokulasi Penyebab Busuk Lunak Isolasi daun anggrek yang bergejala busuk lunak dihasilkan 9 isolat bakteri. Hasil uji Gram menunjukkan 4 isolat termasuk bakteri Gram positif
HASIL DAN PEMBAHASAN Isolasi dan Inokulasi Penyebab Busuk Lunak Isolasi daun anggrek yang bergejala busuk lunak dihasilkan 9 isolat bakteri. Hasil uji Gram menunjukkan 4 isolat termasuk bakteri Gram positif
BAHAN DAN METODE Tempat dan Waktu Bahan Peremajaan Aktinomiset dari Kultur Penyimpanan Perbanyakan Sclerotium rolfsii dari Kultur Penyimpanan
 BAHAN DAN METODE Tempat dan Waktu Penelitian dilaksanakan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor (IPB) mulai Maret 2011 sampai
BAHAN DAN METODE Tempat dan Waktu Penelitian dilaksanakan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor (IPB) mulai Maret 2011 sampai
III. BAHAN DAN METODE. Penelitian ini dilaksanakan di Laboratorium Bioteknologi Fakultas Pertanian
 9 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Bioteknologi Fakultas Pertanian Universitas Lampung sejak Juli sampai dengan September 2015. Pengambilan
9 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Bioteknologi Fakultas Pertanian Universitas Lampung sejak Juli sampai dengan September 2015. Pengambilan
BAHAN DAN METODE Tempat dan Waktu Penelitian Wawancara Pengamatan dan Pengambilan Contoh
 21 BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilakukan di enam perkebunan buah naga di Provinsi Daerah Istimewa Yogyakarta yang terdiri dari tiga kabupaten. Kebun pengamatan di Kabupaten
21 BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilakukan di enam perkebunan buah naga di Provinsi Daerah Istimewa Yogyakarta yang terdiri dari tiga kabupaten. Kebun pengamatan di Kabupaten
BAHAN DAN METODE Tempat dan Waktu Penelitian Bahan dan Alat Metode Penelitian Penyiapan tanaman uji
 BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilakukan pada bulan Juli 2010 Maret 2011. Penelitian dilakukan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian,
BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilakukan pada bulan Juli 2010 Maret 2011. Penelitian dilakukan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian,
III. BAHAN DAN METODE. Penelitian ini dilaksanakan pada bulan Juli sampai bulan November 2009, di
 III. BAHAN DAN METODE A. Tempat dan Waktu Penelitian Penelitian ini dilaksanakan pada bulan Juli sampai bulan November 2009, di Laboratorium Kesuburan Tanah, dan Laboratorium Bioteknologi Pertanian Fakultas
III. BAHAN DAN METODE A. Tempat dan Waktu Penelitian Penelitian ini dilaksanakan pada bulan Juli sampai bulan November 2009, di Laboratorium Kesuburan Tanah, dan Laboratorium Bioteknologi Pertanian Fakultas
EKSPLORASI Pseudomonad fluorescens DARI PERAKARAN GULMA PUTRI MALU (Mimosa invisa)
 EKSPLORASI Pseudomonad fluorescens DARI PERAKARAN GULMA PUTRI MALU (Mimosa invisa) A. Pendahuluan Pseudomonad fluorescens merupakan anggota kelompok Pseudomonas yang terdiri atas Pseudomonas aeruginosa,
EKSPLORASI Pseudomonad fluorescens DARI PERAKARAN GULMA PUTRI MALU (Mimosa invisa) A. Pendahuluan Pseudomonad fluorescens merupakan anggota kelompok Pseudomonas yang terdiri atas Pseudomonas aeruginosa,
LAPORAN PRAKTIKUM HAMA DAN PENYAKIT TANAMAN TAHUNAN PENYAKIT PADA KOMODITAS PEPAYA. disusun oleh: Vishora Satyani A Listika Minarti A
 LAPORAN PRAKTIKUM HAMA DAN PENYAKIT TANAMAN TAHUNAN PENYAKIT PADA KOMODITAS PEPAYA disusun oleh: Lutfi Afifah A34070039 Vishora Satyani A34070024 Johan A34070034 Listika Minarti A34070071 Dosen Pengajar:
LAPORAN PRAKTIKUM HAMA DAN PENYAKIT TANAMAN TAHUNAN PENYAKIT PADA KOMODITAS PEPAYA disusun oleh: Lutfi Afifah A34070039 Vishora Satyani A34070024 Johan A34070034 Listika Minarti A34070071 Dosen Pengajar:
Haris Dianto Darwindra BAB VI PEMBAHASAN
 Haris Dianto Darwindra BAB VI PEMBAHASAN Berbagai jenis makanan dan minuman yang dibuat melalui proses fermentasi telah lama dikenal. Dalam prosesnya, inokulum atau starter berperan penting dalam fermentasi.
Haris Dianto Darwindra BAB VI PEMBAHASAN Berbagai jenis makanan dan minuman yang dibuat melalui proses fermentasi telah lama dikenal. Dalam prosesnya, inokulum atau starter berperan penting dalam fermentasi.
III. BAHAN DAN METODE
 10 III. BAHAN DAN METODE 3.1 Waktu dan Tempat Penelitian dilaksanakan dari bulan Oktober 2011 sampai Oktober 2012. Sampel gubal dan daun gaharu diambil di Desa Pulo Aro, Kecamatan Tabir Ulu, Kabupaten
10 III. BAHAN DAN METODE 3.1 Waktu dan Tempat Penelitian dilaksanakan dari bulan Oktober 2011 sampai Oktober 2012. Sampel gubal dan daun gaharu diambil di Desa Pulo Aro, Kecamatan Tabir Ulu, Kabupaten
BAHAN DAN METODE. Pengambilan sampel tanaman nanas dilakukan di lahan perkebunan PT. Great
 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Pengambilan sampel tanaman nanas dilakukan di lahan perkebunan PT. Great Giant Pineapple (GGP) di Lampung Timur dan PT. Nusantara Tropical Farm, Lampung
III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Pengambilan sampel tanaman nanas dilakukan di lahan perkebunan PT. Great Giant Pineapple (GGP) di Lampung Timur dan PT. Nusantara Tropical Farm, Lampung
BAHAN DAN METODE Waktu dan Tempat Penelitian Bahan Penelitian Metode Penelitian Isolasi dan Identifikasi Cendawan Patogen
 14 BAHAN DAN METODE Waktu dan Tempat Penelitian Percobaan dilaksanakan dari bulan Maret sampai bulan Juli 2012 di Laboratorium Mikologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut
14 BAHAN DAN METODE Waktu dan Tempat Penelitian Percobaan dilaksanakan dari bulan Maret sampai bulan Juli 2012 di Laboratorium Mikologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut
BAHAN DAN METODE. Metode Penelitian
 BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilaksanakan di Laboratorium Mikologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor, dari bulan Februari sampai
BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilaksanakan di Laboratorium Mikologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor, dari bulan Februari sampai
BAHAN DAN METODE. Pertanian Universitas Sumatera Utara, Medan dengan ketinggian tempat + 25
 BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Penyakit Tumbuhan Fakultas Pertanian, Medan dengan ketinggian tempat + 25 meter di atas permukaan laut pada bulan
BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Penyakit Tumbuhan Fakultas Pertanian, Medan dengan ketinggian tempat + 25 meter di atas permukaan laut pada bulan
III. BAHAN DAN METODE
 III. BAHAN DAN METODE 3.1. Tempat dan Waktu Penelitian ini telah dilaksanakan di Laboratorium Penyakit Tumbuhan Fakultas Pertanian Universitas Riau, Pekanbaru yang berlangsung selama 4 bulan, dimulai dari
III. BAHAN DAN METODE 3.1. Tempat dan Waktu Penelitian ini telah dilaksanakan di Laboratorium Penyakit Tumbuhan Fakultas Pertanian Universitas Riau, Pekanbaru yang berlangsung selama 4 bulan, dimulai dari
BAB 2 TINJAUAN PUSTAKA
 BAB 2 TINJAUAN PUSTAKA 2.1 Kitin dan Bakteri Kitinolitik Kitin adalah polimer kedua terbanyak di alam setelah selulosa. Kitin merupakan komponen penyusun tubuh serangga, udang, kepiting, cumi-cumi, dan
BAB 2 TINJAUAN PUSTAKA 2.1 Kitin dan Bakteri Kitinolitik Kitin adalah polimer kedua terbanyak di alam setelah selulosa. Kitin merupakan komponen penyusun tubuh serangga, udang, kepiting, cumi-cumi, dan
III. BAHAN DAN METODE. Penelitian ini dilaksanakan di Laboratorium Penyakit Tanaman dan Laboratorium
 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Penyakit Tanaman dan Laboratorium Lapangan Terpadu Fakultas Pertanian Universitas Lampung pada bulan November
III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Penyakit Tanaman dan Laboratorium Lapangan Terpadu Fakultas Pertanian Universitas Lampung pada bulan November
HASIL DAN PEMBAHASAN Keadaan Umum Lokasi Isolasi Cendawan Rizosfer
 10 HASIL DAN PEMBAHASAN Keadaan Umum Lokasi Lokasi pengambilan sampel berada di dua tempat yang berbeda : lokasi pertama, Kabupaten Bogor. Kabupaten Bogor memiliki ketinggian + 400 m dpl (diatas permukaan
10 HASIL DAN PEMBAHASAN Keadaan Umum Lokasi Lokasi pengambilan sampel berada di dua tempat yang berbeda : lokasi pertama, Kabupaten Bogor. Kabupaten Bogor memiliki ketinggian + 400 m dpl (diatas permukaan
BAB III METODE PENELITIAN. Biologi, Fakultas Sains dan Teknologi, Universitas Airlangga Surabaya dan
 BAB III METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Mikrobiologi Departemen Biologi, Fakultas Sains dan Teknologi, Universitas Airlangga Surabaya dan kumbung
BAB III METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Mikrobiologi Departemen Biologi, Fakultas Sains dan Teknologi, Universitas Airlangga Surabaya dan kumbung
II. TINJAUAN PUSTAKA. Penyakit antraknosa pada tanaman cabai disebabkan oleh tiga spesies cendawan
 5 II. TINJAUAN PUSTAKA 2.1 Penyakit Antraknosa Cabai Penyakit antraknosa pada tanaman cabai disebabkan oleh tiga spesies cendawan Colletotrichum yaitu C. acutatum, C. gloeosporioides, dan C. capsici (Direktorat
5 II. TINJAUAN PUSTAKA 2.1 Penyakit Antraknosa Cabai Penyakit antraknosa pada tanaman cabai disebabkan oleh tiga spesies cendawan Colletotrichum yaitu C. acutatum, C. gloeosporioides, dan C. capsici (Direktorat
BAHAN DAN METODE Waktu dan Tempat Bahan dan Alat Metode Penelitian Penyediaan Isolat Fusarium sp. dan Bakteri Aktivator
 BAHAN DAN METODE Waktu dan Tempat Penelitian ini dilakukan di Laboratorium Mikologi, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor, dan Laboratorium Mikrobiologi dan Kesehatan
BAHAN DAN METODE Waktu dan Tempat Penelitian ini dilakukan di Laboratorium Mikologi, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor, dan Laboratorium Mikrobiologi dan Kesehatan
BAB III METODELOGI PENELITIAN
 BAB III METODELOGI PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada Tanggal 01 Februari 31 Juni 2011 di Laboratorium Mikrobiologi dan Rumah Kaca Balai Penelitian Tanaman Kacangkacangan
BAB III METODELOGI PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada Tanggal 01 Februari 31 Juni 2011 di Laboratorium Mikrobiologi dan Rumah Kaca Balai Penelitian Tanaman Kacangkacangan
III. BAHAN DAN METODE. Laboratorium Produksi Perkebunan Fakultas Pertanian Universitas Lampung
 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian dilaksanakan di Rumah Kaca, Laboratorium Produksi Tanaman, dan Laboratorium Produksi Perkebunan Fakultas Pertanian Universitas Lampung mulai
III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian dilaksanakan di Rumah Kaca, Laboratorium Produksi Tanaman, dan Laboratorium Produksi Perkebunan Fakultas Pertanian Universitas Lampung mulai
III. BAHAN DAN METODE. Penelitian ini dilaksanakan di Laboratorium Penyakit Tumbuhan dan Kebun
 17 III. BAHAN DAN MEODE 3.1 empat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Penyakit umbuhan dan ebun Percobaan di dalam kampus di Program Studi Agroteknologi Fakultas Pertanian,
17 III. BAHAN DAN MEODE 3.1 empat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Penyakit umbuhan dan ebun Percobaan di dalam kampus di Program Studi Agroteknologi Fakultas Pertanian,
III. BAHAN DAN METODE PENELITIAN. Percobaan ini dilaksanakan di rumah plastik, dan Laboratorium Produksi
 III. BAHAN DAN METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Percobaan ini dilaksanakan di rumah plastik, dan Laboratorium Produksi Perkebunan Fakultas Pertanian, Universitas Lampung Bandar Lampung,
III. BAHAN DAN METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Percobaan ini dilaksanakan di rumah plastik, dan Laboratorium Produksi Perkebunan Fakultas Pertanian, Universitas Lampung Bandar Lampung,
Haris Dianto Darwindra BAB VI PEMBAHASAN
 BAB VI PEMBAHASAN Praktikum kali ini membahas mengenai isolasi khamir pada cider nanas. Cider merupakan suatu produk pangan berupa minuman hasil fermentasi dengan kandungan alkohol antara 6,5% sampai sekitar
BAB VI PEMBAHASAN Praktikum kali ini membahas mengenai isolasi khamir pada cider nanas. Cider merupakan suatu produk pangan berupa minuman hasil fermentasi dengan kandungan alkohol antara 6,5% sampai sekitar
BAB III METODE PENELITIAN. Mikrobiologi Tanah dan Rumah Kaca Balai Penelitian Tanaman Kacang- kacangan dan Umbiumbian
 BAB III METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian dilaksanakan pada tanggal 01 Februari sampai 31 Mei 2011 di Laboratorium Mikrobiologi Tanah dan Rumah Kaca Balai Penelitian Tanaman
BAB III METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian dilaksanakan pada tanggal 01 Februari sampai 31 Mei 2011 di Laboratorium Mikrobiologi Tanah dan Rumah Kaca Balai Penelitian Tanaman
III. BAHAN DAN METODE. Sampel tanah diambil dari daerah di sekitar risosfer tanaman nanas di PT. Great
 9 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Sampel tanah diambil dari daerah di sekitar risosfer tanaman nanas di PT. Great Giant Pineapple (GGP) Terbanggi Besar, Lampung Tengah dan PT. Nusantara
9 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Sampel tanah diambil dari daerah di sekitar risosfer tanaman nanas di PT. Great Giant Pineapple (GGP) Terbanggi Besar, Lampung Tengah dan PT. Nusantara
BAB III METODE PENELITIAN. eksplorasi dengan cara menggunakan isolasi jamur endofit dari akar kentang
 BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Jenis penelitian ini adalah penelitian eksplorasi dan eksperimen. Penelitian eksplorasi dengan cara menggunakan isolasi jamur endofit dari akar kentang
BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Jenis penelitian ini adalah penelitian eksplorasi dan eksperimen. Penelitian eksplorasi dengan cara menggunakan isolasi jamur endofit dari akar kentang
MENGENAL LEBIH DEKAT PENYAKIT LAYU BEKTERI Ralstonia solanacearum PADA TEMBAKAU
 PEMERINTAH KABUPATEN PROBOLINGGO DINAS PERKEBUNAN DAN KEHUTANAN JL. RAYA DRINGU 81 TELPON 0335-420517 PROBOLINGGO 67271 MENGENAL LEBIH DEKAT PENYAKIT LAYU BEKTERI Ralstonia solanacearum PADA TEMBAKAU Oleh
PEMERINTAH KABUPATEN PROBOLINGGO DINAS PERKEBUNAN DAN KEHUTANAN JL. RAYA DRINGU 81 TELPON 0335-420517 PROBOLINGGO 67271 MENGENAL LEBIH DEKAT PENYAKIT LAYU BEKTERI Ralstonia solanacearum PADA TEMBAKAU Oleh
TINJAUAN PUSTAKA. merata sepanjang tahun. Curah hujan (CH) untuk pertanaman pepaya berkisar
 4 TINJAUAN PUSTAKA Pepaya (Carica papaya L.) Asal-usul Pepaya Pepaya merupakan tanaman buah berupa herba yang diduga berasal dari Amerika Tropis, diantaranya Meksiko dan Nikaragua. Penyebaran tanaman pepaya
4 TINJAUAN PUSTAKA Pepaya (Carica papaya L.) Asal-usul Pepaya Pepaya merupakan tanaman buah berupa herba yang diduga berasal dari Amerika Tropis, diantaranya Meksiko dan Nikaragua. Penyebaran tanaman pepaya
BAB I PENDAHULUAN. Memasuki pasar global, persyaratan produk-produk pertanian ramah
 BAB I PENDAHULUAN 1.1 Latar Belakang Kemajuan ilmu pengetahuan dan penerapan teknologi budidaya tanaman yang dilakukan perlu berorientasi pada pemanfaatan sumber daya alam yang efektif penggunaannya, sehingga
BAB I PENDAHULUAN 1.1 Latar Belakang Kemajuan ilmu pengetahuan dan penerapan teknologi budidaya tanaman yang dilakukan perlu berorientasi pada pemanfaatan sumber daya alam yang efektif penggunaannya, sehingga
PEMERINTAH KABUPATEN PROBOLINGGO
 PEMERINTAH KABUPATEN PROBOLINGGO Jalan Raya Dringu Nomor 81 Telp. (0335) 420517 Fax. (4238210) PROBOLINGGO 67271 POTENSI JAMUR ANTAGONIS Trichoderma spp PENGENDALI HAYATI PENYAKIT LANAS DI PEMBIBITAN TEMBAKAU
PEMERINTAH KABUPATEN PROBOLINGGO Jalan Raya Dringu Nomor 81 Telp. (0335) 420517 Fax. (4238210) PROBOLINGGO 67271 POTENSI JAMUR ANTAGONIS Trichoderma spp PENGENDALI HAYATI PENYAKIT LANAS DI PEMBIBITAN TEMBAKAU
III. METODE PENELITIAN. Persiapan alat dan bahan yang akan digunakan. Pembuatan media PDA (Potato Dextrose Agar)
 III. METODE PENELITIAN A. Bagan Alir Penelitian Persiapan alat dan bahan yang akan digunakan Pembuatan media PDA (Potato Dextrose Agar) Pengambilan sampel tanah dekat perakaran tanaman Cabai merah (C.
III. METODE PENELITIAN A. Bagan Alir Penelitian Persiapan alat dan bahan yang akan digunakan Pembuatan media PDA (Potato Dextrose Agar) Pengambilan sampel tanah dekat perakaran tanaman Cabai merah (C.
III. BAHAN DAN METODE. Penelitian dilakukan pada lahan alang-alang di Kelurahan Segalamider,
 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian dilakukan pada lahan alang-alang di Kelurahan Segalamider, Kecamatan Tanjung Karang Barat, Kota Bandar Lampung. Lokasi percobaan secara
III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian dilakukan pada lahan alang-alang di Kelurahan Segalamider, Kecamatan Tanjung Karang Barat, Kota Bandar Lampung. Lokasi percobaan secara
II. TELAAH PUSTAKA. bio.unsoed.ac.id
 II. TELAAH PUSTAKA Koloni Trichoderma spp. pada medium Malt Extract Agar (MEA) berwarna putih, kuning, hijau muda, dan hijau tua. Trichoderma spp. merupakan kapang Deutromycetes yang tersusun atas banyak
II. TELAAH PUSTAKA Koloni Trichoderma spp. pada medium Malt Extract Agar (MEA) berwarna putih, kuning, hijau muda, dan hijau tua. Trichoderma spp. merupakan kapang Deutromycetes yang tersusun atas banyak
TINJAUAN PUSTAKA. Adapun klasifikasi Colletotrichum gloeosporioides Penz. Sacc. menurut. : Colletotrichum gloeosporioides Penz. Sacc.
 TINJAUAN PUSTAKA Biologi Penyakit Adapun klasifikasi Colletotrichum gloeosporioides Penz. Sacc. menurut Dwidjoseputro (1978) sebagai berikut : Divisio Subdivisio Kelas Ordo Family Genus Spesies : Mycota
TINJAUAN PUSTAKA Biologi Penyakit Adapun klasifikasi Colletotrichum gloeosporioides Penz. Sacc. menurut Dwidjoseputro (1978) sebagai berikut : Divisio Subdivisio Kelas Ordo Family Genus Spesies : Mycota
KAJIAN MIKROBA RIZOSFER DI KAWASAN PERTANIAN ORGANIK KEBUN PERCOBAAN CANGAR PENDAHULUAN
 P R O S I D I N G 51 KAJIAN MIKROBA RIZOSFER DI KAWASAN PERTANIAN ORGANIK KEBUN PERCOBAAN CANGAR Restu Rizkyta Kusuma, Luqman Qurata Aini, dan Luthfiyyah Khoirunnisaa 1) Jurusan Hama dan Penyakit Tumbuhan,
P R O S I D I N G 51 KAJIAN MIKROBA RIZOSFER DI KAWASAN PERTANIAN ORGANIK KEBUN PERCOBAAN CANGAR Restu Rizkyta Kusuma, Luqman Qurata Aini, dan Luthfiyyah Khoirunnisaa 1) Jurusan Hama dan Penyakit Tumbuhan,
BAB I PENDAHULUAN. Teknologi pertanian, khususnya dalam pengendalian penyakit tanaman di
 BAB I PENDAHULUAN A. Latar Belakang Teknologi pertanian, khususnya dalam pengendalian penyakit tanaman di Indonesia masih banyak mengandalkan penggunaan pestisida. Penggunaan pestisida yang tidak bijaksana
BAB I PENDAHULUAN A. Latar Belakang Teknologi pertanian, khususnya dalam pengendalian penyakit tanaman di Indonesia masih banyak mengandalkan penggunaan pestisida. Penggunaan pestisida yang tidak bijaksana
III. BAHAN DAN METODE
 III. BAHAN DAN METODE Penelitian I. Populasi dan Keanekaragaman Cendawan Mikoriza Arbuskular pada Lahan Sayuran dan Semak 3.1 Tempat dan Waktu Penelitian Sampel tanah untuk penelitian ini diambil dari
III. BAHAN DAN METODE Penelitian I. Populasi dan Keanekaragaman Cendawan Mikoriza Arbuskular pada Lahan Sayuran dan Semak 3.1 Tempat dan Waktu Penelitian Sampel tanah untuk penelitian ini diambil dari
BAB I PENDAHULUAN. 1993). Yang dimaksud dengan hama ialah semua binatang yang mengganggu dan
 BAB I PENDAHULUAN 1.1 Latar Belakang Masalah kerusakan tanaman akibat serangan hama menjadi bagian budidaya pertanian sejak manusia mengusahakan pertanian ribuan tahun yang lalu. Mula-mula manusia membunuh
BAB I PENDAHULUAN 1.1 Latar Belakang Masalah kerusakan tanaman akibat serangan hama menjadi bagian budidaya pertanian sejak manusia mengusahakan pertanian ribuan tahun yang lalu. Mula-mula manusia membunuh
III. METODE PENELITIAN. Penelitian dilaksanakan di Laboratorium Penyakit Tumbuhan Jurusan
 14 III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian dilaksanakan di Laboratorium Penyakit Tumbuhan Jurusan Agroteknologi Fakultas Pertanian Universitas Lampung. Pelaksanaan penelitian
14 III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian dilaksanakan di Laboratorium Penyakit Tumbuhan Jurusan Agroteknologi Fakultas Pertanian Universitas Lampung. Pelaksanaan penelitian
METODE PENELITIAN. Penelitian dilaksanakan pada bulan Agustus sampai Februari 2014.
 10 METODE PENELITIAN Waktu dan Tempat Penelitian dilaksanakan pada bulan Agustus sampai Februari 2014. Pengambilan sampel tanah dilakukan di Hutan mangrove Percut Sei Tuan Kabupaten Deli Serdang. Analisis
10 METODE PENELITIAN Waktu dan Tempat Penelitian dilaksanakan pada bulan Agustus sampai Februari 2014. Pengambilan sampel tanah dilakukan di Hutan mangrove Percut Sei Tuan Kabupaten Deli Serdang. Analisis
III. BAHAN DAN METODE. Penelitian ini dilaksanakan di Kebun Percobaan Tanaman Industri dan Penyegar
 25 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Kebun Percobaan Tanaman Industri dan Penyegar Cahaya Negeri, Abung Barat, Lampung Utara dan Laboratorium Penyakit
25 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Kebun Percobaan Tanaman Industri dan Penyegar Cahaya Negeri, Abung Barat, Lampung Utara dan Laboratorium Penyakit
BAHAN DAN METODE. Hrp -, IAA +, BPF Hrp -, IAA + + , BPF Hrp. , BPF Hrp -, IAA +, BPF + Hrp. , BPF Hrp. , BPF Hrp. Penambat Nitrogen Penambat Nitrogen
 BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Mikrobiologi, Departemen Biologi, FMIPA, IPB dan lahan pertanian Kampung Bongkor, Desa Situgede, Karang Pawitan-Wanaraja,
BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Mikrobiologi, Departemen Biologi, FMIPA, IPB dan lahan pertanian Kampung Bongkor, Desa Situgede, Karang Pawitan-Wanaraja,
komersial, pupuk SP 36, pupuk KCl, NaCl, Mannitol, K 2 HPO 4, MgSO 4.7H 2 O,
 BAB III METODOLOGI PENELITIAN 3.1 Waktu dan tempat Penelitian ini dilakukan pada tanggal 01 Februari 31 Juni 2011 di Laboratorium Mikrobiologi, Bioteknologi, Kultur Jaringan dan Rumah Kaca Balai Penelitian
BAB III METODOLOGI PENELITIAN 3.1 Waktu dan tempat Penelitian ini dilakukan pada tanggal 01 Februari 31 Juni 2011 di Laboratorium Mikrobiologi, Bioteknologi, Kultur Jaringan dan Rumah Kaca Balai Penelitian
III. BAHAN DAN METODE. Penelitian dilaksanakan di Laboratorium Ilmu Penyakit Tumbuhan, Bidang
 8 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian dilaksanakan di Laboratorium Ilmu Penyakit Tumbuhan, Bidang Proteksi Tanaman, Jurusan Agroteknologi, Fakultas Pertanian Universitas Lampung
8 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian dilaksanakan di Laboratorium Ilmu Penyakit Tumbuhan, Bidang Proteksi Tanaman, Jurusan Agroteknologi, Fakultas Pertanian Universitas Lampung
IDENTIFIKASI DAN PENANGGULANGAN PENYAKIT PADA BUDIDAYA CABAI MERAH
 IDENTIFIKASI DAN PENANGGULANGAN PENYAKIT PADA BUDIDAYA CABAI MERAH Nurbaiti Pendahuluan Produktifitas cabai di Aceh masih rendah 10.3 ton/ha (BPS, 2014) apabila dibandingkan dengan potensi produksi yang
IDENTIFIKASI DAN PENANGGULANGAN PENYAKIT PADA BUDIDAYA CABAI MERAH Nurbaiti Pendahuluan Produktifitas cabai di Aceh masih rendah 10.3 ton/ha (BPS, 2014) apabila dibandingkan dengan potensi produksi yang
III. METODE PENELITIAN
 III. METODE PENELITIAN A. Materi, Lokasi dan Waktu Penelitian 1. Materi Penelitian a. Bahan Bahan yang digunakan dalam penelitian ini adalah jamur yang memiliki tubuh buah, serasah daun, ranting, kayu
III. METODE PENELITIAN A. Materi, Lokasi dan Waktu Penelitian 1. Materi Penelitian a. Bahan Bahan yang digunakan dalam penelitian ini adalah jamur yang memiliki tubuh buah, serasah daun, ranting, kayu
III. BAHAN DAN METODE
 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian dilaksanakan di Laboratorium Lapang Terpadu dan di Laboratorium Penyakit Tumbuhan, Fakultas Pertanian, Universtitas Lampung dari Desember
III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian dilaksanakan di Laboratorium Lapang Terpadu dan di Laboratorium Penyakit Tumbuhan, Fakultas Pertanian, Universtitas Lampung dari Desember
Volume 5 No. 1 Februari 2017 ISSN:
 IDENTIFIKASI MIKROBA ASAL EKSTRAK BUAH YANG DIAPLIKASIKAN PADA PERTANAMAN JERUK ORGANIK DI KABUPATEN PANGKEP Dian Ekawati Sari e-mail: dianekawatisari@rocketmail.com Program Studi Agroteknologi Fakultas
IDENTIFIKASI MIKROBA ASAL EKSTRAK BUAH YANG DIAPLIKASIKAN PADA PERTANAMAN JERUK ORGANIK DI KABUPATEN PANGKEP Dian Ekawati Sari e-mail: dianekawatisari@rocketmail.com Program Studi Agroteknologi Fakultas
III. BAHAN DAN METODE. Tanaman, serta Laboratorium Lapang Terpadu, Fakultas Pertanian, Universitas
 13 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Hama dan Penyakit Bidang Proteksi Tanaman, serta Laboratorium Lapang Terpadu, Fakultas Pertanian, Universitas
13 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Hama dan Penyakit Bidang Proteksi Tanaman, serta Laboratorium Lapang Terpadu, Fakultas Pertanian, Universitas
LAMPIRAN. Sterilisasi alat dan bahan. Mengisolasi dan Menghitung Populasi Awal dari Bakteri yang Terkandung dalam Biofertilizer komersial
 LAMPIRAN 22 LAMPIRAN Lampiran 1: Bagan Alir Cara Kerja Persiapan alat dan bahan penelitian di laboratorium Sterilisasi alat dan bahan Mengisolasi dan Menghitung Populasi Awal dari Bakteri yang Terkandung
LAMPIRAN 22 LAMPIRAN Lampiran 1: Bagan Alir Cara Kerja Persiapan alat dan bahan penelitian di laboratorium Sterilisasi alat dan bahan Mengisolasi dan Menghitung Populasi Awal dari Bakteri yang Terkandung
bio.unsoed.ac.id III. METODE PENELITIAN
 III. METODE PENELITIAN A. Materi, Lokasi dan Waktu Penelitian 1. Materi Penelitian 1.1. Bahan Materi yang digunakan dalam penelitian ini adalah sampel tanah dari rizosfer tanaman Cabai merah (Capsicum
III. METODE PENELITIAN A. Materi, Lokasi dan Waktu Penelitian 1. Materi Penelitian 1.1. Bahan Materi yang digunakan dalam penelitian ini adalah sampel tanah dari rizosfer tanaman Cabai merah (Capsicum
III. METODE PENELITIAN. Penelitian dilaksanakan pada Oktober 2011 sampai Maret 2012 di Rumah Kaca
 III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian dilaksanakan pada Oktober 2011 sampai Maret 2012 di Rumah Kaca dan di Laboratorium Penyakit Tumbuhan Jurusan Proteksi Tanaman Fakultas Pertanian Universitas
III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian dilaksanakan pada Oktober 2011 sampai Maret 2012 di Rumah Kaca dan di Laboratorium Penyakit Tumbuhan Jurusan Proteksi Tanaman Fakultas Pertanian Universitas
PERAN DAUN CENGKEH TERHADAP PENGENDALIAN LAYU FUSARIUM PADA TANAMAN TOMAT
 ISSN 1411939 PERAN DAUN CENGKEH TERHADAP PENGENDALIAN LAYU FUSARIUM PADA TANAMAN TOMAT Trias Novita Jurusan Budidaya Pertanian Fakultas Pertanian Universitas Jambi Kampus Pinang Masak, Mendalo Darat, Jambi
ISSN 1411939 PERAN DAUN CENGKEH TERHADAP PENGENDALIAN LAYU FUSARIUM PADA TANAMAN TOMAT Trias Novita Jurusan Budidaya Pertanian Fakultas Pertanian Universitas Jambi Kampus Pinang Masak, Mendalo Darat, Jambi
III. BAHAN DAN METODE. Penelitian ini telah dilaksanakan di laboratorium Makanan Ternak, Jurusan
 III. BAHAN DAN METODE A. Tempat dan Waktu Penelitian Penelitian ini telah dilaksanakan di laboratorium Makanan Ternak, Jurusan Peternakan, Fakultas Pertanian, Universitas Lampung dari Januari sampai dengan
III. BAHAN DAN METODE A. Tempat dan Waktu Penelitian Penelitian ini telah dilaksanakan di laboratorium Makanan Ternak, Jurusan Peternakan, Fakultas Pertanian, Universitas Lampung dari Januari sampai dengan
BAHAN DAN METODE. Penelitian dilaksanakan di Laboratorium Penyakit Tumbuhan Jurusan Proteksi
 11 III. BAHAN DAN METODE 3.1 Tempat Penelitian dan Waktu Penelitian dilaksanakan di Laboratorium Penyakit Tumbuhan Jurusan Proteksi Tanaman Fakultas Pertanian Universitas Lampung. Pelaksanaan penelitian
11 III. BAHAN DAN METODE 3.1 Tempat Penelitian dan Waktu Penelitian dilaksanakan di Laboratorium Penyakit Tumbuhan Jurusan Proteksi Tanaman Fakultas Pertanian Universitas Lampung. Pelaksanaan penelitian
LAMPIRAN. Universitas Sumatera Utara
 LAMPIRAN Lampiran 1. Sterilisasi Alat dan Bahan Semua peralatan yang akan digunakan dalam penelitian disterilisasikan terlebih dahulu. Peralatan mikrobiologi disterilisasi dengan oven pada suhu 171 o C
LAMPIRAN Lampiran 1. Sterilisasi Alat dan Bahan Semua peralatan yang akan digunakan dalam penelitian disterilisasikan terlebih dahulu. Peralatan mikrobiologi disterilisasi dengan oven pada suhu 171 o C
II. TINJAUAN PUSTAKA. udara yang baik untuk pertumbuhan tanaman cabai adalah 25-27º C pada siang
 10 II. TINJAUAN PUSTAKA 2.1 Deskripsi Umum Tanaman Cabai Tanaman cabai mempunyai daya adaptasi yang cukup luas. Tanaman ini dapat diusahakan di dataran rendah maupun dataran tinggi sampai ketinggian 1400
10 II. TINJAUAN PUSTAKA 2.1 Deskripsi Umum Tanaman Cabai Tanaman cabai mempunyai daya adaptasi yang cukup luas. Tanaman ini dapat diusahakan di dataran rendah maupun dataran tinggi sampai ketinggian 1400
HASIL DAN PEMBAHASAN
 HASIL DAN PEMBAHASAN Isolasi Bakteri Endofit Asal Bogor, Cipanas, dan Lembang Bakteri endofit yang digunakan dalam penelitian ini berasal dari tiga tempat yang berbeda dalam satu propinsi Jawa Barat. Bogor,
HASIL DAN PEMBAHASAN Isolasi Bakteri Endofit Asal Bogor, Cipanas, dan Lembang Bakteri endofit yang digunakan dalam penelitian ini berasal dari tiga tempat yang berbeda dalam satu propinsi Jawa Barat. Bogor,
II. METODOLOGI 2.1 Persiapan Wadah dan Ikan Uji 2.2 Persiapan Pakan Uji
 II. METODOLOGI 2.1 Persiapan Wadah dan Ikan Uji Wadah yang digunakan dalam penelitian ini adalah bak terpal dengan ukuran 2 m x1m x 0,5 m sebanyak 12 buah (Lampiran 2). Sebelum digunakan, bak terpal dicuci
II. METODOLOGI 2.1 Persiapan Wadah dan Ikan Uji Wadah yang digunakan dalam penelitian ini adalah bak terpal dengan ukuran 2 m x1m x 0,5 m sebanyak 12 buah (Lampiran 2). Sebelum digunakan, bak terpal dicuci
Pengendalian Penyakit pada Tanaman Jagung Oleh : Ratnawati
 Pengendalian Penyakit pada Tanaman Jagung Oleh : Ratnawati Tanaman jagung disamping sebagai bahan baku industri pakan dan pangan pada daerah tertentu di Indonesia dapat juga sebagai makanan pokok. Karena
Pengendalian Penyakit pada Tanaman Jagung Oleh : Ratnawati Tanaman jagung disamping sebagai bahan baku industri pakan dan pangan pada daerah tertentu di Indonesia dapat juga sebagai makanan pokok. Karena
II. MATERI DAN METODE PENELITIAN
 8 II. MATERI DAN METODE PENELITIAN 1. Materi, Lokasi, dan Waktu Penelitian 1.1 Materi Penelitian 1.1.1 Bahan Bahan yang digunakan dalam penelitian ini adalah jamur yang bertubuh buah, serasah daun, batang/ranting
8 II. MATERI DAN METODE PENELITIAN 1. Materi, Lokasi, dan Waktu Penelitian 1.1 Materi Penelitian 1.1.1 Bahan Bahan yang digunakan dalam penelitian ini adalah jamur yang bertubuh buah, serasah daun, batang/ranting
BAB 5. HASIL DAN PEMBAHASAN. Percobaan 1 : Isolasi dan identifikasi bakteri penambat nitrogen nonsimbiotik
 Tahap I BAB 5. HASIL DAN PEMBAHASAN Percobaan 1 : Isolasi dan identifikasi bakteri penambat nitrogen nonsimbiotik Hasil pengukuran sampel tanah yang digunakan pada percobaan 1 meliputi ph tanah, kadar
Tahap I BAB 5. HASIL DAN PEMBAHASAN Percobaan 1 : Isolasi dan identifikasi bakteri penambat nitrogen nonsimbiotik Hasil pengukuran sampel tanah yang digunakan pada percobaan 1 meliputi ph tanah, kadar
III. METODE PENELITIAN. dan Ilmu Pengetahuan Alam, Universitas Lampung dari bulan Januari sampai
 23 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Mikrobiologi Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Lampung dari bulan Januari sampai
23 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Mikrobiologi Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Lampung dari bulan Januari sampai
III. BAHAN DAN METODE. Penelitian ini dilaksanakan di Laboratorium Penyakit Tumbuhan Jurusan
 11 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Penyakit Tumbuhan Jurusan Agroteknologi Bidang Proteksi Tanaman Fakultas Pertanian Universitas Lampung
11 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Penyakit Tumbuhan Jurusan Agroteknologi Bidang Proteksi Tanaman Fakultas Pertanian Universitas Lampung
LAPORAN AKHIR PROGRAM KREATIVITAS MAHASISWA PENELITIAN
 LAPORAN AKHIR PROGRAM KREATIVITAS MAHASISWA PENELITIAN PEMANFAATAN BAKTERI KITINOLITIK DALAM PENGENDALIAN PENYAKIT ANTRAKNOSA (Colletotrichum gloeosporioides) SEBAGAI PENYAKIT PENTING PASCAPANEN PADA BUAH
LAPORAN AKHIR PROGRAM KREATIVITAS MAHASISWA PENELITIAN PEMANFAATAN BAKTERI KITINOLITIK DALAM PENGENDALIAN PENYAKIT ANTRAKNOSA (Colletotrichum gloeosporioides) SEBAGAI PENYAKIT PENTING PASCAPANEN PADA BUAH
METODE PENELITIAN. Penelitian ini dilakukan dari Bulan April sampai dengan Juni 2013, di
 17 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian ini dilakukan dari Bulan April sampai dengan Juni 2013, di Laboratorium Mikrobiologi Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas
17 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian ini dilakukan dari Bulan April sampai dengan Juni 2013, di Laboratorium Mikrobiologi Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas
HASIL DAN PEMBAHASAN Kondisi Umum
 13 HASIL DAN PEMBAHASAN Kondisi Umum Curah hujan harian di wilayah Kebun Percobaan PKBT IPB Tajur 1 dan 2 pada Februari sampai Juni 2009 berkisar 76-151 mm. Kelembaban udara harian rata-rata kebun tersebut
13 HASIL DAN PEMBAHASAN Kondisi Umum Curah hujan harian di wilayah Kebun Percobaan PKBT IPB Tajur 1 dan 2 pada Februari sampai Juni 2009 berkisar 76-151 mm. Kelembaban udara harian rata-rata kebun tersebut
II. MATERI DAN METODE
 II. MATERI DAN METODE 2.1 Materi, Lokasi, dan Waktu Penelitian 2.1.1 Materi Alat yang digunakan dalam penelitian adalah cawan petri, tabung reaksi, gelas ukur, pembakar spiritus, pipet, jarum ose, erlenmeyer,
II. MATERI DAN METODE 2.1 Materi, Lokasi, dan Waktu Penelitian 2.1.1 Materi Alat yang digunakan dalam penelitian adalah cawan petri, tabung reaksi, gelas ukur, pembakar spiritus, pipet, jarum ose, erlenmeyer,
BAB I PENDAHULUAN. A. Latar Belakang
 A. Latar Belakang BAB I PENDAHULUAN Biakan murni merupakan tahapan awal di dalam pembuatan bibit jamur. Pembuatan biakan murni diperlukan ketelitian, kebersihan, dan keterampilan. Pertumbuhan miselium
A. Latar Belakang BAB I PENDAHULUAN Biakan murni merupakan tahapan awal di dalam pembuatan bibit jamur. Pembuatan biakan murni diperlukan ketelitian, kebersihan, dan keterampilan. Pertumbuhan miselium
BAHAN DAN METODE Tempat dan Waktu Metode Penelitian Perbanyakan Propagul Agens Antagonis Perbanyakan Massal Bahan Pembawa Biopestisida
 7 BAHAN DAN METODE Tempat dan Waktu Penelitian ini dilaksanakan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor dan Balai Penelitian Tanaman
7 BAHAN DAN METODE Tempat dan Waktu Penelitian ini dilaksanakan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor dan Balai Penelitian Tanaman
BAHAN DAN METODE Bahan dan Alat
 23 III. BAHAN DAN METODE 3.1. Tempat dan Waktu Penelitian Penelitian dilakukan di Laboratorium Bioteknologi Tanah, Departemen Ilmu Tanah dan Sumberdaya Lahan, Fakultas Pertanian, Institut Pertanian Bogor
23 III. BAHAN DAN METODE 3.1. Tempat dan Waktu Penelitian Penelitian dilakukan di Laboratorium Bioteknologi Tanah, Departemen Ilmu Tanah dan Sumberdaya Lahan, Fakultas Pertanian, Institut Pertanian Bogor
HASIL DAN PEMBAHASAN
 HASIL DAN PEMBAHASAN Eksplorasi Cendawan Rhizosfer Hasil eksplorasi cendawan yang dilakukan pada tanah rhizosfer yang berasal dari areal tanaman karet di PT Perkebunan Nusantara VIII, Jalupang, Subang,
HASIL DAN PEMBAHASAN Eksplorasi Cendawan Rhizosfer Hasil eksplorasi cendawan yang dilakukan pada tanah rhizosfer yang berasal dari areal tanaman karet di PT Perkebunan Nusantara VIII, Jalupang, Subang,
III. MATERI DAN METODE
 III. MATERI DAN METODE 3.1. Waktu dan Tempat Penelitian Penelitian ini telah dilaksanakan pada bulan Maret 2015 sampai Juli 2015. Sempel tanah diambil pada dua tempat yaitu pengambilan sempel tanah hutan
III. MATERI DAN METODE 3.1. Waktu dan Tempat Penelitian Penelitian ini telah dilaksanakan pada bulan Maret 2015 sampai Juli 2015. Sempel tanah diambil pada dua tempat yaitu pengambilan sempel tanah hutan
BAB III METODE PENELITIAN. Pangan dan Hortikultura Sidoarjo dan Laboratorium Mikrobiologi, Depertemen
 BAB III METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di UPT Pengembangan Agrobisnis Tanaman Pangan dan Hortikultura Sidoarjo dan Laboratorium Mikrobiologi, Depertemen Biologi,
BAB III METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di UPT Pengembangan Agrobisnis Tanaman Pangan dan Hortikultura Sidoarjo dan Laboratorium Mikrobiologi, Depertemen Biologi,
BAHAN DAN METODE. Kasa Fakultas Pertanian Universitas Sumatera Utara, Medan dengan ketinggian tempat
 BAHAN DAN METODE Tempat dan waktu penelitian Penelitian ini dilaksanakan di Laboratorium Penyakit Tumbuhan dan di Rumah Kasa Fakultas Pertanian, Medan dengan ketinggian tempat + 25 m dpl pada Bulan Mei
BAHAN DAN METODE Tempat dan waktu penelitian Penelitian ini dilaksanakan di Laboratorium Penyakit Tumbuhan dan di Rumah Kasa Fakultas Pertanian, Medan dengan ketinggian tempat + 25 m dpl pada Bulan Mei
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1 Tempat dan waktu penelitian Penelitian ini dilaksanakan di rumah kaca Fakultas Sains dan Teknologi, Universitas Airlangga Surabaya sebagai tempat pengambilan sampel limbah
BAB III METODE PENELITIAN 3.1 Tempat dan waktu penelitian Penelitian ini dilaksanakan di rumah kaca Fakultas Sains dan Teknologi, Universitas Airlangga Surabaya sebagai tempat pengambilan sampel limbah
UJI PATOGENISITAS Fusarium moniliforme SHELDON PADA JAGUNG ABSTRAK
 Nurasiah Djaenuddin dan Amran Muis: Uji Patogenitas F. moniliforme.. UJI PATOGENISITAS Fusarium moniliforme SHELDON PADA JAGUNG Nurasiah Djaenuddin dan Amran Muis Balai Penelitian Tanaman Serealia ABSTRAK
Nurasiah Djaenuddin dan Amran Muis: Uji Patogenitas F. moniliforme.. UJI PATOGENISITAS Fusarium moniliforme SHELDON PADA JAGUNG Nurasiah Djaenuddin dan Amran Muis Balai Penelitian Tanaman Serealia ABSTRAK
PENDAHULUAN Latar Belakang
 PENDAHULUAN Latar Belakang Ditinjau dari aspek pertanaman maupun nilai produksi, cabai (Capsicum annuum L. ) merupakan salah satu komoditas hortikultura andalan di Indonesia. Tanaman cabai mempunyai luas
PENDAHULUAN Latar Belakang Ditinjau dari aspek pertanaman maupun nilai produksi, cabai (Capsicum annuum L. ) merupakan salah satu komoditas hortikultura andalan di Indonesia. Tanaman cabai mempunyai luas
METODOLOGI. Kerapatan jenis (K)
 METODOLOGI Tempat dan waktu penelitian Penelitian dilakukan di lahan bekas penambangan timah PT. Koba Tin, Koba-Bangka, dan Pusat Penelitian Sumber Daya Hayati dan Bioteknologi IPB (PPSHB IPB). Penelitian
METODOLOGI Tempat dan waktu penelitian Penelitian dilakukan di lahan bekas penambangan timah PT. Koba Tin, Koba-Bangka, dan Pusat Penelitian Sumber Daya Hayati dan Bioteknologi IPB (PPSHB IPB). Penelitian
III. BAHAN DAN METODE. Penelitian ini dilaksanakan di Laboratorium Ilmu Penyakit Tanaman Fakultas
 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Ilmu Penyakit Tanaman Fakultas Pertanian Universitas Lampung. Pelaksanaan penelitian dimulai dari September
III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Ilmu Penyakit Tanaman Fakultas Pertanian Universitas Lampung. Pelaksanaan penelitian dimulai dari September
BAB III METODE PENELITIAN. Biologi dan Laboratorium Biokimia, Departemen Kimia Fakultas Sains dan
 BAB III METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Mikrobiologi, Departemen Biologi dan Laboratorium Biokimia, Departemen Kimia Fakultas Sains dan Teknologi,
BAB III METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Mikrobiologi, Departemen Biologi dan Laboratorium Biokimia, Departemen Kimia Fakultas Sains dan Teknologi,
III. BAHAN DAN METODE. Penelitian ini dilaksanakan pada bulan Maret Oktober 2014 di
 III. BAHAN DAN METODE 3.1 Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan Maret 2014 - Oktober 2014 di Laboratorium Hama Tumbuhan, Jurusan Agroteknologi, Fakultas Pertanian Universitas
III. BAHAN DAN METODE 3.1 Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan Maret 2014 - Oktober 2014 di Laboratorium Hama Tumbuhan, Jurusan Agroteknologi, Fakultas Pertanian Universitas
