Titrasi Potensiometri
|
|
|
- Hartanti Kusumo
- 7 tahun lalu
- Tontonan:
Transkripsi
1 Modul 1 Titrasi Potensiometri Dr. Anna Permanasari, M.Si. K egiatan praktikum ini dimaksudkan untuk melatih mahasiswa agar terampil dalam melakukan praktikum yang berhubungan dengan titrasi potensiometri. Beberapa keterampilan yang diharapkan muncul meliputi keterampilan menggunakan dan membaca serta mengkalibrasi alat potensiometer, keterampilan dalam membedakan penggunaan alat-alat ukur gelas yang berbeda ketelitiannya, keterampilan mengolah data hasil percobaan menjadi data yang dapat dianalisis, serta keterampilan dalam menyimpulkan hasil percobaan serta mengomunikasikannya dalam bentuk tertulis. Kegiatan praktikum yang bersifat eksplorasi ini dapat dilaksanakan selama 4 60 menit, dan dilakukan secara individu atau kelompok (satu kelompok terdiri dari 2-3 mahasiswa). Untuk menjamin kesiapan mahasiswa dalam melaksanakan praktikum, sebaiknya dilakukan terlebih dahulu tes awal tentang pengetahuan dasar yang diperlukan (pengertian ph, K a, potensial sel, sel elektrokimia, keterkaitan antara ph dengan potensial sel), serta tahap-tahap percobaan yang akan dilakukan. Keterampilan prasyarat untuk kegiatan ini adalah telah pernah melakukan praktikum titrasi secara konvensional. Tujuan yang diharapkan setelah Anda mengikuti Kegiatan Praktikum Modul 1 ini, Anda dapat: 1. terampil menggunakan instrumen untuk titrasi potensiometri; 2. terampil menggunakan dan mengkalibrasi ph meter; 3. terampil menggunakan alat ukur yang tepat sesuai dengan keperluannya; 4. memahami prinsip kerja dan landasan teori tentang potensiometri; 5. menentukan konsentrasi larutan NaOH; 6. mengomunikasikan hasil percobaan dalam bentuk laporan tertulis; 7. menentukan nilai K a asam asetat berdasarkan data percobaan.
2 1.2 Praktikum Kimia 2 Untuk mencapai tujuan tersebut maka Modul 1 ini dibagi menjadi 2 Kegiatan Praktikum, yaitu: Kegiatan Praktikum 1 : Penentuan Konsentrasi Larutan NaOH dengan Titrasi Potensiometri; Kegiatan Praktikum 2 : Penentuan Tetapan Disosiasi Asam Lemah dengan Titrasi Potensiometri. Dalam mempelajari Modul 1 ini, diharapkan Anda membaca setiap topik/subtopik yang tersedia, memahami isinya, melaksanakan percobaan, mencatat data yang diperoleh, melakukan analisis data, membuat gambar/tabel/grafik bila diperlukan, melakukan perhitungan, menuliskan persamaan reaksi, membuat kesimpulan dari setiap percobaan serta menjawab tes formatif yang tersedia pada setiap akhir kegiatan belajar. Selamat belajar, semoga Anda berhasil!
3 PEKI4420/MODUL P Kegiatan Praktikum 1 Penentuan Konsentrasi Larutan NaOH dengan Titrasi Potensiometri otensiometri adalah suatu teknik analisis pengukuran konsentrasi sebagai fungsi dari potensial dalam suatu sel elektrokimia. Metode ini sangat berguna untuk menentukan titik ekuivalen suatu titrasi secara instrumen sebagai pengganti indikator visual. Ketelitian titrasi potensiometri lebih tinggi dibandingkan dengan titrasi visual yang menggunakan indikator. Titrasi potensiometri dapat diaplikasikan pada titrasi-titrasi redoks, kompleksometri, asam basa, dan pengendapan. Alat-alat yang diperlukan dalam titrasi potensiometri adalah elektrode pembanding, elektrode indikator dan alat pengukur potensial. Pengukuran potensial dapat dilakukan secara langsung dengan alat potensiometer atau tidak langsung melalui pengukuran ph dengan alat ph meter. Pada penggunaan alat ukur potensiometer, pembacaan potensial dilakukan pada setiap periode penambahan titran. Penambahan titran dihentikan bila nilai potensial terukur relatif tidak berubah pada penambahan volume titran, setelah terjadi lompatan potensial yang tajam. Titik setara atau titik ekuivalen dapat ditentukan dengan membuat kurva hubungan antara potensial (volt) terhadap ml titran. Volume di mana terjadi lompatan tajam dari potensial dinyatakan sebagai volume titik setara. Gambar 1.1. Kurva titrasi potensiometri (ml titran terhadap potensial).
4 1.4 Praktikum Kimia 2 Kadang-kadang kita mengalami kesulitan untuk menentukan titik ekuivalen titrasi dari kurva di atas. Untuk mempermudahnya maka dibuat kurva turunan pertama dari data potensial dan ml titran sehingga diperoleh kurva ΔE/ΔV terhadap ml titran. Gambar 1.2. Cara lain yang lebih mudah dalam menentukan titik ekuivalen titrasi adalah dengan membuat kurva turunan kedua potensial, Δ 2 E/ΔV 2 terhadap ml titran. Gambar 1.3. Umumnya pada titrasi potensiometri yang melibatkan ion H + dalam larutan, alat ukur yang digunakan adalah ph meter. ph meter merupakan alat
5 PEKI4420/MODUL pengukur ph yang menggunakan elektrode membran sebagai elektrode indikator. Alat ini dilengkapi pula dengan elektrode pembanding gelas atau kalomel atau kombinasi kedua elektrode tersebut, di mana keduanya tercelup ke dalam larutan yang diukur. ph meter merupakan alat ukur tidak langsung untuk pengukuran potensial suatu reaksi dalam sel elektrokimia. ph meter dilengkapi dengan elektrode kalomel jenuh dan elektrode membran gelas sebagai elektrode pembanding. Hubungan antara ph dengan potensial larutan dinyatakan oleh rumus: Ev L ph, 0,059 di mana E v adalah potensial sel, L adalah tetapan yang tergantung dari potensial elektrode pembanding dan potensial yang berasal dari permukaan membran. Gambar 1.4. Pada praktiknya, kita tidak perlu melakukan konversi ph menjadi potensial. Kita dapat melakukan hal yang sama, seperti terhadap data potensial untuk data ph yang diperoleh dari percobaan. Nilai ph dari setiap penambahan ml titran dapat langsung diplot ke dalam kurva ph vs ml titran. Demikian pula untuk mendapatkan titik
6 1.6 Praktikum Kimia 2 ekuivalen yang lebih teliti, dapat dilakukan dengan membuat kurva turunan pertama ΔpH/ΔV vs ml titran, atau turunan keduanya, Δ 2 ph/δv 2 vs ml titran. Bila kita menggunakan instrumen untuk pengukuran maka hal yang harus kita jamin adalah bahwa alat tersebut layak digunakan, dalam arti dapat mengukur dengan benar apa yang akan diukur. Untuk itu perlu dilakukan kalibrasi terlebih dahulu. Kalibrasi alat ph meter untuk keperluan titrasi potensiometer dapat dilakukan dengan mudah. Kalibrasi ph meter perlu dilakukan untuk mengetahui apakah respons elektrode terhadap perubahan ph sudah benar dan dapat terekam dengan benar. Gambar 1.5. ph meter dengan larutan buffer ph 4 dan ph 7 untuk kalibrasi Titrasi asam basa merupakan salah satu jenis titrasi yang dapat dilakukan dengan metode potensiometri. Pada penetapan asam-asam digunakan basa sebagai titran, demikian pula sebaliknya. NaOH adalah basa kuat yang dapat digunakan sebagai standar sekunder untuk titrasi asam basa. NaOH termasuk standar sekunder karena sukar
7 PEKI4420/MODUL diperoleh dalam keadaan murni, mudah berubah dalam keadaan padatnya karena higroskopis. Karena sifatnya sebagai standar sekunder, maka untuk penggunaannya perlu distandarisasi konsentrasinya dalam larutan dengan cara titrasi menggunakan standar primer asam. Salah satu standar primer asam yang paling sering digunakan adalah asam oksalat, (COOH) 2. 2 H 2 O. Asam oksalat termasuk standar primer karena mudah diperoleh dalam keadaan murni dan stabil dalam waktu relatif lama, baik sebagai padatannya maupun dalam bentuk larutannya. Kapan kita menghentikan titrasi? Titrasi dapat dihentikan bila penambahan titran tidak lagi menyebabkan perubahan potensial atau ph dari larutan yang dititrasi. Tetapi ini bukan merupakan titik akhir titrasi atau titik ekuivalen, seperti yang kita yakini pada titrasi dengan cara konvensional (titik akhir titrasi/titik ekuivalen terjadi saat terjadi perubahan warna indikator). Titik ekuivalen dalam titrasi potensiometri terjadi saat terjadi lonjakan potensial atau ph terhadap penambahan titran. Titik ekuivalen titrasi sangat sulit ditentukan berdasarkan data pengamatan ph atau potensial saja. Titik ekuivalen titrasi dapat dengan mudah ditentukan melalui pembuatan kurva titrasi. Kurva titrasi dapat dibuat dengan dua cara, yaitu melalui kurva potensial vs ml titran atau ph vs ml titran. Kurva ph terhadap ml titran hampir mirip bentuknya dengan kurva E vs ml titran. Gambar 1.6. Kurva titrasi potensiometri (ml titran vs ph)
8 1.8 Praktikum Kimia 2 PERCOBAAN : PEMBUATAN LARUTAN STANDAR ASAM OKSALAT DAN PENENTUAN KONSENTRASI LARUTAN NaOH A. Alat Dan Bahan 1. Alat a. gelas kimia 50 ml, b. batang pengaduk, c. neraca analitik, d. labu ukur 100 ml, e. corong pendek kecil, f. botol semprot, g. neraca teknis, h. gelas kimia 600 ml, i. buret 50 ml, j. pipet volume10 ml, k. alat pengaduk magnet dan batang magnetnya. 2. Bahan a. asam oksalat, (COOH) 2. 2 H 2 O, b. aquadest, c. buffer ph 4, d. buffer ph 7, e. indikator fenolftalin 0,1 %. B. Prosedur Percobaan 1. Pembuatan larutan standar asam oksalat a. Timbanglah secara kuantitatif 0,63 g asam oksalat dalam gelas kimia 50 ml. Larutkan dengan sedikit aquadest. Bila perlu panaskan sedikit agar asam oksalat cepat larut. b. Bila telah larut dan larutan mendingin kembali, tuangkan larutan di dalam gelas kimia ke dalam labu ukur melalui corong
9 PEKI4420/MODUL pendek. Bilas sisa larutan dalam gelas kimia sampai kita yakin bahwa semua asam oksalat telah masuk ke dalam labu. c. Encerkan larutan dalam labu ukur sampai tanda batas. Kocok sampai benar-benar homogen. Larutan siap dipakai untuk standarisasi. 2. Pembuatan larutan NaOH a. Timbang kira-kira 2 g NaOH dalam gelas kimia 50 ml. b. Pindahkan ke dalam gelas kimia 600 ml, dan larutkan di dalam 500 ml aquadest yang bebas CO 2 (aqudest yang telah dididihkan dan didinginkan kembali). Aduk hingga homogen. 3. Kalibrasi ph meter a. Siapkan larutan buffer ph 4 dan ph 7 masing-masing di dalam gelas kimia 100 ml yang kering dan bersih. b. Bersihkan elektrode ph meter dengan cara menyemprotkan aquadest ke sekeliling ujung elektrode. Keringkan dengan menggunakan kertas tisu. c. Sambungkan elektrode dengan alat bacaan ph. d. Celupkan elektrode ke dalam larutan buffer ph 4, goyanggoyang sebentar untuk menghomogenkan, lalu biarkan beberapa saat. Pijit tombol On pada ph meter. Amati pembacaannya. Bila bacaan tidak menunjukkan ph 4 maka putarlah tombol kalibrasi sehingga ph pada bacaan menunjukkan nilai 4. e. Angkat elektrode dari larutan. Cuci kembali dengan aquadest, lalu keringkan dengan kertas tisu kembali. f. Celupkan elektrode ke dalam larutan buffer ph 7. Pijit tombol On pada ph meter. Bila bacaan ph menunjukkan ph 7 maka alat siap digunakan. Bila tidak menunjukkan ph 7, mintalah instruktur Anda untuk memperbaiki atau mengganti alat. g. Cucilah dan keringkan elektrode selalu setiap akan digunakan untuk larutan yang berbeda.
10 1.10 Praktikum Kimia 2 Harap diperhatikan! Bila ph meter tidak digunakan lakukanlah pemeliharaan yang baik terutama terhadap elektrodenya. Bila tidak digunakan elektrode harus selalu dalam keadaan tercelup di dalam larutan jenuh KCl atau larutan KCl 3,5 M. Perhatikan isi cairan di dalam elektrode. Elektrode masih dapat digunakan dengan baik bila isi cairan (larutan KCl) di dalamnya tetap penuh (sampai tanda batasnya). 4. Penentuan konsentrasi larutan NaOH a. Set alat potensiometer dan perangkatnya seperti terlihat dalam gambar. b. Cucilah buret sebelum digunakan, dan bilas dengan larutan NaOH yang akan diisikan minimal dua kali. Masukkan larutan NaOH ke dalamnya. Nol-kan pembacaan volume NaOH pada buret. c. Sementara itu pipet 10 ml larutan asam oksalat menggunakan pipet volume yang telah bersih dan telah dibilas dua kali dengan larutan asam tersebut. Masukkan ke dalam gelas kimia 100 ml. Encerkan larutan dengan menambahkan aquadest 20 ml. d. Masukkan batang magnet ke dalam gelas kimia, lalu masukkan elektrode yang telah bersih dan kering ke dalamnya. Putarlah tombol pengaduk untuk menghomogenkan larutan. e. Setelah beberapa saat hentikan pengadukan, bacalah nilai ph pada ph meter (ini adalah data nilai ph untuk volume 0 ml titran). f. Mulailah titrasi dengan cara menambahkan larutan NaOH dari buret. Lakukan pembacaan ph setiap penambahan 0,5 ml larutan NaOH. Jika telah mendekati titik akhir, pembacaan dilakukan setiap penambahan 0,2 ml. g. Pembacaan sampai volume titran mencapai 15 ml. h. Lakukan pekerjaan titrasi ini dengan cara duplo (dua kali pengulangan).
11 PEKI4420/MODUL i. Buatlah kurva titrasi ph vs ml titran atau kurva turunan satu dan turunan keduanya pada kertas grafik. j. Tentukan titik ekuivalennya berdasarkan kurva titrasi yang telah dibuat k. Hitunglah konsentrasi larutan NaOH dalam satuan mol ekuivalen/l (normal, N). Gambar 1.7. Set alat titrasi potensiometri C. Pengamatan dan Analisis Data Penentuan konsentrasi larutan NaOH 1. Penimbangan asam oksalat : Massa gelas kimia + Zat =.. g Massa gelas kimia = g Massa zat = g Perhitungan : Konsentrasi asam oksalat (N) =.. = = N (4 desimal)
12 1.12 Praktikum Kimia 2 2. Titrasi asam oksalat dengan titran larutan NaOH Volume NaOH Percobaan I Percobaan II Titik akhir titrasi. ml. ml (berdasarkan kurva titrasinya) Pembacaan awal. ml. ml Pemakaian. ml. ml Rata-rata pemakaian. ml Perhitungan konsentrasi NaOH Jadi [NaOH] = N (4 desimal) D. Pertanyaan 1. Jelaskan mengapa percobaan NaOH dilakukan dengan neraca teknis, sementara percobaan asam oksalat dilakukan dengan neraca analitik! 2. Hitunglah berapa gram asam oksalat harus ditimbang untuk membuat 100 ml larutan asam oksalat 0,1 N? 3. Berikan penjelasan, bolehkah Anda menggunakan gelas ukur untuk mengukur volume asam oksalat dalam titrasi? 4. Tuliskan reaksi yang terjadi selama titrasi berlangsung! 5. Apa pengertian titik akhir titrasi dan titik ekuivalen? E. Kesimpulan
13 PEKI4420/MODUL T Kegiatan Praktikum 2 Penentuan Tetapan Disosiasi Asam Lemah dengan Titrasi Potensiometri etapan disosiasi suatu asam lemah atau basa lemah dapat ditentukan melalui prinsip titrasi potensiometri. Suatu asam lemah HA, dalam air akan mengalami ionisasi/disosiasi dengan reaksi sebagai berikut. HA (aq) H aq A aq Maka tetapan ionisasi asamnya adalah maka [H ][A ] Ka [HA] [A ] [A ] log Ka log[h ] log log ph [HA] [HA] [A ] log log Ka ph [HA] Dengan mengalurkan nilai ph sebagai fungsi dari [A ] log [HA] maka nilai K a dapat ditentukan. Berdasarkan persamaan di atas, besarnya log K a adalah intersep pada kurva. Dengan demikian maka nilai K a dapat dihitung. Gambar 1.8. Pada praktiknya, larutan NaOH dapat digunakan sebagai titran, sedangkan asam asetat yang akan ditentukan nilai K a -nya digunakan sebagai
14 1.14 Praktikum Kimia 2 titrat. A pada setiap penambahan NaOH dapat dihitung setara dengan [NaOH], sedangkan [HA] dapat dihitung berdasarkan pengurangan [H + ] selama titrasi karena bereaksi dengan OH - dari NaOH. Asam asetat yang digunakan harus telah diketahui dengan pasti konsentrasinya. Penetapan konsentrasi asam asetat dapat langsung dilakukan bersamaan dengan pekerjaan menentukan K a. Ada cara yang lebih mudah untuk menentukan tetapan disosiasi asam/basa (K a atau K b ). Data yang diperoleh dari titrasi, dialurkan ke dalam bentuk kurva ph terhadap ml titran. Dari kurva tersebut kita dapat menentukan volume titran pada titik ekuivalen. Selanjutnya volume titran tersebut dibagi dua untuk memperoleh volume pada setengah titik ekuivalen. Misalnya bila volume pada setengah titik ekuivalen tersebut x maka tariklah garis tegak lurus memotong kurva. Tariklah garis ke samping untuk menentukan ph. Nilai ph tersebut merupakan nilai ph pada perbandingan jumlah sisa asam dan asam dalam larutan 1:1. Bila data tersebut di masukkan ke dalam persamaan: [HA] ph pka log maka ph = pk [A a ] sehingga nilai K a dapat dihitung. PERCOBAAN: PENENTUAN TETAPAN DISOSIASI ASAM ASETAT A. Alat Dan Bahan 1. Alat a. gelas kimia 50 ml, b. batang pengaduk, c. neraca analitik, d. corong pendek kecil, e. botol semprot, f. neraca teknis, g. gelas kimia 600 ml, h. buret 50 ml, i. pipet volume 10 ml, j. alat pengaduk magnet.
15 PEKI4420/MODUL Bahan a. asam oksalat, (COOH) 2.2H 2 O, b. aquadest, c. buffer ph 4, d. labu ukur 100 ml, e. buffer ph 7, f. asam asetat 99% (mj. 1,05 g/ml). B. Prosedur Percobaan 1. Pembuatan larutan asam asetat + 0,1 N a. Siapkan kira-kira 250 ml aquadest dalam gelas kimia 400 ml. b. Pipetlah + 10 ml asam asetat pekat p.a (99 % w/w, m.j. 1,04 g/ml), kemudian masukkan perlahan-lahan ke dalam gelas kimia yang berisi aquadest tersebut. Aduk dengan batang pengaduk perlahan-lahan sampai homogen. Ambil 25 ml larutan asam asetat yang telah dibuat, kemudian masukkan ke dalam gelas kimia 400 ml yang lain. Encerkan dengan aquadest sampai volumenya 250 ml. Konsentrasi larutan terakhir kurang lebih 0,1 N. Larutan terakhir inilah yang akan digunakan untuk penetapan selanjutnya. 2. Penentuan tetapan disosiasi asam asetat (K a CH 3 COOH) a. Siapkan peralatan untuk titrasi potensiometer. Lakukan kalibrasi terlebih dahulu terhadap ph meter yang akan digunakan dengan cara yang sama, seperti pada langkah kegiatan praktikum sebelumnya. b. Masukkan 10 ml asam asetat yang yang telah dibuat ke dalam gelas kimia 10 ml. Encerkan sampai kira-kira 25 ml dengan aquadest. Celupkan elektrode yang telah dikeringkan ke dalamnya. Masukkan pula batang magnetnya. c. Jalankan pengaduk magnetnya. Setelah beberapa saat baca ph larutan dalam meteran. d. Mulailah melakukan titrasi dengan larutan NaOH yang telah dibakukan (distandarkan, yang dibuat pada percobaan pertama).
16 1.16 Praktikum Kimia 2 Bacalah ph larutan setiap penambahan 0,5 ml NaOH. Jika telah mendekati titik akhir titrasi, pembacaan ph dilakukan setiap penambahan 0,2 ml. Lakukan pembacaan sampai volume titran 15 ml. e. Buatlah kurva ph vs ml titran atau ΔpH/ΔV, atau Δ 2 ph/δv 2. f. Tentukan titik ekuivalennya berdasarkan kurva tersebut. g. Tentukan volume titran pada titik ekuivalen berdasarkan kurva yang telah dibuat. h. Gunakan kurva titrasi yang sama untuk menentukan ph pada setengah volume ekuivalennya. i. ph pada setengah volume ekuivalen adalah pk a asam. Hitunglah K a -nya. j. Catat suhu ruangan saat melakukan percobaan. k. Carilah nilai K a asam asetat dalam literatur. Bandingkan dengan nilai hasil percobaan. Tentukan % kesalahannya. l. Buatlah laporan tertulis tentang percobaan yang Anda lakukan sesuai dengan format laporan yang telah ditentukan.
17 PEKI4420/MODUL C. Pengamatan dan Analisis Data Nama: LEMBAR PENGAMATAN DAN ANALISIS DATA Percobaan : Penentuan Ka Asam Asetat ml NaOH ph ΔpH/ΔV Δ 2 ph/δv 2 ml NaOH 0 10,20 0,50 10,40 1,00 10,60 1,50 10,80 2,00 11,00 2,50 11,20 3,00 11,40 3,50 11,60 4,00 11,80 4,50 12,00 5,00 12,50 5,50 13,00 6,00 13,50 6,50 14,00 7,00 14,50 7,50 15,00 8,00 8,20 8,40 8,60 8,80 9,00 9,20 9,40 9,60 9,80 10,00 ph ΔpH/ΔV Δ 2 ph/δv 2 Suhu Percobaan : o C
18 1.18 Praktikum Kimia 2 Penetapan Tetapan disosiasi asam asetat Berdasarkan kurva ph terhadap ml titran maka diperoleh: ml titran pada titik ekuivalen =... ph pada setengah volume kuivalen titran =... (pka) Ka asam asetat =... ( o C) Ka asam asetat (literatur) =... ( o C) % Kesalahan =... D. Pertanyaan 1. Carilah faktor-faktor yang dapat menyebabkan kesalahan pada percobaan di atas? 2. Hitunglah molaritas larutan asam asetat yang dibuat dengan mencampurkan 10 ml asam asetat pekat p.a (99 % w/w, m.j. 1,04 g/ml) dengan aquadest sampai volume akhirnya 250 ml? 3. Tuliskan reaksi ionisasi basa lemah, dan turunkan bagaimana di peroleh hubungan ph dengan K b dari basa lemah tersebut! E. Kesimpulan
19 PEKI4420/MODUL Glosarium Asam lemah : Asam yang hanya terdisosiasi sebagian dalam air. Asam lemah memiliki tetapan disosiasi K a. Contoh asam lemah: asam asetat, asam benzoat, asamasam organik. Baku primer : Zat baku yang langsung dapat digunakan untuk menentukan konsentrasi zat lain. Contoh: asam oksalat p.a, natrium karbonat p.a, boraks p.a. Baku sekunder : Zat baku yang harus ditentukan terlebih dahulu konsentrasinya (dengan zat baku primer) sebelum digunakan lebih lanjut. Contoh: NaOH, HCl, K 2 Cr 2 O 7, KMNo 4. Basa lemah : Basa yang hanya terdisosiasi sebagian dalam air. Basa lemah memiliki tetapan disosiasi basa lemah, K b. Contoh basa lemah: NH 4 OH, Al(OH) 3, Ca(OH) 2, dan lain-lain. Buffer : Penyangga, yaitu campuran larutan yang dapat mempertahankan ph larutan terhadap penambahan asam, basa atau pengenceran. Elektrode kalomel Elektrode gelas : Elektrode pembanding (standar) Hg/Hg 2 Cl 2 : Elektrode indikator dalam ph meter. Elektrode gelas termasuk jenis elektrode membran selektif ion yang bekerja dengan mekanisme pertukaran ion. Kalibrasi : Pemeriksaan awal terhadap suatu alat/instrumen, yang harus dilakukan untuk mengetahui apakah alat tersebut layak pakai atau tidak. Kalibrasi rutin dilakukan dengan cara yang lebih mudah dan dilakukan setiap kali alat akan digunakan. Kalibrasi berkala melibatkan pengukuran parameter alat yang lebih banyak lagi, dan umumnya dilakukan periodik dalam jangka waktu tertentu (misalnya 6 bulan sekali, satu tahun sekali, dan sebagainya). Potensiometri : Suatu teknik pengukuran yang melibatkan pengamatan potensial sebagai fungsi dari konsentrasi.
20 1.20 Praktikum Kimia 2 ph : Adalah parameter derajat keasaman suatu zat dalam larutannya (dalam air). Suatu larutan yang memiliki ph = 7 bersifat netral. Ph> 7 bersifat basa, dan ph < 7 bersifat asam. Ph = - log [H + ] Sel elektrokimia : Tempat di mana reaksi elektrokimia terjadi.
21 PEKI4420/MODUL Daftar Pustaka Tim Kimia Instrumen Jurusan P. Kimia UPI. (2003). Penuntun Praktikum Kimia Instrumen. Bandung: FPMIPA-UPI dan JICA. Sumar Hendayana Dkk. (1994). Kimia Analitik Instrumen. Semarang: IKIP Semarang Press. Day, R.A and Underwood, A.L. (1994). Analisis Kimia Kuantitatif. Edisi 4. (Penerjemah: Soendoro, Dkk.). Surabaya: Penerbit Erlangga. Sawyer, D.T., et al. (1989). Chemistry Experiments for Instrumental Methods, 3 rd Ed. Kanada: John Wiley and Sons, Inc.
Titrasi Volumetri. Modul 1 PENDAHULUAN
 Modul 1 Titrasi Volumetri Dr. Anna Permanasari, M.Si. K PENDAHULUAN egiatan praktikum ini dimaksudkan untuk melatih keterampilan dasar Anda dalam melakukan pekerjaan laboratorium, melatih Anda dalam bekerja
Modul 1 Titrasi Volumetri Dr. Anna Permanasari, M.Si. K PENDAHULUAN egiatan praktikum ini dimaksudkan untuk melatih keterampilan dasar Anda dalam melakukan pekerjaan laboratorium, melatih Anda dalam bekerja
TITRASI POTENSIOMETRI
 TITRASI PTENSIMETRI TITRASI PTENSIMETRI I. TUJUAN PERCBAAN Menentukan titik ekivalen secara potensiometri. II. DASAR TERI Suatu eksperimen dapat diukur dengan menggunakan dua metode yaitu, pertama (potensiometri
TITRASI PTENSIMETRI TITRASI PTENSIMETRI I. TUJUAN PERCBAAN Menentukan titik ekivalen secara potensiometri. II. DASAR TERI Suatu eksperimen dapat diukur dengan menggunakan dua metode yaitu, pertama (potensiometri
PRAKTIKUM POTENSIOMETRI DAN PH METRI. Laporan. disusun untuk memenuhi salah satu tugas mata kuliah Instrumentasi Analitik. Oleh.
 PRAKTIKUM POTENSIOMETRI DAN PH METRI Laporan disusun untuk memenuhi salah satu tugas mata kuliah Instrumentasi Analitik Oleh Kelompok 1 Abdul Kholik (141411001) Aldi Muhamad R. (141411002) Arif Imanuddin
PRAKTIKUM POTENSIOMETRI DAN PH METRI Laporan disusun untuk memenuhi salah satu tugas mata kuliah Instrumentasi Analitik Oleh Kelompok 1 Abdul Kholik (141411001) Aldi Muhamad R. (141411002) Arif Imanuddin
LABORATORIUM INSTRUMENTASI ANALITIK
 LABORATORIUM INSTRUMENTASI ANALITIK SEMESTER GENAP TAHUN AJARAN 2013 MODUL : Potensiometri dan ph-metri PEMBIMBING : Haryadi.PhD Praktikum : 13 Maret 2013 Penyerahan : 20 Maret 2013 (Laporan) Oleh : Kelompok
LABORATORIUM INSTRUMENTASI ANALITIK SEMESTER GENAP TAHUN AJARAN 2013 MODUL : Potensiometri dan ph-metri PEMBIMBING : Haryadi.PhD Praktikum : 13 Maret 2013 Penyerahan : 20 Maret 2013 (Laporan) Oleh : Kelompok
KIMIA DASAR PRINSIP TITRASI TITRASI (VOLUMETRI)
 KIMIA DASAR TITRASI (VOLUMETRI) Drs. Saeful Amin, M.Si., Apt. PRINSIP TITRASI Titrasi (volumetri) merupakan metode analisis kimia yang cepat, akurat dan sering digunakan untuk menentukan kadar suatu unsur
KIMIA DASAR TITRASI (VOLUMETRI) Drs. Saeful Amin, M.Si., Apt. PRINSIP TITRASI Titrasi (volumetri) merupakan metode analisis kimia yang cepat, akurat dan sering digunakan untuk menentukan kadar suatu unsur
PENUNTUN PRAKTIKUM KIMIA DASAR II KI1201
 PENUNTUN PRAKTIKUM KIMIA DASAR II KI1201 Disusun Ulang Oleh: Dr. Deana Wahyuningrum Dr. Ihsanawati Dr. Irma Mulyani Dr. Mia Ledyastuti Dr. Rusnadi LABORATORIUM KIMIA DASAR PROGRAM TAHAP PERSIAPAN BERSAMA
PENUNTUN PRAKTIKUM KIMIA DASAR II KI1201 Disusun Ulang Oleh: Dr. Deana Wahyuningrum Dr. Ihsanawati Dr. Irma Mulyani Dr. Mia Ledyastuti Dr. Rusnadi LABORATORIUM KIMIA DASAR PROGRAM TAHAP PERSIAPAN BERSAMA
LAPORAN PRAKTIKUM STANDARISASI LARUTAN NaOH
 LAPORAN PRAKTIKUM STANDARISASI LARUTAN NaOH I. Tujuan Praktikan dapat memahami dan menstandarisasi larutan baku sekunder NaOH dengan larutan baku primer H 2 C 2 O 4 2H 2 O II. Dasar Teori Reaksi asam basa
LAPORAN PRAKTIKUM STANDARISASI LARUTAN NaOH I. Tujuan Praktikan dapat memahami dan menstandarisasi larutan baku sekunder NaOH dengan larutan baku primer H 2 C 2 O 4 2H 2 O II. Dasar Teori Reaksi asam basa
Metodologi Penelitian
 16 Bab III Metodologi Penelitian Penelitian dilakukan dengan menggunakan metode titrasi redoks dengan menggunakan beberapa oksidator (K 2 Cr 2 O 7, KMnO 4 dan KBrO 3 ) dengan konsentrasi masing-masing
16 Bab III Metodologi Penelitian Penelitian dilakukan dengan menggunakan metode titrasi redoks dengan menggunakan beberapa oksidator (K 2 Cr 2 O 7, KMnO 4 dan KBrO 3 ) dengan konsentrasi masing-masing
PENENTUAN KADAR ASAM ASETAT DALAM ASAM CUKA DENGAN ALKALIMETRI
 PENENTUAN KADAR ASAM ASETAT DALAM ASAM CUKA DENGAN ALKALIMETRI I. CAPAIAN PEMBELAJARAN Praktikan mampu menetapkan kadar CH3COOH (asam asetat) dan asam cuka (HCl) menggunakan prinsip reaksi asam-basa. II.
PENENTUAN KADAR ASAM ASETAT DALAM ASAM CUKA DENGAN ALKALIMETRI I. CAPAIAN PEMBELAJARAN Praktikan mampu menetapkan kadar CH3COOH (asam asetat) dan asam cuka (HCl) menggunakan prinsip reaksi asam-basa. II.
TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN
 TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN I. JUDUL PERCOBAAN : TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN II. TUJUAN PERCOBAAN : 1. Membuat dan
TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN I. JUDUL PERCOBAAN : TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN II. TUJUAN PERCOBAAN : 1. Membuat dan
Metodologi Penelitian
 Bab III Metodologi Penelitian Pembuatan larutan buffer menggunakan metode pencampuran antara asam lemah dengan basa konjugasinya. Selanjutnya larutan buffer yang sudah dibuat diuji kemampuannya dalam mempertahankan
Bab III Metodologi Penelitian Pembuatan larutan buffer menggunakan metode pencampuran antara asam lemah dengan basa konjugasinya. Selanjutnya larutan buffer yang sudah dibuat diuji kemampuannya dalam mempertahankan
I. LARUTAN BUFFER. 1. Membuat Larutan Buffer 2. Mempelajari Daya Sanggah Larutan Buffer TINJAUAN PUSTAKA
 I. LARUTAN BUFFER II. TUJUAN 1. Membuat Larutan Buffer 2. Mempelajari Daya Sanggah Larutan Buffer III. TINJAUAN PUSTAKA Larutan penyangga atau larutan buffer atau larutan dapar merupakan suatu larutan
I. LARUTAN BUFFER II. TUJUAN 1. Membuat Larutan Buffer 2. Mempelajari Daya Sanggah Larutan Buffer III. TINJAUAN PUSTAKA Larutan penyangga atau larutan buffer atau larutan dapar merupakan suatu larutan
 VISIT MY WEBSITE : KLIK AJA LINKNYA SOB http://dionlegionis.blogspot.com/search/label/education%20mipa http://dionlegionis.blogspot.com/2015/03/klasifikasi-kodok-beranak-darisulawesi.html http://dionlegionis.blogspot.com/2015/03/download-pdf-statistika-datatunggal.html
VISIT MY WEBSITE : KLIK AJA LINKNYA SOB http://dionlegionis.blogspot.com/search/label/education%20mipa http://dionlegionis.blogspot.com/2015/03/klasifikasi-kodok-beranak-darisulawesi.html http://dionlegionis.blogspot.com/2015/03/download-pdf-statistika-datatunggal.html
LARUTAN PENYANGGA (BUFFER)
 LARUTAN PENYANGGA (BUFFER) Larutan penyangga Larutan penyangga atau larutan buffer adalah larutan yang ph-nya praktis tidak berubah walaupun kepadanya ditambahkan sedikit asam, sedikit basa, atau bila
LARUTAN PENYANGGA (BUFFER) Larutan penyangga Larutan penyangga atau larutan buffer adalah larutan yang ph-nya praktis tidak berubah walaupun kepadanya ditambahkan sedikit asam, sedikit basa, atau bila
Nova Nurfauziawati Kelompok 11A V. PEMBAHASAN
 V. PEMBAHASAN Praktikum yang dilaksanakan tanggal 3 Oktober 2011 mengenai pembuatan larutan buffer dan pengujian kestabilannya. Larutan buffer adalah campuran asam/basa lemah dan basa/asam konjugasinya
V. PEMBAHASAN Praktikum yang dilaksanakan tanggal 3 Oktober 2011 mengenai pembuatan larutan buffer dan pengujian kestabilannya. Larutan buffer adalah campuran asam/basa lemah dan basa/asam konjugasinya
MODUL I SIFAT KOLIGATIF LARUTAN Penurunan Titik Beku Larutan
 MODUL I SIFAT KOLIGATIF LARUTAN Penurunan Titik Beku Larutan - Siswa mampu membuktikan penurunan titik beku larutan akibat penambahan zat terlarut. - Siswa mampu membedakan titik beku larutan elektrolit
MODUL I SIFAT KOLIGATIF LARUTAN Penurunan Titik Beku Larutan - Siswa mampu membuktikan penurunan titik beku larutan akibat penambahan zat terlarut. - Siswa mampu membedakan titik beku larutan elektrolit
PRAKTIKUM II TITRASI ASAM BASA OLEH RONIADI SAGULANI 85AK14020
 PRAKTIKUM II TITRASI ASAM BASA OLEH RONIADI SAGULANI 85AK14020 PROGRAM STUDI D3 ANALISIS KESEHATAN STIKES BINA MANDIRI GORONTALO 2014 LAPORAN AKHIR PERCOBAAN II A. JUDUL : Titrasi Asam Basa B. TUJUAN Dengan
PRAKTIKUM II TITRASI ASAM BASA OLEH RONIADI SAGULANI 85AK14020 PROGRAM STUDI D3 ANALISIS KESEHATAN STIKES BINA MANDIRI GORONTALO 2014 LAPORAN AKHIR PERCOBAAN II A. JUDUL : Titrasi Asam Basa B. TUJUAN Dengan
Penambahan oleh sedikit asam-kuat (H + ) menyebabkan kesetimbangan. CH 3 COOH(aq) CH 3 COO - (aq) + H + (aq) (9.1) asam lemah
 Larutan bufer* merupakan sistem larutan yang dapat mempertahankan lingkungannya dari pengaruh seperti oleh penambahan sedikit asam/basa kuat, atau oleh pengenceran. Sistem bufer terdiri atas dua komponen,
Larutan bufer* merupakan sistem larutan yang dapat mempertahankan lingkungannya dari pengaruh seperti oleh penambahan sedikit asam/basa kuat, atau oleh pengenceran. Sistem bufer terdiri atas dua komponen,
Penentuan Kesadahan Dalam Air
 Penentuan Kesadahan Dalam Air I. Tujuan 1. Dapat menentukan secara kualitatif dan kuantitatif kation (Ca²+,Mg²+) 2. Dapat membuat larutan an melakukan pengenceran II. Latar Belakang Teori Semua makhluk
Penentuan Kesadahan Dalam Air I. Tujuan 1. Dapat menentukan secara kualitatif dan kuantitatif kation (Ca²+,Mg²+) 2. Dapat membuat larutan an melakukan pengenceran II. Latar Belakang Teori Semua makhluk
LARUTAN PENYANGGA (BUFFER)
 LARUTAN PENYANGGA (BUFFER) Larutan penyangga Larutan penyangga atau larutan buffer adalah larutan yang ph-nya praktis tidak berubah walaupun kepadanya ditambahkan sedikit asam, sedikit basa, atau bila
LARUTAN PENYANGGA (BUFFER) Larutan penyangga Larutan penyangga atau larutan buffer adalah larutan yang ph-nya praktis tidak berubah walaupun kepadanya ditambahkan sedikit asam, sedikit basa, atau bila
Laporan Praktikum Kimia Dasar II. Standarisasi Larutan NaOH 0,1 M dan Penggunaannya Dalam Penentuan Kadar Asam Cuka Perdagangan.
 Laporan Praktikum Kimia Dasar II Standarisasi Larutan NaOH 0,1 M dan Penggunaannya Dalam Penentuan Kadar Asam Cuka Perdagangan Oleh: Kelompok : I (satu) Nama Nim Prodi : Ardinal : F1D113002 : Teknik Pertambangan
Laporan Praktikum Kimia Dasar II Standarisasi Larutan NaOH 0,1 M dan Penggunaannya Dalam Penentuan Kadar Asam Cuka Perdagangan Oleh: Kelompok : I (satu) Nama Nim Prodi : Ardinal : F1D113002 : Teknik Pertambangan
LAPORAN PRAKTIKUM KIMIA DASAR I
 LAPORAN PRAKTIKUM KIMIA DASAR I NAMA KELOMPOK : MELVIA PERMATASARI (08121006013) MELANY AMDIRA (08121006027) ANIS ALAFIFAH (08121006029) PUTRI WULANDARI (08121006071) MUTIARA BELLA (08121006073) JURUSAN
LAPORAN PRAKTIKUM KIMIA DASAR I NAMA KELOMPOK : MELVIA PERMATASARI (08121006013) MELANY AMDIRA (08121006027) ANIS ALAFIFAH (08121006029) PUTRI WULANDARI (08121006071) MUTIARA BELLA (08121006073) JURUSAN
TITRASI DENGAN INDIKATOR GABUNGAN DAN DUA INDIKATOR
 TITRASI DENGAN INDIKATOR GABUNGAN DAN DUA INDIKATOR I. TUJUAN 1. Memahami prinsip kerja dari percobaan. 2. Menentukan konsentrasi dari NaOH dan Na 2 CO 3. 3. Mengetahui kegunaan dari titrasi dengan indikator
TITRASI DENGAN INDIKATOR GABUNGAN DAN DUA INDIKATOR I. TUJUAN 1. Memahami prinsip kerja dari percobaan. 2. Menentukan konsentrasi dari NaOH dan Na 2 CO 3. 3. Mengetahui kegunaan dari titrasi dengan indikator
BAB III METODOLOGI PENELITIAN. Ruang lingkup penelitian ini adalah Ilmu Kimia Analisis.
 BAB III METODOLOGI PENELITIAN 3.1 Ruang Lingkup Penelitian Ruang lingkup penelitian ini adalah Ilmu Kimia Analisis. 3.2 Lokasi dan Waktu Penelitian Penelitian ini telah dilakukan pada tanggal 18 hingga
BAB III METODOLOGI PENELITIAN 3.1 Ruang Lingkup Penelitian Ruang lingkup penelitian ini adalah Ilmu Kimia Analisis. 3.2 Lokasi dan Waktu Penelitian Penelitian ini telah dilakukan pada tanggal 18 hingga
POTENSIOMETRI DAN KONDUKTOMETRI
 POTENSIOMETRI DAN KONDUKTOMETRI Listiana Cahya Lestari (G44120093), Felina K, Afiyatina Awaliah, dan Zulhan Arif MSi Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian
POTENSIOMETRI DAN KONDUKTOMETRI Listiana Cahya Lestari (G44120093), Felina K, Afiyatina Awaliah, dan Zulhan Arif MSi Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian
Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi. Bab17. Kesetimbangan Asam-Basa dan Kesetimbangan Kelarutan
 Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi Bab17 Kesetimbangan Asam-Basa dan Kesetimbangan Kelarutan Larutan buffer adalah larutan yg terdiri dari: 1. asam lemah/basa
Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi Bab17 Kesetimbangan Asam-Basa dan Kesetimbangan Kelarutan Larutan buffer adalah larutan yg terdiri dari: 1. asam lemah/basa
PERCOBAAN POTENSIOMETRI (PENGUKURAN ph)
 PERCOBAAN POTENSIOMETRI (PENGUKURAN ph) I. Tujuan. Membuat kurva hubungan ph - volume pentiter 2. Menentukan titik akhir titrasi 3. Menghitung kadar zat II. Prinsip Prinsip potensiometri didasarkan pada
PERCOBAAN POTENSIOMETRI (PENGUKURAN ph) I. Tujuan. Membuat kurva hubungan ph - volume pentiter 2. Menentukan titik akhir titrasi 3. Menghitung kadar zat II. Prinsip Prinsip potensiometri didasarkan pada
kimia TITRASI ASAM BASA
 Kurikulum 2006/2013 2013 kimia K e l a s XI TITRASI ASAM BASA Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami definisi dan macam-macam titrasi.
Kurikulum 2006/2013 2013 kimia K e l a s XI TITRASI ASAM BASA Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami definisi dan macam-macam titrasi.
kimia ASAM-BASA III Tujuan Pembelajaran
 KTSP K-13 kimia K e l a s XI ASAM-BASA III Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami mekanisme reaksi asam-basa. 2. Memahami stoikiometri
KTSP K-13 kimia K e l a s XI ASAM-BASA III Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami mekanisme reaksi asam-basa. 2. Memahami stoikiometri
Metode titrimetri dikenal juga sebagai metode volumetri
 Metode titrimetri dikenal juga sebagai metode volumetri? yaitu, merupakan metode analisis kuantitatif yang didasarkan pada prinsip pengukuran volume. 1 Macam Analisa Volumetri 1. Gasometri adalah volumetri
Metode titrimetri dikenal juga sebagai metode volumetri? yaitu, merupakan metode analisis kuantitatif yang didasarkan pada prinsip pengukuran volume. 1 Macam Analisa Volumetri 1. Gasometri adalah volumetri
PERCOBAAN I PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA
 LAPORAN PRAKTIKUM KIMIA ANALITIK KI-2122 PERCOBAAN I PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA Nama Praktikan : Anggi Febrina NIM : 13010107 Kelompok : 5 (Shift Pagi) Tanggal
LAPORAN PRAKTIKUM KIMIA ANALITIK KI-2122 PERCOBAAN I PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA Nama Praktikan : Anggi Febrina NIM : 13010107 Kelompok : 5 (Shift Pagi) Tanggal
MODUL I Pembuatan Larutan
 MODUL I Pembuatan Larutan I. Tujuan percobaan - Membuat larutan dengan metode pelarutan padatan. - Melakukan pengenceran larutan dengan konsentrasi tinggi untuk mendapatkan larutan yang diperlukan dengan
MODUL I Pembuatan Larutan I. Tujuan percobaan - Membuat larutan dengan metode pelarutan padatan. - Melakukan pengenceran larutan dengan konsentrasi tinggi untuk mendapatkan larutan yang diperlukan dengan
SOAL UJIAN OLIMPIADE SAINS NASIONAL 2014
 Hak Cipta Dilindungi Undang-undang SOAL UJIAN OLIMPIADE SAINS NASIONAL 2014 CALON PESERTA INTERNATIONAL CHEMISTRY OLYMPIAD (IChO) 2015 Mataram, Lombok 1-7 September 2014 Kimia Praktikum A Waktu: 120 menit
Hak Cipta Dilindungi Undang-undang SOAL UJIAN OLIMPIADE SAINS NASIONAL 2014 CALON PESERTA INTERNATIONAL CHEMISTRY OLYMPIAD (IChO) 2015 Mataram, Lombok 1-7 September 2014 Kimia Praktikum A Waktu: 120 menit
OLIMPIADE SAINS NASIONAL Medan, 1-7 Agustus 2010 BIDANG KIMIA. Ujian Praktikum KIMIA ANALISIS. Waktu 150 menit
 LIMPIADE SAINS NASINAL 2010 Medan, 1-7 Agustus 2010 BIDANG KIMIA Ujian Praktikum KIMIA ANALISIS Waktu 150 menit Kementerian Pendidikan Nasional Direktorat Jenderal Manajemen Pendidikan Dasar dan Menengah
LIMPIADE SAINS NASINAL 2010 Medan, 1-7 Agustus 2010 BIDANG KIMIA Ujian Praktikum KIMIA ANALISIS Waktu 150 menit Kementerian Pendidikan Nasional Direktorat Jenderal Manajemen Pendidikan Dasar dan Menengah
Titrasi asam kuat-basa kuat
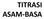 TITRASI ASAM-BASA KURVA TITRASI plot atau kurva antara ph atau poh terhadap volume titran untuk menguji apakah suatu reaksi dapat digunakan untuk analisa titrimetri ataukah tidak memilih indikator Titrasi
TITRASI ASAM-BASA KURVA TITRASI plot atau kurva antara ph atau poh terhadap volume titran untuk menguji apakah suatu reaksi dapat digunakan untuk analisa titrimetri ataukah tidak memilih indikator Titrasi
Laporan Praktikum TITRASI KOMPLEKSOMETRI Standarisasi EDTA dengan CaCO3
 Laporan Praktikum TITRASI KOMPLEKSOMETRI Standarisasi EDTA dengan CaCO3 TITRASI KOMPLEKSOMETRI Standarisasi EDTA dengan CaCO3 I. Waktu / Tempat Praktikum : Rabu,15 Februari 2012 / Lab Kimia Jur. Analis
Laporan Praktikum TITRASI KOMPLEKSOMETRI Standarisasi EDTA dengan CaCO3 TITRASI KOMPLEKSOMETRI Standarisasi EDTA dengan CaCO3 I. Waktu / Tempat Praktikum : Rabu,15 Februari 2012 / Lab Kimia Jur. Analis
Bab IV Hasil dan Pembahasan
 Bab IV Hasil dan Pembahasan IV.1 Pembuatan Larutan Buffer Semua zat yang digunakan untuk membuat larutan buffer dapat larut dengan sempurna. Larutan yang diperoleh jernih, homogen, dan tidak berbau. Data
Bab IV Hasil dan Pembahasan IV.1 Pembuatan Larutan Buffer Semua zat yang digunakan untuk membuat larutan buffer dapat larut dengan sempurna. Larutan yang diperoleh jernih, homogen, dan tidak berbau. Data
LARUTAN PENYANGGA (BUFFER)
 LARUTAN PENYANGGA (BUFFER) Larutan penyangga Larutan penyangga atau larutan buffer adalah larutan yang ph-nya praktis tidak berubah walaupun kepadanya ditambahkan sedikit asam, sedikit basa, atau bila
LARUTAN PENYANGGA (BUFFER) Larutan penyangga Larutan penyangga atau larutan buffer adalah larutan yang ph-nya praktis tidak berubah walaupun kepadanya ditambahkan sedikit asam, sedikit basa, atau bila
GALAT TITRASI. Ilma Nugrahani
 GALAT TITRASI Ilma Nugrahani Galat Titrasi Adalah galat yang terjadi karena indikator berubah warna sebelum atau sesudah titik setara ditunjukkan dari kurva titrasi titik akhir titik ekivalen. Dapat disebabkan
GALAT TITRASI Ilma Nugrahani Galat Titrasi Adalah galat yang terjadi karena indikator berubah warna sebelum atau sesudah titik setara ditunjukkan dari kurva titrasi titik akhir titik ekivalen. Dapat disebabkan
BAB I PENDAHULUAN A. Judul Percobaan B. Tujuan Percobaan
 BAB I PENDAHULUAN A. Judul Percobaan Penentuan kadar karbonat dan bikarbonat dalam larutan. B. Tujuan Percobaan Menyelidiki kadar karbonat dan bikarbonat dalam larutan secara asidimetri dengan menggunakan
BAB I PENDAHULUAN A. Judul Percobaan Penentuan kadar karbonat dan bikarbonat dalam larutan. B. Tujuan Percobaan Menyelidiki kadar karbonat dan bikarbonat dalam larutan secara asidimetri dengan menggunakan
Modul 1 Analisis Kualitatif 1
 Modul 1 Analisis Kualitatif 1 Indikator Alami I. Tujuan Percobaan 1. Mengidentifikasikan perubahan warna yang ditunjukkan indikator alam. 2. Mengetahui bagian tumbuhan yang dapat dijadikan indikator alam.
Modul 1 Analisis Kualitatif 1 Indikator Alami I. Tujuan Percobaan 1. Mengidentifikasikan perubahan warna yang ditunjukkan indikator alam. 2. Mengetahui bagian tumbuhan yang dapat dijadikan indikator alam.
Lampiran 1. Prosedur kerja analisa bahan organik total (TOM) (SNI )
 41 Lampiran 1. Prosedur kerja analisa bahan organik total (TOM) (SNI 06-6989.22-2004) 1. Pipet 100 ml contoh uji masukkan ke dalam Erlenmeyer 300 ml dan tambahkan 3 butir batu didih. 2. Tambahkan KMnO
41 Lampiran 1. Prosedur kerja analisa bahan organik total (TOM) (SNI 06-6989.22-2004) 1. Pipet 100 ml contoh uji masukkan ke dalam Erlenmeyer 300 ml dan tambahkan 3 butir batu didih. 2. Tambahkan KMnO
LABORATORIUM ANALITIK INSTRUMEN
 LABORATORIUM ANALITIK INSTRUMEN SEMESTER GENAP TAHUN AJARAN 2012/2013 MODUL PEMBIMBING : Titrasi Konduktometri : Riniati S.Pd., M.Si. Tanggal Praktikum : 25 April 2013 Tanggal Penyerahan : 2 Mei Oleh :
LABORATORIUM ANALITIK INSTRUMEN SEMESTER GENAP TAHUN AJARAN 2012/2013 MODUL PEMBIMBING : Titrasi Konduktometri : Riniati S.Pd., M.Si. Tanggal Praktikum : 25 April 2013 Tanggal Penyerahan : 2 Mei Oleh :
LAPORAN PRATIKUM II PRATIKUM PH METER DAN PERSIAPAN LARUTAN PENYANGGA
 LAPORAN PRATIKUM II PRATIKUM PH METER DAN PERSIAPAN LARUTAN PENYANGGA NAMA : ASTRID SISKA PRATIWI (147008007) IKA WARAZTUTY (147008019) PRODI : MAGISTER ILMU BIOMEDIK TGL PRATIKUM : 10 MARET 2015 TUJUAN
LAPORAN PRATIKUM II PRATIKUM PH METER DAN PERSIAPAN LARUTAN PENYANGGA NAMA : ASTRID SISKA PRATIWI (147008007) IKA WARAZTUTY (147008019) PRODI : MAGISTER ILMU BIOMEDIK TGL PRATIKUM : 10 MARET 2015 TUJUAN
LAPORAN PRAKTIKUM 3 ph METER, BUFFER, dan PENGENCERAN DISUSUN OLEH : MARIA LESTARI DAN YULIA FITRI GHAZALI Kamis 04 Oktober s/d 16.
 LAPORAN PRAKTIKUM 3 ph METER, BUFFER, dan PENGENCERAN DISUSUN OLEH : MARIA LESTARI DAN YULIA FITRI GHAZALI Kamis 04 Oktober 2012 14.00 s/d 16.00 wib TUJUAN : 1. Agar mahasiswa dapat memahami prinsip-prinsip
LAPORAN PRAKTIKUM 3 ph METER, BUFFER, dan PENGENCERAN DISUSUN OLEH : MARIA LESTARI DAN YULIA FITRI GHAZALI Kamis 04 Oktober 2012 14.00 s/d 16.00 wib TUJUAN : 1. Agar mahasiswa dapat memahami prinsip-prinsip
UJIAN PRAKTIKUM KI2121 DASAR-DASAR KIMIA ANALITIK PENENTUAN KADAR BIKARBONAT DALAM SODA KUE
 UJIAN PRAKTIKUM KI2121 DASAR-DASAR KIMIA ANALITIK PENENTUAN KADAR BIKARBONAT DALAM SODA KUE Kelompok : Kelompok 5 Tanggal Persentasi : 14 November 2016 Tanggal Percobaan : 21 November 2016 Sahlillah Dwi
UJIAN PRAKTIKUM KI2121 DASAR-DASAR KIMIA ANALITIK PENENTUAN KADAR BIKARBONAT DALAM SODA KUE Kelompok : Kelompok 5 Tanggal Persentasi : 14 November 2016 Tanggal Percobaan : 21 November 2016 Sahlillah Dwi
III. METODOLOGI. 1. Analisis Kualitatif Natrium Benzoat (AOAC B 1999) Persiapan Sampel
 III. METODOLOGI A. BAHAN DAN ALAT Bahan-bahan yang digunakan dalam penelitian ini adalah saus sambal dan minuman dalam kemasan untuk analisis kualitatif, sedangkan untuk analisis kuantitatif digunakan
III. METODOLOGI A. BAHAN DAN ALAT Bahan-bahan yang digunakan dalam penelitian ini adalah saus sambal dan minuman dalam kemasan untuk analisis kualitatif, sedangkan untuk analisis kuantitatif digunakan
Bandung, 02 Februari Penulis, M.HAM
 KATA PENGANTAR Diakui, analisis kimia kini telah beralih dari cara konvensional ke cara instrumentasi. Namun hal ini tidaklah berarti bahwa caracara konvensional telah ditinggalkan sama sekali. Pada dasarnya,
KATA PENGANTAR Diakui, analisis kimia kini telah beralih dari cara konvensional ke cara instrumentasi. Namun hal ini tidaklah berarti bahwa caracara konvensional telah ditinggalkan sama sekali. Pada dasarnya,
Larutan penyangga dapat terbentuk dari campuran asam lemah dan basa
 Larutan penyangga dapat terbentuk dari campuran asam lemah dan basa konjugasinya atau campuran basa lemah dan asam konjugasinya. Larutan penyangga disebut juga larutan penahan atau larutan dapar atau buffer.
Larutan penyangga dapat terbentuk dari campuran asam lemah dan basa konjugasinya atau campuran basa lemah dan asam konjugasinya. Larutan penyangga disebut juga larutan penahan atau larutan dapar atau buffer.
Basic laboratory skills terampil menggunakan alat dasar
 Basic laboratory skills terampil menggunakan alat dasar Memanaskan menyaring meneteskan larutan ke dalam tabung reaksi Memastikan kesempurnaan endapan mengocok larutan melarutkan Memilih wadah untuk menimbang
Basic laboratory skills terampil menggunakan alat dasar Memanaskan menyaring meneteskan larutan ke dalam tabung reaksi Memastikan kesempurnaan endapan mengocok larutan melarutkan Memilih wadah untuk menimbang
2. Eveline Fauziah. 3. Fadil Hardian. 4. Fajar Nugraha
 Modul Praktikum Nama Pembimbing Nama Mahasiswa : Kimia Fisik : Bapak Drs.Budi Santoso, Apt.MT : 1. Azka Muhammad Syahida 2. Eveline Fauziah 3. Fadil Hardian 4. Fajar Nugraha Tanggal Praktek : 21 Semptember
Modul Praktikum Nama Pembimbing Nama Mahasiswa : Kimia Fisik : Bapak Drs.Budi Santoso, Apt.MT : 1. Azka Muhammad Syahida 2. Eveline Fauziah 3. Fadil Hardian 4. Fajar Nugraha Tanggal Praktek : 21 Semptember
Laporan Praktikum Kimia ~Titrasi asam basa~
 Laporan Praktikum Kimia ~Titrasi asam basa~ -Menentukan konsentrasi NaOH dengan HCl 0,1 M- Latifa Dinna Prayudipta XI IPA 1 SMAN 3 TANGERANG SELATAN TAHUN AJARAN 2009/2010 Laporan praktikum kimia -titrasi
Laporan Praktikum Kimia ~Titrasi asam basa~ -Menentukan konsentrasi NaOH dengan HCl 0,1 M- Latifa Dinna Prayudipta XI IPA 1 SMAN 3 TANGERANG SELATAN TAHUN AJARAN 2009/2010 Laporan praktikum kimia -titrasi
PERCOBAAN 3 REAKSI ASAM BASA
 PERCOBAAN 3 REAKSI ASAM BASA I. Teori Dasar Kita sering menjumpai asam dan basa dalam kehidupan sehari-hari. Buah-buahan, seperti jeruk, apel, dll., mengandung asam. Amonia rumah tangga, bahan pembersih,
PERCOBAAN 3 REAKSI ASAM BASA I. Teori Dasar Kita sering menjumpai asam dan basa dalam kehidupan sehari-hari. Buah-buahan, seperti jeruk, apel, dll., mengandung asam. Amonia rumah tangga, bahan pembersih,
ASIDI-ALKALIMETRI PENETAPAN KADAR ASAM SALISILAT
 ASIDI-ALKALIMETRI PENETAPAN KADAR ASAM SALISILAT I. DASAR TEORI I.1 Asidi-Alkalimetri Asidi-alkalimetri merupakan salah satu metode analisis titrimetri. Analisis titrimetri mengacu pada analisis kimia
ASIDI-ALKALIMETRI PENETAPAN KADAR ASAM SALISILAT I. DASAR TEORI I.1 Asidi-Alkalimetri Asidi-alkalimetri merupakan salah satu metode analisis titrimetri. Analisis titrimetri mengacu pada analisis kimia
METODE PENELITIAN. Penelitian ini telah dilaksanakan pada bulan April sampai September 2015 dengan
 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini telah dilaksanakan pada bulan April sampai September 2015 dengan tahapan isolasi selulosa dan sintesis CMC di Laboratorium Kimia Organik
III. METODE PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini telah dilaksanakan pada bulan April sampai September 2015 dengan tahapan isolasi selulosa dan sintesis CMC di Laboratorium Kimia Organik
LOGO TEORI ASAM BASA
 LOGO TEORI ASAM BASA TIM DOSEN KIMIA DASAR FTP 2012 Beberapa ilmuan telah memberikan definisi tentang konsep asam basa Meskipun beberapa definisi terlihat kurang jelas dan berbeda satu sama lain, tetapi
LOGO TEORI ASAM BASA TIM DOSEN KIMIA DASAR FTP 2012 Beberapa ilmuan telah memberikan definisi tentang konsep asam basa Meskipun beberapa definisi terlihat kurang jelas dan berbeda satu sama lain, tetapi
BAB IV HASIL PENELITIAN DAN PEMBAHASAN
 BAB IV HASIL PENELITIAN DAN PEMBAHASAN 4.1 Hasil Penelitian 4.1.1 Keadaan Lokasi Pengambilan Sampel Sampel yang digunakan adalah sampel bermerek dan tidak bermerek yang diambil dibeberapa tempat pasar
BAB IV HASIL PENELITIAN DAN PEMBAHASAN 4.1 Hasil Penelitian 4.1.1 Keadaan Lokasi Pengambilan Sampel Sampel yang digunakan adalah sampel bermerek dan tidak bermerek yang diambil dibeberapa tempat pasar
Praktikum Kimia Fisika II Hidrolisis Etil Asetat dalam Suasana Asam Lemah & Asam Kuat
 I. Judul Percobaan Hidrolisis Etil Asetat dalam Suasana Asam Lemah & dalam Suasana Asam Kuat II. Tanggal Percobaan Senin, 8 April 2013 pukul 11.00 14.00 WIB III. Tujuan Percobaan Menentukan orde reaksi
I. Judul Percobaan Hidrolisis Etil Asetat dalam Suasana Asam Lemah & dalam Suasana Asam Kuat II. Tanggal Percobaan Senin, 8 April 2013 pukul 11.00 14.00 WIB III. Tujuan Percobaan Menentukan orde reaksi
3 Metodologi Penelitian
 3 Metodologi Penelitian 3.1 Alat Peralatan yang digunakan dalam tahapan sintesis ligan meliputi laboratory set dengan labu leher tiga, thermolyne sebagai pemanas, dan neraca analitis untuk penimbangan
3 Metodologi Penelitian 3.1 Alat Peralatan yang digunakan dalam tahapan sintesis ligan meliputi laboratory set dengan labu leher tiga, thermolyne sebagai pemanas, dan neraca analitis untuk penimbangan
KIMIA ANALITIK TITRASI ASAM-BASA
 KIMIA ANALITIK TITRASI ASAM-BASA KIMIA ANALITIK 02 REGULER KELOMPOK 6 Disusun oleh: 1. Jang Jin Joo 1306399071 (11) 2. Robby Samuel 1306402204 (12) TEKNIK METALURGI DAN MATERIAL 2014 Pengertian Titrasi
KIMIA ANALITIK TITRASI ASAM-BASA KIMIA ANALITIK 02 REGULER KELOMPOK 6 Disusun oleh: 1. Jang Jin Joo 1306399071 (11) 2. Robby Samuel 1306402204 (12) TEKNIK METALURGI DAN MATERIAL 2014 Pengertian Titrasi
BAB III METODOLOGI PENELITIAN. Penelitian ini dilakukan di Laboratorium Penelitian Jurusan Pendidikan
 BAB III METODOLOGI PENELITIAN 3.1 Lokasi dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Penelitian Jurusan Pendidikan Kimia FPMIPA UPI. Sementara analisis dengan menggunakan instrumen dilakukan
BAB III METODOLOGI PENELITIAN 3.1 Lokasi dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Penelitian Jurusan Pendidikan Kimia FPMIPA UPI. Sementara analisis dengan menggunakan instrumen dilakukan
Bab VIII Reaksi Penetralan dan Titrasi Asam-Basa
 Bab VIII Reaksi Penetralan dan Titrasi Asam-Basa Sumber: James Mapple, Chemistry an Enquiry-Based Approach Pengukuran ph selama titrasi akan lebih akurat dengan menggunakan alat ph-meter. TUJUAN PEMBELAJARAN
Bab VIII Reaksi Penetralan dan Titrasi Asam-Basa Sumber: James Mapple, Chemistry an Enquiry-Based Approach Pengukuran ph selama titrasi akan lebih akurat dengan menggunakan alat ph-meter. TUJUAN PEMBELAJARAN
VOLUMETRI / TITRIMETRI
 VLUMETRI / TITRIMETRI Volumetri atau titrimetri merupakan suatu metode analisis kuantitatif didasarkan pada pengukuran volume titran yang bereaksi sempurna dengan analit. Titran merupakan zat yang digunakan
VLUMETRI / TITRIMETRI Volumetri atau titrimetri merupakan suatu metode analisis kuantitatif didasarkan pada pengukuran volume titran yang bereaksi sempurna dengan analit. Titran merupakan zat yang digunakan
Bab IV Hasil dan Diskusi
 Bab IV Hasil dan Diskusi IV.1 Hasil Eksperimen Eksperimen dikerjakan di laboratorium penelitian Kimia Analitik. Suhu ruang saat bekerja berkisar 24-25 C. Data yang diperoleh mencakup data hasil kalibrasi
Bab IV Hasil dan Diskusi IV.1 Hasil Eksperimen Eksperimen dikerjakan di laboratorium penelitian Kimia Analitik. Suhu ruang saat bekerja berkisar 24-25 C. Data yang diperoleh mencakup data hasil kalibrasi
ADLN - PERPUSTAKAAN UNIVERSITAS AIRLANGGA
 LAMPIRAN Lampiran 1. Data Absorbansi Larutan Naphthol Blue Black pada Berbagai Konsentrasi No. Konsentrasi (ppm) Absorbansi 1. 3 0.224 2. 4 0,304 3. 5 0,391 4. 6 0,463 5. 7 0,547 6. 8 0,616 7. 9 0,701
LAMPIRAN Lampiran 1. Data Absorbansi Larutan Naphthol Blue Black pada Berbagai Konsentrasi No. Konsentrasi (ppm) Absorbansi 1. 3 0.224 2. 4 0,304 3. 5 0,391 4. 6 0,463 5. 7 0,547 6. 8 0,616 7. 9 0,701
II. PRINSIP Elektroda gelas yang mempunyai kemampuan untuk mengukur konsentrasi H + dalam air secara potensio meter.
 ph I. TUJUAN Tujuan praktikum ini adalah mengetahui tingkat keasaman (nilai ph) suatu sampel air,konsetrasi H + yang terkandung dalam sampel air dengan menggunakan elektroda gelas yang melakukan pengukuran
ph I. TUJUAN Tujuan praktikum ini adalah mengetahui tingkat keasaman (nilai ph) suatu sampel air,konsetrasi H + yang terkandung dalam sampel air dengan menggunakan elektroda gelas yang melakukan pengukuran
Analisis Fisiko Kimia
 Analisis Fisiko Kimia POTENSIOMETRI Oleh : Dr. Harmita Tujuan Penetapan kadar secara volumetri dengan menggunakan potensiometer sebagai penunjuk titik akhir titrasi. Teori Potensiometri adalah cabang ilmu
Analisis Fisiko Kimia POTENSIOMETRI Oleh : Dr. Harmita Tujuan Penetapan kadar secara volumetri dengan menggunakan potensiometer sebagai penunjuk titik akhir titrasi. Teori Potensiometri adalah cabang ilmu
PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA
 PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA 1 Tujuan Percobaan Tujuan dari percobaan ini adalah menentukan kadar natrium karbonat dan natrium hidrogen karbonat dengan titrasi
PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA 1 Tujuan Percobaan Tujuan dari percobaan ini adalah menentukan kadar natrium karbonat dan natrium hidrogen karbonat dengan titrasi
UJIAN PRAKTIKUM KI2121 DASAR-DASAR KIMIA ANALITIK PENENTUAN KADAR KALSIUM DALAM KAPUR TULIS
 UJIAN PRAKTIKUM KI2121 DASAR-DASAR KIMIA ANALITIK PENENTUAN KADAR KALSIUM DALAM KAPUR TULIS Kelompok : Kelompok 1 Tanggal Persentasi : 14 November 2016 Tanggal Percobaan : 21 November 2016 Alfontius Linata
UJIAN PRAKTIKUM KI2121 DASAR-DASAR KIMIA ANALITIK PENENTUAN KADAR KALSIUM DALAM KAPUR TULIS Kelompok : Kelompok 1 Tanggal Persentasi : 14 November 2016 Tanggal Percobaan : 21 November 2016 Alfontius Linata
LAPORAN PRAKTIKUM KIMIA DASAR. Percobaan 3 INDIKATOR DAN LARUTAN
 LAPORAN PRAKTIKUM KIMIA DASAR Percobaan 3 INDIKATOR DAN LARUTAN Disusun oleh Nama : Cinderi Maura Restu NPM : 10060312009 Shift / kelompok : 1 / 2 Tanggal Praktikum : 29 Oktober 2012 Tanggal Laporan :
LAPORAN PRAKTIKUM KIMIA DASAR Percobaan 3 INDIKATOR DAN LARUTAN Disusun oleh Nama : Cinderi Maura Restu NPM : 10060312009 Shift / kelompok : 1 / 2 Tanggal Praktikum : 29 Oktober 2012 Tanggal Laporan :
Jenis reaksi yang terjadi pada titrimetri ini dapat dibagi menjadi 2 bagian yaitu :
 Analisis Titrimetri Analisis adalah pemeriksaan atau penentuan sesuatu bahan dengan teliti. Analisis ini dapat dibagi menjadi 2 bagian yaitu analisis kuantitatif dan analisis kulitatif. Analisis kulitatif
Analisis Titrimetri Analisis adalah pemeriksaan atau penentuan sesuatu bahan dengan teliti. Analisis ini dapat dibagi menjadi 2 bagian yaitu analisis kuantitatif dan analisis kulitatif. Analisis kulitatif
Haris Dianto Darwindra BAB V PEMBAHASAN
 BAB V PEMBAHASAN Titrasi merupakan suatu metoda untuk menentukan kadar suatu zat dengan menggunakan zat lain yang sudah diketahui konsentrasinya. Titrasi biasanya dibedakan berdasarkan jenis reaksi yang
BAB V PEMBAHASAN Titrasi merupakan suatu metoda untuk menentukan kadar suatu zat dengan menggunakan zat lain yang sudah diketahui konsentrasinya. Titrasi biasanya dibedakan berdasarkan jenis reaksi yang
Lampiran 1. Kriteria penilaian beberapa sifat kimia tanah
 30 LAMPIRAN 31 Lampiran 1. Kriteria penilaian beberapa sifat kimia tanah No. Sifat Tanah Sangat Rendah Rendah Sedang Tinggi Sangat Tinggi 1. C (%) < 1.00 1.00-2.00 2.01-3.00 3.01-5.00 > 5.0 2. N (%)
30 LAMPIRAN 31 Lampiran 1. Kriteria penilaian beberapa sifat kimia tanah No. Sifat Tanah Sangat Rendah Rendah Sedang Tinggi Sangat Tinggi 1. C (%) < 1.00 1.00-2.00 2.01-3.00 3.01-5.00 > 5.0 2. N (%)
Larutan Penyangga XI MIA
 Larutan Penyangga XI MIA Komponen Larutan Penyangga Larutan Penyangga Asam Terdiri dari Asam lemah dan basa konjugasinya (Contoh : CH 3 COOH dan CH 3 COO -, HF dan F - ) Cara membuatnya : 1. Mencampurkan
Larutan Penyangga XI MIA Komponen Larutan Penyangga Larutan Penyangga Asam Terdiri dari Asam lemah dan basa konjugasinya (Contoh : CH 3 COOH dan CH 3 COO -, HF dan F - ) Cara membuatnya : 1. Mencampurkan
LAPORAN PRAKTIKUM KIMIA FISIK BASA
 LAPORAN PRAKTIKUM KIMIA FISIK MODUL PRAKTIKUM NAMA PEMBIMBING NAMA MAHASISWA : STANDARISASI LARUTAN ASAM DAN BASA : Drs. AGUSTINUS NGATIN, MT. : SIFA FUZI ALLAWIYAH TANGGAL PRAKTEK : 9 Oktober 2013 TANGGAL
LAPORAN PRAKTIKUM KIMIA FISIK MODUL PRAKTIKUM NAMA PEMBIMBING NAMA MAHASISWA : STANDARISASI LARUTAN ASAM DAN BASA : Drs. AGUSTINUS NGATIN, MT. : SIFA FUZI ALLAWIYAH TANGGAL PRAKTEK : 9 Oktober 2013 TANGGAL
II. HARI DAN TANGGAL PERCOBAAN
 I. JUDUL PERCOBAAN Titrasi Penetralan dan Aplikasinya II. HARI DAN TANGGAL PERCOBAAN Jum at, 4 Desember 2015 III. SELESAI PERCOBAAN Jum at, 4 Desember 2015 IV. TUJUAN PERCOBAAN 1. Membuat dan menentukan
I. JUDUL PERCOBAAN Titrasi Penetralan dan Aplikasinya II. HARI DAN TANGGAL PERCOBAAN Jum at, 4 Desember 2015 III. SELESAI PERCOBAAN Jum at, 4 Desember 2015 IV. TUJUAN PERCOBAAN 1. Membuat dan menentukan
OLIMPIADE SAINS NASIONAL Ke III. Olimpiade Kimia Indonesia. Kimia UJIAN PRAKTEK
 OLIMPIADE SAINS NASIONAL Ke III Olimpiade Kimia Indonesia Kimia UJIAN PRAKTEK Petunjuk : 1. Isilah Lembar isian data pribadi anda dengan lengkap (jangan disingkat) 2. Soal Praktikum terdiri dari 2 Bagian:
OLIMPIADE SAINS NASIONAL Ke III Olimpiade Kimia Indonesia Kimia UJIAN PRAKTEK Petunjuk : 1. Isilah Lembar isian data pribadi anda dengan lengkap (jangan disingkat) 2. Soal Praktikum terdiri dari 2 Bagian:
BAB I PRAKTIKUM ASIDI AL-KALIMETRI
 BAB I PRAKTIKUM ASIDI AL-KALIMETRI I. TUJUAN a. Mahasiswa dapat menjelaskan proses titrasi asidi alkalimetri. b. Mahasiswa mampu menghitung konsentrasi sampel dengan metode asidi alkalimetri. II. DASAR
BAB I PRAKTIKUM ASIDI AL-KALIMETRI I. TUJUAN a. Mahasiswa dapat menjelaskan proses titrasi asidi alkalimetri. b. Mahasiswa mampu menghitung konsentrasi sampel dengan metode asidi alkalimetri. II. DASAR
LAPORAN INSTRUMEN DASAR PENGENALAN ALAT PH METER
 LAPORAN INSTRUMEN DASAR PENGENALAN ALAT PH METER Oleh: Khoirun Nisa ( P1337434116078) SEMESTER 1 REGULER B DIII TEKNOLOGI LABORATORIUM MEDIK POLITEKNIK KESEHATAN KEMENKES SEMARANG 2016/2017 LAPORAN INSTRUMEN
LAPORAN INSTRUMEN DASAR PENGENALAN ALAT PH METER Oleh: Khoirun Nisa ( P1337434116078) SEMESTER 1 REGULER B DIII TEKNOLOGI LABORATORIUM MEDIK POLITEKNIK KESEHATAN KEMENKES SEMARANG 2016/2017 LAPORAN INSTRUMEN
PERCOBAAN IV PEMBUATAN BUFFER Tujuan Menghitung dan pembuat larutan buffer atau dapar untuk aplikasi dalam bidang farmasi.
 A B PERCOBAAN IV PEMBUATAN BUFFER Tujuan Menghitung dan pembuat larutan buffer atau dapar untuk aplikasi dalam bidang farmasi. Dasar Teori Larutan penyangga atau larutan buffer atau larutan dapar merupakan
A B PERCOBAAN IV PEMBUATAN BUFFER Tujuan Menghitung dan pembuat larutan buffer atau dapar untuk aplikasi dalam bidang farmasi. Dasar Teori Larutan penyangga atau larutan buffer atau larutan dapar merupakan
LARUTAN PENYANGGA Bahan Ajar Kelas XI IPA Semester Gasal 2012/2013
 LARUTAN PENYANGGA [Yea r] LARUTAN PENYANGGA Bahan Ajar Kelas XI IPA Semester Gasal 2012/2013 MARI BELAJAR Indikator Produk Menjelaskan komponen pembentuk larutan penyangga dengan berpikir kritis. Menjelaskan
LARUTAN PENYANGGA [Yea r] LARUTAN PENYANGGA Bahan Ajar Kelas XI IPA Semester Gasal 2012/2013 MARI BELAJAR Indikator Produk Menjelaskan komponen pembentuk larutan penyangga dengan berpikir kritis. Menjelaskan
BAB 7. ASAM DAN BASA
 BAB 7. ASAM DAN BASA 7. 1 TEORI ASAM BASA 7. 2 TETAPAN KESETIMBANGAN PENGIONAN ASAM DAN BASA 7. 3 KONSENTRASI ION H + DAN ph 7. 4 INDIKATOR ASAM-BASA (INDIKATOR ph) 7. 5 CAMPURAN PENAHAN 7. 6 APLIKASI
BAB 7. ASAM DAN BASA 7. 1 TEORI ASAM BASA 7. 2 TETAPAN KESETIMBANGAN PENGIONAN ASAM DAN BASA 7. 3 KONSENTRASI ION H + DAN ph 7. 4 INDIKATOR ASAM-BASA (INDIKATOR ph) 7. 5 CAMPURAN PENAHAN 7. 6 APLIKASI
METODOLOGI PENELITIAN. sampel dilakukan di satu blok (25 ha) dari lahan pe rkebunan kelapa sawit usia
 III. METODOLOGI PENELITIAN 3.1. Waktu dan Tempat Penelitian ini dilaksanakan pada bulan April 2014 s/d juni 2014. Lokasi penelitian dilaksanakan di perkebunan PT. Asam Jawa Kecamatan Torgamba, Kabupaten
III. METODOLOGI PENELITIAN 3.1. Waktu dan Tempat Penelitian ini dilaksanakan pada bulan April 2014 s/d juni 2014. Lokasi penelitian dilaksanakan di perkebunan PT. Asam Jawa Kecamatan Torgamba, Kabupaten
LAMPIRAN A PROSEDUR ANALISIS
 LAMPIRAN A PROSEDUR ANALISIS A.1 Pengujian Viskositas (menggunakan viskosimeter) (Jacobs, 1958) Viskositas Saos Tomat Kental diukur dengan menggunakan viskosimeter (Rion Viscotester Model VT-04F). Sebelum
LAMPIRAN A PROSEDUR ANALISIS A.1 Pengujian Viskositas (menggunakan viskosimeter) (Jacobs, 1958) Viskositas Saos Tomat Kental diukur dengan menggunakan viskosimeter (Rion Viscotester Model VT-04F). Sebelum
HASIL KALI KELARUTAN (Ksp)
 LAPORAN PRAKTIKUM KIMIA FISIKA HASIL KALI KELARUTAN (Ksp) NAMA : YUSI ANDA RIZKY NIM : H311 08 003 KELOMPOK : II (DUA) HARI/TGL PERC. : SENIN/08 MARET 2010 ASISTEN : FITRI JUNIANTI LABORATORIUM KIMIA FISIKA
LAPORAN PRAKTIKUM KIMIA FISIKA HASIL KALI KELARUTAN (Ksp) NAMA : YUSI ANDA RIZKY NIM : H311 08 003 KELOMPOK : II (DUA) HARI/TGL PERC. : SENIN/08 MARET 2010 ASISTEN : FITRI JUNIANTI LABORATORIUM KIMIA FISIKA
PRAKTIKUM KIMIA ANALITIK II
 PRAKTIKUM KIMIA ANALITIK II PENENTUAN KADAR KLORIDA Selasa, 1 April 2014 EKA NOVIANA NINDI ASTUTY 1112016200016 PROGRAM STUDI PENDIDIKAN KIMIA JURUSAN PEDIDIKAN ILMU PENGETAHUAN ALAM FAKULTAS ILMU TARBIYAH
PRAKTIKUM KIMIA ANALITIK II PENENTUAN KADAR KLORIDA Selasa, 1 April 2014 EKA NOVIANA NINDI ASTUTY 1112016200016 PROGRAM STUDI PENDIDIKAN KIMIA JURUSAN PEDIDIKAN ILMU PENGETAHUAN ALAM FAKULTAS ILMU TARBIYAH
LAPORAN PRAKTIKUM KIMIA FISIKA II PENENTUAN LAJU REAKSI DAN TETAPAN LAJU
 LAPORAN PRAKTIKUM KIMIA FISIKA II PENENTUAN LAJU REAKSI DAN TETAPAN LAJU Nama NIM Prodi Anggota kelompok Disusun oleh: : Edi Siswanto : H13112071 : Kimia : 1. Alpius Suriadi 2. Gloria Sindora 3. Indri
LAPORAN PRAKTIKUM KIMIA FISIKA II PENENTUAN LAJU REAKSI DAN TETAPAN LAJU Nama NIM Prodi Anggota kelompok Disusun oleh: : Edi Siswanto : H13112071 : Kimia : 1. Alpius Suriadi 2. Gloria Sindora 3. Indri
BAB III METODOLOGI PENELITIAN. Penelitian ini dilaksanakan di Laboratorium Jurusan Pendidikan Kimia dan
 BAB III METODOLOGI PENELITIAN 3.1 Tempat dan Waktu Penelitian 3.1.1 Tempat Penelitian Penelitian ini dilaksanakan di Laboratorium Jurusan Pendidikan Kimia dan Laboratorium Jurusan Pendidikan Biologi FMIPA
BAB III METODOLOGI PENELITIAN 3.1 Tempat dan Waktu Penelitian 3.1.1 Tempat Penelitian Penelitian ini dilaksanakan di Laboratorium Jurusan Pendidikan Kimia dan Laboratorium Jurusan Pendidikan Biologi FMIPA
Tentukan ph dari suatu larutan yang memiliki konsentrasi ion H + sebesar 10 4 M dengan tanpa bantuan alat hitung kalkulator!
 Kimia Study Center - Contoh soal dan pembahasan tentang cara menghitung ph dan poh larutan asam basa berdasarkan konsentrasi ion [H + ] dan [OH ] SMA kelas 11 IPA. Berikut contoh-contoh soal yang bisa
Kimia Study Center - Contoh soal dan pembahasan tentang cara menghitung ph dan poh larutan asam basa berdasarkan konsentrasi ion [H + ] dan [OH ] SMA kelas 11 IPA. Berikut contoh-contoh soal yang bisa
BAB IV TEMUAN DAN PEMBAHASAN. Untuk mengembangkan strategi pembelajaran pada materi titrasi asam basa
 BAB IV TEMUAN DAN PEMBAHASAN Untuk mengembangkan strategi pembelajaran pada materi titrasi asam basa dilakukan tiga tahap yaitu tahap pertama melakukan analisis standar kompetensi dan kompetensi dasar
BAB IV TEMUAN DAN PEMBAHASAN Untuk mengembangkan strategi pembelajaran pada materi titrasi asam basa dilakukan tiga tahap yaitu tahap pertama melakukan analisis standar kompetensi dan kompetensi dasar
Lampiran 1. Laporan Hasil Pengujian Residu Pestisida
 LAMPIRAN Lampiran 1. Laporan Hasil Pengujian Residu Pestisida 53 Lampiran 2. Aplikasi Dosis Herbisida Selama 1 Musim Tanam No Blok Kebun Petak Luas (Ha) Aplikasi 1 (Liter) Aplikasi 2 (Liter) Ametryn 2,4-D
LAMPIRAN Lampiran 1. Laporan Hasil Pengujian Residu Pestisida 53 Lampiran 2. Aplikasi Dosis Herbisida Selama 1 Musim Tanam No Blok Kebun Petak Luas (Ha) Aplikasi 1 (Liter) Aplikasi 2 (Liter) Ametryn 2,4-D
PERCOBAAN I PEMBUATAN DAN PENENTUAN KONSENTRASI LARUTAN
 PERCOBAAN I PEMBUATAN DAN PENENTUAN KONSENTRASI LARUTAN I. TUJUAN PERCOBAAN Tujuan percobaan praktikum ini adalah agar praktikan dapat membuat larutan dengan konsentrasi tertentu, mengencerkan larutan,
PERCOBAAN I PEMBUATAN DAN PENENTUAN KONSENTRASI LARUTAN I. TUJUAN PERCOBAAN Tujuan percobaan praktikum ini adalah agar praktikan dapat membuat larutan dengan konsentrasi tertentu, mengencerkan larutan,
BAB 6. Jika ke dalam air murni ditambahkan asam atau basa meskipun dalam jumlah. Larutan Penyangga. Kata Kunci. Pengantar
 Kimia XI SMA 179 BAB 6 Larutan Penyangga Tujuan Pembelajaran: Setelah mempelajari bab ini, Anda diharapkan mampu: 1. Menjelaskan pengertian larutan penyangga dan komponen penyusunnya. 2. Merumuskan persamaan
Kimia XI SMA 179 BAB 6 Larutan Penyangga Tujuan Pembelajaran: Setelah mempelajari bab ini, Anda diharapkan mampu: 1. Menjelaskan pengertian larutan penyangga dan komponen penyusunnya. 2. Merumuskan persamaan
BAB III METODOLOGI PENELITIAN
 20 BAB III METODOLOGI PENELITIAN Percobaan yang dilakukan pada penelitian ini yaitu membuat nata dari kulit pisang dengan menggunakan sumber nitrogen alami dari ekstrak kacang hijau. Nata yang dihasilkan
20 BAB III METODOLOGI PENELITIAN Percobaan yang dilakukan pada penelitian ini yaitu membuat nata dari kulit pisang dengan menggunakan sumber nitrogen alami dari ekstrak kacang hijau. Nata yang dihasilkan
DERAJAT KEASAMAN (ph)
 LAPORAN PRAKTIKUM KIMIA DASAR DERAJAT KEASAMAN (ph) DISUSUN OLEH FAISAL ARSYAD (13513128) NURUL FIKRI (13513136) JURUSAN TEKNIK LINGKUNGAN FAKULTAS TEKNIK SIPIL DAN PERENCANAAN UNIVERSITAS ISLAM INDONESIA
LAPORAN PRAKTIKUM KIMIA DASAR DERAJAT KEASAMAN (ph) DISUSUN OLEH FAISAL ARSYAD (13513128) NURUL FIKRI (13513136) JURUSAN TEKNIK LINGKUNGAN FAKULTAS TEKNIK SIPIL DAN PERENCANAAN UNIVERSITAS ISLAM INDONESIA
BAB III METODOLOGI PENELITIAN. waterbath, set alat sentrifugase, set alat Kjedalh, AAS, oven dan autoklap, ph
 BAB III METODOLOGI PENELITIAN 3.1. Alat dan Bahan Dalam pembuatan dan analisis kualitas keju cottage digunakan peralatan waterbath, set alat sentrifugase, set alat Kjedalh, AAS, oven dan autoklap, ph meter,
BAB III METODOLOGI PENELITIAN 3.1. Alat dan Bahan Dalam pembuatan dan analisis kualitas keju cottage digunakan peralatan waterbath, set alat sentrifugase, set alat Kjedalh, AAS, oven dan autoklap, ph meter,
Kimia Study Center - Contoh soal dan pembahasan tentang hidrolisis larutan garam dan menentukan ph atau poh larutan garam, kimia SMA kelas 11 IPA.
 Kimia Study Center - Contoh soal dan pembahasan tentang hidrolisis larutan garam dan menentukan ph atau poh larutan garam, kimia SMA kelas 11 IPA. Soal No. 1 Dari beberapa larutan berikut ini yang tidak
Kimia Study Center - Contoh soal dan pembahasan tentang hidrolisis larutan garam dan menentukan ph atau poh larutan garam, kimia SMA kelas 11 IPA. Soal No. 1 Dari beberapa larutan berikut ini yang tidak
Reaksi dalam larutan berair
 Reaksi dalam larutan berair Drs. Iqmal Tahir, M.Si. iqmal@gadjahmada.edu Larutan - Suatu campuran homogen dua atau lebih senyawa. Pelarut (solven) - komponen dalam larutan yang membuat penuh larutan (ditandai
Reaksi dalam larutan berair Drs. Iqmal Tahir, M.Si. iqmal@gadjahmada.edu Larutan - Suatu campuran homogen dua atau lebih senyawa. Pelarut (solven) - komponen dalam larutan yang membuat penuh larutan (ditandai
TITRASI KOMPLEKSOMETRI
 TITRASI KOMPLEKSOMETRI I. TUJUAN a. Menstandarisasi EDTA dengan larutan ZnSO 4 b. Menentukan konsentrasi larutan Ni 2+ c. Memahami prinsip titrasi kompleksometri II. TEORI Titrasi kompleksometri adalah
TITRASI KOMPLEKSOMETRI I. TUJUAN a. Menstandarisasi EDTA dengan larutan ZnSO 4 b. Menentukan konsentrasi larutan Ni 2+ c. Memahami prinsip titrasi kompleksometri II. TEORI Titrasi kompleksometri adalah
LAPORAN PRAKTIKUM KIMIA ANALITIK 2. Titrasi Permanganometri. Selasa, 6 Mei Disusun Oleh: Yeni Setiartini. Kelompok 3: Fahmi Herdiansyah
 LAPORAN PRAKTIKUM KIMIA ANALITIK 2 Titrasi Permanganometri Selasa, 6 Mei 2014 Disusun Oleh: Yeni Setiartini 1112016200050 Kelompok 3: Fahmi Herdiansyah Huda Rahmawati Aida Nadia Rizky Harry Setiawan. PROGRAM
LAPORAN PRAKTIKUM KIMIA ANALITIK 2 Titrasi Permanganometri Selasa, 6 Mei 2014 Disusun Oleh: Yeni Setiartini 1112016200050 Kelompok 3: Fahmi Herdiansyah Huda Rahmawati Aida Nadia Rizky Harry Setiawan. PROGRAM
