BAB VIII STRUKTUR ATOM
|
|
|
- Hartono Indradjaja
- 7 tahun lalu
- Tontonan:
Transkripsi
1 BAB VIII STRUKTUR ATOM Pengertian mengenai struktur atom berguna untuk menjelaskan gaya-gaya diantara atom yang akhirnya mengarah pada pembentukan molekul. Dalam bab ini akan dipelajari struktur listrik atom yang diartikan sebagai : di mana elektron dalam suatu atom paling mungkin diternukan Partikel Penyusun Atom Teori atom Dalton yang dikembangkan selama periode didasarkan atas tiga asumsi pokok : 1. Tiap unsur kimia tersusun atas partikei terkecil yang disebut atom. Selama perubahan kimia, atom tidak bisa diciptakan ataupun dimusnahkan. 2. Semua atom dari suatu unsur mempunyai massa (berat) dan sifat yang sama. Atom-atom dari unsur yang berbeda massa dan sifat-sifatnya berlainan. 3. Dalam senyawa kimia, atom-atom dari unsur yang berlainan melakukan ikatan dengan perbandingan numerik sederhana. Teori Dalton tentang atom diterima oleh kebanyakan ilmuwan. Konsepnya hampir 100 tahun, turut berperan dalam mendorong terciptanya karya-karya eksperimen dari para ahli kimia dan fisika. Namun menjelang akhir tahun 1803, teori atom Dalton tumbang oleh sederetan penemuan mutakhir, misalnya sinar-x (1895), radioaktif (1896), elektron (1897) dan radium (1898). Studi atas gejala-gejala tersebut menunjukkan bahwa atom merupakan struktur yang rumit yang dibangun oleh partikel-partikel penyusun atom. Berbagai penelitian mengenai bangun atom dilakukan. Michael Faraday mengemukakan hasil eksperimen kuantitafnya mengenai elektrolisa. Kenyataan bahwa arus listrik dapat menyebabkan penguraian, menunjukkan adanya hubungan antara listrik dan zat. Karena zat (materi) terdiri atas atom-atom maka atom-atom tentunya mempunyai struktur yang bersifat listrik. Sebelum sampai pada bahasan mengenai penemuan partikel subatom, akan dikemukakan ciri benda bermuatan listrik : 1. Suatu arus listrik ialah gerakan partikel bermuatan dalam suatu penghantar. 2. Partikel dengan mualan yang berlawanan saling menarik sedangkan yang muatannya berlawanan akan saling tolak. 3. Partikel bermuatan dapat bergerak di antara kawat atau lempeng bermuatan yang disebut elektrode. Elektrode bermuatan positif disebut anode dan yang bermuatan negatif disebut katode Penemuan Elektron Penelitian mengenai bangun atom antara lain didasarkan pada eksperimen yang dilakukan dengan tabung (kaca) hampa atau tabung sinar katoda. Sir William Crookes merancang suatu tabung hampa yang merupakan penyempurnaan dari tabung sinar katoda yang disebut Tabung Crookes. 1
2 Jika dua kawat diberi potensial listrik yang tinggi kemudian didekatkan, akan terjadi bunga api dari satu kawat ke kawat lain. Bila ujung kawat ditaruh dalam tabung hampa akan terlihat adanya bara hijau kekuningan dari arah katode. Sinar ini disebut Sinar Katoda. Sifat-sifat sinar katoda disimpulkan oleh Plucker, Hittorf, Crookes dan Thomson sebagai berikut : 1. Sinar katoda dipancarkan oleh katoda dalam sebuah tabung hampa bila dilewati arus listrik 2. Sinar katoda berjalan dalam garis lurus 3. Sinar katoda bila membentur gelas atau benda tertentu akan mengeluarkan cahaya sehingga dapat disimpulkan bahwa sinar katoda terdiri atas partikelpartikel 4. Sinar katode dibelokkan oleh medan listrik dan magnet ke arah partikel yang diketahui bermuatan negatif 5. Sifat sinar katoda tidak dipengaruhi oleh bahan elektroda (besi, platina, dan. lain-lain). Dari kelima sifat tersebut, disimpulkan bahwa sinar katoda terdiri dari partikelpartikel yang bermuatan negatif dan diberi nama elektron oleh Joseph John Thomson. J. J. Thomson berhasil menentukan harga ratio muatan elektron terhadap massa elektron (e/m) yaitu sebesar -1,76 x 10 8 coulomb/gram. Sementara itu Robert Andrew Millikan (1917) berhasil menentukan harga muatan mutlak dari elektron yaitu sebesar -1,6022 x coulomb. Dengan demikian massa elektron dapat dihitung yaitu sebesar 9,1 x gram Penemuan Proton Pada tahun 1886 Eugene Goldstein dengan memakai tabung Crookes yang dilubangi katodenya, dapat mengamati sinar yang menembus lubang-lubang tersebut. Sinar ini disebut Sinar Saluran. Ternyata sinar saluran ini terdiri atas partikel-partikel bermuatan positif. Partikel tersebut memiliki muatan yang sama dengan elektron tetapi nilainya positif (+1,76 x coulomb). Partikel ini kemudian diberi nama proton. Massa proton dihitung oleh J.J Thomson yaitu sebesar 1,67 x gram atau hampir 1840 kali massa elektron Penemuan Neutron Pada tahun 1932 James Chadwick berhasil menemukan partikel sub-atom yang ketiga yang disebut neutron. Neutron adalah partikel yang tidak bermuatan ( = 0) dan massanya hampir sama dengan massa proton (1,674 x gram). Berdasarkan eksperimen-eksperirnen yang dilakukan, dapat dibuktikan bahwa atom terdiri atas partikel-partikel subatom yaitu proton, elektron dan neutron. Tabel 8.1. Sifat-sifat Partikel Subatom Muatan Massa Partikel Lambang Metrik (Coulomb) Atomik Metrik (gram) Atomik (sma) Elektron Proton Neutron -1e 0 +1p 0 0n 1-1,602 x ,602 x ,1 x ,670 x ,674 x , ,0073 1,0087 Keterangan: sma = satuan massa atom 2
3 8.2. PERKEMBANGAN MODEL ATOM Setelah diketahui bahwa suatu atom tersusun atas tiga partikel dasar. Selanjutnya dipertanyakan bagaimana partikel subatom ditata dalam atom. Dalam perkembangannya terdapat empat gagasan model atom yang dikemukakan Model Atom Thomson Model atom yang dikemukakan oleh JJ.Thomson lebih dikenal dengan istilah model atom roti kismis. Gambar Model Atom Thomson Menurut Thomson : Atom merupakan bola bermuatan positif dan di dalamnya pada tempat tertentu terdapat elektron, sehingga atom secara keseluruhan bermuatan netral Model atom Thomson mempunyai banyak kelemahan dan tidak dapat dipertahankan Model Atom Rutherford Ernest Rutherford (1911) menguji kebenaran dari model atom Thomson dan mengemukakan pendapatnya berdasarkan percobaan yang dilakukannya. Gambar Model Atom Rutherford dan Lintasan Spiral Menurut E. Rutherford : Atom terdiri dan inti atom yang bermuatan positif dan dikelilingi oleh elektron-elektron yang bermuatan negatif yang bergerak mengelilingi inti atom dengan lintasan yang berbentuk elips. Model atom Rutherford pun mempunyai beberapa kelemahan, antara lain: 1. Lintasan akan berbentuk spiral Hal ini tidak sesuai dengan teori fisika klasik yang menyatakan bahwa bila suatu partikel bermuatan (elektron) mengelilingi inti, maka energinya akan berkurang. Suatu saat elektron akan jatuh ke inti dan atom jadi tidak stabil (ambruk). Padahal kenyataannya atom stabil. 2. Tidak dapat menerangkan spektrum hidrogen 3
4 Menurut Rutherford spektrum atom adalah spektrum kontinu. Kenyataannya spektrum atom adalah spektrum garis. Artinya bila suatu atom menyala hanya akan memancarkan warna-warna tertentu Model Atom Bohr Niels Bohr (1913) berusaha memperbaiki model atom Rutherford. Gagasan Bohr mengenai susunan atom adalah: Elektron bergerak mengelilingi inti dengan lintasan tertentu sehingga elektron berada pada tingkat energi tertentu sesuai dengan lintasannya. Elektron dapat berpindah dan lintasan yang satu ke lintasan lain dengan memancarkan atau menyerap energi. Selama elektron berada dalam lintasannya, tidak terjadi penyerapan atau pemancaran energi. Gambar Model Atom Bohr Model atom Bohr pun menemui kegagalan karena tidak dapat menerangkan spektrum atom yang lebih rumit. Bohr hanya mampu menerangkan spektrum atom hidrogen Model Atom Mekanika Kuantum Merupakan penyempurnaan dari model atom Bohr. Mekanika kuantum (mekanika gelombang) merupakan bentuk teori kuantum yang didasarkan pada konsep dualitas gelombang-partikel, prinsip ketidakpastian dan pandangan elektron sebagai gelombang materi. Model atom mekanika kuantum merupakan gambaran matematik mengenai hukum-hukum gerakan yang diaplikasikan pada partikel yang sangat kecil (elektron) yang dapat bersifat pasti, sebagai partikel atau gelombang. Dengan teori ini energi masing-masing elektron dapat dihitung secara matematik. Model atom Mekanika kuantum menyatakan bahwa : Posisi elektron di dalam atom tidak dapat ditentukan dengan pasti. Hanya dapat diperkirakan kemungkinan ditemukannya elektron pada suatu tempat tertentu, yang disebut orbital. Menurut teori ini elektron-elektron dalam suatu atom menempati beberapa tingkat energi (sering disebut sebagai kulit) disekeliling inti dan setiap tingkat energi terdiri dari beberapa subtingkat energi (atau subkulit) serta setiap subtingkat energi terdiri atas satu atau lebih orbital. Orbital adalah suatu daerah dalam ruang berbentuk spesifik dan dalam daerah ini besar kemungkinan ditemukannya elektron. Dengan mekanika kuantum dapat dibuktikan bahwa elektron yang dapat menempati kulit tertentu, jumlahnya terbatas. Model atom mekanika kuantum merupakan model yang paling baik dan dipakai hingga saat ini. 4
5 8.3. ELEKTRON DALAM ATOM Berdasarkan teori mekanika kuantum, elektron-elektron dalam atom tersusun dalam berbagai tingkat energi (kulit), subtingkat energi (subkulit) dan orbital. Kulit-kulit yang terletak paling dekat ke inti memiliki energi terendah; dan diberi simbol huruf K. Dan seterusnya semakin jauh dan inti diberi simbol L, M, N, dan energinya semakin tinggi. Dengan demikian tingkat-tingkat energi memiliki energi yang berbeda. Setiap kulit tersusun atas subkulit-subkulit yang diberi simbol s, p, d, dan f. Subkulit s memiliki energi yang lebih rendah dibandingkan subkulit p dan seterusnya. Dengan demikian subkulit memiliki energi yang berbeda. Setiap subkulit terdiri atas satu atau lebih orbital. Setiap orbital dalam subkulit mempunyai energi yang sama. Banyaknya orbital dalam subkulit tergantung macam kulitnya. Pada Tabel 8.2. dituliskan macam kulit, sub-kulit dan jumlah orbital dari empat kulit pertama. Tabel 8.2. Kulit, Sub-kulit dan Jumlah Orbital pada 4 Kulit Pertama Bilangan Kuantum Untuk menerangkan kedudukan elektron di dalam atom, Shcrodinger menyusun persamaan matematik yang sangat rumit yang disebut persamaan Schrodinger. Penyelesaian persamaan ini untuk atom H (atom paling sederhana) dapat memberikan informasi mengenai orbital-orbital atom yaitu mengenai besarnya, bentuknya dan kedudukannya dalam ruang. Informasi ini dapat diperoleh dari jawaban-jawaban yang mungkin dari persamaan Schrodinger. Setiap jawaban yang mungkin menghasilkan suatu kumpulan yang terdiri atas tiga bilangan kuantum, yaitu bilangan kuantum utama (n), bilangan kuantum azimuth (l) dan bilangan kuantum magnetik (m). Ketiga bilangan kuantum ini saling berhubungan. 5
6 Selanjutnya untuk membedakan elektron dalam suatu orbital adalah berdasarkan arah putarannya (berlawanan) yaitu dengan bilangan kuantum spin (s). Dengan demikian posisi atau kedudukan elektron di dalam suatu atom ditentukan oleh keempat bilangan kuantum Bilangan Kuantum Utama (n) Menentukan tingkat energi elektron atau menunjukkan besarnya orbital yang ditempati oleh elektron atau jaraknya dari inti. Bilangan kuantum utama hanya mempunyai harga positif dan bilangan bulat bukan nol, yaitu n = 1, 2, 3, 4,... Angka-angka tersebut mewakili simbol huruf (K, L, M, N,...) yang telah dikemukakan sebelumnya Bilangan Kuantum Azimut (l) Menunjukkan subtingkat energi atau bentuk geometrik orbital yang ditempati oleh elektron. Harga bilangan kuantum azimut bergantung pada harga bilangan kuantum utama (n). Harga yang mungkin adalah nol atau bilangan bulat positif yaitu l = 0, 1, 2, 3,... n-1. Angka-angka tersebut mewakili gimbal humf s, p, d,.. untuk subtingkat energi Bilangan Kuantum Magnetik (m) Menunjukkan kedudukan orbital yang ditempati oleh elektron. Harganya ditentukan oleh harga bilangan kuantum azimut (l). Untuk setiap harga l tertentu, nilai m adalah -1 sampai +1. Dengan demikian nilai m adalah bilangan bulat (negatif, nol dan positif). Setiap nilai m menunjukkan orbitalnya Bilangan Kuantum Spin (s) Menunjukkan arah perputaran elektron pada sumbunya. Ada dua kemungkinan arah yaitu searah jarum jam dinyatakan dengan harga ½ atau berlawanan arah jarum jam dinyatakan dengan harga + ½. Karena hanya terdapat dua arah perputaran, maka di dalam setiap orbital hanya terdapat 2 elektron, yaitu elektron pertama dengan s = + ½ dan elektron kedua dengan s = - ½. Berdasarkan hal tersebut, tidak mungkin di dalam suatu atom yang sama memiliki empat bilangan kuantum yang sama. Bila n, l, dan m nya sama, pasti s- nya berbeda. 6
7 Tabel 8.3..Jumlah Elektron pada Kulit dan Subkulit Keterangan : * = jumlah orbital (berdasarkan harga m; setiap harga m menunjukkan 1 orbital) ** = jumlah elektron maksimum per orbital *** = jumlah elektron maksimum dalam setiap sub kulit **** = jumlah elektron maksimum dalam setiap kulit Mengingat jumlah elektron maksimum yang terdapat dalam satu orbital hanya dua, maka dapat ditentukan jumlah elektron maksimum yang dapat berada pada suatu subkulit atau pada kulit tertentu. Bentuk Orbital Setiap jenis orbital s,p,d, dan f mempunyai bentuk geometri yang khas : a. Orbital s berbentuk bola b. Orbital p berbentuk seperti balon terpilin c. Orbital d bentuknya agak rumit d. Orbital f bentuknya sangat rumit sehingga sulit digambarkan 7
8 Konfigurasi Elektron Gambaran penyebaran elektron yang paling mungkin ke dalam orbital-orbital kulit elektron dinamakan konfigurasi elektron. Ada tiga aturan atau prinsip yang harus dipertimbangkan dalam penentuan konfigurasi clektron suatu atom dan prinsip ini berlaku untuk semua unsur. 1. Aturan Aufbau Elektron menempati orbital sedemikian rupa untuk meminimumkan energi atom tersebut Dengan kata lain aturan atau proses Aufbau menunjukkan cara pengisian elektron dengan urutan energi orbital dari yang terendah ke yang tertinggi. Elektron mulai mengisi orbital pada kulit (tingkat energi) terendah digambarkan pada diagram berikut: Gambar Urutan Pengisian Elektron Berdasarkan Aturan Aufbau Berdasarkan diagram di atas, maka dengan mudah dapat dituliskan konfigurasi elektron untuk setiap unsur. Misalnya : 1H = 1 s 1 11Na = 1s 2 2s 2 2p 6 3s 1 19K = 1s 2 2s 2 2p 6 3S 2 3p 6 4s 1 Namun untuk unsur dengan tingkat energi yang tinggi (nomor atom besar) terdapat penyimpangan dari pengisian elektron ke dalam orbital, yaitu : 1. Pada orbital 4f dan 5d Satu elektron masuk ke orbital 5d, kemudian masuk ke 4f sampai penuh. Misalnya pada unsur 57La 2. Pada orbital 5f dan 6d Misalnya pada unsur 92U Kedua penyimpangan tersebut terjadi karena pada tingkat energi yang tinggi terjadi pertumpangtindihan sehingga orbital-orbital berada sangat berdekatan. 8
9 2. Aturan Hund Menurut aturan ini pada sekumpulan orbital yang mempunyai energi sama (misalnya ketiga orbital p), masuknya elektron kedua ke dalam suatu orbital tidak akan terjadi sebelum semua orbital pada subkulit yang bersangkutan terisi masing-masing dengan satu elektron. Akibatnya atom cenderung mempunyai sebanyak mungkin elektron tak berpasangan. Sifat ini dapat diterima karena semua elektron membawa muatan listrik yang sama sehingga mereka mencari orbital kosong yang energinya sama, sebelum berpasangan dengan elektron yang telah mengisi orbital setengah penuh. Tabel 8. 4 Diagram Orbital Sepuluu Unsur Pertama 3. Prinsip Larangan Pauli Prinsip ini menyatakan bahwa dalam suatu atom yang sama tidak mungkin ada dua elektron dengan keempat bilangan kuantum yang sama. Berdasarkan prinsip ini suatu orbital hanya dapat diisi maksimum oleh dua elektron UNSUR-UNSUR KIMIA Sebanyak 106 unsur kimia telah diketahui Tiap unsur kimia mempunyai nama dan lambang. Lambang kimia merupakan bentuk singkatan sederhana dari nama Inggris, Latin atau nama penemunya. Lambang tersebut terdiri dari satu atau dua huruf. Misalnya : Oksigen ditulis O (Inggris) Ferrum ditulis Fe (Latin) Wolfram ditulis W (nama penemunya) 9
10 Nomor Atom dan Nomor Massa Setiap unsur kimia diberi nomor yang disebut nomor atom dan nomor massa : Dimana : X = lambang unsur A = nomor massa Z = nomor atom Z X Nomor Atom Pada atom netral (tidak dalam bentuk ionnya) nomor atom menunjukkan jumlah proton dan sekaligus jumlah elektron yang mengelilingi inti atom. Misalnya 6C berarti 6 proton dan 6 elektron. Nomor atom merupakan sifat yang menentukan perilaku kimianya, sehingga jenis atom dicirikan oleh nomor atomnya. Nomor Massa Menunjukkan jumlah proton dan neutron di dalam inti atom. Misalnya : 11Na 23, artinya atom Na memiliki 11 proton dan 11 elektron dan jumlah neutronnya = no massa proton = = 12 n Untuk atom yang berubah menjadi ion, yang berubah adalah jumlah elektronnya. Jumlah proton dan neutronnya tetap. Misalnya pada ion Na + dan ion Cl. a. ion Na + = 11 p, 12 n dan 10 e b. ion Cl = 17 p, 18 n dan 18 e Isotop Thomson menemukan adanya atom-atom dari unsur yang sama, namun ternyata massanya sedikit berbeda. Keadaan tersebut dikenal sebagal isotop. Pengertian dari isotop adalah atom-atom suatu unsur yang karena perbedaan jumlah neutron dalam intinya mengakibatkan perbedaan massa. Dalam bahasa yang sederhana isotop adalah atom-atom yang memiliki nomor atom sama tetapi nomor massa berbeda. Misalnya : Isotop Neon (Ne) : 10Ne 20 : terdiri dari 10 proton, 10 elektron dan 10 neutron 10Ne 21 : terdiri dari 10 proton, 10 elektron dan 11 neutron 10Ne 22 : terdiri dart 10 proton, 10 elektron dan 12 neutron A 10
(I) MATERI. Pengertian materi sifat materi, Perubahan materi, Klasifikasi materi, serta hukum-hukum yang berhubungan dengan materi.
 (I) MATERI Pengertian materi sifat materi, Perubahan materi, Klasifikasi materi, serta hukum-hukum yang berhubungan dengan materi. Ilmu kimia Merupakan bagian dari ilmu pengetahuan alam yang mempelajari
(I) MATERI Pengertian materi sifat materi, Perubahan materi, Klasifikasi materi, serta hukum-hukum yang berhubungan dengan materi. Ilmu kimia Merupakan bagian dari ilmu pengetahuan alam yang mempelajari
BAB I MATERI. Perb kimia. Unsur : Senyawa : Zat yang tidak dapat dipisahkan lagi. Kombinasi kimia dari dua atau lebih unsur.
 BAB I MATERI Materi adalah sesuatu yang menempati ruang dan memiliki massa. Ilmu kimia adalah ilmu yang mempelajari materi dan perubahan yang terjadi pada materi tersebut.sifat dan perubahan materi dapat
BAB I MATERI Materi adalah sesuatu yang menempati ruang dan memiliki massa. Ilmu kimia adalah ilmu yang mempelajari materi dan perubahan yang terjadi pada materi tersebut.sifat dan perubahan materi dapat
STRUKTUR ATOM. Perkembangan Teori Atom
 STRUKTUR ATOM Perkembangan Teori Atom 400 SM filsuf Yunani Demokritus materi terdiri dari beragam jenis partikel kecil 400 SM dan memiliki sifat dari materi yang ditentukan sifat partikel tersebut Dalton
STRUKTUR ATOM Perkembangan Teori Atom 400 SM filsuf Yunani Demokritus materi terdiri dari beragam jenis partikel kecil 400 SM dan memiliki sifat dari materi yang ditentukan sifat partikel tersebut Dalton
STRUKTUR ATOM A. PENGERTIAN DASAR
 STRUKTUR ATOM A. PENGERTIAN DASAR 1. Partikel dasar : partikel-partikel pembentuk atom yang terdiri dari elektron, proton den neutron. 1. Proton : partikel pembentuk atom yang mempunyai massa sama dengan
STRUKTUR ATOM A. PENGERTIAN DASAR 1. Partikel dasar : partikel-partikel pembentuk atom yang terdiri dari elektron, proton den neutron. 1. Proton : partikel pembentuk atom yang mempunyai massa sama dengan
Bunyi Teori Atom Dalton:
 Bunyi Teori Atom Dalton: Pada 1808, ilmuwan berkebangsaan Inggris, John Dalton, mengemuka- kan teorinya tentang materi atom yang dipublikasikan dalam A New System of Chemical Philosophy. Berdasarkan penelitian
Bunyi Teori Atom Dalton: Pada 1808, ilmuwan berkebangsaan Inggris, John Dalton, mengemuka- kan teorinya tentang materi atom yang dipublikasikan dalam A New System of Chemical Philosophy. Berdasarkan penelitian
BAB 1 PERKEMBANGAN TEORI ATOM
 BAB 1 PERKEMBANGAN TEORI ATOM 1.1 Teori Atom Perkembangan teori atom merupakan sumbangan pikiran dari banyak ilmuan. Konsep dari suatu atom bukanlah hal yang baru. Ahli-ahli filsafah Yunani pada tahun
BAB 1 PERKEMBANGAN TEORI ATOM 1.1 Teori Atom Perkembangan teori atom merupakan sumbangan pikiran dari banyak ilmuan. Konsep dari suatu atom bukanlah hal yang baru. Ahli-ahli filsafah Yunani pada tahun
Penyusun bagian-bagian atom sangat menentukan sifat benda/materi. Untuk mengetahui bagaimana atom bergabung sehingga dapat mengubah bahan sesuai
 Struktur Atom Mengapa atom dipelajari? Penyusun bagian-bagian atom sangat menentukan sifat benda/materi. Untuk mengetahui bagaimana atom bergabung sehingga dapat mengubah bahan sesuai dengan kebutuhan.
Struktur Atom Mengapa atom dipelajari? Penyusun bagian-bagian atom sangat menentukan sifat benda/materi. Untuk mengetahui bagaimana atom bergabung sehingga dapat mengubah bahan sesuai dengan kebutuhan.
TEORI ATOM. Awal Perkembangan Teori Atom
 TEORI ATOM Awal Perkembangan Teori Atom Teori atom pada masa peradaban Yunani Demokritus, Epicurus, Strato, Carus Materi tersusun dari partikel yang sangat kecil yang tidak dapat dibagi lagi Partikel
TEORI ATOM Awal Perkembangan Teori Atom Teori atom pada masa peradaban Yunani Demokritus, Epicurus, Strato, Carus Materi tersusun dari partikel yang sangat kecil yang tidak dapat dibagi lagi Partikel
Apa yang dimaksud dengan atom? Atom adalah bagian terkecil dari suatu unsur
 Struktur Atom Apa yang dimaksud dengan atom? Atom adalah bagian terkecil dari suatu unsur Atom tersusun atas partikel apa saja? Partikel-partikel penyusun atom : Partikel Lambang Penemu Muatan Massa 9,11x10-28g
Struktur Atom Apa yang dimaksud dengan atom? Atom adalah bagian terkecil dari suatu unsur Atom tersusun atas partikel apa saja? Partikel-partikel penyusun atom : Partikel Lambang Penemu Muatan Massa 9,11x10-28g
RANGKUMAN MATERI. Struktur Atom
 RANGKUMAN MATERI Struktur Atom Atom terdiri dari proton, neutron dan elektron. Proton dan neutron berada di dalam inti atom. Sedangkan elektron terus berputar mengelilingi inti atom karena muatan listriknya.
RANGKUMAN MATERI Struktur Atom Atom terdiri dari proton, neutron dan elektron. Proton dan neutron berada di dalam inti atom. Sedangkan elektron terus berputar mengelilingi inti atom karena muatan listriknya.
Struktur Atom. Sulistyani, M.Si.
 Struktur Atom Sulistyani, M.Si. sulistyani@uny.ac.id DEFINISI ATOM Salah satu konsep ilmiah tertua adalah bahwa semua materi dapat dipecah menjadi zarah (partikel) terkecil, dimana partikel-partikel itu
Struktur Atom Sulistyani, M.Si. sulistyani@uny.ac.id DEFINISI ATOM Salah satu konsep ilmiah tertua adalah bahwa semua materi dapat dipecah menjadi zarah (partikel) terkecil, dimana partikel-partikel itu
PERKEMBANGAN MODEL ATOM DI SUSUN OLEH YOSI APRIYANTI A1F012044
 PERKEMBANGAN MODEL ATOM DI SUSUN OLEH YOSI APRIYANTI A1F012044 PERKEMBANGAN MODEL ATOM Seorang filsuf Yunani yang bernama Democritus berpendapat bahwa jika suatu benda dibelah terus menerus, maka pada
PERKEMBANGAN MODEL ATOM DI SUSUN OLEH YOSI APRIYANTI A1F012044 PERKEMBANGAN MODEL ATOM Seorang filsuf Yunani yang bernama Democritus berpendapat bahwa jika suatu benda dibelah terus menerus, maka pada
STRUKTUR ATOM DAN PERKEMBANGAN TEORI ATOM 0leh: Ramadani. sinar bermuatan negatif. kecil pembentuk atom tersebut yaitu
 STRUKTUR ATOM DAN PERKEMBANGAN TEORI ATOM 0leh: Ramadani A. PENDAHULUAN Istilah atom pertama kali dikemukakan oleh filsuf Yunani bernama Demokritus dengan istilah atomos yang artinya tidak dapat dibagi.
STRUKTUR ATOM DAN PERKEMBANGAN TEORI ATOM 0leh: Ramadani A. PENDAHULUAN Istilah atom pertama kali dikemukakan oleh filsuf Yunani bernama Demokritus dengan istilah atomos yang artinya tidak dapat dibagi.
Perkembangan Model Atom. Semester 1
 Perkembangan Model Atom Semester 1 Model atom adalah suatu gambar rekaan atom berdasarkan eksperimen ataupun kajian teoritis, karena para ahli tidak tahu pasti seperti apakah bentuk atom itu sebenarnya.
Perkembangan Model Atom Semester 1 Model atom adalah suatu gambar rekaan atom berdasarkan eksperimen ataupun kajian teoritis, karena para ahli tidak tahu pasti seperti apakah bentuk atom itu sebenarnya.
Struktur Atom. Setelah mempelajari bab ini, Anda diharapkan mampu mengidentifikasi atom dan strukturnya berdasarkan Tabel Periodik Unsur.
 I Pernahkah Anda membayangkan bahwa keberadaan alam semesta, dunia dan seisinya termasuk juga kita hanya mungkin terjadi dengan adanya keseimbangan yang teramat halus dan teliti? Atom adalah bagian terkecil
I Pernahkah Anda membayangkan bahwa keberadaan alam semesta, dunia dan seisinya termasuk juga kita hanya mungkin terjadi dengan adanya keseimbangan yang teramat halus dan teliti? Atom adalah bagian terkecil
Struktur Atom. Struktur atom merupakan satuan dasar materi yang terdiri dari inti atom beserta awan elektron bermuatan negatif yang
 Struktur atom merupakan satuan dasar materi yang terdiri dari inti atom beserta awan elektron bermuatan negatif yang mengelilinginya. Inti atom mengandung campuran proton (bermuatan positif) dan neutron
Struktur atom merupakan satuan dasar materi yang terdiri dari inti atom beserta awan elektron bermuatan negatif yang mengelilinginya. Inti atom mengandung campuran proton (bermuatan positif) dan neutron
Bab 1 STRUKTUR ATOM. Pada pelajaran bab pertama ini akan dipelajari tentang perkembangan teori atom, notasi unsur, Isotop, isobar, dan isoton.
 Bab STRUKTUR ATOM Gambar. Teori Atom Rutherford. Sumber: Ensiklopedia Iptek Pada pelajaran bab pertama ini akan dipelajari tentang perkembangan teori atom, notasi unsur, Isotop, isobar, dan isoton. Struktur
Bab STRUKTUR ATOM Gambar. Teori Atom Rutherford. Sumber: Ensiklopedia Iptek Pada pelajaran bab pertama ini akan dipelajari tentang perkembangan teori atom, notasi unsur, Isotop, isobar, dan isoton. Struktur
B. Macam macam Model Atom a. Model Atom John Dalton. a. Atom merupakan bagian terkecil dari materi yang sudah tidak dapat. Makalah Struktur Atom 1
 BAB I PENDAHULUAN A. Latar Belakang Atom adalah suatu satuan dasar materi, yang terdiri atas beberapa struktur. Istilah atom berasal dari Bahasa Yunani (átomos), yang berarti tidak dapat dipotong ataupun
BAB I PENDAHULUAN A. Latar Belakang Atom adalah suatu satuan dasar materi, yang terdiri atas beberapa struktur. Istilah atom berasal dari Bahasa Yunani (átomos), yang berarti tidak dapat dipotong ataupun
BAB 2 STRUKTUR ATOM PERKEMBANGAN TEORI ATOM
 BAB 2 STRUKTUR ATOM PARTIKEL MATERI Bagian terkecil dari materi disebut partikel. Beberapa pendapat tentang partikel materi :. Menurut Democritus, pembagian materi bersifat diskontinyu ( jika suatu materi
BAB 2 STRUKTUR ATOM PARTIKEL MATERI Bagian terkecil dari materi disebut partikel. Beberapa pendapat tentang partikel materi :. Menurut Democritus, pembagian materi bersifat diskontinyu ( jika suatu materi
STRUKTUR ATOM DAN SISTEM PERIODIK Kimia SMK KELAS X SEMESTER 1 SMK MUHAMMADIYAH 3 METRO
 STRUKTUR ATOM DAN SISTEM PERIODIK Kimia SMK KELAS X SEMESTER 1 SMK MUHAMMADIYAH 3 METRO SK DAN KD Standar Kompetensi Mengidentifikasi struktur atom dan sifat-sifat periodik pada tabel periodik unsur Kompetensi
STRUKTUR ATOM DAN SISTEM PERIODIK Kimia SMK KELAS X SEMESTER 1 SMK MUHAMMADIYAH 3 METRO SK DAN KD Standar Kompetensi Mengidentifikasi struktur atom dan sifat-sifat periodik pada tabel periodik unsur Kompetensi
Struktur atom. Bagian terkecil dari materi disebut partikel. Beberapa pendapat tentang partikel materi :
 Struktur atom A PARTIKEL MATERI Bagian terkecil dari materi disebut partikel. Beberapa pendapat tentang partikel materi : Menurut Democritus, pembagian materi bersifat diskontinyu ( jika suatu materi dibagi
Struktur atom A PARTIKEL MATERI Bagian terkecil dari materi disebut partikel. Beberapa pendapat tentang partikel materi : Menurut Democritus, pembagian materi bersifat diskontinyu ( jika suatu materi dibagi
ATOM DAN SISTEM PERIODIK UNSUR
 ATOM DAN SISTEM PERIODIK UNSUR I. Perkembangan teori atom a. Teori atom Dalton: Materi tersusun atas partikel-partikel terkecil yang disebut atom. Atom merupakan bagian terkecil dari materi yang tidak
ATOM DAN SISTEM PERIODIK UNSUR I. Perkembangan teori atom a. Teori atom Dalton: Materi tersusun atas partikel-partikel terkecil yang disebut atom. Atom merupakan bagian terkecil dari materi yang tidak
BAHAN AJAR KIMIA KONFIGURASI ELEKTRON DAN BILANGAN KUANTUM
 BAHAN AJAR KIMIA KONFIGURASI ELEKTRON DAN BILANGAN KUANTUM CHEMISTRY IS FUN Oleh : Hana Nazelia AfrianI 1 Konfigurasi Elektron dan Bilangan KONFIGURASI ELEKTRON Konfigurasi elektron adalah susunan elektron
BAHAN AJAR KIMIA KONFIGURASI ELEKTRON DAN BILANGAN KUANTUM CHEMISTRY IS FUN Oleh : Hana Nazelia AfrianI 1 Konfigurasi Elektron dan Bilangan KONFIGURASI ELEKTRON Konfigurasi elektron adalah susunan elektron
TEORI PERKEMBANGAN ATOM
 TEORI PERKEMBANGAN ATOM A. Teori atom Dalton Teori atom dalton ini didasarkan pada 2 hukum, yaitu : hukum kekekalan massa (hukum Lavoisier), massa total zat-zat sebelum reaksi akan selalu sama dengan massa
TEORI PERKEMBANGAN ATOM A. Teori atom Dalton Teori atom dalton ini didasarkan pada 2 hukum, yaitu : hukum kekekalan massa (hukum Lavoisier), massa total zat-zat sebelum reaksi akan selalu sama dengan massa
INFORMASI KIMIA ENERGI ATOM
 Kimia SMAN 113 Jakarta (www.kimiavegas.wordpress.com) Guru Mata Pelajaran : Gianto, SPd Facebook: multios2009@gmail.com INFORMASI KIMIA ENERGI ATOM Energi atom adalah energi yang bersumber dari atom. Setiap
Kimia SMAN 113 Jakarta (www.kimiavegas.wordpress.com) Guru Mata Pelajaran : Gianto, SPd Facebook: multios2009@gmail.com INFORMASI KIMIA ENERGI ATOM Energi atom adalah energi yang bersumber dari atom. Setiap
Struktur atom merupakan satuan dasar materi yang terdiri dari inti atom beserta awan elektron bermuatan negatif yang mengelilinginya.
 Struktur atom merupakan satuan dasar materi yang terdiri dari inti atom beserta awan elektron bermuatan negatif yang mengelilinginya. Inti atom mengandung campuran proton (bermuatan positif) dan neutron
Struktur atom merupakan satuan dasar materi yang terdiri dari inti atom beserta awan elektron bermuatan negatif yang mengelilinginya. Inti atom mengandung campuran proton (bermuatan positif) dan neutron
BAB FISIKA ATOM. Model ini gagal karena tidak sesuai dengan hasil percobaan hamburan patikel oleh Rutherford.
 1 BAB FISIKA ATOM Perkembangan teori atom Model Atom Dalton 1. Atom adalah bagian terkecil dari suatu unsur yang tidak dapat dibagi-bagi 2. Atom-atom suatu unsur semuanya serupa dan tidak dapat berubah
1 BAB FISIKA ATOM Perkembangan teori atom Model Atom Dalton 1. Atom adalah bagian terkecil dari suatu unsur yang tidak dapat dibagi-bagi 2. Atom-atom suatu unsur semuanya serupa dan tidak dapat berubah
SMA NEGERI 48 JAKARTA
 Nama : Kelas : Tanggal : PEMERINTAH PROPINSI DAERAH KHUSUS IBUKOTA JAKARTA DINAS PENDIDIKAN SMA NEGERI 48 JAKARTA Jln. Pinang Ranti II TMII, Tel. 8009437-8006204/Fax.(021) 8009437 Jakarta Timur 13560 Website:www.sman48-jkt.sch.com,:
Nama : Kelas : Tanggal : PEMERINTAH PROPINSI DAERAH KHUSUS IBUKOTA JAKARTA DINAS PENDIDIKAN SMA NEGERI 48 JAKARTA Jln. Pinang Ranti II TMII, Tel. 8009437-8006204/Fax.(021) 8009437 Jakarta Timur 13560 Website:www.sman48-jkt.sch.com,:
Bilangan Kuantum Utama (n)
 Bilangan Kuantum Utama (n) Menyatakan nomer kulit tempat elektron berada atau bilangan ini juga menyatakan ukuran orbital/ jarak/ jari-jari atom. Dinyatakan dengan bilangan bulat positif. Mempunyai dua
Bilangan Kuantum Utama (n) Menyatakan nomer kulit tempat elektron berada atau bilangan ini juga menyatakan ukuran orbital/ jarak/ jari-jari atom. Dinyatakan dengan bilangan bulat positif. Mempunyai dua
PENDAHULUAN. Atom berasal dari bahasa Yunani atomos yang artinya tidak dapat dibagi-bagi lagi.
 PENDAHULUAN Atom berasal dari bahasa Yunani atomos yang artinya tidak dapat dibagi-bagi lagi. Demokritus (460-370-S.M) Bagian terkecil yang tidak dapat dibagi lagi disebut: ATOM Konsep atom yang dikemukakan
PENDAHULUAN Atom berasal dari bahasa Yunani atomos yang artinya tidak dapat dibagi-bagi lagi. Demokritus (460-370-S.M) Bagian terkecil yang tidak dapat dibagi lagi disebut: ATOM Konsep atom yang dikemukakan
MATERIAL TEKNIK. 2 SKS Ruang B2.3 Jam Dedi Nurcipto, MT
 MATERIAL TEKNIK 2 SKS Ruang B2.3 Jam 8.40-11.10 Dedi Nurcipto, MT dedinurcipto@dsn.dinus.ac.id Struktur Atom Struktur atom merupakan satuan dasar materi yang terdiri dari inti atom beserta elektron bermuatan
MATERIAL TEKNIK 2 SKS Ruang B2.3 Jam 8.40-11.10 Dedi Nurcipto, MT dedinurcipto@dsn.dinus.ac.id Struktur Atom Struktur atom merupakan satuan dasar materi yang terdiri dari inti atom beserta elektron bermuatan
TEORI ATOM DAN STRUKTUR ATOM
 TEORI ATOM DAN STRUKTUR ATOM KOMPETENSI INTI KOMPETENSI DASAR 1. Menghayati dan mengamalkan ajaran agama yang dianutnya 2. Menghayati dan mengamalkan perilaku jujur, disiplin, tanggungjawab, peduli (gotong
TEORI ATOM DAN STRUKTUR ATOM KOMPETENSI INTI KOMPETENSI DASAR 1. Menghayati dan mengamalkan ajaran agama yang dianutnya 2. Menghayati dan mengamalkan perilaku jujur, disiplin, tanggungjawab, peduli (gotong
Terdiri atas inti atom dan elektron yang berada diluar atom. Inti atom tersusun atas proton dan netron.
 PARTIKEL-PARTIKEL DASAR ATOM (Sumber : www.chem-is-try-org) Kimia SMAN 113 Jakarta (www.kimiavegas.wordpress.com) Guru Mata Pelajaran : Gianto, SPd Facebook: multios2009@gmail.com Terdiri atas inti atom
PARTIKEL-PARTIKEL DASAR ATOM (Sumber : www.chem-is-try-org) Kimia SMAN 113 Jakarta (www.kimiavegas.wordpress.com) Guru Mata Pelajaran : Gianto, SPd Facebook: multios2009@gmail.com Terdiri atas inti atom
Bab I Teori Atom Bohr dan Mekanika Kuantum
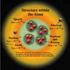 Bab I Teori Atom Bohr dan Mekanika Kuantum Model atom Rutherford Model atom Schrodinger Model atom Bohr Sumber: Encarta Encclopedia, 005 Teori atom berkembang mulai dari teori atom Rutherford, Bohr, sampai
Bab I Teori Atom Bohr dan Mekanika Kuantum Model atom Rutherford Model atom Schrodinger Model atom Bohr Sumber: Encarta Encclopedia, 005 Teori atom berkembang mulai dari teori atom Rutherford, Bohr, sampai
BAB 19 A T O M. A. Pendahuluan
 BAB 19 A T O M A. Pendahuluan Pemikiran ke arah penemuan atom dan inti atom telah berkembang di setiap peradaban sejak manusia mengenal tulisan atau yang lebih dikenal sebagai zaman permulaan sejarah.
BAB 19 A T O M A. Pendahuluan Pemikiran ke arah penemuan atom dan inti atom telah berkembang di setiap peradaban sejak manusia mengenal tulisan atau yang lebih dikenal sebagai zaman permulaan sejarah.
I. Perkembangan Teori Atom
 I. Perkembangan Teori Atom Perkembangan pemahaman struktur atom sejalan dengan awal perkembangan ilmu Fisika modern. Ilmuwan pertama yang membangun model (struktur) atom adalah John Dalton, kemudian disempurnakan
I. Perkembangan Teori Atom Perkembangan pemahaman struktur atom sejalan dengan awal perkembangan ilmu Fisika modern. Ilmuwan pertama yang membangun model (struktur) atom adalah John Dalton, kemudian disempurnakan
Struktur Atom dan Sistem Periodik Unsur. Kelompok 1 Atifa Rahmi ( ) Lelly Shelviyani ( ) Nur Ayu Fitriani ( ) Suhartini ( )
 Struktur Atom dan Sistem Periodik Unsur Kelompok 1 Atifa Rahmi (1102867) Lelly Shelviyani (1105121) Nur Ayu Fitriani (1101979) Suhartini (1106554) Mari Kita Pretest Jawablah pernyataan di bawah ini dengan
Struktur Atom dan Sistem Periodik Unsur Kelompok 1 Atifa Rahmi (1102867) Lelly Shelviyani (1105121) Nur Ayu Fitriani (1101979) Suhartini (1106554) Mari Kita Pretest Jawablah pernyataan di bawah ini dengan
Atom netral. Ion bermuatan listrik positif : melepas elektron negatif ; menerima elektron Atom Inti atom o proton o neutron Elektron Contoh:
 Atom netral Ion bermuatan listrik positif : melepas elektron negatif ; menerima elektron Atom Inti atom o proton o neutron Elektron Contoh: 11 23 Na p = 11 e = 11 n = 12 Percobaan Lempeng emas Oleh Rutherford
Atom netral Ion bermuatan listrik positif : melepas elektron negatif ; menerima elektron Atom Inti atom o proton o neutron Elektron Contoh: 11 23 Na p = 11 e = 11 n = 12 Percobaan Lempeng emas Oleh Rutherford
MODUL KIMIA SMA IPA Kelas 10
 SMA IPA Kelas Atom Bagian terkecil dari materi yang sudah tidak dapat dibagi lagi disebut atom (berasal dari bahasa Yunani atomos yang berarti tidak dapat dibagi lagi). Namun, berakhir pendapat tersebut
SMA IPA Kelas Atom Bagian terkecil dari materi yang sudah tidak dapat dibagi lagi disebut atom (berasal dari bahasa Yunani atomos yang berarti tidak dapat dibagi lagi). Namun, berakhir pendapat tersebut
Struktur Atom dan Sistem Periodik
 Struktur Atom dan Sistem Periodik Struktur Atom Elektron Inti Atom Gelombang Radiasi Elektromagnet Model Bohr untuk atom Hidrogen Teori Gelombang Elektron Prinsip Ketidakpastian Heisenberg Model Quantum
Struktur Atom dan Sistem Periodik Struktur Atom Elektron Inti Atom Gelombang Radiasi Elektromagnet Model Bohr untuk atom Hidrogen Teori Gelombang Elektron Prinsip Ketidakpastian Heisenberg Model Quantum
Mekanika Kuantum. Orbital dan Bilangan Kuantum
 Standar Kompetensi Kompetensi Dasar Mendeskripsikan struktur atom dan sifat-sifat periodik serta struktur molekul dan sifat-sifatnya. Menerapkan teori atom mekanika kuantum untuk menuliskan konfigurasi
Standar Kompetensi Kompetensi Dasar Mendeskripsikan struktur atom dan sifat-sifat periodik serta struktur molekul dan sifat-sifatnya. Menerapkan teori atom mekanika kuantum untuk menuliskan konfigurasi
STRUKTUR ATOM. Penulis : Niyata Sirat, S.Pd. Penyunting Materi : Drs. Ucu Cahyana, M.Si. Penyunting Media : Drs. Slamet Soetanto, M.Si.
 STRUKTUR ATOM Mata Pelajaran K e l a s Nomor Modul : Kimia : X (Sepuluh) : Kim.X.02 Penulis : Niyata Sirat, S.Pd. Penyunting Materi : Drs. Ucu Cahyana, M.Si. Penyunting Media : Drs. Slamet Soetanto, M.Si.
STRUKTUR ATOM Mata Pelajaran K e l a s Nomor Modul : Kimia : X (Sepuluh) : Kim.X.02 Penulis : Niyata Sirat, S.Pd. Penyunting Materi : Drs. Ucu Cahyana, M.Si. Penyunting Media : Drs. Slamet Soetanto, M.Si.
kimia Kelas X REVIEW I K-13 A. Hakikat Ilmu Kimia
 K-13 Kelas X kimia REVIEW I Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami hakikat ilmu kimia dan metode ilmiah. 2. Memahami teori atom dan
K-13 Kelas X kimia REVIEW I Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami hakikat ilmu kimia dan metode ilmiah. 2. Memahami teori atom dan
GENTA GROUP in PLAY STORE. Kode Aktivasi Aplikasi: 74DSM. Kode Aktivasi Aplikasi: P859 FPM KIMIA
 GENTA GROUP in PLAY STORE CBT UN SMA IPA Aplikasi CBT UN SMA IPA android dapat di download di play store dengan kata kunci genta group atau gunakan qr-code di bawah. CBT Psikotes Aplikasi CBT Psikotes
GENTA GROUP in PLAY STORE CBT UN SMA IPA Aplikasi CBT UN SMA IPA android dapat di download di play store dengan kata kunci genta group atau gunakan qr-code di bawah. CBT Psikotes Aplikasi CBT Psikotes
kimia KONFIGURASI ELEKTRON
 K-13 Kelas X kimia KONFIGURASI ELEKTRON Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami konfigurasi elektron kulit dan subkulit. 2. Menyelesaikan
K-13 Kelas X kimia KONFIGURASI ELEKTRON Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami konfigurasi elektron kulit dan subkulit. 2. Menyelesaikan
PARTIKEL PENYUSUN ATOM
 Semester 1 PARTIKEL PENYUSUN ATOM ELEKTRON 0 1 e NEUTRON PROTON 1 1 1 0 p n ELEKTRON Elektron ditemukan pertama kali oleh J.J Thomson pada tahun 1897 dengan percobaan sinar katoda (www.geocities.com )
Semester 1 PARTIKEL PENYUSUN ATOM ELEKTRON 0 1 e NEUTRON PROTON 1 1 1 0 p n ELEKTRON Elektron ditemukan pertama kali oleh J.J Thomson pada tahun 1897 dengan percobaan sinar katoda (www.geocities.com )
Purwanti Widhy H, M.Pd Pendidikan IPA FMIPA UNY
 Purwanti Widhy H, M.Pd Pendidikan IPA FMIPA UNY Teori Atom Dalton (1808) 1. Unsur tersusun atas partikel yang sangat kecil, yang disebut atom. Semua atom unsur tertentu adalah identik, yaitu mempunyai
Purwanti Widhy H, M.Pd Pendidikan IPA FMIPA UNY Teori Atom Dalton (1808) 1. Unsur tersusun atas partikel yang sangat kecil, yang disebut atom. Semua atom unsur tertentu adalah identik, yaitu mempunyai
Struktur Atom Untuk SMK Teknologi dan Pertanian. Kelas X Semester 1 Penyusun : SMK Negeri 7 Bandung
 Struktur Atom Untuk SMK Teknologi dan Pertanian Kelas X Semester 1 Penyusun : SMK Negeri 7 Bandung Kompetensi Dasar Mengidentifikasi partikel atom Memahami eksperimen tentang inti atom Mengidentifikasi
Struktur Atom Untuk SMK Teknologi dan Pertanian Kelas X Semester 1 Penyusun : SMK Negeri 7 Bandung Kompetensi Dasar Mengidentifikasi partikel atom Memahami eksperimen tentang inti atom Mengidentifikasi
IR. STEVANUS ARIANTO 1
 8/7/017 PNDAHULUAN TORI ATOM DALTON KLMAHAN TORI ATOM DALTON SINAR KATODA SIFAT SINAR KATODA TORI ATOM JJ.THOMSON HAMBURAN SINAR ALFA TORI ATOM RUTHRFORD KLMAHAN TORI ATOM RUTHRFORD SPKTRUM UAP HIDROGN
8/7/017 PNDAHULUAN TORI ATOM DALTON KLMAHAN TORI ATOM DALTON SINAR KATODA SIFAT SINAR KATODA TORI ATOM JJ.THOMSON HAMBURAN SINAR ALFA TORI ATOM RUTHRFORD KLMAHAN TORI ATOM RUTHRFORD SPKTRUM UAP HIDROGN
YAYASAN PEMBINA UNIVERSITAS NEGERI JAKARTA SMA LABSCHOOL KEBAYORAN
 YAYASAN PEMBINA UNIVERSITAS NEGERI JAKARTA SMA LABSCHOOL KEBAYORAN ULANGAN HARIAN TERPROGRAM Mata Pelajaran : Kimia Kelas/Program : X / Reguler Hari, Tanggal : Selasa, 9 September 05 Waktu : 07.30 09.00
YAYASAN PEMBINA UNIVERSITAS NEGERI JAKARTA SMA LABSCHOOL KEBAYORAN ULANGAN HARIAN TERPROGRAM Mata Pelajaran : Kimia Kelas/Program : X / Reguler Hari, Tanggal : Selasa, 9 September 05 Waktu : 07.30 09.00
Aristoteles. Leukipos dan Demokritos. John Dalton. Perkembangan Model Atom. J.J. Thomson. Rutherford. Niels Bohr. Mekanika Kuatum
 What is an Atom? Aristoteles Leukipos dan Demokritos Perkembangan Model Atom John Dalton J.J. Thomson Rutherford Niels Bohr Mekanika Kuatum 1. Pendapat Aristoteles Materi bersifat kontinue, artinya materi
What is an Atom? Aristoteles Leukipos dan Demokritos Perkembangan Model Atom John Dalton J.J. Thomson Rutherford Niels Bohr Mekanika Kuatum 1. Pendapat Aristoteles Materi bersifat kontinue, artinya materi
RENCANA PELAKSANAAN PEMBELAJARAN (RPP)
 RENCANA PELAKSANAAN PEMBELAJARAN (RPP) Sekolah Mata Pelajaran Kelas/ Semester Materi Pokok Alokasi Waktu : SMAN 1 SANDEN : Kimia : X / Ganjil : Struktur Atom : 3 x 45 menit A. Kompetensi Inti KI 1 : Menghayati
RENCANA PELAKSANAAN PEMBELAJARAN (RPP) Sekolah Mata Pelajaran Kelas/ Semester Materi Pokok Alokasi Waktu : SMAN 1 SANDEN : Kimia : X / Ganjil : Struktur Atom : 3 x 45 menit A. Kompetensi Inti KI 1 : Menghayati
SMP kelas 8 - KIMIA BAB 1. ATOM, ION DAN MOLEKULLatihan soal 1.1. Dalton. Thomson. Rutherford. Bohr
 SMP kelas 8 - KIMIA BAB 1. ATOM, ION DAN MOLEKULLatihan soal 1.1 1. Atom merupakan bola pejal bermuatan positif dengan elektron - elektron yang tersebar merata merupakan teori atom... Thomson Bohr Atom
SMP kelas 8 - KIMIA BAB 1. ATOM, ION DAN MOLEKULLatihan soal 1.1 1. Atom merupakan bola pejal bermuatan positif dengan elektron - elektron yang tersebar merata merupakan teori atom... Thomson Bohr Atom
Atom menyusun elemen dengan bilangan sederhana. Setiap atom dari elemen yang berbeda memiliki massa yang berbeda.
 Review Model Atom Model Atom Dalton Atom menyusun elemen dengan bilangan sederhana. Setiap atom dari elemen yang berbeda memiliki massa yang berbeda. Model Atom Thomson Secara garis besar atom berupa bola
Review Model Atom Model Atom Dalton Atom menyusun elemen dengan bilangan sederhana. Setiap atom dari elemen yang berbeda memiliki massa yang berbeda. Model Atom Thomson Secara garis besar atom berupa bola
BANK SOAL SELEKSI MASUK PERGURUAN TINGGI BIDANG KIMIA 1 BAB I STRUKTUR ATOM
 BANK SOAL SELEKSI MASUK PERGURUAN TINGGI BIDANG KIMIA 1 BAB I 1. Suatu partikel X memiliki 16 proton, 16 neutron, dan 18 elektron. Partikel tersebut dapat dikategorikan sebagai A. Anion X bermuatan -1
BANK SOAL SELEKSI MASUK PERGURUAN TINGGI BIDANG KIMIA 1 BAB I 1. Suatu partikel X memiliki 16 proton, 16 neutron, dan 18 elektron. Partikel tersebut dapat dikategorikan sebagai A. Anion X bermuatan -1
ATOM. (Makalah Kimia Dasar 1) Oleh CHRISTIYANTO INDRA P
 ATOM (Makalah Kimia Dasar 1) Oleh ANISA SEKAR P BAYU ANTRAKUSUMA CHICI YULIANA NADI CHRISTIYANTO INDRA P FERA ASTUTI HANS FITRHIA FAJRI K3311007 K3311011 K3311013 K3311014 K3311028 K3311035 FAKULTAS KEGURUAN
ATOM (Makalah Kimia Dasar 1) Oleh ANISA SEKAR P BAYU ANTRAKUSUMA CHICI YULIANA NADI CHRISTIYANTO INDRA P FERA ASTUTI HANS FITRHIA FAJRI K3311007 K3311011 K3311013 K3311014 K3311028 K3311035 FAKULTAS KEGURUAN
TEORI ATOM. Ramadoni Syahputra
 TEORI ATOM Ramadoni Syahputra STRUKTUR ATOM Teori tentang atom pertama kali dikemukakan oleh filsafat Yunani yaitu Leoclipus dan Democritus, pada abad ke-5 sebelum Masehi. Atom berasal dari kata Yunani:
TEORI ATOM Ramadoni Syahputra STRUKTUR ATOM Teori tentang atom pertama kali dikemukakan oleh filsafat Yunani yaitu Leoclipus dan Democritus, pada abad ke-5 sebelum Masehi. Atom berasal dari kata Yunani:
STRUKTUR ATOM. 3. Perhatikan gambar berikut :
 STRUKTUR ATOM. Elektron - elektron dalam atom beredar mengelilingi inti dan berada pada lintasan (tingkat energi) tertentu. Elektron dapat berpindah dari satu tingkat energi ke tingkat energi lainnya di
STRUKTUR ATOM. Elektron - elektron dalam atom beredar mengelilingi inti dan berada pada lintasan (tingkat energi) tertentu. Elektron dapat berpindah dari satu tingkat energi ke tingkat energi lainnya di
FISIKA. Sesi TEORI ATOM A. TEORI ATOM DALTON B. TEORI ATOM THOMSON
 FISIKA KELAS XII IPA - KURIKULUM GABUNGAN 11 Sesi NGAN TEORI ATOM A. TEORI ATOM DALTON 1. Atom adalah bagian terkecil suatu unsur yang tidak dapat dibagi lagi.. Atom suatu unsur serupa semuanya, dan tak
FISIKA KELAS XII IPA - KURIKULUM GABUNGAN 11 Sesi NGAN TEORI ATOM A. TEORI ATOM DALTON 1. Atom adalah bagian terkecil suatu unsur yang tidak dapat dibagi lagi.. Atom suatu unsur serupa semuanya, dan tak
UJI KOMPETENSI A. PILIHAN GANDA
 UJI KOMPETENSI A. PILIHAN GANDA 1. percobaan yang mendasari teori atom Bohr adalah a. percobaan tabung pembawa muatan b. percobaan penghamburan sinar c. percobaan tetesan minyak d. percobaan sepectrum
UJI KOMPETENSI A. PILIHAN GANDA 1. percobaan yang mendasari teori atom Bohr adalah a. percobaan tabung pembawa muatan b. percobaan penghamburan sinar c. percobaan tetesan minyak d. percobaan sepectrum
PENEMUAN RADIOAKTIVITAS. Sulistyani, M.Si.
 PENEMUAN RADIOAKTIVITAS Sulistyani, M.Si. Email: sulistyani@uny.ac.id APA ITU KIMIA INTI? Kimia inti adalah ilmu yang mempelajari struktur inti atom dan pengaruhnya terhadap kestabilan inti serta reaksi-reaksi
PENEMUAN RADIOAKTIVITAS Sulistyani, M.Si. Email: sulistyani@uny.ac.id APA ITU KIMIA INTI? Kimia inti adalah ilmu yang mempelajari struktur inti atom dan pengaruhnya terhadap kestabilan inti serta reaksi-reaksi
KIMIA (2-1)
 03035307 KIMIA (2-1) Dr.oec.troph.Ir.Krishna Purnawan Candra, M.S. Kuliah ke-2 Perkembangan teori atom, teori atom Dalton dan Rutherford, teori atom modern Faperta UNMUL 2011 Perkembangan teori atom Perkembangan
03035307 KIMIA (2-1) Dr.oec.troph.Ir.Krishna Purnawan Candra, M.S. Kuliah ke-2 Perkembangan teori atom, teori atom Dalton dan Rutherford, teori atom modern Faperta UNMUL 2011 Perkembangan teori atom Perkembangan
PENDAHULUAN PENGENALAN ILMU KIMIA
 PENDAHULUAN PENGENALAN ILMU KIMIA A. Pengertian Ilmu Kimia Bangsa Yunani menyebut kimia sebagai chemie yaitu segala macam aktivitas seni pengerjaan logam. Pada saat itu, setiap orang yang beraktivitas
PENDAHULUAN PENGENALAN ILMU KIMIA A. Pengertian Ilmu Kimia Bangsa Yunani menyebut kimia sebagai chemie yaitu segala macam aktivitas seni pengerjaan logam. Pada saat itu, setiap orang yang beraktivitas
MODUL -1. STRUKTUR ATOM dan SISTEM PERIODIK UNSUR- UNSUR
 MODUL -1 STRUKTUR ATOM dan SISTEM PERIODIK UNSUR- UNSUR Standar Kompetensi ( SK ) : Memahami struktur untuk meramalkan sifat-sifat periodik unsur,struktur molekul, dan sifat-sifat senyawa Kompetensi Dasar
MODUL -1 STRUKTUR ATOM dan SISTEM PERIODIK UNSUR- UNSUR Standar Kompetensi ( SK ) : Memahami struktur untuk meramalkan sifat-sifat periodik unsur,struktur molekul, dan sifat-sifat senyawa Kompetensi Dasar
KATA PENGANTAR... 1 DAFTAR ISI... 2 LATAR BELAKANG... 3
 By: 1 Puji syukur kepada Tuhan yang Maha Kuasa dan terlebih Maha Kasih, Karena selesainya modul ini ternyata bukan semata-mata hasil usaha saya tetapi semua ini karena Kasih dan AnugerahNya. Dalam pembahasan
By: 1 Puji syukur kepada Tuhan yang Maha Kuasa dan terlebih Maha Kasih, Karena selesainya modul ini ternyata bukan semata-mata hasil usaha saya tetapi semua ini karena Kasih dan AnugerahNya. Dalam pembahasan
"Atom merupakan bola pejal yang bermuatan positif dan didalamya tersebar muatan negatif elektron"
 Model Atom Thomson Berdasarkan penemuan tabung katode yang lebih baik oleh William Crookers, maka J.J. Thomson meneliti lebih lanjut tentang sinar katode dan dapat dipastikan bahwa sinar katode merupakan
Model Atom Thomson Berdasarkan penemuan tabung katode yang lebih baik oleh William Crookers, maka J.J. Thomson meneliti lebih lanjut tentang sinar katode dan dapat dipastikan bahwa sinar katode merupakan
PENGANTAR KIMIA INDUSTRI _KIMIA INDUSTRI_ DEWI HARDININGTYAS, ST, MT, MBA WIDHA KUSUMA NINGDYAH, ST, MT AGUSTINA EUNIKE, ST, MT, MBA
 PENGANTAR KIMIA INDUSTRI _KIMIA INDUSTRI_ DEWI HARDININGTYAS, ST, MT, MBA WIDHA KUSUMA NINGDYAH, ST, MT AGUSTINA EUNIKE, ST, MT, MBA 1. Pengukuran Ilmiah 2. Teori Atom 3. Tabel Periodik 4. Molekul dan
PENGANTAR KIMIA INDUSTRI _KIMIA INDUSTRI_ DEWI HARDININGTYAS, ST, MT, MBA WIDHA KUSUMA NINGDYAH, ST, MT AGUSTINA EUNIKE, ST, MT, MBA 1. Pengukuran Ilmiah 2. Teori Atom 3. Tabel Periodik 4. Molekul dan
BAB I STRUKTUR ATOM DAN SISTEM PERIODIK UNSUR
 BAB I STRUKTUR ATOM DAN SISTEM PERIODIK UNSUR A. STANDAR KOMPOTENSI 1 : Mendeskripsikan struktur atom,sifat-sifat periodik unsur, dan ikatan kimia serta struktur molekul dan sifat-sifatnya. B. KOMPETENSI
BAB I STRUKTUR ATOM DAN SISTEM PERIODIK UNSUR A. STANDAR KOMPOTENSI 1 : Mendeskripsikan struktur atom,sifat-sifat periodik unsur, dan ikatan kimia serta struktur molekul dan sifat-sifatnya. B. KOMPETENSI
MODEL ATOM DALTON. Atom ialah bagian terkecil suatu zat yang tidak dapat dibagi-bagi. Atom tidak dapat dimusnahkan & diciptakan
 MODEL ATOM MODEL ATOM DALTON Atom ialah bagian terkecil suatu zat yang tidak dapat dibagi-bagi. Atom tidak dapat dimusnahkan & diciptakan MODEL ATOM DALTON Konsep Model Atom Dalton : 1. Setiap benda (zat)
MODEL ATOM MODEL ATOM DALTON Atom ialah bagian terkecil suatu zat yang tidak dapat dibagi-bagi. Atom tidak dapat dimusnahkan & diciptakan MODEL ATOM DALTON Konsep Model Atom Dalton : 1. Setiap benda (zat)
Teori Atom Mekanika Klasik
 Teori Atom Mekanika Klasik -Thomson -Rutherford -Bohr -Bohr-Rutherford -Bohr-Sommerfeld Kelemahan Teori Atom Bohr: -Bohr hanya dapat menjelaskan spektrum gas hidrogen, tidak dapat menjelaskan spektrum
Teori Atom Mekanika Klasik -Thomson -Rutherford -Bohr -Bohr-Rutherford -Bohr-Sommerfeld Kelemahan Teori Atom Bohr: -Bohr hanya dapat menjelaskan spektrum gas hidrogen, tidak dapat menjelaskan spektrum
Ikatan dan Isomeri. Prof. Dr. Jumina Robby Noor Cahyono, S.Si., M.Sc.
 Ikatan dan Isomeri Prof. Dr. Jumina Robby Noor Cahyono, S.Si., M.Sc. Susunan Elektron dalam Atom Mulai dikenalkan oleh Rutherford: Atom terdiri atas inti yg kecil & padat dan dikelilingi oleh elektron-elektron
Ikatan dan Isomeri Prof. Dr. Jumina Robby Noor Cahyono, S.Si., M.Sc. Susunan Elektron dalam Atom Mulai dikenalkan oleh Rutherford: Atom terdiri atas inti yg kecil & padat dan dikelilingi oleh elektron-elektron
kimia REVIEW I TUJUAN PEMBELAJARAN
 KTSP kimia K e l a s XI REVIEW I TUJUAN PEMBELAJARAN Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami teori atom mekanika kuantum dan hubungannya dengan bilangan
KTSP kimia K e l a s XI REVIEW I TUJUAN PEMBELAJARAN Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami teori atom mekanika kuantum dan hubungannya dengan bilangan
KEGIATAN BELAJAR 2 KONFIGURASI ELEKTRON, HUBUNGANNYA DENGAN LETAK UNSUR DALAM SISTEM PERIODIK, DAN SIFAT PERIODIK UNSUR
 KEGIATAN BELAJAR 2 KONFIGURASI ELEKTRON, HUBUNGANNYA DENGAN LETAK UNSUR DALAM SISTEM PERIODIK, DAN SIFAT PERIODIK UNSUR A. CAPAIAN PEMBELAJARAN 1. Menentukan letak suatu unsur dalam SPU berdasarkan konfigurasi
KEGIATAN BELAJAR 2 KONFIGURASI ELEKTRON, HUBUNGANNYA DENGAN LETAK UNSUR DALAM SISTEM PERIODIK, DAN SIFAT PERIODIK UNSUR A. CAPAIAN PEMBELAJARAN 1. Menentukan letak suatu unsur dalam SPU berdasarkan konfigurasi
DAFTAR PUSTAKA. 1. Dra. Sukmriah M & Dra. Kamianti A, Kimia Kedokteran, edisi 2, Penerbit Binarupa Aksara, 1990
 DAFTAR PUSTAKA 1. Dra. Sukmriah M & Dra. Kamianti A, Kimia Kedokteran, edisi 2, Penerbit Binarupa Aksara, 1990 2. Drs. Hiskia Achmad, Kimia Unsur dan Radiokimia, Penerbit PT. Citra Aditya Bakti, 2001 3.
DAFTAR PUSTAKA 1. Dra. Sukmriah M & Dra. Kamianti A, Kimia Kedokteran, edisi 2, Penerbit Binarupa Aksara, 1990 2. Drs. Hiskia Achmad, Kimia Unsur dan Radiokimia, Penerbit PT. Citra Aditya Bakti, 2001 3.
Demonstrasi kembang api. Sumber: Encarta Encyclopedia, 2006
 9 FISIKA ATOM Demonstrasi kembang api. Sumber: Encarta Encyclopedia, 006 Segala sesuatu yang ada di alam terdiri atas materi, yang bentuknya bermacam-macam. Tiap materi tersusun atas unsur dan tiap unsur
9 FISIKA ATOM Demonstrasi kembang api. Sumber: Encarta Encyclopedia, 006 Segala sesuatu yang ada di alam terdiri atas materi, yang bentuknya bermacam-macam. Tiap materi tersusun atas unsur dan tiap unsur
RENCANA PELAKSANAAN PEMBELAJARAN Nama Sekolah : SMA Negeri 1 Sanden Mata Pelajaran : Kimia Kelas/Semester : XI/1 Alokasi Waktu : 2 JP
 RENCANA PELAKSANAAN PEMBELAJARAN Nama Sekolah : SMA Negeri 1 Sanden Mata Pelajaran : Kimia Kelas/Semester : XI/1 Alokasi Waktu : 2 JP Standar Kompetensi 1. Memahami struktur atom untuk meramalkan sifat-sifat
RENCANA PELAKSANAAN PEMBELAJARAN Nama Sekolah : SMA Negeri 1 Sanden Mata Pelajaran : Kimia Kelas/Semester : XI/1 Alokasi Waktu : 2 JP Standar Kompetensi 1. Memahami struktur atom untuk meramalkan sifat-sifat
KATA PENGANTAR BANDUNG, DESEMBER 2002 TIM KONSULTAN KIMIA FPTK UPI
 BAGIAN PROYEK PENGEMBANGAN KURIKULUM DIREKTORAT PENDIDIKAN MENENGAH KEJURUAN DIREKTORAT JENDERAL PENDIDIKAN DASAR DAN MENENGAH DEPARTEMEN PENDIDIKAN NASIONAL JAKARTA 2002 KATA PENGANTAR Pendidikan Menengah
BAGIAN PROYEK PENGEMBANGAN KURIKULUM DIREKTORAT PENDIDIKAN MENENGAH KEJURUAN DIREKTORAT JENDERAL PENDIDIKAN DASAR DAN MENENGAH DEPARTEMEN PENDIDIKAN NASIONAL JAKARTA 2002 KATA PENGANTAR Pendidikan Menengah
Pentalogy FISIKA SMA
 GENTA GROUP in PLAY STORE CBT UN SMA IPA Buku ini dilengkapi aplikasi CBT UN SMA IPA android yang dapat di-download di play store dengan kata kunci genta group atau gunakan qr-code di bawah. Kode Aktivasi
GENTA GROUP in PLAY STORE CBT UN SMA IPA Buku ini dilengkapi aplikasi CBT UN SMA IPA android yang dapat di-download di play store dengan kata kunci genta group atau gunakan qr-code di bawah. Kode Aktivasi
4. Atom atau kumpulan atom yang bermuatan listrik disebut. a. zat tunggal d. ion b. molekul e. gugus fungsi c. senyawa
 1. Dari rumus kimia dibawah ini 1. NH 3 3. SO 2 2. Br 2 4. O 2 Yang menyatakan rumus molekul semyawa adalah a. 1,2, dan 3 d. 4 saja b. 1 dan 3 e. 1,2,3, dan 4 2 dan 4 2. Kadar zat besi yang diperbolehkan
1. Dari rumus kimia dibawah ini 1. NH 3 3. SO 2 2. Br 2 4. O 2 Yang menyatakan rumus molekul semyawa adalah a. 1,2, dan 3 d. 4 saja b. 1 dan 3 e. 1,2,3, dan 4 2 dan 4 2. Kadar zat besi yang diperbolehkan
DEPARTEMEN PENDIDIKAN NASIONAL UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM Alamat: Karangmalang, Yogyakarta 55281
 DEPARTEMEN PENDIDIKAN NASIONAL UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM Alamat: Karangmalang, Yogyakarta 55281 RENCANA PERKULIAHAN SEMESTER (Silabus) Fakultas : FMIPA
DEPARTEMEN PENDIDIKAN NASIONAL UNIVERSITAS NEGERI YOGYAKARTA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM Alamat: Karangmalang, Yogyakarta 55281 RENCANA PERKULIAHAN SEMESTER (Silabus) Fakultas : FMIPA
BAB 2 TINJAUAN PUSTAKA
 BAB 2 TINJAUAN PUSTAKA 2.1. Struktur atom Struktur atom merupakan satuan dasar materi yang terdiri dari inti atom beserta awan elektron bermuatan negatif yang mengelilinginya. Inti atom mengandung campuran
BAB 2 TINJAUAN PUSTAKA 2.1. Struktur atom Struktur atom merupakan satuan dasar materi yang terdiri dari inti atom beserta awan elektron bermuatan negatif yang mengelilinginya. Inti atom mengandung campuran
PENEMUAN RADIOAKTIVITAS. Sulistyani, M.Si.
 PENEMUAN RADIOAKTIVITAS Sulistyani, M.Si. Email: sulistyani@uny.ac.id SINAR KATODE Penemuan sinar katode telah menginspirasi penemuan sinar-x dan radioaktivitas Sinar katode ditemukan oleh J.J Thomson
PENEMUAN RADIOAKTIVITAS Sulistyani, M.Si. Email: sulistyani@uny.ac.id SINAR KATODE Penemuan sinar katode telah menginspirasi penemuan sinar-x dan radioaktivitas Sinar katode ditemukan oleh J.J Thomson
LEMBARAN SOAL 8. Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH )
 LEMBARAN SOAL 8 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah soal dengan
LEMBARAN SOAL 8 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah soal dengan
RENCANA PELAKSANAAN PEMBELAJARAN (RPP)
 RENCANA PELAKSANAAN PEMBELAJARAN (RPP) Sekolah Mata Pelajaran Kelas/ Semester Materi Pokok Alokasi Waktu : SMAN 1 SANDEN : Kimia : X / Ganjil : Struktur Atom : 3 x 45 menit A. Kompetensi Inti KI 1 : Menghayati
RENCANA PELAKSANAAN PEMBELAJARAN (RPP) Sekolah Mata Pelajaran Kelas/ Semester Materi Pokok Alokasi Waktu : SMAN 1 SANDEN : Kimia : X / Ganjil : Struktur Atom : 3 x 45 menit A. Kompetensi Inti KI 1 : Menghayati
Inti Atom dan Penyusunnya. Sulistyani, M.Si.
 Inti Atom dan Penyusunnya Sulistyani, M.Si. Email: sulistyani@uny.ac.id Eksperimen Marsden dan Geiger Pendahuluan Teori tentang atom pertama kali dikemukakan oleh Dalton bahwa atom bagian terkecil dari
Inti Atom dan Penyusunnya Sulistyani, M.Si. Email: sulistyani@uny.ac.id Eksperimen Marsden dan Geiger Pendahuluan Teori tentang atom pertama kali dikemukakan oleh Dalton bahwa atom bagian terkecil dari
Spektrum Gelombang Elektromagnetik
 Spektrum Gelombang Elektromagnetik Hubungan spektrum dengan elektron Berkaitan dengan energi energi cahaya. energi gerak elektron dan Keadaan elektron : Saat arus dilewatkan melalui gas pada tekanan rendah,
Spektrum Gelombang Elektromagnetik Hubungan spektrum dengan elektron Berkaitan dengan energi energi cahaya. energi gerak elektron dan Keadaan elektron : Saat arus dilewatkan melalui gas pada tekanan rendah,
RENCANA PELAKSANAAN PEMBELAJARAN
 RENCANA PELAKSANAAN PEMBELAJARAN Nama Sekolah Kelas/semester Subtopik Alokasi waktu : SMA N 1 Muntilan : XI/I : Bilangan Kuantum dan Bentuk Orbital : 2 x 35 menit A. Standar Kompetensi Memahami struktur
RENCANA PELAKSANAAN PEMBELAJARAN Nama Sekolah Kelas/semester Subtopik Alokasi waktu : SMA N 1 Muntilan : XI/I : Bilangan Kuantum dan Bentuk Orbital : 2 x 35 menit A. Standar Kompetensi Memahami struktur
LAPORAN TUGAS MIKROELEKTONIKA
 LAPORAN TUGAS MIKROELEKTONIKA Struktur Internal Atom Disusun oleh : Nama : Bayu Saputra NIM : 13081245 Kelas : 13.4A.11 Dosen : Juniar Synaga BINA SARANA INFORMATIKA 2010 BAB 1 PENDAHULUAN A.Maksud dan
LAPORAN TUGAS MIKROELEKTONIKA Struktur Internal Atom Disusun oleh : Nama : Bayu Saputra NIM : 13081245 Kelas : 13.4A.11 Dosen : Juniar Synaga BINA SARANA INFORMATIKA 2010 BAB 1 PENDAHULUAN A.Maksud dan
BAB I MATERI, STRUKTUR ATOM DAN SISTEM PERIODIK
 BAB I MATERI, STRUKTUR ATOM DAN SISTEM PERIODIK A. Standar Kompetensi: Memahami tentang ilmu kimia dan dasar-dasarnya serta mampu menerapkannya dalam kehidupan se-hari-hari terutama yang berhubungan langsung
BAB I MATERI, STRUKTUR ATOM DAN SISTEM PERIODIK A. Standar Kompetensi: Memahami tentang ilmu kimia dan dasar-dasarnya serta mampu menerapkannya dalam kehidupan se-hari-hari terutama yang berhubungan langsung
STRUKTUR ATOM, SPU, & IKATAN KIMIA
 Bidang: KIMIA DASAR Materi ini dapat diunduh di https://arisarianto.wordpress.com Materi tambahan lainnya, kunjungi portal https://school.quipper.com/id/index.html buka kelas khusus SMAN MODEL TERPADU
Bidang: KIMIA DASAR Materi ini dapat diunduh di https://arisarianto.wordpress.com Materi tambahan lainnya, kunjungi portal https://school.quipper.com/id/index.html buka kelas khusus SMAN MODEL TERPADU
MAKALAH IKATAN KIMIA STRUKTUR ATOM
 MAKALAH IKATAN KIMIA STRUKTUR ATOM Disusun Oleh: Kelompok I 1. Panji Mulyotomo 1112096000037 2. Henggar Wahyu Siswanti 1112096000038 3. Desi Iftalia 1112096000048 4. Ihya Sulthonuddin 1112096000055 PROGRAM
MAKALAH IKATAN KIMIA STRUKTUR ATOM Disusun Oleh: Kelompok I 1. Panji Mulyotomo 1112096000037 2. Henggar Wahyu Siswanti 1112096000038 3. Desi Iftalia 1112096000048 4. Ihya Sulthonuddin 1112096000055 PROGRAM
X Z. ISOTOP Atom atom yang sama mempunyai nomor atom sama tetapi nomor massa berbeda disebut isotop Contoh : H 1 H 1 H 1
 MODUL -1 NOTASI UNSUR & JUMLAH PROTON, ELEKTRON & NEUTRON Standar Kompetensi : : 1. Memahami struktur atom, sifat-sifat periodik unsur, dan ikatan kimia Kompetensi Dasar : 1.1.Memahami struktur atom berdasarkan
MODUL -1 NOTASI UNSUR & JUMLAH PROTON, ELEKTRON & NEUTRON Standar Kompetensi : : 1. Memahami struktur atom, sifat-sifat periodik unsur, dan ikatan kimia Kompetensi Dasar : 1.1.Memahami struktur atom berdasarkan
WEEK II ATOM, MOLEKUL, DAN ION
 1 WEEK II ATOM, MOLEKUL, DAN ION 2 TEORI ATOM Gagasan tentang atom sudah dimulai sejak abad ke-5 SM. Democratus mengungkapkan bahwa semua materi terdiri atas partikel yang sangat kecil dan tidak dapat
1 WEEK II ATOM, MOLEKUL, DAN ION 2 TEORI ATOM Gagasan tentang atom sudah dimulai sejak abad ke-5 SM. Democratus mengungkapkan bahwa semua materi terdiri atas partikel yang sangat kecil dan tidak dapat
KATA PENGANTAR. Surabaya, 30 Juni Penulis
 KATA PENGANTAR Puji syukur Alhamdulillah saya panjatkan kehadirat Allah SWT, karena hanya berkat rahmat dan hidayah-nya lah saya bisa menyelesaikan tugas dari dosen mata kuliah Fisika Dasar II untuk membuat
KATA PENGANTAR Puji syukur Alhamdulillah saya panjatkan kehadirat Allah SWT, karena hanya berkat rahmat dan hidayah-nya lah saya bisa menyelesaikan tugas dari dosen mata kuliah Fisika Dasar II untuk membuat
LEMBARAN SOAL 1. Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH ) SOAL
 LEMBARAN SOAL 1 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH ) PETUNJUK UMUM 1. Tulis nomor nama Anda pada lembar jawaban yang disediakan 2. Periksa bacalah soal dengan teliti
LEMBARAN SOAL 1 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH ) PETUNJUK UMUM 1. Tulis nomor nama Anda pada lembar jawaban yang disediakan 2. Periksa bacalah soal dengan teliti
RENCANA PELAKSANAAN PEMBELAJARAN
 RENCANA PELAKSANAAN PEMBELAJARAN Nama Sekolah Kelas/semester Subtopik Alokasi waktu : SMA N 1 Muntilan : XI/I : Bilangan Kuantum dan Bentuk Orbital : 2 x 35 menit A. Standar Kompetensi Memahami struktur
RENCANA PELAKSANAAN PEMBELAJARAN Nama Sekolah Kelas/semester Subtopik Alokasi waktu : SMA N 1 Muntilan : XI/I : Bilangan Kuantum dan Bentuk Orbital : 2 x 35 menit A. Standar Kompetensi Memahami struktur
BAB FISIKA ATOM I. SOAL PILIHAN GANDA
 FISIK TOM I. SOL PILIHN GND 0. Pernyataan berikut yang termasuk teori atom menurut Dalton adala... agian terkecil suatu atom adala elektron. lektron dari suatu unsur sama dengan elektron dari unsure lain.
FISIK TOM I. SOL PILIHN GND 0. Pernyataan berikut yang termasuk teori atom menurut Dalton adala... agian terkecil suatu atom adala elektron. lektron dari suatu unsur sama dengan elektron dari unsure lain.
FISIKA ATOM & RADIASI
 FISIKA ATOM & RADIASI Atom bagian terkecil dari suatu elemen yang berperan dalam reaksi kimia, bersifat netral (muatan positif dan negatif sama). Model atom: J.J. Thomson (1910), Ernest Rutherford (1911),
FISIKA ATOM & RADIASI Atom bagian terkecil dari suatu elemen yang berperan dalam reaksi kimia, bersifat netral (muatan positif dan negatif sama). Model atom: J.J. Thomson (1910), Ernest Rutherford (1911),
LK S I.A. M. Partikel Materi Ion. Atom.Molekul SMP. ƙ ǐ. 8 B MTs. ĺƿȃ NAMA : KELAS : NO. ABSEN : SEKOLAH : Lembar Kegiatan Siswa SMP / MTs Kelas 8 B
 LK S I.A. M SMP 8 B MTs ĺƿȃ ɱ ǐ ƙ ǐ ά Partikel Materi Ion. Atom.Molekul NAMA : KELAS : NO. ABSEN : SEKOLAH : LK [ S I.A. M Partikel Materi Ion. Atom.Molekul PE NY AAM MAESAROH (1004571) MEGA WIJAYANTI
LK S I.A. M SMP 8 B MTs ĺƿȃ ɱ ǐ ƙ ǐ ά Partikel Materi Ion. Atom.Molekul NAMA : KELAS : NO. ABSEN : SEKOLAH : LK [ S I.A. M Partikel Materi Ion. Atom.Molekul PE NY AAM MAESAROH (1004571) MEGA WIJAYANTI
Model Atom. Modul 1 PENDAHULUAN
 Modul 1 Model Atom Drs. Alimufi Arief, M.Pd. P PENDAHULUAN ara ilmuwan telah menduga bahwa materi walaupun kelihatannya kontinu dia memiliki struktur tertentu pada tingkat mikroskopik di luar jangkauan
Modul 1 Model Atom Drs. Alimufi Arief, M.Pd. P PENDAHULUAN ara ilmuwan telah menduga bahwa materi walaupun kelihatannya kontinu dia memiliki struktur tertentu pada tingkat mikroskopik di luar jangkauan
