BAB 2 STRUKTUR ATOM PERKEMBANGAN TEORI ATOM
|
|
|
- Yanti Chandra
- 7 tahun lalu
- Tontonan:
Transkripsi
1 BAB 2 STRUKTUR ATOM PARTIKEL MATERI Bagian terkecil dari materi disebut partikel. Beberapa pendapat tentang partikel materi :. Menurut Democritus, pembagian materi bersifat diskontinyu ( jika suatu materi dibagi dan terus dibagi maka akhirnya diperoleh partikel terkecil yang sudah tidak dapat dibagi lagi = disebut Atom ) 2. Menurut Plato dan Aristoteles, pembagian materi bersifat kontinyu ( pembagian dapat berlanjut tanpa batas ) Postulat Dasar dari Teori Atom Dalton : ) Setiap materi terdiri atas partikel yang disebut atom 2) Unsur adalah materi yang terdiri atas sejenis atom 3) Atom suatu unsur adalah identik tetapi berbeda dengan atom unsur lain ( mempunyai massa yang berbeda ) 4) Senyawa adalah materi yang terdiri atas 2 atau lebih jenis atom dengan perbandingan tertentu 5) Atom tidak dapat diciptakan atau dimusnahkan dan tidak dapat diubah menjadi atom lain melalui reaksi kimia biasa. Reaksi kimia hanyalah penataan ulang ( reorganisasi ) atom-atom yang terlibat dalam reaksi tersebut Kelemahan dari postulat teori Atom Dalton : ) Atom bukanlah sesuatu yang tak terbagi, melainkan terdiri dari partikel subatom 2) Atom-atom dari unsur yang sama, dapat mempunyai massa yang berbeda ( disebut Isotop ) 3) Atom dari suatu unsur dapat diubah menjadi atom unsur lain melalui Reaksi Nuklir 4) Beberapa unsur tidak terdiri dari atom-atom melainkan molekul-molekul PERKEMBANGAN TEORI ATOM ). Model Atom Dalton a) Atom digambarkan sebagai bola pejal yang sangat kecil. b) Atom merupakan partikel terkecil yang tidak dapat dipecah lagi. c) Atom suatu unsur sama memiliki sifat yang sama, sedangkan atom unsur berbeda, berlainan dalam massa dan sifatnya. d) Senyawa terbentuk jika atom bergabung satu sama lain. e) Reaksi kimia hanyalah reorganisasi dari atom-atom, sehingga tidak ada atom yang berubah akibat reaksi kimia. Gambar Model Atom Dalton Teori atom Dalton ditunjang oleh 2 hukum alam yaitu :. Hukum Kekekalan Massa ( hukum Lavoisier ) : massa zat sebelum dan sesudah reaksi adalah sama. 2. Hukum Perbandingan Tetap ( hukum Proust ) : perbandingan massa unsur-unsur yang menyusun suatu zat adalah tetap.
2 Kelemahan Model Atom Dalton : ) Tidak dapat menjelaskan perbedaan antara atom unsur yang satu dengan unsur yang lain 2) Tidak dapat menjelaskan sifat listrik dari materi 3) Tidak dapat menjelaskan cara atom-atom saling berikatan 4) Menurut teori atom Dalton nomor 5, tidak ada atom yang berubah akibat reaksi kimia. Kini ternyata dengan reaksi kimia 238 U 92 nuklir, suatu atom dapat berubah menjadi atom lain. 234 Th He + 4 N He 7 O 8 + H 2). Model Atom Thomson Setelah ditemukannya elektron oleh J.J Thomson, disusunlah model atom Thomson yang merupakan penyempurnaan dari model atom Dalton. Menurut Thomson : a) Atom terdiri dari materi bermuatan positif dan di dalamnya tersebar elektron (bagaikan kismis dalam roti kismis) b) Atom bersifat netral, yaitu muatan positif dan muatan negatif jumlahnya sama Perhatikan Gambar Model Atom Thomson dari Buku Paket Kimia A halaman 25! 3). Model Atom Rutherford a) Rutherford menemukan bukti bahwa dalam atom terdapat inti atom yang bermuatan positif, berukuran lebih kecil daripada ukuran atom tetapi massa atom hampir seluruhnya berasal dari massa intinya. b) Atom terdiri dari inti atom yang bermuatan positif dan berada pada pusat atom serta elektron bergerak melintasi inti (seperti planet dalam tata surya). c) Atom bersifat netral. d) Jari-jari inti atom dan jari-jari atom sudah dapat ditentukan. Kelemahan Model Atom Rutherford : Ketidakmampuan untuk menjelaskan mengapa elektron tidak jatuh ke inti atom akibat gaya tarik elektrostatis inti terhadap elektron. Menurut teori Maxwell, jika elektron sebagai partikel bermuatan mengitari inti yang memiliki muatan yang berlawanan maka lintasannya akan berbentuk spiral dan akan kehilangan tenaga/energi dalam bentuk radiasi sehingga akhirnya jatuh ke inti. Perhatikan Gambar Model Atom Rutherford dari Buku Paket Kimia A halaman 27! 4). Model Atom Niels Bohr Model atomnya didasarkan pada teori kuantum untuk menjelaskan spektrum gas hidrogen. Menurut Bohr, spektrum garis menunjukkan bahwa elektron hanya menempati tingkat-tingkat energi tertentu dalam atom. Menurutnya : a) Atom terdiri dari inti yang bermuatan positif dan di sekitarnya beredar elektron-elektron yang bermuatan negatif. b) Elektron beredar mengelilingi inti atom pada orbit tertentu yang dikenal sebagai keadaan gerakan yang stasioner (tetap) yang selanjutnya disebut dengan tingkat energi utama (kulit elektron) yang dinyatakan dengan bilangan kuantum utama (n). c) Selama elektron berada dalam lintasan stasioner, energinya akan tetap sehingga tidak ada cahaya yang dipancarkan. 2
3 d) Elektron hanya dapat berpindah dari lintasan stasioner yang lebih rendah ke lintasan stasioner yang lebih tinggi jika menyerap energi. Sebaliknya, jika elektron berpindah dari lintasan stasioner yang lebih tinggi ke rendah terjadi pelepasan energi. e) Pada keadaan normal (tanpa pengaruh luar), elektron menempati tingkat energi terendah (disebut tingkat dasar = ground state). Perhatikan Gambar Model Atom Niels Bohr dari Buku Paket Kimia A halaman 29! Kelemahan Model Atom Niels Bohr :. Hanya dapat menerangkan spektrum dari atom atau ion yang mengandung satu elektron dan tidak sesuai dengan spektrum atom atau ion yang berelektron banyak. 2. Tidak mampu menerangkan bahwa atom dapat membentuk molekul melalui ikatan kimia. 5). Model Atom Modern Dikembangkan berdasarkan teori mekanika kuantum yang disebut mekanika gelombang; diprakarsai oleh 3 ahli : a) Louis Victor de Broglie Menyatakan bahwa materi mempunyai dualisme sifat yaitu sebagai materi dan sebagai gelombang. b) Werner Heisenberg Mengemukakan prinsip ketidakpastian untuk materi yang bersifat sebagai partikel dan gelombang. Jarak atau letak elektron-elektron yang mengelilingi inti hanya dapat ditentukan dengan kemungkinan kemungkinan saja. c) Erwin Schrodinger (menyempurnakan model Atom Bohr) Berhasil menyusun persamaan gelombang untuk elektron dengan menggunakan prinsip mekanika gelombang. Elektronelektron yang mengelilingi inti terdapat di dalam suatu orbital yaitu daerah 3 dimensi di sekitar inti dimana elektron dengan energi tertentu dapat ditemukan dengan kemungkinan terbesar. Model atom Modern : a) Atom terdiri dari inti atom yang mengandung proton dan neutron sedangkan elektron-elektron bergerak mengitari inti atom dan berada pada orbital-orbital tertentu yang membentuk kulit atom. b) Orbital yaitu daerah 3 dimensi di sekitar inti dimana elektron dengan energi tertentu dapat ditemukan dengan kemungkinan terbesar. c) Kedudukan elektron pada orbital-orbitalnya dinyatakan dengan bilangan kuantum. Orbit Orbital Gambar Perbedaan antara orbit dan orbital untuk electron Orbital digambarkan sebagai awan elektron yaitu : bentuk-bentuk ruang dimana suatu elektron kemungkinan ditemukan. Semakin rapat awan elektron maka semakin besar kemungkinan elektron ditemukan dan sebaliknya. Catatan : Pelajari sejarah penemuan elektron, neutron, proton dan inti atom dari Buku Paket Kimia A halaman 22-33! 3
4 PARTIKEL DASAR PENYUSUN ATOM Partikel Notasi Massa Muatan Sesungguhnya Relatif thd proton Sesungguhnya Relatif thd proton Proton p,67 x 0-24 g sma,6 x 0-9 C + Neutron n,67 x 0-24 g sma 0 0 Elektron e 9, x 0-28 g 840 sma -,6 x 0-9 C - Catatan : massa partikel dasar dinyatakan dalam satuan massa atom ( sma ). sma =,66 x 0-24 gram NOMOR ATOM Menyatakan jumlah proton dalam atom. Untuk atom netral, jumlah proton = jumlah elektron (nomor atom juga menyatakan jumlah elektron). Diberi simbol huruf Z Atom yang melepaskan elektron berubah menjadi ion positif, sebaliknya yang menerima elektron berubah menjadi ion negatif. 9K Artinya.. NOMOR MASSA Menunjukkan jumlah proton dan neutron dalam inti atom. Proton dan neutron sebagai partikel penyusun inti atom disebut Nukleon. Jumlah nukleon dalam atom suatu unsur dinyatakan sebagai Nomor Massa (diberi lambang huruf A), sehingga : A A = nomor massa = jumlah proton ( p ) + jumlah neutron ( n ) = p + n = Z + n Penulisan atom tunggal dilengkapi dengan nomor atom di sebelah kiri bawah dan nomor massa di sebelah kiri atas dari lambang atom tersebut. Notasi semacam ini disebut dengan Nuklida. A X Z Keterangan : X = lambang atom A = nomor massa Z = nomor atom SUSUNAN ION 238 U 92 Suatu atom dapat kehilangan/melepaskan elektron atau mendapat/menerima elektron tambahan. Atom yang kehilangan/melepaskan elektron, akan menjadi ion positif (kation). Atom yang mendapat/menerima elektron, akan menjadi ion negatif (anion). Dalam suatu Ion, yang berubah hanyalah jumlah elektron saja, sedangkan jumlah proton dan neutronnya tetap. 4
5 Spesi Proton Elektron Neutron Atom Na 2 Ion Ion Na 0 2 Na 2 2 Rumus umum untuk menghitung jumlah proton, neutron dan elektron : ). Untuk nuklida atom netral : A Z X : p = Z e = Z n = (A-Z) 2). Untuk nuklida kation : A y Z X : p = Z e = Z (+y) n = (A-Z) 3). Untuk nuklida anion : A y Z X : p = Z e = Z (-y) n = (A-Z) ISOTOP, ISOBAR DAN ISOTON ). ISOTOP Adalah atom-atom dari unsur yang sama (mempunyai nomor atom yang sama) tetapi berbeda nomor massanya. 2 C 3 ; C 4 ; C ). ISOBAR Adalah atom-atom dari unsur yang berbeda (mempunyai nomor atom berbeda) tetapi mempunyai nomor massa yang sama. 4 C 4 dengan N 6 7 3). ISOTON Adalah atom-atom dari unsur yang berbeda (mempunyai nomor atom berbeda) tetapi mempunyai jumlah neutron yang sama. 3 P 5 dengan S
6 KONFIGURASI ELEKTRON Persebaran elektron dalam kulit-kulit atomnya disebut konfigurasi. Kulit atom yang pertama (yang paling dekat dengan inti) diberi lambang K, kulit ke-2 diberi lambang L dst. Jumlah maksimum elektron pada setiap kulit memenuhi rumus 2n 2 (n = nomor kulit). Kulit K (n = ) maksimum 2 x 2 = 2 elektron Kulit L (n = 2) maksimum 2 x 2 2 = 8 elektron Kulit M (n = 3) maksimum 2 x 3 2 = 8 elektron Kulit N (n = 4) maksimum 2 x 4 2 = 32 elektron Kulit O (n = 5) maksimum 2 x 5 2 = 50 elektron Catatan : Meskipun kulit O, P dan Q dapat menampung lebih dari 32 elektron, namun kenyataannya kulit-kulit tersebut belum pernah terisi penuh. Langkah-Langkah Penulisan Konfigurasi Elektron :. Kulit-kulit diisi mulai dari kulit K, kemudian L dst. 2. Khusus untuk golongan utama (golongan A) : Jumlah kulit = nomor periode Jumlah elektron valensi = nomor golongan 3. Jumlah maksimum elektron pada kulit terluar (elektron valensi) adalah 8. o Elektron valensi berperan pada pembentukan ikatan antar atom dalam membentuk suatu senyawa. o Sifat kimia suatu unsur ditentukan juga oleh elektron valensinya. Oleh karena itu, unsur-unsur yang memiliki elektron valensi sama, akan memiliki sifat kimia yang mirip. 4. Untuk unsur golongan utama ( golongan A ), konfigurasi elektronnya dapat ditentukan sebagai berikut : a) Sebanyak mungkin kulit diisi penuh dengan elektron. b) Tentukan jumlah elektron yang tersisa. Jika jumlah elektron yang tersisa > 32, kulit berikutnya diisi dengan 32 elektron. Jika jumlah elektron yang tersisa < 32, kulit berikutnya diisi dengan 8 elektron. Jika jumlah elektron yang tersisa < 8, kulit berikutnya diisi dengan 8 elektron. Penting untuk dipahami! Jika jumlah elektron yang tersisa < 8, semua elektron diisikan pada kulit berikutnya. Unsur Nomor Atom K L M N O He 2 2 Li 3 2 Ar Ca Sr Catatan : Konfigurasi elektron untuk unsur-unsur golongan B (golongan transisi) sedikit berbeda dari golongan A (golongan utama). 6
7 Elektron tambahan tidak mengisi kulit terluar, tetapi mengisi kulit ke-2 terluar; sedemikian sehingga kulit ke-2 terluar itu berisi 8 elektron. Unsur Nomor Atom K L M N Sc Ti Mn Zn Konfigurasi Elektron Beberapa Unsur Golongan A ( Utama ) dan Golongan B ( Transisi ) Periode Nomor Atom ( Z ) K L M N O P Q *** *** *** Keterangan : Tanda ( *** ) = termasuk Golongan B ( Transisi ) 7
8 MASSA ATOM RELATIF ( Ar ) ( Pelajari Buku Paket Kimia A halaman 42 sampai 45! ) Adalah perbandingan massa antar atom yang terhadap atom yang lainnya. Pada umumnya, unsur terdiri dari beberapa isotop maka pada penetapan massa atom relatif ( Ar ) digunakan massa rata-rata dari isotop-isotopnya. Menurut IUPAC, sebagai pembanding digunakan atom C-2 yaitu dari massa atom C-2; sehingga dirumuskan : 2 Ar unsur X = massa rata rata atom unsur X massa atom C 2 2 () Karena : massa atom C-2 = sma ; maka : 2 Ar unsur X = massa rata rata atom unsur X sma (2) MASSA MOLEKUL RELATIF ( Mr ) Adalah perbandingan massa antara suatu molekul dengan suatu standar. Besarnya massa molekul relatif ( Mr ) suatu zat = jumlah massa atom relatif ( Ar ) dari atom-atom penyusun molekul zat tersebut. Khusus untuk senyawa ion digunakan istilah Massa Rumus Relatif ( Mr ) karena senyawa ion tidak terdiri atas molekul. Mr = Ar Diketahui : massa atom relatif ( Ar ) H = ; C = 2; N = 4 dan O = 6. Berapa massa molekul relatif ( Mr ) dari CO(NH2)2 Jawab : Mr CO(NH2)2 = ( x Ar C) + ( x Ar O) + (2 x Ar N) + (4 x Ar H) = ( x 2) + ( x 6) + (2 x 4) + (4 x ) =
Struktur atom. Bagian terkecil dari materi disebut partikel. Beberapa pendapat tentang partikel materi :
 Struktur atom A PARTIKEL MATERI Bagian terkecil dari materi disebut partikel. Beberapa pendapat tentang partikel materi : Menurut Democritus, pembagian materi bersifat diskontinyu ( jika suatu materi dibagi
Struktur atom A PARTIKEL MATERI Bagian terkecil dari materi disebut partikel. Beberapa pendapat tentang partikel materi : Menurut Democritus, pembagian materi bersifat diskontinyu ( jika suatu materi dibagi
Apa yang dimaksud dengan atom? Atom adalah bagian terkecil dari suatu unsur
 Struktur Atom Apa yang dimaksud dengan atom? Atom adalah bagian terkecil dari suatu unsur Atom tersusun atas partikel apa saja? Partikel-partikel penyusun atom : Partikel Lambang Penemu Muatan Massa 9,11x10-28g
Struktur Atom Apa yang dimaksud dengan atom? Atom adalah bagian terkecil dari suatu unsur Atom tersusun atas partikel apa saja? Partikel-partikel penyusun atom : Partikel Lambang Penemu Muatan Massa 9,11x10-28g
Perkembangan Model Atom. Semester 1
 Perkembangan Model Atom Semester 1 Model atom adalah suatu gambar rekaan atom berdasarkan eksperimen ataupun kajian teoritis, karena para ahli tidak tahu pasti seperti apakah bentuk atom itu sebenarnya.
Perkembangan Model Atom Semester 1 Model atom adalah suatu gambar rekaan atom berdasarkan eksperimen ataupun kajian teoritis, karena para ahli tidak tahu pasti seperti apakah bentuk atom itu sebenarnya.
Penyusun bagian-bagian atom sangat menentukan sifat benda/materi. Untuk mengetahui bagaimana atom bergabung sehingga dapat mengubah bahan sesuai
 Struktur Atom Mengapa atom dipelajari? Penyusun bagian-bagian atom sangat menentukan sifat benda/materi. Untuk mengetahui bagaimana atom bergabung sehingga dapat mengubah bahan sesuai dengan kebutuhan.
Struktur Atom Mengapa atom dipelajari? Penyusun bagian-bagian atom sangat menentukan sifat benda/materi. Untuk mengetahui bagaimana atom bergabung sehingga dapat mengubah bahan sesuai dengan kebutuhan.
PERKEMBANGAN MODEL ATOM DI SUSUN OLEH YOSI APRIYANTI A1F012044
 PERKEMBANGAN MODEL ATOM DI SUSUN OLEH YOSI APRIYANTI A1F012044 PERKEMBANGAN MODEL ATOM Seorang filsuf Yunani yang bernama Democritus berpendapat bahwa jika suatu benda dibelah terus menerus, maka pada
PERKEMBANGAN MODEL ATOM DI SUSUN OLEH YOSI APRIYANTI A1F012044 PERKEMBANGAN MODEL ATOM Seorang filsuf Yunani yang bernama Democritus berpendapat bahwa jika suatu benda dibelah terus menerus, maka pada
Struktur Atom. Struktur atom merupakan satuan dasar materi yang terdiri dari inti atom beserta awan elektron bermuatan negatif yang
 Struktur atom merupakan satuan dasar materi yang terdiri dari inti atom beserta awan elektron bermuatan negatif yang mengelilinginya. Inti atom mengandung campuran proton (bermuatan positif) dan neutron
Struktur atom merupakan satuan dasar materi yang terdiri dari inti atom beserta awan elektron bermuatan negatif yang mengelilinginya. Inti atom mengandung campuran proton (bermuatan positif) dan neutron
BAB 1 PERKEMBANGAN TEORI ATOM
 BAB 1 PERKEMBANGAN TEORI ATOM 1.1 Teori Atom Perkembangan teori atom merupakan sumbangan pikiran dari banyak ilmuan. Konsep dari suatu atom bukanlah hal yang baru. Ahli-ahli filsafah Yunani pada tahun
BAB 1 PERKEMBANGAN TEORI ATOM 1.1 Teori Atom Perkembangan teori atom merupakan sumbangan pikiran dari banyak ilmuan. Konsep dari suatu atom bukanlah hal yang baru. Ahli-ahli filsafah Yunani pada tahun
STRUKTUR ATOM A. PENGERTIAN DASAR
 STRUKTUR ATOM A. PENGERTIAN DASAR 1. Partikel dasar : partikel-partikel pembentuk atom yang terdiri dari elektron, proton den neutron. 1. Proton : partikel pembentuk atom yang mempunyai massa sama dengan
STRUKTUR ATOM A. PENGERTIAN DASAR 1. Partikel dasar : partikel-partikel pembentuk atom yang terdiri dari elektron, proton den neutron. 1. Proton : partikel pembentuk atom yang mempunyai massa sama dengan
STRUKTUR ATOM. Perkembangan Teori Atom
 STRUKTUR ATOM Perkembangan Teori Atom 400 SM filsuf Yunani Demokritus materi terdiri dari beragam jenis partikel kecil 400 SM dan memiliki sifat dari materi yang ditentukan sifat partikel tersebut Dalton
STRUKTUR ATOM Perkembangan Teori Atom 400 SM filsuf Yunani Demokritus materi terdiri dari beragam jenis partikel kecil 400 SM dan memiliki sifat dari materi yang ditentukan sifat partikel tersebut Dalton
MODUL KIMIA SMA IPA Kelas 10
 SMA IPA Kelas Atom Bagian terkecil dari materi yang sudah tidak dapat dibagi lagi disebut atom (berasal dari bahasa Yunani atomos yang berarti tidak dapat dibagi lagi). Namun, berakhir pendapat tersebut
SMA IPA Kelas Atom Bagian terkecil dari materi yang sudah tidak dapat dibagi lagi disebut atom (berasal dari bahasa Yunani atomos yang berarti tidak dapat dibagi lagi). Namun, berakhir pendapat tersebut
Struktur Atom Untuk SMK Teknologi dan Pertanian. Kelas X Semester 1 Penyusun : SMK Negeri 7 Bandung
 Struktur Atom Untuk SMK Teknologi dan Pertanian Kelas X Semester 1 Penyusun : SMK Negeri 7 Bandung Kompetensi Dasar Mengidentifikasi partikel atom Memahami eksperimen tentang inti atom Mengidentifikasi
Struktur Atom Untuk SMK Teknologi dan Pertanian Kelas X Semester 1 Penyusun : SMK Negeri 7 Bandung Kompetensi Dasar Mengidentifikasi partikel atom Memahami eksperimen tentang inti atom Mengidentifikasi
BAB I MATERI. Perb kimia. Unsur : Senyawa : Zat yang tidak dapat dipisahkan lagi. Kombinasi kimia dari dua atau lebih unsur.
 BAB I MATERI Materi adalah sesuatu yang menempati ruang dan memiliki massa. Ilmu kimia adalah ilmu yang mempelajari materi dan perubahan yang terjadi pada materi tersebut.sifat dan perubahan materi dapat
BAB I MATERI Materi adalah sesuatu yang menempati ruang dan memiliki massa. Ilmu kimia adalah ilmu yang mempelajari materi dan perubahan yang terjadi pada materi tersebut.sifat dan perubahan materi dapat
Bunyi Teori Atom Dalton:
 Bunyi Teori Atom Dalton: Pada 1808, ilmuwan berkebangsaan Inggris, John Dalton, mengemuka- kan teorinya tentang materi atom yang dipublikasikan dalam A New System of Chemical Philosophy. Berdasarkan penelitian
Bunyi Teori Atom Dalton: Pada 1808, ilmuwan berkebangsaan Inggris, John Dalton, mengemuka- kan teorinya tentang materi atom yang dipublikasikan dalam A New System of Chemical Philosophy. Berdasarkan penelitian
STRUKTUR ATOM DAN SISTEM PERIODIK Kimia SMK KELAS X SEMESTER 1 SMK MUHAMMADIYAH 3 METRO
 STRUKTUR ATOM DAN SISTEM PERIODIK Kimia SMK KELAS X SEMESTER 1 SMK MUHAMMADIYAH 3 METRO SK DAN KD Standar Kompetensi Mengidentifikasi struktur atom dan sifat-sifat periodik pada tabel periodik unsur Kompetensi
STRUKTUR ATOM DAN SISTEM PERIODIK Kimia SMK KELAS X SEMESTER 1 SMK MUHAMMADIYAH 3 METRO SK DAN KD Standar Kompetensi Mengidentifikasi struktur atom dan sifat-sifat periodik pada tabel periodik unsur Kompetensi
Mekanika Kuantum. Orbital dan Bilangan Kuantum
 Standar Kompetensi Kompetensi Dasar Mendeskripsikan struktur atom dan sifat-sifat periodik serta struktur molekul dan sifat-sifatnya. Menerapkan teori atom mekanika kuantum untuk menuliskan konfigurasi
Standar Kompetensi Kompetensi Dasar Mendeskripsikan struktur atom dan sifat-sifat periodik serta struktur molekul dan sifat-sifatnya. Menerapkan teori atom mekanika kuantum untuk menuliskan konfigurasi
SMA NEGERI 48 JAKARTA
 Nama : Kelas : Tanggal : PEMERINTAH PROPINSI DAERAH KHUSUS IBUKOTA JAKARTA DINAS PENDIDIKAN SMA NEGERI 48 JAKARTA Jln. Pinang Ranti II TMII, Tel. 8009437-8006204/Fax.(021) 8009437 Jakarta Timur 13560 Website:www.sman48-jkt.sch.com,:
Nama : Kelas : Tanggal : PEMERINTAH PROPINSI DAERAH KHUSUS IBUKOTA JAKARTA DINAS PENDIDIKAN SMA NEGERI 48 JAKARTA Jln. Pinang Ranti II TMII, Tel. 8009437-8006204/Fax.(021) 8009437 Jakarta Timur 13560 Website:www.sman48-jkt.sch.com,:
BAB I STRUKTUR ATOM DAN SISTEM PERIODIK UNSUR
 BAB I STRUKTUR ATOM DAN SISTEM PERIODIK UNSUR A. STANDAR KOMPOTENSI 1 : Mendeskripsikan struktur atom,sifat-sifat periodik unsur, dan ikatan kimia serta struktur molekul dan sifat-sifatnya. B. KOMPETENSI
BAB I STRUKTUR ATOM DAN SISTEM PERIODIK UNSUR A. STANDAR KOMPOTENSI 1 : Mendeskripsikan struktur atom,sifat-sifat periodik unsur, dan ikatan kimia serta struktur molekul dan sifat-sifatnya. B. KOMPETENSI
TEORI ATOM. Ramadoni Syahputra
 TEORI ATOM Ramadoni Syahputra STRUKTUR ATOM Teori tentang atom pertama kali dikemukakan oleh filsafat Yunani yaitu Leoclipus dan Democritus, pada abad ke-5 sebelum Masehi. Atom berasal dari kata Yunani:
TEORI ATOM Ramadoni Syahputra STRUKTUR ATOM Teori tentang atom pertama kali dikemukakan oleh filsafat Yunani yaitu Leoclipus dan Democritus, pada abad ke-5 sebelum Masehi. Atom berasal dari kata Yunani:
kimia Kelas X REVIEW I K-13 A. Hakikat Ilmu Kimia
 K-13 Kelas X kimia REVIEW I Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami hakikat ilmu kimia dan metode ilmiah. 2. Memahami teori atom dan
K-13 Kelas X kimia REVIEW I Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami hakikat ilmu kimia dan metode ilmiah. 2. Memahami teori atom dan
Bab 1 STRUKTUR ATOM. Pada pelajaran bab pertama ini akan dipelajari tentang perkembangan teori atom, notasi unsur, Isotop, isobar, dan isoton.
 Bab STRUKTUR ATOM Gambar. Teori Atom Rutherford. Sumber: Ensiklopedia Iptek Pada pelajaran bab pertama ini akan dipelajari tentang perkembangan teori atom, notasi unsur, Isotop, isobar, dan isoton. Struktur
Bab STRUKTUR ATOM Gambar. Teori Atom Rutherford. Sumber: Ensiklopedia Iptek Pada pelajaran bab pertama ini akan dipelajari tentang perkembangan teori atom, notasi unsur, Isotop, isobar, dan isoton. Struktur
BAB FISIKA ATOM. Model ini gagal karena tidak sesuai dengan hasil percobaan hamburan patikel oleh Rutherford.
 1 BAB FISIKA ATOM Perkembangan teori atom Model Atom Dalton 1. Atom adalah bagian terkecil dari suatu unsur yang tidak dapat dibagi-bagi 2. Atom-atom suatu unsur semuanya serupa dan tidak dapat berubah
1 BAB FISIKA ATOM Perkembangan teori atom Model Atom Dalton 1. Atom adalah bagian terkecil dari suatu unsur yang tidak dapat dibagi-bagi 2. Atom-atom suatu unsur semuanya serupa dan tidak dapat berubah
ATOM DAN SISTEM PERIODIK UNSUR
 ATOM DAN SISTEM PERIODIK UNSUR I. Perkembangan teori atom a. Teori atom Dalton: Materi tersusun atas partikel-partikel terkecil yang disebut atom. Atom merupakan bagian terkecil dari materi yang tidak
ATOM DAN SISTEM PERIODIK UNSUR I. Perkembangan teori atom a. Teori atom Dalton: Materi tersusun atas partikel-partikel terkecil yang disebut atom. Atom merupakan bagian terkecil dari materi yang tidak
Struktur atom merupakan satuan dasar materi yang terdiri dari inti atom beserta awan elektron bermuatan negatif yang mengelilinginya.
 Struktur atom merupakan satuan dasar materi yang terdiri dari inti atom beserta awan elektron bermuatan negatif yang mengelilinginya. Inti atom mengandung campuran proton (bermuatan positif) dan neutron
Struktur atom merupakan satuan dasar materi yang terdiri dari inti atom beserta awan elektron bermuatan negatif yang mengelilinginya. Inti atom mengandung campuran proton (bermuatan positif) dan neutron
Struktur Atom. Setelah mempelajari bab ini, Anda diharapkan mampu mengidentifikasi atom dan strukturnya berdasarkan Tabel Periodik Unsur.
 I Pernahkah Anda membayangkan bahwa keberadaan alam semesta, dunia dan seisinya termasuk juga kita hanya mungkin terjadi dengan adanya keseimbangan yang teramat halus dan teliti? Atom adalah bagian terkecil
I Pernahkah Anda membayangkan bahwa keberadaan alam semesta, dunia dan seisinya termasuk juga kita hanya mungkin terjadi dengan adanya keseimbangan yang teramat halus dan teliti? Atom adalah bagian terkecil
X Z. ISOTOP Atom atom yang sama mempunyai nomor atom sama tetapi nomor massa berbeda disebut isotop Contoh : H 1 H 1 H 1
 MODUL -1 NOTASI UNSUR & JUMLAH PROTON, ELEKTRON & NEUTRON Standar Kompetensi : : 1. Memahami struktur atom, sifat-sifat periodik unsur, dan ikatan kimia Kompetensi Dasar : 1.1.Memahami struktur atom berdasarkan
MODUL -1 NOTASI UNSUR & JUMLAH PROTON, ELEKTRON & NEUTRON Standar Kompetensi : : 1. Memahami struktur atom, sifat-sifat periodik unsur, dan ikatan kimia Kompetensi Dasar : 1.1.Memahami struktur atom berdasarkan
kimia KONFIGURASI ELEKTRON
 K-13 Kelas X kimia KONFIGURASI ELEKTRON Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami konfigurasi elektron kulit dan subkulit. 2. Menyelesaikan
K-13 Kelas X kimia KONFIGURASI ELEKTRON Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami konfigurasi elektron kulit dan subkulit. 2. Menyelesaikan
BAB VIII STRUKTUR ATOM
 BAB VIII STRUKTUR ATOM Pengertian mengenai struktur atom berguna untuk menjelaskan gaya-gaya diantara atom yang akhirnya mengarah pada pembentukan molekul. Dalam bab ini akan dipelajari struktur listrik
BAB VIII STRUKTUR ATOM Pengertian mengenai struktur atom berguna untuk menjelaskan gaya-gaya diantara atom yang akhirnya mengarah pada pembentukan molekul. Dalam bab ini akan dipelajari struktur listrik
Atom menyusun elemen dengan bilangan sederhana. Setiap atom dari elemen yang berbeda memiliki massa yang berbeda.
 Review Model Atom Model Atom Dalton Atom menyusun elemen dengan bilangan sederhana. Setiap atom dari elemen yang berbeda memiliki massa yang berbeda. Model Atom Thomson Secara garis besar atom berupa bola
Review Model Atom Model Atom Dalton Atom menyusun elemen dengan bilangan sederhana. Setiap atom dari elemen yang berbeda memiliki massa yang berbeda. Model Atom Thomson Secara garis besar atom berupa bola
STRUKTUR ATOM. 3. Perhatikan gambar berikut :
 STRUKTUR ATOM. Elektron - elektron dalam atom beredar mengelilingi inti dan berada pada lintasan (tingkat energi) tertentu. Elektron dapat berpindah dari satu tingkat energi ke tingkat energi lainnya di
STRUKTUR ATOM. Elektron - elektron dalam atom beredar mengelilingi inti dan berada pada lintasan (tingkat energi) tertentu. Elektron dapat berpindah dari satu tingkat energi ke tingkat energi lainnya di
B. Macam macam Model Atom a. Model Atom John Dalton. a. Atom merupakan bagian terkecil dari materi yang sudah tidak dapat. Makalah Struktur Atom 1
 BAB I PENDAHULUAN A. Latar Belakang Atom adalah suatu satuan dasar materi, yang terdiri atas beberapa struktur. Istilah atom berasal dari Bahasa Yunani (átomos), yang berarti tidak dapat dipotong ataupun
BAB I PENDAHULUAN A. Latar Belakang Atom adalah suatu satuan dasar materi, yang terdiri atas beberapa struktur. Istilah atom berasal dari Bahasa Yunani (átomos), yang berarti tidak dapat dipotong ataupun
STRUKTUR ATOM DAN PERKEMBANGAN TEORI ATOM 0leh: Ramadani. sinar bermuatan negatif. kecil pembentuk atom tersebut yaitu
 STRUKTUR ATOM DAN PERKEMBANGAN TEORI ATOM 0leh: Ramadani A. PENDAHULUAN Istilah atom pertama kali dikemukakan oleh filsuf Yunani bernama Demokritus dengan istilah atomos yang artinya tidak dapat dibagi.
STRUKTUR ATOM DAN PERKEMBANGAN TEORI ATOM 0leh: Ramadani A. PENDAHULUAN Istilah atom pertama kali dikemukakan oleh filsuf Yunani bernama Demokritus dengan istilah atomos yang artinya tidak dapat dibagi.
TEORI ATOM. Awal Perkembangan Teori Atom
 TEORI ATOM Awal Perkembangan Teori Atom Teori atom pada masa peradaban Yunani Demokritus, Epicurus, Strato, Carus Materi tersusun dari partikel yang sangat kecil yang tidak dapat dibagi lagi Partikel
TEORI ATOM Awal Perkembangan Teori Atom Teori atom pada masa peradaban Yunani Demokritus, Epicurus, Strato, Carus Materi tersusun dari partikel yang sangat kecil yang tidak dapat dibagi lagi Partikel
CREATED BY : KKN-PPL UNY 2012
 STRUKTUR DAN SISTEM PERIODIK UNSUR CREATED BY : KKN-PPL UNY 2012 STRUKTUR DAN SISTEM PERIODIK UNSUR DEMOKRITUS DALTON J.J THOMSON RUTHERFORD Emm.. Anu.. Apakah partikel terkecil dari suatu BOHR unsur?
STRUKTUR DAN SISTEM PERIODIK UNSUR CREATED BY : KKN-PPL UNY 2012 STRUKTUR DAN SISTEM PERIODIK UNSUR DEMOKRITUS DALTON J.J THOMSON RUTHERFORD Emm.. Anu.. Apakah partikel terkecil dari suatu BOHR unsur?
FISIKA. Sesi TEORI ATOM A. TEORI ATOM DALTON B. TEORI ATOM THOMSON
 FISIKA KELAS XII IPA - KURIKULUM GABUNGAN 11 Sesi NGAN TEORI ATOM A. TEORI ATOM DALTON 1. Atom adalah bagian terkecil suatu unsur yang tidak dapat dibagi lagi.. Atom suatu unsur serupa semuanya, dan tak
FISIKA KELAS XII IPA - KURIKULUM GABUNGAN 11 Sesi NGAN TEORI ATOM A. TEORI ATOM DALTON 1. Atom adalah bagian terkecil suatu unsur yang tidak dapat dibagi lagi.. Atom suatu unsur serupa semuanya, dan tak
MATERIAL TEKNIK. 2 SKS Ruang B2.3 Jam Dedi Nurcipto, MT
 MATERIAL TEKNIK 2 SKS Ruang B2.3 Jam 8.40-11.10 Dedi Nurcipto, MT dedinurcipto@dsn.dinus.ac.id Struktur Atom Struktur atom merupakan satuan dasar materi yang terdiri dari inti atom beserta elektron bermuatan
MATERIAL TEKNIK 2 SKS Ruang B2.3 Jam 8.40-11.10 Dedi Nurcipto, MT dedinurcipto@dsn.dinus.ac.id Struktur Atom Struktur atom merupakan satuan dasar materi yang terdiri dari inti atom beserta elektron bermuatan
TEORI ATOM DAN STRUKTUR ATOM
 TEORI ATOM DAN STRUKTUR ATOM KOMPETENSI INTI KOMPETENSI DASAR 1. Menghayati dan mengamalkan ajaran agama yang dianutnya 2. Menghayati dan mengamalkan perilaku jujur, disiplin, tanggungjawab, peduli (gotong
TEORI ATOM DAN STRUKTUR ATOM KOMPETENSI INTI KOMPETENSI DASAR 1. Menghayati dan mengamalkan ajaran agama yang dianutnya 2. Menghayati dan mengamalkan perilaku jujur, disiplin, tanggungjawab, peduli (gotong
INFORMASI KIMIA ENERGI ATOM
 Kimia SMAN 113 Jakarta (www.kimiavegas.wordpress.com) Guru Mata Pelajaran : Gianto, SPd Facebook: multios2009@gmail.com INFORMASI KIMIA ENERGI ATOM Energi atom adalah energi yang bersumber dari atom. Setiap
Kimia SMAN 113 Jakarta (www.kimiavegas.wordpress.com) Guru Mata Pelajaran : Gianto, SPd Facebook: multios2009@gmail.com INFORMASI KIMIA ENERGI ATOM Energi atom adalah energi yang bersumber dari atom. Setiap
RANGKUMAN MATERI. Struktur Atom
 RANGKUMAN MATERI Struktur Atom Atom terdiri dari proton, neutron dan elektron. Proton dan neutron berada di dalam inti atom. Sedangkan elektron terus berputar mengelilingi inti atom karena muatan listriknya.
RANGKUMAN MATERI Struktur Atom Atom terdiri dari proton, neutron dan elektron. Proton dan neutron berada di dalam inti atom. Sedangkan elektron terus berputar mengelilingi inti atom karena muatan listriknya.
TEORI PERKEMBANGAN ATOM
 TEORI PERKEMBANGAN ATOM A. Teori atom Dalton Teori atom dalton ini didasarkan pada 2 hukum, yaitu : hukum kekekalan massa (hukum Lavoisier), massa total zat-zat sebelum reaksi akan selalu sama dengan massa
TEORI PERKEMBANGAN ATOM A. Teori atom Dalton Teori atom dalton ini didasarkan pada 2 hukum, yaitu : hukum kekekalan massa (hukum Lavoisier), massa total zat-zat sebelum reaksi akan selalu sama dengan massa
Bab I Teori Atom Bohr dan Mekanika Kuantum
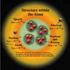 Bab I Teori Atom Bohr dan Mekanika Kuantum Model atom Rutherford Model atom Schrodinger Model atom Bohr Sumber: Encarta Encclopedia, 005 Teori atom berkembang mulai dari teori atom Rutherford, Bohr, sampai
Bab I Teori Atom Bohr dan Mekanika Kuantum Model atom Rutherford Model atom Schrodinger Model atom Bohr Sumber: Encarta Encclopedia, 005 Teori atom berkembang mulai dari teori atom Rutherford, Bohr, sampai
RENCANA PELAKSANAAN PEMBELAJARAN Nama Sekolah : SMA Negeri 1 Sanden Mata Pelajaran : Kimia Kelas/Semester : XI/1 Alokasi Waktu : 2 JP
 RENCANA PELAKSANAAN PEMBELAJARAN Nama Sekolah : SMA Negeri 1 Sanden Mata Pelajaran : Kimia Kelas/Semester : XI/1 Alokasi Waktu : 2 JP Standar Kompetensi 1. Memahami struktur atom untuk meramalkan sifat-sifat
RENCANA PELAKSANAAN PEMBELAJARAN Nama Sekolah : SMA Negeri 1 Sanden Mata Pelajaran : Kimia Kelas/Semester : XI/1 Alokasi Waktu : 2 JP Standar Kompetensi 1. Memahami struktur atom untuk meramalkan sifat-sifat
GENTA GROUP in PLAY STORE. Kode Aktivasi Aplikasi: 74DSM. Kode Aktivasi Aplikasi: P859 FPM KIMIA
 GENTA GROUP in PLAY STORE CBT UN SMA IPA Aplikasi CBT UN SMA IPA android dapat di download di play store dengan kata kunci genta group atau gunakan qr-code di bawah. CBT Psikotes Aplikasi CBT Psikotes
GENTA GROUP in PLAY STORE CBT UN SMA IPA Aplikasi CBT UN SMA IPA android dapat di download di play store dengan kata kunci genta group atau gunakan qr-code di bawah. CBT Psikotes Aplikasi CBT Psikotes
RENCANA PELAKSANAAN PEMBELAJARAN (RPP)
 RENCANA PELAKSANAAN PEMBELAJARAN (RPP) Sekolah Mata Pelajaran Kelas/ Semester Materi Pokok Alokasi Waktu : SMAN 1 SANDEN : Kimia : X / Ganjil : Struktur Atom : 3 x 45 menit A. Kompetensi Inti KI 1 : Menghayati
RENCANA PELAKSANAAN PEMBELAJARAN (RPP) Sekolah Mata Pelajaran Kelas/ Semester Materi Pokok Alokasi Waktu : SMAN 1 SANDEN : Kimia : X / Ganjil : Struktur Atom : 3 x 45 menit A. Kompetensi Inti KI 1 : Menghayati
YAYASAN PEMBINA UNIVERSITAS NEGERI JAKARTA SMA LABSCHOOL KEBAYORAN
 YAYASAN PEMBINA UNIVERSITAS NEGERI JAKARTA SMA LABSCHOOL KEBAYORAN ULANGAN HARIAN TERPROGRAM Mata Pelajaran : Kimia Kelas/Program : X / Reguler Hari, Tanggal : Selasa, 9 September 05 Waktu : 07.30 09.00
YAYASAN PEMBINA UNIVERSITAS NEGERI JAKARTA SMA LABSCHOOL KEBAYORAN ULANGAN HARIAN TERPROGRAM Mata Pelajaran : Kimia Kelas/Program : X / Reguler Hari, Tanggal : Selasa, 9 September 05 Waktu : 07.30 09.00
Struktur Atom. Sulistyani, M.Si.
 Struktur Atom Sulistyani, M.Si. sulistyani@uny.ac.id DEFINISI ATOM Salah satu konsep ilmiah tertua adalah bahwa semua materi dapat dipecah menjadi zarah (partikel) terkecil, dimana partikel-partikel itu
Struktur Atom Sulistyani, M.Si. sulistyani@uny.ac.id DEFINISI ATOM Salah satu konsep ilmiah tertua adalah bahwa semua materi dapat dipecah menjadi zarah (partikel) terkecil, dimana partikel-partikel itu
Struktur atom. Kunci : A Pembahasan Partikel dasar penyusun atom adalah proton, elektron dan neutron
 Struktur atom 1. Partikel-partikel berikut yang termasuk partikel dasar atom adalah... (A) Proton, elektron, neutron (D) Proton, elektron, neutron, nukleon, (B) Nukleon, muon, positron (E) Proton, neutron,
Struktur atom 1. Partikel-partikel berikut yang termasuk partikel dasar atom adalah... (A) Proton, elektron, neutron (D) Proton, elektron, neutron, nukleon, (B) Nukleon, muon, positron (E) Proton, neutron,
LEMBARAN SOAL 8. Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH )
 LEMBARAN SOAL 8 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah soal dengan
LEMBARAN SOAL 8 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah soal dengan
SMP kelas 8 - KIMIA BAB 1. ATOM, ION DAN MOLEKULLatihan soal 1.1. Dalton. Thomson. Rutherford. Bohr
 SMP kelas 8 - KIMIA BAB 1. ATOM, ION DAN MOLEKULLatihan soal 1.1 1. Atom merupakan bola pejal bermuatan positif dengan elektron - elektron yang tersebar merata merupakan teori atom... Thomson Bohr Atom
SMP kelas 8 - KIMIA BAB 1. ATOM, ION DAN MOLEKULLatihan soal 1.1 1. Atom merupakan bola pejal bermuatan positif dengan elektron - elektron yang tersebar merata merupakan teori atom... Thomson Bohr Atom
Pilihan ganda Soal Sistem Periodik Unsur dan Struktur atom. A. Berilah tanda silang (X) pada huruf A, B, C, D, atau E di depan jawaban yang tepat!
 Pilihan ganda Soal Sistem Periodik Unsur dan Struktur atom. A. Berilah tanda silang (X) pada huruf A, B, C, D, atau E di depan jawaban yang tepat! 1. Unsur dengan nomor atom 32 terletak pada. A. periode
Pilihan ganda Soal Sistem Periodik Unsur dan Struktur atom. A. Berilah tanda silang (X) pada huruf A, B, C, D, atau E di depan jawaban yang tepat! 1. Unsur dengan nomor atom 32 terletak pada. A. periode
PERKEMBANGAN TEORI ATOM
 DEMOKRITUS PERKEMBANGAN TEORI ATOM DALTON THOMSON RUTHERFORD BOHR MEKANIKA KUANTUM + + GAMBAR GAMBAR GAMBAR GAMBAR GAMBAR CATATAN : CATATAN : CATATAN : CATATAN : CATATAN : 1 PENEMUAN DERET BALMER Peralatan
DEMOKRITUS PERKEMBANGAN TEORI ATOM DALTON THOMSON RUTHERFORD BOHR MEKANIKA KUANTUM + + GAMBAR GAMBAR GAMBAR GAMBAR GAMBAR CATATAN : CATATAN : CATATAN : CATATAN : CATATAN : 1 PENEMUAN DERET BALMER Peralatan
Teori Atom Mekanika Klasik
 Teori Atom Mekanika Klasik -Thomson -Rutherford -Bohr -Bohr-Rutherford -Bohr-Sommerfeld Kelemahan Teori Atom Bohr: -Bohr hanya dapat menjelaskan spektrum gas hidrogen, tidak dapat menjelaskan spektrum
Teori Atom Mekanika Klasik -Thomson -Rutherford -Bohr -Bohr-Rutherford -Bohr-Sommerfeld Kelemahan Teori Atom Bohr: -Bohr hanya dapat menjelaskan spektrum gas hidrogen, tidak dapat menjelaskan spektrum
BANK SOAL SELEKSI MASUK PERGURUAN TINGGI BIDANG KIMIA 1 BAB I STRUKTUR ATOM
 BANK SOAL SELEKSI MASUK PERGURUAN TINGGI BIDANG KIMIA 1 BAB I 1. Suatu partikel X memiliki 16 proton, 16 neutron, dan 18 elektron. Partikel tersebut dapat dikategorikan sebagai A. Anion X bermuatan -1
BANK SOAL SELEKSI MASUK PERGURUAN TINGGI BIDANG KIMIA 1 BAB I 1. Suatu partikel X memiliki 16 proton, 16 neutron, dan 18 elektron. Partikel tersebut dapat dikategorikan sebagai A. Anion X bermuatan -1
LEMBARAN SOAL 1. Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH ) SOAL
 LEMBARAN SOAL 1 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH ) PETUNJUK UMUM 1. Tulis nomor nama Anda pada lembar jawaban yang disediakan 2. Periksa bacalah soal dengan teliti
LEMBARAN SOAL 1 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH ) PETUNJUK UMUM 1. Tulis nomor nama Anda pada lembar jawaban yang disediakan 2. Periksa bacalah soal dengan teliti
Aristoteles. Leukipos dan Demokritos. John Dalton. Perkembangan Model Atom. J.J. Thomson. Rutherford. Niels Bohr. Mekanika Kuatum
 What is an Atom? Aristoteles Leukipos dan Demokritos Perkembangan Model Atom John Dalton J.J. Thomson Rutherford Niels Bohr Mekanika Kuatum 1. Pendapat Aristoteles Materi bersifat kontinue, artinya materi
What is an Atom? Aristoteles Leukipos dan Demokritos Perkembangan Model Atom John Dalton J.J. Thomson Rutherford Niels Bohr Mekanika Kuatum 1. Pendapat Aristoteles Materi bersifat kontinue, artinya materi
LAPORAN TUGAS MIKROELEKTONIKA
 LAPORAN TUGAS MIKROELEKTONIKA Struktur Internal Atom Disusun oleh : Nama : Bayu Saputra NIM : 13081245 Kelas : 13.4A.11 Dosen : Juniar Synaga BINA SARANA INFORMATIKA 2010 BAB 1 PENDAHULUAN A.Maksud dan
LAPORAN TUGAS MIKROELEKTONIKA Struktur Internal Atom Disusun oleh : Nama : Bayu Saputra NIM : 13081245 Kelas : 13.4A.11 Dosen : Juniar Synaga BINA SARANA INFORMATIKA 2010 BAB 1 PENDAHULUAN A.Maksud dan
ANALISIS SOAL UJIAN HARIAN KELAS XI BAB: TEORI ATOM MEKANIKA KUANTUM, BENTUK MOLEKUL, DAN GAYA ANTARMOLEKUL
 ANALISIS SOAL UJIAN HARIAN KELAS XI BAB: TEORI ATOM MEKANIKA KUANTUM, BENTUK MOLEKUL, DAN Petunjuk Umum : GAYA ANTARMOLEKUL Telitilah soal terlebih dahulu, perangkat soal terdiri dari 20 soal pilihan ganda
ANALISIS SOAL UJIAN HARIAN KELAS XI BAB: TEORI ATOM MEKANIKA KUANTUM, BENTUK MOLEKUL, DAN Petunjuk Umum : GAYA ANTARMOLEKUL Telitilah soal terlebih dahulu, perangkat soal terdiri dari 20 soal pilihan ganda
Pentalogy FISIKA SMA
 GENTA GROUP in PLAY STORE CBT UN SMA IPA Buku ini dilengkapi aplikasi CBT UN SMA IPA android yang dapat di-download di play store dengan kata kunci genta group atau gunakan qr-code di bawah. Kode Aktivasi
GENTA GROUP in PLAY STORE CBT UN SMA IPA Buku ini dilengkapi aplikasi CBT UN SMA IPA android yang dapat di-download di play store dengan kata kunci genta group atau gunakan qr-code di bawah. Kode Aktivasi
UJIAN AKHIR SEMESTER 1 SEKOLAH MENENGAH TAHUN AJARAN 2014/2015 Mata Pelajaran : Kimia
 Nama : UJIAN AKHIR SEMESTER 1 SEKOLAH MENENGAH TAHUN AJARAN 2014/2015 Mata Pelajaran : Kimia Kelas : 8 Waktu : 09.30-11.00 No.Induk : Hari/Tanggal : Jumat, 05 Desember 2014 Petunjuk Umum: Nilai : 1. Isikan
Nama : UJIAN AKHIR SEMESTER 1 SEKOLAH MENENGAH TAHUN AJARAN 2014/2015 Mata Pelajaran : Kimia Kelas : 8 Waktu : 09.30-11.00 No.Induk : Hari/Tanggal : Jumat, 05 Desember 2014 Petunjuk Umum: Nilai : 1. Isikan
I. Perkembangan Teori Atom
 I. Perkembangan Teori Atom Perkembangan pemahaman struktur atom sejalan dengan awal perkembangan ilmu Fisika modern. Ilmuwan pertama yang membangun model (struktur) atom adalah John Dalton, kemudian disempurnakan
I. Perkembangan Teori Atom Perkembangan pemahaman struktur atom sejalan dengan awal perkembangan ilmu Fisika modern. Ilmuwan pertama yang membangun model (struktur) atom adalah John Dalton, kemudian disempurnakan
MODUL -1. STRUKTUR ATOM dan SISTEM PERIODIK UNSUR- UNSUR
 MODUL -1 STRUKTUR ATOM dan SISTEM PERIODIK UNSUR- UNSUR Standar Kompetensi ( SK ) : Memahami struktur untuk meramalkan sifat-sifat periodik unsur,struktur molekul, dan sifat-sifat senyawa Kompetensi Dasar
MODUL -1 STRUKTUR ATOM dan SISTEM PERIODIK UNSUR- UNSUR Standar Kompetensi ( SK ) : Memahami struktur untuk meramalkan sifat-sifat periodik unsur,struktur molekul, dan sifat-sifat senyawa Kompetensi Dasar
ULANGAN SUSULAN TENGAH SEMESTER 1 TAHUN AJARAN 2009/2010 SMA KRISTEN PETRA 1 SURABAYA
 ULANGAN SUSULAN TENGAH SEMESTER 1 TAHUN AJARAN 2009/2010 SMA KRISTEN PETRA 1 SURABAYA Mata Pelajaran : KIMIA Hari / Tgl : Kelas / Semester : X / Ganjil Waktu : 60 Menit Guru Pengajar : Rachel F, S.T &
ULANGAN SUSULAN TENGAH SEMESTER 1 TAHUN AJARAN 2009/2010 SMA KRISTEN PETRA 1 SURABAYA Mata Pelajaran : KIMIA Hari / Tgl : Kelas / Semester : X / Ganjil Waktu : 60 Menit Guru Pengajar : Rachel F, S.T &
PENDAHULUAN. Atom berasal dari bahasa Yunani atomos yang artinya tidak dapat dibagi-bagi lagi.
 PENDAHULUAN Atom berasal dari bahasa Yunani atomos yang artinya tidak dapat dibagi-bagi lagi. Demokritus (460-370-S.M) Bagian terkecil yang tidak dapat dibagi lagi disebut: ATOM Konsep atom yang dikemukakan
PENDAHULUAN Atom berasal dari bahasa Yunani atomos yang artinya tidak dapat dibagi-bagi lagi. Demokritus (460-370-S.M) Bagian terkecil yang tidak dapat dibagi lagi disebut: ATOM Konsep atom yang dikemukakan
Struktur Atom dan Sistem Periodik Unsur. Kelompok 1 Atifa Rahmi ( ) Lelly Shelviyani ( ) Nur Ayu Fitriani ( ) Suhartini ( )
 Struktur Atom dan Sistem Periodik Unsur Kelompok 1 Atifa Rahmi (1102867) Lelly Shelviyani (1105121) Nur Ayu Fitriani (1101979) Suhartini (1106554) Mari Kita Pretest Jawablah pernyataan di bawah ini dengan
Struktur Atom dan Sistem Periodik Unsur Kelompok 1 Atifa Rahmi (1102867) Lelly Shelviyani (1105121) Nur Ayu Fitriani (1101979) Suhartini (1106554) Mari Kita Pretest Jawablah pernyataan di bawah ini dengan
KIMIA (2-1)
 03035307 KIMIA (2-1) Dr.oec.troph.Ir.Krishna Purnawan Candra, M.S. Kuliah ke-2 Perkembangan teori atom, teori atom Dalton dan Rutherford, teori atom modern Faperta UNMUL 2011 Perkembangan teori atom Perkembangan
03035307 KIMIA (2-1) Dr.oec.troph.Ir.Krishna Purnawan Candra, M.S. Kuliah ke-2 Perkembangan teori atom, teori atom Dalton dan Rutherford, teori atom modern Faperta UNMUL 2011 Perkembangan teori atom Perkembangan
4. Atom atau kumpulan atom yang bermuatan listrik disebut. a. zat tunggal d. ion b. molekul e. gugus fungsi c. senyawa
 1. Dari rumus kimia dibawah ini 1. NH 3 3. SO 2 2. Br 2 4. O 2 Yang menyatakan rumus molekul semyawa adalah a. 1,2, dan 3 d. 4 saja b. 1 dan 3 e. 1,2,3, dan 4 2 dan 4 2. Kadar zat besi yang diperbolehkan
1. Dari rumus kimia dibawah ini 1. NH 3 3. SO 2 2. Br 2 4. O 2 Yang menyatakan rumus molekul semyawa adalah a. 1,2, dan 3 d. 4 saja b. 1 dan 3 e. 1,2,3, dan 4 2 dan 4 2. Kadar zat besi yang diperbolehkan
DAFTAR PUSTAKA. 1. Dra. Sukmriah M & Dra. Kamianti A, Kimia Kedokteran, edisi 2, Penerbit Binarupa Aksara, 1990
 DAFTAR PUSTAKA 1. Dra. Sukmriah M & Dra. Kamianti A, Kimia Kedokteran, edisi 2, Penerbit Binarupa Aksara, 1990 2. Drs. Hiskia Achmad, Kimia Unsur dan Radiokimia, Penerbit PT. Citra Aditya Bakti, 2001 3.
DAFTAR PUSTAKA 1. Dra. Sukmriah M & Dra. Kamianti A, Kimia Kedokteran, edisi 2, Penerbit Binarupa Aksara, 1990 2. Drs. Hiskia Achmad, Kimia Unsur dan Radiokimia, Penerbit PT. Citra Aditya Bakti, 2001 3.
Isi Teori Niels Bohr. Kelebihan Niels Bohr. Kekurangan
 dan Model Atom Kelompok 3 : Wahyu Trifandi Octa Cyntya Dewi Syarifah Aini Yayu Purnamasari Dini Andriani Shella Satiwi Guci Dian Apriliya KELUAR dan Model Atom Di dalam fisika atom, model adalah model
dan Model Atom Kelompok 3 : Wahyu Trifandi Octa Cyntya Dewi Syarifah Aini Yayu Purnamasari Dini Andriani Shella Satiwi Guci Dian Apriliya KELUAR dan Model Atom Di dalam fisika atom, model adalah model
Struktur Atom dan Sistem Periodik
 Struktur Atom dan Sistem Periodik Struktur Atom Elektron Inti Atom Gelombang Radiasi Elektromagnet Model Bohr untuk atom Hidrogen Teori Gelombang Elektron Prinsip Ketidakpastian Heisenberg Model Quantum
Struktur Atom dan Sistem Periodik Struktur Atom Elektron Inti Atom Gelombang Radiasi Elektromagnet Model Bohr untuk atom Hidrogen Teori Gelombang Elektron Prinsip Ketidakpastian Heisenberg Model Quantum
LK S I.A. M. Partikel Materi Ion. Atom.Molekul SMP. ƙ ǐ. 8 B MTs. ĺƿȃ NAMA : KELAS : NO. ABSEN : SEKOLAH : Lembar Kegiatan Siswa SMP / MTs Kelas 8 B
 LK S I.A. M SMP 8 B MTs ĺƿȃ ɱ ǐ ƙ ǐ ά Partikel Materi Ion. Atom.Molekul NAMA : KELAS : NO. ABSEN : SEKOLAH : LK [ S I.A. M Partikel Materi Ion. Atom.Molekul PE NY AAM MAESAROH (1004571) MEGA WIJAYANTI
LK S I.A. M SMP 8 B MTs ĺƿȃ ɱ ǐ ƙ ǐ ά Partikel Materi Ion. Atom.Molekul NAMA : KELAS : NO. ABSEN : SEKOLAH : LK [ S I.A. M Partikel Materi Ion. Atom.Molekul PE NY AAM MAESAROH (1004571) MEGA WIJAYANTI
IR. STEVANUS ARIANTO 1
 8/7/017 PNDAHULUAN TORI ATOM DALTON KLMAHAN TORI ATOM DALTON SINAR KATODA SIFAT SINAR KATODA TORI ATOM JJ.THOMSON HAMBURAN SINAR ALFA TORI ATOM RUTHRFORD KLMAHAN TORI ATOM RUTHRFORD SPKTRUM UAP HIDROGN
8/7/017 PNDAHULUAN TORI ATOM DALTON KLMAHAN TORI ATOM DALTON SINAR KATODA SIFAT SINAR KATODA TORI ATOM JJ.THOMSON HAMBURAN SINAR ALFA TORI ATOM RUTHRFORD KLMAHAN TORI ATOM RUTHRFORD SPKTRUM UAP HIDROGN
PENGANTAR KIMIA INDUSTRI _KIMIA INDUSTRI_ DEWI HARDININGTYAS, ST, MT, MBA WIDHA KUSUMA NINGDYAH, ST, MT AGUSTINA EUNIKE, ST, MT, MBA
 PENGANTAR KIMIA INDUSTRI _KIMIA INDUSTRI_ DEWI HARDININGTYAS, ST, MT, MBA WIDHA KUSUMA NINGDYAH, ST, MT AGUSTINA EUNIKE, ST, MT, MBA 1. Pengukuran Ilmiah 2. Teori Atom 3. Tabel Periodik 4. Molekul dan
PENGANTAR KIMIA INDUSTRI _KIMIA INDUSTRI_ DEWI HARDININGTYAS, ST, MT, MBA WIDHA KUSUMA NINGDYAH, ST, MT AGUSTINA EUNIKE, ST, MT, MBA 1. Pengukuran Ilmiah 2. Teori Atom 3. Tabel Periodik 4. Molekul dan
PENDAHULUAN PENGENALAN ILMU KIMIA
 PENDAHULUAN PENGENALAN ILMU KIMIA A. Pengertian Ilmu Kimia Bangsa Yunani menyebut kimia sebagai chemie yaitu segala macam aktivitas seni pengerjaan logam. Pada saat itu, setiap orang yang beraktivitas
PENDAHULUAN PENGENALAN ILMU KIMIA A. Pengertian Ilmu Kimia Bangsa Yunani menyebut kimia sebagai chemie yaitu segala macam aktivitas seni pengerjaan logam. Pada saat itu, setiap orang yang beraktivitas
Partikel Materi. Bab. Peta Konsep. Gambar 8.1 Molekul senyawa. Atom. bermuatan listrik. jenisnya Ion. bergabung menjadi. Molekul
 Bab 8 Partikel Materi Sumber: Encarta 2005 Gambar 8.1 Molekul senyawa Perhatikan gambar molekul senyawa (lihat Gambar 8.1). Molekul senyawa tersebut disusun oleh atom-atom dari unsur yang berbeda. Molekul
Bab 8 Partikel Materi Sumber: Encarta 2005 Gambar 8.1 Molekul senyawa Perhatikan gambar molekul senyawa (lihat Gambar 8.1). Molekul senyawa tersebut disusun oleh atom-atom dari unsur yang berbeda. Molekul
RENCANA PELAKSANAAN PEMBELAJARAN Nama Sekolah : SMA Negeri 1 Sanden Mata Pelajaran : Kimia Kelas/Semester : XI/1 Alokasi Waktu : 3 JP
 RENCANA PELAKSANAAN PEMBELAJARAN Nama Sekolah : SMA Negeri 1 Sanden Mata Pelajaran : Kimia Kelas/Semester : XI/1 Alokasi Waktu : 3 JP Standar Kompetensi 1. Memahami struktur atom untuk meramalkan sifat-sifat
RENCANA PELAKSANAAN PEMBELAJARAN Nama Sekolah : SMA Negeri 1 Sanden Mata Pelajaran : Kimia Kelas/Semester : XI/1 Alokasi Waktu : 3 JP Standar Kompetensi 1. Memahami struktur atom untuk meramalkan sifat-sifat
UJI KOMPETENSI A. PILIHAN GANDA
 UJI KOMPETENSI A. PILIHAN GANDA 1. percobaan yang mendasari teori atom Bohr adalah a. percobaan tabung pembawa muatan b. percobaan penghamburan sinar c. percobaan tetesan minyak d. percobaan sepectrum
UJI KOMPETENSI A. PILIHAN GANDA 1. percobaan yang mendasari teori atom Bohr adalah a. percobaan tabung pembawa muatan b. percobaan penghamburan sinar c. percobaan tetesan minyak d. percobaan sepectrum
KEGIATAN BELAJAR 2 KONFIGURASI ELEKTRON, HUBUNGANNYA DENGAN LETAK UNSUR DALAM SISTEM PERIODIK, DAN SIFAT PERIODIK UNSUR
 KEGIATAN BELAJAR 2 KONFIGURASI ELEKTRON, HUBUNGANNYA DENGAN LETAK UNSUR DALAM SISTEM PERIODIK, DAN SIFAT PERIODIK UNSUR A. CAPAIAN PEMBELAJARAN 1. Menentukan letak suatu unsur dalam SPU berdasarkan konfigurasi
KEGIATAN BELAJAR 2 KONFIGURASI ELEKTRON, HUBUNGANNYA DENGAN LETAK UNSUR DALAM SISTEM PERIODIK, DAN SIFAT PERIODIK UNSUR A. CAPAIAN PEMBELAJARAN 1. Menentukan letak suatu unsur dalam SPU berdasarkan konfigurasi
Inti Atom dan Penyusunnya. Sulistyani, M.Si.
 Inti Atom dan Penyusunnya Sulistyani, M.Si. Email: sulistyani@uny.ac.id Eksperimen Marsden dan Geiger Pendahuluan Teori tentang atom pertama kali dikemukakan oleh Dalton bahwa atom bagian terkecil dari
Inti Atom dan Penyusunnya Sulistyani, M.Si. Email: sulistyani@uny.ac.id Eksperimen Marsden dan Geiger Pendahuluan Teori tentang atom pertama kali dikemukakan oleh Dalton bahwa atom bagian terkecil dari
(I) MATERI. Pengertian materi sifat materi, Perubahan materi, Klasifikasi materi, serta hukum-hukum yang berhubungan dengan materi.
 (I) MATERI Pengertian materi sifat materi, Perubahan materi, Klasifikasi materi, serta hukum-hukum yang berhubungan dengan materi. Ilmu kimia Merupakan bagian dari ilmu pengetahuan alam yang mempelajari
(I) MATERI Pengertian materi sifat materi, Perubahan materi, Klasifikasi materi, serta hukum-hukum yang berhubungan dengan materi. Ilmu kimia Merupakan bagian dari ilmu pengetahuan alam yang mempelajari
RENCANA PELAKSANAAN PEMBELAJARAN ( RPP) : SMP NEGERI 1 KOTA MUNGKID. Mata Pelajaran
 RENCANA PELAKSANAAN PEMBELAJARAN ( RPP) Sekolah Mata Pelajaran Kelas/Semester Bahan Kajian Alokasi Waktu : SMP NEGERI 1 KOTA MUNGKID : IPA : VIII (Delapan) / Gasal : Atom, Ion Dan Molekul : 5 x 40 menit
RENCANA PELAKSANAAN PEMBELAJARAN ( RPP) Sekolah Mata Pelajaran Kelas/Semester Bahan Kajian Alokasi Waktu : SMP NEGERI 1 KOTA MUNGKID : IPA : VIII (Delapan) / Gasal : Atom, Ion Dan Molekul : 5 x 40 menit
LEMBARAN SOAL 7. Sat. Pendidikan. Pilihlah Satu Jawaban yang Palin Tepat 1. Perhatikan bagan percobaan penghamburan sinar alfa berikut:
 Mata Pelajaran Sat. Pendidikan Kelas / Program LEMBARAN SOAL 7 : Kimia : SMA : X / INTI PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah soal dengan
Mata Pelajaran Sat. Pendidikan Kelas / Program LEMBARAN SOAL 7 : Kimia : SMA : X / INTI PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah soal dengan
Pendahuluan Fisika Inti. Oleh: Lailatul Nuraini, S.Pd, M.Pd
 Pendahuluan Fisika Inti Oleh: Lailatul Nuraini, S.Pd, M.Pd Biodata Email: lailatul.fkip@unej.ac.id No hp: 085 236 853 668 Terdapat 6 bab. Produk matakuliah berupa bahan ajar. Tugas mandiri 20%, tugas terstruktur
Pendahuluan Fisika Inti Oleh: Lailatul Nuraini, S.Pd, M.Pd Biodata Email: lailatul.fkip@unej.ac.id No hp: 085 236 853 668 Terdapat 6 bab. Produk matakuliah berupa bahan ajar. Tugas mandiri 20%, tugas terstruktur
Xpedia Fisika. Soal Fismod 1
 Xpedia Fisika Soal Fismod 1 Doc. Name: XPPHY0501 Version: 2013-04 halaman 1 01. Pertanyaan 01-02 : Sebuah botol tertutup berisi 100 gram iodin radioaktif. Setelah 24 hari, botol itu berisi 12,5 gram iodin
Xpedia Fisika Soal Fismod 1 Doc. Name: XPPHY0501 Version: 2013-04 halaman 1 01. Pertanyaan 01-02 : Sebuah botol tertutup berisi 100 gram iodin radioaktif. Setelah 24 hari, botol itu berisi 12,5 gram iodin
kimia REVIEW I TUJUAN PEMBELAJARAN
 KTSP kimia K e l a s XI REVIEW I TUJUAN PEMBELAJARAN Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami teori atom mekanika kuantum dan hubungannya dengan bilangan
KTSP kimia K e l a s XI REVIEW I TUJUAN PEMBELAJARAN Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami teori atom mekanika kuantum dan hubungannya dengan bilangan
Pusat Pendidikan dan Pelatihan Badan Tenaga Nuklir Nasional
 Pusat Pendidikan dan Pelatihan Badan Tenaga Nuklir Nasional 1 Pokok Bahasan STRUKTUR ATOM DAN INTI ATOM A. Struktur Atom B. Inti Atom PELURUHAN RADIOAKTIF A. Jenis Peluruhan B. Aktivitas Radiasi C. Waktu
Pusat Pendidikan dan Pelatihan Badan Tenaga Nuklir Nasional 1 Pokok Bahasan STRUKTUR ATOM DAN INTI ATOM A. Struktur Atom B. Inti Atom PELURUHAN RADIOAKTIF A. Jenis Peluruhan B. Aktivitas Radiasi C. Waktu
Schrodinger s Wave Function
 SPEKTRA RADIASI ELEKTROMAGNET SPEKTRUM KONTINYU TEORI MAX PLANK TEORI ATOM BOHR SIFAT GELOMBANG Schrodinger s Wave Function MODEL ATOM MEKANIKA KUANTUM Persamaan gelombang Schrodinger TEORI MEKANIKA KUANTUM
SPEKTRA RADIASI ELEKTROMAGNET SPEKTRUM KONTINYU TEORI MAX PLANK TEORI ATOM BOHR SIFAT GELOMBANG Schrodinger s Wave Function MODEL ATOM MEKANIKA KUANTUM Persamaan gelombang Schrodinger TEORI MEKANIKA KUANTUM
FISIKA ATOM & RADIASI
 FISIKA ATOM & RADIASI Atom bagian terkecil dari suatu elemen yang berperan dalam reaksi kimia, bersifat netral (muatan positif dan negatif sama). Model atom: J.J. Thomson (1910), Ernest Rutherford (1911),
FISIKA ATOM & RADIASI Atom bagian terkecil dari suatu elemen yang berperan dalam reaksi kimia, bersifat netral (muatan positif dan negatif sama). Model atom: J.J. Thomson (1910), Ernest Rutherford (1911),
Intan Pariwara. Depdiknas. halaman Kelas X. 2. Buku PR Kimia. 3. BSE Kimia X, positif dengan elektron. bergerak mengelilinginya.
 Pendidikan karakter (*) Gemar Membaca Ekonomi kreatif ( ) Pantang Menyerah Kimia Kelas X 1 Silabus Sekolah : Kelas/Semester : X/1 : Kimia Standar Kompetensi : 1 Memahami struktur atom, sifat-sifat periodik
Pendidikan karakter (*) Gemar Membaca Ekonomi kreatif ( ) Pantang Menyerah Kimia Kelas X 1 Silabus Sekolah : Kelas/Semester : X/1 : Kimia Standar Kompetensi : 1 Memahami struktur atom, sifat-sifat periodik
ELEKTRONIKA DASAR. Program Studi S1 Informatika Sekolah Tinggi Teknologi Telematika Telkom 2016
 ELEKTONIKA DASA Program Studi S1 Informatika Sekolah Tinggi Teknologi Telematika Telkom 2016 1 Luruskan Niat Pokok Bahasan Teori Atom (15 ) Hukum Kirchoff Tegangan (15 ) Hukum Kirchoff Arus (15 ) esistansi
ELEKTONIKA DASA Program Studi S1 Informatika Sekolah Tinggi Teknologi Telematika Telkom 2016 1 Luruskan Niat Pokok Bahasan Teori Atom (15 ) Hukum Kirchoff Tegangan (15 ) Hukum Kirchoff Arus (15 ) esistansi
Bilangan Kuantum Utama (n)
 Bilangan Kuantum Utama (n) Menyatakan nomer kulit tempat elektron berada atau bilangan ini juga menyatakan ukuran orbital/ jarak/ jari-jari atom. Dinyatakan dengan bilangan bulat positif. Mempunyai dua
Bilangan Kuantum Utama (n) Menyatakan nomer kulit tempat elektron berada atau bilangan ini juga menyatakan ukuran orbital/ jarak/ jari-jari atom. Dinyatakan dengan bilangan bulat positif. Mempunyai dua
BAB 19 A T O M. A. Pendahuluan
 BAB 19 A T O M A. Pendahuluan Pemikiran ke arah penemuan atom dan inti atom telah berkembang di setiap peradaban sejak manusia mengenal tulisan atau yang lebih dikenal sebagai zaman permulaan sejarah.
BAB 19 A T O M A. Pendahuluan Pemikiran ke arah penemuan atom dan inti atom telah berkembang di setiap peradaban sejak manusia mengenal tulisan atau yang lebih dikenal sebagai zaman permulaan sejarah.
CATATAN KULIAH ATOM, INTI DAN RADIOAKTIF. Diah Ayu Suci Kinasih Departemen Fisika Universitas Diponegoro Semarang 2016
 CATATAN KULIAH ATOM, INTI DAN RADIOAKTIF Diah Ayu Suci Kinasih -24040115130099- Departemen Fisika Universitas Diponegoro Semarang 2016 FISIKA NUKLIR Atom, Inti dan Radioaktif 1. Pekembangan Teori Atom
CATATAN KULIAH ATOM, INTI DAN RADIOAKTIF Diah Ayu Suci Kinasih -24040115130099- Departemen Fisika Universitas Diponegoro Semarang 2016 FISIKA NUKLIR Atom, Inti dan Radioaktif 1. Pekembangan Teori Atom
TEORI ATOM Materi 1 : Baca teori ini, kerjakan soal yang ada di halaman paling belakang ini
 TEORI ATOM Materi 1 : Baca teori ini, kerjakan soal yang ada di alaman paling belakang ini 1. Model atom Dalton a. Atom adala bagian terkecil suatu unsur yang tidak dapat dibagi-bagi lagi b. Atom suatu
TEORI ATOM Materi 1 : Baca teori ini, kerjakan soal yang ada di alaman paling belakang ini 1. Model atom Dalton a. Atom adala bagian terkecil suatu unsur yang tidak dapat dibagi-bagi lagi b. Atom suatu
MODEL ATOM DALTON. Atom ialah bagian terkecil suatu zat yang tidak dapat dibagi-bagi. Atom tidak dapat dimusnahkan & diciptakan
 MODEL ATOM MODEL ATOM DALTON Atom ialah bagian terkecil suatu zat yang tidak dapat dibagi-bagi. Atom tidak dapat dimusnahkan & diciptakan MODEL ATOM DALTON Konsep Model Atom Dalton : 1. Setiap benda (zat)
MODEL ATOM MODEL ATOM DALTON Atom ialah bagian terkecil suatu zat yang tidak dapat dibagi-bagi. Atom tidak dapat dimusnahkan & diciptakan MODEL ATOM DALTON Konsep Model Atom Dalton : 1. Setiap benda (zat)
SILABUS PEMBELAJARAN
 SILABUS PEMBELAJARAN Sekolah : SMA... Kelas / Semester : XII / II Mata Pelajaran : FISIKA Standar : 3. Menganalisis berbagai besaran fisis pada gejala kuantum dan batas-batas berlakunya relativitas Einstein
SILABUS PEMBELAJARAN Sekolah : SMA... Kelas / Semester : XII / II Mata Pelajaran : FISIKA Standar : 3. Menganalisis berbagai besaran fisis pada gejala kuantum dan batas-batas berlakunya relativitas Einstein
Atom netral. Ion bermuatan listrik positif : melepas elektron negatif ; menerima elektron Atom Inti atom o proton o neutron Elektron Contoh:
 Atom netral Ion bermuatan listrik positif : melepas elektron negatif ; menerima elektron Atom Inti atom o proton o neutron Elektron Contoh: 11 23 Na p = 11 e = 11 n = 12 Percobaan Lempeng emas Oleh Rutherford
Atom netral Ion bermuatan listrik positif : melepas elektron negatif ; menerima elektron Atom Inti atom o proton o neutron Elektron Contoh: 11 23 Na p = 11 e = 11 n = 12 Percobaan Lempeng emas Oleh Rutherford
Bahan Kuliah Minggu I ELEKTRONIKA DASAR. Program Studi S1 Informatika Sekolah Tinggi Teknologi Telematika Telkom 2015
 Bahan Kuliah Minggu I ELEKTONIKA DASA Program Studi S1 Informatika Sekolah Tinggi Teknologi Telematika Telkom 2015 1 Pokok Bahasan Teori Atom (15 ) Hukum Kirchoff Tegangan (15 ) Hukum Kirchoff Arus (15
Bahan Kuliah Minggu I ELEKTONIKA DASA Program Studi S1 Informatika Sekolah Tinggi Teknologi Telematika Telkom 2015 1 Pokok Bahasan Teori Atom (15 ) Hukum Kirchoff Tegangan (15 ) Hukum Kirchoff Arus (15
PENDAHULUAN RADIOAKTIVITAS TUJUAN
 PENDAHULUAN RADIOAKTIVITAS TUJUAN Maksud dan tujuan kuliah ini adalah memberikan dasar-dasar dari fenomena radiaktivitas serta sumber radioaktif Diharapkan agar dengan pengetahuan dasar ini kita akan mempunyai
PENDAHULUAN RADIOAKTIVITAS TUJUAN Maksud dan tujuan kuliah ini adalah memberikan dasar-dasar dari fenomena radiaktivitas serta sumber radioaktif Diharapkan agar dengan pengetahuan dasar ini kita akan mempunyai
Fisika Umum (MA 301) Topik hari ini. Fisika Atom & Inti
 Fisika Umum (MA 301) Topik hari ini Fisika Atom & Inti 8/14/2007 Fisika Atom Model Awal Atom Model atom J.J. Thomson Bola bermuatan positif Muatan-muatan negatif (elektron)) yang sama banyak-nya menempel
Fisika Umum (MA 301) Topik hari ini Fisika Atom & Inti 8/14/2007 Fisika Atom Model Awal Atom Model atom J.J. Thomson Bola bermuatan positif Muatan-muatan negatif (elektron)) yang sama banyak-nya menempel
STRUKTUR ATOM. Penulis : Niyata Sirat, S.Pd. Penyunting Materi : Drs. Ucu Cahyana, M.Si. Penyunting Media : Drs. Slamet Soetanto, M.Si.
 STRUKTUR ATOM Mata Pelajaran K e l a s Nomor Modul : Kimia : X (Sepuluh) : Kim.X.02 Penulis : Niyata Sirat, S.Pd. Penyunting Materi : Drs. Ucu Cahyana, M.Si. Penyunting Media : Drs. Slamet Soetanto, M.Si.
STRUKTUR ATOM Mata Pelajaran K e l a s Nomor Modul : Kimia : X (Sepuluh) : Kim.X.02 Penulis : Niyata Sirat, S.Pd. Penyunting Materi : Drs. Ucu Cahyana, M.Si. Penyunting Media : Drs. Slamet Soetanto, M.Si.
1. Pernyataan di bawah ini yang bukan merupakan sifat periodik unsur-unsur adalah.
 TUGAS Jawablah soal-soa berikut dengan tepat dan benar. 1. Pernyataan di bawah ini yang bukan merupakan sifat periodik unsur-unsur adalah. A. Dari atas ke bawah dalam satu golongan energi ionisasi makin
TUGAS Jawablah soal-soa berikut dengan tepat dan benar. 1. Pernyataan di bawah ini yang bukan merupakan sifat periodik unsur-unsur adalah. A. Dari atas ke bawah dalam satu golongan energi ionisasi makin
