ANALISIS MUTASI GEN EGFR
|
|
|
- Ade Hartanto
- 8 tahun lalu
- Tontonan:
Transkripsi
1 ANALISIS MUTASI GEN EGFR DAN KRAS BERBASIS PCR- HRM (High Resolution Melting) DAN RFLP (Restriction Fragment Length Polymorphisme) TERHADAP CAIRAN PLEURA PASIEN KANKER PARU YANG DISIMPAN PADA KERTAS SARING ASEP MUHAMAD RIDWANULOH SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR BOGOR
2 2
3 3 PERNYATAAN MENGENAI TESIS DAN SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA Dengan ini saya menyatakan bahwa Tesis yang berjudul Analisis Mutasi Gen EGFR dan KRAS Berbasis PCR-HRM (High Resolution Melting) dan RFLP (Restriction Fragment Length Polymorphisme) terhadap Cairan Pleura Pasien Kanker Paru yang Disimpan pada Kertas Saring adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir Tesis ini. Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor. Bogor, Maret 2013 Asep M. Ridwanuloh NRP P
4 4 RINGKASAN ASEP MUHAMAD RIDWANULOH. Analisis Mutasi Gen EGFR dan KRAS Berbasis PCR-HRM (High Resolution Melting) dan RFLP (Restriction Fragment Length Polymorphisme) terhadap Cairan Pleura Pasien Kanker Paru yang Disimpan pada Kertas Saring. Dibimbing oleh SUHARSONO, AHMAD R.H. UTOMO dan JUDHI RACHMAT. Penyakit kanker paru merupakan penyakit yang paling banyak menyebabkan kematian akibat kanker di dunia, termasuk di Indonesia. Saat ini pengobatan pasien kanker paru seperti terapi target telah banyak dikembangkan untuk menurunkan angka kematian. Teknik pengobatan ini membutuhkan hasil diagnosa yang cepat dan akurat berbasis analisis molekuler terhadap gen yang mengalami mutasi seperti KRAS dan EGFR. Penelitian ini mengembangkan teknik analisis PCR-HRM dan PCR-RFLP untuk mengetahui terjadinya mutasi gen EGFR dan KRAS pada sampel efusi pleura pasien kanker paru. Hasil uji sensitivitas menggunakan metode dilusi menunjukkan bahwa PCR-HRM mampu mendeteksi mutasi gen KRAS dan EGFR pada konsentrasi 12,5% DNA mutan dalam campuran DNA wild type, sedangkan metode PCR-RFLP mampu mendeteksi adanya mutasi hingga konsentrasi DNA mutan dalam campuran DNA wild type sebesar 3,125%. Penelitian ini menggunakan 63 sampel cairan pleura pasien kanker paru yang disimpan dalam kertas saring. Hasil analisis menunjukkan bahwa 1,6% (1/63) memiliki mutasi gen KRAS dan 15,9% (10/63) memiliki mutasi gen EGFR. Mutasi EGFR yang terjadi pada pasien pria adalah 21,43% (6/28) dan pada wanita sebesar 15,3% (4/26). Hasil penelitian ini menunjukkan bahwa HRM dan RFLP merupakan metode yang sensitif untuk mendeteksi mutasi gen KRAS dan EGFR pada sampel pasien kanker paru. Kertas saring memiliki potensi yang besar digunakan dalam analisis molekuler kanker paru, khususnya sebagai media penyimpanan dan pengiriman sampel yang berasal dari efusi pleura. Kata kunci: kanker paru, efusi pleura, KRAS, EGFR, HRM, RFLP dan kertas saring
5 5 SUMMARY ASEP MUHAMAD RIDWANULOH. EGFR and KRAS Genes Mutation Analysis Based on PCR-HRM (High Resolution Melting) and RFLP (Restriction Fragment Length Polymorphisme) of Pleural Liquid from Lung Cancer Patients that Collected at Filter Paper. Supervised by SUHARSONO, AHMAD R.H. UTOMO and JUDHI RACHMAT. Lung cancer is the most frequent cause of cancer-related mortality worldwide, including in Indonesia. Today, a medical treatment for lung cancer patient, such as targeted therapies, has been developed to decrease the mortality. The methods need a rapid and a robust molecular characterisation technique to diagnose any gene mutations such as the KRAS and the EGFR. We developed a PCR-HRM and a PCR-RFLP for screening the EGFR and the KRAS mutations in pleural effusion of lung cancer patients. Sensitivity studies using the dilution assay revealed that the PCR-HRM was able to detect KRAS and EGFR mutations as little as 12.5% of mutant DNA in wild type DNA, while the PCR-RPLF was able to detect as little as % of DNA mutant in wild type DNA. We analysed 63 of pleural effusion from lung cancer patient that were collected in filter paper. From our sample, we found that 1.6% (1/63) of them had the KRAS mutation; meanwhile 15.9 % (10/63) of them had the EGFR mutations. We also found that the EGFR mutation was more prevalent in men 21.43% (6/28) compared to women 15.3% (4/26). These results showed that the HRM and the RFLP are useful methods to detect the KRAS and the EGFR mutations in the clinical samples of lung cancer. The filter paper was also very potential material to be used in molecular analysis of lung cancer, especially for collecting and transferring the pleural effusion samples. Key words: Lung cancer, pleural effusion, KRAS, EGFR, HRM, RFLP and filter paper
6 6 Hak Cipta milik IPB, tahun 2013 Hak Cipta dilindungi Undang-undang Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; pengutipan tersebut tidak merugikan kepentingan yang wajar IPB Dilarang mengumumkan dan memperbanyak sebagian atau seluruh Karya Tulis dalam bentuk apapun tanpa izin IPB
7 7 ANALISIS MUTASI GEN EGFR DAN KRAS BERBASIS PCR- HRM (High Resolution Melting) DAN RFLP (Restriction Fragment Length Polymorphisme) TERHADAP CAIRAN PLEURA PASIEN KANKER PARU YANG DISIMPAN PADA KERTAS SARING ASEP MUHAMAD RIDWANULOH Tesis Sebagai salahsatu syarat untuk memperoleh gelar Magister Sains pada Program Studi Bioteknologi SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR 2013
8 8 Penguji Luar Komisi: Prof drh Dondin Sajuthi, MST PhD
9 9 Judul Penelitian Nama NIM : Analisis Mutasi Gen EGFR dan KRAS Berbasis PCR- HRM (High Resolution Melting) dan RFLP (Restriction Fragment Length Polymorphisme) terhadap Cairan Pleura Pasien Kanker Paru yang Disimpan pada Kertas Saring : Asep M. Ridwanuloh : P Disetujui oleh Komisi Pembimbing Prof Dr Ir Suharsono, DEA Ketua Ahmad R. H. Utomo, PhD Anggota Judhi Rachmat, PhD Anggota Diketahui oleh, Ketua Program Studi Bioteknologi Dekan Sekolah Pascasarjana Prof Dr Ir Suharsono, DEA Dr Ir Dahrul Syah, MScAgr Tanggal Ujian: 10 Januari 2013 Tanggal Lulus: 20 Maret 2013
10 10 PRAKATA Puji serta syukur penulis ucapkan kehadirat Alloh SWT karena berkat Rahmat dan Hidayah-Nya penulis dapat menyelesaikan penelitian dengan judul Analisis Mutasi Gen EGFR dan KRAS Berbasis PCR-HRM (High Resolution Melting) dan RFLP (Restriction Fragment Length Polymorphisme) terhadap Cairan Pleura Pasien Kanker Paru yang Disimpan pada Kertas Saring. Ucapan terimakasih penulis sampaikan kepada: 1. Prof Dr Ir Suharsono, DEA sebagai ketua komisi pembimbing, Ahmad R.H. Utomo, PhD dan Judhi Rachmat, PhD sebagai anggota komisi pembimbing yang telah memberikan bimbingan, arahan dan ilmunya kepada penulis. 2. Prof drh Dondin Sajuthi, MST PhD selaku dosen penguji luar komisi yang telah memberikan saran dan masukan yang sangat berguna demi kesempurnaan tesis ini. 3. Kementerian Riset dan Teknologi yang telah memberikan beasiswa pendidikan, hingga penulis bisa menyelesaikan studi pada program Pascasarjana Bioteknologi IPB. 4. dr Achmad Hudoyo, SpP(K) beserta tim dokter spesialis paru RS Persahabatan Jakarta yang telah memberikan kesempatan kepada penulis untuk melaksanakan sebagian dari proyek penelitian besarnya. 5. Keluarga besar laboratorium Kalbe Genomic-SCI, PT Kalbe Farma, Tbk., dan keluarga besar laboratorium Diagnostik Kesehatan Pusat Penelitian Bioteknologi LIPI yang telah banyak memberikan bantuan atas kelancaran penelitian ini. 6. Kedua orangtua beserta adik-adik yang telah memberikan begitu banyak perhatian, dukungan dan do anya kepada penulis. 7. Segenap sahabat mahasiswa S2 Bioteknologi IPB angkatan 2010 yang telah banyak memberikan motivasi dan bantuannya. Terimakasih atas kebersamaan kita selama ini. 8. Segenap karyawan serta staff administrasi Program Studi Bioteknologi IPB, yang telah banyak membantu penulis dalam proses administrasi. Serta semua pihak yang telah banyak memberikan motivasi, dan dukungannya serta menjadi inspirasi bagi penulis. Semoga karya ilmiah ini bermanfaat. Bogor, Maret 2013 Asep Muhamad Ridwanuloh
11 11 DAFTAR ISI DAFTAR ISI DAFTAR TABEL DAFTAR GAMBAR DAFTAR LAMPIRAN Halaman PENDAHULUAN 1 Latar Belakang 1 Tujuan 3 TINJAUAN PUSTAKA 4 Kanker Paru 4 Biomarker Kanker Paru 6 High Resolution Melting Analysis (HRM) 11 Restriction Fragment Length Polymorphism (RFLP) 13 METODOLOGI 16 Waktu dan Tempat Penelitian 16 Bahan 16 Prosedur Kerja 16 HASIL DAN PEMBAHASAN 18 Analisis Mutasi Gen KRAS Menggunakan Metode HRM dan RFLP pada DNA Standar Sel Kultur 18 Uji Sensitivitas Metode HRM dan RFLP dalam Analisis Mutasi Gen KRAS 21 Analisis Mutasi Gen EGFR menggunakan Metode HRM dan RFLP pada DNA Standar 23 Uji Sensitivitas Metode HRM dan RFLP dalam Analisis Mutasi Gen EGFR 24 Isolasi DNA dari Sampel yang Disimpan dalam Kertas Saring 26 Analisis HRM dan RFLP Cairan Pleura Pasien Kanker Paru yang Disimpan dalam Kertas Saring 26 Prevalensi mutasi gen KRAS dan EGFR 29 Potensi pengembangan kertas saring sebagai media pengiriman sampel 32 SIMPULAN DAN SARAN 34 Simpulan 34 Saran 34 DAFTAR PUSTAKA 35 LAMPIRAN 42 DAFTAR RIWAYAT HIDUP 45 x xi xi xiii
12 12 DAFTAR TABEL Halaman 1 Data prevalensi mutasi gen EGFR pada pasien kanker paru 7 2 Data prevalensi mutasi gen EGFR pada pasien kanker paru di beberapa negara 31 3 Prevalensi mutasi gen EGFR dan KRAS berdasarkan jenis kelamin 31 DAFTAR GAMBAR Halaman 1 Fase pertumbuhan kanker pada pasien perokok dan non-perokok 4 2 Anatomi pleura paru 5 3 Grafik prevalensi mutasi gen pada pasien kanker paru 7 4 Skema jalur transduksi sinyal EGFR 8 5 Mutasi EGFR exon 19 dan Perubahan struktur asam amino pada mutasi gen EGFR exon Siklus aktivasi protein Ras 11 8 Proses PCR-HRM yang diamati penurunan sinyal fluoresen 12 9 Pola pita DNA mutan dan DNA wild type pada analisis mutasi gen KRAS dan EGFR menggunakan metode RFLP Hasil analisis mutasi gen KRAS DNA standar sel kultur menggunakan metode HRM Hasil analisis mutasi gen KRAS menggunakan metode RFLP Hasil uji sensitivitas analisis mutasi gen KRAS menggunakan metode HRM Hasil uji sensitivitas metode RFLP dalam analisis mutasi gen KRAS Hasil analisis mutasi gen EGFR menggunakan metode HRM Hasil analisis mutasi gen EGFR menggunakan metode RFLP Hasil uji sensitivitas analisis mutasi gen EGFR menggunakan metode HRM Hasil uji sensitivitas metode RFLP pada analisis mutasi gen EGFR Grafik analisis mutasi gen KRAS pada sampel pasien kanker paru Hasil analisis mutasi gen KRAS sampel pasien kanker paru menggunakan metode RFLP Grafik analisis mutasi gen EGFR exon 19 pada sampel pasien kanker paru Grafik analisis mutasi gen EGFR exon 21 pada sampel pasien kanker paru Hasil analisis gel elektroforesis amplikon produk PCR-HRM DNA sampel dalam analisis mutasi gen EGFR exon Prevalensi mutasi gen KRAS dan EGFR pada pasien kanker paru 30
13 13 DAFTAR LAMPIRAN Halaman 1 Ethical Clearance 41 2 Tabel hasil analisis mutasi gen KRAS dan EGFR pada sampel pasien kanker paru menggunakan metode HRM dan RFLP 42
14 14 PENDAHULUAN Latar Belakang Kanker paru merupakan jenis penyakit kanker yang sulit disembuhkan, sehingga telah menjadi penyebab kematian dengan frekuensi yang tinggi di dunia (Dienstmann et al. 2011). Angka tahan hidup lima tahun penderita kanker paru hanya sekitar 16%, jauh dibawah kanker kolon, kanker prostat, kanker payudara dan kanker serviks yang rata-rata bisa mencapai lebih dari 70% (American Cancer Society 2012). Di Indonesia, angka kematian akibat kanker paru juga cukup tinggi. Rata-rata tercatat pasien kanker paru setiap tahun dengan angka tahan hidup rata-rata hanya sekitar 6 bulan (Hudoyo 2012). Berbagai upaya pengobatan seperti pembedahan, radioterapi, dan kemoterapi dilakukan untuk meningkatkan angka tahan hidup pasien kanker paru (Spira & Ettinger 2004). Namun demikian, pasien kanker paru 80 90% diketahui telah berada pada stadium III dan IV ketika diagnosa pertama dilakukan (Sone et al. 2007). Tindakan pembedahan dan radioterapi pada stadium ini sudah tidak efektif dilakukan karena sel kanker telah menyebar, sehingga pengobatan berbasis kemoterapi merupakan pilihan utama yang saat ini dilakukan (Hudoyo 2012). Dalam perkembangannya, target terapi dari jenis obat kemoterapi yang ada terus dikembangkan untuk mengurangi terjadinya dampak negatif terhadap pasien. Pengobatan berbasis sistem terapi target terhadap protein spesifik pada sel kanker dalam berbagai bentuk seperti senyawa kimia sederhana dan antibodi menjadi solusi yang saat ini telah dikembangkan (Shawver et al. 2002; Kim et al. 2005). Dua jenis protein yang menjadi target terapi pada kasus kanker paru diantaranya adalah EGFR (Epidermal Growth Factor Reseptor) dan KRAS (Kirsten Rat Sarcoma) (Mok et al.2009). Protein EGFR dan KRAS merupakan dua jenis protein yang berperan penting dalam mengendalikan pertumbuhan dan kematian sel (Sakurada et al. 2006; Ronen et al. 2006). Pada sel normal protein ini berperan mengatur jalannya sinyal pertumbuhan sel secara teratur. Namun, pada sel kanker kedua protein ini mengalami perubahan karakteristik akibat adanya perubahan struktur asam amino penyusunnya (Rosell et al. 2006). Susunan asam amino protein tersebut disandikan oleh gen EGFR dan gen KRAS (Sakurada et al. 2006; Ronen et al. 2006). Mutasi pada gen EGFR dapat menyebabkan perubahan karakteristik enzim tirosin kinase, bagian dari protein EGFR, yang memicu proliferasi sel secara terus menerus dan menghambat apoptosis (Sakurada et al. 2006). Mutasi pada gen KRAS juga dapat menyebabkan dampak yang sama dengan mutasi pada gen EGFR (Ronen et al. 2006). Analisis perubahan karakteristik protein EGFR dan KRAS dapat dilakukan dengan menggunakan metode analisis DNA berbasis biologi molekuler (Sung & Cho 2008). Analisis mutasi gen berbasis biologi molekuler sebagai diagnosa utama pasien kanker paru menjadi sangat penting dilakukan untuk memilih tindakan pengobatan yang tepat antara obat kemoterapi yang umum dan obat terapi target yang lebih spesifik agar pasien memperoleh peningkatan kualitas kesehatan. Secara keseluruhan pengobatan kemoterapi dan terapi target menunjukkan median survival yang sama sekitar 6 bulan, namun demikian hasil
15 15 analisis lebih lanjut penggunaan obat berbasis terapi target pada pasien yang tepat dapat memperlama tingkat kekambuhan. Pengobatan kemoterapi pada pasien yang mengalami mutasi gen EGFR hanya memberikan dampak peningkatan ketahanan terhadap kekambuhan sekitar 5,4 bulan, sedangkan dengan menggunakan obat terapi inhibitor tirosin kinase dapat meningkat hingga 10,4 bulan. Dampak sebaliknya terjadi jika obat inhibitor tirosin kinase diberikan kepada pasien yang tidak mengalami mutasi gen EGFR, pasien dapat mengalami penurunan ketahanan terhadap kekambuhan hingga dibawah 3 bulan (Mok et al. 2009). Metode standar analisis mutasi gen yang digunakan saat ini adalah DNA sekuensing. Teknik ini paling akurat untuk mendeteksi adanya perubahan nukleotida pada sekuen DNA. Namun demikian, untuk aplikasi medis metode ini memiliki kekurangan diantaranya limit deteksi mutasi yang rendah, sehingga kurang cocok digunakan untuk sampel dengan frekuensi mutasi yang rendah (Krypuy et al. 2006). Beberapa peneliti telah melakukan pengembangan teknik deteksi yang cepat, dan memiliki sensitivitas serta akurasi yang tinggi, namun sederhana dan mudah dilakukan sebagai alternatif dari teknik sekuensing seperti teknik pyrosequensing (Ogino et al. 2005), mutant enrichment-pcr (Kawada et al. 2008), Denaturing Gradient Gel Electrophoresis (DGGE) (Siegfried et al. 1997), dan Denaturing High Performance Liquid Chromatography (DHPLC) (Karim et al. 2011). Teknik High Resolution Melting (HRM) dan Restriction Fragment Length Polymorphisme (RFLP) merupakan teknik deteksi mutasi gen lainnya yang telah dikembangkan. Teknik ini lebih sederhana, cepat dan memiliki akurasi serta sensitivitas yang tinggi jika dibandingkan dengan teknik DNA sekuensing (Krypuy et al. 2006; Kawada et al. 2008). Aplikasi kedua metode ini dalam analisis sampel pasien kanker telah dikembangkan secara terpisah. Krypuy et al. (2006) telah melakukan deteksi mutasi gen KRAS pada 30 sampel kanker paru dari hasil biopsi menggunakan teknik HRM, dan berhasil mendeteksi mutasi gen KRAS kodon 12 dan 13 dengan performa dan sensitivitas yang baik. Namoto et al. (2006) telah melakukan analisis mutasi gen EGFR dari sampel sitologi kanker paru menggunakan teknik HRM. Teknik RFLP telah dilakukan oleh Kawada et al. (2008) untuk mengetahui terjadinya mutasi pada gen EGFR pada kasus kanker paru menggunakan enzim restriksi spesifik untuk membedakan antara jenis gen mutan dan wild type. Teknik RFLP juga telah dilakukan untuk mendeteksi mutasi gen KRAS pada kanker kolon (Nollau et al. 1996). Di Indonesia, analisis mutasi gen EGFR dan KRAS berbasis biologi molekuler sebagai diagnosa utama untuk menentukan tindakan pengobatan belum banyak dilakukan. Keterbatasan fasilitas pengujian sel kanker berbasis mutasi gen merupakan kendala utama. Penyediaan sampel berbasis histologi yang saat ini digunakan sebagai sampel standar untuk pengujian mutasi gen juga hanya dapat dilakukan melalui proses operasi yang cenderung terbatas pada rumah sakit tertentu, tersedia dalam jumlah sedikit dan bersifat invasif (melukai pasien) (Pang et al. 2012). Cairan pleura yang banyak dihasilkan pada pasien kanker paru stadium lanjut telah digunakan sebagai bahan untuk mengetahui adanya mutasi gen melalui preparasi sampel sitologi, namun teknik ini juga terbatas hanya dapat dilakukan oleh rumahsakit yang memiliki fasilitas analisis patologi sel. Rumah sakit daerah yang memiliki fasilitas terbatas memiliki kesulitan untuk
16 16 mengirimkan sampel pada laboratorium rujukan yang telah memiliki fasilitas lengkap. Penggunaan cairan pleura yang disimpan dalam kertas saring sebagai media pengiriman sampel untuk analisis mutasi gen merupakan harapan solusi yang belum pernah dilakukan. Analisis mutasi gen sebagai diagnosa utama untuk menentukan tindakan pengobatan yang tepat merupakan hal yang sangat penting, maka pengembangan kombinasi metode analisis PCR-HRM dan RFLP untuk mengetahui adanya mutasi gen pada sampel cairan pleura pasien kanker paru yang disimpan dalam kertas saring sebagai media penyimpanan sementara dan pengiriman sampel dilakukan dalam penelitian ini. Selain itu, penelitian ini diarahkan untuk mengetahui profil mutasi gen pada pasien kanker paru di Indonesia, sehingga dapat dijadikan sebagai data awal untuk mengetahui karakteristik pola mutasi gen pada pasien kanker paru di Indonesia. Adapun analisis mutasi gen yang menjadi fokus utama pada penelitian ini adalah analisis mutasi gen EGFR pada ekson 19 dan 21 serta mutasi gen KRAS pada kodon 12 dan 13. Pemilihan jenis dan posisi gen ini didasarkan pada hasil penelitian di beberapa negara yang menunjukkan bahwa kedua jenis mutasi ini memiliki prevalensi yang dominan (Lynch et al. 2004). Mutasi gen EGFR sering terjadi pada ekson 18, 19, 20 dan 21, namun menurut Lynch et al. (2004) mutasi yang paling banyak ditemukan adalah delesi pada ekson 19 dan mutasi titik pada ekson 21. Mutasi gen KRAS ditemukan pada ekson 2 kodon 12 dan 13 (sering) dan ekson 3 kodon 59 dan 61 (jarang) (Cox & Der 2003; Molina & Adjei 2006). Tujuan Tujuan penelitian ini adalah untuk mengetahui penggunaan metode PCR- HRM dan RFLP dalam mendeteksi adanya mutasi gen EGFR dan KRAS pada sampel cairan pleura yang disimpan dalam kertas saring, dan untuk mengetahui prevalensi mutasi gen EGFR dan KRAS pada pasien kanker paru.
17 17 TINJAUAN PUSTAKA Kanker Paru Kanker paru merupakan tumor ganas pada organ paru, dan terletak pada daerah saluran nafas atau epitel bronkus. Terjadinya kanker paru ditandai dengan pertumbuhan sel yang tidak normal, tidak terbatas dan cenderung merusak jaringan normal (Herbst et al. 2008). Masa pertumbuhan kanker mulai dari fase prakanker, stadium awal dan stadium lanjut dapat dilihat pada Gambar 1. Normal Pra kanker Stadium awal Stadium Lanjut Perokok Perbesaran Asap rokok Kerentanan Faktor lain Bukan Perokok Herbst et al. (2008) Gambar 1 Fase pertumbuhan kanker pada pasien perokok dan non-perokok Kanker paru terbagi menjadi dua kelompok besar yaitu Small-Cell Lung Cancer (SCLC) dan Non-Small Cell Lung Cancer (NSCLC). Kasus kanker paru jenis NSCLC lebih banyak terjadi (85%) jika dibandingkan dengan jenis SCLC (15%) (Herbst et al. 2008). NSCLC dapat dibagi menjadi tiga subtipe utama yaitu squamous-cell carcinoma, adenocarcinoma, dan large cell lung cancer. Jenis squamous-cell carcinoma dan small-cell lung cancer banyak ditemukan pada pasien perokok, sedangkan jenis sel adenocarcinoma banyak ditemukan pada pasien non-perokok. Asap rokok dan polusi lingkungan lainnya dapat memicu terjadinya karsinogenesis. Disamping itu, faktor lain seperti keturunan, hormonal dan virus juga dapat menjadi pemicu karsinogenesis pada paru (Sun et al. 2007). Kerusakan jaringan paru diawali dengan perubahan genetik dan epigenetik, seperti mutasi gen dan metilasi yang tidak normal, dan perubahan transkriptomik, seperti inflamasi dan apoptosis. Perubahan ini terjadi dalam jangka waktu yang cukup lama dan mengarah kepada terjadinya perubahan pada jalur regulasi sel, seperti ketidakteraturan proses proliferasi dan apoptosis, sehingga sel berubah menjadi ganas (Spira et al. 2004). Perubahan karakteristik molekuler juga menyebabkan terjadinya angiogenesis, invasi dan metastasis sel (Sato et al. 2007).
18 18 Perubahan karakteristik molekuler pada setiap pasien kanker paru berbedabeda (Gambar 1). Pasien kanker paru yang memiliki riwayat merokok misalnya, memiliki perbedaan karakteristik pola mutasi gen dengan pasien yang tidak memiliki riwayat perokok. Mutasi gen KRAS banyak ditemukan pada pasien perokok, sedangkan mutasi gen EGFR banyak ditemukan pada pasien nonperokok. Sel kanker pada pasien perokok umumnya terbentuk pada bagian saluran utama sistem pertukaran udara, sedangkan pada kasus pasien non-perokok umumnya terbentuk pada daerah perifer (Mao et al. 1997; Wistuba et al. 2000; Zudaire et al. 2008) Pasien kanker paru memiliki harapan kesembuhan lebih besar jika pada saat dilakukan diagnosa pertama kali masih berada pada stadium awal (I dan II). Pada kondisi ini sel kanker paru masih dapat diangkat melalui pembedahan. Namun demikian, 80 90% pasien penderita kanker paru sudah diketahui berada pada stadium III dan IV ketika diagnosa pertama kali dilakukan (Sone et al. 2007). Pada stadium ini sel kanker sudah menyebar menuju organ lain, dan pada beberapa pasien umumnya disertai pembengkakan dan penumpukan cairan pada rongga pleura, yang sering disebut efusi pleura. Pleura adalah membran serosa yang licin, mengkilat, tipis dan transparan. Membran ini menutupi jaringan paru dan terdiri atas 2 lapisan yaitu pleura viseralis yang terletak pada bagian dalam, langsung menutupi permukaan paru, dan pleura parietalis yang terletak pada bagian luar dan berhubungan dengan dinding dada (Gambar 2a). Pada rongga pleura terdapat cairan yang keluar dari pembuluh darah melalui pleura parietal dan kemudian diserap oleh pleura viseralis, dialirkan ke pembuluh limfe dan kembali ke darah (Gambar 2b). Rongga pleura dalam keadaan normal memiliki ukuran tebal µm, berisi sekitar ml cairan jernih yang tidak berwarna, mengandung protein <1,5 gr/dl dan ± 1500 sel/µl. Sel cairan pleura didominasi oleh sel monosit, sejumlah kecil sel limfosit, makrofag, sel darah merah dalam jumlah yang sangat kecil dan sel mesotel (Light 2000). Pleura viseral Rongga pleura Pleura parietal Rongga pleura Mediastinum Efusi pleura (a) (b) Gambar 2 Anatomi pleura paru. (a) pleura normal; (b) efusi pleura Efusi pleura adalah penumpukan cairan pada rongga pleura, yang terjadi akibat produksi cairan melebihi kemampuan normal penyerapan sehingga terjadi akumulasi cairan melebihi volume normal. Umumnya efusi pleura disebabkan oleh infeksi dan kasus keganasan/kanker pada paru atau organ lainnya (Sato 2006). Efusi pleura yang disebabkan oleh kanker sering disebut sebagai efusi pleura ganas (EPG). EPG dibuktikan dengan adanya penemuan sel tumor pada
19 19 pemeriksaan sitologi cairan pleura atau biopsi cairan pleura. Efusi pleura ganas bersifat metastatik berasal dari penyebaran langsung sel-sel ganas dari tempat sekitar (seperti pada keganasan paru, payudara, dan dinding dada) (Heffner & Klein 2008). Pada umumnya hanya sekitar 25% dari effusi pleura ganas yang disertai penemuan sel tumor pada pemeriksaan sitologi. Meskipun tidak ditemukan sel tumor pada cairan pleura, akan tetapi ditemukan kanker primer pada paru dan cairan pada pleura timbul berulang, masif dan pasien tidak respon terhadap obat antiinfeksi maka pasien tetap dikategorikan menderita EPG (Syahruddin et al. 2009). Terjadinya EPG pada penderita kanker paru sangat menyulitkan pengambilan tindakan yang tepat. Penderita pada kondisi ini sudah dikategorikan berada pada stadium IIIB yang prognosisnya tidak dapat disamakan dengan stadium IIIB tanpa EPG. Penderita juga memiliki prognosis yang buruk, namun demikian penanganan yang tepat dapat meningkatkan kualitas kesehatan penderita (Burrows et al. 2000). Penelitian-penelitian terakhir berusaha untuk mengungkapkan patogenesis EPG pada tingkat molekuler untuk dapat menjawab tantangan dalam hal diagnosis dan penetalaksanaannya yang sangat kompleks. Penelitian-penelitian tersebut banyak melihat peranan protein inflamasi dan penanda tumor lainnya dalam hubungannya dengan EPG (Ngurah Rai 2009). Optimasi analisis kanker paru berdasarkan penanda protein CEA pada efusi pleura telah dilakukan Arbaningsih (2010). Analisis karakteristik molekuler yang memanfaatkan cairan pleura dari pasien kanker paru juga telah banyak dilakukan (Krypuy et al. 2006; Kimura et al. 2006). Biomarker Kanker Paru Pengembangan teknologi pengobatan berbasis sistem terapi target dan aplikasinya kepada pasien kanker telah mendorong dikembangkannya jenis biomarker spesifik yang dapat digunakan sebagai acuan dalam diagnosa untuk pengambilan tindakan pengobatan yang tepat. Biomarker prediktif dikembangkan, divalidasi dan diaplikasikan dalam diagnosa pasien untuk meningkatkan ketepatan dalam pemberian obat terapi target, serta melihat kemungkinan adanya resistensi yang terjadi. Adanya biomarker spesifik ini dapat membantu pasien menerima tindakan pengobatan yang tepat dan mengurangi biaya pengobatan (Tappenden et al. 2006; Simon 2010). Pengembangan penelitian untuk menemukan dan memvalidasi biomarker spesifik kanker paru telah dilakukan beberapa tahun ini. Salahsatu jenis biomarker yang dikembangkan, diarahkan pada pengobatan berbasis inhibitor enzim tirosin kinase pada reseptor faktor pertumbuhan/egfr. Dua jenis obat terapi target gefitinib (IRESSA TM ) dan erlotinib (TARCEVA TM ) telah menunjukkan respon pengobatan yang lebih baik terhadap pasien yang mengalami mutasi gen EGFR, sehingga menunjukkan pentingnya analisis mutasi gen EGFR sebagai biomarker kanker paru pada pasien (Dassonville et al. 2007; Hirsch & Bunn 2005; Dahabreh et al. 2010). Hasil penelitian sejak tahun 2004 menunjukkan bahwa penggunaan obat terapi target gefitinib pada pasien yang mengalami mutasi gen EGFR menunjukkan respon yang lebih baik jika dibandingkan dengan pemberian obat pada pasien yang memiliki profil gen EGFR wild type (Tabel 1).
20 20 Tabel 1 Data prevalensi mutasi gen EGFR pada pasien kanker paru Penelitian Etnis pasien Prevalensi mutasi Respon gefitinib terhadap pasien dengan EGFR Respon gefitinib terhadap pasien yang mengalami mutasi gen EGFR wild type Huang et al. (2004) Cina 8/16 (50%) 0/8 (0%) 6/8 (75%) Tokumo et al. (2005) Jepang 10/21 (48%) 2/12 (17%) 7/9 (78%) Zhang et al. (2005) Cina 12/30 (40%) 1/18 (6%) 8/12 (67%) Han et al. (2005) Korea 17/90 (19%) 10/73 (14%) 11/17 (65%) Kim et al. (2005 Korea 6/27 (22%) 2/21 (10%) 6/6 (100%) Pengembangan penemuan biomarker spesifik lain dalam rangka menemukan obat terapi target yang lebih spesifik untuk setiap pasien terus dikembangkan. Penemuan jenis mutasi pada gen-gen lain yang mengatur regulasi sel terus berkembang. Menurut Crystal & Alice (2011) beberapa jenis mutasi gen yang ditemukan pada pasien kanker paru selain gen EGFR adalah KRAS, ALK, PIK3CA, HER2, BRAF, AKT, MET dan sebagian besar mutasi gen masih belum diketahui (Gambar 3). Mutasi gen KRAS dan EGFR memiliki prevalensi cukup besar jika dibandingkan dengan gen yang lain. Tidak diketahui Gambar 3 Grafik prevalensi mutasi gen pada pasien kanker paru Mutasi Gen EGFR Gen EGFR (Epidermal Growth Factor Receptor) terletak pada lengan pendek kromosom 7 dan berfungsi untuk mengkode protein reseptor faktor pertumbuhan. EGFR terletak pada bagian transmembran sel epitel dan memiliki aktivitas tirosin kinase (Yarden & Sliwkowski 2001). Menurut Carpenter (1987) EGFR merupakan glikoprotein membran plasma yang berukuran 170 kda, dan tersusun dari bagian ekstraseluler, daerah transmembran dan daerah intraseluler. Daerah ekstraseluler merupakan bagian yang berikatan dengan ligan, sedangkan daerah intraseluler merupakan bagian aktivitas enzim trosin kinase. Ikatan ligan dengan reseptor menginduksi terjadinya dimerisasi antara dua reseptor EGFR. Proses dimerisasi tidak hanya terjadi antara reseptor yang sama (homo-dimerisasi) namun dapat terjadi antara dua reseptor yang berbeda (hetero-dimerisasi) (Riese & Stern 1998). Heterodimerisasi terjadi antara sesama kelompok reseptor tirosin kinase/erbb seperti ErbB2, ErbB3 dan ErbB4. EGFR berfungsi sebagai penyampai sinyal transduksi dari luar sel menuju inti sel melalui protein-protein di dalam sitoplasma, dan mengarah kepada proses
21 21 pengendalian pertumbuhan dan kematian sel, diferensiasi dan migrasi sel, angiogenesis, serta invasi sel (Santos et al. 2011). Sinyal ini terjadi setelah proses pengikatan ligan oleh reseptor EGFR yang dilanjutkan dengan adanya proses dimerisasi dan autofosforilasi (Ogiso et al. 2002; Schlessinger 2002). Proses ini memicu aktivasi jalur transduksi sinyal dibawah protein EGFR seperti jalur Akt, STAT dan RAS. Jalur sinyal Akt berkaitan erat dengan proses ketahanan (survival) sel (Goswami et al. 2006). Proses autofosforilasi jalur Akt melalui proses docking protein Gab1 pada protein PI3K yang selanjutnya akan mengaktivasi protein Akt, mtor dan akhirnya menyampaikan sinyal ke inti sel (Matton et al. 2004). Menurut Sordella et al. (2004) jalur Akt dan STAT memiliki peran penting dalam proses antiapoptosis untuk ketahanan sel. Pada jalur lain terjadi proses aktivasi sinyal Raf/MEK/Erk melalui aktivasi protein RAS. Protein Grb2 SH2 yang terikat pada EGFR menghasilkan sinyal yang mengaktivasi protein RAS dan terjadi fosforilasi pada protein dibawahnya (Katz et al. 2007). Jalur RAS terutama berperan terhadap proses proliferasi sel (Katz et al. 2007; Robets & Der 2007). Yoshida et al Gambar 4 Skema jalur transduksi sinyal EGFR Ket: ERK= extracytoplasmic-regulated kinase, Grb-2= Growth factor receptor-bound protein 2, MAPK= mitogen-activated protein kinase, MEK= MAPK kinase, mtor= mammalian target rapamycin, PI3K= phosphoinositide 3-kinase, PTEN= phospatase and tensin homolog, RAF= v-raf murine leukimia viral oncogene homolog, RAS= rat sarcoma viral oncogene homolog, SOS= sister of sevenless, STAT= signal transducer and activator of transcription. Pada kondisi normal EGFR akan menyampaikan sinyal melalui protein yang berada pada jalur dibawahnya ke inti sel, sehingga sel melakukan regulasi secara normal. Proses proliferasi dan apoptosis sel berjalan secara teratur. Akan tetapi, ketika terjadi perubahan prilaku pada protein EGFR yang disebabkan oleh adanya
22 22 mutasi gen, EGFR memberikan sinyal pertumbuhan sel yang secara konstitutif melakukan proliferasi dan menghambat aktivasi protein yang berperan dalam proses apoptosis, sehingga sel berubah menjadi kanker (Sakurada et al. 2006). Mutasi gen EGFR menyebabkan aktivasi tirosin kinase secara terus menerus akibat adanya perusakan pada sistem autoinhibitor (Yun et al. 2007) dan induksi terjadinya proses fosforilasi lebih tinggi jika dibandingkan dengan keadaan normal (Lynch et al. 2004; Mulloy et al. 2007). Selain itu, pada sel kanker paru NSCLC mutasi EGFR menyebabkan terjadinya dimerisasi reseptor tanpa membutuhkan bantuan ligan, sehingga aktivasi EGFR dan jalur tranduksi sinyal dibawahnya terjadi secara konstitutif (Okabe et al. 2007; Choi et al. 2007). Mutasi gen EGFR meliputi jenis mutasi titik, delesi dan insersi yang terjadi pada ekson 18, 19, 20, 21 dan 24 (Shigematsu et al. 2005; Paez et al. 2004; Lynch et al. 2004). Delesi yang terjadi merupakan jenis delesi in-frame akibat kehilangan 4-6 asam amino (kodon 746 kodon 752) pada ekson 19 (Sakurada et al. 2006; Kawada et al. 2008). Jenis mutasi berikutnya yang terjadi adalah substitusi satu nukleotida yang dapat terjadi pada ekson 18 dan 21, serta duplikasi in-frame dan atau insersi yang banyak terjadi pada ekson 20 (Shigematsu & Gazdar 2006). Pada umumnya mutasi yang paling sering terjadi (85-90%) adalah mutasi pada ekson 19 dan 21 kodon 858 (Gambar 5) (Shigematsu et al. 2005; Paez et al. 2004; Lynch et al. 2004). Substitusi pada mutan Substitusi dua sekuen terdeteksi dua nukleotida terdeteksi Gambar 5 Mutasi EGFR ekson 19 dan 21 (Santos et al. 2011) Mutasi EGFR pada ekson 21 kodon 858 menyebabkan terjadinya perubahan konformasi struktur enzim tirosin kinase. Substitusi basa Timin menjadi Guanin (CTG>CGG) menyebabkan perubahan translasi asam amino leusin menjadi arginin. Asam amino arginin bersifat hidrofil dan polar, sedangkan leusin bersifat hidrofob dan cenderung nonpolar. Asam amino hidrofil lebih banyak berada di bagian permukaan protein, sedangkan asam amino hidrofob memiliki struktur berlipat dan hampir selalu ada di bagian dalam protein (Yun el al. 2007)
23 23 Gambar 6 Perubahan struktur asam amino pada mutasi EGFR exon 21. (a) EGFR dengan asam amino Leusin; (b) EGFR dengan asam amino Arginin Mutasi Gen KRAS Penelitian mengenai gen RAS bukanlah hal yang baru dilakukan akhir-akhir ini. Edward Scolnick dan tim risetnya sejak 30 tahun yang lalu telah mengidentifikasi gen RAS (Rat Sarcoma Virus) sebagai suatu gen virus dengan karakteristik yang bersifat onkogenik/memicu terjadinya tumor, dan kemudian diidentifikasi merupakan gen yang terkait dengan karsinogenesis (Linordau et al. 2011). Gen RAS pada awalnya ditemukan dari virus penginduksi leukimia pada tikus. Gen tersebut kemudian diidentifikasi sebagai HRAS (Harvey RAS) dan KRAS (Kirsten RAS) setelah ditemukan dari turunan sekuen genom tikus. Pada tahun 1982, penelitian mengenai kloning gen dari sel kultur manusia menemukan adanya homologi gen manusia dengan gen HRAS dan KRAS. Satu tahun kemudian jenis gen RAS yang lain, NRAS (Neuroblastoma RAS), ditemukan (Rielly et al. 2008). Gen RAS mengekspresikan protein RAS yang termasuk kedalam famili protein G (Guanine triphosphate-binding protein), suatu protein berukuran kda, yang berperan dalam proses penyampaian sinyal transduksi di dalam sel (Linordau et al. 2011), dan berfungsi sebagai saklar molekuler penghubung aktivasi tirosin kinase yang mengkonversi sinyal dari membran ke inti sel (Adjei 2001). Protein Ras teraktivasi secara langsung melalui faktor pertukaran nukleotida guanin (Guanine nucleotide exchange factors/gep) yang mengubah guanosin diposfat (GDP) menjadi guanosin triposfat (GTP), dan kembali pada keadaan tidak aktif ketika terjadi hidrolisis GTP menjadi GDP, suatu reaksi yang dikatalisasi oleh enzim GTPase (Gambar 7) (Hall et al. 2002; Cox & Der 2003).
24 24 Tidak aktif Aktif Efektor RAS (Raf, MEK, Erk) Gambar 7 Siklus aktivasi protein RAS Respon sel (Linardou et al. 2011) Menurut Linordau et al. (2011) proses aktivasi RAS dibantu protein GRB2 dan SHC, protein adaptor yang mengikat RAS pada fosfotirosin spesifik. Interaksi ini menjadi mediasi masuknya SOS ke dalam membran plasma yang akan mendorong konversi RAS dari GDP menjadi bentuk GTP. Reseptor-reseptor lain yang tidak secara langsung terintegrasi dengan tirosin kinase seperti Src-like tirosin kinase juga mengaktivasi protein RAS. Proses inaktivasi RAS terjadi melalui proses perubahan GTP menjadi GDP oleh GAPs, suatu proses yang belum diketahui secara detail. Ada suatu pendapat yang menyatakan bahwa fosforilasi SOS oleh jalur Raf/MAP kinase dapat menginduksi disosiasi SOS dari GRB2 sebagai hasil peralihan menjadi bentuk GDP. Protein GAP p120 bertindak sebagai regulator negatif RAS dan diatur oleh fosporilasi tirosin. Aktivasi RAS menyebabkan fungsinya sebagai adaptor untuk mengaktifkan jalur-jalur sinyal transduksi berikutnya berlangsung dan pada akhirnya menyampaikan sinyal ke inti sel. Mutasi gen RAS merupakan perubahan onkogen yang paling banyak terjadi pada kasus kanker manusia. Mutasi gen RAS yang umum terjadi disebabkan adanya substitusi satu basa nukleotida pada daerah kodon 12, 13 dan kodon 61 (Bos 1989). Letak mutasi KRAS yang jarang terjadi adalah pada kodon 11, 18 dan 59 (Cox & Der 2003; Molina & Adjei 2006; Krypuy et al. 2006) dan kodon 22 (Miyakura et al. 2002). High Resolution Melting Analysis (HRM) Analisis HRM adalah suatu metode yang dikembangkan untuk mengetahui adanya mutasi atau variasi pada susunan basa nukleotida secara tepat dan cepat. Metode ini mampu mendeteksi dan mengidentifikasi mutasi gen secara cepat, mengidentifikasi variasi genetik tanpa sekuensing dan atau membedakan adanya variasi genetik pada suatu populasi (Kapa Biosystem 2007). HRM banyak
25 25 digunakan untuk SNP (Single nucleotide polymorphisme) genotyping, analisis DNA metilasi, fingerprint DNA, identifikasi spesies, dan penemuan adanya mutasi DNA (Corbett Research 2006). HRM merupakan teknik yang sederhana, tidak memerlukan proses pemisahan DNA atau proses rumit lainnya. Teknik ini menjadi solusi yang tepat untuk diagnostik setelah teknik HRM ini dikombinasikan dengan rapid cycle PCR (Reed et al. 2007). Proses HRM diawali dengan amplifikasi sekuen DNA target menggunakan teknik PCR. Senyawa dye ditambahkan agar dapat terikat pada DNA utas ganda hasil PCR secara spesifik dan menghasilkan fluoresen yang jelas. Dye tidak terikat dan memancarkan fluoresen pada DNA utas tunggal. Perbedaan sinyal fluoresen ini digunakan untuk mengamati proses amplifikasi DNA dan proses selama HRM. Analisis HRM dimulai setelah proses PCR selesai, DNA yang dihasilkan didenaturasi secara bertahap dengan cara menaikkan temperatur secara perlahan dengan tujuan untuk mendapatkan profil pola melting point DNA. Pola ini dapat diamati dari penurunan fluoresen senyawa dye akibat perubahan DNA dari utas ganda menjadi utas tunggal (Kapa Biosystem 2007). DNA utas ganda DNA utas tunggal Gambar 8 Proses PCR-HRM yang diamati penurunan sinyal fluoresen HRM menggunakan mesin PCR yang dilengkapi dengan instrumen beresolusi tinggi untuk menentukan pola melting DNA, sehingga tidak semua mesin PCR dapat digunakan. Pola melting yang terbentuk menunjukkan karakteristik DNA yang terbentuk. Karakterisasi DNA dengan HRM dilakukan berdasarkan pada panjang sekuen, kandungan basa guanin dan sitosin, serta komplementaritas sekuen DNA. HRM sangat sensitif untuk mendeteksi adanya perubahan satu basa nukleotida. Dengan demikian, adanya mutasi titik pada basa DNA akan menghasilkan pola melting yang berbeda (Wittwer 2009). HRM terjadi setelah proses PCR, sehingga sangat bergantung kepada keberhasilan proses PCR. Tingkat sensitivitas yang tinggi sangat dipengaruhi oleh kondisi PCR yang digunakan. Faktor-faktor yang dapat mempengaruhi keberhasilan analisis seperti faktor mesin dan faktor proses PCR yang meliputi desain primer, reagen PCR, senyawa dye dan kondisi siklus PCR perlu
26 26 diperhatikan. Sedikit perbedaan pada kondisi mesin dan kondisi campuran reagen PCR dapat menyebabkan perubahan pada hasil analisis (Reed et al. 2007). Kualitas DNA cetakan, primer, konsentrasi MgCl2, dan keberadan inhibitor dapat mempengaruhi pola melting DNA. Selain itu keberadaan senyawa dye sebagai indikator melalui sinyal fluoresen yang dihasilkan juga sangat penting. Beberapa jenis dye yang telah dikembangkan diantaranya adalah SYBR green, LCGreen, dan Syto9 (White & Potts 2006). Penggunaan SYBR Green dapat menghambat proses PCR ketika konsentrasi DNA utas ganda yang terbentuk telah mencapai jumlah yang hampir jenuh. Hal ini dapat menyebabkan dye jumping selama proses melting amplikon sehingga dapat menurunkan sensitivitas deteksi HRM (Wittwer et al. 2003). LCGreen digunakan untuk menyempurnakan fungsi dye SYBR green. Dye ini tidak menghambat proses amplifikasi selama PCR sehingga sensitivitas dan spesifitas analisis lebih baik jika dibandingkan dengan SYBR Green (Wittwer et al. 2003; Herrmann et al. 2006). Jenis dye berikutnya adalah SYTO9 yang memiliki tingkat sensitivitas dan spesifisitas deteksi yang lebih tinggi daripada LCGreen. SYTO9 menunjukkan hasil analisis melting curve yang lebih reprodusibel, tidak menghambat proses PCR dan tidak bersifat selektif terhadap amplikon tertentu (Monis et al. 2004). Restriction Fragment Lenght Polymorphisme (RFLP) Metode RFLP merupakan salah satu metode yang umum digunakan untuk mengetahui adanya variasi pada susunan basa DNA suatu organisme. Analisis dilakukan pada DNA atau cdna hasil amplifikasi, kemudian dipotong menggunakan enzim restriksi dan dipisahkan menggunakan elektroforesis gel. Meskipun teknik ini merupakan teknik yang sangat sensitif dan sangat mudah digunakan untuk mengetahui variasi pada sekuen DNA, akan tetapi banyak polimorfisme terjadi akibat adanya perubahan pada satu pasang basa nukleotida, sehingga dibutuhkan enzim restriksi yang secara spesifik mengenali daerah tempat terjadinya perubahan tersebut (Nakashima et al. 2003). Teknik RFLP relatif sederhana, tidak membutuhkan peralatan yang rumit dan mahal, namun dapat digunakan untuk analisis genotyping (Zhang et al. 2005). Enzim restriksi endonuklease yang dapat memutuskan molekul DNA pada daerah yang spesifik digunakan pada suhu dan jumlah tertentu. Daerah pengenalan enzim restriksi umumnya berjumlah 4-6 basa. Semakin pendek daerah yang dikenali maka semakin besar jumlah fragmen yang dihasilkan. Besar kecilnya ukuran fragmen yang dihasilkan dapat dianalisis menggunakan gel elektroforesis (Lodish et al. 2000).
27 27 (a) (Nollau et al.1996) MscI PvuII (Kawada et al. 2008) (b) Gambar 9 Pola pita DNA mutan dan DNA wild type pada analisis mutasi gen KRAS dan EGFR menggunakan metode RFLP. (a) KRAS; (b) EGFR Penggunaan metode RFLP dalam analisis mutasi gen KRAS dan EGFR telah dilakukan oleh Nollau et al. (1996) dan Kawada et al. (2008). Analisis mutasi gen KRAS dan EGFR menggunakan metode RFLP secara jelas dapat membedakan DNA mutan dengan DNA Wild type (Gambar 9). Enzim BstN 1 memotong susunan basa 5 -CC WGG-3 (W= A atau T) pada kodon 12, sedangkan enzim BglI memiliki situs pemotongan 5 -GCCNNNN NGGC-3 (N= A, T, G, atau C). Mutasi gen KRAS kodon 12 dapat diketahui dengan adanya pita tunggal berukuran sekitar 157 pb setelah dipotong menggunakan enzim BstNI dan mutasi kodon 13 ditunjukkan dengan adanya pita berukuran sekitar 157 pb setelah dipotong menggunakan enzim BglI. Kedua jenis enzim tersebut memotong DNA yang tidak mengalami mutasi wild type (Nollau et al. 1996). Analisis mutasi gen EGFR ekson 21 dapat dibedakan pada dua kodon yaitu 858 dan 861. Mutasi titik L858R ditunjukkan dengan adanya pita tunggal berukuran sekitar 348 pb setelah dipotong menggunakan enzim MscI, dan mutasi titik L861Q ditunjukkan dengan adanya dua pita berukuran sekitar 200 pb dan 148 pb setelah dipotong menggunakan enzim PvuII. Enzim MscI memotong daerah 5 -TGG CCA-3 pada exon 21 kodon 858 dan enzim PvuII memotong daerah 5 - CAG CTG-3 pada ekson 21 kodon 861. Analisis mutasi EGFR ekson 19 tidak
28 28 membutuhkan proses restriksi. Profil hasil elektroforesis produk amplifikasi menunjukkan adanya dua pita berukuran sekitar 254 dan 239 pb. Pita 254 pb merupakan sekuen DNA Wild type dan pita 239 pb merupakan pita sekuen DNA mutan. Delesi yang terjadi pada mutan ekson 19 menyebabkan kehilangan 15 pasang basa pada DNA wild type, sehingga ukuran sekuen hasil amplifikasi menjadi lebih pendek (Kawada et al. 2008).
29 29 METODOLOGI Waktu dan Tempat Penelitian Penelitian ini dilakukan mulai Bulan September 2011 sampai dengan Bulan September 2012 di Laboratorium Kalbe Genomic, Stem cell and Cancer Institute (SCI), PT Kalbe Farma, Tbk. Jakarta. Bahan Sel kultur yang digunakan sebagai kontrol adalah sel HCT-116 (Human Colon Tumour), BT-549 (Human Breast Carcinoma), dan A-549 (Human Lung Carcinoma), yang diperoleh dari koleksi sel kultur Laboratorium Kalbe Genomic, SCI. DNA standar EGFR ekson 21 diperoleh dari IDT DNA (Iowa, USA) yang telah memiliki sertifikat kemurnian dan ketepatan susunan basa yang teruji. Sampel cairan pleura pasien kanker paru diperoleh dari Departemen Pulmonologi dan Respirasi FKUI/SMF Paru Rumah Sakit Persahabatan Jakarta melalui prosedur dan etika pengambilan sampel yang telah disetujui Komisi Etika Penelitian Kesehatan Fakultas Kedokteran Universitas Indonesia (Lampiran 1). Sampel yang diperoleh dalam bentuk kertas saring. Koleksi sampel cairan pleura dan pengeringan pada kertas saring dilakukan oleh dokter ahli dan secara selektif dipilih dari pasien kanker paru, bukan dari penderita penyakit Tuberkulosis atau infeksi lainnya. Prosedur Kerja 1) Pengembangan metode HRM dan RFLP untuk mengenali mutasi gen KRAS dan EGFR pada DNA standar Dalam tahapan ini dilakukan penentuan pola grafik standar DNA wild type dan DNA mutan pada hasil analisis HRM dan pola pita hasil pemotongan enzim pada analisis metode RFLP. DNA yang digunakan sebagai DNA cetakan diperoleh dari DNA sel kultur standar yang diketahui memiliki mutasi gen KRAS dan sekuen DNA yang memiliki mutasi gen EGFR. Analisis PCR-HRM KRAS dan EGFR Analisis HRM dilakukan menggunakan alat Real Time-PCR Rotor-Gene 6000 TM (Corbett Research, Sydney, Australia). Analisis PCR-HRM KRAS dilakukan sesuai dengan metode yang telah dilakukan Krypuy et al. (2006). Reagen PCR terdiri atas: 1x PCR buffer, 2,5 mm MgCl 2, 200 nm primer, 200 µm dntps, 5µM SYTO9, 0,5 U Enzim Taq Polymerase dan air PCR grade hingga volume 20 µl. Kondisi PCR yang digunakan adalah prapcr pada suhu 95 0 C selama 15 menit, 40 siklus PCR dengan tahapan denaturasi pada suhu 95 0 C selama 15 detik, annealing pada suhu 67,5 0 C selama 15 detik, polimerisasi pada suhu72 0 C selama 15 detik dan satu siklus post-pcr pada suhu 95 0 C selama 1 detik, dilanjutkan dengan melting DNA (HRM) pada suhu C dengan kecepatan kenaikan temperatur sebesar 0,2 0 C/detik.
30 30 Analisis PCR-HRM EGFR dilakukan menurut Hongdo et al. (2008). Reagen PCR terdiri atas: 1x PCR buffer, 2,5 nm MgCl 2, nm primer, 200 µm dntps, 5µM SYTO9, 0,5 U enzim Taq Polymerase dan air PCR grade hingga volume 20 µl. Kondisi PCR yang digunakan adalah pra-pcr pada suhu 95 0 C selama 15 menit, 50 siklus PCR dengan tahapan denaturasi pada suhu 95 0 C selama 10 detik, annealing pada suhu 65 0 C selama 10 detik, dan polimerisasi pada suhu 72 0 C selama 30 detik, dan post-pcr pada suhu 97 0 C selama 1 detik, dilanjutkan dengan melting DNA pada suhu C dengan kecepatan kenaikan temperatur sebesar 0,2 0 C/detik. Analisis RFLP KRAS kodon 12 dan 13 Produk PCR gen KRAS diperoleh melalui 2 kali proses PCR, first PCR dan nested PCR. Mix PCR terdiri atas 500 nm primer, 1 x PCR buffer+mgcl 2, 200 nm dntp, 1,25 U enzim TaqPolymerase, H 2 O dan DNA cetakan. Kondisi PCR yang digunakan adalah 1 siklus pra-pcr pada suhu 95 0 C selama 5 menit, siklus PCR dengan tahapan denaturasi pada suhu 95 0 C selama 1 menit, annealing pada suhu C selama 1 menit, dan polimerisasi pada suhu 72 0 C selama 2 menit, dan satu siklus post-pcr pada suhu 72 0 C selama 2 menit. Untuk suhu penempelan primer pada first PCR KRAS kodon 13 dilakukan pada suhu 63 0 C selama 1 menit. Suhu annealing PCR KRAS 12 dan 13 dilakukan secara gradien pada suhu C. First PCR dilakukan selama siklus dan nested PCR dilakukan selama siklus. Analisis RFLP produk PCR KRAS kodon 12 menggunakan produk PCR sebanyak 15 µl yang dipotong dengan 20 U enzim BstNI. Analisis RFLP hasil nested PCR KRAS kodon 13 menggunakan produk PCR sebanyak 15 µl yang dipotong dengan 20 U enzim Bgl I. Hasil RFLP dimigrasikan dengan elektroforesis pada gel agarosa dengan konsentrasi agarosa 2,5%. Elektroforesis dilakukan selama 60 menit pada tegangan 100 volt. Gel diwarnai dengan 0,5 µg/ml EtBr dan dilihat pita yang terbentuk menggunkan transiluminator UV. Analisis RFLP EGFR ekson 21 Produk PCR gen EGFR ekson 21 diperoleh melalui 2 kali proses PCR, first PCR dan nested PCR menurut prosedur Kawada et al. (2008). Larutan mix PCR terdiri atas 0,2 µm primer, 1 x PCR buffer+mgcl 2, 0,2 µm dntp, 0,5 U enzim taq polymerase, H 2 O dan DNA cetakan. Kondisi PCR yang digunakan adalah 1 siklus pra-pcr pada suhu 95 0 C selama 15 menit, siklus PCR dengan tahapan denaturasi pada suhu 95 0 C selama 30 detik, annealing pada suhu 63 0 C selama 30 detik, polimerisasi pada suhu 72 0 C selama 1 menit, dan satu siklus post-pcr pada suhu 72 0 C selama 3 menit. First PCR dan nested PCR masingmasing dilakukan selama siklus. Analisis RFLP produk PCR EGFR ekson 21 kodon L858R menggunakan produk PCR sebanyak 10 µl yang dipotong dengan 5 U enzim MscI. Analisis RFLP produk PCR EGFR ekson 21 kodon L861Q menggunakan produk PCR sebanyak 10 µl yang dipotong dengan 10 U enzim PvuII. Hasil RFLP dimigrasikan dengan elektroforesis pada gel agarosa dengan konsentrasi agarosa 2,5%. Elektroforesis dilakukan selama 60 menit pada tegangan 100 volt. Gel diwarnai dengan 0,5 µg/ml EtBr dan dilihat pita yang terbentuk menggunkan transiluminator UV.
31 31 2) Uji sensitivitas Metode HRM dan RFLP Uji sensitivitas dilakukan untuk mengetahui jumlah minimum sel kanker pada sampel sehingga analisis mutasi gen menghasilkan data yang akurat. Dalam hal ini digunakan perbandingan komposisi DNA yang diisolasi dari sel kultur yang sudah diketahui merupakan sel yang mengalami mutasi gen dengan DNA dari sel yang tidak mengalami mutasi/wild type. Uji sensitivitas metode HRM dan RFLP dalam analisis mutasi gen KRAS dilakukan dengan mencampurkan DNA kultur sel HCT116 (kontrol mutan heterozigot) dengan DNA kultur sel BT549 (kontrol wild type) dan DNA kultur sel A549 (kontrol mutan homozigot) dengan DNA kultur sel BT (kontrol wild type). DNA yang digunakan memiliki konsentrasi 25 ng/µl dengan perbandingan konsentrasi DNA sel mutan dan DNA sel wild type sebesar 100%:0%, 50%:50%, 25%:75%, 12,5%:87,5%, 6,25%:93,75%, 3,125%:96,875%, dan 0%:100%. Uji sensitivitas metode HRM dan RFLP dalam analisis muatsi gen EGFR dilakukan dengan mencampurkan sekuen DNA yang memiliki mutasi titik L858R pada ekson 21 dengan sekuen DNA yang tidak memiliki mutasi (kontrol wild type). DNA yang digunakan memiliki konsentrasi 1 ng/µl dengan perbandingan komposisi DNA mutan dan DNA wild type sebesar 100%:0%, 50%:50%, 25%:75%, 12,5%:87,5%, 6,25%:93,75%, 3,125%:96,875%, dan 0%:100%. 3) Isolasi DNA dari Cairan Pleura pada Kertas Saring Kertas saring yang mengandung cairan pleura kering dipotong dengan ukuran 0,5 cm x 0,5 cm. Isolasi DNA dilakukan dengan menggunakan reagen High Pure PCR Template Isolation Kit (Rosche). Prosedur isolasi DNA dilakukan sesuai dengan protokol yang terdapat pada manual instruction kit, kemudian disimpan pada suhu C sebelum digunakan. DNA yang telah diisolasi ditentukan konsentrasinya menggunakan alat nanodrop. 4) Analisis mutasi gen KRAS dan EGFR pada sampel kertas saring yang mengandung cairan pleura DNA hasil isolasi dari kertas saring sebanyak 1 µl kemudian dijadikan sebagai DNA cetakan pada proses analisis menggunakan metode PCR-HRM dan RFLP sesuai dengan prosedur yang telah dilakukan pada pada analisis DNA standar. 5) Analisis Data Hasil analisa profil HRM dan RFLP gen KRAS dan EGFR sampel dibandingkan dengan profil DNA standar wild type dan DNA standar mutan sehingga dapat diketahui jenis profil gen sampel apakah termasuk wild type atau mutan. Penentuan prevalensi mutasi gen EGFR dan KRAS dilihat berdasarkan presentasi jumlah sampel yang menunjukkan profil mutan.
32 Normalized minus wild type Normalized Fluorescen 32 HASIL DAN PEMBAHASAN Analisis Mutasi Gen KRAS Menggunakan Metode HRM dan RFLP pada DNA Standar Sel Kultur Analisis mutasi gen KRAS menggunakan metode HRM telah dilakukan terhadap DNA standar untuk mengetahui bentuk standar kurva DNA yang tidak mengalami mutasi/wild type dan DNA mutan. DNA wild type diisolasi dari sel kultur BT549 (Breast Tumor), DNA standar mutan diperoleh dari sel kultur A549 (Human Lung Carcinoma) yang diketahui memiliki mutasi homozigot pada kodon 12 (GGT>AGT), dan sel kultur HCT 116 (Human Colon Tumor) yang diketahui memiliki mutasi heterozigot pada kodon 13 (GGC>GAC) (Krypuy et al. 2006) Temperatur ( 0 C) (a) Temperatur ( 0 C) (b) Gambar 10 Hasil analisis mutasi gen KRAS DNA standar menggunakan metode HRM. Ket (a) normalized graph dan (b) differential graph BT549: Kontrol wild type A549: Kontrol mutan homozigot kodon 12 HCT116: Kontrol mutan heterozigot kodon 13 Hasil analisis HRM DNA standar menunjukkan perbedaan bentuk kurva DNA wild type dan DNA mutan dalam bentuk normalized graph (Gambar 10a) dan differential graph (Gambar 10b). Bentuk kurva yang diperoleh pada analisis HRM menurut (Reed et al. 2007) berasal dari kurva penurunan intensitas fluoresen yang terjadi seiring dengan kenaikan suhu, akibat adanya perubahan dari bentuk DNA utas ganda menjadi DNA utas tunggal. Nilai fluoresen dalam kurva
33 33 tersebut kemudian dinormalisasi dalam skala menjadi bentuk kurva normalized graph. Krypuy et al. (2006) menggunakan kurva differential graph untuk menunjukkan perbedaan bentuk kurva yang lebih jelas antara DNA yang mengalami mutasi dengan DNA wild type. Kurva differential graph diperoleh dengan cara menjadikan kurva standar wild type sebagai kurva acuan yang bernilai 0. Nilai kurva standar mutan diperoleh dari hasil pengurangan nilai-nilai normalized fluorescence yang diperoleh terhadap normalized fluorescence kurva standar DNA wild type. Transformasi nilai fluoresen menjadi bentuk normalized graph dan differential graph dilakukan secara terintegrasi di dalam software HRM, sehingga bisa diperoleh data secara langsung dalam bentuk grafik. Untuk memudahkan interpretasi hasil analisis HRM selanjutnya hanya digunakan bentuk kurva differential graph. Analisis HRM gen KRAS dilakukan terhadap produk hasil amplifikasi yang memiliki ukuran sekitar 92 pb. Ukuran panjang basa ini dipilih sesuai dengan hasil penelitian Krypuy et al. (2006) yang telah melakukan analisa HRM terhadap gen KRAS dengan menggunakan produk PCR sebesar 189 pb dan 92 pb. Hasil analisis HRM yang terbaik dengan tingkat sensitivitas data yang lebih tinggi diperoleh pada produk PCR dengan ukuran 92 pb. Hal ini diduga karena adanya perbedaan jumlah basa Guanin dan Sitosin pada kedua produk PCR tersebut. Produk PCR yang memiliki ukuran yang lebih besar, memiliki jumlah basa Guanin dan Sitosin yang lebih banyak, sehingga menyebabkan tingginya energi yang dibutuhkan untuk merubah DNA utas ganda menjadi utas tunggal akibat banyaknya ikatan rangkap tiga yang dimilikinya. Hal ini didukung pula oleh Liew et al. (2004) yang menyatakan bahwa analisis genotyping untuk melihat perbedaan pola mutasi akibat terjadinya perubahan satu basa menggunakan metode HRM diperoleh dengan menggunakan produk PCR yang berukuran kecil. Namun demikian, ukuran amplikon untuk mendapatkan bentuk kurva yang optimal sebaiknya diperoleh berdasarkan hasil optimasi. Hasil analisis mutasi gen KRAS menggunakan metode RFLP pada DNA standar menunjukkan perbedaan pita yang jelas (Gambar 11). Hasil analisis mutasi kodon 12 (Gambar 11a) menunjukkan bahwa DNA mutan kodon 12 (A549) memiliki ukuran sekitar 157 pb, sedangkan DNA wild type BT549 dan DNA mutan kodon 13 memiliki ukuran sekitar 128 pb. Hasil analisis mutasi kodon 13 (Gambar 11b) menunjukkan bahwa DNA mutan kodon 13 (HCT116) memiliki ukuran sekitar 157 pb, sedangkan DNA wild type BT549 memiliki ukuran sekitar 125 pb dan DNA mutan kodon 12 memiliki ukuran yang beragam pb 500 pb M A549 BT HCT 3000 pb 1000 pb 500 pb M A549 BT HCT 200 pb 100 pb Mutan Wild type 200 pb 100 pb Mutan Wild type (a) (b) Gambar 11 Hasil analisis mutasi gen KRAS menggunakan metode RFLP. (a) kodon 12; (b) kodon 13
34 Normalized minus wild type normalized minus wild type 34 Analisis RFLP gen KRAS kodon 12 dan 13 menggunakan enzim yang memiliki daerah pemotongan pada DNA wild type, sehingga DNA yang mengalami mutasi tidak terpotong. Analisis RFLP pada kodon 13 menggunakan primer forward yang dimodifikasi agar terjadi perubahan basa pada kodon 10 dan 11 (GGA GCA > GGC CCA) sehingga diperoleh sekuen yang dikenali oleh enzim restriksi BglI pada tipe wild type (Kimura et al. 2007). DNA yang mengalami mutasi pada kodon 13 tidak akan terpotong oleh enzim tersebut, sedangkan DNA yang mengalami mutasi pada kodon 12 terpotong pada beberapa titik oleh enzim BglI, sehingga menghasilkan beberapa pita pada hasil analisis gel elektroforesis. Uji Sensitivitas Metode HRM dan RFLP dalam Analisis Mutasi Gen KRAS Hasil uji sensitivitas metode HRM terhadap analisis mutasi gen KRAS pada kodon 12 dan 13 (Gambar 12) menunjukkan bahwa pada komposisi DNA mutan sebesar 6,25% kurva DNA mutan sudah mendekati garis kurva wild type. Sehingga batas sensitivitas yang menunjukkan kurva DNA mutan yang masih dapat diamati dengan jelas diperoleh pada konsentrasi DNA mutan sebesar 12,5% Temperatur ( 0 C) 100% mutan 50% mutan 25% mutan 12,5% mutan 6,25% mutan 3,125% mutan 1,625% mutan 0% mutan (a) Temperatur ( 0 C) 100% mutan 50% mutan 25% mutan 12,5% mutan 6,25% mutan 3,125% mutan 1,625% mutan 0% mutan (b) Gambar 12 Hasil uji sensitivitas analisis mutasi gen KRAS menggunakan metode HRM. (a) kodon 12; (b) kodon 13.
35 35 Hasi uji sensitivitas mutasi gen KRAS kodon 12 menunjukkan bahwa pada konsentrasi 100% DNA mutan nampak secara jelas kurva yang terbentuk mencapai suhu melting DNA optimum sekitar 82 0 C. Ketika komposisi DNA mutan diturunkan dengan penambahan DNA wild type sebesar 50%, kurva melting DNA bergeser ke sebelah kiri yang mirip dengan jenis mutasi heterozigot pada analisis mutasi gen KRAS kodon 13. Hal ini menunjukkan bahwa dalam analisis mutasi gen menggunakan metode HRM keberadaan DNA wild type akan membentuk pola hasil analisa seperti bentuk mutasi jenis heterozigot. Oleh karena itu, hasil analisis HRM hanya dapat menunjukkan kemungkinan terjadinya variasi/mutasi pada sekuen DNA, tanpa diketahui letak terjadinya mutasi. Metode lain yang digunakan untuk mengetahui terjadinya mutasi umumnya adalah metode RFLP dan sekuensing DNA. Hasil uji sensitivitas teknik RFLP menunjukkan bahwa terdapat perbedaan pita yang jelas antara DNA mutan dan DNA wild type. Hasil analisis gel elektroforesis pada produk pemotongan menggunakan enzim restriksi menunjukkan bahwa adanya perbedaan antara pita DNA mutan dan DNA wild type masih nampak jelas pada komposisi DNA mutan sebesar 3,125%. Pita DNA yang tipis dan cenderung tidak jelas nampak pada komposisi DNA mutan dibawah 3,125% (Gambar 13). Dengan demikian, dapat diketahui bahwa komposisi DNA mutan minimal yang terdapat dalam sampel sebesar 3,125%. 300 pb 200 pb A B C D E F G H 100 pb (a) 300 pb 200 pb 100 pb A B C D E F G H (b) Gambar 13 Hasil uji sensitivitas metode RFLP dalam analisis mutasi gen KRAS. (a) kodon 12 dan (b) kodon 13. Ket A= 100% mutan, B= 50%:50%, C= 25%:75%, D= 12,5%:87,5%, E= 6,25%:93,75%, F= 3,125%: 96,875%, G= 1,625%: 98,375% dan H= 100% wild type.
36 Normalized minus normal Normalized minus normal 36 Analisis Mutasi Gen EGFR menggunakan Metode HRM dan RFLP pada DNA Standar Analisis mutasi gen EGFR dilakukan terhadap ekson 19 dan ekson 21. Mutasi ekson 19 terjadi akibat adanya delesi pada posisi kodon 746 sampai kodon 752. Jumlah kodon yang mengalami mutasi bervariasi pada setiap sampel, sehingga ukuran panjang basa pada produk amplifikasi akan bervariasi (Kawada et al. 2008). Analisis HRM EGFR exon 19 menghasilkan data perbedaan pola kurva yang nampak jelas antara DNA mutan dengan DNA wild type (Gambar 14a). Bentuk kurva DNA mutan menunjukkan adanya satu puncak dan satu lembah, sebagai akibat dari keberadaan alel mutan yang mempengaruhi produk hasil amplifikasi Temperatur ( 0 C) (a) Temperatur ( 0 C) 0 86,5 87,5 88,5 89,5 (b) Gambar 14 Hasil analisis mutasi gen EGFR menggunakan metode HRM. (a) ekson 19 dan (b) ekson 21 HCT116: DNA standar wild type 55b : DNA standar mutan ekson 19 DNA standar 100% mutan ekson 21 L858R DNA standar 50% mutan ekson 21 L858R Mutasi yang terjadi pada ekson 21 adalah susbtitusi satu pasang basa. Perubahan jenis basa pada sekuen DNA wild type menyebabkan terjadinya pergeseran kurva yang dihasilkan sesuai dengan jenis perubahan basa. DNA standar mutan yang digunakan memiliki mutasi kodon 858 T>G, sehingga akan menghasilkan melting DNA pada suhu yang lebih besar dibandingkan dengan
37 37 DNA wild type (Gambar 14b). Kurva yang muncul pada DNA mutan 100% berbentuk satu puncak, sedangkan pada DNA mutan yang dicampur dengan 50% DNA wild type nampak terdapat kurva yang berbentuk satu lembah dan satu puncak. Hal ini terjadi karena pada DNA standar 100% mutan produk PCR yang terbentuk adalah 100% DNA yang mengalami mutasi, sedangkan pada komposisi DNA mutan 50% terdapat DNA wild type ikut teramplifikasi dan memepengaruhi kurva yang terbentuk. Hasil analisis RFLP gen EGFR ekson 21 menunjukkan adanya pola yang jelas antara DNA mutan dengan DNA wild type. Mutasi kodon 858 ditandai dengan adanya pita yang berukuran sekitar 348 pb (Gambar 15b), sedangkan mutasi pada kodon 861 ditandai dengan adanya dua pita berukuran sekitar 200 pb dan 148 pb (Gambar 15c). Hasil ini sesuai dengan penelitian Kawada, et al. (2008). WT Mu M WT Mu M 3000 pb WT Mu M 3000 pb 1000 pb 1000 pb 1000 pb 500 pb 500 pb 500 pb 300 pb 200 pb 300 pb 200 pb 300 pb 200 pb 100 pb 100 pb 100 pb (a) (b) (c) Gambar 15 Hasil analisis mutasi gen EGFR menggunakan metode RFLP. (a) ekson 19, (b) ekson 21 kodon 858 dan (c) ekson 21 kodon 861. Ket: WT = wild type, Mu = mutan, M = marker Analisis RFLP untuk mengetahui mutasi pada ekson 19 tidak dilakukan karena analisis elektroforesis gel terhadap produk hasil amplifikasi menghasilkan dua pita yang berukuran sekitar 254 pb dan 239 pb (Gambar 15a), sehingga DNA wild type dan DNA yang mengalami mutasi dapat dibedakan dengan jelas. Menurut Kawada et al. (2008) delesi yang terjadi pada gen EGFR ekson 19 dapat bervariasi sesuai dengan jumlah basa yang hilang, sehingga ukuran dua pita yang terbentuk akan bervariasi. Uji Sensitivitas Metode HRM dan RFLP dalam Analisis Mutasi Gen EGFR Hasil uji sensitivitas analisis mutasi gen EGFR menunjukkan bahwa pada komposisi DNA mutan sebesar 6,25%, bentuk kurva yang dihasilkan sudah mendekati bentuk kurva DNA wild type. Bentuk kurva DNA mutan yang masih dapat jelas berbeda dengan DNA wild type diperoleh pada komposisi DNA mutan sebesar 12,5%, sehingga batas sensitivitas metode HRM dalam analisis mutasi gen EGFR adalah 12,5% DNA mutan (Gambar 16). Bentuk kurva pada DNA
38 Normalized minuw wild type 38 cetakan yang memiliki komposisi 100% DNA mutan berupa satu puncak dominan yang berbeda dengan DNA wild type. Bentuk kurva yang muncul ketika komposisi DNA mutan dikombinasikan dengan DNA wild type berubah menjadi berbentuk satu lembah dan satu puncak yang sama dengan bentuk hasil HRM exon ,5 87,5 88,5 89, Temperatur ( 0 C) 100% mutan 50% mutan 25% mutan 12,50% mutan 6,25% mutan 3,125% mutan 1,625% mutan 0% mutan Gambar 16 Hasil uji sensitivitas analisis mutasi gen EGFR menggunakan metode HRM. Hasil uji sensitivitas teknik RFLP terhadap produk nested PCR exon 21 menggunakan enzim MscI menunjukkan adanya perbedaan pita yang jelas antara DNA mutan dan DNA wild type (Gambar 17). Pita DNA dengan komposisi 3,125% mutan masih menunjukkan pita berukuran sekitar 348 pb yang merupakan penanda adanya mutasi. DNA yang memiliki komposisi DNA mutan lebih rendah dari 3,125% DNA mutan sudah tidak menghasilkan pita yang berukuran sekitar 348 pb. Dengan demikian, batas sensitivitas metode RFLP dalam menganalisis mutasi gen EGFR adalah 3,125% DNA mutan. A B C D E F G H M A B C D E F G H M 500 pb 300 pb 200 pb 100 pb A B C D E F G H Mutan Wild type Gambar 17 Hasil uji sensitivitas metode RFLP pada analisis mutasi gen EGFR. Ket: perbandingan DNA mutan dengan DNA wild type A= 100% mutan, B= 50%:50%, C= 25%:75%, D= 12,5%:87,5%, E= 6,25%: 93,75%, F= 3,125%:96,875%, dan H= 100% wild type. M= DNA marker. Hasil uji sensitivitas metode HRM dan RFLP terhadap gen KRAS dan EGFR menunjukkan nilai sensitivitas yang sama. Metode HRM memiliki nilai
39 39 sensitivitas sebesar 12,5% dan metode RFLP memiliki nilai sensitivitas sebesar 3,125%. Batas sensitivitas kedua metode ini lebih tinggi dibandingkan dengan metode DNA sekuensing. DNA sekuensing membutuhkan minimal 30% DNA mutan di dalam sampel agar dapat menghasilkan data analisis yang jelas (Bosari et al. 1995). Metode HRM dan RFLP dapat digunakan sebagai metode alternatif yang lebih sensitif untuk menganalisis mutasi gen pada sampel yang memiliki banyak pengotor dari DNA wild type, DNA sel normal dan serat jaringan sel. Isolasi DNA dari Sampel yang Disimpan dalam Kertas Saring Hasil isolasi DNA dari setiap sampel kertas saring menunjukkan variasi yang sangat beragam (Lampiran 1). Konsentrasi DNA yang diperoleh berkisar antara 5,7 ng/µl - 369,2 ng/µl. Konsentrasi ini relatif sedikit, namun cukup untuk digunakan sebagai DNA cetakan dalam proses PCR. Semua sampel kertas saring menghasilkan DNA yang dapat diamplifikasi dengan primer gen KRAS dan gen EGFR sehingga dapat diketahui termasuk jenis mutan atau wild type. Menurut Hong Do et al. (2008) jumlah sampel DNA yang diperlukan sebagai DNA cetakan untuk terjadinya amplifikasi menggunakan metode HRM tidak harus besar. Konsentrasi DNA sebesar 1 ng/µl masih dapat menghasilkan pola analisis HRM yang masih bisa terbaca dengan baik. Hal ini didukung pula oleh hasil penelitian Pang et al. (2012) yang menyatakan bahwa kuantitas DNA tidak memiliki pengaruh yang signifikan terhadap hasil analisis genotyping. Hasil penelitian ini membuktikan bahwa kertas saring dapat dijadikan sebagai media penyimpanan sementara sampel cairan pleura sebelum digunakan dalam analisis molekuler. Analisis HRM dan RFLP Cairan Pleura Pasien Kanker Paru yang Disimpan dalam Kertas Saring Analisis mutasi gen KRAS Hasil analisis mutasi gen KRAS terhadap 63 sampel pasien kanker paru menunjukkan hasil yang cukup signifikan. Satu pasien mengalami mutasi pada kodon 12. Sebanyak 62 sampel lainnya memiliki profil mutasi gen KRAS wild type. Mutasi gen KRAS pada kodon 13 tidak ditemukan. Hasil analisis ini diperoleh berdasarkan kemiripan bentuk kurva pada DNA sampel dengan bentuk kurva DNA standar pada analisis HRM dan keberadaan pita penanda adanya mutasi pada analisis RFLP. Hasil analisis HRM menunjukkan terdapat kemiripan bentuk kurva pada pasien P07 dengan bentuk kurva standar mutan (Gambar 18). Bentuk kurva P07 memiliki pola yang sama dengan kurva DNA sel mutan HCT116. Bentuk kurva ini berbeda dengan beberapa sampel lain seperti sampel P08, P20, P26, P37, dan P46 yang menunjukkan kemiripan dengan DNA wild type. Berdasarkan hasil analisis tersebut dapat disimpulkan bahwa sampel P07 memiliki mutasi gen KRAS kodon 13. Kesimpulan ini belum bisa digunakan, karena analisis HRM hanya bisa digunakan untuk melihat adanya variasi atau mutasi tanpa mengetahui posisi terjadinya mutasi. Kurva yang terbentuk disebabkan adanya perubahan satu pasang basa pada untai DNA P07 yang mirip dengan DNA mutan (Wittwer 2009).
40 Normalized minus wild type A BT -4 HCT -6 P07-8 P08-10 P20-12 P26-14 P37-16 Temperatur ( 0 C) P46 Gambar 18 Grafik analisis mutasi gen KRAS pada sampel pasien kanker paru Analisis letak terjadinya mutasi gen KRAS pada kodon 12 atau 13 lebih lanjut diketahui berdasarkan data RFLP. Hasil pemotongan amplikon gen KRAS sampel menggunakan enzim BstNI menunjukkan bahwa pada sampel P07 terdapat pita tunggal berukuran sekitar 157 pb, sama seperti DNA standar sel A549 yang memiliki mutasi pada gen KRAS kodon 12 (Gambar 19a). Hasil pemotongan dengan menggunakan enzim BglI menunjukkan tidak ada sampel yang menghasilkan pita berukuran sekitar 157 pb seperti DNA sel HCT116 yang memiliki mutasi pada gen KRAS kodon 13 (Gambar 19b). Dengan demikian dapat diketahui bahwa sampel P07 memiliki mutasi gen KRAS pada kodon pb 500 pb M A549 BT HCT P07 P08 P20 P26 P37 P pb 200 pb 100 pb Mutan Wild type 3000 pb (a) M A549 BT HCT P07 P08 P20 P26 P37 P pb 500 pb 300 pb 200 pb 100 pb Mutan Wild type (b) Gambar 19 Hasil analisis mutasi gen KRAS sampel pasien kanker paru menggunakan metode RFLP. (a) pemotongan amplikon dengan enzim BstN1; (b) pemotongan amplikon dengan enzim BglI.
41 Normalized minus wild type 41 Analisis mutasi gen EGFR Hasil analisis mutasi gen EGFR terhadap 63 sampel pasien kanker paru menunjukkan sebanyak lima sampel mengalami mutasi pada ekson 19 yaitu sampel P16, P18, P19, P42 dan P52, dan sebanyak lima sampel yaitu sampel P13, P37, P43, P48, dan P53 mengalami mutasi pada ekson 21 kodon 858. Mutasi gen EGFR ekson 21 pada kodon 13 tidak ditemukan. Sebanyak 53 sampel lainnya memiliki profil gen EGFR wild type (Lampiran 2). Hasil analisis HRM mutasi EGFR ekson 19 menunjukkan adanya kemiripan bentuk kurva DNA sampel yang mengalami mutasi dengan bentuk kurva DNA standar mutan yang dapat diamati dengan jelas (Gambar 20). Sampel yang mengalami mutasi memiliki bentuk kurva yang sama dengan bentuk kurva DNA standar mutan (55b), sedangkan pada sampel yang wild type selain bentuk kurva tidak menunjukkan satu lembah dan satu puncak seperti bentuk kurva DNA standar mutan, letak kurva juga hampir mendekati DNA standar wild type Temperatur ( 0 C) HCT 55b P16 P42 P10 P38 P58 Gambar 20 Grafik analisis mutasi gen EGFR ekson 19 pada sampel pasien kanker paru. Hasil analisis mutasi gen EGFR ekson 21 menggunakan metode HRM menunjukkan adanya kemiripan bentuk kurva DNA sampel yang mengalami mutasi dengan bentuk kurva DNA standar mutan (Gambar 21). Sampel yang mengalami mutasi memiliki bentuk kurva yang mirip dengan kurva DNA standar mutan dan sampel yang wild type memiliki bentuk kurva yang mirip DNA standar wild type serta letaknya hampir berimpitan. DNA standar mutan yang digunakan adalah DNA sintetik dengan konsentrasi 50% mutan (M50) dan sampel sitologi pleura (515) yang telah diketahui memiliki mutasi pada kodon 858 berdasarkan hasil sekuensing.
42 Normalized minus wild type ,5 87,5 88,5 89, Temperatur ( 0 C) HCT Gambar 21 Grafik analisis mutasi gen EGFR ekson 21 pada sampel pasien kanker paru M P13 P37 P43 P53 P pb M HCT P13 P14 P37 P43 P48 P53 P09 P26 P35 P pb 500 pb 200 pb Mutan Wild type 100 pb 3000 pb (a) M HCT P13 P14 P37 P43 P48 P53 P09 P26 P35 P pb 500 pb 200 pb Wild type Mutan (b) Gambar 22 Hasil analisis gel elektroforesis amplikon produk PCR-HRM DNA sampel dalam analisis mutasi gen EGFR ekson 21. (a) pemotongan amplikon menggunakan enzim MscI; (b) pemotongan amplikon menggunakan enzim PvuII Hasil analisis RFLP EGFR ekson 21 menunjukkan bahwa lima sampel DNA pasien memiliki pita berukuran sekitar 348 pb setelah dipotong menggunakan enzim MscI yang menunjukkan adanya mutasi pada ekson 21 kodon 858 (Gambar 22a). Enzim MscI memotong DNA wild type pada kodon 858 (Kawada et al. 2008), sehingga DNA yang mengalami mutasi pada kodon 858 tidak mengalami pemotongan. Mutasi ekson 21 pada kodon 861 tidak ditemukan pada penelitian ini, yang ditunjukkan dengan tidak diperolehnya pita berukuran sekitar 200 pb dan 148 pb pada hasil restriksi menggunakan enzim PvuII seperti
43 43 pada pita standar mutan 140 (Gambar 22b). Enzim PvuII memotong gen yang mengalami mutasi pada daerah kodon 861, gen yang tidak mengalami mutasi tidak terpotong (Kawada et al. 2008). Prevalensi mutasi gen KRAS dan EGFR Berdasarkan hasil analisis menggunakan metode HRM dan RFLP dari 63 pasien kanker paru diketahui satu pasien (1,6%) mengalami mutasi gen KRAS, dan 10 pasien (15,9%) memiliki mutasi gen EGFR, sedangkan 52 pasien (82,5%) menunjukkan profil gen KRAS dan EGFR wild type (Gambar 23). 1,60% 15,90% 82,50% KRAS EGFR Wild type Gambar 23 Prevalensi mutasi gen KRAS dan EGFR pada pasien kanker paru Nilai prevalensi mutasi gen KRAS dan EGFR yang diperoleh menunjukkan nilai yang lebih rendah jika dibandingkan dengan hasil penelitian yang telah dilaporkan. Beberapa hasil penelitian analisis mutasi gen KRAS dan EGFR dengan menggunakan sampel standar (dahak, sitologi pleura dan FFPE) menunjukkan prevalensi mutasi gen KRAS pasien kanker paru sekitar 18% - 33% (Lu et al. 2004; Ramirez et al. 2003; Krypuy et al. 2006), dan prevalensi mutasi gen EGFR sekitar 12% 50% (Cortes-Funes et al. 2005; Huang et al. 2004; Tokumo et al. 2005; Zhang et al. 2005; Han et al. 2005). Di Indonesia data mengenai prevalensi mutasi gen KRAS dan EGFR pada kasus kanker paru belum pernah dilaporkan. Data hasil analisis Laboratorium KalGen (Kalbe Genomic)-SCI PT Kalbe Farma, Tbk (KalGen Lab, 2012) menunjukkan jumlah prevalensi mutasi gen EGFR pasien kanker paru sebesar 28% (46/164). Perbedaan nilai prevalensi mutasi gen sangat ditentukan oleh perbedaan karakteristik faktor genetik pasien di setiap daerah. Beberapa hasil analisis mutasi gen EGFR misalnya, di beberapa daerah menunjukkan nilai yang bervariasi (Tabel 2). Selain itu ras dan keturunan pasien juga mempengaruhi profil mutasi gen pada pasien kanker paru (Tabel 2). Mutasi gen EGFR banyak ditemukan pada pasien yang berasal dari keturunan asia, wanita, tidak memiliki riwayat perokok dan jenis sel kanker adenokarsinoma (Shigematsu et al. 2005; Bell et al. 2005), sedangkan mutasi gen KRAS lebih banyak ditemukan pada pasien yang berasal dari keturunan non-asia dibandingkan dengan pasien asia timur (Lung et al. 1992; Wang et al. 1998), memiliki riwayat perokok, wanita dan jenis sel kanker adenokarsinoma (Graziano et al. 1999).
44 44 Tabel 2 Data prevalensi mutasi gen EGFR pada pasien kanker paru di beberapa negara Penelitian Asal pasien Ras Prevalensi mutasi Huang et al. (2004) Cina Asia 8/16 (50%) Tokumo et al. (2005) Jepang Asia 10/21 (48%) Zhang et al. (2005) Cina Asia 12/30 (40%) Han et al. (2005) Korea Asia 17/90 (19%) Kim et al. (2005) Korea Asia 6/27 (22%) Cortes-Funes et al. (2005) Spanyol Kaukasia 10/83 (12%) Cappuzo et al. (2005) Italia Kaukasia 15/89 (17%) Taron et al. (2005) Jepang, USA, Eropa Asia, kaukasia 17/68 (25%) Jika dilihat berdasarkan jenis kelamin, hasil penelitian ini menunjukkan bahwa prevalensi mutasi gen EGFR ditemukan 21,43% pada pria dan 15,3% pada wanita (Tabel 3). Hasil penelitian ini menunjukkan bahwa mutasi gen EGFR banyak ditemukan pada pasien pria dibandingkan dengan wanita. Hasil ini berbeda dengan hasil penelitian yang telah dilakukan sebelumnya yang menyebutkan bahwa mutasi gen EGFR lebih banyak ditemukan pada pasien wanita. Hal ini menjadi sebuah penemuan yang menarik. Serangkaian penelitian lebih lanjut perlu dilakukan untuk memperoleh data pasti mengenai prevalensi mutasi gen EGFR pada pasien kanker paru Indonesia. Kondisi lingkungan, hormonal, genetik maupun kemungkinan adanya faktor lain yang berpengaruh perlu dianalisis. Tabel 3. Prevalensi mutasi gen EGFR dan KRAS berdasarkan jenis kelamin Jenis kelamin Jumlah Prevalensi Mutasi EGFR Mutasi KRAS Pria 28 6/28 (21,43%) - Wanita 26 4/26 (15,3%) - Tidak diketahui 9-1 Total 63 10/63 (15,9%) 1/63 (1,6%) Sumber sampel sebagai bahan analisis molekuler juga memiliki pengaruh terhadap hasil analisis. Sampel histologi seperti hasil biopsi dan mikrodiseksi menunjukkan akurasi yang lebih tinggi dibandingkan dengan sampel sitologi. Namun demikian, sampel yang berasal dari sitologi lebih banyak dipilih dibandingkan dengan sampel histologi karena pengambilan sampel yang relatif lebih mudah tanpa operasi, dan dapat tersedia dalam jumlah banyak sehingga tidak harus dilakukan pengambilan sampel ulang jika sampel tidak memenuhi standar untuk dilakukan analisa (Pang et al. 2012). Faktor berikutnya yang berpengaruh terhadap data hasil analisis mutasi gen adalah tingkat sensitivitas metode analisis yang dipilih. Beberapa hasil penelitian yang telah dilakukan umumnya menunjukkan data prevalensi mutasi berdasarkan hasil analisis menggunakan metode sekuensing. Pada penelitian ini digunakan metode HRM dan RFLP yang menunjukkan nilai sensitivitas yang tinggi. Kedua metode ini mampu mendeteksi adanya DNA mutan dalam campuran DNA wild
45 45 type dan senyawa lain yang pada umumnya menjadi pengotor di dalam sampel, dalam batasan deteksi 12,5% dan 3,125% DNA mutan. Nilai ini jauh lebih tinggi jika dibandingkan dengan metode sekuensing yang memiliki batasan deteksi 30% DNA mutan. Berdasarkan hal tersebut, aplikasi metode HRM dan RFLP ini dapat dilakukan dalam analisis sampel yang berasal dari cairan pleura yang banyak memiliki pengotor. Pada cairan pleura selain sel-sel tumor banyak ditemukan sel leukosit, protein dengan kadar tinggi, glukosa dengan kadar rendah dan DNA sel epitel normal yang turut terbawa (Arbaningsih 2010). Dengan demikian, pemilihan metode HRM dan RFLP bukan menjadi faktor penyebab rendahnya nilai prevalensi mutasi yang diperoleh pada penelitian ini. Hasil penelitian ini menunjukkan bahwa mutasi gen KRAS dan EGFR terjadi pada pasien yang berbeda. Pasien yang menunjukkan hasil analisis mengalami mutasi gen KRAS memiliki profil gen EGFR wild type, demikian pula sebaliknya. Menurut Marchetti et al. (2005) mutasi gen KRAS dan EGFR bersifat mutually exclusive. Kedua jenis mutasi gen ini sangat jarang terjadi secara bersamaan dalam satu pasien. Kasus terjadinya mutasi gen KRAS dan EGFR secara bersamaan dalam satu pasien hanya pernah dilaporkan terdapat pada dua pasien oleh Han et al. (2005). Mutasi gen EGFR umumnya terjadi dalam satu lokasi. Sesuai dengan hasil peneliian tersebut, hasil penelitian ini menunjukkan bahwa mutasi gen EGFR dan KRAS tidak terjadi secara bersamaan pada satu pasien. Demikian pula, mutasi EGFR ekson 19 tidak ditemukan bersamaan dengan mutasi pada ekson 21. Pang et al. (2012) melaporkan bahwa mutasi gen EGFR dapat terjadi pada dua ekson secara bersamaan. Hasil penelitiannya menunjukkan mutasi ganda terjadi sebanyak 2,7% dan umumnya ditemukan bersamaan dengan mutasi pada ekson 18. Hasil penelitian ini terbatas hanya diarahkan untuk mengetahui prevalensi mutasi pada gen EGFR yang difokuskan pada ekson 19 dan 21, analisis lebih lanjut dapat dilakukan untuk mengetahui profil mutasi gen EGFR pada ekson 18, sehingga prevalensi mutasi gen EGFR secara keseluruhan kemungkinan besar bisa bertambah. Analisis mutasi gen EGFR ekson 18 meskipun secara prevalensi jarang ditemukan dibandingkan mutasi pada ekson 19 dan 21 namun banyak dilakukan seiring dengan hasil penelitian yang menunjukkan adanya resistensi obat terapi target gefitinib dan erlotinib pada pasien yang memiliki mutasi gen EGFR ekson 18. Hasil penelitian ini menunjukkan bahwa masih ada 82,5% pasien yang masih belum diketahui profil mutasi gen yang menyebabkan terjadinya kanker. Dengan demikian penelitian lebih lanjut dapat dilakukan dengan melakukan analisis molekuler pasien kanker paru menggunakan jenis biomarker gen lain seperti PIK3CA, RAF, EML4-ALK, dan lain-lain. Potensi Pengembangan Kertas Saring sebagai Media Pengiriman Sampel Pada penelitian ini telah berhasil membuktikan bahwa DNA dapat diisolasi dari kertas saring yang berisi sampel cairan pleura dengan konsentrasi yang beragam mulai dari 5,7 ng/µl hingga 369,2 ng/µl. DNA yang diperoleh dari kertas saring tersebut dapat digunakan sebagai DNA cetakan dalam proses PCR sehingga adanya mutasi gen KRAS dan EGFR dapat dianalisis. Meskipun konsentrasi DNA yang diperoleh dalam jumlah sedikit namun data hasil analisis
46 46 HRM dan RFLP masih dapat diperoleh dengan jelas. Menurut Pang et al. (2012) konsentrasi DNA bukan merupakan syarat utama keberhasilan analisis mutasi gen menggunakan metode berbasis PCR dibandingkan dengan faktor kualitas DNA. Meskipun jumlah DNA yang berhasil diisolasi sedikit namun kualitasnya baik maka teknik tersebut dapat digunakan. Penggunaan kertas saring sebagai media peyimpanan dan pengiriman sampel medis seperti darah, virus dan protein telah banyak dilakukan (Dobbs et al. 2002; Chaisomchit et al. 2005). Chaisomchit et al.(2005) telah melakukan uji kestabilan penyimpanan DNA dalam bentuk kertas saring selama kurun waktu 11 tahun. DNA berhasil diisolasi dari sampel darah yang disimpan dalam kertas saring pada suhu ruang selama kurun waktu 11 tahun. DNA tersebut masih bisa digunakan sebagai DNA cetakan dalam proses PCR. Hasil penelitiannya telah membuktikan bahwa kertas saring dapat digunakan untuk menyimpan sampel darah selama lebih dari 10 tahun. Dobbs et al. (2002) telah menggunakan kertas saring sebagai media penyimpanan dan pengiriman sampel sel tumor hasil operasi. Berdasarkan hasil penelitiannya, kualitas DNA yang diisolasi dari kertas saring memiliki kualitas yang sama dengan DNA yang diisolasi dari sel tumor secara langsung. Metode analisis mutasi gen KRAS dan EGFR menggunakan cairan pleura sebagai sumber sampel umumnya disimpan dalam bentuk bentuk pulasan sitologi (Krypuy et al. 2006; Namoto et al. 2006; Hong Do et al. 2008). Sel tumor yang terdapat dalam cairan pleura terlebih dahulu dilihat menggunakan mikroskop sehingga dalam analisis molekuler dapat dipilih hanya sel-sel tumor yang dijadikan sebagai sumber isolasi DNA sampel. Berbeda halnya dengan sampel yang disimpan dalam kertas saring. DNA yang diisolasi berasal dari DNA bebas yang terdapat dalam cairan dan beberapa sel yang tidak bisa diketahui kanker atau wild type. Jumlah DNA dari sel normal yang terserap dalam kertas saring dalam jumlah yang relatif besar kemungkinan besar dapat menyebabkan hasil analisis negatif data mutasi yang diperoleh. Kertas saring memiliki potensi yang besar untuk diaplikasikan sebagai media penyimpanan sampel yang tahan lama dan menjadi model pengiriman sampel yang efisien jika dibandingkan dengan sampel dalam bentuk cairan. Teknik ini juga lebih sederhana, tidak membutuhkan peralatan khusus. Teknik ini memiliki potensi manfaat lebih besar sebagai media pengiriman sampel dari rumah sakit daerah yang tidak memiliki fasilitas analisis molekuler ke Laboratorium analisis molekuler yang jaraknya cukup jauh, seperti dari rumah sakit daerah di Nusa Tenggara Barat dan Papua ke Laboratorium di Jakarta. Serangkaian penelitian lebih lanjut untuk melakukan validasi dan stadarisasi aplikasi metode penyimpanan sampel cairan pleura dalam kertas saring perlu dilakukan sebelum dapat diaplikasikan secara rutin dalam aplikasi medis.
47 47 SIMPULAN DAN SARAN Simpulan 1. Metode HRM dan RFLP dapat menunjukkan perbedaan pola DNA wild type dan DNA mutan, sehingga kedua metode ini dapat digunakan untuk mengetahui adanya mutasi gen KRAS dan EGFR pada pasien kanker paru. 2. Hasil uji sensitivitas metode HRM dan RFLP berturut-turut menunjukkan persentase minimal DNA mutan yang dapat dianalisis menggunakan metode tersebut adalah sebesar 12,5% dan 3,125%. 3. Analisis terhadap 63 pasien kanker paru menunjukkan bahwa 1 pasien mengalami mutasi gen KRAS dan 10 pasien mengalami mutasi pada gen EGFR 4. Penggunaan kertas saring sebagai media penyimpanan dan pengiriman sampel cairan pleura memiliki peluang yang prospektif. DNA pasien telah berhasil diisolasi dari kertas saring dengan kualitas yang baik, dan dapat digunakan sebagai DNA cetakan dalam proses PCR, sehingga analisis mutasi gen KRAS dan EGFR dapat dilakukan. Saran 1 Perlu dilakukan penelitian lebih lanjut untuk mengetahui pola mutasi gen pada pasien kanker paru dengan menggunakan jenis biomarker yang berbeda dan jumlah sampel pasien yang lebih banyak. 2 Perlu dilakukan uji validasi dan standarisasi penggunaan kertas saring sebagai media penyimpanan dan pengiriman sampel kertas saring sebelum digunakan dalam aplikasi medis secara rutin.
48 48 DAFTAR PUSTAKA [ACS] American Cancer Society Cancer fact and figures. research/cancerfactsfigures/acspc html. [ 2 Okt 2012] [Corbet Research] High resolution melt assay design and analysis CorProtocol Corbet life science. Australia. [KalGen Lab] Kalbe Genomic Laboratory Laporan analisis mutasi gen EGFR pada pasien kanker paru [Unpublished Data] [Kapa Biosystem] Introduction to High Resolution Melting Analysis. Boston, Massachusetts, United States. Adjei AA Blocking oncogenic Ras signaling for cancer therapy. J Natl Cancer Inst 93(14): Arbaningsih SR Sensitivitas dan spesifisitas pemeriksaan CEA cairan pleura dalam diagnosis efusi pleura ganas karena kanker paru [Tesis]. Sumatra Utara: Fakultas Ilmu Kedokteran Universitas Sumatera Utara. Bell DW, Lynch TJ, Haserlat SM, Harris PL, Okimoto RA, Brannigan BW, Sgroi DC, Muir B, Riemenschneider MJ, Iacona RB, et al Epidermal growth factor receptor mutations and gene amplification in non-small-cell lung cancer: molecular analysis of the IDEAL/INTACT gefitinib trials. J Clin Oncol 23: Bos JL Ras oncogenic in human cancer. A Review. Cancer Res Bosari S, Marchetti A, Buttitta F, Graziani D, Borsani G, Loda M, Bevilacqua G, Coggi G Detection of p53 mutations by single-strand conformation polymorphisms (SSCP) gel electrophoresis: a comparative study of radioactive and nonradioactive silver-stained SSCP analysis. Diagn Mol Pathol 4: Burrows CM, Mathews WC, Colt HG Predicting survival in patients with recurrent symptomatic malignant pleural effusions. Chest 104: Cappuzzo F, Hirsch FR, Rossi E, Bartolini S, Ceresoli GL, Bemis L, Haney J, Witta S, Danenberg K, Domenichini I, et al Epidermal growth factor receptor gene and protein and gefitinib sensitivity in non-small-cell lung cancer. J Natl Cancer Inst 97: Carpenter G Receptors for epidermal growth factor and other polypeptide mitogens. Annu Rev Biochem 56: Chaisomchit S, Wichajarn R, Janejai N, Chareonsiriwatana W Stability of genomic DNA in dried blood spots stored on filter paper. Southeast Asian J Trop Med Public Health 36(1): Choi SH, Mendrola JM, Lemmon MA EGF-independent activation of cellsurface EGF receptors harboring mutations found in gefitinib-sensitive lung cancer. Oncogene 26: Cortes-Funes H, Gomez C, Rosell R, Valero P, Garcia-Giron C, Velasco A, Izquierdo A, Diz P, Camps C, Castellanos D, et al Epidermal growth factor receptor activating mutations in Spanish gefitinib-treated non-smallcell lung cancer patients. Ann Oncol 16:
49 Cox AD, Der CJ The dark side of ras: regulation of apoptosis. Oncogene 22: Crystal AS, Alice TS New targets in advanced NSCLC: EML4-ALK. Clin Adv in Hematol & Oncol. Vol 9 issue 3 Dahabreh IJ, Linardou H, Siannis F, Kosmidis P, Bafaloukos D, Murray S Somatic EGFR mutation and gene copy gain as predictive biomarkers for response to tyrosine kinase inhibitors in non-small cell lung cancer. Clin Cancer Res 16(1): Dassonville O, Bozec A, Fischel JL, Milano G EGFR targeting therapies: monoclonal antibodies versus tyrosine kinase inhibitors. Similarities and differences. Crit Rev Oncol Hematol 62(1): Dienstmann R, Pablo M, Enriqueta F Personalizing therapy with targeted agents in Non-Small Cell Lung Cancer. Oncotarget 2: Dobbs LJ, Madigan MN, Carter AB, Earls L Use of FTA gene guard filter paper for the storage and transportation of tumor cells for molecular testing. Arch Pathol Lab Med 126(1):56-63 Goswami A, Ranganathan P, Rangnekar VM The phosphoinositide 3- kinase/akt1/par-4 axis: a cancer-selective therapeutic target. Cancer Res 66: Graziano SL, Gamble GP, Newman NB, Abbott LZ, Rooney M, Mookherjee S, Lamb ML, Kohman LJ, Poiesz BJ Prognostic significance of K-ras codon 12 mutations in patients with resected stage I and II non-small-cell lung cancer. J Clin Oncol 17: Hall BE, Bar-Sagi D, Nassar N The structural basis for the transition from Ras-GTP to Ras-GDP. Proc Natl Acad Sci USA 99(19): Han SW, Kim TY, Hwang PG, Jeong S, Kim J, Choi IS, Oh DY, Kim JH, Kim DW, Chung DH, et al Predictive and prognostic impact of epidermal growth factor receptor mutation in non-small-cell lung cancer patients treated with gefitinib. J of Clin Oncol 23: Heffner JE, Klein JS Recent advances in the diagnosis and management of malignant pleural effusions. Mayo clinic Proc 83(2): Herbst RS, Heymach JV, Lippman SM Lung cancer. N Engl J Med 359(13): Hermann MG, Durtschl JD, Bromley K, Wittwer CT, Voelkerding KV Amplicon DNA melting analysis for mutation scanning and genotyping: crossplatform comparison of instruments and dyes. Clin Chem 52: Hirsch FR, Bunn Jr PA Epidermal growth factor receptor inhibitors in lung cancer: smaller or larger molecules, selected or unselected populations. J Clin Oncol 23(36): Hongdo Do, Michael K, Paul LM, Stephen BF, Alexander D High resolution melting analysis for rapid and sensitive EGFR and KRAS mutation detection in formalin fixed paraffin embedded biopsies. BMC Cancer 8:142. Huang SF, Liu HP, Li LH, Ku YC, Fu YN, Tsai HY, Chen YT, Lin YF, Chang WC, Kuo HP, et al High frequency of epidermal growth factor receptor mutations with complex patterns in non-small cell lung cancers related to gefitinib responsiveness in Taiwan. Clin Cancer Res 10:
50 50 Hudoyo A Mengoptimalkan manajemen kanker paru. Farmacia Karim B, Florence C, Kamel R, Nadia K, Ines O, Raja M, Sarra BJ, Florent S, Amel BA KRAS mutation detection in Tunisian sporadic coloractal cancer patients with direct sequencing, high resolution melting and denaturating high performance liquid chromatography. Cancer Biomark 8(6): Katz M, Amit I, Yarden Y Regulation of MAPKs by growth factors and receptor tyrosine kinases. Biochim Biophys Acta 1773: Kawada I, Soejima K, Watanabe H, Nakachi I, Yasuda H, Naoki K, Kawamura M, Eguchi K, Kobayashi K, Ishizaka A An Alternative Method for Screening EGFR Mutation Using RFLP in Non-small Cell Lung Cancer Patients. J Thorac Oncol. Kim KS, Jeong JY, Kim YC, Na KJ, Kim YH, Ahn SJ, Baek SM, Park CS, Park CM, Kim YI, et al Predictors of the response to gefitinib in refractory non-small cell lung cancer. Clin Cancer Res 11: Kimura, Fujiwara Y, Sone T, Kunitoh H, Tamura T, Kasahara K, Nishio K EGFR mutation status in tumour-derived DNA from pleural effusion fluid is a practical basis for predicting the response to geftinib. Br J Cancer 95: Kimura, Nagasaka T, Hoshizima N, Sasamoto H, Notohara K, Takeda M, Kominami K, Iishii T, Tanaka N, Matsubara N No duplicate KRAS mutation is identified on the same allele in gastric or colorectal cancer cells with multiple KRAS mutations. J Int Med Res 35(4): Krypuy M, Genni MN, David MT, Matthew C, Alexander D High resolution melting analysis for the rapid and sensitive detection of mutations in clinical samples: KRAS codon 12 and 13 mutations in non-small cell lung cancer. BMC cancer 6: 295. Liew M, Pryor R, Palais R, Meadows C, Erali M, Lyon E, Wittwer C Genotyping of single-nucleotide polymorphisms by high-resolution melting of small amplicons. Clin Chem 50(7): Light RW Pleural effusions related to metastatic malignancies. In: Pleural disease. 5th ed. Philadelphia: Lippincott Williams & Wilkins 10: Linardou H, Briasoulis E, Dahabreh IJ, Mountzios G, Papadimitriou C, Papadopoulos S, Bafaloukos D, Kosmidis P, Murray S All about KRAS for clinical oncology practice: Gene profile, clinical implications and laboratory recommendations for somatic mutational testing in colorectal cancer. Cancer Treat Rev 37: Lodish H et al Molecular Cell Biology. Freeman Company. New York Lu C, Soria JC, Tang X, Xu XC, Wang L, Mao L, Lotan R, Kemp B, Bekele BN, Feng L, Hong WK, Khuri FR Prognostic factors in resected stage I non-small-cell lung cancer: a multivariate analysis of six molecular markers. J Clin Oncol 22: Lung ML, Wong M, Lam WK, Lau KS, Kwan S, Fu KH, Cheung H, Yew WW Incidence of ras oncogene activation in lung carcinomas in Hong Kong. Cancer 70: Lynch TJ, Bell DW, Sordella R, Gurubhagavatula S, Okimoto RA, Brannigan BW, Harris PL, Haserlat SM, Supko JG, Haluska FG, et al Activating mutations in the epidermal growth factor receptor underlying
51 responsiveness of non-small-cell lung cancer to gefitinib. N Engl J Med 350: Mao L, Lee JS, Kurie JM, Fan YH, Lippman SM, Lee JJ, Ro JY, Broxson A, Yu R, Morice RC, et al Clonal genetic alterations in the lungs of current and former smokers. J Natl Cancer Inst 89: Marchetti A, Martella C, Felicioni L, Barassi F, Salvatore S, Chella A, Camplese PP, Iarussi T, Mucilli F, Mezzetti A, et al EGFR mutations in nonsmall-cell lung cancer: analysis of a large series of cases and development of a rapid and sensitive method for diagnostic screening with potential implications on pharmacologic treatment. J Clin Oncol 23(4): Mattoon DR, Lamothe B, Lax I, Schlessinger J The docking protein Gab1 is the primary mediator of EGF-stimulated activation of the PI-3K/Akt cell survival pathway. BMC Biol 2:24. Mok TS, Wu YL, Thongprasert S, Yang CH, Chu DT, Saijo N, Sunpaweravong P, Han B, Margono B, Ichinose Y, et al Gefitinib or carboplatinpaclitaxel in pulmonary adenocarcinoma. N Engl J Med 361(10): Molina JR, Adjei AA The Ras/Raf/MAPK pathway. J Thorac Oncol 1:7-9. Monis PT, Steven G, Christopher PS Comparison of SYTO9 and SYBR Green I for real-time polymerase chain reaction and investigation of the efect of dye concentration on amplification and DNA melting curve analysis. Analytical Biochemistry 340:24 34 Mulloy R, Ferrand A, Kim Y, Sordella R, Bell DW, Haber DA, Anderson KS, Settleman J Epidermal growth factor receptor mutants from human lung cancers exhibit enhanced catalytic activity and increased sensitivity to gefitinib. Cancer Res 67: Nakashima H, Mitsuteru A, Yosuke T Mutation detection using RT-PCR- RFLP. Methods in molecular biology 226: Namoto K, Tsuta K, Takano T, Fukui T, Fukui T, Yokozawa K, Sakamoto H, Yoshida T, Maeshima AM, Shibata T, et al Detection of EGFR Mutations in archived cytologic specimens of non small cell lung cancer using high-resolution melting analysis. Clin Lung Cancer, Vol. 7, Suppl. 4, S138-S144. Ngurah Rai, IB Efusi pleura maligna: diagnosis dan penatalaksanaan terkini. J Peny Dalam 10(3). Nollau P, Carsten M, Gunter W, Cristoph W Detection of K-Ras mutations in stools of patients with colorectal cancer by mutant-enriched PCR. Int. J. Cancer 66: Ogino S, Kawasaki T, Brahmandam M, Yan L, Cantor M, Namgyal C, Minokenudson M, Lauwers GY, Loda M, Fuchs CS Sensitive sequencing method for KRAS mutation detection by Pyrosequencing. J Mol Diagn 7(3): Ogiso H, Ishitani R, Nureki O, Fukai S, Yamanaka M, Kim JH, Saito K, Sakamoto A, Inoue M, Shirouzu M, Yokoyama S Crystal structure of the complex of human epidermal growth factor and receptor extracellular domains. Cell 110: Okabe T, Okamoto I, Tamaru K, Terashima M, Yoshida T, Satoh T, Takada M, Fukuoka M, Nakagawa K, Differential constitutive activation of the 51
52 52 epidermal growth factor receptor in non-small cell lung cancer cells bearing EGFR gene mutation and amplification. Cancer Res 67: Paez GJ, Jänne PA, Lee JC, Tracy S, Greulich H, Gabriel S, Herman P, Kaye FJ, Lindeman N, Boggon TJ, et al EGFR mutations in lung cancer: correlation with clinical response to gefitinib therapy. Science 304(5676): Pang B, Matthias D, Ong CW, Dhewar AN, Gupta S, Lim GL, Nga ME, Seet JE, Qasim A, Chin TM, et al The positive impact of cytological specimens for EGFR mutation testing in non-small cell lung cancer: a single South East Asian laboratory s analysis of 670 cases. Cytophatol 23: Ramirez JL, Sarries C, de Castro PL, Roig B, Queralt C, Escuin D, de Aguirre I, Sanchez JM, Manzano JL, Margelí M, et al Methylation patterns and K-ras mutations in tumor and paired serum of resected non-small-cell lung cancer patients. Cancer Lett 193: Reed GH, Kent JO, Wittwer CT High-resolution DNA melting analysis for simple and efficient molecular diagnostics. Pharmacogenomics 8(6): Riely GJ, Jenifer M, William P KRAS Mutations in Non Small Cell Lung Cancer. Proc Am Thorac Soc 6: Riese DJ, Stern DF Specificity within the EGF family/erbb receptor family signaling network. Bioessays 20:41 8. Roberts PJ, Der CJ Targeting the Raf-MEK-ERK mitogen-activated protein kinase cascade for the treatment of cancer. Oncogene 26: Ronen SA, Blackhall FH, Shepherd FA, Tsao MS K-ras Mutations in Non Small-Cell Lung Carcinoma: A Review. Clinical Lung Cancer 8(1): Rosell R, Taron M, Reguart N, Isla D, Moran T Epidermal growth factor receptor activation: how exon 19 and 21 mutations changed our understanding of the pathway. Clin Cancer Res 12: Sakurada A, Frances AS, Ming-Shound T Epidermal growth factor receptor tyrosine kinase inhibitors in lung cancer: impact of primary or secondary mutations. Clin Lung Cancer 7(4):S138-S144 Santos GC, Shepherd FA, Tsao MS EGFR mutation and lung cancer. Annu Rev Pathol Mech Dis 6:49-69 Sato M, Shames DS, Gazdar AF, Minna JD A translational view of the molecular pathogenesis of lung cancer. J Thorac Oncol 2: Sato T Differential diagnosis of pleural effusion. JMAJ 49(9-10): Schlessinger J Ligand-induced, receptor-mediated dimerization and activation of EGF receptor. Cell 110: Shawver LK, Slamon D, Ullrich A Smart drugs:tyrosine kinase inhibitors in cancer therapy. Cancer Cell 1: Shigematsu H, Lin L, Takahashi T, Nomura M, Suzuki M, Wistuba II, Fong KM, Lee H, Toyooka S, Shimizu N, et al Clinical and biological features of epidermal growth factor receptor mutations in lung cancers. J Natl Cancer Inst 97: Shigematsu H, Gazdar AF Somatic mutations of epidermal growth factor receptor signaling pathway in lung cancers. Int. J. Cancer 118:257 62
53 Siegfried JM, Gillespie AT, Mera R, Casey TJ, Keohavong P, Testa JR, Hunt JD Prognostic value of specific KRAS mutations in lung adenocarcinomas. Cancer Epidemiol Biomarkers Prev 6: Simon R Clinical trials for predictive medicine: new challenges and paradigms. Clin Trials. Sone S, Nakayama T, Honda T, Tsushima K, Li F, Haniuda M, Takahashi Y, Suzuki T, Yamanda T, Kondo R, et al Long-term follow-up study of a population-based mass screening programme for lung cancer using mobile low-dose spiral computed tomography. Lung Cancer 58: Sordella R, Bell DW, Haber DA, Settleman J Gefitinib-sensitizing EGFR mutations in lung cancer activate antiapoptotic pathways. Science 305: Spira A, Beane J, Shah V, Liu G, Schembri F, Yang X, Palma J, Brody JS Effects of cigarette smoke on the human airway epithelial cell transcriptome. Proc Natl Acad Sci USA 101: Spira A, Ettinger DS Multidisciplinary management of lung cancer. N Engl J Med 350: Sun S, Schiller JH, Gazdar AF Lung cancer in never smokers a different disease. Nat Rev Cancer 7: Sung HJ, Cho JY Biomarkers for the lung cancer diagnosis and their advances in proteomics. BMB Reports 41(9): Syahruddin E, Hudoyo A, Arief N Efusi pleura ganas pada kanker paru. Jurnal Respirologi Indonesia 26(4). Tappenden P, Chilcott J, Ward S, Eggington S, Hind D, Hummel S Methodological issues in the economic analysis of cancer treatments. Eur J Cancer 42(17): Taron M, Ichinose Y, Rosell R, Mok T, Massuti B, Zamora L, Mate JL, Manegold C, Ono M, Queralt C, et al Activating mutations in the tyrosine kinase domain of the epidermal growth factor receptor are associated with improved survival in gefitinibtreated chemorefractory lung adenocarcinomas. Clin Cancer Res 11: Tokumo M, Toyooka S, Kiura K, Shigematsu H, Tomii K, Aoe M, Ichimura K, Tsuda T, Yano M, Tsukuda K, et al The relationship between epidermal growth factor receptor mutations and clinicopathologic features in non-small cell lung cancers. Clin Cancer Res 11: Wang YC, Lee HS, Chen SK, Yang SC, Chen CY Analysis of K-ras gene mutations in lung carcinomas: correlation with gender, histological subtypes, and clinical outcome. J Cancer Res Clin Oncol 124: Weinberg RA The biology of cancer. Garland Science. Newyork White H, Potts G Mutation scanning by high resolution melt analysis. Evaluation of Rotor-Gene 6000 (Corbett Life Science), HR-1 and 384 well LightScanner (Idaho Technology). National Genetics Reference Laboratory (Wessex, 2006) ( Wistuba II, Berry J, Behrens C, Maitra A, Shivapurkar N, Milchgrub S, Mackay B, Minna JD, Gazdar AF Molecular changes in the bronchial epithelium of patients with small cell lung cancer. Clin Cancer Res 6:
54 54 Wittwer CT, Gudrun HR, Cameron NG, Joshua GV, Robert JP Highresolution genotyping by amplicon melting analysis using LC green. Clin Chem 49: Wittwer CT High-Resolution DNA melting analysis: advancements and limitations. Human mutation 30(6): Yarden Y, Sliwkowski MX Untagling the ErbB signaling network Nat Rev Mol Cell Biol 2: Yoshida T, Zhang G, Haura EB Targeting epidermal growth factor receptor: central signaling kinase in lung cancer. Biochem Pharm 80: Yun CH, Boggon TJ, Li Y, Woo MS, Greulich H, Meyerson M, Eck MJ Structures of lung cancer-derived EGFR mutants and inhibitor complexes: mechanism of activation and insights into differential inhibitor sensitivity. Cancer Cell 11: Zhang XT, Li LY, Mu XL, Cui QC, Chang XY, Song W, Wang SL, Wang MZ, Zhong W, Zhang L The EGFR mutation and its correlation with response of gefitinib in previously treated Chinese patients with advanced non-small-cell lung cancer. Ann Oncol 16: Zudaire I, Lozano MD, Vazquez MF, Pajares MJ, Agorreta J, Pio R, Zulueta JJ, Yankelevitz DF, Henschke CI, Montuenga LM Molecular characterization of small peripheral lung tumors based on the analysis of fine needle aspirates. Histol Histopathol 23:33-40.
55 Lampiran 1 Ethical clearance 55
56 56 Lampiran 2 Tabel hasil analisis mutasi gen KRAS dan EGFR pada sampel pasien kanker paru menggunakna metode HRM dan RFLP Pasien Hasil analisis jenis mutasi Jenis [DNA] Gen KRAS Gen EGFR kelamin ng/µl HRM RFLP HRM RFLP P01 TD 29,7 Wild type Wild type Wild type Wild type P02 TD 65,8 Wild type Wild type Wild type Wild type P03 TD 46 Wild type Wild type Wild type Wild type P04 TD 29 Wild type Wild type Wild type Wild type P05 TD 73,7 Wild type Wild type Wild type Wild type P06 TD 31,6 Wild type Wild type Wild type Wild type P07 TD 58,4 Mutasi Mutasi kodon 12 Wild type Wild type P08 TD 86,5 Wild type Wild type Wild type Wild type P09 TD 33,7 Wild type Wild type Wild type Wild type P10 Wanita 42,7 Wild type Wild type Wild type Wild type P11 Pria 28 Wild type Wild type Wild type Wild type P12 Pria 24,6 Wild type Wild type Wild type Wild type P13 Pria 8,4 Wild type Wild type Mutasi exon 21 Mutasi L858R P14 Wanita 8 Wild type Wild type Wild type Wild type P15 Wanita 9,9 Wild type Wild type Wild type Wild type P16 Wanita 7,7 Wild type Wild type Mutasi exon 19 Delesi exon 19 P17 Wanita 16,2 Wild type Wild type Wild type Wild type P18 Pria 18,5 Wild type Wild type Mutasi exon 19 Delesi exon 19 P19 Pria 5,7 Wild type Wild type Mutasi exon 19 Delesi exon 19 P20 Pria 8 Wild type Wild type Wild type Wild type P21 Wanita 17,6 Wild type Wild type Wild type Wild type P22 Pria 45,7 Wild type Wild type Wild type Wild type P23 Wanita 99,7 Wild type Wild type Wild type Wild type P24 Pria 43,2 Wild type Wild type Wild type Wild type P25 Wanita 97,2 Wild type Wild type Wild type Wild type P26 Pria 12,5 Wild type Wild type Wild type Wild type P27 Wanita 103,3 Wild type Wild type Wild type Wild type P28 Wanita 8,7 Wild type Wild type Wild type Wild type P29 Pria 27,2 Wild type Wild type Wild type Wild type P30 Pria 19,6 Wild type Wild type Wild type Wild type P31 Pria 369,2 Wild type Wild type Wild type Wild type P32 Pria 114,8 Wild type Wild type Wild type Wild type P33 Pria 33,5 Wild type Wild type Wild type Wild type P34 Wanita 21,2 Wild type Wild type Wild type Wild type P35 Wanita 13,8 Wild type Wild type Wild type Wild type P36 Wanita 12,8 Wild type Wild type Wild type Wild type P37 Wanita 14,2 Wild type Wild type Mutasi exon 21 Mutasi L858R P38 Pria 70 Wild type Wild type Wild type Wild type P39 Wanita 7 Wild type Wild type Wild type Wild type P40 Pria 10,3 Wild type Wild type Wild type Wild type P41 Pria 96,2 Wild type Wild type Wild type Wild type P42 Pria 7,9 Wild type Wild type Mutasi exon 19 Delesi exon 19 P43 Pria 28 Wild type Wild type Mutasi exon 21 Mutasi L858R P44 Pria 357 Wild type Wild type Wild type Wild type P45 Pria 305 Wild type Wild type Wild type Wild type P46 Wanita 18,6 Wild type Wild type Wild type Wild type
57 57 Pasien Hasil analisis jenis mutasi Jenis [DNA] Gen KRAS Gen EGFR kelamin ng/µl HRM RFLP HRM RFLP P47 Pria 29,5 Wild type Wild type Wild type Wild type P48 Wanita 110,3 Wild type Wild type Mutasi exon 21 Mutasi L858R P49 Wanita 15,2 Wild type Wild type Wild type Wild type P50 Wanita 14,8 Wild type Wild type Wild type Wild type P51 Wanita 38,9 Wild type Wild type Wild type Wild type P52 Wanita 12,7 Wild type Wild type Mutasi exon 19 Delesi exon 19 P53 Pria 8,8 Wild type Wild type Mutasi exon 21 Mutasi L858R P54 Pria 28 Wild type Wild type Wild type Wild type P55 Wanita 15,2 Wild type Wild type Wild type Wild type P56 Pria 12,5 Wild type Wild type Wild type Wild type P57 Pria 19,6 Wild type Wild type Wild type Wild type P58 Pria 234,4 Wild type Wild type Wild type Wild type P59 Wanita 32,4 Wild type Wild type Wild type Wild type P60 Wanita 33,4 Wild type Wild type Wild type Wild type P61 Wanita 8,9 Wild type Wild type Wild type Wild type P62 Wanita 154,4 Wild type Wild type Wild type Wild type P63 Pria 6,4 Wild type Wild type Wild type Wild type Ket : TD = Tidak diketahui
58 58 RIWAYAT HIDUP Penulis dilahirkan pada tanggal 12 Agustus 1984 di desa Mekarraharja Kecamatan Talaga Kabupaten Majalengka-Jawa Barat. Penulis menyelesaikan pendidikan sekolah dasar di SDN Mekarraharja II pada tahun 1996, sekolah menengah pertama di MTsN Talaga tahun 1999 dan sekolah menengah umum di MAN Talaga tahun Pada tahun 2002 penulis melanjutkan studi pada program studi Kimia Fakultas Sains dan Teknik Universitas Jenderal Soedirman. Pada tahun 2007 penulis berhasil menyelesaikan pendidikan sarjana dengan tugas akhir bidang Kimia Organik berjudul: Sintesis senyawa 2-hidroksibenzoil-metiloktanoil- serin-ester dan 2-hidroksibenzoil-heksanoil-metil-serin-ester serta uji sitotoksisitasnya Terhadap sel kanker murine leukemia P-388. Penulis mengawali karir dalam bidang penelitian sejak melaksanakan magang di Laboratorium Kimia Polimer Pusat Penelitian Kimia Lembaga Ilmu Pengetahuan Indonesia (LIPI) pada pertengahan tahun Pada tahun 2008 penulis bekerja sebagai kandidat peneliti di Laboratorium Diagnostik Kesehatan Pusat Penelitian Bioteknologi-LIPI sampai dengan saat ini. Pada tahun 2011, penulis mendapatkan kesempatan untuk melakukan penelitian mengenai analisis mutasi gen pada pasien kanker paru yang dilaporkan dalam bentuk Tesis, sebagai salah satu syarat menyelesaikan program Pascasarjana Bioteknologi IPB. Penelitian tersebut merupakan bagian dari proyek kerjasama riset antara Fakultas Kedokteran Universitas Indonesia dan Divisi Kanker Stem cell and Cancer Institute PT Kalbe Farma, Tbk.
TINJAUAN PUSTAKA. Herbst et al. (2008) Gambar 1 Fase pertumbuhan kanker pada pasien perokok dan non-perokok
 17 TINJAUAN PUSTAKA Kanker Paru Kanker paru merupakan tumor ganas pada organ paru, dan terletak pada daerah saluran nafas atau epitel bronkus. Terjadinya kanker paru ditandai dengan pertumbuhan sel yang
17 TINJAUAN PUSTAKA Kanker Paru Kanker paru merupakan tumor ganas pada organ paru, dan terletak pada daerah saluran nafas atau epitel bronkus. Terjadinya kanker paru ditandai dengan pertumbuhan sel yang
HASIL DAN PEMBAHASAN
 32 HASIL DAN PEMBAHASAN Analisis Mutasi Gen KRAS Menggunakan Metode HRM dan RFLP pada DNA Standar Sel Kultur Analisis mutasi gen KRAS menggunakan metode HRM telah dilakukan terhadap DNA standar untuk mengetahui
32 HASIL DAN PEMBAHASAN Analisis Mutasi Gen KRAS Menggunakan Metode HRM dan RFLP pada DNA Standar Sel Kultur Analisis mutasi gen KRAS menggunakan metode HRM telah dilakukan terhadap DNA standar untuk mengetahui
BAB I PENDAHULUAN. A. Latar Belakang Kanker paru merupakan keganasan penyebab kematian. nomer satu di dunia (Cancer Research UK, 2012).
 BAB I PENDAHULUAN A. Latar Belakang Kanker paru merupakan keganasan penyebab kematian nomer satu di dunia (Cancer Research UK, 2012). Mortalitas kanker ini tercatat sebesar 1.590.000 jiwa pada tahun 2012
BAB I PENDAHULUAN A. Latar Belakang Kanker paru merupakan keganasan penyebab kematian nomer satu di dunia (Cancer Research UK, 2012). Mortalitas kanker ini tercatat sebesar 1.590.000 jiwa pada tahun 2012
ROLE OF EGFR TESTING IN LUNG CANCER
 ROLE OF EGFR TESTING IN LUNG CANCER (Epidermal Growth Factor Receptor) ACHMAD MULAWARMAN JAYUSMAN Bandung, 06 Februari 2016 METRO POCKET MAP SIGNALING PATHWAY IN CANCER PENDAHULUAN Pada kasus kanker paru,
ROLE OF EGFR TESTING IN LUNG CANCER (Epidermal Growth Factor Receptor) ACHMAD MULAWARMAN JAYUSMAN Bandung, 06 Februari 2016 METRO POCKET MAP SIGNALING PATHWAY IN CANCER PENDAHULUAN Pada kasus kanker paru,
Bab IV HASIL DAN PEMBAHASAN. jalan Dr. Soetomo No.16, Semarang, Jawa Tengahmerupakan Satuan
 Bab IV HASIL DAN PEMBAHASAN A. Hasil 1. Deskripsi Lokasi Penelitian Rumah Sakit Umum Pusat Dr. Kariadi Semarang yang beralamat di jalan Dr. Soetomo No.16, Semarang, Jawa Tengahmerupakan Satuan Kerja atau
Bab IV HASIL DAN PEMBAHASAN A. Hasil 1. Deskripsi Lokasi Penelitian Rumah Sakit Umum Pusat Dr. Kariadi Semarang yang beralamat di jalan Dr. Soetomo No.16, Semarang, Jawa Tengahmerupakan Satuan Kerja atau
BAB I PENDAHULUAN. I. A. Latar Belakang. Kanker paru merupakan salah satu dari keganasan. tersering pada pria dan wanita dengan angka mortalitas
 BAB I PENDAHULUAN I. A. Latar Belakang Kanker paru merupakan salah satu dari keganasan tersering pada pria dan wanita dengan angka mortalitas tertinggi di dunia, yaitu sebesar 1.590.000 kematian di tahun
BAB I PENDAHULUAN I. A. Latar Belakang Kanker paru merupakan salah satu dari keganasan tersering pada pria dan wanita dengan angka mortalitas tertinggi di dunia, yaitu sebesar 1.590.000 kematian di tahun
BAB I PENDAHULUAN. I.A Latar Belakang. Kanker paru merupakan penyebab tertinggi kematian. akibat kanker di dunia, baik negara-negara maju maupun
 BAB I PENDAHULUAN I.A Latar Belakang Kanker paru merupakan penyebab tertinggi kematian akibat kanker di dunia, baik negara-negara maju maupun berkembang (Jemal et al., 2010). Di Amerika Serikat, kanker
BAB I PENDAHULUAN I.A Latar Belakang Kanker paru merupakan penyebab tertinggi kematian akibat kanker di dunia, baik negara-negara maju maupun berkembang (Jemal et al., 2010). Di Amerika Serikat, kanker
BAB I PENDAHULUAN 1.1 Latar Belakang
 BAB I PENDAHULUAN 1.1 Latar Belakang Kanker paru adalah kanker yang paling sering didiagnosis di dunia dan merupakan penyebab utama kematian akibat kanker. Data kasus baru kanker paru di Amerika Serikat
BAB I PENDAHULUAN 1.1 Latar Belakang Kanker paru adalah kanker yang paling sering didiagnosis di dunia dan merupakan penyebab utama kematian akibat kanker. Data kasus baru kanker paru di Amerika Serikat
BAB I PENDAHULUAN. Karsinoma kolorektal (KKR) merupakan masalah kesehatan serius yang
 BAB I PENDAHULUAN 1.1 Latar Belakang Karsinoma kolorektal (KKR) merupakan masalah kesehatan serius yang kejadiannya cukup sering, terutama mengenai penduduk yang tinggal di negara berkembang. Kanker ini
BAB I PENDAHULUAN 1.1 Latar Belakang Karsinoma kolorektal (KKR) merupakan masalah kesehatan serius yang kejadiannya cukup sering, terutama mengenai penduduk yang tinggal di negara berkembang. Kanker ini
BAB V KESIMPULAN, SARAN & RINGKASAN
 BAB V KESIMPULAN, SARAN & RINGKASAN V.1. Kesimpulan Berdasarkan hasil penelitian dapat disimpulkan bahwa: 1. Ekspresi hsa-mir-155-5p lebih tinggi 1,13 kali pada plasma darah penderita kanker nasofaring
BAB V KESIMPULAN, SARAN & RINGKASAN V.1. Kesimpulan Berdasarkan hasil penelitian dapat disimpulkan bahwa: 1. Ekspresi hsa-mir-155-5p lebih tinggi 1,13 kali pada plasma darah penderita kanker nasofaring
BAB IV HASIL PENELITIAN DAN PEMBAHASAN
 BAB IV HASIL PENELITIAN DAN PEMBAHASAN A. Hasil Penelitian 1. Deskripsi Lokasi Penelitian Rumah Sakit Umum Pemerintah Dr. Kariadi Semarang yang beralamat di jalan Dr. Soetomo No.16, Semarang, Jawa Tengah
BAB IV HASIL PENELITIAN DAN PEMBAHASAN A. Hasil Penelitian 1. Deskripsi Lokasi Penelitian Rumah Sakit Umum Pemerintah Dr. Kariadi Semarang yang beralamat di jalan Dr. Soetomo No.16, Semarang, Jawa Tengah
BAB I. PENDAHULUAN. I.1. Latar Belakang. adanya heterogenitas pada perubahan genetik. Kanker payudara menjadi penyebab
 BAB I. PENDAHULUAN I.1. Latar Belakang Kanker payudara merupakan penyakit kompleks yang ditandai dengan adanya heterogenitas pada perubahan genetik. Kanker payudara menjadi penyebab utama kematian di dunia.
BAB I. PENDAHULUAN I.1. Latar Belakang Kanker payudara merupakan penyakit kompleks yang ditandai dengan adanya heterogenitas pada perubahan genetik. Kanker payudara menjadi penyebab utama kematian di dunia.
4 Hasil dan Pembahasan
 4 Hasil dan Pembahasan Dalam bab ini akan dipaparkan hasil dari tahap-tahap penelitian yang telah dilakukan. Melalui tahapan tersebut diperoleh urutan nukleotida sampel yang positif diabetes dan sampel
4 Hasil dan Pembahasan Dalam bab ini akan dipaparkan hasil dari tahap-tahap penelitian yang telah dilakukan. Melalui tahapan tersebut diperoleh urutan nukleotida sampel yang positif diabetes dan sampel
BAB V. KESIMPULAN, SARAN, DAN RINGKASAN. V. I. Kesimpulan. 1. Frekuensi genotip AC dan CC lebih tinggi pada kelompok obesitas
 BAB V. KESIMPULAN, SARAN, DAN RINGKASAN V. I. Kesimpulan 1. Frekuensi genotip AC dan CC lebih tinggi pada kelompok obesitas dibandingkan dengan kelompok normal namun secara statistik tidak berbeda signifikan
BAB V. KESIMPULAN, SARAN, DAN RINGKASAN V. I. Kesimpulan 1. Frekuensi genotip AC dan CC lebih tinggi pada kelompok obesitas dibandingkan dengan kelompok normal namun secara statistik tidak berbeda signifikan
Kolokium Departemen Biologi FMIPA IPB: Ria Maria
 Kolokium Departemen Biologi FMIPA IPB: Ria Maria Ria Maria (G34090088), Achmad Farajallah, Maria Ulfah. 2012. Karakterisasi Single Nucleotide Polymorphism Gen CAST pada Ras Ayam Lokal. Makalah Kolokium
Kolokium Departemen Biologi FMIPA IPB: Ria Maria Ria Maria (G34090088), Achmad Farajallah, Maria Ulfah. 2012. Karakterisasi Single Nucleotide Polymorphism Gen CAST pada Ras Ayam Lokal. Makalah Kolokium
I. PENDAHULUAN. Kanker merupakan masalah utama bagi masyarakat karena menjadi salah
 I. PENDAHULUAN 1.1. Latar Belakang Kanker merupakan masalah utama bagi masyarakat karena menjadi salah satu penyebab kematian terbesar di dunia. Salah satu jenis kanker yang memiliki potensi kematian terbesar
I. PENDAHULUAN 1.1. Latar Belakang Kanker merupakan masalah utama bagi masyarakat karena menjadi salah satu penyebab kematian terbesar di dunia. Salah satu jenis kanker yang memiliki potensi kematian terbesar
MATERI DAN METODE. Lokasi dan Waktu. Materi
 MATERI DAN METODE Lokasi dan Waktu Penelitian ini dilaksanakan di Laboratorium Genetika Molekuler, Bagian Pemuliaan dan Genetika Ternak, Departemen Ilmu Produksi dan Teknologi Peternakan, Fakultas Peternakan,
MATERI DAN METODE Lokasi dan Waktu Penelitian ini dilaksanakan di Laboratorium Genetika Molekuler, Bagian Pemuliaan dan Genetika Ternak, Departemen Ilmu Produksi dan Teknologi Peternakan, Fakultas Peternakan,
BAB I PENDAHULUAN. merupakan penyebab kematian pada wanita setelah kanker payudara. Hal ini
 BAB I PENDAHULUAN 1.1 Latar Belakang Kanker serviks uteri merupakan salah satu masalah penting pada wanita di dunia. Karsinoma serviks uteri adalah keganasan kedua yang paling sering terjadi dan merupakan
BAB I PENDAHULUAN 1.1 Latar Belakang Kanker serviks uteri merupakan salah satu masalah penting pada wanita di dunia. Karsinoma serviks uteri adalah keganasan kedua yang paling sering terjadi dan merupakan
BAB I PENDAHULUAN. dikalangan wanita sedunia, meliputi 16% dari semua jenis kanker yang diderita
 1.1 Latar Belakang BAB I PENDAHULUAN Kanker payudara merupakan jenis kanker yang paling sering ditemui dikalangan wanita sedunia, meliputi 16% dari semua jenis kanker yang diderita oleh kaum wanita dan
1.1 Latar Belakang BAB I PENDAHULUAN Kanker payudara merupakan jenis kanker yang paling sering ditemui dikalangan wanita sedunia, meliputi 16% dari semua jenis kanker yang diderita oleh kaum wanita dan
ABSTRAK ANGKA KEJADIAN KANKER PARU DI RUMAH SAKIT IMMANUEL BANDUNG PERIODE 1 JANUARI DESEMBER 2010
 ABSTRAK ANGKA KEJADIAN KANKER PARU DI RUMAH SAKIT IMMANUEL BANDUNG PERIODE 1 JANUARI 2009 31 DESEMBER 2010 Stevanus, 2011; Pembimbing I : dr. Hartini Tiono, M.Kes. Pembimbing II : dr. Sri Nadya J Saanin,
ABSTRAK ANGKA KEJADIAN KANKER PARU DI RUMAH SAKIT IMMANUEL BANDUNG PERIODE 1 JANUARI 2009 31 DESEMBER 2010 Stevanus, 2011; Pembimbing I : dr. Hartini Tiono, M.Kes. Pembimbing II : dr. Sri Nadya J Saanin,
BAB I PENDAHULUAN. A. Latar Belakang Kanker adalah pertumbuhan yang tidak terkendali dari sel-sel, yang dapat
 BAB I PENDAHULUAN A. Latar Belakang Kanker adalah pertumbuhan yang tidak terkendali dari sel-sel, yang dapat menyerang dan menyebar ke bagian tubuh yang jauh. Kanker dapat memiliki konsekuensi kesehatan
BAB I PENDAHULUAN A. Latar Belakang Kanker adalah pertumbuhan yang tidak terkendali dari sel-sel, yang dapat menyerang dan menyebar ke bagian tubuh yang jauh. Kanker dapat memiliki konsekuensi kesehatan
BAB 4 HASIL PERCOBAAN DAN PEMBAHASAN
 BAB 4 HASIL PERCOBAAN DAN PEMBAHASAN Sebelum melakukan PCR, terlebih dahulu dilakukan perancangan primer menggunakan program DNA Star. Pemilihan primer dilakukan dengan mempertimbangkan parameter spesifisitas,
BAB 4 HASIL PERCOBAAN DAN PEMBAHASAN Sebelum melakukan PCR, terlebih dahulu dilakukan perancangan primer menggunakan program DNA Star. Pemilihan primer dilakukan dengan mempertimbangkan parameter spesifisitas,
I. PENDAHULUAN. Kanker payudara (KPD) merupakan salah satu tumor ganas penyebab
 I. PENDAHULUAN 1.1 Latar Belakang Kanker payudara (KPD) merupakan salah satu tumor ganas penyebab kematian wanita nomor satu (14,7%) di seluruh dunia (Globocan-IARC, 2012). International Agency for Research
I. PENDAHULUAN 1.1 Latar Belakang Kanker payudara (KPD) merupakan salah satu tumor ganas penyebab kematian wanita nomor satu (14,7%) di seluruh dunia (Globocan-IARC, 2012). International Agency for Research
BAB IV HASIL DAN PEMBAHASAN. Deteksi genom virus avian influenza pada penelitian dilakukan
 30 BAB IV HASIL DAN PEMBAHASAN A. KONDISI OPTIMAL REAKSI AMPLIFIKASI Deteksi genom virus avian influenza pada penelitian dilakukan menggunakan primer NA. Primer NA dipilih karena protein neuraminidase,
30 BAB IV HASIL DAN PEMBAHASAN A. KONDISI OPTIMAL REAKSI AMPLIFIKASI Deteksi genom virus avian influenza pada penelitian dilakukan menggunakan primer NA. Primer NA dipilih karena protein neuraminidase,
BAB IV HASIL DAN PEMBAHASAN. Sintesis fragmen gen HA Avian Influenza Virus (AIV) galur
 20 BAB IV HASIL DAN PEMBAHASAN A. KONDISI OPTIMAL REAKSI AMPLIFIKASI Sintesis fragmen 688--1119 gen HA Avian Influenza Virus (AIV) galur A/Indonesia/5/2005 dilakukan dengan teknik overlapping extension
20 BAB IV HASIL DAN PEMBAHASAN A. KONDISI OPTIMAL REAKSI AMPLIFIKASI Sintesis fragmen 688--1119 gen HA Avian Influenza Virus (AIV) galur A/Indonesia/5/2005 dilakukan dengan teknik overlapping extension
BIO306. Prinsip Bioteknologi
 BIO306 Prinsip Bioteknologi KULIAH 7. PUSTAKA GENOM DAN ANALISIS JENIS DNA Konstruksi Pustaka DNA Pustaka gen merupakan sumber utama isolasi gen spesifik atau fragmen gen. Koleksi klon rekombinan dari
BIO306 Prinsip Bioteknologi KULIAH 7. PUSTAKA GENOM DAN ANALISIS JENIS DNA Konstruksi Pustaka DNA Pustaka gen merupakan sumber utama isolasi gen spesifik atau fragmen gen. Koleksi klon rekombinan dari
BAB I PENDAHULUAN. Karsinoma payudara merupakan penyakit keganasan yang paling sering
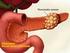 BAB I PENDAHULUAN 1.1 Latar Belakang Karsinoma payudara merupakan penyakit keganasan yang paling sering dijumpai pada wanita dan penyebab kematian terbanyak. Pengobatannya sangat tergantung dari stadium
BAB I PENDAHULUAN 1.1 Latar Belakang Karsinoma payudara merupakan penyakit keganasan yang paling sering dijumpai pada wanita dan penyebab kematian terbanyak. Pengobatannya sangat tergantung dari stadium
BAB 1 PENDAHULUAN 1.1. Latar Belakang
 BAB 1 PENDAHULUAN 1.1. Latar Belakang Karsinoma nasofaring (KNF) merupakan tumor ganas epitel nasofaring. Etiologi tumor ganas ini bersifat multifaktorial, faktor etnik dan geografi mempengaruhi risiko
BAB 1 PENDAHULUAN 1.1. Latar Belakang Karsinoma nasofaring (KNF) merupakan tumor ganas epitel nasofaring. Etiologi tumor ganas ini bersifat multifaktorial, faktor etnik dan geografi mempengaruhi risiko
HASIL DAN PEMBAHASAN
 HASIL DAN PEMBAHASAN Amplifikasi Gen Calpastatin (CAST MspI) Amplifikasi fragmen gen calpastatin (CAST MspI) pada setiap bangsa sapi dilakukan dengan menggunakan mesin thermal cycler (AB Bio System) pada
HASIL DAN PEMBAHASAN Amplifikasi Gen Calpastatin (CAST MspI) Amplifikasi fragmen gen calpastatin (CAST MspI) pada setiap bangsa sapi dilakukan dengan menggunakan mesin thermal cycler (AB Bio System) pada
BAB III. METODOLOGI PENELITIAN. Pengambilan sampel. Penyiapan templat mtdna dengan metode lisis sel
 16 BAB III. METODOLOGI PENELITIAN Bab ini menggambarkan tahapan penelitian yang terdiri dari pengambilan sampel, penyiapan templat mtdna dengan metode lisis sel, amplifikasi D-loop mtdna dengan teknik
16 BAB III. METODOLOGI PENELITIAN Bab ini menggambarkan tahapan penelitian yang terdiri dari pengambilan sampel, penyiapan templat mtdna dengan metode lisis sel, amplifikasi D-loop mtdna dengan teknik
MATERI DAN METODE. Lokasi dan Waktu. Materi. Tabel 1. Jumah Sampel Darah Ternak Sapi Indonesia Ternak n Asal Sapi Bali 2 4
 MATERI DAN METODE Lokasi dan Waktu Penelitian dilaksanakan di Laboratorium Genetika Molekuler Ternak, Bagian Pemuliaan dan Genetika Ternak, Fakultas Peternakan, Institut Pertanian Bogor. penelitian ini
MATERI DAN METODE Lokasi dan Waktu Penelitian dilaksanakan di Laboratorium Genetika Molekuler Ternak, Bagian Pemuliaan dan Genetika Ternak, Fakultas Peternakan, Institut Pertanian Bogor. penelitian ini
BAB III METODE PENELITIAN. Dalam penelitian ini dilakukan lima tahap utama yang meliputi tahap
 BAB III METODE PENELITIAN Dalam penelitian ini dilakukan lima tahap utama yang meliputi tahap penyiapan templat mtdna, amplifikasi fragmen mtdna pada daerah D-loop mtdna manusia dengan teknik PCR, deteksi
BAB III METODE PENELITIAN Dalam penelitian ini dilakukan lima tahap utama yang meliputi tahap penyiapan templat mtdna, amplifikasi fragmen mtdna pada daerah D-loop mtdna manusia dengan teknik PCR, deteksi
BAB 4 HASIL PERCOBAAN DAN BAHASAN. Oligonukleotida sintetis daerah pengkode IFNα2b sintetis dirancang menggunakan
 BAB 4 HASIL PERCOBAAN DAN BAHASAN Oligonukleotida sintetis daerah pengkode IFNα2b sintetis dirancang menggunakan program komputer berdasarkan metode sintesis dua arah TBIO, dimana proses sintesis daerah
BAB 4 HASIL PERCOBAAN DAN BAHASAN Oligonukleotida sintetis daerah pengkode IFNα2b sintetis dirancang menggunakan program komputer berdasarkan metode sintesis dua arah TBIO, dimana proses sintesis daerah
BAB I PENDAHULUAN. kompleks, mencakup faktor genetik, infeksi Epstein-Barr Virus (EBV) dan
 1 BAB I PENDAHULUAN 1.1 Latar Belakang Karsinoma nasofaring (KNF) adalah tumor ganas yang cenderung didiagnosis pada stadium lanjut dan merupakan penyakit dengan angka kejadian tertinggi serta menjadi
1 BAB I PENDAHULUAN 1.1 Latar Belakang Karsinoma nasofaring (KNF) adalah tumor ganas yang cenderung didiagnosis pada stadium lanjut dan merupakan penyakit dengan angka kejadian tertinggi serta menjadi
HASIL DAN PEMBAHASAN. divisualisasikan padaa gel agarose seperti terlihat pada Gambar 4.1. Ukuran pita
 IV. HASIL DAN PEMBAHASAN 4.1. Amplifikasi Gen Mx Amplifikasi gen Mx telah berhasil dilakukan. Hasil amplifikasi gen Mx divisualisasikan padaa gel agarose seperti terlihat pada Gambar 4.1. Ukuran pita yang
IV. HASIL DAN PEMBAHASAN 4.1. Amplifikasi Gen Mx Amplifikasi gen Mx telah berhasil dilakukan. Hasil amplifikasi gen Mx divisualisasikan padaa gel agarose seperti terlihat pada Gambar 4.1. Ukuran pita yang
BAB 4 HASIL PERCOBAAN DAN BAHASAN
 14 BAB 4 HASIL PERCOBAAN DAN BAHASAN Konfirmasi bakteri C. violaceum dan B. cereus dilakukan dengan pewarnaan Gram, identifikasi morfologi sel bakteri, sekuensing PCR 16s rdna dan uji kualitatif aktivitas
14 BAB 4 HASIL PERCOBAAN DAN BAHASAN Konfirmasi bakteri C. violaceum dan B. cereus dilakukan dengan pewarnaan Gram, identifikasi morfologi sel bakteri, sekuensing PCR 16s rdna dan uji kualitatif aktivitas
ABSTRAK GAMBARAN PENDERITA PENYAKIT KANKER PARU PERIODE 1 JANUARI DESEMBER 2012 DI RS. IMMANUEL KOTA BANDUNG
 ABSTRAK GAMBARAN PENDERITA PENYAKIT KANKER PARU PERIODE 1 JANUARI 2011 31 DESEMBER 2012 DI RS. IMMANUEL KOTA BANDUNG Dwirama Ivan Prakoso Rahmadi, 1110062 Pembimbing I : dr. Sri Nadya J Saanin, M.Kes Pembimbing
ABSTRAK GAMBARAN PENDERITA PENYAKIT KANKER PARU PERIODE 1 JANUARI 2011 31 DESEMBER 2012 DI RS. IMMANUEL KOTA BANDUNG Dwirama Ivan Prakoso Rahmadi, 1110062 Pembimbing I : dr. Sri Nadya J Saanin, M.Kes Pembimbing
BAB III METODE PENELITIAN Bagan Alir Penelitian ini secara umum dapat digambarkan pada skema berikut:
 BAB III METODE PENELITIAN Tahapan-tahapan yang dilakukan dalam penelitian ini adalah: pengumpulan sampel, lisis terhadap sampel mtdna yang telah diperoleh, amplifikasi daerah HVI mtdna sampel dengan menggunakan
BAB III METODE PENELITIAN Tahapan-tahapan yang dilakukan dalam penelitian ini adalah: pengumpulan sampel, lisis terhadap sampel mtdna yang telah diperoleh, amplifikasi daerah HVI mtdna sampel dengan menggunakan
BAB IV. HASIL DAN PEMBAHASAN
 BAB IV. HASIL DAN PEMBAHASAN Pada bab ini akan disajikan hasil dan pembahasan berdasarkan langkah-langkah penelitian yang telah diuraikan dalam bab sebelumnya dalam empat bagian yang meliputi; sampel mtdna,
BAB IV. HASIL DAN PEMBAHASAN Pada bab ini akan disajikan hasil dan pembahasan berdasarkan langkah-langkah penelitian yang telah diuraikan dalam bab sebelumnya dalam empat bagian yang meliputi; sampel mtdna,
BAB II TINJAUAN PUSTAKA. 1. Staging tumor, nodus, metastasis (TNM) Semakin dini semakin baik. di bandingkan dengan karsinoma yang sudah invasif.
 7 BAB II TINJAUAN PUSTAKA 2.1. Prognosis Kanker Payudara Prognosis dipengaruhi oleh ukuran tumor, metastasis, derajat diferensiasi, dan jenis histopatologi. Menurut Ramli (1994), prognosis kanker payudara
7 BAB II TINJAUAN PUSTAKA 2.1. Prognosis Kanker Payudara Prognosis dipengaruhi oleh ukuran tumor, metastasis, derajat diferensiasi, dan jenis histopatologi. Menurut Ramli (1994), prognosis kanker payudara
BAB III METODE PENELITIAN. amplifikasi daerah HVI mtdna sampel dengan menggunakan teknik PCR;
 BAB III METODE PENELITIAN Secara garis besar, langkah-langkah yang dilakukan dalam penelitian ini adalah: pengumpulan sampel; lisis terhadap sampel mtdna yang telah diperoleh; amplifikasi daerah HVI mtdna
BAB III METODE PENELITIAN Secara garis besar, langkah-langkah yang dilakukan dalam penelitian ini adalah: pengumpulan sampel; lisis terhadap sampel mtdna yang telah diperoleh; amplifikasi daerah HVI mtdna
BAB I PENDAHULUAN. A. Latar Belakang
 BAB I PENDAHULUAN A. Latar Belakang Retinoblastoma merupakan keganasan intraokular paling sering pada anak, yang timbul dari retinoblas immature pada perkembangan retina. Keganasan ini adalah keganasan
BAB I PENDAHULUAN A. Latar Belakang Retinoblastoma merupakan keganasan intraokular paling sering pada anak, yang timbul dari retinoblas immature pada perkembangan retina. Keganasan ini adalah keganasan
BAB 6 PEMBAHASAN. ekstrak Phaleria macrocarpa terhadap penurunan indek mitosis dan
 BAB 6 PEMBAHASAN Penelitian ini bertujuan untuk membuktikan pengaruh pemberian ekstrak Phaleria macrocarpa terhadap penurunan indek mitosis dan menurunnya atau penghambatan pertumbuhan karsinoma epidermoid
BAB 6 PEMBAHASAN Penelitian ini bertujuan untuk membuktikan pengaruh pemberian ekstrak Phaleria macrocarpa terhadap penurunan indek mitosis dan menurunnya atau penghambatan pertumbuhan karsinoma epidermoid
MATERI DAN METODE. Kota Padang Sumatera Barat pada bulan Oktober Amplifikasi gen Growth
 III. MATERI DAN METODE 3.1 Waktu dan Tempat Pengambilan sampel darah domba dilakukan di Kecamatan Koto Tengah Kota Padang Sumatera Barat pada bulan Oktober 2012. Amplifikasi gen Growth Hormone menggunakan
III. MATERI DAN METODE 3.1 Waktu dan Tempat Pengambilan sampel darah domba dilakukan di Kecamatan Koto Tengah Kota Padang Sumatera Barat pada bulan Oktober 2012. Amplifikasi gen Growth Hormone menggunakan
BAB 1 PENDAHULUAN. Kanker merupakan penyakit yang melibatkan faktor genetik dalam proses
 BAB 1 PENDAHULUAN 1.1. Latar Belakang Masalah Kanker merupakan penyakit yang melibatkan faktor genetik dalam proses patogenesisnya, proses pembelahan sel menjadi tidak terkontrol karena gen yang mengatur
BAB 1 PENDAHULUAN 1.1. Latar Belakang Masalah Kanker merupakan penyakit yang melibatkan faktor genetik dalam proses patogenesisnya, proses pembelahan sel menjadi tidak terkontrol karena gen yang mengatur
PRAKATA. Alhamdulillah syukur senantiasa penulis panjatkan kepada Allah swt., atas
 PRAKATA Alhamdulillah syukur senantiasa penulis panjatkan kepada Allah swt., atas segala nikmat dan karunia-nya, penulisan Tugas Akhir dengan judul Keragaman Genetik Abalon (Haliotis asinina) Selat Lombok
PRAKATA Alhamdulillah syukur senantiasa penulis panjatkan kepada Allah swt., atas segala nikmat dan karunia-nya, penulisan Tugas Akhir dengan judul Keragaman Genetik Abalon (Haliotis asinina) Selat Lombok
BAB III METODOLOGI PENELITIAN. Penelitian akan diawali dengan preparasi alat dan bahan untuk sampling
 16 BAB III METODOLOGI PENELITIAN Penelitian akan diawali dengan preparasi alat dan bahan untuk sampling sel folikel akar rambut. Sampel kemudian dilisis, diamplifikasi dan disekuensing dengan metode dideoksi
16 BAB III METODOLOGI PENELITIAN Penelitian akan diawali dengan preparasi alat dan bahan untuk sampling sel folikel akar rambut. Sampel kemudian dilisis, diamplifikasi dan disekuensing dengan metode dideoksi
BAB I PENDAHULUAN. Diperkirakan terdapat kasus baru kanker ovarium dan kasus meninggal
 BAB I PENDAHULUAN I.1. Latar Belakang Kanker ovarium merupakan penyebab kematian ketujuh pada wanita di dunia. Diperkirakan terdapat 239.000 kasus baru kanker ovarium dan 152.000 kasus meninggal dunia
BAB I PENDAHULUAN I.1. Latar Belakang Kanker ovarium merupakan penyebab kematian ketujuh pada wanita di dunia. Diperkirakan terdapat 239.000 kasus baru kanker ovarium dan 152.000 kasus meninggal dunia
ANALISA HASIL TRANSFORMASI DENGAN MENGGUNAKAN PCR KOLONI DAN RESTRIKSI
 1 ANALISA HASIL TRANSFORMASI DENGAN MENGGUNAKAN PCR KOLONI DAN RESTRIKSI PENDAHULUAN Polimerase Chain Reaction (PCR) PCR adalah suatu reaksi invitro untuk menggandakan jumlah molekul DNA pada target tertentu
1 ANALISA HASIL TRANSFORMASI DENGAN MENGGUNAKAN PCR KOLONI DAN RESTRIKSI PENDAHULUAN Polimerase Chain Reaction (PCR) PCR adalah suatu reaksi invitro untuk menggandakan jumlah molekul DNA pada target tertentu
MUTASI C825T GEN katg ISOLAT L5 MULTIDRUG RESISTANT Mycobacterium tuberculosis TESIS RINA BUDI SATIYARTI NIM: Program Studi Kimia
 MUTASI C825T GEN katg ISOLAT L5 MULTIDRUG RESISTANT Mycobacterium tuberculosis TESIS Karya tulis sebagai salah satu syarat untuk memperoleh gelar Magister dari Institut Teknologi Bandung Oleh: RINA BUDI
MUTASI C825T GEN katg ISOLAT L5 MULTIDRUG RESISTANT Mycobacterium tuberculosis TESIS Karya tulis sebagai salah satu syarat untuk memperoleh gelar Magister dari Institut Teknologi Bandung Oleh: RINA BUDI
BAB I PENDAHULUAN. A. Latar Belakang Penelitian. kepala leher dan paling sering ditemukan di Indonesia dan sampai saat ini belum
 1 BAB I PENDAHULUAN A. Latar Belakang Penelitian Karsinoma nasofarings (KNF) merupakan keganasan yang menyerang daerah kepala leher dan paling sering ditemukan di Indonesia dan sampai saat ini belum diketahui
1 BAB I PENDAHULUAN A. Latar Belakang Penelitian Karsinoma nasofarings (KNF) merupakan keganasan yang menyerang daerah kepala leher dan paling sering ditemukan di Indonesia dan sampai saat ini belum diketahui
HASIL DAN PEMBAHASAN. Amplifikasi Gen GH Exon 2
 HASIL DAN PEMBAHASAN Amplifikasi Gen GH Exon 2 Gen GH exon 2 pada ternak kambing PE, Saanen, dan persilangannya (PESA) berhasil diamplifikasi menggunakan teknik PCR (Polymerase Chain Reaction). Pasangan
HASIL DAN PEMBAHASAN Amplifikasi Gen GH Exon 2 Gen GH exon 2 pada ternak kambing PE, Saanen, dan persilangannya (PESA) berhasil diamplifikasi menggunakan teknik PCR (Polymerase Chain Reaction). Pasangan
III. METODOLOGI PENELITIAN. Penelitian ini menggunakan metode eksperimental yang bertujuan untuk
 56 III. METODOLOGI PENELITIAN A. Rancangan Penelitian Penelitian ini menggunakan metode eksperimental yang bertujuan untuk mengamplifikasi Gen FNBP1L. B. Tempat dan Waktu Penelitian 1. Tempat Penelitian
56 III. METODOLOGI PENELITIAN A. Rancangan Penelitian Penelitian ini menggunakan metode eksperimental yang bertujuan untuk mengamplifikasi Gen FNBP1L. B. Tempat dan Waktu Penelitian 1. Tempat Penelitian
BAB I PENDAHULUAN. Karsinoma nasofaring (KNF) merupakan tumor ganas yang berasal dari epitel
 BAB I PENDAHULUAN 1.1. Latar Belakang Karsinoma nasofaring (KNF) merupakan tumor ganas yang berasal dari epitel mukosa nasofaring dengan predileksi di fossa Rossenmuller. Kesulitan diagnosis dini pada
BAB I PENDAHULUAN 1.1. Latar Belakang Karsinoma nasofaring (KNF) merupakan tumor ganas yang berasal dari epitel mukosa nasofaring dengan predileksi di fossa Rossenmuller. Kesulitan diagnosis dini pada
BAB 1 PENDAHULUAN 1.1. Latar Belakang
 BAB 1 PENDAHULUAN 1.1. Latar Belakang Kanker telah menjadi masalah kesehatan di dunia, termasuk di Indonesia. Data Badan Kesehatan Dunia (WHO) tahun 2014 menunjukkan kanker merupakan penyebab kematian
BAB 1 PENDAHULUAN 1.1. Latar Belakang Kanker telah menjadi masalah kesehatan di dunia, termasuk di Indonesia. Data Badan Kesehatan Dunia (WHO) tahun 2014 menunjukkan kanker merupakan penyebab kematian
HASIL DAN PEMBAHASAN. Amplifikasi Gen Pituitary-Specific Positive Transcription Factor 1 (Pit1) Exon 3
 HASIL DAN PEMBAHASAN Amplifikasi Gen Pituitary-Specific Positive Transcription Factor 1 (Pit1) Exon 3 Amplifikasi gen Pit1 exon 3 pada sapi FH yang berasal dari BIB Lembang, BBIB Singosari, BPPT Cikole,
HASIL DAN PEMBAHASAN Amplifikasi Gen Pituitary-Specific Positive Transcription Factor 1 (Pit1) Exon 3 Amplifikasi gen Pit1 exon 3 pada sapi FH yang berasal dari BIB Lembang, BBIB Singosari, BPPT Cikole,
TINJAUAN PUSTAKA Sapi Perah Friesian Holstein
 TINJAUAN PUSTAKA Sapi Perah Friesian Holstein Sapi Friesian Holstein (FH) merupakan bangsa sapi yang paling banyak terdapat di Amerika Serikat, sekitar 80-90% dari seluruh sapi perah yang berada di sana.
TINJAUAN PUSTAKA Sapi Perah Friesian Holstein Sapi Friesian Holstein (FH) merupakan bangsa sapi yang paling banyak terdapat di Amerika Serikat, sekitar 80-90% dari seluruh sapi perah yang berada di sana.
BAB I PENDAHULUAN. A.Latar belakang. orang yang sudah meninggal, kegunaan golongan darah lebih tertuju pada
 1 BAB I PENDAHULUAN A.Latar belakang Golongan darah sistem ABO yang selanjutnya disebut golongan darah merupakan salah satu indikator identitas seseorang. Pada orang hidup, golongan darah sering digunakan
1 BAB I PENDAHULUAN A.Latar belakang Golongan darah sistem ABO yang selanjutnya disebut golongan darah merupakan salah satu indikator identitas seseorang. Pada orang hidup, golongan darah sering digunakan
BAB III METODE PENELITIAN. Secara garis besar langkah-langkah yang dilakukan dalam penelitian ini
 BAB III METODE PENELITIAN Secara garis besar langkah-langkah yang dilakukan dalam penelitian ini adalah: pengumpulan sampel; lisis terhadap sampel mtdna yang telah diperoleh; amplifikasi daerah D-loop
BAB III METODE PENELITIAN Secara garis besar langkah-langkah yang dilakukan dalam penelitian ini adalah: pengumpulan sampel; lisis terhadap sampel mtdna yang telah diperoleh; amplifikasi daerah D-loop
BAB III METODOLOGI PENELITIAN. Pada penelitian ini terdapat lima tahapan penelitian yang dilakukan yaitu
 BAB III METODOLOGI PENELITIAN Pada penelitian ini terdapat lima tahapan penelitian yang dilakukan yaitu pengumpulan sampel berupa akar rambut, ekstraksi mtdna melalui proses lisis akar rambut, amplifikasi
BAB III METODOLOGI PENELITIAN Pada penelitian ini terdapat lima tahapan penelitian yang dilakukan yaitu pengumpulan sampel berupa akar rambut, ekstraksi mtdna melalui proses lisis akar rambut, amplifikasi
HASIL DAN PEMBAHASAN. Gambar 4. Hasil Amplifikasi Gen FSHR Alu-1pada gel agarose 1,5%.
 HASIL DAN PEMBAHASAN Amplifikasi Gen FSHR Alu-1 Amplifikasi fragmen gen FSHR Alu-1 dengan metode Polymerase Chain Reaction (PCR) dilakukan dengan kondisi annealing 60 C selama 45 detik dan diperoleh produk
HASIL DAN PEMBAHASAN Amplifikasi Gen FSHR Alu-1 Amplifikasi fragmen gen FSHR Alu-1 dengan metode Polymerase Chain Reaction (PCR) dilakukan dengan kondisi annealing 60 C selama 45 detik dan diperoleh produk
KARAKTERISTIK GAMBARAN HISTOPATOLOGI PENDERITA KANKER PAYUDARA BERDASARKAN UMUR DI KOTA MEDAN PERIODE
 KARAKTERISTIK GAMBARAN HISTOPATOLOGI PENDERITA KANKER PAYUDARA BERDASARKAN UMUR DI KOTA MEDAN PERIODE 2010-2012 Oleh : NATHANIA VICKI RIANA 100100066 FAKULTAS KEDOKTERAN UNIVERSITAS SUMATERA UTARA MEDAN
KARAKTERISTIK GAMBARAN HISTOPATOLOGI PENDERITA KANKER PAYUDARA BERDASARKAN UMUR DI KOTA MEDAN PERIODE 2010-2012 Oleh : NATHANIA VICKI RIANA 100100066 FAKULTAS KEDOKTERAN UNIVERSITAS SUMATERA UTARA MEDAN
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN A. Jenis Penelitian deskriptif. Jenis penelitian yang digunakan adalah penelitian dasar dengan metode B. Objek Penelitian Objek penelitian ini adalah sampel DNA koleksi hasil
BAB III METODE PENELITIAN A. Jenis Penelitian deskriptif. Jenis penelitian yang digunakan adalah penelitian dasar dengan metode B. Objek Penelitian Objek penelitian ini adalah sampel DNA koleksi hasil
Abstrak Thesis Mochamad Syaiful Rijal Hasan G
 Abstrak Thesis Mochamad Syaiful Rijal Hasan G352090161 Mochamad Syaiful Rijal Hasan. Achmad Farajallah, dan Dyah Perwitasari. 2011. Polymorphism of fecundities genes (BMPR1B and BMP15) on Kacang, Samosir
Abstrak Thesis Mochamad Syaiful Rijal Hasan G352090161 Mochamad Syaiful Rijal Hasan. Achmad Farajallah, dan Dyah Perwitasari. 2011. Polymorphism of fecundities genes (BMPR1B and BMP15) on Kacang, Samosir
KARYA TULIS ILMIAH HUBUNGAN OVEREKSPRESI HUMAN EPIDERMAL GROWTH FACTOR RECEPTOR 2 (HER-2) DENGAN USIA PADA PASIEN KANKER PAYUDARA
 KARYA TULIS ILMIAH HUBUNGAN OVEREKSPRESI HUMAN EPIDERMAL GROWTH FACTOR RECEPTOR 2 (HER-2) DENGAN USIA PADA PASIEN KANKER PAYUDARA Diajukan untuk Memenuhi Sebagian Syarat Memperoleh Derajat Sarjana Kedokteran
KARYA TULIS ILMIAH HUBUNGAN OVEREKSPRESI HUMAN EPIDERMAL GROWTH FACTOR RECEPTOR 2 (HER-2) DENGAN USIA PADA PASIEN KANKER PAYUDARA Diajukan untuk Memenuhi Sebagian Syarat Memperoleh Derajat Sarjana Kedokteran
HALAMAN PENGESAHAN KTI HUBUNGAN OVEREKSPRESI HUMAN EPIDERMAL GROWTH FACTOR RECEPTOR 2 (HER-2) DENGAN GRADE HISTOLOGI PADA PASIEN KANKER PAYUDARA
 HALAMAN PENGESAHAN KTI HUBUNGAN OVEREKSPRESI HUMAN EPIDERMAL GROWTH FACTOR RECEPTOR 2 (HER-2) DENGAN GRADE HISTOLOGI PADA PASIEN KANKER PAYUDARA Disusun Oleh: AFIF ARIYANWAR 20130310063 Telah disetujui
HALAMAN PENGESAHAN KTI HUBUNGAN OVEREKSPRESI HUMAN EPIDERMAL GROWTH FACTOR RECEPTOR 2 (HER-2) DENGAN GRADE HISTOLOGI PADA PASIEN KANKER PAYUDARA Disusun Oleh: AFIF ARIYANWAR 20130310063 Telah disetujui
YOHANES NOVI KURNIAWAN KONSTRUKSI DAERAH PENGKODE INTERFERON ALFA-2B (IFNα2B) DAN KLONINGNYA PADA Escherichia coli JM109
 YOHANES NOVI KURNIAWAN 10702026 KONSTRUKSI DAERAH PENGKODE INTERFERON ALFA-2B (IFNα2B) DAN KLONINGNYA PADA Escherichia coli JM109 Program Studi Sains dan Teknologi Farmasi INSTITUT TEKNOLOGI BANDUNG 2007
YOHANES NOVI KURNIAWAN 10702026 KONSTRUKSI DAERAH PENGKODE INTERFERON ALFA-2B (IFNα2B) DAN KLONINGNYA PADA Escherichia coli JM109 Program Studi Sains dan Teknologi Farmasi INSTITUT TEKNOLOGI BANDUNG 2007
BAB I PENDAHULUAN. Kanker merupakan penyebab kematian utama yang memberikan kontribusi
 1 BAB I PENDAHULUAN 1.1 Latar Belakang Kanker merupakan penyebab kematian utama yang memberikan kontribusi 13% kematian dari 22% kematian akibat penyakit tidak menular utama di dunia (Shibuya et al., 2006).
1 BAB I PENDAHULUAN 1.1 Latar Belakang Kanker merupakan penyebab kematian utama yang memberikan kontribusi 13% kematian dari 22% kematian akibat penyakit tidak menular utama di dunia (Shibuya et al., 2006).
I. PENDAHULUAN. perempuan di dunia dan urutan pertama untuk wanita di negara sedang
 I. PENDAHULUAN Kanker serviks menduduki urutan kedua dari penyakit kanker yang menyerang perempuan di dunia dan urutan pertama untuk wanita di negara sedang berkembang (Emilia, dkk., 2010). Berdasarkan
I. PENDAHULUAN Kanker serviks menduduki urutan kedua dari penyakit kanker yang menyerang perempuan di dunia dan urutan pertama untuk wanita di negara sedang berkembang (Emilia, dkk., 2010). Berdasarkan
I. PENDAHULUAN. sehingga berpengaruh pada kondisi kesehatan dan kemungkinan mengakibatkan. berbagai penyakit-penyakit yang dapat dialaminya.
 I. PENDAHULUAN 1.1 Latar Belakang Kesehatan merupakan faktor penting dalam menunjang segala aktifitas hidup seseorang. Namun banyak orang yang menganggap remeh sehingga mengabaikan kesehatan dengan berbagai
I. PENDAHULUAN 1.1 Latar Belakang Kesehatan merupakan faktor penting dalam menunjang segala aktifitas hidup seseorang. Namun banyak orang yang menganggap remeh sehingga mengabaikan kesehatan dengan berbagai
Saintek Vol 5, No 6, Tahun 2010 POLYMERASE CHAIN REACTION (PCR) Zuhriana K.Yusuf
 Saintek Vol 5, No 6, Tahun 2010 POLYMERASE CHAIN REACTION (PCR) Zuhriana K.Yusuf Staf Pengajar Jurusan Kesehatan Masyarakat FIKK Universitas Negeri Gorontalo Abstrak (Polymerase Chain Reaction, PCR) adalah
Saintek Vol 5, No 6, Tahun 2010 POLYMERASE CHAIN REACTION (PCR) Zuhriana K.Yusuf Staf Pengajar Jurusan Kesehatan Masyarakat FIKK Universitas Negeri Gorontalo Abstrak (Polymerase Chain Reaction, PCR) adalah
HASIL DAN PEMBAHASAN. Uji Kualitatif dan Kuantitatif Hasil Isolasi RNA
 6 konsentrasinya. Untuk isolasi kulit buah kakao (outer pod wall dan inner pod wall) metode sama seperti isolasi RNA dari biji kakao. Uji Kualitatif dan Kuantitatif Hasil Isolasi RNA Larutan RNA hasil
6 konsentrasinya. Untuk isolasi kulit buah kakao (outer pod wall dan inner pod wall) metode sama seperti isolasi RNA dari biji kakao. Uji Kualitatif dan Kuantitatif Hasil Isolasi RNA Larutan RNA hasil
BAB III METODE PENELITIAN. Penelitian ini merupakan penelitian eksperimental dengan 7 sampel dari 7
 BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian ini merupakan penelitian eksperimental dengan 7 sampel dari 7 individu udang Jari yang diambil dari Segara Anakan Kabupaten Cilacap Jawa Tengah.
BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian ini merupakan penelitian eksperimental dengan 7 sampel dari 7 individu udang Jari yang diambil dari Segara Anakan Kabupaten Cilacap Jawa Tengah.
Teknik-teknik Dasar Bioteknologi
 Teknik-teknik Dasar Bioteknologi Oleh: TIM PENGAMPU Program Studi Agroteknologi Fakultas Pertanian Universitas Jember Tujuan Perkuliahan 1. Mahasiswa mengetahui macam-macam teknik dasar yang digunakan
Teknik-teknik Dasar Bioteknologi Oleh: TIM PENGAMPU Program Studi Agroteknologi Fakultas Pertanian Universitas Jember Tujuan Perkuliahan 1. Mahasiswa mengetahui macam-macam teknik dasar yang digunakan
ABSTRAK. OPTIMASI AMPLIFIKASI GEN flic DENGAN METODE PCR UNTUK DETEKSI Salmonella typhi GALUR INDONESIA
 ABSTRAK OPTIMASI AMPLIFIKASI GEN flic DENGAN METODE PCR UNTUK DETEKSI Salmonella typhi GALUR INDONESIA T. Robertus, 2007. Pembimbing I : Johan Lucianus, dr., M.Si. Pembimbing II : Ernawati Arifin Giri
ABSTRAK OPTIMASI AMPLIFIKASI GEN flic DENGAN METODE PCR UNTUK DETEKSI Salmonella typhi GALUR INDONESIA T. Robertus, 2007. Pembimbing I : Johan Lucianus, dr., M.Si. Pembimbing II : Ernawati Arifin Giri
MUTASI EGFR PADA PEMERIKSAAN SITOLOGI ADENOKARSINOMA PARU
 MUTASI EGFR PADA PEMERIKSAAN SITOLOGI ADENOKARSINOMA PARU Tinjauan terhadap faktor usia, jenis kelamin, dan kebiasaan merokok Ika Kustiyah Oktaviyanti Bagian Patologi Anatomi Fakultas Kedokteran Universitas
MUTASI EGFR PADA PEMERIKSAAN SITOLOGI ADENOKARSINOMA PARU Tinjauan terhadap faktor usia, jenis kelamin, dan kebiasaan merokok Ika Kustiyah Oktaviyanti Bagian Patologi Anatomi Fakultas Kedokteran Universitas
BAB I. PENDAHULUAN. I.1. Latar Belakang. prevalensinya yang signifikan dalam 30 tahun terakhir. Prevalensi overweight dan
 BAB I. PENDAHULUAN I.1. Latar Belakang Obesitas telah menarik perhatian masyarakat dunia karena peningkatan prevalensinya yang signifikan dalam 30 tahun terakhir. Prevalensi overweight dan obesitas meningkat
BAB I. PENDAHULUAN I.1. Latar Belakang Obesitas telah menarik perhatian masyarakat dunia karena peningkatan prevalensinya yang signifikan dalam 30 tahun terakhir. Prevalensi overweight dan obesitas meningkat
REKAYASA GENETIKA. By: Ace Baehaki, S.Pi, M.Si
 REKAYASA GENETIKA By: Ace Baehaki, S.Pi, M.Si Dalam rekayasa genetika DNA dan RNA DNA (deoxyribonucleic Acid) : penyimpan informasi genetika Informasi melambangkan suatu keteraturan kebalikan dari entropi
REKAYASA GENETIKA By: Ace Baehaki, S.Pi, M.Si Dalam rekayasa genetika DNA dan RNA DNA (deoxyribonucleic Acid) : penyimpan informasi genetika Informasi melambangkan suatu keteraturan kebalikan dari entropi
HASIL DAN PEMBAHASAN
 HASIL DAN PEMBAHASAN Virus Hepatitis B Gibbon Regio Pre-S1 Amplifikasi Virus Hepatitis B Regio Pre-S1 Hasil amplifikasi dari 9 sampel DNA owa jawa yang telah berstatus serologis positif terhadap antigen
HASIL DAN PEMBAHASAN Virus Hepatitis B Gibbon Regio Pre-S1 Amplifikasi Virus Hepatitis B Regio Pre-S1 Hasil amplifikasi dari 9 sampel DNA owa jawa yang telah berstatus serologis positif terhadap antigen
2.3.2 Faktor Risiko Prognosis...16 BAB III KERANGKA BERPIKIR DAN KONSEP PENELITIAN Kerangka Berpikir
 DAFTAR ISI SAMPUL DALAM... i LEMBAR PERSETUJUAN PEMBIMBING.... ii PENETAPAN PANITIA PENGUJI... iii PERNYATAAN KEASLIAN PENELITIAN... iv ABSTRAK...v ABSTRACT... vi RINGKASAN... vii SUMMARY... viii KATA
DAFTAR ISI SAMPUL DALAM... i LEMBAR PERSETUJUAN PEMBIMBING.... ii PENETAPAN PANITIA PENGUJI... iii PERNYATAAN KEASLIAN PENELITIAN... iv ABSTRAK...v ABSTRACT... vi RINGKASAN... vii SUMMARY... viii KATA
TUGAS TERSTRUKTUR BIOTEKNOLOGI PERTANIAN VEKTOR DNA
 TUGAS TERSTRUKTUR BIOTEKNOLOGI PERTANIAN VEKTOR DNA Oleh: Gregorius Widodo Adhi Prasetyo A2A015009 KEMENTERIAN RISET TEKNOLOGI DAN PENDIDIKAN TINGGI UNIVERSITAS JENDERAL SOEDIRMAN FAKULTAS PERTANIAN PROGRAM
TUGAS TERSTRUKTUR BIOTEKNOLOGI PERTANIAN VEKTOR DNA Oleh: Gregorius Widodo Adhi Prasetyo A2A015009 KEMENTERIAN RISET TEKNOLOGI DAN PENDIDIKAN TINGGI UNIVERSITAS JENDERAL SOEDIRMAN FAKULTAS PERTANIAN PROGRAM
BAB I PENDAHULUAN. Selama tiga dasawarsa terakhir, kanker ovarium masih merupakan masalah
 1 BAB I PENDAHULUAN 1.1 Latar Belakang Masalah Selama tiga dasawarsa terakhir, kanker ovarium masih merupakan masalah kesehatan perempuan di dunia, termasuk Indonesia. Hal ini terkait dengan tingginya
1 BAB I PENDAHULUAN 1.1 Latar Belakang Masalah Selama tiga dasawarsa terakhir, kanker ovarium masih merupakan masalah kesehatan perempuan di dunia, termasuk Indonesia. Hal ini terkait dengan tingginya
BAB II TINJAUAN PUSTAKA
 5 BAB II TIJAUA PUSTAKA A. Kanker dan Kanker Payudara Kanker adalah suatu penyakit yang ditandai dengan adanya abnormalitas regulasi pertumbuhan sel dan meyebabkan sel dapat berinvasi ke jaringan serta
5 BAB II TIJAUA PUSTAKA A. Kanker dan Kanker Payudara Kanker adalah suatu penyakit yang ditandai dengan adanya abnormalitas regulasi pertumbuhan sel dan meyebabkan sel dapat berinvasi ke jaringan serta
BAB I PENDAHULUAN. A. Latar Belakang. Karsinoma larings merupakan keganasan yang cukup sering dan bahkan
 BAB I PENDAHULUAN A. Latar Belakang Karsinoma larings merupakan keganasan yang cukup sering dan bahkan kedua tersering pada keganasan daerah kepala leher di beberapa Negara Eropa (Chu dan Kim 2008). Rata-rata
BAB I PENDAHULUAN A. Latar Belakang Karsinoma larings merupakan keganasan yang cukup sering dan bahkan kedua tersering pada keganasan daerah kepala leher di beberapa Negara Eropa (Chu dan Kim 2008). Rata-rata
DAFTAR ISI. LEMBAR PERSETUJUAN PEMBIMBING... ii PENETAPAN PANITIA PENGUJI... iii
 DAFTAR ISI Halaman SAMPUL DALAM... i LEMBAR PERSETUJUAN PEMBIMBING.... ii PENETAPAN PANITIA PENGUJI... iii PERNYATAAN KEASLIAN PENELITIAN... iv ABSTRAK...v ABSTRACT... vi KATA PENGANTAR... vii DAFTAR ISI...
DAFTAR ISI Halaman SAMPUL DALAM... i LEMBAR PERSETUJUAN PEMBIMBING.... ii PENETAPAN PANITIA PENGUJI... iii PERNYATAAN KEASLIAN PENELITIAN... iv ABSTRAK...v ABSTRACT... vi KATA PENGANTAR... vii DAFTAR ISI...
BAB I PENDAHULUAN. yang ditandai dengan meningkatnya sel myeloid (Perrotti et al., 2010). Di Asia,
 BAB I PENDAHULUAN I.1. Latar Belakang Chronic myelogenous leukemia (CML) merupakan keganasan hematologi yang ditandai dengan meningkatnya sel myeloid (Perrotti et al., 2010). Di Asia, CML merupakan keganasan
BAB I PENDAHULUAN I.1. Latar Belakang Chronic myelogenous leukemia (CML) merupakan keganasan hematologi yang ditandai dengan meningkatnya sel myeloid (Perrotti et al., 2010). Di Asia, CML merupakan keganasan
BAB III BAHAN DAN CARA KERJA. Penelitian dilakukan di Laboratorium Institute of Human Virology and
 23 BAB III BAHAN DAN CARA KERJA A. LOKASI DAN WAKTU PENELITIAN Penelitian dilakukan di Laboratorium Institute of Human Virology and Cancer Biology of the University of Indonesia (IHVCB-UI), Jl. Salemba
23 BAB III BAHAN DAN CARA KERJA A. LOKASI DAN WAKTU PENELITIAN Penelitian dilakukan di Laboratorium Institute of Human Virology and Cancer Biology of the University of Indonesia (IHVCB-UI), Jl. Salemba
I. PENDAHULUAN. Jenis kelamin menjadi salah satu studi genetik yang menarik pada tanaman
 I. PENDAHULUAN 1.1 Latar Belakang Jenis kelamin menjadi salah satu studi genetik yang menarik pada tanaman dioecious. Jenis kelamin betina menjamin keberlangsungan hidup suatu individu, dan juga penting
I. PENDAHULUAN 1.1 Latar Belakang Jenis kelamin menjadi salah satu studi genetik yang menarik pada tanaman dioecious. Jenis kelamin betina menjamin keberlangsungan hidup suatu individu, dan juga penting
BAB 1 PENDAHULUAN. wanita dan merupakan kanker kelima paling sering pada wanita di seluruh dunia
 BAB 1 PENDAHULUAN 1.1 Latar Belakang Kanker endometrium adalah kanker paling sering pada saluran genitalia wanita dan merupakan kanker kelima paling sering pada wanita di seluruh dunia setelah payudara,
BAB 1 PENDAHULUAN 1.1 Latar Belakang Kanker endometrium adalah kanker paling sering pada saluran genitalia wanita dan merupakan kanker kelima paling sering pada wanita di seluruh dunia setelah payudara,
ABSTRAK. Analisis Mutasi Gen Pengekspresi Domain B dan C DNA Polimerase HBV Dari Pasien Yang Terinfeksi Dengan Titer Rendah.
 ABSTRAK Analisis Mutasi Gen Pengekspresi Domain B dan C DNA Polimerase HBV Dari Pasien Yang Terinfeksi Dengan Titer Rendah. Natalia, 2006 Pembimbing Utama Pembimbing Pendamping : Johan Lucianus, dr., M.Si.
ABSTRAK Analisis Mutasi Gen Pengekspresi Domain B dan C DNA Polimerase HBV Dari Pasien Yang Terinfeksi Dengan Titer Rendah. Natalia, 2006 Pembimbing Utama Pembimbing Pendamping : Johan Lucianus, dr., M.Si.
D. Kerangka Teori E. Kerangka Konsep F. Hipotesis... 36
 vi DAFTAR ISI HALAMAN JUDUL... i LEMBAR PENGESAHAN... ii PERNYATAAN... iii KATA PENGANTAR... iv DAFTAR ISI... vi DAFTAR TABEL... viii DAFTAR GAMBAR... ix DAFTAR SINGKATAN... x INTISARI... xi ABSTRACT...
vi DAFTAR ISI HALAMAN JUDUL... i LEMBAR PENGESAHAN... ii PERNYATAAN... iii KATA PENGANTAR... iv DAFTAR ISI... vi DAFTAR TABEL... viii DAFTAR GAMBAR... ix DAFTAR SINGKATAN... x INTISARI... xi ABSTRACT...
BAB I PENDAHULUAN. Kanker payudara merupakan jenis keganasan terbanyak pada wanita
 BAB I PENDAHULUAN 1.1 Latar Belakang Kanker payudara merupakan jenis keganasan terbanyak pada wanita diseluruh dunia dan menjadi penyebab kematian tertinggi kedua setelah kanker paru-paru. Kanker payudara
BAB I PENDAHULUAN 1.1 Latar Belakang Kanker payudara merupakan jenis keganasan terbanyak pada wanita diseluruh dunia dan menjadi penyebab kematian tertinggi kedua setelah kanker paru-paru. Kanker payudara
SUHARTO WIJANARKO PERTEMUAN ILMIAH TAHUNAN (PIT) KE-21 TAHUN 2016 PERHIMPUNAN DOKTER SPESIALIS BEDAH INDONESIA (IKABI) MEDAN, 12 AGUSTUS 2016
 SUHARTO WIJANARKO PERTEMUAN ILMIAH TAHUNAN (PIT) KE-21 TAHUN 2016 PERHIMPUNAN DOKTER SPESIALIS BEDAH INDONESIA (IKABI) MEDAN, 12 AGUSTUS 2016 BSK sudah lama diketahui diderita manusia terbukti ditemukan
SUHARTO WIJANARKO PERTEMUAN ILMIAH TAHUNAN (PIT) KE-21 TAHUN 2016 PERHIMPUNAN DOKTER SPESIALIS BEDAH INDONESIA (IKABI) MEDAN, 12 AGUSTUS 2016 BSK sudah lama diketahui diderita manusia terbukti ditemukan
DAFTAR ISI DAFTAR TABEL... DAFTAR GAMBAR... DAFTAR LAMPIRAN...
 DAFTAR ISI Bab Halaman DAFTAR TABEL... DAFTAR GAMBAR... DAFTAR LAMPIRAN... ix x xii I II III PENDAHULUAN 1.1 Latar Belakang... 1 1.2 Identifikasi Masalah... 2 1.3 Tujuan Penelitian... 2 1.4 Kegunaan Penelitian...
DAFTAR ISI Bab Halaman DAFTAR TABEL... DAFTAR GAMBAR... DAFTAR LAMPIRAN... ix x xii I II III PENDAHULUAN 1.1 Latar Belakang... 1 1.2 Identifikasi Masalah... 2 1.3 Tujuan Penelitian... 2 1.4 Kegunaan Penelitian...
BAB 1 PENDAHULUAN. dari semua kanker pada organ reproduksi. Diantara kanker yang ditemukan pada
 1 BAB 1 PENDAHULUAN 1.1. Latar Belakang Penelitian Kanker ovarium adalah kanker ginekologi yang dijumpai hampir 30% dari semua kanker pada organ reproduksi. Diantara kanker yang ditemukan pada perempuan,
1 BAB 1 PENDAHULUAN 1.1. Latar Belakang Penelitian Kanker ovarium adalah kanker ginekologi yang dijumpai hampir 30% dari semua kanker pada organ reproduksi. Diantara kanker yang ditemukan pada perempuan,
IDENTIFIKASI KERAGAMAN GEN PITUITARY SPECIFIC POSITIVE TRANSCRIPTION FACTOR
 IDENTIFIKASI KERAGAMAN GEN PITUITARY SPECIFIC POSITIVE TRANSCRIPTION FACTOR 1 (PIT1) PADA KERBAU LOKAL (Bubalus bubalis) DAN SAPI FH (Friesian-Holstein) SKRIPSI RESTU MISRIANTI DEPARTEMEN ILMU PRODUKSI
IDENTIFIKASI KERAGAMAN GEN PITUITARY SPECIFIC POSITIVE TRANSCRIPTION FACTOR 1 (PIT1) PADA KERBAU LOKAL (Bubalus bubalis) DAN SAPI FH (Friesian-Holstein) SKRIPSI RESTU MISRIANTI DEPARTEMEN ILMU PRODUKSI
BAB I PENDAHULUAN. Karsinoma payudara merupakan kanker yang paling. sering pada wanita di negara maju dan berkembang, dan
 BAB I PENDAHULUAN I.1. Latar Belakang Karsinoma payudara merupakan kanker yang paling sering pada wanita di negara maju dan berkembang, dan merupakan penyebab kematian kedua pada wanita setelah kanker
BAB I PENDAHULUAN I.1. Latar Belakang Karsinoma payudara merupakan kanker yang paling sering pada wanita di negara maju dan berkembang, dan merupakan penyebab kematian kedua pada wanita setelah kanker
