III. METODE PENELITIAN. Penelitian ini dilaksanakan pada Maret sampai Mei Lokasi pengambilan
|
|
|
- Hengki Sudirman
- 6 tahun lalu
- Tontonan:
Transkripsi
1 III. METODE PENELITIAN 3.1. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada Maret sampai Mei Lokasi pengambilan sampel meliputi wilayah Kalianda Kabupaten Lampung Selatan yang melalui pengamatan di Laboratorium Budidaya Perikanan Universitas Lampung dan Stasiun Karantina Ikan, Pengendalian Mutu dan Keamanan Hasil Perikanan Kelas I Lampung Peralatan dan Bahan Tabel. 3. Alat dan Bahan Uji PCR Alat Bahan PCR Sampel udang windu dan udang vannamei Alat bedah Lysis Buffer Cold box DNA molecular weight marker Microtube 1.5 ml Larutan kloroform (CHCl3 ) Microtube 0.2 ml Dissolving solution Timbangan digital Larutan RNA extraction Vortex Etanol 95 % Mikropipet Larutan DEPC DDH2O Water bath First PCR premix Thermalcycler RT-PCR premix Aluminium foil Iqzyme DNA polymerase Microwave NaCl fisiologis Tangki elektroforesis P(+) standard WSSV Uv transilluminator Kontrol negatif (yeast trna) Gelred 1x TAE Buffer 6x loading dye 38
2 Tabel. 4. Alat dan Bahan Pengamatan Kualitas Benih Udang Alat Mikroskop Akuarium Cold box Beaker glass Senter atau lampu pijar Kaca preparat Cawan petri Sprider Tabung reaksi Timbangan digital Bahan Sampel udang windu dan vannamei Media TCBS 3.3. Prosedur Penelitian Data dikumpulkan melalui teknik wawancara, metode dokumentasi, penentuan lokasi pengambilan sampel, pengamatan kesehatan dan identifikasi penyakit Wawancara Wawancara dilakukan untuk memperoleh berbagai informasi yang dibutuhkan dalam penelitian (Lampiran 1). Wawancara dilakukan kepada teknisi atau pemilik panti benih mengenai fasilitas, air dan udang, manajemen karantina, kesehatan udang, manajemen pemeliharaan dan manajemen personil. Wawancara dilakukan untuk memperoleh hasil penerapan manajemen kesehatan udang yang diterapkan pada masing-masing panti benih. Adapun kriteria wawancara pada panti benih antara lain : Air dan Benur Air merupakan media hidup dari benih udang yang menjadi unsur terpenting bagi kelangsungan hidup benih udang. Sedangkan benur (benih udang) merupakan organisme budidaya yang akan dibudidayakan. Benih udang yang baik dihasilkan 39
3 dari indukan yang baik juga. Kriteria air dan benih udang yang baik antara lain : menggunakan sumber air yang bebas dari hewan air lainnya, air difilter terlebih dahulu menggunakan filter dengan ukuran kecil untuk mencegah telur atau larva hewan masuk melalui air, air diperlakukan desinfeksi yang dirancang untuk mematikan karier udang liar, air yang telah dipersiapkan untuk budidaya telah dipastikan tidak terdapat potensi karier patogen tertentu, fasilitas budidaya dirancang untuk mencegah transmisi patogen melalui udara dari sumber air yang masuk, fasilitas budidaya dirancang untuk mencegah transmisi patogen dari sekitar panti benih dan sumber air yang masuk, naupli yang dipelihara dalam fasilitas budidaya bersertifikat bebas dari patogen target, naupli dikarantina dahulu setelah sampai di fasilitas budidaya, naupli dipindahkan dari dalam panti benih selama transportasi atau kotak kemasan tidak menggunakan air yang berasal dari tempat asal Karantina Karantina merupakan sistem yang menanggulangi penularan penyakit dengan cara mengisolasi penyakit agar tidak menginfeksi organisme yang lain. Kriteria karantina antara lain : sistem karantina udang atau udang sakit dirancang lebih awal sesuai dengan prosedur operasional standar perusahaan terhadap panti benih, petak karantina dibedakan pada ruang, gedung, atau area yang terisolasi secara fisik dengan panti benih produksi, karantina digunakan secara tersendiri (isolasi), dengan mengunakan sumber air dan pembuangan air yang terpisah dari panti benih produksi, apakah naupli atau telur baru diaklimatisasi untuk diobservasi ketidaknormalan dalam tingkah laku dan perubahan badan dan untuk mengkonfirmasi konsumsi pakannya, 40
4 Saat benih udang teramati tidak normal, apakah sampel benih udangnya diuji, benih udang normal diambil sampelnya untuk diuji pada target patogen tertentu (parasit, bakteri, dan virus), sampel benih udang yang mati (masih segar) dan hidup diambil setiap waktu tertentu, udang yang dipelihara dalam kondisi kepadatan yang sama, pengelola, operator mencuci tangan sampai lengan sebelum pergi antara wilayah sistem karantina dan produksi, operator panti benih bekerja pada panti benih tertentu yang sudah menjadi bagian tanpa bekerja di bagian lain, peralatan karantina hanya digunakan dalam wilayah sistem karantina Kesehatan Udang Kesehatan udang merupakan faktor-faktor akumulasi dan sinergi antara beberapa bidang ilmu parsial (penyakit, nutrisi, kualitas air, dan keteknikan) dengan tindakan manajemen sehingga mewujudkan satu kesatuan aksi yang potensial dapat mencegah dan mengurangi akibat dari penyakit ikan. Kriteria untuk kesehatan udang antara lain : pengawasan kesehatan udang direncanakan bersama manajemen fasilitas budidaya, kualitas air diawasi dan diatur untuk kondisi yang sesuai dengan kebutuhan udang, kualitas pakan disediakan untuk memberikan status nutrisi yang optimal untuk pertumbuhan, naupli dibeli berasal dari induk yang berusia produktif pada masa pematangan yang optimal, bahan kimia yang digunakan untuk pencegahan penyakit dalam sistem manajemen yang baik, pakan bervitamin digunakan untuk pencegahan penyakit dalam sistem manajemen yang baik, obat-obatan termasuk antibiotik digunakan untuk pencegahan penyakit, benih udang abnormal, sakit, dan mati dibunuh untuk mencegah menyebarnya patogen. 41
5 Pemeliharaan Pemeliharaan merupakan tahapan benih udang untuk di pelihara untuk mencapai ukuran tertentu dengan pertambahan berat dan panjang serta menghindari kontaminasi dengan patogen. Kriteria pemeliharaan yang baik antara lain : tempat pencucian alas kaki disediakan pada saat memasuki area produksi dan dibersihkan dan larutan diganti pada waktu tertentu, operator mencuci tangan dan lengan sebelum memasuki daerah budidaya, tersedia wilayah untuk desinfeksi dan mencuci perlengkapan budidaya seperti ember, baskom, jaring, pengukur oksigen terlarut, termometer dan perlengkapan lainnya, peralatan yang sudah bersih sudah disediakan tempat tertentu, prosedur pemeliharaan dibuat untuk semua tahapan seperti pembuangan feses, pakan sisa, algae, tanaman air, udang mati dan buangan terdekomposisi dari dasar bak, pipa kedalam dan pipa keluar, peralatan aerasi, pipa oksigen dan peralatan lain dalam petak bak, tangan dicuci dengan sabun mengandung desinfektan pada saat bekerja pada bagian pemeliharaan yang berbeda, terdapat jadwal bekerja pada pemberian pakan benih udang, pada bak panti benih yang sama dalam siklus produksi, setiap bak panti benih diperlakukan terpisah untuk mengetahui meminimalisasi potensi kontaminasi silang pada patogen, peralatan didesinfeksi sebelum digunakan untuk bak panti benih yang berbeda, lingkungan tambak diberi keterangan terkontaminasi dan dibersihkan dengan benar, semua bagian dari sistem pemeliharaan diinspeksi dan dibersihkan, setidaknya satu bulan sekali, lingkungan panti benih yang bersih menjadi kebiasaan, terdapat waktu 42
6 tertentu untuk membersihkan lingkungan panti benih secara keseluruhan, binatang peliharaan, rodensia, burung, dan vertebrata lain berada diluar wilayah budidaya Manajemen Personil Manajemen personil merupakan proses penting dalam menjalankan budidaya setiap pembudidaya harus menaati peraturan dan menjaga bak pemeliharaan agak tidak terkontaminasi. Kriteria dalam manajemen personil antara lain : terdapat prosedur operasional standar untuk operator panti benih atau pegawai lain untuk penerapan biosekuritas dan manajemen kesehatan, membersihkan diri misalnya mencuci tangan dan lengan dengan sabun antibakteri merupakan standar kerja, jadwal kerja diatur untuk memperkecil jumlah orang yang berbeda bekerja pada petak panti benih, kendaraan di desinfeksi sebelum masuk dalam wilayah budidaya, parkir kendaraan pengunjung sudah disesuaikan dengan tempat yang tersedia jauh dari fasilitas budidaya, akses bak panti benih terlarang untuk jumlah orang yang banyak, jumlah kunjungan diperkecil dan terbatas untuk jumlah sedikit untuk mempermudah pengaturan kelompok orang, terdapat pencatatan setiap kejadian pada setiap bak pemeliharaan, pengunjung dihimbau untuk membersihkan diri misalnya mencuci tangan dan lengan dengan sabun antibakteri selama kunjungan, pengunjung dihimbau untuk tidak memegang apapun dalam panti benih. Setelah jam kunjungan bak pencuci alas kaki dan lantai dibersihkan. 43
7 Metode Dokumentasi Metode dokumentasi merupakan metode yang digunakan untuk mengumpulkan data sekunder, meliputi foto-foto fasilitas panti benih, bak pemeliharaan benih udang, sistem biosekuriti dan lingkungan Penentuan Lokasi Pengambilan Sampel Sampel diambil di Kalianda Lampung selatan yang terdiri dari 4 desa yaitu Canti, Banding, Rajabasa dan Way Muli. Sampel diambil setelah proses wawancara pada stadia naupli, fase zoea, fase mysis, dan post larva pada panti benih udang windu dan vannamei di pesisir Lampung Selatan Pengambilan Sampel Sampel diambil secara acak dalam bak pemeliharaan benih pada setiap lokasi. Pengambian dengan alat tangkap berupa jaring. Sampel diambil dari bak pemeliharaan dalam keadaan hidup dan langsung dimasukkan ke dalam plastik yang berisi air Pengamatan Kesehatan Benih Udang Udang diamati dengan menggunakan mikroskop dan diamati didalam laboratorium. adapun kriteria dan prosedur pengamatan yang dilakukan pada kesehatan benih antara lain : 44
8 A. Respon Cahaya Adapun proses pengamatannya antara lain : 1. Sampel diambil larva atau post larva diambil sebanyak 100 ekor 2. Sampel larva atau post larva di letakkan pada beaker glass yang telah diisi dengan air 3. Semua cahaya dimatikan 4. Udang diamati dengan menggunakan senter antau lampu belajar 5. Persentase larva atau post larva yang mendekati cahaya dan yang menjauhi cahaya kemudian dihitung. B. Pengamatan Aktivitas Adapun proses pengamatannya antara lain : 1. Sampel diambil larva atau post larva diambil sebanyak 100 ekor 2. Sampel larva atau post larva diletakkan pada beaker glass yang telah diisi dengan air. 3. Air kemudian diberi arus searah sehingga terbentuk arus. 4. Sampel diamati dan dihitung persentase larva yang aktif melawan arus dan yang mengikuti arus 5. Prevalensi larva atau post larva yang lemah dihitung persentasenya. 45
9 C. Pengamatan Feeding Rate Adapun proses pengamatannya antara lain : 1. Sampel diambil sebanyak minimal 30 ekor dengan menggunakan pipet tetes atau disaring kedalam mangkok pisin (untuk stadia PL), diletakkan pada kaca objek. 2. Sampel larva atau post larva diamati dengan menggunakan mikroskop hingga seluruh pencernaan terlihat jelas dengan menggunakan perbesaran 100 kali. 3. Panjang diperkirakan saluran pencernaan yang terisi yaitu : Full,1 atau 2 atau kosong. 4. Kelompokkan feeding rate tersebut dalam tiga bagian yaitu : 1 penuh atau 2 dan kosong. 5. Feeding rate dikatakan full apabila usus benih udang terisi pakan dari belakang hepatopankreas hingga melewati segmen ke 4. Dan dikatakan 1 atau 2 apabila usus benih udang terisi pakan dari belakang hepatopankreas hingga segmen ke 1 atau di segmen ke 4 dan feeding rate dikatakan kosong apabila usus benih udang kelihatan bening ( kosong atau tidak ada makanan ). 46
10 D. Pengamatan Pigmentasi Adapun proses pengamatannya antara lain : 1. Sampel diambil sebanyak minimal 30 ekor dengan menggunakan pipet tetes atau disaring ke dalam mangkok pisin dan diletakkan pada kaca objek. 2. Penampakan warna tubuh larva atau post larva terutama pada bagian mata, abdomen dan ekor diamati dengan menggunakan mikroskop perbesaran kali. 3. Pada keadaan normal warna tubuh larva atau post larva akan terlihat transparan dengan titik-titik kromatofor yang berwarna merah,biru, kuning dan oranye yang berderet di sepanjang sisi tubuh bagian bawah. Sedangkan pada kondisi yang tidak normal kromatofor akan terlihat melebar hingga seluruh bagian mata, tubuh maupun ekor. Adanya tanda-tanda erosi pada bagian luar tubuh (eksoskeleton) dikategorikan pada kelompok tubuh yang kusam (pale). 4. Prevalensi benih udang yang pigmentasinya tidak normal dihitung persentasenya. E. Parasit Adapun proses pengamatannya antara lain : 1. Sampel diambil sebanyak minimal 30 ekor dengan menggunakan pipet tetes atau disaring ke dalam mangkok pisin dan letakkan pada kaca objek 2. Sampel dibasahi dan ditutup dengan kaca penutup 47
11 3. Sampel diamati di bawah mikroskop dengan pembesaran kali pada seluruh bagian tubuh luar larva atau post larva untuk mendeteksi adanya ektoparasit dari jenis ciliophora seperti : Epistylis, Zoothamnium, Vorticella dan lain-lain. 4. Prevalensi benih udang yang terinfeksi ektoparasit dihitung persentasenya. F. Pengamatan Abnormalitas Adapun proses pengamatannya antara lain : 1. Sampel diambil sebanyak minimal 30 ekor dengan menggunakan pipet tetes atau disaring dan diletakkan pada kaca objek 2. Larva atau post larva diamati dengan menggunakan perbesaran 100 kali. 3. Seluruh bagian tubuh larva atau post larva diobservasi 4. Hasil observasi dicatat dengan membedakan jenis abnormalitas yang ditemukan G. Pengamatan Hepatopankreas Adapun proses pengamatannya antara lain : 1. Sampel diambil sebanyak minimal 30 ekor dengan menggunakan pipet tetes atau disaring ke dalam mangkok pisin dan letakkan pada kaca objek 2. Penampakan hepatopankreas larva atau post larva diamati dengan menggunakan mikroskop perbesaran kali. 3. Pada keadaan normal (Good) : Pada stadia zoea bentuk hepatopankreas seperti kupu-kupu bentuk simetris antara sisi kiri dan kanan, 48
12 Medium : Pada stadia zoea bentuk hepatopankreas tidak simetris antara sisi kiri dan kanan atau mungkin hepatopankreas menagalami pembengkakan, Bad : Hepatopankreas sudah tidak berbentuk, warna kehitaman. 4. Prevalensi benih udang yang hepatopankreasnya dihitung persentasenya. H. Pengamatan Lipid Adapun proses pengamatannya antara lain : 1. Sampel diambil sebanyak minimal 30 ekor dengan menggunakan pipet tetes atau disaring ke dalam mangkok pisin dan letakkan pada kaca objek 2. Penampakan lipid diamati pada hepatopankreas larva atau post larva dengan menggunakan mikroskop perbesaran kali High : apabila jumlah lipid banyak, sebaran merata, lipid menutupi seluruh hepatopankreas Medium : apabila jumlah lipid sangat sedang, sebaran kurang merata, atau lipid hanya menutupi sebagian hepatopankreas Low : apabila jumlah lipid sangat sedikit atau bahkan tidak ada, sebaran hanya disalah satu bagian hepato, atau lipid hanya menutupi seperempat bagian hepatopankreas. 3. Prevalensi benih udang yang hepatopankreasnya dihitung persentasenya. 49
13 Identifikasi Penyakit pada Udang Metode identifikasi penyakit pada udang dapat dilakukan dengan tiga cara, yaitu secara visual, mikroskopis dan PCR (Yanto, 2006). A. Identifikasi Secara Visual Pemeriksaan visual dapat dilakukan dengan cara mengamati secara langsung baik fisik maupun tingkah laku udang hidup, karena udang yang sakit akan memperlihatkan gejala yang berbeda dari udang sehat (Subaidah, 2006). Beberapa penyakit terutama parasit yang ukurannya besar dapat dilihat secara visual dengan menggunakan kaca pembesar. Pemeriksaan secara visual juga dapat dilakukan dengan melihat organ dalam pada udang, seperti usus dengan cara pembedahan (Afrianto,1992). Adanya infeksi penyakit dapat mengakibatkan ketidaknormalan bentuk dan warna organ dalam udang (Alifuddin,1993). 50
14 Tabel 5. Gejala Udang Terkena Penyakit Bakteri dan Parasit Bagian yang diserang Karapas dan seluruh tubuh Sistem otot dan sistem kekebalan tubuh Organ Pencernaan Antena, uropod, pleopod dan bagian tambahan lainnya Haemolymph Eksoskeleton Bentuk tubuh Daerah branchial insang Dinding proventriculus dan usus. Sepanjang syaraf bagian ventral Hepatopankreas Gejala Klinis Bercak merah dan kelihatan menyala Larva kelihatan lemah dan tidak aktif Nafsu makan menurun Mengalami luka dan berwarna coklat Terjadi defisiensi kekurangan vitamin C dan terdapat sel-sel bakteri dalam darah udang Molting tidak sempurna Bengkok menghambat perkembangan gonad pada udang Nafsu makan menurun Gerakan yang tidak terkendali Nafsu makan menurun B. Identifikasi Penyakit Secara Mikroskopis Prosedur kerja identifikasi penyakit diawali dengan mengambil sampel benih udang. Sampel udang yang diperiksa adalah udang yang menunjukkan gejala klinis terserang penyakit berupa bakteri dan parasit. Udang yang terserang penyakit kemudian dibawa ke laboratorium untuk diperiksa. Teknik pemeriksaan dan identifikasi parasit pada udang windu yaitu: 1. Sampel udang diambil kemudian dimatikan; 2. Sampel udang diletakkan pada kaca objek dan ditetesi dengan air laut dan ditutupi dengan kaca penutup; 3. Preparat diamati di bawah mikroskop dengan pembesaran. Hasil pengamatan dicocokkan pada gambar atau buku identifikasi (Afrianto, 1992). 51
15 Prosedur identifikasi penyakit oleh bakteri dilakukan dengan melihat kepadatan bakteri pada udang. Adapun prosedur kerja pengamatan bakteri antara lain dengan menggunakan metode plate count : 1. Sampel udang diambil secara acak dari bak pemeliharaan dalam keadaan hidup 2. Sampel diambil pada bagian insang dan usus 3. Sampel kemudian dimasukkan kedalam media agar TCBS 4. Kemudian sampel diinkubasi selama 24 jam 5. Biakan Agar Plate diambil dari Inkubator; 6. Dengan menggunakan Colony Counter dan Hand-Counter diamati dan dihitung koloni yang tumbuh. Jumlah koloni yang dapat dihitung berkisar antara koloni; 7. Kalkulasikan jumlah koloni terhitung dengan cara mengalikan koloni yang terhitung dengan faktor pengencernya (Dermawan et al.,2004). Kriteria bakteri dengan menggunakan metode plate count : a. Jumlah koloni rendah < 30 b. Jumlah koloni sedang c. Jumlah koloni tinggi >300 (Dermawan et al.,2004) 52
16 C. Identifikasi Sampel Dengan PCR Pengujian sampel dilakukan dengan metode Polymerase Chain Reaction yang dilaksanakan berdasarkan Instruction Manual IQ2000TM Detection and Prevention System. Prosedur yang dilakukan antara lain : 1. Ekstraksi DNA Sebanyak mg jaringan udang bisa berupa pleopod dan insang udang juvenil atau subadult hidup, postlarva 11, keseluruhan jaringan untuk postlarva 10 atau 0,1 ml haemolymph dimasukkan ke dalam mikrotube 1,5 ml. Jaringan dihancurkan dalam mikrotube dengan menggunakan pellet pastle, kemudian tambahkan 1ml DNAzol reagent. Lalu jaringan disentrifugasi pada kecepatan 10000X g selama 10 menit pada 4 o C atau suhu ruang. Supernatan hasil sentrifugasi dipindahkan ke dalam mikrotube baru, kemudian ditambahkan 0,5 ml etanol 96%. Mikrotube dibolak-balik agar tercampur lalu diamkan selama 1-3 menit pada suhu ruang. Setelah itu disentrifugasi kembali mikrotube dengan kecepatan 4000X g selama 1-2 menit pada 4 o C atau suhu ruang. Etanol 96% yang ada di dalam mikrotube dibuang sehingga hanya tersisa pellet lalu cuci pellet tersebut dengan 0,8-1 ml etanol 75% dan diamkan selama detik. Selanjutnya etanol 75% dibuang kemudian keringkan selama 5-15 detik. Pellet dicuci kembali dengan penambahan 0,8-1 ml etanol 75% dan diamkan selama detik. Etanol 75% dibuang kemudian keringkan selama 5-15 detik. Lalu pellet di dalam mikrotube ditambahkan 8 mm NaOH sebanyak 0,2-0,3 ml, kemudian dihomogenkan. Lalu pellet disimpan pada suhu -20 o C ( LULP2IL-S, 2013). 53
17 Amplifikasi PCR Konvensional Komponen-komponen PCR (master mix) berikut dimasukkan ke dalam microtube 0.2 ml : ddh2o μl, 5X PCR buffer 5 μl, 25 mm MgCl2 1.5 μl, dntps 0.5 μl, primer forward 146F1 0.5 μl, primer reverse 146R1 0.5 μl, Taq DNA Polymerase μl. Master mix disiapkan sebanyak 1,1 X dari setiap reaksi. Microtube dibagi ke dalam sampel, kontrol positif dan kontrol negatif, kemudian ditambahkan sampel DNA dan kontrol positif masing-masing sebanyak 1 μl. Microtube dimasukkan ke dalam mesin PCR, kemudian dijalankan proses amplifikasi (PCR) step 1sebagai berikut: hotstart pada suhu 95 o C selama 5 menit, denaturasi pada suhu 95 o C selama 30 detik, annealing pada suhu 52.5 o C selama 30 detik, ekstensi pada suhu 72 o C selama 1.5 menit. Siklus denaturasi-annealing-ekstensi diulang sebanyak 30 kali.siklus PCR diakhiri dengan ekstra ekstensi pada suhu 72 o C selama 5 menit.sampel hasil PCR dapat disimpan pada suhu 4 o C atau dilanjutkan ke tahap berikutnya yaitu step 2 (Nested PCR). Proses PCR kedua (nested PCR) sebanyak 1 μl larutan hasil PCR awal dimasukkan ke dalam microtube yang telah berisi master mix. Komposisi mastermix sama dengan amplifikasi tahap pertama, perbedaannya terletak pada jenis primer yang digunakan (Primer 146F2 & 146R2). Selanjutnya dijalankan kembali siklus amplifikasi PCR dengan pola siklus: hotstart pada suhu 95 o C selama 5 menit, denaturasi pada suhu 95 o C selama 30 detik, annealing pada suhu 54 o C selama 30 detik, ekstensi pada suhu 72 o C selama 1 menit. Siklus denaturasi-annealing-ekstensi diulang sebanyak 30 kali. 54
18 Siklus amplifikasi PCR diakhiri dengan ekstra ekstensi pada suhu 72 o C selama 5 menit. Hasil PCR disimpan pada suhu 4 o C dan siap untuk digunakan elektroforesis (LULP2IL-S, 2013). WSSV dideteksi dengan prosedur OIE chapter (2012). WSSV adalah virus bergenom DNA yang dapat dilakukan amplifikasi langsung setelah proses isolasi genom. Karena genom WSSV yang sangat panjang ( bp) maka untuk meningkatkan spesifisitas deteksi tahapan PCR tidak hanya dilakukan satu tahap, tetapi dua tahap dengan nested PCR (Hulten, 2001). Nested PCR adalah metode PCR yang digunakan untuk mengamplifikasi segmen DNA spesifik (target sequences) dengan menggunakan dua pasang primer. Primer pertama digunakan untuk mengamplifikasi segmen DNA yang lebih panjang dari segmen target yang mengikutsertakan segmen target di dalamnya. Siklus PCR kedua digunakan untuk mengamplifikasi segmen DNA target dengan primer spesifik yang terletak di kedua ujung segmen target. Fungsi dari nested PCR adalah untuk peningkatan spesifisitas karena kemampuan amplifikasi oleh primer kedua tergantung pada produk amplifikasi oleh primer pertama (Davidson, 2002). 2. Elektroforosis Gel Agarose dimasukkan ke dalam mesin elektroforesis horizontal. Lalu ditambahkan larutan TBE 1X ke dalam mesin elektroforesis hingga gel agarose terendam. Sebanyak 5 µl produk hasil PCR yang menggunakan 5X PCR buffercolourless diambil dan ditambahkan dengan Loading dye 6X sebanyak 1 µl dan 55
19 dicampurkan dengan baik. Kemudian hasil PCRyang telah ditambahkan larutan diatas disuntik ke dalam lubang sumur gel dengan menggunakan mikropipet. Untuk sampel PCR yang menggunakan 5X PCR buffergreen tidak perlu lagi ditambahkan dengan Loading dye 6X. Selain sampel juga dimasukkan marker sebagai penanda ukuran pita DNA. Setelah itu penutup elektroforesis dipasang lalu operasikan mesin pada 100V selama 30 menit, setelah semua sampel dimasukkan. Kemudian gel Agarose diangkat dan direndam dalam larutan Gelred TM (3X in water) selama menit. Selanjutnya bilas gel agarose dengan cara direndam kedalam akuades selama menit untuk menghentikan proses pewarnaan. Setelah itu gel agarose diamati pada UV transilluminator. Hasil positif terdeteksi WSSV bila terlihat perpendaran jauh pita DNA pada ukuran 1447 bp dan 941 bp atau 941 bp saja. Hasil negatif WSSV bila tidak terlihat perpendaran pita DNA pada ukuran 1447 bp dan 941 bp (LULP2IL-S, 2013). 4. Analisis PCR Menggunakan IQ2000TM System Virus didiagnosis menggunakan IQ2000TM System yang terdiri dari ekstraksi bahan genetik sampel.ekstraksi bertujuan memperoleh ekstraksi DNA udang maupun virus WSSV yang menginfeksi udang. Rangkaian analisis PCR yang terdiri dari First PCR dan Nested PCR bertujuan untuk memperbanyak DNA virus WSSV sesuai dengan primer yang telah disediakan. Langkah PCR yang terakhir adalah proses elektroforesis dan pembacaan hasil PCR (interpretasi) yang berupa pendaran band (pita) pada lubang-lubang kecil lempengan agarose (chip chamber). Setiap proses analisis sampel selalu disertai dengan kontrol positif dan kontrol negatif untuk 56
20 menghindari kesalahan positif (false-positive result) maupun kesalahan negatif (falsenegative result) (OIE, 2009) Parameter yang Diamati Parameter yang diamati adalah: a. Prinsip manajemen kesehatan yang diterapkan di lokasi panti benih (dengan kuisioner). b. Kualitas benih udang windu dan udang vannamei yang dihasilkan oleh panti benih yang ada di Kalianda Lampung Selatan. c. Hubungan antara penerapan manajemen kualitas benih dengan kualitas benih yang dihasilkan Analisis Data Data yang diperoleh berupa hasil kuisioner (penerapan manajemen kesehatan benih udang) dan pengamatan kualitas benur akan dianalisis secara regresi polinomial dengan menggunakan Microsoft Excel. Data hasil penelitian dianalisis untuk mengetahui hubungan antara penerapan manajemen kesehatan udang dengan kualitas benih udang yang dihasilkan oleh panti benih di Kalianda Lampung Selatan. 57
Benih udang vaname (Litopenaeus vannamei) kelas benih sebar
 Standar Nasional Indonesia Benih udang vaname (Litopenaeus vannamei) kelas benih sebar ICS 65.150 Badan Standardisasi Nasional Daftar isi Daftar isi... i Prakata... ii 1 Ruang lingkup... 1 2 Acuan normatif...
Standar Nasional Indonesia Benih udang vaname (Litopenaeus vannamei) kelas benih sebar ICS 65.150 Badan Standardisasi Nasional Daftar isi Daftar isi... i Prakata... ii 1 Ruang lingkup... 1 2 Acuan normatif...
BAB III METODE PENELITIAN. Penelitian ini merupakan penelitian eksperimental dengan 7 sampel dari 7
 BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian ini merupakan penelitian eksperimental dengan 7 sampel dari 7 individu udang Jari yang diambil dari Segara Anakan Kabupaten Cilacap Jawa Tengah.
BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian ini merupakan penelitian eksperimental dengan 7 sampel dari 7 individu udang Jari yang diambil dari Segara Anakan Kabupaten Cilacap Jawa Tengah.
METODOLOGI PENELITIAN. Tempat dan Waktu Penelitian. Bahan dan Alat Penelitian
 14 METODOLOGI PENELITIAN Tempat dan Waktu Penelitian Tempat penelitian dilakukan di Laboratorium Unit Pelayanan Mikrobiologi Terpadu, Bagian Mikrobiologi Kesehatan, Departemen Ilmu Penyakit Hewan dan Kesehatan
14 METODOLOGI PENELITIAN Tempat dan Waktu Penelitian Tempat penelitian dilakukan di Laboratorium Unit Pelayanan Mikrobiologi Terpadu, Bagian Mikrobiologi Kesehatan, Departemen Ilmu Penyakit Hewan dan Kesehatan
III. METODE PENELITIAN
 11 III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilakukan pada Januari sampai Mei 2011 bertempat di Laboratorium Kesehatan Ikan, Departemen Budidaya Perairan, Fakultas Perikanan dan Ilmu
11 III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilakukan pada Januari sampai Mei 2011 bertempat di Laboratorium Kesehatan Ikan, Departemen Budidaya Perairan, Fakultas Perikanan dan Ilmu
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN A. Jenis Penelitian deskriptif. Jenis penelitian yang digunakan adalah penelitian dasar dengan metode B. Objek Penelitian Objek penelitian ini adalah sampel DNA koleksi hasil
BAB III METODE PENELITIAN A. Jenis Penelitian deskriptif. Jenis penelitian yang digunakan adalah penelitian dasar dengan metode B. Objek Penelitian Objek penelitian ini adalah sampel DNA koleksi hasil
III. METODOLOGI PENELITIAN. Penelitian ini menggunakan metode eksperimental yang bertujuan untuk
 56 III. METODOLOGI PENELITIAN A. Rancangan Penelitian Penelitian ini menggunakan metode eksperimental yang bertujuan untuk mengamplifikasi Gen FNBP1L. B. Tempat dan Waktu Penelitian 1. Tempat Penelitian
56 III. METODOLOGI PENELITIAN A. Rancangan Penelitian Penelitian ini menggunakan metode eksperimental yang bertujuan untuk mengamplifikasi Gen FNBP1L. B. Tempat dan Waktu Penelitian 1. Tempat Penelitian
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian tentang Pengaruh Suhu Annealing pada Program PCR terhadap Keberhasilan Amplifikasi DNA Udang Jari (Metapenaeus elegans) Laguna Segara Anakan
BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian tentang Pengaruh Suhu Annealing pada Program PCR terhadap Keberhasilan Amplifikasi DNA Udang Jari (Metapenaeus elegans) Laguna Segara Anakan
BAB III BAHAN DAN METODE
 BAB III BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini terdiri dari dua tahap, tahap pertama dilaksanakan di laboratorium bioteknologi Fakultas Perikanan dan Ilmu Kelautan Unpad, tahap
BAB III BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini terdiri dari dua tahap, tahap pertama dilaksanakan di laboratorium bioteknologi Fakultas Perikanan dan Ilmu Kelautan Unpad, tahap
MATERI DAN METODE. Materi
 MATERI DAN METODE Lokasi dan Waktu Penelitian dilaksanakan di Laboratorium Genetika Molekuler Ternak, Departemen Ilmu Produksi dan Teknologi Peternakan, Fakultas Peternakan IPB dan Laboratorium Terpadu,
MATERI DAN METODE Lokasi dan Waktu Penelitian dilaksanakan di Laboratorium Genetika Molekuler Ternak, Departemen Ilmu Produksi dan Teknologi Peternakan, Fakultas Peternakan IPB dan Laboratorium Terpadu,
BAB II. BAHAN DAN METODE
 BAB II. BAHAN DAN METODE 2.1 Kultur Bakteri Pembawa Vaksin Bakteri Escherichia coli pembawa vaksin DNA (Nuryati, 2010) dikultur dengan cara menginokulasi satu koloni bakteri media LB tripton dengan penambahan
BAB II. BAHAN DAN METODE 2.1 Kultur Bakteri Pembawa Vaksin Bakteri Escherichia coli pembawa vaksin DNA (Nuryati, 2010) dikultur dengan cara menginokulasi satu koloni bakteri media LB tripton dengan penambahan
III. METODOLOGI PENELITIAN. Penelitian ini menggunakan metode eksperimental yang bertujuan untuk
 27 III. METODOLOGI PENELITIAN 3.1 Desain Penelitian Penelitian ini menggunakan metode eksperimental yang bertujuan untuk mengamplifikasi Gen STX1A. 3.2 Tempat dan Waktu Penelitian 1. Tempat Penelitian
27 III. METODOLOGI PENELITIAN 3.1 Desain Penelitian Penelitian ini menggunakan metode eksperimental yang bertujuan untuk mengamplifikasi Gen STX1A. 3.2 Tempat dan Waktu Penelitian 1. Tempat Penelitian
VISUALISASI HASIL PCR DENGAN METODE PCR LANGSUNG DAN TIDAK LANGSUNG PADA SAMPEL BAKTERI Pseudomonas fluorescens dan Ralstonia solanacearum
 VISUALISASI HASIL PCR DENGAN METODE PCR LANGSUNG DAN TIDAK LANGSUNG PADA SAMPEL BAKTERI Pseudomonas fluorescens dan Ralstonia solanacearum Pendahuluan Polymerase Chain Reaction (PCR) adalah suatu teknik
VISUALISASI HASIL PCR DENGAN METODE PCR LANGSUNG DAN TIDAK LANGSUNG PADA SAMPEL BAKTERI Pseudomonas fluorescens dan Ralstonia solanacearum Pendahuluan Polymerase Chain Reaction (PCR) adalah suatu teknik
BAHAN DAN METODE Tempat dan Waktu Penelitian Bahan dan Alat
 12 BAHAN DAN METODE Tempat dan Waktu Penelitian Survei penyakit klorosis dan koleksi sampel tanaman tomat sakit dilakukan di sentra produksi tomat di daerah Cianjur, Cipanas, Lembang, dan Garut. Deteksi
12 BAHAN DAN METODE Tempat dan Waktu Penelitian Survei penyakit klorosis dan koleksi sampel tanaman tomat sakit dilakukan di sentra produksi tomat di daerah Cianjur, Cipanas, Lembang, dan Garut. Deteksi
BAB III BAHAN DAN METODE PENELITIAN
 BAB III BAHAN DAN METODE PENELITIAN 3.1 Waktu dan Lokasi Penelitian 3.1.1. Lokasi Penelitian Penelitian ini dilakukan di Laboratorium Bioteknologi Perikanan dan Kelautan Fakultas Perikanan dan Ilmu Kelautan
BAB III BAHAN DAN METODE PENELITIAN 3.1 Waktu dan Lokasi Penelitian 3.1.1. Lokasi Penelitian Penelitian ini dilakukan di Laboratorium Bioteknologi Perikanan dan Kelautan Fakultas Perikanan dan Ilmu Kelautan
LAMPIRAN. Lampiran 1. Alur Kerja Isolasi Bakteri Endofit dari Batang dan Akar Tanaman Dara metode Radu & Kqueen (2002) yang dimodifikasi
 LAMPIRAN Lampiran 1. Alur Kerja Isolasi Bakteri Endofit dari Batang dan Akar Tanaman Dara metode Radu & Kqueen (2002) yang dimodifikasi Bagian akar dan batang (3-5 cm) Dicuci dengan air mengalir selama
LAMPIRAN Lampiran 1. Alur Kerja Isolasi Bakteri Endofit dari Batang dan Akar Tanaman Dara metode Radu & Kqueen (2002) yang dimodifikasi Bagian akar dan batang (3-5 cm) Dicuci dengan air mengalir selama
3. METODE PENELITIAN
 19 3. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Maret sampai Juni 2010 di Laboratorium Mikrobiologi, Biokimia dan Bioteknologi Hasil Perairan Departemen Teknologi Hasil
19 3. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Maret sampai Juni 2010 di Laboratorium Mikrobiologi, Biokimia dan Bioteknologi Hasil Perairan Departemen Teknologi Hasil
III. METODOLOGI. Penelitian dilakukan selama 40 hari dari bulan Februari sampai dengan Maret. Bahan yang digunakan dalam penelitian antara lain:
 21 III. METODOLOGI A. Waktu dan Tempat Penelitian Penelitian dilakukan selama 40 hari dari bulan Februari sampai dengan Maret 2013 bertempat di Laboratorium Budidaya Perairan Fakultas Pertanian Universitas
21 III. METODOLOGI A. Waktu dan Tempat Penelitian Penelitian dilakukan selama 40 hari dari bulan Februari sampai dengan Maret 2013 bertempat di Laboratorium Budidaya Perairan Fakultas Pertanian Universitas
II. BAHAN DAN METODE. Betina BEST BB NB RB. Nirwana BN NN RN. Red NIFI BR NR RR
 II. BAHAN DAN METODE Ikan Uji Ikan uji yang digunakan adalah ikan nila hibrida hasil persilangan resiprok 3 strain BEST, Nirwana dan Red NIFI koleksi Balai Riset Perikanan Budidaya Air Tawar Sempur, Bogor.
II. BAHAN DAN METODE Ikan Uji Ikan uji yang digunakan adalah ikan nila hibrida hasil persilangan resiprok 3 strain BEST, Nirwana dan Red NIFI koleksi Balai Riset Perikanan Budidaya Air Tawar Sempur, Bogor.
BAB III METODE PENELITIAN. Secara garis besar langkah-langkah yang dilakukan dalam penelitian ini
 BAB III METODE PENELITIAN Secara garis besar langkah-langkah yang dilakukan dalam penelitian ini adalah: pengumpulan sampel; lisis terhadap sampel mtdna yang telah diperoleh; amplifikasi daerah D-loop
BAB III METODE PENELITIAN Secara garis besar langkah-langkah yang dilakukan dalam penelitian ini adalah: pengumpulan sampel; lisis terhadap sampel mtdna yang telah diperoleh; amplifikasi daerah D-loop
MATERI DAN METODE. Kota Padang Sumatera Barat pada bulan Oktober Amplifikasi gen Growth
 III. MATERI DAN METODE 3.1 Waktu dan Tempat Pengambilan sampel darah domba dilakukan di Kecamatan Koto Tengah Kota Padang Sumatera Barat pada bulan Oktober 2012. Amplifikasi gen Growth Hormone menggunakan
III. MATERI DAN METODE 3.1 Waktu dan Tempat Pengambilan sampel darah domba dilakukan di Kecamatan Koto Tengah Kota Padang Sumatera Barat pada bulan Oktober 2012. Amplifikasi gen Growth Hormone menggunakan
III. METODE PENELITIAN. Penelitian ini dilaksanakan pada bulan Mei Juni Lokasi penelitian di
 III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan Mei Juni 2014. Lokasi penelitian di Laboratorium Budidaya Perikanan, Program Studi Budidaya Perairan, Fakultas
III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan Mei Juni 2014. Lokasi penelitian di Laboratorium Budidaya Perikanan, Program Studi Budidaya Perairan, Fakultas
III. METODE PENELITIAN. Stasiun Karantina Ikan Pengendalian Mutu dan Keamanan Hasil Perikanan
 18 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian dilakukan pada bulan September November 2011 yang bertempat di Laboratorium Bioteknologi Lantai 3 Program Studi Budidaya Perairan Universitas Lampung,
18 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian dilakukan pada bulan September November 2011 yang bertempat di Laboratorium Bioteknologi Lantai 3 Program Studi Budidaya Perairan Universitas Lampung,
Asam Asetat Glacial = 5,7 ml EDTA 0,5 M ph 8.0 = 10 ml Aquades ditambahkan hingga volume larutan 100 ml
 36 Lampiran 1. Pembuatan Larutan Stok dan Buffer A. Pembuatan Larutan Stok Tris HCL 1 M ph 8.0 (100 ml) : Timbang Tris sebanyak 12,114 g. Masukkan Tris ke dalam Erlenmeyer dan ditambahkan 80 ml aquades.
36 Lampiran 1. Pembuatan Larutan Stok dan Buffer A. Pembuatan Larutan Stok Tris HCL 1 M ph 8.0 (100 ml) : Timbang Tris sebanyak 12,114 g. Masukkan Tris ke dalam Erlenmeyer dan ditambahkan 80 ml aquades.
Benih udang windu Penaeus monodon (Fabricius, 1798) kelas benih sebar
 Standar Nasional Indonesia Benih udang windu Penaeus monodon (Fabricius, 1798) kelas benih sebar ICS 65.150 Badan Standardisasi Nasional Daftar isi Daftar isi...i Prakata...ii 1 Ruang lingkup...1 2 Acuan
Standar Nasional Indonesia Benih udang windu Penaeus monodon (Fabricius, 1798) kelas benih sebar ICS 65.150 Badan Standardisasi Nasional Daftar isi Daftar isi...i Prakata...ii 1 Ruang lingkup...1 2 Acuan
BAB III BAHAN DAN METODE
 BAB III BAHAN DAN METODE 3.1. Tempat dan Waktu Penelitian 3.1.1. Tempat Penelitian Penelitian dilaksanakan di Laboratorium Bioteknologi Perikanan dan Kelautan Fakultas Perikanan dan Ilmu Kelautan Universitas
BAB III BAHAN DAN METODE 3.1. Tempat dan Waktu Penelitian 3.1.1. Tempat Penelitian Penelitian dilaksanakan di Laboratorium Bioteknologi Perikanan dan Kelautan Fakultas Perikanan dan Ilmu Kelautan Universitas
3 METODOLOGI 3.1 Waktu dan Tempat 3.2 Bahan dan Alat
 3 METODOLOGI 3.1 Waktu dan Tempat Penelitian Autentikasi Bahan Baku Ikan Tuna (Thunnus sp.) dalam Rangka Peningkatan Keamanan Pangan dengan Metode Berbasis DNA dilaksanakan pada bulan Januari sampai dengan
3 METODOLOGI 3.1 Waktu dan Tempat Penelitian Autentikasi Bahan Baku Ikan Tuna (Thunnus sp.) dalam Rangka Peningkatan Keamanan Pangan dengan Metode Berbasis DNA dilaksanakan pada bulan Januari sampai dengan
III. BAHAN DAN METODE
 III. BAHAN DAN METODE Tempat dan Waktu Penelitian dilakukan di Laboratorium BIORIN (Biotechnology Research Indonesian - The Netherlands) Pusat Penelitian Sumberdaya Hayati dan Bioteknologi IPB. Penelitian
III. BAHAN DAN METODE Tempat dan Waktu Penelitian dilakukan di Laboratorium BIORIN (Biotechnology Research Indonesian - The Netherlands) Pusat Penelitian Sumberdaya Hayati dan Bioteknologi IPB. Penelitian
PRAKTIKUM ISOLASI DNA DAN TEKNIK PCR
 PRAKTIKUM ISOLASI DNA DAN TEKNIK PCR Tujuan: i) Mengerti metode umum mengisolasi DNA ii) Mengisolasi DNA dari buah dan sel-sel epithelial mulut iii) Mengerti dan mempraktek teknik PCR dengan sempel DNA
PRAKTIKUM ISOLASI DNA DAN TEKNIK PCR Tujuan: i) Mengerti metode umum mengisolasi DNA ii) Mengisolasi DNA dari buah dan sel-sel epithelial mulut iii) Mengerti dan mempraktek teknik PCR dengan sempel DNA
III. MATERI DAN METODE
 III. MATERI DAN METODE 3.1 Tempat dan Waktu Penelitian Sampel tanah diambil dari Hutan Larangan Adat Rumbio Kabupaten Kampar. Sedangkan Enumerasi dan Analisis bakteri dilakukan di Laboratorium Patologi,
III. MATERI DAN METODE 3.1 Tempat dan Waktu Penelitian Sampel tanah diambil dari Hutan Larangan Adat Rumbio Kabupaten Kampar. Sedangkan Enumerasi dan Analisis bakteri dilakukan di Laboratorium Patologi,
Lampiran 1. Road-map Penelitian
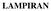 LAMPIRAN Lampiran 1. Road-map Penelitian Persiapan Penelitian Persiapan wadah dan ikan uji Bak ukuran 40x30x30cm sebanyak 4 buah dicuci, didesinfeksi, dan dikeringkan Diletakkan secara acak dan diberi
LAMPIRAN Lampiran 1. Road-map Penelitian Persiapan Penelitian Persiapan wadah dan ikan uji Bak ukuran 40x30x30cm sebanyak 4 buah dicuci, didesinfeksi, dan dikeringkan Diletakkan secara acak dan diberi
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN A. Jenis Penelitian Penelitian ini merupakan penelitian murni yang dilakukan dengan metode deskriptif, yaitu suatu metode penelitian untuk membuat deskripsi, gambaran atau lukisan
BAB III METODE PENELITIAN A. Jenis Penelitian Penelitian ini merupakan penelitian murni yang dilakukan dengan metode deskriptif, yaitu suatu metode penelitian untuk membuat deskripsi, gambaran atau lukisan
METODE PENELITIAN. Penelitian ini dilaksanakan pada bulan Agustus - Oktober 2013 di Balai Besar
 III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Agustus - Oktober 2013 di Balai Besar Pengembangan Budidaya Laut (BBPBL) Lampung tepatnya di Laboratorium Pembenihan Kuda
III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Agustus - Oktober 2013 di Balai Besar Pengembangan Budidaya Laut (BBPBL) Lampung tepatnya di Laboratorium Pembenihan Kuda
1. Kualitas DNA total Udang Jari (Metapenaeus elegans De Man, 1907) Hasil. Tangkapan dari Laguna Segara Anakan, Cilacap, Jawa Tengah dengan
 Lampiran 1. Data dan analisis karakterisasi genetik Udang Jari (Metapenaeus elegans De Man, 1907) Hasil Tangkapan dari Laguna Segara Anakan, Cilacap, Jawa Tengah. 1. Kualitas DNA total Udang Jari (Metapenaeus
Lampiran 1. Data dan analisis karakterisasi genetik Udang Jari (Metapenaeus elegans De Man, 1907) Hasil Tangkapan dari Laguna Segara Anakan, Cilacap, Jawa Tengah. 1. Kualitas DNA total Udang Jari (Metapenaeus
BAB III. METODOLOGI PENELITIAN. Pengambilan sampel. Penyiapan templat mtdna dengan metode lisis sel
 16 BAB III. METODOLOGI PENELITIAN Bab ini menggambarkan tahapan penelitian yang terdiri dari pengambilan sampel, penyiapan templat mtdna dengan metode lisis sel, amplifikasi D-loop mtdna dengan teknik
16 BAB III. METODOLOGI PENELITIAN Bab ini menggambarkan tahapan penelitian yang terdiri dari pengambilan sampel, penyiapan templat mtdna dengan metode lisis sel, amplifikasi D-loop mtdna dengan teknik
III. METODE PENELITIAN. Penelitian ini dilaksanakan pada Mei - Juni 2014 di Laboratorium Basah Jurusan
 III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada Mei - Juni 2014 di Laboratorium Basah Jurusan Budidaya Perairan Fakultas Pertanian Universitas Lampung. 3.2 Alat dan Bahan Alat
III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada Mei - Juni 2014 di Laboratorium Basah Jurusan Budidaya Perairan Fakultas Pertanian Universitas Lampung. 3.2 Alat dan Bahan Alat
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Bioteknologi Perikanan dan Ilmu Kelautan, Fakultas Perikanan dan Ilmu Kelautan (FPIK) Universitas Padjadjaran.
BAB III METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Bioteknologi Perikanan dan Ilmu Kelautan, Fakultas Perikanan dan Ilmu Kelautan (FPIK) Universitas Padjadjaran.
LAMPIRAN. Lampiran 1. Pembuatan Larutan Stok dan Buffer
 LAMPIRAN Lampiran 1. Pembuatan Larutan Stok dan Buffer A. LARUTAN STOK CTAB 5 % (100 ml) - Ditimbang NaCl sebanyak 2.0 gram - Ditimbang CTAB sebanyak 5.0 gram. - Dimasukkan bahan kimia ke dalam erlenmeyer
LAMPIRAN Lampiran 1. Pembuatan Larutan Stok dan Buffer A. LARUTAN STOK CTAB 5 % (100 ml) - Ditimbang NaCl sebanyak 2.0 gram - Ditimbang CTAB sebanyak 5.0 gram. - Dimasukkan bahan kimia ke dalam erlenmeyer
METODE PENELITIAN. A. Tempat dan Waktu
 10 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian dilaksanakan pada bulan September 2015 sampai Februari 2016. Isolasi dan visualisasi RNA Colletrotichum dilaksanakan di Laboratorium Hama Penyakit
10 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian dilaksanakan pada bulan September 2015 sampai Februari 2016. Isolasi dan visualisasi RNA Colletrotichum dilaksanakan di Laboratorium Hama Penyakit
II. MATERI DAN METODE. Tempat pengambilan sampel daun jati (Tectona grandis Linn. f.) dilakukan di
 II. MATERI DAN METODE 2.1 Waktu dan Tempat Penelitian Tempat pengambilan sampel daun jati (Tectona grandis Linn. f.) dilakukan di enam desa yaitu tiga desa di Kecamatan Grokgak dan tiga desa di Kecamatan
II. MATERI DAN METODE 2.1 Waktu dan Tempat Penelitian Tempat pengambilan sampel daun jati (Tectona grandis Linn. f.) dilakukan di enam desa yaitu tiga desa di Kecamatan Grokgak dan tiga desa di Kecamatan
bio.unsoed.ac.id METODE PENELITIAN A. Materi, Lokasi, dan Waktu Penelitian 1. Materi Penelitian
 III. METODE PENELITIAN A. Materi, Lokasi, dan Waktu Penelitian 1. Materi Penelitian 1.1. Peralatan Penelitian Alat yang digunakan dalam penelitian ini adalah botol sampel, beaker glass, cool box, labu
III. METODE PENELITIAN A. Materi, Lokasi, dan Waktu Penelitian 1. Materi Penelitian 1.1. Peralatan Penelitian Alat yang digunakan dalam penelitian ini adalah botol sampel, beaker glass, cool box, labu
FAKULTAS BIOLOGI LABORATORIUM GENETIKA & PEMULIAAN INSTRUKSI KERJA UJI
 Halaman : 1 dari 5 ISOLASI TOTAL DNA HEWAN DENGAN KIT EKSTRAKSI DNA 1. RUANG LINGKUP Metode ini digunakan untuk mengisolasi DNA dari sampel jaringan hewan, dapat dari insang, otot, darah atau jaringan
Halaman : 1 dari 5 ISOLASI TOTAL DNA HEWAN DENGAN KIT EKSTRAKSI DNA 1. RUANG LINGKUP Metode ini digunakan untuk mengisolasi DNA dari sampel jaringan hewan, dapat dari insang, otot, darah atau jaringan
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Manajemen Sumberdaya Perairan Fakultas Perikanan dan Ilmu Kelautan Universitas Padjadjaran Jatinangor
BAB III METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Manajemen Sumberdaya Perairan Fakultas Perikanan dan Ilmu Kelautan Universitas Padjadjaran Jatinangor
LAMPIRAN. Lampiran 1. Deskripsi Pembuatan Larutan Stok dan Buffer
 LAMPIRAN Lampiran 1. Deskripsi Pembuatan Larutan Stok dan Buffer 1. Pembuatan Larutan Stok a. CTAB 5 % Larutan dibuat dengan melarutkan : - NaCl : 2.0 gr - CTAB : 5.0 gr - Aquades : 100 ml b. Tris HCl
LAMPIRAN Lampiran 1. Deskripsi Pembuatan Larutan Stok dan Buffer 1. Pembuatan Larutan Stok a. CTAB 5 % Larutan dibuat dengan melarutkan : - NaCl : 2.0 gr - CTAB : 5.0 gr - Aquades : 100 ml b. Tris HCl
BAB III BAHAN DAN CARA KERJA. Penelitian dilakukan di Laboratorium Institute of Human Virology and
 23 BAB III BAHAN DAN CARA KERJA A. LOKASI DAN WAKTU PENELITIAN Penelitian dilakukan di Laboratorium Institute of Human Virology and Cancer Biology of the University of Indonesia (IHVCB-UI), Jl. Salemba
23 BAB III BAHAN DAN CARA KERJA A. LOKASI DAN WAKTU PENELITIAN Penelitian dilakukan di Laboratorium Institute of Human Virology and Cancer Biology of the University of Indonesia (IHVCB-UI), Jl. Salemba
II. BAHAN DAN METODE
 II. BAHAN DAN METODE 2.1. Waktu dan Lokasi Penelitian Penelitian ini dilaksanakan dari bulan Agustus sampai September tahun 2011. Sampel ikan berasal dari 3 lokasi yaitu Jawa (Jawa Barat), Sumatera (Jambi),
II. BAHAN DAN METODE 2.1. Waktu dan Lokasi Penelitian Penelitian ini dilaksanakan dari bulan Agustus sampai September tahun 2011. Sampel ikan berasal dari 3 lokasi yaitu Jawa (Jawa Barat), Sumatera (Jambi),
III. BAHAN DAN METODE
 8 III. BAHAN DAN METODE 3.1 Waktu dan Tempat Penelitian ini dilakukan pada bulan Oktober 2008 sampai dengan bulan Juli 2009 di Kolam Percobaan Babakan, Laboratorium Pengembangbiakkan dan Genetika Ikan
8 III. BAHAN DAN METODE 3.1 Waktu dan Tempat Penelitian ini dilakukan pada bulan Oktober 2008 sampai dengan bulan Juli 2009 di Kolam Percobaan Babakan, Laboratorium Pengembangbiakkan dan Genetika Ikan
BAB III METODE PENELITIAN Bagan Alir Penelitian ini secara umum dapat digambarkan pada skema berikut:
 BAB III METODE PENELITIAN Tahapan-tahapan yang dilakukan dalam penelitian ini adalah: pengumpulan sampel, lisis terhadap sampel mtdna yang telah diperoleh, amplifikasi daerah HVI mtdna sampel dengan menggunakan
BAB III METODE PENELITIAN Tahapan-tahapan yang dilakukan dalam penelitian ini adalah: pengumpulan sampel, lisis terhadap sampel mtdna yang telah diperoleh, amplifikasi daerah HVI mtdna sampel dengan menggunakan
Lampiran 1 Ekstraksi dan isolasi DNA dengan metode GeneAid
 LAMPIRAN 9 Lampiran 1 Ekstraksi dan isolasi DNA dengan metode GeneAid Satu ruas tungkai udang mantis dalam etanol dipotong dan dimasukkan ke dalam tube 1,5 ml. Ruas tungkai yang telah dipotong (otot tungkai)
LAMPIRAN 9 Lampiran 1 Ekstraksi dan isolasi DNA dengan metode GeneAid Satu ruas tungkai udang mantis dalam etanol dipotong dan dimasukkan ke dalam tube 1,5 ml. Ruas tungkai yang telah dipotong (otot tungkai)
DETEKSI PENYAKIT VIRAL PADA UDANG VANNAMEI (Litopennaeus vannamei) DENGAN METODE Polymerase Chain Reaction (PCR)
 Samakia: Jurnal Ilmu Perikanan Volume 6, No. 1, Februari 2015 ISSN : 2086-3861 DETEKSI PENYAKIT VIRAL PADA UDANG VANNAMEI (Litopennaeus vannamei) DENGAN METODE Polymerase Chain Reaction (PCR) VIRAL DISEASE
Samakia: Jurnal Ilmu Perikanan Volume 6, No. 1, Februari 2015 ISSN : 2086-3861 DETEKSI PENYAKIT VIRAL PADA UDANG VANNAMEI (Litopennaeus vannamei) DENGAN METODE Polymerase Chain Reaction (PCR) VIRAL DISEASE
BAHAN DAN METODE Tempat dan Waktu Bahan dan Alat Metode Penelitian Isolasi Aktinomiset
 BAHAN DAN METODE Tempat dan Waktu Penelitian dilaksanakan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor, dari bulan Februari sampai dengan
BAHAN DAN METODE Tempat dan Waktu Penelitian dilaksanakan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor, dari bulan Februari sampai dengan
BAB III METODE PENELITIAN
 25 BAB III METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian telah berlangsung sejak bulan Januari 2012 - Juli 2012 di Laboratorium Mikrobiologi, Lab. Optik, Lab. Genetika dan Lab. Biologi Molekuler Jurusan
25 BAB III METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian telah berlangsung sejak bulan Januari 2012 - Juli 2012 di Laboratorium Mikrobiologi, Lab. Optik, Lab. Genetika dan Lab. Biologi Molekuler Jurusan
BAB III METODE PENELITIAN. amplifikasi daerah HVI mtdna sampel dengan menggunakan teknik PCR;
 BAB III METODE PENELITIAN Secara garis besar, langkah-langkah yang dilakukan dalam penelitian ini adalah: pengumpulan sampel; lisis terhadap sampel mtdna yang telah diperoleh; amplifikasi daerah HVI mtdna
BAB III METODE PENELITIAN Secara garis besar, langkah-langkah yang dilakukan dalam penelitian ini adalah: pengumpulan sampel; lisis terhadap sampel mtdna yang telah diperoleh; amplifikasi daerah HVI mtdna
II. METODE PENELITIAN
 II. METODE PENELITIAN 1. Materi, Lokasi, dan Waktu Penelitian 1.1. Materi Alat yang digunakan dalam penelitian ini adalah botol sampel, cawan petri, tabung reaksi, labu Erlenmeyer, beaker glass, object
II. METODE PENELITIAN 1. Materi, Lokasi, dan Waktu Penelitian 1.1. Materi Alat yang digunakan dalam penelitian ini adalah botol sampel, cawan petri, tabung reaksi, labu Erlenmeyer, beaker glass, object
BAHAN DAN METODE Waktu dan Tempat Bahan Metode Isolasi C. gloeosporioides dari Buah Avokad
 15 BAHAN DAN METODE Waktu dan Tempat Penelitian dilaksanakan di Laboratorium Balai Besar Karantina Pertanian (BBKP) Tanjung Priok Wilayah Kerja Bogor, mulai bulan Oktober 2011 sampai Februari 2012. Bahan
15 BAHAN DAN METODE Waktu dan Tempat Penelitian dilaksanakan di Laboratorium Balai Besar Karantina Pertanian (BBKP) Tanjung Priok Wilayah Kerja Bogor, mulai bulan Oktober 2011 sampai Februari 2012. Bahan
Lampiran 1. Road-map Penelitian
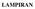 LAMPIRAN Lampiran 1. Road-map Penelitian Persiapan Penelitian Persiapan wadah dan ikan uji (15-30 Agustus 2013) Bak ukuran 45x30x35cm sebanyak 4 buah dicuci, didesinfeksi, dan dikeringkan Diletakkan secara
LAMPIRAN Lampiran 1. Road-map Penelitian Persiapan Penelitian Persiapan wadah dan ikan uji (15-30 Agustus 2013) Bak ukuran 45x30x35cm sebanyak 4 buah dicuci, didesinfeksi, dan dikeringkan Diletakkan secara
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN A. Jenis Penelitian Jenis penelitian yang digunakan adalah penelitian dasar dengan metode deskriptif (Nazir, 1983). B. Populasi dan Sampel Populasi dalam penelitian ini adalah
BAB III METODE PENELITIAN A. Jenis Penelitian Jenis penelitian yang digunakan adalah penelitian dasar dengan metode deskriptif (Nazir, 1983). B. Populasi dan Sampel Populasi dalam penelitian ini adalah
III. METODE PENELITIAN. Penelitian ini dilaksanakan pada bulan September-Oktober 2014 di
 III. METODE PENELITIAN 3.1 Tempat Dan Waktu Penelitian Penelitian ini dilaksanakan pada bulan September-Oktober 2014 di Laboratorium dan Fasilitas Karantina Marine Research Center (MRC) PT.Central Pertiwi
III. METODE PENELITIAN 3.1 Tempat Dan Waktu Penelitian Penelitian ini dilaksanakan pada bulan September-Oktober 2014 di Laboratorium dan Fasilitas Karantina Marine Research Center (MRC) PT.Central Pertiwi
III. METODOLOGI 3.1 Waktu dan Tempat 3.2 Induk 3.3 Metode Penelitian
 III. METODOLOGI 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan November 2009 sampai dengan Februari 2010 di Stasiun Lapangan Laboratorium Reproduksi dan Genetika Organisme Akuatik, Departemen
III. METODOLOGI 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan November 2009 sampai dengan Februari 2010 di Stasiun Lapangan Laboratorium Reproduksi dan Genetika Organisme Akuatik, Departemen
III. METODE PENELITIAN. Penelitian dilaksanakan pada bulan Agustus sampai Oktober 2011, di
 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian dilaksanakan pada bulan Agustus sampai Oktober 2011, di Laboratorium Program Studi Budidaya Perairan, Fakultas Pertanian, Universitas Lampung. B. Alat
III. METODE PENELITIAN A. Waktu dan Tempat Penelitian dilaksanakan pada bulan Agustus sampai Oktober 2011, di Laboratorium Program Studi Budidaya Perairan, Fakultas Pertanian, Universitas Lampung. B. Alat
III. Bahan dan Metode
 III. Bahan dan Metode A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan selama 3 bulan dari bulan Mei-Juli 2011 yang dilakukan di LPPT UGM Yogyakarta. B. Bahan Penelitian Sampel yang digunakan
III. Bahan dan Metode A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan selama 3 bulan dari bulan Mei-Juli 2011 yang dilakukan di LPPT UGM Yogyakarta. B. Bahan Penelitian Sampel yang digunakan
Zoea Syndrome (ZS) pada Larva Udang Vannamei (Litopenaeus vannamei)
 Zoea Syndrome (ZS) pada Larva Udang Vannamei (Litopenaeus vannamei) Rubiyanto Widodo Haliman 1), Tommy Hemawan 1), Lilik Wirastiani 2), Dicky Prania Al Amurullah 2), Muhammad Murdjani 3), Yani Lestari
Zoea Syndrome (ZS) pada Larva Udang Vannamei (Litopenaeus vannamei) Rubiyanto Widodo Haliman 1), Tommy Hemawan 1), Lilik Wirastiani 2), Dicky Prania Al Amurullah 2), Muhammad Murdjani 3), Yani Lestari
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN A. Jenis penelitian Jenis penelitian ini adalah penelitian deskriptif yang mengangkat fenomena alam sebagai salah satu masalah dalam penelitian, sehingga dapat menerangkan arti
BAB III METODE PENELITIAN A. Jenis penelitian Jenis penelitian ini adalah penelitian deskriptif yang mengangkat fenomena alam sebagai salah satu masalah dalam penelitian, sehingga dapat menerangkan arti
BAB III METODE PENELITIAN. Dalam penelitian ini dilakukan lima tahap utama yang meliputi tahap
 BAB III METODE PENELITIAN Dalam penelitian ini dilakukan lima tahap utama yang meliputi tahap penyiapan templat mtdna, amplifikasi fragmen mtdna pada daerah D-loop mtdna manusia dengan teknik PCR, deteksi
BAB III METODE PENELITIAN Dalam penelitian ini dilakukan lima tahap utama yang meliputi tahap penyiapan templat mtdna, amplifikasi fragmen mtdna pada daerah D-loop mtdna manusia dengan teknik PCR, deteksi
METODE PENELITIAN. Penelitian dilaksanakan pada bulan Januari - Februari 2010, di Laboratorium
 28 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian dilaksanakan pada bulan Januari - Februari 2010, di Laboratorium Stasiun Karantina Ikan Kelas I Panjang, Bandar Lampung dan Laboratorium Budidaya
28 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian dilaksanakan pada bulan Januari - Februari 2010, di Laboratorium Stasiun Karantina Ikan Kelas I Panjang, Bandar Lampung dan Laboratorium Budidaya
BAHAN DAN METODE Tempat dan Waktu Metode Penelitian Pengambilan Sampel Kutukebul dan Tanaman Tomat Sumber TICV
 BAHAN DAN METODE Tempat dan Waktu Kegiatan survei dan pengambilan sampel kutukebul dilakukan di sentra produksi tomat di Kecamatan Cikajang (kabupaten Garut), Kecamatan Pacet (Kabupaten Cianjur), Kecamatan
BAHAN DAN METODE Tempat dan Waktu Kegiatan survei dan pengambilan sampel kutukebul dilakukan di sentra produksi tomat di Kecamatan Cikajang (kabupaten Garut), Kecamatan Pacet (Kabupaten Cianjur), Kecamatan
MATERI DAN METODE. Lokasi dan Waktu. Materi. Tabel 1. Jumah Sampel Darah Ternak Sapi Indonesia Ternak n Asal Sapi Bali 2 4
 MATERI DAN METODE Lokasi dan Waktu Penelitian dilaksanakan di Laboratorium Genetika Molekuler Ternak, Bagian Pemuliaan dan Genetika Ternak, Fakultas Peternakan, Institut Pertanian Bogor. penelitian ini
MATERI DAN METODE Lokasi dan Waktu Penelitian dilaksanakan di Laboratorium Genetika Molekuler Ternak, Bagian Pemuliaan dan Genetika Ternak, Fakultas Peternakan, Institut Pertanian Bogor. penelitian ini
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian tentang Karakterisasi genetik Udang Jari (Metapenaeus elegans De Man, 1907) hasil tangkapan dari Laguna Segara Anakan berdasarkan haplotipe
BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian tentang Karakterisasi genetik Udang Jari (Metapenaeus elegans De Man, 1907) hasil tangkapan dari Laguna Segara Anakan berdasarkan haplotipe
III. METODE PENELITIAN. Penelitian ini dilakukan di Laboratorium Mikrobiologi Jurusan Biologi
 13 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung. Penelitian
13 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung. Penelitian
DEPARTEMEN BIOLOGI FMIPA USU LAMPIRAN
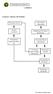 LAMPIRAN Lampiran 1. Diagram Alir Penelitian Peremajaan Bacillus Isolasi Bakteri Oportunistik Produksi Antimikrob Penghitungan Sel Bakteri Oportunistik Pengambilan Supernatan Bebas Sel Pemurnian Bakteri
LAMPIRAN Lampiran 1. Diagram Alir Penelitian Peremajaan Bacillus Isolasi Bakteri Oportunistik Produksi Antimikrob Penghitungan Sel Bakteri Oportunistik Pengambilan Supernatan Bebas Sel Pemurnian Bakteri
BAB III METODOLOGI PENELITIAN. Penelitian akan diawali dengan preparasi alat dan bahan untuk sampling
 16 BAB III METODOLOGI PENELITIAN Penelitian akan diawali dengan preparasi alat dan bahan untuk sampling sel folikel akar rambut. Sampel kemudian dilisis, diamplifikasi dan disekuensing dengan metode dideoksi
16 BAB III METODOLOGI PENELITIAN Penelitian akan diawali dengan preparasi alat dan bahan untuk sampling sel folikel akar rambut. Sampel kemudian dilisis, diamplifikasi dan disekuensing dengan metode dideoksi
BAB III BAHAN DAN METODE
 BAB III BAHAN DAN METODE 3.1. Tempat dan Waktu Penelitian 3.1.1. Tempat Penelitian Sampling bakteri kitinolitik dilakukan di beberapa lokasi sekitar Pelabuhan Perikanan Nusantara (PPN) Kejawanan Cirebon.
BAB III BAHAN DAN METODE 3.1. Tempat dan Waktu Penelitian 3.1.1. Tempat Penelitian Sampling bakteri kitinolitik dilakukan di beberapa lokasi sekitar Pelabuhan Perikanan Nusantara (PPN) Kejawanan Cirebon.
III. MATERI DAN METODE. Fakultas Pertanian dan Peternakan Universitas Islam Negeri Sultan Syarif Kasim
 III. MATERI DAN METODE 3.1 Waktu dan Tempat Penelitian ini akan dilaksanakan di Laboratorium Genetika dan Pemuliaan Fakultas Pertanian dan Peternakan Universitas Islam Negeri Sultan Syarif Kasim Riau Pekanbaru
III. MATERI DAN METODE 3.1 Waktu dan Tempat Penelitian ini akan dilaksanakan di Laboratorium Genetika dan Pemuliaan Fakultas Pertanian dan Peternakan Universitas Islam Negeri Sultan Syarif Kasim Riau Pekanbaru
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Januari 2012 sampai bulan Juli 2012, yang bertempat di Laboratorium Genetika dan Biologi Molekuler Jurusan Biologi
BAB III METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Januari 2012 sampai bulan Juli 2012, yang bertempat di Laboratorium Genetika dan Biologi Molekuler Jurusan Biologi
FAKULTAS BIOLOGI LABORATORIUM GENETIKA & PEMULIAAN INSTRUKSI KERJA UJI
 ISOLASI TOTAL DNA TUMBUHAN DENGAN KIT EKSTRAKSI DNA PHYTOPURE Halaman : 1 dari 5 1. RUANG LINGKUP Metode ini digunakan untuk mengisolasi DNA dari sampel jaringan tumbuhan, dapat dari daun, akar, batang,
ISOLASI TOTAL DNA TUMBUHAN DENGAN KIT EKSTRAKSI DNA PHYTOPURE Halaman : 1 dari 5 1. RUANG LINGKUP Metode ini digunakan untuk mengisolasi DNA dari sampel jaringan tumbuhan, dapat dari daun, akar, batang,
BAB 3 METODOLOGI PENELITIAN
 20 BAB 3 METODOLOGI PENELITIAN 3.1. Desain Penelitian Penelitian ini bersifat deskriptif cross sectional molekuler. Data yang diperoleh berasal dari pemeriksaan langsung yang dilakukan peneliti sebanyak
20 BAB 3 METODOLOGI PENELITIAN 3.1. Desain Penelitian Penelitian ini bersifat deskriptif cross sectional molekuler. Data yang diperoleh berasal dari pemeriksaan langsung yang dilakukan peneliti sebanyak
LAPORAN PRAKTIKUM REKAYASA GENETIKA
 LAPORAN PRAKTIKUM REKAYASA GENETIKA LAPORAN IV (ISOLASI RNA DARI TANAMAN) KHAIRUL ANAM P051090031/BTK BIOTEKNOLOGI SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR 2010 0 ISOLASI RNA DARI TANAMAN TUJUAN Tujuan
LAPORAN PRAKTIKUM REKAYASA GENETIKA LAPORAN IV (ISOLASI RNA DARI TANAMAN) KHAIRUL ANAM P051090031/BTK BIOTEKNOLOGI SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR 2010 0 ISOLASI RNA DARI TANAMAN TUJUAN Tujuan
Lampiran A. Isolat Virus Metode Malole et al. (2006): Ikan kerapu macan positif VNN
 Lampiran A. Isolat Virus Metode Malole et al. (2006): Ikan kerapu macan positif VNN Diambil organ mata dan otaknya. Digerus dengan mortal. Ditambahkan NaCl fisiologis. Virus konsentrasi 10% Disentrifugasi
Lampiran A. Isolat Virus Metode Malole et al. (2006): Ikan kerapu macan positif VNN Diambil organ mata dan otaknya. Digerus dengan mortal. Ditambahkan NaCl fisiologis. Virus konsentrasi 10% Disentrifugasi
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN A. Jenis Penelitian Jenis penelitian ini adalah penelitian deskriptif yang mengangkat fenomena alam sebagai salah satu masalah dalam penelitian. Penelitian ini dapat menerangkan
BAB III METODE PENELITIAN A. Jenis Penelitian Jenis penelitian ini adalah penelitian deskriptif yang mengangkat fenomena alam sebagai salah satu masalah dalam penelitian. Penelitian ini dapat menerangkan
METODE PENELITIAN Waktu dan Tempat Penelitian Bahan dan Alat
 21 METODE PENELITIAN Waktu dan Tempat Penelitian Penelitian dilaksanakan selama 6 bulan, mulai Maret sampai dengan Agustus 2010 di laboratorium Mikrobiologi Medis, laboratorium Terpadu unit pelayanan mikrobiologi
21 METODE PENELITIAN Waktu dan Tempat Penelitian Penelitian dilaksanakan selama 6 bulan, mulai Maret sampai dengan Agustus 2010 di laboratorium Mikrobiologi Medis, laboratorium Terpadu unit pelayanan mikrobiologi
NOTULENSI DISKUSI PHARM-C. Hari, tanggal : Sabtu, 23 Juli 2017 : WIB Tempat : Online (LINE Grup Pharm-C Kloter 1)
 NOTULENSI DISKUSI PHARM-C Hari, tanggal : Sabtu, 23 Juli 2017 Waktu : 19.00 21.00 WIB Tempat : Online (LINE Grup Pharm-C Kloter 1) Pemateri : Anis Fitriani Tema Diskusi : Isolasi dan Pemanfaatan Bakteri
NOTULENSI DISKUSI PHARM-C Hari, tanggal : Sabtu, 23 Juli 2017 Waktu : 19.00 21.00 WIB Tempat : Online (LINE Grup Pharm-C Kloter 1) Pemateri : Anis Fitriani Tema Diskusi : Isolasi dan Pemanfaatan Bakteri
II. METODE PENELITIAN
 II. METODE PENELITIAN 2.1 Prosedur Penelitian Penelitian ini terdiri atas beberapa tahapan, dimulai dengan pemeliharaan udang vaname ke stadia uji, persiapan wadah dan media, pembuatan pakan meniran, persiapan
II. METODE PENELITIAN 2.1 Prosedur Penelitian Penelitian ini terdiri atas beberapa tahapan, dimulai dengan pemeliharaan udang vaname ke stadia uji, persiapan wadah dan media, pembuatan pakan meniran, persiapan
Deteksi DNA Seara Visual Dengan Teknik Elektroforesis
 Deteksi DNA Seara Visual Dengan Teknik Elektroforesis Laurencius Sihotang I. Tujuan 1. Mempelajari 2. Mendeteksi DNA yang telah di isolasi dengan teknik spektrofotometrik 2. mengetahui konsentrasi dan
Deteksi DNA Seara Visual Dengan Teknik Elektroforesis Laurencius Sihotang I. Tujuan 1. Mempelajari 2. Mendeteksi DNA yang telah di isolasi dengan teknik spektrofotometrik 2. mengetahui konsentrasi dan
Pengujian DNA, Prinsip Umum
 Pengujian DNA, Prinsip Umum Pengujian berbasis DNA dalam pengujian mutu benih memang saat ini belum diregulasikan sebagai salah satu standar kelulusan benih dalam proses sertifikasi. Dalam ISTA Rules,
Pengujian DNA, Prinsip Umum Pengujian berbasis DNA dalam pengujian mutu benih memang saat ini belum diregulasikan sebagai salah satu standar kelulusan benih dalam proses sertifikasi. Dalam ISTA Rules,
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Kegiatan penelitan ini meliputi kegiatan kultivasi kandidat bakteri probiotik dari saluran pencernaan ikan sidat (Anguilla bicolor), uji aktivitas
BAB III METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Kegiatan penelitan ini meliputi kegiatan kultivasi kandidat bakteri probiotik dari saluran pencernaan ikan sidat (Anguilla bicolor), uji aktivitas
METODE PENELITIAN. Metode Penelitian
 METODE PENELITIAN Waktu dan Tempat Penelitian Penelitian ini dilakukan selama 6 bulan, mulai Maret 2010 sampai dengan Agustus 2010 di laboratorium Terpadu Bagian Mikrobiologi Medik dan laboratorium Bakteriologi
METODE PENELITIAN Waktu dan Tempat Penelitian Penelitian ini dilakukan selama 6 bulan, mulai Maret 2010 sampai dengan Agustus 2010 di laboratorium Terpadu Bagian Mikrobiologi Medik dan laboratorium Bakteriologi
BAB III MATERI DAN METODE. Penelitian tentang populasi bakteri dan keberadaan bakteri gram pada
 10 BAB III MATERI DAN METODE Penelitian tentang populasi bakteri dan keberadaan bakteri gram pada pellet calf starter dengan penambahan bakteri asam laktat dari limbah kubis terfermentasi telah dilaksanakan
10 BAB III MATERI DAN METODE Penelitian tentang populasi bakteri dan keberadaan bakteri gram pada pellet calf starter dengan penambahan bakteri asam laktat dari limbah kubis terfermentasi telah dilaksanakan
4.1. Alat dan Bahan Penelitian a. Alat Penelitian. No. URAIAN ALAT. A. Pengambilan sampel
 7 IV. METODE PENELITIAN Ikan Lais diperoleh dari hasil penangkapan ikan oleh nelayan dari sungaisungai di Propinsi Riau yaitu S. Kampar dan S. Indragiri. Identifikasi jenis sampel dilakukan dengan menggunakan
7 IV. METODE PENELITIAN Ikan Lais diperoleh dari hasil penangkapan ikan oleh nelayan dari sungaisungai di Propinsi Riau yaitu S. Kampar dan S. Indragiri. Identifikasi jenis sampel dilakukan dengan menggunakan
MATERI DAN METODE. Lokasi dan Waktu
 MATERI DAN METODE Lokasi dan Waktu Analisis Polymerase Chain Reaction (PCR) serta analisis penciri Polymerase Chain Reaction-Restriction Fragment Length Polymorphism (PCR-RFLP) dilaksanakan di Laboratorium
MATERI DAN METODE Lokasi dan Waktu Analisis Polymerase Chain Reaction (PCR) serta analisis penciri Polymerase Chain Reaction-Restriction Fragment Length Polymorphism (PCR-RFLP) dilaksanakan di Laboratorium
III. METODE PENELITIAN. Penelitian ini dilaksanakan pada bulan Mei sampai Oktober 2014, di
 III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Mei sampai Oktober 2014, di Laboratorium dan Fasilitas Karantina Marine Research Center (MRC) PT. Central Pertiwi Bahari
III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Mei sampai Oktober 2014, di Laboratorium dan Fasilitas Karantina Marine Research Center (MRC) PT. Central Pertiwi Bahari
BAB III BAHAN DAN METODE
 BAB III BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Fisiologi Hewan Air Fakultas Perikanan dan Ilmu Kelautan, pada bulan Maret 2013 sampai dengan April 2013.
BAB III BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Fisiologi Hewan Air Fakultas Perikanan dan Ilmu Kelautan, pada bulan Maret 2013 sampai dengan April 2013.
MATERI DAN METODE. Lokasi dan Waktu. Materi
 MATERI DAN METODE Lokasi dan Waktu Penelitian ini dilaksanakan di Laboratorium Genetika Molekuler, Bagian Pemuliaan dan Genetika Ternak, Departemen Ilmu Produksi dan Teknologi Peternakan, Fakultas Peternakan,
MATERI DAN METODE Lokasi dan Waktu Penelitian ini dilaksanakan di Laboratorium Genetika Molekuler, Bagian Pemuliaan dan Genetika Ternak, Departemen Ilmu Produksi dan Teknologi Peternakan, Fakultas Peternakan,
III. BAHAN DAN METODE. Tanaman, serta Laboratorium Lapang Terpadu, Fakultas Pertanian, Universitas
 13 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Hama dan Penyakit Bidang Proteksi Tanaman, serta Laboratorium Lapang Terpadu, Fakultas Pertanian, Universitas
13 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Hama dan Penyakit Bidang Proteksi Tanaman, serta Laboratorium Lapang Terpadu, Fakultas Pertanian, Universitas
III. METODOLOGI. (Cr 3+ ). Faktor suhu menggunakan 2 level suhu media yaitu T i (suhu 20±2
 III. METODOLOGI Waktu dan Tempat Penelitian ini dilaksanakan bulan Mei hingga November 2006 di Laboratorium Kesehatan Ikan Balai Besar Pengembangan Budidaya Air Tawar (BBPBAT) Sukabumi dan Laboratorium
III. METODOLOGI Waktu dan Tempat Penelitian ini dilaksanakan bulan Mei hingga November 2006 di Laboratorium Kesehatan Ikan Balai Besar Pengembangan Budidaya Air Tawar (BBPBAT) Sukabumi dan Laboratorium
3. METODE PENELITIAN
 29 3. METODE PENELITIAN 3.1. Lokasi dan Waktu Penelitian Lokasi penelitian meliputi Laut Sulawesi, Selat Makassar, Teluk Bone, Laut Flores, Laut Banda, Teluk Tolo, Laut Maluku dan Teluk Tomini (Gambar
29 3. METODE PENELITIAN 3.1. Lokasi dan Waktu Penelitian Lokasi penelitian meliputi Laut Sulawesi, Selat Makassar, Teluk Bone, Laut Flores, Laut Banda, Teluk Tolo, Laut Maluku dan Teluk Tomini (Gambar
BAB III METODE PENELITIAN. konsentrasi limbah cair tapioka (10%, 20%, 30%, 40%, 50% dan 0% atau kontrol)
 34 BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian disusun menggunakan metoda statistika rancangan acak lengkap (RAL) satu faktor, dimana faktor yang diujikan adalah pengaruh konsentrasi
34 BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian disusun menggunakan metoda statistika rancangan acak lengkap (RAL) satu faktor, dimana faktor yang diujikan adalah pengaruh konsentrasi
BAB III METODE PENELITIAN. Rancangan Acak Lengkap (RAL) dengan 2 faktor, faktor pertama terdiri dari 3
 BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian ini merupakan penelitian eksperimental menggunakan Rancangan Acak Lengkap (RAL) dengan 2 faktor, faktor pertama terdiri dari 3 perlakuan, sedangkan
BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian ini merupakan penelitian eksperimental menggunakan Rancangan Acak Lengkap (RAL) dengan 2 faktor, faktor pertama terdiri dari 3 perlakuan, sedangkan
BAB IV METODE PENELITIAN. Ruang lingkup dari penelitian ini meliputi bidang ilmu sitogenetika.
 BAB IV METODE PENELITIAN 4.1 Ruang lingkup penelitian Ruang lingkup dari penelitian ini meliputi bidang ilmu sitogenetika. 4.2 Tempat dan waktu penelitian Penelitian ini dilaksanakan di Pusat Riset Biomedik
BAB IV METODE PENELITIAN 4.1 Ruang lingkup penelitian Ruang lingkup dari penelitian ini meliputi bidang ilmu sitogenetika. 4.2 Tempat dan waktu penelitian Penelitian ini dilaksanakan di Pusat Riset Biomedik
III. METODE PENELITIAN. Penelitian ini dilakukan di Laboratorium Mikrobiologi Jurusan Biologi
 17 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung pada Januari
17 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung pada Januari
METODE PENELITIAN. Penelitian ini dilakukan dari Bulan April sampai dengan Juni 2013, di
 17 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian ini dilakukan dari Bulan April sampai dengan Juni 2013, di Laboratorium Mikrobiologi Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas
17 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian ini dilakukan dari Bulan April sampai dengan Juni 2013, di Laboratorium Mikrobiologi Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas
BAB III METODE PENELITIAN. Faktor I adalah variasi konsentrasi kitosan yang terdiri dari 4 taraf meliputi:
 BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian akan dilakukan menggunakan Rancangan Acak Lengkap (RAL) faktorial. Faktor pertama adalah kadar kitosan yang terdiri dari : 2%, 2,5%, dan 3%.
BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian akan dilakukan menggunakan Rancangan Acak Lengkap (RAL) faktorial. Faktor pertama adalah kadar kitosan yang terdiri dari : 2%, 2,5%, dan 3%.
