Pemungutan Kurkumin dari Kunyit (Curcuma domestica val.) dan Pemakaiannya Sebagai Indikator Analisis Volumetri
|
|
|
- Ari Kusuma
- 7 tahun lalu
- Tontonan:
Transkripsi
1 Jurnal Rekayasa Proses, Vol. 2, No. 2, Pemungutan Kurkumin dari Kunyit (Curcuma domestica val.) dan Pemakaiannya Sebagai Indikator Analisis Volumetri Ratna Sri Harjanti* Politeknik LPP, Jl Urip Sumoharjo, Balapan Yogyakarta Abstract Volumetric analysis is one of quantitative analysis methods; a very important method used in determining the concentration of substances in solution. The success of this analysis was determined by the existence of an appropriate indicator that can show the exact end-point of titration. Curcumin, a natural dye contained in the plant root of turmeric (Curcuma domestica val.) was able to function as an indicator for the color change from light yellow brown to brown at ph around 4.5 to 9.9. Curcumin is extracted from the tuber which result is called oleoresin extraction. In the case of extraction of oleoresin, the role of solvent, extraction duration, temperature, and the fineness of particles is very important. In the present work curcumin pigment was extracted from turmeric paste in ethanol as solvent at varying operating conditions; i.e temperature, duration of extraction, and particle size of turmeric powder. The extract was further distilled and weighed. The curcumin obtained at optimum conditions was then determined using a TLC Scanner. The use of curcumin as an indicator in volumetric analysis was done by mean of titration using a few acid-basic samples. The results were compared with results from titrations using phenolphthalein (pp) and methyl-orange (mo) as indicators. The results showed that the optimum condition of curcumin extraction were at a temperature of 70 C for 120 minutes with a turmeric particle size of 100 mesh. The curcumin produced had a relatively high concentration of mg/ml. In order to use it as an indicator for the end-point of volumetric analysis, the curcumin should be diluted to obtain 5% solution and use as much as 4 drops of the solution for the titration. Key words: indicator, curcumin, titration, extraction Abstrak Analisa volumetri merupakan salah satu metode analisa kwantitatif, yang sangat penting penggunaannya dalam menentukan konsentrasi zat yang ada dalam larutan. Keberhasilan analisa volumetri ini sangat ditentukan oleh adanya indikator yang tepat sehingga mampu menunjukkan titik akhir titrasi yang tepat. Kurkumin, zat warna yang terkandung dalam umbi tanaman kunyit (Curcuma domestica val.) ternyata mampu berfungsi sebagai indikator karena terjadinya perubahan warna dari kuning muda coklat menjadi coklat pada ph sekitar 4,5 9,9. Untuk mengambil kurkumin dari umbinya, dilakukan dengan cara ekstraksi. Hasil ekstraksi disebut oleoresin. Dalam hal ekstraksi oleoresin, peranan pelarut, lama ekstraksi, suhu ekstraksi, dan kehalusan partikel sangat penting. Pada pengambilan zat warna kurkumin, kunyit yang sudah dihaluskan dikenakan proses ekstraksi dengan variasi suhu operasi, lama ekstraksi, dan kehalusan serbuk kunyit. Solven yang digunakan adalah etanol. Hasil ekstraksi kemudian didistilasi dan ditimbang. Kurkumin yang diperoleh pada kondisi optimum diuji kadarnya menggunakan TLC Scanner. Pemanfaatan kurkumin sebagai indikator dalam analisa volumetri dilakukan dengan cara titrasi menggunakan beberapa sampel asam basa dan membandingkannya dengan titrasi menggunakan indikator pp dan mo. Hasil penelitian menunjukkan bahwa kondisi optimum pengambilan kurkumin adalah pada suhu 70 C, ukuran partikel kunyit 100 mesh selama 120 menit menggunakan pelarut alcohol. Kurkumin yang dihasilkan memiliki kadar 5,158 mg/ml. Kurkumin yang akan digunakan sebagai indikator titik akhir pada analisa volumetri harus diencerkan terlebih dahulu menjadi 5% volume sebanyak 4 tetes. Kata kunci: indikator, kurkumin, titrasi, ekstraksi Pendahuluan Rimpang kunyit mengandung kurkuminoid sekitar 10%, kurkumin 1-5%, dan sisanya terdiri atas demektosikurkumin serta bisdemetoksikurkumin. Komponen yang terpenting dari umbi kunyit adalah zat warna kurkumin dan minyak atsirinya. Kurkumin merupakan zat warna yang * Alamat korespondensi: ratna_sh_st@yahoo.com secara biogenetis berasal dari fenil alanin, asam malonat, dan asam sitrat. (Stahl, E., 1985). Zat warna kurkumin merupakan kristal berwarna kuning orange, tidak larut dalam ether, larut dalam minyak, dalam alkali berwarna merah kecoklatan, sedangkan dalam asam berwarna kuning muda (Nugroho, 1998). Menurut Mohammad R, dkk. (2007) kurkumin memberikan perubahan warna yang jelas dan cepat yaitu
2 50 kurang lebih 5 detik sehingga dimungkinkan digunakan sebagai indikator. Kurkumin memberikan warna yang berbeda pada setiap harga ph seperti tersaji pada Tabel 1 (Kusumopradono, 1990). R 1 HO O R1 = R2 = OCH3 R1 = OCH3 ; R2 = H R1 = R2 = H O kurkumin demetoksikurkumin bisdemetoksikurkumin Gambar 1. Rumus bangun kurkumin demetoksikurkumin bisdemetoksikurkumin Tabel 1. Warna kurkumin pada pelbagai ph ph Larutan Warna 4,5 kuning muda pucat 6,7 kuning 7,2 kuning merah 7,5 kuning merah coklat 8,0 kuning coklat 8,3 kuning coklat 8,5 kuning coklat 9,7 coklat kemerahan 9,9 coklat Indikator asam-basa ialah zat yang dapat berubah warna apabila ph lingkungannya berubah. Apabila dalam suatu titrasi, asam maupun basanya merupakan elektrolit kuat, larutan pada titik ekivalen akan mempunyai ph=7. Tetapi bila asamnya ataupun basanya merupakan elektrolit lemah, garam yang terjadi akan mengalami hidrolisis dan pada titik ekivalen larutan akan mempunyai ph > 7 (bereaksi basa) atau ph < 7 (bereaksi asam). Harga ph yang tepat dapat dihitung dari tetapan ionisasi dari asam atau basa lemah tersebut dan dari konsentrasi larutan yang diperoleh. Titik akhir titrasi asam basa dapat ditentukan dengan indikator asam basa (Underwood, 1983). Indikator yang digunakan harus memberikan perubahan warna yang nampak di sekitar ph titik ekivalen titrasi yang dilakukan, sehingga titik akhirnya masih jatuh pada kisaran perubahan ph indikator tersebut. Haryadi (1986) menyebutkan bila suatu indikator digunakan untuk menunjukkan titik akhir titrasi, maka : 1. Indikator harus berubah warna tepat pada saat titrant menjadi ekivalen dengan titrat. 2. Perubahan warna itu harus terjadi secara mendadak, agar tidak ada keraguan-keraguan tentang kapan titrasi harus dihentikan. R 2 OH (1) Jurnal Rekayasa Proses, Vol. 2, No. 2, 2008 Reaksi titrasi yang akan dilakukan untuk membuktikan bahwa kurkumin dapat digunakan sebagai indikator dalam menunjukkan titik akhir titrasi adalah titrasi basa kuat dengan asam kuat dan titrasi basa lemah dengan asam kuat. Disamping itu, digunakan juga indikator pembanding fenolftalein (pp) dan methyl orange (mo). Contoh titrasi basa kuat dengan asam kuat adalah titrasi NaOH dengan HCl. Reaksi sebagai berikut: NaOH + HCl NaCl + H 2 O (2) dalam bentuk ion, H + + OH H 2 O (3) Karena larutan yang terbentuk pada saat titik ekivalen (TE) itu larutan NaCl, maka larutan tersebut netral, sehingga [H + ] = [OH ] = 10 7 pada 25 C. Kenetralan ini juga nyata dari reaksi ion titrasi yang menyatakan bahwa yang sebenarnya bereaksi ialah ion-ion H + dan OH dan hasilnya H 2 O. maka konstanta keseimbangan reaksi titrasi ini ialah : (4) Untuk perhitungan kurva titrasi asam basa digunakan persamaan sebagai berikut: 1. Kondisi Awal ; Basa kuat [OH ] = Cb (5) ph = 14 p [OH ] (6) 2. Selama Titrasi ; Basa kuat + garamnya [OH ] = Cb (7) ph larutan ditentukan oleh basa yang tersisa. 3. Titik Ekivalen ; Garam (Basa Kuat Asam Kuat) [OH ] = [H + ] = 10 7 (8) 4. Lewat Titik Ekivalen ; Garam + Asam Kuat [H + ] = Ca (9) ph larutan ditentukan oleh asam kuat yang tersisa. Contoh titrasi basa lemah oleh asam kuat adalah titrasi NH 4 OH oleh HCl, dengan reaksi sebagai berikut: NH 4 OH + HCl H 2 O + NH 4 Cl (10) Reaksi ionnya : H NH 4 OH H 2 O + NH 4 (11) (12) (13) Untuk perhitungan kurva titrasinya digunakan persamaan sebagai berikut: 1. Kondisi Awal ; Basa Lemah - (14) 2. Selama Titrasi ; Basa Lemah + Garamnya - (15)
3 berat hasil kurkumin (gram) hasil kurkumin (gram) Jurnal Rekayasa Proses, Vol. 2, No. 2, Titik Ekivalen ; Garam Basa Lemah Asam Kuat ( Hidrolisis ) [ H ] ( Kw / Kb ).Cg (16) 4. Lewat Titik Ekivalen ; Garam + Asam Kuat [ H + ] = Ca (17) Metode Penelitian Bahan Kunyit yang sudah dikupas dan dicuci bersih, dijemur kemudian dihaluskan. Serbuk kunyit dihaluskan dalam beberapa ukuran. Kadar air sebesar 10,256%. Pengambilan kurkumin dari serbuk kunyit dilakukan dengan cara ekstraksi menggunakan pelarut etanol 96%. Alat Ekstraksi dilakukan dalam labu leher tiga dengan kelengkapannya seperti terlukis pada Gambar 2. Setelah ekstraksi selama waktu tertentu, larutan hasil didistilasi untuk menguapkan etanolnya. Distilasi dihentikan bila sudah tidak ada lagi uap alkohol yang menetes. Residu yang dihasilkan segera dipindahkan dan didinginkan, dalam keadaan dingin, residu disaring sehingga terbentuk kristal. Keterangan: 1. Labu leher tiga 2. Pengaduk 3. Termometer 4. Pemanas air 5. Pendingin balik 6. Motor pengaduk 7. Statip Gambar 2. Rangkaian Alat Ekstraksi Kristal dioven sampai diperoleh berat yang relatif tetap. Kristal yang berisi kurkumin ini dicek kadarnya menggunakan TLC Scanner (Thin Layer Chromatoghrafi Scanner). Kristal kurkumin ini kemudian dilarutkan dalam alkohol dalam berbagai persen volume, dan siap digunakan sebagai indikator dalam titrasi asam basa. Hasil dan Pembahasan Pada penelitian ini dipelajari pengaruh waktu, suhu dan ukuran butir. Pengaruh waktu Hasil penelitian untuk peubah waktu tersaji pada Gambar 3 menunjukan bahwa semakin lama waktu ekstraksi semakin banyak kurkumin yang terambil Gambar 3. Hubungan waktu ekstraksi dengan berat kurkumin Hal ini disebabkan karena waktu kontak antara kurkumin dengan pelarutnya semakin lama. Namun pada waktu 120 menit ternyata hasil kurkumin mencapai puncaknya, apabila waktu diperpanjang lagi ternyata sudah tidak efektif lagi karena waktu kontak yang diperlukan pelarut dengan bahan kunyit sudah cukup dan mencapai kondisi kesetimbangan. Pengaruh Suhu waktu ekstraksi (menit) suhu reaksi (C) Gambar 4. Hubungan antara suhu ekstraksi dengan berat kurkumin Pengaruh suhu pada proses ekstrasi dapat dilihat pada Gambar 4. Semakin tinggi suhu reaksi, kurkumin yang dihasilkan juga semakin bertambah untuk waktu reaksi yang sama, sebab gerakan molekul-molekul pereaksi semakin besar. Dengan demikian, kemungkinan terjadinya tumbukan antara molekul-molekul pereaksi yang berlanjut dengan reaksi kimia juga semakin besar. Pada suhu 70 C diperoleh hasil yang maksimal, apabila suhu dinaikkan lagi, kurkumin yang dihasilkan akan menurun. Hal ini disebabkan karena titik didih etanol adalah 78,4 C, sehingga pada suhu ekstraksi di atas titik
4 berat kurkumin (gram) 52 didihnya akan menyebabkan sebagian besar etanol menguap. Pada suhu ekstraksi di atas titik didih etanol, daya larut etanol sudah tidak efektif lagi. Pengaruh ukuran partikel Pengaruh ukuran butir kunyit disajikan pada Gambar 5 yang memaparkan bahwa ukuran serbuk kunyit yang semakin kecil ternyata akan menghasilkan kurkumin yang semakin banyak Ukuran partikel (mesh) Gambar 5. Grafik hubungan antata ukuran partikel dengan berat kurkumin Hal ini disebabkan pada ukuran butir semakin kecil akan memudahkan pelarut dalam melarutkan minyak atsiri, beserta zat warna, resin, dan zat-zat lain seperti protein dan waxe yang terkandung dalam serbuk kunyit. Pencarian kondisi optimum ukuran partikel dihentikan pada ukuran 100 mesh, karena ukuran ini sudah sangat kecil bagi serbuk kunyit. Dari Gambar 3, 4 dan 5 dapat diambil suatu kondisi optimum ekstraksi kunyit dengan etanol untuk menghasilkan kurkumin, yaitu 50 gram serbuk kunyit dengan 200 ml etanol pada suhu 70 C, ukuran partikel 100 mesh, selama 120 menit. Kurkumin yang diperoleh pada kondisi ini sebanyak 6,519 gram. Kurkumin ini dianalisa kadarnya menggunakan TLC Scanner, ternyata mempunyai kadar 5,158 mg/ml. Penentuan jumlah penggunaan larutan kurkumin Kurkumin dengan kadar 5,158 mg/ml diencerkan dengan pelarut alkohol (berdasarkan persen volume) dalam berbagai variasi. Hasil yang diperoleh digunakan sebagai indikator titrasi, untuk mengetahui seberapa banyak kurkumin yang digunakan, agar perubahan warna pada saat akhir titrasi terlihat jelas. Data yang diperoleh disajikan dalam Tabel 2. Jurnal Rekayasa Proses, Vol. 2, No. 2, 2008 Tabel 2. Penggunaan Indikator Kurkumin pada Titrasi 0,1 M HCl dengan 0,1 M NaOH Lar Jumlah Penggunaan (% vol) 1 tetes 2 tetes 3 tetes 4 tetes 1 # # # # 3 # # ## ## 5 * ** ** *** Pada penambahan indikator kurkumin 5% sebanyak 4 tetes pada 10 ml HCl 0,1 M yang akan dititrasi dengan NaOH 0,1 M menunjukkan perubahan warna yang sangat jelas dan terjadi secara mendadak, sehingga indikator kurkumin yang dipakai pada percobaan selanjutnya adalah larutan indikator kurkumin 5% sebanyak 4 tetes. Titrasi NaOH oleh HCl Penentuan titik akhir titrasi 10 ml NaOH 0,1 N oleh HCl 0,1 N dengan indikator kurkumin dan pembanding indikator pp dapat disajikan pada Tabel 3. Tabel 3. Titik akhir titrasi 10 ml NaOH 0,1 N oleh HCl 0,1N Volume HCl, ml No Indikator pp Indikator kurkumin 1 9,50 9,55 2 9,50 9,55 3 9,50 9,60 4 9,50 9,55 5 9,50 9,55 Rerata 9,50 9,56 ph = 9,0015 ph = 8,6989 Penyimpangan sebesar 0,63% yaitu perbedaan titik akhir yang ditunjukkan oleh indikator pp dan indikator kurkumin sangat kecil, sehingga kurkumin layak digunakan sebagai indikator dalam titrasi asam basa untuk alternatif pengganti fenolftalein (pp). Titrasi NH 4 OH oleh HCl Penentuan titik akhir titrasi 10 ml NH 4 OH 0,1 N oleh HCl 0,1 N dengan indikator kurkumin dan pembanding indikator mo dapat disajikan pada Tabel 4. Prosentase kesalahan 0,18% ditunjukkan oleh indikator kurkumin terhadap indikator mo pada titrasi di atas sangat kecil, sehingga kurkumin layak digunakan sebagai indikator dalam reaksi titrasi asam basa untuk alternatif pengganti methyl orange (mo). Apabila ph yang terjadi pada titik akhir titrasi kita bandingkan dengan ph titrasi asam basa pada umumnya, akan terlihat bahwa pada titrasi NaOH oleh HCl, penggunaan indikator fenol-ftalein sangat tepat karena pada kondisi inilah merupakan daerah curam yang perubahan warnanya terjadi secara mendadak. Perbedaan ph yang diperoleh pada penggunaan indikator
5 Jurnal Rekayasa Proses, Vol. 2, No. 2, kurkumin tidak jauh berbeda dengan indikator fenolftalein. ph yang diperoleh masih berada pada daerah curam. Hal ini merupakan salah satu syarat dipakainya suatu indikator titik akhir titrasi dapat digunakan. Tabel 4. Titik akhir titrasi 10 ml NH 4 OH 0,1 N oleh HCl 0,1 N Volume HCl, ml No Indikator mo Indikator kurkumin 1 10,73 10, ,73 10, ,73 10, ,73 10, ,73 10,71 Rerata 10,73 10,71 ph = 4,2668 ph = 5,8568 Gambar 6. Kurva titrasi basa kuat dengan asam kuat berbagai konsentrasi Gambar 7. Kurva titrasi 0,1 M NH 4 OH oleh 0,1 HCl Hal yang sama juga dapat dilihat saat kurkumin digunakan indikator dalam titrasi NH 4 OH oleh HCl dengan indikator pembanding mo (methyl orange). Perbandingan dengan hasil lain Penelitian serupa pernah dilakukan, namun kondisi operasi yang digunakan berbeda. Kusumopradono (1990) meneliti perubahan ph yang terjadi pada zat warna kurkumin dengan ph meter, hasilnya dapat dilihat pada Tabel 1. Sedangkan Harjanti, dkk (2003) menggunakan serbuk kunyit dengan ukuran 40 mesh sebanyak 45 gram diekstraksi dengan 300 ml etanol, pada suhu 70 C, selama 4 jam. Kurkumin yang dihasilkan mempunyai kadar 1,585 mg/ml. Apabila dibandingkan dengan penelitian ini, terdapat perbedaan yang sangat nyata pada ukuran partikel 40 mesh dengan 100 mesh. Di samping itu, waktu yang diperlukan dalam proses ekstraksi relatif lama. Pada penelitian terdahulu memerlukan 4 jam untuk menghasilkan kurkumin dengan kadar 1,585 mg/ml, sedangkan pada penelitian ini hanya membutuhkan 120 menit untuk menghasilkan kurkumin dengan kadar 5,158 mg/ml. Semakin kecil ukuran partikel yang diekstraksi, semakin singkat waktu ekstraksinya untuk menghasilkan kurkumin dengan kadar yang lebih tinggi. Kesimpulan Dari uraian diatas dapat ditarik kesimpulan sebagai berikut. 1. Proses pengambilan kurkumin dengan cara ekstraksi merupakan proses yang sederhana dan dapat dilakukan dalam skala kecil dengan biaya yang tidak terlalu tinggi. 2. Kondisi operasi yang optimum dalam ekstraksi kunyit adalah pada suhu 70 C, dengan ukuran partikel 100 mesh selama 120 menit, kurkumin yang dihasilkan 6,519 gram mempunyai kadar 5,158 gr/ml. 3. Penggunaan kurkumin sebagai indikator harus diencerkan sampai 5% volume sebanyak 4 tetes. 4. Kurkumin dapat digunakan sebagai indikator titik akhir titrasi dalam analisis volumetri menggantikan fenolftalein dan methyl orange. Daftar Lambang [ ] : konsentrasi Cb : konsentrasi basa, mol/l Ca : konsentrasi asam, mol/l Cg : konsentrasi garam, mol/l BL : basa lemah BK : basa kuat K : konstanta keseimbangan reaksi titrasi Kb : derajat kebasaan Ka : derajat keasaman Kw : Konstanta disosiasi air ph : -log [H+]
6 54 poh : -log [OH ] ff : fenolftalein # : tidak terlihat perubahan warna ## : perubahan warna tidak jelas * : perubahan warna agak jelas ** : perubahan warna jelas tetapi agak lama *** : perubahan warna jelas dan sekonyongkonyong Jurnal Rekayasa Proses, Vol. 2, No. 2, 2008 Daftar Pustaka Harjadi, Ilmu Kimia Analitik Dasar, hal , , Gramedia, Jakarta. Harjanti, R.S., Purwanti, E., Sarto, Zat Warna Kunyit (Kurkumin) sebagai Indikator Titrasi Asam Basa, Prossiding Semnas Teknik Kimia Indonesia, Kusumopradono, Perubahan Warna Kurkumin pada Pelbagai ph, Laporan Penelitian Laboratorium Proses, Universitas Diponegoro. Mohammad, R., Ahmad, M., Daud, J.M., Potensi Kurkumin Sebagai Penunjuk ph Semula jadi Untuk Pembangunan Sensor Optik ph, M.J.A.S II, Nugroho, N.A., Manfaat dan Prospek Pengembangan Kunyit, hal. 3, 4, 40-41, PT Trubus Agriwidya, Ungaran. Stahl, E., Analisa Obat Secara Kromatografi dan Mikroskopi, hal. 3-18, , Institut Teknologi Bandung. Underwood, A.L. dan Day, R.A., Analisa Kimia Kwantitatif, edisi 4, hal , Erlangga, Jakarta.
PEMANFAATAN DAN EFISIENSI KURKUMIN KUNYIT (CURCUMA DOMESTICA VAL) SEBAGAI INDIKATOR TITRASI ASAM BASA
 PEMANFAATAN DAN EFISIENSI KURKUMIN KUNYIT (CURCUMA DOMESTICA VAL) SEBAGAI INDIKATOR TITRASI ASAM BASA Ratna Sundari Magister Teknik Industri, Fakultas Teknologi Industri, Universitas Islam Indonesia, Jl.
PEMANFAATAN DAN EFISIENSI KURKUMIN KUNYIT (CURCUMA DOMESTICA VAL) SEBAGAI INDIKATOR TITRASI ASAM BASA Ratna Sundari Magister Teknik Industri, Fakultas Teknologi Industri, Universitas Islam Indonesia, Jl.
Regina Tutik Padmaningrum, UNY
 TITRASI ASAM LEMAH DENGAN BASA KUAT Oleh: Regina Tutik Padmaningrum, M.Si Jurusan Pendidikan Kimia, FMIPA, Universitas Negeri Yogyakarta regina_tutikp@uny.ac.id Pada titrasi asam lemah dengan basa kuat,
TITRASI ASAM LEMAH DENGAN BASA KUAT Oleh: Regina Tutik Padmaningrum, M.Si Jurusan Pendidikan Kimia, FMIPA, Universitas Negeri Yogyakarta regina_tutikp@uny.ac.id Pada titrasi asam lemah dengan basa kuat,
PRAKTIKUM II TITRASI ASAM BASA OLEH RONIADI SAGULANI 85AK14020
 PRAKTIKUM II TITRASI ASAM BASA OLEH RONIADI SAGULANI 85AK14020 PROGRAM STUDI D3 ANALISIS KESEHATAN STIKES BINA MANDIRI GORONTALO 2014 LAPORAN AKHIR PERCOBAAN II A. JUDUL : Titrasi Asam Basa B. TUJUAN Dengan
PRAKTIKUM II TITRASI ASAM BASA OLEH RONIADI SAGULANI 85AK14020 PROGRAM STUDI D3 ANALISIS KESEHATAN STIKES BINA MANDIRI GORONTALO 2014 LAPORAN AKHIR PERCOBAAN II A. JUDUL : Titrasi Asam Basa B. TUJUAN Dengan
GALAT TITRASI. Ilma Nugrahani
 GALAT TITRASI Ilma Nugrahani Galat Titrasi Adalah galat yang terjadi karena indikator berubah warna sebelum atau sesudah titik setara ditunjukkan dari kurva titrasi titik akhir titik ekivalen. Dapat disebabkan
GALAT TITRASI Ilma Nugrahani Galat Titrasi Adalah galat yang terjadi karena indikator berubah warna sebelum atau sesudah titik setara ditunjukkan dari kurva titrasi titik akhir titik ekivalen. Dapat disebabkan
3 Percobaan. Untuk menentukan berat jenis zeolit digunakan larutan benzena (C 6 H 6 ).
 3 Percobaan 3.1 Bahan dan Alat 3.1.1 Bahan Bahan yang digunakan untuk menyerap ion logam adalah zeolit alam yang diperoleh dari daerah Tasikmalaya, sedangkan ion logam yang diserap oleh zeolit adalah berasal
3 Percobaan 3.1 Bahan dan Alat 3.1.1 Bahan Bahan yang digunakan untuk menyerap ion logam adalah zeolit alam yang diperoleh dari daerah Tasikmalaya, sedangkan ion logam yang diserap oleh zeolit adalah berasal
KIMIA ANALITIK TITRASI ASAM-BASA
 KIMIA ANALITIK TITRASI ASAM-BASA KIMIA ANALITIK 02 REGULER KELOMPOK 6 Disusun oleh: 1. Jang Jin Joo 1306399071 (11) 2. Robby Samuel 1306402204 (12) TEKNIK METALURGI DAN MATERIAL 2014 Pengertian Titrasi
KIMIA ANALITIK TITRASI ASAM-BASA KIMIA ANALITIK 02 REGULER KELOMPOK 6 Disusun oleh: 1. Jang Jin Joo 1306399071 (11) 2. Robby Samuel 1306402204 (12) TEKNIK METALURGI DAN MATERIAL 2014 Pengertian Titrasi
Metodologi Penelitian
 16 Bab III Metodologi Penelitian Penelitian dilakukan dengan menggunakan metode titrasi redoks dengan menggunakan beberapa oksidator (K 2 Cr 2 O 7, KMnO 4 dan KBrO 3 ) dengan konsentrasi masing-masing
16 Bab III Metodologi Penelitian Penelitian dilakukan dengan menggunakan metode titrasi redoks dengan menggunakan beberapa oksidator (K 2 Cr 2 O 7, KMnO 4 dan KBrO 3 ) dengan konsentrasi masing-masing
LAPORAN PRAKTIKUM KIMIA DASAR I
 LAPORAN PRAKTIKUM KIMIA DASAR I NAMA KELOMPOK : MELVIA PERMATASARI (08121006013) MELANY AMDIRA (08121006027) ANIS ALAFIFAH (08121006029) PUTRI WULANDARI (08121006071) MUTIARA BELLA (08121006073) JURUSAN
LAPORAN PRAKTIKUM KIMIA DASAR I NAMA KELOMPOK : MELVIA PERMATASARI (08121006013) MELANY AMDIRA (08121006027) ANIS ALAFIFAH (08121006029) PUTRI WULANDARI (08121006071) MUTIARA BELLA (08121006073) JURUSAN
Tentukan ph dari suatu larutan yang memiliki konsentrasi ion H + sebesar 10 4 M dengan tanpa bantuan alat hitung kalkulator!
 Kimia Study Center - Contoh soal dan pembahasan tentang cara menghitung ph dan poh larutan asam basa berdasarkan konsentrasi ion [H + ] dan [OH ] SMA kelas 11 IPA. Berikut contoh-contoh soal yang bisa
Kimia Study Center - Contoh soal dan pembahasan tentang cara menghitung ph dan poh larutan asam basa berdasarkan konsentrasi ion [H + ] dan [OH ] SMA kelas 11 IPA. Berikut contoh-contoh soal yang bisa
Derajat Keasaman dan kebasaan (ph dan poh)
 Derajat Keasaman dan kebasaan (ph dan poh) Berdasarkan teori asam basa Arhenius, suatu larutan dapat bersifat asam, basa atau netral tergantung pada konsentrasi ion H+ atau ion OH dalam larutan tersebut.
Derajat Keasaman dan kebasaan (ph dan poh) Berdasarkan teori asam basa Arhenius, suatu larutan dapat bersifat asam, basa atau netral tergantung pada konsentrasi ion H+ atau ion OH dalam larutan tersebut.
ASIDI-ALKALIMETRI PENETAPAN KADAR ASAM SALISILAT
 ASIDI-ALKALIMETRI PENETAPAN KADAR ASAM SALISILAT I. DASAR TEORI I.1 Asidi-Alkalimetri Asidi-alkalimetri merupakan salah satu metode analisis titrimetri. Analisis titrimetri mengacu pada analisis kimia
ASIDI-ALKALIMETRI PENETAPAN KADAR ASAM SALISILAT I. DASAR TEORI I.1 Asidi-Alkalimetri Asidi-alkalimetri merupakan salah satu metode analisis titrimetri. Analisis titrimetri mengacu pada analisis kimia
LOGO TEORI ASAM BASA
 LOGO TEORI ASAM BASA TIM DOSEN KIMIA DASAR FTP 2012 Beberapa ilmuan telah memberikan definisi tentang konsep asam basa Meskipun beberapa definisi terlihat kurang jelas dan berbeda satu sama lain, tetapi
LOGO TEORI ASAM BASA TIM DOSEN KIMIA DASAR FTP 2012 Beberapa ilmuan telah memberikan definisi tentang konsep asam basa Meskipun beberapa definisi terlihat kurang jelas dan berbeda satu sama lain, tetapi
TITRASI DENGAN INDIKATOR GABUNGAN DAN DUA INDIKATOR
 TITRASI DENGAN INDIKATOR GABUNGAN DAN DUA INDIKATOR I. TUJUAN 1. Memahami prinsip kerja dari percobaan. 2. Menentukan konsentrasi dari NaOH dan Na 2 CO 3. 3. Mengetahui kegunaan dari titrasi dengan indikator
TITRASI DENGAN INDIKATOR GABUNGAN DAN DUA INDIKATOR I. TUJUAN 1. Memahami prinsip kerja dari percobaan. 2. Menentukan konsentrasi dari NaOH dan Na 2 CO 3. 3. Mengetahui kegunaan dari titrasi dengan indikator
Lampiran 1. Prosedur Karakterisasi Komposisi Kimia 1. Analisa Kadar Air (SNI ) Kadar Air (%) = A B x 100% C
 LAMPIRAN Lampiran 1. Prosedur Karakterisasi Komposisi Kimia 1. Analisa Kadar Air (SNI 01-2891-1992) Sebanyak 1-2 g contoh ditimbang pada sebuah wadah timbang yang sudah diketahui bobotnya. Kemudian dikeringkan
LAMPIRAN Lampiran 1. Prosedur Karakterisasi Komposisi Kimia 1. Analisa Kadar Air (SNI 01-2891-1992) Sebanyak 1-2 g contoh ditimbang pada sebuah wadah timbang yang sudah diketahui bobotnya. Kemudian dikeringkan
Lampiran Sumber Belajar : Purba, Michael Kimia SMA. Erlangga. Jakarta
 Lampiran 3 95 INTRUKSI 1. Setiap siswa harus membaca penuntun praktikum ini dengan seksama. 2. Setelah alat dan bahan siap tersedia, laksanakanlah percobaan menurut prosedur percobaan. 3. Setelah melakukan
Lampiran 3 95 INTRUKSI 1. Setiap siswa harus membaca penuntun praktikum ini dengan seksama. 2. Setelah alat dan bahan siap tersedia, laksanakanlah percobaan menurut prosedur percobaan. 3. Setelah melakukan
KIMIA DASAR PRINSIP TITRASI TITRASI (VOLUMETRI)
 KIMIA DASAR TITRASI (VOLUMETRI) Drs. Saeful Amin, M.Si., Apt. PRINSIP TITRASI Titrasi (volumetri) merupakan metode analisis kimia yang cepat, akurat dan sering digunakan untuk menentukan kadar suatu unsur
KIMIA DASAR TITRASI (VOLUMETRI) Drs. Saeful Amin, M.Si., Apt. PRINSIP TITRASI Titrasi (volumetri) merupakan metode analisis kimia yang cepat, akurat dan sering digunakan untuk menentukan kadar suatu unsur
BAB III METODOLOGI PENELITIAN
 BAB III METODOLOGI PENELITIAN 3.1 LOKASI PENELITIAN Penelitian dilakukan di Laboratorium Kimia Analisa dan Laboratorium Proses Industri Kimia, Departemen Teknik Kimia, Fakultas Teknik Universitas Sumatera
BAB III METODOLOGI PENELITIAN 3.1 LOKASI PENELITIAN Penelitian dilakukan di Laboratorium Kimia Analisa dan Laboratorium Proses Industri Kimia, Departemen Teknik Kimia, Fakultas Teknik Universitas Sumatera
TUGAS KIMIA SMA NEGERI 1 BAJAWA TITRASI ASAM BASA. Nama : Kelas. Disusun oleh:
 TUGAS KIMIA TITRASI ASAM BASA Disusun oleh: Nama : Kelas : SMA NEGERI 1 BAJAWA 2015 TITRASI ASAM BASA 1. Prinsip Dasar Titrasi netralisasi adalah titrasi yang didasarkan pada reaksi antara suatu asam dengan
TUGAS KIMIA TITRASI ASAM BASA Disusun oleh: Nama : Kelas : SMA NEGERI 1 BAJAWA 2015 TITRASI ASAM BASA 1. Prinsip Dasar Titrasi netralisasi adalah titrasi yang didasarkan pada reaksi antara suatu asam dengan
EKSTRAKSI KURKUMIN DARI KUNYIT
 PROSIDING SEMINAR NASIONAL REKAYASA KIMIA DAN PROSES 2004 ISSN : 1411-4216 EKSTRAKSI KURKUMIN DARI KUNYIT Wahyuni, A. Hardjono, dan Paskalina Hariyantiwasi Yamrewav Jurusan Teknik Kimia, Sekolah Tinggi
PROSIDING SEMINAR NASIONAL REKAYASA KIMIA DAN PROSES 2004 ISSN : 1411-4216 EKSTRAKSI KURKUMIN DARI KUNYIT Wahyuni, A. Hardjono, dan Paskalina Hariyantiwasi Yamrewav Jurusan Teknik Kimia, Sekolah Tinggi
kimia ASAM-BASA III Tujuan Pembelajaran
 KTSP K-13 kimia K e l a s XI ASAM-BASA III Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami mekanisme reaksi asam-basa. 2. Memahami stoikiometri
KTSP K-13 kimia K e l a s XI ASAM-BASA III Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami mekanisme reaksi asam-basa. 2. Memahami stoikiometri
CH 3 COONa 0,1 M K a CH 3 COOH = 10 5
 Soal No. 1 Dari beberapa larutan berikut ini yang tidak mengalami hidrolisis adalah... A. NH 4 Cl C. K 2 SO 4 D. CH 3 COONa E. CH 3 COOK Yang tidak mengalami peristiwa hidrolisis adalah garam yang berasal
Soal No. 1 Dari beberapa larutan berikut ini yang tidak mengalami hidrolisis adalah... A. NH 4 Cl C. K 2 SO 4 D. CH 3 COONa E. CH 3 COOK Yang tidak mengalami peristiwa hidrolisis adalah garam yang berasal
Dikenal : - Asidimetri : zat baku asam - Alkalimetri : zat baku basa DASAR : Reaksi penetralan Asam + Basa - hidrolisis - buffer - hal lain ttg lart
 Dikenal : - Asidimetri : zat baku asam - Alkalimetri : zat baku basa DASAR : Reaksi penetralan Asam + Basa - hidrolisis - buffer - hal lain ttg lart a. AK + BK ph = 7 B. AK + BL ph < 7 C. AL + BK ph >
Dikenal : - Asidimetri : zat baku asam - Alkalimetri : zat baku basa DASAR : Reaksi penetralan Asam + Basa - hidrolisis - buffer - hal lain ttg lart a. AK + BK ph = 7 B. AK + BL ph < 7 C. AL + BK ph >
PENENTUAN KOMPOSISI MAGNESIUM HIDROKSIDA DAN ALUMINIUM HIDROKSIDA DALAM OBAT MAAG
 PENENTUAN KOMPOSISI MAGNESIUM HIDROKSIDA DAN ALUMINIUM HIDROKSIDA DALAM OBAT MAAG PENDAHULUAN Obat maag atau antasida adalah obat yang mengandung bahan-bahan yang efektif yang menetralkan asam dilambung.
PENENTUAN KOMPOSISI MAGNESIUM HIDROKSIDA DAN ALUMINIUM HIDROKSIDA DALAM OBAT MAAG PENDAHULUAN Obat maag atau antasida adalah obat yang mengandung bahan-bahan yang efektif yang menetralkan asam dilambung.
1.Penentuan Kadar Air. Cara Pemanasan (Sudarmadji,1984). sebanyak 1-2 g dalam botol timbang yang telah diketahui beratnya.
 57 Lampiran I. Prosedur Analisis Kimia 1.Penentuan Kadar Air. Cara Pemanasan (Sudarmadji,1984). Timbang contoh yang telah berupa serbuk atau bahan yang telah dihaluskan sebanyak 1-2 g dalam botol timbang
57 Lampiran I. Prosedur Analisis Kimia 1.Penentuan Kadar Air. Cara Pemanasan (Sudarmadji,1984). Timbang contoh yang telah berupa serbuk atau bahan yang telah dihaluskan sebanyak 1-2 g dalam botol timbang
Titrasi asam kuat-basa kuat
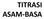 TITRASI ASAM-BASA KURVA TITRASI plot atau kurva antara ph atau poh terhadap volume titran untuk menguji apakah suatu reaksi dapat digunakan untuk analisa titrimetri ataukah tidak memilih indikator Titrasi
TITRASI ASAM-BASA KURVA TITRASI plot atau kurva antara ph atau poh terhadap volume titran untuk menguji apakah suatu reaksi dapat digunakan untuk analisa titrimetri ataukah tidak memilih indikator Titrasi
MATERI KIMIA KELAS XI SEMESTER 2 Tinggalkan Balasan
 MATERI KIMIA KELAS XI SEMESTER 2 Tinggalkan Balasan A. Pengertian Asam Basa Asam dan basa sudah dikenal sejak zaman dulu. Istilah asam (acid) berasal dari bahasa Latin acetum yang berarti cuka. Istilah
MATERI KIMIA KELAS XI SEMESTER 2 Tinggalkan Balasan A. Pengertian Asam Basa Asam dan basa sudah dikenal sejak zaman dulu. Istilah asam (acid) berasal dari bahasa Latin acetum yang berarti cuka. Istilah
TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN
 TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN I. JUDUL PERCOBAAN : TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN II. TUJUAN PERCOBAAN : 1. Membuat dan
TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN I. JUDUL PERCOBAAN : TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN II. TUJUAN PERCOBAAN : 1. Membuat dan
Haris Dianto Darwindra BAB V PEMBAHASAN
 BAB V PEMBAHASAN Titrasi merupakan suatu metoda untuk menentukan kadar suatu zat dengan menggunakan zat lain yang sudah diketahui konsentrasinya. Titrasi biasanya dibedakan berdasarkan jenis reaksi yang
BAB V PEMBAHASAN Titrasi merupakan suatu metoda untuk menentukan kadar suatu zat dengan menggunakan zat lain yang sudah diketahui konsentrasinya. Titrasi biasanya dibedakan berdasarkan jenis reaksi yang
MATERI HIDROLISIS GARAM KIMIA KELAS XI SEMESTER GENAP
 MATERI HIDROLISIS GARAM KIMIA KELAS XI SEMESTER GENAP PENDAHULUAN Kalian pasti mendengar penyedap makanan. Penyedap makanan yang sering digunakan adalah vitsin. Penyedap ini mengandung monosodium glutamat
MATERI HIDROLISIS GARAM KIMIA KELAS XI SEMESTER GENAP PENDAHULUAN Kalian pasti mendengar penyedap makanan. Penyedap makanan yang sering digunakan adalah vitsin. Penyedap ini mengandung monosodium glutamat
BAB I PENDAHULUAN A. Judul Percobaan B. Tujuan Percobaan
 BAB I PENDAHULUAN A. Judul Percobaan Penentuan kadar karbonat dan bikarbonat dalam larutan. B. Tujuan Percobaan Menyelidiki kadar karbonat dan bikarbonat dalam larutan secara asidimetri dengan menggunakan
BAB I PENDAHULUAN A. Judul Percobaan Penentuan kadar karbonat dan bikarbonat dalam larutan. B. Tujuan Percobaan Menyelidiki kadar karbonat dan bikarbonat dalam larutan secara asidimetri dengan menggunakan
wanibesak.wordpress.com 1
 Ringkasan, contoh soal dan pembahasan mengenai asam, basa dan larutan penyangga atau larutan buffer Persamaan ionisasi air H 2O H + + OH Dari reaksi di atas sesuai hukum kesetimbangan, tetapan kesetimbangan
Ringkasan, contoh soal dan pembahasan mengenai asam, basa dan larutan penyangga atau larutan buffer Persamaan ionisasi air H 2O H + + OH Dari reaksi di atas sesuai hukum kesetimbangan, tetapan kesetimbangan
DERAJAT KEASAMAN (ph)
 LAPORAN PRAKTIKUM KIMIA DASAR DERAJAT KEASAMAN (ph) DISUSUN OLEH FAISAL ARSYAD (13513128) NURUL FIKRI (13513136) JURUSAN TEKNIK LINGKUNGAN FAKULTAS TEKNIK SIPIL DAN PERENCANAAN UNIVERSITAS ISLAM INDONESIA
LAPORAN PRAKTIKUM KIMIA DASAR DERAJAT KEASAMAN (ph) DISUSUN OLEH FAISAL ARSYAD (13513128) NURUL FIKRI (13513136) JURUSAN TEKNIK LINGKUNGAN FAKULTAS TEKNIK SIPIL DAN PERENCANAAN UNIVERSITAS ISLAM INDONESIA
Bab VIII Reaksi Penetralan dan Titrasi Asam-Basa
 Bab VIII Reaksi Penetralan dan Titrasi Asam-Basa Sumber: James Mapple, Chemistry an Enquiry-Based Approach Pengukuran ph selama titrasi akan lebih akurat dengan menggunakan alat ph-meter. TUJUAN PEMBELAJARAN
Bab VIII Reaksi Penetralan dan Titrasi Asam-Basa Sumber: James Mapple, Chemistry an Enquiry-Based Approach Pengukuran ph selama titrasi akan lebih akurat dengan menggunakan alat ph-meter. TUJUAN PEMBELAJARAN
kimia TITRASI ASAM BASA
 Kurikulum 2006/2013 2013 kimia K e l a s XI TITRASI ASAM BASA Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami definisi dan macam-macam titrasi.
Kurikulum 2006/2013 2013 kimia K e l a s XI TITRASI ASAM BASA Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami definisi dan macam-macam titrasi.
Lampiran 1. Prosedur kerja analisa bahan organik total (TOM) (SNI )
 41 Lampiran 1. Prosedur kerja analisa bahan organik total (TOM) (SNI 06-6989.22-2004) 1. Pipet 100 ml contoh uji masukkan ke dalam Erlenmeyer 300 ml dan tambahkan 3 butir batu didih. 2. Tambahkan KMnO
41 Lampiran 1. Prosedur kerja analisa bahan organik total (TOM) (SNI 06-6989.22-2004) 1. Pipet 100 ml contoh uji masukkan ke dalam Erlenmeyer 300 ml dan tambahkan 3 butir batu didih. 2. Tambahkan KMnO
Kimia Study Center - Contoh soal dan pembahasan tentang hidrolisis larutan garam dan menentukan ph atau poh larutan garam, kimia SMA kelas 11 IPA.
 Kimia Study Center - Contoh soal dan pembahasan tentang hidrolisis larutan garam dan menentukan ph atau poh larutan garam, kimia SMA kelas 11 IPA. Soal No. 1 Dari beberapa larutan berikut ini yang tidak
Kimia Study Center - Contoh soal dan pembahasan tentang hidrolisis larutan garam dan menentukan ph atau poh larutan garam, kimia SMA kelas 11 IPA. Soal No. 1 Dari beberapa larutan berikut ini yang tidak
Regina Tutik Padmaningrum, Jurdik Kimia, UNY. TITRASI ASIDIMETRI *) Oleh : Regina Tutik Padmaningrum**)
 TITRASI ASIDIMETRI *) Oleh : Regina Tutik Padmaningrum**) regina_tutikp@uny.ac.id A. Beberapa Pengertian Umum dalam Titrasi Titrasi merupakan suatu proses analisis dimana suatu volum larutan standar ditambahkan
TITRASI ASIDIMETRI *) Oleh : Regina Tutik Padmaningrum**) regina_tutikp@uny.ac.id A. Beberapa Pengertian Umum dalam Titrasi Titrasi merupakan suatu proses analisis dimana suatu volum larutan standar ditambahkan
LARUTAN PENYANGGA DAN HIDROLISIS
 6 LARUTAN PENYANGGA DAN HIDROLISIS A. LARUTAN PENYANGGA B. HIDROLISIS Pada bab sebelumnya, kita sudah mempelajari tentang reaksi asam-basa dan titrasi. Jika asam direaksikan dengan basa akan menghasilkan
6 LARUTAN PENYANGGA DAN HIDROLISIS A. LARUTAN PENYANGGA B. HIDROLISIS Pada bab sebelumnya, kita sudah mempelajari tentang reaksi asam-basa dan titrasi. Jika asam direaksikan dengan basa akan menghasilkan
KIMIa ASAM-BASA II. K e l a s. A. Kesetimbangan Air. Kurikulum 2006/2013
 Kurikulum 2006/2013 KIMIa K e l a s XI ASAM-BASA II Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami kesetimbangan air. 2. Memahami pengaruh asam
Kurikulum 2006/2013 KIMIa K e l a s XI ASAM-BASA II Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami kesetimbangan air. 2. Memahami pengaruh asam
LAMPIRAN. Lampiran 1. Umbi talas (Xanthosoma sagittifolium (L.) Schott) Lampiran 2. Pati umbi talas (Xanthosoma sagittifolium (L.
 LAMPIRAN Lampiran 1. Umbi talas (Xanthosoma sagittifolium (L.) Schott) Lampiran 2. Pati umbi talas (Xanthosoma sagittifolium (L.) Schott) 47 Lampiran. Oven Lampiran 4. Autoklaf 48 Lampiran 5. Tanur Lampiran
LAMPIRAN Lampiran 1. Umbi talas (Xanthosoma sagittifolium (L.) Schott) Lampiran 2. Pati umbi talas (Xanthosoma sagittifolium (L.) Schott) 47 Lampiran. Oven Lampiran 4. Autoklaf 48 Lampiran 5. Tanur Lampiran
BAB IV HASIL PENGAMATAN DAN PERHITUNGAN
 BAB IV HASIL PENGAMATAN DAN PERHITUNGAN A. HASIL PENGAMATAN 1. Standarisasi AgNO 3 terhadap NaCl 0.1 N (Cara Mohr) Kelompok Vol. NaCl Vol. AgNO 3 7 10 ml 4 ml 8 10 ml 4.2 ml 9 10 ml 4.2 ml 10 10 ml 4.3
BAB IV HASIL PENGAMATAN DAN PERHITUNGAN A. HASIL PENGAMATAN 1. Standarisasi AgNO 3 terhadap NaCl 0.1 N (Cara Mohr) Kelompok Vol. NaCl Vol. AgNO 3 7 10 ml 4 ml 8 10 ml 4.2 ml 9 10 ml 4.2 ml 10 10 ml 4.3
Bab IV Hasil dan Diskusi
 Bab IV Hasil dan Diskusi IV.1 Hasil Eksperimen Eksperimen dikerjakan di laboratorium penelitian Kimia Analitik. Suhu ruang saat bekerja berkisar 24-25 C. Data yang diperoleh mencakup data hasil kalibrasi
Bab IV Hasil dan Diskusi IV.1 Hasil Eksperimen Eksperimen dikerjakan di laboratorium penelitian Kimia Analitik. Suhu ruang saat bekerja berkisar 24-25 C. Data yang diperoleh mencakup data hasil kalibrasi
Percobaan 6 DISTRIBUSI ZAT TERLARUT ANTARA DUA JENIS PELARUT YANG BERCAMPUR. Lab. Kimia Fisika Jurusan Kimia Universitas Negeri Semarang
 Percobaan 6 DISTRIBUSI ZAT TERLARUT ANTARA DUA JENIS PELARUT YANG BERCAMPUR Candra Tri Kurnianingsih Lab. Kimia Fisika Jurusan Kimia Universitas Negeri Semarang Gedung D8 Lt 2 Sekaran Gunungpati Semarang,
Percobaan 6 DISTRIBUSI ZAT TERLARUT ANTARA DUA JENIS PELARUT YANG BERCAMPUR Candra Tri Kurnianingsih Lab. Kimia Fisika Jurusan Kimia Universitas Negeri Semarang Gedung D8 Lt 2 Sekaran Gunungpati Semarang,
Modul 1 Analisis Kualitatif 1
 Modul 1 Analisis Kualitatif 1 Indikator Alami I. Tujuan Percobaan 1. Mengidentifikasikan perubahan warna yang ditunjukkan indikator alam. 2. Mengetahui bagian tumbuhan yang dapat dijadikan indikator alam.
Modul 1 Analisis Kualitatif 1 Indikator Alami I. Tujuan Percobaan 1. Mengidentifikasikan perubahan warna yang ditunjukkan indikator alam. 2. Mengetahui bagian tumbuhan yang dapat dijadikan indikator alam.
Lampiran 1. Karakteristik Metode GC-AOAC dan Liquid Chromatography AOAC (Wood et al., 2004)
 49 Lampiran. Karakteristik Metode GC-AOAC dan Liquid Chromatography AOAC (Wood et al., 004) Performance characteristics for benzoic acid in almond paste, fish homogenate and apple juice (GC method) Samples
49 Lampiran. Karakteristik Metode GC-AOAC dan Liquid Chromatography AOAC (Wood et al., 004) Performance characteristics for benzoic acid in almond paste, fish homogenate and apple juice (GC method) Samples
STUDI PEMANFAATAN EKSTRAK KULIT UBI JALAR (Ipomoea batatas Poir) SEBAGAI INDIKATOR PADA TITRASI ASAM BASA SKRIPSI
 1 STUDI PEMANFAATAN EKSTRAK KULIT UBI JALAR (Ipomoea batatas Poir) SEBAGAI INDIKATOR PADA TITRASI ASAM BASA SKRIPSI FERDINAND RICARDO HUTABARAT 040802048 DEPARTEMEN KIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN
1 STUDI PEMANFAATAN EKSTRAK KULIT UBI JALAR (Ipomoea batatas Poir) SEBAGAI INDIKATOR PADA TITRASI ASAM BASA SKRIPSI FERDINAND RICARDO HUTABARAT 040802048 DEPARTEMEN KIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN
LAPORAN PRAKTIKUM KIMIA DASAR. Percobaan 3 INDIKATOR DAN LARUTAN
 LAPORAN PRAKTIKUM KIMIA DASAR Percobaan 3 INDIKATOR DAN LARUTAN Disusun oleh Nama : Cinderi Maura Restu NPM : 10060312009 Shift / kelompok : 1 / 2 Tanggal Praktikum : 29 Oktober 2012 Tanggal Laporan :
LAPORAN PRAKTIKUM KIMIA DASAR Percobaan 3 INDIKATOR DAN LARUTAN Disusun oleh Nama : Cinderi Maura Restu NPM : 10060312009 Shift / kelompok : 1 / 2 Tanggal Praktikum : 29 Oktober 2012 Tanggal Laporan :
PRESENTASI POWERPOINT PENGAJAR OLEH PENERBIT ERLANGGA DIVISI PERGURUAN TINGGI. BAB 16. ASAM DAN BASA
 PRESENTASI POWERPOINT PENGAJAR OLEH PENERBIT ERLANGGA DIVISI PERGURUAN TINGGI. BAB 16. ASAM DAN BASA Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi Bab 16 Asam dan Basa Asam
PRESENTASI POWERPOINT PENGAJAR OLEH PENERBIT ERLANGGA DIVISI PERGURUAN TINGGI. BAB 16. ASAM DAN BASA Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi Bab 16 Asam dan Basa Asam
PRAKTIKUM KIMIA ANALITIK II
 PRAKTIKUM KIMIA ANALITIK II PENENTUAN KADAR KLORIDA Selasa, 1 April 2014 EKA NOVIANA NINDI ASTUTY 1112016200016 PROGRAM STUDI PENDIDIKAN KIMIA JURUSAN PEDIDIKAN ILMU PENGETAHUAN ALAM FAKULTAS ILMU TARBIYAH
PRAKTIKUM KIMIA ANALITIK II PENENTUAN KADAR KLORIDA Selasa, 1 April 2014 EKA NOVIANA NINDI ASTUTY 1112016200016 PROGRAM STUDI PENDIDIKAN KIMIA JURUSAN PEDIDIKAN ILMU PENGETAHUAN ALAM FAKULTAS ILMU TARBIYAH
LAMPIRAN. Lampiran 1. Pembakuan HCl dan Perhitungan Kadar Kandungan Boraks
 61 LAMPIRAN Lampiran 1. Pembakuan HCl dan Perhitungan Kadar Kandungan Boraks A. Pembakuan HCl dengan NaOH Molaritas HCl Pekat 37% yaitu: M = gram x 1000 Mr ml M = 37 gram 36,5 M = 10,1 M x 1000 100 Diperoleh
61 LAMPIRAN Lampiran 1. Pembakuan HCl dan Perhitungan Kadar Kandungan Boraks A. Pembakuan HCl dengan NaOH Molaritas HCl Pekat 37% yaitu: M = gram x 1000 Mr ml M = 37 gram 36,5 M = 10,1 M x 1000 100 Diperoleh
Larutan Penyangga XI MIA
 Larutan Penyangga XI MIA Komponen Larutan Penyangga Larutan Penyangga Asam Terdiri dari Asam lemah dan basa konjugasinya (Contoh : CH 3 COOH dan CH 3 COO -, HF dan F - ) Cara membuatnya : 1. Mencampurkan
Larutan Penyangga XI MIA Komponen Larutan Penyangga Larutan Penyangga Asam Terdiri dari Asam lemah dan basa konjugasinya (Contoh : CH 3 COOH dan CH 3 COO -, HF dan F - ) Cara membuatnya : 1. Mencampurkan
Lampiran 1. Prosedur Analisis Pati Sagu
 LAMPIRAN Lampiran 1. Prosedur Analisis Pati Sagu 1. Bentuk Granula Suspensi pati, untuk pengamatan dibawah mikroskop polarisasi cahaya, disiapkan dengan mencampur butir pati dengan air destilasi, kemudian
LAMPIRAN Lampiran 1. Prosedur Analisis Pati Sagu 1. Bentuk Granula Suspensi pati, untuk pengamatan dibawah mikroskop polarisasi cahaya, disiapkan dengan mencampur butir pati dengan air destilasi, kemudian
LARUTAN PENYANGGA (BUFFER)
 LARUTAN PENYANGGA (BUFFER) Larutan penyangga Larutan penyangga atau larutan buffer adalah larutan yang ph-nya praktis tidak berubah walaupun kepadanya ditambahkan sedikit asam, sedikit basa, atau bila
LARUTAN PENYANGGA (BUFFER) Larutan penyangga Larutan penyangga atau larutan buffer adalah larutan yang ph-nya praktis tidak berubah walaupun kepadanya ditambahkan sedikit asam, sedikit basa, atau bila
LAPORAN PRAKTIKUM STANDARISASI LARUTAN NaOH
 LAPORAN PRAKTIKUM STANDARISASI LARUTAN NaOH I. Tujuan Praktikan dapat memahami dan menstandarisasi larutan baku sekunder NaOH dengan larutan baku primer H 2 C 2 O 4 2H 2 O II. Dasar Teori Reaksi asam basa
LAPORAN PRAKTIKUM STANDARISASI LARUTAN NaOH I. Tujuan Praktikan dapat memahami dan menstandarisasi larutan baku sekunder NaOH dengan larutan baku primer H 2 C 2 O 4 2H 2 O II. Dasar Teori Reaksi asam basa
LAPORAN PRAKTIKUM 3 ph METER, BUFFER, dan PENGENCERAN DISUSUN OLEH : MARIA LESTARI DAN YULIA FITRI GHAZALI Kamis 04 Oktober s/d 16.
 LAPORAN PRAKTIKUM 3 ph METER, BUFFER, dan PENGENCERAN DISUSUN OLEH : MARIA LESTARI DAN YULIA FITRI GHAZALI Kamis 04 Oktober 2012 14.00 s/d 16.00 wib TUJUAN : 1. Agar mahasiswa dapat memahami prinsip-prinsip
LAPORAN PRAKTIKUM 3 ph METER, BUFFER, dan PENGENCERAN DISUSUN OLEH : MARIA LESTARI DAN YULIA FITRI GHAZALI Kamis 04 Oktober 2012 14.00 s/d 16.00 wib TUJUAN : 1. Agar mahasiswa dapat memahami prinsip-prinsip
CH 3 COOH (aq) + NaOH (aq) CH 3 COONa (aq) + H 2 O (l)
 PENGEMBANGAN PROSEDUR PENENTUAN KADAR ASAM CUKA SECARA TITRASI ASAM BASA DENGAN BERBAGAI INDIKATOR ALAMI (SEBAGAI ALTERNATIF PRAKTIKUM TITRASI ASAM BASA DI SMA) Das Salirawati, M.Si dan Regina Tutik Padmaningrum,
PENGEMBANGAN PROSEDUR PENENTUAN KADAR ASAM CUKA SECARA TITRASI ASAM BASA DENGAN BERBAGAI INDIKATOR ALAMI (SEBAGAI ALTERNATIF PRAKTIKUM TITRASI ASAM BASA DI SMA) Das Salirawati, M.Si dan Regina Tutik Padmaningrum,
LAPORAN PRAKTIKUM KIMIA ANALITIK 2 PENENTUAN KADAR KLORIDA. Senin, 21 April Disusun Oleh: MA WAH SHOFWAH KELOMPOK 1
 LAPORAN PRAKTIKUM KIMIA ANALITIK 2 PENENTUAN KADAR KLORIDA Senin, 21 April 2014 Disusun Oleh: MA WAH SHOFWAH 1112016200040 KELOMPOK 1 MILLAH HANIFAH (1112016200073) YASA ESA YASINTA (1112016200062) WIDYA
LAPORAN PRAKTIKUM KIMIA ANALITIK 2 PENENTUAN KADAR KLORIDA Senin, 21 April 2014 Disusun Oleh: MA WAH SHOFWAH 1112016200040 KELOMPOK 1 MILLAH HANIFAH (1112016200073) YASA ESA YASINTA (1112016200062) WIDYA
UJIAN PRAKTIK KIMIA SMA NEGERI 4 MATARAM TAHUN 2013
 UJIAN PRAKTIK KIMIA SMA NEGERI 4 MATARAM TAHUN 2013 Standar Kompetensi Lulusan : Mendeskripsikan sifat-sifat larutan, metode pengukuran dan terapannya. Indikator : Siswa dapat meramalkan harga ph suatu
UJIAN PRAKTIK KIMIA SMA NEGERI 4 MATARAM TAHUN 2013 Standar Kompetensi Lulusan : Mendeskripsikan sifat-sifat larutan, metode pengukuran dan terapannya. Indikator : Siswa dapat meramalkan harga ph suatu
NETRALISASI ASAM BASA SEDERHANA
 NETRALISASI ASAM BASA SEDERHANA Dosen Pembimbing : Zora Olivia, S. Farm., M.Farm, Apt GOLONGAN/KELOMPOK : A / 3 Anindiya Tazkiyah Aji Gesang Jati Abrar Rivanio Putra Siti Sofiya Miranda Faradilla Rozziqa
NETRALISASI ASAM BASA SEDERHANA Dosen Pembimbing : Zora Olivia, S. Farm., M.Farm, Apt GOLONGAN/KELOMPOK : A / 3 Anindiya Tazkiyah Aji Gesang Jati Abrar Rivanio Putra Siti Sofiya Miranda Faradilla Rozziqa
Kelas : XI IPA Guru : Tim Guru HSPG Tanggal : Senin, 23 Mei 2016 Mata pelajaran : Kimia Waktu : WIB
 Kelas : XI IPA Guru : Tim Guru HSPG Tanggal : Senin, 23 Mei 2016 Mata pelajaran : Kimia Waktu : 10.15 11.45 WIB Petunjuk Pengerjaan Soal Berdoa terlebih dahulu sebelum mengerjakan! Isikan identitas Anda
Kelas : XI IPA Guru : Tim Guru HSPG Tanggal : Senin, 23 Mei 2016 Mata pelajaran : Kimia Waktu : 10.15 11.45 WIB Petunjuk Pengerjaan Soal Berdoa terlebih dahulu sebelum mengerjakan! Isikan identitas Anda
 VISIT MY WEBSITE : KLIK AJA LINKNYA SOB http://dionlegionis.blogspot.com/search/label/education%20mipa http://dionlegionis.blogspot.com/2015/03/klasifikasi-kodok-beranak-darisulawesi.html http://dionlegionis.blogspot.com/2015/03/download-pdf-statistika-datatunggal.html
VISIT MY WEBSITE : KLIK AJA LINKNYA SOB http://dionlegionis.blogspot.com/search/label/education%20mipa http://dionlegionis.blogspot.com/2015/03/klasifikasi-kodok-beranak-darisulawesi.html http://dionlegionis.blogspot.com/2015/03/download-pdf-statistika-datatunggal.html
PENUNTUN PRAKTIKUM KIMIA DASAR II KI1201
 PENUNTUN PRAKTIKUM KIMIA DASAR II KI1201 Disusun Ulang Oleh: Dr. Deana Wahyuningrum Dr. Ihsanawati Dr. Irma Mulyani Dr. Mia Ledyastuti Dr. Rusnadi LABORATORIUM KIMIA DASAR PROGRAM TAHAP PERSIAPAN BERSAMA
PENUNTUN PRAKTIKUM KIMIA DASAR II KI1201 Disusun Ulang Oleh: Dr. Deana Wahyuningrum Dr. Ihsanawati Dr. Irma Mulyani Dr. Mia Ledyastuti Dr. Rusnadi LABORATORIUM KIMIA DASAR PROGRAM TAHAP PERSIAPAN BERSAMA
H + + OH - > H 2 O. Jumlah mol asam (proton) sama dengan jumlah mol basa (ion hidroksida). Stoikiometri netralisasi
 Netralisasi a. Netralisasi Neutralisasi dapat didefinisikan sebagai reaksi antara proton (atau ion hidronium) dan ion hidroksida membentuk air. Dalam bab ini kita hanya mendiskusikan netralisasi di larutan
Netralisasi a. Netralisasi Neutralisasi dapat didefinisikan sebagai reaksi antara proton (atau ion hidronium) dan ion hidroksida membentuk air. Dalam bab ini kita hanya mendiskusikan netralisasi di larutan
Pilihan Ganda Soal dan Jawaban Sifat Koligatif Larutan 20 butir. 5 uraian Soal dan Jawaban Sifat Koligatif Larutan.
 1 Pilihan Ganda Soal dan Jawaban Sifat Koligatif Larutan 20 butir. 5 uraian Soal dan Jawaban Sifat Koligatif Larutan. Berilah tanda silang (X) pada huruf A, B, C, D atau E di depan jawaban yang benar!
1 Pilihan Ganda Soal dan Jawaban Sifat Koligatif Larutan 20 butir. 5 uraian Soal dan Jawaban Sifat Koligatif Larutan. Berilah tanda silang (X) pada huruf A, B, C, D atau E di depan jawaban yang benar!
PERCOBAAN I PEMBUATAN DAN PENENTUAN KONSENTRASI LARUTAN
 PERCOBAAN I PEMBUATAN DAN PENENTUAN KONSENTRASI LARUTAN I. TUJUAN PERCOBAAN Tujuan percobaan praktikum ini adalah agar praktikan dapat membuat larutan dengan konsentrasi tertentu, mengencerkan larutan,
PERCOBAAN I PEMBUATAN DAN PENENTUAN KONSENTRASI LARUTAN I. TUJUAN PERCOBAAN Tujuan percobaan praktikum ini adalah agar praktikan dapat membuat larutan dengan konsentrasi tertentu, mengencerkan larutan,
BAB III METODE PENELITIAN. mengujikan L. plantarum dan L. fermentum terhadap silase rumput Kalanjana.
 BAB III METODE PENELITIAN 3.1 Rancangan Percobaan Penelitian ini merupakan penelitian eksperimental yaitu dengan cara mengujikan L. plantarum dan L. fermentum terhadap silase rumput Kalanjana. Rancangan
BAB III METODE PENELITIAN 3.1 Rancangan Percobaan Penelitian ini merupakan penelitian eksperimental yaitu dengan cara mengujikan L. plantarum dan L. fermentum terhadap silase rumput Kalanjana. Rancangan
BAB I PRAKTIKUM ASIDI AL-KALIMETRI
 BAB I PRAKTIKUM ASIDI AL-KALIMETRI I. TUJUAN a. Mahasiswa dapat menjelaskan proses titrasi asidi alkalimetri. b. Mahasiswa mampu menghitung konsentrasi sampel dengan metode asidi alkalimetri. II. DASAR
BAB I PRAKTIKUM ASIDI AL-KALIMETRI I. TUJUAN a. Mahasiswa dapat menjelaskan proses titrasi asidi alkalimetri. b. Mahasiswa mampu menghitung konsentrasi sampel dengan metode asidi alkalimetri. II. DASAR
LARUTAN PENYANGGA (BUFFER)
 LARUTAN PENYANGGA (BUFFER) Larutan penyangga Larutan penyangga atau larutan buffer adalah larutan yang ph-nya praktis tidak berubah walaupun kepadanya ditambahkan sedikit asam, sedikit basa, atau bila
LARUTAN PENYANGGA (BUFFER) Larutan penyangga Larutan penyangga atau larutan buffer adalah larutan yang ph-nya praktis tidak berubah walaupun kepadanya ditambahkan sedikit asam, sedikit basa, atau bila
Larutan Dapar Dapar adalah senyawa-senyawa atau campuran senyawa yang dapat meniadakan perubahan ph terhadap penambahan sedikit asam atau basa.
 Larutan Dapar Dapar adalah senyawa-senyawa atau campuran senyawa yang dapat meniadakan perubahan ph terhadap penambahan sedikit asam atau basa. Peniadaan perubahan ph tersebut dikenal sebagai aksi dapar.
Larutan Dapar Dapar adalah senyawa-senyawa atau campuran senyawa yang dapat meniadakan perubahan ph terhadap penambahan sedikit asam atau basa. Peniadaan perubahan ph tersebut dikenal sebagai aksi dapar.
BAB I PENDAHULUAN 1.1 Latar Belakang 1.2 Perumusan Masalah
 BAB I PENDAHULUAN 1.1 Latar Belakang Lemak dan minyak adalah trigliserida yang berarti triester (dari) gliserol. Perbedaan antara suatu lemak adalah pada temperatur kamar, lemak akan berbentuk padat dan
BAB I PENDAHULUAN 1.1 Latar Belakang Lemak dan minyak adalah trigliserida yang berarti triester (dari) gliserol. Perbedaan antara suatu lemak adalah pada temperatur kamar, lemak akan berbentuk padat dan
LARUTAN PENYANGGA (BUFFER)
 LARUTAN PENYANGGA (BUFFER) Larutan penyangga Larutan penyangga atau larutan buffer adalah larutan yang ph-nya praktis tidak berubah walaupun kepadanya ditambahkan sedikit asam, sedikit basa, atau bila
LARUTAN PENYANGGA (BUFFER) Larutan penyangga Larutan penyangga atau larutan buffer adalah larutan yang ph-nya praktis tidak berubah walaupun kepadanya ditambahkan sedikit asam, sedikit basa, atau bila
PERCOBAAN I PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA
 LAPORAN PRAKTIKUM KIMIA ANALITIK KI-2122 PERCOBAAN I PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA Nama Praktikan : Anggi Febrina NIM : 13010107 Kelompok : 5 (Shift Pagi) Tanggal
LAPORAN PRAKTIKUM KIMIA ANALITIK KI-2122 PERCOBAAN I PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA Nama Praktikan : Anggi Febrina NIM : 13010107 Kelompok : 5 (Shift Pagi) Tanggal
LAPORAN PRAKTIKUM KIMIA ANALITIK DASAR PENENTUAN KADAR NIKEL SECARA GRAVIMETRI. Pembimbing : Dra. Ari Marlina M,Si. Oleh.
 LAPORAN PRAKTIKUM KIMIA ANALITIK DASAR PENENTUAN KADAR NIKEL SECARA GRAVIMETRI Pembimbing : Dra. Ari Marlina M,Si Oleh Kelompok V Indra Afiando NIM 111431014 Iryanti Triana NIM 111431015 Lita Ayu Listiani
LAPORAN PRAKTIKUM KIMIA ANALITIK DASAR PENENTUAN KADAR NIKEL SECARA GRAVIMETRI Pembimbing : Dra. Ari Marlina M,Si Oleh Kelompok V Indra Afiando NIM 111431014 Iryanti Triana NIM 111431015 Lita Ayu Listiani
LAPORAN LENGKAP PRAKTIKUM KIMIA ANORGANIK PERCOBAAN 3 PENENTUAN BILANGAN KOORDINAI KOMPLEKS TEMBAGA (II)
 LAPORAN LENGKAP PRAKTIKUM KIMIA ANORGANIK PERCOBAAN 3 PENENTUAN BILANGAN KOORDINAI KOMPLEKS TEMBAGA (II) OLEH : NAMA : IMENG NIM: ACC 109 011 KELOMPOK : 2 ( DUA ) HARI, TANGGAL : RABU, 8 JUNI 2011 ASISTEN
LAPORAN LENGKAP PRAKTIKUM KIMIA ANORGANIK PERCOBAAN 3 PENENTUAN BILANGAN KOORDINAI KOMPLEKS TEMBAGA (II) OLEH : NAMA : IMENG NIM: ACC 109 011 KELOMPOK : 2 ( DUA ) HARI, TANGGAL : RABU, 8 JUNI 2011 ASISTEN
Penentuan Kadar Vitamin C dengan Titrasi Iodometri Langsung
 Laporan Praktikum Nama : Linda Trivana Kimia Analitik 1 NRP : G44080075 Kelompok : B-Siang Asisten : Yuyun Yunita Hari, tanggal : Selasa, 11 Mei 2010 PJP : Zulhan A, S.Si Penentuan Kadar Vitamin C dengan
Laporan Praktikum Nama : Linda Trivana Kimia Analitik 1 NRP : G44080075 Kelompok : B-Siang Asisten : Yuyun Yunita Hari, tanggal : Selasa, 11 Mei 2010 PJP : Zulhan A, S.Si Penentuan Kadar Vitamin C dengan
PENUNTUN PRAKTIKUM PENGANTAR TEKNIK KIMIA II
 PENUNTUN PRAKTIKUM PENGANTAR TEKNIK KIMIA II NAMA MAHASISWA : STAMBUK : KELOMPOK / KLS : LABORATORIUM PENGANTAR TEKNIK KIMIA JURUSAN TEKNIK KIMIA FAKULTAS TEKNOLOGI INDUSTRI UNIVERSITAS MUSLIM INDONESIA
PENUNTUN PRAKTIKUM PENGANTAR TEKNIK KIMIA II NAMA MAHASISWA : STAMBUK : KELOMPOK / KLS : LABORATORIUM PENGANTAR TEKNIK KIMIA JURUSAN TEKNIK KIMIA FAKULTAS TEKNOLOGI INDUSTRI UNIVERSITAS MUSLIM INDONESIA
Laporan Praktikum Kimia ~Titrasi asam basa~
 Laporan Praktikum Kimia ~Titrasi asam basa~ -Menentukan konsentrasi NaOH dengan HCl 0,1 M- Latifa Dinna Prayudipta XI IPA 1 SMAN 3 TANGERANG SELATAN TAHUN AJARAN 2009/2010 Laporan praktikum kimia -titrasi
Laporan Praktikum Kimia ~Titrasi asam basa~ -Menentukan konsentrasi NaOH dengan HCl 0,1 M- Latifa Dinna Prayudipta XI IPA 1 SMAN 3 TANGERANG SELATAN TAHUN AJARAN 2009/2010 Laporan praktikum kimia -titrasi
PEMBUANTAN NIKEL DMG KIMIA ANORGANIK II KAMIS, 10 APRIL 2014
 PEMBUANTAN NIKEL DMG KIMIA ANORGANIK II KAMIS, 10 APRIL 2014 Disusun oleh : AMELIA DESIRIA KELOMPOK: Ma wah shofwah, Rista Firdausa Handoyo, Rizky Dayu utami, Yasa Esa Yasinta PROGRAM STUDI PENDIDIKAN
PEMBUANTAN NIKEL DMG KIMIA ANORGANIK II KAMIS, 10 APRIL 2014 Disusun oleh : AMELIA DESIRIA KELOMPOK: Ma wah shofwah, Rista Firdausa Handoyo, Rizky Dayu utami, Yasa Esa Yasinta PROGRAM STUDI PENDIDIKAN
METODE PENELITIAN. Penelitian ini dilaksanakan dari bulan Oktober sampai Februari 2014, dengan
 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian ini dilaksanakan dari bulan Oktober sampai Februari 2014, dengan tahapan kegiatan, yaitu : bahan baku berupa singkong yang dijadikan bubur singkong,
III. METODE PENELITIAN A. Tempat dan Waktu Penelitian ini dilaksanakan dari bulan Oktober sampai Februari 2014, dengan tahapan kegiatan, yaitu : bahan baku berupa singkong yang dijadikan bubur singkong,
PEMANFAATAN BUNGA TAPAK DARA SEBAGAI ALTERNATIF PEMBUATAN INDIKATOR ph ASAM BASA
 PEMANFAATAN BUNGA TAPAK DARA SEBAGAI ALTERNATIF PEMBUATAN INDIKATOR ph ASAM BASA Muhammad Hizbul W., Eko Yuliyanto, dan Martina Retnoyuanni Mahasiswa FMIPA Universitas Negeri Yogyakarta Abstract This research
PEMANFAATAN BUNGA TAPAK DARA SEBAGAI ALTERNATIF PEMBUATAN INDIKATOR ph ASAM BASA Muhammad Hizbul W., Eko Yuliyanto, dan Martina Retnoyuanni Mahasiswa FMIPA Universitas Negeri Yogyakarta Abstract This research
EKSTRAKSI KURKUMIN DARI TEMULAWAK DENGAN MENGGUNAKAN ETANOL
 EKSTRAKSI KURKUMIN DARI TEMULAWAK DENGAN MENGGUNAKAN ETANOL A. F. Ramdja, R.M. Army Aulia, Pradita Mulya Jurusan Teknik Kimia Fakultas Teknik Universitas Sriwijaya ABSTRAK Temulawak ( Curcuma xanthoriza
EKSTRAKSI KURKUMIN DARI TEMULAWAK DENGAN MENGGUNAKAN ETANOL A. F. Ramdja, R.M. Army Aulia, Pradita Mulya Jurusan Teknik Kimia Fakultas Teknik Universitas Sriwijaya ABSTRAK Temulawak ( Curcuma xanthoriza
OAL TES SEMESTER II. I. Pilihlah jawaban yang paling tepat!
 KIMIA XI SMA 217 S OAL TES SEMESTER II I. Pilihlah jawaban yang paling tepat! 1. Basa menurut Arhenius adalah senyawa yang bila dilarutkan dalam air akan menghasilkan a. proton d. ion H b. elektron e.
KIMIA XI SMA 217 S OAL TES SEMESTER II I. Pilihlah jawaban yang paling tepat! 1. Basa menurut Arhenius adalah senyawa yang bila dilarutkan dalam air akan menghasilkan a. proton d. ion H b. elektron e.
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1. Diagram Alir Penelitian Tahapan penelitian secara umum tentang pemanfaatan daun matoa sebagai adsorben untuk menyerap logam Pb dijelaskan dalam diagram pada Gambar 3.1. Preparasi
BAB III METODE PENELITIAN 3.1. Diagram Alir Penelitian Tahapan penelitian secara umum tentang pemanfaatan daun matoa sebagai adsorben untuk menyerap logam Pb dijelaskan dalam diagram pada Gambar 3.1. Preparasi
SKL- 3: LARUTAN. Ringkasan Materi. 1. Konsep Asam basa menurut Arrhenius. 2. Konsep Asam-Basa Bronsted dan Lowry
 SKL- 3: LARUTAN 3 Menjelaskan sifat-sifat larutan, metode pengukuran dan terapannya. o Menganalisis data daya hantar listrik beberapa larutan o Mendeskripsikan konsep ph larutan o Menghitung konsentrasi
SKL- 3: LARUTAN 3 Menjelaskan sifat-sifat larutan, metode pengukuran dan terapannya. o Menganalisis data daya hantar listrik beberapa larutan o Mendeskripsikan konsep ph larutan o Menghitung konsentrasi
III. BAHAN DAN METODE
 III. BAHAN DAN METODE 3.1. BAHAN DAN ALAT 3.1.1 Bahan Baku Bahan baku yang digunakan adalah temulawak (Curcuma xanthorrhiza Roxb.) berumur sembilan bulan yang telah diiris dan dikeringkan. Temulawak tersebut
III. BAHAN DAN METODE 3.1. BAHAN DAN ALAT 3.1.1 Bahan Baku Bahan baku yang digunakan adalah temulawak (Curcuma xanthorrhiza Roxb.) berumur sembilan bulan yang telah diiris dan dikeringkan. Temulawak tersebut
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN A. Desain Penelitian Penelitian ini merupakan penelitian yang dilakukan secara eksperimental laboratorium. B. Tempat dan Waktu Penelitian ini dilakukan di Laboratorium Fakultas
BAB III METODE PENELITIAN A. Desain Penelitian Penelitian ini merupakan penelitian yang dilakukan secara eksperimental laboratorium. B. Tempat dan Waktu Penelitian ini dilakukan di Laboratorium Fakultas
BAB III METODOLOGI PENELITIAN. Penelitian ini dilaksanakan di Laboratorium Jurusan Pendidikan Kimia dan
 BAB III METODOLOGI PENELITIAN 3.1 Tempat dan Waktu Penelitian 3.1.1 Tempat Penelitian Penelitian ini dilaksanakan di Laboratorium Jurusan Pendidikan Kimia dan Laboratorium Jurusan Pendidikan Biologi FMIPA
BAB III METODOLOGI PENELITIAN 3.1 Tempat dan Waktu Penelitian 3.1.1 Tempat Penelitian Penelitian ini dilaksanakan di Laboratorium Jurusan Pendidikan Kimia dan Laboratorium Jurusan Pendidikan Biologi FMIPA
PENENTUAN KADAR ASAM ASETAT DALAM ASAM CUKA DENGAN ALKALIMETRI
 PENENTUAN KADAR ASAM ASETAT DALAM ASAM CUKA DENGAN ALKALIMETRI I. CAPAIAN PEMBELAJARAN Praktikan mampu menetapkan kadar CH3COOH (asam asetat) dan asam cuka (HCl) menggunakan prinsip reaksi asam-basa. II.
PENENTUAN KADAR ASAM ASETAT DALAM ASAM CUKA DENGAN ALKALIMETRI I. CAPAIAN PEMBELAJARAN Praktikan mampu menetapkan kadar CH3COOH (asam asetat) dan asam cuka (HCl) menggunakan prinsip reaksi asam-basa. II.
Lampiran 1. Prosedur Analisis Karakteristik Pati Sagu. Kadar Abu (%) = (C A) x 100 % B
 Lampiran 1. Prosedur Analisis Karakteristik Pati Sagu 1. Analisis Kadar Air (Apriyantono et al., 1989) Cawan Alumunium yang telah dikeringkan dan diketahui bobotnya diisi sebanyak 2 g contoh lalu ditimbang
Lampiran 1. Prosedur Analisis Karakteristik Pati Sagu 1. Analisis Kadar Air (Apriyantono et al., 1989) Cawan Alumunium yang telah dikeringkan dan diketahui bobotnya diisi sebanyak 2 g contoh lalu ditimbang
II. HARI DAN TANGGAL PERCOBAAN
 I. JUDUL PERCOBAAN Titrasi Penetralan dan Aplikasinya II. HARI DAN TANGGAL PERCOBAAN Jum at, 4 Desember 2015 III. SELESAI PERCOBAAN Jum at, 4 Desember 2015 IV. TUJUAN PERCOBAAN 1. Membuat dan menentukan
I. JUDUL PERCOBAAN Titrasi Penetralan dan Aplikasinya II. HARI DAN TANGGAL PERCOBAAN Jum at, 4 Desember 2015 III. SELESAI PERCOBAAN Jum at, 4 Desember 2015 IV. TUJUAN PERCOBAAN 1. Membuat dan menentukan
8. ASIDI-ALKALINITAS
 Asidialkalinitas 8. ASIDIALKALINITAS 8.1. Umum Pengertian asiditas adalah kemampuan air untuk menetralkan larutan basa, sedangkan alkalinitas adalah kemampuan air untuk menetralkan larutan asam. Asidialkalinitas
Asidialkalinitas 8. ASIDIALKALINITAS 8.1. Umum Pengertian asiditas adalah kemampuan air untuk menetralkan larutan basa, sedangkan alkalinitas adalah kemampuan air untuk menetralkan larutan asam. Asidialkalinitas
III. METODOLOGI. 1. Analisis Kualitatif Natrium Benzoat (AOAC B 1999) Persiapan Sampel
 III. METODOLOGI A. BAHAN DAN ALAT Bahan-bahan yang digunakan dalam penelitian ini adalah saus sambal dan minuman dalam kemasan untuk analisis kualitatif, sedangkan untuk analisis kuantitatif digunakan
III. METODOLOGI A. BAHAN DAN ALAT Bahan-bahan yang digunakan dalam penelitian ini adalah saus sambal dan minuman dalam kemasan untuk analisis kualitatif, sedangkan untuk analisis kuantitatif digunakan
LAPORAN PRAKTIKUM KIMIA DASAR II PERCOBAAN II REAKSI ASAM BASA : OSU OHEOPUTRA. H STAMBUK : A1C : PENDIDIKAN MIPA
 LAPORAN PRAKTIKUM KIMIA DASAR II PERCOBAAN II REAKSI ASAM BASA NAMA : OSU OHEOPUTRA. H STAMBUK : A1C4 07 017 KELOMPOK PROGRAM STUDI JURUSAN : II : PENDIDIKAN KIMIA : PENDIDIKAN MIPA ASISTEN PEMBIMBING
LAPORAN PRAKTIKUM KIMIA DASAR II PERCOBAAN II REAKSI ASAM BASA NAMA : OSU OHEOPUTRA. H STAMBUK : A1C4 07 017 KELOMPOK PROGRAM STUDI JURUSAN : II : PENDIDIKAN KIMIA : PENDIDIKAN MIPA ASISTEN PEMBIMBING
BAB III METODOLOGI PENELITIAN
 BAB III METODOLOGI PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian dilaksanakan dari bulan Nopember 2012 sampai Januari 2013. Lokasi penelitian di Laboratorium Riset dan Laboratorium Kimia Analitik
BAB III METODOLOGI PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian dilaksanakan dari bulan Nopember 2012 sampai Januari 2013. Lokasi penelitian di Laboratorium Riset dan Laboratorium Kimia Analitik
Soal dan Pembahasan Asam Basa, Larutan Penyangga, Hidrolisis Garam, dan K SP
 Soal dan Pembahasan Asam Basa, Larutan Penyangga, Hidrolisis Garam, dan K SP Θ Asam Basa 1. Jelaskan Pengertian Asam Basa menurut arrhenius! Asam Zat yang dalam air melepaskan ion H + Basa Senyawa yang
Soal dan Pembahasan Asam Basa, Larutan Penyangga, Hidrolisis Garam, dan K SP Θ Asam Basa 1. Jelaskan Pengertian Asam Basa menurut arrhenius! Asam Zat yang dalam air melepaskan ion H + Basa Senyawa yang
PENENTUAN TETAPAN PENGIONAN INDIKATOR METIL MERAH SECARA SPEKTROFOTOMETRI
 PENENTUAN TETAPAN PENGIONAN INDIKATOR METIL MERAH SECARA SPEKTROFOTOMETRI A. Tujuan Percobaan Percobaan. Menentukan tetapan pengionan indikator metil merah secara spektrofotometri. B. Dasar Teori Dalam
PENENTUAN TETAPAN PENGIONAN INDIKATOR METIL MERAH SECARA SPEKTROFOTOMETRI A. Tujuan Percobaan Percobaan. Menentukan tetapan pengionan indikator metil merah secara spektrofotometri. B. Dasar Teori Dalam
Praktikum Kimia Fisika II Hidrolisis Etil Asetat dalam Suasana Asam Lemah & Asam Kuat
 I. Judul Percobaan Hidrolisis Etil Asetat dalam Suasana Asam Lemah & dalam Suasana Asam Kuat II. Tanggal Percobaan Senin, 8 April 2013 pukul 11.00 14.00 WIB III. Tujuan Percobaan Menentukan orde reaksi
I. Judul Percobaan Hidrolisis Etil Asetat dalam Suasana Asam Lemah & dalam Suasana Asam Kuat II. Tanggal Percobaan Senin, 8 April 2013 pukul 11.00 14.00 WIB III. Tujuan Percobaan Menentukan orde reaksi
STANDAR PROSEDUR OPERASIONAL PENANGANAN PASCA PANEN KUNYIT. Feri Manoi
 STANDAR PROSEDUR OPERASIONAL PENANGANAN PASCA PANEN KUNYIT Feri Manoi PENDAHULUAN Untuk memperoleh produk yang bermutu tinggi, maka disusun SPO penanganan pasca panen tanaman kunyit meliputi, waktu panen,
STANDAR PROSEDUR OPERASIONAL PENANGANAN PASCA PANEN KUNYIT Feri Manoi PENDAHULUAN Untuk memperoleh produk yang bermutu tinggi, maka disusun SPO penanganan pasca panen tanaman kunyit meliputi, waktu panen,
Soal dan Jawaban Titrasi Asam Basa
 Soal dan Jawaban Titrasi Asam Basa Rabu, 16 Januari 20130 komentar Inilah beberapa contoh soal dan jawaban tentang titrasi asam basa. Bacalah benarbenar setiap latihan soal asam basa berikut. Kalau perlu,
Soal dan Jawaban Titrasi Asam Basa Rabu, 16 Januari 20130 komentar Inilah beberapa contoh soal dan jawaban tentang titrasi asam basa. Bacalah benarbenar setiap latihan soal asam basa berikut. Kalau perlu,
