KIMIA KARBON (ORGANIK)
|
|
|
- Verawati Sudjarwadi
- 7 tahun lalu
- Tontonan:
Transkripsi
1 KIMIA KARBN (RGANIK) A. Isomeri Isomeri adalah senyawa-senyawa kimia yang mempunyai rumus molekul sama tetapi rumus strukturnya berbeda, sehingga sifat-sifatnya pun berbeda. Macam-macam isomer : 1. Isomer Rantai : adanya pernedaan susunan rantai karbon dari senyawa segolongan n pentana dengan 2-metil butana (iso pentana) 2. Isomer Posisi : adanya perbedaab letak gugus fungsi pada rantai karbon dari senyawa segolongan 1-butanol dengan 2-butanol 3. Isomer Fungsi : adanya gugus fungsi yang berbeda Pasangan isomer fungsi : Alkena dengan sikloalkana [ C n H 2n ] Alkuna dengan alkandiena [ C n H 2n 2 ] Alkohol dengan eter [ C n H 2n + 2 ] Aldehid dengan keton [ C n H 2n ] Alkanoat dengan ester [ C n H 2n 2 ] 4. Isomer Geometri : isomer sis-trans terjadi jika pada ikatan karbon rangkap dua mengandung dua atom atau gugus yang sama Isomer cis : atom / gugus yang sama letak satu sisi Isomer trans : atom / gugus yang sama letak berseberangan 1. CH 3 CH 2 CH CH CH 2 CH 3 2. CH 3 CH 2 CH C(CH 3 ) CH 2 CH 3 5. Isomer ptik : senyawa yang dapat memutar bidang polarisasi cahaya (eksperimen) dan mempunyai atom C asimetris (teoritis). Atom C asimetris : atom C yang mengikat empat gugus / atom yang berbeda. CH 2 CH(H)CH (asam laktat) Senyawa dekstro (d) : senyawa optis aktif yang memutar bidang polarisasi cahaya kearah kanan. Senyawa levo ( l ) : senyawa optis aktif yang memutar bidang polarisasi cahaya ke kiri. Jumlah maksimal isomer optis = 2 n, dimana n = jumlah atom C asimetris. B. Gugus Fungsional Gugus fungsional adalah atom atau kelompok atom yang memberikan beberapa sifat khas dan pusat aktif dari molekul yang mengikatnya. Beberapa gugus fungsional : Nama Rumus Molekul Rumus Struktur Alkana C n H 2n + 2 C C Alkena C n H 2n C = C Alkuna C n H 2n 2 C C Alkanol C n H 2n + 2 H Eter C n H 2n + 2 Alkanal C n H 2n C H Alkanon C n H 2 C Alkanoat C n H 2 2 Ester C n H 2 2 C H C 1
2 Nama Rumus Molekul Rumus Struktur Amina primer NH 2 R NH 2 R NH R NH Amina sekunder R R N R Amina tersier N R Alkil halida X R X C. Reaksi-reaksi Kimia Karbon 1. Reaksi Substitusi : Penggantian gugus atau atom yang terikat pada atom karbon. R H + Cl 2 R Cl + HCl R CH + Cl 2 R CH + HCl R CH + PCl 5 C CCl + HCl + PCl 3 R H + PCl 5 R Cl + HXCL + PCl 3 R Cl + NaH R H + NaCl R CH + R H R CR + H 2 (reaksi esterifikasi) RX + R Na R R + NaX (Sintetis Wiliamson) 2. Reaksi Adisi : Reaksi pemutusan ikatan rangkap CH 3 CH = CH + H 2 CH 3 CH 2 CH 3 + H 2 C H C H H Cl H CH 3 CH 2 CH = CH 2 + H Cl CH 3 CH 2 CH CH 2 (adisi markovnikov) 3. Reaksi Eliminasi : Reaksi pembentukan ikatan rangkap CH H 2 S 4 3 CH CH 2 CH 3 CH 2 CH = CH 2 + H 2 (dehidrogenasi) H H CH Katalis 2 CH 2 CH 2 = CH 2 + H 2 H H CH 3 CH CH CH 3 + CH 3 K CH 3 CH = CH CH 3 + CH 3 K + KCl (aturan saytzef) H Cl 4. Reaksi Redoks 1. ksidasi sempurna senyawa hidrokarbon menghasilkan gas C 2 dan H 2 (uap). ksidasi C x H y C 2co 2 H 2 2. ksidasi alkohol - Alkohol primer ks Aldehid ks Asam karboksilat - Alkohol sekunder ks Keton - Alkohol tersier ks D. Macam-macam Senyawa Karbon 1. Alkana dan Alkil - Rumus alkana : C n H 2n Rumus alkil : C n H 2n + 1 Sumber senyawa alkana : minyak bumi, batubara, gas alam. 2
3 Sifat fisik : - Non polar, tarik-menarik antar molekul lemah, tidak larut dalam air, larut dalam senyawa organik (non polar) dan sedikit polar. - Pada suhu kamar dan tekanan 1 atm : C 1 C 4 = gas (tidak berbau) C 5 C 17 = cair (berbau bensin) C 18 dst = padat (tidak berbau) - Titik didih senyawa rantai lurus > titik didih senyawa rantai bercabang. - Mr >> titik didih >> Sifat kimia : - Kurang reaktif dibanding senyawa organik yang memiliki gugus fungsi. - Tidak bereaksi dengan asam (stabil) - Dapat bereaksi dengan halogen CH 4 : metana CH 3 : metil C 2 H 6 : etana C 2 H 5 : etil 2. Alkena ( C n H 2n ) a. Gugus fungsi : C = C b. Tatanama 1. Nama alkena yang mengandung satu ikatan rangkap mempunyai nama dari alkana yang sesuai dengan mengganti ankhiran ana menjadi ena. 2. Bila terdapat dua atau lebih ikatan rangkap namanya menjadi alkadiena, alkatriena dan sebagainya. 3. Tempat ikatan rangkap dinyatakan dengan nomor atom karbon yang mendahului sesuai dengan alkana. c. Reaksi pengenalan alkena Alkena dapat menghilangkan warna merah coklat dari bromium. CH 2 = CH 2 + Br 2 CH 2 CH 2 merah coklat Br Br tidak berwarna 3. Alkuna ( C n H 2n 2 ) a. Gugus fungsi : C C b. Tatanama 1. Sama dengan tatanama pada alkena, akhiran ena digati una. 2. Aturan selanjutnya sama dengan aturan pada alkuna, yag perlu diingat bahwa pada alkuna memiliki ikatan rangkap 3. CH 3 CH 2 C C CH 3 : 2 pentuna CH 3 CH C CH : 3 metil 1 butena CH 3 c. Reaksi pengenalan alkuna Alkuna dapat menghilangkan warna merah coklat dari bromin Br Br CH + 2 Br + 2 Br 2 CH CH CH CH CH Br Br Br Br Br 4. Alkohol ( C n H 2n + 1 H ) a. Gugus fungsi : H b. Tatanama Alkohol dapat dipandang sebagai turunan alkana, dimana satu atom H dari alkana diganti dengan gugus hidroksil ( H ). Sehingga nama alkohol diambil dari alkana dimana akhiran a diganti dengan akhiran ol, sedangkan letak gugus H terikat dinyatakan dengan angka. Atau diambil nama radikal alkil + alkohol. CH 3 CH 2 CH 2 H : 1 propanol = propil alkohol CH 3 CH CH 3 : 2 propanol = isopropil alkohol H 3
4 Berdasarkan letak ikatan H pada atom C, alkohol dibedakan menjadi : - Alkohol primer : gugus H terikat pada atom C primer - Alkohol sekunder : gugus H terikat pada atom C sekunder - Alkohol tersier : gugus H terikat pada atom C tersier c. Reaksi pengenalan alkohol 1. Bereaksi dengan logam natrium menghasilkan gas hidrogen R na + Na R Na + ½ H 2 2. Bereaksi dengan hidrogen halida menggunakan katalis ZnCl mebentuk alkil halida. R H + HCl R Cl + H 2 Reaksi ini dapat dipakai untuk membedakan alkohol primer, sekunder dan tersier (disebut test Lucas) - Alkohol primer + HCl sangat lambat - Alkohol sekunder + HCl cepat - Alkohol tersier + HCl sangat cepat 3. Alkohol bereaksi dengan fosfor pentaklorida menghasilkan alkil klorida, HCl dan PCl. R H + PCl 5 R Cl + PCl 3 + HCl d. Sifat-sifat fisik alkohol 1. Cairan encer, mudah bercampur dengan air dalam segala perbandingan. 2. Alkohol mempunyai titik didih tinggi dibanding alkana yang jumlah atom C sama, karena antar molekul alkohol membentuk ikatan hidrogen. e. Kegunaan Alkohol 1. Etanol didapatkan pada minuman keras, dalam jumlah kecil menyebabkan pembuluh darah dan tekanan darah menurun. Dalam jumlah besar menyebabkan keracunan, merusak hati dan menyebabkan kematian. 2. Etanol digunakan sebagai pelarut yang baik. 3. Gasohol adalah campuran etanol dengan gasolin dipakai untuk bahan bakar. 4. Spiritus adalah campuran metanol + etanol + zat warna metilen blue. 5. Etanol 70% dipakai untuk desinfektan. 6. Metanol dikenal sebagai alkohol kayu, merupakan racun dapat menyebabkan kebutaan, kehilangan kontrol dan menimbulkan kematian. 7. Metanol juga sebagai pelarut dan sebagai bahan dasar pembuatan formaldehid. Poli Alkohol Poli alkohol adalah alkohol yang mempunyai lebih dari satu gugus fungsi H. glikol dan gliserol. Glikol (1,2 etandiol) : CH 2 CH 2 H H Glikol berupa cairan manis, tidak berwarna, kental. Dibuat dengan oksidasi etena dengan katalisator perak, hasilnya kemudian dihidrolisa dalam suasana asam. CH 2 = CH 2 2 H + H 2 2 C CH CH 2 CH 2 2 (Ag) H + H H etena etilen oksida glikol Kegunaan : Glikol dipakai untuk cairan anti beku dalam radiator mobil, juga untuk industri plastik dan serat poliester dan fiber dan sebagai zat aditif untuk mencegah pertumbuhan jamur. Gliserol (1,2,3 propantriol) H Diperoleh sebagai hasil samping pembuatan sabu. Minyak + NaH sabun + gliserol. 2 C H Glisero berupa cairan kental, tidak berwarna, bersifat higroskopis, berasa manis, larut H C H dalam air dalam segala perbandingan. Penggunaan : 1. Digunakan dalam makanan dan gula-gula untuk membuatnya lunak dan lembab H 2 C H 2. Sebagai zat anti beku 3. Kadang ditambahkan pada minuman beralkohol untuk mengurangi ketajaman rasa. 4
5 5. Eter ( R R ) a. Tatanama Nama eter, mula-mula disebutkan dulu nama alkil pertama kemudian alkil kedua diikuti kata eter. Alkil pertama adalah huruf awalnya terletak lebih depan dalam urutan abjad. Eter dapat dipandang sebagai turunan alkana dimana sebuah atom H-nya diganti dengan gugus alkoksi : C n H 2n+1. Sehingga nama eter mula-mula disebutkan dulu nama alkoksi, alkil yang lain disebutkan senama alkana yang bersangkutan. CH 3 CH 3 : dimetil eter = metoksi metana CH 3 CH 2 CH 3 : etil metil eter = metoksi etana CH 3 CH 2 CH 2 CH 3 : dietil eter = etoksi etana b. Reaksi pengenalan eter Eter bereaksi dengan PCl 5 jika dipanaskan. R R + PCl 5 R Cl + R 1 Cl + PCl 3 Tidak dibebaskannya HCl dalam reaksi tersebut bisa untuk membedakan eter dengan alkohol. Perbedaan antara alkohol dan alkoksi alkana / eter ALKHL - dapat bereaksi dengan logam alkali - dapat dioksidasi menjadi aldehid/keton - dapat bereaksi dengan PCl 5 atau PCl 3 membebaskan HCl - titik didih relatif tinggi karena adanya ikatan hidrogen ALKKSI ALKANA / ETER - tidak dapat bereaksi dengan logam alkali - tidak dapat dioksidasi - dapat bereaksi dengan PCl 5 jika dipanaskan tapi tidak membebaskan HCl - titik didih relatif rendah c. Kegunaan eter 1. Sebagai pelarut zat-zat organik 2. Untuk obat bius 6. Alkanal ( R C H ) a. Tatanama Nama alkanal (aldehid) berasal dari nama alkana yang bersangkutan dengan mengganti akhiran ana dengan al. CH 3 CH 2 CH 2 CH 2 C H CH 3 CH 2 CH 2 C H ( pentanal (IUPAC) = valeraldehida (Trivial) ) ( butanal (IUPAC) = butiraldehida (Trivial) ) Isomer pada alkanol bisa disebabkan perbedaan posisi gugus fungsi (isomer posisi) dan pada rantai karbonnya. b. Reaksi pengenalan 1. Aldehid dengan reagen Tollens (larutan AgN 3 dalam amoniak yang mengandung Ag(NH 3 ) 2 menghasilkan cermin perak. R C H + Ag(NH 3 ) 2 + H - R C H + Ag (s) + NH 3 + H 2 2. Aldehid dengan pereaksi Fehling menghasilkan endapan Cu 2 yang berwarna merah bata. R C H + Cu R C H + Cu 2 (merah bata) Pereaksi Fehling dibuat dengan mencampurkan Fehling A (larutan CuS 4 ) dengan Fehling B (campuran KNa Tartrat + NaH). 5
6 c. Kegunaan 1. Larutan 40% formaldehid disebut formalin digunakan untuk pengawet preparat anatomi. Formaldehid bersifat mengubah protein menjadi zat yang kenyal dan padat. 2. Formaldehid dengan fenol berpolimerisasi membentuk plastik. 3. Formaldehid untuk pembuatan lem kayu. 4. Asetaldehid adalah bahan baku DDT 7. Alkanon ( R C R 1 ) a. Tatanama Nama alkanon (keton) berasal dari alkana yang bersangkutan dengan mengganti akhiran ana dengan akhiran anon. CH 3 CH 3 CH CH 2 C CH 3 ( 4-metil, 2-pentanon ) Isomer pada alkanon terjadi karena perbedaan posisi gugus karbonil dan rantai karbonnya, juga dijumpai isomer fungsional dengan aldehida. b. Kegunaan 1. Bahan yang penting bagi berbagai sintesis 2. Bahan pembuatan kosmetik (cat kuku, parfum, dsb) 3. Bahan dasar pembuatan kloroform, iodoform c. Perbedaan aldehida dan keton ALDEHIDA 1. Bereaksi dengan reagen Fehling menghasilkan endapan merah bata, Cu Bereaksi dengan reagen Tollens menghasilkan cermin perak, Ag. 3. Bereaksi dengan reagen Benedict menghasilkan endapan merah bata, Cu Dioksidasi menjadi asam karboksilat. KETN 1. Tidak bereaksi dengan reagen Fehling. 2. Tidak bereaksi dengan reagen Tollens. 3. Tidak bereaksi dengan reagen Benedict. 4. Sukar dioksidasi. 8. Asam Alkanoat / Karboksilat a. Tatanama - Asam karboksilat alifatik diberi nama mengikuti nama alkana dengan jumlah atom C yang sama dengan mengganti akhiran ana menjadi anoat. - Atom C pada gugus CH selalu diberi nomor satu. - Nama trivial (biasa) asam karboksilat seringkali diturunkan dari nama seumbernya. Untuk menyebutkan letak substitusinya atom-atom karbon diberi tanda α, β, γ, dan seterusnya. - Atom C alfa adalah atom C yang terletak langsung dibelakang gugus CH. Asam 2-metil propanoat (IUPAC) = Asam isobutirat = asam 2- CH 3 CH C H metil propionat (Trivial) CH 3 CH 3 CH 2 CH 2 C H Asam butanoat (IUPAC) = Asam butirat (Trivial) Berikut ini contoh asam yang paling banyak dijumpai sehari-hari. 1. Asam Format (HCH Sifat-sifat - Berupa zat cair tidak berwarna, berbau merangsang dan jika terkena kulit akan melepuh. - Karena mengandung gugus aldehid, asam format dapat bereaksi dengan reagen Tollens maupun Fehling - Mudah dioksidasi membentuk gas C 2 dan H 2. 6
7 Pembuatan 1. ksidasi metanol 2. Hidrolisis HCN Reaksi : HCn + 2 H 2 HCH + NH 3 3. Dalam teknik dibuat dari C + uap air yang dialirkan melalui katalis oksida logam, pada 200 o C dan tekanan besar. Reaksi : C + H 2 HCH Kegunaan Asam format banyak digunakan untuk menggumpalkan getah karet (lateks); dalam industri tekstil penyamakan kulit, pembuatan plastik. 2. Asam asetat Adalah zat cair jernih berbau merangsang, tidak berwarna membeku pada 16,6 o C. berbentuk kristal serupa dengan es karena itu asam asetat murni disebut juga asam asetat glasial. Pembuatan 1. Terbentuk pada oksida etanol karena pengaruh berbagai jenis bakteri seperti acetobakter. 2. Dalam teknik dengan mengalirkan campuran berupa etanol dan udara melalui katalisator. CH 3 CH 2 H [] CH 3 CH [] CH 3 CH - H 2 Penggunaan Asam asetat banyak digunakan untuk penyedap makanan dengan nama cuka, untuk pembuatan selulosa asetat, plastik, parfum, zat warna dan obat. Asam alkanoat yang lain : 1. Asam alkanoat tak jenuh Asam-asam ini mengandung ikatan rangkap C = C dalam rantai alkilnya. - C 17 H 35 CH Asam leat - C 17 H 33 CH Asam Linoleat - C 17 H 29 CH Asam Linolenat Asam-asam tersebut dapat mengalami adisi : C 17 H 33 CH + H 2 C 17 H 35 CH C 17 H 31 CH + 2H 2 C 17 H 35 CH 2. Asam alkanadioat Asam-asam ini mengandung dua gugus karboksilat. HC CH asam oksalat (etanadioat) HC CH 2 CH asam malonat (propanadioat) 3. Asam hidroksi Asam-asam ini mengandung gugus hidroksi ( - H ) CH 3 CH CH H 9. Ester ( R C R ) HC CH CH CH H H Asam laktat Asam tartrat Ester adalah hsil reaksi asam karboksilat dan alkohol. R C H + R H R C R + H 2 Reaksi pembentukan ester disebut esterifikasi. 7
8 Tatanama Nama ester diawali dengan nama alkil dari alkohol diikuti nama asam asalnya (alkil alkanoat). CH 3 C CH 2 H 3 CH 3 CH 2 C H 3 : Etil etanoat (IUPAC) = Etil asetat (Trivial) : Metil propanoat (IUPAC) = Metil propionat (Trivial) CH 3 CH 2 CH 2 C CH 2 CH 3 : Etil butanoat (IUPAC) = Etil butirat (Trivial) Sifat Ester 1. Banyak ester dari alkohol suku rendah dengan asam karboksilat suku rendahnya berbau jharum / buah sehingga digunakan sebagai essence dan parfum. CH 3 CC 8 H 17 CH 3 CC 5 H 11 C 4 H 9 CC 5 H 11 C 3 H 7 CC 5 H 11 C 3 H 7 CC 4 H 9 Asam Karboksilat ktil asetat Amil asetat Amil valerat Amil butirat Butil butirat Ester Jeruk Pisang Apel Jambu Nanas 2. Lebih mudah menguap dibandingkan alkohol dan asamnya, sedikit larut dalam air. 3. Ester bereaksi dengan air (hidrolisis). R C R + R H R C H + H 2 Hidrolisis ester kebalikan dari esterifikasi. 4. Penyabunan / saponifikasi : reaksi ester dengan basa R C R + NaH R C Na + R H 10. Lemak dan Minyak ( Trigliserida ) Lemak dan minyak adalah ester dari gliserol dengan asam karboksilat suku tinggi (asam lemak). Gliserida padat (lemak) terutama berasal dari sumber hewani adalah ester dari gliserol dengan asam karboksilat jenuh. gliserida cair (minyak berasal dari sumber nabati seperti minyak kelapa, minyak jagung, minyak wijen) adalah ester dari gliserol dengan asam karboksilat tidak jenuh (mempunyai ikatan rangkap). Gliserol + asam lemak trigliserida Beberapa contoh asam lemak Struktur Asam-asam lemak jenuh (lemak hewani) CH 3 (CH 2 ) 10 CH Rumus Molekul C 11 H 23 CH Nama Biasa Asam laurat Titik Cair ( o C ) 44,2 CH 3 (CH 2 ) 14 CH C 15 H 32 CH Asam palmitat 63,1 CH 3 (CH 2 ) 16 CH C 17 H 35 CH Asam stearat 69,6 Asam-asam lemak tak jenuh minyak CH 3 (CH 2 ) 7 CH=CH(CH 2 ) 7 CH C 17 H 33 CH Asam oleat 13,4 8
9 Sifat-sifat Lemak Reaksi hidrolisis a. Lemak/minyak + air 180o C gliserol + asam lemak 10 atm b. Lemak/minyak + air suhu kamar gliserol + asam lemak Enzim lipase Adisi hidrogen (hidrogenasi) Minyak yang mengandung asam-asam tak jenuh (mempunyai ikatan rangkap) dapat mengadisi H 2 dengan katalis serbuk NiKCl membentuk lemak padat. Proses ini dipakai untuk membuat mentega tiruan atau margarin. Triolein + 3H 2 Ni Tristearin Proses tengik Minyak dan lemak yang telah tersimpan lama akan sedikit terhidrolisa, asam akan terjadi terutama yang tidak jenuh teroksidasi oleh udara menghasilkan aldehid, keton dan asam-asam yang lebih sederhana seperti asam butirat yang berbau tengik. Reaksi penyabunan / saponifikasi Reaksi antara minyak. lemak dengan basa kuat menghasilkan gliserol dan natrium alkanoat yang juga disebut sabun karena itu reaksi ini disebut reaksi penyabunan. 11. Haloalkana ( R X ) Halogen alkana adalah turunan alkana yang sama atom H-nya diganti gugus halogen (Cl, Br, I) a. Tatanama - Gugus halogen disebut terlebih dahulu sebelum gugus (cabang) yang lain. - Sedangkan aturan yang lain sama dengan alkana. CH 3 CH 3 C CH 3 2 kloro 2-metil propana Cl b. Kegunaan 1. Kloroform (CHCl 3 ) : sebagai obat bius lokal tetapi sangat beracun 2. Tetra klor metana (CCl) : - sebagai pelarut - pembersih minyak dan lemak - bahan pemadam kebakaran 3. Monoklor etana (CH 3 CH 2 Cl) : obat bius lokal 4. Freon (Freon 11, CCl 3 F; Freon-12, CCl 2 F 2 ) - refrigeran (pendingin) pada kulkas dan AC - bahan pengabut pada deodoran dan hair spray E. Senyawa Benzena dan Turunannya 1). Benzena ( C 6 H 6 ) HC HC CH HC CH CH Di dalam benzena terdapat ikatan rangkap selang-seling ( terkonjugasi ). Sifat-sifat benzena a. semua atom C dan H mempunyai kedudukan sama b. benzena lebih mudah mengalami substitusi dibanding alkana. 9
10 2). Turunan Benzena Nama Sifat Rumus Struktur Kegunaan Toluena Dapat dioksidasi menjadi asam benzoat CH 2 Fenol Bersifat asam Dapat bereaksi dengan NaH membentuk Na-fenolat Dapat bereaksi dengan asam karboksilat membentuk ester Fenol lebih reaktif daripada benzena H - Sebagai desinfektan (karbol) - Sebagai pelarut Anilina Zat cair seperti minyak, tidak berwarna Sukar larut dalam air Bersifat basa lemah NH 2 Stirena CH = CH 2 - Sebagai bahan dasar pembuatan plastik Asam benzoat Dibuat dari oksidasi toluena CH - Sebagai pengawet F. Polimer Polimer : Senyawa makromolekul yang tersusun dari molekul-molekul kecil (monomer). Berdasarkan sumbernya polimer dibedakan atas : 1. Polimer alam Karet alam : berasal dari monomer isoprena ( 2-metil 1,3 butadiena) Selulosa, pati : berasal dari monomer glukosa Protein : berasal dari monomer asam amino 2. Polimer sintetik / buatan Ada dua jenis reaksi polimerisasi a. Polimerisasi kondensasi : pembentukan polimer disertai pelepasan molekul kecil seperti H 2 dan CH 3 H. - Nilon 66 : berasal dari monomer asam adipat dan heksametilendiamin - Tetoron : berasal dari monomer tereftalat dan etanadiol b. Polimerisasi adisi : adisi antara monomer-monomer berikatan rangkap membentuk polimer tanpa disertai pelepasan molekul kecil. - Polietelina (PE) : berasal dari monomer etilena - Polivinil Klorida (PVC) : berasal dari monomer vinil klorida - Poli stirena : berasal dari monomer stirena Berdasarkan monomer pembentuknya, polimer dibedakan menjadi : 1. Kopolimer : jika monomernya berbeda Nilon 66, monomernya adalah asam adipat dan heksametilendiamin 10
11 2. Homopolimer : jika monomernya sama Polivinil klorida, monomernya adalah vinil klorida. G. Karbohidrat a. Klasifikasi 1. Monosakarida Aldosa - Aldopentosa (ribosa) - Aldoheksosa (glukosa dan galaktosa) Ketosa - Ketopentosa - Ketoheksosa (fruktosa) 2. Disakarida ( C 12 H ) Sukrosa Maltosa Laktosa 3. Polisakarida Amilum Dekstrin Selulosa Glikogen b. Sifat karbohidrat 1). Sifat Glukosa - Dapat mereduksi reagen Fehling, Benedict, dan reagen Tollens - Larut dalam air, larutannya memutar bidang cahaya terpolarisasi ke kanan ( d ) - Rasanya manis 2). Sifat Sukrosa (gula tebu) - Dapat mereduksi reagen Fehling, Benedict, dan reagen Tollens - Rasanya manis - Dapat dihidrolisis bila dipanaskan dengan asam encer menjadi glukosa dan fruktosa Sukrosa 2 Glukosa + Fruktosa 3). Sifat Maltosa dan Laktosa - Dapat mereduksi reagen Fehling, Benedict, dan reagen Tollens - Larut dalam air - Rasanya manis Laktosa 2 Glukosa + Galaktosa Maltosa 2 Glukosa + Glukosa 4). Sifat Amilum - Tidak dapat mereduksi reagen Fehling - Larut dalam air panas - Dapat dihidrolisis Amilum 2 Glukosa - Bahan makanan cadangan bagi tumbuh-tumbuhan 5). Sifat Glikogen - Dapat mereduksi reagen Fehling - Larut dalam air panas - Dapat dihidrolisis Asam Glikogen Glukosa Glikogen Enzim Diastase Maltosa - Bahan makanan cadangan dalam hati (hepar) 11
12 6). Sifat Selulosa - Berwarna putih - Tidak larut dal;am hampir semua zat pelarut - Dapat dihidrolisis dengan asam terbentuk glukosa - Tidak terurai oleh enzim H. Asam Amino dan Protein 1. Asam Amino a. Rumus : NH 2 H NH 2 H ( glisin ) (α - alanin ) b. Sifat Asam Amino 1. Dapat bereaksi dengan asam, basa atau logam a. R CH(NH 2 )CH + HCl R CH CH + Cl - b. R CH(NH 2 )CH + NaH R CH(NH 2 )CNa + H 2 c. R CH(NH 2 )CH + Na R CH(NH 2 )CNa + ½ H 2 2. Bersifat amfoter dan dapat membentuk zwitter ion (bermuatan ganda (+) dan (-)) 3. Bersifat optis aktif (kecuali asam amino glisin) 4. Zat penyusn protein. 2. Protein Protein : senyawa makromolekul yang tersusun dari asam-asam amino yang etrikat melalui ikatan peptida. Ikatan Peptida : R CH C NH 2 H H CH C C NH a. Sifat-sifat protein 1. Mengalami penguraian jika : - dipanaskan hingga 100 o C - dicampur dengan asam cuka - dilarutkan dalam alkohol 2. Bereaksi dengan air (hidrolisis) membentuk asam amino, asam nukleat dan asam fosfat. 3. Membentuk sistem koloid hidrofil. CH 3 CH C NH
13 SAL-SAL LATIHAN 1. Dari senyawa berikut : CH 3 CH 2 CH 2 CH 2 NH 2 dan CH 3 CH NH 2 menunjukkan keisomeran. A. kerangka B. posisi C. fungsiona D. geometris E. optis 2. Senyawa yang mempunyai isomer optis adalah A. CH 3 CH B. CH 3 CHHCH C. C 6 H 5 CH D. C 2 H 5 H E. C 4 H 9 H 3. Sebuah zat yang optis aktif mempunyai rumus molekul C 5 H 12. Jika dioksidasikan akan menghasilkan aldehid. Zat itu adalah. A. etoksi propana B. 3-pentanol C. 2-metil 2-butanol D. isopentanol E. 2-metil 1-butanol 4. Manakah di antara pernyataan berikut yang bukan merupakan sifat benzena? A. merupakan senyawa tak jenuh B. ikatan karbon-karbon lebih pendek dari ikatan karbon-karbon tunggal C. ikatan karbon-karbon lebih panjang dari ikatan karbon-karbon rangkap D. terdapat elektron yang terdelokalisasi E. mudah mengalami reaksi adisi 5. Fenol dan etanol mempunyai persamaan dalam hal. A. keduanya bersifat asam B. keduanya bersifat netral C. keduanya bersifat basa D. mempunyai gugus H E. keduanya mudah dioksidasi 6. Manakah satu di antara yang berikut ini bukan polimer? A. plastik B. karet C. nilon D. protein E. lemak 7. Diberikan lima macam hasil polimer 1. poli vinil klorida 2. poli isoprena 3. polietilena 4. selulosa 5. poli vinil asetat 13 Yang termasuk polimer alam adalah. A. 1, 2, 3 B. 1, 3 C. 2, 4 D. 4 E. 3, 4, 5 8. Manakah satu di antara senyawa berikut yang paling mungkin sebagai monomer dalam suatu polimerisasi adisi? A. HCH 2 CH 2 CH B. CH 3 CH 2 CH 2 NH 2 C. CH 3 CH 2 CH D. CH 3 CH 2 CCl E. CH 3 CH=CH 2 9. Polimer yang dibentuk oleh kondensasi glukosa disebut polisakarida. Yang termasuk polisakarida adalah. (1) protein (2) kanji (3) DNA (4) selulosa 10. Perhatikan struktur polimer berikut : [ CH 2 C = CH CH 2 CH 2 C = CH CH 3 ] CH 3 CH 3 Monomernya adalah. A. 2-metil 2-butena B. 2,3 butadiena C. 2-metil 1,3-butadiena D. 2-metil 2-propena E. 3-metil 1,3-butadiena 11. Polivinil klorida adalah plastik hasil polimerisasi dari. A. ClHC = CHCl B. ClHC = Cl 2 C. HC = CCl D. H 2 C = CHCl E. H 2 C = CCl Hidrokarbon yang tidak mempunyaui isomer adalah. (1) C 2 H 4 (2) C 2 H 5 Cl (3) C 2 H 6 (4) C 2 H 2 Cl Isomer cis-trans dapat terjadi pada senyawa. A. CH 3 CH 2 CH = CH 2 B. C 2 H 5 CH = CHC 2 H 5 C. CH 2 = CH 2 D. (CH 3 ) 2C = C(CH 3 ) 2 E. CHCl = CCl 2
14 14. Propil alkohol dapat dibedakan dari isopropil alkohol, karena oksidasi isopropil alkohol menghasilkan. A. asetaldehid B. propanol C. aseton D. propandiol E. propena 15. Reaksi antara etanol dan asam sulfat pekat pada suhu 140 o C akan memberikan hasil utama A. C 2 H 5 C 2 H 5 B. C 2 H 5 HS 4 C. CH 2 CH 2 D. (C 2 H 5 ) 2 C E. CH 3 CH Senyawa berikut adalah isomer dari asam pentanoat, kecuali. A. dietil keton B. etil propanoat C. asam 2-metil butanoat D. propil asetat E. butil formiat 17. Pasangan senyawa berikut merupakan isomer fungsional. A. propanol dan propanal B. aseton dan asetaldehid C. propanal dan etil metil eter D. etanol dan metoksi metana E. 1-propanol dan 2-propanol 18. Trisubstitusi dari benzena dimana ketiga substituennya sama akan menghasilkan. A. 1 isomer B. 2 isomer C. 3 isomer D. 4 isomer E. 5 isomer 19. Pada oksidasi 3-metil 2-butanol dihasilkan. A. butanol B. 2-pentanon C. 3-metil 2-butanon D. metoksi butana E. pentanal 20. Zat berikut merupakan isomer optik adalah A. 2-metil 2-propanol B. asam amino asetat C. 3-metil 2-butanol D. gliserol E. isopropil alkohol 21. Reaksi berikut yang digunakan untuk mengenal adanya gugus CH pada alkanal yaitu direaksikan dengan. A. gas H 2 menghasilkan alkohol B. logam Na menghasilkan alkoksida C. PCl 3 menghasilkan R Cl D. reagen Tollens menghasilkan endapan Ag E. gas brom menjadi dibromo alkana 22. Larutan metanal 40% di dalam air dalam perdagangan dikenal dengan nama. A. formalin B. asam formiat C. spiritus D. cuka E. aspirin 23. Pernyataan yang tidak benar tentang senyawa etanol adalah bahwa senyawa ini. A. dapat dihasilkan dari reduksi etanal B. dapat dihasilkan dari peragian glukosa C. dapat didehidrasi menghasilkan etilena D. dapat dioksidasi menjadi asam asetat E. merupakan isomer struktur dari dietil eter 24. Ada berapa kemungkinan senyawa dengan rumus C 4 H 10 yang bereaksi dengan logam Na dan bila bereaksi dengan larutan K 2 Cr 2 7 akan menghasilkan asam karboksilat? A. 1 B. 2 C. 3 D. 4 E Ester merupakan salah satu turunan dari asam karboksilat yang. (1) pada umumnya berbau harum (2) dapat dipakai sebagai essence buatan (3) terdapat juga sebagai kulit jeruk (4) dapat dipakai sebagai pelarut 26. Suatu senyawa karbon jika dihidrogenasi membentuk alkohol tetapi tidak bereaksi dengan reagen Fehling. Senyawa tersebut adalah. A. eter B. aseton C. formaldehid D. metanol E. asetaldehid 27. Monomer penyusunan karet alam ialah. A. butadiena B. isoprena C. vinil klorida D. stirena E. isoprena dan stirena 28. Kelompok senyawa berikut yang terdiri atas monosakarida, disakarida dan polisakarida secara berurutan adalah. A. laktosa fruktosa selulosa B. galaktosa maltosa glikogen 14
15 C. glikogen maltosa selulosa D. amilum selulosa glikogen E. galaktosa maltosa glikogen 29. Hidrolisis sukrosa akan menghasilkan. A. glukosa + glukosa B. glukosa dan fruktosa C. glukosa + galaktosa D. fruktosa + galaktosa E. ribosa + fruktosa 30. Manakah satu di antara karbohidrat berikut tidak mereduksi pereaksi Fehling atau pereaksi Benedict? A. glukosa B. fruktosa C. maltosa D. sukrosa E. laktosa 31. Jumlah isomer optis glukosa adalah. A. 2 B. 4 C. 8 D. 12 E Karbohidrat yang terdapat dalam susu. A. maltosa B. sukrosa C. galaktosa D. laktosa E. glukosa 33. Protein adalah polimer dari asam alpha amino. Gugus fungsi yang terdapat dalam molekul asam alpha amino adalah. A. H dan NH 2 B. C dan NH 2 C. CH dan NH 2 D. NH 3 dan CH E. H dan CH 34. Struktur yang disebut ikatan peptida adalah. A. B. C. H 3 N C D. C NH E. C NH C NH 2 HN C 35. Ikatan peptida antara asam-asam amino yang terdapat dalam protein adalah. A. gugus alkohol dan gugus metil B. gugus metil dan gugus asam amino C. gugus amino dan gugus karboksilat D. gugus karboksilat dan gugus metil E. gugus amino dan gugus alkohol 36. Jika kedalam larutan zat X ditambahkan CuS 4 1 % dan NaH 0,1 M akan terbentuk warna ungu, maka zat X mengandung. A. ikatan peptida B. asam amino C. inti benzena D. ikatan S S E. glukosa 15
16 BIMLEKUL DAN METABLISME A. Biomolekul Biomolekul adalah senyawa-senyawa yang terdapat dalam sel hidup seperti karbohidrat, protein, lemak dan asam nukleat. 1). Reaksi Pengenalan Karbohidrat Nama Tes Pereaksi Hasil Fehling CuS 4, K-Na tartrat dalam Positip untuk aldosa, menghasilkan KH / NaH endapan merah bata Negatip untuk ketosa Benedict CuS 4, K-Na tartrat dalam Na 2 C 3 atau NaHC 3 Positip untuk aldosa, menghasilkan endapan merah Negatip untuk ketosa Molisch α-naftol dalam alkohol Positip untuk semua karbohidrat Hasil : warna ungu Iodo test Tollens sazon Seliwanoff Iodium Ag 2 / NH 4 H Hidrazin Resorsinol, HCl Positip untuk amilum Hasil : warna biru Positip untuk aldosa, menghasilkan endapan cermin perak Negatip untuk ketosa Positip untuk monosakarida, hasil warna kuning yang tidak larut dalam air Positip untuk ketoheksosa Hasil : warna merah 2). Reaksi Pengenalan Protein Nama Tes Pereaksi Hasil Xantoprotein HN 3 pekat Positip terhadap protein yang mengandung asam amino dengan gugus fenil (tirosin), hasil : warna kuning Millon Biuret Uji Belerang Hg 2 (N 3 ) 2 + HN 2 NaH, CuS 4 NaH + larutan Pb(II) asetat positip terhadap gugus fenol, hasil : endapan / warna merah positip untuk dua gugus peptida, hasil : warna ungu positip terhadap sistein, hasil : endapan hitam PbS 3). Enzim Adalah protein yang berfungsi sebagai katalis dalam proses biokimia. Nama enzim diberi akhiran ase dan didasarkan pada : a. Nama zat diubah oleh enzim - maltase untuk penguraian maltosa - lipase untuk penguraian lipida b. Nama reaksi yang dipengaruhi - oksidase yang mempengaruhi reaksi oksidasi 16
17 Faktor-faktor yang mempengaruhi kerja enzim adalah : a. ph c. koenzim b. temperatur d. inhibitor Koenzim : zat yang membantu kerja enzim Koenzim berupa mineral, vitamin, dan hormon. 4). Lipida Adalah senyawa yang merupakan ester dari asam lemak dengan gliserol. Lipida dibagi menjadi 2 bagian yaitu : a. Lipida sederhana : tidak dapat dihidrolisis terpena dan steroida b. Lipida kompleks : dapat dihidrolisis trigliserida, fosfolipida Trigliserida : Fosfolipida : terdiri dari gliserol dan 3 molekul asam lemak lipida yang mengandung asam fosfat Rumus umum : R C CH 2 CH 2 C R R C CH CH C R H CH 2 P H CH 2 C R Asam fosfatida H 5). Asam Nukleat Adalah satu golongan biopolimer yang terdapat dalams emua sel hidup. Ada dua golongan asam nukleat, yaitu - asam ribonukleat (RNA) : terdapat di luar inti sel dalam sitoplasma - asam deoksiribonukleat (DNA) : terdapat dalam inti sel Monomer dari asam nukleat adalah nukleotida. Setiap nukleotida terdiri dari satu pentosa, satu basa nitrogen dan asam fosfat. Perbedaan antara DNA dan RNA terletak pada pentosanya. DNA terdiri dari deoksiribosa dan RNA terdiri dari ribosa. Basa-basa nitrogen adalah turunan dari Purin dan Pirimidin. Basa-basa nitrogen turunan Purin : Adenin dan Guanin. Basa-basa nitrogen turunan Pirimidin : Sitosin, Urasil, dan Timin. Basa yang terdapat DNA RNA Adenin Guanin Sitosin Timin Urasil Struktur Nukleotida H H P CH 2 BASA P CH 2 BASA H C H H H C C C H H C H H H C C C H H H (Ribonukleotida) H H (Deoksiribonukleotida) 17
18 B. Metabolisme Adalah semua perubahan kimia dan energi yang terjadi dalam sel hidup. Ada dua macam metabolisme : a. Anabolisme : proses pembentukan molekul yang lebih kompleks dengan energi yang tinggi proses fotosintesis tumbuhan b. Katabolisme : proses penguraian untuk membebaskan energi kimia yang tersimpan dalam senyawasenyawa organik. hidrolisis karbohidrat menjadi monosakarida yang diuraikan lagi menjadi asam pirufat dan akhirnya menjadi gas C 2 dan H 2 disertai energi. SAL-SAL LATIHAN 1. Yang merupakan fungsi mineral adalah. (1) sumber energi (2) pembangun (3) pelindung (4) pengatur 2. Senyawa organik dalam tubuh makhluk hidup dapat digolongkan ke dalam (1) karbohidrat (2) protein (3) lipida (4) asam nukleat (5) vitamin Yang dapat menghasilkan energi dalam tubuh adalah. A. (1), (2), (3), (4), dan (5) B. (1), (2), (3), dan (4) C. (1), (2), dan (3) D. (1), (3), dan (5) E. (1), (2), (4) 3. Biomolekul yang berfungsi sebagai katalisator dalam tubuh tergolong. A. lipida B. protein C. karbohidrat D. asam nukleat E. protein dan lipida 4. Senyawa biomolekul yang berfungsi sebagai faktor genetika adalah. A. asam nukleat B. karbohidrat C. hormon D. lipida E. protein 5. Kertas dihidrolisis dengan katalis H 2 S 4. Hasil hidrolisis direaksikan dengan larutan Fehling menghasilkan endapan merah bata. Hasil hidrolisis kertas tersebut adalah. A. glukosa B. amilosa C. fruktosa D. sukrosa E. maltosa DNA merupakan suatu biopolimer. Monomernya adalah : A. RNA B. asam alfa-amino C. asam karboksilat D. nukleotida E. nukleosida 7. Basa nitrogen penyusun DNA dan tidak terdapat pada RNA adalah. A. sitosin B. adenin C. timin D. guanin E. urasil 8. Sumber energi utama dalam tubuh kita adalah A. karbohidrat B. protein C. lemak D. asam nukleat E. ATP 9. Energi yang dibebaskan oleh reaksi dalam tubuh digunakan untuk mengubah. A. ATP menjadi ADP B. ADP menjadi ATP C. glukosa menjadi glikogen D. glukosa menjadi lemak E. ADP menjadi AMP 10. Hidrolisis lemak menghasilkan. A. gliserol B. asam-asam amino C. gliserol dan asam karboksilat D. gliserol dan sabun E. gliserol dan asam amino 11. Hidrolisis lemak dalam sistem pencernaan manusia dikatalisis oleh. A. enzim ptialin B. enzim pepsin C. enzim lipase D. enzim tripsin E. insulin
19 12. Fungsi enzim diastase dalam organisme hidup adalah untuk menguraikan. A. amilum B. selulosa C. sukrosa D. maltosa E. lipida 13. Zat yang masuk pada sisi aktif enzim sehingga menghalangi masuknya substrat, disebut. A. kofaktor B. koenzim C. inhibitor D. inhibitor nonkompetitif E. inhibitor irreversibel 14. Dalam tubuh terdapat berbagai jenis lipida seperti lemak, fosfolipid dan steroid. Lipid yang berfungsi sebagai sumber energi adalah A. lemak B. fosfolipid C. steroid D. lemak dan fosfolipid E. fosfolipid dan steroid 15. Pernyataan yang benar tentang DNA adalah (1) merupakan suatu biopolimer dengan monomernya nukleosida (2) berfungsi menurunkan sifat-sifat genetika (3) terdapat di luar inti sel dalam sitoplasma (4) setiap monomernya terdiri atas satu pentosa, satu basa nitrogen dan asam fosfat 16. Pernyataan yang benar untuk protein adalah. (1) polimer dari asam-asam amino (2) terbentuk melalui ikatan peptida (3) terdiri dari unsur-unsur C, H, dan N (4) berfungsi sebagai pembangun sel tubuh 17. Haemoglobin termasuk jenis protein pengangkut, SEBAB Haemoglobin dalam darah dapat mengikat oksigen dan menyebarkannya ke seluruh tubuh. 18. Proses berikut yang menghasilkan energi diperlukan dalam tubuh makhluk hidup adalah A. proses : C 2 + H 2 C 6 H 12 6 B. proses ADP menjadi ATP C. proses ATP menjadi ADP D. proses AMP menjadi ADP E. proses glukosa menjadi amilum 19
OAL TES SEMESTER II. I. Pilihlah huruf a, b, c, d, atau e pada jawaban yang tepat!
 KIMIA XII SMA 249 S AL TES SEMESTER II I. Pilihlah huruf a, b, c, d, atau e pada jawaban yang tepat! 1. Suatu senyawa karbondioksida dengan tembaga pijar dan hasil oksidasinya diuji dengan pereaksi fehling
KIMIA XII SMA 249 S AL TES SEMESTER II I. Pilihlah huruf a, b, c, d, atau e pada jawaban yang tepat! 1. Suatu senyawa karbondioksida dengan tembaga pijar dan hasil oksidasinya diuji dengan pereaksi fehling
Soal-Soal. Bab 14. Latihan. Kimia Karbon II: Gugus Fungsi. Alkohol dan Eter. 1. Rumus struktur alkohol ditunjukkan oleh. (A) C 2
 Bab 14 Kimia Karbon II: Gugus Fungsi Soal-Soal Latihan Alkohol dan Eter 1. Rumus struktur alkohol ditunjukkan oleh. (A) C 2 (B) -CH (C) -CH(H)-C 2 (D) C 3 H 7 -C- (E) -CH 2. Suatu senyawa dengan rumus
Bab 14 Kimia Karbon II: Gugus Fungsi Soal-Soal Latihan Alkohol dan Eter 1. Rumus struktur alkohol ditunjukkan oleh. (A) C 2 (B) -CH (C) -CH(H)-C 2 (D) C 3 H 7 -C- (E) -CH 2. Suatu senyawa dengan rumus
Senyawa Alkohol dan Senyawa Eter. Sulistyani, M.Si
 Senyawa Alkohol dan Senyawa Eter Sulistyani, M.Si sulistyani@uny.ac.id Konsep Dasar Senyawa Organik Senyawa organik adalah senyawa yang sumber utamanya berasal dari tumbuhan, hewan, atau sisa-sisa organisme
Senyawa Alkohol dan Senyawa Eter Sulistyani, M.Si sulistyani@uny.ac.id Konsep Dasar Senyawa Organik Senyawa organik adalah senyawa yang sumber utamanya berasal dari tumbuhan, hewan, atau sisa-sisa organisme
KIMIA. Sesi HIDROKARBON (BAGIAN II) A. ALKANON (KETON) a. Tata Nama Alkanon
 KIMIA KELAS XII IPA - KURIKULUM GABUNGAN 16 Sesi NGAN HIDROKARBON (BAGIAN II) Gugus fungsional adalah sekelompok atom dalam suatu molekul yang memiliki karakteristik khusus. Gugus fungsional adalah bagian
KIMIA KELAS XII IPA - KURIKULUM GABUNGAN 16 Sesi NGAN HIDROKARBON (BAGIAN II) Gugus fungsional adalah sekelompok atom dalam suatu molekul yang memiliki karakteristik khusus. Gugus fungsional adalah bagian
Struktur Aldehid. Tatanama Aldehida. a. IUPAC Nama aldehida dinerikan dengan mengganti akhiran a pada nama alkana dengan al.
 Kamu tentunya pernah menyaksikan berita tentang penyalah gunaan formalin. Formalin merupakan salah satu contoh senyawa aldehid. Melalui topik ini, kamu tidak hanya akan mempelajari kegunaan aldehid yang
Kamu tentunya pernah menyaksikan berita tentang penyalah gunaan formalin. Formalin merupakan salah satu contoh senyawa aldehid. Melalui topik ini, kamu tidak hanya akan mempelajari kegunaan aldehid yang
A. zat pengoksidasi D. inhibitor B. zat pereduksi E. zat pembius C. katalis POLIMER, KARBOHIDRAT, PROTEIN DAN LEMAK
 POLIMER, KARBOHIDRAT, PROTEIN DAN LEMAK 1. Diantara beberapa monomer di bawah ini : Monomer manakah yang dapat membentuk polimer adisi. A. zat pengoksidasi D. inhibitor B. zat pereduksi E. zat pembius
POLIMER, KARBOHIDRAT, PROTEIN DAN LEMAK 1. Diantara beberapa monomer di bawah ini : Monomer manakah yang dapat membentuk polimer adisi. A. zat pengoksidasi D. inhibitor B. zat pereduksi E. zat pembius
Antiremed Kelas 12 Kimia
 Antiremed Kelas 12 Kimia BAb 8 - Senyawa Karbon - Reaksi Identifikasi - Soal Doc. Name: AR12KIM0899 Version : 2013-10 halaman 1 01. Senyawa X mempunyai sifat-sifat sebagai berikut. (1) Titik didih relative
Antiremed Kelas 12 Kimia BAb 8 - Senyawa Karbon - Reaksi Identifikasi - Soal Doc. Name: AR12KIM0899 Version : 2013-10 halaman 1 01. Senyawa X mempunyai sifat-sifat sebagai berikut. (1) Titik didih relative
GUGUS FUNGSI, ISOMER DAN REAKSI
 GUGUS FUNGSI, ISOMER DAN REAKSI 1. C2H5Cl + C3H7ONa C2H5 - O - C3H7 + NaCl. Reaksi di atas merupakan reaksi. A. penyabunan adisi eliminasi netralisasi subtitusi 2. Dua senyawa yang saling berisomer mempunyai
GUGUS FUNGSI, ISOMER DAN REAKSI 1. C2H5Cl + C3H7ONa C2H5 - O - C3H7 + NaCl. Reaksi di atas merupakan reaksi. A. penyabunan adisi eliminasi netralisasi subtitusi 2. Dua senyawa yang saling berisomer mempunyai
1. Senyawa di bawah ini yang memiliki ikatan hidrogen antarmolekulnya adalah. A. CH 3 -CHO D. CH 3 E. CH 3
 KIMIA KELAS XII IPA - KURIKULUM GABUNGAN 20 Sesi NGAN Review III (HIDROKARBON, REAKSI-REAKSI SENYAWA KARBON DAN ISOMER, BENZENA, POLIMER) A. HIDROKARBON 1. Senyawa di bawah ini yang memiliki ikatan hidrogen
KIMIA KELAS XII IPA - KURIKULUM GABUNGAN 20 Sesi NGAN Review III (HIDROKARBON, REAKSI-REAKSI SENYAWA KARBON DAN ISOMER, BENZENA, POLIMER) A. HIDROKARBON 1. Senyawa di bawah ini yang memiliki ikatan hidrogen
Gugus Fungsi Senyawa Karbon
 Gugus Fungsi Senyawa Karbon Gugus fungsi merupakan bagian aktif dari senyawa karbon yang menentukan sifat-sifat senyawa karbon. Gugus fungsi tersebut berupa ikatan karbon rangkap dua, ikatan karbon rangkap
Gugus Fungsi Senyawa Karbon Gugus fungsi merupakan bagian aktif dari senyawa karbon yang menentukan sifat-sifat senyawa karbon. Gugus fungsi tersebut berupa ikatan karbon rangkap dua, ikatan karbon rangkap
Antiremed Kelas 12 Kimia
 Antiremed Kelas 12 Kimia Persiapan UAS 2 Doc. Name: AR12KIM02UAS Version : 2016-09 halaman 1 01. Nama yang tepat untuk senyawa : CH 3 - CH 2 - CH - CH 2 - OH CH 3 - CH - C 2 H 5 (A) 2 - butil - 1 - butanol,3
Antiremed Kelas 12 Kimia Persiapan UAS 2 Doc. Name: AR12KIM02UAS Version : 2016-09 halaman 1 01. Nama yang tepat untuk senyawa : CH 3 - CH 2 - CH - CH 2 - OH CH 3 - CH - C 2 H 5 (A) 2 - butil - 1 - butanol,3
tanya-tanya.com Soal No.1 Tuliskan nama senyawa alkohol dan eter berikut PEMBAHASAN : Soal No.2
 Soal No.1 Tuliskan nama senyawa alkohol dan eter berikut Soal No.2 Tuliskan nama senyawa berikut dengan benar. a. (CH3)2C(OH)(CH2)2CH3 b. (CH3)3COCH3 c. CH3(CH2)2CH(C2H5)CH2OH LIHAT JUGA : Rangkuman Materi
Soal No.1 Tuliskan nama senyawa alkohol dan eter berikut Soal No.2 Tuliskan nama senyawa berikut dengan benar. a. (CH3)2C(OH)(CH2)2CH3 b. (CH3)3COCH3 c. CH3(CH2)2CH(C2H5)CH2OH LIHAT JUGA : Rangkuman Materi
Jawaban: b Alasan: Jumlah atom C dan H sama. Siklo alkana berisomer dengan alkena, alkana tidak berisomer dengan alkena.
 1. Senyawa 2-metil 1-pentanol berisomer dengan... a. metil propil eter b. dipropil eter c. isopentanol d. etil propil eter e. 3-pentanol Jawaban: b Alasan: Jumlah atom C pada soal adalah 6. Pada jawaban,
1. Senyawa 2-metil 1-pentanol berisomer dengan... a. metil propil eter b. dipropil eter c. isopentanol d. etil propil eter e. 3-pentanol Jawaban: b Alasan: Jumlah atom C pada soal adalah 6. Pada jawaban,
SENYAWA TURUNAN ALKANA `
 SENYAWA TURUNAN ALKANA ` 1. Gugus Fungsi 2. Tata Nama 3. Keisomeran 4. Reaksi-reaksi Senyawa Karbon 5. Kegunaan dan Dampak Beberapa Senyawa Turunan Alkana GUGUS FUNGSI Definisi: Atom / kelompok atom yang
SENYAWA TURUNAN ALKANA ` 1. Gugus Fungsi 2. Tata Nama 3. Keisomeran 4. Reaksi-reaksi Senyawa Karbon 5. Kegunaan dan Dampak Beberapa Senyawa Turunan Alkana GUGUS FUNGSI Definisi: Atom / kelompok atom yang
MODUL SENYAWA KARBON ( Alkohol dan Eter )
 MODUL SENYAWA KARBON ( Alkohol dan Eter ) A. TATANAMA IUPAC ( Internasional Union of Pure and Applied Chemistry )/sistematika Trivial/Lazim/Dagang CONTOH A.1. ALKOHOL IUPAC 1. Tentukan rantai atom C terpanjang
MODUL SENYAWA KARBON ( Alkohol dan Eter ) A. TATANAMA IUPAC ( Internasional Union of Pure and Applied Chemistry )/sistematika Trivial/Lazim/Dagang CONTOH A.1. ALKOHOL IUPAC 1. Tentukan rantai atom C terpanjang
MODUL KIMIA SMA IPA Kelas 11
 SMA IPA Kelas 11 Senyawa-senyawa karbon dapat diturunkan dari senyawa alkana dengan cara mereaksikan alkana dengan zatzat lain. Senyawa ini dapat di jumpai di sekeliling kita seperti alkohol, formalin,
SMA IPA Kelas 11 Senyawa-senyawa karbon dapat diturunkan dari senyawa alkana dengan cara mereaksikan alkana dengan zatzat lain. Senyawa ini dapat di jumpai di sekeliling kita seperti alkohol, formalin,
Strukt Gugus Strukt. Singkat Nama Gugus Nama Klmp. Seny. Rumus Umum
 9.2. SENYAWA TURUNAN ALKANA 1 A. PENGGLNGAN SENYAWA RGANIK 1. Gugus Fungsi Pada molekul organik ada bagian molekul yang tak-reaktif dan ada bagian yang reaktif terhadap zat/pereaksi tertentu. Dalam Kimia
9.2. SENYAWA TURUNAN ALKANA 1 A. PENGGLNGAN SENYAWA RGANIK 1. Gugus Fungsi Pada molekul organik ada bagian molekul yang tak-reaktif dan ada bagian yang reaktif terhadap zat/pereaksi tertentu. Dalam Kimia
GUGUS FUNGSI, ISOMER DAN REAKSI
 GUGUS FUNGSI, ISOMER DAN REAKSI 1. C2H5Cl + C3H7ONa C2H5 - O - C3H7 + NaCl. Reaksi di atas merupakan reaksi. A. penyabunan D. adisi B. eliminasi E. netralisasi C. subtitusi SMU/Ebtanas/Kimia/Tahun 1988
GUGUS FUNGSI, ISOMER DAN REAKSI 1. C2H5Cl + C3H7ONa C2H5 - O - C3H7 + NaCl. Reaksi di atas merupakan reaksi. A. penyabunan D. adisi B. eliminasi E. netralisasi C. subtitusi SMU/Ebtanas/Kimia/Tahun 1988
Alkena dan Alkuna. Pertemuan 4
 Alkena dan Alkuna Pertemuan 4 Alkena/Olefin hidrokarbon alifatik tak jenuh yang memiliki satu ikatan rangkap (C = C) Senyawa yang mempunyai dua ikatan rangkap: alkadiena tiga ikatan rangkap: alkatriena,
Alkena dan Alkuna Pertemuan 4 Alkena/Olefin hidrokarbon alifatik tak jenuh yang memiliki satu ikatan rangkap (C = C) Senyawa yang mempunyai dua ikatan rangkap: alkadiena tiga ikatan rangkap: alkatriena,
berupa ikatan tunggal, rangkap dua atau rangkap tiga. o Atom karbon mempunyai kemampuan membentuk rantai (ikatan yang panjang).
 HIDROKARBON Senyawa hidrokarbon merupakan senyawa karbon yang paling sederhana. Dari namanya, senyawa hidrokarbon adalah senyawa karbon yang hanya tersusun dari atom hidrogen dan atom karbon. Dalam kehidupan
HIDROKARBON Senyawa hidrokarbon merupakan senyawa karbon yang paling sederhana. Dari namanya, senyawa hidrokarbon adalah senyawa karbon yang hanya tersusun dari atom hidrogen dan atom karbon. Dalam kehidupan
LAPORAN PRAKTIKUM KIMIA ORGANIK KI-2051 PERCOBAAN 7 & 8 ALDEHID DAN KETON : SIFAT DAN REAKSI KIMIA PROTEIN DAN KARBOHIDRAT : SIFAT DAN REAKSI KIMIA
 LAPORAN PRAKTIKUM KIMIA ORGANIK KI-2051 PERCOBAAN 7 & 8 ALDEHID DAN KETON : SIFAT DAN REAKSI KIMIA PROTEIN DAN KARBOHIDRAT : SIFAT DAN REAKSI KIMIA Disusun oleh Nama : Gheady Wheland Faiz Muhammad NIM
LAPORAN PRAKTIKUM KIMIA ORGANIK KI-2051 PERCOBAAN 7 & 8 ALDEHID DAN KETON : SIFAT DAN REAKSI KIMIA PROTEIN DAN KARBOHIDRAT : SIFAT DAN REAKSI KIMIA Disusun oleh Nama : Gheady Wheland Faiz Muhammad NIM
SENYAWA KARBON. Indriana Lestari
 SENYAWA KARBON Indriana Lestari A. Keunikan Atom Karbon ( C ) Atom Karbon ( C ) memiliki 4 elektron valensi. Dengan nomor atom 6, atom C memiliki 4 elektron valensi, sehingga untuk mencapai kestabilan
SENYAWA KARBON Indriana Lestari A. Keunikan Atom Karbon ( C ) Atom Karbon ( C ) memiliki 4 elektron valensi. Dengan nomor atom 6, atom C memiliki 4 elektron valensi, sehingga untuk mencapai kestabilan
FAKULTAS TEKNIK UNIVERSITAS NEGERI YOGYAKARTA BAHAN AJAR KIMIA DASAR BAB VII KIMIA ORGANIK
 BAAN AJAR KIMIA DASAR No. BAK/TBB/SBG201 Revisi : 00 Tgl. 01 Mei 2008 al 1 dari 19 BAB VII KIMIA ORGANIK Dari 109 unsur yang ada di alam ini, karbon mempunyai sifat-sifat istimewa : 1. Karbon dapat membentuk
BAAN AJAR KIMIA DASAR No. BAK/TBB/SBG201 Revisi : 00 Tgl. 01 Mei 2008 al 1 dari 19 BAB VII KIMIA ORGANIK Dari 109 unsur yang ada di alam ini, karbon mempunyai sifat-sifat istimewa : 1. Karbon dapat membentuk
Aldehid dan Keton. Sulistyani, M.Si
 Aldehid dan Keton Sulistyani, M.Si sulistyani@uny.ac.id Konsep Dasar Golongan aldehid disebut juga alkanal dan golongan keton disebut juga alkanon. Keduanya berisomer fungsional, karena mempunyai rumus
Aldehid dan Keton Sulistyani, M.Si sulistyani@uny.ac.id Konsep Dasar Golongan aldehid disebut juga alkanal dan golongan keton disebut juga alkanon. Keduanya berisomer fungsional, karena mempunyai rumus
Materi Penunjang Media Pembelajaran Kimia Organik SMA ALKENA
 ALKENA Nama lain alkena adalah olefin atau senyawa vinil. Alkena termasuk senyawa organik tak jenuh. Alkena merupakan senyawa yang relatif stabil, akan tetapi lebih reaktif dari alkana karena terdapatnya
ALKENA Nama lain alkena adalah olefin atau senyawa vinil. Alkena termasuk senyawa organik tak jenuh. Alkena merupakan senyawa yang relatif stabil, akan tetapi lebih reaktif dari alkana karena terdapatnya
UJI IDENTIFIKASI ETANOL DAN METANOL
 UJI IDENTIFIKASI ETANOL DAN METANOL Alkohol merupakan senyawa turunan alkana yang mengandung gugus OH dan memiliki rumus umum R-OH, dimana R merupakan gugus alkil. Adapun rumus molekul dari alkohol yaitu
UJI IDENTIFIKASI ETANOL DAN METANOL Alkohol merupakan senyawa turunan alkana yang mengandung gugus OH dan memiliki rumus umum R-OH, dimana R merupakan gugus alkil. Adapun rumus molekul dari alkohol yaitu
KIMIA. Sesi BIOMOLEKUL L KARBOHIDRAT A. PENGGOLONGAN
 KIMIA KELAS XII IPA - KURIKULUM GABUNGAN 21 Sesi NGAN BIOMOLEKUL L KARBOHIDRAT Karbohidrat adalah kelompok senyawa aldehid dan keton terpolihidroksilasi yang tersusun dari atom C, H, dan O. Karbohidrat
KIMIA KELAS XII IPA - KURIKULUM GABUNGAN 21 Sesi NGAN BIOMOLEKUL L KARBOHIDRAT Karbohidrat adalah kelompok senyawa aldehid dan keton terpolihidroksilasi yang tersusun dari atom C, H, dan O. Karbohidrat
Atom unsur karbon dengan nomor atom Z = 6 terletak pada golongan IVA dan periode-2 konfigurasi elektronnya 1s 2 2s 2 2p 2.
 SENYAWA ORGANIK A. Sifat khas atom karbon Atom unsur karbon dengan nomor atom Z = 6 terletak pada golongan IVA dan periode-2 konfigurasi elektronnya 1s 2 2s 2 2p 2. Atom karbon mempunyai 4 elektron valensi,
SENYAWA ORGANIK A. Sifat khas atom karbon Atom unsur karbon dengan nomor atom Z = 6 terletak pada golongan IVA dan periode-2 konfigurasi elektronnya 1s 2 2s 2 2p 2. Atom karbon mempunyai 4 elektron valensi,
Kurikulum 2013 Kelas 12 Kimia
 Kurikulum 2013 Kelas 12 Kimia Persiapan UAS Semester Genap 2015 / 2016 Doc. Name: K13AR12KIM02UAS Version : 2016-04 halaman 1 01. Nama yang tepat untuk senyawa : CH 3 - CH 2 - CH - CH 2 - OH CH 3 - CH
Kurikulum 2013 Kelas 12 Kimia Persiapan UAS Semester Genap 2015 / 2016 Doc. Name: K13AR12KIM02UAS Version : 2016-04 halaman 1 01. Nama yang tepat untuk senyawa : CH 3 - CH 2 - CH - CH 2 - OH CH 3 - CH
Kurikulum 2013 Kelas 12 Kimia
 Kurikulum 2013 Kelas 12 Kimia Persiapan UAS Semester Genap 2015 / 2016 Doc. Name: K13AR12KIM02UAS Version : 2016-04 halaman 1 01. Nama yang tepat untuk senyawa : CH 3 - CH 2 - CH - CH 2 - OH CH 3 - CH
Kurikulum 2013 Kelas 12 Kimia Persiapan UAS Semester Genap 2015 / 2016 Doc. Name: K13AR12KIM02UAS Version : 2016-04 halaman 1 01. Nama yang tepat untuk senyawa : CH 3 - CH 2 - CH - CH 2 - OH CH 3 - CH
ASAM KARBOKSILAT. Deskripsi: Struktur, tata nama, penggolongan dan manfaat asam karboksilat
 ASAM KARBKSILAT Deskripsi: Struktur, tata nama, penggolongan dan manfaat asam karboksilat DEFINISI ASAM KARBKSILAT Senyawa yang mempunyai satu gugus karbonil yang berikatan dengan satu gugus hidroksil
ASAM KARBKSILAT Deskripsi: Struktur, tata nama, penggolongan dan manfaat asam karboksilat DEFINISI ASAM KARBKSILAT Senyawa yang mempunyai satu gugus karbonil yang berikatan dengan satu gugus hidroksil
SIFAT KIMIA DAN FISIK SENYAWA HIDROKARBON
 SIFAT KIMIA DAN FISIK SENYAWA HIDROKARBON Muhammad Ja far Sodiq (0810920047) 1. ALKANA Pada suhu biasa, metana, etana, propana, dan butana berwujud gas. Pentena sampai heptadekana (C 17 H 36 ) berwujud
SIFAT KIMIA DAN FISIK SENYAWA HIDROKARBON Muhammad Ja far Sodiq (0810920047) 1. ALKANA Pada suhu biasa, metana, etana, propana, dan butana berwujud gas. Pentena sampai heptadekana (C 17 H 36 ) berwujud
SENYAWA KARBON TURUNAN ALKANA
 5 SENYAWA KARBN TURUNAN ALKANA A. ALALKANA B. ALKANL C. ALKKSIALKANA D. ALKANAL E. ALKANN F. ASAM ALKANAT G. ALKIL ALKANAT Di alam terdapat jutaan senyawa karbon. Senyawa karbon turunan alkana adalah senyawa
5 SENYAWA KARBN TURUNAN ALKANA A. ALALKANA B. ALKANL C. ALKKSIALKANA D. ALKANAL E. ALKANN F. ASAM ALKANAT G. ALKIL ALKANAT Di alam terdapat jutaan senyawa karbon. Senyawa karbon turunan alkana adalah senyawa
SENYAWA TURUNAN ALKANA. Alkohol - Eter, Aldehid - Keton, Asam Karboksilat - Ester
 SENYAWA TURUNAN ALKANA Alkohol - Eter, Aldehid - Keton, Asam Karboksilat - Ester Tata Nama Senyawa Turunan Alkana Nomor cabang-cabang-nama cabang urut abjad-nomor gugus fungsi-nama induk 1. Mengidentifikasi
SENYAWA TURUNAN ALKANA Alkohol - Eter, Aldehid - Keton, Asam Karboksilat - Ester Tata Nama Senyawa Turunan Alkana Nomor cabang-cabang-nama cabang urut abjad-nomor gugus fungsi-nama induk 1. Mengidentifikasi
STANDART KOMPETENSI INDIKATOR MATERI EVALUASI DAFTAR PUSTAKA
 STANDART KOMPETENSI INDIKATOR MATERI EVALUASI DAFTAR PUSTAKA STANDART KOMPETENSI Mendeskripsikan struktur, cara penulisan, tata nama, sifat, kegunaan, dan identifikasi senyawa karbon. (halo alkan, alkanol,
STANDART KOMPETENSI INDIKATOR MATERI EVALUASI DAFTAR PUSTAKA STANDART KOMPETENSI Mendeskripsikan struktur, cara penulisan, tata nama, sifat, kegunaan, dan identifikasi senyawa karbon. (halo alkan, alkanol,
BAB 7 HIDROKARBON DAN MINYAK BUMI
 BAB 7 HIDROKARBON DAN MINYAK BUMI A. Kekhasan / Keunikan Atom Karbon o Terletak pada golongan IVA dengan Z = 6 dan mempunyai 4 elektron valensi. o Untuk mencapai konfigurasi oktet maka atom karbon mempunyai
BAB 7 HIDROKARBON DAN MINYAK BUMI A. Kekhasan / Keunikan Atom Karbon o Terletak pada golongan IVA dengan Z = 6 dan mempunyai 4 elektron valensi. o Untuk mencapai konfigurasi oktet maka atom karbon mempunyai
Gugus Fungsi. Gugus Fungsi. Gugus Fungsi. Gugus Fungsi CH 3 -CH 3 O O H 2 C CH 2 C O C C S C O CH 3 C OCH 2 CH 3 H C NH 2 CH 3 C NH 2. Alkana.
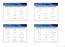 Gugus Fungsi Struktur Golongan Senyawa ontoh spesifik Gugus Fungsi Struktur Golongan Senyawa ontoh spesifik Alkana - Alkohol Alkena Fenol Alkuna Arena (aromatik) S Tiol (Merkaptan) S Eter X Alkil halida
Gugus Fungsi Struktur Golongan Senyawa ontoh spesifik Gugus Fungsi Struktur Golongan Senyawa ontoh spesifik Alkana - Alkohol Alkena Fenol Alkuna Arena (aromatik) S Tiol (Merkaptan) S Eter X Alkil halida
kimia HIDROKARBON III DAN REVIEW Tujuan Pembelajaran
 K-13 kimia K e l a s XI HIDROKARBON III DAN REVIEW Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut 1 Memahami definisi dan jenis-jenis isomer beserta contohnya
K-13 kimia K e l a s XI HIDROKARBON III DAN REVIEW Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut 1 Memahami definisi dan jenis-jenis isomer beserta contohnya
Senyawa Hidrokarbon. Linda Windia Sundarti
 Senyawa Hidrokarbon Senyawa Hidrokarbon adalah senyawa yang mengandung hanya karbon dan hidrogen C + H Carbon sebagai unsur pokok memiliki keistimewaan sbb : 1. Dengan ev = 4 membentuk 4 ikatan kovalen
Senyawa Hidrokarbon Senyawa Hidrokarbon adalah senyawa yang mengandung hanya karbon dan hidrogen C + H Carbon sebagai unsur pokok memiliki keistimewaan sbb : 1. Dengan ev = 4 membentuk 4 ikatan kovalen
Asam Karboksilat dan Ester. Sulistyani, M.Si
 Asam Karboksilat dan Ester Sulistyani, M.Si sulistyani@uny.ac.id Konsep Dasar Asam karboksilat disebut juga golongan asam alkanoat, sedangkan ester disebut juga golongan alkil alkanoat. Asam karboksilat
Asam Karboksilat dan Ester Sulistyani, M.Si sulistyani@uny.ac.id Konsep Dasar Asam karboksilat disebut juga golongan asam alkanoat, sedangkan ester disebut juga golongan alkil alkanoat. Asam karboksilat
Wardaya College. Tes Simulasi Ujian Nasional SMA Berbasis Komputer. Mata Pelajaran Kimia Tahun Ajaran 2017/2018. Departemen Kimia - Wardaya College
 Tes Simulasi Ujian Nasional SMA Berbasis Komputer Mata Pelajaran Kimia Tahun Ajaran 2017/2018-1. Sebuah unsur X memiliki no massa 52 dan jumlah neutron sebesar 28. Kongurasi elektron dari ion X + adalah...
Tes Simulasi Ujian Nasional SMA Berbasis Komputer Mata Pelajaran Kimia Tahun Ajaran 2017/2018-1. Sebuah unsur X memiliki no massa 52 dan jumlah neutron sebesar 28. Kongurasi elektron dari ion X + adalah...
JURNAL PRAKTIKUM KIMIA ORGANIK : Identifikasi Gugus Fungsional Senyawa Organik
 Paraf Asisten Judul JURNAL PRAKTIKUM KIMIA ORGANIK : Identifikasi Gugus Fungsional Senyawa Organik Tujuan Percobaan : 1. Mempelajari teknik pengukuran fisik untuk mengidentifikasi suatu senyawa organik
Paraf Asisten Judul JURNAL PRAKTIKUM KIMIA ORGANIK : Identifikasi Gugus Fungsional Senyawa Organik Tujuan Percobaan : 1. Mempelajari teknik pengukuran fisik untuk mengidentifikasi suatu senyawa organik
ALDEHID DAN KETON. Putri Anjarsari, S.Si., M.Pd
 ALDEHID DAN KETN Putri Anjarsari, S.Si., M.Pd putri_anjarsari@uny.ac.id ontoh senyawa-senyawa karbonil penting H 3 H Asam asetat (asam cuka) H N H H 3 Asetaminofen (analgesik, antipiretik) H H 3 Asam asetil
ALDEHID DAN KETN Putri Anjarsari, S.Si., M.Pd putri_anjarsari@uny.ac.id ontoh senyawa-senyawa karbonil penting H 3 H Asam asetat (asam cuka) H N H H 3 Asetaminofen (analgesik, antipiretik) H H 3 Asam asetil
Evaluasi Belajar Tahap Akhir K I M I A Tahun 2005
 Evaluasi Belajar Tahap Akhir K I M I A Tahun 2005 UN-SMK-05-01 Perhatikan perubahan materi yang terjadi di bawah ini: (1) sampah membusuk (2) fotosintesis (3) fermentasi (4) bensin menguap (5) air membeku
Evaluasi Belajar Tahap Akhir K I M I A Tahun 2005 UN-SMK-05-01 Perhatikan perubahan materi yang terjadi di bawah ini: (1) sampah membusuk (2) fotosintesis (3) fermentasi (4) bensin menguap (5) air membeku
KIMIA. Sesi. Review IV A. KARBOHIDRAT
 KIMIA KELAS XII IPA - KURIKULUM GABUNGAN 24 Sesi NGAN Review IV A. KARBOHIDRAT 1. Di bawah ini adalah monosakarida golongan aldosa, kecuali... A. Ribosa D. Eritrosa B. Galaktosa E. Glukosa C. Fruktosa
KIMIA KELAS XII IPA - KURIKULUM GABUNGAN 24 Sesi NGAN Review IV A. KARBOHIDRAT 1. Di bawah ini adalah monosakarida golongan aldosa, kecuali... A. Ribosa D. Eritrosa B. Galaktosa E. Glukosa C. Fruktosa
KONSEP DASAR KIMIA ORGANIK YANG MENUNJANG PEMBELAJARAN KIMIA SMA GEBI DWIYANTI
 KNSEP DASAR KIMIA RGANIK YANG MENUNJANG PEMBELAJARAN KIMIA SMA GEBI DWIYANTI 1. Kekhasan Atom Karbon Atom karbon adalah atom yang memiliki enam elektron dengan dengan konfigurasi 1s 2 2s 2 2p 2. Empat
KNSEP DASAR KIMIA RGANIK YANG MENUNJANG PEMBELAJARAN KIMIA SMA GEBI DWIYANTI 1. Kekhasan Atom Karbon Atom karbon adalah atom yang memiliki enam elektron dengan dengan konfigurasi 1s 2 2s 2 2p 2. Empat
MAKALAH PEMBELAJARAN E-LEARNING MATA PELAJARAN KIMIA KELAS XI SEMESTER 2 SENYAWA KARBON
 MAKALAH PEMBELAJARAN E-LEARNING MATA PELAJARAN KIMIA KELAS XI SEMESTER 2 SENYAWA KARBN DISUSUN GUNA MEMENUHI SALAH SATU TUGAS PRTFLI PELATIHAN JARDIKNAS TAHUN 2007 Disusun oleh : SUWARJI, S.Pd NIP 131907874
MAKALAH PEMBELAJARAN E-LEARNING MATA PELAJARAN KIMIA KELAS XI SEMESTER 2 SENYAWA KARBN DISUSUN GUNA MEMENUHI SALAH SATU TUGAS PRTFLI PELATIHAN JARDIKNAS TAHUN 2007 Disusun oleh : SUWARJI, S.Pd NIP 131907874
1.Pengertian alkohol 2.Klasifikasi alkohol 3.Sifat-sifat fisika dan kimia alkohol 4.Sintesis alkohol 5.Reaksi-reaksi alkohol 6.
 1.Pengertian alkohol 2.Klasifikasi alkohol 3.Sifat-sifat fisika dan kimia alkohol 4.Sintesis alkohol 5.Reaksi-reaksi alkohol 6.Tata nama alkohol 7.Contoh-contoh alkohol dan kegunaannya senyawa organik
1.Pengertian alkohol 2.Klasifikasi alkohol 3.Sifat-sifat fisika dan kimia alkohol 4.Sintesis alkohol 5.Reaksi-reaksi alkohol 6.Tata nama alkohol 7.Contoh-contoh alkohol dan kegunaannya senyawa organik
- 1 - KIMIA MAKROMOLEKUL
 - 1 - KIMIA MAKRMLEKUL KARBIDRAT» Merupakan senyawa yang mengandung gugus fungsi keton atau aldehid, dan gugus hidroksi» Ditinjau dari gugus fungsi yang diikat:» Aldosa: karbohidrat yang mengikat gugus
- 1 - KIMIA MAKRMLEKUL KARBIDRAT» Merupakan senyawa yang mengandung gugus fungsi keton atau aldehid, dan gugus hidroksi» Ditinjau dari gugus fungsi yang diikat:» Aldosa: karbohidrat yang mengikat gugus
LKS HIDROKARBON. Nama : Kelas/No.Abs :
 Nama : Kelas/No.Abs : LKS HIDROKARBON 1. Kekhasan / Keunikan Atom Karbon 1. Terletak pada golongan IVA dengan Z = 6 dan mempunyai 4 elektron valensi. 2. Untuk mencapai konfigurasi oktet maka atom karbon
Nama : Kelas/No.Abs : LKS HIDROKARBON 1. Kekhasan / Keunikan Atom Karbon 1. Terletak pada golongan IVA dengan Z = 6 dan mempunyai 4 elektron valensi. 2. Untuk mencapai konfigurasi oktet maka atom karbon
KIMIA HIDROKARBON GUGUS FUNGSI
 KMA HDRKARBN GUGUS FUNGS Gugus fungsi adalah bagian suatu molekul (substituen pada rangka hidrokarbon) yang berfungsi secara kimia Dapat bereaksi, tidak lembam Substituen (gugus fungsi) diantaranya mengandung
KMA HDRKARBN GUGUS FUNGS Gugus fungsi adalah bagian suatu molekul (substituen pada rangka hidrokarbon) yang berfungsi secara kimia Dapat bereaksi, tidak lembam Substituen (gugus fungsi) diantaranya mengandung
THE MEANING. The measurement of the speed of reaction. The change in amount of reactant or product against time.
 RATE OF REACTION THE MEANING The measurement of the speed of reaction. The change in amount of reactant or product against time. FAST REACTION SLOW REACTION Sodium metal reacts quickly with water to release
RATE OF REACTION THE MEANING The measurement of the speed of reaction. The change in amount of reactant or product against time. FAST REACTION SLOW REACTION Sodium metal reacts quickly with water to release
KARBOHIDRAT. Sulistyani, M.Si
 KARBOHIDRAT Sulistyani, M.Si sulistyani@uny.ac.id KONSEP TEORI Karbohidrat merupakan senyawa yang terdiri dari unsur karbon, hidrogen, dan oksigen yang terdapat di alam. Karbohidarat berasal dari kata
KARBOHIDRAT Sulistyani, M.Si sulistyani@uny.ac.id KONSEP TEORI Karbohidrat merupakan senyawa yang terdiri dari unsur karbon, hidrogen, dan oksigen yang terdapat di alam. Karbohidarat berasal dari kata
TRY OUT UJIAN NASIONAL TAHUN AJARAN 2008 / 2009
 TRY UT UJIAN NASINAL TAHUN AJARAN 2008 / 2009 LEMBAR SAL B Bidang Studi : KIMIA Kelas/Program : XII (Dua Belas)/IPA PETUNJUK UMUM 1. Berdo alah sebelum mengerjakan soal 2. Tulislah dahulu nama dan kelas
TRY UT UJIAN NASINAL TAHUN AJARAN 2008 / 2009 LEMBAR SAL B Bidang Studi : KIMIA Kelas/Program : XII (Dua Belas)/IPA PETUNJUK UMUM 1. Berdo alah sebelum mengerjakan soal 2. Tulislah dahulu nama dan kelas
BAB III KOMPOSISI KIMIA DALAM SEL. A. STANDAR KOMPETENSI Mahasiswa diharapkan Mampu Memahami Komposisi Kimia Sel.
 BAB III KOMPOSISI KIMIA DALAM SEL A. STANDAR KOMPETENSI Mahasiswa diharapkan Mampu Memahami Komposisi Kimia Sel. B. KOMPETENSI DASAR 1. Mahasiswa dapat membedakan komposisi kimia anorganik dan organik
BAB III KOMPOSISI KIMIA DALAM SEL A. STANDAR KOMPETENSI Mahasiswa diharapkan Mampu Memahami Komposisi Kimia Sel. B. KOMPETENSI DASAR 1. Mahasiswa dapat membedakan komposisi kimia anorganik dan organik
Bab. Senyawa Karbon. Kata Kunci
 Bab V Tujuan Pembelajaran Setelah mempelajari bab ini, Anda mampu mendeskripsikan struktur, cara penulisan, tata nama, sifat, kegunaan, dan identifikasi senyawa karbon. Setelah Friederick Wohler dapat
Bab V Tujuan Pembelajaran Setelah mempelajari bab ini, Anda mampu mendeskripsikan struktur, cara penulisan, tata nama, sifat, kegunaan, dan identifikasi senyawa karbon. Setelah Friederick Wohler dapat
kimia K-13 HIDROKARBON II K e l a s A. Alkena Tujuan Pembelajaran
 K-13 kimia K e l a s XI HIDROKARBON II Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut 1 Memahami pengertian, rumus umum, serta tata nama senyawa hidrokarbon
K-13 kimia K e l a s XI HIDROKARBON II Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut 1 Memahami pengertian, rumus umum, serta tata nama senyawa hidrokarbon
MAKALAH PRAKTIKUM KIMIA DASAR REAKSI-REAKSI ALKOHOL DAN FENOL
 MAKALAH PRAKTIKUM KIMIA DASAR REAKSI-REAKSI ALKOHOL DAN FENOL Oleh : ZIADUL FAIEZ (133610516) PROGRAM STUDI TEKNIK GEOLOGI FAKULTAS TEKNIK UNIVERSITAS ISLAM RIAU PEKANBARU 2015 BAB I PENDAHULUAN LatarBelakang
MAKALAH PRAKTIKUM KIMIA DASAR REAKSI-REAKSI ALKOHOL DAN FENOL Oleh : ZIADUL FAIEZ (133610516) PROGRAM STUDI TEKNIK GEOLOGI FAKULTAS TEKNIK UNIVERSITAS ISLAM RIAU PEKANBARU 2015 BAB I PENDAHULUAN LatarBelakang
A. RUMUS STRUKTUR DAN NAMA LEMAK B. SIFAT-SIFAT LEMAK DAN MINYAK C. FUNGSI DAN PERAN LEMAK DAN MINYAK
 8 LEMAK DAN MINYAK A. RUMUS STRUKTUR DAN NAMA LEMAK B. SIFAT-SIFAT LEMAK DAN MINYAK C. FUNGSI DAN PERAN LEMAK DAN MINYAK Lipid berasal dari kata Lipos (bahasa Yunani) yang berarti lemak. Lipid didefinisikan
8 LEMAK DAN MINYAK A. RUMUS STRUKTUR DAN NAMA LEMAK B. SIFAT-SIFAT LEMAK DAN MINYAK C. FUNGSI DAN PERAN LEMAK DAN MINYAK Lipid berasal dari kata Lipos (bahasa Yunani) yang berarti lemak. Lipid didefinisikan
HIDROKARBON (C dan H)
 BAB 8 IDROKARBON ( dan ) Keunikan atom Mampu berikatan dengan atom karbon lain membentuk rantai yang panjang terdiri dari berjuta atom Katenasi, Bercabang, Melingkar ALKANA : idrokarbon jenuh Ikatan tunggal
BAB 8 IDROKARBON ( dan ) Keunikan atom Mampu berikatan dengan atom karbon lain membentuk rantai yang panjang terdiri dari berjuta atom Katenasi, Bercabang, Melingkar ALKANA : idrokarbon jenuh Ikatan tunggal
KARBOHIDRAT PROTEIN LEMAK KIMIA KESEHATAN KELAS XII SEMESTER 5
 KARBOHIDRAT PROTEIN LEMAK n KIMIA KESEHATAN KELAS XII SEMESTER 5 SK dan KD Standar Kompetensi Menjelaskan sistem klasifikasi dan kegunaan makromolekul (karbohidrat, lipid, protein) Kompetensi Dasar Menjelaskan
KARBOHIDRAT PROTEIN LEMAK n KIMIA KESEHATAN KELAS XII SEMESTER 5 SK dan KD Standar Kompetensi Menjelaskan sistem klasifikasi dan kegunaan makromolekul (karbohidrat, lipid, protein) Kompetensi Dasar Menjelaskan
KARBOHIDRAT PROTEIN LEMAK
 KARBOHIDRAT PROTEIN LEMAK Kimia SMK KELAS XII SEMESTER 2 SMKN 7 BANDUNG SK DAN KD Standar Kompetensi Menjelaskan sistem klasifikasi dan kegunaan makromolekul (karbohidrat, lipid, protein) Kompetensi Dasar
KARBOHIDRAT PROTEIN LEMAK Kimia SMK KELAS XII SEMESTER 2 SMKN 7 BANDUNG SK DAN KD Standar Kompetensi Menjelaskan sistem klasifikasi dan kegunaan makromolekul (karbohidrat, lipid, protein) Kompetensi Dasar
KARBOHIDRAT. Klasifikasi karbohidrat menurut lokasi gugus karbonil C H C C CH 2 OH H H C C OH OH
 KARBIDRAT Pendahuluan Kata karbohidrat berasal dari kata karbon dan air. Secara sederhana karbohidrat didefinisikan sebagai polimer gula. Karbohidrat adalah senyawa karbon yang mengandung sejumlah besar
KARBIDRAT Pendahuluan Kata karbohidrat berasal dari kata karbon dan air. Secara sederhana karbohidrat didefinisikan sebagai polimer gula. Karbohidrat adalah senyawa karbon yang mengandung sejumlah besar
2. Substitusi dengan kelompok halogen OH. Halogen gugus-oh diganti dengan menggunakan pereaksi atau PCl5 PCL3:
 Analisa gugus fungsi Reaksi Kimia adalah suatu perubahan dari suatu senyawa atau molekul menjadi senyawa atau molekul lain. Reaksi yang terjadi pada senyawa anorganik biasanya reaksi antar ion, sedangkan
Analisa gugus fungsi Reaksi Kimia adalah suatu perubahan dari suatu senyawa atau molekul menjadi senyawa atau molekul lain. Reaksi yang terjadi pada senyawa anorganik biasanya reaksi antar ion, sedangkan
KIMIA. Sesi. Hidrokarbon (Bagian III) A. REAKSI-REAKSI SENYAWA KARBON. a. Adisi
 KIMIA KELAS XII IPA - KURIKULUM GABUNGAN 17 Sesi NGAN Hidrokarbon (Bagian III) A. REAKSI-REAKSI SENYAWA KARBON Reaksi-reaksi kimia yang terjadi pada senyawa hidrokarbon secara umum adalah reaksi adisi,
KIMIA KELAS XII IPA - KURIKULUM GABUNGAN 17 Sesi NGAN Hidrokarbon (Bagian III) A. REAKSI-REAKSI SENYAWA KARBON Reaksi-reaksi kimia yang terjadi pada senyawa hidrokarbon secara umum adalah reaksi adisi,
ALKOHOL / ALKANOL. Contoh pemberian nama IUPAC. 2 Butanol. a. CH 3 CH 2 CH CH 3 OH. Alkohol/Alkanol dan Eter/Alkoksi Alkana by Anton B.H.
 ALKOL / ALKANOL a. Tata nama IUPAC : sebagai ALKANOL 1) Langkah pemberian nama IUPAC Rantai C terpanjang (Rantai utama / induk) harus mengandung gugus. Nama rantai utama sesuai nama alkana, akhiran ana
ALKOL / ALKANOL a. Tata nama IUPAC : sebagai ALKANOL 1) Langkah pemberian nama IUPAC Rantai C terpanjang (Rantai utama / induk) harus mengandung gugus. Nama rantai utama sesuai nama alkana, akhiran ana
SAINS II (KIMIA) LEMAK OLEH : KADEK DEDI SANTA PUTRA
 SAINS II (KIMIA) LEMAK OLEH : KADEK DEDI SANTA PUTRA 1629061030 PROGRAM STUDI PENDIDIKAN IPA PROGRAM PASCASARAJANA UNIVERSITAS PENDIDIKAN GANESHA 2017 SOAL: Soal Pilihan Ganda 1. Angka yang menunjukkan
SAINS II (KIMIA) LEMAK OLEH : KADEK DEDI SANTA PUTRA 1629061030 PROGRAM STUDI PENDIDIKAN IPA PROGRAM PASCASARAJANA UNIVERSITAS PENDIDIKAN GANESHA 2017 SOAL: Soal Pilihan Ganda 1. Angka yang menunjukkan
HIDROKARBON A. PENGERTIAN SENYAWA KARBON B. HIDROKARBON
 7 HIDROKARBON A. PENGERTIAN SENYAWA KARBON B. HIDROKARBON Apabila kita membakar kayu, maka akan didapat suatu zat berwarna hitam yang kita sebut arang. Arang yang dihasilkan dari peristiwa pembakaran adalah
7 HIDROKARBON A. PENGERTIAN SENYAWA KARBON B. HIDROKARBON Apabila kita membakar kayu, maka akan didapat suatu zat berwarna hitam yang kita sebut arang. Arang yang dihasilkan dari peristiwa pembakaran adalah
Keunikan atom C?? Atom karbon primer, sekunder, tersier dan kuartener
 Keunikan atom C?? Atom karbon primer, sekunder, tersier dan kuartener Jenis ikatan karbon edakan : Propena (tak jenuh) Propuna (tak jenuh) Propana (jenuh) Rantai Atom Karbon Bedakan : 2-metil butana siklobutana
Keunikan atom C?? Atom karbon primer, sekunder, tersier dan kuartener Jenis ikatan karbon edakan : Propena (tak jenuh) Propuna (tak jenuh) Propana (jenuh) Rantai Atom Karbon Bedakan : 2-metil butana siklobutana
ALKANA 04/03/2013. Sifat-sifat fisik alkana. Alkana : 1. Oksidasi dan pembakaran
 ALKANA Sifat-sifat fisik alkana Alkana : senyawa hidrokarbon jenuh (ikatan tunggal), atom C : hibridisasi sp 3 rumus molekul : C n H 2n+2 struktur : alifatik (rantai lurus) dan siklik (sikloalkana) Tidak
ALKANA Sifat-sifat fisik alkana Alkana : senyawa hidrokarbon jenuh (ikatan tunggal), atom C : hibridisasi sp 3 rumus molekul : C n H 2n+2 struktur : alifatik (rantai lurus) dan siklik (sikloalkana) Tidak
BAB 9 HIDROKARBON. Gambar 9.1 Asam askorbat Sumber: Kimia Dasar Konsep-konsep Inti
 BAB 9 HIDROKARBON Gambar 9.1 Asam askorbat Sumber: Kimia Dasar Konsep-konsep Inti Pada pelajaran bab kesembilan ini akan dipelajari tentang kekhasan atom karbon, identitifikasi senyawa karbon, alkana,
BAB 9 HIDROKARBON Gambar 9.1 Asam askorbat Sumber: Kimia Dasar Konsep-konsep Inti Pada pelajaran bab kesembilan ini akan dipelajari tentang kekhasan atom karbon, identitifikasi senyawa karbon, alkana,
ALKHOHOL-ETER. Putri Anjarsari, S.Si., M.Pd
 ALKOOL-ETER Putri Anjarsari, S.Si., M.Pd putri_anjarsari@uny.ac.id 1 STRUKTUR ALKOOL Alkohol adalah senyawa yang molekulnya memiliki suatu gugus hidroksil, yang terikat pada suatu atom karbon jenuh. C
ALKOOL-ETER Putri Anjarsari, S.Si., M.Pd putri_anjarsari@uny.ac.id 1 STRUKTUR ALKOOL Alkohol adalah senyawa yang molekulnya memiliki suatu gugus hidroksil, yang terikat pada suatu atom karbon jenuh. C
PAKET UJIAN NASIONAL 14 Pelajaran : KIMIA Waktu : 120 Menit
 PAKET UJIAN NASINAL 14 Pelajaran : KIMIA Waktu : 120 Menit Pilihlah salah satu jawaban yang tepat! Jangan lupa Berdoa dan memulai dari yang mudah. 1. Diketahui ion X 3+ mempunyai 10 elektron dan 14 neutron.
PAKET UJIAN NASINAL 14 Pelajaran : KIMIA Waktu : 120 Menit Pilihlah salah satu jawaban yang tepat! Jangan lupa Berdoa dan memulai dari yang mudah. 1. Diketahui ion X 3+ mempunyai 10 elektron dan 14 neutron.
PAKET UJIAN NASIONAL 17 Pelajaran : KIMIA Waktu : 120 Menit
 PAKET UJIAN NASIONAL 17 Pelajaran : KIMIA Waktu : 120 Menit Pilihlah salah satu jawaban yang tepat! Jangan lupa Berdoa dan memulai dari yang mudah. 01. Diketahui ion X 3+ mempunyai 10 elektron dan 14 neutron.
PAKET UJIAN NASIONAL 17 Pelajaran : KIMIA Waktu : 120 Menit Pilihlah salah satu jawaban yang tepat! Jangan lupa Berdoa dan memulai dari yang mudah. 01. Diketahui ion X 3+ mempunyai 10 elektron dan 14 neutron.
SIMULASI UJIAN NASIONAL 1
 SIMULASI UJIAN NASIONAL 1 1. Bilangan-bilangan kuantum yang mungkin dimiliki oleh suatu elektron (A) n = 2, l = 2, m = 0, s = - 1 2 (B) n = 3, l = 0, m = +1, s = + 1 2 (C) n = 4, l = 2, m = - 3, s = -
SIMULASI UJIAN NASIONAL 1 1. Bilangan-bilangan kuantum yang mungkin dimiliki oleh suatu elektron (A) n = 2, l = 2, m = 0, s = - 1 2 (B) n = 3, l = 0, m = +1, s = + 1 2 (C) n = 4, l = 2, m = - 3, s = -
Pengantar KO2 (Kimia Organik Gugus Fungsi)
 Pengantar KO2 (Kimia Organik Gugus Fungsi) Sasaran : pengenalan gugus fungsi. Mengetahui sifat fisika dan kimia suatu bahan yang digunakan sebagai obat, kosmetika, bahan makanan dan minuman. Untuk digunaka
Pengantar KO2 (Kimia Organik Gugus Fungsi) Sasaran : pengenalan gugus fungsi. Mengetahui sifat fisika dan kimia suatu bahan yang digunakan sebagai obat, kosmetika, bahan makanan dan minuman. Untuk digunaka
Komponen Kimia penyusun Sel (Biologi) Ditulis pada September 27, 2012
 Komponen Kimia penyusun Sel (Biologi) Ditulis pada September 27, 2012 Sel disusun oleh berbagai senyawa kimia, seperti karbohidrat, protein,lemak, asam nukleat dan berbagai senyawa atau unsur anorganik.
Komponen Kimia penyusun Sel (Biologi) Ditulis pada September 27, 2012 Sel disusun oleh berbagai senyawa kimia, seperti karbohidrat, protein,lemak, asam nukleat dan berbagai senyawa atau unsur anorganik.
Senyawa organik adalah senyawa kimia yang molekulnya mengandung karbon, kecuali karbida, karbonat, dan oksida karbon.
 PENDAULUAN Definisi senyawa organik Kimia organik adalah studi ilmiah mengenai struktur, sifat, komposisi, reaksi, dan sintesis senyawa organik. Senyawa organik dibangun oleh karbon dan hidrogen, dan dapat
PENDAULUAN Definisi senyawa organik Kimia organik adalah studi ilmiah mengenai struktur, sifat, komposisi, reaksi, dan sintesis senyawa organik. Senyawa organik dibangun oleh karbon dan hidrogen, dan dapat
Protein (asal kata protos dari bahasa Yunani yang berarti "yang paling utama") adalah senyawa organik kompleks berbobot molekul tinggi yang merupakan
 A. Protein Protein (asal kata protos dari bahasa Yunani yang berarti "yang paling utama") adalah senyawa organik kompleks berbobot molekul tinggi yang merupakan polimer dari monomer-monomer asam amino
A. Protein Protein (asal kata protos dari bahasa Yunani yang berarti "yang paling utama") adalah senyawa organik kompleks berbobot molekul tinggi yang merupakan polimer dari monomer-monomer asam amino
REAKSI-REAKSI ALKOHOL DAN FENOL
 REAKSI-REAKSI ALKHL DAN FENL TUJUAN Tujuan dari Percobaan ini adalah: 1. Membedakan alkohol dengan fenol berdasarkan reaksinya dengan asam karboksilat 2. Membedakan alkohol dan fenol berdasarkan reaksi
REAKSI-REAKSI ALKHL DAN FENL TUJUAN Tujuan dari Percobaan ini adalah: 1. Membedakan alkohol dengan fenol berdasarkan reaksinya dengan asam karboksilat 2. Membedakan alkohol dan fenol berdasarkan reaksi
Addres: Fb: Khayasar ALKANA. Rumus umum alkana: C n H 2n + 2. R (alkil) = C n H 2n + 1
 ALKANA Rumus umum alkana: C n H 2n + 2 R (alkil) = C n H 2n + 1 Alkana Adalah rantai karbon yang memiliki ikatan tunggal (jenuh) A. Alkana 1. Alkana disebut juga senyawa hidrokarbon jenuh (senyawa parafin).
ALKANA Rumus umum alkana: C n H 2n + 2 R (alkil) = C n H 2n + 1 Alkana Adalah rantai karbon yang memiliki ikatan tunggal (jenuh) A. Alkana 1. Alkana disebut juga senyawa hidrokarbon jenuh (senyawa parafin).
B. Struktur Umum dan Tatanama Lemak
 A. Pengertian Lemak Lemak adalah ester dari gliserol dengan asam-asam lemak (asam karboksilat pada suku tinggi) dan dapat larut dalam pelarut organik non-polar, misalnya dietil eter (C2H5OC2H5), Kloroform
A. Pengertian Lemak Lemak adalah ester dari gliserol dengan asam-asam lemak (asam karboksilat pada suku tinggi) dan dapat larut dalam pelarut organik non-polar, misalnya dietil eter (C2H5OC2H5), Kloroform
Senyawa yang hanya tersusun oleh karbon dan hidrogen Banyak terdapat di alam (Contoh : gas alam, minyak bumi) Dibagi menjadi 3 yaitu : 1.
 Senyawa yang hanya tersusun oleh karbon dan hidrogen Banyak terdapat di alam (Contoh : gas alam, minyak bumi) Dibagi menjadi 3 yaitu : 1. Jenuh : alkana, mempunyai ikatan tunggal dibagi menjadi 2 yaitu
Senyawa yang hanya tersusun oleh karbon dan hidrogen Banyak terdapat di alam (Contoh : gas alam, minyak bumi) Dibagi menjadi 3 yaitu : 1. Jenuh : alkana, mempunyai ikatan tunggal dibagi menjadi 2 yaitu
LATIHAN ULANGAN KIMIA : HIDROKARBON KELAS X
 LATIHAN ULANGAN KIMIA : HIDROKARBON KELAS X Pilihlah salah satu jawaban yang paling tepat! 1. Alkana yang tidak mengandung lima atom karbon yaitu.... a. n-pentena b. 2-metil-butana c. isopentana d. 2-metil-pentana
LATIHAN ULANGAN KIMIA : HIDROKARBON KELAS X Pilihlah salah satu jawaban yang paling tepat! 1. Alkana yang tidak mengandung lima atom karbon yaitu.... a. n-pentena b. 2-metil-butana c. isopentana d. 2-metil-pentana
OH (Metil alkohol = Metanol) CH 2. OH (etil alkohol = etanol) OH (1-propanol = n-propanol)
 Rumus umum R-O Gugus fungsional: O (gugus hidroksil) Tata nama Diturunkan dari gugus alkil yang melekat pada O, kemudian ditambah kata alkohol. Dalam sistem IUPAC: akhiran ol menunjukan adanya gugus hidroksil
Rumus umum R-O Gugus fungsional: O (gugus hidroksil) Tata nama Diturunkan dari gugus alkil yang melekat pada O, kemudian ditambah kata alkohol. Dalam sistem IUPAC: akhiran ol menunjukan adanya gugus hidroksil
LEMBARAN SOAL 6. Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH )
 LEMBARAN SOAL 6 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah soal dengan
LEMBARAN SOAL 6 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah soal dengan
Materi Penunjang Media Pembelajaran Kimia Organik SMA ALKANA
 ALKANA Alkana rantai pendek (metana dan etana) terdapat dalam atmosfer beberapa planet seperti jupiter, saturnus, uranus, dan neptunus. Bahkan di titan (satelit saturnus) terdapat danau metana/etana yang
ALKANA Alkana rantai pendek (metana dan etana) terdapat dalam atmosfer beberapa planet seperti jupiter, saturnus, uranus, dan neptunus. Bahkan di titan (satelit saturnus) terdapat danau metana/etana yang
SOAL DAN PEMBAHASAN TRY OUT 1 KOMPETISI KIMIA NASIONAL 2017
 1. Nomor atom unsur A, B, C, D, dan E berturut-turut 6, 8, 9, 16, 19. Pasangan unsur yang dapat membentuk ikatan ion adalah a. A dan D d. D dan C b. C dan E e. A dan B c. B dan E Jawaban : b ikatan ion
1. Nomor atom unsur A, B, C, D, dan E berturut-turut 6, 8, 9, 16, 19. Pasangan unsur yang dapat membentuk ikatan ion adalah a. A dan D d. D dan C b. C dan E e. A dan B c. B dan E Jawaban : b ikatan ion
ALKOHOL DAN ETER. Tim Dosen Kimia Dasar II/ Kimia Organik
 ALKOHOL DAN ETER Tim Dosen Kimia Dasar II/ Kimia Organik 1 SUMBER ALKOHOL DAN ETER Alkohol didapatkan dengan berbagai cara yaitu dapat dibuat dengan cara fermentasi terhadap bahan bahan yang mengandung
ALKOHOL DAN ETER Tim Dosen Kimia Dasar II/ Kimia Organik 1 SUMBER ALKOHOL DAN ETER Alkohol didapatkan dengan berbagai cara yaitu dapat dibuat dengan cara fermentasi terhadap bahan bahan yang mengandung
PAKET UJIAN NASIONAL 16 Pelajaran : KIMIA Waktu : 120 Menit
 PAKET UJIAN NASIONAL 16 Pelajaran : KIMIA Waktu : 120 Menit Pilihlah salah satu jawaban yang tepat! Jangan lupa Berdoa dan memulai dari yang mudah. 01. 27 Isotop 13 Al terdiri dari... A. 13 proton,14 elektron
PAKET UJIAN NASIONAL 16 Pelajaran : KIMIA Waktu : 120 Menit Pilihlah salah satu jawaban yang tepat! Jangan lupa Berdoa dan memulai dari yang mudah. 01. 27 Isotop 13 Al terdiri dari... A. 13 proton,14 elektron
Kimia EBTANAS Tahun 2000
 Kimia EBTANAS Tahun 2000 EBTANAS-00-01 Seorang siswa mencampurkan dua zat kimia. Diantara pernyataan di bawah ini yang tidak menunjukkan telah terjadi reaksi kimia adalah A. timbul gas B. terjadi endapan
Kimia EBTANAS Tahun 2000 EBTANAS-00-01 Seorang siswa mencampurkan dua zat kimia. Diantara pernyataan di bawah ini yang tidak menunjukkan telah terjadi reaksi kimia adalah A. timbul gas B. terjadi endapan
Chapter 20 ASAM KARBOKSILAT
 Chapter 20 ASAM KARBOKSILAT Pengantar Gugus fungsi dari asam karboksilat terdiri atas ikatan C=O dengan OH pada karbon yang sama. Gugus karboksil biasanya ditulis -COOH. Asam alifatik memiliki gugus alkil
Chapter 20 ASAM KARBOKSILAT Pengantar Gugus fungsi dari asam karboksilat terdiri atas ikatan C=O dengan OH pada karbon yang sama. Gugus karboksil biasanya ditulis -COOH. Asam alifatik memiliki gugus alkil
Kimia Dasar II / Kimia Organik. Shinta Rosalia D. (SRD) Angga Dheta S. (ADS) Sudarma Dita W. (SDW) Nur Lailatul R. (NLR) Feronika Heppy S (FHS)
 Kimia Dasar II / Kimia Organik Shinta Rosalia D. (SRD) Angga Dheta S. (ADS) Sudarma Dita W. (SDW) Nur Lailatul R. (NLR) Feronika Heppy S (FHS) Kontrak perkuliahan : 1. Ujian : 50% 2. Tugas : 10% 3. Kuis
Kimia Dasar II / Kimia Organik Shinta Rosalia D. (SRD) Angga Dheta S. (ADS) Sudarma Dita W. (SDW) Nur Lailatul R. (NLR) Feronika Heppy S (FHS) Kontrak perkuliahan : 1. Ujian : 50% 2. Tugas : 10% 3. Kuis
MODUL KIMIA SMA IPA Kelas 12
 A. BENZENA 1. Rumus a. Rumus molekul : C 6H 6 b. Rumus bangun : 2. Hibridisasi Struktur Kekule, setiap atom C dalam benzena membentuk 3 ikatan sigma = ( sp 2 ) 3 dan 1 ikatan phi = ( p-p ) 1. Hal ini dapat
A. BENZENA 1. Rumus a. Rumus molekul : C 6H 6 b. Rumus bangun : 2. Hibridisasi Struktur Kekule, setiap atom C dalam benzena membentuk 3 ikatan sigma = ( sp 2 ) 3 dan 1 ikatan phi = ( p-p ) 1. Hal ini dapat
LAPORAN PRAKTIKUM KIMIA ORGANIK
 LAPORAN PRAKTIKUM KIMIA ORGANIK ACARA 4 SENYAWA ASAM KARBOKSILAT DAN ESTER Oleh: Kelompok 5 Nova Damayanti A1M013012 Nadhila Benita Prabawati A1M013040 KEMENTRIAN PENDIDIKAN DAN KEBUDAYAAN UNIVERSITAS
LAPORAN PRAKTIKUM KIMIA ORGANIK ACARA 4 SENYAWA ASAM KARBOKSILAT DAN ESTER Oleh: Kelompok 5 Nova Damayanti A1M013012 Nadhila Benita Prabawati A1M013040 KEMENTRIAN PENDIDIKAN DAN KEBUDAYAAN UNIVERSITAS
BIOKIMIA Kuliah 1 KARBOHIDRAT
 BIOKIMIA Kuliah 1 KARBOHIDRAT 1 Karbohidrat Karbohidrat adalah biomolekul yang paling banyak terdapat di alam. Setiap tahunnya diperkirakan kira-kira 100 milyar ton CO2 dan H2O diubah kedalam molekul selulosa
BIOKIMIA Kuliah 1 KARBOHIDRAT 1 Karbohidrat Karbohidrat adalah biomolekul yang paling banyak terdapat di alam. Setiap tahunnya diperkirakan kira-kira 100 milyar ton CO2 dan H2O diubah kedalam molekul selulosa
 TRY OUT SELEKSI OLIMPIADE TINGKAT KABUPATEN/KOTA 2010 TIM OLIMPIADE KIMIA INDONESIA 2011 Waktu: 150 Menit PUSAT KLINIK PENDIDIKAN INDONESIA (PKPI) bekerjasama dengan LEMBAGA BIMBINGAN BELAJAR SSCIntersolusi
TRY OUT SELEKSI OLIMPIADE TINGKAT KABUPATEN/KOTA 2010 TIM OLIMPIADE KIMIA INDONESIA 2011 Waktu: 150 Menit PUSAT KLINIK PENDIDIKAN INDONESIA (PKPI) bekerjasama dengan LEMBAGA BIMBINGAN BELAJAR SSCIntersolusi
PAKET UJIAN NASIONAL 8 Pelajaran : KIMIA Waktu : 120 Menit
 PAKET UJIAN NASIONAL 8 Pelajaran : KIMIA Waktu : 120 Menit Pilihlah salah satu jawaban yang tepat! Jangan lupa Berdoa dan memulai dari yang mudah. 1. Di antara unsur-unsur 12 P, 16 Q, 19 R, 34 S dan 53
PAKET UJIAN NASIONAL 8 Pelajaran : KIMIA Waktu : 120 Menit Pilihlah salah satu jawaban yang tepat! Jangan lupa Berdoa dan memulai dari yang mudah. 1. Di antara unsur-unsur 12 P, 16 Q, 19 R, 34 S dan 53
Dari data di atas yang tergolong polimer jenis termoplastik adalah. A. 1 dan 5 B. 2 dan 5
 Latihan contoh soal dan jawaban soal polimer Berilah tanda silang (X) pada huruf A, B, C, D atau E di depan jawaban yang benar! 1. Polimer berikut yang tidak termasuk polimer alam adalah. A. tetoron B.
Latihan contoh soal dan jawaban soal polimer Berilah tanda silang (X) pada huruf A, B, C, D atau E di depan jawaban yang benar! 1. Polimer berikut yang tidak termasuk polimer alam adalah. A. tetoron B.
: Mengidentifikasi bahan makanan yang mengandung karbohidrat (amilum dan gula ), protein, lemak dan vitamin C secara kuantitatif.
 II. Tujuan : Mengidentifikasi bahan makanan yang mengandung karbohidrat (amilum dan gula ), protein, lemak dan vitamin C secara kuantitatif. III. Alat dan bahan : Rak tabung reaksi Tabung reaksi Gelas
II. Tujuan : Mengidentifikasi bahan makanan yang mengandung karbohidrat (amilum dan gula ), protein, lemak dan vitamin C secara kuantitatif. III. Alat dan bahan : Rak tabung reaksi Tabung reaksi Gelas
