Materi kimia kelas XI semester gasal Smk ma arif 1 Kebumen 1.SENYAWA HIDROKARBON DAN KEGUNAANNYA
|
|
|
- Yuliana Irawan
- 6 tahun lalu
- Tontonan:
Transkripsi
1 Materi kimia kelas XI semester gasal Smk ma arif 1 Kebumen 1.SENYAWA IDROKARBON DAN KEGUNAANNYA Senyawa idrokarbon hidrogen + karbon adalah senyawa yang terbentuk dari atom C dan. Senyawa Organik dan Senyawa Karbon Senyawa Organik adalah senyawa yang berasal dari makhluk hidup. Senyawa Anorganik adalah senyawa yang berasal dari alam selain makhluk hidup Seiring berkembangnya analisis kimia, diketahui bahwa senyawa-senyawa organik tersusun oleh atom karbon sehingga senyawa organik disebut pula senyawa karbon. Namun demikian, ada pula persenyawaan karbon yang tergolong senyawa anorganik. Kekhasan Atom Karbon 1. Karbon mempunyai 4 elektron valensi Dalam Sistem Periodik Unsur, atom C terletak pada golongan IV A. 6C : 4 C C. Jari-jari atom karbon relatif kecil Sesuai letaknya di periode kedua, karbon hanya memiliki dua kulit atom yang menyebabkan jari-jari atom karbon relatif kecil sehingga: - ikatan kovalen yang dibentuk karbon relatif kuat - dapat membentuk ikatan rangkap dua dan ikatan rangkap tiga 3. Atom Karbon Dapat Membentuk Rantai Karbon. Keadaan atom karbon yang demikian menyebabkan atom karbon dapat membentuk rantai karbon yang sangat panjang dengan ikatan kovalen, baik ikatan kovalen tunggal, rangkap, maupun rangkap 3. Selain itu dapat pula membentuk rantai lingkar (siklik). Ikatan kovalen tunggal :: C3 C C C C C3 Ikatan kovalen rangkap : :C= C C C3 Ikatan kovalen rangkap 3 :: C3 C C C C3 4. Atom Karbon memiliki perbedaan kedudukan dalam suatu rantai karbon * Atom C primer atom C yang mengikat langsung 1 atom C yang lain *Atom C sekunder atom C yang mengikat langsung atom C yang lain *Atom C tersier atom C yang mengikat langsung 3 atom C yang lain *Atom C kuarterner :atom C yang mengikat langsung 4 atom C yang lain Pengelompokkan Senyawa idrokarbon Berdasarkan ada tidaknya cincin benzena, senyawa hidrokarbon dikelompokkan menjadi yaitu hidrokarbon alifatik dan hidrokarbon aromatis. benzena A. Senyawa idrokarbon Alifatik adalah senyawa hidrokarbon yang tidak mengandung cincin benzena. Berdasarkan bentuk rantai karbonnya, senyawa hidrokarbon alifatik dibedakan menjadi yaitu asiklik dan siklik. 1. Asiklik bentuk rantai terbuka Contoh : 3C C C C C C3. Siklik bentuk rantai melingkar / tertutup Contoh: C C C C C C C C C C C Siklopropana siklobutana C C Sikloheksana Berdasarkan jenis ikatan antaratom karbonnya, senyawa hidrokarbon alifatik dibedakan menjadi yaitu jenuh dan tak jenuh. 1. Jenuh semua ikatan karbon-karbon merupakan ikatan tunggal Contoh : 3C C C C C3 3C C C C3 C3. Tak Jenuh terdapat ikatan karbon rangkap dua atau rangkap tiga Contoh : C = C C C3 3C C C C C3 Materi kimia kelas xi semester gasal Page 1
2 Berdasarkan ikatan karbon jenuh dan tak jenuh dibagi menjadi 3 yaitu alkana, alkena, dan alkuna 1. Alkana merupakan hidrokarbon alifatik jenuh dimana semua ikatan karbon-karbonnya adalah ikatan tunggal. Rumus molekul : C n n+ Deret homolognya: Jumlah atom C Rumus molekul Nama Jumlah atom C Rumus molekul Nama C4 C6 C38 C410 C51 Metana Etana Propana Butana Pentana Tata nama Alkana a) Bila rantai atom karbon lurus, beri nama sesuai jumlah atom C dengan awalan n (normal). b) Bila rantai atom karbon bercabang: 1. Tentukan rantai induk (jumlah C terpanjang/terbanyak). Tentukan cabang/gugus alkil 3. Beri nomor pada tiap atom C rantai induk dimulai dari atom C yang paling dekat dengan cabang 4. Beri nama dengan format berikut: nomor cabang (nama cabang)(nama rantai induk) Penamaan cabang/alkil Rumus alkil: C n n+1 Penamaan alkil: Jumlah C Nama alkil Jumlah C Nama alkil Metil Etil Propil Butil Amil eksil eptil Oktil Nonil Dekil Bila ada lebih dari satu cabang - Berbeda penulisan alkil diurutkan sesuai abjad - Sama diberi awalan di- =, tri- = 3, tetra- = 4, penta- = 5 dst Contoh: Beri nama senyawa karbon berikut! 1. 3C C C C C C3 jawab: n-heksana C C C C3 jawab: metilbutana C3 C C C C C C C3 jawab: 3 etil,4 dimetilpentana C614 C716 C818 C90 C10 eksana eptana Oktana Nonana Dekana C3 C3 Sifat-sifat alkana: 1) C1 C4 berwujud gas, C5 C17 berwujud cair, C18 seterusnya berwujud padat. ) Makin panjang rantai, titik didih makin tinggi. 3) Bersifat nonpolar sehingga tidak larut dalam air. 4) Sukar bereaksi. SIKLOALKANA merupakan hidrokarbon alifatik jenuh dimana semua ikatan karbon-karbonnya tunggal dengan bentuk rantai tertutup/melingkar/siklik. Rumus umum sama dengan alkena. Penamaan seperti pada alkana, hanya menambahkan awalan siklo. Contoh: C C C C C C C C C C C Siklopropana siklobutana (kubana). Alkena merupakan hidrokarbon alifatik tak jenuh dimana terdapat ikatan karbon rangkap dua. C C Sikloheksana Rumus : C n n Deret homolognya: Jumlah atom C Rumus molekul Nama Jumlah atom C Rumus molekul Nama C4 C36 C48 C510 Etena Propena Butena Pentena C61 C714 C816 C918 eksena eptena Oktena Nonena Materi kimia kelas xi semester gasal Page
3 Tata nama alkena Penamaan alkena mengikuti aturan alkana hanya ada beberapa ketentuan lain yaitu: 1. Akhiran ana diganti ena. Penomoran rantai induk dimulai dari atom C yang terdekat dengan ikatan rangkap 3. Format pemberian nama: a. Rantai lurus nomor C ikatan rangkap nama rantai b. Rantai bercabang nmr cabang nama cabang nmr C iktn rgkp nama rantai induk 4. Bila dalam satu rantai ada lebih dari satu ikatan rangkap maka akhiran ena diganti: diena = ikatan rangkap triena = 3 ikatan rangkap tetraena = 4 ikatan rangkap, dan seterusnya Contoh: Beri nama senyawa karbon berikut! C = C C C3 jawab: 1 butena C C C = C C3 jawab: 3 metil pentena C C = C C = C C3 jawab: 1, 3 pentadiena Sifat-sifat alkena: 1. Semakin panjang rantai, titik didih makin tinggi.. C1 C4 berwujud gas, C5 C17 berwujud cair, C18 seterusnya berwujud padat. 3. Adanya ikatan rangkap dua yang memungkinkan terjadinya beberapa reaksi kimia yang tidak dapat dilakukan oleh alkana. 3. Alkuna merupakan hidrokarbon alifatik tak jenuh dimana terdapat ikatan karbon rangkap tiga. Rumus : C n n- Deret homolognya: Jumlah atom C Rumus molekul Nama Jumlah atom C Rumus molekul Nama C Etena 6 C610 eksena C34 C46 C58 Propena Butena Pentena C71 C814 C916 eptena Oktena Nonena Tata nama alkuna Penamaan untuk alkuna mengikuti aturan alkena hanya akhiran ena diganti una Contoh: Beri nama senyawa karbon berikut! C C C jawab: 1 propuna C C C C jawab: 3 metil 1 pentuna 4 5 C C3 Isomer adalah senyawa-senyawa yang memiliki rumus molekul sama tetapi rumus strukturnya berbeda. Contoh: Tentukan rumus struktur dan nama dari isomer senyawa n heksana! Jawab: n-heksana : C614 3C C C C C C3 isomernya adalah: 1. 3C C C C C3 metilpentana C3. 3C C C C C3 3 metilpentana C3 3. 3C C C C3,3 dimetilbutana C3 C3 C3 4. 3C C C C3, dimetilbutana C3 Jadi, n-heksana mempunyai 4 isomer B. Senyawa idrokarbon Aromatik adalah senyawa hidrokarbon yang mengandung cincin benzena. Disebut juga senyawa arena. Istilah aromatik dipakai karena senyawa arena mengeluarkan aroma yang khas. Materi kimia kelas xi semester gasal Page 3
4 Rumus umum: Struktur Cincin Benzena (C66) atau atau atau Contoh senyawa aromatik: Naftalena Antrasena Fenantrena Minyak Bumi Salah satu kegunaan terpenting dari senyawa hidrokarbon adalah sebagai senyawa penyusun (sumber) minyak bumi. Sumber energi yang banyak digunakan untuk memasak, kendaraan bermotor, dan industri petrokimia berasal dari minyak bumi. Minyak bumi berasal dari pembusukan sisa-sisa organisme (jasad renik lautan, hewan, tumbuhan) yang mengendap di dasar lautan kemudian tertutup lumpur. Lapisan lumpur lambat laun mengeras menjadi batuan akibat tekanan dan suhu lapisan atasnya sedangkan bakteri anaerob menguraikan sisasisa organisme tersebut, mengubahnya menjadi minyak bumi. Proses tersebut memakan waktu jutaan tahun. Kandungan Utama Minyak Bumi Minyak bumi adalah suatu campuran kompleks yang sebagian besar terdiri atas hidrokarbon. idrokarbon yang terkandung dalam minyak bumi terutama adalah alkana (parafin) dan sikloalkana (nafta/sikloparafin). Komponen lainnya adalah hidrokarbon aromatik, sed ikit alkena (olefin), dan berbagai senyawa karbon yang mengandung oksigen, nitrogen, dan belerang. Pengolahan Minyak Bumi Minyak mentah (crude oil) berbentuk cairan hitam kental dan berbau kurang sedap dan belum dapat digunakan secara langsung sebagai bahan bakar, maka perlu diolah terlebih dahulu. Pengolahan minyak bumi dimulai dengan memanaskan minyak mentah pada suhu sekitar 400 C kemudian dialirkan ke dalam menara fraksionasi dimana akan terjadi pemisahan berdasarkan perbedaan titik didihnya. Proses pemisahan tersebut dinamakan proses destilasi fraksionasi. Pada proses destilasi tersebut, fraksi minyak bumi yang titik didihnya rendah akan menguap terlebih dahulu lalu diikuti fraksi yang titik didihnya lebih tinggi. Semakin ke atas, suhu semakin rendah, sehingga tiap kali fraksi minyak bumi yang titik didihnya tinggi akan mengembun dan terpisah, sedangkan yang titik didihnya rendah akan terus naik ke atas hingga fraksi yang mencapai puncak menara adalah yang berupa gas pada suhu kamar disebut gas petroleum. Melalui kompresi dan pendinginan, gas petroleum dicairkan sehingga diperoleh LPG (Liquified Petroleum Gas). Tabel Fraksi idrokarbon asil Penyulingan Minyak Bumi Fraksi Ukuran Kegunaan Titik Didih ( C) Molekul Gas alam (LNG) Gas Elpiji (LPG) Petroleum Eter Bensin (gasoline) Nafta Kerosin Solar Minyak pelumas Parafin Aspal C1 C C3 C4 C5 C6 C7 C8 C9 C10 C11 C13 C14 C16 C17 C0 C1 C4 C36 dst -100 sampai sampai 0 0 sampai sampai sampai sampai sampai 350 di atas 350 Sumber hidrogen Bahan bakar (tabung) Pelarut, Dry Cleaning Bahan bakar motor Bahan baku industri Bahan bakar industri Bahan bakar motor Pelumas Bahan baku lilin dll Pelapis jalan raya Bensin (Petrol atau Gasolin) Bensin merupakan salah satu fraksi minyak bumi yang penggunaannya sangat luas di bidang transportasi sebagai bahan bakar kendaraan bermotor. Di dalam mesin, bensin dibakar untuk menghasilkan energi yang berfungsi menjalankan mesin kendaraan bermotor. Di dalam bensin terdapat dua senyawa utama yaitu n-heptana dan isooktana. Efisiensi / mutu (performance) bensin ditentukan oleh jumlah ketukan (knocking) yang dinyatakan sebagai nilai oktan. Nilai oktan adalah perbandingan n-heptana dan isooktana dalam bensin untuk menghasilkan ketukan.
5 Ketukan (knocking) adalah pembakaran yang terjadi terlalu dini sebelum piston / silinder mesin berada pada posisi yang tepat. Ketukan menyebabkan Isooktana menghasilkan ketukan yang sedikit sehingga nilai oktannya 100, sedangkan n-heptana menghasilkan ketukan paling banyak sehingga nilai oktannya 0 (nol). Semakin tinggi nilai oktan suatu bensin, isooktana yang dikandung semakin banyak sehingga mutunya semakin baik. Tiga jenis bensin yang ada adalah: a. Premium : nilai oktan 88 (88% isooktana + 1% n-heptana) b. Pertamax : nilai oktan 9 (9% isooktana + 8% n-heptana) c. Pertamax Plus : nilai oktan 94 (94% isooktana + 6% n-heptana) Fraksi bensin dari penyulingan mempunyai nilai oktan 60. Cara meningkatkan mutu bensin adalah: 1) Reforming adalah suatu proses untuk mengubah alkana rantai lurus menjadi rantai bercabang. Alkana rantai bercabang memiliki nilai oktan yang lebih tinggi dari rantai lurus. ) Menambahkan zat antiketukan - Zat aditif yang biasa digunakan adalah TEL (Tetra Etil Lead), Pb(C5)4. - Penambahan -3 ml TEL ke dalam 1 galon bensin dapat menaikkan nilai oktan sebesar 15 poin. - Pembakaran bensin dengan TEL akan menghasilkan Pb (timbal) berupa asap PbBr dalam asap kendaraan yang merupakan racun yang dapat merusak otak. - Zat antiketukan yang ramah lingkungan adalah MTBE (Metil Tersier Butil Eter). - Campuran bensin premium dengan 0% MTBE disebut bensin premix-94 yang berarti memiliki nilai oktan Zat aditif yang lain: benzena, etanol, dan tersier-butil alkohol. Materi kimia kelas xi semester gasal Page 5
6 UJI KOMPETENSI XI SEMESTER GANJIL TAUN PELAJARAN 015/016 Mata Diklat : Kimia Program Keahlian : TKR,TEI dan TAV Kelas : XI Kompetensi : idrokarbon dan Minyak Bumi Kerjakan Soal Soal berikut ini! Jawaban dikirim melalui dengan alamat: efaizatun@gmail.com ( bagi siswa yang sedang prakerind ) A. Pilihan Ganda 1. Jumlah ikatan yang terdapat pada molekul C 3 8 adalah... a. dua d. delapan b. empat e. sepuluh c. enam. Ikatan karbon jenuh adalah ikatan antar atom C yang merupakan... a. ikatan tunggal b. ikatan rangkap c. ikatan rangkap 3 d. ikatan rantai terbuka e. ikatan rantai tertutup 3. Manakah senyawa berikut yang bersifat jenuh? a. C 3 6 d. C 4 8 b. C 3 4 e. C 4 9 c. C Diantara senyawa berikut ini yang bukan senyawa hidrokarbon adalah... a. elpiji d. solar b. bensin e. alkohol c. bitumen 5. Diantara senyawa berikut : 1) C 4 8 4) C 4 10 ) C 5 1 5) C 5 8 3) C 6 1 Yang merupakan satu homolog/satu golongan adalah... a. 1- d. 1-3 b. -3 e. -5 c Perhatikan deretan senyawa berikut : C 6, C 3 8, C Suku tertinggi berikutnya adalah... a. C 4 1 d. C 5 1 b. C 5 8 e. C 6 1 c. C Senyawa : C 3 I C 3 C C C C C C 3 І I C C 3 І C 3 Mengandung atom karbon primer, sekunder, dan tersier berturut-turut sebanyak... a d b e c Dari senyawa-senyawa berikut : (1) C 3 C C (3) C 3 C C -C 3 І C3 C () C 3 (4) C 3 C C C 3 І І І C 3 C C 3 C 3 C 3 І C 3 Yang merupakan isomer adalah... a. 1- d. -4 b. 1-3 e. -3 c. 1-4 Materi kimia kelas xi semester gasal Page 6
7 9. Senyawa yang merupakan isomer dari oktana adalah : a. 3-metil heksana d.,-dimetil pentana b.,3-dimetil pentana e.,-dimetil butana c.,3,4-trimetil pentana 10. Senyawa manakah yang merupakan isomer dari,3-dimetil, 3-etil pentana? a. 1-nonuna d. 3-etil,-metil, heksana b. n-nonena e. 4-etil, pentana. c. -metil, -hekena 11. Senyawa : C 3 C C 3 І І C 3 C C C C C C 3 І C 3 a. 3,5-diisopropil heksana. b.,3-dimetil,5-etil, heptana. c. 3-etil, -metil, 5-heptuna. d.,3-dimetil, heptana. e. 3-etil,5,6-dimetil, heptana. 1. Pada senyawa,-dimetil propana terdapat ikatan C sebanyak... a. 8 d.11 b. 9 e. 1 c Diantara senyawa berikut yang mempunyai titik didih paling tinggi adalah... a. n-propana d. -metil butana b.,-dimetil propana e. -metil propana c. n-pentana 14. Senyawa : C 3 І C 3 C = C C C 3 Berdasarkan tatanama IUPAC adalah... a. -metil, -pentena d. 4-metil, -pentana b. 4-metil, -pentena e. -metil, pentana c. -metil, 4-pentuna 15. Bensin premix merupakan campuran bensin premium dengan aditif... a. alkohol d. Benzena b. TEL e. Tertier Butil Alkohol c. MTBE B. Essay 1. Gambarkan struktur lewis : a. idrogen ( Golongan IA, Periode 1) b. Karbon ( Golongan IVA, Periode ). Sebutkan 3 kekhasan yang dimiliki atom C! (Berikut soal untuk no 3 dan 4) Tuliskan nama IUPAC dan rumus molekul dari struktur rangka berikut : 3. C 3 І C 3 C C C C 3 І І C 3 C І C 3 4. C 3 C C = C C C 3 І І C 3 C І C 3 5. Jelaskan : a. Bilangan Oktan b. Komponen utama dari senyawa hidrokarbon penyusun bensin! c. Premix memiliki nilai oktan 94. Jelaskan maksudnya! Materi kimia kelas xi semester gasal Page 7
8 .TERMOKIMIA Sistem adalah bagian dari alam yang menjadi pusat perhatian kita. Lingkungan adalah segala sesuatu yang berada di luar sistem. Pengelompokkan Sistem Ada tiga jenis sistem berdasarkan jenis pertukaran (materi dan energi) yang terjadi antara sistem dan lingkungan: 1. Sistem Terbuka terjadi pertukaran materi dan energi antara sistem dan lingkungan. Pertukaran materi artinya ada hasil reaksi yang dapat meninggalkan sistem (misalnya gas) atau ada sesuatu dari lingkungan yan g dapat memasuki sistem.. Sistem Tertutup terjadi pertukaran energi tetapi tidak terjadi pertukaran materi. 3. Sistem Terisolasi tidak terjadi pertukaran materi dan energi antara sistem dengan lingkungan. Entalpi () dan Perubahan Entalpi (Δ) Entalpi adalah jumlah energi/kalor yang masuk atau keluar dari sistem pada tekanan tetap. Besarnya entalpi dalam sistem tidak bisa diukur, tetapi perubahan entalpinya dapat diukur. Perubahan Entalpi adalah perbedaan keadaan awal dan keadaan akhir dari sistem yang berubah. Reaksi Eksoterm dan Reaksi Endoterm Tabel 6 Perbedaan Reaksi Eksoterm dan Reaksi Endoterm Reaksi Eksoterm Reaksi Endoterm reaksi yang melepaskan panas/kalor/ energi. reaksi yang menyerap panas/kalor/ energi. terjadi perpindahan energi dari sistem ke lingkungan. sistem lingkungan terjadi perpindahan energi dari lingkungan ke sistem. sistem lingkungan Karena energi dilepas maka energi sistem berkurang sehingga Δ = (negatif). Karena energi diserap maka energi sistem bertambah sehingga Δ = + (positif). ENERGI reaktan produk Δ = p r < 0 ENERGI produk reaktan Δ = p r > 0 Macam-macam entalpi reaksi 1. Entalpi Pembentukan Standar (Δ f) formation adalah perubahan entalpi pada reaksi pembentukan 1 mol senyawa dari unsur-unsurnya pada keadaan standar. Reaksi pembentukan : Unsur + Unsur Senyawa. Entalpi Penguraian Standar (Δ d) decomposition adalah perubahan entalpi pada reaksi penguraian 1 mol senyawa menjadi unsur-unsurnya pada keadaan standar. Reaksi penguraian : Senyawa Unsur + Unsur 3. Entalpi Pembakaran Standar (Δ c) combustion adalah perubahan entalpi pada reaksi pembakaran 1 mol unsur atau senyawa. Reaksi Pembakaran: Senyawa 1 + O Senyawa + Senyawa 3 4. Entalpi Penetralan (Δn) neutralisation adalah perubahan entalpi pada reaksi pembentukan O dari asam dan basa. 5. Entalpi Pelarutan (Δl) liquification adalah perubahan entalpi pada pelarutan 1 mol zat. 6. Entalpi Peleburan (Δm) melt adalah perubahan entalpi pada proses perubahan 1 mol zat padat menjadi cair. 7. Entalpi Penyubliman (Δs) sublimation adalah perubahan entalpi pada proses perubahan 1 mol zat padat menjadi gas pada suhu tertentu. 8. Entalpi Penguapan (Δv) vapourisation adalah perubahan entalpi pada proses perubahan 1 mol zat cair menjadi gas pada suhu tertentu. Menghitung Perubahan Entalpi (Δ) Reaksi Persamaan Termokimia secara umum: m A + n B y C + z D 1. Menggunakan Data Entalpi Pembentukan Standar (Δ f) Tips : KANAN dikurangi KIRI Rumus: Δ ΣΔ ο f (produk) ΣΔ ο f (reaktan) Δ = x kj/mol Materi kimia kelas xi semester gasal Page 8
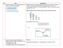
9 Keterangan : Δ = perubahan entalpi ΣΔ f (produk) = jumlah entalpi pembentukan standar zat-zat produk/hasil reaksi ΣΔ f (reaktan) = jumlah entalpi pembentukan standar zat-zat reaktan/pereaksi Contoh soal: Entalpi pembentukan CO, O, C4, dan O masing-masing adalah 393,5 kj, 85,9 kj, 74,8 kj, dan 0 kj. Tentukan perubahan entalpi pembakaran metana menurut reaksi : C4(g) + O(g) CO(g) + O(l)! Jawab: Catatan : Koefisien reaksi mempengaruhi perhitungan! Δ ο ΣΔ ο f (produk) 1 Δ ο CO Δ ΣΔ ο f (reaktan) ο ο O 1 Δ C Δ 4 = 1 393,5 + ( 85,9) 1 74,8 + ( 0) kj = 890,5 kj. Menggunakan Data Energi Ikatan Tips : KIRI dikurangi KANAN Energi ikatan adalah energi yang diperlukan untuk memutus ikatan kimia dalam 1 mol senyawa dalam fase gas pada keadaan standar menjadi atom-atom gasnya. Energi atomisasi adalah energi yang diperlukan untuk memecah molekul kompleks dalam 1 mol senyawa dalam fase gas pada keadaan standar menjadi atom-atom gasnya. Rumus: Δ Σ energi pemutusan ikatan Σ energi pembentuka n ikatan Contoh soal: Diketahui energi ikatan: DC = C = 145 kkal/mol DC C = 83 kkal/mol D = 104 kkal/mol DC = 99 kkal/mol Tentukan Δ dari reaksi C4(g) + (g) C6(g) Jawab: reaksi C4(g) + (g) C6(g) C = C + C C Δ = {(4 x DC ) + (1 x DC = C) + (1 x D )} {(6 x DC ) + (1 x DC C)} = { (4 x 99) + (1 x 145) + (1 x 104) } { (6 x 99) + (1 x 83) } = ( ) (594+83) = = 3 kkal/mol Pedoman menentukan ikatan kimia: C (karbon) berada di golongan IV A, menerima 4 elektron C C = C = C = ο O (hidrogen) berada di golongan I A, melepas 1 elektron O (oksigen) berada di golongan VI A, menerima elektron O O = N (nitrogen) berada di golongan V A, menerima 3 elektron N N = N F, Cl, Br, I berada di golongan VII A, menerima 1 elektron F Cl Br I Untuk idrokarbon alkana,alkena,alkuna Alkana : Cnn+ C C C Alkena : Cnn C = C C Alkuna : Cnn- C C C 3. Menggunakan ukum ess Germain enri ess (tahun 1840) menyatakan ukum ess atau ukum Penjumlahan Kalor yaitu harga Δ reaksi hanya bergantung pa da keadaan awal dan keadaan akhir reaksi, tidak bergantung pada jalannya reaksi. Tips: - Jika reaksi dikalikan x, maka Δ harus dikali x - Jika reaksi dibalik, tanda Δ harus dibalik Contoh soal: Diketahui reaksi: S(s) + O(g) SO(g) Δ = 300 kj SO(g) + O(g) SO3(g) Δ = 190 kj itunglah Δ reaksi: S(s) + 3 O(g) SO3(g) Jawab: Materi kimia kelas xi semester gasal Page 9
10 S(s) + O(g) SO(g) Δ = 600 kj SO(g) + O(g) SO3(g) Δ = 190 kj S(s) + 3 O(g) SO3(g) Δ = 790 kj Secara grafik/diagram tingkat energi: S + O 1 = + 3 =? 1 = 300 = 1 3 kj/mol SO3 = 300 (+ 95) 3 = + 95 kj/mol = 395 kj/mol SO + ½ O 4. Menggunakan Data Percobaan Alat yang digunakan untuk mengukur kalor reaksi adalah kalorimeter. Langkah-langkah: a. Tentukan reaksinya dan tanda Δ-nya b. itung Δ menggunakan rumus: = Q reaksi = m. c. t jika kalor kalorimeter diabaikan Δ Q reaksi m.c.δtc.δt Ket: Δ m c = perubahan entalpi (kj) = massa zat pereaksi (gram) = kalor jenis zat (J/gK atau J/g C) Δt = perubahan suhu (Kelvin = C + 73) C = kapasitas kalor kalorimeter (J/K atau J/ C) jika kalor kalorimeter diperhitungkan Contoh soal: Sebanyak 50 ml larutan Cl 1 M bersuhu 7 C dicampur dengan 50 ml larutan NaO 1 M yang bersuhu 7 C dalam suatu kalorimeter. Ternyata suhu larutan naik sampai 33,5 C. Jika kalor jenis larutan dianggap sama dengan kalor jenis air yaitu 4,18 J/gK, tentukan perubahan entalpi reaksi tersebut! Penyelesaian: Diket : suhu naik eksoterm Δ = (negatif) m = 50 ml Cl + 50 ml NaO = 100 ml = 100 gram c = 4,18 J/gK Δt = takhir tawal =(33,5+73) (7+73)=306,5 300= 6,5 K Ditanya : Δ...? Jawab: Δ = Qreaksi = (m. c. Δt) = (100. 4,18. 6,5) = 717 J = -,717 Kj UJI KOMPETENSI XI SEMESTER GANJIL TAUN PELAJARAN 015/016 Mata Diklat : Kimia Program Keahlian : TKR,TEI dan TAV Kelas : XI Kompetensi : Termokimia Kerjakan Soal Soal berikut ini! Jawaban dikirim melalui dengan alamat: efaizatun@gmail.com ( bagi siswa yang sedang prakerind ) 1. Apa perbedaan antara sistem tertutup dengan sistem terisolasi!. Bagaimana bunyi ukum Pertama Termodinamika (Azas Kekekalan Energi)! 3. Berapakah kalor yang harus dikeluarkan dari 1 kg air panas, sehingga suhunya turun dari C menjadi 5 0 C? kalor jenis air= 4,18Jg -1 K Kapasitas kalor suatu Kalorimeter adalah 800 jk -1. itung jumlah kalor yang diserap Kalorimeter itu jika suhunya berubah dari 7 0 C menjadi 35 0 C. 5. Manakah diantara yang berikut ini benar untuk reaksi eksoterm? 1. Kalor mengalir dari sistem ke lingkungan.. Entalpi sistem bertambah 3. Berlangsung pada suhu rendah 4. Suhu lingkungan naik 5. Perubahan entalpi reaksi naik. 6. Tuliskanlah persamaan termokimia untuk masing-masing reaksi berikut : Pembakaran 1 mol gas etana membentuk karbon dioksida dan uap air menghasilkan 14 kj. 7. Diketahui persamaan termokimia : Materi kimia kelas xi semester gasal Page 10
11 SO + O SO 3, = -198 kj. Berapakah perubahan entalpi jika SO 3 yang terbentuk sebanyak 0 gram? ( Ar S =3, O=16 ). 8. Jika data : f º CO = kj / mol f º O = kj / mol f º C 6 = kj / mol Tentukan reaksi: C 6 + O CO + O 9. Diketahui Data : S + O SO, = kj SO + O SO 3, = kj Tentukan reaksi: S + 30 SO Diketahui data energi ikat beberapa senyawa sebagai berikut : C = 60 kkal C C = 80 kkal C = C = 15 kkal Cl = 100 kkal C - Cl = 0 kkal Tentukan reaksi: C Cl C 3 7Cl SELAMAT MENGERJAKAN Materi kimia kelas xi semester gasal Page 11
12 4. LAJU REAKSI Standar Kompetensi : Memahami kinetika dan kesetimbangan reaksi kimia serta faktor-faktor yang mempengaruhinya A. Kemolaran Kemolaran (molaritas) dinyatakan dengan lambang M, adalah jumlah mol zat terlarut dalam setiap liter. Larutan. Satuan molaritas adalah mol L -1 Rumus kemolaran : M = n M = V gram Mr V (L) M = M = gr 1000 Mr V ( ml) % 10 Mr ρ = massa jenis larutan Contoh : 1. Sebanyak 1,6 gram NaO (Mr = 40) dilarutkan dalam air, sehingga volume larutan mencapai 00 ml. itung kemolaran larutan yang terjadi! Jawab = M = = gr 1000 Mr V ml 1, = 0, M. Larutan NO3 63 % massa mempunyai masa jenis 1,3 gr/ml, jika Mr NO3 = 63. itung kemolaran larutan tersebut! Jawab = M = = % 10 Mr 63% 1,3 gr ml = 13 M Pengenceran larutan Larutan pekat (mempunyai kemolaran besar) dapat diencerkan dengan menambah volum pelarut sehingga akan diperoleh larutan yang lebih encer (kemolarannya kecil). Pada pengenceran berlaku rumus : V1 = volum sebelum pengenceran M1 = kemolaran sebelum pengenceran V V = volum sesudah pengenceran 1 M 1 = V M M = kemolaran sesudah pengenceran Volum pelarutan = V V1 Pada pengenceran hanya terjadi pertambahan volum, sedang jumlah zat terlatur tetap, maka M < M1. Contoh : Satu ml larutan CI 1 M ditambah air sehingga volum larutan mencapai 100 ml. itung kemolaran larutan CI yang terjadi! B. Faktor yang Mempengaruhi Laju Reaksi 1. Luas bidang sentuh (Sifat / keadaan zat) Reaksi senyawa ion pada umumnya berlangsung lebih cepat daripada reaksi senyawa kovalen. Makin luas permukaan zat, reaksi akan berlangsung lebih cepat. Materi kimia kelas xi semester gasal Page 1
13 . Konsentrasi Makin banyak jumlah molekulnya, reaksi akan berlangsung lebih cepat. 3. Suhu Suhu semakin tinggi akan memperbesar energi kinetik sehingga reaksi berlangsung lebih cepat. 4. Katalis Katalis dapat mempercepat / memperlambat reaksi, tetapi pada akhir reaksi zat ini tidak berubah. Fungsi katalis untuk menurunkan energi aktivasi. Contoh : Data reaksi antara logam zink dengan asam klorida : No. Bentuk Ligam Zn Konsentrasi CI Granula Lempeng Serbuk Granula Serbuk 0,50 M 0,50 M 0,5 M 0,5 M 0,50 M Reaksi yang berlangsung paling cepat terjadi pada percobaan : A. 1 D. 4 B. E. 5 C. 3 Jawab : (E) Laju reaksi dipengaruhi oleh luas permukaan dan konsentrasi. Makin luas permukaan, laju reaksi semakin cepat dan makin besar konsentrasi, laju reaksi juga semakin cepat. Pada percobaan 5, bentuk serbuk luas permukaannya lebih besar dibanding granula atau lempeng dan konsentrasinya besar. C. Persamaan laju reaksi Untuk reaksi = pa + qb rc + s D Persamaan laju reaksinya = v = laju reaksi (M/dt) V=k [ A] m.[b] n m = orde reaksi terhadap A n = orde reaksi terhadap B k = tetapan laju reaksi [ ] = konsentrasi pereaksi pada saat itu (mol/l) atau molar ( M ) Koefisien suhu reaksi Jika suhu naik 10 o C, maka laju reaksi umumnya berlangsung dua kali lebih cepat, maka = Untuk suhu naik (T > T1) 1 t t = n 1 v = n. v1 Untuk suhu turun (T < T1) t = n. v1 1 t T 10 v = n 1 Di mana : n = t = waktu laju reaksi v = laju reaksi Contoh soal. CARA MENGITUNG ORDE REAKSI 1. Data percobaan laju reaksi diperoleh dari reaksi A + B C, sebagai berikut : No. (A) Molar (B) molar Tentukan : 0,01 0,0 0,03 0,04 0,0 0,0 0,0 0,40 Laju reaksi (molar / detik) Materi kimia kelas xi semester gasal Page 13
14 a) Orde reaksi terhadap zat A b) Orde reaksi terhadap zat B c) Rumus laju reaksi d) Orde reaksi / orde reaksi total e) arga k PENYELESAIAN. Setiap kenaikan 10 o C, laju reaksi menjadi kali lebih cepat. Suatu reaksi pada suhu 30 o C lajunya = a. Bila suhu dinaikan menjadi 100 o C. Tentukan laju reaksinya! Jawab : Jika setiap kenaikan suhu 10oC laju reaksi menjadi kali semula, maka V t /10 V = V100 = 10 V1 V100 = 7. V1 = 18 a D. Teori tumbukan Suatu pereaksi dapat berlangsung jika molekul-molekul reaksi saling bertumbukan/bertabrakan. Tumbukan antar molekul pereaksi yang dapat menghasilkan reaksi harus memenuhi syarat : a.memiliki energi aktivasi yang cukup (energi aktivasi / energi pengaktifan ( Ea ) adalah energi minimum yang diperlukan untuk menghasilkan tumbukan efektif agar terjadi reaksi. b. Posisi tumbukan menguntungkan Materi kimia kelas xi semester gasal Page 14
15 UJI KOMPETENSI XI SEMESTER GANJIL TAUN PELAJARAN 015/016 Mata Diklat : Kimia Program Keahlian : TKR,TEI dan TAV Kelas : XI Kompetensi : Laju Reaksi Kerjakan Soal Soal berikut ini! Jawaban dikirim melalui dengan alamat: efaizatun@gmail.com ( bagi siswa yang sedang prakerind ) Soal Uraian: (Berikut untuk soal no 1 dan ): Jelaskan definisi dari: 1. a. Laju reaksi b. Katalisator. a. Orde reaksi b. Energi aktivasi 3. Suatu reaksi: N (g) + 3 (g) N 3(g), tuliskanlah laju reaksi untuk masing-masing pereaksi dan produk. 4. Reaksi : A + B C + D Reaksi diatas berlangsung pada suhu 0 o C dalam waktu 30 menit. Apabila setiap kenaikan suhu 10 o C, laju reaksi menjadi dua kali semula, berapakah waktu yang dibutuhkan untuk berlangsungnya reaksi pada suhu 60 o C? (Berikut adalah soal no 5 s/d 9) Berdasarkan percobaan diperoleh data sebagai berikut: Percobaan [A] awal mol/l [B] awal mol/l Laju Reaksi 1 0, 0, 0,003 0, 0,4 0, ,6 0, 0,009 Tentukan : 5. Orde reaksi terhadap A 6. Orde reaksi terhadap B 7. Orde reaksi total 8. Persamaan laju reaksi 9. Laju reaksi jika konsentrasi [A] dan [B] masing-masing 0,5 M. 10. Sebutkan faktor-faktor yang mempengaruhi laju reaksi Materi kimia kelas xi semester gasal Page 15
16 4.KESETIMBANGAN KIMIA A. Pengertian 1. Reaksi dapat dibalik (revelsibel) Suatu reaksi berlangsung dengan arah berlawanan (zat-zat hasil reaksi dapat bereaksi kembali membentuk zat-zat pereaksi.. Reaksi kesetimbangan Reaksi yang berlangsung dalam dua arah yang berlawanan dengan kecepatan yang sama. 3. Kesetimbangan dinamis Reaksi kesetimbangan yang secara makroskopis (dapat dilihat dan diukur ) tidak terjadi perubahan konsentrasi lagi, tetapi secara mikroskopis (tidak dapat diamati dan diukur) reaksi masih tetap terus. Grafik Kesetimbangan 1. ubungan antara kesetimbangan dengan konsentrasi ( A B ) [ B ] [ C ] [ A ] 0 saat setimbang t (waktu). ubungan antara kesetimbangan dengan konsentrasi ( A B ) V A V V A = V B V B 0 Contoh : t (waktu) Suatu reaksi bolak-balik mencapai kesetimbangan pada saat.... A. Reaksi telah terhenti B. Jumlah pereaksi telah habis C. Laju reaksi ke kanan sama laju reaksi ke kiri D. Jumlah mol rekatan sama jumlah mol produk E. Massa zat reaktan sama massa zat produk Jawab = C Reaksi dikatakan setimbang jika laju reaksi ke kanan sama dengan laju reaksi ke kiri. Pada kesetimbangan : a A b B V V 1 c C d D Saat setimbang : V1 = V k1 [A] a [B] b = k [C] c [D] d B. ukum kesetimbangan Menurut Guldberg & Waage Materi kimia kelas xi semester gasal Page 16
17 Pada sistem kessetimbangan pada suhu tertentu, hasil kali konsentrasi zat-zat reaksi dibagi hasil kali konsentrasi zat-zat pereaksi dan masing-masing konsentrasi dipangkatkan dengan koefisien reaksinya adalah tetap (konstan) Kesetimbangan omogen Pada kesetimbangan : aa(g) + bb(g) cc(g) + dd(g) Jika satuan konsentrasi dalam mol/liter, tetapan kesetimbangannya dinyatakan Kp. Kp c d C D = A a B b Jika satuan konsentrasi dalam tekanan parsial (atmosfer), tetapan kesetimbangan dinyatakan dengan Kp. c d PC PD Kp = a P P b A PA = total ubungan antara Kp dan Kc. Untuk gas berlaku : V nrt n V RT B mol A P mol total n V = konsentrasi Dari persamaan Kc dan Kp di atas, maka : Kp = KC. (RT) n R = tetapan gas = 0,08 liter atm/mol K T = suhu Kelvin = (73 + t) o C n = (c + d) (a + b) Jika n = 0, maka Kp = Kc Contoh : Dalam ruang 5 liter direaksikan 0,5 mol gas N dengan 0,4 mol gas O sesuai reaksi : N(g) + O(g) NO(g) setelah tercapai kesetimbangan, terbentuk 0, mol gas NO. itung harga Kc dan Kp. Jawab : N(g) + O(g) NO(g) Mula-mula = 0,5 0,4 Bereaksi = 0,1 0,1 0, Setimbang = 0,4 0,3 0, Kc = NO N O 0, 5 0,04 1 0,4 0,3 0,1 3 Dari persamaan reaksi n = (1 + 1) = = 0 Maka harga Kp = Kc 5 5 Kp = 3 1 C. Kesetimbangan eterogen Kesetimbangan heterogen adalah kesetimbangan di mana fase zat-zatnya terdiri dari fasa atau lebih. Contoh : C(s) + O(g) CO(g) + (g) NaCO3(s) NaCO3(s) + CO(g) + O(g) Pada suhu tertentu konsentrasi zat padat murni atau cairan murni adalah konstan. Pada kesetimbangan : C(s) + O(g) CO(g) + (g) Materi kimia kelas xi semester gasal Page 17
18 Kc CO = C O Kc[C] CO = O Kc CO = O Kp = P CO P P O Untuk kesetimbangan heterogen, tidak terdapat konsentrasi zat padat dan pencairan pada tatapan kesetimbangannya. Contoh : Jika natrium bikarbonat dipanaskan menurut reaksi = NaCO3(s) NaCO3(s) + CO(g) + O(g) Ternyata tekanan total saat setimbang = 0,04 atm, hitung harga Kp. Jawab = Reaksi setimbang = NaCO3(s) NaCO3(s) + CO(g) + O(g) Yang berfasa gas = CO dan O Berdasarkan persamaan reaksi = mol CO = mol O mol zat P mol total Maka : P CO = P O = total = 1 x 0,04 atm = 0,0 atm Kp = PCO x P O konstan = (0,0 x 0,0) atm = 4 x 10-4 atm D. Pergeseran Kesetimbangan Asas Le Chatelier Jika sistem kesetimbangan diadakan suatu aksi, maka sistem akan berubah sedemikian sehingga pengaruh aksi sekecil mungkin Jika konsentrasi ditambah dari dikurangi reaksi bergeser ke arah zat itu Faktor-faktor yang mempengaruhi kesetimbangan dinaikkan Jika suhu diturunkan diperbesar Jika volume diperkecil endoterm reaksi bergeser kearah eksoterm diperkecil = tekanan diperbesar reaksi menuju ke arah koefisien besar koefisien kecil jika koefisien reaksi kanan = koefisien reaksi kiri, maka perubahan volume atau tekanan tidak mempengaruhi kesetimbangan Materi kimia kelas xi semester gasal Page 18
19 Katalis tidak mempengaruhi kesetimbangan, hanya mempercepat tercapainya kesetimbangan Contoh = Pada sistem kesetimbangan = NO3(g) NO(g) + NO(g), = + 39,7 kj. Ramalkan ke mana arah pergeseran kesetimbangan jika : a. Konsentrasi NO ditambah b. Suhu dinaikkan c. Volume container diperkecil pada suhu tetap Jawab = a. Berdasarkan asas Le Chatelier. Jika konsentrasi NO ditambah, maka kesetimbangan akan bergeser ke arah pengurangan NO, yaitu ke kiri. b. Jika suhu dinaikkan, kesetimbangan akan bergeser ke arah reaksi endotermis, yaitu ke kanan. c. Jika volume diperkecil, kesetimbangan bergeser ke jumlah mol (koefisien) yang kecil, yaitu ke kiri. E. Kesetimbangan dalam Industri 1. Proses aber Bosch (pembuatan amoniak) N(g) + (g) N3(g), = - kkal. Berdasarkan asas Le Chatelier agar kesetimbangan bergeser ke kanan maka proses dilakukan pada tekanan tinggi dan suhu yang rendah. Kenyataannya, untuk memperoleh hasil yang optimum (hasil banyak, berlangsung cepat dan ekonomis), dilakukan pada tekanan tinggi atm dan pada suhu cukup tinggi o C, hasil yang diperoleh + 30%.. Proses kontak (pembuatan SO4) SO(g) + O(g) SO3(g), = -45 kkal. asil optimum diperoleh jika dilakukan pada tekanan yang tidak terlalu tinggi dan suhu o C. UJI KOMPETENSI XI SEMESTER GANJIL TAUN PELAJARAN 015/016 Mata Diklat : Kimia Program Keahlian : TKR,TEI dan TAV Kelas : XI Kompetensi : Kesetimbangan Kerjakan Soal Soal berikut ini! Jawaban dikirim melalui dengan alamat: efaizatun@gmail.com ( bagi siswa yang sedang prakerind ) Kerjakan soal uraian no 1 s/d no 10 berikut dengan jelas! 1. a. Apakah yang dimaksud dengan kesetimbangan bersifat dinamis? b. Jelaskan fungsi katalisator terhadap kesetimbangan reaksi? (Berikut adalah soal no dan 3) Tuliskan rumus kesetimbangan dari reaksi-reaksi berikut:. a. SO (g) + O (g) SO 3(g) b. PCl 5(g) PCl 3(g) + Cl (g) 3. 5a. FeO (s) + CO (g) Fe (s) + CO (g) b. N O (g) +N 4(g) 3N (g) + O (g) Materi kimia kelas xi semester gasal Page 19
20 4. Pada kesetimbangan berikut: SO (g) + O (g) SO 3(g) =-45 kkal. Kemanakah reaksi akan bergeser jika: a. Tekanan diperbesar b. Suhu diturunkan c. Konsentrasi O diperbesar b. Konsentrasi SO 3 diperbesar 5. Pada suhu tertentu, dalam bejana 1 liter direaksikan 1 mol zat A dan 1 mol zat B sehingga tercapai kesetimbangan: A (g) + B (g) C (g) + D (g) Setelah tercapai kesetimbangan ternyata terbentuk 0,5 mol C. Tentukan konstanta kesetimbangan! 6.arga Kp untuk reaksi kesetimbangan: X (g) 3Y (g) Pada suhu tertentu adalah 1/8. Jika dalam kesetimbangan tekanan parsial X adalah 8 atm, maka tentukan tekanan parsial parsial Y! 7.Satu mol A dan satu mol B direaksikan sampai tercapai kesetimbangan menurut reaksi: A (g) + B (g) C (g) + D (g) Pada kesetimbangan diperoleh zat sebanyak 0,33 mol. Tentukan tetapan kesetimbangannya! 8.Pada suhu tertentu dalam bejana 10 liter terjadi kesetimbangan berikut: SO 3(g) SO (g) + O (g) Jika 80 gram SO 3 (Ar S=3, O=16) dipanaskan pada suhu tertentu hingga tercapai kesetimbangan dan didapatkan perbandingan mol SO 3 : O = :, hitunglah tetapan kesetimbangan reaksi tersebut! 9.Diketahui kesetimbangan: PCl 5(g) PCl 3(g) + Cl (g) Pada suhu 50OC, Kp=1,78 (R=0,08 L atm/ o K mol) maka hitunglah harga KC! Kebumen, 14 Juli 016 Guru Mapel Kimia XI Eti Faizatun M, S.Pd Materi kimia kelas xi semester gasal Page 0
1. Perhatikan struktur senyawa berikut!
 . Perhatikan struktur senyawa berikut! CH CH CH CH CH CH CH Jumlah atom C primer, atom C sekunder, dan atom C tersier dari senyawa di atas adalah...,, dan D.,, dan,, dan E.,, dan,, dan. Di bawah ini merupakan
. Perhatikan struktur senyawa berikut! CH CH CH CH CH CH CH Jumlah atom C primer, atom C sekunder, dan atom C tersier dari senyawa di atas adalah...,, dan D.,, dan,, dan E.,, dan,, dan. Di bawah ini merupakan
FAKULTAS TEKNIK UNIVERSITAS NEGERI YOGYAKARTA BAHAN AJAR KIMIA DASAR BAB VII KIMIA ORGANIK
 BAAN AJAR KIMIA DASAR No. BAK/TBB/SBG201 Revisi : 00 Tgl. 01 Mei 2008 al 1 dari 19 BAB VII KIMIA ORGANIK Dari 109 unsur yang ada di alam ini, karbon mempunyai sifat-sifat istimewa : 1. Karbon dapat membentuk
BAAN AJAR KIMIA DASAR No. BAK/TBB/SBG201 Revisi : 00 Tgl. 01 Mei 2008 al 1 dari 19 BAB VII KIMIA ORGANIK Dari 109 unsur yang ada di alam ini, karbon mempunyai sifat-sifat istimewa : 1. Karbon dapat membentuk
BAB IX SENYAWA HIDROKARBON ALKANA, ALKENA, ALKUNA
 BAB IX SENYAWA IDROKARBON ALKANA, ALKENA, ALKUNA BAB IX SENYAWA IDROKARBON ALKANA, ALKENA, ALKUNA Standar Kompetensi : Menggolongkan senyawa hidrokarbon berdasarkan strukturnya dan mendeskripsikan proses
BAB IX SENYAWA IDROKARBON ALKANA, ALKENA, ALKUNA BAB IX SENYAWA IDROKARBON ALKANA, ALKENA, ALKUNA Standar Kompetensi : Menggolongkan senyawa hidrokarbon berdasarkan strukturnya dan mendeskripsikan proses
ALKANA 04/03/2013. Sifat-sifat fisik alkana. Alkana : 1. Oksidasi dan pembakaran
 ALKANA Sifat-sifat fisik alkana Alkana : senyawa hidrokarbon jenuh (ikatan tunggal), atom C : hibridisasi sp 3 rumus molekul : C n H 2n+2 struktur : alifatik (rantai lurus) dan siklik (sikloalkana) Tidak
ALKANA Sifat-sifat fisik alkana Alkana : senyawa hidrokarbon jenuh (ikatan tunggal), atom C : hibridisasi sp 3 rumus molekul : C n H 2n+2 struktur : alifatik (rantai lurus) dan siklik (sikloalkana) Tidak
1. Salah satu faktor yang menyebabkan senyawa karbon banyak jumlahnya adalah...
 1. Salah satu faktor yang menyebabkan senyawa karbon banyak jumlahnya adalah... A. Karbon melimpah di kulit bumi B. Karbon memiliki 4 elektron valensi C. Dapat membentuk rantai atom karbon D. Titik didih
1. Salah satu faktor yang menyebabkan senyawa karbon banyak jumlahnya adalah... A. Karbon melimpah di kulit bumi B. Karbon memiliki 4 elektron valensi C. Dapat membentuk rantai atom karbon D. Titik didih
Addres: Fb: Khayasar ALKANA. Rumus umum alkana: C n H 2n + 2. R (alkil) = C n H 2n + 1
 ALKANA Rumus umum alkana: C n H 2n + 2 R (alkil) = C n H 2n + 1 Alkana Adalah rantai karbon yang memiliki ikatan tunggal (jenuh) A. Alkana 1. Alkana disebut juga senyawa hidrokarbon jenuh (senyawa parafin).
ALKANA Rumus umum alkana: C n H 2n + 2 R (alkil) = C n H 2n + 1 Alkana Adalah rantai karbon yang memiliki ikatan tunggal (jenuh) A. Alkana 1. Alkana disebut juga senyawa hidrokarbon jenuh (senyawa parafin).
PENGANTAR. Kekhasan atom Karbon Perbedaan Rantai Karbon Perbedaan Atom Karbon. Hidrokarbon EVALUASI PENUTUP. Created By EXIT
 Loading. 5 4 3 2 1 : : Atom C mempunyai nomor atom 6 memiliki konfigurasi elektron : K L C (z=6) : 2 4 maka elektron valensinya = 4 Atom C dapat mengikat 4 atom yang lain dan dapat mengikat 4 atom C yang
Loading. 5 4 3 2 1 : : Atom C mempunyai nomor atom 6 memiliki konfigurasi elektron : K L C (z=6) : 2 4 maka elektron valensinya = 4 Atom C dapat mengikat 4 atom yang lain dan dapat mengikat 4 atom C yang
berupa ikatan tunggal, rangkap dua atau rangkap tiga. o Atom karbon mempunyai kemampuan membentuk rantai (ikatan yang panjang).
 HIDROKARBON Senyawa hidrokarbon merupakan senyawa karbon yang paling sederhana. Dari namanya, senyawa hidrokarbon adalah senyawa karbon yang hanya tersusun dari atom hidrogen dan atom karbon. Dalam kehidupan
HIDROKARBON Senyawa hidrokarbon merupakan senyawa karbon yang paling sederhana. Dari namanya, senyawa hidrokarbon adalah senyawa karbon yang hanya tersusun dari atom hidrogen dan atom karbon. Dalam kehidupan
kimia HIDROKARBON 1 Tujuan Pembelajaran
 K-13 kimia K e l a s XI IDROKARBON 1 Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami kekhasan atom karbon dan karakteristik atom karbon dalam
K-13 kimia K e l a s XI IDROKARBON 1 Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami kekhasan atom karbon dan karakteristik atom karbon dalam
kimia HIDROKARBON III DAN REVIEW Tujuan Pembelajaran
 K-13 kimia K e l a s XI HIDROKARBON III DAN REVIEW Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut 1 Memahami definisi dan jenis-jenis isomer beserta contohnya
K-13 kimia K e l a s XI HIDROKARBON III DAN REVIEW Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut 1 Memahami definisi dan jenis-jenis isomer beserta contohnya
Keunikan atom C?? Atom karbon primer, sekunder, tersier dan kuartener
 Keunikan atom C?? Atom karbon primer, sekunder, tersier dan kuartener Jenis ikatan karbon edakan : Propena (tak jenuh) Propuna (tak jenuh) Propana (jenuh) Rantai Atom Karbon Bedakan : 2-metil butana siklobutana
Keunikan atom C?? Atom karbon primer, sekunder, tersier dan kuartener Jenis ikatan karbon edakan : Propena (tak jenuh) Propuna (tak jenuh) Propana (jenuh) Rantai Atom Karbon Bedakan : 2-metil butana siklobutana
BAB 9 HIDROKARBON. Gambar 9.1 Asam askorbat Sumber: Kimia Dasar Konsep-konsep Inti
 BAB 9 HIDROKARBON Gambar 9.1 Asam askorbat Sumber: Kimia Dasar Konsep-konsep Inti Pada pelajaran bab kesembilan ini akan dipelajari tentang kekhasan atom karbon, identitifikasi senyawa karbon, alkana,
BAB 9 HIDROKARBON Gambar 9.1 Asam askorbat Sumber: Kimia Dasar Konsep-konsep Inti Pada pelajaran bab kesembilan ini akan dipelajari tentang kekhasan atom karbon, identitifikasi senyawa karbon, alkana,
HIDROKARBON DAN KEGUNAANNYA
 Modul 3. 10. IDROKARBON DAN KEGUNAANNYA Standar Kompetensi Mengkomunikasikan Senyawa idrokarbon dan Kegunaannya Kompetensi Dasar 1. Mendeskripsikan kekhasan atom karbon yang membentuk senyawa hidrokarbon
Modul 3. 10. IDROKARBON DAN KEGUNAANNYA Standar Kompetensi Mengkomunikasikan Senyawa idrokarbon dan Kegunaannya Kompetensi Dasar 1. Mendeskripsikan kekhasan atom karbon yang membentuk senyawa hidrokarbon
BAB IX SENYAWA HIDROKARBON ALKANA, ALKENA, ALKUNA
 BAB IX SENYAWA IDROKARBON ALKANA, ALKENA, ALKUNA Standar Kompetensi : Menggolongkan senyawa hidrokarbon berdasarkan strukturnya dan mendeskripsikan proses pembentukan dan teknik penyulingan minyak bumi
BAB IX SENYAWA IDROKARBON ALKANA, ALKENA, ALKUNA Standar Kompetensi : Menggolongkan senyawa hidrokarbon berdasarkan strukturnya dan mendeskripsikan proses pembentukan dan teknik penyulingan minyak bumi
SOAL UJIAN AKHIR SEMESTER 2 KIMIA KELAS X (SEPULUH) TP. 2008/2009
 SOAL UJIAN AKHIR SEMESTER 2 KIMIA KELAS X (SEPULUH) TP. 2008/2009 1. Dari suatu percobaan daya hantar listrik suatu larutan diperoleh data sebagai berikut: Percobaan Larutan Lampu Gelembung gas 1 2 3 4
SOAL UJIAN AKHIR SEMESTER 2 KIMIA KELAS X (SEPULUH) TP. 2008/2009 1. Dari suatu percobaan daya hantar listrik suatu larutan diperoleh data sebagai berikut: Percobaan Larutan Lampu Gelembung gas 1 2 3 4
A. Pembentukan dan Komposisi Minyak Bumi
 A. Pembentukan dan Komposisi Minyak Bumi Istilah minyak bumi diterjemahkan dari bahasa latin (petroleum), artinya petrol (batuan) dan oleum (minyak). Nama petroleum diberikan kepada fosil hewan dan tumbuhan
A. Pembentukan dan Komposisi Minyak Bumi Istilah minyak bumi diterjemahkan dari bahasa latin (petroleum), artinya petrol (batuan) dan oleum (minyak). Nama petroleum diberikan kepada fosil hewan dan tumbuhan
Senyawa Hidrokarbon. Linda Windia Sundarti
 Senyawa Hidrokarbon Senyawa Hidrokarbon adalah senyawa yang mengandung hanya karbon dan hidrogen C + H Carbon sebagai unsur pokok memiliki keistimewaan sbb : 1. Dengan ev = 4 membentuk 4 ikatan kovalen
Senyawa Hidrokarbon Senyawa Hidrokarbon adalah senyawa yang mengandung hanya karbon dan hidrogen C + H Carbon sebagai unsur pokok memiliki keistimewaan sbb : 1. Dengan ev = 4 membentuk 4 ikatan kovalen
MODUL 1 TERMOKIMIA. A. Hukum Pertama Termodinamika. B. Kalor Reaksi
 MODUL 1 TERMOKIMIA Termokimia adalah ilmu yang mempelajari hubungan antara energi panas dan energi kimia. Sebagai prasyarat untuk mempelajari termokimia, kita harus mengetahui tentang perbedaan kalor (Q)
MODUL 1 TERMOKIMIA Termokimia adalah ilmu yang mempelajari hubungan antara energi panas dan energi kimia. Sebagai prasyarat untuk mempelajari termokimia, kita harus mengetahui tentang perbedaan kalor (Q)
BAB 7 HIDROKARBON DAN MINYAK BUMI
 BAB 7 HIDROKARBON DAN MINYAK BUMI A. Kekhasan / Keunikan Atom Karbon o Terletak pada golongan IVA dengan Z = 6 dan mempunyai 4 elektron valensi. o Untuk mencapai konfigurasi oktet maka atom karbon mempunyai
BAB 7 HIDROKARBON DAN MINYAK BUMI A. Kekhasan / Keunikan Atom Karbon o Terletak pada golongan IVA dengan Z = 6 dan mempunyai 4 elektron valensi. o Untuk mencapai konfigurasi oktet maka atom karbon mempunyai
LEMBARAN SOAL 6. Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH )
 LEMBARAN SOAL 6 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah soal dengan
LEMBARAN SOAL 6 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah soal dengan
K13 Revisi Antiremed Kelas 11 Kimia
 K13 Revisi Antiremed Kelas 11 Kimia Persiapan UTS Semester Ganjil Doc. Name: RK13AR11KIM01UTS Doc. Version: 2016-10 halaman 1 01. Sebenarnya kimia organik dan anorganik tidaklah perlu dipisah-pisahkan,
K13 Revisi Antiremed Kelas 11 Kimia Persiapan UTS Semester Ganjil Doc. Name: RK13AR11KIM01UTS Doc. Version: 2016-10 halaman 1 01. Sebenarnya kimia organik dan anorganik tidaklah perlu dipisah-pisahkan,
MODUL KIMIA SMA IPA Kelas 11
 SMA IPA Kelas 11 A. Senyawa Karbon Hidrokarbon termasuk senyawa organik yang hanya terdiri atas unsur karbon (C) dan hidrogen (H). Contohnya adalah metana (CH 4), etena (C 2H 4), dan asetilena (C 2H 2).
SMA IPA Kelas 11 A. Senyawa Karbon Hidrokarbon termasuk senyawa organik yang hanya terdiri atas unsur karbon (C) dan hidrogen (H). Contohnya adalah metana (CH 4), etena (C 2H 4), dan asetilena (C 2H 2).
LKS HIDROKARBON. Nama : Kelas/No.Abs :
 Nama : Kelas/No.Abs : LKS HIDROKARBON 1. Kekhasan / Keunikan Atom Karbon 1. Terletak pada golongan IVA dengan Z = 6 dan mempunyai 4 elektron valensi. 2. Untuk mencapai konfigurasi oktet maka atom karbon
Nama : Kelas/No.Abs : LKS HIDROKARBON 1. Kekhasan / Keunikan Atom Karbon 1. Terletak pada golongan IVA dengan Z = 6 dan mempunyai 4 elektron valensi. 2. Untuk mencapai konfigurasi oktet maka atom karbon
kimia MINYAK BUMI Tujuan Pembelajaran
 K-13 kimia K e l a s XI MINYAK BUMI Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami definisi dan pembentukan minyak bumi. 2. Memahami fraksi-fraksi
K-13 kimia K e l a s XI MINYAK BUMI Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami definisi dan pembentukan minyak bumi. 2. Memahami fraksi-fraksi
Atom unsur karbon dengan nomor atom Z = 6 terletak pada golongan IVA dan periode-2 konfigurasi elektronnya 1s 2 2s 2 2p 2.
 SENYAWA ORGANIK A. Sifat khas atom karbon Atom unsur karbon dengan nomor atom Z = 6 terletak pada golongan IVA dan periode-2 konfigurasi elektronnya 1s 2 2s 2 2p 2. Atom karbon mempunyai 4 elektron valensi,
SENYAWA ORGANIK A. Sifat khas atom karbon Atom unsur karbon dengan nomor atom Z = 6 terletak pada golongan IVA dan periode-2 konfigurasi elektronnya 1s 2 2s 2 2p 2. Atom karbon mempunyai 4 elektron valensi,
OAL TES SEMESTER I. I. Pilihlah jawaban yang paling tepat! a. 2d d. 3p b. 2p e. 3s c. 3d 6. Unsur X dengan nomor atom
 KIMIA XI SMA 3 S OAL TES SEMESTER I I. Pilihlah jawaban yang paling tepat!. Elektron dengan bilangan kuantum yang tidak diizinkan n = 3, l = 0, m = 0, s = - / n = 3, l =, m =, s = / c. n = 3, l =, m =
KIMIA XI SMA 3 S OAL TES SEMESTER I I. Pilihlah jawaban yang paling tepat!. Elektron dengan bilangan kuantum yang tidak diizinkan n = 3, l = 0, m = 0, s = - / n = 3, l =, m =, s = / c. n = 3, l =, m =
KESETIMBANGAN KIMIA SOAL DAN PEMBAHASAN
 KESETIMBANGAN KIMIA SOAL DAN PEMBAHASAN 1. Suatu reaksi dikatakan mencapai kesetimbangan apabila. A. laju reaksi ke kiri sama dengan ke kanan B. jumlah koefisien reaksi ruas kiri sama dengan ruas kanan
KESETIMBANGAN KIMIA SOAL DAN PEMBAHASAN 1. Suatu reaksi dikatakan mencapai kesetimbangan apabila. A. laju reaksi ke kiri sama dengan ke kanan B. jumlah koefisien reaksi ruas kiri sama dengan ruas kanan
KIMIA 2 KELAS X. D. molekul-molekul kovalen yang bereaksi dengan air E. molekul-molekul kovalen yang bergerak bebas di dalam air
 KIMIA 2 KELAS X PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah soal dengan teliti sebelum Anda bekerja 3. Kerjakanlah soal anda pada lembar jawaban
KIMIA 2 KELAS X PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah soal dengan teliti sebelum Anda bekerja 3. Kerjakanlah soal anda pada lembar jawaban
Kesetimbangan Kimia. Bab 4
 Kesetimbangan Kimia Bab 4 Standar Kompetensi 3. Memahami kinetika reaksi, kesetimbangan kimia, dan faktor-faktor yang memengaruhinya, serta penerapannya dalam kehidupan sehari-hari dan industri Kompetensi
Kesetimbangan Kimia Bab 4 Standar Kompetensi 3. Memahami kinetika reaksi, kesetimbangan kimia, dan faktor-faktor yang memengaruhinya, serta penerapannya dalam kehidupan sehari-hari dan industri Kompetensi
OAL TES SEMESTER II. I. Pilihlah jawaban yang paling tepat!
 176 KIMIA X SMA S AL TES SEMESTER II I. Pilihlah jawaban yang paling tepat! 1. Suatu zat padat dilarutkan dalam air, ternyata larutannya dapat menghantarkan arus listrik. Pernyataan yang benar tentang
176 KIMIA X SMA S AL TES SEMESTER II I. Pilihlah jawaban yang paling tepat! 1. Suatu zat padat dilarutkan dalam air, ternyata larutannya dapat menghantarkan arus listrik. Pernyataan yang benar tentang
RENCANA PELAKSANAAN PEMBELAJARAN
 RENCANA PELAKSANAAN PEMBELAJARAN Satuan Pelajaran : SMA Kelas/Semester : X/2 Mata Pelajaran Materi Pokok Sub Materi Pokok Alokasi Waktu : Kimia : Hidrokarbon : Minyak Bumi : 2 x 45 menit Standar Kompetensi
RENCANA PELAKSANAAN PEMBELAJARAN Satuan Pelajaran : SMA Kelas/Semester : X/2 Mata Pelajaran Materi Pokok Sub Materi Pokok Alokasi Waktu : Kimia : Hidrokarbon : Minyak Bumi : 2 x 45 menit Standar Kompetensi
TUGAS KELOMPOK BAB TERAKHIR KIMIA MENGENAI ALKANA. kelompok II x5
 TUGAS KELOMPOK BAB TERAKHIR KIMIA MENGENAI ALKANA kelompok II x5 DI SUSUN OLEH: ARIEF NURRAHMAN FARID SUHADA GERRY REGUS M. HANIEF IQBAL S. ILHAM SYAHBANI ALKANA ALKANA adalah Hidrokarbon jenuh yang paling
TUGAS KELOMPOK BAB TERAKHIR KIMIA MENGENAI ALKANA kelompok II x5 DI SUSUN OLEH: ARIEF NURRAHMAN FARID SUHADA GERRY REGUS M. HANIEF IQBAL S. ILHAM SYAHBANI ALKANA ALKANA adalah Hidrokarbon jenuh yang paling
H = H hasil reaksi H pereaksi. Larutan HCl
 Standar Kompetensi Kompetensi Dasar Memahami perubahan energi dalam kimia, cara pengukuran dan sifat ketidakteraturan dalam alam semesta. Menjelaskan pengertian tentang entalpi suatu zat dan perubahannya.
Standar Kompetensi Kompetensi Dasar Memahami perubahan energi dalam kimia, cara pengukuran dan sifat ketidakteraturan dalam alam semesta. Menjelaskan pengertian tentang entalpi suatu zat dan perubahannya.
kimia K-13 HIDROKARBON II K e l a s A. Alkena Tujuan Pembelajaran
 K-13 kimia K e l a s XI HIDROKARBON II Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut 1 Memahami pengertian, rumus umum, serta tata nama senyawa hidrokarbon
K-13 kimia K e l a s XI HIDROKARBON II Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut 1 Memahami pengertian, rumus umum, serta tata nama senyawa hidrokarbon
APAKAH LUMPUR DI SIDOARJO MENGANDUNG SENYAWA HIDROKARBON?
 APAKAH LUMPUR DI SIDOARJO MENGANDUNG SENYAWA HIDROKARBON? Oleh: Didi S. Agustawijaya dan Feny Andriani Bapel BPLS I. Umum Hidrokarbon adalah sebuah senyawa yang terdiri dari unsur karbon (C) dan hidrogen
APAKAH LUMPUR DI SIDOARJO MENGANDUNG SENYAWA HIDROKARBON? Oleh: Didi S. Agustawijaya dan Feny Andriani Bapel BPLS I. Umum Hidrokarbon adalah sebuah senyawa yang terdiri dari unsur karbon (C) dan hidrogen
a. Ion c. Molekul senyawa e. Campuran b. Molekul unsur d. Unsur a. Air c. Kuningan e. Perunggu b. Gula d. Besi
 A. PILIHAN GANDA 1. Molekul oksigen atau O2 merupakan lambang dari partikel a. Ion c. Molekul senyawa e. Campuran b. Molekul unsur d. Unsur 2. Di antara zat berikut yang merupakan unsur ialah... a. Air
A. PILIHAN GANDA 1. Molekul oksigen atau O2 merupakan lambang dari partikel a. Ion c. Molekul senyawa e. Campuran b. Molekul unsur d. Unsur 2. Di antara zat berikut yang merupakan unsur ialah... a. Air
K13 Revisi Antiremed Kelas 11 Kimia
 K1 Revisi Antiremed Kelas 11 Kimia Hidrokarbon - Soal Doc Name: RK1AR11KIM0101 Version: 016-10 halaman 1 01 Untuk mengenali adanya senyawa karbon dalam suatu bahan dapat dilakukan dengan cara membakar
K1 Revisi Antiremed Kelas 11 Kimia Hidrokarbon - Soal Doc Name: RK1AR11KIM0101 Version: 016-10 halaman 1 01 Untuk mengenali adanya senyawa karbon dalam suatu bahan dapat dilakukan dengan cara membakar
BAB 1 1. Atom karbon mempunyai ke khasan. Pernyataan yang tepat mengenai kekhasan atom karbon
 SOAL DAN PEMBAHASAN KIMIA KELAS XI SEMESTER 1 BAB 1 1. Atom karbon mempunyai ke khasan. Pernyataan yang tepat mengenai kekhasan atom karbon adalah A. Karbon mempunyai 4 elektron valensi yang mampu membentuk
SOAL DAN PEMBAHASAN KIMIA KELAS XI SEMESTER 1 BAB 1 1. Atom karbon mempunyai ke khasan. Pernyataan yang tepat mengenai kekhasan atom karbon adalah A. Karbon mempunyai 4 elektron valensi yang mampu membentuk
1. Perbedaan Senyawa Organik Dan Senyawa Anorganik
 Salah satu sumber daya alam yang tidak asing lagi adalah minyak bumi. Bahan alam ini amat mempengaruhi kehidupan. Ummat manusia masih menggantungkan sebagian besar aktivitas kehidupannya pada bahan alam
Salah satu sumber daya alam yang tidak asing lagi adalah minyak bumi. Bahan alam ini amat mempengaruhi kehidupan. Ummat manusia masih menggantungkan sebagian besar aktivitas kehidupannya pada bahan alam
SOAL KIMIA 2 KELAS : XI IPA
 SOAL KIMIA KELAS : XI IPA PETUNJUK UMUM. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan. Periksa dan bacalah soal dengan teliti sebelum Anda bekerja. Kerjakanlah soal anda pada lembar jawaban
SOAL KIMIA KELAS : XI IPA PETUNJUK UMUM. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan. Periksa dan bacalah soal dengan teliti sebelum Anda bekerja. Kerjakanlah soal anda pada lembar jawaban
LATIHAN ULANGAN KIMIA : HIDROKARBON KELAS X
 LATIHAN ULANGAN KIMIA : HIDROKARBON KELAS X Pilihlah salah satu jawaban yang paling tepat! 1. Alkana yang tidak mengandung lima atom karbon yaitu.... a. n-pentena b. 2-metil-butana c. isopentana d. 2-metil-pentana
LATIHAN ULANGAN KIMIA : HIDROKARBON KELAS X Pilihlah salah satu jawaban yang paling tepat! 1. Alkana yang tidak mengandung lima atom karbon yaitu.... a. n-pentena b. 2-metil-butana c. isopentana d. 2-metil-pentana
Alkena dan Alkuna. Pertemuan 4
 Alkena dan Alkuna Pertemuan 4 Alkena/Olefin hidrokarbon alifatik tak jenuh yang memiliki satu ikatan rangkap (C = C) Senyawa yang mempunyai dua ikatan rangkap: alkadiena tiga ikatan rangkap: alkatriena,
Alkena dan Alkuna Pertemuan 4 Alkena/Olefin hidrokarbon alifatik tak jenuh yang memiliki satu ikatan rangkap (C = C) Senyawa yang mempunyai dua ikatan rangkap: alkadiena tiga ikatan rangkap: alkatriena,
Kesetimbangan Kimia KIM 2 A. PENDAHULUAN B. REAKSI KESETIMBANGAN. α = KESETIMBANGAN KIMIA. materi78.co.nr. setimbang
 konsentrasi laju reaksi materi78.co.nr Kesetimbangan Kimia A. PENDAHULUAN Reaksi satu arah (irreversible) atau reaksi tidak dapat balik adalah reaksi yang terjadi pada satu arah, dan produknya tidak dapat
konsentrasi laju reaksi materi78.co.nr Kesetimbangan Kimia A. PENDAHULUAN Reaksi satu arah (irreversible) atau reaksi tidak dapat balik adalah reaksi yang terjadi pada satu arah, dan produknya tidak dapat
Pelatihan Online I OSN Bidang Kimia Page 1 PETUNJUK PENGERJAAN SOAL
 PETUNJUK PENGERJAAN SOAL 1. Periksalah terlebih dahulu soal yang Anda terima, apakah dalam keadaan baik, terbaca, lengkap, dan jelas, sebelum Anda mengerjakan. 2. Jawaban dikerjakan pada lembar jawaban
PETUNJUK PENGERJAAN SOAL 1. Periksalah terlebih dahulu soal yang Anda terima, apakah dalam keadaan baik, terbaca, lengkap, dan jelas, sebelum Anda mengerjakan. 2. Jawaban dikerjakan pada lembar jawaban
Senyawa Alkohol dan Senyawa Eter. Sulistyani, M.Si
 Senyawa Alkohol dan Senyawa Eter Sulistyani, M.Si sulistyani@uny.ac.id Konsep Dasar Senyawa Organik Senyawa organik adalah senyawa yang sumber utamanya berasal dari tumbuhan, hewan, atau sisa-sisa organisme
Senyawa Alkohol dan Senyawa Eter Sulistyani, M.Si sulistyani@uny.ac.id Konsep Dasar Senyawa Organik Senyawa organik adalah senyawa yang sumber utamanya berasal dari tumbuhan, hewan, atau sisa-sisa organisme
PAKET UJIAN NASIONAL 14 Pelajaran : KIMIA Waktu : 120 Menit
 PAKET UJIAN NASINAL 14 Pelajaran : KIMIA Waktu : 120 Menit Pilihlah salah satu jawaban yang tepat! Jangan lupa Berdoa dan memulai dari yang mudah. 1. Diketahui ion X 3+ mempunyai 10 elektron dan 14 neutron.
PAKET UJIAN NASINAL 14 Pelajaran : KIMIA Waktu : 120 Menit Pilihlah salah satu jawaban yang tepat! Jangan lupa Berdoa dan memulai dari yang mudah. 1. Diketahui ion X 3+ mempunyai 10 elektron dan 14 neutron.
Siswa diingatkan tentang struktur atom, bilangan kuantum, bentuk-bentuk orbital, dan konfigurasi elektron
 RENCANA PELAKSANAAN PEMBELAJARAN NO: 1 Mata Pelajaran : Kimia Kelas/Semester : XI/1 Materi Pokok : Stuktur atom dan sistem periodik unsur Pertemuan Ke- : 1 dan 2 Alokasi Waktu : 2 x pertemuan (4 x 45 menit)
RENCANA PELAKSANAAN PEMBELAJARAN NO: 1 Mata Pelajaran : Kimia Kelas/Semester : XI/1 Materi Pokok : Stuktur atom dan sistem periodik unsur Pertemuan Ke- : 1 dan 2 Alokasi Waktu : 2 x pertemuan (4 x 45 menit)
Bab 12 Pengenalan Kimia Organik
 Bab 12 Pengenalan Kimia Organik Sikloalkana Ikhtisar Sumber: hang Bab 11 Alkuna idrokarbon Aromatik Gugus Fungsi Departemen Kimia FMIPA IPB Kimia Organik berfokus pada kimia karbon. Beberapa karakteristik
Bab 12 Pengenalan Kimia Organik Sikloalkana Ikhtisar Sumber: hang Bab 11 Alkuna idrokarbon Aromatik Gugus Fungsi Departemen Kimia FMIPA IPB Kimia Organik berfokus pada kimia karbon. Beberapa karakteristik
LEMBAR KERJA SISWA Nama Siswa : Kelas/Semester : X/2 : Penggolongan hidrokarbon dan Tata nama senyawa alkana, alkena, dan alkuna.
 LEMBAR KERJA SISWA Nama Siswa : Kelas/Semester : X/2 Materi : Penggolongan hidrokarbon dan Tata nama senyawa alkana, alkena, dan alkuna. SENYAWA IDROKARBON Senyawa hidrokarbon adalah senyawa-senyawa karbon
LEMBAR KERJA SISWA Nama Siswa : Kelas/Semester : X/2 Materi : Penggolongan hidrokarbon dan Tata nama senyawa alkana, alkena, dan alkuna. SENYAWA IDROKARBON Senyawa hidrokarbon adalah senyawa-senyawa karbon
PAKET UJIAN NASIONAL 17 Pelajaran : KIMIA Waktu : 120 Menit
 PAKET UJIAN NASIONAL 17 Pelajaran : KIMIA Waktu : 120 Menit Pilihlah salah satu jawaban yang tepat! Jangan lupa Berdoa dan memulai dari yang mudah. 01. Diketahui ion X 3+ mempunyai 10 elektron dan 14 neutron.
PAKET UJIAN NASIONAL 17 Pelajaran : KIMIA Waktu : 120 Menit Pilihlah salah satu jawaban yang tepat! Jangan lupa Berdoa dan memulai dari yang mudah. 01. Diketahui ion X 3+ mempunyai 10 elektron dan 14 neutron.
Materi Penunjang Media Pembelajaran Kimia Organik SMA ALKANA
 ALKANA Alkana rantai pendek (metana dan etana) terdapat dalam atmosfer beberapa planet seperti jupiter, saturnus, uranus, dan neptunus. Bahkan di titan (satelit saturnus) terdapat danau metana/etana yang
ALKANA Alkana rantai pendek (metana dan etana) terdapat dalam atmosfer beberapa planet seperti jupiter, saturnus, uranus, dan neptunus. Bahkan di titan (satelit saturnus) terdapat danau metana/etana yang
 TRY OUT SELEKSI OLIMPIADE TINGKAT KABUPATEN/KOTA 2010 TIM OLIMPIADE KIMIA INDONESIA 2011 Waktu: 150 Menit PUSAT KLINIK PENDIDIKAN INDONESIA (PKPI) bekerjasama dengan LEMBAGA BIMBINGAN BELAJAR SSCIntersolusi
TRY OUT SELEKSI OLIMPIADE TINGKAT KABUPATEN/KOTA 2010 TIM OLIMPIADE KIMIA INDONESIA 2011 Waktu: 150 Menit PUSAT KLINIK PENDIDIKAN INDONESIA (PKPI) bekerjasama dengan LEMBAGA BIMBINGAN BELAJAR SSCIntersolusi
LEMBARAN SOAL 5. Pilih satu jawaban yang benar!
 LEMBARAN SOAL 5 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah
LEMBARAN SOAL 5 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah
Waktu (t) Gambar 3.1 Grafik hubungan perubahan konsentrasi terhadap waktu
 3 LAJU REAKSI Setelah mempelajari bab ini, kamu diharapkan mampu: Menghitung konsentrasi larutan (molaritas larutan). Menganalisis faktor-faktor yang mempengaruhi laju reaksi (konsentrasi, luas permukaan,
3 LAJU REAKSI Setelah mempelajari bab ini, kamu diharapkan mampu: Menghitung konsentrasi larutan (molaritas larutan). Menganalisis faktor-faktor yang mempengaruhi laju reaksi (konsentrasi, luas permukaan,
HIDROKARBON A. PENGERTIAN SENYAWA KARBON B. HIDROKARBON
 7 HIDROKARBON A. PENGERTIAN SENYAWA KARBON B. HIDROKARBON Apabila kita membakar kayu, maka akan didapat suatu zat berwarna hitam yang kita sebut arang. Arang yang dihasilkan dari peristiwa pembakaran adalah
7 HIDROKARBON A. PENGERTIAN SENYAWA KARBON B. HIDROKARBON Apabila kita membakar kayu, maka akan didapat suatu zat berwarna hitam yang kita sebut arang. Arang yang dihasilkan dari peristiwa pembakaran adalah
HIDROKARBON DAN MINYAK BUMI
 BAB VII HIDROKARBON DAN MINYAK BUMI Kimia adalah ilmu yang mempelajari susunan, struktur, sifat dan perubahan materi serta energi yang menyertai perubahan tersebut. A. HIDROKARBON Atom karbon merupakan
BAB VII HIDROKARBON DAN MINYAK BUMI Kimia adalah ilmu yang mempelajari susunan, struktur, sifat dan perubahan materi serta energi yang menyertai perubahan tersebut. A. HIDROKARBON Atom karbon merupakan
Kesetimbangan dinamis adalah keadaan dimana dua proses yang berlawanan terjadi dengan laju yang sama, akibatnya tidak terjadi perubahan bersih dalam
 Kesetimbangan dinamis adalah keadaan dimana dua proses yang berlawanan terjadi dengan laju yang sama, akibatnya tidak terjadi perubahan bersih dalam sistem pada kesetimbangan Uap mengembun dengan laju
Kesetimbangan dinamis adalah keadaan dimana dua proses yang berlawanan terjadi dengan laju yang sama, akibatnya tidak terjadi perubahan bersih dalam sistem pada kesetimbangan Uap mengembun dengan laju
Kimia Dasar II / Kimia Organik. Shinta Rosalia D. (SRD) Angga Dheta S. (ADS) Sudarma Dita W. (SDW) Nur Lailatul R. (NLR) Feronika Heppy S (FHS)
 Kimia Dasar II / Kimia Organik Shinta Rosalia D. (SRD) Angga Dheta S. (ADS) Sudarma Dita W. (SDW) Nur Lailatul R. (NLR) Feronika Heppy S (FHS) Kontrak perkuliahan : 1. Ujian : 50% 2. Tugas : 10% 3. Kuis
Kimia Dasar II / Kimia Organik Shinta Rosalia D. (SRD) Angga Dheta S. (ADS) Sudarma Dita W. (SDW) Nur Lailatul R. (NLR) Feronika Heppy S (FHS) Kontrak perkuliahan : 1. Ujian : 50% 2. Tugas : 10% 3. Kuis
OLIMPIADE KIMIA INDONESIA
 OLIMPIADE KIMIA INDONESIA OLIMPIADE SAINS NASIONAL SELEKSI KABUPATEN / KOTA UjianTeori Waktu 2 Jam Departemen Pendidikan Nasional Direktorat Jenderal Managemen Pendidikan Dasar dan Menengah Direktorat
OLIMPIADE KIMIA INDONESIA OLIMPIADE SAINS NASIONAL SELEKSI KABUPATEN / KOTA UjianTeori Waktu 2 Jam Departemen Pendidikan Nasional Direktorat Jenderal Managemen Pendidikan Dasar dan Menengah Direktorat
STOIKIOMETRI I. HUKUM DASAR ILMU KIMIA
 STOIKIOMETRI I. HUKUM DASAR ILMU KIMIA a. Hukum Kekekalan Massa (Hukum Lavoisier) Massa zat sebelum dan sesudah reaksi adalah sama. Contoh: S + O 2 SO 2 2 gr 32 gr 64 gr b. Hukum Perbandingan Tetap (Hukum
STOIKIOMETRI I. HUKUM DASAR ILMU KIMIA a. Hukum Kekekalan Massa (Hukum Lavoisier) Massa zat sebelum dan sesudah reaksi adalah sama. Contoh: S + O 2 SO 2 2 gr 32 gr 64 gr b. Hukum Perbandingan Tetap (Hukum
kimia KTSP & K-13 TERMOKIMIA I K e l a s A. HUKUM KEKEKALAN ENERGI TUJUAN PEMBELAJARAN
 KTSP & K-13 kimia K e l a s XI TERMOKIMIA I TUJUAN PEMBELAJARAN Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Menjelaskan hukum kekekalan energi, membedakan sistem dan
KTSP & K-13 kimia K e l a s XI TERMOKIMIA I TUJUAN PEMBELAJARAN Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Menjelaskan hukum kekekalan energi, membedakan sistem dan
BAB VIII SENYAWA ORGANIK
 BAB VIII SENYAWA ORGANIK Standar Kompetensi : Memahami senyawa organik dan mikromolekul, menentukan hasil reaksi dan mensintesa serta kegunaannya. Sebagian besar zat yang ada di sekitar kita merupakan
BAB VIII SENYAWA ORGANIK Standar Kompetensi : Memahami senyawa organik dan mikromolekul, menentukan hasil reaksi dan mensintesa serta kegunaannya. Sebagian besar zat yang ada di sekitar kita merupakan
Termodinamika dan Kesetimbangan Kimia
 Termodinamika dan Kesetimbangan Kimia Dalam kesetimbangan kimia terdapat 2 reaksi yaitu reaksi irreversible dan reaksi reversible. Reaksi irreversible (reaksi searah) adalah reaksi yang berlangsung searah.
Termodinamika dan Kesetimbangan Kimia Dalam kesetimbangan kimia terdapat 2 reaksi yaitu reaksi irreversible dan reaksi reversible. Reaksi irreversible (reaksi searah) adalah reaksi yang berlangsung searah.
Bab 10 MINYAK BUMI. A. Komponen Minyak Bumi
 Bab 10 MINYAK BUMI A. Komponen Minyak Bumi Minyak bumi dalam kehidupan sehari-hari memegang peranan yang strategis, mulai kegiatan memasak, bahan kendaraan bermotor, tenaga listrik sampai pada bahan dasar
Bab 10 MINYAK BUMI A. Komponen Minyak Bumi Minyak bumi dalam kehidupan sehari-hari memegang peranan yang strategis, mulai kegiatan memasak, bahan kendaraan bermotor, tenaga listrik sampai pada bahan dasar
LEMBARAN SOAL 10. Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH) Pilihlah jawaban yang paling tepat.
 LEMBARAN SOAL 10 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan. Periksa dan bacalah soal dengan
LEMBARAN SOAL 10 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan. Periksa dan bacalah soal dengan
Disampaikan oleh : Dr. Sri Handayani 2013
 Disampaikan oleh : Dr. Sri Handayani 2013 PENGERTIAN Termokimia adalah cabang dari ilmu kimia yang mempelajari hubungan antara reaksi dengan panas. HAL-HAL YANG DIPELAJARI Perubahan energi yang menyertai
Disampaikan oleh : Dr. Sri Handayani 2013 PENGERTIAN Termokimia adalah cabang dari ilmu kimia yang mempelajari hubungan antara reaksi dengan panas. HAL-HAL YANG DIPELAJARI Perubahan energi yang menyertai
BAB 6. (lihat diktat kuliah KIMIA : Bab 6 dan 7)
 BAB 6 (lihat diktat kuliah KIMIA : Bab 6 dan 7) KONSEP KESETIMBANGAN KIMIA 1. HUKUM KEKEKALAN ENERGI 2. PENGERTIAN KERJA DAN KALOR 3. PENGERTIAN SISTEM, LINGKUNGAN, DAN FUNGSI KEADAAN 4. HUKUM PERTAMA
BAB 6 (lihat diktat kuliah KIMIA : Bab 6 dan 7) KONSEP KESETIMBANGAN KIMIA 1. HUKUM KEKEKALAN ENERGI 2. PENGERTIAN KERJA DAN KALOR 3. PENGERTIAN SISTEM, LINGKUNGAN, DAN FUNGSI KEADAAN 4. HUKUM PERTAMA
A. KESEIMBANGAN DINAMIS
 1 Tugas Kimia IV Prakerin KESEIMBANGAN KIMIA Coba kamu perhatikan proses pendidihan air dengan panci tertutup. Pada waktu air menguap, uap air akan tertahan dalam tutup panci. Selanjutnya, uap air akan
1 Tugas Kimia IV Prakerin KESEIMBANGAN KIMIA Coba kamu perhatikan proses pendidihan air dengan panci tertutup. Pada waktu air menguap, uap air akan tertahan dalam tutup panci. Selanjutnya, uap air akan
UJIAN NASIONAL TAHUN PELAJARAN 2007/2008
 UJIAN NASIONAL TAHUN PELAJARAN 2007/2008 PANDUAN MATERI SMA DAN MA K I M I A PROGRAM STUDI IPA PUSAT PENILAIAN PENDIDIKAN BALITBANG DEPDIKNAS KATA PENGANTAR Dalam rangka sosialisasi kebijakan dan persiapan
UJIAN NASIONAL TAHUN PELAJARAN 2007/2008 PANDUAN MATERI SMA DAN MA K I M I A PROGRAM STUDI IPA PUSAT PENILAIAN PENDIDIKAN BALITBANG DEPDIKNAS KATA PENGANTAR Dalam rangka sosialisasi kebijakan dan persiapan
PENGANTAR. Konsep Dasar Kimia untuk PGSD 203
 PENGANTAR Materi termasuk zat yang telah dibahas pada BBM terdahulu, kebanyakan berkaitan dengan unsur dan senyawa anorganik. Golongan senyawa lainnya adalah senyawa organik. Dalam kehidupan, justeru golongan
PENGANTAR Materi termasuk zat yang telah dibahas pada BBM terdahulu, kebanyakan berkaitan dengan unsur dan senyawa anorganik. Golongan senyawa lainnya adalah senyawa organik. Dalam kehidupan, justeru golongan
SOAL-SOAL KESETIMBANGAN KIMIA
 H=+380 kj/mol SOAL-SOAL KESETIMBANGAN KIMIA 1. Ebtanas 99 Suatu reaksi berada dalam keadaan setimbang apabila A. Reaksi ke kanan dan kiri telah berhenti B. Mol pereaksi selalu sama dengan mol hasil reaksi
H=+380 kj/mol SOAL-SOAL KESETIMBANGAN KIMIA 1. Ebtanas 99 Suatu reaksi berada dalam keadaan setimbang apabila A. Reaksi ke kanan dan kiri telah berhenti B. Mol pereaksi selalu sama dengan mol hasil reaksi
1. Isilah Biodata anda dengan lengkap (di lembar Jawaban) Tulis dengan huruf cetak dan jangan disingkat!
 Petunjuk : 1. Isilah Biodata anda dengan lengkap (di lembar Jawaban) Tulis dengan huruf cetak dan jangan disingkat! 2. Soal Teori ini terdiri dari dua bagian: A. 30 soal pilihan Ganda : 60 poin B. 5 Nomor
Petunjuk : 1. Isilah Biodata anda dengan lengkap (di lembar Jawaban) Tulis dengan huruf cetak dan jangan disingkat! 2. Soal Teori ini terdiri dari dua bagian: A. 30 soal pilihan Ganda : 60 poin B. 5 Nomor
Penggolongan hidrokarbon
 Penggolongan hidrokarbon idrokarbon Alifatik Alisiklik Aromatik Jenuh Tidak jenuh Jenuh Tidak jenuh Alkana Sikloalkana Sikloalkena Alkena Alkuna Sifat Fisika Alkana yang memiliki massa molekul rendah yaitu
Penggolongan hidrokarbon idrokarbon Alifatik Alisiklik Aromatik Jenuh Tidak jenuh Jenuh Tidak jenuh Alkana Sikloalkana Sikloalkena Alkena Alkuna Sifat Fisika Alkana yang memiliki massa molekul rendah yaitu
Wardaya College. Tes Simulasi Ujian Nasional SMA Berbasis Komputer. Mata Pelajaran Kimia Tahun Ajaran 2017/2018. Departemen Kimia - Wardaya College
 Tes Simulasi Ujian Nasional SMA Berbasis Komputer Mata Pelajaran Kimia Tahun Ajaran 2017/2018-1. Sebuah unsur X memiliki no massa 52 dan jumlah neutron sebesar 28. Kongurasi elektron dari ion X + adalah...
Tes Simulasi Ujian Nasional SMA Berbasis Komputer Mata Pelajaran Kimia Tahun Ajaran 2017/2018-1. Sebuah unsur X memiliki no massa 52 dan jumlah neutron sebesar 28. Kongurasi elektron dari ion X + adalah...
KIMIA ORGANIK. = Kimia Senyawa Karbon. Kajian Struktur, Sifat, & Reaksi. Ikatan Kovalen : Rumus Kimia : CH 3 C : H = 1 : 3
 KIMIA ORGANIK? = Kimia Senyawa Karbon Kajian Struktur, Sifat, & Reaksi Ikatan Kovalen : Penggunaan sepasang elektron antara dua atom Rumus Kimia : Rumus Empirik : Menggambarkan Jenis atom dan perbandingannya
KIMIA ORGANIK? = Kimia Senyawa Karbon Kajian Struktur, Sifat, & Reaksi Ikatan Kovalen : Penggunaan sepasang elektron antara dua atom Rumus Kimia : Rumus Empirik : Menggambarkan Jenis atom dan perbandingannya
kimia KESETIMBANGAN KIMIA 2 Tujuan Pembelajaran
 KTSP & K-13 kimia K e l a s XI KESETIMBANGAN KIMIA 2 Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami faktor-faktor yang memengaruhi kesetimbangan.
KTSP & K-13 kimia K e l a s XI KESETIMBANGAN KIMIA 2 Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami faktor-faktor yang memengaruhi kesetimbangan.
Sebutkan data pada kalor yang diserap atau dikeluarkan pada sistem reaksi!
 contoh soal termokimia dan pembahasannya 1. Apa yang dimaksud dengan energi kinetik dan energi potensial? Jawab : Energi kinetik adalah energi yang terkandung di dalam materi yang bergerak, sedangkan energi
contoh soal termokimia dan pembahasannya 1. Apa yang dimaksud dengan energi kinetik dan energi potensial? Jawab : Energi kinetik adalah energi yang terkandung di dalam materi yang bergerak, sedangkan energi
OLIMPIADE SAINS NASIONAL 2012 SELEKSI KABUPATEN / KOTA SOAL. UjianTeori. Waktu: 100 menit
 OLIMPIADE SAINS NASIONAL 2012 SELEKSI KABUPATEN / KOTA SOAL UjianTeori Waktu: 100 menit Kementerian Pendidikan dan Kebudayaan Direktorat Jenderal Pendidikan Menengah Direktorat Pembinaan Sekolah Menengah
OLIMPIADE SAINS NASIONAL 2012 SELEKSI KABUPATEN / KOTA SOAL UjianTeori Waktu: 100 menit Kementerian Pendidikan dan Kebudayaan Direktorat Jenderal Pendidikan Menengah Direktorat Pembinaan Sekolah Menengah
Kesetimbangan Kimia. Chapter 9 P N2 O 4. Kesetimbangan akan. Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi
 Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi Kesetimbangan adalah suatu keadaan di mana tidak ada perubahan yang terlihat seiring berjalannya waktu. Kesetimbangan kimia
Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi Kesetimbangan adalah suatu keadaan di mana tidak ada perubahan yang terlihat seiring berjalannya waktu. Kesetimbangan kimia
RINGKASAN MATERI DAN LEMBAR KEGIATAN SISWA (LKS) TATA NAMA SENYAWA HIDROKARBON (ALKANA, ALKENA, DAN ALKUNA)
 RINGKASAN MATERI DAN LEMBAR KEGIATAN SISWA (LKS) TATA NAMA SENYAWA HIDROKARBON (ALKANA, ALKENA, DAN ALKUNA) Kompetensi Dasar 3.1 Menganalisis struktur dan sifat senyawa hidrokarbon berdasarkan pemahaman
RINGKASAN MATERI DAN LEMBAR KEGIATAN SISWA (LKS) TATA NAMA SENYAWA HIDROKARBON (ALKANA, ALKENA, DAN ALKUNA) Kompetensi Dasar 3.1 Menganalisis struktur dan sifat senyawa hidrokarbon berdasarkan pemahaman
1s 2 2s 2 2p 6 3s 2 2p 6 3d 4s 1 4p 4d 4f 5s 5p 5d 5f
 NO SOAL PEMBAHASAN 1 Konfigurasi elekttron ion X - yang memiliki nomor massa 39 dan 21 neutron adalah.. A. 1s2 2s2 2p6 3s2 3p6 4s2 3d1 B. 1s2 2s2 2p6 3s2 3p6 4s1 C. 1s2 2s2 2p6 3s2 3p6 3d1 D. 1s2 2s2 2p6
NO SOAL PEMBAHASAN 1 Konfigurasi elekttron ion X - yang memiliki nomor massa 39 dan 21 neutron adalah.. A. 1s2 2s2 2p6 3s2 3p6 4s2 3d1 B. 1s2 2s2 2p6 3s2 3p6 4s1 C. 1s2 2s2 2p6 3s2 3p6 3d1 D. 1s2 2s2 2p6
H 2 O (l) H 2 O (g) Kesetimbangan kimia. N 2 O 4 (g) 2NO 2 (g)
 Purwanti Widhy H Kesetimbangan adalah suatu keadaan di mana tidak ada perubahan yang terlihat seiring berjalannya waktu. Kesetimbangan kimia tercapai jika: Laju reaksi maju dan laju reaksi balik sama besar
Purwanti Widhy H Kesetimbangan adalah suatu keadaan di mana tidak ada perubahan yang terlihat seiring berjalannya waktu. Kesetimbangan kimia tercapai jika: Laju reaksi maju dan laju reaksi balik sama besar
MODUL KESETIMBANGAN. Perhatikan reaksi berikut
 MODUL KESETIMBANGAN Perhatikan reaksi berikut a.n 2 (g) + 3H 2 (g) 2NH 3 (g), di sebut juga reaksi... b. N 2 (g) + 3H 2 (g) 2NH 3 (g), di sebut juga reaksi... Perhatikan reaksi: Maka persamaan laju reaksi
MODUL KESETIMBANGAN Perhatikan reaksi berikut a.n 2 (g) + 3H 2 (g) 2NH 3 (g), di sebut juga reaksi... b. N 2 (g) + 3H 2 (g) 2NH 3 (g), di sebut juga reaksi... Perhatikan reaksi: Maka persamaan laju reaksi
2. Konfigurasi elektron dua buah unsur tidak sebenarnya:
 . Atom X memiliki elektron valensi dengan bilangan kuantum: n =, l =, m = 0, dan s =. Periode dan golongan yang mungkin untuk atom X adalah A. dan IIIB B. dan VA C. 4 dan III B D. 4 dan V B E. 5 dan III
. Atom X memiliki elektron valensi dengan bilangan kuantum: n =, l =, m = 0, dan s =. Periode dan golongan yang mungkin untuk atom X adalah A. dan IIIB B. dan VA C. 4 dan III B D. 4 dan V B E. 5 dan III
BAB VI KINETIKA REAKSI KIMIA
 BANK SOAL SELEKSI MASUK PERGURUAN TINGGI BIDANG KIMIA 1 BAB VI 1. Padatan NH 4 NO 3 diaduk hingga larut selama 77 detik dalam akuades 100 ml sesuai persamaan reaksi berikut: NH 4 NO 2 (s) + H 2 O (l) NH
BANK SOAL SELEKSI MASUK PERGURUAN TINGGI BIDANG KIMIA 1 BAB VI 1. Padatan NH 4 NO 3 diaduk hingga larut selama 77 detik dalam akuades 100 ml sesuai persamaan reaksi berikut: NH 4 NO 2 (s) + H 2 O (l) NH
HIDROKARBON DAN POLIMER
 HIDROKARBON DAN POLIMER Hidrokarbon Senyawa karbon disebut senyawa organik karena pada mulanya senyawa-senyawa tersebut hanya dapat dihasilkan oleh organisme Senyawa lain yang tidak berasal dari makhluk
HIDROKARBON DAN POLIMER Hidrokarbon Senyawa karbon disebut senyawa organik karena pada mulanya senyawa-senyawa tersebut hanya dapat dihasilkan oleh organisme Senyawa lain yang tidak berasal dari makhluk
OLIMPIADE KIMIA INDONESIA
 OLIMPIADE KIMIA INDONESIA OLIMPIADE SAINS NASIONAL SELEKSI KABUPATEN / KOTA UjianTeori Waktu 2 Jam Departemen Pendidikan Nasional Direktorat Jenderal Managemen Pendidikan Dasar dan Menengah Direktorat
OLIMPIADE KIMIA INDONESIA OLIMPIADE SAINS NASIONAL SELEKSI KABUPATEN / KOTA UjianTeori Waktu 2 Jam Departemen Pendidikan Nasional Direktorat Jenderal Managemen Pendidikan Dasar dan Menengah Direktorat
BAB III KESETIMBANGAN KIMIA. AH = 92 kj
 BAB III KESETIMBANGAN KIMIA Amonia (NH 3 ) merupakan salah satu zat kimia yang paling banyak diproduksi. Amonia digunakan terutama untuk membuat pupuk, yaitu urea dan ZA. Penggunaan amonia yang lain, yaitu
BAB III KESETIMBANGAN KIMIA Amonia (NH 3 ) merupakan salah satu zat kimia yang paling banyak diproduksi. Amonia digunakan terutama untuk membuat pupuk, yaitu urea dan ZA. Penggunaan amonia yang lain, yaitu
RENCANA PELAKSANAAN PEMBELAJARAN (RPP)
 1 No. Dokumen : F/751/WKS1/P/5 No. Revisi : 1 Tanggal Berlaku : 1 Juli 2016 RENCANA PELAKSANAAN PEMBELAJARAN (RPP) Satuan Pendidikan : SMA Negeri 1 Godean Mata Pelajaran : Kimia Kelas/Semester : XI/ Gasal
1 No. Dokumen : F/751/WKS1/P/5 No. Revisi : 1 Tanggal Berlaku : 1 Juli 2016 RENCANA PELAKSANAAN PEMBELAJARAN (RPP) Satuan Pendidikan : SMA Negeri 1 Godean Mata Pelajaran : Kimia Kelas/Semester : XI/ Gasal
H 2 O (L) H 2 O (G) KESETIMBANGAN KIMIA. N 2 O 4 (G) 2NO 2 (G)
 H 2 O (L) H 2 O (G) KESETIMBANGAN KIMIA. N 2 O 4 (G) 2NO 2 (G) Purwanti Widhy H Kesetimbangan adalah suatu keadaan di mana tidak ada perubahan yang terlihat seiring berjalannya waktu. Kesetimbangan kimia
H 2 O (L) H 2 O (G) KESETIMBANGAN KIMIA. N 2 O 4 (G) 2NO 2 (G) Purwanti Widhy H Kesetimbangan adalah suatu keadaan di mana tidak ada perubahan yang terlihat seiring berjalannya waktu. Kesetimbangan kimia
Analisis Keterkaitan KI - KD dengan IPK dan Materi Pembelajaran. Kompetensi Inti Kompetensi Dasar Indikator Pencapaian Kompetensi
 No. Dokumen : F/751/WKS1/P/6 No. Revisi : 1 Tanggal Berlaku : 1 Juli 2016 Analisis Keterkaitan KI - KD dengan IPK dan Sekolah : SMA NEGERI 1 GODEAN Mata Pelajaran : Kimia Kelas / Program : XI/MIPA Semester
No. Dokumen : F/751/WKS1/P/6 No. Revisi : 1 Tanggal Berlaku : 1 Juli 2016 Analisis Keterkaitan KI - KD dengan IPK dan Sekolah : SMA NEGERI 1 GODEAN Mata Pelajaran : Kimia Kelas / Program : XI/MIPA Semester
Kesetimbangan Kimia. Tim Dosen Kimia Dasar FTP
 Kesetimbangan Kimia Tim Dosen Kimia Dasar FTP Pengertian kesetimbangan kimia Suatu sistem dikatakan setimbang jika dua proses yang berlawanan terjadi dengan laju yang sama atau dengan kata lain tidak terjadi
Kesetimbangan Kimia Tim Dosen Kimia Dasar FTP Pengertian kesetimbangan kimia Suatu sistem dikatakan setimbang jika dua proses yang berlawanan terjadi dengan laju yang sama atau dengan kata lain tidak terjadi
BAB IV TERMOKIMIA A. PENGERTIAN KALOR REAKSI
 BAB IV TERMOKIMIA A. Standar Kompetensi: Memahami tentang ilmu kimia dan dasar-dasarnya serta mampu menerapkannya dalam kehidupan se-hari-hari terutama yang berhubungan langsung dengan kehidupan. B. Kompetensi
BAB IV TERMOKIMIA A. Standar Kompetensi: Memahami tentang ilmu kimia dan dasar-dasarnya serta mampu menerapkannya dalam kehidupan se-hari-hari terutama yang berhubungan langsung dengan kehidupan. B. Kompetensi
KATA PENGANTAR. Puji syukur kami ucapkan kehadirat Tuhan Yang Maha Esa, karena. dengan rahmat dan karunia-nya kami masih diberi kesempatan untuk
 KATA PENGANTAR Puji syukur kami ucapkan kehadirat Tuhan Yang Maha Esa, karena dengan rahmat dan karunia-nya kami masih diberi kesempatan untuk menyelesaikan makalah ini. Tidak lupa kami ucapkan kepada
KATA PENGANTAR Puji syukur kami ucapkan kehadirat Tuhan Yang Maha Esa, karena dengan rahmat dan karunia-nya kami masih diberi kesempatan untuk menyelesaikan makalah ini. Tidak lupa kami ucapkan kepada
LEMBARAN SOAL 7. Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA )
 LEMBARAN SOAL 7 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA ) PETUNJUK UMUM. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan. Periksa dan bacalah soal
LEMBARAN SOAL 7 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA ) PETUNJUK UMUM. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan. Periksa dan bacalah soal
RENCANA PELAKSANAAN PEMBELAJARAN (RPP)
 1 No. Dokumen : F/751/WKS1/P/5 No. Revisi : 1 Tanggal Berlaku : 1 Juli 2016 RENCANA PELAKSANAAN PEMBELAJARAN (RPP) Satuan Pendidikan : SMA Negeri 1 Godean Mata Pelajaran : Kimia Kelas/Semester : XI/ Gasal
1 No. Dokumen : F/751/WKS1/P/5 No. Revisi : 1 Tanggal Berlaku : 1 Juli 2016 RENCANA PELAKSANAAN PEMBELAJARAN (RPP) Satuan Pendidikan : SMA Negeri 1 Godean Mata Pelajaran : Kimia Kelas/Semester : XI/ Gasal
SOAL SELEKSI OLIMPIADE SAINS TINGKAT KABUPATEN/KOTA 2004 CALON TIM OLIMPIADE KIMIA INDONESIA
 SOAL SELEKSI OLIMPIADE SAINS TINGKAT KABUPATEN/KOTA 2004 CALON TIM OLIMPIADE KIMIA INDONESIA 2005 Bidang Kimia KEMENTERIAN PENDIDIKAN DAN KEBUDAYAAN DIREKTORAT JENDERAL PENDIDIKAN MENENGAH DIREKTORAT PEMBINAAN
SOAL SELEKSI OLIMPIADE SAINS TINGKAT KABUPATEN/KOTA 2004 CALON TIM OLIMPIADE KIMIA INDONESIA 2005 Bidang Kimia KEMENTERIAN PENDIDIKAN DAN KEBUDAYAAN DIREKTORAT JENDERAL PENDIDIKAN MENENGAH DIREKTORAT PEMBINAAN
TERMOKIMIA. Sistem terbagi atas: 1. Sistem tersekat: Antara sistem dan lingkungan tidak dapat terjadi pertukaran energi maupun materi
 TERMOKIMIA almair amrulloh 12:04:00 AM 11 IPAKimia 11 IPA Asas kekekalan energi menyatakan bahwa energi tidak dapat diciptakan atau dimusnahkan, tetapi energi dapat diubah dari satu bentuk kebentuk lain
TERMOKIMIA almair amrulloh 12:04:00 AM 11 IPAKimia 11 IPA Asas kekekalan energi menyatakan bahwa energi tidak dapat diciptakan atau dimusnahkan, tetapi energi dapat diubah dari satu bentuk kebentuk lain
LEMBAR AKTIVITAS SISWA ( LAS )_ 1
 LEMBAR AKTIVITAS SISWA ( LAS )_ 1 1. Perhatikan reaksi berikut: CaCO 2 (s) CaO (s) + CO 2 (g) H = 178 KJ/mol. Jelaskan! a. Arah kesetimbangan ditambahkan CaCO 2 (s) b. Tiga kemungkinan yang dapat dilakukan
LEMBAR AKTIVITAS SISWA ( LAS )_ 1 1. Perhatikan reaksi berikut: CaCO 2 (s) CaO (s) + CO 2 (g) H = 178 KJ/mol. Jelaskan! a. Arah kesetimbangan ditambahkan CaCO 2 (s) b. Tiga kemungkinan yang dapat dilakukan
D. H 2 S 2 O E. H 2 S 2 O 7
 1. Jika gas belerang dioksida dialirkan ke dalam larutan hidrogen sulfida, maka zat terakhir ini akan teroksidasi menjadi... A. S B. H 2 SO 3 C. H 2 SO 4 D. H 2 S 2 O E. H 2 S 2 O 7 Reaksi yang terjadi
1. Jika gas belerang dioksida dialirkan ke dalam larutan hidrogen sulfida, maka zat terakhir ini akan teroksidasi menjadi... A. S B. H 2 SO 3 C. H 2 SO 4 D. H 2 S 2 O E. H 2 S 2 O 7 Reaksi yang terjadi
