Bab VIII Reaksi Penetralan dan Titrasi Asam-Basa
|
|
|
- Deddy Sanjaya
- 7 tahun lalu
- Tontonan:
Transkripsi
1 Bab VIII Reaksi Penetralan dan Titrasi Asam-Basa Sumber: James Mapple, Chemistry an Enquiry-Based Approach Pengukuran ph selama titrasi akan lebih akurat dengan menggunakan alat ph-meter. TUJUAN PEMBELAJARAN Setelah mengikuti pembelajaran siswa dapat : 1. menjelaskan reaksi penetralan, 2. melakukan percobaan titrasi asam-basa dengan teliti, 3. menjelaskan pengertian titrasi asam-basa, titik akhir titrasi, dan titik ekivalen, 4. menggambarkan grafik titrasi asam-basa, 5. menghitung banyaknya pereaksi dan hasil reaksi dari titrasi asam-basa. Reaksi Reaksi Penetralan dan dan Titrasi Asam-Basa 187
2 PETA KONSEP Titrasi Asam Basa digunakan pada dapat menggambarkan Reaksi Penetralan Grafik Titrasi dibantu oleh Indikator Asam Basa bergantung pada Kekuatan Asam Basa digunakan untuk menentukan Titik Ekivalen untuk menunjukkan Titik Akhir Titrasi untuk menghitung Konsentrasi Asam Basa 188 Kimia Kelas XI SMA dan MA
3 Pernahkah kamu makan obat maag? Obat maag atau antacid dimakan untuk mengurangi keasaman pada lambung karena obat maag mengandung basa. Tanah pertanian yang bersifat asam biasanya diberi kapur agar keasamannya berkurang sehingga phnya cocok untuk tanaman yang akan ditanam. Proses ini disebut reaksi penetralan. Di laboratorium reaksi penetralan dapat dilakukan dengan cara titrasi asam-basa. Melalui titrasi juga dapat dihitung banyaknya pereaksi dan hasil reaksi dalam larutan. Bagaimana cara melalukan titrasi, alat-alat apa yang digunakan, titrasi asambasa apa saja yang dapat dilakukan? Pada bab ini akan diuraikan tentang reaksi penetralan, titrasi asam-basa, grafik-grafik titrasi asam-basa, dan perhitungan konsentrasi larutan melalui titrasi atau data hasil titrasi. A. Reaksi Penetralan Reaki penetralan termasuk reaksi pada larutan elektrolit yaitu reaksi antara asam dengan basa sampai terjadi suasana netral. Bagaimana terjadinya penetralan pada larutan asam dan basa? Coba perhatikan gambar pada saat larutan asam klorida direaksikan dengan larutan natrium hidroksida. larutan asam H + (aq) Cl (aq) larutan basa Na + (aq) OH (aq) HCl(aq) + NaOH(aq) NaCl(aq) + H 2 O(l) asam basa garam air Pada reaksi antara asam dan basa, ion hidrogen, H + (aq) dan ion hidroksida, OH (aq) bergabung membentuk molekul air yang bersifat netral. H + (aq) + OH (aq) H 2 O(l) Ion Na + (aq) dan ion Cl (aq) tetap di Na + (aq) dalam larutan NaCl. Jika diuapkan akan Cl (aq) dihasilkan NaCl padat atau garam dapur. H 2 O(l) Jika jumlah mol ion H + dari asam sama dengan jumlah mol ion OH dari basa Sumber: Michael Lewis, Thinking Chemistry maka hasil reaksi akan bersifat netral. Gambar 8.1 Reaksi HCl dengan NaOH Reaksi tersebut dinamakan reaksi penetralan. Contoh reaksi penetralan yang lain yaitu: HCl(aq) + KOH(aq) KCl(aq) + H 2 O(l) CH 3 COOH(aq) + NaOH(aq) CH 3 COONa(aq) + H 2 O(l) Latihan 8.1 Tulis persamaan reaksi penetralan pada zat-zat berikut. a. Larutan kalsium hidroksida + asam sulfat b. Kalium hidroksida + asam sulfat c. Larutan natrium karbonat + larutan kalsium klorida Reaksi Penetralan dan Titrasi Asam-Basa 189
4 B. Titrasi Asam Kuat-Basa Kuat Reaksi penetralan asam atau basa dapat dilakukan dengan tepat melalui cara titrasi. Titrasi asam basa adalah penambahan larutan standar atau larutan yang telah diketahui konsentrasinya. Larutan standar ditambahkan ke dalam larutan asam atau basa sampai suasana netral. Keadaan netral pada titrasi ditunjukkan oleh indikator yang digunakan yaitu indikator yang berubah warna pada suasana netral yaitu ph 7. Misalnya indikator fenolftalein. Sebenarnya indikator ini memiliki trayek ph 8,2 10 tetapi biasa digunakan karena perubahan warnanya mudah diamati yaitu dari tidak berwarna menjadi merah. Titrasi asam basa dapat pula dilakukan untuk menentukan konsentrasi larutan asam atau basa yang konsentrasinya belum diketahui, sehingga kita dapat menghitung jumlah zat pereaksi atau hasil reaksi pada suatu reaksi. Bagaimana cara melakukan titrasi? Lakukan Kegiatan 8.1. KEGIATAN 8.1 Penentuan Konsentrasi Asam Klorida melalui Titrasi Langkah-langkah menentukan konsentrasi asam klorida oleh natrium hidroksida melalui titrasi tertera pada gambar berikut. buret 1 pipet volumetric NaOH HCl labu erlenmeyer 1. Ambil 20 ml larutan HCl dengan pipet volumetrik ukuran 20 ml dan masukkan ke dalam labu erlenmeyer 125 ml (gambar 1 dan 2). 2. Tambahkan 3 tetes indikator fenolftalein. 3. Siapkan buret yang telah diisi larutan NaOH 0,1 M. Catat volum awal dengan melihat skala pada buret (Gambar 5). 4. Teteskan larutan NaOH dari buret sambil menggoyangkan labu erlenmeyer agar asam dengan basa bereaksi sempurna sampai indikator tepat berubah warna atau titik akhir titrasi (Gambar 4). 5. Catat lagi volum NaOH pada skala buret. Hitung volum NaOH yang digunakan (Gambar 5). 6. Ulangi percobaan sehingga diperoleh hasil yang sama atau hampir sama Kimia Kelas XI SMA dan MA
5 Cara menghitung konsentrasi HCl dari data titrasi adalah sebagai berikut. Pada saat titik akhir titrasi atau saat indikator fenolftalein berubah warna yaitu ph = 7, akan dicapai titik ekivalen. Mol H + = mol OH. Oleh karena mol zat = volum larutan x molaritas maka V asam x M asam = V basa x M basa Catatan: V = volum M asam = molaritas H + M basa = molaritas OH Misalkan pada percobaan di atas didapat data sebagai berikut. No. Volum HCl (ml) Mula-Mula Volum NaOH (ml) Akhir Titrasi , ,35 26, ,75 15,14 Untuk menghitung konsentrasi HCl dilakukan dengan cara: Volum NaOH: Pada percobaan 1 : 50 ml 38,35 ml = 11,65 ml Pada percobaan 2 : 38,35 ml 26,75 ml = 11,60 ml Pada percobaan 3 : 26,75 ml 15,14 ml = 11,61 ml Volum NaOH rata-rata = 1165, ml + 11,60 ml + 11,61 ml 3 = 11,62 ml V A. M A = V B. M B 20 ml. M A = 11,62 ml. 0,1 M M A = 1162, ml 0,1 M = 0,0581 M 20 ml Jadi, konsentrasi HCl = 0,058 M Contoh Soal ml HCl yang tidak diketahui konsentrasinya dititrasi oleh larutan NaOH 0,1 M. Pada titik akhir titrasi ternyata rata-rata volum NaOH 0,1 M yang digunakan adalah 12,52 ml. Hitung konsentrasi HCl yang dititrasi. Penyelesaian: V asam x M asam = V basa x M basa 10 ml x M asam = 12,52 ml x 0,1 M 12,52 ml M asam = 0,1 M = 0,1252 M 10 ml Jadi konsentrasi HCl adalah 0,125 M. Reaksi Penetralan dan Titrasi Asam-Basa 191
6 2. 10 ml HCl X M dititrasi oleh larutan Ba(OH) 2 0,1 M diperlukan 15 ml. Hitunglah konsentrasi HCl yang dititrasi. Penyelesaian: HCl(aq) H + (aq) + Cl (aq) Ba(OH) 2 (aq) Ba 2+ (aq) + 2 OH (aq) V asam x M asam = V basa x M basa 10 ml x M asam = 15 ml x 0,2 M 10 M asam =3 M asam = 3 10 = 0,3 Molaritas asam = molaritas H + = 0,3 M Jadi, konsentrasi HCl adalah 0,3 M. Latihan 8.2 Selesaikan soal-soal berikut! 1. Tentukan molaritas KOH jika 5 ml asam klorida 0,1 M dapat dinetralkan oleh 10 ml larutan KOH. 2. Titrasi dihentikan apabila sudah tercapai titik akhir titrasi. a. Apa yang dimaksud dengan titik ekivalen dan titik akhir titrasi? b. Bagaimana cara menentukan titik akhir titrasi antara 25 ml larutan NaOH 0,1 M dengan larutan HCl 0,1 M? c. Indikator apa yang paling tepat digunakan untuk titrasi tersebut? ml larutan H 2 dititrasi oleh larutan NaOH 0,1 M. Jika dibutuhkan 10 ml larutan NaOH, tentukanlah kemolaran larutan H 2! 4. Data hasil percobaan titrasi CH 3 COOH dengan NaOH 0,05 M, adalah sebagai berikut: Percobaan Volum CH 3 COOH (ml) Vol NaOH (ml) , , ,1 Tentukan konsentrasi CH 3 COOH! C. Grafik Titrasi Asam-Basa Grafik titrasi menggambarkan alur ph terhadap volum asam atau basa yang ditambahkan pada saat titrasi. Pada grafik ini dapat dilihat titik ekivalen dari reaksi asam-basa pada titrasi. 192 Kimia Kelas XI SMA dan MA
7 Berikut ini contoh pembuatan grafik titrasi asam kuat dengan basa kuat dan asam lemah dengan basa kuat pada percobaan titrasi 25 ml HCl 0,1 M dengan larutan NaOH 0,1 M dan 25 ml CH 3 COOH 0,1 M dengan larutan NaOH 0,1 M. Setiap perubahan ph dicatat volum NaOH yang ditambahkannya. Data yang diperoleh tertera pada Tabel 8.1. Tabel 8.1 Harga ph pada titrasi asam kuat dengan basa kuat dan asam lemah dengan basa kuat Volum NaOH 0,1 M yang ditambahkan (ml) HCl 0,1 M ph pada titrasi CH 3 COOH 0,1 M 0,0 1,00 2,87 5,0 1,18 4,14 10,0 1,37 4,57 15,0 1,60 4,92 20,0 1,95 5,35 22,0 2,20 5,61 24,0 2,69 6,13 24,5 3,00 6,44 24,9 3,70 7,14 25,0 7,00 8,72 25,1 10,30 10,30 25,5 11,00 11,00 26,0 11,29 11,29 28,0 11,75 11,75 30,0 11,96 11,96 35,0 12,22 12,22 40,0 12,36 12,36 45,0 12,46 12,46 50,0 12,52 12,52 Data tersebut dibuat grafik sebagai berikut ph ph titik ekivalen Volum NaOH 0,1 M (ml) ph ph Volum NaOH 0,1 M (ml) titik ekivalen Gambar 8.2 Grafik titrasi HCl dan NaOH Gambar 8.3 Grafik titrasi CH 3 COOH dan NaOH Reaksi Penetralan dan Titrasi Asam-Basa 193
8 Pada titrasi HCl dengan NaOH, mula-mula ph naik sangat lambat kemudian terjadi lonjakan ph dan selanjutnya kenaikan ph lambat lagi. Titik tengah bagian vertikal grafik adalah titik ekivalen titrasi. Pada titrasi asam kuat dan basa kuat titik ekivalen terjadi pada ph 7. Larutan dengan ph 7 bersifat netral karena jumlah ion H + sama dengan ion OH. Titrasi asam lemah dengan basa kuat prinsipnya sama tetapi ada sedikit perbedaan. Pada titrasi CH 3 COOH dengan NaOH, ph dimulai dari ph 3 dan titik ekivalen terjadi pada ph yang lebih tinggi pula. Hal ini disebabkan CH 3 COOH adalah asam lemah dan menghasilkan ion H + dalam jumlah yang sedikit. Titik ekivalen terjadi pada ph 8,72. Pada campuran terdapat pula natrium asetat yang bersifat basa lemah dan meningkatkan ph. Setelah titik ekivalen, kedua grafik sama kembali karena ph hanya bergantung pada ion hidroksida yang ditambahkan. Grafik titrasi membantu untuk menentukan indikator apa yang cocok untuk suatu titrasi. Pada titrasi asam kuat dengan basa kuat, dapat digunakan indikator fenolftalein walaupun trayek ph mulai ph 8,72. Pada ph 8,72 atau titik akhir penambahan NaOH hanya 0,01 ml, jadi dapat diabaikan. Untuk titrasi asam lemah dengan basa kuat indikator fenolftalein sudah tepat digunakan karena titik ekivalen berada pada awal trayek ph (8,3). Latihan 8.3 Selesaikan soal-soal berikut! 1. Perkirakan gambar grafik titrasi jika larutan NH 3 dititrasi oleh HCl dan CH 3 COOH dititrasi oleh NH 3 (aq). 2. Mengapa pada titrasi asam basa lebih sering digunakan indikator fenolftalein daripada brom timol biru? 3. Jelaskan mengapa titik ekivalen titrasi HCl dengan NaOH berbeda dengan titik ekivalen titrasi CH 3 COOH dengan NaOH? D. Perhitungan Jumlah Pereaksi atau Hasil Reaksi melalui Reaksi Penetralan atau Titrasi Pada reaksi penetralan jumlah mol ion H + sama dengan jumlah ion OH. Atas dasar itu jumlah pereaksi atau hasil reaksi dapat diperhitungkan. Perhatikan cara perhitungannya pada contoh soal berikut. Contoh Soal ml larutan NaOH dinetralkan melalui titrasi oleh 25 ml larutan HCl 0,2 M Berapa massa NaOH yang terdapat pada larutan tersebut? 194 Kimia Kelas XI SMA dan MA
9 Penyelesaian: V A M A = V B M B 25 ml.0,2 M = 50 ml.m NaOH M NaOH = 25 ml., 0 2 M = 0,1 M 50 M Jumlah mol NaOH pada larutan tersebut = 50 ml x 0,1 M = 5 mmol = mol. Massa NaOH yang terdapat dalam larutan tersebut = x 40 = 0,2 gram. 2. Sebanyak 250 ml H 2 0,1 M dapat dinetralkan melalui titrasi oleh larutan KOH 0,3 M. Berapa ml volum KOH yang diperlukan? Penyelesaian: H 2 2 H ,1 M 0,2 M V A.M A = V B.M B 250 ml.0,2 M = V B.0,3 M V KOH = 250 ml. 02 M = 166,7 ml. 03, M ml larutan NH 4 OH 0,2 M dicampurkan dengan 100 ml larutan HCl 0,02 M. Hitung berapa gram garam yang terbentuk! (A r N = 14, H = 1, Cl = 35,5). Penyelesaian: Persamaan reaksi: NH 4 OH(aq) + HCl(aq) NH 4 Cl(aq) + H 2 O(l) NH 4 OH yang ada = 40 ml x 0,2 mmol ml 1 = 8 mmol HCl yang ada = 100 ml x 0,02 mmol ml 1 = 2 mmol Pada persamaan reaksi, mol NH 4 OH ~ mol HCl maka HCl yang habis bereaksi = 2 mmol NH 4 Cl yang terbentuk = 1 x 2 mmol = 2 mmol 1 NH 4 Cl yang terbentuk = 2 x 53,5 = 107 mg Latihan 8.4 Selesaikan soal-soal berikut! ml larutan Ca(OH) 2 tepat dinetralkan oleh 100 ml larutan HCl 0,05 M Tentukan konsentrasi larutan Ca(OH) 2! ml larutan cuka 3 M dititrasi dengan 50 ml larutan NaOH. Tentukan massa NaOH yang terdapat dalam larutan tersebut! (A r Na = 23, O = 16, H = 1). Reaksi Penetralan dan Titrasi Asam-Basa 195
10 3. Bila A r H = 1, O = 16, Mg = 24, dan Cl = 35,5, hitung berapa jumlah HCl yang diperlukan untuk tepat menetralkan 11,6 gram Mg(OH) 2! 4. Sebanyak 5,8 gram basa M(OH) 2 tepat bereaksi dengan 200 ml HCl 1 M menurut persamaan reaksi: M(OH) 2 (s) + 2 HCl(aq) MCl 2 (aq) + 2 H 2 O(l). Berapa massa atom relatif (A r ) logam M? E. Penerapan Titrasi Asam-Basa Cara titrasi asam basa dapat digunakan untuk mengetahui kadar zat, misalnya kadar asam di dalam produk cuka, minuman, atau di dalam buah-buahan. Bagaimana cara menentukan kadar asam asetat dalam cuka dapur? Lakukan titrasi larutan cuka dapur oleh larutan NaOH, encerkan dulu larutan cuka tersebut pada saat titrasi. Contoh perhitungan: Misalkan titrasi 2 ml larutan asam cuka memerlukan 35 ml larutan NaOH 0,1 M. Massa jenis larutan 950 g L 1. a. Tentukan molaritas asam cuka! b. Berapa % kadar asam cuka tersebut? Penyelesaian: a. M asam = V basa M basa 35 ml 0,1 M = = 1,75 M Vasam 2 ml b. Dalam 1 liter larutan cuka terdapat 1,75 x 60 gram cuka = 105 gram cuka. Berat 1 liter larutan = 950 gram % larutan cuka = 105 gram x 100 % = 11,05 % 950 gram Latihan 8.5 Selesaikan soal-soal berikut! ml larutan H 2 tepat dinetralkan oleh 60 ml larutan NaOH 0,1 M. Tentukan molaritas larutan H Cuplikan Ca(OH) 2 sebanyak 0,6 gram dilarutkan dalam air sampai volum 100 ml. 25 ml larutan tersebut dititrasi dengan larutan HCl 0,1 M dan ternyata diperlukan 10 ml HCl untuk mencapai titik ekivalen. Tentukan kadar Ca(OH) 2 dalam cuplikan tersebut M r Ca(OH) 2 = Kimia Kelas XI SMA dan MA
11 INFO KIMIA Sengatan lebah sangat menyakitkan sebab lebah menyuntikan asam ke dalam kulit. Sengatan tawon juga menyakitkan, tawon menyuntikkan basa ke dalam kulit. Obat penetral bisa yang digunakan pada sengatan lebah dan tawon tentu berbeda. Sekarang dikenal pengobatan tradisional dengan sengatan lebah. Sumber: CD Image Rangkuman 1. Reaksi penetralan adalah reaksi antara asam dan basa dengan jumlah mol ion H + = mol ion OH. 2. Titrasi asam-basa adalah penambahan larutan standar atau larutan yang telah diketahui konsentrasinya ke dalam larutan asam atau basa sampai suasana netral. 3. Titik akhir titrasi adalah saat indikator berubah warna. 4. Titik ekivalen terjadi pada saat [H + ] = [OH ]. 5. Grafik titrasi asam-basa menggambarkan alur ph terhadap volum asam atau basa yang ditambahkan pada saat titrasi. 6. Titrasi asam-basa menggunakan rumus Catatan: V = volum V asam x M asam = V basa x M basa M asam = molaritas H + M basa = molaritas OH 7. Titik ekivalen pada titrasi asam kuat dengan basa kuat adalah ph = Titik ekivalen pada titrasi asam lemah dengan basa kuat ph > Titik ekivalen pada titrasi asam kuat dengan basa lemah ph < 7. Kata Kunci Reaksi Penetralan Titik akhir titrasi Titrasi Molaritas H + Indikator Molaritas OH Titik ekivalen Reaksi Penetralan dan Titrasi Asam-Basa 197
12 Evaluasi Akhir Bab A. Pilihlah salah satu jawaban yang paling benar. 1. Istilah penetralan ada kaitannya dengan.... A. reaksi antara asam dengan basa B. penggunaan pipet untuk menambahkan asam atau basa ke dalam suatu wadah C. reaksi antara satu ion hidrogen dengan satu ion hidroksida D. reaksi antara ion hidrogen dengan air E. pengambilan zat terlarut dari suatu larutan 2. Dari hasil titrasi larutan KOH 0,1 M dengan HNO 3 0,15 M didapat data sebagai berikut. No. Volum KOH 0,1 M Volum HNO 3 0,15 M 1. 2 ml 20 ml 2. 8 ml 20 ml ml 20 ml ml 20 ml ml 20 ml Dari data di atas yang menunjukkan terjadinya titik ekivalen terletak pada percobaan nomor.... A. 1 D. 4 B. 2 E. 5 C ml HCl XM dititrasi pada titik ekivalen dan membutuhkan 5 ml larutan NaOH 0,1 M. Konsentrasi (X) larutan HCl adalah.... A. 2 M B. 1 M C. 0,5 M D. 0,1 M E. 0,05 M 4. Jika 20 ml larutan NaOH 0,1 M dapat dinetralkan oleh 25 ml larutan H 2, maka 1 liter H 2 mengandung H 2 sebanyak.... A. 0,04 mol D. 0,25 mol B. 0,05 mol E. 0,10 mol C. 0,08 mol 198 Kimia Kelas XI SMA dan MA
13 5. Grafik berikut yang menunjukkan kurva titrasi basa kuat dengan asam lemah adalah.... A. D. ph ph 7 7 vol. basa vol. basa B. ph E. ph 7 7 vol. basa vol. basa C. ph 7 vol. basa 6. Indikator yang paling tepat digunakan untuk titrasi asam lemah CH 3 COOH 0,1 M dengan basa kuat NaOH 0,1 M adalah.... A. metil merah (rentang ph 3,5 4,8) B. brom kresol hijau (rentang ph 4,6 5,8) C. brom timol biru (rentang ph 6,0 8,0) D. fenolftalein (rentang ph 8,0 10,0) E. alazarin kuning (rentang ph 10,0 12,5) 7. Jika 20 ml HNO 3 0,1 M dititrasi dengan larutan NaOH 0,2 M maka volum basa yang dipergunakan untuk mencapai titik ekivalen adalah.... A. 10 ml D. 30 ml B. 20 ml E. 40 ml C. 25 ml 8. Besarnya ph campuran dari larutan 500 ml NaOH 0,02 M dan 1500 ml KOH 0,02 M adalah.... A. 2 log 2 D log 5 B. 12 log 2 E log 5 C log 2 Reaksi Penetralan dan Titrasi Asam-Basa 199
14 9. Pada penentuan kadar amonia secara titrasi dengan asam klorida, ternyata ph akhir titrasi = 5,12. Indikator yang sesuai untuk titrasi ini adalah.... A. metil oranye dengan trayek ph perubahan warna adalah 3,1 4,4 B. metil merah dengan trayek ph perubahan warna adalah 4,8 6,0 C. fenolftalein dengan trayek ph perubahan warna adalah 8,3 10,0 D. brom timol biru dengan trayek ph perubahan warna adalah 8,0 10,0 E. indigo karmen dengan trayek ph perubahan warna adalah 11,4 13, ml larutan asam HA ditambah 25 ml larutan NaOH 0,1 M (berlebih), sisanya membutuhkan 10 ml HCl 0,1 M untuk dinetralkan. Konsentrasi HA adalah.... A. 0,06 B. 0,6 C. 1,0 D. 6 E. 0, Suatu cuplikan natrium hidroksida sebanyak 0,3 gram apabila dilarutkan dalam air memerlukan 25 ml larutan 0,1 molar HCl untuk menetralkan. Tentukan kadar NaOH dalam cuplikan tersebut jika A r H = 1, O = 16, Na = 23! A. 16,7 % B. 33,3 % C. 60,0 % D. 66,7 % E. 50,0 % 12. Menurut reaksi: H 2 (aq) + NaOH(aq) Na 2 (aq) + 2 H 2 O(l) Jika 75 ml larutan H 2 0,1 M direaksikan dengan 50 ml larutan NaOH 0,2 M maka pada reaksi tersebut yang tersisa adalah.... A. 2,5 x 10 3 mol H 2 B. 5 x 10 3 mol H 2 C. 2,5 x 10 3 mol NaOH D. 5 x 10 3 mol NaOH E. 7,5 x 10 3 mol NaOH 13. Seorang siswa sedang melakukan percobaan titrasi larutan CH 3 COOH dengan larutan NaOH dan menggunakan indikator fenolftalein, titik akhir titrasi dicapai bila.... B. dalam erlenmeyer terbentuk endapan A. dalam erlenmeyer terbentuk gas C. larutan dalam erlenmeyer tidak berwarna D. warna larutan dalam erlenmeyer menjadi merah tua E. warna larutan dalam erlenmeyer menjadi merah muda 200 Kimia Kelas XI SMA dan MA
15 14. 2 gram contoh tablet vitamin C dengan rumus HC 6 H 7 O 6 dilarutkan dalam air sampai volum 100 ml. 10 ml larutan ini dititrasi dengan NaHCO 3 0,03 M sebanyak 13 ml, maka kadar vitamin C dalam tablet tersebut adalah.... (A r C = 12, H = 1, O = 16). A. 24,96 % D. 34,32 % B. 29,6 % E. 36,36 % C. 30,6 % 15. Untuk menentukan kadar cuka dapur dari larutan encer asam asetat CH 3 COOH, 5 ml larutan cuka ini dititrasi dengan larutan NaOH 0,2 M memerlukan 96 ml NaOH. Jika massa jenis cuka 1,05 g ml 1 maka kadar % asam asetat dalam cuka dapur tersebut adalah.... A. 21,19 % D. 24,16 % B. 20,5 % E. 26 % C. 22,6 % B. Selesaikan soal-soal berikut dengan jelas dan singkat. 1. Jelaskan apa yang dimaksud dengan: a. reaksi penetralan, c. titik akhir titrasi, b. titrasi asam basa, d. titik ekivalen ml larutan H 2 dititrasi dengan larutan Ba(OH) 2 0,1 M, sebanyak 15 ml. a. Tentukan molaritas larutan H 2 b. Buatlah grafik jika penambahkan larutan Ba(OH) 2 0,1 M yang ditambahkan 1 ml, 2 ml, 3 ml, 4 ml, 5 ml, 10 ml, dan 15 ml. 3. Sebanyak 112 gram KOH dilarutkan ke dalam air hingga volum larutannya 500 ml. Kemudian seluruh larutan yang terbentuk direaksikan dengan larutan HCl sampai larutan yang dihasilkan bersifat netral. Jika HCl yang diperlukan sebanyak150 ml tentukan: (A r K = 39, O = 16, H = 1). a. molaritas larutan KOH, b. molaritas larutan HCl. 4. X gram NaOH dilarutkan dalam 200 ml air. 10 ml larutan NaOH dapat dinetralkan oleh 28,5 ml HCl 0,155 M. Hitunglah harga X (A r Na = 23, O = 16, H = 1). 5. Untuk menentukan kadar kapur CaO dalam kapur tohor, ditimbang 2,8 gram cuplikan kapur tohor lalu dilarutkan ke dalam air sampai volumnya 100 ml. 10 ml larutan yang terjadi dititrasi dengan HCl 0,05 M. Titik akhir titrasi dicapai bila volum HCl 0,05 M 50 ml. (A r Ca = 40, O = 16). a. Berapa molaritas larutan air kapur? b. Tentukan kadar CaO dalam cuplikan kapur tohor tersebut. Reaksi Penetralan dan Titrasi Asam-Basa 201
16 T u g a s Rancanglah percobaan untuk menguji kadar asam asetat di dalam cuka dapur dengan berbagai merk yang diperdagangkan. a. Catat harganya dan hitung harga per liternya! b Berapa masing-masing konsentrasinya? Apakah kadar yang tertera pada labelnya sesuai dengan konsentrasi hasil penelitian? c. Berikan saran yang tepat untuk membeli cuka dapur di pasaran! 202 Kimia Kelas XI SMA dan MA
Sumber: Silberberg, Chemistry: The Molecular Nature of Matter and Change
 Bab VII ph Larutan Asam-Basa Sumber: Silberberg, Chemistry: The Molecular Nature of Matter and Change Indikator universal dan kertas lakmus digunakan untuk mengindentifikasi ph larutan asam-basa. TUJUAN
Bab VII ph Larutan Asam-Basa Sumber: Silberberg, Chemistry: The Molecular Nature of Matter and Change Indikator universal dan kertas lakmus digunakan untuk mengindentifikasi ph larutan asam-basa. TUJUAN
wanibesak.wordpress.com 1
 Ringkasan, contoh soal dan pembahasan mengenai asam, basa dan larutan penyangga atau larutan buffer Persamaan ionisasi air H 2O H + + OH Dari reaksi di atas sesuai hukum kesetimbangan, tetapan kesetimbangan
Ringkasan, contoh soal dan pembahasan mengenai asam, basa dan larutan penyangga atau larutan buffer Persamaan ionisasi air H 2O H + + OH Dari reaksi di atas sesuai hukum kesetimbangan, tetapan kesetimbangan
Larutan penyangga adalah larutan yang dapat mempertahankan harga ph terhadap pengaruh penambahan sedikit asam atau basa, atau terhadap pengenceran.
 Standar Kompetensi Kompetensi Dasar Memahami sifatsifat larutan asambasa, metode pengukuran, dan terapannya. Mendeskripsikan sifat larutan penyangga dan peranan larutan penyangga dalam tubuh makhluk hidup.
Standar Kompetensi Kompetensi Dasar Memahami sifatsifat larutan asambasa, metode pengukuran, dan terapannya. Mendeskripsikan sifat larutan penyangga dan peranan larutan penyangga dalam tubuh makhluk hidup.
LEMBARAN SOAL 4. Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA )
 LEMBARAN SOAL 4 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah
LEMBARAN SOAL 4 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah
ASAM -BASA, STOIKIOMETRI LARUTAN DAN TITRASI ASAM-BASA
 ASAM -BASA, STOIKIOMETRI LARUTAN DAN TITRASI ASAM-BASA Asam merupakan zat yang yang mengion dalam air menghasilkan ion H + dan basa merupakan zat yang mengion dalam air menghasilkan ion OH -. ASAM Asam
ASAM -BASA, STOIKIOMETRI LARUTAN DAN TITRASI ASAM-BASA Asam merupakan zat yang yang mengion dalam air menghasilkan ion H + dan basa merupakan zat yang mengion dalam air menghasilkan ion OH -. ASAM Asam
kimia ASAM-BASA III Tujuan Pembelajaran
 KTSP K-13 kimia K e l a s XI ASAM-BASA III Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami mekanisme reaksi asam-basa. 2. Memahami stoikiometri
KTSP K-13 kimia K e l a s XI ASAM-BASA III Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami mekanisme reaksi asam-basa. 2. Memahami stoikiometri
BAB 5. Larutan Asam dan Basa. Kata Kunci. Pengantar Asam dan basa sudah dikenal sejak zaman dulu. Istilah asam (acid) berasal dari
 Kimia XI SMA 147 BAB 5 Larutan Asam dan Basa Tujuan Pembelajaran: Setelah mempelajari bab ini, Anda diharapkan mampu: 1. Menjelaskan pengertian asam-basa menurut Arrhenius. 2. Membandingkan kekuatan asam-basa.
Kimia XI SMA 147 BAB 5 Larutan Asam dan Basa Tujuan Pembelajaran: Setelah mempelajari bab ini, Anda diharapkan mampu: 1. Menjelaskan pengertian asam-basa menurut Arrhenius. 2. Membandingkan kekuatan asam-basa.
Teori Asam-Basa Arrhenius
 Standar Kompetensi emahami terapannya. sifatsifat larutan asambasa, metode pengukuran, dan Kompetensi Dasar enjelaskan teori asam basa menurut Arrhenius mengklasifikasi berbagai larutan asam, netral, dan
Standar Kompetensi emahami terapannya. sifatsifat larutan asambasa, metode pengukuran, dan Kompetensi Dasar enjelaskan teori asam basa menurut Arrhenius mengklasifikasi berbagai larutan asam, netral, dan
Reaksi dalam larutan berair
 Reaksi dalam larutan berair Drs. Iqmal Tahir, M.Si. iqmal@gadjahmada.edu Larutan - Suatu campuran homogen dua atau lebih senyawa. Pelarut (solven) - komponen dalam larutan yang membuat penuh larutan (ditandai
Reaksi dalam larutan berair Drs. Iqmal Tahir, M.Si. iqmal@gadjahmada.edu Larutan - Suatu campuran homogen dua atau lebih senyawa. Pelarut (solven) - komponen dalam larutan yang membuat penuh larutan (ditandai
1. Dari pengujian larutan dengan kertas lakmus diperoleh data berikut:
 SOAL-SOAL BAB 5 LARUTAN ASAM BASA/ Kimia Erlangga 2B 1. Dari pengujian larutan dengan kertas lakmus diperoleh data berikut: No Larutan yang diuji Warna lakmus Merah Biru 1 X Merah Biru 2 Y Merah Merah
SOAL-SOAL BAB 5 LARUTAN ASAM BASA/ Kimia Erlangga 2B 1. Dari pengujian larutan dengan kertas lakmus diperoleh data berikut: No Larutan yang diuji Warna lakmus Merah Biru 1 X Merah Biru 2 Y Merah Merah
Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi. Bab17. Kesetimbangan Asam-Basa dan Kesetimbangan Kelarutan
 Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi Bab17 Kesetimbangan Asam-Basa dan Kesetimbangan Kelarutan Larutan buffer adalah larutan yg terdiri dari: 1. asam lemah/basa
Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi Bab17 Kesetimbangan Asam-Basa dan Kesetimbangan Kelarutan Larutan buffer adalah larutan yg terdiri dari: 1. asam lemah/basa
LARUTAN PENYANGGA DAN HIDROLISIS
 6 LARUTAN PENYANGGA DAN HIDROLISIS A. LARUTAN PENYANGGA B. HIDROLISIS Pada bab sebelumnya, kita sudah mempelajari tentang reaksi asam-basa dan titrasi. Jika asam direaksikan dengan basa akan menghasilkan
6 LARUTAN PENYANGGA DAN HIDROLISIS A. LARUTAN PENYANGGA B. HIDROLISIS Pada bab sebelumnya, kita sudah mempelajari tentang reaksi asam-basa dan titrasi. Jika asam direaksikan dengan basa akan menghasilkan
LOGO TEORI ASAM BASA
 LOGO TEORI ASAM BASA TIM DOSEN KIMIA DASAR FTP 2012 Beberapa ilmuan telah memberikan definisi tentang konsep asam basa Meskipun beberapa definisi terlihat kurang jelas dan berbeda satu sama lain, tetapi
LOGO TEORI ASAM BASA TIM DOSEN KIMIA DASAR FTP 2012 Beberapa ilmuan telah memberikan definisi tentang konsep asam basa Meskipun beberapa definisi terlihat kurang jelas dan berbeda satu sama lain, tetapi
BAB 7. ASAM DAN BASA
 BAB 7. ASAM DAN BASA 7. 1 TEORI ASAM BASA 7. 2 TETAPAN KESETIMBANGAN PENGIONAN ASAM DAN BASA 7. 3 KONSENTRASI ION H + DAN ph 7. 4 INDIKATOR ASAM-BASA (INDIKATOR ph) 7. 5 CAMPURAN PENAHAN 7. 6 APLIKASI
BAB 7. ASAM DAN BASA 7. 1 TEORI ASAM BASA 7. 2 TETAPAN KESETIMBANGAN PENGIONAN ASAM DAN BASA 7. 3 KONSENTRASI ION H + DAN ph 7. 4 INDIKATOR ASAM-BASA (INDIKATOR ph) 7. 5 CAMPURAN PENAHAN 7. 6 APLIKASI
Soal-Soal. Bab 7. Latihan Larutan Penyangga, Hidrolisis Garam, serta Kelarutan dan Hasil Kali Kelarutan. Larutan Penyangga
 Bab 7 Soal-Soal Latihan Larutan Penyangga, Hidrolisis Garam, serta Kelarutan dan Hasil Kali Kelarutan Larutan Penyangga 1. Berikut ini yang merupakan pasangan asam basa terkonjugasi (A) H 3 O + dan OH
Bab 7 Soal-Soal Latihan Larutan Penyangga, Hidrolisis Garam, serta Kelarutan dan Hasil Kali Kelarutan Larutan Penyangga 1. Berikut ini yang merupakan pasangan asam basa terkonjugasi (A) H 3 O + dan OH
SMA NEGERI 6 SURABAYA LARUTAN ASAM & BASA. K a = 2.M a. 2. H 2 SO 4 (asam kuat) α = 1 H 2 SO 4 2H + 2
 SMA NEGERI 6 SURABAYA LARUTAN ASAM & BASA K I M I A 1). TEORI ARCHENIUS Asam adalah zat yang jika di dalam air melepaskan ion H +, dengan kata lain pembawa sifat asam adalah ion H +. jumlah ion H+ yang
SMA NEGERI 6 SURABAYA LARUTAN ASAM & BASA K I M I A 1). TEORI ARCHENIUS Asam adalah zat yang jika di dalam air melepaskan ion H +, dengan kata lain pembawa sifat asam adalah ion H +. jumlah ion H+ yang
PETA KONSEP. Larutan Penyangga. Larutan Penyangga Basa. Larutan Penyangga Asam. Asam konjugasi. Basa lemah. Asam lemah. Basa konjugasi.
 PETA KONSEP Larutan Penyangga mempertahankan berupa ph Larutan Penyangga Asam mengandung Larutan Penyangga Basa mengandung Asam lemah Basa konjugasi Asam konjugasi Basa lemah contoh contoh contoh contoh
PETA KONSEP Larutan Penyangga mempertahankan berupa ph Larutan Penyangga Asam mengandung Larutan Penyangga Basa mengandung Asam lemah Basa konjugasi Asam konjugasi Basa lemah contoh contoh contoh contoh
Larutan penyangga dapat terbentuk dari campuran asam lemah dan basa
 Larutan penyangga dapat terbentuk dari campuran asam lemah dan basa konjugasinya atau campuran basa lemah dan asam konjugasinya. Larutan penyangga disebut juga larutan penahan atau larutan dapar atau buffer.
Larutan penyangga dapat terbentuk dari campuran asam lemah dan basa konjugasinya atau campuran basa lemah dan asam konjugasinya. Larutan penyangga disebut juga larutan penahan atau larutan dapar atau buffer.
LAPORAN PRAKTIKUM 3 ph METER, BUFFER, dan PENGENCERAN DISUSUN OLEH : MARIA LESTARI DAN YULIA FITRI GHAZALI Kamis 04 Oktober s/d 16.
 LAPORAN PRAKTIKUM 3 ph METER, BUFFER, dan PENGENCERAN DISUSUN OLEH : MARIA LESTARI DAN YULIA FITRI GHAZALI Kamis 04 Oktober 2012 14.00 s/d 16.00 wib TUJUAN : 1. Agar mahasiswa dapat memahami prinsip-prinsip
LAPORAN PRAKTIKUM 3 ph METER, BUFFER, dan PENGENCERAN DISUSUN OLEH : MARIA LESTARI DAN YULIA FITRI GHAZALI Kamis 04 Oktober 2012 14.00 s/d 16.00 wib TUJUAN : 1. Agar mahasiswa dapat memahami prinsip-prinsip
MATERI HIDROLISIS GARAM KIMIA KELAS XI SEMESTER GENAP
 MATERI HIDROLISIS GARAM KIMIA KELAS XI SEMESTER GENAP PENDAHULUAN Kalian pasti mendengar penyedap makanan. Penyedap makanan yang sering digunakan adalah vitsin. Penyedap ini mengandung monosodium glutamat
MATERI HIDROLISIS GARAM KIMIA KELAS XI SEMESTER GENAP PENDAHULUAN Kalian pasti mendengar penyedap makanan. Penyedap makanan yang sering digunakan adalah vitsin. Penyedap ini mengandung monosodium glutamat
TUGAS KIMIA SMA NEGERI 1 BAJAWA TITRASI ASAM BASA. Nama : Kelas. Disusun oleh:
 TUGAS KIMIA TITRASI ASAM BASA Disusun oleh: Nama : Kelas : SMA NEGERI 1 BAJAWA 2015 TITRASI ASAM BASA 1. Prinsip Dasar Titrasi netralisasi adalah titrasi yang didasarkan pada reaksi antara suatu asam dengan
TUGAS KIMIA TITRASI ASAM BASA Disusun oleh: Nama : Kelas : SMA NEGERI 1 BAJAWA 2015 TITRASI ASAM BASA 1. Prinsip Dasar Titrasi netralisasi adalah titrasi yang didasarkan pada reaksi antara suatu asam dengan
LARUTAN ELEKTROLIT DAN NON ELEKTROLIT
 BAB 6 LARUTAN ELEKTROLIT DAN NON ELEKTROLIT Standar Kompetensi Memahami sifat-sifat larutan non elektrolit dan elektrolit, serta reaksi oksidasi-reduksi Kompetensi Dasar Mengidentifikasi sifat larutan
BAB 6 LARUTAN ELEKTROLIT DAN NON ELEKTROLIT Standar Kompetensi Memahami sifat-sifat larutan non elektrolit dan elektrolit, serta reaksi oksidasi-reduksi Kompetensi Dasar Mengidentifikasi sifat larutan
I. STANDAR KOMPETENSI 4. Memahami sifat-sifat larutan asam-basa, metode pengukuran, dan terapannya.
 RENCANA PELAKSANAAN PEMBELAJARAN (RPP) TITRASI ASAM-BASA SEKOLAH : SMAN 16 SURABAYA MATA PELAJARAN : KIMIA KELAS / SEMESTER : XI / 2 (dua) ALOKASI WAKTU : 2 Jam Pelajaran I. STANDAR KOMPETENSI 4. Memahami
RENCANA PELAKSANAAN PEMBELAJARAN (RPP) TITRASI ASAM-BASA SEKOLAH : SMAN 16 SURABAYA MATA PELAJARAN : KIMIA KELAS / SEMESTER : XI / 2 (dua) ALOKASI WAKTU : 2 Jam Pelajaran I. STANDAR KOMPETENSI 4. Memahami
MATERI KIMIA KELAS XI SEMESTER 2 Tinggalkan Balasan
 MATERI KIMIA KELAS XI SEMESTER 2 Tinggalkan Balasan A. Pengertian Asam Basa Asam dan basa sudah dikenal sejak zaman dulu. Istilah asam (acid) berasal dari bahasa Latin acetum yang berarti cuka. Istilah
MATERI KIMIA KELAS XI SEMESTER 2 Tinggalkan Balasan A. Pengertian Asam Basa Asam dan basa sudah dikenal sejak zaman dulu. Istilah asam (acid) berasal dari bahasa Latin acetum yang berarti cuka. Istilah
Tentukan ph dari suatu larutan yang memiliki konsentrasi ion H + sebesar 10 4 M dengan tanpa bantuan alat hitung kalkulator!
 Kimia Study Center - Contoh soal dan pembahasan tentang cara menghitung ph dan poh larutan asam basa berdasarkan konsentrasi ion [H + ] dan [OH ] SMA kelas 11 IPA. Berikut contoh-contoh soal yang bisa
Kimia Study Center - Contoh soal dan pembahasan tentang cara menghitung ph dan poh larutan asam basa berdasarkan konsentrasi ion [H + ] dan [OH ] SMA kelas 11 IPA. Berikut contoh-contoh soal yang bisa
BAB IV TEMUAN DAN PEMBAHASAN. Untuk mengembangkan strategi pembelajaran pada materi titrasi asam basa
 BAB IV TEMUAN DAN PEMBAHASAN Untuk mengembangkan strategi pembelajaran pada materi titrasi asam basa dilakukan tiga tahap yaitu tahap pertama melakukan analisis standar kompetensi dan kompetensi dasar
BAB IV TEMUAN DAN PEMBAHASAN Untuk mengembangkan strategi pembelajaran pada materi titrasi asam basa dilakukan tiga tahap yaitu tahap pertama melakukan analisis standar kompetensi dan kompetensi dasar
FAKULTAS TEKNIK UNIVERSITAS NEGERI YOGYAKARTA BAHAN AJAR KIMIA DASAR
 No. BAK/TBB/SBG201 Revisi : 00 Tgl. 01 Mei 2008 Hal 1 dari 11 BAB VIII LARUTAN ASAM DAN BASA Asam dan basa sudah dikenal sejak dahulu. Istilah asam (acid) berasal dari bahasa Latin acetum yang berarti
No. BAK/TBB/SBG201 Revisi : 00 Tgl. 01 Mei 2008 Hal 1 dari 11 BAB VIII LARUTAN ASAM DAN BASA Asam dan basa sudah dikenal sejak dahulu. Istilah asam (acid) berasal dari bahasa Latin acetum yang berarti
ASAM, BASA, DAN GARAM
 ASAM, BASA, DAN GARAM Standar Kompetensi : Memahami klasifikasi zat Kompetensi Dasar : Mengelompokkan sifat larutan asam, larutan basa, dan larutan garam melalui alat dan indikator yang tepat A. Sifat
ASAM, BASA, DAN GARAM Standar Kompetensi : Memahami klasifikasi zat Kompetensi Dasar : Mengelompokkan sifat larutan asam, larutan basa, dan larutan garam melalui alat dan indikator yang tepat A. Sifat
kimia TITRASI ASAM BASA
 Kurikulum 2006/2013 2013 kimia K e l a s XI TITRASI ASAM BASA Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami definisi dan macam-macam titrasi.
Kurikulum 2006/2013 2013 kimia K e l a s XI TITRASI ASAM BASA Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami definisi dan macam-macam titrasi.
Soal dan Jawaban Titrasi Asam Basa
 Soal dan Jawaban Titrasi Asam Basa Rabu, 16 Januari 20130 komentar Inilah beberapa contoh soal dan jawaban tentang titrasi asam basa. Bacalah benarbenar setiap latihan soal asam basa berikut. Kalau perlu,
Soal dan Jawaban Titrasi Asam Basa Rabu, 16 Januari 20130 komentar Inilah beberapa contoh soal dan jawaban tentang titrasi asam basa. Bacalah benarbenar setiap latihan soal asam basa berikut. Kalau perlu,
BAB 6. Jika ke dalam air murni ditambahkan asam atau basa meskipun dalam jumlah. Larutan Penyangga. Kata Kunci. Pengantar
 Kimia XI SMA 179 BAB 6 Larutan Penyangga Tujuan Pembelajaran: Setelah mempelajari bab ini, Anda diharapkan mampu: 1. Menjelaskan pengertian larutan penyangga dan komponen penyusunnya. 2. Merumuskan persamaan
Kimia XI SMA 179 BAB 6 Larutan Penyangga Tujuan Pembelajaran: Setelah mempelajari bab ini, Anda diharapkan mampu: 1. Menjelaskan pengertian larutan penyangga dan komponen penyusunnya. 2. Merumuskan persamaan
BAB I PRAKTIKUM ASIDI AL-KALIMETRI
 BAB I PRAKTIKUM ASIDI AL-KALIMETRI I. TUJUAN a. Mahasiswa dapat menjelaskan proses titrasi asidi alkalimetri. b. Mahasiswa mampu menghitung konsentrasi sampel dengan metode asidi alkalimetri. II. DASAR
BAB I PRAKTIKUM ASIDI AL-KALIMETRI I. TUJUAN a. Mahasiswa dapat menjelaskan proses titrasi asidi alkalimetri. b. Mahasiswa mampu menghitung konsentrasi sampel dengan metode asidi alkalimetri. II. DASAR
PEMERINTAH KOTA SURABAYA DINAS PENDIDIKAN SMA NEGERI 16 SURABAYA JL. RAYA PRAPEN TELP FAX KODE POS 60299
 PEMERINTAH KOTA SURABAYA DINAS PENDIDIKAN SMA NEGERI 16 SURABAYA JL. RAYA PRAPEN TELP. 031-8415492 FAX 031-8430673 KODE POS 60299 ULANGAN AKHIR SEMESTER 2 (DUA) TAHUN PELAJARAN 2011 2012 Hari/Tanggal :
PEMERINTAH KOTA SURABAYA DINAS PENDIDIKAN SMA NEGERI 16 SURABAYA JL. RAYA PRAPEN TELP. 031-8415492 FAX 031-8430673 KODE POS 60299 ULANGAN AKHIR SEMESTER 2 (DUA) TAHUN PELAJARAN 2011 2012 Hari/Tanggal :
BERKAS SOAL BIDANG STUDI: KIMIA PRAKTIKUM MODUL I KOMPETISI SAINS MADRASAH NASIONAL 2012
 BERKAS SOAL BIDANG STUDI: KIMIA PRAKTIKUM MODUL I KOMPETISI SAINS MADRASAH NASIONAL 2012 Hal-0 Instruksi Pastikan bahwa nama dan kode peserta Anda sudah tertulis pada halaman pertama lembar soal dan lembar
BERKAS SOAL BIDANG STUDI: KIMIA PRAKTIKUM MODUL I KOMPETISI SAINS MADRASAH NASIONAL 2012 Hal-0 Instruksi Pastikan bahwa nama dan kode peserta Anda sudah tertulis pada halaman pertama lembar soal dan lembar
LEMBARAN SOAL 11. Sat. Pendidikan
 LEMBARAN SOAL 11 Mata Pelajaran Sat. Pendidikan Kelas / Program : KIMIA : SMA : XI IPA PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah soal dengan
LEMBARAN SOAL 11 Mata Pelajaran Sat. Pendidikan Kelas / Program : KIMIA : SMA : XI IPA PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah soal dengan
LAPORAN PRAKTIKUM KIMIA MENENTUKAN KONSENTRASI LARUTAN H 2 SO 4 DAN KONSENTRASI LARUTAN CH 3 COOH DENGAN TITRASI ASAM BASA (ASIDI-ALKALIMETRI)
 LAPORAN PRAKTIKUM KIMIA MENENTUKAN KONSENTRASI LARUTAN H 2 SO 4 DAN KONSENTRASI LARUTAN CH 3 COOH DENGAN TITRASI ASAM BASA (ASIDI-ALKALIMETRI) Disusun Oleh : 1. Ela Bintang Bahari (XI IPA 4 / 03) 2. Alfian
LAPORAN PRAKTIKUM KIMIA MENENTUKAN KONSENTRASI LARUTAN H 2 SO 4 DAN KONSENTRASI LARUTAN CH 3 COOH DENGAN TITRASI ASAM BASA (ASIDI-ALKALIMETRI) Disusun Oleh : 1. Ela Bintang Bahari (XI IPA 4 / 03) 2. Alfian
CH 3 COONa 0,1 M K a CH 3 COOH = 10 5
 Soal No. 1 Dari beberapa larutan berikut ini yang tidak mengalami hidrolisis adalah... A. NH 4 Cl C. K 2 SO 4 D. CH 3 COONa E. CH 3 COOK Yang tidak mengalami peristiwa hidrolisis adalah garam yang berasal
Soal No. 1 Dari beberapa larutan berikut ini yang tidak mengalami hidrolisis adalah... A. NH 4 Cl C. K 2 SO 4 D. CH 3 COONa E. CH 3 COOK Yang tidak mengalami peristiwa hidrolisis adalah garam yang berasal
Larutan Asam-Basa. Sifat Larutan Asam dan Basa. Penentuan ph Larutan Asam Kuat dan Basa Kuat. Penentuan ph Larutan Asam Lemah dan Basa Lemah
 Setelah mempelajari bab ini, peserta didik dapat: 1. menjelaskan konsep asam-basa serta sifat larutan asam dan basa; 2. menentukan ph larutan asam kuat, asam lemah, basa kuat, dan basa lemah; 3. terampil
Setelah mempelajari bab ini, peserta didik dapat: 1. menjelaskan konsep asam-basa serta sifat larutan asam dan basa; 2. menentukan ph larutan asam kuat, asam lemah, basa kuat, dan basa lemah; 3. terampil
Kimia Study Center - Contoh soal dan pembahasan tentang hidrolisis larutan garam dan menentukan ph atau poh larutan garam, kimia SMA kelas 11 IPA.
 Kimia Study Center - Contoh soal dan pembahasan tentang hidrolisis larutan garam dan menentukan ph atau poh larutan garam, kimia SMA kelas 11 IPA. Soal No. 1 Dari beberapa larutan berikut ini yang tidak
Kimia Study Center - Contoh soal dan pembahasan tentang hidrolisis larutan garam dan menentukan ph atau poh larutan garam, kimia SMA kelas 11 IPA. Soal No. 1 Dari beberapa larutan berikut ini yang tidak
LARUTAN PENYANGGA Bahan Ajar Kelas XI IPA Semester Gasal 2012/2013
 LARUTAN PENYANGGA [Yea r] LARUTAN PENYANGGA Bahan Ajar Kelas XI IPA Semester Gasal 2012/2013 MARI BELAJAR Indikator Produk Menjelaskan komponen pembentuk larutan penyangga dengan berpikir kritis. Menjelaskan
LARUTAN PENYANGGA [Yea r] LARUTAN PENYANGGA Bahan Ajar Kelas XI IPA Semester Gasal 2012/2013 MARI BELAJAR Indikator Produk Menjelaskan komponen pembentuk larutan penyangga dengan berpikir kritis. Menjelaskan
H + + OH - > H 2 O. Jumlah mol asam (proton) sama dengan jumlah mol basa (ion hidroksida). Stoikiometri netralisasi
 Netralisasi a. Netralisasi Neutralisasi dapat didefinisikan sebagai reaksi antara proton (atau ion hidronium) dan ion hidroksida membentuk air. Dalam bab ini kita hanya mendiskusikan netralisasi di larutan
Netralisasi a. Netralisasi Neutralisasi dapat didefinisikan sebagai reaksi antara proton (atau ion hidronium) dan ion hidroksida membentuk air. Dalam bab ini kita hanya mendiskusikan netralisasi di larutan
BAB 5 LARUTAN ASAM BASA. Gambar 5.1 Macam-macam Larutan Sumber: Ensiklopedi Sains dan Kehidupan
 BAB 5 LARUTAN ASAM BASA Gambar 5.1 Macam-macam Larutan Sumber: Ensiklopedi Sains dan Kehidupan Pada bab kelima ini akan dipelajari tentang teori asam basa menurut Arrhenius, konsep asam basa Bronsted-Lowry,
BAB 5 LARUTAN ASAM BASA Gambar 5.1 Macam-macam Larutan Sumber: Ensiklopedi Sains dan Kehidupan Pada bab kelima ini akan dipelajari tentang teori asam basa menurut Arrhenius, konsep asam basa Bronsted-Lowry,
Bab 7. Stoikiometri Larutan dan Titrasi Asam Basa. A. Reaksi dalam Larutan B. Titrasi Asam Basa
 Bab 7 Stoikiometri Larutan dan Titrasi Asam Basa Hasil yang harus Anda capai: memahami sifat-sifat larutan asam basa, metode pengukuran, dan terapannya. Sumber: powerlabs.org Titrasi merupakan metode untuk
Bab 7 Stoikiometri Larutan dan Titrasi Asam Basa Hasil yang harus Anda capai: memahami sifat-sifat larutan asam basa, metode pengukuran, dan terapannya. Sumber: powerlabs.org Titrasi merupakan metode untuk
NETRALISASI ASAM BASA SEDERHANA
 NETRALISASI ASAM BASA SEDERHANA Dosen Pembimbing : Zora Olivia, S. Farm., M.Farm, Apt GOLONGAN/KELOMPOK : A / 3 Anindiya Tazkiyah Aji Gesang Jati Abrar Rivanio Putra Siti Sofiya Miranda Faradilla Rozziqa
NETRALISASI ASAM BASA SEDERHANA Dosen Pembimbing : Zora Olivia, S. Farm., M.Farm, Apt GOLONGAN/KELOMPOK : A / 3 Anindiya Tazkiyah Aji Gesang Jati Abrar Rivanio Putra Siti Sofiya Miranda Faradilla Rozziqa
Soal dan Pembahasan Asam Basa, Larutan Penyangga, Hidrolisis Garam, dan K SP
 Soal dan Pembahasan Asam Basa, Larutan Penyangga, Hidrolisis Garam, dan K SP Θ Asam Basa 1. Jelaskan Pengertian Asam Basa menurut arrhenius! Asam Zat yang dalam air melepaskan ion H + Basa Senyawa yang
Soal dan Pembahasan Asam Basa, Larutan Penyangga, Hidrolisis Garam, dan K SP Θ Asam Basa 1. Jelaskan Pengertian Asam Basa menurut arrhenius! Asam Zat yang dalam air melepaskan ion H + Basa Senyawa yang
LARUTAN. Zat terlarut merupakan komponen yang jumlahnya sedikit, sedangkan pelarut adalah komponen yang terdapat dalam jumlah banyak.
 LARUTAN Larutan merupakan campuran yang homogen,yaitu campuran yang memiliki komposisi merata atau serba sama di seluruh bagian volumenya. Suatu larutan mengandung dua komponen atau lebih yang disebut
LARUTAN Larutan merupakan campuran yang homogen,yaitu campuran yang memiliki komposisi merata atau serba sama di seluruh bagian volumenya. Suatu larutan mengandung dua komponen atau lebih yang disebut
Disusun Oleh: Anastasia Latif ( XI IPA 1 ) Christine ( XI IPA 1 ) Josephine Putri ( XI IPA 2 ) Kelvin Ricky (XI IPA 2 ) Patty Regina (XI IPA 1 )
 LAPORAN PRAKTIKUM KIMIA Asam dan Basa Disusun Oleh: Anastasia Latif ( XI IPA 1 ) Christine ( XI IPA 1 ) Josephine Putri ( XI IPA 2 ) Kelvin Ricky (XI IPA 2 ) Patty Regina (XI IPA 1 ) Windy Saputra ( XI
LAPORAN PRAKTIKUM KIMIA Asam dan Basa Disusun Oleh: Anastasia Latif ( XI IPA 1 ) Christine ( XI IPA 1 ) Josephine Putri ( XI IPA 2 ) Kelvin Ricky (XI IPA 2 ) Patty Regina (XI IPA 1 ) Windy Saputra ( XI
Bab VI Larutan Elektrolit dan Nonelektrolit
 Bab VI Larutan Elektrolit dan Nonelektrolit Sumber: Dokumentasi Penerbit Air laut merupakan elektrolit karena di dalamnya terdapat ion-ion seperti Na, K, Ca 2, Cl, 2, dan CO 3 2. TUJUAN PEMBELAJARAN Setelah
Bab VI Larutan Elektrolit dan Nonelektrolit Sumber: Dokumentasi Penerbit Air laut merupakan elektrolit karena di dalamnya terdapat ion-ion seperti Na, K, Ca 2, Cl, 2, dan CO 3 2. TUJUAN PEMBELAJARAN Setelah
Bab II Studi Pustaka
 Bab II Studi Pustaka II.1 Kelarutan Larutan adalah campuran yang bersifat homogen. Larutan yang menggunakan air sebagai pelarut dinamakan larutan dalam air. Larutan yang mengandung zat terlarut dalam jumlah
Bab II Studi Pustaka II.1 Kelarutan Larutan adalah campuran yang bersifat homogen. Larutan yang menggunakan air sebagai pelarut dinamakan larutan dalam air. Larutan yang mengandung zat terlarut dalam jumlah
LAPORAN PRAKTIKUM KIMIA DASAR I STOIKIOMETRI REAKSI
 LAPORAN PRAKTIKUM KIMIA DASAR I STOIKIOMETRI REAKSI Nama Anggota: Isrenna Ratu Rezky Suci 1157040029 Helmi Fauzi 1157040025 Fajar Gunawan 1157040022 Fresa Agustini 1157040024 JURUSAN KIMIA 1A FAKULTAS
LAPORAN PRAKTIKUM KIMIA DASAR I STOIKIOMETRI REAKSI Nama Anggota: Isrenna Ratu Rezky Suci 1157040029 Helmi Fauzi 1157040025 Fajar Gunawan 1157040022 Fresa Agustini 1157040024 JURUSAN KIMIA 1A FAKULTAS
kimia ASAM-BASA I Tujuan Pembelajaran
 KTSP & K-13 kimia K e l a s XI ASAM-BASA I Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami definisi dan sifat asam serta basa. 2. Memahami teori
KTSP & K-13 kimia K e l a s XI ASAM-BASA I Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami definisi dan sifat asam serta basa. 2. Memahami teori
INTRUKSI Kompetensi Dasar Indikator Sumber Belajar
 Lampiran 3 89 INTRUKSI 1. Setiap siswa harus membaca penuntun praktikum ini dengan seksama. 2. Setelah alat dan bahan siap tersedia, laksanakanlah percobaan menurut prosedur percobaan. 3. Setelah melakukan
Lampiran 3 89 INTRUKSI 1. Setiap siswa harus membaca penuntun praktikum ini dengan seksama. 2. Setelah alat dan bahan siap tersedia, laksanakanlah percobaan menurut prosedur percobaan. 3. Setelah melakukan
K13 Revisi Antiremed Kelas 11 Kimia
 K13 Revisi Antiremed Kelas 11 Kimia Stoikiometri Larutan - Soal Doc. Name: RK13AR11KIM0601 Doc. Version : 2016-12 01. Zat-zat berikut ini dapat bereaksi dengan larutan asam sulfat, kecuali... (A) kalsium
K13 Revisi Antiremed Kelas 11 Kimia Stoikiometri Larutan - Soal Doc. Name: RK13AR11KIM0601 Doc. Version : 2016-12 01. Zat-zat berikut ini dapat bereaksi dengan larutan asam sulfat, kecuali... (A) kalsium
PERCOBAAN 3 REAKSI ASAM BASA
 PERCOBAAN 3 REAKSI ASAM BASA I. Teori Dasar Kita sering menjumpai asam dan basa dalam kehidupan sehari-hari. Buah-buahan, seperti jeruk, apel, dll., mengandung asam. Amonia rumah tangga, bahan pembersih,
PERCOBAAN 3 REAKSI ASAM BASA I. Teori Dasar Kita sering menjumpai asam dan basa dalam kehidupan sehari-hari. Buah-buahan, seperti jeruk, apel, dll., mengandung asam. Amonia rumah tangga, bahan pembersih,
b. Mengubah Warna Indikator Selain rasa asam yang kecut, sifat asam yang lain dapat mengubah warna beberapa zat alami ataupun buatan.
 ASAM DAN BASA A. Asam Apa yang kamu ketahui tentang asam? Asam berkaitan dengan salah satu tanggapan indra pengecap kita terhadap suatu rasa masam. Kata asam berasal dari bahasa Latin, yaitu acidus yang
ASAM DAN BASA A. Asam Apa yang kamu ketahui tentang asam? Asam berkaitan dengan salah satu tanggapan indra pengecap kita terhadap suatu rasa masam. Kata asam berasal dari bahasa Latin, yaitu acidus yang
SOAL KIMIA 1 KELAS : XI IPA
 SOAL KIIA 1 KELAS : XI IPA PETUNJUK UU 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah soal dengan teliti sebelum Anda bekerja 3. Kerjakanlah soal anda pada lembar
SOAL KIIA 1 KELAS : XI IPA PETUNJUK UU 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah soal dengan teliti sebelum Anda bekerja 3. Kerjakanlah soal anda pada lembar
Reaksi Dan Stoikiometri Larutan
 A. PERSAMAAN REAKSI ION Reaksi Dan Stoikiometri Larutan Persamaan reaksi ion adalah persamaan reaksi yang menjelaskan bagaimana reaksi antar-ion terjadi pada elektrolit. Persamaan reaksi ion terdiri dari:
A. PERSAMAAN REAKSI ION Reaksi Dan Stoikiometri Larutan Persamaan reaksi ion adalah persamaan reaksi yang menjelaskan bagaimana reaksi antar-ion terjadi pada elektrolit. Persamaan reaksi ion terdiri dari:
Reaksi dan Stoikiometri Larutan
 Reaksi dan Stoikiometri Larutan A. PERSAMAAN REAKSI ION Persamaan reaksi ion adalah persamaan reaksi yang menjelaskan bagaimana reaksi antar-ion terjadi pada larutan elektrolit. Persamaan reaksi ion terdiri
Reaksi dan Stoikiometri Larutan A. PERSAMAAN REAKSI ION Persamaan reaksi ion adalah persamaan reaksi yang menjelaskan bagaimana reaksi antar-ion terjadi pada larutan elektrolit. Persamaan reaksi ion terdiri
Titrasi Volumetri. Modul 1 PENDAHULUAN
 Modul 1 Titrasi Volumetri Dr. Anna Permanasari, M.Si. K PENDAHULUAN egiatan praktikum ini dimaksudkan untuk melatih keterampilan dasar Anda dalam melakukan pekerjaan laboratorium, melatih Anda dalam bekerja
Modul 1 Titrasi Volumetri Dr. Anna Permanasari, M.Si. K PENDAHULUAN egiatan praktikum ini dimaksudkan untuk melatih keterampilan dasar Anda dalam melakukan pekerjaan laboratorium, melatih Anda dalam bekerja
Modul 1 Analisis Kualitatif 1
 Modul 1 Analisis Kualitatif 1 Indikator Alami I. Tujuan Percobaan 1. Mengidentifikasikan perubahan warna yang ditunjukkan indikator alam. 2. Mengetahui bagian tumbuhan yang dapat dijadikan indikator alam.
Modul 1 Analisis Kualitatif 1 Indikator Alami I. Tujuan Percobaan 1. Mengidentifikasikan perubahan warna yang ditunjukkan indikator alam. 2. Mengetahui bagian tumbuhan yang dapat dijadikan indikator alam.
KONSEP MOL DAN STOIKIOMETRI
 BAB V KONSEP MOL DAN STOIKIOMETRI Dalam ilmu fisika, dikenal satuan mol untuk besaran jumlah zat. Dalam bab ini, akan dibahas mengenai konsep mol yang mendasari perhitungan kimia (stoikiometri). A. KONSEP
BAB V KONSEP MOL DAN STOIKIOMETRI Dalam ilmu fisika, dikenal satuan mol untuk besaran jumlah zat. Dalam bab ini, akan dibahas mengenai konsep mol yang mendasari perhitungan kimia (stoikiometri). A. KONSEP
L A R U T A N _KIMIA INDUSTRI_ DEWI HARDININGTYAS, ST, MT, MBA WIDHA KUSUMA NINGDYAH, ST, MT AGUSTINA EUNIKE, ST, MT, MBA
 L A R U T A N _KIMIA INDUSTRI_ DEWI HARDININGTYAS, ST, MT, MBA WIDHA KUSUMA NINGDYAH, ST, MT AGUSTINA EUNIKE, ST, MT, MBA 1. Larutan Elektrolit 2. Persamaan Ionik 3. Reaksi Asam Basa 4. Perlakuan Larutan
L A R U T A N _KIMIA INDUSTRI_ DEWI HARDININGTYAS, ST, MT, MBA WIDHA KUSUMA NINGDYAH, ST, MT AGUSTINA EUNIKE, ST, MT, MBA 1. Larutan Elektrolit 2. Persamaan Ionik 3. Reaksi Asam Basa 4. Perlakuan Larutan
TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN
 TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN I. JUDUL PERCOBAAN : TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN II. TUJUAN PERCOBAAN : 1. Membuat dan
TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN I. JUDUL PERCOBAAN : TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN II. TUJUAN PERCOBAAN : 1. Membuat dan
Standar Kompetensi: Mendiskripsikan sifat-sifat larutan, metode pengukuran serta terapannya
 LARUTAN ASAM BASA Standar Kompetensi: Mendiskripsikan sifat-sifat larutan, metode pengukuran serta terapannya Kompetensi Dasar: Menyelidiki teori asam basa menurut Arrchenius, mengklasifikasi berbagai
LARUTAN ASAM BASA Standar Kompetensi: Mendiskripsikan sifat-sifat larutan, metode pengukuran serta terapannya Kompetensi Dasar: Menyelidiki teori asam basa menurut Arrchenius, mengklasifikasi berbagai
OAL TES SEMESTER II. I. Pilihlah jawaban yang paling tepat!
 KIMIA XI SMA 217 S OAL TES SEMESTER II I. Pilihlah jawaban yang paling tepat! 1. Basa menurut Arhenius adalah senyawa yang bila dilarutkan dalam air akan menghasilkan a. proton d. ion H b. elektron e.
KIMIA XI SMA 217 S OAL TES SEMESTER II I. Pilihlah jawaban yang paling tepat! 1. Basa menurut Arhenius adalah senyawa yang bila dilarutkan dalam air akan menghasilkan a. proton d. ion H b. elektron e.
Larutan Penyangga XI MIA
 Larutan Penyangga XI MIA Komponen Larutan Penyangga Larutan Penyangga Asam Terdiri dari Asam lemah dan basa konjugasinya (Contoh : CH 3 COOH dan CH 3 COO -, HF dan F - ) Cara membuatnya : 1. Mencampurkan
Larutan Penyangga XI MIA Komponen Larutan Penyangga Larutan Penyangga Asam Terdiri dari Asam lemah dan basa konjugasinya (Contoh : CH 3 COOH dan CH 3 COO -, HF dan F - ) Cara membuatnya : 1. Mencampurkan
Ensiklopedi: 27 dan 342. Asam, basa dan garam. dikelompokkan berdasarkan. Alat ukur
 BAB 2 ASAM, BASA DAN GARAM Ensiklopedi: 27 dan 342 Kompetensi Dasar: Mengelompokkan sifat larutan asam, larutan basa, dan larutan garam melalui alat dan indikator yang tepat. Melakukan percobaan sederhana
BAB 2 ASAM, BASA DAN GARAM Ensiklopedi: 27 dan 342 Kompetensi Dasar: Mengelompokkan sifat larutan asam, larutan basa, dan larutan garam melalui alat dan indikator yang tepat. Melakukan percobaan sederhana
Antiremed Kelas 11 Kimia
 Antiremed Kelas 11 Kimia Stoikiometri Larutan - Latihan Soal Doc. Name: AR11KIM0699 Doc. Version : 2012-07 01. Zat-zat berikut ini dapat bereaksi dengan larutan asam sulfat, kecuali... (A) kalsium oksida
Antiremed Kelas 11 Kimia Stoikiometri Larutan - Latihan Soal Doc. Name: AR11KIM0699 Doc. Version : 2012-07 01. Zat-zat berikut ini dapat bereaksi dengan larutan asam sulfat, kecuali... (A) kalsium oksida
Hubungan koefisien dalam persamaan reaksi dengan hitungan
 STOIKIOMETRI Pengertian Stoikiometri adalah ilmu yang mempelajari dan menghitung hubungan kuantitatif dari reaktan dan produk dalam reaksi kimia (persamaan kimia) Stoikiometri adalah hitungan kimia Hubungan
STOIKIOMETRI Pengertian Stoikiometri adalah ilmu yang mempelajari dan menghitung hubungan kuantitatif dari reaktan dan produk dalam reaksi kimia (persamaan kimia) Stoikiometri adalah hitungan kimia Hubungan
Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi. Bab 16. Asam dan Basa
 Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi Bab 16 Asam dan Basa Asam Memiliki rasa masam; misalnya cuka mempunyai rasa dari asam asetat, dan lemon serta buah-buahan sitrun
Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi Bab 16 Asam dan Basa Asam Memiliki rasa masam; misalnya cuka mempunyai rasa dari asam asetat, dan lemon serta buah-buahan sitrun
TITRASI DENGAN INDIKATOR GABUNGAN DAN DUA INDIKATOR
 TITRASI DENGAN INDIKATOR GABUNGAN DAN DUA INDIKATOR I. TUJUAN 1. Memahami prinsip kerja dari percobaan. 2. Menentukan konsentrasi dari NaOH dan Na 2 CO 3. 3. Mengetahui kegunaan dari titrasi dengan indikator
TITRASI DENGAN INDIKATOR GABUNGAN DAN DUA INDIKATOR I. TUJUAN 1. Memahami prinsip kerja dari percobaan. 2. Menentukan konsentrasi dari NaOH dan Na 2 CO 3. 3. Mengetahui kegunaan dari titrasi dengan indikator
STOIKIOMETRI LARUTAN. Andian Ari Anggraeni, M.Sc
 STOIKIOMETRI LARUTAN Andian Ari Anggraeni, M.Sc A.1. MASSA ATOM RELATIF (A r ) DAN MASSA MOLEKUL RELATIF (M r ) Dari percobaan diketahui bahwa perbandingan massa hidrogen dan oksigen dalam air adalah 1
STOIKIOMETRI LARUTAN Andian Ari Anggraeni, M.Sc A.1. MASSA ATOM RELATIF (A r ) DAN MASSA MOLEKUL RELATIF (M r ) Dari percobaan diketahui bahwa perbandingan massa hidrogen dan oksigen dalam air adalah 1
KIMIA (2-1)
 03035307 KIMIA (2-1) Dr.oec.troph.Ir.Krishna Purnawan Candra, M.S. Kuliah ke-9 Teori Asam Basa Bahan kuliah ini disarikan dari Chemistry 4th ed. McMurray and Fay Faperta UNMUL 2011 Pengertian Asam dan
03035307 KIMIA (2-1) Dr.oec.troph.Ir.Krishna Purnawan Candra, M.S. Kuliah ke-9 Teori Asam Basa Bahan kuliah ini disarikan dari Chemistry 4th ed. McMurray and Fay Faperta UNMUL 2011 Pengertian Asam dan
GALAT TITRASI. Ilma Nugrahani
 GALAT TITRASI Ilma Nugrahani Galat Titrasi Adalah galat yang terjadi karena indikator berubah warna sebelum atau sesudah titik setara ditunjukkan dari kurva titrasi titik akhir titik ekivalen. Dapat disebabkan
GALAT TITRASI Ilma Nugrahani Galat Titrasi Adalah galat yang terjadi karena indikator berubah warna sebelum atau sesudah titik setara ditunjukkan dari kurva titrasi titik akhir titik ekivalen. Dapat disebabkan
BAB III METODOLOGI PENELITIAN
 BAB III METODOLOGI PENELITIAN A. Lokasi dan Subjek Penelitian Penelitian ini dilakukan di salah satu SMA Negeri di Kota Bandung. Subjek penelitian ini adalah enam orang siswa SMA kelas XI IPA yang sudah
BAB III METODOLOGI PENELITIAN A. Lokasi dan Subjek Penelitian Penelitian ini dilakukan di salah satu SMA Negeri di Kota Bandung. Subjek penelitian ini adalah enam orang siswa SMA kelas XI IPA yang sudah
BAB VI REAKSI KIMIA. Reaksi Kimia. Buku Pelajaran IPA SMP Kelas IX 67
 BAB VI REAKSI KIMIA Pada bab ini akan dipelajari tentang: 1. Ciri-ciri reaksi kimia dan faktor-faktor yang mempengaruhi kecepatan reaksi kimia. 2. Pengelompokan materi kimia berdasarkan sifat keasamannya.
BAB VI REAKSI KIMIA Pada bab ini akan dipelajari tentang: 1. Ciri-ciri reaksi kimia dan faktor-faktor yang mempengaruhi kecepatan reaksi kimia. 2. Pengelompokan materi kimia berdasarkan sifat keasamannya.
ASAM, BASA DAN GARAM
 ASAM, BASA DAN GARAM Larutan terdiri dari zat terlarut (solute) dan pelarut (solvent). Dalam suatu larutan, jumlah pelarut lebih banyak dibandingkan jumlah zat terlarut. Penggolongan larutan dapat juga
ASAM, BASA DAN GARAM Larutan terdiri dari zat terlarut (solute) dan pelarut (solvent). Dalam suatu larutan, jumlah pelarut lebih banyak dibandingkan jumlah zat terlarut. Penggolongan larutan dapat juga
KIMIa ASAM-BASA II. K e l a s. A. Kesetimbangan Air. Kurikulum 2006/2013
 Kurikulum 2006/2013 KIMIa K e l a s XI ASAM-BASA II Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami kesetimbangan air. 2. Memahami pengaruh asam
Kurikulum 2006/2013 KIMIa K e l a s XI ASAM-BASA II Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami kesetimbangan air. 2. Memahami pengaruh asam
LAPORAN PRAKTIKUM KIMIA DASAR I
 LAPORAN PRAKTIKUM KIMIA DASAR I NAMA KELOMPOK : MELVIA PERMATASARI (08121006013) MELANY AMDIRA (08121006027) ANIS ALAFIFAH (08121006029) PUTRI WULANDARI (08121006071) MUTIARA BELLA (08121006073) JURUSAN
LAPORAN PRAKTIKUM KIMIA DASAR I NAMA KELOMPOK : MELVIA PERMATASARI (08121006013) MELANY AMDIRA (08121006027) ANIS ALAFIFAH (08121006029) PUTRI WULANDARI (08121006071) MUTIARA BELLA (08121006073) JURUSAN
tujuh1asam - - ASAM BASA GARAM - - Asam Basa Garam 7202 Kimia Les Privat dirumah bimbelaqila.com - Download Format Word di belajar.bimbelaqila.
 - - ASAM BASA GARAM - - Modul ini singkron dengan Aplikasi Android, Download melalui Play Store di HP Kamu, ketik di pencarian tujuh1asam Jika Kamu kesulitan, Tanyakan ke tentor bagaimana cara downloadnya.
- - ASAM BASA GARAM - - Modul ini singkron dengan Aplikasi Android, Download melalui Play Store di HP Kamu, ketik di pencarian tujuh1asam Jika Kamu kesulitan, Tanyakan ke tentor bagaimana cara downloadnya.
SIMULASI UJIAN NASIONAL 2
 SIMULASI UJIAN NASIONAL 2. Diketahui nomor atom dan nomor massa dari atom X adalah 29 dan 63. Jumlah proton, elektron, dan neutron dalam ion X 2+ (A) 29, 27, dan 63 (B) 29, 29, dan 34 (C) 29, 27, dan 34
SIMULASI UJIAN NASIONAL 2. Diketahui nomor atom dan nomor massa dari atom X adalah 29 dan 63. Jumlah proton, elektron, dan neutron dalam ion X 2+ (A) 29, 27, dan 63 (B) 29, 29, dan 34 (C) 29, 27, dan 34
LEMBAR AKTIVITAS SISWA ( LAS )
 LEMBAR AKTIVITAS SISWA ( LAS ) 1. Sebanyak 2 gram suatu logam alkali tanah dilarutkan dalam asam klorida menghasilan 1,25 liter gas hidrogen ( T,P ).Pada ( T,P ) yang sama 5,6 gram N 2 mempunyai volume
LEMBAR AKTIVITAS SISWA ( LAS ) 1. Sebanyak 2 gram suatu logam alkali tanah dilarutkan dalam asam klorida menghasilan 1,25 liter gas hidrogen ( T,P ).Pada ( T,P ) yang sama 5,6 gram N 2 mempunyai volume
LEMBAR SOAL. Mata pelajaran : Kimia. Kelas/Program : XI/IPA Hari, tanggal : Selasa, 8 April 2008 Alokasi waktu : 90 Menit
 DEPARTEMEN PENDIDIKAN NASIONAL UNIVERSITAS NEGERI SEMARANG FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM JURUSAN KIMIA Gedung D6. Kampus Sekaran Gunungpati Semarang 50229 Telp. 8508035 LEMBAR SOAL Mata
DEPARTEMEN PENDIDIKAN NASIONAL UNIVERSITAS NEGERI SEMARANG FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM JURUSAN KIMIA Gedung D6. Kampus Sekaran Gunungpati Semarang 50229 Telp. 8508035 LEMBAR SOAL Mata
Standar Kompetensi Kompetensi Dasar Nilai Indikator. Larutan Asam-Basa
 Model Pengintegrasian Nilai Pendidikan Karakter Standar Kompetensi Kompetensi Dasar Nilai Indikator 4. Memahami sifat-sifat larutan asam-basa, metode pengukuran, dan terapannya. 4.2 Menghitung banyaknya
Model Pengintegrasian Nilai Pendidikan Karakter Standar Kompetensi Kompetensi Dasar Nilai Indikator 4. Memahami sifat-sifat larutan asam-basa, metode pengukuran, dan terapannya. 4.2 Menghitung banyaknya
PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA
 PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA 1 Tujuan Percobaan Tujuan dari percobaan ini adalah menentukan kadar natrium karbonat dan natrium hidrogen karbonat dengan titrasi
PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA 1 Tujuan Percobaan Tujuan dari percobaan ini adalah menentukan kadar natrium karbonat dan natrium hidrogen karbonat dengan titrasi
PEMERINTAH KABUPATEN BANYUMAS DINAS PENDIDIKAN SMA NEGERI PATIKRAJA Jalan Adipura 3 Patikraja Telp (0281) Banyumas 53171
 PEMERINTAH KABUPATEN BANYUMAS DINAS PENDIDIKAN SMA NEGERI PATIKRAJA Jalan Adipura 3 Patikraja Telp (0281) 6844576 Banyumas 53171 ULANGAN KENAIKAN KELAS TAHUN PELAJARAN 2010/ 2011 Mata Pelajaran : Kimia
PEMERINTAH KABUPATEN BANYUMAS DINAS PENDIDIKAN SMA NEGERI PATIKRAJA Jalan Adipura 3 Patikraja Telp (0281) 6844576 Banyumas 53171 ULANGAN KENAIKAN KELAS TAHUN PELAJARAN 2010/ 2011 Mata Pelajaran : Kimia
Metodologi Penelitian
 Bab III Metodologi Penelitian Pembuatan larutan buffer menggunakan metode pencampuran antara asam lemah dengan basa konjugasinya. Selanjutnya larutan buffer yang sudah dibuat diuji kemampuannya dalam mempertahankan
Bab III Metodologi Penelitian Pembuatan larutan buffer menggunakan metode pencampuran antara asam lemah dengan basa konjugasinya. Selanjutnya larutan buffer yang sudah dibuat diuji kemampuannya dalam mempertahankan
A. TEORI ASAM DAN BASA B. INDIKATOR ASAM BASA C. MENGHITUNG ph LARUTAN ASAM BASA D. TITRASI ASAM BASA
 5 ASAM BASA A. TEORI ASAM DAN BASA B. INDIKATOR ASAM BASA C. MENGHITUNG ph LARUTAN ASAM BASA D. TITRASI ASAM BASA Buah-buahan seperti sirsak, jeruk, duku dan mangga, bagaimana rasanya? Berbeda bila secara
5 ASAM BASA A. TEORI ASAM DAN BASA B. INDIKATOR ASAM BASA C. MENGHITUNG ph LARUTAN ASAM BASA D. TITRASI ASAM BASA Buah-buahan seperti sirsak, jeruk, duku dan mangga, bagaimana rasanya? Berbeda bila secara
Laporan Praktikum Kimia Dasar II. Standarisasi Larutan NaOH 0,1 M dan Penggunaannya Dalam Penentuan Kadar Asam Cuka Perdagangan.
 Laporan Praktikum Kimia Dasar II Standarisasi Larutan NaOH 0,1 M dan Penggunaannya Dalam Penentuan Kadar Asam Cuka Perdagangan Oleh: Kelompok : I (satu) Nama Nim Prodi : Ardinal : F1D113002 : Teknik Pertambangan
Laporan Praktikum Kimia Dasar II Standarisasi Larutan NaOH 0,1 M dan Penggunaannya Dalam Penentuan Kadar Asam Cuka Perdagangan Oleh: Kelompok : I (satu) Nama Nim Prodi : Ardinal : F1D113002 : Teknik Pertambangan
Penambahan oleh sedikit asam-kuat (H + ) menyebabkan kesetimbangan. CH 3 COOH(aq) CH 3 COO - (aq) + H + (aq) (9.1) asam lemah
 Larutan bufer* merupakan sistem larutan yang dapat mempertahankan lingkungannya dari pengaruh seperti oleh penambahan sedikit asam/basa kuat, atau oleh pengenceran. Sistem bufer terdiri atas dua komponen,
Larutan bufer* merupakan sistem larutan yang dapat mempertahankan lingkungannya dari pengaruh seperti oleh penambahan sedikit asam/basa kuat, atau oleh pengenceran. Sistem bufer terdiri atas dua komponen,
2. Konfigurasi elektron dua buah unsur tidak sebenarnya:
 . Atom X memiliki elektron valensi dengan bilangan kuantum: n =, l =, m = 0, dan s =. Periode dan golongan yang mungkin untuk atom X adalah A. dan IIIB B. dan VA C. 4 dan III B D. 4 dan V B E. 5 dan III
. Atom X memiliki elektron valensi dengan bilangan kuantum: n =, l =, m = 0, dan s =. Periode dan golongan yang mungkin untuk atom X adalah A. dan IIIB B. dan VA C. 4 dan III B D. 4 dan V B E. 5 dan III
Titrasi asam kuat-basa kuat
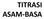 TITRASI ASAM-BASA KURVA TITRASI plot atau kurva antara ph atau poh terhadap volume titran untuk menguji apakah suatu reaksi dapat digunakan untuk analisa titrimetri ataukah tidak memilih indikator Titrasi
TITRASI ASAM-BASA KURVA TITRASI plot atau kurva antara ph atau poh terhadap volume titran untuk menguji apakah suatu reaksi dapat digunakan untuk analisa titrimetri ataukah tidak memilih indikator Titrasi
Silabus dan Rencana Pelaksanaan Pembelajaran (RPP)
 Endang Susilowati MODEL Silabus dan Rencana Pelaksanaan Pembelajaran (RPP) SAINS KIMIA Prinsip dan Terapannya untuk Kelas XI SMA dan MA Semester 2 Program Ilmu Pengetahuan Alam 2B Berdasarkan Permendiknas
Endang Susilowati MODEL Silabus dan Rencana Pelaksanaan Pembelajaran (RPP) SAINS KIMIA Prinsip dan Terapannya untuk Kelas XI SMA dan MA Semester 2 Program Ilmu Pengetahuan Alam 2B Berdasarkan Permendiknas
Bab 7. Stoikiometri Larutan dan Titrasi Asam Basa. A. Reaksi dalam Larutan B. Titrasi Asam Basa
 Bab 7 Stoikiometri Larutan dan Titrasi Asam Basa Hasil yang harus Anda capai: memahami sifat-sifat larutan asam basa, metode pengukuran, dan terapannya. Sumber: powerlabs.org Titrasi merupakan metode untuk
Bab 7 Stoikiometri Larutan dan Titrasi Asam Basa Hasil yang harus Anda capai: memahami sifat-sifat larutan asam basa, metode pengukuran, dan terapannya. Sumber: powerlabs.org Titrasi merupakan metode untuk
BAB II TINJAUAN PUSTAKA
 BAB II TINJAUAN PUSTAKA 2.1 Strategi Pembelajaran Belajar adalah proses bagi siswa dalam membangun gagasan atau pemahaman sendiri. Oleh karena itu kegiatan belajar mengajar hendaknya memberikan kesempatan
BAB II TINJAUAN PUSTAKA 2.1 Strategi Pembelajaran Belajar adalah proses bagi siswa dalam membangun gagasan atau pemahaman sendiri. Oleh karena itu kegiatan belajar mengajar hendaknya memberikan kesempatan
MODUL MATA PELAJARAN IPA
 KERJASAMA DINAS PENDIDIKAN KOTA SURABAYA DENGAN FAKULTAS MIPA UNIVERSITAS NEGERI SURABAYA MODUL MATA PELAJARAN IPA Sifat larutan, perubahan fisika, dan perubahan kimia untuk kegiatan PELATIHAN PENINGKATAN
KERJASAMA DINAS PENDIDIKAN KOTA SURABAYA DENGAN FAKULTAS MIPA UNIVERSITAS NEGERI SURABAYA MODUL MATA PELAJARAN IPA Sifat larutan, perubahan fisika, dan perubahan kimia untuk kegiatan PELATIHAN PENINGKATAN
Asam Basa dan Garam. Asam Basa dan Garam
 Asam Basa dan Garam Asam Basa dan Garam A Sifat Asam, Basa, dan Garam 1. Sifat asam Buah-buahan yang masih muda pada umumnya berasa masam. Sebenarnya rasa masam dalam buah-buahan tersebut disebabkan karena
Asam Basa dan Garam Asam Basa dan Garam A Sifat Asam, Basa, dan Garam 1. Sifat asam Buah-buahan yang masih muda pada umumnya berasa masam. Sebenarnya rasa masam dalam buah-buahan tersebut disebabkan karena
Teori Asam. Pengertian
 Teori Asam Pengertian Asam (yang sering diwakili dengan rumus umum HA) secara umum merupakan senyawa kimia yang bila dilarutkan dalam air akan menghasilkan larutan dengan ph lebih kecil dari 7. Dalam definisi
Teori Asam Pengertian Asam (yang sering diwakili dengan rumus umum HA) secara umum merupakan senyawa kimia yang bila dilarutkan dalam air akan menghasilkan larutan dengan ph lebih kecil dari 7. Dalam definisi
LOGO. Stoikiometri. Tim Dosen Pengampu MK. Kimia Dasar
 LOGO Stoikiometri Tim Dosen Pengampu MK. Kimia Dasar Konsep Mol Satuan jumlah zat dalam ilmu kimia disebut mol. 1 mol zat mengandung jumlah partikel yang sama dengan jumlah partikel dalam 12 gram C 12,
LOGO Stoikiometri Tim Dosen Pengampu MK. Kimia Dasar Konsep Mol Satuan jumlah zat dalam ilmu kimia disebut mol. 1 mol zat mengandung jumlah partikel yang sama dengan jumlah partikel dalam 12 gram C 12,
PENENTUAN KOMPOSISI MAGNESIUM HIDROKSIDA DAN ALUMINIUM HIDROKSIDA DALAM OBAT MAAG
 PENENTUAN KOMPOSISI MAGNESIUM HIDROKSIDA DAN ALUMINIUM HIDROKSIDA DALAM OBAT MAAG PENDAHULUAN Obat maag atau antasida adalah obat yang mengandung bahan-bahan yang efektif yang menetralkan asam dilambung.
PENENTUAN KOMPOSISI MAGNESIUM HIDROKSIDA DAN ALUMINIUM HIDROKSIDA DALAM OBAT MAAG PENDAHULUAN Obat maag atau antasida adalah obat yang mengandung bahan-bahan yang efektif yang menetralkan asam dilambung.
