PENAMBAHAN BUNGA ROSELLA (HIBISCUS SABDARIFFA L.)
|
|
|
- Doddy Halim
- 6 tahun lalu
- Tontonan:
Transkripsi
1 87 PENAMBAHAN BUNGA ROSELLA (HIBISCUS SABDARIFFA L.) PADA PAKAN TERHADAP KETAHANAN TUBUH IKAN GURAMI (OSPHRONEMUS GOURAMY) YANG DIUJI TANTANG DENGAN BAKTERI AEROMONAS HYDROPHILA SUPPLEMENTATION OF ROSELLA (HIBISCUS SABDARIFFA L.) IN THE FOOD AGAINST IMMUNITY OF GIANT GOURAMY (OSPHRONEMUS GOURAMY) FRY HAD BEEN CHALLENGED WITH AEROMONAS HYDROPHILA BACTERIA Annita Mustikhasary 1, Mulyana 1 dan Rosmawati 1 1 Jurusan Perikanan, Fakultas Pertanian, Universitas Djuanda Bogor ABSTRACT This research is aimed to know the dosage of rosella against immunity of giant gouramy fry had been challenged with Aeromonas hydrophila bacteria. The treatments are 0 g of rosella/kg of food (control), 10 g of rosella/kg of food, 20 g of rosella/kg of food, and 30 g of rosella/kg of food. The challenged test is done after the fishes had been given the food for 30 days. Each giant gouramy fry is injected by 10 6 cell of bacteria via intramuscular. Total leucocyte, hematocrite, phagocytic index, and mortality of giant gouramy fry had been evaluated. The result of research showed that the best of total leucocyte and hematocrite get from the fish had been given the 20 g dosage of rosella/kg of food, but phagocytic index, immunity, and fish mortality get from the fish had been given the 30 g dosage of rosella/kg of food. Supplementation of rosella in the food could increased immunity of giant gouramy fry. Key Words: Aeromonas hydrophila, giant gouramy fry, immunity, rosella. ABSTRAK Penelitian ini bertujuan untuk mengetahui dosis bunga rosella (Hibiscus sabdariffa L) terhadap ketahanan tubuh benih ikan gurami (Osphronemus gouramy) yang diuji tantang dengan bakteri Aeromonas hydrophila. Perlakuan yang diberikan yaitu: (A) pakan tanpa penambahan bunga Rosella, (B) pakan dengan penambahan bunga Rosella 10 g/kg, (C) pakan dengan penambahan bunga Rosella 20 g/kg, dan (D) pakan dengan penambahan bunga Rosella 30 g/kg. Uji tantang dilakukan setelah ikan uji diberi pakan sesuai perlakuan selama 30 hari. Setiap benih ikan gurami disuntik dengan 10 6 sel bakteri via intramuskular, Parameter yang diamati adalah total leukosit, indeks pagosit, kadar hematokrit serta mortalitas. Hasil penelitian menunjukkan bahwa total sel darah putih daan hematokrit terbaik diperoleh pada ikan yang diberi 20 g rosella/kg pakan, tetapi fagositik indeks, imunitas dan mortalitas terbaik diperoleh pada ikan yang diberi 30 g rosella/kg pakan. Penambahan rosella ke dalam pakan dapat meningkatkan imunitas benih ikan gurami. Kata Kunci: Aeromonas hydrophila, benih ikan gurami, imunitas, rosella.
2 88 PENDAHULUAN Latar Belakang Indonesia merupakan negara kepulauan yang wilayahnya mencakup 70% perairan yang terdiri dari sungai, rawa, danau, tambak, dan laut. Kekayaan alam ini merupakan salah satu kesempatan besar bagi pengembangan perikanan, baik perikanan darat maupun perikanan laut. Berbagai macam hasil perikanan merupakan sumber bahan makanan berprotein tinggi yang sangat berguna untuk memenuhi kebutuhan gizi penduduk Indonesia (Sutisna dan Sutarmanto 1995). Budidaya ikan secara intensif semakin berkembang sejalan dengan meningkatnya permintaan ikan sebagai sumber protein hewani. Ikan gurami (Osphronemus gouramy) adalah salah satu ikan ekonomis penting yang menjadi sasaran utama peningkatan produksi dan pendapatan budidaya ikan air tawar di Indonesia. Faktorfaktor yang mempengaruhi keberhasilan sistem budidaya adalah sistem pemeliharaan, nutrisi, kualitas benih, kualitas air, dan serangan hama dan penyakit. Salah satu penyakit yang ditakuti oleh para pembudidaya ikan adalah penyakit bercak merah atau Motile Aeromonas Septicemia yang disebabkan oleh bakteri Aeromonas hydrophila. Bakteri ini sering menyerang ikan budidaya air tawar seperti mas, gurami, nila, dan ikan-ikan peliharaan dalam akuarium (Bullock et al. 1971). Ikan yang terserang bakteri ini akan mengalami pendarahan pada bagian tubuh terutama di bagian dada, perut, dan pangkal sirip. Penyakit yang disebabkan oleh bakteri Aeromonas hydrophila ini mudah menular. Penyebaran penyakit ini yaitu melalui air yang telah terkontaminasi Aeromonas hydrophila atau penularan dari ikan yang sakit. Penyakit ikan disebabkan adanya interaksi yang tidak serasi antara ikan, patogen dan lingkungan, sehingga menyebabkan stres pada ikan dan mengakibatkan melemahnya pertahanan tubuh sehingga penyakit mudah menginfeksi. Penyakit bakterial dapat diobati menggunakan antibiotika. Namun, penggunaan antibiotika yang tidak tepat dapat menimbulkan resistensi bakteri terhadap antibiotika tersebut dan dampak dari bahaya residu antibiotika. Untuk menghindari hal tersebut dapat diupayakan melalui peningkatan kekebalan tubuh. Salah satu cara untuk meningkatkan kekebalan tubuh ikan adalah dengan penambahan immunostimulan pada ikan. Beberapa vitamin seperti vitamin A, B dan vitamin C juga dapat digunakan sebagai imunostimulan. Berbagai kandungan yang terdapat dalam tanaman rosella membuatnya populer sebagai tanaman obat tradisional. Kandungan vitamin dalam bunga rosella cukup lengkap, yaitu vitamin A, C, D, B1, dan B2. Bahkan kandungan vitamin C atau asam askorbat diketahui 3 kali lebih banyak dari anggur hitam, 9 kali dari jeruk sitrus, 10 kali
3 89 dari buah belimbing, dan 2,5 kali dari jambu biji. Vitamin C merupakan salah satu antioksidan penting (Tanjung 2011). Oleh sebab itu perlu dikaji penambahan rosella dalam pakan untuk meningkatkan ketahanan tubuh ikan. Tujuan Penelitian Penelitian ini bertujuan untuk mengetahui dosis bunga rosella (Hibiscus sabdariffa L) terhadap ketahanan tubuh benih ikan gurami (Osphronemus gouramy Lac.) yang diuji tantang dengan bakteri Aeromonas hydrophila. Hipotesis Semakin tinggi dosis bunga rosella pada pakan akan meningkatkan ketahanan tubuh ikan gurami (Osphronemus gouramy Lac.) terhadap infeksi Aeromonas hydrophila. MATERI DAN METODE Waktu dan Tempat Penelitian ini dilakukan pada bulan April-September 2012, bertempat di Laboratorium Perikanan, Universitas Djuanda Bogor. Untuk pengujian darah dilakukan di Laboratorium Kesehatan Ikan, Fakultas Perikanan dan Ilmu Kelautan IPB, Bogor. Alat dan Bahan Wadah yang digunakan untuk kegiatan penelitian ini antara lain dua belas unit akuarium dengan ukuran 50 x 30 x 30 cm³, blower, timbangan elektrik digital Hitachi dengan ketelitian 0,01 gram, thermometer air raksa, heater dan lampu 50 watt. Adapun alat tambahan yang digunakan untuk menghaluskan bunga rosella yaitu oven, blender, wadah dan saringan 100 mesh, cawan petri, sentrifuse, jarum ose, gelas objek, mikropipet, penggaris, alat bedah, tabung mikrohematokrit, critoseal, sentrifuge, haemositometer, kaca penutup, mikroskop, eppendorf, dan inkubator. Bahan lain digunakan untuk analisis kualitas air (ph, oksigen terlarut, CO2 dan NH3). Bahan yang digunakan adalah bunga rosella, benih ikan gurami sebanyak 300 ekor dengan ukuran 3-4 gram, pelet komersil (hiprovit), akuades, larutan turks, suspensi Staphylococcus aureus, metanol, pewarna giemsa, dan bakteri Aeromonas hydrophila yang berasal dari Balai Penelitian Perikanan Air Tawar Sempur Bogor. Prosedur Penelitian Tahap persiapan dimulai dengan membersihkan semua akuarium dengan menggunakan air bersih dan dijemur selama 24 jam. Setelah kering, akuarium diletakkan pada rak kayu dan diisi air sebanyak 34 liter dengan menggunakan air tandon. Setelah akuarium terisi air selanjutnya pemasangan instalasi aerasi untuk meningkatkan kandungan oksigen terlarut (DO) dalam air kemudian memasang heater dan lampu 50 watt untuk menstabilkan suhu dalam akuarium.
4 90 Benih ikan gurami yang baru datang kemudian diadaptasi terhadap pakan dan lingkungannya selama 1 minggu di dalam tandon sebelum ikan dimasukkan kedalam akuarium uji. Selama masa adaptasi, ikan diberi pakan pellet komersil dengan frekuensi pemberian pakan 2 kali sehari yaitu pada pagi dan sore hari yaitu jam WIB dan WIB. Untuk menjaga kualitas air, dilakukan penyiponan dan pergantian air satu kali sehari. Setelah masa adaptasi, ikan diseleksi dan ditimbang sebanyak 25 ekor ikan per akuarium. Ikan dipelihara selama 30 hari dan selama pemeliharaan ikan diberi pakan sesuai dengan perlakuan, diberikan secara ad libitum atau sampai sekenyang-kenyangnya dengan frekuensi pemberian pakan dua kali sehari, yaitu pada jam dan WIB. Kualitas air merupakan faktor yang paling penting dalam budidaya ikan sebab air diperlukan sebagai media hidup ikan. Air yang digunakan berasal dari sumber air tanah yang kemudian diendapkan terlebih dahulu selama tiga hari dan diberikan aerasi. Untuk menjaga kualitas air di dalam akuarium percobaan tetap stabil, maka dilakukan penyiponan setiap hari dan penambahan air. Penyiponan dilakukan dengan cara mengangkat sisa pakan dan kotoran hasil metabolisme benih ikan gurami sebanyak 70 % dari jumlah total air per akuarium percobaan dan penambahan air sebanyak jumlah total air per akuarium yang disipon. Penyiponan dilakukan pada jam WIB sebelum pemberian pakan pertama diberikan. Suhu media pemeliharaan diusahakan konstan antara C, dan untuk menjaga suhu media pemeliharaan dipasang lampu 50 watt dan heater pada setiap akuarium percobaan. Uji Tantang Setelah semua ikan uji memperoleh perlakuan pemberian pellet selama 30 hari yang mengandung rosella dengan dosis yang berbeda kemudian dilakukan uji tantang. Sebelum dilakukan uji tantang, ikan diambil darahnya untuk mengetahui gambaran darah (total leukosit, indeks pagositik, kadar hematokrit) sebelum uji tantang. Ikan kemudian diuji tantang yaitu dengan menyuntikkan bakteri Aeromonas hydrophila 10 7 /ml secara intra muscular yaitu pada otot punggung ikan sebanyak 0,1 ml. Ikan yang telah disuntik dimasukkan kembali ke dalam akuarium untuk pengamatan selama 24 jam terhadap ikan-ikan yang telah terinfeksi dan mortalitas. Dua puluh empat jam setelah uji tantang dilakukan kembali uji darah untuk mengetahui gambaran darah ikan setelah uji tantang. Parameter Pengamatan Pengukuran Kadar Hematokrit (Anderson dan Siwicky, 1993) Sampel darah ikan dihisap menggunakan tabung mikrohematokrit berlapis heparin dengan kapiler. Fungsi
5 91 heparin adalah untuk mencegah pembekuan darah di dalam tabung (Amlacher 1970). Setelah darah mencapai ¾ bagian tabung, kemudian salah satu ujung tabung disumbat dengan critoseal. Tabung kapiler yang berisi darah kemudian disentrifusi pada 600 rpm selama 5 menit. Pengukuran dilakukan dengan membandingkan volume sel darah terhadap volume seluruh darah dengan menggunakan skala hematokrit. Total Leukosit (Blaxhall and Daisley 1973) Perhitungan dilakukan dengan mengencerkan darah dengan larutan Turks di dalam pipet pemcampuran berskala maksimum 11. Darah dicampur dengan pipet pencampur hingga skala 0,5 kemudian pipet yang sama dihisap larutan Turks hingga skala 11. Pipet kemudian digoyang membentuk angka delapan selama 3-5 menit agar tercampur secara merata. Sebelum dilakukan perhitungan, larutan pada ujung pipet yang tidak teraduk dibuang, tetesan berikutnya dimasukkan ke dalam haemositometer yang telah dilengkapi dengan kaca penutup kemudian diamati di bawah mikroskop. Indeks Fagositik (Anderson and Siwicky 1993) Pengukuran indeks fagositik dilakukan dengan cara: sebanyak 50 µl sampel darah dimasukkan ke dalam eppendorf, ditambahkan 50 µl suspensi Staphylococcus aureus dalam PBS (10 8 sel/ml). Sampel darah dihomogenkan dan diinkubasi dalam suhu ruang selama 20 menit. Selanjutnya 5 µl sampel darah dibuat sediaan ulas dan dikeringudarakan, kemudian difiksasi dengan metanol selama 5 menit dan dikeringkan. Sediaan ulas direndam dalam pewarna Giemsa selama 15 menit, kemudian dicuci dengan air mengalir dan dikeringkan dengan tissue. Selanjutnya dihitung jumlah sel yang menunjukkan proses fagositosis dari 100 sel fagosit yang diamati dengan rumus : Indeks fagositik = {(Jumlah sel fagosit yang melakukan fagositosis) / (jumlah sel fagosit)} x 100% Mortalitas Menghitung mortalitas menggunakan rumus sebagai berikut : Mo = Mt x 100% No Keterangan : Mo = tingkat kematian ikan (ekor) Mt = jumlah ikan mati (ekor) No = populasi ikan pada hari ke-0 (ekor) Rancangan Percobaan Rancangan percobaan yang digunakan pada penelitian ini adalah Rancangan Acak Lengkap (RAL), dengan 4 perlakuan dan 3 ulangan. Satu satuan percobaan adalah satu akuarium yang diisi air sebanyak 34 liter dengan jumlah ikan setiap akuarium sebanyak 25 ekor, yang diberikan adalah dosis rosella yang berbeda dan masing-masing perlakuan diulang 3 kali. Perlakuan yang diberikan yaitu :
6 92 1. Perlakuan A : pakan tanpa penambahan bunga Rosella 2. Perlakuan B : pakan dengan penambahan bunga Rosella 10 g/kg 3. Perlakuan C : pakan dengan penambahan bunga Rosella 20 g/kg 4. Perlakuan D : pakan dengan penambahan bunga Rosella 30 g/kg Model persamaan linier berdasarkan Steel dan Torrie (1991). Yij = µ + δi + εij J = Ulangan (j = 1,2,3) Analisa Data Mortalitas dan gambaran darah dianalisis secara deskriptif. HASIL DAN PEMBAHASAN Mortalitas Ikan Pasca Penyuntikan Dengan Bakteri Aeromonas hydrophila Ketahanan ikan gurame dapat dilihat melalui perkembangan tingkat kematian ikan gurame setelah diuji tantang dengan bakteri Keterangan : Yij = Data hasil pengamatan pada perlakuan ke-i dan ulangan ke-j Aeromonas hydrophila. Adapun perkembangan tingkat kematian ikan gurame pasca µ = Nilai tengah dari populasi δi = Pengaruh perlakuan ke-i penyuntikan dengan bakteri Aeromonas εij = Galat perlakuan ke-i dan ulangan ke-j i = Perlakuan (i = A,B,C,D) hydrophila dapat dilihat pada Tabel 1 di bawah ini. Tabel 1 Perkembangan tingkat kematian ikan gurame pasca penyuntikan dengan Ikan mati pasca injeksi Aeromonas hydrophila (ekor) Perlakuan A1 A2 A3 B1 B2 B3 C1 C2 C3 D1 D2 D3 H1-H2 H3 1 H H H H H H H H H H H H H16 1 H H18 1 H19 1 H20 1 H21-H23 H24 2 Jumlah
7 93 Kematian ikan pertama terjadi pada jam ke-3 setelah uji tantang. Hasil pengamatan tingkat kematian ikan dari jam ke-3 sampai jam ke-24 semakin tinggi. Setelah dilakukan uji tantang menggunakan bakteri Aeromonas hydrophila melalui penyuntikan secara intramuscular, mortalitas ikan gurame mencapai lebih dari 50 persen pada 6 jam pasca penyuntikan pada perlakuan A, pada 10 jam pasca penyuntikan pada perlakuan B, pada 11 jam pasca penyuntikan pada perlakuan C, dan pada 14 jam pasca penyuntikan pada perlakuan D. Mortalitas ikan gurami mencapai lebih dari 75 persen pada 12 jam pasca penyuntikan pada perlakuan A, pada 13 jam pasca penyuntikan pada perlakuan B dan C, dan pada 17 jam pasca penyuntikan pada perlakuan D. Mortalitas ikan gurami mencapai 100 persen terjadi dalam waktu 24 jam pasca penyuntikan pada perlakuan A, B dan C, dan lebih dari 24 jam pasca penyuntikan pada perlakuan D. Penggunaan pemberian bunga rosella yang ditambahkan ke dalam pakan ikan gurami pada perlakuan A terkontrol, 10 g/kg pakan pada perlakuan B, 20 g/kg pakan pada perlakuan C dan 30 g/kg pakan pada perlakuan D, ternyata telah memberikan rangsangan bagi sel darah putih ikan gurami untuk meningkatkan ketahanan ikan serhadap serangan infeksi bakteri Aeromonas hydrophila melalui peningkatan antibodi. Hasil tersebut dapat dilihat dari mortalitas setiap perlakuan (Tabel 2), yakni semakin rendah dosis pemberian rosella maka mortalitas akan semakin tinggi dan sebaliknya semakin besar dosis yang diberikan maka mortalitas ikan akan semakin rendah. Sel Darah Putih (Lekosit) dan Hematokrit Total lekosit dan hematokrit pada ikan gurami sebelum dan setelah uji tantang dengan bakteri Aeromonas hydrophila dapat dilihat pada Tabel 2 di bawah ini.
8 94 Tabel 2 Total lekosit dan hematokrit pada ikan gurami sebelum dan setelah uji tantang dengan bakteri Aeromonas hydrophila Perlakuan Total Leukosit Hematokrit (%) (sel/mm 3 ) Sebelum Setelah uji Sebelum uji Setelah uji uji tantang tantang tantang tantang A ,82 A ,66 A ,93 Rataan ,80 B ,87 B ,66 B ,04 Rataan ,19 C ,93 C ,14 C ,07 Rataan ,38 D ,21 7,14 D ,50 D ,60 7,14 Rataan ,10 7,14 Hasil penelitian menunjukkan rataan total sel darah putih pada perlakuan A sebesar 864 sel/mm 3, pada perlakuan B 771 sel/mm 3, pada perlakuan C 855 sel/mm 3, dan pada perlakuan D 730 sel/mm 3, nilai ini sangat rendah karena ikan mengalami stres. Setelah dilakukan uji tantang rataan total leukosit pada perlakukan D 970 sel/mm 3 (Tabel 2). Terjadinya peningkatan jumlah leukosit dapat dijadikan sebagai tanda adanya infeksi, stres ataupun leukemia. Adanya infeksi akan menyebabkan inflamasi yang merupakan karakteristik tanggap kebal nonspesifik. Respon serupa juga akan muncul akibat adanya beberapa faktor seperti trauma, bahan kimia, toksin, parasit, bakteri, dan virus (Anderson dan Siwicki 1993). Hasil percobaan memperlihatkan bahwa rataan kadar hematokrit sebelum uji tantang adalah perlakuan A 16,80%, B 19,19%, C 20,38 %, D 14,10%, dan setelah uji tantang nilai kadar hematokrit lebih rendah dari 22% yakni 7,14%, ini menunjukkan bahwa ikan gurami yang terdapat dalam wadah percobaan diduga kuat terdapat dalam keadaan stress dan dianggap mengalami anemia. Penurunan hematokrit merupakan petunjuk akan rendahnya kandungan protein pakan, defisiensi vitamin atau ikan terkena
9 95 infeksi. Sedangkan peningkatan kadar hematokrit menunjukkan bahwa ikan dalam keadaan stress. Menurut Anisha dkk (2012)hasil pengukuran hematokrit ikan gurami sakit memiliki nilai yang rendah (dibawah 22%) hal ini diduga karena ikan berada dalam keadaan sakit. Hal ini didukung oleh pendapat Randal (1970) dalam Dopongtanung (2008) dalam Anisha dkk (2012) yangmenyatakan bahwa bila nilai hematokrit ikan di bawah 22% menunjukkan bahwa ikan mengalami anemia dan kemungkinan mengalami infeksi penyakit bakteri. Indeks Pagositik Indeks pagositik yang diperoleh sebelum dan sesudah uji tantang dengan Aeromonas hydrophila tercantum pada Tabel 3 di bawah ini. Tabel 3 Indeks pagositik sebelum dan setelah uji tantang dengan Aeromonas hydrophila Perlakuan Indeks Pagositik (%) Sebelum uji tantang Setelah uji tantang A1 3 A2 3 A3 3 B1 3 B2 3 B3 3 C1 5 C2 5 C3 5 D1 7 - D2 7 D3 6 - Hasil penelitian menunjukkan indeks fagositik ikan gurami yang diberi rosella berkisar antara 3-7 % dan ada peningkatan pada perlakuan C dan D dibandingkan dengan kontrol walaupun nilai ini masih belum optimal karena nilainya masih rendah. Menurut Brown dalam Zakki (2007), meningkatnya indeks fagositik menunjukkan adanya peningkatan kekebalan tubuh yaitu peningkatan kekebalan tubuh dapat diketahui dari peningkatan aktivitas sel fagosit dari hemosit. Sel fagosit berfungsi untuk melakukan fagositosis terhadap benda asing yang masuk ke dalam tubuh inang. Fagositosis adalah
10 96 ingesti bahan partikel terutama bakteri ke dalam sitoplasma sel darah. Pola peningkatan persentase indeks fagositik ini merupakan fungsi dari peningkatan total leukosit maupun prosentase jenis leukosit masing-masing pada limfosit, monosit, dan neutrophil (Amrullah 2004 dalam Zakki 2007) Sedangkan menurut Spector (1993) dalam Mudjiutami dkk (2002) proses fagositosis terjadi apabila kontak antara partikel dengan permukaan sel fagosit. Membran sel kemudian mengalami invaginasi dimana dua lengan sitoplasma menelan partikel sehingga terkurung dalam sitoplasma sel, terletak dalam vakuola yang dilapisi membran (fagosom). Lisosom yang ada di dekatnya melebur ke dalam fagosom dan mengeluarkan enzim-enzim membentuk fagolisosom atau lisosom sekunder sehingga bakteri atau partikel tersebut mati dan hancur dalam sel fagositosis tersebut. Kualitas Air Data parameter kualitas air selama percobaan disajikan pada Tabel 4 di bawah ini. Tabel 4 Kisaran hasil kualitas air selama penelitian Parameter Kualitas Air Perlakuan A B C D Tandon Suhu ( 0 C) DO (ppm) 4,2 4,4 3,8 3,5 2,9 ph 5,5 5,4 5,0 5,0 5,0 Amoniak (ppm) 0,027 0,035 0,037 0,037 0,0012 CO2 (ppm) 7,49 8,79 8,93 8,99 8,95 Rendahnya nilai ph 5,0 5,5 pada percobaan ini menyebabkan ikan stres karena menurut Susanto (1987), ph yang sesuai untuk semua jenis ikan berkisar antara 6,7 8,6. Sedangkan menurut Cholik et al. (1986) dalam Hastuti (2010) ikan akan mati pada kondisi ph lebih kecil dari 4 dan lebih besar dari 11 karena ph yang demikian itu bersifat toksik pada ikan dan menyebabkan ikan mati. Nilai ph yang rendah bukan disebabkan karena adanya penambahan rosella, tetapi sumber air yang berasal dari sumur yang memiliki ph rendah yaitu sebesar 5. Menurut Hickling (1962) dalam Sriharti (1992), batas minimum toleransi ikan air tawar pada umumnya adalah ph 4 dan batas
11 97 maksimum 11. Kadar karbondioksida yang diperuntukkan bagi kepentingan perikanan sebaiknya mengandung kadar karbondioksida bebas < 5 mg/l. Karbondioksida bebas sebesar 10 mg/l masih dapat ditolerir oleh organisme akuatik, asal disertai dengan kadar oksigen yang cukup (Effendi 2003). KESIMPULAN Berdasarkan hasil penelitian yang dilakukan, semakin tinggi dosis bunga rosella pada pakan akan meningkatkan sistem ketahanan tubuh bagi ikan gurami yang terinfeksi bakteri Aeromonas hydrophilla. Total rataan leukosit yang masih rendah, namun terjadi peningkatan setelah uji tantang sebagai tanda adanya infeksi. Rataan kadar hematokrit dan indeks pagositik masih rendah dikarenakan kondisi ikan stres. Adapun penyebab stres pada ikan dikarenakan ph air rendah. DAFTAR PUSTAKA Anderson DP, Siwicky AK Basic Haematology and Serology for Fish Health Program. Paper Presented in Second Symposium on Disease in Asia Aquaculture Aquatic Animal Health and Enviroment, Phuket, Thailand Minaka A, Sarjito, Hastuti S Identifikasi Agensia Penyebab dan Profil Darah Ikan Gurami (Osphronemus gouramy) yang Terserang Penyakit Bakteri. Fakultas Perikanan dan Ilmu Kelautan, Universitas Diponegoro. Journal of Aquaculture Management and Technology 1 (1): Baxhall PC, Daisley KW Routine haematological methods for use with fish blood. Fish Biology 5: Effendi H Telaah Kualitas Air. Yogyakarta: Kanisius. Mudjiutami E, Ciptoroso, Zainun Z, Sumarjo, Rahmat Pemanfaatan Immunostimulan Untuk Pengendalian Penyakit Pada Ikan Mas. Jurnal Budidaya Air Tawar 4 (1):1-9. Sriharti Budidaya Ikan. Balai Pengembangan Teknologi Tepat Guna P3FT-LIPI. Subang Sutisna HD, Sutarmanto R Pembenihan Ikan Air Tawar. Yogjakarta: Kanisius. Tanjong A Pengaruh Konsentrasi Ekstrak Kelopak Bunga Rosella (Hibiscus sabdariffa L) Terhadap Koloni Candida albicans yang Terdapat Pada Plat Gigi Tiruan. Skripsi. Fakultas Kedokteran Gigi. Universitas Hasanudin. Makasar. Zainun Z Pengamatan Parameter Hematologis Pada Ikan Mas Yang Diberi Immunostimulan. Jurnal Balai Besar Pengembangan Budidaya Ikan Air Tawar Sukabumi. Sukabumi
26 Mulyana et al. Bunga rosela dan ketahanan ikan gurami
 26 Mulyana et al. Bunga rosela dan ketahanan ikan gurami PENAMBAHAN BUNGA ROSELA (Hibiscus sabdariffa L.) PADA PAKAN TERHADAP KETAHANAN TUBUH IKAN GURAMI (Osphronemus gouramy) YANG DIUJI TANTANG DENGAN
26 Mulyana et al. Bunga rosela dan ketahanan ikan gurami PENAMBAHAN BUNGA ROSELA (Hibiscus sabdariffa L.) PADA PAKAN TERHADAP KETAHANAN TUBUH IKAN GURAMI (Osphronemus gouramy) YANG DIUJI TANTANG DENGAN
III. BAHAN DAN METODE
 III. BAHAN DAN METODE 3.1 Waktu Pelaksanaan Penelitian ini dilaksanakan pada bulan Mei sampai September 2009. Penelitian dilakukan di Laboratorium Kesehatan Ikan dan Laboratorium Lapangan, Departemen Budidaya
III. BAHAN DAN METODE 3.1 Waktu Pelaksanaan Penelitian ini dilaksanakan pada bulan Mei sampai September 2009. Penelitian dilakukan di Laboratorium Kesehatan Ikan dan Laboratorium Lapangan, Departemen Budidaya
III. METODOLOGI 3.1. Waktu dan Tempat 3.2. Alat dan Bahan Metode Penelitian Persiapan Wadah
 III. METODOLOGI 3.1. Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Juli hingga Desember 2007. Bertempat di Laboratorium Kesehatan Ikan, Departemen Budidaya Perairan, Fakultas Perikanan dan Ilmu
III. METODOLOGI 3.1. Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Juli hingga Desember 2007. Bertempat di Laboratorium Kesehatan Ikan, Departemen Budidaya Perairan, Fakultas Perikanan dan Ilmu
II. BAHAN DAN METODE 2.1 Prosedur kerja Kemampuan puasa ikan Tingkat konsumsi oksigen Laju ekskresi amoniak
 II. BAHAN DAN METODE Kegiatan penelitian ini terbagi dalam dua tahap yaitu tahap penelitian pendahuluan dan tahap utama. Penelitian pendahuluan meliputi hasil uji kapasitas serap zeolit, kapasitas serap
II. BAHAN DAN METODE Kegiatan penelitian ini terbagi dalam dua tahap yaitu tahap penelitian pendahuluan dan tahap utama. Penelitian pendahuluan meliputi hasil uji kapasitas serap zeolit, kapasitas serap
III. MATERI DAN METODE PENELITIAN. Penelitian ini dilaksanakan pada bulan September sampai Oktober 2011, di
 III. MATERI DAN METODE PENELITIAN A. Waktu dan Tempat Penelitian ini dilaksanakan pada bulan September sampai Oktober 2011, di Laboratorium Budidaya Perairan Fakultas Pertanian Universitas Lampung. B.
III. MATERI DAN METODE PENELITIAN A. Waktu dan Tempat Penelitian ini dilaksanakan pada bulan September sampai Oktober 2011, di Laboratorium Budidaya Perairan Fakultas Pertanian Universitas Lampung. B.
METODE PENELITIAN. Penelitian ini dilaksanakan pada bulan Februari sampai dengan April 2015 di
 III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan Februari sampai dengan April 2015 di Laboratorium Perikanan Program Studi Budidaya Perairan Fakultas Pertanian
III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan Februari sampai dengan April 2015 di Laboratorium Perikanan Program Studi Budidaya Perairan Fakultas Pertanian
III. METODE PENELITIAN. Penelitian ini dilaksanakan pada bulan Mei-Juni Lokasi penelitian di
 23 III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan Mei-Juni 2014. Lokasi penelitian di Laboratorium Budidaya Perikanan, Jurusan Budidaya Perairan, Fakultas
23 III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan Mei-Juni 2014. Lokasi penelitian di Laboratorium Budidaya Perikanan, Jurusan Budidaya Perairan, Fakultas
Lampiran 1. Road-map Penelitian
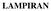 LAMPIRAN Lampiran 1. Road-map Penelitian Persiapan Penelitian Persiapan wadah dan ikan uji Bak ukuran 40x30x30cm sebanyak 4 buah dicuci, didesinfeksi, dan dikeringkan Diletakkan secara acak dan diberi
LAMPIRAN Lampiran 1. Road-map Penelitian Persiapan Penelitian Persiapan wadah dan ikan uji Bak ukuran 40x30x30cm sebanyak 4 buah dicuci, didesinfeksi, dan dikeringkan Diletakkan secara acak dan diberi
BAB III BAHAN DAN METODE
 BAB III BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini terdiri dari dua tahap, tahap pertama dilaksanakan di laboratorium bioteknologi Fakultas Perikanan dan Ilmu Kelautan Unpad, tahap
BAB III BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini terdiri dari dua tahap, tahap pertama dilaksanakan di laboratorium bioteknologi Fakultas Perikanan dan Ilmu Kelautan Unpad, tahap
II. METODOLOGI 2.1 Penyediaan Bakteri Probiotik 2.2 Ekstraksi Oligosakarida/Prebiotik
 II. METODOLOGI 2.1 Penyediaan Bakteri Probiotik Bakteri probiotik yang digunakan dalam penelitian ini adalah bakteri NP5, yang merupakan bakteri dari genus Bacillus. Bakteri NP5 ini merupakan bakteri yang
II. METODOLOGI 2.1 Penyediaan Bakteri Probiotik Bakteri probiotik yang digunakan dalam penelitian ini adalah bakteri NP5, yang merupakan bakteri dari genus Bacillus. Bakteri NP5 ini merupakan bakteri yang
III. METODE PENELITIAN. Penelitian dilaksanakan pada bulan Agustus sampai Oktober 2011, di
 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian dilaksanakan pada bulan Agustus sampai Oktober 2011, di Laboratorium Program Studi Budidaya Perairan, Fakultas Pertanian, Universitas Lampung. B. Alat
III. METODE PENELITIAN A. Waktu dan Tempat Penelitian dilaksanakan pada bulan Agustus sampai Oktober 2011, di Laboratorium Program Studi Budidaya Perairan, Fakultas Pertanian, Universitas Lampung. B. Alat
III. METODOLOGI. (Cr 3+ ). Faktor suhu menggunakan 2 level suhu media yaitu T i (suhu 20±2
 III. METODOLOGI Waktu dan Tempat Penelitian ini dilaksanakan bulan Mei hingga November 2006 di Laboratorium Kesehatan Ikan Balai Besar Pengembangan Budidaya Air Tawar (BBPBAT) Sukabumi dan Laboratorium
III. METODOLOGI Waktu dan Tempat Penelitian ini dilaksanakan bulan Mei hingga November 2006 di Laboratorium Kesehatan Ikan Balai Besar Pengembangan Budidaya Air Tawar (BBPBAT) Sukabumi dan Laboratorium
METODE PENELITIAN. Penelitian ini dilaksanakan pada bulan September sampai dengan Oktober 2013 di
 III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan September sampai dengan Oktober 2013 di Laboratorium Balai Besar Pengembangan Budidaya Laut (BBPBL) Lampung dan juga di
III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan September sampai dengan Oktober 2013 di Laboratorium Balai Besar Pengembangan Budidaya Laut (BBPBL) Lampung dan juga di
II. METODOLOGI 2.1 Metode Penelitian Karakterisasi Sifat Biokimia dan Fisiologi A. hydrophila Uji Postulat Koch
 II. METODOLOGI 2.1 Metode Penelitian 2.1.1 Karakterisasi Sifat Biokimia dan Fisiologi A. hydrophila Pewarnaan Gram adalah salah satu teknik pewarnaan yang penting dan luas yang digunakan untuk mengidentifikasi
II. METODOLOGI 2.1 Metode Penelitian 2.1.1 Karakterisasi Sifat Biokimia dan Fisiologi A. hydrophila Pewarnaan Gram adalah salah satu teknik pewarnaan yang penting dan luas yang digunakan untuk mengidentifikasi
III. HASIL DAN PEMBAHASAN
 III. HASIL DAN PEMBAHASAN 3.1 Hasil Hasil dari penelitian yang dilakukan berupa parameter yang diamati seperti kelangsungan hidup, laju pertumbuhan bobot harian, pertumbuhan panjang mutlak, koefisien keragaman
III. HASIL DAN PEMBAHASAN 3.1 Hasil Hasil dari penelitian yang dilakukan berupa parameter yang diamati seperti kelangsungan hidup, laju pertumbuhan bobot harian, pertumbuhan panjang mutlak, koefisien keragaman
II. METODE PENELITIAN
 II. METODE PENELITIAN A. Materi, Waktu dan Lokasi Penelitian 1. Materi Penelitian Bahan yang akan digunakan meliputi ikan plati, kultur mikroorganisme yang diisolasi dari asinan sawi, Paramaecium sp.,
II. METODE PENELITIAN A. Materi, Waktu dan Lokasi Penelitian 1. Materi Penelitian Bahan yang akan digunakan meliputi ikan plati, kultur mikroorganisme yang diisolasi dari asinan sawi, Paramaecium sp.,
Lampiran 1. Road-map Penelitian
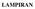 LAMPIRAN Lampiran 1. Road-map Penelitian Persiapan Penelitian Persiapan wadah dan ikan uji (15-30 Agustus 2013) Bak ukuran 45x30x35cm sebanyak 4 buah dicuci, didesinfeksi, dan dikeringkan Diletakkan secara
LAMPIRAN Lampiran 1. Road-map Penelitian Persiapan Penelitian Persiapan wadah dan ikan uji (15-30 Agustus 2013) Bak ukuran 45x30x35cm sebanyak 4 buah dicuci, didesinfeksi, dan dikeringkan Diletakkan secara
III. METODOLOGI 3.1 Waktu dan Tempat 3.2 Induk 3.3 Metode Penelitian
 III. METODOLOGI 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan November 2009 sampai dengan Februari 2010 di Stasiun Lapangan Laboratorium Reproduksi dan Genetika Organisme Akuatik, Departemen
III. METODOLOGI 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan November 2009 sampai dengan Februari 2010 di Stasiun Lapangan Laboratorium Reproduksi dan Genetika Organisme Akuatik, Departemen
METODE PENELITIAN. Pemilihan Ikan Uji dan Bakteri (Patogen dan Probiotik)
 METODE PENELITIAN Waktu dan Tempat Penelitian Penelitian ini dilakukan selama 5 bulan, mulai Januari Juni 2011 di Laboratorium Patologi Ikan, Balai Riset Perikanan Budidaya Air Tawar, Bogor, Jawa Barat.
METODE PENELITIAN Waktu dan Tempat Penelitian Penelitian ini dilakukan selama 5 bulan, mulai Januari Juni 2011 di Laboratorium Patologi Ikan, Balai Riset Perikanan Budidaya Air Tawar, Bogor, Jawa Barat.
I. METODE PENELITIAN. Penelitian dan pembuatan preparat ulas darah serta perhitungan hematokrit sel
 I. METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian dan pembuatan preparat ulas darah serta perhitungan hematokrit sel darah merah dilakukan pada bulan Juli 2012 di Laboratorium Perikanan Jurusan
I. METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian dan pembuatan preparat ulas darah serta perhitungan hematokrit sel darah merah dilakukan pada bulan Juli 2012 di Laboratorium Perikanan Jurusan
III. METODE PENELITIAN. Penelitian ini dilaksanakan pada bulan September-Oktober 2014 di
 III. METODE PENELITIAN 3.1 Tempat Dan Waktu Penelitian Penelitian ini dilaksanakan pada bulan September-Oktober 2014 di Laboratorium dan Fasilitas Karantina Marine Research Center (MRC) PT.Central Pertiwi
III. METODE PENELITIAN 3.1 Tempat Dan Waktu Penelitian Penelitian ini dilaksanakan pada bulan September-Oktober 2014 di Laboratorium dan Fasilitas Karantina Marine Research Center (MRC) PT.Central Pertiwi
BAB IV HASIL DAN PEMBAHASAN. Gambar 7. Bakteri Bacillus Sumber : Dokumentasi Pribadi
 BAB IV HASIL DAN PEMBAHASAN 4.1 Pembentukan Organisme Bioflok 4.1.1 Populasi Bakteri Populasi bakteri pada teknologi bioflok penting untuk diamati, karena teknologi bioflok didefinisikan sebagai teknologi
BAB IV HASIL DAN PEMBAHASAN 4.1 Pembentukan Organisme Bioflok 4.1.1 Populasi Bakteri Populasi bakteri pada teknologi bioflok penting untuk diamati, karena teknologi bioflok didefinisikan sebagai teknologi
BAB II. BAHAN DAN METODE
 BAB II. BAHAN DAN METODE 2.1 Kultur Bakteri Pembawa Vaksin Bakteri Escherichia coli pembawa vaksin DNA (Nuryati, 2010) dikultur dengan cara menginokulasi satu koloni bakteri media LB tripton dengan penambahan
BAB II. BAHAN DAN METODE 2.1 Kultur Bakteri Pembawa Vaksin Bakteri Escherichia coli pembawa vaksin DNA (Nuryati, 2010) dikultur dengan cara menginokulasi satu koloni bakteri media LB tripton dengan penambahan
III. METODE PENELITIAN. UNILA dan Laboratorium Kesehatan Lingkungan Balai Besar Pengembangan dan
 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Agustus sampai dengan Oktober 2013 di Laboratorium Budidaya Perikanan Jurusan Budidaya Perairan Fakultas Pertanian UNILA
III. METODE PENELITIAN A. Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Agustus sampai dengan Oktober 2013 di Laboratorium Budidaya Perikanan Jurusan Budidaya Perairan Fakultas Pertanian UNILA
III. METODOLOGI PENELITIAN. Penelitian dilaksanakan pada bulan September sampai dengan bulan Nopember
 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian dilaksanakan pada bulan September sampai dengan bulan Nopember 2011, bertempat di laboratorium ikan Clownfish Balai Besar Pengembangan
III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian dilaksanakan pada bulan September sampai dengan bulan Nopember 2011, bertempat di laboratorium ikan Clownfish Balai Besar Pengembangan
BAB III BAHAN DAN METODE PENELITIAN
 BAB III BAHAN DAN METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian dilaksanakan pada April 2013 sampai dengan Mei 2013 di laboratorium Nutrisi Fakultas Perikanan dan Ilmu Kelautan Universitas
BAB III BAHAN DAN METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian dilaksanakan pada April 2013 sampai dengan Mei 2013 di laboratorium Nutrisi Fakultas Perikanan dan Ilmu Kelautan Universitas
III. METODE PENELITIAN
 17 III. METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Lingkungan Departemen Budidaya Perairan, Institut Pertanian Bogor dan dilaksanakan selama 3 (tiga) bulan
17 III. METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Lingkungan Departemen Budidaya Perairan, Institut Pertanian Bogor dan dilaksanakan selama 3 (tiga) bulan
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Manajemen Sumberdaya Perairan Fakultas Perikanan dan Ilmu Kelautan Universitas Padjadjaran Jatinangor
BAB III METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Manajemen Sumberdaya Perairan Fakultas Perikanan dan Ilmu Kelautan Universitas Padjadjaran Jatinangor
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1 Tempat Dan Waktu Penelitian Penelitian ini dilaksanakan di Hatchery Ciparanje dan Laboratorium Akuakultur Fakultas Perikanan dan Ilmu Kelautan Universitas Padjadjaran. Penelitian
BAB III METODE PENELITIAN 3.1 Tempat Dan Waktu Penelitian Penelitian ini dilaksanakan di Hatchery Ciparanje dan Laboratorium Akuakultur Fakultas Perikanan dan Ilmu Kelautan Universitas Padjadjaran. Penelitian
Lampiran 1a. Pengenceran konsentrasi bakteri dalam biakan murni dengan teknik pengenceran berseri
 Lampiran 1a. Pengenceran konsentrasi bakteri dalam biakan murni dengan teknik pengenceran berseri A 2 lup biakan bakteri padat Inkubasi+shaker (suhu kamar, 18-24 jam) a b b b 0.1 ml 0.1 ml 0.1ml 1:10-1
Lampiran 1a. Pengenceran konsentrasi bakteri dalam biakan murni dengan teknik pengenceran berseri A 2 lup biakan bakteri padat Inkubasi+shaker (suhu kamar, 18-24 jam) a b b b 0.1 ml 0.1 ml 0.1ml 1:10-1
II. BAHAN DAN METODE 2.1 Alat dan Bahan 2.2 Tahap Penelitian
 II. BAHAN DAN METODE 2.1 Alat dan Bahan Alat yang digunakan adalah akuarium dengan dimensi 50 x 30 x 30 cm 3 untuk wadah pemeliharaan ikan, DO-meter, termometer, ph-meter, lakban, stoples bervolume 3 L,
II. BAHAN DAN METODE 2.1 Alat dan Bahan Alat yang digunakan adalah akuarium dengan dimensi 50 x 30 x 30 cm 3 untuk wadah pemeliharaan ikan, DO-meter, termometer, ph-meter, lakban, stoples bervolume 3 L,
III. METODE PENELITIAN. Stasiun Karantina Ikan Pengendalian Mutu dan Keamanan Hasil Perikanan
 18 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian dilakukan pada bulan September November 2011 yang bertempat di Laboratorium Bioteknologi Lantai 3 Program Studi Budidaya Perairan Universitas Lampung,
18 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian dilakukan pada bulan September November 2011 yang bertempat di Laboratorium Bioteknologi Lantai 3 Program Studi Budidaya Perairan Universitas Lampung,
II. METODELOGI 2.1 Waktu dan Tempat 2.2 Alat dan Bahan 2.3 Tahap Penelitian
 II. METODELOGI 2.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan November sampai dengan Desember 2011 di Laboratorium Lingkungan dan Laboratorium Kesehatan Ikan, Budidaya Perairan, Fakultas Perikanan
II. METODELOGI 2.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan November sampai dengan Desember 2011 di Laboratorium Lingkungan dan Laboratorium Kesehatan Ikan, Budidaya Perairan, Fakultas Perikanan
II. BAHAN DAN METODE 2.1 Tahap Penelitian 2.2 Prosedur Kerja Penelitian Pendahuluan Tingkat Kelangsungan Hidup Ikan Selama Pemuasaan
 II. BAHAN DAN METODE 2.1 Tahap Penelitian Kegiatan penelitian ini terbagi dalam dua tahap yaitu tahap penelitian pendahuluan dan tahap utama. Penelitian pendahuluan meliputi hasil uji kapasitas serap zeolit,
II. BAHAN DAN METODE 2.1 Tahap Penelitian Kegiatan penelitian ini terbagi dalam dua tahap yaitu tahap penelitian pendahuluan dan tahap utama. Penelitian pendahuluan meliputi hasil uji kapasitas serap zeolit,
BAB I PENDAHULUAN. penyakit MAS (Motile Aeromonas Septicemia). Penyakit ini juga dikenal sebagai
 1 BAB I PENDAHULUAN 1.1 Latar Belakang Ikan patin siam (P. hypophthalmus) merupakan salah satu komoditas ikan konsumsi air tawar yang bernilai ekonomis penting karena beberapa kelebihan yang dimiliki seperti
1 BAB I PENDAHULUAN 1.1 Latar Belakang Ikan patin siam (P. hypophthalmus) merupakan salah satu komoditas ikan konsumsi air tawar yang bernilai ekonomis penting karena beberapa kelebihan yang dimiliki seperti
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Bioteknologi Kelautan untuk membuat ekstrak daun sirih, Laboratorium Fisiologi Hewan Air (FHA) untuk
BAB III METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Bioteknologi Kelautan untuk membuat ekstrak daun sirih, Laboratorium Fisiologi Hewan Air (FHA) untuk
II. BAHAN DAN METODE
 II. BAHAN DAN METODE 2.1 Tahap Penelitian Penelitian ini terdiri dari dua tahap, yaitu tahap pendahuluan dan utama. Metodologi penelitian sesuai dengan Supriyono, et al. (2010) yaitu tahap pendahuluan
II. BAHAN DAN METODE 2.1 Tahap Penelitian Penelitian ini terdiri dari dua tahap, yaitu tahap pendahuluan dan utama. Metodologi penelitian sesuai dengan Supriyono, et al. (2010) yaitu tahap pendahuluan
METODE PENELITIAN. Penelitian ini dilaksanakan pada bulan Agustus - Oktober 2013 di Balai Besar
 III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Agustus - Oktober 2013 di Balai Besar Pengembangan Budidaya Laut (BBPBL) Lampung tepatnya di Laboratorium Pembenihan Kuda
III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Agustus - Oktober 2013 di Balai Besar Pengembangan Budidaya Laut (BBPBL) Lampung tepatnya di Laboratorium Pembenihan Kuda
II. BAHAN DAN METODE
 II. BAHAN DAN METODE 2.1 Rancangan Percobaan Penelitian dilakukan menggunakan rancangan acak lengkap (RAL) tiga perlakuan dengan masing-masing tiga ulangan yaitu : 1) Perlakuan A dengan pergantian air
II. BAHAN DAN METODE 2.1 Rancangan Percobaan Penelitian dilakukan menggunakan rancangan acak lengkap (RAL) tiga perlakuan dengan masing-masing tiga ulangan yaitu : 1) Perlakuan A dengan pergantian air
MATERI DAN METODE. Materi
 MATERI DAN METODE Lokasi dan Waktu Penelitian ini telah dilaksanakan dari bulan April sampai dengan bulan Mei 2011, bertempat di kandang pemuliaan ternak, Departemen Ilmu Produksi dan Teknologi Peternakan,
MATERI DAN METODE Lokasi dan Waktu Penelitian ini telah dilaksanakan dari bulan April sampai dengan bulan Mei 2011, bertempat di kandang pemuliaan ternak, Departemen Ilmu Produksi dan Teknologi Peternakan,
II. METODOLOGI 2.1 Metode Penelitian Identifikasi Bakteri Uji Peningkatan Virulensi Bakteri Uji
 II. METODOLOGI 2.1 Metode Penelitian Penelitian ini terdiri dari dua uji utama yaitu uji in vitro dan uji in vivo. Identifikasi dan peningkatan virulensi bakteri uji, penentuan nilai LD 50 (Lethal Dosage
II. METODOLOGI 2.1 Metode Penelitian Penelitian ini terdiri dari dua uji utama yaitu uji in vitro dan uji in vivo. Identifikasi dan peningkatan virulensi bakteri uji, penentuan nilai LD 50 (Lethal Dosage
BAB III BAHAN DAN METODE
 BAB III BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Fisiologi Hewan Air Fakultas Perikanan dan Ilmu Kelautan, pada bulan Maret 2013 sampai dengan April 2013.
BAB III BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Fisiologi Hewan Air Fakultas Perikanan dan Ilmu Kelautan, pada bulan Maret 2013 sampai dengan April 2013.
BAB IV HASIL DAN PEMBAHASAN
 BAB IV HASIL DAN PEMBAHASAN 4.1 Kadar Hematokrit Ikan Hematokrit adalah persentase sel darah merah dalam darah, bila kadar hematokrit 40% berarti dalam darah tersebut terdiri dari 40% sel darah merah dan
BAB IV HASIL DAN PEMBAHASAN 4.1 Kadar Hematokrit Ikan Hematokrit adalah persentase sel darah merah dalam darah, bila kadar hematokrit 40% berarti dalam darah tersebut terdiri dari 40% sel darah merah dan
BAHAN dan METODE PENELlTIAN
 BAHAN dan METODE PENELlTIAN Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Patologi Balai Penelitian Perikanan Air Tawar Sukamandi. Peneiitian dilaksanakan selama lima bulan. sejak
BAHAN dan METODE PENELlTIAN Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Patologi Balai Penelitian Perikanan Air Tawar Sukamandi. Peneiitian dilaksanakan selama lima bulan. sejak
I. PENDAHULUAN 1.1 Latar Belakang
 1 I. PENDAHULUAN 1.1 Latar Belakang Ikan lele dumbo (Clarias sp.) merupakan ikan air tawar yang banyak dibudidaya secara intensif hampir di seluruh wilayah Indonesia. Hal ini disebabkan ikan lele dumbo
1 I. PENDAHULUAN 1.1 Latar Belakang Ikan lele dumbo (Clarias sp.) merupakan ikan air tawar yang banyak dibudidaya secara intensif hampir di seluruh wilayah Indonesia. Hal ini disebabkan ikan lele dumbo
III. METODE PENELITIAN. Penelitian ini dilaksanakan pada bulan April sampai Juni 2012 di Laboratorium
 III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan April sampai Juni 2012 di Laboratorium Basah Program Studi Budidaya Perairan, Fakultas Pertanian, Universitas Lampung.
III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan April sampai Juni 2012 di Laboratorium Basah Program Studi Budidaya Perairan, Fakultas Pertanian, Universitas Lampung.
BAB III BAHAN DAN METODE
 BAB III BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Bioteknologi dan Laboratorium Akuakultur Fakultas Perikanan dan Ilmu Kelautan Universitas Padjadjaran.
BAB III BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Bioteknologi dan Laboratorium Akuakultur Fakultas Perikanan dan Ilmu Kelautan Universitas Padjadjaran.
IV. METODE PENELITIAN Waktu dan Tempat. Penelitian ini dilaksanakan pada bulan Juli hingga bulan September 2004 di
 IV. METODE PENELITIAN 4.1. Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Juli hingga bulan September 2004 di Laboratorium Parasit dan Penyakit Ikan Fakultas Perikanan dan Ilmu Kelautan Universitas
IV. METODE PENELITIAN 4.1. Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Juli hingga bulan September 2004 di Laboratorium Parasit dan Penyakit Ikan Fakultas Perikanan dan Ilmu Kelautan Universitas
1) Staf Pengajar pada Prog. Studi. Budidaya Perairan, Fakultas
 Media Litbang Sulteng 2 (2) : 126 130, Desember 2009 1) Staf Pengajar pada Prog. Studi. Budidaya Perairan, Fakultas Pertanian Universitas Tadulako, Palu ISSN : 1979-5971 PERTUMBUHAN DAN KELANGSUNGAN HIDUP
Media Litbang Sulteng 2 (2) : 126 130, Desember 2009 1) Staf Pengajar pada Prog. Studi. Budidaya Perairan, Fakultas Pertanian Universitas Tadulako, Palu ISSN : 1979-5971 PERTUMBUHAN DAN KELANGSUNGAN HIDUP
METODE PENELITIAN. Penelitian dilakukan di Laboratorium Kesehatan Ikan Jurusan Budidaya
 III. METODE PENELITIAN 3.1.Waktu dan Tempat Penelitian dilakukan di Laboratorium Kesehatan Ikan Jurusan Budidaya Perairan Universitas Lampung pada Mei-Juli 2014. 3.2.Alat dan Bahan Alat yang digunakan
III. METODE PENELITIAN 3.1.Waktu dan Tempat Penelitian dilakukan di Laboratorium Kesehatan Ikan Jurusan Budidaya Perairan Universitas Lampung pada Mei-Juli 2014. 3.2.Alat dan Bahan Alat yang digunakan
III. BAHAN DAN METODE
 12 III. BAHAN DAN METODE 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Juli 2009 sampai dengan bulan September 2009 bertempat di Laboratorium Sistem Produksi dan Manajemen Akuakultur, Departemen
12 III. BAHAN DAN METODE 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Juli 2009 sampai dengan bulan September 2009 bertempat di Laboratorium Sistem Produksi dan Manajemen Akuakultur, Departemen
METODE PENELITIAN. Penelitian dilaksanakan pada bulan Februari sampai April 2015 selama 50
 III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian dilaksanakan pada bulan Februari sampai April 2015 selama 50 hari di Laboratorium Nutrisi dan Pakan Jurusan Budidaya Perairan, Fakultas
III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian dilaksanakan pada bulan Februari sampai April 2015 selama 50 hari di Laboratorium Nutrisi dan Pakan Jurusan Budidaya Perairan, Fakultas
III. METODE PENELITIAN. Penelitian dilaksanakan mulai tanggal 10 Mei 30 Juni 2013 selama 50
 III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian dilaksanakan mulai tanggal 10 Mei 30 Juni 2013 selama 50 hari di Balai Benih Ikan (BBI) Natar, Kabupaten Lampung Selatan. Pembuatan pakan
III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian dilaksanakan mulai tanggal 10 Mei 30 Juni 2013 selama 50 hari di Balai Benih Ikan (BBI) Natar, Kabupaten Lampung Selatan. Pembuatan pakan
III. MATERI DAN METODE PENELITIAN. Penelitian ini dilaksanakan pada bulan Oktober sampai dengan Desember 2012 di
 21 III. MATERI DAN METODE PENELITIAN A. Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Oktober sampai dengan Desember 2012 di Laboratorium Jurusan Perikanan Fakultas Pertanian Universitas Lampung.
21 III. MATERI DAN METODE PENELITIAN A. Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Oktober sampai dengan Desember 2012 di Laboratorium Jurusan Perikanan Fakultas Pertanian Universitas Lampung.
GAMBARAN DARAH IKAN II (SDP, AF DAN DL)
 Laporan Praktikum ke-3 Hari/Tanggal : Jumat/ 17 Maret 2017 m.k Manajemen Kesehatan Kelompok : VII Organisme Akuatik Asisten : Niar Suryani GAMBARAN DARAH IKAN II (SDP, AF DAN DL) Disusun oleh: Nuralim
Laporan Praktikum ke-3 Hari/Tanggal : Jumat/ 17 Maret 2017 m.k Manajemen Kesehatan Kelompok : VII Organisme Akuatik Asisten : Niar Suryani GAMBARAN DARAH IKAN II (SDP, AF DAN DL) Disusun oleh: Nuralim
BAB III BAHAN DAN METODE
 BAB III BAHAN DAN METODE 3.1. Tempat dan Waktu Penelitian Penelitian dilaksanakan di Hatchery Ciparanje Fakultas Perikanan Dan Ilmu Kelautan Universitas Padjadjaran. Waktu pelaksanaan dimulai dari bulan
BAB III BAHAN DAN METODE 3.1. Tempat dan Waktu Penelitian Penelitian dilaksanakan di Hatchery Ciparanje Fakultas Perikanan Dan Ilmu Kelautan Universitas Padjadjaran. Waktu pelaksanaan dimulai dari bulan
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Balai Riset Ikan Hias Depok. Penelitian berlangsung pada tanggal 15 Agustus hingga 5 Oktober 2012. Penelitian diawali
BAB III METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Balai Riset Ikan Hias Depok. Penelitian berlangsung pada tanggal 15 Agustus hingga 5 Oktober 2012. Penelitian diawali
I. PENDAHULUAN. Indonesia adalah negara kepulauan yang 70% alamnya merupakan perairan
 I. PENDAHULUAN A. Latar Belakang Indonesia adalah negara kepulauan yang 70% alamnya merupakan perairan yang terdiri dari rawa, sungai, danau, telaga, sawah, tambak, dan laut. Kekayaan alam ini sangat potensial
I. PENDAHULUAN A. Latar Belakang Indonesia adalah negara kepulauan yang 70% alamnya merupakan perairan yang terdiri dari rawa, sungai, danau, telaga, sawah, tambak, dan laut. Kekayaan alam ini sangat potensial
METODE PENELITIAN. M 1 V 1 = M 2 V 2 Keterangan : M 1 V 1 M 2 V 2
 11 METODE PENELITIAN Tempat dan waktu Penelitian dilaksanakan di Laboratorium Lingkungan Akuakultur, Departemen Budidaya Perairan, Fakultas Perikanan dan Ilmu Kelautan Institut Pertanian Bogor untuk pemeliharaan
11 METODE PENELITIAN Tempat dan waktu Penelitian dilaksanakan di Laboratorium Lingkungan Akuakultur, Departemen Budidaya Perairan, Fakultas Perikanan dan Ilmu Kelautan Institut Pertanian Bogor untuk pemeliharaan
II. METODOLOGI 2.1 Persiapan Wadah dan Ikan Uji 2.2 Persiapan Pakan Uji
 II. METODOLOGI 2.1 Persiapan Wadah dan Ikan Uji Wadah yang digunakan dalam penelitian ini adalah bak terpal dengan ukuran 2 m x1m x 0,5 m sebanyak 12 buah (Lampiran 2). Sebelum digunakan, bak terpal dicuci
II. METODOLOGI 2.1 Persiapan Wadah dan Ikan Uji Wadah yang digunakan dalam penelitian ini adalah bak terpal dengan ukuran 2 m x1m x 0,5 m sebanyak 12 buah (Lampiran 2). Sebelum digunakan, bak terpal dicuci
II. BAHAN DAN METODE
 II. BAHAN DAN METODE 2.1 Prosedur Penelitian 2.1.1 Pembuatan Media Pembuatan air bersalinitas 4 menggunakan air laut bersalinitas 32. Penghitungan dilakukan dengan menggunakan rumus pengenceran sebagai
II. BAHAN DAN METODE 2.1 Prosedur Penelitian 2.1.1 Pembuatan Media Pembuatan air bersalinitas 4 menggunakan air laut bersalinitas 32. Penghitungan dilakukan dengan menggunakan rumus pengenceran sebagai
III. METODE PENELITIAN
 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian dilaksanakan bulan Juli 2011 sampai September 2011 bertempat di Balai Benih Ikan Sentral (BBIS) Purbolinggo, kecamatan Purbolinggo, kabupaten Lampung
III. METODE PENELITIAN A. Waktu dan Tempat Penelitian dilaksanakan bulan Juli 2011 sampai September 2011 bertempat di Balai Benih Ikan Sentral (BBIS) Purbolinggo, kecamatan Purbolinggo, kabupaten Lampung
BAB III BAHAN DAN METODE
 BAB III BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian ini dilaksanakan di LaboratoriumPembenihan Ikan Ciparanje, Fakultas Perikanan dan Ilmu Kelautan Universitas Padjadjaran pada bulan Maret sampai
BAB III BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian ini dilaksanakan di LaboratoriumPembenihan Ikan Ciparanje, Fakultas Perikanan dan Ilmu Kelautan Universitas Padjadjaran pada bulan Maret sampai
3 METODOLOGI 3.1 Waktu dan Tempat 3.2 Bahan dan Alat Metode Penelitian
 3 METODOLOGI 3.1 Waktu dan Tempat Penelitian berjudul Pengujian Biji Pala (Myristica sp.) sebagai Bahan Anestesi Lobster air tawar (Cherax quadricarinatus) dilaksanakan di Laboratorium Bahan Baku dan Industri
3 METODOLOGI 3.1 Waktu dan Tempat Penelitian berjudul Pengujian Biji Pala (Myristica sp.) sebagai Bahan Anestesi Lobster air tawar (Cherax quadricarinatus) dilaksanakan di Laboratorium Bahan Baku dan Industri
III. METODE PENELITIAN. Penelitian dilaksanakan pada bulan September-Oktober 2011 bertempat di. Balai Budidaya Ikan Hias, Natar, Lampung Selatan.
 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian Penelitian dilaksanakan pada bulan September-Oktober 2011 bertempat di Balai Budidaya Ikan Hias, Natar, Lampung Selatan. B. Alat dan Bahan Penelitian
III. METODE PENELITIAN A. Waktu dan Tempat Penelitian Penelitian dilaksanakan pada bulan September-Oktober 2011 bertempat di Balai Budidaya Ikan Hias, Natar, Lampung Selatan. B. Alat dan Bahan Penelitian
III. METODE PENELITIAN. Penelitian dilaksanakan pada bulan Juli 2011 sampai September 2011 bertempat
 III. METODE PENELITIAN A. Waktu Dan Tempat Penelitian dilaksanakan pada bulan Juli 2011 sampai September 2011 bertempat di Balai Benih Ikan Sentral (BBIS) Probolinggo, Lampung Timur dan analisis sampel
III. METODE PENELITIAN A. Waktu Dan Tempat Penelitian dilaksanakan pada bulan Juli 2011 sampai September 2011 bertempat di Balai Benih Ikan Sentral (BBIS) Probolinggo, Lampung Timur dan analisis sampel
BAB III METODOLOGI PENELITIAN
 BAB III METODOLOGI PENELITIAN 3.1 Tempat dan Waktu Penelitian Pengambilan data penelitian telah dilaksanakan pada bulan Desember 2012 sampai bulan Januari 2013 bertempat di Hatcery Kolam Percobaan Ciparanje
BAB III METODOLOGI PENELITIAN 3.1 Tempat dan Waktu Penelitian Pengambilan data penelitian telah dilaksanakan pada bulan Desember 2012 sampai bulan Januari 2013 bertempat di Hatcery Kolam Percobaan Ciparanje
METODE PENELITIAN. : Nilai pengamatan perlakuan ke-i, ulangan ke-j : Rata-rata umum : Pengaruh perlakuan ke-i. τ i
 13 METODE PENELITIAN Waktu dan Tempat Penelitian Penelitian ini dilaksanakan di Lab. KESDA provinsi DKI Jakarta (analisis kandungan senyawa aktif, Pimpinella alpina), Lab. Percobaan Babakan FPIK (pemeliharaan
13 METODE PENELITIAN Waktu dan Tempat Penelitian Penelitian ini dilaksanakan di Lab. KESDA provinsi DKI Jakarta (analisis kandungan senyawa aktif, Pimpinella alpina), Lab. Percobaan Babakan FPIK (pemeliharaan
GAMBARAN DARAH IKAN NILA (Oreochromis niloticus) DENGAN PENAMBAHAN DOSIS PREBIOTIK YANG BERBEDA DALAM PAKAN
 GAMBARAN DARAH IKAN NILA (Oreochromis niloticus) DENGAN PENAMBAHAN DOSIS PREBIOTIK YANG BERBEDA DALAM PAKAN (Tilapia Blood Parameters with The Addition of Different Dose of Prebiotics in Feed) Riski Hartika
GAMBARAN DARAH IKAN NILA (Oreochromis niloticus) DENGAN PENAMBAHAN DOSIS PREBIOTIK YANG BERBEDA DALAM PAKAN (Tilapia Blood Parameters with The Addition of Different Dose of Prebiotics in Feed) Riski Hartika
III. METODE PENELITIAN. Penelitian dilaksanakan pada bulan Februari sampai dengan Maret 2014 di
 III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian dilaksanakan pada bulan Februari sampai dengan Maret 2014 di Laboratorium Jurusan Budidaya Perairan Universitas Lampung. Analisis proksimat
III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian dilaksanakan pada bulan Februari sampai dengan Maret 2014 di Laboratorium Jurusan Budidaya Perairan Universitas Lampung. Analisis proksimat
III. METODE PENELITIAN
 19 III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian telah dilakukan pada bulan November Desember 2013, bertempat di Laboratorium Budidaya Perairan Fakultas Pertanian Universitas Lampung. 3.2 Alat
19 III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian telah dilakukan pada bulan November Desember 2013, bertempat di Laboratorium Budidaya Perairan Fakultas Pertanian Universitas Lampung. 3.2 Alat
Angki Ismayadi, Rosmawati, Mulyana Jurusan Perikanan, Fakultas Pertanian, Universitas Djuanda Bogor
 Jurnal Mina Sains ISSN: 2407-9030 Volume 2 Nomor 1, April 2016 24 Kelangsungan Hidup dan Pertumbuhan Benih Ikan Nilem (Osteochillus hasselti) yang Dipelihara pada Tingkat Kepadatan Berbeda The Survivability
Jurnal Mina Sains ISSN: 2407-9030 Volume 2 Nomor 1, April 2016 24 Kelangsungan Hidup dan Pertumbuhan Benih Ikan Nilem (Osteochillus hasselti) yang Dipelihara pada Tingkat Kepadatan Berbeda The Survivability
BAB I PENDAHULUAN 1.1 Latar Belakang
 BAB I PENDAHULUAN 1.1 Latar Belakang Ikan mas (Cyprinus carpio L.) sudah tidak asing lagi bagi masyarakat Indonesia. Ikan air tawar yang bernilai ekonomis cukup penting ini sudah sangat dikenal luas oleh
BAB I PENDAHULUAN 1.1 Latar Belakang Ikan mas (Cyprinus carpio L.) sudah tidak asing lagi bagi masyarakat Indonesia. Ikan air tawar yang bernilai ekonomis cukup penting ini sudah sangat dikenal luas oleh
BAB IV HASIL DAN PEMBAHASAN
 BAB IV HASIL DAN PEMBAHASAN 4.1 Hasil Pengamatan Gejala Klinis Pengamatan gejala klinis pada benih ikan mas yang diinfeksi bakteri Aeromonas hydrophila meliputi kelainan fisik ikan, uji refleks, dan respon
BAB IV HASIL DAN PEMBAHASAN 4.1 Hasil Pengamatan Gejala Klinis Pengamatan gejala klinis pada benih ikan mas yang diinfeksi bakteri Aeromonas hydrophila meliputi kelainan fisik ikan, uji refleks, dan respon
BAB III BAHAN DAN METODE
 BAB III BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Bioteknologi dan Laboratorium Akuakultur Fakultas Perikanan dan Ilmu Kelautan Universitas Padjadjaran.
BAB III BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Bioteknologi dan Laboratorium Akuakultur Fakultas Perikanan dan Ilmu Kelautan Universitas Padjadjaran.
II. BAHAN DAN METODE
 II. BAHAN DAN METODE 2.1 Tahap Penelitian Penelitian ini terdiri dari dua tahap, yaitu tahap pendahuluan dan utama. Pada tahap pendahuluan dilakukan penentuan kemampuan puasa ikan, tingkat konsumsi oksigen,
II. BAHAN DAN METODE 2.1 Tahap Penelitian Penelitian ini terdiri dari dua tahap, yaitu tahap pendahuluan dan utama. Pada tahap pendahuluan dilakukan penentuan kemampuan puasa ikan, tingkat konsumsi oksigen,
METODE PENELITIAN. Penelitian ini dilaksanakan pada bulan Oktober sampai dengan Desember 2012 di
 22 III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Oktober sampai dengan Desember 2012 di Laboratorium Budidaya Perikanan dan Laboratorium Bioteknologi Fakultas Pertanian
22 III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada bulan Oktober sampai dengan Desember 2012 di Laboratorium Budidaya Perikanan dan Laboratorium Bioteknologi Fakultas Pertanian
METODE PENELITIAN. Waktu dan Tempat Penelitian. Alat dan Bahan
 33 METODE PENELITIAN Waktu dan Tempat Penelitian Pemeliharaan ikan dilakukan di Laboratorium Sistem dan Teknologi Budidaya, IPB. Histologi gonad dilakukan di Laboratorium Kesehatan Ikan (LKI), uji glukosa
33 METODE PENELITIAN Waktu dan Tempat Penelitian Pemeliharaan ikan dilakukan di Laboratorium Sistem dan Teknologi Budidaya, IPB. Histologi gonad dilakukan di Laboratorium Kesehatan Ikan (LKI), uji glukosa
BAB I PENDAHULUAN 1.1 Latar Belakang
 BAB I PENDAHULUAN 1.1 Latar Belakang Ikan nilem (Osteochilus vittatus) merupakan ikan air tawar yang termasuk kedalam famili Cyprinidae yang bersifat herbivore. Ikan ini menyebar di Asia Tenggara, di Indonesia
BAB I PENDAHULUAN 1.1 Latar Belakang Ikan nilem (Osteochilus vittatus) merupakan ikan air tawar yang termasuk kedalam famili Cyprinidae yang bersifat herbivore. Ikan ini menyebar di Asia Tenggara, di Indonesia
MATERI DAN METODA Waktu dan Tempat Penelitian Bahan dan Alat Penelitian Hewan Percobaan Vaksin AI-ND Pakan Kandang dan Perlengkapannya
 10 MATERI DAN METODA Waktu Tempat Penelitian Penelitian dilakukan di Laboratorium Terpadu FKH-IPB, Departemen Ilmu Penyakit Hewan Kesehatan Masyarakat Veteriner, Fakultas Kedokteran Hewan, Institut Pertanian
10 MATERI DAN METODA Waktu Tempat Penelitian Penelitian dilakukan di Laboratorium Terpadu FKH-IPB, Departemen Ilmu Penyakit Hewan Kesehatan Masyarakat Veteriner, Fakultas Kedokteran Hewan, Institut Pertanian
BAB I PENDAHULUAN. di Jawa Tengah (Purwanti et al., 2014). Lele dumbo merupakan jenis persilangan lele
 BAB I PENDAHULUAN 1.1 Latar Belakang Ikan lele dumbo (Clarias gariepinus) adalah salah satu komoditas ikan air tawar yang bernilai ekonomis tinggi dan dapat dipelihara pada padat penebaran tinggi. Ikan
BAB I PENDAHULUAN 1.1 Latar Belakang Ikan lele dumbo (Clarias gariepinus) adalah salah satu komoditas ikan air tawar yang bernilai ekonomis tinggi dan dapat dipelihara pada padat penebaran tinggi. Ikan
III. METODE 3.1. Waktu dan Tempat 3.2. Alat dan Bahan 3.3. Tahap Persiapan Hewan Percobaan Aklimatisasi Domba
 17 III. METODE 3.1. Waktu dan Tempat Penelitian ini dilaksanakan selama delapan bulan yang dimulai pada bulan Mei sampai dengan bulan Desember 2010. Penelitian dilakukan di kandang Mitra Maju yang beralamat
17 III. METODE 3.1. Waktu dan Tempat Penelitian ini dilaksanakan selama delapan bulan yang dimulai pada bulan Mei sampai dengan bulan Desember 2010. Penelitian dilakukan di kandang Mitra Maju yang beralamat
IMUNITAS NON-SPESIFIK DAN SINTASAN LELE MASAMO (Clarias sp.) DENGAN APLIKASI PROBIOTIK, VITAMIN C DAN DASAR KOLAM BUATAN ABSTRAK
 e-jurnal Rekayasa dan Teknologi Budidaya Perairan Volume IV No 2 Februari 2016 ISSN: 2302-3600 IMUNITAS NON-SPESIFIK DAN SINTASAN LELE MASAMO (Clarias sp.) DENGAN APLIKASI PROBIOTIK, VITAMIN C DAN DASAR
e-jurnal Rekayasa dan Teknologi Budidaya Perairan Volume IV No 2 Februari 2016 ISSN: 2302-3600 IMUNITAS NON-SPESIFIK DAN SINTASAN LELE MASAMO (Clarias sp.) DENGAN APLIKASI PROBIOTIK, VITAMIN C DAN DASAR
BAB III BAHAN DAN METODE
 BAB III BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian ini dilaksanakan di Hatchery Ciparanje Fakultas Perikanan dan Ilmu Kelautan Universitas Padjadjaran pada bulan April sampai Mei 2013. Tahapan yang
BAB III BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian ini dilaksanakan di Hatchery Ciparanje Fakultas Perikanan dan Ilmu Kelautan Universitas Padjadjaran pada bulan April sampai Mei 2013. Tahapan yang
MATERI DAN METODA. Kandang dan Perlengkapannya Pada penelitian ini digunakan dua kandang litter sebesar 2x3 meter yang
 11 MATERI DAN METODA Waktu dan Tempat Penelitian Penelitian ini berlangsung dari bulan Juni 2010 sampai dengan Juni 2011. Penelitian dilakukan di kandang FKH-IPB. Pengujian sampel dilakukan di Laboratorium
11 MATERI DAN METODA Waktu dan Tempat Penelitian Penelitian ini berlangsung dari bulan Juni 2010 sampai dengan Juni 2011. Penelitian dilakukan di kandang FKH-IPB. Pengujian sampel dilakukan di Laboratorium
METODE PENELITIAN. Penelitian dilaksanakan bulan Agustus sampai September 2011 bertempat di
 III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian dilaksanakan bulan Agustus sampai September 2011 bertempat di Laboratorium Jurusan Budidaya Perairan, Fakultas Pertanian, Universitas Lampung. Penelitian
III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian dilaksanakan bulan Agustus sampai September 2011 bertempat di Laboratorium Jurusan Budidaya Perairan, Fakultas Pertanian, Universitas Lampung. Penelitian
III. METODE PENELITIAN. Penelitian ini dilakukan selama dua bulan pada bulan September-Oktober 2013,
 22 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan selama dua bulan pada bulan September-Oktober 2013, bertempat di Laboratorium Program Studi Budidaya Perairan Fakultas
22 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan selama dua bulan pada bulan September-Oktober 2013, bertempat di Laboratorium Program Studi Budidaya Perairan Fakultas
BAB III BAHAN DAN METODE
 BAB III BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian ini dilaksanakan di Laboratorium Akuakultur Fakultas Perikanan dan Ilmu Kelautan, Universitas Padjadjaran, Jatinangor Sumedang, Jawa Barat. Penelitian
BAB III BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian ini dilaksanakan di Laboratorium Akuakultur Fakultas Perikanan dan Ilmu Kelautan, Universitas Padjadjaran, Jatinangor Sumedang, Jawa Barat. Penelitian
II. METODE 2.1 Rancangan Penelitian 2.2 Isolasi Bakteri Kandidat Probiotik
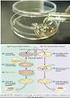 II. METODE 2.1 Rancangan Penelitian Rancangan percobaan yang digunakan dalam penelitian ini adalah Rancangan Acak Lengkap (RAL) dengan 6 perlakuan dan 2 ulangan pada uji patogenisitas, serta 4 perlakuan
II. METODE 2.1 Rancangan Penelitian Rancangan percobaan yang digunakan dalam penelitian ini adalah Rancangan Acak Lengkap (RAL) dengan 6 perlakuan dan 2 ulangan pada uji patogenisitas, serta 4 perlakuan
BAB III METODE PENELITIAN. Jenis penelitian yang dilakukan merupakan penelitian eksperimen, karena
 BAB III METODE PENELITIAN A. Jenis Penelitian Jenis penelitian yang dilakukan merupakan penelitian eksperimen, karena dalam penelitian ini dilakukan dengan mengadakan manipulasi terhadap objek penelitian
BAB III METODE PENELITIAN A. Jenis Penelitian Jenis penelitian yang dilakukan merupakan penelitian eksperimen, karena dalam penelitian ini dilakukan dengan mengadakan manipulasi terhadap objek penelitian
METODE PENELITIAN Persiapan Penelitian Penelitian Pendahuluan Tahap 1 Waktu dan Tempat
 41 METODE PENELITIAN Penelitian ini terdiri atas 2 tahap yaitu penelitian pendahuluan dan penelitian inti. Penelitian pendahuluan terdiri atas 2 tahap yaitu uji nilai kisaran (range value test) dan uji
41 METODE PENELITIAN Penelitian ini terdiri atas 2 tahap yaitu penelitian pendahuluan dan penelitian inti. Penelitian pendahuluan terdiri atas 2 tahap yaitu uji nilai kisaran (range value test) dan uji
BAB III BAHAN DAN METODE PENELITIAN
 BAB III BAHAN DAN METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Hatchery Gedung 4 Fakultas Perikanan dan Ilmu Kelautan Universitas Padjadjaran Jatinangor. Pelaksanaan
BAB III BAHAN DAN METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Hatchery Gedung 4 Fakultas Perikanan dan Ilmu Kelautan Universitas Padjadjaran Jatinangor. Pelaksanaan
BAB III MATERI DAN METODE. Penelitian dilaksanakan pada bulan Desember 2015 di kandang peternak di
 14 BAB III MATERI DAN METODE Penelitian dilaksanakan pada bulan Desember 2015 di kandang peternak di Desa Kedu Temanggung dan pada bulan April 2016 di kandang unggas Fakultas Peternakan dan Pertanian Universitas
14 BAB III MATERI DAN METODE Penelitian dilaksanakan pada bulan Desember 2015 di kandang peternak di Desa Kedu Temanggung dan pada bulan April 2016 di kandang unggas Fakultas Peternakan dan Pertanian Universitas
METODE PENELITIAN. Penelitian dilaksanakan pada bulan Januari - Februari 2010, di Laboratorium
 28 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian dilaksanakan pada bulan Januari - Februari 2010, di Laboratorium Stasiun Karantina Ikan Kelas I Panjang, Bandar Lampung dan Laboratorium Budidaya
28 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian dilaksanakan pada bulan Januari - Februari 2010, di Laboratorium Stasiun Karantina Ikan Kelas I Panjang, Bandar Lampung dan Laboratorium Budidaya
III. METODOLOGI. Penelitian dilakukan selama 40 hari dari bulan Februari sampai dengan Maret. Bahan yang digunakan dalam penelitian antara lain:
 21 III. METODOLOGI A. Waktu dan Tempat Penelitian Penelitian dilakukan selama 40 hari dari bulan Februari sampai dengan Maret 2013 bertempat di Laboratorium Budidaya Perairan Fakultas Pertanian Universitas
21 III. METODOLOGI A. Waktu dan Tempat Penelitian Penelitian dilakukan selama 40 hari dari bulan Februari sampai dengan Maret 2013 bertempat di Laboratorium Budidaya Perairan Fakultas Pertanian Universitas
METODE PENELITIAN. Penelitian Tahap 1: Uji Efektivitas Enzim Cairan Rumen Domba Terhadap Penurunan Kandungan Serat Kasar Bungkil Kelapa
 17 METODE PENELITIAN Penelitian dilakukan dalam dua tahapan. Tahap 1 adalah uji efektivitas enzim cairan rumen domba terhadap penurunan kandungan serat kasar bungkil kelapa. Uji Tahap 2 adalah mengevaluasi
17 METODE PENELITIAN Penelitian dilakukan dalam dua tahapan. Tahap 1 adalah uji efektivitas enzim cairan rumen domba terhadap penurunan kandungan serat kasar bungkil kelapa. Uji Tahap 2 adalah mengevaluasi
BAB I PENDAHULUAN. 1.1 Latar Belakang. Penyakit ikan merupakan salah satu masalah serius yang dihadapi oleh
 BAB I PENDAHULUAN 1.1 Latar Belakang Penyakit ikan merupakan salah satu masalah serius yang dihadapi oleh para pembudidaya karena berpotensi menimbulkan kerugian yang sangat besar. Kerugian yang terjadi
BAB I PENDAHULUAN 1.1 Latar Belakang Penyakit ikan merupakan salah satu masalah serius yang dihadapi oleh para pembudidaya karena berpotensi menimbulkan kerugian yang sangat besar. Kerugian yang terjadi
BAB III BAHAN DAN METODE
 BAB III BAHAN DAN METODE 3.1 Tempat dan Waktu Pelaksanaan Penelitian ini dilaksanakan di Laboratorium Bioteknologi dan Laboratorium Pembenihan Ikan dan Kolam Percobaan Ciparanje untuk penelitian pendahuluan
BAB III BAHAN DAN METODE 3.1 Tempat dan Waktu Pelaksanaan Penelitian ini dilaksanakan di Laboratorium Bioteknologi dan Laboratorium Pembenihan Ikan dan Kolam Percobaan Ciparanje untuk penelitian pendahuluan
BAB III BAHAN DAN METODE
 BAB III BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Pembuatan ekstrak ubi jalar merah dilaksanakan di Laboratorium Bioteknologi Gedung 4 Fakultas Perikanan dan Ilmu Kelautan Universitas Padjadjaran,
BAB III BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Pembuatan ekstrak ubi jalar merah dilaksanakan di Laboratorium Bioteknologi Gedung 4 Fakultas Perikanan dan Ilmu Kelautan Universitas Padjadjaran,
III. METODE PENELITIAN
 III. METODE PENELITIAN Alat dan Bahan Alat-alat yang digunakan untuk pengambilan sampel darah yaitu obyek glass, cover glass, Haemicitometer, jarum suntik, pipet kapiler, mikroskop monokuler. Vitamin E
III. METODE PENELITIAN Alat dan Bahan Alat-alat yang digunakan untuk pengambilan sampel darah yaitu obyek glass, cover glass, Haemicitometer, jarum suntik, pipet kapiler, mikroskop monokuler. Vitamin E
