Tempat dan Waktu Penelitian
|
|
|
- Sukarno Widjaja
- 6 tahun lalu
- Tontonan:
Transkripsi
1 BAHAN DAN METODE Tempat dan Waktu Penelitian Survei penyebaran penyakit dan intensitasnya dilakukan sejak bulan Agustus 1989 hingga bulan Desember 1990, secara bertahap. Untuk penyebaran penyakit, pengamatan dilakukan pada semua areal pertanaman kedelai di Kalimantan Selatan berdasarkan ada tidaknya penyakit pustul. Untuk intensitas penyakit pengamatan dilakukan pada seluruh kabupaten yang ada di Kalimantan Selatan, 9 kabupaten, dan dari tiap kabupaten diambil satu lokasi contoh secara acak, kecuali untuk kabupaten yang hanya mempunyai satu lokasi yang mengusahakan tanaman kedelai. Pekerjaan di laboratorium dan percobaan pot dilaksanakan sejak bulan Agustus 1989 sampai bulan Juli 1990 di Jurusan Hama dan Penyakit Tumbuhan, Fakultas Pertanian Universitas Lambung Mangkurat, Banjarbaru, Kalimantan Selatan. Khusus untuk percobaan penularan penyakit melalui polong kedelai dilaksanakan sejak bulan Desember 1991 sampai bulan Februari 1992, di Jurusan Hama dan Penyakit Tumbuhan, Fakultas Pertanian IPB. Isolasi Patogen dan Uji Postulat Koch Sumber isolat berasal dari tanaman sakit yang berada di lingkungan Kampus Unlam Banjarbaru, Kalimantan Selatan. Medium YDCA (Yeast Extract-Dextrose-CaC03 Agar) digunakan untuk isolasi. Setiap liter YDCA mengandung 10 g ekstrak
2 23 ragi, 20 g dektrosa, 20 g CaC03, dan 15 g agar. Kalsium karbonat disterilisasi dalam otoklaf secara terpisah. Daun kedelai yang menunjukkan gejala awal pustul digunting dengan ukuran kira-kira 0.5 x 0.5 cm, dibuat beberapa potongan. Tiap potongan dicelup dalam larutan alkohol 70% selama 2 detik dan dilanjutkan dalam larutan HgC % selama 55 detik. Setelah itu potongan dibilas dalam akuades steril. Potongan dikeringkan dengan meletakkannya di atas kertas hisap steril. Kemudian potongan daun bergejala ini digunting lagi melalui bercak dan dimasukkan dalam larutan 0.85% NaCl dalam tabung reaksi yang berisi 5 ml. Kemudian dengan menggunakan jarum ose diambil suspensinya dan digoreskan di atas medium YDCA yang telah disiapkan di dalam cawan petri, yang kemudian diinkubasikan selama 4 hari pada suhu kamar. Berdasarkan warna dan bentuk koloninya, masing-masing koloni bakteri yang tumbuh pada medium dimurnikan dengan cara menumbuhkannya pada medium GYCA (Glucose Yeast Extract Calcium Carbonate Agar) miring dan diinkubasikan selama 2 hari. Pada masing-masing biakan miring ditambahkan akuades steril dan diaduk dengan jarum ose serta digoyang-goyang sehingga tersuspensi merata. Untuk mendapatkan konsentrasi inokulum sebesar 2 10*cfu/ml, suspensi ditera dengan larutan McFarland hingga diperoleh skala no. 3. Sebagai tanaman uji digunakan kedelai varietas Galunggung yang rentan terhadap penyakit pustul, berumur 1 bulan. Sebelum dan sesudah inokulasi, tanaman
3 24 diletakkan dalam ruangan lembab dan mendapatkan setengah naungan. Inokulasi dilakukan dengan semprotan. Dari gejala khas yang terbentuk, dilakukan isolasi dan inokulasi ulang. Berdasarkan hasil dari dua tahapan isolasi dan inokulasi, isolat yang mampu menimbulkan gejala serupa di lapangan, kemudian diperbanyak pada medium YDCA dan disimpan dalam suhu 30 C, untuk keperluan selanjutnya. Daerah sebaran penyaki t Survei Penyebaran dan Intensitas Serangan Patogen Pustul Kedelai di Kalimantan Selatan Untuk mendapatkan data sebaran penyakit pustul, penga- matan dilakukan diseluruh lokasi yang ada tanaman kedelai- nya di Kalimantan Selatan, yang dilaksanakan sejak Nopember 1989 sampai Oktober Setiap tanaman yang bergejala mirip pustul diambil daunnya sebagai sampel dan dibawa ke laboratorium untuk diisolasi dan diidentifikasi. Metode yang digunakan sama dengan yang telah diuraikan sebelumnya. Intensitas penyakit Karena jumlah lokasi yang penduduknya melaksanakan usahatani kedelai tidak cukup banyak, maka survei diadakan pada seluruh kabupaten. Di tiap kabupaten diambil satu lokasi pertanaman kedelai secara acak. Pada tiap lokasi ditentukan petak-petak contoh berukuran 1 m x 1 m secara lintas sektoral. Tiap petak contoh yang berurutan berjarak
4 25 sekitar 25 m. Dengan demikian, jumlah petak contoh tiap lokasi tidak sama banyaknya karena tergantung pada luas dan bentuk areal pertanaman kedelai secara keseluruhan. Skor penyakit ditentukan berdasarkan penilaian global gejala penyakit pada tiap rumpun tanaman, yaitu sebagai berikut : Skor 1 = bebas, tidak ada daun yang terserang Skor 2 = terserang ringan, kurang dari 2/3 bagian tajuk bergejala Skor 3 = terserang berat, lebih dari 2/3 bagian tajuk berge jala Identifikasi Patogen Identifikasibakteri patogen dilakukan berdasarkan uji fisiologis dan biokimia menurut Lelliott dan Stead (1987), yang mengacu langsung pada pernbuktian bahwa isolat yang diuji adalah salah satu spesies Xanthomonas campestris. Diantara karakteristik yang diperlukan adalah uji reaksi Gram, uji katalase, uji oksidase, harnbatan pertumbuhan oleh TZC 1% dan 0.023, perturnbuhan kuning madu pada medium kentang, dan uji metabolisme oksidatif-fermentatif. Uji Reaksi Gram Pada permukaan sebuah gelas obyek diletakkan setetes larutan KOH 33, kemudian ditambahkan 1 lup biakan bakteri yang berumur 48 jam, serta diaduk merata selama 10 detik.
5 26 Kemudian lup diangkat perlahan dan diperhatikan timbulnya benang lendir yang lengket. Adanya benang lendir menunjukkan reaksi Gram negatif (Fahy dan Hayward, 1983). Uji katalase Ke atas koloni bakteri yang sedang tumbuh di permukaan medium NA ("nutrient agar") diteteskan 2 tetes larutan H202 3%. Bila dalam waktu singkat terbentuk gelembung udara berarti uji katalase positif. Uji oksidase Bila uji oksidase ini positif, maka berarti bakteri yang diuji mengandung ensim sitokhrom-c oksidase. Beberapa tetes reagen tetrametilfenilen diamin dihidrokhlorida 1% diteteskan pada kertas saring. Dengan menggunakan lup emas, bakteri diusapkan pada kertas saring yang telah diimpregnasi dengan reagen tersebut. Bila dalam 10 detik telah terjadi perubahan warna menjadi ungu, maka reaksi oksidase adalah positif. Bila perubahan terjadi dalam selang waktu antara detik, reaksi dinyatakan positif lambat. Bila perubahan terjadi setelah 60 detik, reaksi dinyatakan negatif.
6 Uji hambatan pertumbuhan oleh TZC Sebagai larutan dasar, ke dalam 100 ml akuades steril ditambahkan 1.0 g TZC (2,3,5 trifenil tetrazolium khlorida) sehingga didapatkan larutan TZC 1%. Untuk mendapatkan me- dium NA yang mengandung 0.1% TZC, maka ke dalam 9 ml NA yang sedang mencair (55O~) ditambahkan 1 ml larutan dasar TZC, dan segera dituangkan ke dalam cawan petri. Medium NA yang mengandung TZC 0.02% didapatkan dari campuran sebanyak 9.8 ml NA yang sedang mencair dan 0.2 ml larutan dasar TZC. Pada masing-masing medium NA yang mengandung 0.1% dan 0.02% TZC di cawan petri, ditanamkan bakteri yang diuji dengan ujung jarum. Selama 3 hari inkubasi, diperhatikan ada atau tidak pertumbuhan koloni yang berawal dari ukuran sebesar titik. Uji warna pertumbuhan bakteri pada medium sumbat kentang Dari sebuah kentang bersih dibuat bentukan sumbat dengan menggunakan "cork borer" berdiameter 1 cm, sepanjang 5 cm. Salah satu ujung diiris dengan kemiringan 4S0 dan ujung lainnya dibuat rata. Sumbat kentang dimasukkan ke dalam tabung reaksi dengan posisi bagian yang rata di dasar tabung. Kemudian tabung diisi akuades setinggi 2.5 cm, dan sediaan disterilkan dengan otoklaf pada suhu 115 C selama 10 menit. Sedikit bakteri diusapkan pada bagian irisan miring dan diinkubasikan selama 3 hari pada suhu kamar. Yang
7 Uji hambatan pertumbuhan oleh TZC Sebagai larutan dasar, ke dalam 100 ml akuades steril ditambahkan 1.0 g TZC (2,3,5 trifenil tetrazolium khlorida) sehingga didapatkan larutan TZC 1%. Untuk mendapatkan medium NA yang mengandung 0.1% TZC, maka ke dalam 9 ml NA yang sedang mencair (55OC) ditambahkan 1 ml larutan dasar TZC, dan segera dituangkan ke dalam cawan petri. Medium NA yang mengandung TZC 0.02% didapatkan dari campuran sebanyak 9.8 ml NA yang sedang mencair dan 0.2 ml larutan dasar TZC. Pada masing-masing medium NA yang mengandung 0.1% dan 0.02% TZC di cawan petri, ditanamkan bakteri yang diuji dengan ujung jarum. Selama 3 hari inkubasi, diperhatikan ada atau tidak pertumbuhan koloni yang berawal dari ukuran sebesar titik. Uji warna pertumbuhan bakteri pada medium sumbat kentang Dari sebuah kentang bersih dibuat bentukan sumbat dengan menggunakan "cork borer" berdiameter 1 cm, sepanjang 5 cm. Salah satu ujung diiris dengan kemiringan 45O dan ujung lainnya dibuat rata. Sumbat kentang dimasukkan ke dalam tabung reaksi dengan posisi bagian yang rata di dasar tabung. Kemudian tabung diisi akuades setinggi 2.5 cm, dan sediaan disterilkan dengan otoklaf pada suhu 115 C selama 10 menit. Sedikit bakteri diusapkan pada bagian irisan miring dan diinkubasikan selama 3 hari pada suhu kamar. Yang
8 dicatat adalah berkembangnya koloni bakteri dengan warna kuning madu. 28 Uji metabolisme oksidatif-fermentatif Disiapkan satu liter medium dasar yang mengandung 5.0 g NaC1, 2.0 g pepton, 0.3 g K2HP04, 3.0 g agar, 15 ml larutan bromothymol biru 0.2% (dalam air), dengan ph 7.1. Sebelum disterilkan, medium dibagi dalam tabung Erlenmeyer ukuran 250 ml, masing-masing 90 ml. Setelah disterilkan dengan otoklaf pada suhu 121 C selama 15 menit, tabung diletakkan dalam penangas air dengan suhu 50 C dan ke dalamnya ditambahkan 10 ml larutan glukosa 10% steril (disterilkan dengan filtrasi). Medium dibagi-bagi ke dalam tabung reaksi masing-masing sebanyak 6 ml. Bakteri diinokulasikan secara tusuk ("stab") masing-masing pada 2 tabung reaksi. Pada salah satu tabung, diatas medium diberi parafin cair. Inkubasi dilakukan selama 3 hari pada suhu kamar kemudian dilihat adanya perubahan warna dari biru menjadi kuning sebagai pertanda terjadinya asam. Bila asam terjadi pada tabung tanpa parafin berarti metabolisme oksidatif (aerobik) positif dan bila terjadi pada tabung dengan parafin maka metabolisme fermentatif (oksidasi anaerobik) positif. Identifikasi patovar hanya berdasarkan kekhasan inang. Namun untuk Xanthomonas campestris pv. glycines beberapa sifat fisiologisnya telah diketahui, dan dapat dicocokkan,
9 29 antara lain: sangat cepat menghidrolisis pati, dapat mencairkan gelatin, dan menghasilkan asam (bukan gas) dari sukrosa (Sinclair, 1982). Hidrolisis pati Ke dalam medium YNA ("Yeast Extract Nutrient Agar") ditambahkan 0.2% amilum yang mudah larut. Dalam 1 liter YNA mengandung 5.0 g ekstrak ragi, 5.0 g pepton, 5.0 g ekstrak daging, dan 15 g agar, serta ph 6.8. Bakteri ditempatkan pada medium, dalam cawan petri, dan diinkubasikan pada suhu kamar selama 3 sampai 7 hari. Setelah itu kultur digenangi dengan larutan Lugol sehingga amilum berwarna biru kehitaman. Zona jernih di sekitar kultur bakteri menggambarkan terjadinya hidrolisis pati (Fahy & Hayward, 1983). Larutan Lugol dibuat dari 1.0 g I2, 2.0 g KI, dan 300 ml akuades (Kiraly et al., 1974). Pencairan gelatin Satu liter medium gelatin dibuat dari 3.0 g ekstrak daging, 5.0 g pepton, dan g gelatin. Medium dibagikan 10 ml per tabung reaksi dan disterilkan dengan otoklaf pada suhu 121 C selama 15 menit. Pada tiap tabung diinokulasikan bakteri yang diuji secara tusuk ("stab") dan diinkubasikan pada suhu 20 C selama 7-14 hari. Untuk pembacaan pencairan, tabung diletakkan pada suhu 4 C atau es yang sedang mencair.
10 30 Pembentukan asam dari sukrosa Disediakan medium C-Dye, yang ditambahkan dengan 0.5% sukrosa yang telah disterilkan dengan filtrasi. Satu liter medium C-Dye mengandung 0.5 gnh4h2p04, 0.5 g K2HP04, 0.2 g MgS04.7H20, 5.0 g NaC1, 1.0 g ekstrak ragi, 12.0 g agar, dan 0.7 ml larutan Bromokresol ungu 1.5% (dilarutkan dalam alkohol). Tingkat ph medium 6.8. Bakteri yang diuji ditanamkan secara tusuk dan diamati 2, 4, 7, 21, dan 28 hari setelah tanam. Warna kuning menunjukkan terbentuknya asam. Kehilangan Hasil Untuk mengetahui pengaruh penyakit terhadap hasil, maka disusun sebuah percobaan faktorial, yang terdiri atas dua faktor, yaitu faktor penyakit dan faktor varietas kede- lai. Faktor penyakit terdiri atas dua taraf, yaitu po (tidak diinokulasi bakteri patogen) dan pl (diinokulasi bakteri patogen). Berdasarkan pengalaman pada Kebun Bibit dan Benih Unlam, faktor varietas kedelai dibagi atas tiga taraf, yaitu w = Wilis (relatif le-bih tahan), 1 = Lokon (sedang), dan g = Galunggung (relatif lebih rentan). De- ngan demikian, kombinasi perlakuan menjadi 6 buah, yaitu: powl pol, pog, plw, pll, dan plg. Tiap kombinasi perlakuan diulang lima kali. Percobaan menggunakan pot plastik yang mempunyai diameter 28 cm, sebanyak 30 buah. Rancangan
11 30 Pembentukan asam dari sukrosa Disediakan medium C-Dye, yang ditambahkan dengan 0.5% sukrosa yang telah disterilkan dengan filtrasi. Satu liter medium C-Dye mengandung 0.5 gnh4h2p04, 0.5 g K2HP04, 0.2 g MgS04. 7H20, 5.0 g NaC1, 1.0 g ekstrak ragi, 12.0 g agar, dan 0.7 ml larutan Bromokresol ungu 1.5% (dilarutkan dalam alkohol). Tingkat ph medium 6.8. Bakteri yang diuji ditanamkan secara tusuk dan diamati 2, 4, 7, 21, dan 28 hari setelah tanam. Warna kuning menunjukkan terbentuknya asam. Kehilangan Hasil Untuk mengetahui pengaruh penyakit terhadap hasil, maka disusun sebuah percobaan faktorial, yang terdiri atas dua faktor, yaitu faktor penyakit dan faktor varietas kede- lai. Faktor penyakit terdiri atas dua taraf, yaitu po (tidak diinokulasi bakteri patogen) dan pl (diinokulasi bakteri patogen). Berdasarkan pengalaman pada Kebun Bibit dan Benih Unlam, faktor varietas kedelai dibagi atas tiga taraf, yaitu w = Wilis (relatif le-bih tahan), 1 = Lokon (sedang), dan g = Galunggung (relatif lebih rentan). De- ngan demikian, kombinasi perlakuan menjadi 6 buah, yaitu: pow, pol, pog, plw, pll, dan pig. Tiap kombinasi perlakuan diulang lima kali. Percobaan menggunakan pot plastik yang mempunyai diameter 28 cm, sebanyak 30 buah. Rancangan
12 lingkungan yang dipilih adalah Rancangan Acak Lengkap. Tiap pot diisi dengan 10 kg tanah yang telah disterilkan dengan uap panas selama 1 jam. Pot disusun secara acak di atas meja papan yang tingginya 1 m. Tiap pot berjarak 1 m, dan masing-masing pot dipupuk dengan 0.51 g Urea, 0.67 g TSP, dan 0.60 g KC1. Sebelum ditanam, benih terlebih da- hulu diberi inokulan bakteri Rhizobium dengan cara mencam- pur 1.0 g inokulan sedikit air dan dicampur merata dengan 0.1 kg benih. Inokulasi bakteri patogen dilakukan pada saat tanaman berumur 21 hari, dengan cara menyemprotkan suspensi bakteri pada permukaan bawah daun. Kepadatan inokulum adalah sekitar 10' sel hiduplml (ditera menggunakan dedar McFarland). Setelah disemprot, tanaman ditutup dengan kantong plastik selama 24 jam. Setelah kantong itu dibuka, pot diletakkan di tempat teduh selama 4 jam untuk penyesuaian, dan kemudi- an diletakkan pada meja papan menurut pengacakan semula. Selama percobaan berlangsung, tanaman disemprot secara berkala, satu kali dalam seminggu, dengan insektisida Decis 2.5 EC (bahan aktifnya deltamethrin) dengan dosis 0.5 ml/l air. Tanaman disiram 1-2 kali sehari. Pengamatan dilakukan terhadap hasil (berupa berat biji per pot) dan komponen hasil (berupa jumlah polong per po- hon, jumlah biji per polong, dan berat 100 biji). Untuk melengkapi gambaran keadaan penyakit, maka 15 hari sebelum panen dicatat intensitas penyakit bersangkutan. 31
13 Hubungan Patogen dengan Benih Kedelai Persentase benih terinfeksi dan lokasi bakteri Benih berasal dari tanaman kedelai yang terserang. Untuk maksud tersebut, disediakan lahan berukuran 2 m x 4 m. Pada lahan tersebut dibuat bedengan-bedengan kecil sejajar sisi terpendek, dengan jarak masing-masing 0.5 m. Pada tiap bedengan ditanami kedelai, satu benih satu lobang, dengan jarak 25 cm. Sebelum ditanami, lahan dipupuk dengan 81.8 g Urea, g TSP, dan 96 g KC1. Karena lahan yang digunakan adalah bekas tanaman kedelai juga, maka tidak diperlukan pemberian Rhizobiurn. Inokulasi dilakukan pada waktu tanaman berumur 3 minggu dengan kepadatan inokulum lo8 sel hidup/ml, dengan cara menyemprot pada permukaan bawah daun. Setelah panen, biji dipisahkan dari polong dan diletakkan dalam tampah serta diaduk merata. Dari sejumlah benih yang ada diambil secara acak sebanyak 100 biji untuk keperluan selanjutnya. Tiap benih, setelah dicelup dalam larutan NaOCl 1% 5 menit, dikeringkan menggunakan kertas hisap steril. Kemudian, benih dipisahkan atas kulit, sisa endosperma, hilum, kotiledon, dan sumbu embrio. Bagian-bagian tersebut dile- takkan di atas medium YDC dalam cawan petri. Satu cawan medium untuk dua benih. Bakteri yang tumbuh dan koloninya berwarna kuning, diperbanyak dan diuj i dengan cara "bio- assayw yakni langsung diinokulasikan pada daun kedelai
14 varietas Galunggung. Perkembangan gejala diamati tiap hari hingga timbul gejala yang khas. 33 Persentase tanaman sakit yang benihnya berasal dari tanaman terserang Benih diambil dari karung, hasil panen dari areal terserang, dengan alat pengambil contoh sebanyak 50 benih. Untuk itu disediakan 50 buah pot plastik yang berdiameter f 20 cm dan masing-masing diisi dengan 3 kg tanah steril. Pot disusun di atas meja papan yang tingginya 1 m, dengan jarak 1 m. Tanah dipupuk dengan 0.15 g Urea, 0.2 g TSP, dan 0.18 KC1 per pot. Kurang lebih 1 g Rhizobium diberi sedikit air dan diaduk dengan benih yang akan ditanam. Tiap pot ditanami satu benih kedelai. Pengamatan adanya gejala penyakit dilakukan sejak munculnya kotiledon sampai tanaman berbunga. Pot yang tanamannya terserang penyakit dikeluarkan dari meja papan. Infeksi melalui polong Untuk maksud ini disediakan 60 buah "polybagm, yang masing-masing diisi 5 kg tanah. Tiap pot dipupuk dengan 0.25 g Urea, 0.33 g TSP, dan 0.30 g KC1. Sekitar 0.2 g inokulan Rhizobium dicampur dengan sedikit air dan diaduk merata dengan sekitar 200 benih kedelai varietas Lokon. Tiap pot semula ditanami dengan tiga benih kedelai dan setelah berumur satu minggu disisakan dua tanaman. Inokulasi dengan suspensi bakteri pustul, dengan kepadatan sekitar
15 34 lo7 sel hidup/ml, dilakukan pada waktu polong berumur 7 dan 21 hari terhitung sejak bunga muncul. Perlakuan terdiri atas 3 perlakuan utama, masing-masing dengan satu kontrolnya, sehingga secara lengkap ada enam perlakuan: a) bagian sisi polong dioles dengan suspensi bakteri, b) bagian dorsal polong dioles dengan suspensi bakteri, c) bagian sisi polong diinokulasi secara Itpin prickgt, d) bagian sisi polong diinokulasi dengan air sterill e) bagian dorsal polong dioles dengan air steril, dan f) bagian sisi polong diinokulasi secara "pin pricktt namun dengan air steril. Pengolesan dilakukan dengan kapas dan cara pin prick dilakukan dengan jarum yang dekat ujungnya dibalut kapas. Pengamatan adanya gejala dilakukan pada saat polong berumur satu bulan. Perkembangan populasi bakteri pada benih dalam kurun waktu Prosedur yang digunakan berasal dari Lovrekovich dan Klement (dalam Kiraly et al., 1974). Seratus biji kedelai dimasukkan ke dalam tabung yang berisi 50 ml larutan NaOCl 1% dan mempunyai klep pembuangan. Setelah dibiarkan selama 5 menit, biji dibilas dengan air steril selama 2 menit. Setelah direndam selama 2 jam dalam air steril biji tersebut dihancurkan menggunakan "blenderw selama 15 menit. Hancuran biji tersebut diencerkan dengan air steril, dan
16 hancuran disentrifus dengan kecepatan 1000 rpm selama 3 me- 35 nit. Supernatan diambil sebanyak 0.3 ml dan ditanamkan merata pada permukaan medium YDCA dalam cawan petri. Bakteri yang tumbuh dan berwarna kuning kemudian dimurnikan dan diuji dengan bakteriofag bakteri pustul. Pada pengujian reaksi terhadap bakteriofag, mula-mula disediakan medium SPA dalam tabung reaksi yang masing-masing berisi 7 ml medium, dan dibiarkan cair pada penangas air dengan suhu 42 C. Di samping itu, disediakan 2 ml suspensi bakteri pustul dengan kepadatan lo7-10' sel hidup/ml dalam tabung reaksi. Kedua sediaan dicampur dan dikocok, dan segera dimasukkan ke dalam cawan petri. Bakteriofag didapatkan dari hasil percobaan serasah. Di atas plak yang besar diteteskan air steril secukupnya dan diaduk dengan jarum ose. Jarum diangkat dan digoreskan pads sediaan campuran terdahulu. Inkubasi dilakukan pada suhu 20 c selama 24 jam. Kecocokan bakteriofag terlihat sebagai adanya zona jernih di sekitar goresan. Setelah adanya kecocokan antara bakteri dan fag penguji, maka jumlah koloni pada percobaan utama dihitung dengan alat cacah. ~emeriksaan pertama dilakukan saat satu bulan setelah panen. Pemeriksaan kedua dan seterusnya dilakukan berselang satu bulan, sampai benih kehilangan daya tumbuh.
17 36 Peranan Benih dalam Penularan Penyakit Benih terinfeksi didapatkan dari polong yang diinoku- lasi pada waktu polong berumur 21 hari. Tiap polong diino kulasi dengan cara menyuntikkan 0.01 ml suspensi bakteri dengan menggunakan ttspuittt berukuran 1 ml, dengan kerapatan 3 x lo7 sel hidup/ml, pada posisi dorsal polong. Setelah panen, benih yang dihasilkan diuji terlebih dahulu kepasti- annya mengandung bakteri patogen tersebut. Sepuluh butir benih diambil secara acak dan dicelupkan dalam larutan NaOCl 1% selama 5 menit, dibilas dengan air steril 2 kali dan kemudian dikering-anginkan pada kertas hisap steril. Sebelum benar-benar kering, benih dipisahkan antara kulit (masih bersama sisa endosperma) dan kotiledon. Kulit dan kotiledon yang telah dibelah menurut keping diletakkan di atas meja medium YDCA dalam cawan petri dan diinkubasikan dalam inkubator selama 3 hari. Bakteri yang tumbuh, khu- susnya yang koloninya berwarna kuning, cembung, dan mengki- lap, diperbanyak pada medium GYCA miring. Setelah berumur 3 hari, bakteri diinokulasikan pada daun kedelai dengan ca- ra semprot. Setelah 10 hari diamati timbulnya gejala khas pustul. Benih yang dipanen siap dipergunakan dalam proses selanjutnya sebagai benih terinfeksi. Benih sehat didapatkan dari tanaman yang dipelihara dalam pot berdiameter 28 cm yang berisi 10 kg tanah steril. Pot diletakkan di atas meja kayu yang tingginya 1 m dari
18 permukaan tanah untuk menghindari infeksi bakteri yang berasal dari tanah/percikan air. Polong dari tanaman sehat dipanen dan diambil benihnya. sehat. Benih ini merupakan benih Percobaan penularan melalui benih menggunakan bak kayu berukuran panjang dan lebarnya masing-masing 1 m dan ting- ginya 30 cm, yang diisi dengan tanah steril. Digunakan sembilan bak untuk perlakuan benih terinfeksi dan satu bak untuk kontrol. Tiap bak ditanami dengan satu benih terinfeksi, kecuali kontrol, pada titik pusat permukaan bak, 24 benih sehat mengelilingi tanaman pusat tersebut dengan jarak tanam 25 cm, seperti tertera pada Gambar 3. Bak diberi kaki setinggi 70 cm dan diletakkan tanpa atap agar Gambar 3. Tata letak penanaman benih terinfeksi dan benih sehat. o = benih sehat = benih terinfeksi
19 38 dapat tertimpa air hujan. Kalau tidak ada hujan, penyiraman menggunakan air ledeng dengan cara semprotan. Pengamatan dilakukan untuk: 1). melihat benih terinf eksi yang tumbuh men jadi tanaman sakit; 2). mengetahui penyebaran penyakit dari tanaman terinfeksi yang berada di tengah-tengah bak. Pengamatan perkembangan jumlah tanaman sakit dilakukan tiap minggu terhitung setelah tanaman tengah bergejala. Inang Kacang-kacangan Lain Tanaman yang diuji adalah kacang panjang (Vigna sinen- sis), kacang hi jau (Phaseolus radiatus), kacang tanah (Ara- chis hypogaea), kacang buncis putih (Phaseolus vulgaris), kacang jogo (Phaseolus vulgaris), kacang asu (Calopogonium mucunoides), dan Pueraria japonica. Tiap jenis tanaman ditumbuhkan dalam pot plastik berdiameter 28 cm yang diisi 10 kg campuran tanah dengan pupuk kandang (perbandingan 2 : 1), tiga pot per tanaman. Tanaman diinokulasi pada umur satu bulan setelah tanam. Dua puluh empat jam sebelum inokulasi, tanaman diletakkan dalam ruang lembab agar stomata terbuka. Kemudian, permukaan bawah daun disemprot dengan inokulum yang kepa- datannya 10'-lo6 sel hidup/ml, menggunakan semprotan obat nyamuk yang telah dimodifikasi. Sebelum inokulasi daun tanaman yang akan diinokulasi direndam selama 10 menit. Setelah inokulasi, tanaman dile-
20 39 takkan kembali di dalam ruang lembab selama 48 jam, kemudian diletakkan di tempat terbuka. Dari gejala yang tampak diadakan isolasi patogennya dan dilakukan uji postulat Koch. Apabila patogennya bakteri, maka dapat langsung diuji dengan cara menginokulasi daun kedelai. Kelangsungan Hidup Patogen dalam Tanah Pemberaan tanah Kelangsungan hidup bakteri pustul di dalam tanah dapat diketahui dari dua aspek, yaitu keadaan populasi bakteri itu sendiri dan dari kemampuan tanah tersebut berlaku sebagai sumber inokulum. Untuk keperluan itu, tanah bekas pertanaman kedelai yang terserang pustul dimasukkan ke dalam empat pot plastik berdiameter 28 cm, masing-masing sebanyak 10 kg. Tanah dalam pot diberakan masing-masing 1 bulan, 2 bulan, 3 bulan, dan 4 bulan. Setiap hari tanah disiram sampai batas kapasitas lapang. Dari pot, sesuai masa pemberaannya, diambil 150 g contoh tanah untuk uji bakteriofag (percobaan pertama), dan sisanya untuk pengujian kemampuan riil tanah sebagai sumber inokulum (percobaan kedua). Secara rinci kedua percobaan tersebut adalah sebagai berikut. Perkembangan populasi bakteri pustul dalam tanah Setelah masa pemberaan, dari tiap perlakuan diambil contoh tanah secara komposit sebanyak 150 g dan dimasukkan ke dalam tabung gelas steril serta ditambahkan akuades
21 steril sebanyak 100 ml dan diaduk merata. Larutan disen- trifugasi dengan kecepatan 3000 rpm selama 30 menit. Su- pernatannya diambil untuk dideteksi bakterinya menggunakan IgPoured Plate MethodM. Supernatan disiapkan dalam tiga ukuran, yaitu 0.1 ml, 1 ml, dan 2 ml dalam tabung reaksi. Disamping itu, disediakan masing-masing sebanyak 2 ml suspensi bakteri pustul dari biakan murni dalam media ber- umur 3 hari dengan kepadatan lo7-lo8 sel hidup/ml. Medium SPA (llsucrose Peptone Agar") yang mengandung 20 gr agar11 medium, disediakan sebanyak 7 ml per tabung. Medium ini diletakkan di dalam penangas air yang telah diatur suhunya pada 45 C, sehingga medium tetap dalam keadaan cair, namun tidak mematikan bakteri maupun bakteriofag dalam proses se- lanjutnya. Ketiga sediaan dicampur; diawali dengan mencam- pur suspensi bakteri dan ekstrak tanah, dan kemudian segera dimasukkan ke dalam tabung mengandung SPA cair. Campuran tersebut dengan segera dimasukkan ke dalam cawan petri, dan diratakan. Inkubasi dilakukan pada suhu 28 C selama 24 jam. Jumlah plak dihitung dengan alat cacah. Bila popu- lasi patogen dalam tanah sangat rendah maka dengan teknik tersebut tidak dapat menghasilkan plak bakteriofag pada medium agar. Agar bakterinya dapat dihitung larutan contoh tanah diperkaya terlebih dahulu dengan cara ke dalam 150 g contoh ta-nah di dalam tabung gelas steril ditambahkan kul- tur bakteri yang berumur 48 jam ke dalam medium "Nutrient Brothu yang mengandung gliserin 2%. 40
22 4 1 Potensi Lahan yang Diberakan sebagai Sumber Inokulum Tiap pot yang telah diambil contoh tanahnya pada percobaan pertama, masing-masing ditanami dengan 10 benih varietas Galunggung. Pengamatan gejala penyakit pustul bakteri dilakukan pada waktu tanaman berumur 14 hari sampai 21 hari setelah tanam. Pencatatan data hanya secara kualitatif yaitu berkisar pada ada tidaknya gejala penyakit tersebut. Sebagai perlakuan cek, disediakan 10 kg tanah steril dalam pot serupa dan ditanami dengan 10 contoh benih yang digunakan pada percobaan utama. Rotasi tanaman Disediakan delapan pot plastik berdiameter 28 cm, masing-masing diisi 10 kg tanah dari bekas areal terserang pustul bakteri. Masing-masing pot ditanami kacang tanah, kacang hijau, kacang panjang, terong, padi gogo, padi sa- wah, kacang kedelai, dan bera. Setelah tanaman itu dipa- nen, tanah bekasnya kembali ditanami kedelai varietas Ga- lunggung, sebanyak 10 benih per pot. Pengamatan timbulnya gejala bakteri pustul dilakukan tiap hari. bergejala segera dicabut dan dibuang. Tanaman yang Kelangsungan Hidup Patogen dalam Serasah Serasah daun tanaman kedelai sakit sebanyak 35 g berat segar diletakkan di atas nampan plastik yang berukuran
23 panjang 30 cm, lebar 20 cm dan tinggi 5 cm, telah diberi lapisan tanah setebal 1 cm. Nampan dibenamkan pada keda- laman 15 cm dari permukaan tanah. Separoh jumlah nampan diletakkan sedemikian rupa sehingga permukaan serasah tepat di permukaan tanah. Skema cara meletakkan nampan tersebut tercantum pada Gambar 4. permukaan tanah Gambar 4. Skema penampang peletakan nampan yang berisi serasah; s = serasah, b = nampan, t = tanah, kp = kasa plastik. Permukaan nampan yang berisi serasah ditutup dengan kasa plastik agar serasah tidak terserak, terutama bagi yang dipemukaan tanah. Lahan tempat meletakkan nampan adalah lahan alang-alang, yang belum pernah ditanami kede- lai. Pengamatan populasi bakterilpatogen dalam serasah dilakukan satu kali dalam sebulan menggunakan metode bakteriofag (Jones et al., 1986). Tiap pengamatan memerlukan satu baki serasah untuk tiap perlakuan. Selama empat bulan (empat kali) pengamatan untuk tiap perlakuan diperlukan empat baki serasah. Seluruh serasah yang ada dalam tiap
24 baki perlakuan dimasukkan ke dalam gelas Erlenmeyer 250 ml yang berisi 200 ml larutan CaC03 0.1% kemudian digoyang 43 dengan tangan selama 20 menit. Larutan yang terjadi siap untuk diperiksa. Pengamatan dilakukan satu kali dalam se- bulan dengan menggunakan metode bakteriofag (Jones et al., 1986).
BAHAN DAN METODE Tempat dan Waktu Penelitian Bahan dan Alat Metode Penelitian Pra-pengamatan atau survei
 BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilaksanakan di Kebun Percobaan Pusat Kajian Buah-Buahan Tropika IPB (PKBT-IPB) Pasir Kuda, Desa Ciomas, Bogor, dan Laboratorium Bakteriologi Tumbuhan,
BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilaksanakan di Kebun Percobaan Pusat Kajian Buah-Buahan Tropika IPB (PKBT-IPB) Pasir Kuda, Desa Ciomas, Bogor, dan Laboratorium Bakteriologi Tumbuhan,
HASIL. Survei Daerah Sebaran clan Intensitas Penyakit Pustul Bakteri Kedelai di Kalirnantan Selatan
 Daerah sebaran penyakit HASIL Survei Daerah Sebaran clan Intensitas Penyakit Pustul Bakteri Kedelai di Kalirnantan Selatan Berdasarkan survei yang dilakukan dalam kurun waktu antara bulan November 1989
Daerah sebaran penyakit HASIL Survei Daerah Sebaran clan Intensitas Penyakit Pustul Bakteri Kedelai di Kalirnantan Selatan Berdasarkan survei yang dilakukan dalam kurun waktu antara bulan November 1989
BAHAN DAN METODE Tempat dan Waktu . Bahan dan Alat Metode Penelitian Survei Buah Pepaya Sakit
 5 BAHAN DAN METODE Tempat dan Waktu Penelitian dilaksanakan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman dan Kebun Percobaan Leuwikopo, Fakultas Pertanian, Institut Pertanian Bogor.
5 BAHAN DAN METODE Tempat dan Waktu Penelitian dilaksanakan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman dan Kebun Percobaan Leuwikopo, Fakultas Pertanian, Institut Pertanian Bogor.
III. BAHAN DAN METODE. Penelitian ini dilaksanakan pada bulan Juli sampai dengan Desember 2014.
 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan pada bulan Juli sampai dengan Desember 2014. Isolasi dan karakterisasi penyebab penyakit dilakukan di Laboratorium Penyakit
III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan pada bulan Juli sampai dengan Desember 2014. Isolasi dan karakterisasi penyebab penyakit dilakukan di Laboratorium Penyakit
BAHAN DAN METODE. Tempat dan Waktu
 15 BAHAN DAN METODE Tempat dan Waktu Penelitian dilaksanakan di laboratorium dan rumah kaca Hama dan Penyakit dan rumah kaca Balai penelitian Tanaman Obat dan Aromatik (BALITTRO), Bogor; pada bulan Oktober
15 BAHAN DAN METODE Tempat dan Waktu Penelitian dilaksanakan di laboratorium dan rumah kaca Hama dan Penyakit dan rumah kaca Balai penelitian Tanaman Obat dan Aromatik (BALITTRO), Bogor; pada bulan Oktober
III. BAHAN DAN METODE. Penelitian ini dilaksanakan di Laboratorium Bioteknologi Fakultas Pertanian
 9 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Bioteknologi Fakultas Pertanian Universitas Lampung sejak Juli sampai dengan September 2015. Pengambilan
9 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Bioteknologi Fakultas Pertanian Universitas Lampung sejak Juli sampai dengan September 2015. Pengambilan
Gambar 1 Tanaman uji hasil meriklon (A) anggrek Phalaenopsis, (B) bunga Phalaenopsis yang berwarna putih
 BAHAN DAN METODE Tempat dan Waktu Penelitian Isolasi dan perbanyakan sumber inokulum E. carotovora dilakukan di Laboratorium Bakteriologi Departemen Proteksi Tanaman Fakultas Pertanian, Institut Pertanian
BAHAN DAN METODE Tempat dan Waktu Penelitian Isolasi dan perbanyakan sumber inokulum E. carotovora dilakukan di Laboratorium Bakteriologi Departemen Proteksi Tanaman Fakultas Pertanian, Institut Pertanian
BAHAN DAN METODE. Pengambilan sampel tanaman nanas dilakukan di lahan perkebunan PT. Great
 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Pengambilan sampel tanaman nanas dilakukan di lahan perkebunan PT. Great Giant Pineapple (GGP) di Lampung Timur dan PT. Nusantara Tropical Farm, Lampung
III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Pengambilan sampel tanaman nanas dilakukan di lahan perkebunan PT. Great Giant Pineapple (GGP) di Lampung Timur dan PT. Nusantara Tropical Farm, Lampung
komersial, pupuk SP 36, pupuk KCl, NaCl, Mannitol, K 2 HPO 4, MgSO 4.7H 2 O,
 BAB III METODOLOGI PENELITIAN 3.1 Waktu dan tempat Penelitian ini dilakukan pada tanggal 01 Februari 31 Juni 2011 di Laboratorium Mikrobiologi, Bioteknologi, Kultur Jaringan dan Rumah Kaca Balai Penelitian
BAB III METODOLOGI PENELITIAN 3.1 Waktu dan tempat Penelitian ini dilakukan pada tanggal 01 Februari 31 Juni 2011 di Laboratorium Mikrobiologi, Bioteknologi, Kultur Jaringan dan Rumah Kaca Balai Penelitian
BAB III METODE PENELITIAN. Mikrobiologi Tanah dan Rumah Kaca Balai Penelitian Tanaman Kacang- kacangan dan Umbiumbian
 BAB III METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian dilaksanakan pada tanggal 01 Februari sampai 31 Mei 2011 di Laboratorium Mikrobiologi Tanah dan Rumah Kaca Balai Penelitian Tanaman
BAB III METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian dilaksanakan pada tanggal 01 Februari sampai 31 Mei 2011 di Laboratorium Mikrobiologi Tanah dan Rumah Kaca Balai Penelitian Tanaman
BAHAN DAN METODE. Pembiakan P. fluorescens dari Kultur Penyimpanan
 BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilaksanakan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor mulai bulan Februari
BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilaksanakan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor mulai bulan Februari
BAB III METODELOGI PENELITIAN
 BAB III METODELOGI PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada Tanggal 01 Februari 31 Juni 2011 di Laboratorium Mikrobiologi dan Rumah Kaca Balai Penelitian Tanaman Kacangkacangan
BAB III METODELOGI PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan pada Tanggal 01 Februari 31 Juni 2011 di Laboratorium Mikrobiologi dan Rumah Kaca Balai Penelitian Tanaman Kacangkacangan
III. BAHAN DAN METODE. Penelitian ini dilaksanakan di Laboratorium Penyakit Tanaman dan Laboratorium
 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Penyakit Tanaman dan Laboratorium Lapangan Terpadu Fakultas Pertanian Universitas Lampung pada bulan November
III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Penyakit Tanaman dan Laboratorium Lapangan Terpadu Fakultas Pertanian Universitas Lampung pada bulan November
III. BAHAN DAN METODE. Penelitian dilakukan di Laboratorium Penyakit Tanaman, Fakultas Pertanian,
 16 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian dilakukan di Laboratorium Penyakit Tanaman, Fakultas Pertanian, Universitas Lampung dan penelitian ini dilaksanakan pada bulan Juni 2014
16 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian dilakukan di Laboratorium Penyakit Tanaman, Fakultas Pertanian, Universitas Lampung dan penelitian ini dilaksanakan pada bulan Juni 2014
BAHAN DAN METODE. Metode Penelitian
 BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilakukan di Laboratorium Bakteriologi Tumbuhan dan Rumah Kaca University Farm, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian
BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilakukan di Laboratorium Bakteriologi Tumbuhan dan Rumah Kaca University Farm, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian
III. BAHAN DAN METODE
 III. BAHAN DAN METODE 3.1. Tempat dan Waktu Penelitian ini telah dilaksanakan di Laboratorium Penyakit Tumbuhan Fakultas Pertanian Universitas Riau, Pekanbaru yang berlangsung selama 4 bulan, dimulai dari
III. BAHAN DAN METODE 3.1. Tempat dan Waktu Penelitian ini telah dilaksanakan di Laboratorium Penyakit Tumbuhan Fakultas Pertanian Universitas Riau, Pekanbaru yang berlangsung selama 4 bulan, dimulai dari
III. BAHAN DAN METODE. Penelitian ini dilaksanakan di Laboratorium Penyakit Tumbuhan Jurusan
 11 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Penyakit Tumbuhan Jurusan Agroteknologi Bidang Proteksi Tanaman Fakultas Pertanian Universitas Lampung
11 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Penyakit Tumbuhan Jurusan Agroteknologi Bidang Proteksi Tanaman Fakultas Pertanian Universitas Lampung
BAHAN DAN METODE Tempat dan Waktu Bahan Peremajaan Aktinomiset dari Kultur Penyimpanan Perbanyakan Sclerotium rolfsii dari Kultur Penyimpanan
 BAHAN DAN METODE Tempat dan Waktu Penelitian dilaksanakan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor (IPB) mulai Maret 2011 sampai
BAHAN DAN METODE Tempat dan Waktu Penelitian dilaksanakan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor (IPB) mulai Maret 2011 sampai
LAMPIRAN. Lampiran 1. Alur Kerja Isolasi Bakteri Endofit dari Batang dan Akar Tanaman Dara metode Radu & Kqueen (2002) yang dimodifikasi
 LAMPIRAN Lampiran 1. Alur Kerja Isolasi Bakteri Endofit dari Batang dan Akar Tanaman Dara metode Radu & Kqueen (2002) yang dimodifikasi Bagian akar dan batang (3-5 cm) Dicuci dengan air mengalir selama
LAMPIRAN Lampiran 1. Alur Kerja Isolasi Bakteri Endofit dari Batang dan Akar Tanaman Dara metode Radu & Kqueen (2002) yang dimodifikasi Bagian akar dan batang (3-5 cm) Dicuci dengan air mengalir selama
II. METODOLOGI PENELITIAN. Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Udayana,
 II. METODOLOGI PENELITIAN 2.1. Metode Pengumpulan Data 2.1.1. Tempat dan waktu penelitian Penelitian dilaksanakan di Laboratorium Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam
II. METODOLOGI PENELITIAN 2.1. Metode Pengumpulan Data 2.1.1. Tempat dan waktu penelitian Penelitian dilaksanakan di Laboratorium Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam
BAHAN DAN METODE Tempat dan Waktu Penelitian Bahan dan Alat Metode Penelitian Penyiapan tanaman uji
 BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilakukan pada bulan Juli 2010 Maret 2011. Penelitian dilakukan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian,
BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilakukan pada bulan Juli 2010 Maret 2011. Penelitian dilakukan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian,
LAMPIRAN. Universitas Sumatera Utara
 LAMPIRAN Lampiran 1. Sterilisasi Alat dan Bahan Semua peralatan yang akan digunakan dalam penelitian disterilisasikan terlebih dahulu. Peralatan mikrobiologi disterilisasi dengan oven pada suhu 171 o C
LAMPIRAN Lampiran 1. Sterilisasi Alat dan Bahan Semua peralatan yang akan digunakan dalam penelitian disterilisasikan terlebih dahulu. Peralatan mikrobiologi disterilisasi dengan oven pada suhu 171 o C
BAHAN DAN METODE. Bahan
 9 BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilaksanakan di Laboratorium Patologi Serangga, dan Laboratorium Fisiologi dan Toksikologi Serangga, Departemen Proteksi Tanaman, Fakultas Pertanian,
9 BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilaksanakan di Laboratorium Patologi Serangga, dan Laboratorium Fisiologi dan Toksikologi Serangga, Departemen Proteksi Tanaman, Fakultas Pertanian,
Koloni bakteri endofit
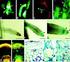 Lampiran : 1 Isolasi Bakteri Endofit pada tanaman V. varingaefolium Tanaman Vaccinium varingaefolium Diambil bagian akar tanaman Dicuci (menghilangkan kotoran) Dimasukkan ke dalam plastik Dimasukkan ke
Lampiran : 1 Isolasi Bakteri Endofit pada tanaman V. varingaefolium Tanaman Vaccinium varingaefolium Diambil bagian akar tanaman Dicuci (menghilangkan kotoran) Dimasukkan ke dalam plastik Dimasukkan ke
III. METODE PENELITIAN. Penelitian dilaksanakan di Laboratorium Penyakit Tumbuhan Jurusan
 14 III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian dilaksanakan di Laboratorium Penyakit Tumbuhan Jurusan Agroteknologi Fakultas Pertanian Universitas Lampung. Pelaksanaan penelitian
14 III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian dilaksanakan di Laboratorium Penyakit Tumbuhan Jurusan Agroteknologi Fakultas Pertanian Universitas Lampung. Pelaksanaan penelitian
BAHAN DAN METODE Tempat dan waktu penelitian Bahan dan Alat Isolasi dan Uji Reaksi Hipersensitif Bakteri Penghasil Siderofor
 BAHAN DAN METODE Tempat dan waktu penelitian Penelitian dilaksanakan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor, dari Oktober 2010
BAHAN DAN METODE Tempat dan waktu penelitian Penelitian dilaksanakan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor, dari Oktober 2010
III. METODE PENELITIAN. Penelitian ini dilaksanakan di Laboratorium Botani, Fakultas Matematika dan Ilmu
 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Botani, Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung pada bulan Agustus 2012 sampai
III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Botani, Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung pada bulan Agustus 2012 sampai
III. BAHAN DAN METODE
 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian dilaksanakan di Laboratorium Lapang Terpadu dan di Laboratorium Penyakit Tumbuhan, Fakultas Pertanian, Universtitas Lampung dari Desember
III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian dilaksanakan di Laboratorium Lapang Terpadu dan di Laboratorium Penyakit Tumbuhan, Fakultas Pertanian, Universtitas Lampung dari Desember
METODE PENELITIAN. Penelitian dilaksanakan pada bulan Agustus sampai Februari 2014.
 10 METODE PENELITIAN Waktu dan Tempat Penelitian dilaksanakan pada bulan Agustus sampai Februari 2014. Pengambilan sampel tanah dilakukan di Hutan mangrove Percut Sei Tuan Kabupaten Deli Serdang. Analisis
10 METODE PENELITIAN Waktu dan Tempat Penelitian dilaksanakan pada bulan Agustus sampai Februari 2014. Pengambilan sampel tanah dilakukan di Hutan mangrove Percut Sei Tuan Kabupaten Deli Serdang. Analisis
PENYAKIT BAKTERI PADA KEDELAI Dl KALIMAWTAN SELATAN : IDENTIFIKASI, KEHILANGAN HASIL, DAN KELANGSUNGAN HlDUP PATOGEN
 PENYAKIT BAKTERI PADA KEDELAI Dl KALIMAWTAN SELATAN : IDENTIFIKASI, KEHILANGAN HASIL, DAN KELANGSUNGAN HlDUP PATOGEN Oleh M. HANAFIAH AlNl PROGRAM PASCASARJANA INSTITUT PERTANIAN BOGOR 1992 PENYAKIT BAKTERI
PENYAKIT BAKTERI PADA KEDELAI Dl KALIMAWTAN SELATAN : IDENTIFIKASI, KEHILANGAN HASIL, DAN KELANGSUNGAN HlDUP PATOGEN Oleh M. HANAFIAH AlNl PROGRAM PASCASARJANA INSTITUT PERTANIAN BOGOR 1992 PENYAKIT BAKTERI
Lampiran 1. Penyiapan media bakteri Aeromonas hydrophila
 Lampiran 1. Penyiapan media bakteri Aeromonas hydrophila a. Media TSA (Trypticase Soy Agar) Untuk membuat media TSA, dilarutkan 4 gram TSA dalam 100 ml akuades yang ditempatkan dalam erlenmeyer dan dipanaskan
Lampiran 1. Penyiapan media bakteri Aeromonas hydrophila a. Media TSA (Trypticase Soy Agar) Untuk membuat media TSA, dilarutkan 4 gram TSA dalam 100 ml akuades yang ditempatkan dalam erlenmeyer dan dipanaskan
BAHAN DAN METODE. Penelitian dilaksanakan di Laboratorium Penyakit Tumbuhan Jurusan Proteksi
 11 III. BAHAN DAN METODE 3.1 Tempat Penelitian dan Waktu Penelitian dilaksanakan di Laboratorium Penyakit Tumbuhan Jurusan Proteksi Tanaman Fakultas Pertanian Universitas Lampung. Pelaksanaan penelitian
11 III. BAHAN DAN METODE 3.1 Tempat Penelitian dan Waktu Penelitian dilaksanakan di Laboratorium Penyakit Tumbuhan Jurusan Proteksi Tanaman Fakultas Pertanian Universitas Lampung. Pelaksanaan penelitian
III. METODE PENELITIAN. Penelitian ini dilakukan di Laboratorium Mikrobiologi Jurusan Biologi
 13 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung. Penelitian
13 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung. Penelitian
Penelitian ini dilakukan di laboratorium Mikrobiologi Pangan Universitas Katolik Soegijapranata pada Agustus 2013 hingga Januari 2014.
 2. MATERI DAN METODE 2.1. Waktu dan Tempat Penelitian Penelitian ini dilakukan di laboratorium Mikrobiologi Pangan Universitas Katolik Soegijapranata pada Agustus 2013 hingga Januari 2014. 2.2. Materi
2. MATERI DAN METODE 2.1. Waktu dan Tempat Penelitian Penelitian ini dilakukan di laboratorium Mikrobiologi Pangan Universitas Katolik Soegijapranata pada Agustus 2013 hingga Januari 2014. 2.2. Materi
Sampel air panas. Pengenceran 10-1
 Lampiran 1. Metode kerja Sampel air panas Diambil 10 ml Dicampur dengan media selektif 90ml Di inkubasi 24 jam, suhu 50 C Pengenceran 10-1 Di encerkan sampai 10-10 Tiap pengenceran di tanam di cawan petri
Lampiran 1. Metode kerja Sampel air panas Diambil 10 ml Dicampur dengan media selektif 90ml Di inkubasi 24 jam, suhu 50 C Pengenceran 10-1 Di encerkan sampai 10-10 Tiap pengenceran di tanam di cawan petri
III. BAHAN DAN METODE. Tanaman, serta Laboratorium Lapang Terpadu, Fakultas Pertanian, Universitas
 13 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Hama dan Penyakit Bidang Proteksi Tanaman, serta Laboratorium Lapang Terpadu, Fakultas Pertanian, Universitas
13 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Hama dan Penyakit Bidang Proteksi Tanaman, serta Laboratorium Lapang Terpadu, Fakultas Pertanian, Universitas
III. METODOLOGIPENELITIAN
 III. METODOLOGIPENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian ini dilaksanakan antara Februari-Agustus 2007, di Laboratorium Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan
III. METODOLOGIPENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian ini dilaksanakan antara Februari-Agustus 2007, di Laboratorium Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan
BAB III METODE PENELITIAN. Pangan dan Hortikultura Sidoarjo dan Laboratorium Mikrobiologi, Depertemen
 BAB III METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di UPT Pengembangan Agrobisnis Tanaman Pangan dan Hortikultura Sidoarjo dan Laboratorium Mikrobiologi, Depertemen Biologi,
BAB III METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di UPT Pengembangan Agrobisnis Tanaman Pangan dan Hortikultura Sidoarjo dan Laboratorium Mikrobiologi, Depertemen Biologi,
BAB III BAHAN DAN METODE
 BAB III BAHAN DAN METODE 3.1 Waktu dan Tempat Penelitian Penelitian dilaksanakan pada bulan September sampai Oktober 2009. Pengambilan sampel susu dilakukan di beberapa daerah di wilayah Jawa Barat yaitu
BAB III BAHAN DAN METODE 3.1 Waktu dan Tempat Penelitian Penelitian dilaksanakan pada bulan September sampai Oktober 2009. Pengambilan sampel susu dilakukan di beberapa daerah di wilayah Jawa Barat yaitu
III. BAHAN DAN METODE. Penelitian ini dilaksanakan di Laboratorium Penyakit Tumbuhan dan Kebun
 17 III. BAHAN DAN MEODE 3.1 empat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Penyakit umbuhan dan ebun Percobaan di dalam kampus di Program Studi Agroteknologi Fakultas Pertanian,
17 III. BAHAN DAN MEODE 3.1 empat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Penyakit umbuhan dan ebun Percobaan di dalam kampus di Program Studi Agroteknologi Fakultas Pertanian,
III. METODE PENELITIAN. Penelitian ini dilaksanakan di Laboratorium Botani, Jurusan Biologi, Fakultas
 17 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Botani, Jurusan Biologi, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Lampung, pada bulan
17 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Botani, Jurusan Biologi, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Lampung, pada bulan
IV. KULTIVASI MIKROBA
 IV. KULTIVASI MIKROBA PENDAHULUAN Untuk memperoleh kultur murni hasil isolasi dari berbagai tempat maka dibutuhkan alat, bahan dan metode seperti ilistrasi di bawah ini : Media Umum Diferensial Selektif
IV. KULTIVASI MIKROBA PENDAHULUAN Untuk memperoleh kultur murni hasil isolasi dari berbagai tempat maka dibutuhkan alat, bahan dan metode seperti ilistrasi di bawah ini : Media Umum Diferensial Selektif
II. MATERI DAN METODE
 II. MATERI DAN METODE 2.1 Materi, Lokasi, dan Waktu Penelitian 2.1.1 Materi Alat yang digunakan dalam penelitian adalah cawan petri, tabung reaksi, gelas ukur, pembakar spiritus, pipet, jarum ose, erlenmeyer,
II. MATERI DAN METODE 2.1 Materi, Lokasi, dan Waktu Penelitian 2.1.1 Materi Alat yang digunakan dalam penelitian adalah cawan petri, tabung reaksi, gelas ukur, pembakar spiritus, pipet, jarum ose, erlenmeyer,
METODE PENELITIAN. Penelitian ini dilakukan di Laboratorium Mikrobiologi Jurusan Biologi Fakultas
 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung dari bulan
III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung dari bulan
III. BAHAN DAN METODE. Penelitian dilaksanakan di Laboratorium Ilmu Penyakit Tumbuhan, Bidang
 8 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian dilaksanakan di Laboratorium Ilmu Penyakit Tumbuhan, Bidang Proteksi Tanaman, Jurusan Agroteknologi, Fakultas Pertanian Universitas Lampung
8 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian dilaksanakan di Laboratorium Ilmu Penyakit Tumbuhan, Bidang Proteksi Tanaman, Jurusan Agroteknologi, Fakultas Pertanian Universitas Lampung
III. METODOLOGI PENELITIAN. Penelitian ini akan dilakukan pada bulan Juli sampai September 2012,
 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini akan dilakukan pada bulan Juli sampai September 2012, bertempat di Laboratorium Biokimia Jurusan Kimia Fakultas MIPA Universitas
III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini akan dilakukan pada bulan Juli sampai September 2012, bertempat di Laboratorium Biokimia Jurusan Kimia Fakultas MIPA Universitas
III. METODE PENELITIAN. Penelitian dilaksanakan pada Oktober 2011 sampai Maret 2012 di Rumah Kaca
 III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian dilaksanakan pada Oktober 2011 sampai Maret 2012 di Rumah Kaca dan di Laboratorium Penyakit Tumbuhan Jurusan Proteksi Tanaman Fakultas Pertanian Universitas
III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian dilaksanakan pada Oktober 2011 sampai Maret 2012 di Rumah Kaca dan di Laboratorium Penyakit Tumbuhan Jurusan Proteksi Tanaman Fakultas Pertanian Universitas
III. BAHAN DAN METODE. Penelitian ini dilaksanakan pada bulan Maret Oktober 2014 di
 III. BAHAN DAN METODE 3.1 Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan Maret 2014 - Oktober 2014 di Laboratorium Hama Tumbuhan, Jurusan Agroteknologi, Fakultas Pertanian Universitas
III. BAHAN DAN METODE 3.1 Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan Maret 2014 - Oktober 2014 di Laboratorium Hama Tumbuhan, Jurusan Agroteknologi, Fakultas Pertanian Universitas
III. BAHAN DAN METODE. Penelitian ini dilaksanakan pada bulan Juli sampai bulan November 2009, di
 III. BAHAN DAN METODE A. Tempat dan Waktu Penelitian Penelitian ini dilaksanakan pada bulan Juli sampai bulan November 2009, di Laboratorium Kesuburan Tanah, dan Laboratorium Bioteknologi Pertanian Fakultas
III. BAHAN DAN METODE A. Tempat dan Waktu Penelitian Penelitian ini dilaksanakan pada bulan Juli sampai bulan November 2009, di Laboratorium Kesuburan Tanah, dan Laboratorium Bioteknologi Pertanian Fakultas
BAHAN DAN METODE. Kasa Fakultas Pertanian Universitas Sumatera Utara, Medan dengan ketinggian tempat
 BAHAN DAN METODE Tempat dan waktu penelitian Penelitian ini dilaksanakan di Laboratorium Penyakit Tumbuhan dan di Rumah Kasa Fakultas Pertanian, Medan dengan ketinggian tempat + 25 m dpl pada Bulan Mei
BAHAN DAN METODE Tempat dan waktu penelitian Penelitian ini dilaksanakan di Laboratorium Penyakit Tumbuhan dan di Rumah Kasa Fakultas Pertanian, Medan dengan ketinggian tempat + 25 m dpl pada Bulan Mei
III. METODE PENELITIAN. Penelitian ini dilakukan pada bulan Januari sampai bulan April 2014.
 14 III. METODE PENELITIAN A. Tempat Dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Mikrobiologi Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas
14 III. METODE PENELITIAN A. Tempat Dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Mikrobiologi Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas
BAHAN DAN METODE Tempat dan Waktu Metode Penelitian Perbanyakan Propagul Agens Antagonis Perbanyakan Massal Bahan Pembawa Biopestisida
 7 BAHAN DAN METODE Tempat dan Waktu Penelitian ini dilaksanakan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor dan Balai Penelitian Tanaman
7 BAHAN DAN METODE Tempat dan Waktu Penelitian ini dilaksanakan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor dan Balai Penelitian Tanaman
BAB III METODELOGI PENELITIAN
 BAB III METODELOGI PENELITIAN 3.1 JENIS PENELITIAN : Eksperimental Laboratoris 3.2 LOKASI PENELITIAN : Laboratorium Fatokimia Fakultas Farmasi UH & Laboratorium Mikrobiologi FK UH 3.3 WAKTU PENELITIAN
BAB III METODELOGI PENELITIAN 3.1 JENIS PENELITIAN : Eksperimental Laboratoris 3.2 LOKASI PENELITIAN : Laboratorium Fatokimia Fakultas Farmasi UH & Laboratorium Mikrobiologi FK UH 3.3 WAKTU PENELITIAN
BAB III METODE PENELITIAN. Penelitian dilakukan di Laboratorium Mikrobiologi Analis Kesehatan
 BAB III METODE PENELITIAN A. Desain Penelitian Desain penelitian yang akan dilakukan menggunakan metode deskriptif. B. Tempat dan waktu Penelitian Penelitian dilakukan di Laboratorium Mikrobiologi Analis
BAB III METODE PENELITIAN A. Desain Penelitian Desain penelitian yang akan dilakukan menggunakan metode deskriptif. B. Tempat dan waktu Penelitian Penelitian dilakukan di Laboratorium Mikrobiologi Analis
III. BAHAN DAN METODE. Penelitian ini dilaksanakan di Laboratorium Ilmu Penyakit Tanaman Fakultas
 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Ilmu Penyakit Tanaman Fakultas Pertanian Universitas Lampung. Pelaksanaan penelitian dimulai dari September
III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Ilmu Penyakit Tanaman Fakultas Pertanian Universitas Lampung. Pelaksanaan penelitian dimulai dari September
BAB III METODE PENELITIAN. Biologi, Fakultas Sains dan Teknologi, Universitas Airlangga Surabaya dan
 BAB III METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Mikrobiologi Departemen Biologi, Fakultas Sains dan Teknologi, Universitas Airlangga Surabaya dan kumbung
BAB III METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Mikrobiologi Departemen Biologi, Fakultas Sains dan Teknologi, Universitas Airlangga Surabaya dan kumbung
III. BAHAN DAN METODE
 10 III. BAHAN DAN METODE 3.1 Waktu dan Tempat Penelitian dilaksanakan dari bulan Oktober 2011 sampai Oktober 2012. Sampel gubal dan daun gaharu diambil di Desa Pulo Aro, Kecamatan Tabir Ulu, Kabupaten
10 III. BAHAN DAN METODE 3.1 Waktu dan Tempat Penelitian dilaksanakan dari bulan Oktober 2011 sampai Oktober 2012. Sampel gubal dan daun gaharu diambil di Desa Pulo Aro, Kecamatan Tabir Ulu, Kabupaten
III. METODE PENELITIAN. Penelitian ini dilakukan di Laboratorium Mikrobiologi Jurusan Biologi
 17 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung pada Januari
17 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung pada Januari
METODE PENELITIAN. Penelitian ini dilakukan dari Bulan April sampai dengan Juni 2013, di
 17 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian ini dilakukan dari Bulan April sampai dengan Juni 2013, di Laboratorium Mikrobiologi Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas
17 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian ini dilakukan dari Bulan April sampai dengan Juni 2013, di Laboratorium Mikrobiologi Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas
NATA DE COCO 1. PENDAHULUAN
 NATA DE COCO 1. PENDAHULUAN Nata adalah biomassa yang sebagian besar terdiri dari sellulosa, berbentuk agar dan berwarna putih. Massa ini berasal dari pertumbuhan Acetobacter xylinum pada permukaan media
NATA DE COCO 1. PENDAHULUAN Nata adalah biomassa yang sebagian besar terdiri dari sellulosa, berbentuk agar dan berwarna putih. Massa ini berasal dari pertumbuhan Acetobacter xylinum pada permukaan media
BAHAN DAN METODE. Tabel 1 Kombinasi perlakuan yang dilakukan di lapangan
 13 BAHAN DAN METODE Tempat dan waktu Penelitian ini dilaksanakan di Desa Ciburuy, Kecamatan Cigombong, Kabupaten Bogor serta di Laboratorium Bakteriologi, Departemen Proteksi Tanaman, Fakultas Pertanian,
13 BAHAN DAN METODE Tempat dan waktu Penelitian ini dilaksanakan di Desa Ciburuy, Kecamatan Cigombong, Kabupaten Bogor serta di Laboratorium Bakteriologi, Departemen Proteksi Tanaman, Fakultas Pertanian,
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1. Rancangan Penelitian Penelitian ini merupakan penelitian eksperimental. Rancangan yang digunakan dalam penelitian ini adalah rancangan acak lengkap (RAL) tunggal, dengan
BAB III METODE PENELITIAN 3.1. Rancangan Penelitian Penelitian ini merupakan penelitian eksperimental. Rancangan yang digunakan dalam penelitian ini adalah rancangan acak lengkap (RAL) tunggal, dengan
BAB 4. METODE PENELITIAN
 BAB 4. METODE PENELITIAN Pada Tahun I penelitian ini dilakukan 3 tahap percobaan sebagai berikut: 1. Percobaan 1 : Penentuan bahan baku pupuk organik Tujuan percobaan adalah untuk mendapatkan komposisi
BAB 4. METODE PENELITIAN Pada Tahun I penelitian ini dilakukan 3 tahap percobaan sebagai berikut: 1. Percobaan 1 : Penentuan bahan baku pupuk organik Tujuan percobaan adalah untuk mendapatkan komposisi
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian dilaksanakan dari Bulan April sampai Bulan Agustus 2013. Penelitian pengaruh penambahan edible coat kitosan sebagai anti jamur pada
BAB III METODE PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian dilaksanakan dari Bulan April sampai Bulan Agustus 2013. Penelitian pengaruh penambahan edible coat kitosan sebagai anti jamur pada
BAB III METODE PENELITIAN. Jenis penelitian ini adalah penelitian deskriptif. Tempat penelitian di laboratorium lab. Mikrobiologi, Lantai II di kampus
 BAB III METODE PENELITIAN A. Jenis Penelitian Jenis penelitian ini adalah penelitian deskriptif. B. Tempat dan Waktu Penelitian Tempat penelitian di laboratorium lab. Mikrobiologi, Lantai II di kampus
BAB III METODE PENELITIAN A. Jenis Penelitian Jenis penelitian ini adalah penelitian deskriptif. B. Tempat dan Waktu Penelitian Tempat penelitian di laboratorium lab. Mikrobiologi, Lantai II di kampus
BAB III METODE PENELITIAN. terdiri atas 5 perlakuan dengan 3 ulangan yang terdiri dari:
 BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian ini menggunakan rancangan acak lengkap (RAL) yang terdiri atas 5 perlakuan dengan 3 ulangan yang terdiri dari: 1. 0 ppm: perbandingan media
BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian ini menggunakan rancangan acak lengkap (RAL) yang terdiri atas 5 perlakuan dengan 3 ulangan yang terdiri dari: 1. 0 ppm: perbandingan media
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan di Laboratorium dan Rumah Kaca Departemen Silvikultur, Fakultas Kehutanan, Institut Pertanian Bogor, mulai bulan Januari 2012
BAB III METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian ini dilaksanakan di Laboratorium dan Rumah Kaca Departemen Silvikultur, Fakultas Kehutanan, Institut Pertanian Bogor, mulai bulan Januari 2012
BAB III METODE PENELITIAN. eksplorasi dengan cara menggunakan isolasi jamur endofit dari akar kentang
 BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Jenis penelitian ini adalah penelitian eksplorasi dan eksperimen. Penelitian eksplorasi dengan cara menggunakan isolasi jamur endofit dari akar kentang
BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Jenis penelitian ini adalah penelitian eksplorasi dan eksperimen. Penelitian eksplorasi dengan cara menggunakan isolasi jamur endofit dari akar kentang
BAB III METODE PENELITIAN. Rancangan penelitian yang digunakan adalah rancangan penelitian
 BAB III METODE PENELITIAN 3.1 Rancangan Penelitian dan Analisis Data Rancangan penelitian yang digunakan adalah rancangan penelitian deskriptif. Data yang diperoleh disajikan secara deskriptif meliputi
BAB III METODE PENELITIAN 3.1 Rancangan Penelitian dan Analisis Data Rancangan penelitian yang digunakan adalah rancangan penelitian deskriptif. Data yang diperoleh disajikan secara deskriptif meliputi
III. METODE PENELITIAN. Persiapan alat dan bahan yang akan digunakan. Pembuatan media PDA (Potato Dextrose Agar)
 III. METODE PENELITIAN A. Bagan Alir Penelitian Persiapan alat dan bahan yang akan digunakan Pembuatan media PDA (Potato Dextrose Agar) Pengambilan sampel tanah dekat perakaran tanaman Cabai merah (C.
III. METODE PENELITIAN A. Bagan Alir Penelitian Persiapan alat dan bahan yang akan digunakan Pembuatan media PDA (Potato Dextrose Agar) Pengambilan sampel tanah dekat perakaran tanaman Cabai merah (C.
BAB III METODE PENELITIAN. diperoleh dari perhitungan kepadatan sel dan uji kadar lipid Scenedesmus sp. tiap
 BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Jenis penelitian ini adalah eksperimental. Pengambilan data penelitian diperoleh dari perhitungan kepadatan sel dan uji kadar lipid Scenedesmus sp. tiap
BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Jenis penelitian ini adalah eksperimental. Pengambilan data penelitian diperoleh dari perhitungan kepadatan sel dan uji kadar lipid Scenedesmus sp. tiap
III. BAHAN DAN METODE PENELITIAN. Penelitian Laboratorium dilaksanakan di Laboratorium Agroteknologi,
 III. BAHAN DAN METODE PENELITIAN 3.1. Tempat dan Waktu Penelitian Penelitian Laboratorium dilaksanakan di Laboratorium Agroteknologi, Universitas Medan Area. Penelitian Lapangan dilaksanakan di desa Durin
III. BAHAN DAN METODE PENELITIAN 3.1. Tempat dan Waktu Penelitian Penelitian Laboratorium dilaksanakan di Laboratorium Agroteknologi, Universitas Medan Area. Penelitian Lapangan dilaksanakan di desa Durin
BAB III METODA PENELITIAN
 BAB III METODA PENELITIAN A. Jenis penelitian Jenis penelitian ini adalah deskriptif. B. Tempat dan waktu penelitian Penelitian dilakukan di laboratorium mikrobiologi, Universitas Muhammadiyah Semarang.
BAB III METODA PENELITIAN A. Jenis penelitian Jenis penelitian ini adalah deskriptif. B. Tempat dan waktu penelitian Penelitian dilakukan di laboratorium mikrobiologi, Universitas Muhammadiyah Semarang.
NATA DE SOYA. a) Pemeliharaan Biakan Murni Acetobacter xylinum.
 NATA DE SOYA 1. PENDAHULUAN Nata adalah biomassa yang sebagian besar terdiri dari selulosa, berbentuk agar dan berwarna putih. Massa ini berasal pertumbuhan Acetobacter xylinum pada permukaan media cair
NATA DE SOYA 1. PENDAHULUAN Nata adalah biomassa yang sebagian besar terdiri dari selulosa, berbentuk agar dan berwarna putih. Massa ini berasal pertumbuhan Acetobacter xylinum pada permukaan media cair
BAB III METODE PENELITIAN. Penelitian ini merupakan penelitian eksplorasi yang dilakukan dengan cara
 30 BAB III METODE PENELITIAN 3.1 Jenis Penelitian Penelitian ini merupakan penelitian eksplorasi yang dilakukan dengan cara identifikasi bakteri dari probiotik yang berpotensi sebagai bahan biodekomposer.
30 BAB III METODE PENELITIAN 3.1 Jenis Penelitian Penelitian ini merupakan penelitian eksplorasi yang dilakukan dengan cara identifikasi bakteri dari probiotik yang berpotensi sebagai bahan biodekomposer.
BAHAN DAN METODE Bahan dan Alat
 19 Metode ekstraksi tergantung pada polaritas senyawa yang diekstrak. Suatu senyawa menunjukkan kelarutan yang berbeda-beda dalam pelarut yang berbeda. Hal-hal yang harus diperhatikan dalam pemilihan pelarut
19 Metode ekstraksi tergantung pada polaritas senyawa yang diekstrak. Suatu senyawa menunjukkan kelarutan yang berbeda-beda dalam pelarut yang berbeda. Hal-hal yang harus diperhatikan dalam pemilihan pelarut
BAHAN DAN METODE Waktu dan Tempat Bahan dan Alat Metode Penelitian Penyediaan Isolat Fusarium sp. dan Bakteri Aktivator
 BAHAN DAN METODE Waktu dan Tempat Penelitian ini dilakukan di Laboratorium Mikologi, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor, dan Laboratorium Mikrobiologi dan Kesehatan
BAHAN DAN METODE Waktu dan Tempat Penelitian ini dilakukan di Laboratorium Mikologi, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor, dan Laboratorium Mikrobiologi dan Kesehatan
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Jenis penelitian ini adalah penelitian eksplorasi dan eksperimental dengan menguji isolat bakteri endofit dari akar tanaman kentang (Solanum tuberosum
BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Jenis penelitian ini adalah penelitian eksplorasi dan eksperimental dengan menguji isolat bakteri endofit dari akar tanaman kentang (Solanum tuberosum
TATA CARA PENELITIAN. A. Tempat dan waktu penelitian Penelitian dilakukan di green house milik UMY dan Laboratorium
 III. TATA CARA PENELITIAN A. Tempat dan waktu penelitian Penelitian dilakukan di green house milik UMY dan Laboratorium Agrobioteknologi, Fakultas Pertanian Universitas Muhammadiyah Yogyakarta. Penelitian
III. TATA CARA PENELITIAN A. Tempat dan waktu penelitian Penelitian dilakukan di green house milik UMY dan Laboratorium Agrobioteknologi, Fakultas Pertanian Universitas Muhammadiyah Yogyakarta. Penelitian
BAB III METODE PERCOBAAN. Kelompok (RAK) Faktorial dengan 2 faktor perlakuan, yaitu perlakuan jenis
 BAB III METODE PERCOBAAN 3.1 Rancangan Penelitian Rancangan yang digunakan dalam penelitian ini adalah Rancangan Acak Kelompok (RAK) Faktorial dengan 2 faktor perlakuan, yaitu perlakuan jenis isolat (HJMA-5
BAB III METODE PERCOBAAN 3.1 Rancangan Penelitian Rancangan yang digunakan dalam penelitian ini adalah Rancangan Acak Kelompok (RAK) Faktorial dengan 2 faktor perlakuan, yaitu perlakuan jenis isolat (HJMA-5
BAHAN DAN METODE. Pertanian Universitas Sumatera Utara, Medan dengan ketinggian tempat + 25
 BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Penyakit Tumbuhan Fakultas Pertanian, Medan dengan ketinggian tempat + 25 meter di atas permukaan laut pada bulan
BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Penyakit Tumbuhan Fakultas Pertanian, Medan dengan ketinggian tempat + 25 meter di atas permukaan laut pada bulan
III. METODOLOGI PENELITIAN. Penelitian ini dilakukan pada bulan Juli 2012 sampai bulan Desember 2012 di
 23 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan Juli 2012 sampai bulan Desember 2012 di Laboratorium Biokimia Jurusan Kimia Fakultas Matematika dan Ilmu
23 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan Juli 2012 sampai bulan Desember 2012 di Laboratorium Biokimia Jurusan Kimia Fakultas Matematika dan Ilmu
BAHAN DAN METODE Tempat dan Waktu Penyiapan Tanaman Uji Pemeliharaan dan Penyiapan Suspensi Bakteri Endofit dan PGPR
 17 BAHAN DAN METODE Tempat dan Waktu Penelitian dilakukan di Laboratorium Bakteriologi Tumbuhan Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor dan di Rumah Kaca, University Farm,
17 BAHAN DAN METODE Tempat dan Waktu Penelitian dilakukan di Laboratorium Bakteriologi Tumbuhan Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor dan di Rumah Kaca, University Farm,
III. BAHAN DAN METODE. Penelitian dilakukan pada lahan alang-alang di Kelurahan Segalamider,
 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian dilakukan pada lahan alang-alang di Kelurahan Segalamider, Kecamatan Tanjung Karang Barat, Kota Bandar Lampung. Lokasi percobaan secara
III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian dilakukan pada lahan alang-alang di Kelurahan Segalamider, Kecamatan Tanjung Karang Barat, Kota Bandar Lampung. Lokasi percobaan secara
BAB III METODE PENELITIAN. lengkap (RAL) pola faktorial yang terdiri dari 2 faktor. Faktor pertama adalah variasi
 BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Rancangan yang digunakan dalam penelitian ini adalah rancangan acak lengkap (RAL) pola faktorial yang terdiri dari 2 faktor. Faktor pertama adalah variasi
BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Rancangan yang digunakan dalam penelitian ini adalah rancangan acak lengkap (RAL) pola faktorial yang terdiri dari 2 faktor. Faktor pertama adalah variasi
III. METODE PENELITIAN
 III. METODE PENELITIAN A. Materi, Lokasi dan Waktu Penelitian 1. Materi Penelitian a. Bahan Bahan yang digunakan dalam penelitian ini adalah jamur yang memiliki tubuh buah, serasah daun, ranting, kayu
III. METODE PENELITIAN A. Materi, Lokasi dan Waktu Penelitian 1. Materi Penelitian a. Bahan Bahan yang digunakan dalam penelitian ini adalah jamur yang memiliki tubuh buah, serasah daun, ranting, kayu
PEMANFAATAN RADIASI SINAR GAMMA (Co-60) UNTUK PENINGKATAN PERTUMBUHAN DAN KETAHANAN TANAMAN KEDELAI TERHADAP PENYAKIT PUSTUL DAUN
 PEMANFAATAN RADIASI SINAR GAMMA (Co-60) UNTUK PENINGKATAN PERTUMBUHAN DAN KETAHANAN TANAMAN KEDELAI TERHADAP PENYAKIT PUSTUL DAUN KARYA ILMIAH TERTULIS (SKRIPSI) Diajukan Guna Memenuhi Salah Satu Syarat
PEMANFAATAN RADIASI SINAR GAMMA (Co-60) UNTUK PENINGKATAN PERTUMBUHAN DAN KETAHANAN TANAMAN KEDELAI TERHADAP PENYAKIT PUSTUL DAUN KARYA ILMIAH TERTULIS (SKRIPSI) Diajukan Guna Memenuhi Salah Satu Syarat
BAB III MATERI DAN METODE. Penelitian tentang populasi bakteri dan keberadaan bakteri gram pada
 10 BAB III MATERI DAN METODE Penelitian tentang populasi bakteri dan keberadaan bakteri gram pada pellet calf starter dengan penambahan bakteri asam laktat dari limbah kubis terfermentasi telah dilaksanakan
10 BAB III MATERI DAN METODE Penelitian tentang populasi bakteri dan keberadaan bakteri gram pada pellet calf starter dengan penambahan bakteri asam laktat dari limbah kubis terfermentasi telah dilaksanakan
III. BAHAN DAN METODE
 III. BAHAN DAN METODE 3.1. Tempat dan waktu Penelitian ini dilaksanakan di Laboratorium Penyakit Tumbuhan Fakultas Pertanian Universitas Riau kampus Bina Widya Jl. H.R Soebrantas Km 12,5 Simpang Baru Panam
III. BAHAN DAN METODE 3.1. Tempat dan waktu Penelitian ini dilaksanakan di Laboratorium Penyakit Tumbuhan Fakultas Pertanian Universitas Riau kampus Bina Widya Jl. H.R Soebrantas Km 12,5 Simpang Baru Panam
II. METODELOGI PENELITIAN
 II. METODELOGI PENELITIAN 2.1 Metode Pengumpulan Data 2.1.1 Waktu dan Tempat Penelitian Penelitian ini dilakukan di UPT Laboratorium Biosain dan Bioteknologi Universitas Udayana. Penelitian ini berlangsung
II. METODELOGI PENELITIAN 2.1 Metode Pengumpulan Data 2.1.1 Waktu dan Tempat Penelitian Penelitian ini dilakukan di UPT Laboratorium Biosain dan Bioteknologi Universitas Udayana. Penelitian ini berlangsung
III BAHAN DAN METODE
 meliputi daerah Jawa, Kalimantan dan Sumatera. Tanaman Kilemo di daerah Jawa banyak ditemui pada daerah dengan ketinggian 230 700 meter di atas permukaan laut (mdpl). Tanaman ini terutama banyak ditemui
meliputi daerah Jawa, Kalimantan dan Sumatera. Tanaman Kilemo di daerah Jawa banyak ditemui pada daerah dengan ketinggian 230 700 meter di atas permukaan laut (mdpl). Tanaman ini terutama banyak ditemui
BAHAN DAN METODE. Penelitian ini dilaksanakan di Laboratorium Penyakit Tumbuhan dan di halaman
 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Penyakit Tumbuhan dan di halaman Jurusan Proteksi Tanaman Fakultas Pertanian Universitas Lampung dari bulan
III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Penyakit Tumbuhan dan di halaman Jurusan Proteksi Tanaman Fakultas Pertanian Universitas Lampung dari bulan
II. MATERI DAN METODE PENELITIAN
 8 II. MATERI DAN METODE PENELITIAN 1. Materi, Lokasi, dan Waktu Penelitian 1.1 Materi Penelitian 1.1.1 Bahan Bahan yang digunakan dalam penelitian ini adalah jamur yang bertubuh buah, serasah daun, batang/ranting
8 II. MATERI DAN METODE PENELITIAN 1. Materi, Lokasi, dan Waktu Penelitian 1.1 Materi Penelitian 1.1.1 Bahan Bahan yang digunakan dalam penelitian ini adalah jamur yang bertubuh buah, serasah daun, batang/ranting
METODE PENELITIAN. Waktu Penelitian. Penelitian dilaksanakan pada bulan Juni 2011 sampai dengan bulan April Bahan dan Alat.
 23 METODE PENELITIAN Tempat Penelitian Pengambilan sampel daging sapi impor untuk penelitian ini dilakukan di Instalasi Karantina Produk Hewan (IKPH). Pengujian sampel dilakukan di laboratorium Balai Besar
23 METODE PENELITIAN Tempat Penelitian Pengambilan sampel daging sapi impor untuk penelitian ini dilakukan di Instalasi Karantina Produk Hewan (IKPH). Pengujian sampel dilakukan di laboratorium Balai Besar
III. BAHAN DAN METODE. Penelitian ini dilaksanakan di Laboratorium Hama Tumbuhan Jurusan
 12 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Hama Tumbuhan Jurusan Agroteknologi Fakultas Pertanian Universitas Lampung dan Laboratorium Lapangan
12 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Hama Tumbuhan Jurusan Agroteknologi Fakultas Pertanian Universitas Lampung dan Laboratorium Lapangan
III. BAHAN DAN METODE. Penelitian ini dilaksanakan di Kebun Percobaan Tanaman Industri dan Penyegar
 25 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Kebun Percobaan Tanaman Industri dan Penyegar Cahaya Negeri, Abung Barat, Lampung Utara dan Laboratorium Penyakit
25 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Kebun Percobaan Tanaman Industri dan Penyegar Cahaya Negeri, Abung Barat, Lampung Utara dan Laboratorium Penyakit
MATERI DAN METODE. Kasim Riau yang beralamat di Jl. HR. Soebrantas KM 15 Panam, Pekanbaru.
 III. MATERI DAN METODE 3.1. Waktu Dan Tempat Penelitian Penelitian ini dilaksanakan di laboratorium Patologi, Entomologi, dan Mikrobiologi (PEM) dan lahan kampus Universitas Islam Negeri Sultan Syarif
III. MATERI DAN METODE 3.1. Waktu Dan Tempat Penelitian Penelitian ini dilaksanakan di laboratorium Patologi, Entomologi, dan Mikrobiologi (PEM) dan lahan kampus Universitas Islam Negeri Sultan Syarif
BAHAN DAN METODE Bahan dan Alat
 23 III. BAHAN DAN METODE 3.1. Tempat dan Waktu Penelitian Penelitian dilakukan di Laboratorium Bioteknologi Tanah, Departemen Ilmu Tanah dan Sumberdaya Lahan, Fakultas Pertanian, Institut Pertanian Bogor
23 III. BAHAN DAN METODE 3.1. Tempat dan Waktu Penelitian Penelitian dilakukan di Laboratorium Bioteknologi Tanah, Departemen Ilmu Tanah dan Sumberdaya Lahan, Fakultas Pertanian, Institut Pertanian Bogor
bio.unsoed.ac.id III. METODE PENELITIAN
 III. METODE PENELITIAN A. Materi, Lokasi dan Waktu Penelitian 1. Materi Penelitian 1.1. Bahan Materi yang digunakan dalam penelitian ini adalah sampel tanah dari rizosfer tanaman Cabai merah (Capsicum
III. METODE PENELITIAN A. Materi, Lokasi dan Waktu Penelitian 1. Materi Penelitian 1.1. Bahan Materi yang digunakan dalam penelitian ini adalah sampel tanah dari rizosfer tanaman Cabai merah (Capsicum
III. BAHAN DAN METODE. Penelitian ini dilaksanakan di kebun PT NTF (Nusantara Tropical Farm) Way
 31 III. BAHAN DAN METODE A. Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di kebun PT NTF (Nusantara Tropical Farm) Way Jepara, Lampung Timur dan Laboratorium Penyakit Tumbuhan, Bidang Proteksi
31 III. BAHAN DAN METODE A. Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di kebun PT NTF (Nusantara Tropical Farm) Way Jepara, Lampung Timur dan Laboratorium Penyakit Tumbuhan, Bidang Proteksi
