PENGGUNAAN KITOSAN SEBAGAI ANTI BROWNING PADA PEMBUATAN TEPUNG KENTANG
|
|
|
- Deddy Makmur
- 6 tahun lalu
- Tontonan:
Transkripsi
1 SEMINAR NASIONAL KIMIA DAN PENDIDIKAN KIMIA VII Penguatan Profesi Bidang Kimia dan Pendidikan Kimia Melalui Riset dan Evaluasi Program Studi Pendidikan Kimia Jurusan P.MIPA FKIP UNS Surakarta, 18 April 2015 MAKALAH PENDAMPING KIMIA FISIK DAN ANORGANIK ISBN : PENGGUNAAN KITOSAN SEBAGAI ANTI BROWNING PADA PEMBUATAN TEPUNG KENTANG Zackiyah 1, *, Florentina Maria T.S 1, dan Winda Ayulestari 1 1 FPMIPA, Universitas Pendidikan Indonesia, Bandung, Indonesia tel/fax : , zackiyah_da@upi.edu ABSTRAK Pada pembuatan tepung kentang browning harus dihindari karena dapat menurunkan kualitas, hal ini terjadi karena oksidasi senyawa fenolik pada kentang yang dikatalisis oleh tirosinase (polifenoloksidase=ppo). Browning dapat dihindari dengan beberapa cara, yaitu pengaturan ph, menaikkan temperatur, menghindari kontak dengan oksigen, dan inhibisi PPO. Pada penelitian ini irisan kentang kupas sebelum dijadikan tepung dilindungi dengan larutan kitosan agar kontak dengan oksigen dapat dicegah dan browning dapat dihindari. Waktu kontak kitosan-irisan kentang dan luas permukaan irisan dapat menentukan keberkasilan anti browning sehingga pada penelitian ini dilakukan perendaman irisan kentang pada kitosan 2,5% dalam asam asetat 1% pada perbandingan larutan kitosan-kentang 1:10; 1:20; 1:30; 1:40; dan 1:50 selama 60 menit, sebagai kontrol perendaman dalam air yang dikoreksi dengan perendaman dalam asam asetat 1% tanpa kitosan. Analisis fenolik total dilakukan dengan metode Folin-Ciocalteu terhadap larutan hasil perendaman,. Pada perbandingan terbaik dilakukan perendaman pada variasi waktu 30; 60; 90; 120; dan 150 menit. Irisan kentang ditiriskan, dikeringkan dan dijadikan tepung. Analisis kecerahan dilakukan dengan Kromameter terhadap tepung kentang dari hasil rendaman. Hasil penelitian menunjukkan bahwa total fenolik pada berbagai perbandingan dan kontrol masing-masing adalah 34,41; 30,14; 43,34; 49,99; 48,30; dan 86,00 mg/l dengan tingkat kecerahannya (L*) berturut-turut adalah 57,04; 61,71; 61,58; 60,53; 61,43; dan 55,23. Total fenolik pada berbagai waktu perendaman masing-masing adalah 44,32; 43,34; 37,69; 33,42; 28,75; dan 53,26 mg/l dengan tingkat kecerahan 61,22; 61,50; 61,45; 61,75; 62,28; 58,00. Dapat disimpulkan bahwa perbandingan terbaik terjadi pada perbandingan 1:20 dan waktu perendaman pada 150 menit. Kata Kunci: kitosan, browning, tingkat kecerahan, tepung kentang.
2 PENDAHULUAN Masalah yang sering dihadapi dalam pembuatan tepung kentang adalah terjadinya browning enzimatis yang menyebabkan turunnya kualitas. Browning enzimatis tersebut disebabkan karena reaksi oksidasi senyawa fenolik dalam kentang seperti asam klorogenat, asam kafeat, asam vanilat, asam p-kumarat, asam galat, katekol, DOPA, p-cresol, m- cresol, p-hidroksifenil asam propionat, dan p-hidroksifenil asam piruvat yang dikatalisis oleh tirosinase (polifenoloksidase=ppo) pada ph sekitar 5-7 menjadi senyawa kuinon dan selanjutnya berpolimerisasi membentuk melanin yang berwarna coklat [4]. Browning enzimatis dapat diatasi dengan cara menghindari kontak dengan oksigen, inaktifasi PPO, menaikkan temperatur, dan menurunkan ph. Pada umumnya untuk menghindari browning banyak digunakan senyawa sulfurdioksida, bisulfit, ataupun metabisulfit. Senyawasenyawa tersebut dapat menimbulkan asmatik [1,4] sehingga perlu dicari senyawa anti browning yang aman bagi kesehatan diantaranya kitosan. Kitosan (1 4)-2-amino-2-deoksi-Dglukosa) merupakan biopolimer turunan polisakarida, disintesis dari deasetilasi kitin yang mempunyai gugus amina pada posisi C-2 dan gugus hidroksil pada C-3 dan C-6 seperti terlihat pada Gambar 1. Gambar 1. Struktur kimia molekul kitosan merupakan turunan polisakarida (1 4) 2- amino-2-deoksi-ß-d-glukosa Kitin disintesis dari limbah hewan berkulit keras seperti udang, kepiting, dan sejeninya, adalah merupakan senyawa terbanyak kedua setelah selulosa sehingga bahan baku untuk pembuatan kitosan berlimpah dan mudah diperoleh. Pada ph di bawah 6 kitosan lebih mudah larut dan menjadikan kitosan bermuatan positif [8,9]. Kitosan tidak beracun sehingga sering digunakan sebagai bahan tambahan pada makanan, dapat digunakan untuk mencegah browning karena pada suasana asam muatan positif dari kitosan akan mudah berikatan dengan gugus hidroksil pada polisakarida di permukaan umbi kentang, akibatnya kontak senyawasenyawa fenolik dengan oksigen dapat dihambat dan polifenoloksidase (PPO) menjadi inaktif [1]. Kitosan sebagai anti browning telah diaplikasikan pada mangga dan apel Fuji [6,8], uji pendahuluan telah kami lakukan terhadap penentuan konsentrasi kitosan terbaik untuk menghambat browning pada pembuatan tepung kentang, hasil penelitian menunjukkan bahwa konsentrasi kitosan terbaik sebesar 2,5%, untuk mengoptimalkan kinerja kitosan sebagai anti browning, maka pada penelitian ini dilakukan penentuan kondisi terbaik dari perbandingan kitosan dengan kentang dan waktu perendaman kentang dalam kitosan dengan tujuan untuk menjaga kualitas tepung kentang yang dihasilkan. METODOLOGI PENELITIAN Alat dan Bahan Alat-alat: Alat-alat gelas laboratorium kimia pada umumnya, pemanas listrik, oven, neraca analitik, filler, magnetic stirrer, spatula, pisau, botol vial, saringan, blender,
3 loyang, kuvet, Spektrofotometer UV-Vis mini (Shimadzu, 1240), dan kromameter (Minolta, CR-310). Bahan-bahan: kentang dieng, kitosan, asam asetat (Merck), aquades, aquabides, natrium karbonat (Merck), dan perekasi Folin-Ciocalteu. Prosedur Penelitian : Penentuan Perbandingan Terbaik antara Kitosan dengan Kentang Kentang yang akan digunakan dikupas, dibersihkan dan dipotong dengan ketebalan yang sama, 2 mm. Selanjutnya irisan kentang tersebut direndam dalam larutan kitosan 2,5% dalam asam asetat 1% selama 60 menit dengan variasi perbandingan kitosan-kentang 1:10, 1:20, 1:30, 1:40, 1:50. Sebagai kontrol digunakan kentang yang direndam dalam air dan dikoreksi dengan kentang yang direndam dalam larutan asam asetat 1%. Antara kentang dengan larutan hasil perendaman dipisahkan; pada larutan hasil perendaman dilakukan analisis total fenolik sedangkan kentang hasil perendaman ditiriskan, dikeringkan menggunakan oven, dan dijadikan tepung. Dilakukan analisis tingkat kecerahan terhadap tepung kentang menggunakan kromameter. Berdasarkan data total fenolik dan tingkat kecerahan diperoleh perbandingan terbaik antara kitosan-kentang. Penentuan Waktu Perendaman Kentang Terbaik Terhadap perbandingan kitosankentang terbaikyang telah diketahui pada tahap sebelumnya direndam dalam larutan kitosan 2,5% selama waktu yang ber variasi, yaitu 30, 60, 90, 120, dan 150 menit. Selanjutnya antara kentang dengan larutan hasil perendaman dipisahkan. Larutan hasil perendaman dianalisis total fenoliknya sedangkan kentang yang telah direndam dikeringkan menggunakan oven, dan dibuat tepung. Tepung kentang dianalisis tingkat kecerahannya menggunakan kromameter dan diperoleh waktu perendaman kentang dalam kitosan yang terbaik. Penentuan Kandungan Total Fenolik Penentuan kandungan total fenolik dimaksudkan untuk mengetahui total fenolik sisa yang terdapat pada larutan hasil perendaman yang menunjukkan keberhasilan anti browning. Penentuan kandungan total fenolik dilakukan dengan metode folin-ciocalteu secara spektrometri visible, pembuatan kurva kalibrasi dilakukan pada konsentrasi larutan asam galat 100, 200, 300, 400, dan 500 mg/l. Larutan hasil perendaman dipipet sebanyak 0,2 ml, ditambah 15,8 ml aquabides, 1 ml reagen Folin-Ciocalteu, dan dikocok hingga homogen. Didiamkan seama 8 menit, ditambahkan 3 ml larutan Na2CO3 dan dikocok hingga homogen. Didiamkan selama 2 jam pada suhu kamar. Diukur serapan larutan pada panjang gelombang maksimum λ = 745 nm [7]. Kontrol yang digunakan merupakan filtrat hasil perendaman kentang menggunakan air yang dikontrol dengan perendaman kentang dalam asam asetat 1%. Absorbansi sampel dapat dihitung berdasarkan : Absorbansi sampel = absorbans kontrol absorbansi larutan air absorbansi larutan asam asetat 1%. Berdasarkan nilai absorbansi tersebut
4 selanjutnya disubstitusikan terhadap persamaan regresi kurva kalibrasi. Preparasi Sampel untuk Analisis Tingkat Kecerahan Tepung Kentang Kentang yang telah dikeringkan dengan oven kemudian dihaluskan. Setelah halus, tepung kentang diayak dengan ukuran 100 mess. Tepung kentang yang diperoleh diukur tingkat kecerahannya menggunakan kromameter. HASIL DAN PEMBAHASAN Penentuan Perbandingan Kitosan- Kentang Terbaik Perbandingan kitosan-kentang terbaik dapat dilketahui melalui analisis kandungan total fenolik pada filtrat hasil perendaman. Analisis total fenolik menggunakan metode Folin-Ciocalteu yang prinsipnya adalah reaksi oksidasi-reduksi. Pereaksi Folin-Ciocalteu yang merupakan pereaksi campuran asam fosfotungstat (H3PW12O40) dan asam fosfomolibdat (H3PMo12O40) akan tereduksi oleh gugus hidroksil dari senyawa fenolik pada kentang yang kemudian menghasilkan campuran oksida biru tungstat (W8O23) dan molibdenum (Mo8O23) [3]. Pada penentuan kandungan total senyawa fenolik pada sampel, dibuat kurva kalibrasi dari asam galat, diperoleh persamaan regresi y = 0,001008x + 0, dengan koefisien korelasi 0,9963. Dalam menentukan perbandingan terbaik antara kitosan dan kentang, digunakan variasi perbandingan 1:10 (A), 1:20 (B), 1:30 (C), 1:40 (D), dan 1:50 (E), masingmasing direndam dalam 100 ml larutan kitosan selama 60 menit dan kontrol kentang yang direndam dalam asam asetat 1%. Filtrat hasil rendaman berupa larutan berwarna kuning kecoklatan, kemudian dianalisis kandungan total fenoliknya. Hasil pengujian kandungan total fenolik ditunjukkan pada Gambar 2. Total Fenolik Sisa (mg/l) , kontrol A B C D E Gambar 2. Pengaruh berbagai perbandingan kitosan-kentang A = 1:10, B = 1:20, C = 1:30, D = 1:40, dan E=1:50 terhadap total fenolik sisa pada larutan rendaman Pada Gambar 2, dapat dilihat bahwa kontrol (tanpa kitosan) menghasilkan intensitas warna coklat yang lebih tinggi dan memiliki kandungan total fenolik sebesar 86,00 mg/l, lebih tinggi bila dibandingkan dengan kentang yang direndam menggunakan larutan kitosan pada perbandingan 1:10, 1:20, 1:30, 1:40, dan 1:50 masing-masing adalah 34,41; 30,14; 43,34; 49,99; dan 48,30mg/L. Semakin besar massa kentang semakin besar pula situs aktif (gugus hidroksil) pada umbi kentang. Pada masa umbi kentang yang semakin tinggi, masih ada situs aktif dari kentang yang belum berikatan dengan molekul kitosan, akibatnya total fenoliknya semakin besar dan intensitas warna coklatnya semakin besar. Pada perbandingan kitosan dengan kentang 1:20 (B) mempunyai nilai total fenolik yang paling rendah, yaitu 30,14mg/L hal ini menunjukkan bahwa kentang telah terlapisi kitosan sehingga kontak senyawa fenolik
5 dengan oksigen berkurang dan browning dapat dihambat. Hasil Analisis Tingkat kecerahan Tepung pada Variasi Perbandingan Kitosan dan Kentang Pengujian tingkat kecerahan tepung kentang hasil rendaman pada kondisi terbaik dilakukan menggunakan kromameter. Hasil pengujian diperoleh data berupa nilai L*, a*, dan b*. Dimana nilai L* menunjukkan warna dari hitam ke putih dengan nilai 0 sampai 100, a* menunjukkan warna merah sampai hijau (+a* : 0 sampai 80 untuk warna merah, -a*: 0 sampai -80 untuk warna hijau), dan b* menunjukkan warna kuning sampai biru (+b*: 0 sampai 70 untuk warna kuning, -b* : 0 sampai -70 untuk warna biru). Tepung kentang yang diperoleh berwarna putih kekuningan dan sepintas tidak memiliki perbedaan warna yang mencolok, sedangkan tepung kentang tanpa kitosan berwarna lebih gelap. Hasil analisis kecerahan tepung kentang hasil perendaman bada berbagai perbandingan kitosan dengan kentang dapat dilihat pada Gambar 3. Intensitas Warna kontrol 0 25A 50B 75C 100 D 125 E L* a* b* Larutan Hasil Perendaman Gambar 3. Pengaruh perbandingan kitosan-kentang terhadapkecerahan Pada Gambar 3. dapat dilihat bahwa perbandingan kitosan dan kentang yang semakin besar mengakibatkan terjadinya penurunan tingkat kecerahan tepung. Hal ini disebabkan oleh konsentrasi kitosan yang diberikan tidak sebanding dengan luas permukaan kentang yang ada sehingga belum mampu melapisi seluruh permukaan kentang dengan sempurna. Pada data tersebut terlihat bahwa tepung kentang yang tidak dilapisi larutan kitosan memiliki tingkat kecerahan yang paling rendah jika dibandingkan dengan yang dilapisi larutan kitosan. Tepung kentang yang tidak dilapisi larutan kitosan memiliki warna yang kurang cerah dengan nilai L* 55,23. Hal ini menunjukkan bahwa larutankitosan mampu menghambat browning pada tepung kentang. Sampel tepung A mempunyai nilai L* sebesar 57,04 serta nilai a* dan b* masing-masing 1,15 dan 5,82. Nilai L* ini relatif lebih kecil serta nilai a* dan b* relatif lebih kecil jika dibandingkan dengan tepung yang memiliki massa lebih besar. Sedangkan tepung D mempunyai nilai L*, a*, dan b* masing-masing 61,71; 1,33; dan 7,37. Nilai ini menunjukkan nilai L* yang relatif lebih besar dan nilai a* dan b* yang relatif lebih kecil dari tepung yang memiliki massa yang lebih besar. Hal ini menunjukkan pada perbandingan 1:20 (D), larutan kitosan mampu menghambat pencoklatan sehingga browning dapat dihambat karena kontak oksigen dengan permukaan kentang dapat diminimalisir [4]. Hasil Analisis Total Fenolik Sisa pada Berbagai Waktu Perendaman Kentang Terbaik Perbandingan kitosan dan kentang 1:20 digunakan pada tahap ini dengan
6 variasi waktu perendaman kentang dalam larutankitosan 2,5% pada 30 menit, 60 menit, 90 menit, 120 menit, 150 menit, dengan kontrol kentang tanpa perendaman dalam larutan kitosan. Hasil analisis total fenolik sisa pada larutan perendam dapat dilihat pada Gambar 4. Total Fenolik Sisa (mg/l) kontro 0l Waktu Perendaman Kentang (menit) Gambar 4. Pengaruh waktu perendaman terhadap total fenolik sisa pada larutan perendam Pada Gambar 4 dapat dilihat bahwa secara umum terjadi penurunan kandungan total fenolik seiring dengan meningkatnya waktu perendaman kentang dalam larutan kitosan. Kentang yang tidak dilapisi kitosan memiliki total fenolik yang lebih tinggi dibandingkan dengan yang dilapisi kitosan yaitu sebesar 53,26 mg/l. Hal ini menunjukkan kitosan mampu menghambat browning. Pada waktu perendaman kentang 30 menit kandungan total fenolik yang dimiliki lebih besar dari sampel lainnya yaitu sebesar 44,32 mg/l. Hal ini menunjukkan bahwa edible coat yang melapisi tepung kentang belum sempurna dan belum mampu menghambat pencoklatan, artinya filtrat masih berwarna coklat sehingga ditentukan waktu perendaman kentang 30 menit bukan waktu perendaman terbaik. Sedangkan, kentang dengan waktu perendaman 150 menit memiliki kandungan total fenolik yang paling kecil yaitu sebesar 28,75 mg/l. Hal ini menunjukkan bahwa larutan kitosan mampu menutupi permukaan makanan dan dapat menghambat terjadinya kontak dengan oksigen sehingga pencoklatan dapat dihambat. Hasil Analisis Tingkat Kecerahan Tepung pada Variasi Waktu Perendaman Kentang Sampel yang digunakan adalah tepung kentang yang diperoleh dari kentang hasil perendaman pada berbagai variasi waktu yang telah dikeringkan dan dihaluskan. Tepung kentang yang dihasilkan berwarna putih dan secara kasat mata perbedaan warna tepung tidak terlihat dengan jelas,sedangkan tepung kentang tanpa perendaman larutan kitosan berwarna lebih gelap. Hasil analisis tingkat kecerahan tepung kentang hasil perendaman pada berbagai waktu dapatilihat pada Gambar 5. Intensitas Warna 58, , , kontrol Waktu Perendaman Kentang (menit) Gambar 5. Nilai kecerahan tepung kentang hasil perendaman pada kitosan dengan berbagai variasi waktu perendaman. Pada Gambar 5, dapat dilihat bahwa dengan meningkatnya waktu perendaman, tingkat kecerahan tepung semakin meningkat. Hal ini disebabkan semakin lama kentang direndam dalam larutan kitosan, maka situsaktifsemakin sempurna dilapisi kitosan sehingga oksidasi L* a* b*
7 senyawa fenolik dapat dihalangi dan browning pada tepung kentang dapat dihambat. Pada tepung kentang yang tidak dilapisi larutankitosan, tepung tersebut memiliki warna yang kurang cerah ditunjukkan dengan nilai L* yang rendah yakni 58,00. Hal ini menunjukkan tepung kentang yang tidak dilapisi larutan kitosan, masih terjadi browning.. Tepung kentang dengan perbandingan kitosan dan kentang 1:20 hasil rendaman selama 30 menit memiliki nilai L* 61,22, nilai a* 1,37, dan nilai b* 6,64. Nilai kecerahan kentang yang direndam selama 30 menit memiliki nilai L* yang lebih rendah serta a*, dan b* yang lebih tinggi dibandingkan dengan sampel tepung lainnya. Sedangkan tepung kentang hasil rendaman selama 150 menit memilki nilai L* 62,28 serta nilai a* dan b* masingmasing 1,15 dan 6,40. Nilai ini menunjukkan kentang yang direndam selama 150 menit memiliki nilai L* lebih tinggi serta a* dan b* lebih rendah dibandingkan dengan sampel lainnya. Edible coat kitosan sudah mampu menghambat pencoklatan dengan meminimalisir kontak oksigen dengan permukaan kentang [5]. Dari hasil tersebut menunjukkan sampel tepung yang memiliki tingkat kecerahan paling tinggi adalah kentang yang direndam selama 150 menit. KESIMPULAN Berdasarkan uji fenolik total dan tingkat kecerahan yang telah dilakukan, dapat disimpulkan bahwa perbandingan antara kitosan dan kentang terbaik adalah 1:20 dan waktu perendaman pada 150 menit. UCAPAN TERIMA KASIH Terimakasih, kami ucapkan kepada Santi Muliyanti atas partisipasinya pada penelitian ini. DAFTAR RUJUKAN [1] Apai, W, V. Sardsud, P. Boonprasom and U. Sardsud.,2009. Effects of Chitosan and Citric Acid on Pericarp Browning and Polyphenol Oxidase Activity of Longan Fruit. Journal Science Technology, 31, (6), [2] Hui, Y.H (editor).,2006. Food Biochemistry and Food Processing. USA: Blackwell Publishing, p 75. [3] International Organisation of Vine and Wine. (2009).Folin-Ciocalteu Index. Compendium of International Methods of Analysis Method OIV-MA-AS2-10. [4] Marshall, M.R, Kim J and Wei C. I., 2000, Enzymatic browning in Fruits, Vegetables and Seafoods, FAO.5] Nongtaodum, S., and Jangchud A.,2009, Effects of Edible Chitosan Coating on Quality of Fresh-Cut Mangoes (Fa-lun) During Storage Kasetsart Journal,43, [6] Orak, H.H., 2006, Total Antioxidant Activities, Phenolics, Anthocyanins, Polyphenoloxidase Activities in Red Grape Varieties. Electronic Journal of Polish Agricultural University Food Science and Technology. 9, 118.
8 [7] Qi H, Hu W, Jiang A, Tian M, Li Y.,2010, Extending Shelf-life of Fresh-cut Fuji Apples with Chitosan-Coatings. Innovative Food Science & Emerging Technologies. [8] Shahidi, F, Arachchi, J.K.V, and Jeon, Y.J.,1999, Food applications of chitin and chitosans, Trends in Food Science, 10, [9] Yogeshkumar, G.N., Gurav A.S., dan Yadav A.V., 2013, Chitosan and Its Applications: A Review of Literature. International Journal of Research in Pharmaceutical and Biomedical Sciences,
9 TANYA JAWAB PENANYA : Nanik Dwi Nurhayati Pertanyaan : a) Kitosan yang dipakai merupakan sintesis dari cangkang udang atau beli? b) Keunggulan apakah yang dimiliki kitosan sehingga dapat menghambat reaksi dengan oksigen? Dan kentang menjadi tidak langsung berwarna cokelat? c) Apakah tepung yang dihasilkan aman untuk dikonsumsi? Jawaban : a) Kitosan yang dipakai tidak dari sintesis tetapi beli. b) Gugus hidroksil pada karbohidrat (kentang) dapat berikatan dengan gugus amina dari kitosan dalam suasana asam (-NH3-) sehingga interaksi senyawa fenolik pada kentang dapat dihambat. Antisipasi agar kentang tidak langsung berwarna cokelat yaitu dengan cara kentang direndam dengan ukuran tertentu yang relatif sama. Kitosan dapat digunakan untuk anti browning. c) Hasil tepung belum sampai pada tahap "aman". Karena belum diuji. PENANYA : Jadigia Ginting Pertanyaan : a) Asam yang digunakan asam asetat atau asam asetat glasial? Jawaban : a) Asam asetat, karena ph tidak harus asam asetat glasial. Dengan menggunakan asam asetat tetap larut.
BAB I PENDAHULUAN 1.1 Latar Belakang
 BAB I PENDAHULUAN 1.1 Latar Belakang Kentang (Solanum tuberosum L.) merupakan salah satu komoditas hortikultura dari kelompok tanaman sayuran umbi yang sangat potensial sebagai sumber karbohidrat dan mempunyai
BAB I PENDAHULUAN 1.1 Latar Belakang Kentang (Solanum tuberosum L.) merupakan salah satu komoditas hortikultura dari kelompok tanaman sayuran umbi yang sangat potensial sebagai sumber karbohidrat dan mempunyai
BAB III METODE PENELITIAN. Penelitian ini dilaksanakan pada bulan Maret sampai dengan Juni 2012.
 26 BAB III METODE PENELITIAN 3.1 Lokasi Penelitian Penelitian ini dilakukan di Laboratorium Kimia Riset Makanan dan Material Jurusan Pendidikan Kimia, Universitas Pendidikan Indonesia (UPI). Penelitian
26 BAB III METODE PENELITIAN 3.1 Lokasi Penelitian Penelitian ini dilakukan di Laboratorium Kimia Riset Makanan dan Material Jurusan Pendidikan Kimia, Universitas Pendidikan Indonesia (UPI). Penelitian
BAB III METODOLOGI PENELITIAN. Penelitian ini dilakukan di Laboratorium Riset, Jurusan Pendidikan Kimia,
 BAB III METODOLOGI PENELITIAN 3.1. Lokasi Penelitian Penelitian ini dilakukan di Laboratorium Riset, Jurusan Pendidikan Kimia, Universitas Pendidikan Indonesia yang bertempat di jalan Dr. Setiabudhi No.
BAB III METODOLOGI PENELITIAN 3.1. Lokasi Penelitian Penelitian ini dilakukan di Laboratorium Riset, Jurusan Pendidikan Kimia, Universitas Pendidikan Indonesia yang bertempat di jalan Dr. Setiabudhi No.
BAB III. Penelitian ini dilakukan di Laboratorium Riset, Jurusan Pendidikan Kimia,
 BAB III METODE PENELITIAN 3.1 Lokasi Penelitian Penelitian ini dilakukan di Laboratorium Riset, Jurusan Pendidikan Kimia, Universitas Pendidikan Indonesia (UPI) yang bertempat di jalan Dr. Setiabudhi No.229
BAB III METODE PENELITIAN 3.1 Lokasi Penelitian Penelitian ini dilakukan di Laboratorium Riset, Jurusan Pendidikan Kimia, Universitas Pendidikan Indonesia (UPI) yang bertempat di jalan Dr. Setiabudhi No.229
BAB III METODOLOGI PENELITIAN. Instrumen Jurusan Pendidikan Kimia FPMIPA Universitas Pendidikan
 21 BAB III METODOLOGI PENELITIAN 3.1 Lokasi Penelitian Penelitian ini dimulai pada bulan Maret sampai Juni 2012 di Laboratorium Riset Kimia dan Material Jurusan Pendidikan Kimia FPMIPA Universitas Pendidikan
21 BAB III METODOLOGI PENELITIAN 3.1 Lokasi Penelitian Penelitian ini dimulai pada bulan Maret sampai Juni 2012 di Laboratorium Riset Kimia dan Material Jurusan Pendidikan Kimia FPMIPA Universitas Pendidikan
BAB III METODE PENELITIAN. di Laboratorium Kimia Riset Makanan dan Laboratorium Kimia Analitik
 30 BAB III METODE PENELITIAN 3.1. Tempat dan Waktu Penelitian Penelitian dilakukan dari bulan November 2011 sampai Mei 2012 di Laboratorium Kimia Riset Makanan dan Laboratorium Kimia Analitik Instrumen
30 BAB III METODE PENELITIAN 3.1. Tempat dan Waktu Penelitian Penelitian dilakukan dari bulan November 2011 sampai Mei 2012 di Laboratorium Kimia Riset Makanan dan Laboratorium Kimia Analitik Instrumen
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian dilaksanakan dari Bulan Maret sampai Bulan Juni 2013. Pengujian aktivitas antioksidan, kadar vitamin C, dan kadar betakaroten buah pepaya
BAB III METODE PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian dilaksanakan dari Bulan Maret sampai Bulan Juni 2013. Pengujian aktivitas antioksidan, kadar vitamin C, dan kadar betakaroten buah pepaya
BAB III METODOLOGI PENELITIAN
 BAB III METODOLOGI PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian ini dilakukan dari bulan April 2013 sampai Agustus 2013 di Laboratoium Kimia Riset Makanan dan Material serta di Laboratorium Instrumen
BAB III METODOLOGI PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian ini dilakukan dari bulan April 2013 sampai Agustus 2013 di Laboratoium Kimia Riset Makanan dan Material serta di Laboratorium Instrumen
BAB III METODE PENELITIAN. Penelitian ini dilakukan dengan menggunakan metodologi penelitian
 BAB III METODE PENELITIAN A. METODOLOGI PENELITIAN Penelitian ini dilakukan dengan menggunakan metodologi penelitian eksperimental yaitu metode penelitian yang digunakan untuk mencari pengaruh perlakuan
BAB III METODE PENELITIAN A. METODOLOGI PENELITIAN Penelitian ini dilakukan dengan menggunakan metodologi penelitian eksperimental yaitu metode penelitian yang digunakan untuk mencari pengaruh perlakuan
BAB III METODOLOGI PENELITIAN. di Laboratorium Kimia Riset Makanan dan Material Jurusan Pendidikan
 BAB III METODOLOGI PENELITIAN 3.1 Lokasi Penelitian Penelitian ini dilakukan dari bulan Februari sampai dengan Juli 2010 di Laboratorium Kimia Riset Makanan dan Material Jurusan Pendidikan Kimia FPMIPA
BAB III METODOLOGI PENELITIAN 3.1 Lokasi Penelitian Penelitian ini dilakukan dari bulan Februari sampai dengan Juli 2010 di Laboratorium Kimia Riset Makanan dan Material Jurusan Pendidikan Kimia FPMIPA
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian ini dilakukan dari bulan Agustus hingga bulan Desember 2013 di Laboratorium Bioteknologi Kelautan Fakultas Perikanan dan Ilmu Kelautan
BAB III METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian ini dilakukan dari bulan Agustus hingga bulan Desember 2013 di Laboratorium Bioteknologi Kelautan Fakultas Perikanan dan Ilmu Kelautan
BAB III METODE PENELITIAN. Penelitian mengenai penggunaan aluminium sebagai sacrificial electrode
 BAB III METODE PENELITIAN 3.1 Deskripsi Penelitian Penelitian mengenai penggunaan aluminium sebagai sacrificial electrode dalam proses elektrokoagulasi larutan yang mengandung pewarna tekstil hitam ini
BAB III METODE PENELITIAN 3.1 Deskripsi Penelitian Penelitian mengenai penggunaan aluminium sebagai sacrificial electrode dalam proses elektrokoagulasi larutan yang mengandung pewarna tekstil hitam ini
BAB III METODE PENELITIAN. Alat-alat yang digunakan dalam penelitian ini, antara lain: waterbath,
 31 BAB III METODE PENELITIAN 3.1 Alat dan Bahan Alat dan bahan yang digunakan dalam penelitian ini adalah sebagai berikut: 3.1.1 Alat Alat-alat yang digunakan dalam penelitian ini, antara lain: waterbath,
31 BAB III METODE PENELITIAN 3.1 Alat dan Bahan Alat dan bahan yang digunakan dalam penelitian ini adalah sebagai berikut: 3.1.1 Alat Alat-alat yang digunakan dalam penelitian ini, antara lain: waterbath,
BAB III METODE PENELITIAN. Metode penelitian yang dilakukan adalah penelitian eksperimental, karena
 BAB III METODE PENELITIAN Metode penelitian yang dilakukan adalah penelitian eksperimental, karena penelitian bertujuan untuk mengetahui pengaruh/hubungan antara variabel bebas dengan variabel terikat.
BAB III METODE PENELITIAN Metode penelitian yang dilakukan adalah penelitian eksperimental, karena penelitian bertujuan untuk mengetahui pengaruh/hubungan antara variabel bebas dengan variabel terikat.
3 METODOLOGI PENELITIAN
 3 METODOLOGI PENELITIAN 3.1 Alat dan bahan 3.1.1 Alat Peralatan yang digunakan dalam penelitian ini menggunakan alat yang berasal dari Laboratorium Tugas Akhir dan Laboratorium Kimia Analitik di Program
3 METODOLOGI PENELITIAN 3.1 Alat dan bahan 3.1.1 Alat Peralatan yang digunakan dalam penelitian ini menggunakan alat yang berasal dari Laboratorium Tugas Akhir dan Laboratorium Kimia Analitik di Program
BAB III METODOLOGI PENELITIAN
 21 BAB III METODOLOGI PENELITIAN 3.1 Lokasi Penelitian Penelitian ini dilaksanakan di Laboratorium Riset Kimia Universitas Pendidikan Indonesia, Jl. Setiabudhi No. 229, Bandung. 3.2 Alat dan Bahan 3.2.1
21 BAB III METODOLOGI PENELITIAN 3.1 Lokasi Penelitian Penelitian ini dilaksanakan di Laboratorium Riset Kimia Universitas Pendidikan Indonesia, Jl. Setiabudhi No. 229, Bandung. 3.2 Alat dan Bahan 3.2.1
BAB III METODE PENELITIAN. Neraca analitik, tabung maserasi, rotary evaporator, water bath,
 BAB III METODE PENELITIAN 3.1 Alat dan Bahan 3.1.1 Alat Neraca analitik, tabung maserasi, rotary evaporator, water bath, termometer, spatula, blender, botol semprot, batang pengaduk, gelas kimia, gelas
BAB III METODE PENELITIAN 3.1 Alat dan Bahan 3.1.1 Alat Neraca analitik, tabung maserasi, rotary evaporator, water bath, termometer, spatula, blender, botol semprot, batang pengaduk, gelas kimia, gelas
BAB III METODE PENELITIAN. Matematika dan Ilmu Pengetahuan Alam Universitas Udayana. Untuk sampel
 BAB III METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian dilakukan di laboratorium penelitian jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Udayana. Untuk sampel kulit
BAB III METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian dilakukan di laboratorium penelitian jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Udayana. Untuk sampel kulit
BAB III METODOLOGI PENELITIAN. FPMIPA Universitas Pendidikan Indonesia dan Laboratorium Kimia Instrumen
 19 BAB III METODOLOGI PENELITIAN 3.1 Lokasi Penelitian Penelitian ini dilakukan dari bulan Maret sampai dengan bulan Juni 2012 di Laboratorium Kimia Riset Makanan dan Material Jurusan Pendidikan Kimia
19 BAB III METODOLOGI PENELITIAN 3.1 Lokasi Penelitian Penelitian ini dilakukan dari bulan Maret sampai dengan bulan Juni 2012 di Laboratorium Kimia Riset Makanan dan Material Jurusan Pendidikan Kimia
BAB III METODE PENELITIAN. 3.2 Waktu Penelitian Penelitian ini dimulai pada bulan februari 2015 dan berakhir pada bulan agustus 2015.
 BAB III METODE PENELITIAN 3.1 Deskripsi Penelitian Penelitian ini dilakukan di laboratorium riset departemen pendidikan kimia FPMIPA, Universitas Pendidikan Indonesia. Secara garis besar penelitian ini
BAB III METODE PENELITIAN 3.1 Deskripsi Penelitian Penelitian ini dilakukan di laboratorium riset departemen pendidikan kimia FPMIPA, Universitas Pendidikan Indonesia. Secara garis besar penelitian ini
BAB IV HASIL DAN PEMBAHASAN. Sampel yang digunakan pada penelitian ini adalah kentang merah dan
 BAB IV HASIL DAN PEMBAHASAN 4.1 Pembuatan Tepung Kentang Sampel yang digunakan pada penelitian ini adalah kentang merah dan kentang. Pembuatan tepung kentang dilakukan dengan tiga cara yaitu tanpa pengukusan,
BAB IV HASIL DAN PEMBAHASAN 4.1 Pembuatan Tepung Kentang Sampel yang digunakan pada penelitian ini adalah kentang merah dan kentang. Pembuatan tepung kentang dilakukan dengan tiga cara yaitu tanpa pengukusan,
BIOKIMIA (Kode : F-08) AKTIVITAS INHIBITOR TIROSINASE SENYAWA BIOAKTIF KULIT BATANG Artocarpus heterophyllus Lamk: PROSPEKTIF SEBAGAI ANTI-BROWNING
 MAKALAH PENDAMPING BIOKIMIA (Kode : F-08) ISBN : 978-979-1533-85-0 AKTIVITAS INHIBITOR TIROSINASE SENYAWA BIOAKTIF KULIT BATANG Artocarpus heterophyllus Lamk: PROSPEKTIF SEBAGAI ANTI-BROWNING Zackiyah
MAKALAH PENDAMPING BIOKIMIA (Kode : F-08) ISBN : 978-979-1533-85-0 AKTIVITAS INHIBITOR TIROSINASE SENYAWA BIOAKTIF KULIT BATANG Artocarpus heterophyllus Lamk: PROSPEKTIF SEBAGAI ANTI-BROWNING Zackiyah
PEMANFAATAN SERAT DAUN NANAS (ANANAS COSMOSUS) SEBAGAI ADSORBEN ZAT WARNA TEKSTIL RHODAMIN B
 SEMINAR NASIONAL KIMIA DAN PENDIDIKAN KIMIA V Kontribusi Kimia dan Pendidikan Kimia dalam Pembangunan Bangsa yang Berkarakter Program Studi Pendidikan Kimia Jurusan PMIPA FKIP UNS Surakarta, 6 April 13
SEMINAR NASIONAL KIMIA DAN PENDIDIKAN KIMIA V Kontribusi Kimia dan Pendidikan Kimia dalam Pembangunan Bangsa yang Berkarakter Program Studi Pendidikan Kimia Jurusan PMIPA FKIP UNS Surakarta, 6 April 13
III BAHAN DAN METODE PENELITIAN. tambahan. Bahan utama berupa daging sapi bagian sampil (chuck) dari sapi
 III BAHAN DAN METODE PENELITIAN 3.1 Bahan dan Peralatan Penelitian 3.1.1 Bahan Penelitian Bahan yang digunakan dalam penelitian terdiri dari bahan utama dan bahan tambahan. Bahan utama berupa daging sapi
III BAHAN DAN METODE PENELITIAN 3.1 Bahan dan Peralatan Penelitian 3.1.1 Bahan Penelitian Bahan yang digunakan dalam penelitian terdiri dari bahan utama dan bahan tambahan. Bahan utama berupa daging sapi
BAB III METODOLOGI PENELITIAN
 BAB III METODOLOGI PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian ini dilakukan di Laboratorium Riset Kimia Makanan dan Material dan Laboratorium Kimia Analitik Instrumen, Jurusan Pendidikan Kimia,
BAB III METODOLOGI PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian ini dilakukan di Laboratorium Riset Kimia Makanan dan Material dan Laboratorium Kimia Analitik Instrumen, Jurusan Pendidikan Kimia,
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1 Alat dan Bahan 3.3.1 Alat Alat yang digunakan dalam penelitian ini adalah pemanas listrik, panci alumunium, saringan, peralatan gelas (labu Erlenmayer, botol vial, gelas ukur,
BAB III METODE PENELITIAN 3.1 Alat dan Bahan 3.3.1 Alat Alat yang digunakan dalam penelitian ini adalah pemanas listrik, panci alumunium, saringan, peralatan gelas (labu Erlenmayer, botol vial, gelas ukur,
BAB III METODELOGI PENELITIAN
 BAB III METODELOGI PENELITIAN 3.1. Waktu dan Lokasi Penelitian Penelitian ini dilakukan dari bulan Maret sampai bulan Juli 2014 yang sebagian besar dilakukan di Laboratorium Riset Jurusan Pendidikan Kimia
BAB III METODELOGI PENELITIAN 3.1. Waktu dan Lokasi Penelitian Penelitian ini dilakukan dari bulan Maret sampai bulan Juli 2014 yang sebagian besar dilakukan di Laboratorium Riset Jurusan Pendidikan Kimia
BAB III METODE PENELITIAN. 3.1 Lokasi Penelitian Penelitian ini dilakukan dari bulan Maret sampai dengan Juni 2010 di
 BAB III METODE PENELITIAN 3.1 Lokasi Penelitian Penelitian ini dilakukan dari bulan Maret sampai dengan Juni 2010 di Laboratorium Kimia Riset Makanan dan Material Jurusan Pendidikan Kimia FPMIPA Universitas
BAB III METODE PENELITIAN 3.1 Lokasi Penelitian Penelitian ini dilakukan dari bulan Maret sampai dengan Juni 2010 di Laboratorium Kimia Riset Makanan dan Material Jurusan Pendidikan Kimia FPMIPA Universitas
BAB III METODOLOGI PENELITIAN
 17 BAB III METODOLOGI PENELITIAN 3.1. Waktu dan Lokasi Penelitian Penelitian ini dilakukan dari bulan Maret sampai dengan bulan April 2013 di Laboratorium Kimia Instrumen dan Laboratorium Kimia Riset Makanan
17 BAB III METODOLOGI PENELITIAN 3.1. Waktu dan Lokasi Penelitian Penelitian ini dilakukan dari bulan Maret sampai dengan bulan April 2013 di Laboratorium Kimia Instrumen dan Laboratorium Kimia Riset Makanan
ADSORBSI ZAT WARNA TEKSTIL RHODAMINE B DENGAN MEMANFAATKAN AMPAS TEH SEBAGAI ADSORBEN
 SEMINAR NASIONAL KIMIA DAN PENDIDIKAN KIMIA V Kontribusi Kimia dan Pendidikan Kimia dalam Pembangunan Bangsa yang Berkarakter Program Studi Pendidikan Kimia Jurusan PMIPA FKIP UNS Surakarta, 6 April 2013
SEMINAR NASIONAL KIMIA DAN PENDIDIKAN KIMIA V Kontribusi Kimia dan Pendidikan Kimia dalam Pembangunan Bangsa yang Berkarakter Program Studi Pendidikan Kimia Jurusan PMIPA FKIP UNS Surakarta, 6 April 2013
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN Dalam melakukan kegiatan penelitian diperlukan peralatan laboratorium, bahan serta prosedur penelitian yang akan dilakukan. Tiga hal tersebut dapat diuraikan sebagai berikut:
BAB III METODE PENELITIAN Dalam melakukan kegiatan penelitian diperlukan peralatan laboratorium, bahan serta prosedur penelitian yang akan dilakukan. Tiga hal tersebut dapat diuraikan sebagai berikut:
BAB III METODOLOGI PENELITIAN
 BAB III METODOLOGI PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian ini dilaksanakan dari bulan April sampai dengan bulan Juli 2013 di Laboratorium Kimia Riset Makanan dan Material, dan Laboratorium
BAB III METODOLOGI PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian ini dilaksanakan dari bulan April sampai dengan bulan Juli 2013 di Laboratorium Kimia Riset Makanan dan Material, dan Laboratorium
BAB III METODOLOGI PENELITIAN
 BAB III METODOLOGI PENELITIAN 3.1. Waktu dan Lokasi Penelitian Penelitian ini dilakukan dari bulan Maret sampai dengan bulan Juni 2014 di Laboratorium Kimia Instrumen dan Laboratorium Kimia Riset Makanan
BAB III METODOLOGI PENELITIAN 3.1. Waktu dan Lokasi Penelitian Penelitian ini dilakukan dari bulan Maret sampai dengan bulan Juni 2014 di Laboratorium Kimia Instrumen dan Laboratorium Kimia Riset Makanan
BAB III METODE PENELITIAN. Penelitian ini dilakukan di Laboratorium Riset Kimia Lingkungan Jurusan
 BAB III METODE PENELITIAN 3.1 Lokasi dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Riset Kimia Lingkungan Jurusan Pendidikan Kimia FPMIPA UPI. Untuk keperluan Analisis digunakan Laboratorium
BAB III METODE PENELITIAN 3.1 Lokasi dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Riset Kimia Lingkungan Jurusan Pendidikan Kimia FPMIPA UPI. Untuk keperluan Analisis digunakan Laboratorium
BAB III METODE PENELITIAN. pendahuluan berupa uji warna untuk mengetahui golongan senyawa metabolit
 BAB III METODE PENELITIAN 3.1 Tahapan Penelitian Penelitian yang dilakukan terdiri dari beberapa tahap, yaitu tahap uji pendahuluan berupa uji warna untuk mengetahui golongan senyawa metabolit sekunder
BAB III METODE PENELITIAN 3.1 Tahapan Penelitian Penelitian yang dilakukan terdiri dari beberapa tahap, yaitu tahap uji pendahuluan berupa uji warna untuk mengetahui golongan senyawa metabolit sekunder
BAB IV HASIL DAN PEMBAHASAN. (Pandanus amaryllifolius Roxb.) 500 gram yang diperoleh dari padukuhan
 BAB IV HASIL DAN PEMBAHASAN A. Hasil Penelitian 1. Preparasi Sampel Bahan utama yang digunakan dalam penelitian ini adalah pandan wangi (Pandanus amaryllifolius Roxb.) 500 gram yang diperoleh dari padukuhan
BAB IV HASIL DAN PEMBAHASAN A. Hasil Penelitian 1. Preparasi Sampel Bahan utama yang digunakan dalam penelitian ini adalah pandan wangi (Pandanus amaryllifolius Roxb.) 500 gram yang diperoleh dari padukuhan
BAB III METODE PENELITIAN. Penelitian ini dilakukan di Laboratorium Riset Kimia dan Laboratorium
 26 BAB III METODE PENELITIAN 3.1 Lokasi Penelitian dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Riset Kimia dan Laboratorium Kimia Lingkungan Jurusan Pendidikan Kimia FPMIPA UPI yang beralamat
26 BAB III METODE PENELITIAN 3.1 Lokasi Penelitian dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Riset Kimia dan Laboratorium Kimia Lingkungan Jurusan Pendidikan Kimia FPMIPA UPI yang beralamat
BAB III METODE PENELITIAN. Subjek dalam penelitian ini adalah nata de ipomoea. Objek penelitian ini adalah daya adsorpsi direct red Teknis.
 BAB III METODE PENELITIAN A. Subjek dan Objek Penelitian 1. Subjek Penelitian Subjek dalam penelitian ini adalah nata de ipomoea. 2. Objek Penelitian Objek penelitian ini adalah daya adsorpsi direct red
BAB III METODE PENELITIAN A. Subjek dan Objek Penelitian 1. Subjek Penelitian Subjek dalam penelitian ini adalah nata de ipomoea. 2. Objek Penelitian Objek penelitian ini adalah daya adsorpsi direct red
BAB III METODE PENELITIAN Waktu Penelitian Penelitian ini dimulai pada bulan Juni 2013 dan berakhir pada bulan Desember 2013.
 BAB III METODE PENELITIAN 3.1. Lokasi Penelitian Penelitian ini dilakukan di laboratorium Riset Material dan Pangan Jurusan Pendidikan Kimia FPMIPA, UPI. Penelitian ini dilakukan menggunakan sel elektrokoagulasi
BAB III METODE PENELITIAN 3.1. Lokasi Penelitian Penelitian ini dilakukan di laboratorium Riset Material dan Pangan Jurusan Pendidikan Kimia FPMIPA, UPI. Penelitian ini dilakukan menggunakan sel elektrokoagulasi
Nova Nurfauziawati Kelompok 11A V. HASIL PENGAMATAN. Tabel 1. Kontak dengan peralatan pengolahan besi. Sampel Warna Tekstur Warna Tekstur
 V. HASIL PENGAMATAN Tabel 1. Kontak dengan peralatan pengolahan besi Pisau stainless steel Pisau berkarat Warna Tekstur Warna Tekstur kean Terong kean kean Salak Coklat Coklat kean kean Tabel 2. Mengurangi
V. HASIL PENGAMATAN Tabel 1. Kontak dengan peralatan pengolahan besi Pisau stainless steel Pisau berkarat Warna Tekstur Warna Tekstur kean Terong kean kean Salak Coklat Coklat kean kean Tabel 2. Mengurangi
Bab III Metodologi III.1 Waktu dan Tempat Penelitian III.2. Alat dan Bahan III.2.1. Alat III.2.2 Bahan
 Bab III Metodologi III.1 Waktu dan Tempat Penelitian Penelitian dilakukan dari bulan Januari hingga April 2008 di Laboratorium Penelitian Kimia Analitik, Institut Teknologi Bandung. Sedangkan pengukuran
Bab III Metodologi III.1 Waktu dan Tempat Penelitian Penelitian dilakukan dari bulan Januari hingga April 2008 di Laboratorium Penelitian Kimia Analitik, Institut Teknologi Bandung. Sedangkan pengukuran
BAB III METODE PENELITIAN. dengan tempat penelitian sebagai berikut :
 28 BAB III METODE PENELITIAN 3.1 Lokasi Penelitian Penelitian ini dilakukan dari bulan Februari sampai dengan Juli 2012 dengan tempat penelitian sebagai berikut : 1. Laboratorium Mutu Giling Balai Besar
28 BAB III METODE PENELITIAN 3.1 Lokasi Penelitian Penelitian ini dilakukan dari bulan Februari sampai dengan Juli 2012 dengan tempat penelitian sebagai berikut : 1. Laboratorium Mutu Giling Balai Besar
Bab III Metodologi Penelitian
 Bab III Metodologi Penelitian Penelitian ini dilakukan dalam tiga tahap yaitu, tahap isolasi kitin yang terdiri dari penghilangan protein, penghilangan mineral, tahap dua pembuatan kitosan dengan deasetilasi
Bab III Metodologi Penelitian Penelitian ini dilakukan dalam tiga tahap yaitu, tahap isolasi kitin yang terdiri dari penghilangan protein, penghilangan mineral, tahap dua pembuatan kitosan dengan deasetilasi
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian ini dilaksanakan dari bulan April 2014 sampai dengan bulan Januari 2015 bertempat di Laboratorium Riset Kimia Makanan dan Material serta
BAB III METODE PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian ini dilaksanakan dari bulan April 2014 sampai dengan bulan Januari 2015 bertempat di Laboratorium Riset Kimia Makanan dan Material serta
METODOLOGI PENELITIAN. Penelitian ini dilaksanakan pada bulan Januari sampai Juni 2014 bertempat di
 29 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan Januari sampai Juni 2014 bertempat di Laboratorium Kimia Fisik, Laboratorium Biomassa Universitas Lampung
29 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan Januari sampai Juni 2014 bertempat di Laboratorium Kimia Fisik, Laboratorium Biomassa Universitas Lampung
BAB III METODE PENELITIAN. Jenis penelitian yang digunakan adalah penelitian eksperimen. Termasuk
 BAB III METODE PENELITIAN 3.1 Jenis Penelitian Jenis penelitian yang digunakan adalah penelitian eksperimen. Termasuk penelitian eksperimen karena dalam penelitian ini terdapat kontrol sebagai acuan antara
BAB III METODE PENELITIAN 3.1 Jenis Penelitian Jenis penelitian yang digunakan adalah penelitian eksperimen. Termasuk penelitian eksperimen karena dalam penelitian ini terdapat kontrol sebagai acuan antara
BAB III MATERI DAN METODE. Kimia dan Gizi Pangan, Departemen Pertanian, Fakultas Peternakan dan
 13 BAB III MATERI DAN METODE Penelitian ini dilaksanakan pada bulan Desember 2016 di Laboratorium Kimia dan Gizi Pangan, Departemen Pertanian, Fakultas Peternakan dan Pertanian, Universitas Diponegoro,
13 BAB III MATERI DAN METODE Penelitian ini dilaksanakan pada bulan Desember 2016 di Laboratorium Kimia dan Gizi Pangan, Departemen Pertanian, Fakultas Peternakan dan Pertanian, Universitas Diponegoro,
BAB III METODOLOGI PENELITIAN. Objek atau bahan penelitian ini adalah cincau hijau. Lokasi penelitian
 BAB III METODOLOGI PENELITIAN 3.1 Objek dan Lokasi Penelitian Objek atau bahan penelitian ini adalah cincau hijau. Lokasi penelitian dilaksanakan di Laboratorium Riset, dan Laboratorium Kimia Instrumen
BAB III METODOLOGI PENELITIAN 3.1 Objek dan Lokasi Penelitian Objek atau bahan penelitian ini adalah cincau hijau. Lokasi penelitian dilaksanakan di Laboratorium Riset, dan Laboratorium Kimia Instrumen
BAB III METODOLOGI PENELITIAN
 BAB III METODOLOGI PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian ini dilakukan dari bulan Maret sampai dengan bulan Juni 2013 di Laboratorium Kimia Riset Makanan dan Material serta di Laboratorium
BAB III METODOLOGI PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian ini dilakukan dari bulan Maret sampai dengan bulan Juni 2013 di Laboratorium Kimia Riset Makanan dan Material serta di Laboratorium
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN A. Jenis dan Rancangan Penelitian Penelitian ini merupakan penelitian eksperimental laboratorium dengan metode rancangan eksperimental sederhana (posttest only control group design)
BAB III METODE PENELITIAN A. Jenis dan Rancangan Penelitian Penelitian ini merupakan penelitian eksperimental laboratorium dengan metode rancangan eksperimental sederhana (posttest only control group design)
III. METODOLOGI PERCOBAAN. Penelitian ini dilakukan pada bulan Januari 2015 sampai Juni 2015 di
 30 III. METODOLOGI PERCOBAAN A. Waktu dan Tempat Penelitian ini dilakukan pada bulan Januari 2015 sampai Juni 2015 di Laboratorium Kimia Analitik dan Instrumentasi Jurusan Kimia Fakultas Matematika dan
30 III. METODOLOGI PERCOBAAN A. Waktu dan Tempat Penelitian ini dilakukan pada bulan Januari 2015 sampai Juni 2015 di Laboratorium Kimia Analitik dan Instrumentasi Jurusan Kimia Fakultas Matematika dan
III METODELOGI PENELITIAN. Penelitian ini telah dilakukan pada bulan Februari sampai Juni 2014 bertempat di
 31 III METODELOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini telah dilakukan pada bulan Februari sampai Juni 2014 bertempat di Laboratorium Kimia Fisik, Laboratorium Biomassa, Universitas
31 III METODELOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini telah dilakukan pada bulan Februari sampai Juni 2014 bertempat di Laboratorium Kimia Fisik, Laboratorium Biomassa, Universitas
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1. Diagram Alir Penelitian Tahapan penelitian secara umum tentang pemanfaatan daun matoa sebagai adsorben untuk menyerap logam Pb dijelaskan dalam diagram pada Gambar 3.1. Preparasi
BAB III METODE PENELITIAN 3.1. Diagram Alir Penelitian Tahapan penelitian secara umum tentang pemanfaatan daun matoa sebagai adsorben untuk menyerap logam Pb dijelaskan dalam diagram pada Gambar 3.1. Preparasi
3 Metodologi Penelitian
 3 Metodologi Penelitian 3.1 Peralatan Peralatan yang digunakan dalam tahapan sintesis ligan meliputi laboratory set dengan labu leher tiga, thermolyne sebagai pemanas, dan neraca analitis untuk penimbangan
3 Metodologi Penelitian 3.1 Peralatan Peralatan yang digunakan dalam tahapan sintesis ligan meliputi laboratory set dengan labu leher tiga, thermolyne sebagai pemanas, dan neraca analitis untuk penimbangan
BAB III METODE PENELITIAN. Subjek penelitian ini adalah ekstrak etanol daun pandan wangi.
 BAB III METODE PENELITIAN A. Subjek dan Objek Penelitian 1. Subjek Penelitian Subjek penelitian ini adalah ekstrak etanol daun pandan wangi. 2. Objek Penelitian Objek penelitian ini adalah aktivitas antioksidan
BAB III METODE PENELITIAN A. Subjek dan Objek Penelitian 1. Subjek Penelitian Subjek penelitian ini adalah ekstrak etanol daun pandan wangi. 2. Objek Penelitian Objek penelitian ini adalah aktivitas antioksidan
BAB III METODE PENELITIAN. Penelitian ini dimulai dari bulan April 2010 sampai dengan bulan Januari
 BAB III METODE PENELITIAN 3.1 Lokasi Penelitian Penelitian ini dimulai dari bulan April 2010 sampai dengan bulan Januari 2011. Penelitian ini sebagian besar dilakukan di Laboratorium Riset Jurusan Pendidikan
BAB III METODE PENELITIAN 3.1 Lokasi Penelitian Penelitian ini dimulai dari bulan April 2010 sampai dengan bulan Januari 2011. Penelitian ini sebagian besar dilakukan di Laboratorium Riset Jurusan Pendidikan
BAB III METODOLOGI PENELITIAN. Penelitian ini dilakukan di Laboratorium Penelitian Jurusan Pendidikan
 BAB III METODOLOGI PENELITIAN 3.1 Lokasi dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Penelitian Jurusan Pendidikan Kimia FPMIPA UPI. Sementara analisis dengan menggunakan instrumen dilakukan
BAB III METODOLOGI PENELITIAN 3.1 Lokasi dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Penelitian Jurusan Pendidikan Kimia FPMIPA UPI. Sementara analisis dengan menggunakan instrumen dilakukan
MAKALAH PENDAMPING : PARALEL A
 MAKALAH PENDAMPING : PARALEL A SEMINAR NASIONAL KIMIA DAN PENDIDIKAN KIMIA IV Peran Riset dan Pembelajaran Kimia dalam Peningkatan Kompetensi Profesional Program Studi Pendidikan Kimia Jurusan PMIPA FKIP
MAKALAH PENDAMPING : PARALEL A SEMINAR NASIONAL KIMIA DAN PENDIDIKAN KIMIA IV Peran Riset dan Pembelajaran Kimia dalam Peningkatan Kompetensi Profesional Program Studi Pendidikan Kimia Jurusan PMIPA FKIP
BAB III MATERI DAN METODE. Laboratorium Nutrisi dan Pakan Ternak Fakultas Peternakan dan Pertanian,
 11 BAB III MATERI DAN METODE Penelitian dilaksanakan di Laboratorium Kimia dan Gizi Pangan, Laboratorium Nutrisi dan Pakan Ternak Fakultas Peternakan dan Pertanian, Laboratorium Terpadu Universitas Diponegoro,
11 BAB III MATERI DAN METODE Penelitian dilaksanakan di Laboratorium Kimia dan Gizi Pangan, Laboratorium Nutrisi dan Pakan Ternak Fakultas Peternakan dan Pertanian, Laboratorium Terpadu Universitas Diponegoro,
4. Hasil dan Pembahasan
 4. Hasil dan Pembahasan 4.1 Isolasi Kitin dan Kitosan Isolasi kitin dan kitosan yang dilakukan pada penelitian ini mengikuti metode isolasi kitin dan kitosan dari kulit udang yaitu meliputi tahap deproteinasi,
4. Hasil dan Pembahasan 4.1 Isolasi Kitin dan Kitosan Isolasi kitin dan kitosan yang dilakukan pada penelitian ini mengikuti metode isolasi kitin dan kitosan dari kulit udang yaitu meliputi tahap deproteinasi,
BAB III. METODE PENELITIAN. Penelitian ini dilaksanakan dari Bulan Januari sampai dengan bulan Juni 2015
 BAB III. METODE PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan dari Bulan Januari sampai dengan bulan Juni 2015 yang meliputi kegiatan di lapangan dan di laboratorium. Lokasi pengambilan
BAB III. METODE PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan dari Bulan Januari sampai dengan bulan Juni 2015 yang meliputi kegiatan di lapangan dan di laboratorium. Lokasi pengambilan
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian dilakukan pada 4 April 2016 sampai 16 Agustus 2016. Penelitian ini dilaksanakan di Laboratorium Riset Kimia Material dan Hayati Departemen
BAB III METODE PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian dilakukan pada 4 April 2016 sampai 16 Agustus 2016. Penelitian ini dilaksanakan di Laboratorium Riset Kimia Material dan Hayati Departemen
BAB III MATERI DAN METODE. Penelitian dilaksanakan pada bulan September Januari 2016 di
 13 BAB III MATERI DAN METODE Penelitian dilaksanakan pada bulan September 2015 - Januari 2016 di Laboratorium Kimia dan Gizi Pangan Fakultas Peternakan dan Pertanian, dan Laboratorium Terpadu Universitas
13 BAB III MATERI DAN METODE Penelitian dilaksanakan pada bulan September 2015 - Januari 2016 di Laboratorium Kimia dan Gizi Pangan Fakultas Peternakan dan Pertanian, dan Laboratorium Terpadu Universitas
PEMBUATAN KITOSAN DARI KULIT UDANG PUTIH (Penaeus merguiensis) DAN APLIKASINYA SEBAGAI PENGAWET ALAMI UNTUK UDANG SEGAR
 JURNAL TEKNOLOGI AGRO-INDUSTRI Vol. 2 No.2 ; November 2015 PEMBUATAN KITOSAN DARI KULIT UDANG PUTIH (Penaeus merguiensis) DAN APLIKASINYA SEBAGAI PENGAWET ALAMI UNTUK UDANG SEGAR Noor Isnawati, Wahyuningsih,
JURNAL TEKNOLOGI AGRO-INDUSTRI Vol. 2 No.2 ; November 2015 PEMBUATAN KITOSAN DARI KULIT UDANG PUTIH (Penaeus merguiensis) DAN APLIKASINYA SEBAGAI PENGAWET ALAMI UNTUK UDANG SEGAR Noor Isnawati, Wahyuningsih,
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1. Lokasi Penelitian Penelitian ini dilaksanakan pada bulan Februari hingga Juli 2013 di Laboratorium Kimia Riset Makanan dan Material Jurusan Pendidikan Kimia FMIPA Universitas
BAB III METODE PENELITIAN 3.1. Lokasi Penelitian Penelitian ini dilaksanakan pada bulan Februari hingga Juli 2013 di Laboratorium Kimia Riset Makanan dan Material Jurusan Pendidikan Kimia FMIPA Universitas
METODOLOGI PENELITIAN
 III. METODOLOGI PENELITIAN A. Bahan dan Alat Bahan utama yang digunakan dalam penelitian ini adalah teh hitam yang diperoleh dari PT Perkebunan Nusantara VIII Gunung Mas Bogor grade BP1 (Broken Pekoe 1).
III. METODOLOGI PENELITIAN A. Bahan dan Alat Bahan utama yang digunakan dalam penelitian ini adalah teh hitam yang diperoleh dari PT Perkebunan Nusantara VIII Gunung Mas Bogor grade BP1 (Broken Pekoe 1).
BAB III METODE PENELITIAN. elektrokoagulasi sistem batch dan sistem flow (alir) dengan aluminium sebagai
 36 BAB III METODE PENELITIAN 3.1 Deskripsi Penelitian Penelitian ini bertujuan untuk mengolah limbah industri penyamakan kulit, yang dilakukan di laboratorium Riset Jurusan Pendidikan Kimia FPMIPA, Universitas
36 BAB III METODE PENELITIAN 3.1 Deskripsi Penelitian Penelitian ini bertujuan untuk mengolah limbah industri penyamakan kulit, yang dilakukan di laboratorium Riset Jurusan Pendidikan Kimia FPMIPA, Universitas
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1 Deskripsi Penelitian Penelitian ini dilakukan dari bulan Maret sampai Agustus 2013 di Laboratorium Riset dan Kimia Instrumen Jurusan Pendidikan Kimia Universitas Pendidikan
BAB III METODE PENELITIAN 3.1 Deskripsi Penelitian Penelitian ini dilakukan dari bulan Maret sampai Agustus 2013 di Laboratorium Riset dan Kimia Instrumen Jurusan Pendidikan Kimia Universitas Pendidikan
BAB III METODE PENELITIAN
 18 BAB III METODE PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian ini dilakukan dari bulan Juli sampai dengan bulan Oktober 2015 di Laboratorium Kimia Riset Makanan dan Laboratorium Kimia Instrumen
18 BAB III METODE PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian ini dilakukan dari bulan Juli sampai dengan bulan Oktober 2015 di Laboratorium Kimia Riset Makanan dan Laboratorium Kimia Instrumen
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian dilaksanakan dari Bulan April sampai Bulan Agustus 2013. Penelitian pengaruh penambahan edible coat kitosan sebagai anti jamur pada
BAB III METODE PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian dilaksanakan dari Bulan April sampai Bulan Agustus 2013. Penelitian pengaruh penambahan edible coat kitosan sebagai anti jamur pada
III. METODOLOGI PENELITIAN. Penelitian dilaksanakan di Laboratorium Pengolahan Hasil Pertanian, Jurusan
 29 III. METODOLOGI PENELITIAN A. Waktu Dan Tempat Penelitian Penelitian dilaksanakan di Laboratorium Pengolahan Hasil Pertanian, Jurusan Teknologi Hasil Pertanian Universitas Lampung, Laboratorium Jasa
29 III. METODOLOGI PENELITIAN A. Waktu Dan Tempat Penelitian Penelitian dilaksanakan di Laboratorium Pengolahan Hasil Pertanian, Jurusan Teknologi Hasil Pertanian Universitas Lampung, Laboratorium Jasa
REAKSI PENCOKLATAN PANGAN
 REAKSI PENCOKLATAN PANGAN Reaksi pencoklatan (browning) merupakan proses pembentukan pigmen berwarna kuning yang akan segera berubah menjadi coklat gelap. Pembentukan warna coklat ini dipicu oleh reaksi
REAKSI PENCOKLATAN PANGAN Reaksi pencoklatan (browning) merupakan proses pembentukan pigmen berwarna kuning yang akan segera berubah menjadi coklat gelap. Pembentukan warna coklat ini dipicu oleh reaksi
BAB III METODOLOGI PENELITIAN. Peralatan yang digunakan dalam penelitian ini antara lain neraca analitik,
 30 BAB III METODOLOGI PENELITIAN 3.1 Alat dan Bahan 3.1.1 Alat Peralatan yang digunakan dalam penelitian ini antara lain neraca analitik, set alat maserasi, rotary evaporator, phmeter, freezer, pipet mikro,
30 BAB III METODOLOGI PENELITIAN 3.1 Alat dan Bahan 3.1.1 Alat Peralatan yang digunakan dalam penelitian ini antara lain neraca analitik, set alat maserasi, rotary evaporator, phmeter, freezer, pipet mikro,
SEMINAR NASIONAL ke 8 Tahun 2013 : Rekayasa Teknologi Industri dan Informasi
 UPAYA PENINGKATAN KELARUTAN KITOSAN DALAM ASAM ASETAT DENGAN MELAKUKAN PERLAKUAN AWAL PADA PENGOLAHAN LIMBAH KULIT UDANG MENJADI KITOSAN Ani Purwanti 1, Muhammad Yusuf 2 1 Jurusan Teknik Kimia, Fakultas
UPAYA PENINGKATAN KELARUTAN KITOSAN DALAM ASAM ASETAT DENGAN MELAKUKAN PERLAKUAN AWAL PADA PENGOLAHAN LIMBAH KULIT UDANG MENJADI KITOSAN Ani Purwanti 1, Muhammad Yusuf 2 1 Jurusan Teknik Kimia, Fakultas
BAB III METODE PENELITIAN. Penelitian ini dilakukan di Laboratorium Riset Kimia Jurusan Pendidikan
 BAB III METODE PENELITIAN 3.1 Deskripsi Penelitian Penelitian ini dilakukan di Laboratorium Riset Kimia Jurusan Pendidikan Kimia FPMIPA UPI yang beralamat di Jl. Dr. Setiabudi No.229 Bandung. Untuk keperluan
BAB III METODE PENELITIAN 3.1 Deskripsi Penelitian Penelitian ini dilakukan di Laboratorium Riset Kimia Jurusan Pendidikan Kimia FPMIPA UPI yang beralamat di Jl. Dr. Setiabudi No.229 Bandung. Untuk keperluan
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Pangan dan Gizi, Laboratorium Rekayasa Proses Pengolahan Pangan dan Hasil Pertanian, Program Studi Ilmu
BAB III METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Pangan dan Gizi, Laboratorium Rekayasa Proses Pengolahan Pangan dan Hasil Pertanian, Program Studi Ilmu
Lampiran 1. Prosedur Analisis Pati Sagu
 LAMPIRAN Lampiran 1. Prosedur Analisis Pati Sagu 1. Bentuk Granula Suspensi pati, untuk pengamatan dibawah mikroskop polarisasi cahaya, disiapkan dengan mencampur butir pati dengan air destilasi, kemudian
LAMPIRAN Lampiran 1. Prosedur Analisis Pati Sagu 1. Bentuk Granula Suspensi pati, untuk pengamatan dibawah mikroskop polarisasi cahaya, disiapkan dengan mencampur butir pati dengan air destilasi, kemudian
BAB III METODE PENELITIAN
 17 BAB III METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian konversi lignoselulosa tandan pisang menjadi 5-hidroksimetil-2- furfural (HMF) untuk optimasi ZnCl 2 dan CrCl 3 serta eksplorasi
17 BAB III METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian konversi lignoselulosa tandan pisang menjadi 5-hidroksimetil-2- furfural (HMF) untuk optimasi ZnCl 2 dan CrCl 3 serta eksplorasi
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN A. Jenis Penelitian Penelitian ini melibatkan pengujian secara kualitatif dan kuantitatif. Pelaksanaannya dilakukan melalui beberapa tahapan yaitu tahap penyiapan sampel, tahap
BAB III METODE PENELITIAN A. Jenis Penelitian Penelitian ini melibatkan pengujian secara kualitatif dan kuantitatif. Pelaksanaannya dilakukan melalui beberapa tahapan yaitu tahap penyiapan sampel, tahap
3. Metodologi Penelitian
 3. Metodologi Penelitian 3.1 Alat dan bahan 3.1.1 Alat Peralatan gelas yang digunakan dalam penelitian ini adalah gelas kimia, gelas ukur, labu Erlenmeyer, cawan petri, corong dan labu Buchner, corong
3. Metodologi Penelitian 3.1 Alat dan bahan 3.1.1 Alat Peralatan gelas yang digunakan dalam penelitian ini adalah gelas kimia, gelas ukur, labu Erlenmeyer, cawan petri, corong dan labu Buchner, corong
BAB 4 PEMBAHASAN Hasil Kerja Ekstraksi Jahe
 4.1. Hasil Kerja Ekstraksi Jahe BAB 4 PEMBAHASAN Bahan jahe merupakan jenis varietas putih besar yang diapat dari pasar bahan organik Bogor. Prinsip kerja ekstraksi ini adalah dengan melarutkan senyawa
4.1. Hasil Kerja Ekstraksi Jahe BAB 4 PEMBAHASAN Bahan jahe merupakan jenis varietas putih besar yang diapat dari pasar bahan organik Bogor. Prinsip kerja ekstraksi ini adalah dengan melarutkan senyawa
BAB III METODOLOGI PENELITIAN
 BAB III METODOLOGI PENELITIAN A. Metode Penelitian Metode penelitian yang dilakukan adalah metode eksperimen secara kualitatif dan kuantitatif. Metode penelitian ini menjelaskan proses degradasi fotokatalis
BAB III METODOLOGI PENELITIAN A. Metode Penelitian Metode penelitian yang dilakukan adalah metode eksperimen secara kualitatif dan kuantitatif. Metode penelitian ini menjelaskan proses degradasi fotokatalis
BAB III METODE PENELITIAN. kandungan fenolik total, kandungan flavonoid total, nilai IC 50 serta nilai SPF
 BAB III METODE PENELITIAN A. Desain Penelitian Jenis penelitian ini adalah observasional laboratorik untuk mengetahui kandungan fenolik total, kandungan flavonoid total, nilai IC 50 serta nilai SPF pada
BAB III METODE PENELITIAN A. Desain Penelitian Jenis penelitian ini adalah observasional laboratorik untuk mengetahui kandungan fenolik total, kandungan flavonoid total, nilai IC 50 serta nilai SPF pada
BAB III METODE PENELITIAN
 25 BAB III METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian dilaksanakan di Laboratorium Rekaya Proses Pengolahan Pangan dan Hasil Pertanian, Laboratorium Pangan dan Gizi Jurusan Ilmu dan Teknologi
25 BAB III METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian dilaksanakan di Laboratorium Rekaya Proses Pengolahan Pangan dan Hasil Pertanian, Laboratorium Pangan dan Gizi Jurusan Ilmu dan Teknologi
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1 Lokasi Penelitian dan Waktu Penelitian Tahapan penelitian yaitu preparasi ekstrak GN, sintesis hidrogel CRF, dan uji kinerja hidrogel CRF dilakukan di Laboratorium Riset Kimia
BAB III METODE PENELITIAN 3.1 Lokasi Penelitian dan Waktu Penelitian Tahapan penelitian yaitu preparasi ekstrak GN, sintesis hidrogel CRF, dan uji kinerja hidrogel CRF dilakukan di Laboratorium Riset Kimia
BAB III METODOLOGI PENELITIAN
 BAB III METODOLOGI PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian ini dilaksanakan dari bulan Maret sampai dengan Juli 2014 di Laboratorium Kimia Riset Makanan dan Laboratorium Kimia Instrumen Jurusan
BAB III METODOLOGI PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian ini dilaksanakan dari bulan Maret sampai dengan Juli 2014 di Laboratorium Kimia Riset Makanan dan Laboratorium Kimia Instrumen Jurusan
3 Metodologi Penelitian
 3 Metodologi Penelitian 3.1 Alat Peralatan yang digunakan dalam tahapan sintesis ligan meliputi laboratory set dengan labu leher tiga, thermolyne sebagai pemanas, dan neraca analitis untuk penimbangan
3 Metodologi Penelitian 3.1 Alat Peralatan yang digunakan dalam tahapan sintesis ligan meliputi laboratory set dengan labu leher tiga, thermolyne sebagai pemanas, dan neraca analitis untuk penimbangan
BAB III METODE PENELITIAN. Penelitian ini dilakukan di Laboratorium Riset Kimia Jurusan Pendidikan
 22 BAB III METODE PENELITIAN 3.1 Deskripsi Penelitian Penelitian ini dilakukan di Laboratorium Riset Kimia Jurusan Pendidikan Kimia FPMIPA UPI yang beralamat di Jl. Dr. Setiabudi No.229 Bandung. Untuk
22 BAB III METODE PENELITIAN 3.1 Deskripsi Penelitian Penelitian ini dilakukan di Laboratorium Riset Kimia Jurusan Pendidikan Kimia FPMIPA UPI yang beralamat di Jl. Dr. Setiabudi No.229 Bandung. Untuk
Gambar 2. Perbedaan Sampel Brokoli (A. Brokoli yang disimpan selama 2 hari pada suhu kamar; B. Brokoli Segar).
 Lampiran 1. Gambar Sampel dan Lokasi Pengambilan Sampel Gambar 1. Sampel Brokoli Gambar 2. Perbedaan Sampel Brokoli (A. Brokoli yang disimpan selama 2 hari pada suhu kamar; B. Brokoli Segar). 45 Lampiran
Lampiran 1. Gambar Sampel dan Lokasi Pengambilan Sampel Gambar 1. Sampel Brokoli Gambar 2. Perbedaan Sampel Brokoli (A. Brokoli yang disimpan selama 2 hari pada suhu kamar; B. Brokoli Segar). 45 Lampiran
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN A. Jenis Penelitian Jenis penelitian yang digunakan eksperimental. B. Tempat dan Waktu Tempat penelitian ini dilakukan di Laboratorium Kimia Fakultas Ilmu Keperawatan dan Kesehatan
BAB III METODE PENELITIAN A. Jenis Penelitian Jenis penelitian yang digunakan eksperimental. B. Tempat dan Waktu Tempat penelitian ini dilakukan di Laboratorium Kimia Fakultas Ilmu Keperawatan dan Kesehatan
BAB III METODOLOGI PENELITIAN. Peralatan yang digunakan dalam penelitian ini adalah set alat destilasi
 BAB III METODOLOGI PENELITIAN 3.1 Alat dan Bahan 3.1.1 Alat Peralatan yang digunakan dalam penelitian ini adalah set alat destilasi sederhana, neraca analitik, labu maserasi, rotary evaporator vacuum Sibata
BAB III METODOLOGI PENELITIAN 3.1 Alat dan Bahan 3.1.1 Alat Peralatan yang digunakan dalam penelitian ini adalah set alat destilasi sederhana, neraca analitik, labu maserasi, rotary evaporator vacuum Sibata
BAB III METODE PENELITIAN. 3.1 Lokasi Pengambilan Sampel, Waktu dan Tempat Penelitian. Lokasi pengambilan sampel bertempat di sepanjang jalan Lembang-
 18 BAB III METODE PENELITIAN 3.1 Lokasi Pengambilan Sampel, Waktu dan Tempat Penelitian Lokasi pengambilan sampel bertempat di sepanjang jalan Lembang- Cihideung. Sampel yang diambil adalah CAF. Penelitian
18 BAB III METODE PENELITIAN 3.1 Lokasi Pengambilan Sampel, Waktu dan Tempat Penelitian Lokasi pengambilan sampel bertempat di sepanjang jalan Lembang- Cihideung. Sampel yang diambil adalah CAF. Penelitian
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilakukan di Universitas Sebelas Maret (UNS), Surakarta dan Universitas Gadjah Mada (UGM), Yogyakarta. Proses pembuatan tepung ubi
BAB III METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilakukan di Universitas Sebelas Maret (UNS), Surakarta dan Universitas Gadjah Mada (UGM), Yogyakarta. Proses pembuatan tepung ubi
BAB III BAHAN, ALAT DAN CARA KERJA
 BAB III BAHAN, ALAT DAN CARA KERJA Penelitian ini dilakukan di Laboratorium Farmasi Fisik, Kimia, dan Formulasi Tablet Departemen Farmasi FMIPA UI, Depok. Waktu pelaksanaannya adalah dari bulan Februari
BAB III BAHAN, ALAT DAN CARA KERJA Penelitian ini dilakukan di Laboratorium Farmasi Fisik, Kimia, dan Formulasi Tablet Departemen Farmasi FMIPA UI, Depok. Waktu pelaksanaannya adalah dari bulan Februari
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1 Alat dan Bahan 3.1.1 Alat Peralatan yang digunakan pada penelitian ini adalah gelas kimia (50,100, 250, dan 500 ml), ph indikator, gelas ukur 100 ml, thermometer, kaca arloji,
BAB III METODE PENELITIAN 3.1 Alat dan Bahan 3.1.1 Alat Peralatan yang digunakan pada penelitian ini adalah gelas kimia (50,100, 250, dan 500 ml), ph indikator, gelas ukur 100 ml, thermometer, kaca arloji,
LAPORAN KIMIA ANALITIK KI 3121 Percobaan modul 2 PENETAPAN ANION FOSFAT DALAM AIR
 LAPORAN KIMIA ANALITIK KI 3121 Percobaan modul 2 PENETAPAN ANION FOSFAT DALAM AIR Nama : Imana Mamizar NIM : 10511066 Kelompok : 5 Nama Asisten : Rizki Tanggal Percobaan : 25 Oktober 2013 Tanggal Pengumpulan
LAPORAN KIMIA ANALITIK KI 3121 Percobaan modul 2 PENETAPAN ANION FOSFAT DALAM AIR Nama : Imana Mamizar NIM : 10511066 Kelompok : 5 Nama Asisten : Rizki Tanggal Percobaan : 25 Oktober 2013 Tanggal Pengumpulan
III. METODELOGI PENELITIAN. Penelitian ini dilakukan pada bulan Mei sampai Agustus 2013 di Laboratorium
 29 III. METODELOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan Mei sampai Agustus 2013 di Laboratorium Kimia Fisik, Laboratorium Biomassa, Laboratorium Biokimia, dan Laboratorium
29 III. METODELOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan Mei sampai Agustus 2013 di Laboratorium Kimia Fisik, Laboratorium Biomassa, Laboratorium Biokimia, dan Laboratorium
Gambar 6. Kerangka penelitian
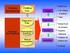 III. BAHAN DAN METODOLOGI A. Bahan dan Alat Bahan baku yang digunakan adalah kayu secang (Caesalpinia sappan L) yang dibeli dari toko obat tradisional pasar Bogor sebagai sumber pigmen brazilein dan sinapic
III. BAHAN DAN METODOLOGI A. Bahan dan Alat Bahan baku yang digunakan adalah kayu secang (Caesalpinia sappan L) yang dibeli dari toko obat tradisional pasar Bogor sebagai sumber pigmen brazilein dan sinapic
Direndam dalam aquades selama sehari semalam Dicuci sampai air cucian cukup bersih
 BAB III METODE PENELITIAN 3.1 Alat dan Bahan Bahan katalis yang digunakan pada penelitian ini adalah zeolit alam yang berasal dari Tasikmalaya Jawa Barat dan phospotungstic acid (HPW, H 3 PW 12 O 40 )
BAB III METODE PENELITIAN 3.1 Alat dan Bahan Bahan katalis yang digunakan pada penelitian ini adalah zeolit alam yang berasal dari Tasikmalaya Jawa Barat dan phospotungstic acid (HPW, H 3 PW 12 O 40 )
LAPORAN PRAKTIKUM ANALISIS SPEKTROMETRI PENETAPAN ANION FOSFAT DALAM AIR. Disusun oleh. Sucilia Indah Putri Kelompok 2
 LAPORAN PRAKTIKUM ANALISIS SPEKTROMETRI PENETAPAN ANION FOSFAT DALAM AIR Disusun oleh Sucilia Indah Putri 10511019 Kelompok 2 Tanggal percobaan : 27 September 2013 Asisten : Lisna Dewi (20513082) Rustianingsih
LAPORAN PRAKTIKUM ANALISIS SPEKTROMETRI PENETAPAN ANION FOSFAT DALAM AIR Disusun oleh Sucilia Indah Putri 10511019 Kelompok 2 Tanggal percobaan : 27 September 2013 Asisten : Lisna Dewi (20513082) Rustianingsih
