ARTIKEL UJI DISOLUSI DAN PENETAPAN KADAR TABLET LORATADIN INOVATOR DAN GENERIK BERMEREK. Mariana Raini,* Daroham Mutiatikum,* Pudji Lastari*
|
|
|
- Yenny Sutedja
- 7 tahun lalu
- Tontonan:
Transkripsi
1 ARTIKEL UJI DISOLUSI DAN PENETAPAN KADAR TABLET LORATADIN INOVATOR DAN GENERIK BERMEREK Mariana Raini,* Daroham Mutiatikum,* Pudji Lastari* DISSOL UTION PROFILE AND DETERMINA TION OF LORA TADINE CONTENT IN INNO VA TOR AND BRANDED GENERIC TABLET: A COMPARATIVE STUDY Abstract Antihistamines Loratadin available in tablet form, as loratadin tablets innovator, branded generic preparations. Socializing generic drugs need information about quality of these drugs, to ensure that the quality of generic drugs not lower or similar to its innovator drugs. The impact of economic crisis caused the price of very expensive drugs. The information quality of generic drugs is expected to increase the use of generic drugs by health practitioners and public. It is necessary for the laboratory data that are qualityparameters, such as dissolution profiles, dissolution testing and determinationof drug dosage levels. Dissolution test method anddetermination of levelsconducted in accordanceto the requirements of the USP (United State of Pharmacopeia). Loratadin dissolution test resultsof tablets A, B and Cin accordancewith the requirements of the USP. Loratadin contentin tablet Ais 103, 73%, B=99,62% and C=100,21%. Loratadin levels in all of these tablets meet the requirements of the USP. Keywords: innovator,branded generic drug, dissolution, content Pendahuluan Antihistamin atau antagonis histamin merupakan salah satu obat yang paling banyak digunakan. 1 Antihistamin ini biasanya digunakan untuk mengobati reaksi alergi. Antihistamin generasi pertama dapat memberikan efek sedasi dan menimbulkan efek antikolinergik yang lebih nyata karena antihistamin ini kurang selektif dan mampu berpenetrasi pada sistem saraf pusat (SSP) lebih besar dibandingkan dengan generasi kedua. Loratadin termasuk antihistamin generasi kedua, secara oral cepat diabsorbsi di saluran pencernaan dan konsentrasi maksimum dalam plasma darah dicapai sekitar satu jam. 1 ' 2 Pemberian tunggal dapat menimbulkan efek hingga 24 jam karena itu loratadin cukup diberikan satu tablet setiap hari. Loratadin juga tidak mempengaruhi kemampuan mengendarai, tingkat kewaspadaan siang hari dan produktivitas kerja. 3 ' 4 Pada dasarnya obat yang beredar di pasaran terbagi menjadi dua yaitu obat innovator atau paten dan obat generik. Obat inovator merupakan obat yang ditemukan berdasarkan penelitian dan memiliki masa paten dalam jangka waktu tertentu. 5 ' 6 Di Amerika Serikat, perlindungan obat paten berlaku selama 20 tahun tetapi dihitung sebelum uji klinik dimulai sehingga masa berlaku paten selama 11 sampai 12 tahun. 5 Sedangkan di Indonesia, berdasarkan Undang-undang No. 14 tahun 2001, masa berlaku paten selama 20 tahun. 6 Selama masa itu perusahaan Farmasi memiliki hak eksklusif untuk memproduksi dan memasarkan obat tersebut kecuali jika memiliki perjanjian khusus dengan perusahaan pemilik paten. 5 ' Perusahaan farmasi yang memproduksi obat inovator hams mengeluarkan biaya yang besar untuk penelitian dan pengembangan obat, keamanan, pemasaran, transportasi sehingga harga obat inovator lebih mahal dari obat generik. Puslitbang Biomedis dan Farmasi 59 Media Litbang Kesehatan Volume XXNomor 2 Tahun 2010
2 Setelah masa berlaku obat paten selesai, maka obat itu boleh ditiru, diproduksi dan dipasarkan oleh perusahaan Farmasi lain. Obat tiruan itu dinamakan obat generik atau obat copy. 7 ' 8 ' 9 Oleh karena itu obat paten yang telah selesai masa patennya (eks paten) juga berubah menjadi obat generik. Mayoritas obat yang beredar di Indonesia saat ini termasuk dalam obat generik. Obat generik dibedakan lagi dengan obat generik berlogo dengan obat generik bermerek. Obat generik berlogo merupakan obat generik yang dijual menggunakan nama generik sebagai nama dagangnya dengan tambahan logo perusahaan produsennya, sedangkan obat generik bermerek menggunakan nama sesuai keinginan produsennya. 10 ' 11 Pada kenyataannya meskipun obat inovator telah habis masa patennya, perusahaan farmasi multinasional tetap menjual obat paten yang telah habis masa patennya (off patent) dengan harga yang sama seperti saat obat tersebut masih berada dalam masa patennya. 6 ' 10 Sedangkan, pada umumnya obat generik bermerek mempunyai harga jual yang lebih rendah dari obat inovator. 6 Pada umumnya, masyarakat menganggap kualitas obat mahal lebih tinggi dari obat yang lebih murah. Pasien seharusnya tidak terjebak pada keharusan membeli obat yang tertulis pada resep padahal tersedia obat yang mempunyai bahan aktif sama dengan kualitas setara dan harga terjangkau. Uji disolusi dan penetapan kadar zat khasiat merupakan faktor penting dalam pengendalian mutu obat. Pengujian ini dipersyaratkan pada produk farmasi yang berbentuk tablet. Uji disolusi ini pada industri farmasi merupakan informasi berharga untuk keseragaman kadar zat khasiat dalam satu produksi obat (batch), perkiraan bioavailabilitas dari zat khasiat obat dalam suaru formulasi, variabel kontrol proses dan untuk melihat pengaruh perubahan formulasi. 12 ' 13 Badan Pemeriksaan Obat dan Makanan (BPOM) mempersyaratkan uji disolusi terbanding (Profil disolusi) berdasarkan perbandingan profil disolusi antara obat inovator dan obat "copy" (generik dan generik bermerek) untuk memastikan kualitas dan sifat-sifat produk obat dengan perubahan minor dalam formulasi atau pembuatan setelah izin pemasaran obat. 14 Sebelum melakukan uji bioekivalensi, BPOM juga menganjurkan untuk melakukan uji disolusi in vitro yang dilaporkan dalam bentuk profil disolusi antara obat uji dan pembanding/inovator. 14 Penelitian ini bertujuan untuk melakukan uji disolusi dan penetapan kadar 2 (dua) produk tablet loratadin generik bermerek dengan loratadin produk inovator. Informasi ini diharapkan dapat memberikan masukan kepada instansi terkait dan masyarakat tentang mutu tablet loratadin baik produk innovator maupun generik bermerek. Metoda uji disolusi dan penetapan kadar dilakukan sesuai dengan The United State of Pharmacopeia 29 (USP) 15 karena monografi loratadin belum tercantum dalam Farmakope Indonesia IV. Metodogi Pengujian yang dilakukan mencakup uji disolusi dan penetapan kadar tablet loratadin inovator A, dan tablet loratadin generik bermerek B dan C. Uji Disolusi Uji disolusi menggunakan alat uji disolusi tipe 2 dengan kecepatan putar dayung 50 rpm dengan media disolusi 900ml HC1 0,1 N. Pada masing-masing basket diletakkan 1 tablet loratadin dari no. Batch yang sama. Penetapan jumlah C 2 2H 2 3C1N 2 O2 yang terlarut, menggunakan spektrofotometri UV, dilakukan dengan mengukur serapan filtrat larutan uji dan serapan larutan baku loratadin dengan media yang sama pada panjang gelombang serapan 280 nm. Penetapan jumlah loratadin yang terlarut dilakukan dengan mengambil alikot dari tiap basket pada menit ke 10, 20, 30, 40, 45, 50 dan 60. Dalam waktu 60 menit tidak boleh larut kurang dari 80% C 2 2H23C1N 2 O2 dari jumlah yang tertera pada etiket. 15 Pengujian dilakukan 3 (tiga) kali. (Disolusi loratadin yang terlarut dari tablet A, B dan C tergambar pada profil disolusi masing-masing tablet tersebut). Penetapan Kadar Penetapan kadar loratadin dilakukan dengan mengambil 20 tablet loratadin, dihomogenkan dan dilarutkan dalam metanol. Penetapan ini dilakukan dengan menggunakan Kromatografi Cair Kinerja tinggi (KCKT) pada panjang gelombang 254 nm, dengan kolom 4 mm x 30cm berisi bahan pengisi LI, fasa gerak (K 2 HPO4 dalam air dan metanol=3:8), laju aliran 2 ml permenit. Pengujian ini menggunakan baku pembanding: loratadin BPFI, dan baku internal: metiltestos-teron, dengan Media Litbang Kesehatan Volume XXNomor 2 Tahun
3 pelarut metanol. Penetapan kadar ini dilakukan 3 (tiga) kali. Persyaratan tablet loratadin mengikuti ketentuan USP, mengandung loratadin tidak kurang dari 90% dan tidak lebih dari 110% dari jumlah yang tertera di etiket. 15 Basil Hasil penetapan kadar dari uji disolusi tablet loratadin produk inovator (A) dan 2 produk generik bermerek (B dan C) yang dilakukan pada menit ke-10, 20, 30, 40, 45, 50 dan 60 dapat dilihat pada tabel 1. Dari hasil penetapan kadar loratadin tablet A, B dan C terlihat kadar loratadin meningkat dengan meningkatnya waktu pengambilan. Pada menit ke-60, loratadin yang terlarut pada tablet A= 109,17%, B= 94,64% dan C= 93,76%, masing-masing tablet larut lebih dari 80% yang sesuai dengan persyaratan USP. Profil uji disolusi dari tablet loratadin produk A, B dan C dapat dilihat pada grafik 1. Tabel 1. Hasil Uji Disolusi Tablet Loratadin A, B dan C No. Waktu Kadar zat aktif loratadin Kadar zat aktif loratadin pengambilan dalam tablet A dalam tablet B alikot (menit) ^> /o) ^/o) 10 46,49 ±4,024 30,08 ±3, ,33 ±10,732 54,20 ± 2, ,94 ±6,710 88,17 ±4, ,20 ±2,829 92,64 ±4, ,97 ±3,370 93,67 ±4, ,54 ±2,296 93,74 ±4, ,17 ±2,475 94,64 ±4,421 Kadar zat aktif loratadin dalam tablet C (%) 90,04 ±6,494 92,65 ±5,442 94,02 ±4,367 94,17 ±3,943 94,53 ±4,099 94,56 ±4,469 93,76 ±6,481 1(adar * / J*" / / y ^ * *- \ \ i A -*-A -*-B C Menit Grafik 1. Profil Uji Disolusi dari Tablet Loratadin Produk A, B dan C 61 Media Litbang Kesehatan Volume XXNomor 2 Tahun 2010
4 Tabel 2. Hasil Penetapan Kadar Tablet Loratadin Tablet A, B dan C No. Nama produk 1. A 2. B 3. C Kadar (%) 104,31 103,33 103,57 100,17 99,7 91,02 99,95 101,43 99,23 Kadar rata-rata (%) 103,74 ±0,511 96,75 ±4, ,20 ±1,122 Grafik uji disolusi menunjukkan bahwa kelarutan loratadin pada 10 menit pertama dari tablet A sekitar 46% meningkat hingga menit ke- 40 dan mulai stabil pada menit ke 45. Pada tablet B, kelarutan pada 10 menit pertama sekitar 30%, mulai stabil pada menit ke-45. Sedangkan tablet C paling mudah larut, kelarutan pada 10 menit pertama sangat tinggi sekitar 90% dan mulai stabil pada menit ke-30. Hasil penetapan kadar tablet loratadin dari tablet A, B dan C dapat dilihat pada tabel 2. Kadar loratadin rata-rata dari masingmasing tablet A, B dan C cukup tinggi, berada dalam interval kadar 90%-110%. Pembahasan Penelitian ini mengikuti persyaratan pengujian yang ditetapkan USP karena loratadin belum tercantum dalam farmakope Indonesia IV. Uji disolusi loratadin menurut USP, dalam waktu 60 menit harus larut > 80%. Absorpsi puncak loratadin terjadi pada 60 menit setelah pelarutan, 5 ini terlihat pada disolusi menit ke 60, loratadin tablet A, Bdan C telah larut lebih dari 90%. Uji disolusi dilakukan juga pada 45 menit untuk melengkapi profil disolusi. Pada grafik profil uji disolusi, kadar zat khasiat loratadin dalam produk inovator A mulai meningkat pada menit ke sepuluh (46,49%) dan mencapai 105,97% pada menit ke 45. Produk loratadin generik bermerek C lebih cepat larut dibandingkan dengan loratadin inovator tablet A, kelarutan pada menit ke sepuluh (90,04%) dan mencapai kadar khasiat 94,53% pada menit ke 45. Sedangkan, tablet loratadin generik bermerk B lebih lambat larut dibandingkan dengan tablet inovator, pada sepuluh menit pertama kadar zat khasiat telah larut 30,08% dan setelah 45 menit mencapai 93,67%. Profil laju disolusi ini menunjukkan bahwa pelepasan zat khasiat obat generik bermerek C pada awal pelarutan (menit ke-10 dan 20), lebih cepat sehingga diharapkan loratadin generik bermerek C bekerja lebih cepat dibandingkan dengan obat inovator A. Sedangkan tablet loratadin generik bermerek B, lebih lambat larut dan bekerja lebih lambat dibandingkan dengan tablet inovator. Meskipun demikian profil ketiga tablet loratadin memenuhi syarat USP karena pada waktu 60 menit telah larut > 80%. Perbedaan laju disolusi ketiga tablet loratadin ini dapat disebabkan beberapa faktor, antara lain: 1) Sifat fisika kimia obat. Adanya perbedaan ukuran partikel dari zat khasiat obat akan mempengaruhi pelarutan. Zat khasiat dalam bentuk kristal lebih sukar larut daripada zat khasiat dalam bentuk amorf karena bentuk kristal lebih keras dan kaku sehingga lebih stabil. Di samping itu kelarutan obat dalam air juga mempengaruhi laju disolusi. Zat khasiat dalarn bentuk garam akan lebih mudah larut dari pada dalam bentuk asamnya. 2) Faktor formulasi. Berbagai macam bahan tambahan yang digunakan pada sediaan obat dapat mempengaruhi tegangan permukaan antara medium tempat obat melarut dengan zat khasiat obat, sehingga mempengaruhi kecepatan pelarutan zat khasiat obat. Penggunaan bahan tambahan yang bersifat hidrofob seperti magnesium stearat, dapat menaikkan tegangan permukaan obat dengan medium disolusi. Beberapa bahan tambahan lain dapat membentuk kompleks dengan bahan obat. Hal ini menyebab- Media Litbang Kesehatan Volume XX Nomor 2 Tahun
5 kan jumlah obat terdisolusi menjadi lebih sedikit, sehingga berpengaruh juga terhadap obat yang diabsorpsi. 3. Faktor alat dan kondisi lingkungan. Adanya perbedaan alat yang digunakan dalam uji disolusi akan mempengaruhi kecepatan pelanitan obat. Kecepatan pengadukan akan mempengaruhi kecepatan pelarutan obat, semakin cepat pengadukan, semakin cepat pergerakan medium sehingga akan meningkatkan kelarutan obat. Selain itu, suhu viskositas dan komposisi medium serta pengambilan sampel juga akan mempengaruhi kecepatan pelarutan obat. 16 ' 1 '' 18 Adanya perbedaan laju disolusi pada awal pelarutan kemungkinan disebabkan, karena perbedaan sifat fisika kimia obat atau faktor formulasi karena penelitian ini dilakukan dengan menggunakan alat dan kondisi yang sama. Bentuk zat khasiat dan formula obat tidak dapat diinformasikan oleh produsen. Pada umumnya kandungan zat aktif obat inovator sama dengan obat generik. Perbedaan antara keduanya bukan pada zat aktifnya, tetapi biasanya pada formula yang mencakup bentuk, warna, rasa atau zat inaktifnya (inactive ingredients).*' 13 Dalam tubuh, absorpsi obat dalam bentuk tablet atau kapsul tergantung dari pelepasan zat khasiat dari tablet, kelarutan obat dalam kondisi fisiologis dan permeabilitas dalam melintasi saluran pencernaan. Sehingga, disolusi obat secara invitro dapat memprediksi kinerja obat secara invivo. 16,17 Hasil penelitian ini, menunjukkan kadar loratadin generik bermerek tablet B dan C mempunyai kualitas relatif sama dengan tablet loratadin inovator A karena tablet B dan C mempunyai profil uji disolusi yang relatif sama. Penetapan kadar senyawa aktif merupakan persyaratan farmakope. Penetapan ini bertujuan unruk menjamin efikasi, keamanan dan mutu obat yang beredar. Penetapan kadar ketiga produk tablet loratadin ini memenuhi persyaratan yang ditetapkan oleh USP. Hal ini menunjukkan mutu ketiga tablet tersebut relatif sama, sehingga diharapkan mempunyai efek terapi yang sama. Kcsimpulan Hasil uji disolusi tablet loratadin produk inovator dan generik bermerek sesuai dengan persyaratan USP, pada waktu 60 menit loratadin telah larut >80%. Loratadin generik bermerek tablet B dan C mempunyai kualitas yang relatif sama dengan tablet loratadin inovator A. Hasil penetapan kadar loratadin dalam tablet inovator A = 103,73%, generik bermerek tablet B = 99,62% dan tablet C = 100,21%. Baik produk inovator A maupun generik bermerek B dan C memenuhi persyaratan USP, berada dalam batas persyaratan kadar 90% - 110%. Daftar Pustaka 1. Optimalisasi Terapi Antihistamin, Majalah Farmacia Edisi Desember 2006, Halaman: 64 (5249 hits) 2. S. Racheva, P. Drumeva, J. Dimitrova, Non- Sedating Antihistamins in the Therapy of Some Dermatoses, 2008, Journal of IMAB - Annual Proceeding (Scientific Papers) book 7,Departemen of Dermato-Venereology, Medical University - Varna, Bulgaria 3. Galenium Pharmasia, Antihistamin yang sesuai untukpasien yang aktif bekerja, diperoleh dari News.aspx?ArtID=274&id=detail&article=d etail 4. File: Loratadin. png, diperoleh dari atadin.png, 10 Agustus Generic Drug, diperoleh dari peroleh, 10 Agustus Bioekivalensi, diperoleh dari /bioekuivalensi/, 16 Juli Massarie logs, Hati-hati Minum Obat, diperoleh dari hrtp:///masarie.wordpress.com/ tag/obat, 10 Agustus Medicastore, Apotek Online, Obat Generik Harga Murah Tapi Mutu Tidak Kalah diperoleh dari obat_generik/, 19Nopember Trisha Torrey, Generic Drugs : Know the Benefits and Differences of Generic Drugs, diperoleh dari drugsandsafety/a/genericdrugs.htm, 10 Agustus Obat generik: Pilihan rasional untuk sehat, mulai dari anak-anak, diperoleh dari 63 Media Litbang Kesehatan Volume XXNomor 2 Tahun 2010
6 is.facebook.com/note.php?note_id= , 15 Juli Antara Komisi dan Nurani, diperoleh dari d=140&id=56&option=com_content&task=v iew, 15 Juli Stippler E, Predictive Dissolution Methods, diperoleh dari eetings/webinars/apq3/dissolution.pdf., 20 Juli Kun Nie et. All, Monitoring Ambroxol Hydrochloride Sustain Release Tablet Release by Fiber-Optic Drug Dissolution In Situ Test System, diperoleh dari 20 Juli Badan Pengawas Obat dan Makanan, Peraturan Kepala Badan Pengawas Obat dan Makanan Indonesia No. HK Tentang Pedoman Uji Bioekivalensi, Jakarta, 29 Maret The USP NF, The Official Compedia of Standards, The United States Pharmacopeia, The National Formulary, 2006, Rockville, hal Hadi L., Disolusi, diperoleh dari 19 Nopember Lee SL, Raw AS, Yu L, Dissolution Testing, Biopharmaceutics Applications in Drug Development, 2007, Food and Drug Administration, Center for Drug Evaluation & Research, 5600 Fishers Lane, Rockville, MD, USA, p Banakar UV, 1992, Pharmaceutical Dissolution Testing with contribution Hanson WA, Drug and Pharmaceuticl Sciences; vol. 49,pl Media Litbang Kesehatan Volume XX Nomor 2 Tahun
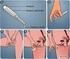
Tahapan-tahapan disintegrasi, disolusi, dan difusi obat.
 I. Pembahasan Disolusi Suatu obat yang di minum secara oral akan melalui tiga fase: fase farmasetik (disolusi), farmakokinetik, dan farmakodinamik, agar kerja obat dapat terjadi. Dalam fase farmasetik,
I. Pembahasan Disolusi Suatu obat yang di minum secara oral akan melalui tiga fase: fase farmasetik (disolusi), farmakokinetik, dan farmakodinamik, agar kerja obat dapat terjadi. Dalam fase farmasetik,
UJI DISOLUSI TERBANDING TABLET METFORMIN HIDROKLORIDA GENERIK BERLOGO DAN BERMEREK
 UJI DISOLUSI TERBANDING TABLET METFORMIN HIDROKLORIDA GENERIK BERLOGO DAN BERMEREK COMPARATIVE DISSOLUTION TEST OF GENERIC DAN BRANDED TABLET METFORMIN HIDROCHLORIDA TABLETS Devia Permata Sari 1, T.N.
UJI DISOLUSI TERBANDING TABLET METFORMIN HIDROKLORIDA GENERIK BERLOGO DAN BERMEREK COMPARATIVE DISSOLUTION TEST OF GENERIC DAN BRANDED TABLET METFORMIN HIDROCHLORIDA TABLETS Devia Permata Sari 1, T.N.
UJI BIOEKIVALENSI IN VITRO PRODUK OBAT BERMEREK DAN GENERIK BERLOGO YANG MEGANDUNG FUROSEMID
 UJI BIOEKIVALENSI IN VITRO PRODUK OBAT BERMEREK DAN GENERIK BERLOGO YANG MEGANDUNG FUROSEMID Ni Luh Dewi Aryani, Christina Avanti, Siti Aisyah, Anis Thohiroh Fakultas Farmasi Universitas Surabaya, Surabaya
UJI BIOEKIVALENSI IN VITRO PRODUK OBAT BERMEREK DAN GENERIK BERLOGO YANG MEGANDUNG FUROSEMID Ni Luh Dewi Aryani, Christina Avanti, Siti Aisyah, Anis Thohiroh Fakultas Farmasi Universitas Surabaya, Surabaya
PERBANDINGAN MUTU TABLET IBUPROFEN GENERIK DAN MEREK DAGANG
 PERBANDINGAN MUTU TABLET IBUPROFEN GENERIK DAN MEREK DAGANG Maria Dona Octavia 1, Fitriani 1, Firmansyah 2 1 Sekolah Tinggi Ilmu Farmasi STIFARM, Padang 2 Fakultas Farmasi, Universitas Andalas (UNAND)
PERBANDINGAN MUTU TABLET IBUPROFEN GENERIK DAN MEREK DAGANG Maria Dona Octavia 1, Fitriani 1, Firmansyah 2 1 Sekolah Tinggi Ilmu Farmasi STIFARM, Padang 2 Fakultas Farmasi, Universitas Andalas (UNAND)
Difusi adalah Proses Perpindahan Zat dari konsentrasi yang tinggi ke konsentrasi yang lebih rendah.
 Difusi adalah Proses Perpindahan Zat dari konsentrasi yang tinggi ke konsentrasi yang lebih rendah. Contoh difusi : a. Difusi gas b. Difusi air Hukum I Ficks : Q = - D dc/dx Ket : D Q dc/dx = Koofisien
Difusi adalah Proses Perpindahan Zat dari konsentrasi yang tinggi ke konsentrasi yang lebih rendah. Contoh difusi : a. Difusi gas b. Difusi air Hukum I Ficks : Q = - D dc/dx Ket : D Q dc/dx = Koofisien
TECHNOLOGY. Yeyet Cahyati Sumirtapura Kelompok Keilmuan Farmasetika Sekolah Farmasi ITB RINGKASAN
 Perkembangan Persyaratan Mutu Biofarmasetik Sediaan Obat Oral Padat Yeyet Cahyati Sumirtapura Kelompok Keilmuan Farmasetika Sekolah Farmasi ITB RINGKASAN Produk obat harus aman, berkhasiat dan memenuhi
Perkembangan Persyaratan Mutu Biofarmasetik Sediaan Obat Oral Padat Yeyet Cahyati Sumirtapura Kelompok Keilmuan Farmasetika Sekolah Farmasi ITB RINGKASAN Produk obat harus aman, berkhasiat dan memenuhi
BIOFARMASI Dhadhang Wahyu Kurniawan Laboratorium Farmasetika
 10/3/2012 BIOFARMASI 1 Dhadhang Wahyu Kurniawan Laboratorium Farmasetika Unsoed @Dhadhang_WK SEJARAH BIOFARMASI Pada akhir tahun 1950-an dan awal tahun 1960- an bermunculan laporan, publikasi dan diskusi
10/3/2012 BIOFARMASI 1 Dhadhang Wahyu Kurniawan Laboratorium Farmasetika Unsoed @Dhadhang_WK SEJARAH BIOFARMASI Pada akhir tahun 1950-an dan awal tahun 1960- an bermunculan laporan, publikasi dan diskusi
BAB II TINJAUAN PUSTAKA. lunak yang dapat larut dalam saluran cerna. Tergantung formulasinya kapsul terbagi
 BAB II TINJAUAN PUSTAKA 2.1 Kapsul Kapsul adalah sediaan padat yang terdiri dari obat dalam cangkang keras atau lunak yang dapat larut dalam saluran cerna. Tergantung formulasinya kapsul terbagi atas kapsul
BAB II TINJAUAN PUSTAKA 2.1 Kapsul Kapsul adalah sediaan padat yang terdiri dari obat dalam cangkang keras atau lunak yang dapat larut dalam saluran cerna. Tergantung formulasinya kapsul terbagi atas kapsul
Uji Disolusi Terbanding Tablet Ofloxacin Berlogo dan Generik Bermerek Terhadap Inovator Dalam Media Dapar HCl ph 4,5
 , Vol. 04, No.01, Februari 2017, hal: 25-33 ISSN-Print. 2355 5386 ISSN-Online. 2460-9560 http://jps.unlam.ac.id/ Research Article 25 Uji Disolusi Terbanding Tablet Ofloxacin Berlogo dan Generik Bermerek
, Vol. 04, No.01, Februari 2017, hal: 25-33 ISSN-Print. 2355 5386 ISSN-Online. 2460-9560 http://jps.unlam.ac.id/ Research Article 25 Uji Disolusi Terbanding Tablet Ofloxacin Berlogo dan Generik Bermerek
BAB I PENDAHULUAN 1.1 Latar Belakang Penelitian
 BAB I PENDAHULUAN 1.1 Latar Belakang Penelitian Hipertensi merupakan penyakit kardiovaskular yang paling sering terjadi dan merupakan penyebab utama stroke, faktor resiko utama arteri koroner, serta kontributor
BAB I PENDAHULUAN 1.1 Latar Belakang Penelitian Hipertensi merupakan penyakit kardiovaskular yang paling sering terjadi dan merupakan penyebab utama stroke, faktor resiko utama arteri koroner, serta kontributor
UJI PRESISI DAN PROFIL DISOLUSI TABLET LOSARTAN INOVATOR DAN COPY PRODUCT DENGAN METODE SPEKTROFOTOMETRI ULTRAVIOLET-VISIBLE
 UJI PRESISI DAN PROFIL DISOLUSI TABLET LOSARTAN INOVATOR DAN COPY PRODUCT DENGAN METODE SPEKTROFOTOMETRI ULTRAVIOLET-VISIBLE Wahyunita Yulia Sari, Ika Yuni Astuti, Didik Setiawan Fakultas Farmasi Universitas
UJI PRESISI DAN PROFIL DISOLUSI TABLET LOSARTAN INOVATOR DAN COPY PRODUCT DENGAN METODE SPEKTROFOTOMETRI ULTRAVIOLET-VISIBLE Wahyunita Yulia Sari, Ika Yuni Astuti, Didik Setiawan Fakultas Farmasi Universitas
METODE PENELITIAN. Penelitian dilakukan di Laboratorium Penelitian Fakultas Farmasi USU
 BAB III METODE PENELITIAN 2.1 Waktu dan Tempat Penelitian Penelitian dilakukan di Laboratorium Penelitian Fakultas Farmasi USU pada bulan Februari 2012 April 2012. 2.2 Alat dan Bahan 2.2.1 Alat-alat Alat-alat
BAB III METODE PENELITIAN 2.1 Waktu dan Tempat Penelitian Penelitian dilakukan di Laboratorium Penelitian Fakultas Farmasi USU pada bulan Februari 2012 April 2012. 2.2 Alat dan Bahan 2.2.1 Alat-alat Alat-alat
Uji Dissolusi Terbanding Sediaan Padat Gemfibrozil Generik dan Merk Dagang yang Beredar di Indonesia
 Jurnal Sains dan Teknologi Farmasi Vol. 19 Suplemen 1 (Desember 2017) Uji Dissolusi Terbanding Sediaan Padat Gemfibrozil Generik dan Merk Dagang yang Beredar di Indonesia Henny Lucida 1*, Dachriyanus 1,
Jurnal Sains dan Teknologi Farmasi Vol. 19 Suplemen 1 (Desember 2017) Uji Dissolusi Terbanding Sediaan Padat Gemfibrozil Generik dan Merk Dagang yang Beredar di Indonesia Henny Lucida 1*, Dachriyanus 1,
REVITALISASI PENGGUNAAN OBAT GENERIK. Nanang Yunarto*
 REVITALISASI PENGGUNAAN OBAT GENERIK Nanang Yunarto* Badan Penelitian dan Pengembangan Kesehatan Kementerian Kesehatan RI Abstrak Pemerintah melalui Kementerian Kesehatan sangat serius ingin merevitalisasi
REVITALISASI PENGGUNAAN OBAT GENERIK Nanang Yunarto* Badan Penelitian dan Pengembangan Kesehatan Kementerian Kesehatan RI Abstrak Pemerintah melalui Kementerian Kesehatan sangat serius ingin merevitalisasi
ii
 PERBANDINGAN PROFIL DISOLUSI TABLET ATORVASTATIN GENERIK DAN MEREK DAGANG TERHADAP INOVATOR DALAM MEDIUM DAPAR FOSFAT PH 6,8 TUGAS AKHIR Diajukan untuk memenuhi salah satu persyaratan memperoleh gelar
PERBANDINGAN PROFIL DISOLUSI TABLET ATORVASTATIN GENERIK DAN MEREK DAGANG TERHADAP INOVATOR DALAM MEDIUM DAPAR FOSFAT PH 6,8 TUGAS AKHIR Diajukan untuk memenuhi salah satu persyaratan memperoleh gelar
UJI DISOLUSI TERBANDING AMLODIPIN DARI BERBAGAI SEDIAAN TABLET YANG BEREDAR DI PASARAN
 UJI DISOLUSI TERBANDING AMLODIPIN DARI BERBAGAI SEDIAAN TABLET YANG BEREDAR DI PASARAN SKRIPSI SARJANA FARMASI OLEH INDAH RELANI No.BP : 0811013153 FAKULTAS FARMASI UNIVERSITAS ANDALAS PADANG 2014 KATA
UJI DISOLUSI TERBANDING AMLODIPIN DARI BERBAGAI SEDIAAN TABLET YANG BEREDAR DI PASARAN SKRIPSI SARJANA FARMASI OLEH INDAH RELANI No.BP : 0811013153 FAKULTAS FARMASI UNIVERSITAS ANDALAS PADANG 2014 KATA
BAB I PENDAHULUAN. kembali pada awal tahun 1920-an. Pada tahun 1995-an, metode kromatografi
 BAB I PENDAHULUAN 1.1 Latar Belakang Analisis senyawa obat baik dalam bahan ruahan (bulk), dalam sediaan farmasi, maupun dalam cairan biologis dengan metode kromatografi dapat dilihat kembali pada awal
BAB I PENDAHULUAN 1.1 Latar Belakang Analisis senyawa obat baik dalam bahan ruahan (bulk), dalam sediaan farmasi, maupun dalam cairan biologis dengan metode kromatografi dapat dilihat kembali pada awal
BAB I PENDAHULUAN. menghambat enzim HMG-CoA reduktase. HMG-CoA merupakan pembentuk
 BAB I PENDAHULUAN 1.1 Latar Belakang Simvastatin merupakan obat antihiperlidemia yang bekerja dengan cara menghambat enzim HMG-CoA reduktase. HMG-CoA merupakan pembentuk kolesterol dengan bantuan katalis
BAB I PENDAHULUAN 1.1 Latar Belakang Simvastatin merupakan obat antihiperlidemia yang bekerja dengan cara menghambat enzim HMG-CoA reduktase. HMG-CoA merupakan pembentuk kolesterol dengan bantuan katalis
PENENTUAN EKIVALENSI ANTAR TABLET SALBUTAMOL NAMA GENERIK DENGAN MEREK DAGANG
 PENENTUAN EKIVALENSI ANTAR TABLET SALBUTAMOL NAMA GENERIK DENGAN MEREK DAGANG Nur Illiyyin Akib, Rifa atul Mahmudah, Wa Ode Sitti Zubaydah Faculty of Pharmacy, Universitas Halu Oleo Kampus Bumi Tridharma
PENENTUAN EKIVALENSI ANTAR TABLET SALBUTAMOL NAMA GENERIK DENGAN MEREK DAGANG Nur Illiyyin Akib, Rifa atul Mahmudah, Wa Ode Sitti Zubaydah Faculty of Pharmacy, Universitas Halu Oleo Kampus Bumi Tridharma
BAB III METODOLOGI. Universitas Sumatera Utara
 BAB III METODOLOGI Metodologi yang dilakukan pada kaplet Omefulvin produksi PT.MUTIFA Medan adalah uji disolusi dengan menggunakan alat uji disolusi tipe dayung dengan kecepatan rotasi 100 rpm dan waktu
BAB III METODOLOGI Metodologi yang dilakukan pada kaplet Omefulvin produksi PT.MUTIFA Medan adalah uji disolusi dengan menggunakan alat uji disolusi tipe dayung dengan kecepatan rotasi 100 rpm dan waktu
BAB II TINJAUAN PUSTAKA
 BAB II TINJAUAN PUSTAKA A. Disolusi Disolusi merupakan suatu proses dimana suatu bahan kimia atau obat menjadi terlarut dalam suatu pelarut (Shargel, 2004). Disolusi secara singkat didefinisikan sebagai
BAB II TINJAUAN PUSTAKA A. Disolusi Disolusi merupakan suatu proses dimana suatu bahan kimia atau obat menjadi terlarut dalam suatu pelarut (Shargel, 2004). Disolusi secara singkat didefinisikan sebagai
UJI STABILITAS FISIK DAN KIMIA SEDIAAN SIRUP RACIKAN
 Prosiding SNaPP2012 : Sains, Teknologi, dan Kesehatan ISSN 2089-3582 UJI STABILITAS FISIK DAN KIMIA SEDIAAN SIRUP RACIKAN YANG MENGANDUNG ERDOSTEIN 1 Fetri Lestari, 2 Hilda Aprilia 1,2 Program Studi Farmasi,
Prosiding SNaPP2012 : Sains, Teknologi, dan Kesehatan ISSN 2089-3582 UJI STABILITAS FISIK DAN KIMIA SEDIAAN SIRUP RACIKAN YANG MENGANDUNG ERDOSTEIN 1 Fetri Lestari, 2 Hilda Aprilia 1,2 Program Studi Farmasi,
PERBANDINGAN MUTU FISIK TABLET METFORMIN HIDROKLORIDA MERK DAGANG DAN GENERIK
 PERBANDINGAN MUTU FISIK TABLET METFORMIN HIDROKLORIDA MERK DAGANG DAN GENERIK Disusun sebagai salah satu syarat menyelesaikan Program Studi Strata I pada Jurusan Farmasi Fakultas Farmasi Oleh : Fitri Wijayanti
PERBANDINGAN MUTU FISIK TABLET METFORMIN HIDROKLORIDA MERK DAGANG DAN GENERIK Disusun sebagai salah satu syarat menyelesaikan Program Studi Strata I pada Jurusan Farmasi Fakultas Farmasi Oleh : Fitri Wijayanti
BAB I PENDAHULUAN A. Latar Belakang Masalah
 BAB I PENDAHULUAN A. Latar Belakang Masalah Secara internasional obat dibagi menjadi 2 yaitu obat paten dan obat generik. Obat paten adalah obat yang baru ditemukan berdasarkan riset dan memiliki masa
BAB I PENDAHULUAN A. Latar Belakang Masalah Secara internasional obat dibagi menjadi 2 yaitu obat paten dan obat generik. Obat paten adalah obat yang baru ditemukan berdasarkan riset dan memiliki masa
PERBANDINGAN MUTU FISIK DAN PROFIL DISOLUSI TABLET GRISEOFULVIN MERK DAGANG DAN GENERIK MAKALAH
 PERBANDINGAN MUTU FISIK DAN PROFIL DISOLUSI TABLET GRISEOFULVIN MERK DAGANG DAN GENERIK MAKALAH Oleh : MONICA YUSLINADIA K 100 040 089 FAKULTAS FARMASI UNIVERSITAS MUHAMMADIYAH SURAKARTA SURAKARTA 2013
PERBANDINGAN MUTU FISIK DAN PROFIL DISOLUSI TABLET GRISEOFULVIN MERK DAGANG DAN GENERIK MAKALAH Oleh : MONICA YUSLINADIA K 100 040 089 FAKULTAS FARMASI UNIVERSITAS MUHAMMADIYAH SURAKARTA SURAKARTA 2013
IV. HASIL DAN PEMBAHASAN. Dari penelitian yang dilakukan diperoleh hasil sebagai berikut:
 IV. HASIL DAN PEMBAHASAN 4.1 Hasil Dari penelitian yang dilakukan diperoleh hasil sebagai berikut: 4.1.1 Pemeriksaan bahan baku Hasil pemeriksan bahan baku ibuprofen, Xanthan Gum,Na CMC, sesuai dengan
IV. HASIL DAN PEMBAHASAN 4.1 Hasil Dari penelitian yang dilakukan diperoleh hasil sebagai berikut: 4.1.1 Pemeriksaan bahan baku Hasil pemeriksan bahan baku ibuprofen, Xanthan Gum,Na CMC, sesuai dengan
BAB IV HASIL DAN PEMBAHASAN
 BAB IV HASIL DAN PEMBAHASAN A. Penentuan Panjang Gelombang Maksimum Penentuan panjang gelombang maksimum ini digunakan untuk mengetahui pada serapan berapa zat yang dibaca oleh spektrofotometer UV secara
BAB IV HASIL DAN PEMBAHASAN A. Penentuan Panjang Gelombang Maksimum Penentuan panjang gelombang maksimum ini digunakan untuk mengetahui pada serapan berapa zat yang dibaca oleh spektrofotometer UV secara
BAB I PENDAHULUAN. juga untuk swamedikasi (pengobatan mandiri). Sedangkan ibuprofen berkhasiat
 BAB I PENDAHULUAN 1.1 Latar Belakang Obat adalah zat aktif berasal dari nabati, hewani, kimiawi alam maupun sintetis dalam dosis atau kadar tertentu dapat dipergunakan untuk preventif (pencegahan), diagnosa
BAB I PENDAHULUAN 1.1 Latar Belakang Obat adalah zat aktif berasal dari nabati, hewani, kimiawi alam maupun sintetis dalam dosis atau kadar tertentu dapat dipergunakan untuk preventif (pencegahan), diagnosa
BAB IV HASIL DAN PEMBAHASAN. Berdasarkan hasil uji formula pendahuluan (Lampiran 9), maka dipilih
 BAB IV HASIL DAN PEMBAHASAN A. HASIL 1. Pembuatan Tablet Mengapung Verapamil HCl Berdasarkan hasil uji formula pendahuluan (Lampiran 9), maka dipilih lima formula untuk dibandingkan kualitasnya, seperti
BAB IV HASIL DAN PEMBAHASAN A. HASIL 1. Pembuatan Tablet Mengapung Verapamil HCl Berdasarkan hasil uji formula pendahuluan (Lampiran 9), maka dipilih lima formula untuk dibandingkan kualitasnya, seperti
BAB 4 HASIL PERCOBAAN DAN PEMBAHASAN. Tabel 4.1 Karakterisasi Fisik Vitamin C
 29 BAB 4 HASIL PERCOBAAN DAN PEMBAHASAN Pada tahap awal penelitian dilakukan pemeriksaan terhadap bahan baku vitamin C meliputi pemerian, kelarutan, identifikasi dan penetapan kadar. Uji kelarutan dilakukan
29 BAB 4 HASIL PERCOBAAN DAN PEMBAHASAN Pada tahap awal penelitian dilakukan pemeriksaan terhadap bahan baku vitamin C meliputi pemerian, kelarutan, identifikasi dan penetapan kadar. Uji kelarutan dilakukan
PROFIL DISOLUSI TERBANDING TABLET RIFAMPISIN MEREK DAN GENERIK. Mutiara Poetri Nurtanti, Anjar Mahardian Kusuma, Agus Siswanto
 PROFIL DISOLUSI TERBANDING TABLET RIFAMPISIN MEREK DAN GENERIK Mutiara Poetri Nurtanti, Anjar Mahardian Kusuma, Agus Siswanto Fakultas Farmasi Universitas Muhammadiyah Purwokerto, Jl. Raya Dukuhwaluh,
PROFIL DISOLUSI TERBANDING TABLET RIFAMPISIN MEREK DAN GENERIK Mutiara Poetri Nurtanti, Anjar Mahardian Kusuma, Agus Siswanto Fakultas Farmasi Universitas Muhammadiyah Purwokerto, Jl. Raya Dukuhwaluh,
BAB I PENDAHULUAN A. Latar Belakang Masalah
 BAB I PENDAHULUAN A. Latar Belakang Masalah Obat adalah suatu bahan baik zat kimia, hewani, maupun nabati dalam dosis yang layak dapat menyembuhkan, meringankan atau mencegah penyakit dan gejalanya, baik
BAB I PENDAHULUAN A. Latar Belakang Masalah Obat adalah suatu bahan baik zat kimia, hewani, maupun nabati dalam dosis yang layak dapat menyembuhkan, meringankan atau mencegah penyakit dan gejalanya, baik
Karakterisasi dan studi disolusi dispersi padat furosemida menggunakan polietilen glikol (PEG), talk dan PEG talk sebagai pembawa dispersi
 Majalah Yandi Syukri Farmasi Indonesia, 15 (1), 37 43, 2004 Karakterisasi dan studi disolusi dispersi padat furosemida menggunakan polietilen glikol (PEG), talk dan PEG talk sebagai pembawa dispersi Characterization
Majalah Yandi Syukri Farmasi Indonesia, 15 (1), 37 43, 2004 Karakterisasi dan studi disolusi dispersi padat furosemida menggunakan polietilen glikol (PEG), talk dan PEG talk sebagai pembawa dispersi Characterization
PERBANDINGAN AVAILABILITAS IN VITRO TABLET METRONIDAZOL PRODUK GENERIK DAN PRODUK DAGANG SKRIPSI
 PERBANDINGAN AVAILABILITAS IN VITRO TABLET METRONIDAZOL PRODUK GENERIK DAN PRODUK DAGANG SKRIPSI Oleh: DIAH MUSTIKA RHOIHANA K 100 030 189 FAKULTAS FARMASI UNIVERSITAS MUHAMMADIYAH SURAKARTA SURAKARTA
PERBANDINGAN AVAILABILITAS IN VITRO TABLET METRONIDAZOL PRODUK GENERIK DAN PRODUK DAGANG SKRIPSI Oleh: DIAH MUSTIKA RHOIHANA K 100 030 189 FAKULTAS FARMASI UNIVERSITAS MUHAMMADIYAH SURAKARTA SURAKARTA
PERBANDINGAN SIFAT FISIK TABLET SALUT CIPROFLOXACIN 500 MG MEREK GENERIK DAN MEREK DAGANG
 Mikhania: Perbandingan Sifat Fisik Tablet 7 PERBANDINGAN SIFAT FISIK TABLET SALUT CIPROFLOXACIN 500 MG MEREK GENERIK DAN MEREK DAGANG Mikhania C.E. *, Dewi rashati, Dadang Putra Mardigantara Akademi Farmasi
Mikhania: Perbandingan Sifat Fisik Tablet 7 PERBANDINGAN SIFAT FISIK TABLET SALUT CIPROFLOXACIN 500 MG MEREK GENERIK DAN MEREK DAGANG Mikhania C.E. *, Dewi rashati, Dadang Putra Mardigantara Akademi Farmasi
BAB 1 PENDAHULUAN. Pada bab ini akan dibahas mengenai latar belakang dan tujuan penelitian.
 BAB 1 PENDAHULUAN Pada bab ini akan dibahas mengenai latar belakang dan tujuan penelitian. 1.1. Latar Belakang Penelitian Asma adalah suatu penyakit obstruksi saluran pernafasan yang bersifat kronis dengan
BAB 1 PENDAHULUAN Pada bab ini akan dibahas mengenai latar belakang dan tujuan penelitian. 1.1. Latar Belakang Penelitian Asma adalah suatu penyakit obstruksi saluran pernafasan yang bersifat kronis dengan
INTISARI PERBANDINGAN KADARNATRIUM DIKLOFENAK DALAM SEDIAAN TABLET DENGAN NAMA GENERIK DAN MERK DAGANGMENGGUNAKAN METODE SPEKTROFOTOMETRI ULTRAVIOLET
 INTISARI PERBANDINGAN KADARNATRIUM DIKLOFENAK DALAM SEDIAAN TABLET DENGAN NAMA GENERIK DAN MERK DAGANGMENGGUNAKAN METODE SPEKTROFOTOMETRI ULTRAVIOLET Novie Widyastuty 1 ; Aditya Maulana Perdana Putra 2
INTISARI PERBANDINGAN KADARNATRIUM DIKLOFENAK DALAM SEDIAAN TABLET DENGAN NAMA GENERIK DAN MERK DAGANGMENGGUNAKAN METODE SPEKTROFOTOMETRI ULTRAVIOLET Novie Widyastuty 1 ; Aditya Maulana Perdana Putra 2
BAB III BAHAN DAN CARA KERJA. Bahan-bahan yang digunakan adalah verapamil HCl (Recordati, Italia),
 BAB III BAHAN DAN CARA KERJA A. BAHAN Bahan-bahan yang digunakan adalah verapamil HCl (Recordati, Italia), pragelatinisasi pati singkong suksinat (Laboratorium Farmasetika, Departemen Farmasi FMIPA UI),
BAB III BAHAN DAN CARA KERJA A. BAHAN Bahan-bahan yang digunakan adalah verapamil HCl (Recordati, Italia), pragelatinisasi pati singkong suksinat (Laboratorium Farmasetika, Departemen Farmasi FMIPA UI),
Prosiding Seminar Nasional Kefarmasian Ke-1
 Prosiding Seminar Nasional Kefarmasian Ke-1 Samarinda, 5 6 Juni 2015 Potensi Produk Farmasi dari Bahan Alam Hayati untuk Pelayanan Kesehatan di Indonesia serta Strategi Penemuannya PENGARUH ph MEDIUM TERHADAP
Prosiding Seminar Nasional Kefarmasian Ke-1 Samarinda, 5 6 Juni 2015 Potensi Produk Farmasi dari Bahan Alam Hayati untuk Pelayanan Kesehatan di Indonesia serta Strategi Penemuannya PENGARUH ph MEDIUM TERHADAP
BAB 1 PENDAHULUAN. Pada bab ini akan dibahas mengenai latar belakang dan tujuan penelitian.
 BAB 1 PENDAHULUAN Pada bab ini akan dibahas mengenai latar belakang dan tujuan penelitian. 1.1. Latar Belakang Penyakit hipertensi adalah penyakit tekanan darah tinggi di mana dalam pengobatannya membutuhkan
BAB 1 PENDAHULUAN Pada bab ini akan dibahas mengenai latar belakang dan tujuan penelitian. 1.1. Latar Belakang Penyakit hipertensi adalah penyakit tekanan darah tinggi di mana dalam pengobatannya membutuhkan
BAB 1 PENDAHULUAN. Pada bab ini akan dibahas mengenai latar belakang dan tujuan penelitian.
 BAB 1 PENDAHULUAN Pada bab ini akan dibahas mengenai latar belakang dan tujuan penelitian. 1.1. Latar Belakang Masalah Dewasa ini di masyarakat kita, banyak ditemukan penyakit kelainan muskuloskeletal
BAB 1 PENDAHULUAN Pada bab ini akan dibahas mengenai latar belakang dan tujuan penelitian. 1.1. Latar Belakang Masalah Dewasa ini di masyarakat kita, banyak ditemukan penyakit kelainan muskuloskeletal
D. Mutiatikum dan Mariana Raini
 PROFIL DISOLUSI DAN PENETAPAN KADAR TABLET MELOKSIKAM INOVATOR DAN GENERIK BERMEREK DENGAN KC'KT ( KROMATOGRAFI CAlR KINERJA TINGGI ) D. Mutiatikum dan Mariana Raini Pusat Penelitian dan Pengembangan Biomedis
PROFIL DISOLUSI DAN PENETAPAN KADAR TABLET MELOKSIKAM INOVATOR DAN GENERIK BERMEREK DENGAN KC'KT ( KROMATOGRAFI CAlR KINERJA TINGGI ) D. Mutiatikum dan Mariana Raini Pusat Penelitian dan Pengembangan Biomedis
DAFTAR ISI. Kata Pengantar. Daftar Gambar. Daftar Lampiran. Intisari... BAB I. PENDAHULUAN..1. A. Latar Belakang.1. B. Perumusan Masalah.
 DAFTAR ISI Kata Pengantar Daftar Isi.. Daftar Gambar Daftar Tabel. Daftar Lampiran. Intisari..... Abstract.. vi viii xi xiii xiv xv xvi BAB I. PENDAHULUAN..1 A. Latar Belakang.1 B. Perumusan Masalah.3
DAFTAR ISI Kata Pengantar Daftar Isi.. Daftar Gambar Daftar Tabel. Daftar Lampiran. Intisari..... Abstract.. vi viii xi xiii xiv xv xvi BAB I. PENDAHULUAN..1 A. Latar Belakang.1 B. Perumusan Masalah.3
Penetapan Simultan Kadar Fenilpropanolamin Hidroklorida dan Klorfeniramin Maleat dalam Tablet secara Spektrofotometri
 JURNAL ILMU KEFARMASIAN INDONESIA, April 2008, hal. 29-34 ISSN 1693-1831 Vol. 6, No. 1 Penetapan Simultan Kadar Fenilpropanolamin Hidroklorida dan Klorfeniramin Maleat dalam Tablet secara Spektrofotometri
JURNAL ILMU KEFARMASIAN INDONESIA, April 2008, hal. 29-34 ISSN 1693-1831 Vol. 6, No. 1 Penetapan Simultan Kadar Fenilpropanolamin Hidroklorida dan Klorfeniramin Maleat dalam Tablet secara Spektrofotometri
relatif kecil sehingga memudahkan dalam proses pengemasan, penyimpanan dan pengangkutan. Beberapa bentuk sediaan padat dirancang untuk melepaskan
 BAB 1 PENDAHULUAN Perkembangan ilmu pengetahuan yang pesat terutama dalam bidang industri farmasi memacu setiap industri farmasi untuk menemukan dan mengembangkan berbagai macam sediaan obat. Dengan didukung
BAB 1 PENDAHULUAN Perkembangan ilmu pengetahuan yang pesat terutama dalam bidang industri farmasi memacu setiap industri farmasi untuk menemukan dan mengembangkan berbagai macam sediaan obat. Dengan didukung
PERBANDINGAN MUTU FISIK DAN PROFIL DISOLUSI TABLET GLIBENKLAMIDA MERK DAGANG DAN GENERIK MAKALAH
 PERBANDINGAN MUTU FISIK DAN PROFIL DISOLUSI TABLET GLIBENKLAMIDA MERK DAGANG DAN GENERIK MAKALAH Oleh : ANITA EDYANINGRUM K 100040039 FAKULTAS FARMASI UNIVERSITAS MUHAMMADIYAH SURAKARTA SURAKARTA 2013
PERBANDINGAN MUTU FISIK DAN PROFIL DISOLUSI TABLET GLIBENKLAMIDA MERK DAGANG DAN GENERIK MAKALAH Oleh : ANITA EDYANINGRUM K 100040039 FAKULTAS FARMASI UNIVERSITAS MUHAMMADIYAH SURAKARTA SURAKARTA 2013
BAB 4 HASIL PERCOBAAN DAN PEMBAHASAN. Tabel 4.1 Hasil Pemeriksaan Bahan Baku Ibuprofen
 BAB 4 HASIL PERCOBAAN DAN PEMBAHASAN Pemeriksaan bahan baku dilakukan untuk menjamin kualitas bahan yang digunakan dalam penelitian ini. Tabel 4.1 dan 4.2 menunjukkan hasil pemeriksaan bahan baku. Pemeriksaan
BAB 4 HASIL PERCOBAAN DAN PEMBAHASAN Pemeriksaan bahan baku dilakukan untuk menjamin kualitas bahan yang digunakan dalam penelitian ini. Tabel 4.1 dan 4.2 menunjukkan hasil pemeriksaan bahan baku. Pemeriksaan
FORMULASI ORALLY DISINTEGRATING TABLET (ODT) METOKLOPRAMIDA HCl MENGGUNAKAN KOMBINASI KROSPOVIDON DAN Ac-Di-Sol DENGAN METODE CETAK LANGSUNG SKRIPSI
 FORMULASI ORALLY DISINTEGRATING TABLET (ODT) METOKLOPRAMIDA HCl MENGGUNAKAN KOMBINASI KROSPOVIDON DAN Ac-Di-Sol DENGAN METODE CETAK LANGSUNG SKRIPSI OLEH: SARIATY FARAH DIBA NIM 071501080 FAKULTAS FARMASI
FORMULASI ORALLY DISINTEGRATING TABLET (ODT) METOKLOPRAMIDA HCl MENGGUNAKAN KOMBINASI KROSPOVIDON DAN Ac-Di-Sol DENGAN METODE CETAK LANGSUNG SKRIPSI OLEH: SARIATY FARAH DIBA NIM 071501080 FAKULTAS FARMASI
BAB III METODE PENELITIAN. Penelitian ini dilakukan pada Laboratorium Penelitian Fakultas Farmasi
 BAB III METODE PENELITIAN 3.1 Tempat dan waktu penelitian Penelitian ini dilakukan pada Laboratorium Penelitian Fakultas Farmasi pada bulan Februari sampai Mei tahun 2012. 3.2 Alat-alat Alat alat yang
BAB III METODE PENELITIAN 3.1 Tempat dan waktu penelitian Penelitian ini dilakukan pada Laboratorium Penelitian Fakultas Farmasi pada bulan Februari sampai Mei tahun 2012. 3.2 Alat-alat Alat alat yang
EVALUASI KUALITAS TABLET GLIBENKLAMIDA GENERIK A DAN MEREK DAGANG B (EVALUATION QUALITY OF GLIBENCLAMIDE TABLETS GENERIC A AND BRANDED B)
 EVALUASI KUALITAS TABLET GLIBENKLAMIDA GENERIK A DAN MEREK DAGANG B (EVALUATION QUALITY OF GLIBENCLAMIDE TABLETS GENERIC A AND BRANDED B) Sartika Dewi, Liza Pratiwi, Siti Nani Nurbaeti Program Studi Farmasi,
EVALUASI KUALITAS TABLET GLIBENKLAMIDA GENERIK A DAN MEREK DAGANG B (EVALUATION QUALITY OF GLIBENCLAMIDE TABLETS GENERIC A AND BRANDED B) Sartika Dewi, Liza Pratiwi, Siti Nani Nurbaeti Program Studi Farmasi,
BAB I PENDAHULUAN. Gates dan George Soros, sehingga terbentuk GF ATM (global fund against
 BAB I PENDAHULUAN 1.1 Latar Belakang Tuberkulosis hingga kini masih jadi masalah kesehatan utama di dunia. Berbagai pihak mencoba bekerja bersama untuk memeranginya. Bahkan penyakit ini akhirnya mampu
BAB I PENDAHULUAN 1.1 Latar Belakang Tuberkulosis hingga kini masih jadi masalah kesehatan utama di dunia. Berbagai pihak mencoba bekerja bersama untuk memeranginya. Bahkan penyakit ini akhirnya mampu
BAB II TINJAUAN PUSTAKA. keadaan patologi dalam rangka penetapan diagnosis, pencegahan,
 BAB II TINJAUAN PUSTAKA 2.1 Pengertian Obat Obat adalah bahan atau paduan bahan, termasuk produk biologi, yang digunakan untuk mempengaruhi atau menyelidiki sistem fisiologi atau keadaan patologi dalam
BAB II TINJAUAN PUSTAKA 2.1 Pengertian Obat Obat adalah bahan atau paduan bahan, termasuk produk biologi, yang digunakan untuk mempengaruhi atau menyelidiki sistem fisiologi atau keadaan patologi dalam
BAB III METODE PENELITIAN. ketoprofen (Kalbe Farma), gelatin (Brataco chemical), laktosa (Brataco
 17 BAB III METODE PENELITIAN A. Alat dan Bahan 1. Bahan yang digunakan Bahan-bahan yang digunakan dalam penelitian ini adalah ketoprofen (Kalbe Farma), gelatin (Brataco chemical), laktosa (Brataco chemical),
17 BAB III METODE PENELITIAN A. Alat dan Bahan 1. Bahan yang digunakan Bahan-bahan yang digunakan dalam penelitian ini adalah ketoprofen (Kalbe Farma), gelatin (Brataco chemical), laktosa (Brataco chemical),
VALIDASI METODE ANALISIS UNTUK PENETAPAN KADAR TABLET ASAM MEFENAMAT SECARA SPEKTROFOTOMETRI ULTRAVIOLET
 VALIDASI METODE ANALISIS UNTUK PENETAPAN KADAR TABLET ASAM MEFENAMAT SECARA SPEKTROFOTOMETRI ULTRAVIOLET Noviny Ramayany Uno 1), Sri Sudewi 1), Widya Astuty Lolo 1) 1) Program Studi Farmasi FMIPA UNSRAT
VALIDASI METODE ANALISIS UNTUK PENETAPAN KADAR TABLET ASAM MEFENAMAT SECARA SPEKTROFOTOMETRI ULTRAVIOLET Noviny Ramayany Uno 1), Sri Sudewi 1), Widya Astuty Lolo 1) 1) Program Studi Farmasi FMIPA UNSRAT
Sedangkan kerugiannya adalah tablet tidak bisa digunakan untuk pasien dengan kesulitan menelan. Absorpsi suatu obat ditentukan melalui disolusi
 BAB 1 PENDAHULUAN Sampai saat ini, sediaan farmasi yang paling banyak digunakan adalah sediaan tablet, yang merupakan sediaan padat kompak, dibuat secara kempa cetak, dalam bentuk tabung pipih atau sirkular,
BAB 1 PENDAHULUAN Sampai saat ini, sediaan farmasi yang paling banyak digunakan adalah sediaan tablet, yang merupakan sediaan padat kompak, dibuat secara kempa cetak, dalam bentuk tabung pipih atau sirkular,
FORMULASI TABLET PARACETAMOL SECARA KEMPA LANGSUNG DENGAN MENGGUNAKAN VARIASI KONSENTRASI AMILUM UBI JALAR (Ipomea batatas Lamk.) SEBAGAI PENGHANCUR
 As-Syifaa Vol 08 (02) : Hal. 64-74, Desember 2016 ISSN : 2085-4714 FORMULASI TABLET PARACETAMOL SECARA KEMPA LANGSUNG DENGAN MENGGUNAKAN VARIASI KONSENTRASI AMILUM UBI JALAR (Ipomea batatas Lamk.) SEBAGAI
As-Syifaa Vol 08 (02) : Hal. 64-74, Desember 2016 ISSN : 2085-4714 FORMULASI TABLET PARACETAMOL SECARA KEMPA LANGSUNG DENGAN MENGGUNAKAN VARIASI KONSENTRASI AMILUM UBI JALAR (Ipomea batatas Lamk.) SEBAGAI
1. Penetapan panjang gelombang serapan maksimum Pembuatan kurva baku... 35
 DAFTAR ISI KATA PENGANTAR... vii DAFTAR ISI... ix DAFTAR TABEL... xii DAFTAR GAMBAR... xiii DAFTAR LAMPIRAN... xiv INTISARI... xv ABSTRACT... xvi BAB I PENDAHULUAN A. Latar Belakang... 1 B. Perumusan Masalah...
DAFTAR ISI KATA PENGANTAR... vii DAFTAR ISI... ix DAFTAR TABEL... xii DAFTAR GAMBAR... xiii DAFTAR LAMPIRAN... xiv INTISARI... xv ABSTRACT... xvi BAB I PENDAHULUAN A. Latar Belakang... 1 B. Perumusan Masalah...
BAB 3 PERCOBAAN. 3.3 Pemeriksaan Bahan Baku Pemeriksaan bahan baku ibuprofen, HPMC, dilakukan menurut Farmakope Indonesia IV dan USP XXIV.
 BAB 3 PERCOBAAN 3.1 Bahan Percobaan Ibuprofen, HPMC 6 cps (Shin-Etsu), PVP K-30, laktosa, acdisol, amprotab, talk, magnesium stearat, kalium dihidrogen fosfat, natrium hidroksida, natrium dihidrogen fosfat,
BAB 3 PERCOBAAN 3.1 Bahan Percobaan Ibuprofen, HPMC 6 cps (Shin-Etsu), PVP K-30, laktosa, acdisol, amprotab, talk, magnesium stearat, kalium dihidrogen fosfat, natrium hidroksida, natrium dihidrogen fosfat,
BAB I PENDAHULUAN. A. Latar Belakang Masalah. Furosemid merupakan obat golongan loop diuretik yang banyak digunakan
 BAB I PENDAHULUAN A. Latar Belakang Masalah Furosemid merupakan obat golongan loop diuretik yang banyak digunakan untuk berbagai macam indikasi, diantaranya: antihipertensi, asites, sindrom kekurangan
BAB I PENDAHULUAN A. Latar Belakang Masalah Furosemid merupakan obat golongan loop diuretik yang banyak digunakan untuk berbagai macam indikasi, diantaranya: antihipertensi, asites, sindrom kekurangan
Perbandingan Bioavailabilitas Pirazinamid Dalam Sediaan Generik Dan Paten Secara In Vitro
 Perbandingan Bioavailabilitas Pirazinamid Dalam Sediaan Generik Dan Paten Secara In Vitro ARTIKEL KARYA TULIS ILIAH Diajukan guna memenuhi tugas dan melengkapi syarat dalam menempuh Program Pendidikan
Perbandingan Bioavailabilitas Pirazinamid Dalam Sediaan Generik Dan Paten Secara In Vitro ARTIKEL KARYA TULIS ILIAH Diajukan guna memenuhi tugas dan melengkapi syarat dalam menempuh Program Pendidikan
BAB I PENDAHULUAN. Obat-obat anti inflamasi non-steroid (AINS) banyak digunakan untuk terapi
 BAB I PENDAHULUAN 1.1. Latar Belakang Penelitian Obat-obat anti inflamasi non-steroid (AINS) banyak digunakan untuk terapi kelainan musculoskeletal, seperti artritis rheumatoid, yang umumnya hanya meringankan
BAB I PENDAHULUAN 1.1. Latar Belakang Penelitian Obat-obat anti inflamasi non-steroid (AINS) banyak digunakan untuk terapi kelainan musculoskeletal, seperti artritis rheumatoid, yang umumnya hanya meringankan
BAB 1 PENDAHULUAN 1.1 Latar Belakang
 BAB 1 PENDAHULUAN 1.1 Latar Belakang Diabetes melitus merupakan penyakit kronis pada homeostasis glukosa yang ditandai dengan beberapa hal yaitu, meningkatnya kadar gula darah, kelainan kerja insulin,
BAB 1 PENDAHULUAN 1.1 Latar Belakang Diabetes melitus merupakan penyakit kronis pada homeostasis glukosa yang ditandai dengan beberapa hal yaitu, meningkatnya kadar gula darah, kelainan kerja insulin,
PERBANDINGAN DISOLUSI ASAM MEFENAMAT DALAM SISTEM DISPERSI PADAT DENGAN PEG 6000 DAN PVP
 PERBANDINGAN DISOLUSI ASAM MEFENAMAT DALAM SISTEM DISPERSI PADAT DENGAN PEG 6000 DAN PVP Yulias Ninik Windriyati (1), Sugiyono (1), Widhi Astuti (1), Maria Faizatul Habibah (1) 1) Fakultas Farmasi Universitas
PERBANDINGAN DISOLUSI ASAM MEFENAMAT DALAM SISTEM DISPERSI PADAT DENGAN PEG 6000 DAN PVP Yulias Ninik Windriyati (1), Sugiyono (1), Widhi Astuti (1), Maria Faizatul Habibah (1) 1) Fakultas Farmasi Universitas
Teknik likuisolid merupakan suatu teknik formulasi dengan obat yang tidak terlarut air dilarutkan dalam pelarut non volatile dan menjadi obat dalam
 BAB 1 PENDAHULUAN Klorfeniramin maleat merupakan obat antihistamin H 1 Reseptor yang dapat menghambat efek histamin pada pembuluh darah, bronkus, dan bermacam-macam otot polos, serta bekerja dengan mengobati
BAB 1 PENDAHULUAN Klorfeniramin maleat merupakan obat antihistamin H 1 Reseptor yang dapat menghambat efek histamin pada pembuluh darah, bronkus, dan bermacam-macam otot polos, serta bekerja dengan mengobati
Lampiran 1. Perhitungan Pembuatan Tablet Asam Folat. Sebagai contoh F1 (Formula dengan penambahan Pharmacoat 615 1%).
 Lampiran 1. Perhitungan Pembuatan Tablet Asam Folat Sebagai contoh F1 (Formula dengan penambahan Pharmacoat 615 1%). Dibuat formula untuk 100 tablet, berat pertablet 00 mg dan penampang tablet 9 mm. Berat
Lampiran 1. Perhitungan Pembuatan Tablet Asam Folat Sebagai contoh F1 (Formula dengan penambahan Pharmacoat 615 1%). Dibuat formula untuk 100 tablet, berat pertablet 00 mg dan penampang tablet 9 mm. Berat
BAB III BAHAN DAN CARA KERJA. Timbangan analitik EB-330 (Shimadzu, Jepang), spektrofotometer UV
 BAB III BAHAN DAN CARA KERJA A. ALAT Timbangan analitik EB-330 (Shimadzu, Jepang), spektrofotometer UV Vis V-530 (Jasco, Jepang), fourrier transformation infra red 8400S (Shimadzu, Jepang), moisture analyzer
BAB III BAHAN DAN CARA KERJA A. ALAT Timbangan analitik EB-330 (Shimadzu, Jepang), spektrofotometer UV Vis V-530 (Jasco, Jepang), fourrier transformation infra red 8400S (Shimadzu, Jepang), moisture analyzer
I. PENDAHULUAN. sumber pemenuhan kebutuhan tubuh untuk melakukan metabolisme hingga
 I. PENDAHULUAN Saluran pencernaan merupakan gerbang utama masuknya zat gizi sebagai sumber pemenuhan kebutuhan tubuh untuk melakukan metabolisme hingga aktivitas sehari-hari. Lambung merupakan tempat yang
I. PENDAHULUAN Saluran pencernaan merupakan gerbang utama masuknya zat gizi sebagai sumber pemenuhan kebutuhan tubuh untuk melakukan metabolisme hingga aktivitas sehari-hari. Lambung merupakan tempat yang
PHARMACY, Vol.07 No. 01 April 2010 ISSN PROFIL DISOLUSI IN VITRO TABLET LEVOFLOKSASIN GENERIK DAN LEVOFLOKSASIN NON GENERIK
 PROFIL DISOLUSI IN VITRO TABLET LEVOFLOKSASIN GENERIK DAN LEVOFLOKSASIN NON GENERIK Frisky Almuksiti*, Ika Yuni Astuti*, Didik Setiawan* Fakultas Farmasi Universitas Muhammadiyah Purwokerto, Jl. Raya Dukuhwaluh,
PROFIL DISOLUSI IN VITRO TABLET LEVOFLOKSASIN GENERIK DAN LEVOFLOKSASIN NON GENERIK Frisky Almuksiti*, Ika Yuni Astuti*, Didik Setiawan* Fakultas Farmasi Universitas Muhammadiyah Purwokerto, Jl. Raya Dukuhwaluh,
BAB 1 PENDAHULUAN 1.1. Latar Belakang Penelitian
 BAB 1 PENDAHULUAN 1.1. Latar Belakang Penelitian Penderita hipertensi yang selalu meningkat jumlahnya dari tahun ke tahun menyebabkan kebutuhan akan obat anti hipertensi meningkat. Industri farmasi sendiri
BAB 1 PENDAHULUAN 1.1. Latar Belakang Penelitian Penderita hipertensi yang selalu meningkat jumlahnya dari tahun ke tahun menyebabkan kebutuhan akan obat anti hipertensi meningkat. Industri farmasi sendiri
bentuk sediaan lainnya; pemakaian yang mudah (Siregar, 1992). Akan tetapi, tablet memiliki kekurangan untuk pasien yang mengalami kesulitan dalam
 BAB 1 PENDAHULUAN Hingga saat ini, kemajuan di bidang teknologi dalam industri farmasi telah mengalami perkembangan yang sangat pesat terutama dalam meningkatkan mutu suatu obat. Tablet adalah sediaan
BAB 1 PENDAHULUAN Hingga saat ini, kemajuan di bidang teknologi dalam industri farmasi telah mengalami perkembangan yang sangat pesat terutama dalam meningkatkan mutu suatu obat. Tablet adalah sediaan
POTENSI EKSTRAK KERING SIRIH MANADO:MIYANA SEBAGAI BAHAN BAKU TABLET HERBAL
 POTENSI EKSTRAK KERING SIRIH MANADO:MIYANA SEBAGAI BAHAN BAKU TABLET HERBAL Awal P, Yun Astuti Nugroho Balai Besar Litbang Tanaman Obat dan Obat Tradisional Badan Litbang Kesehatan Kem Kes RI E-mail: b2p2to2t@gmail.com
POTENSI EKSTRAK KERING SIRIH MANADO:MIYANA SEBAGAI BAHAN BAKU TABLET HERBAL Awal P, Yun Astuti Nugroho Balai Besar Litbang Tanaman Obat dan Obat Tradisional Badan Litbang Kesehatan Kem Kes RI E-mail: b2p2to2t@gmail.com
BAB II TINJAUAN PUSTAKA
 BAB II TINJAUAN PUSTAKA 2.1 Pengertian Obat Obat adalah suatu bahan atau campuran bahan yang dimaksudkan untuk digunakan dalam menentukan diagnosis, mencegah, mengurangi, menghilangkan, menyembuhkan penyakit
BAB II TINJAUAN PUSTAKA 2.1 Pengertian Obat Obat adalah suatu bahan atau campuran bahan yang dimaksudkan untuk digunakan dalam menentukan diagnosis, mencegah, mengurangi, menghilangkan, menyembuhkan penyakit
BAB III METODE PERCOBAAN
 BAB III METODE PERCOBAAN 3.1. Tempat dan Waktu Percobaan Percobaan ini dilakukan di Laboratorium Instrument PT. Kimia Farma (Persero) Tbk. Plant Medan Jalan Raya Tanjung Morawa Km. 9 pada bulan Februari
BAB III METODE PERCOBAAN 3.1. Tempat dan Waktu Percobaan Percobaan ini dilakukan di Laboratorium Instrument PT. Kimia Farma (Persero) Tbk. Plant Medan Jalan Raya Tanjung Morawa Km. 9 pada bulan Februari
BAB II TINJAUAN PUSTAKA
 BAB II TINJAUAN PUSTAKA 2.1 Tablet Menurut Farmakope Indonesia edisi IV, tablet adalah sediaan padat yang mengandung bahan obat dengan atau tanpa bahan pengisi. Berdasarkan metode pembuatan, dapat digolongkan
BAB II TINJAUAN PUSTAKA 2.1 Tablet Menurut Farmakope Indonesia edisi IV, tablet adalah sediaan padat yang mengandung bahan obat dengan atau tanpa bahan pengisi. Berdasarkan metode pembuatan, dapat digolongkan
INDAH USWATUN HASANAH UNIVERSITAS INDONESIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM DEPARTEMEN FARMASI PROGRAM EKSTENSI DEPOK 2008
 STUDI PERBANDINGAN PROFIL DISOLUSI DUA MEREK DAGANG TABLET PROPRANOLOL HIDROKLORIDA 10Mg MENGGUNAKAN PARAMETER FAKTOR PERBEDAAN (F1) dan FAKTOR PERSAMAAN (F2) INDAH USWATUN HASANAH 0305250271 UNIVERSITAS
STUDI PERBANDINGAN PROFIL DISOLUSI DUA MEREK DAGANG TABLET PROPRANOLOL HIDROKLORIDA 10Mg MENGGUNAKAN PARAMETER FAKTOR PERBEDAAN (F1) dan FAKTOR PERSAMAAN (F2) INDAH USWATUN HASANAH 0305250271 UNIVERSITAS
BAB 1 PENDAHULUAN 1.1 Latar Belakang
 BAB 1 PENDAHULUAN 1.1 Latar Belakang Perkembangan industri farmasi baik dalam maupun luar negeri bersaing untuk menghadirkan suatu sediaan obat yang memiliki harga yang murah dengan pemakaian yang mudah.
BAB 1 PENDAHULUAN 1.1 Latar Belakang Perkembangan industri farmasi baik dalam maupun luar negeri bersaing untuk menghadirkan suatu sediaan obat yang memiliki harga yang murah dengan pemakaian yang mudah.
J. Ind. Soc. Integ. Chem., 2013, Volume 5, Nomor 2 UJI KESERAGAMAN VOLUME SUSPENSI AMOKSISILIN YANG DIREKONSTITUSI APOTEK DI KOTA JAMBI.
 UJI KESERAGAMAN VOLUME SUSPENSI AMOKSISILIN YANG DIREKONSTITUSI APOTEK DI KOTA JAMBI Helni Bagian Farmasi, Fakultas Kedokteran dan Ilmu Kesehatan, Universitas Jambi, Jl. Letjen Soeprapto Telanaipura Jambi
UJI KESERAGAMAN VOLUME SUSPENSI AMOKSISILIN YANG DIREKONSTITUSI APOTEK DI KOTA JAMBI Helni Bagian Farmasi, Fakultas Kedokteran dan Ilmu Kesehatan, Universitas Jambi, Jl. Letjen Soeprapto Telanaipura Jambi
BAB II. STUDI PUSTAKA
 DAFTAR ISI KATA PENGANTAR... vi DAFTAR ISI... viii DAFTAR GAMBAR... xi DAFTAR TABEL... xiii DAFTAR LAMPIRAN... xiv INTISARI... xv ABSTRACT... xvi BAB I. PENDAHULUAN... 1 A. Latar Belakang Masalah... 1
DAFTAR ISI KATA PENGANTAR... vi DAFTAR ISI... viii DAFTAR GAMBAR... xi DAFTAR TABEL... xiii DAFTAR LAMPIRAN... xiv INTISARI... xv ABSTRACT... xvi BAB I. PENDAHULUAN... 1 A. Latar Belakang Masalah... 1
BAB I PENDAHULUAN. Hasil Survey Kesehatan Rumah Tangga (SKRT) tahun 2012 menunjukkan bahwa
 BAB I PENDAHULUAN A. LATAR BELAKANG Dewasa ini, jumlah penderita hipertensi di Indonesia semakin meningkat. Hasil Survey Kesehatan Rumah Tangga (SKRT) tahun 2012 menunjukkan bahwa prevalensi hipertensi
BAB I PENDAHULUAN A. LATAR BELAKANG Dewasa ini, jumlah penderita hipertensi di Indonesia semakin meningkat. Hasil Survey Kesehatan Rumah Tangga (SKRT) tahun 2012 menunjukkan bahwa prevalensi hipertensi
UJI PELEPASAN FLUKONAZOL DARI SEDIAAN SUPOSITORIA DENGAN BASIS HIDROFILIK, BASIS LIPOFILIK, DAN BASIS AMFIFILIK SECARA INVITRO
 UJI PELEPASAN FLUKONAZOL DARI SEDIAAN SUPOSITORIA DENGAN BASIS HIDROFILIK, BASIS LIPOFILIK, DAN BASIS AMFIFILIK SECARA INVITRO Sriwidodo, Boesro Soebagio, Ricki Maranata S Fakultas Farmasi Universitas
UJI PELEPASAN FLUKONAZOL DARI SEDIAAN SUPOSITORIA DENGAN BASIS HIDROFILIK, BASIS LIPOFILIK, DAN BASIS AMFIFILIK SECARA INVITRO Sriwidodo, Boesro Soebagio, Ricki Maranata S Fakultas Farmasi Universitas
BAB I PENDAHULUAN. Hidrokortison asetat adalah kortikosteroid yang banyak digunakan sebagai
 BAB I PENDAHULUAN 1.1 Latar Belakang Hidrokortison asetat adalah kortikosteroid yang banyak digunakan sebagai antiinflamasi local akibat dermatitis. Hidrokortison dapat mencegah dan menekan timbulnya gejala
BAB I PENDAHULUAN 1.1 Latar Belakang Hidrokortison asetat adalah kortikosteroid yang banyak digunakan sebagai antiinflamasi local akibat dermatitis. Hidrokortison dapat mencegah dan menekan timbulnya gejala
Validasi metode merupakan proses yang dilakukan
 TEKNIK VALIDASI METODE ANALISIS KADAR KETOPROFEN SECARA KROMATOGRAFI CAIR KINERJA TINGGI Erina Oktavia 1 Validasi metode merupakan proses yang dilakukan melalui penelitian laboratorium untuk membuktikan
TEKNIK VALIDASI METODE ANALISIS KADAR KETOPROFEN SECARA KROMATOGRAFI CAIR KINERJA TINGGI Erina Oktavia 1 Validasi metode merupakan proses yang dilakukan melalui penelitian laboratorium untuk membuktikan
UJI DISOLUSI TABLET ALLOPURINOL YANG DIPRODUKSI OLEH PT MUTIARA MUKTI FARMA (MUTIFA) MEDAN
 UJI DISOLUSI TABLET ALLOPURINOL YANG DIPRODUKSI OLEH PT MUTIARA MUKTI FARMA (MUTIFA) MEDAN TUGAS AKHIR OLEH: HARDINITA HASUGIAN NIM 102410005 PROGRAM STUDI DIPLOMA III ANALIS FARMASI DAN MAKANAN FAKULTAS
UJI DISOLUSI TABLET ALLOPURINOL YANG DIPRODUKSI OLEH PT MUTIARA MUKTI FARMA (MUTIFA) MEDAN TUGAS AKHIR OLEH: HARDINITA HASUGIAN NIM 102410005 PROGRAM STUDI DIPLOMA III ANALIS FARMASI DAN MAKANAN FAKULTAS
oleh tubuh. Pada umumnya produk obat mengalami absorpsi sistemik melalui rangkaian proses yaitu disintegrasi produk obat yang diikuti pelepasan obat;
 BAB 1 PENDAHULUAN Seiring dengan kemajuan teknologi dan pengetahuan dalam bidang farmasi, perkembangan terhadap metode pembuatan sediaan obat untuk meningkatkan mutu obat juga semakin maju. Dengan meningkatnya
BAB 1 PENDAHULUAN Seiring dengan kemajuan teknologi dan pengetahuan dalam bidang farmasi, perkembangan terhadap metode pembuatan sediaan obat untuk meningkatkan mutu obat juga semakin maju. Dengan meningkatnya
BAB 1 PENDAHULUAN 1.1 Latar Belakang Penelitian
 BAB 1 PENDAHULUAN 1.1 Latar Belakang Penelitian Tablet merupakan salah satu sediaan farmasi yang sangat digemari, karena bentuknya yang padat, mudah di bawa dan dapat menghasilkan efek yang cepat. Dalam
BAB 1 PENDAHULUAN 1.1 Latar Belakang Penelitian Tablet merupakan salah satu sediaan farmasi yang sangat digemari, karena bentuknya yang padat, mudah di bawa dan dapat menghasilkan efek yang cepat. Dalam
Faktor yang Berpengaruh Terhadap Proses Pelepasan, Pelarutan dan Absorbsi Obat
 Faktor yang Berpengaruh Terhadap Proses Pelepasan, Pelarutan dan Absorbsi Obat Al Syahril Samsi, S.Farm., M.Si., Apt 1 Faktor yang Mempengaruhi Liberation (Pelepasan), disolution (Pelarutan) dan absorbtion(absorbsi/difusi)lda
Faktor yang Berpengaruh Terhadap Proses Pelepasan, Pelarutan dan Absorbsi Obat Al Syahril Samsi, S.Farm., M.Si., Apt 1 Faktor yang Mempengaruhi Liberation (Pelepasan), disolution (Pelarutan) dan absorbtion(absorbsi/difusi)lda
UJI KEKERASAN, KEREGASAN, DAN WAKTU HANCUR BEBERAPA TABLET RANITIDIN
 UJI KEKERASAN, KEREGASAN, DAN WAKTU HANCUR BEBERAPA TABLET RANITIDIN Yos Banne, Selfie P.J. Ulaen, Fifiliane Lombeng Jurusan Farmasi Politeknik Kesehatan Kemenkes Manado Abstrak : Salah satu bentuk sediaan
UJI KEKERASAN, KEREGASAN, DAN WAKTU HANCUR BEBERAPA TABLET RANITIDIN Yos Banne, Selfie P.J. Ulaen, Fifiliane Lombeng Jurusan Farmasi Politeknik Kesehatan Kemenkes Manado Abstrak : Salah satu bentuk sediaan
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN A. Jenis dan Rancangan Penelitian Jenis penelitian yang dilakukan adalah penelitian eksperimental dengan melakukan percobaan disolusi tablet floating metformin HCl dan tablet
BAB III METODE PENELITIAN A. Jenis dan Rancangan Penelitian Jenis penelitian yang dilakukan adalah penelitian eksperimental dengan melakukan percobaan disolusi tablet floating metformin HCl dan tablet
PENGARUH SUHU TERHADAP STABILITAS BERBAGAI PRODUK TABLET NIFEDIPIN. Elda F. Luawo, Gayatri Citraningtyas, Novel Kojong
 PENGARUH SUHU TERHADAP STABILITAS BERBAGAI PRODUK TABLET NIFEDIPIN Elda F. Luawo, Gayatri Citraningtyas, Novel Kojong Program Studi Farmasi FMIPA UNSRAT Abstrak Penyimpanan obat pada kondisi suhu udara
PENGARUH SUHU TERHADAP STABILITAS BERBAGAI PRODUK TABLET NIFEDIPIN Elda F. Luawo, Gayatri Citraningtyas, Novel Kojong Program Studi Farmasi FMIPA UNSRAT Abstrak Penyimpanan obat pada kondisi suhu udara
BAB I PENDAHULUAN. Pada bab ini akan dibahas mengenai latar belakang dan tujuan penelitian.
 BAB I PENDAHULUAN Pada bab ini akan dibahas mengenai latar belakang dan tujuan penelitian. 1.1 Latar Belakang Masalah Perkembangan teknologi di bidang farmasi begitu pesat, termasuk pengembangan berbagai
BAB I PENDAHULUAN Pada bab ini akan dibahas mengenai latar belakang dan tujuan penelitian. 1.1 Latar Belakang Masalah Perkembangan teknologi di bidang farmasi begitu pesat, termasuk pengembangan berbagai
Zubaidi, J. (1981). Farmakologi dan Terapi. Editor Sulistiawati. Jakarta: UI Press. Halaman 172 Lampiran 1. Gambar Alat Pencetak Kaplet
 Zubaidi, J. (1981). Farmakologi dan Terapi. Editor Sulistiawati. Jakarta: UI Press. Halaman 17 Lampiran 1. Gambar Alat Pencetak Kaplet Lampiran. Perhitungan Karakteristik Pati Kentang Merah Berat kentang
Zubaidi, J. (1981). Farmakologi dan Terapi. Editor Sulistiawati. Jakarta: UI Press. Halaman 17 Lampiran 1. Gambar Alat Pencetak Kaplet Lampiran. Perhitungan Karakteristik Pati Kentang Merah Berat kentang
MIKROENKAPSULASI METFORMIN HIDROKLORIDA DENGAN PENYALUT ETILSELLULOSA MENGGUNAKAN METODA PENGUAPAN PELARUT ABSTRACT
 Jurnal Sains dan Teknologi Farmasi, Vol. 18, No.1, 2013, halaman 75-79 ISSN : 1410-0177 MIKROENKAPSULASI METFORMIN HIDROKLORIDA DENGAN PENYALUT ETILSELLULOSA MENGGUNAKAN METODA PENGUAPAN PELARUT Deni Noviza
Jurnal Sains dan Teknologi Farmasi, Vol. 18, No.1, 2013, halaman 75-79 ISSN : 1410-0177 MIKROENKAPSULASI METFORMIN HIDROKLORIDA DENGAN PENYALUT ETILSELLULOSA MENGGUNAKAN METODA PENGUAPAN PELARUT Deni Noviza
LAPORAN PRAKTIKUM. ISOLASI DNA, Isolasi Protein dan PCR (Elektroforesis agarose dan Acrylamic)
 LAPORAN PRAKTIKUM ISOLASI DNA, Isolasi Protein dan PCR (Elektroforesis agarose dan Acrylamic) Nama : Rebecca Rumesty Lamtiar (127008016) Yulia Fitri Ghazali (127008007) Paska Rahmawati Situmorang (127008011)
LAPORAN PRAKTIKUM ISOLASI DNA, Isolasi Protein dan PCR (Elektroforesis agarose dan Acrylamic) Nama : Rebecca Rumesty Lamtiar (127008016) Yulia Fitri Ghazali (127008007) Paska Rahmawati Situmorang (127008011)
PERBANDINGAN BIOAVAILABILITAS ( BIOEKIVALENSI ) OBAT CIMETIDINE DALAM SEDIAAN GENERIK DAN PATEN SECARA IN VITRO
 PERBANDINGAN BIOAVAILABILITAS ( BIOEKIVALENSI ) OBAT CIMETIDINE DALAM SEDIAAN GENERIK DAN PATEN SECARA IN VITRO ARTIKEL KARYA TULIS ILMIAH Diajukan untuk Memenuhi Tugas dan Melengkapi Persyaratan Dalam
PERBANDINGAN BIOAVAILABILITAS ( BIOEKIVALENSI ) OBAT CIMETIDINE DALAM SEDIAAN GENERIK DAN PATEN SECARA IN VITRO ARTIKEL KARYA TULIS ILMIAH Diajukan untuk Memenuhi Tugas dan Melengkapi Persyaratan Dalam
PROFIL PELEPASAN IN VITRO IBUPROFEN DALAM BENTUK TABLET LEPAS LAMBAT DENGAN MENGGUNAKAN MATRIKS GUAR GUM PADA BERBAGAI KONSENTRASI
 PROFIL PELEPASAN IN VITRO IBUPROFEN DALAM BENTUK TABLET LEPAS LAMBAT DENGAN MENGGUNAKAN MATRIKS GUAR GUM PADA BERBAGAI KONSENTRASI OLEH: MORRIS DINATA 2443005096 FAKULTAS FARMASI UNIVERSITAS KATOLIK WIDYA
PROFIL PELEPASAN IN VITRO IBUPROFEN DALAM BENTUK TABLET LEPAS LAMBAT DENGAN MENGGUNAKAN MATRIKS GUAR GUM PADA BERBAGAI KONSENTRASI OLEH: MORRIS DINATA 2443005096 FAKULTAS FARMASI UNIVERSITAS KATOLIK WIDYA
BAB I PENDAHULUAN. Pada bab ini akan dibahas mengenai latar belakang dan tujuan penelitian.
 BAB I PENDAHULUAN Pada bab ini akan dibahas mengenai latar belakang dan tujuan penelitian. 1.1. Latar Belakang Masalah Dengan perkembangan dunia dewasa ini, industri farmasi mengalami kemajuan yang pesat.
BAB I PENDAHULUAN Pada bab ini akan dibahas mengenai latar belakang dan tujuan penelitian. 1.1. Latar Belakang Masalah Dengan perkembangan dunia dewasa ini, industri farmasi mengalami kemajuan yang pesat.
merupakan masalah umum yang menimpa hampir 35% dari populasi umum, khususnya pediatri, geriatri, pasien stroke, penyakit parkinson, gangguan
 BAB 1 PENDAHULUAN Saat ini indutri farmasi berfokus pada pengembangan sistem penghantaran obat secara oral yang menawarkan kepatuhan pasien dan dosis yang efektif. Rute pemberian oral tidak diragukan lagi
BAB 1 PENDAHULUAN Saat ini indutri farmasi berfokus pada pengembangan sistem penghantaran obat secara oral yang menawarkan kepatuhan pasien dan dosis yang efektif. Rute pemberian oral tidak diragukan lagi
BAB I PENDAHULUAN. Pati merupakan homopolimer glukosa dengan ikatan α-glikosidik. Pati
 BAB I PENDAHULUAN 1.1 Latar Belakang Pati merupakan homopolimer glukosa dengan ikatan α-glikosidik. Pati terdiri dari butiran-butiran kecil yang disebut granula (Jane, 1995). Winarno (2002), menyatakan
BAB I PENDAHULUAN 1.1 Latar Belakang Pati merupakan homopolimer glukosa dengan ikatan α-glikosidik. Pati terdiri dari butiran-butiran kecil yang disebut granula (Jane, 1995). Winarno (2002), menyatakan
PHARMACONJurnal Ilmiah Farmasi UNSRAT Vol. 4 No. 4 NOVEMBER 2015 ISSN
 VALIDASI METODE UNTUK PENETAPAN KADAR CIPROFLOXACIN DALAM SEDIAAN TABLET DENGAN NAMA DAGANG DAN GENERIK SECARA SPEKTROFOTOMETRI ULTRAVIOLET Herlinda I.P Tjaboali 1), Fatimawali 1), Defny S. Wewengkang
VALIDASI METODE UNTUK PENETAPAN KADAR CIPROFLOXACIN DALAM SEDIAAN TABLET DENGAN NAMA DAGANG DAN GENERIK SECARA SPEKTROFOTOMETRI ULTRAVIOLET Herlinda I.P Tjaboali 1), Fatimawali 1), Defny S. Wewengkang
BAB 1 PENDAHULUAN. Pada bab ini akan dibahas mengenai latar belakang dan tujuan penelitian.
 BAB 1 PENDAHULUAN Pada bab ini akan dibahas mengenai latar belakang dan tujuan penelitian. 1.1. Latar Belakang Masalah Obat anti-inflamasi non steroid (AINS) banyak dimanfaatkan pada pengobatan kelainan
BAB 1 PENDAHULUAN Pada bab ini akan dibahas mengenai latar belakang dan tujuan penelitian. 1.1. Latar Belakang Masalah Obat anti-inflamasi non steroid (AINS) banyak dimanfaatkan pada pengobatan kelainan
