LAPORAN PERCOBAAN. HARI/ TANGGAL PERCOBAAN Hari Jum at/ Tanggal 04 Desember 2015 Pukul WIB
|
|
|
- Widyawati Hermanto
- 6 tahun lalu
- Tontonan:
Transkripsi
1 LAPORAN PERCOBAAN I II III IV V JUDUL PERCOBAAN Titrasi Penetralan dan Aplikasinya HARI/ TANGGAL PERCOBAAN Hari Jum at/ Tanggal 04 Desember 2015 Pukul WIB SELESAI PERCOBAAN Hari Jum at/ Tanggal 04 Desember 2015 Pukul WIB TUJUAN PERCOBAAN 1 Membuat dan menentukan standarisasi larutan basa 2 Menentukan kadar H 2 SO 4 dalam accu zuur TINJAUAN PUSTAKA Titrasi Penetralan (asidi alkalimetri) Titrasi adalah proses mengukur volume larutan yang terdapat dalam buret yang ditambahkan ke dalam larutan lain yang diketahui volumenya sampai terjadi reaksi sempurna. Atau dengan perkataan lain untuk mengukur volume titran yang diperlukan untuk mencapai titik ekivalen. Titik ekivalen adalah saat yang menunjukkan bahwa ekivalen perekasi-pereaksi sama. Di dalam prakteknya titik ekivalen sukar diamati, karena hanya meruapakan titik akhir teoritis atau titik akhir stoikometri. Hal ini diatasi dengan pemberian indikator asam-basa yang membantu sehingga titik akhir titrasi dapat diketahui. Titik akhir titrasi meruapakan keadaan di mana penambahan satu tetes zat penitrasi (titran) akan menyebabkan perubahan warna indikator. Kadua cara di atas termasuk analisis titrimetri atau volumetrik. Selama bertahun-tahun istilah analisis volumetrik lebih sering digunakan dari pada titrimetrik. Akan tetatpi, dilihat dari segi yang yang keta, titrimetrik lebih baik, karena pengukuran volume tidak perlu dibatasi oleh titrasi. Reaksi-reaksi kima yang dapat diterima sebagai dasar penentuan titrimetrik asam-basa adalah sebagai berikut : - Jika HA meruapakn asam yang akan ditentukan dan BOH sebabagi basa, maka reksinya adalah : HA + OH A - + H 2 O
2 - Jika BOH merupakan basa yang akan ditentukan dan HA sebagi asam, maka reaksinya adalah ; BOH + H + B + = H 2 O Dalam analisis titrimetri, sebuah reaksi harus memenuhi beberapa persyaratan sebelum reaksi tersebut dapat dipergunakan, diantaranya: 1. Reaksi itu sebaiknya diproses sesuai persamaan kimiawi tertentu dan tidak adanya reaksi sampingan. 2. Reaksi itu sebaiknya diproses sampai benar-benar selesai pada titik ekivalensi. Dengan kata lain konstanta kesetimbangan dari reaksi tersebut haruslah amat besar besar. Maka dari itu dapat terjadi perubahan yang besar dalam konsentrasi analit (atau titran) pada titik ekivalensi. 3. Diharapkan tersedia beberapa metode untuk menentukan kapan titik ekivalen tercapai. Dan diharapkan pula beberapa indikator atau metode instrumental agar analis dapat menghentikan penambahan titran. 4. Diharapkan reaksi tersebut berjalan cepat, sehingga titrasi dapat dilakukan hanya beberapa menit. (anonim, 2009) Reaksi asam -basa adalah reaksi yang terjadi antara larutan asam dengan larutan basa, hasil reaksi ini dapat bersifat netral disebut juga reaksi penetralan asam basa tergantung pada larutan yang direaksikan. Larutan yang direaksikan ini salah satunya disebut larutan baku. Larutan baku adalah larutan yang konsentrasinya diketahui dengan tepat dan dapat digunakan untuk menentukan konsentrasi larutan lain. Larutan baku ada dua yaitu larutan baku primer dan larutan baku sekunder. Asidimetri dan alkalimetri termasuk reaksi netralisasi yakni reaksi antara ion hidrogen yang berasal dari asam dengan ion hidroksida yang berasal dari basa untuk menghasilkan air yang bersifat netral. Netralisasi dapat juga dikatakan sebagai reaksi antara donor proton (asam) dengan penerima proton (basa). H + + OH - H 2 O Asidimetri merupakan penetapan kadar secara kuantitatif terhadap senyawa-senyawa yang bersifat basa dengan menggunakan baku asam, sebaliknya alkalimetri adalah penetapan kadar senyawa-senyawa yang bersifat asam dengan menggunakan baku basa.
3 Untuk menetapkan titik akhir pada proses netralisasi ini digunakan indikator. Menurut W. Ostwald, indikator adalah suatu senyawa organik kompleks dalam bentuk asam (Hin) atau dalam bentuk basa (InOH) yang mampu berada dalam keadaan dua macam bentuk warna yang berbeda dan dapat saling berubah warna dari bentuk satu ke bentuk yang lain pada konsentrasi H + tertentu atau pada ph tertentu. Jalannya proses titrasi netralisasi dapat diikuti dengan melihat perubahan ph larutan selama titrasi, yang terpenting adalah perubahan ph pada saat dan di sekitar titik ekuivalen karena hal ini berhubungan erat dengan pemilihan indikator agar kesalahan titrasi sekecil-kecilnya. Dalam asidi-alkalimetri, 1 ekivalen asam atau basa ialah sebanyak senyawa ini yang dapat melepaskan 1 mol ion H + (atau H 3 O + ). Proses untuk menentukan banyaknya ekivalen asam dibutuhkan untuk menetralkan sevolume larutan basa atau sebaliknya dititrasi, seharusnya: Jumlah ekivalen asam = jumlah ekivalen basa Saat persamaan ini tercapai, disebut titik ekivalen. Bila kita mengerjakan titrasinya, tanda-tanda apa yang memberi petunjuk, yang kita harus mengthentikan titrasinya? Jawabanya : perubahan warna indikator yang menandakan tercapainya titik akhir titrasi. Suatu indikator berubah warnanya pada daerah ph tertentu, misalnya: Metil jingga : merah ph 3,1 ph 4,4 kuning Bromtimol biru : kuning ph 6,0 ph 7,6 biru Fenoftalin : bening ph 8,0 ph 9,8 merah Larutan baku primer adalah larutan baku yang konsentrasinya dapat ditentukan dengan jalan menghitung dari berat zat terlarut yang dilarutkan dengan tepat. Larutan baku primer harus dibuat dengan: a. Penimbangan dengan teliti menggunakan neraca analitik b. Dilarutkan dalam labu ukur Bahan kimia yang dapat digunakan sebagai bahan membuat larutan standar primer harus memenuhi tiga persyaratan berikut: a. Benar-benar ada dalam keadaan murni dengan kadar pengotor b. Stabil secara kimiawi, mudah dikeringkan dan tidak bersifat higroskopis. c. Memiliki berat ekivalen besar, sehingga meminimalkan kesalahan akibat penimbangan.
4 Pada percobaan kali ini larutan yang digunakan sebagai larutan baku primer adalah H 2 C 2 O 4. 2H 2 O (asam oksalat). Asam oksalat adalah zat padat, halus, putih, larut baik dalam air. Asam oksalat adalah asam divalent dan pada titrasinya selalu sampai terbentuk garam normalnya..berat ekivalen asam oksalat adalah 63. Larutan baku sekunder adalah larutan baku yang konsentrasinya harus ditentukan dengan cara titrasi terhadap larutan baku primer. Pada percobaan kali ini larutan yang digunakan sebagai larutan baku sekunder adalah NaOH. Larutan NaOH tergolong dalam larutan baku sekunder yang bersifat basa. Natrium hidroksida (NaOH), juga dikenal sebagai soda kaustik, adalah sejenis basa logam kaustik. Natrium hidroksida membentuk larutan alkalin yang kuat ketika dilarutkan ke dalam air. Natrium hidroksida murni berbentuk putih padat dan tersedia dalam bentuk pelet, serpihan, butiran ataupun larutan jenuh 50%. NaOH bersifat lembab cair dan secara spontan menyerap karbondioksida dari udara bebas. Ia sangat larut dalam air dan akan melepaskan panas ketika dilarutkan. NaOH juga larut dalam etanol dan metanol, walaupun kelarutan NaOH dalam kedua cairan ini lebih kecil daripada kelarutan KOH. NaOH tidak larut dalam dietil eter dan pelarut non polar lainnya. Indikator asam basa sebagai zat penunjuk derajat keasaman kelarutan adalah senyawa organik dengan struktur rumit yang berubah warnanya bila ph larutan berubah. Indikator dapat pula digunakan untuk menetapkan ph dari suatu larutan. Indikator merupakan asam lemah atau basa lemah yang memiliki warna cukup tajam, hanya dengan beberapa tetes larutan encer-encernya, indikator dapat digunakan untuk menetapkan titik ekivalen dalam titrasi asam basa ataupun untuk menentukan tingkat keasaman larutan. Pada percobaan kali ini indikator yang akan digunakan adalah indikator phenolphtalein atau sering disebut dengan indikator PP. Indikator PP memiliki warna asam tak berwarna, rentang ph perubahan warna antara 8,3 10,0 dan warna basa merah. Aplikasi titrasi penetralan ini untuk menentukan kadar H 2 SO 4 dalam accu zuur. Dalam keadaan murni cairan asam sulfat (H 2 SO 4 ) tidak
5 berwarna dan memiliki viskositas tinggi. Didalam air, asam sulfat merupakan asam kuat menurut persamaan reaksi : H 2 SO 4 (aq) + H 2 O (l) [H 3 O] + (aq) + [HSO 4- ] (aq) Didalam larutan encer, asam sulfat (H 2 SO 4 ) dapat mengalami reaksi netralisasi dengan basa (seperti KOH) sesuai dengan persamaan sebagai berikut : H 2 SO 4 (aq) + 2 KOH (aq) K 2 SO 4 (aq) + 2 H 2 O (l) Accu zuur berisi cairan asam sulfat (H 2 SO 4 ). Konsentrasi asam sulfat dalam air accu zuur ini dalam keadaan encer dan kandungannya di pasaran berbeda-beda. Umumnya, konsentrasi asam sulfat dalam accu zuur adalah sebesar 30 % dengan berat jenis sebesar 1,28 kg/l dan pelarut 100 % air murni. Asam sulfat bersifat korosif, jika kontak dengan kulit akan menyebabkan gatal-gatal, jika kontak dengan mata akan menyebabkan iritasi mata, serta gangguan lain pada tubuh. Bahaya H 2 SO 4 terhadap kesehatan tergantung pada konsentrasi larutannya. < 10 % bersifat intan dan > 10 % bersifat korosif. Penentuan konsentrasi asam sulfat (H 2 SO 4 ) dalam accu zuur dilakukan berdasarkan metode titrimetri yang merupakan cara analisis kuantitatif yang didasarkan pada prinsip stoikiometri reaksi kimia. Metode titrimetri yang dilakukan didasarkan pada prinsip netralisasi antara analit (titer) asam sulfat (H 2 SO 4 ) yang dititrasi dengan titran NaOH yang telah diketahui konsentrasinya menurut persamaan sebagai berikut : H 2 SO 4 (aq) + 2 NaOH (aq) Na 2 SO 4 (aq) + 2 H 2 O (l) Penentuan titik akhir titrasi atau titik ekuivalen dilakukan dengan penambahan indicator, metode titrasi potensiometri dan metode titrasi konduktometri. VI ALAT DAN BAHAN : Alat : Buret Statif dan klem Erlenmeyer 250 ml Gelas kimia Corong Neraca analitik Pipet gondok Pro pipet Labu ukur 250 ml Tempat klise film Pipet tetes Spatula
6 Bahan: larutan HCl air suling (aquades) Na 2 CO 3 Indikator PP Air Accu zuur Larutan NaOH 0,1 N H 2 C 2 O 4.2H 2 O Indikator metil jingga VII ALUR KERJA Pembuatan Larutan NaOH ± 0,1N a. Cara pertama b. Cara kedua 4,2 gram - Dilarutkan dalam air suling - Diencerkan sampai volume 1L - Dikocok dengan baik agar tercampur Larutan NaOH 50 gram NaOH - Dituang dalam gelas kimia yang berisi 50ml air suling -Dibiarkan sampai larutan mengendap Endapan Na 2 CO 3 kotor
7 6,5mL larutan NaOH pekat Diencerkan dengan air suling sampai 1L dan disimpan Larutan NaOH 0,1N Pembuatan Larutan NaOH ± 0,1N Dengan asam sebagai baku 1,6 gram H 2 C 2 O 4.2H 2 O - Dipindahkan dalam labu ukur 250mL - Dilarutkan dengan air suling - Diencerkan sampai tanda batas -Kocok labu ukur agar tercampur dengan baik Larutan baku H 2 C 2 O 4.2H 2 O - Dipipet 25mL menggunakan pipet seukuran - Dimasukkan ke dalam erlenmeyer 250mL - Ditambahkan 25mL air suling - Ditambahkan 2-3 tetes indikator PP Perubahan warna -Catat angka pada skala buret Volume NaOH
8 -Dilakukan sebanyak 3 kali Hasil Penentuan Kadar H 2 SO 4 dalam Accu Zuur Accu Zuur Larutan Accu Zuur -Dituang ke dalam labu ukur 100mL yang berisi 10mL aquades - Diambil 10ml menggunakan pipet seukuran - Dimasukkan ke dalam erlenmeyer - Ditambahkan beberapa tetes indikator metil jingga Perubahan warna - Dicatat angka pada skala buret -Dilakukan 3 kali Hasil
9
10 VIII HASIL PENGAMATAN N Prosedur Percobaan 1. Pembuatan Larutan NaOH ± 0,1N c. Cara pertama 4,2 gram d. Cara kedua - Dilarutkan dalam air suling - Diencerkan sampai volume 1L - Dikocok dengan baik agar tercampur Larutan NaOH 50 gram NaOH Endapan Na 2 CO 3 kotor Hasil Pengamatan Sebelu Sesudah m NaOH = tidak NaOH + air berwarna suling = tidak Air suling = berwarna tidak berwarna NaOH = tidak berwarna Air suling = tidak berwarna NaOH + air suling = tidak berwarna Dugaan / Reaksi Kesimpulan NaOH (s) + H 2 O NaOH (aq) H 2 O H + + OH -
11 - Dituang dalam gelas kimia yang berisi 50ml air suling Pembuatan Larutan NaOH ± 0,1N Dengan asam sebagai baku 1,6 gram H 2 C 2 O 4.2H 2 O -Dibiarkan sampai larutan mengendap 6,5mL larutan NaOH pekat -Diencerkan dengan air suling sampai 1L dan disimpan Larutan NaOH 0,1N NaOh pekat = tidak berwarna H 2 C 2 O 4.2H 2 O = serbuk berwarna putih Indikator PP = tidak berwarna NaOH pekat + air suling = todak berwarna H 2 C 2 O 4.2H 2 O + air suling = tidak berwarna H 2 C 2 O 4.2H 2 O + air suling + indikator PP = tidak berwarna H 2 C 2 O 4.2H 2 O + air suling + indikator PP + NaOH = NaOH (s) + H 2 O (l) NaOH (aq) 2NaOH +H 2 C 2 O 4 Na 2 C 2 O 4 H 2 C 2 + H 2 O H 2 C 2 O 4 Penambahan indikator PP bermaksud untuk menentukan titik akhir titrasi (terjadinya perubahan warna akibat terdapat titran berlebih yang mengakibatkan lonjakan asam atau basa) Dalam percobaan ini diperoleh hasil titrasi sebagai berikut: V1 = 1,5mL V2 = 1,5mL V3 = 1,5mL
12 - Dipindahkan dalam labu ukur 250mL - Dilarutkan dengan air suling - Diencerkan sampai tanda batas -Kocok labu ukur agar tercampur dengan baik Larutan baku H 2 C 2 O 4.2H 2 O Larutan baku H 2 C 2 O 4.2H 2 O merah muda Dan mengalami perubahan warna menjadi pink (merah muda soft) Trayek ph pada phenolptalien = 8,0 9,6 Dan perubahan warna yang menunjukkan adanya basa
13 - Dipipet 25mL menggunakan pipet seukuran - Dimasukkan ke dalam erlenmeyer 250mL Perubahan - Ditambahkan warna 25mL air suling -Catat angka pada skala buret Volume NaOH - Ditambahkan 2-3 tetes indikator PP -Dilakukan sebanyak 3 kali Hasil
14 2. Penentuan Kadar H 2 SO 4 dalam Accu Zuur Accu Zuur Larutan Accu Zuur Perubahan warna Hasil Larutan accu zuur = tidak berwarna Indikator metil jingga = jingga NaOH = tidak berwarna Accu zuur + indikator metil jingga = merah Accu zuur + indikator metil jingga + NaOH = kuning H 2 SO4 + 2NaOH Na 2 SO 4 + 2H 2 O Penambahan metil jingga mengubah larutan menjadi berwarna merah Pada saat titik akhir titrasi mengalami perubahan dari merah menjadi kuning Trayek ph indikator metil jingga = 3,1 4,4 Dalam percobaan ini diperoleh hasil titrasi sebagai berikut: V1 = 5,75mL V2 = 5,83mL V3 = 5,92mL Dan perubahan warna yang menunjukkan adanya H 2 SO 4
15 --Dituang Diambil ke 10ml dalam menggunakan labu ukur - pipet 100mL Dicatat seukuran yang angka berisi pada 10mL skala aquades buret - Dimasukkan ke dalam -Dilakukan erlenmeyer 3 kali - Ditambahkan beberapa tetes indikator metil jingga
16 IX ANALISIS DAN PEMBAHASAN 1 Menentukan (standarisasi) larutan NaOH dengan H 2 C 2 O 4. 2H 2 O sebagai baku Sebelum melakukan standarisasi hendaknya membuat larutan NaOH dengan menimbang NaOH 4,2 gram kemudian dilarutkan kedalam air suling dan diencerkan sampai volume 1 liter dengan dikocok agar tercampur dengan baik. Dalam pembuatan standarisasi Asam Oksalat harus menimbang Asam Oksalat 0,09 gram. H 2 C 2 O 4. 2H 2 O yang sudah ditimbang dimasukkan kedalam labu ukur 100 ml. Sisa KIO 3 dalam roll film dicuci hingga tidak ada yang tersisa dan dimasukkan ke dalam labu ukur. Ditambahkan aquades yang berfungsi untuk mengencerkan kedalam labu ukur hingga sebelum tanda batas, ditambahkan lagi aquades menggunakan pipet tepat pada tanda batas. Dikocok hingga menjadi larutan homogen. Sehingga didapatkan larutan H 2 C 2 O 4. 2H 2 O jernih tak berwarna sebagai larutan baku. Diambil 10 ml dengan pipet seukuran, dimasukkan kedalam labu erlenmeyer 250 ml. Kemudian ditambahkan 2-3 tetes indikator PP (phenolptalin) dengan rentang ph 8,0-9,6 tidak berwarna merupakan indikator yang baik untuk larutan basa dan bertujuan untuk mengetahui titik akhir titrasi. Dari penambahan yang dilakukan dihasilkan larutan tidak berwarna, kemudian larutan ini dititrasi dengan larutan NaOH tidak berwarna hingga larutan berwarna merah muda. Perubahan warna dari tidak berwarna menjadi merah muda ketika larutan mencapai ph sekitar 8,2 atau melewatinya. Percobaan ini dilakukan sampai tiga kali dengan diperoleh data volume NaOH yang digunakan sebagai berikut: V 1 = 1,5 ml, V 2 = 1,5 ml, V 3 = 1,5 ml. Untuk menentukan konsentrasi NaOH maka harus diketahui konsentrasi H 2 C 2 O 4. Konsentrasi H 2 C 2 O 4 dapat dicari dengan rumus N= n x gr Mr V, dengan n= 2, massa yang digunakan 0,09 gram, Mr 90 dan volume 0,1 Liter maka diperoleh konsentrasi H 2 C 2 O 4
17 sebesar 0,02 N. Diperoleh konsentrasi NaOH : N 1 = 0,13 N, N 2 = 0,13 N, N 3 = 0,13 N, sehingga N rata-rata = 0,13 N 2 Menentukan kadar H 2 SO 4 dalam Accu Zuur Pada aplikasi titrasi iodometri untuk menentukan kadar H 2 SO 4 dalam Accu Zuur. Langkah pertama yang dilakukan adalah menimbang massa piknometer kosong 18,2649 gram dan massa piknometer isi accu zuur sebanyak 0,8 ml 19,3722 gram dengan volume 25 ml. kemudian accu zuur didalam piknometer dimasukkan kedalam labu ukur 100 ml untuk diencerkan dan didiamkan selama 15 menit. Dari 100 ml diambil 10 ml dari larutan accu zuur (jernih tak berwarna) dan dimasukkan kedalam erlenmeyer lalu ditambahkan beberapa tetes indikator metil jingga dengan rentang ph 3,1-4,4 (jingga) merupakan indikator yang berwarna merah dalam larutan asam serta menjadi kuning dalam larutan alkali dan basa. Dari penambahan yang dilakukan ini diperoleh larutan berwarna merah. Kemudian dititrasi dengan NaOH tidak berwarna sampai larutan berwarna kuning. Percobaan ini dilakukan sampai tiga kali dengan diperoleh data volume NaOH yang digunakan sebagai berikut: V 1 = 5,75 ml, V 2 = 5,83 ml, V 3 = 5,92 ml Dengan diketahuinya massa H 2 SO 4 maka dapat dihitung kadar H 2 SO 4 dengan rumus : % H 2 SO 4 N NaOH V NaOH BE massa total x100 Sehingga diperoleh kadar H 2 SO 4 sebesar 33,07% ; 33,53%; 34,05%,maka kadar H 2 SO 4 rata-rata = 33,55%.
18 X KESIMPULAN Dari percobaan ini dapat diketahui: 1 Normalitas rata-rata NaOH = 0,13N 2 Kadar H 2 SO 4 rata-rata = 33,55%
19 STANDARISASI JAWABAN PERTANYAAN 1. Mengapa pada pembuatan larutan NaOH harus memakai air yang sudah dididihkan? Jawab : Tujuan menggunakan air yang mendidih yaitu untuk menghindari ledakan, sebab reaksi logam alkali (Na) bersifat eksoterm.dan juga logam alkali (Na) mudah bereaksi dengan air.mudah bereaksi dengan air. 2. Apakah beda antara : a. larutanbaku dan larutan standar? b. asidimetri dan alkalimetri? Jawab: a) larutan baku: dimana larutan itu konsentrasinya diketahui dari hasil penimbangan dan pengenceran, konsentrasi ditentukan dari hasil perhitungan larutan standar: dimana larutan itu konsentrasinya sudah ditetapkan dengan akurat. b) asidimetri : dimana menitrasi larutan menggunakan larutan baku asam alkalimetri : dimana menitrasi larutan menggunakan larutan baku basa. 3. Berikan alasan penggunaan indikator pada titrasi di atas! Jawab : Pada titrasi antara HCl dengan Na 2 CO 3 menggunakan indikator metiljingga karena titrasi tersebut antara asam kuat dengan basa lemah yang memiliki rentang ph 3,1-4,4. Pada umumnya indikator digunakan untuk menentukan titik equivalen atau titik akhir titrasi tepat pada ph tertentu.
20 APLIKASI 1. 1,2 gram sampel NaOH dan Na 2 CO 3 dilarutkan dan dititrasi dengan 0,5N HCl dengan indikator pp. setelah penambahan 30 ml HCl larutan menjadi tidak berwarna. Kemudian indikator metil jingga ditambahkan dan dititrasi lagi dengan HCl. Setelah penambahan 5mL HCl larutan menjadi berwarna. Berapa prosentase Na 2 CO 3 dan NaOH dalam sampel? Jawaban: Diketahui: - Massa NaOH = 1,2 gram - Mr NaHCO 3 = 84,008 gr/mol - M HCl = 0,5 N - V1 = 30mL - V2 = 5mL Ditanya: persentase Na 2 CO 3 dan NaOH Jawab: NaOH = M(V1 V2) = 0,5 mmol/ml (30 5)ml = 12,5 mmol = 0,0125 mol Massa NaOH = 0,0125 mol x 40g/mol = 0,5 gram Kadar NaOH = 0,5g x , 667% 1,2 g Na 2 CO 3 = M.V2 = 0,5 mmol/ml. 10ml = 2,5 mmol = 0,0025 mol Massa Na 2 CO 3 = 0,0025 mol x 106 g/mol = 0,265 gram 0, 265g x , 083% 1, 2g Kadar Na 2 CO 3 = 2. Pada ph berapa terjadi perubahan warna indikator pp? Jawaban: Pada rentang ph 8,0-9,6
21 DAFTAR PUSTAKA Chun, van der Titrasi Penetralan Dan Aplikasi (Online) diakses pada tanggal 01 Desember 2015 Day. R.A Underwood. A.L Quantitative Analysis (fifth ed.).new York: Prentice Hall. (Terjemahan oleh A. Hadyana Analisis Kimia Kuantitatif (ed. Ke 5).Jakarta: Erlangga) Harjadi, W Ilmu Kimia Analitik Dasar (cetakan kedua). Jakarta: PT. Gramedia. Harmilton, F. Leicester Calculations of Analytical Chemistry (Sixth ed). New York : MC. Graw Hill Book Company. Inc. Piola, wina Laporan Praktikum Asidi-Alkalimetri (online). diakses pada tanggal 01 Desember 2015 Setiarso, Pirim, dkk Petunjuk Praktikum Kimia Analitik I (DDKA). Surabaya : Unipress Svehla, G Buku Teks Analisis Anorganik Kualitatif Makro dan Semimikro. Edisi ke-5. Jakarta: PT. Kalman Media Pusaka. Widodo, Didik Setyo, dan Retno Ariadi Kimia Analisis Kuantitatif Dasar Penguasaan Aspek Eksperimental. Yogyakarta : Graha Ilmu
22 LAMPIRAN PERHITUNGAN Diketahui : massa H 2 C 2 O 4 = 0,45 Ct = 0,45 x 0,2 = 0,09 gram Volume H 2 C 2 O 4 = 10 ml Mr H 2 C 2 O 4 = 90 gr mol Volume larutan = 100 ml = 0,1 L V NaOH : - percobaan 1 : V awal = 14,25 V akhir = 15,75 1,5 - percobaan 2 : V awal = 11,25 V akhir = 12,75 1,5 - percobaan 3 : V awal = 12,75 V akhir = 14,251,5 ml a.) Percobaan 1 ( 1,5 ml ) H 2 C 2 O 4. xh 2 O = NaOH Va. Na = Vb. Nb Va. n. g Mr.V = Vb. 10 ml. 2. Nb 0,09 g 90 g mol. 0,1 L = 1,5 ml. Nb 0,2 = 1,5 ml. Nb Nb = 0,13 N b.) Percobaan 2 ( 1,5 ml ) H 2 C 2 O 4. xh 2 O = NaOH Va. Na = Vb. Nb Va. n. g Mr.V = Vb. Nb
23 10 ml. 2. 0,09 g 90 g mol. 0,1 L = 1,5 ml. Nb 0,2 = 1,5 ml. Nb Nb = 0,13 N c.) Percobaan 3 ( 1,5 ml ) H 2 C 2 O 4. xh 2 O = NaOH Va. Na = Vb. Nb Va. n. g Mr.V = Vb. 10 ml. 2. Nb 0,09 g 90 g mol. 0,1 L = 1,5 ml. Nb 0,2 = 1,5 ml. Nb Nb = 0,13 N N NaOH rata-rata = 0,13+ 0,13+0,13 =0,13 N 3 Kadar H 2 SO 4 dalam accu zuur Diketahui : N NaOH = 0,13 N M accu zuur = 1,1073 g = 1107,3 mg Mr H 2 SO 4 = 98 gr mol 1.) Percobaan 1 : ( 5,75 ml ) V NaOH = 5,75 ml % H 2 SO 4 = x 100 % V NaOH. N NaOH. Be H 2 SO mgtotal
24 = 5,75 ml. 0,13 N ,3 x 100 % = 0,3307 x 100 % = 33,07 % 2.) Percobaan 2 : ( 5,83 ml ) V NaOH = 5,83 ml % H 2 SO 4 = V NaOH. N NaOH. Be H 2 SO mgtotal x 100 % = 5,83 ml. 0,13 N ,3 x 100 % = 0,3353 x 100 % = 33,53 % 3.) Percobaan 3 : ( 5,92 ml ) V NaOH = 5,92 ml % H 2 SO 4 = V NaOH. N NaOH. Be H 2 SO mgtotal x 100 % = 5,92 ml. 0,13 N ,3 x 100 % = 0,3405 x 100 % = 34,05 % % H 2 SO 4 rata-rata = 33,07 +33, ,05 3 =33,55
TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN
 TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN I. JUDUL PERCOBAAN : TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN II. TUJUAN PERCOBAAN : 1. Membuat dan
TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN I. JUDUL PERCOBAAN : TITRASI PENETRALAN (asidi-alkalimetri) DAN APLIKASI TITRASI PENETRALAN II. TUJUAN PERCOBAAN : 1. Membuat dan
LAPORAN PRAKTIKUM STANDARISASI LARUTAN NaOH
 LAPORAN PRAKTIKUM STANDARISASI LARUTAN NaOH I. Tujuan Praktikan dapat memahami dan menstandarisasi larutan baku sekunder NaOH dengan larutan baku primer H 2 C 2 O 4 2H 2 O II. Dasar Teori Reaksi asam basa
LAPORAN PRAKTIKUM STANDARISASI LARUTAN NaOH I. Tujuan Praktikan dapat memahami dan menstandarisasi larutan baku sekunder NaOH dengan larutan baku primer H 2 C 2 O 4 2H 2 O II. Dasar Teori Reaksi asam basa
Judul Percobaan II. Tujuan Percobaan III. Tanggal Percobaan IV. Selesai Percobaan Dasar Teori:
 I. Judul Percobaan : Titrasi Penetralan dan Aplikasinya II. Tujuan Percobaan : 1. Membuat dan menentukan standarisasi larutan asam 2. Membuat dan menentukan standarisasi larutan basa 3. Menentukan kadar
I. Judul Percobaan : Titrasi Penetralan dan Aplikasinya II. Tujuan Percobaan : 1. Membuat dan menentukan standarisasi larutan asam 2. Membuat dan menentukan standarisasi larutan basa 3. Menentukan kadar
II. HARI DAN TANGGAL PERCOBAAN
 I. JUDUL PERCOBAAN Titrasi Penetralan dan Aplikasinya II. HARI DAN TANGGAL PERCOBAAN Jum at, 4 Desember 2015 III. SELESAI PERCOBAAN Jum at, 4 Desember 2015 IV. TUJUAN PERCOBAAN 1. Membuat dan menentukan
I. JUDUL PERCOBAAN Titrasi Penetralan dan Aplikasinya II. HARI DAN TANGGAL PERCOBAAN Jum at, 4 Desember 2015 III. SELESAI PERCOBAAN Jum at, 4 Desember 2015 IV. TUJUAN PERCOBAAN 1. Membuat dan menentukan
ASIDI-ALKALIMETRI PENETAPAN KADAR ASAM SALISILAT
 ASIDI-ALKALIMETRI PENETAPAN KADAR ASAM SALISILAT I. DASAR TEORI I.1 Asidi-Alkalimetri Asidi-alkalimetri merupakan salah satu metode analisis titrimetri. Analisis titrimetri mengacu pada analisis kimia
ASIDI-ALKALIMETRI PENETAPAN KADAR ASAM SALISILAT I. DASAR TEORI I.1 Asidi-Alkalimetri Asidi-alkalimetri merupakan salah satu metode analisis titrimetri. Analisis titrimetri mengacu pada analisis kimia
Laporan Praktikum Kimia Dasar II. Standarisasi Larutan NaOH 0,1 M dan Penggunaannya Dalam Penentuan Kadar Asam Cuka Perdagangan.
 Laporan Praktikum Kimia Dasar II Standarisasi Larutan NaOH 0,1 M dan Penggunaannya Dalam Penentuan Kadar Asam Cuka Perdagangan Oleh: Kelompok : I (satu) Nama Nim Prodi : Ardinal : F1D113002 : Teknik Pertambangan
Laporan Praktikum Kimia Dasar II Standarisasi Larutan NaOH 0,1 M dan Penggunaannya Dalam Penentuan Kadar Asam Cuka Perdagangan Oleh: Kelompok : I (satu) Nama Nim Prodi : Ardinal : F1D113002 : Teknik Pertambangan
TITRASI DENGAN INDIKATOR GABUNGAN DAN DUA INDIKATOR
 TITRASI DENGAN INDIKATOR GABUNGAN DAN DUA INDIKATOR I. TUJUAN 1. Memahami prinsip kerja dari percobaan. 2. Menentukan konsentrasi dari NaOH dan Na 2 CO 3. 3. Mengetahui kegunaan dari titrasi dengan indikator
TITRASI DENGAN INDIKATOR GABUNGAN DAN DUA INDIKATOR I. TUJUAN 1. Memahami prinsip kerja dari percobaan. 2. Menentukan konsentrasi dari NaOH dan Na 2 CO 3. 3. Mengetahui kegunaan dari titrasi dengan indikator
BAB I PRAKTIKUM ASIDI AL-KALIMETRI
 BAB I PRAKTIKUM ASIDI AL-KALIMETRI I. TUJUAN a. Mahasiswa dapat menjelaskan proses titrasi asidi alkalimetri. b. Mahasiswa mampu menghitung konsentrasi sampel dengan metode asidi alkalimetri. II. DASAR
BAB I PRAKTIKUM ASIDI AL-KALIMETRI I. TUJUAN a. Mahasiswa dapat menjelaskan proses titrasi asidi alkalimetri. b. Mahasiswa mampu menghitung konsentrasi sampel dengan metode asidi alkalimetri. II. DASAR
LAPORAN PRAKTIKUM KIMIA DASAR I
 LAPORAN PRAKTIKUM KIMIA DASAR I NAMA KELOMPOK : MELVIA PERMATASARI (08121006013) MELANY AMDIRA (08121006027) ANIS ALAFIFAH (08121006029) PUTRI WULANDARI (08121006071) MUTIARA BELLA (08121006073) JURUSAN
LAPORAN PRAKTIKUM KIMIA DASAR I NAMA KELOMPOK : MELVIA PERMATASARI (08121006013) MELANY AMDIRA (08121006027) ANIS ALAFIFAH (08121006029) PUTRI WULANDARI (08121006071) MUTIARA BELLA (08121006073) JURUSAN
PERCOBAAN I PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA
 LAPORAN PRAKTIKUM KIMIA ANALITIK KI-2122 PERCOBAAN I PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA Nama Praktikan : Anggi Febrina NIM : 13010107 Kelompok : 5 (Shift Pagi) Tanggal
LAPORAN PRAKTIKUM KIMIA ANALITIK KI-2122 PERCOBAAN I PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA Nama Praktikan : Anggi Febrina NIM : 13010107 Kelompok : 5 (Shift Pagi) Tanggal
PENENTUAN KADAR ASAM ASETAT DALAM ASAM CUKA DENGAN ALKALIMETRI
 PENENTUAN KADAR ASAM ASETAT DALAM ASAM CUKA DENGAN ALKALIMETRI I. CAPAIAN PEMBELAJARAN Praktikan mampu menetapkan kadar CH3COOH (asam asetat) dan asam cuka (HCl) menggunakan prinsip reaksi asam-basa. II.
PENENTUAN KADAR ASAM ASETAT DALAM ASAM CUKA DENGAN ALKALIMETRI I. CAPAIAN PEMBELAJARAN Praktikan mampu menetapkan kadar CH3COOH (asam asetat) dan asam cuka (HCl) menggunakan prinsip reaksi asam-basa. II.
KIMIA ANALITIK TITRASI ASAM-BASA
 KIMIA ANALITIK TITRASI ASAM-BASA KIMIA ANALITIK 02 REGULER KELOMPOK 6 Disusun oleh: 1. Jang Jin Joo 1306399071 (11) 2. Robby Samuel 1306402204 (12) TEKNIK METALURGI DAN MATERIAL 2014 Pengertian Titrasi
KIMIA ANALITIK TITRASI ASAM-BASA KIMIA ANALITIK 02 REGULER KELOMPOK 6 Disusun oleh: 1. Jang Jin Joo 1306399071 (11) 2. Robby Samuel 1306402204 (12) TEKNIK METALURGI DAN MATERIAL 2014 Pengertian Titrasi
BAB I PENDAHULUAN A. Judul Percobaan B. Tujuan Percobaan
 BAB I PENDAHULUAN A. Judul Percobaan Penentuan kadar karbonat dan bikarbonat dalam larutan. B. Tujuan Percobaan Menyelidiki kadar karbonat dan bikarbonat dalam larutan secara asidimetri dengan menggunakan
BAB I PENDAHULUAN A. Judul Percobaan Penentuan kadar karbonat dan bikarbonat dalam larutan. B. Tujuan Percobaan Menyelidiki kadar karbonat dan bikarbonat dalam larutan secara asidimetri dengan menggunakan
PERCOBAAN I PEMBUATAN DAN PENENTUAN KONSENTRASI LARUTAN
 PERCOBAAN I PEMBUATAN DAN PENENTUAN KONSENTRASI LARUTAN I. TUJUAN PERCOBAAN Tujuan percobaan praktikum ini adalah agar praktikan dapat membuat larutan dengan konsentrasi tertentu, mengencerkan larutan,
PERCOBAAN I PEMBUATAN DAN PENENTUAN KONSENTRASI LARUTAN I. TUJUAN PERCOBAAN Tujuan percobaan praktikum ini adalah agar praktikan dapat membuat larutan dengan konsentrasi tertentu, mengencerkan larutan,
KIMIA DASAR PRINSIP TITRASI TITRASI (VOLUMETRI)
 KIMIA DASAR TITRASI (VOLUMETRI) Drs. Saeful Amin, M.Si., Apt. PRINSIP TITRASI Titrasi (volumetri) merupakan metode analisis kimia yang cepat, akurat dan sering digunakan untuk menentukan kadar suatu unsur
KIMIA DASAR TITRASI (VOLUMETRI) Drs. Saeful Amin, M.Si., Apt. PRINSIP TITRASI Titrasi (volumetri) merupakan metode analisis kimia yang cepat, akurat dan sering digunakan untuk menentukan kadar suatu unsur
LAPORAN PRAKTIKUM KIMIA FARMASI SEMESTER GANJIL TITRASI ASIDIMETRI-ALKALIMETRI. Tanggal Praktikum : 17 November 2017.
 LAPORAN PRAKTIKUM KIMIA FARMASI SEMESTER GANJIL 2017-2018 TITRASI ASIDIMETRI-ALKALIMETRI Hari / Jam Praktikum : Kamis/07.00-10.00 Tanggal Praktikum : 17 November 2017 Kelompok : 5 Asisten : 1. Jessica
LAPORAN PRAKTIKUM KIMIA FARMASI SEMESTER GANJIL 2017-2018 TITRASI ASIDIMETRI-ALKALIMETRI Hari / Jam Praktikum : Kamis/07.00-10.00 Tanggal Praktikum : 17 November 2017 Kelompok : 5 Asisten : 1. Jessica
PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA
 PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA 1 Tujuan Percobaan Tujuan dari percobaan ini adalah menentukan kadar natrium karbonat dan natrium hidrogen karbonat dengan titrasi
PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA 1 Tujuan Percobaan Tujuan dari percobaan ini adalah menentukan kadar natrium karbonat dan natrium hidrogen karbonat dengan titrasi
Haris Dianto Darwindra BAB V PEMBAHASAN
 BAB V PEMBAHASAN Titrasi merupakan suatu metoda untuk menentukan kadar suatu zat dengan menggunakan zat lain yang sudah diketahui konsentrasinya. Titrasi biasanya dibedakan berdasarkan jenis reaksi yang
BAB V PEMBAHASAN Titrasi merupakan suatu metoda untuk menentukan kadar suatu zat dengan menggunakan zat lain yang sudah diketahui konsentrasinya. Titrasi biasanya dibedakan berdasarkan jenis reaksi yang
Modul 1 Analisis Kualitatif 1
 Modul 1 Analisis Kualitatif 1 Indikator Alami I. Tujuan Percobaan 1. Mengidentifikasikan perubahan warna yang ditunjukkan indikator alam. 2. Mengetahui bagian tumbuhan yang dapat dijadikan indikator alam.
Modul 1 Analisis Kualitatif 1 Indikator Alami I. Tujuan Percobaan 1. Mengidentifikasikan perubahan warna yang ditunjukkan indikator alam. 2. Mengetahui bagian tumbuhan yang dapat dijadikan indikator alam.
LAPORAN PRAKTIKUM KIMIA FARMASI ASIDIMETRI DAN ALKALIMETRI. Senin, 9 November 2015 KELOMPOK IV Senin, Pukul WIB
 LAPORAN PRAKTIKUM KIMIA FARMASI ASIDIMETRI DAN ALKALIMETRI Senin, 9 November 2015 KELOMPOK IV Senin, Pukul 10.00 13.00 WIB Nama NPM Muhammad Naufal Mu tashim 260110150016 Puty Prianti Novira 260110150017
LAPORAN PRAKTIKUM KIMIA FARMASI ASIDIMETRI DAN ALKALIMETRI Senin, 9 November 2015 KELOMPOK IV Senin, Pukul 10.00 13.00 WIB Nama NPM Muhammad Naufal Mu tashim 260110150016 Puty Prianti Novira 260110150017
BERKAS SOAL BIDANG STUDI: KIMIA PRAKTIKUM MODUL I KOMPETISI SAINS MADRASAH NASIONAL 2012
 BERKAS SOAL BIDANG STUDI: KIMIA PRAKTIKUM MODUL I KOMPETISI SAINS MADRASAH NASIONAL 2012 Hal-0 Instruksi Pastikan bahwa nama dan kode peserta Anda sudah tertulis pada halaman pertama lembar soal dan lembar
BERKAS SOAL BIDANG STUDI: KIMIA PRAKTIKUM MODUL I KOMPETISI SAINS MADRASAH NASIONAL 2012 Hal-0 Instruksi Pastikan bahwa nama dan kode peserta Anda sudah tertulis pada halaman pertama lembar soal dan lembar
LAPORAN PRAKTIKUM KIMIA
 LAPORAN PRAKTIKUM KIMIA MENENTUKAN KADAR NaClO PADA PEMUTIH Disusun oleh : Latifah Suryaningrum (24 / XII IPA 1) SMA Negeri 1 Klaten Jl. Merbabu No. 13 Klaten 2012 / 2013 A. Tujuan Menentukan kadar NaClO
LAPORAN PRAKTIKUM KIMIA MENENTUKAN KADAR NaClO PADA PEMUTIH Disusun oleh : Latifah Suryaningrum (24 / XII IPA 1) SMA Negeri 1 Klaten Jl. Merbabu No. 13 Klaten 2012 / 2013 A. Tujuan Menentukan kadar NaClO
PENENTUAN KOMPOSISI MAGNESIUM HIDROKSIDA DAN ALUMINIUM HIDROKSIDA DALAM OBAT MAAG
 PENENTUAN KOMPOSISI MAGNESIUM HIDROKSIDA DAN ALUMINIUM HIDROKSIDA DALAM OBAT MAAG PENDAHULUAN Obat maag atau antasida adalah obat yang mengandung bahan-bahan yang efektif yang menetralkan asam dilambung.
PENENTUAN KOMPOSISI MAGNESIUM HIDROKSIDA DAN ALUMINIUM HIDROKSIDA DALAM OBAT MAAG PENDAHULUAN Obat maag atau antasida adalah obat yang mengandung bahan-bahan yang efektif yang menetralkan asam dilambung.
PRAKTIKUM II TITRASI ASAM BASA OLEH RONIADI SAGULANI 85AK14020
 PRAKTIKUM II TITRASI ASAM BASA OLEH RONIADI SAGULANI 85AK14020 PROGRAM STUDI D3 ANALISIS KESEHATAN STIKES BINA MANDIRI GORONTALO 2014 LAPORAN AKHIR PERCOBAAN II A. JUDUL : Titrasi Asam Basa B. TUJUAN Dengan
PRAKTIKUM II TITRASI ASAM BASA OLEH RONIADI SAGULANI 85AK14020 PROGRAM STUDI D3 ANALISIS KESEHATAN STIKES BINA MANDIRI GORONTALO 2014 LAPORAN AKHIR PERCOBAAN II A. JUDUL : Titrasi Asam Basa B. TUJUAN Dengan
Laporan Praktikum TITRASI KOMPLEKSOMETRI Standarisasi EDTA dengan CaCO3
 Laporan Praktikum TITRASI KOMPLEKSOMETRI Standarisasi EDTA dengan CaCO3 TITRASI KOMPLEKSOMETRI Standarisasi EDTA dengan CaCO3 I. Waktu / Tempat Praktikum : Rabu,15 Februari 2012 / Lab Kimia Jur. Analis
Laporan Praktikum TITRASI KOMPLEKSOMETRI Standarisasi EDTA dengan CaCO3 TITRASI KOMPLEKSOMETRI Standarisasi EDTA dengan CaCO3 I. Waktu / Tempat Praktikum : Rabu,15 Februari 2012 / Lab Kimia Jur. Analis
LOGO TEORI ASAM BASA
 LOGO TEORI ASAM BASA TIM DOSEN KIMIA DASAR FTP 2012 Beberapa ilmuan telah memberikan definisi tentang konsep asam basa Meskipun beberapa definisi terlihat kurang jelas dan berbeda satu sama lain, tetapi
LOGO TEORI ASAM BASA TIM DOSEN KIMIA DASAR FTP 2012 Beberapa ilmuan telah memberikan definisi tentang konsep asam basa Meskipun beberapa definisi terlihat kurang jelas dan berbeda satu sama lain, tetapi
LAPORAN PRAKTIKUM KIMIA MENENTUKAN KONSENTRASI LARUTAN H 2 SO 4 DAN KONSENTRASI LARUTAN CH 3 COOH DENGAN TITRASI ASAM BASA (ASIDI-ALKALIMETRI)
 LAPORAN PRAKTIKUM KIMIA MENENTUKAN KONSENTRASI LARUTAN H 2 SO 4 DAN KONSENTRASI LARUTAN CH 3 COOH DENGAN TITRASI ASAM BASA (ASIDI-ALKALIMETRI) Disusun Oleh : 1. Ela Bintang Bahari (XI IPA 4 / 03) 2. Alfian
LAPORAN PRAKTIKUM KIMIA MENENTUKAN KONSENTRASI LARUTAN H 2 SO 4 DAN KONSENTRASI LARUTAN CH 3 COOH DENGAN TITRASI ASAM BASA (ASIDI-ALKALIMETRI) Disusun Oleh : 1. Ela Bintang Bahari (XI IPA 4 / 03) 2. Alfian
kimia TITRASI ASAM BASA
 Kurikulum 2006/2013 2013 kimia K e l a s XI TITRASI ASAM BASA Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami definisi dan macam-macam titrasi.
Kurikulum 2006/2013 2013 kimia K e l a s XI TITRASI ASAM BASA Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami definisi dan macam-macam titrasi.
PENUNTUN PRAKTIKUM KIMIA DASAR II KI1201
 PENUNTUN PRAKTIKUM KIMIA DASAR II KI1201 Disusun Ulang Oleh: Dr. Deana Wahyuningrum Dr. Ihsanawati Dr. Irma Mulyani Dr. Mia Ledyastuti Dr. Rusnadi LABORATORIUM KIMIA DASAR PROGRAM TAHAP PERSIAPAN BERSAMA
PENUNTUN PRAKTIKUM KIMIA DASAR II KI1201 Disusun Ulang Oleh: Dr. Deana Wahyuningrum Dr. Ihsanawati Dr. Irma Mulyani Dr. Mia Ledyastuti Dr. Rusnadi LABORATORIUM KIMIA DASAR PROGRAM TAHAP PERSIAPAN BERSAMA
LAPORAN PRAKTIKUM KIMIA FISIK BASA
 LAPORAN PRAKTIKUM KIMIA FISIK MODUL PRAKTIKUM NAMA PEMBIMBING NAMA MAHASISWA : STANDARISASI LARUTAN ASAM DAN BASA : Drs. AGUSTINUS NGATIN, MT. : SIFA FUZI ALLAWIYAH TANGGAL PRAKTEK : 9 Oktober 2013 TANGGAL
LAPORAN PRAKTIKUM KIMIA FISIK MODUL PRAKTIKUM NAMA PEMBIMBING NAMA MAHASISWA : STANDARISASI LARUTAN ASAM DAN BASA : Drs. AGUSTINUS NGATIN, MT. : SIFA FUZI ALLAWIYAH TANGGAL PRAKTEK : 9 Oktober 2013 TANGGAL
BAB V METODOLOGI. 5.1 Alat yang digunakan: Tabel 3. Alat yang digunakan pada penelitian
 14 BAB V METODOLOGI 5.1 Alat yang digunakan: Tabel 3. Alat yang digunakan pada penelitian No. Nama Alat Jumlah 1. Oven 1 2. Hydraulic Press 1 3. Kain saring 4 4. Wadah kacang kenari ketika di oven 1 5.
14 BAB V METODOLOGI 5.1 Alat yang digunakan: Tabel 3. Alat yang digunakan pada penelitian No. Nama Alat Jumlah 1. Oven 1 2. Hydraulic Press 1 3. Kain saring 4 4. Wadah kacang kenari ketika di oven 1 5.
LARUTAN. Zat terlarut merupakan komponen yang jumlahnya sedikit, sedangkan pelarut adalah komponen yang terdapat dalam jumlah banyak.
 LARUTAN Larutan merupakan campuran yang homogen,yaitu campuran yang memiliki komposisi merata atau serba sama di seluruh bagian volumenya. Suatu larutan mengandung dua komponen atau lebih yang disebut
LARUTAN Larutan merupakan campuran yang homogen,yaitu campuran yang memiliki komposisi merata atau serba sama di seluruh bagian volumenya. Suatu larutan mengandung dua komponen atau lebih yang disebut
Praktikum Kimia Fisika II Hidrolisis Etil Asetat dalam Suasana Asam Lemah & Asam Kuat
 I. Judul Percobaan Hidrolisis Etil Asetat dalam Suasana Asam Lemah & dalam Suasana Asam Kuat II. Tanggal Percobaan Senin, 8 April 2013 pukul 11.00 14.00 WIB III. Tujuan Percobaan Menentukan orde reaksi
I. Judul Percobaan Hidrolisis Etil Asetat dalam Suasana Asam Lemah & dalam Suasana Asam Kuat II. Tanggal Percobaan Senin, 8 April 2013 pukul 11.00 14.00 WIB III. Tujuan Percobaan Menentukan orde reaksi
Penentuan Kesadahan Dalam Air
 Penentuan Kesadahan Dalam Air I. Tujuan 1. Dapat menentukan secara kualitatif dan kuantitatif kation (Ca²+,Mg²+) 2. Dapat membuat larutan an melakukan pengenceran II. Latar Belakang Teori Semua makhluk
Penentuan Kesadahan Dalam Air I. Tujuan 1. Dapat menentukan secara kualitatif dan kuantitatif kation (Ca²+,Mg²+) 2. Dapat membuat larutan an melakukan pengenceran II. Latar Belakang Teori Semua makhluk
Metode titrimetri dikenal juga sebagai metode volumetri
 Metode titrimetri dikenal juga sebagai metode volumetri? yaitu, merupakan metode analisis kuantitatif yang didasarkan pada prinsip pengukuran volume. 1 Macam Analisa Volumetri 1. Gasometri adalah volumetri
Metode titrimetri dikenal juga sebagai metode volumetri? yaitu, merupakan metode analisis kuantitatif yang didasarkan pada prinsip pengukuran volume. 1 Macam Analisa Volumetri 1. Gasometri adalah volumetri
LAPORAN PRAKTIKUM KIMIA DASAR. Percobaan 3 INDIKATOR DAN LARUTAN
 LAPORAN PRAKTIKUM KIMIA DASAR Percobaan 3 INDIKATOR DAN LARUTAN Disusun oleh Nama : Cinderi Maura Restu NPM : 10060312009 Shift / kelompok : 1 / 2 Tanggal Praktikum : 29 Oktober 2012 Tanggal Laporan :
LAPORAN PRAKTIKUM KIMIA DASAR Percobaan 3 INDIKATOR DAN LARUTAN Disusun oleh Nama : Cinderi Maura Restu NPM : 10060312009 Shift / kelompok : 1 / 2 Tanggal Praktikum : 29 Oktober 2012 Tanggal Laporan :
PENENTUAN KADAR CuSO 4. Dengan Titrasi Iodometri
 PENENTUAN KADAR CuSO 4 Dengan Titrasi Iodometri 22 April 2014 NURUL MU NISAH AWALIYAH 1112016200008 Kelompok 2 : 1. Widya Kusumaningrum (111201620000) 2. Ipa Ida Rosita (1112016200007) 3. Ummu Kalsum A.L
PENENTUAN KADAR CuSO 4 Dengan Titrasi Iodometri 22 April 2014 NURUL MU NISAH AWALIYAH 1112016200008 Kelompok 2 : 1. Widya Kusumaningrum (111201620000) 2. Ipa Ida Rosita (1112016200007) 3. Ummu Kalsum A.L
LAPORAN LENGKAP PRAKTIKUM KIMIA ANORGANIK PERCOBAAN 3 PENENTUAN BILANGAN KOORDINAI KOMPLEKS TEMBAGA (II)
 LAPORAN LENGKAP PRAKTIKUM KIMIA ANORGANIK PERCOBAAN 3 PENENTUAN BILANGAN KOORDINAI KOMPLEKS TEMBAGA (II) OLEH : NAMA : IMENG NIM: ACC 109 011 KELOMPOK : 2 ( DUA ) HARI, TANGGAL : RABU, 8 JUNI 2011 ASISTEN
LAPORAN LENGKAP PRAKTIKUM KIMIA ANORGANIK PERCOBAAN 3 PENENTUAN BILANGAN KOORDINAI KOMPLEKS TEMBAGA (II) OLEH : NAMA : IMENG NIM: ACC 109 011 KELOMPOK : 2 ( DUA ) HARI, TANGGAL : RABU, 8 JUNI 2011 ASISTEN
UJIAN PRAKTIKUM KI2121 DASAR-DASAR KIMIA ANALITIK PENENTUAN KADAR BIKARBONAT DALAM SODA KUE
 UJIAN PRAKTIKUM KI2121 DASAR-DASAR KIMIA ANALITIK PENENTUAN KADAR BIKARBONAT DALAM SODA KUE Kelompok : Kelompok 5 Tanggal Persentasi : 14 November 2016 Tanggal Percobaan : 21 November 2016 Sahlillah Dwi
UJIAN PRAKTIKUM KI2121 DASAR-DASAR KIMIA ANALITIK PENENTUAN KADAR BIKARBONAT DALAM SODA KUE Kelompok : Kelompok 5 Tanggal Persentasi : 14 November 2016 Tanggal Percobaan : 21 November 2016 Sahlillah Dwi
BAB V METODOLOGI. Pada tahap ini, dilakukan pengupasan kulit biji dibersihkan, penghancuran biji karet kemudian
 BAB V METODOLOGI Penelitian ini akan dilakukan 2 tahap, yaitu : Tahap I : Tahap perlakuan awal (pretreatment step) Pada tahap ini, dilakukan pengupasan kulit biji dibersihkan, penghancuran biji karet kemudian
BAB V METODOLOGI Penelitian ini akan dilakukan 2 tahap, yaitu : Tahap I : Tahap perlakuan awal (pretreatment step) Pada tahap ini, dilakukan pengupasan kulit biji dibersihkan, penghancuran biji karet kemudian
LAPORAN PRAKTIKUM KIMIA DASAR II PERCOBAAN II REAKSI ASAM BASA : OSU OHEOPUTRA. H STAMBUK : A1C : PENDIDIKAN MIPA
 LAPORAN PRAKTIKUM KIMIA DASAR II PERCOBAAN II REAKSI ASAM BASA NAMA : OSU OHEOPUTRA. H STAMBUK : A1C4 07 017 KELOMPOK PROGRAM STUDI JURUSAN : II : PENDIDIKAN KIMIA : PENDIDIKAN MIPA ASISTEN PEMBIMBING
LAPORAN PRAKTIKUM KIMIA DASAR II PERCOBAAN II REAKSI ASAM BASA NAMA : OSU OHEOPUTRA. H STAMBUK : A1C4 07 017 KELOMPOK PROGRAM STUDI JURUSAN : II : PENDIDIKAN KIMIA : PENDIDIKAN MIPA ASISTEN PEMBIMBING
Metodologi Penelitian
 16 Bab III Metodologi Penelitian Penelitian dilakukan dengan menggunakan metode titrasi redoks dengan menggunakan beberapa oksidator (K 2 Cr 2 O 7, KMnO 4 dan KBrO 3 ) dengan konsentrasi masing-masing
16 Bab III Metodologi Penelitian Penelitian dilakukan dengan menggunakan metode titrasi redoks dengan menggunakan beberapa oksidator (K 2 Cr 2 O 7, KMnO 4 dan KBrO 3 ) dengan konsentrasi masing-masing
Titrasi Volumetri. Modul 1 PENDAHULUAN
 Modul 1 Titrasi Volumetri Dr. Anna Permanasari, M.Si. K PENDAHULUAN egiatan praktikum ini dimaksudkan untuk melatih keterampilan dasar Anda dalam melakukan pekerjaan laboratorium, melatih Anda dalam bekerja
Modul 1 Titrasi Volumetri Dr. Anna Permanasari, M.Si. K PENDAHULUAN egiatan praktikum ini dimaksudkan untuk melatih keterampilan dasar Anda dalam melakukan pekerjaan laboratorium, melatih Anda dalam bekerja
Penetapan Kadar Asam Salisilat Secara Alkalimetri LAPORAN PRAKTIKUM KIMIA FARMASI II PENETAPAN KADAR ASAM SALISILAT (C7H6O3) SECARA ALKALIMETRI
 Penetapan Kadar Asam Salisilat Secara Alkalimetri PENETAPAN KADAR ASAM SALISILAT (C7H6O3) SECARA ALKALIMETRI Tanggal Praktikum Kamis, 21 February 2012 D-3 FARMASI POLITEKNIK KESEHATAN TNI AU CIUMBULEUIT
Penetapan Kadar Asam Salisilat Secara Alkalimetri PENETAPAN KADAR ASAM SALISILAT (C7H6O3) SECARA ALKALIMETRI Tanggal Praktikum Kamis, 21 February 2012 D-3 FARMASI POLITEKNIK KESEHATAN TNI AU CIUMBULEUIT
KIMIA ANALISIS ASIDI ALKALIMETRI
 KIMIA ANALISIS LAPORAN PRAKTIKUM ASIDI ALKALIMETRI Disusun oleh: Amalia Ulfa Dyah Ayu Wulandari Herlina Agustyani Nurmaningtyas Fitri Rahmawati Dwi Justitia Aprilia (G1F011001) (G1F011003) (G1F011005)
KIMIA ANALISIS LAPORAN PRAKTIKUM ASIDI ALKALIMETRI Disusun oleh: Amalia Ulfa Dyah Ayu Wulandari Herlina Agustyani Nurmaningtyas Fitri Rahmawati Dwi Justitia Aprilia (G1F011001) (G1F011003) (G1F011005)
Laporan Praktikum Kimia Analitik II. Koefisien Distribusi Iod
 Laporan Praktikum Kimia Analitik II Koefisien Distribusi Iod Oleh : 1. Fitri Aprilia 093194205 2. Wilda Ulin Nuha 093194211 3. Endah Rohmawati 093194216 Universitas Negeri Surabaya Fakultas Matematika
Laporan Praktikum Kimia Analitik II Koefisien Distribusi Iod Oleh : 1. Fitri Aprilia 093194205 2. Wilda Ulin Nuha 093194211 3. Endah Rohmawati 093194216 Universitas Negeri Surabaya Fakultas Matematika
JURNAL PRAKTIKUM. KIMIA ANALITIK II Titrasi Permanganometri. Selasa, 10 Mei Disusun Oleh : YASA ESA YASINTA
 JURNAL PRAKTIKUM KIMIA ANALITIK II Titrasi Permanganometri Selasa, 10 Mei 2014 Disusun Oleh : YASA ESA YASINTA 1112016200062 Kelompok : Ma wah shofwah Millah hanifah Savira aulia Widya fitriani PROGRAM
JURNAL PRAKTIKUM KIMIA ANALITIK II Titrasi Permanganometri Selasa, 10 Mei 2014 Disusun Oleh : YASA ESA YASINTA 1112016200062 Kelompok : Ma wah shofwah Millah hanifah Savira aulia Widya fitriani PROGRAM
LAPORAN PRAKTIKUM KIMIA ANALITIK I PERCOBAAN VI TITRASI REDOKS
 LAPORAN PRAKTIKUM KIMIA ANALITIK I PERCOBAAN VI TITRASI REDOKS O L E H: NAMA : HABRIN KIFLI HS STAMBUK : F1C1 15 034 KELOMPOK : V (LIMA) ASISTEN : SARTINI, S.Si LABORATORIUM KIMIA ANALITIK FAKULTAS MATEMATIKA
LAPORAN PRAKTIKUM KIMIA ANALITIK I PERCOBAAN VI TITRASI REDOKS O L E H: NAMA : HABRIN KIFLI HS STAMBUK : F1C1 15 034 KELOMPOK : V (LIMA) ASISTEN : SARTINI, S.Si LABORATORIUM KIMIA ANALITIK FAKULTAS MATEMATIKA
Laporan Praktikum Kimia ~Titrasi asam basa~
 Laporan Praktikum Kimia ~Titrasi asam basa~ -Menentukan konsentrasi NaOH dengan HCl 0,1 M- Latifa Dinna Prayudipta XI IPA 1 SMAN 3 TANGERANG SELATAN TAHUN AJARAN 2009/2010 Laporan praktikum kimia -titrasi
Laporan Praktikum Kimia ~Titrasi asam basa~ -Menentukan konsentrasi NaOH dengan HCl 0,1 M- Latifa Dinna Prayudipta XI IPA 1 SMAN 3 TANGERANG SELATAN TAHUN AJARAN 2009/2010 Laporan praktikum kimia -titrasi
TUGAS KIMIA SMA NEGERI 1 BAJAWA TITRASI ASAM BASA. Nama : Kelas. Disusun oleh:
 TUGAS KIMIA TITRASI ASAM BASA Disusun oleh: Nama : Kelas : SMA NEGERI 1 BAJAWA 2015 TITRASI ASAM BASA 1. Prinsip Dasar Titrasi netralisasi adalah titrasi yang didasarkan pada reaksi antara suatu asam dengan
TUGAS KIMIA TITRASI ASAM BASA Disusun oleh: Nama : Kelas : SMA NEGERI 1 BAJAWA 2015 TITRASI ASAM BASA 1. Prinsip Dasar Titrasi netralisasi adalah titrasi yang didasarkan pada reaksi antara suatu asam dengan
BAB IV. HASIL PENGAMATAN dan PERHITUNGAN
 BAB IV HASIL PENGAMATAN dan PERHITUNGAN A. HASIL PENGAMATAN 1. Standarisasi KMnO 4 terhadap H 2 C 2 O 4 0.1 N Kelompok Vol. H 2 C 2 O 4 Vol. KMnO 4 7 10 ml 10.3 ml 8 10 ml 10.8 ml 9 10 ml 10.4 ml 10 10
BAB IV HASIL PENGAMATAN dan PERHITUNGAN A. HASIL PENGAMATAN 1. Standarisasi KMnO 4 terhadap H 2 C 2 O 4 0.1 N Kelompok Vol. H 2 C 2 O 4 Vol. KMnO 4 7 10 ml 10.3 ml 8 10 ml 10.8 ml 9 10 ml 10.4 ml 10 10
LAPORAN PRAKTIKUM KIMIA FARMASI ANALISIS II TURUNAN ASAM HIDROKSI BENZOAT
 LAPORAN PRAKTIKUM KIMIA FARMASI ANALISIS II TURUNAN ASAM HIDROKSI BENZOAT KELOMPOK : 10 DESI AGNI MUTIA 31110012 FAUZY RODIAH 31110019 GANJAR TAUFIK F. 31110022 FARMASI 3A PRORGAM STUDI S1 FARMASI STIKes
LAPORAN PRAKTIKUM KIMIA FARMASI ANALISIS II TURUNAN ASAM HIDROKSI BENZOAT KELOMPOK : 10 DESI AGNI MUTIA 31110012 FAUZY RODIAH 31110019 GANJAR TAUFIK F. 31110022 FARMASI 3A PRORGAM STUDI S1 FARMASI STIKes
Bab VIII Reaksi Penetralan dan Titrasi Asam-Basa
 Bab VIII Reaksi Penetralan dan Titrasi Asam-Basa Sumber: James Mapple, Chemistry an Enquiry-Based Approach Pengukuran ph selama titrasi akan lebih akurat dengan menggunakan alat ph-meter. TUJUAN PEMBELAJARAN
Bab VIII Reaksi Penetralan dan Titrasi Asam-Basa Sumber: James Mapple, Chemistry an Enquiry-Based Approach Pengukuran ph selama titrasi akan lebih akurat dengan menggunakan alat ph-meter. TUJUAN PEMBELAJARAN
 VISIT MY WEBSITE : KLIK AJA LINKNYA SOB http://dionlegionis.blogspot.com/search/label/education%20mipa http://dionlegionis.blogspot.com/2015/03/klasifikasi-kodok-beranak-darisulawesi.html http://dionlegionis.blogspot.com/2015/03/download-pdf-statistika-datatunggal.html
VISIT MY WEBSITE : KLIK AJA LINKNYA SOB http://dionlegionis.blogspot.com/search/label/education%20mipa http://dionlegionis.blogspot.com/2015/03/klasifikasi-kodok-beranak-darisulawesi.html http://dionlegionis.blogspot.com/2015/03/download-pdf-statistika-datatunggal.html
Blanching. Pembuangan sisa kulit ari
 BAB V METODOLOGI 5.1 Pengujian Kinerja Alat Press Hidrolik 5.1.1 Prosedur Pembuatan Minyak Kedelai Proses pendahuluan Blanching Pengeringan Pembuangan sisa kulit ari pengepresan 5.1.2 Alat yang Digunakan
BAB V METODOLOGI 5.1 Pengujian Kinerja Alat Press Hidrolik 5.1.1 Prosedur Pembuatan Minyak Kedelai Proses pendahuluan Blanching Pengeringan Pembuangan sisa kulit ari pengepresan 5.1.2 Alat yang Digunakan
Jurnal Teknik Kimia No. 2, Vol. 19, April 2013 Page 1
 Jln. Raya Palembang Prabumulih Km. 32 Inderalaya gan Ilir (I) 30662 ABSTRAK Asidimetri adalah analisa titrimetri yang menggunakan asam kuat sebagai titrannya dan sebagai analitnya adalah basa atau senyawa
Jln. Raya Palembang Prabumulih Km. 32 Inderalaya gan Ilir (I) 30662 ABSTRAK Asidimetri adalah analisa titrimetri yang menggunakan asam kuat sebagai titrannya dan sebagai analitnya adalah basa atau senyawa
Metodologi Penelitian
 Bab III Metodologi Penelitian Pembuatan larutan buffer menggunakan metode pencampuran antara asam lemah dengan basa konjugasinya. Selanjutnya larutan buffer yang sudah dibuat diuji kemampuannya dalam mempertahankan
Bab III Metodologi Penelitian Pembuatan larutan buffer menggunakan metode pencampuran antara asam lemah dengan basa konjugasinya. Selanjutnya larutan buffer yang sudah dibuat diuji kemampuannya dalam mempertahankan
TITRASI KOMPLEKSOMETRI
 TITRASI KOMPLEKSOMETRI I. TUJUAN a. Menstandarisasi EDTA dengan larutan ZnSO 4 b. Menentukan konsentrasi larutan Ni 2+ c. Memahami prinsip titrasi kompleksometri II. TEORI Titrasi kompleksometri adalah
TITRASI KOMPLEKSOMETRI I. TUJUAN a. Menstandarisasi EDTA dengan larutan ZnSO 4 b. Menentukan konsentrasi larutan Ni 2+ c. Memahami prinsip titrasi kompleksometri II. TEORI Titrasi kompleksometri adalah
BAB IV HASIL PENELITIAN DAN PEMBAHASAN
 BAB IV HASIL PENELITIAN DAN PEMBAHASAN 4.1 Hasil Penelitian 4.1.1 Keadaan Lokasi Pengambilan Sampel Sampel yang digunakan adalah sampel bermerek dan tidak bermerek yang diambil dibeberapa tempat pasar
BAB IV HASIL PENELITIAN DAN PEMBAHASAN 4.1 Hasil Penelitian 4.1.1 Keadaan Lokasi Pengambilan Sampel Sampel yang digunakan adalah sampel bermerek dan tidak bermerek yang diambil dibeberapa tempat pasar
Dikenal : - Asidimetri : zat baku asam - Alkalimetri : zat baku basa DASAR : Reaksi penetralan Asam + Basa - hidrolisis - buffer - hal lain ttg lart
 Dikenal : - Asidimetri : zat baku asam - Alkalimetri : zat baku basa DASAR : Reaksi penetralan Asam + Basa - hidrolisis - buffer - hal lain ttg lart a. AK + BK ph = 7 B. AK + BL ph < 7 C. AL + BK ph >
Dikenal : - Asidimetri : zat baku asam - Alkalimetri : zat baku basa DASAR : Reaksi penetralan Asam + Basa - hidrolisis - buffer - hal lain ttg lart a. AK + BK ph = 7 B. AK + BL ph < 7 C. AL + BK ph >
BAB V METODOLOGI. Gambar 6. Pembuatan Minyak wijen
 18 BAB V METODOLOGI 5.1 Pengujian Kinerja Alat Press Hidrolik 5.1.1 Prosedur Pembuatan Minyak Wijen Biji Wijen Pembersihan Biji Wijen Pengovenan Pengepresan Pemisahan Minyak biji wijen Bungkil biji wijen
18 BAB V METODOLOGI 5.1 Pengujian Kinerja Alat Press Hidrolik 5.1.1 Prosedur Pembuatan Minyak Wijen Biji Wijen Pembersihan Biji Wijen Pengovenan Pengepresan Pemisahan Minyak biji wijen Bungkil biji wijen
BAB I PENDAHULUAN A. Judul percobaan B. Tujuan praktikum
 BAB I PENDAHULUAN A. Judul percobaan Pengenceran Suatu Larutan B. Tujuan praktikum Melatih menggunakan labu ukur di dalam membuat pengenceran atau suatu larutan. 1 BAB II METODE A. Alat dan Bahan Alat:
BAB I PENDAHULUAN A. Judul percobaan Pengenceran Suatu Larutan B. Tujuan praktikum Melatih menggunakan labu ukur di dalam membuat pengenceran atau suatu larutan. 1 BAB II METODE A. Alat dan Bahan Alat:
2. Eveline Fauziah. 3. Fadil Hardian. 4. Fajar Nugraha
 Modul Praktikum Nama Pembimbing Nama Mahasiswa : Kimia Fisik : Bapak Drs.Budi Santoso, Apt.MT : 1. Azka Muhammad Syahida 2. Eveline Fauziah 3. Fadil Hardian 4. Fajar Nugraha Tanggal Praktek : 21 Semptember
Modul Praktikum Nama Pembimbing Nama Mahasiswa : Kimia Fisik : Bapak Drs.Budi Santoso, Apt.MT : 1. Azka Muhammad Syahida 2. Eveline Fauziah 3. Fadil Hardian 4. Fajar Nugraha Tanggal Praktek : 21 Semptember
LAPORAN PRAKTIKUM KIMIA ANALITIK DASAR PENENTUAN KADAR NIKEL SECARA GRAVIMETRI. Pembimbing : Dra. Ari Marlina M,Si. Oleh.
 LAPORAN PRAKTIKUM KIMIA ANALITIK DASAR PENENTUAN KADAR NIKEL SECARA GRAVIMETRI Pembimbing : Dra. Ari Marlina M,Si Oleh Kelompok V Indra Afiando NIM 111431014 Iryanti Triana NIM 111431015 Lita Ayu Listiani
LAPORAN PRAKTIKUM KIMIA ANALITIK DASAR PENENTUAN KADAR NIKEL SECARA GRAVIMETRI Pembimbing : Dra. Ari Marlina M,Si Oleh Kelompok V Indra Afiando NIM 111431014 Iryanti Triana NIM 111431015 Lita Ayu Listiani
LAPORAN PRAKTIKUM KIMIA PEMISAHAN PERCOBAAN 1 EKSTRAKSI PELARUT
 LAPORAN PRAKTIKUM KIMIA PEMISAHAN PERCOBAAN 1 EKSTRAKSI PELARUT NAMA NIM KELOMPOK ASISTEN : REGINA ZERUYA : J1B110003 : 1 (SATU) : SUSI WAHYUNI PROGRAM STUDI S-1 KIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN
LAPORAN PRAKTIKUM KIMIA PEMISAHAN PERCOBAAN 1 EKSTRAKSI PELARUT NAMA NIM KELOMPOK ASISTEN : REGINA ZERUYA : J1B110003 : 1 (SATU) : SUSI WAHYUNI PROGRAM STUDI S-1 KIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN
MATERI KIMIA KELAS XI SEMESTER 2 Tinggalkan Balasan
 MATERI KIMIA KELAS XI SEMESTER 2 Tinggalkan Balasan A. Pengertian Asam Basa Asam dan basa sudah dikenal sejak zaman dulu. Istilah asam (acid) berasal dari bahasa Latin acetum yang berarti cuka. Istilah
MATERI KIMIA KELAS XI SEMESTER 2 Tinggalkan Balasan A. Pengertian Asam Basa Asam dan basa sudah dikenal sejak zaman dulu. Istilah asam (acid) berasal dari bahasa Latin acetum yang berarti cuka. Istilah
LAPORAN PRAKTIKUM KIMIA ANALITIK 2 PENENTUAN KADAR KLORIDA. Senin, 21 April Disusun Oleh: MA WAH SHOFWAH KELOMPOK 1
 LAPORAN PRAKTIKUM KIMIA ANALITIK 2 PENENTUAN KADAR KLORIDA Senin, 21 April 2014 Disusun Oleh: MA WAH SHOFWAH 1112016200040 KELOMPOK 1 MILLAH HANIFAH (1112016200073) YASA ESA YASINTA (1112016200062) WIDYA
LAPORAN PRAKTIKUM KIMIA ANALITIK 2 PENENTUAN KADAR KLORIDA Senin, 21 April 2014 Disusun Oleh: MA WAH SHOFWAH 1112016200040 KELOMPOK 1 MILLAH HANIFAH (1112016200073) YASA ESA YASINTA (1112016200062) WIDYA
dimana hasilnya dalam bentuk jumlah atau bilangan kadar.
 VOLUMETRI I Drs Kusumo Hariyadi Apt MS. Analisa Kimia dibagi 2 bagian : 1. Analisa Kualitatif ( analisa jenis) bertujuan mencari adanya unsur / senyawa dalam suatu sampel 2. Analisa Kuantitatif (analisa
VOLUMETRI I Drs Kusumo Hariyadi Apt MS. Analisa Kimia dibagi 2 bagian : 1. Analisa Kualitatif ( analisa jenis) bertujuan mencari adanya unsur / senyawa dalam suatu sampel 2. Analisa Kuantitatif (analisa
BAB III METODOLOGI PENELITIAN. Ruang lingkup penelitian ini adalah Ilmu Kimia Analisis.
 BAB III METODOLOGI PENELITIAN 3.1 Ruang Lingkup Penelitian Ruang lingkup penelitian ini adalah Ilmu Kimia Analisis. 3.2 Lokasi dan Waktu Penelitian Penelitian ini telah dilakukan pada tanggal 18 hingga
BAB III METODOLOGI PENELITIAN 3.1 Ruang Lingkup Penelitian Ruang lingkup penelitian ini adalah Ilmu Kimia Analisis. 3.2 Lokasi dan Waktu Penelitian Penelitian ini telah dilakukan pada tanggal 18 hingga
LAPORAN PRAKTIKUM KIMIA FISIKA II PENENTUAN KADAR KOEFISIEN DISTRIBUSI SELASA, 22 MEI 2014
 LAPORAN PRAKTIKUM KIMIA FISIKA II PENENTUAN KADAR KOEFISIEN DISTRIBUSI SELASA, 22 MEI 2014 Disusun oleh : Fika Rakhmalinda (1112016200003) Fikri Sholihah (1112016200028 ) Naryanto (1112016200018 ) PROGRAM
LAPORAN PRAKTIKUM KIMIA FISIKA II PENENTUAN KADAR KOEFISIEN DISTRIBUSI SELASA, 22 MEI 2014 Disusun oleh : Fika Rakhmalinda (1112016200003) Fikri Sholihah (1112016200028 ) Naryanto (1112016200018 ) PROGRAM
Modul 3 Ujian Praktikum. KI2121 Dasar Dasar Kimia Analitik PENENTUAN KADAR TEMBAGA DALAM KAWAT TEMBAGA
 Modul 3 Ujian Praktikum KI2121 Dasar Dasar Kimia Analitik PENENTUAN KADAR TEMBAGA DALAM KAWAT TEMBAGA Disusun oleh: Sandya Yustitia 10515050 Fritz Ferdinand 10515059 Maulinda Kusumawardani 10515061 Muhammad
Modul 3 Ujian Praktikum KI2121 Dasar Dasar Kimia Analitik PENENTUAN KADAR TEMBAGA DALAM KAWAT TEMBAGA Disusun oleh: Sandya Yustitia 10515050 Fritz Ferdinand 10515059 Maulinda Kusumawardani 10515061 Muhammad
TITRASI IODOMETRI. Siti Masitoh. M. Ikhwan Fillah, Indah Desi Permana, Ira Nurpialawati PROGRAM STUDI PENDIDIKAN KIMIA
 TITRASI IODOMETRI Siti Masitoh 1112016200006 M. Ikhwan Fillah, Indah Desi Permana, Ira Nurpialawati PROGRAM STUDI PENDIDIKAN KIMIA JURUSAN ILMU PENDIDIKAN ILMU PENGETAHUAN ALAM FAKULTAS ILMU TARBIYAH DAN
TITRASI IODOMETRI Siti Masitoh 1112016200006 M. Ikhwan Fillah, Indah Desi Permana, Ira Nurpialawati PROGRAM STUDI PENDIDIKAN KIMIA JURUSAN ILMU PENDIDIKAN ILMU PENGETAHUAN ALAM FAKULTAS ILMU TARBIYAH DAN
BAB III METODOLOGI PENELITIAN. Alur penelitian ini seperti ditunjukkan pada diagram alir di bawah ini:
 BAB III METODOLOGI PENELITIAN 3.1 Desain Penelitian Alur penelitian ini seperti ditunjukkan pada diagram alir di bawah ini: Gambar 3.1 Diagram alir penelitian 22 23 3.2 Metode Penelitian Penelitian ini
BAB III METODOLOGI PENELITIAN 3.1 Desain Penelitian Alur penelitian ini seperti ditunjukkan pada diagram alir di bawah ini: Gambar 3.1 Diagram alir penelitian 22 23 3.2 Metode Penelitian Penelitian ini
ASAM DAN BASA. Adelya Desi Kurniawati, STP., MP., M.Sc.
 ASAM DAN BASA Adelya Desi Kurniawati, STP., MP., M.Sc. Tujuan Pembelajaran 1.Mahasiswa memahami konsep dasar asam dan basa 2.Mahasiswa mampu mendefinisikan dan membedakan sifat-sifat asam dan basa 3.Mahasiswa
ASAM DAN BASA Adelya Desi Kurniawati, STP., MP., M.Sc. Tujuan Pembelajaran 1.Mahasiswa memahami konsep dasar asam dan basa 2.Mahasiswa mampu mendefinisikan dan membedakan sifat-sifat asam dan basa 3.Mahasiswa
LAPORAN PRAKTIKUM LABORATORIUM LINGKUNGAN PERCOBAAN 2 ASIDI ALKALINITAS
 LAPORAN PRAKTIKUM LABORATORIUM LINGKUNGAN PERCOBAAN 2 ASIDI ALKALINITAS OLEH: NAMA : AULIA RAHMA H1E113007 LUTHFI NUR RAHMAN H1E113029 NASRULLAH AKBAR M. H1E113219 KELOMPOK : XV (LIMA BELAS) ASISTEN :
LAPORAN PRAKTIKUM LABORATORIUM LINGKUNGAN PERCOBAAN 2 ASIDI ALKALINITAS OLEH: NAMA : AULIA RAHMA H1E113007 LUTHFI NUR RAHMAN H1E113029 NASRULLAH AKBAR M. H1E113219 KELOMPOK : XV (LIMA BELAS) ASISTEN :
III. METODOLOGI PENELITIAN. Penelitian ini dilaksanakan pada bulan Agustus sampai dengan bulan Oktober
 24 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan Agustus sampai dengan bulan Oktober 2011 di Laboratorium Biomassa Jurusan Kimia Fakultas Matematika dan
24 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan Agustus sampai dengan bulan Oktober 2011 di Laboratorium Biomassa Jurusan Kimia Fakultas Matematika dan
PRAKTIKUM KIMIA ANALITIK II
 PRAKTIKUM KIMIA ANALITIK II PENENTUAN KADAR KLORIDA Selasa, 1 April 2014 EKA NOVIANA NINDI ASTUTY 1112016200016 PROGRAM STUDI PENDIDIKAN KIMIA JURUSAN PEDIDIKAN ILMU PENGETAHUAN ALAM FAKULTAS ILMU TARBIYAH
PRAKTIKUM KIMIA ANALITIK II PENENTUAN KADAR KLORIDA Selasa, 1 April 2014 EKA NOVIANA NINDI ASTUTY 1112016200016 PROGRAM STUDI PENDIDIKAN KIMIA JURUSAN PEDIDIKAN ILMU PENGETAHUAN ALAM FAKULTAS ILMU TARBIYAH
BAB III ALAT, BAHAN, DAN CARA KERJA. Penelitian ini dilakukan di Laboratorium Kimia Farmasi Kuantitatif
 BAB III ALAT, BAHAN, DAN CARA KERJA Penelitian ini dilakukan di Laboratorium Kimia Farmasi Kuantitatif Departemen Farmasi FMIPA UI, dalam kurun waktu Februari 2008 hingga Mei 2008. A. ALAT 1. Kromatografi
BAB III ALAT, BAHAN, DAN CARA KERJA Penelitian ini dilakukan di Laboratorium Kimia Farmasi Kuantitatif Departemen Farmasi FMIPA UI, dalam kurun waktu Februari 2008 hingga Mei 2008. A. ALAT 1. Kromatografi
Standarisasi Larutan
 Standarisasi Larutan Kimia Analitik Kimia analitik: Cabang ilmu kimia yg bertugas mengidentifikasi zat, memisahkannya serta menguraikannya dalam komponenkomponen, menentukan jenis serta jumlahnya. Kimia
Standarisasi Larutan Kimia Analitik Kimia analitik: Cabang ilmu kimia yg bertugas mengidentifikasi zat, memisahkannya serta menguraikannya dalam komponenkomponen, menentukan jenis serta jumlahnya. Kimia
BAB III METODOLOGI PENELITIAN
 digilib.uns.ac.id BAB III METODOLOGI PENELITIAN A. METODE PENELITIAN Penelitian ini dilakukan dengan menggunakan metode penelitian eksperimental. Sepuluh sampel mie basah diuji secara kualitatif untuk
digilib.uns.ac.id BAB III METODOLOGI PENELITIAN A. METODE PENELITIAN Penelitian ini dilakukan dengan menggunakan metode penelitian eksperimental. Sepuluh sampel mie basah diuji secara kualitatif untuk
HASIL KALI KELARUTAN (Ksp)
 LAPORAN PRAKTIKUM KIMIA FISIKA HASIL KALI KELARUTAN (Ksp) NAMA : YUSI ANDA RIZKY NIM : H311 08 003 KELOMPOK : II (DUA) HARI/TGL PERC. : SENIN/08 MARET 2010 ASISTEN : FITRI JUNIANTI LABORATORIUM KIMIA FISIKA
LAPORAN PRAKTIKUM KIMIA FISIKA HASIL KALI KELARUTAN (Ksp) NAMA : YUSI ANDA RIZKY NIM : H311 08 003 KELOMPOK : II (DUA) HARI/TGL PERC. : SENIN/08 MARET 2010 ASISTEN : FITRI JUNIANTI LABORATORIUM KIMIA FISIKA
III. METODOLOGI. 1. Analisis Kualitatif Natrium Benzoat (AOAC B 1999) Persiapan Sampel
 III. METODOLOGI A. BAHAN DAN ALAT Bahan-bahan yang digunakan dalam penelitian ini adalah saus sambal dan minuman dalam kemasan untuk analisis kualitatif, sedangkan untuk analisis kuantitatif digunakan
III. METODOLOGI A. BAHAN DAN ALAT Bahan-bahan yang digunakan dalam penelitian ini adalah saus sambal dan minuman dalam kemasan untuk analisis kualitatif, sedangkan untuk analisis kuantitatif digunakan
CH 3 COOH (aq) + NaOH (aq) CH 3 COONa (aq) + H 2 O (l)
 PENGEMBANGAN PROSEDUR PENENTUAN KADAR ASAM CUKA SECARA TITRASI ASAM BASA DENGAN BERBAGAI INDIKATOR ALAMI (SEBAGAI ALTERNATIF PRAKTIKUM TITRASI ASAM BASA DI SMA) Das Salirawati, M.Si dan Regina Tutik Padmaningrum,
PENGEMBANGAN PROSEDUR PENENTUAN KADAR ASAM CUKA SECARA TITRASI ASAM BASA DENGAN BERBAGAI INDIKATOR ALAMI (SEBAGAI ALTERNATIF PRAKTIKUM TITRASI ASAM BASA DI SMA) Das Salirawati, M.Si dan Regina Tutik Padmaningrum,
BAB III METODE. Penelitian ini dilakukan di Laboratorium Minyak Atsiri dan Bahan
 BAB III METODE 3.1 Tempat dan Waktu Penelitian ini dilakukan di Laboratorium Minyak Atsiri dan Bahan Penyegar, Unit Pelayanan Terpadu Pengunjian dan Sertifikasi Mutu Barang (UPT. PSMB) Medan yang bertempat
BAB III METODE 3.1 Tempat dan Waktu Penelitian ini dilakukan di Laboratorium Minyak Atsiri dan Bahan Penyegar, Unit Pelayanan Terpadu Pengunjian dan Sertifikasi Mutu Barang (UPT. PSMB) Medan yang bertempat
BAB IV HASIL PENGAMATAN DAN PERHITUNGAN
 BAB IV HASIL PENGAMATAN DAN PERHITUNGAN A. HASIL PENGAMATAN 1. Standarisasi AgNO 3 terhadap NaCl 0.1 N (Cara Mohr) Kelompok Vol. NaCl Vol. AgNO 3 7 10 ml 4 ml 8 10 ml 4.2 ml 9 10 ml 4.2 ml 10 10 ml 4.3
BAB IV HASIL PENGAMATAN DAN PERHITUNGAN A. HASIL PENGAMATAN 1. Standarisasi AgNO 3 terhadap NaCl 0.1 N (Cara Mohr) Kelompok Vol. NaCl Vol. AgNO 3 7 10 ml 4 ml 8 10 ml 4.2 ml 9 10 ml 4.2 ml 10 10 ml 4.3
Laporan Praktikum Asidimetri
 Laporan Praktikum Asidimetri I. Tujuan Tujuan dari percobaan ini adalah untuk menentukan kadar NaOH. II. Tinjauan Pustaka Pada prinsipnya asidimetri adalah analisa titrimetri yang menggunakan asam kuat
Laporan Praktikum Asidimetri I. Tujuan Tujuan dari percobaan ini adalah untuk menentukan kadar NaOH. II. Tinjauan Pustaka Pada prinsipnya asidimetri adalah analisa titrimetri yang menggunakan asam kuat
Titrasi asam kuat-basa kuat
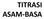 TITRASI ASAM-BASA KURVA TITRASI plot atau kurva antara ph atau poh terhadap volume titran untuk menguji apakah suatu reaksi dapat digunakan untuk analisa titrimetri ataukah tidak memilih indikator Titrasi
TITRASI ASAM-BASA KURVA TITRASI plot atau kurva antara ph atau poh terhadap volume titran untuk menguji apakah suatu reaksi dapat digunakan untuk analisa titrimetri ataukah tidak memilih indikator Titrasi
PERCOBAAN POTENSIOMETRI (PENGUKURAN ph)
 PERCOBAAN POTENSIOMETRI (PENGUKURAN ph) I. Tujuan. Membuat kurva hubungan ph - volume pentiter 2. Menentukan titik akhir titrasi 3. Menghitung kadar zat II. Prinsip Prinsip potensiometri didasarkan pada
PERCOBAAN POTENSIOMETRI (PENGUKURAN ph) I. Tujuan. Membuat kurva hubungan ph - volume pentiter 2. Menentukan titik akhir titrasi 3. Menghitung kadar zat II. Prinsip Prinsip potensiometri didasarkan pada
LAPORAN PRAKTIKUM KIMIA KIMIA ANALITIK II TITRASI IODOMETRI. KAMIS, 24 April 2014
 LAPORAN PRAKTIKUM KIMIA KIMIA ANALITIK II TITRASI IODOMETRI KAMIS, 24 April 2014 DISUSUN OLEH: Fikri Sholiha 1112016200028 KELOMPOK 4 1. Annisa Etika Arum 2. Aini Nadhokhotani Herpi 3. Rhendika Taufik
LAPORAN PRAKTIKUM KIMIA KIMIA ANALITIK II TITRASI IODOMETRI KAMIS, 24 April 2014 DISUSUN OLEH: Fikri Sholiha 1112016200028 KELOMPOK 4 1. Annisa Etika Arum 2. Aini Nadhokhotani Herpi 3. Rhendika Taufik
BAB III METODOLOGI PENELITIAN. Instrumen Jurusan Pendidikan Kimia FPMIPA Universitas Pendidikan
 21 BAB III METODOLOGI PENELITIAN 3.1 Lokasi Penelitian Penelitian ini dimulai pada bulan Maret sampai Juni 2012 di Laboratorium Riset Kimia dan Material Jurusan Pendidikan Kimia FPMIPA Universitas Pendidikan
21 BAB III METODOLOGI PENELITIAN 3.1 Lokasi Penelitian Penelitian ini dimulai pada bulan Maret sampai Juni 2012 di Laboratorium Riset Kimia dan Material Jurusan Pendidikan Kimia FPMIPA Universitas Pendidikan
PENENTUAN KOEFISIEN DISTRIBUSI
 PENENTUAN KOEFISIEN DISTRIBUSI 26 April 2014 DI SUSUN OLEH : NURUL MU NISAH AWALIYAH 1112016200008 Kelompok 1 : 1. Ipa Ida Rosita (1112016200007) 2. Putri Dewi Malya Fatimah (1112016200011) PROGRAM STUDI
PENENTUAN KOEFISIEN DISTRIBUSI 26 April 2014 DI SUSUN OLEH : NURUL MU NISAH AWALIYAH 1112016200008 Kelompok 1 : 1. Ipa Ida Rosita (1112016200007) 2. Putri Dewi Malya Fatimah (1112016200011) PROGRAM STUDI
LAPORAN PRAKTIKUM KIMIA DASAR
 LAPORAN PRAKTIKUM KIMIA DASAR Nama (NIM) : Novita Putri Wahyuni (1516045) Judul Partner : Titrasi Alkalimetri : Riska Dwi Aulia : Alifia Rizky Tanggal : 13 Maret 2017 POLITEKNIK STMI JAKARTA PROGRAM STUDI
LAPORAN PRAKTIKUM KIMIA DASAR Nama (NIM) : Novita Putri Wahyuni (1516045) Judul Partner : Titrasi Alkalimetri : Riska Dwi Aulia : Alifia Rizky Tanggal : 13 Maret 2017 POLITEKNIK STMI JAKARTA PROGRAM STUDI
PERCOBAAN VII PEMBUATAN KALIUM NITRAT
 I. Tujuan Percobaan ini yaitu: PERCOBAAN VII PEMBUATAN KALIUM NITRAT Adapun tujuan yang ingin dicapai praktikan setelah melakukan percobaan 1. Memisahkan dua garam berdasarkan kelarutannya pada suhu tertentu
I. Tujuan Percobaan ini yaitu: PERCOBAAN VII PEMBUATAN KALIUM NITRAT Adapun tujuan yang ingin dicapai praktikan setelah melakukan percobaan 1. Memisahkan dua garam berdasarkan kelarutannya pada suhu tertentu
BAB V METODOLOGI. 5.1 Alat dan Bahan yang Digunakan Alat yang Digunakan
 BAB V METODOLOGI 5.1 Alat dan Bahan yang Digunakan 5.1.1 Alat yang Digunakan Tabel 5. Alat yang Digunakan No. Nama Alat Ukuran Jumlah 1. Baskom - 3 2. Nampan - 4 3. Timbangan - 1 4. Beaker glass 100ml,
BAB V METODOLOGI 5.1 Alat dan Bahan yang Digunakan 5.1.1 Alat yang Digunakan Tabel 5. Alat yang Digunakan No. Nama Alat Ukuran Jumlah 1. Baskom - 3 2. Nampan - 4 3. Timbangan - 1 4. Beaker glass 100ml,
Percobaan 6 DISTRIBUSI ZAT TERLARUT ANTARA DUA JENIS PELARUT YANG BERCAMPUR. Lab. Kimia Fisika Jurusan Kimia Universitas Negeri Semarang
 Percobaan 6 DISTRIBUSI ZAT TERLARUT ANTARA DUA JENIS PELARUT YANG BERCAMPUR Candra Tri Kurnianingsih Lab. Kimia Fisika Jurusan Kimia Universitas Negeri Semarang Gedung D8 Lt 2 Sekaran Gunungpati Semarang,
Percobaan 6 DISTRIBUSI ZAT TERLARUT ANTARA DUA JENIS PELARUT YANG BERCAMPUR Candra Tri Kurnianingsih Lab. Kimia Fisika Jurusan Kimia Universitas Negeri Semarang Gedung D8 Lt 2 Sekaran Gunungpati Semarang,
BAB V METODELOGI. 5.1 Pengujian Kinerja Alat. Produk yang dihasilkan dari alat pres hidrolik, dilakukan analisa kualitas hasil meliputi:
 BAB V METODELOGI 5.1 Pengujian Kinerja Alat Produk yang dihasilkan dari alat pres hidrolik, dilakukan analisa kualitas hasil meliputi: 1. Analisa Fisik: A. Volume B. Warna C. Kadar Air D. Rendemen E. Densitas
BAB V METODELOGI 5.1 Pengujian Kinerja Alat Produk yang dihasilkan dari alat pres hidrolik, dilakukan analisa kualitas hasil meliputi: 1. Analisa Fisik: A. Volume B. Warna C. Kadar Air D. Rendemen E. Densitas
NETRALISASI ASAM BASA SEDERHANA
 NETRALISASI ASAM BASA SEDERHANA Dosen Pembimbing : Zora Olivia, S. Farm., M.Farm, Apt GOLONGAN/KELOMPOK : A / 3 Anindiya Tazkiyah Aji Gesang Jati Abrar Rivanio Putra Siti Sofiya Miranda Faradilla Rozziqa
NETRALISASI ASAM BASA SEDERHANA Dosen Pembimbing : Zora Olivia, S. Farm., M.Farm, Apt GOLONGAN/KELOMPOK : A / 3 Anindiya Tazkiyah Aji Gesang Jati Abrar Rivanio Putra Siti Sofiya Miranda Faradilla Rozziqa
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian ini dilaksanakan dari bulan April 2014 sampai dengan bulan Januari 2015 bertempat di Laboratorium Riset Kimia Makanan dan Material serta
BAB III METODE PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian ini dilaksanakan dari bulan April 2014 sampai dengan bulan Januari 2015 bertempat di Laboratorium Riset Kimia Makanan dan Material serta
BAB IV HASIL PENGAMATAN DAN PERHITUNGAN
 BAB IV HASIL PENGAMATAN DAN PERHITUNGAN A. HASIL PENGAMATAN 1. Standarisasi Na 2 S 2 O 3 terhadap K 2 Cr 2 O 7 0.1 N Kelompok Vol. K 2 Cr 2 O 7 Vol. Na 2 S 2 O 3 7 10 ml 11 ml 8 10 ml 12.7 ml 9 10 ml 11.6
BAB IV HASIL PENGAMATAN DAN PERHITUNGAN A. HASIL PENGAMATAN 1. Standarisasi Na 2 S 2 O 3 terhadap K 2 Cr 2 O 7 0.1 N Kelompok Vol. K 2 Cr 2 O 7 Vol. Na 2 S 2 O 3 7 10 ml 11 ml 8 10 ml 12.7 ml 9 10 ml 11.6
Hubungan koefisien dalam persamaan reaksi dengan hitungan
 STOIKIOMETRI Pengertian Stoikiometri adalah ilmu yang mempelajari dan menghitung hubungan kuantitatif dari reaktan dan produk dalam reaksi kimia (persamaan kimia) Stoikiometri adalah hitungan kimia Hubungan
STOIKIOMETRI Pengertian Stoikiometri adalah ilmu yang mempelajari dan menghitung hubungan kuantitatif dari reaktan dan produk dalam reaksi kimia (persamaan kimia) Stoikiometri adalah hitungan kimia Hubungan
