Lampiran 2.2 (Analisis Rencana Pelaksanaan Pembelajaran)
|
|
|
- Yanti Budiman
- 6 tahun lalu
- Tontonan:
Transkripsi
1 Lampiran 2.2 (Analisis Rencana Pelaksanaan Pembelajaran) I. Analisis Indikator 4. Memahami sifat-sifat larutan asambasa, metode pengukuran, dan terapannya SMAN 1 Dasar SMAN 4 Bandung SMAN 1 Cimahi SMAN 3 Tasikmalaya 4.5 Mendeskripsikan Membedakan Menghitung ph Membedakan atau poh larutan dan bukan dan dan bukan dengan dan bukan melalui melalui melalui menggunakan dalam demonstrasi. demonstrasi. tubuh mahluk percobaan prinsip hidup. kesetimbangan. Menghitung ph atau poh larutan Menjelaskan fungsi dalam tubuh makhluk hidup Mengukur ph dan bukan larutan setelah ditambah sedikit asam, basa atau pengenceran. Menjelskan fungsi dalam tubuh mahluk hidup. Menentukan komponenkomponen yang menyusun dalam melalui demonstrasi Menjelaskan sifat melalui demonstrasi Menentukan komponenkomponen yang menyusun dalam larutan melalui demonstrasi Menjelaskan melalui demonstrasi Mengamati dan bukan melalui video demonstrasi. Menghitung ph dan poh larutan Menghitung ph dengan penambahan sedikit asam atau sedikit basa atau dengan pengenceran.
2 II. Metode Pembelajaran Kurikulum Metode Pembelajaran Video Dasar SMAN 1 SMAN 4 Bandung SMAN 1 Cimahi SMAN 3 Tasikmalaya 5. Memahami sifat-sifat larutan asambasa, metode pengukuran, dan terapannya 4.6 Mendeskripsikan dan dalam tubuh mahluk hidup. Eksperimen Diskusi Diskusi informasi Eksperimen. Demonstrasi Diskusi Demonstrasi Ekspositori III. Model Pembelajaran Kurikulum Model Pembelajaran Video Dasar SMAN 1 SMAN 4 Bandung SMAN 1 Cimahi SMAN 3 Tasikmalaya 6. Memahami sifat-sifat larutan asambasa, metode pengukuran, dan terapannya 4.7 Mendeskripsikan dan dalam tubuh mahluk hidup. Konstruktivisme Cooperative Learning Group Work Induktif Induktif Induktif-Deduktif IV. Pendekatan 7. Memahami sifat-sifat Kurikulum Pendekatan Video Dasar SMAN 13 Bandung SMAN 4 Cimahi SMAN 3 Tasikmalaya SMAN Mendeskripsikan Keterampilan proses Keterampilan proses Konsep Keterampilan Konsep Lingkungan konsep
3 larutan asambasa, metode pengukuran, dan terapannya dan dalam tubuh mahluk hidup. V. Materi Pembelajaran Dasar SMAN 13 Bandung SMAN 4 Cimahi SMAN 3 Tasikmaya SMAN 1 8. Memahami sifat-sifat larutan asambasa, 4.9 Mendeskripsikan dan ph larutan. Larutan. Pengertian larutan (larutan buffer) Pengertian larutan Pengertian Larutan Penyangga metode pengukuran, dalam - Larutan yang Sifat Larutan Penyangga (larutan buffer) Sifat Larutan Penyangga dan tubuh mahluk bersifat asam. Sifat Perhitungan terapannya hidup. - Larutan Larutan Larutan yang Penyangga Penyangga bersifat basa. Larutan disebut juga larutan buffer, larutan ini dapat mempertahankan phnya Larutan dibentuk oleh dua macam zat, misalnya asam asetat dengan natrium asetat, ammonium klorida dengan amoniak Cara pembuatannya pun dapat dengan dua cara, yaitu : - mencampurkan langsung dua macam zat tersebut - mencampurkan asam lemah dengan basa kuat tetapi asam lemahnya berlebih atau basa lemah dengan asam kuat Fungsi Larutan Penyangga dalam Darah
4 tetapi basa lemahnya berlebih ph dapat ditentukan dari jumlah [ H+ ] atau [ OH- ] pada larutan tersebut yaitu : [ H+ ] = Ka [ asam ] [ basa konjugasi ] atau [ OH- ] = Kb [ basa ] [ asam konjugasi ] Dasar SMAN 13 Bandung SMAN 4 Cimahi SMAN 3 Tasikmaya SMAN 1 sedikit asam, asam tersebut akan bereaksi dengan zat yang bersifat basa. Jika ke dalam larutan ditambahkan sedikit basa, basa tersebut akan bereaksi dengan zat yang bersifat asam. Perhatikan larutan yang terbentuk dari campuran asam lemah CH 3 COOH dan basa konjugasinya ( ion CH 3 COO- ), Jika ke dalam campuran tersebut ditambahkan sedikit asam, misal HCl akan terjadi reaksi sebagai berikut : - CH 3 COO- (aq) +
5 HCl (aq) CH 3 COOH (aq) + Cl- (aq) Berdasarkan reaksi ini, berarti jumlah basa konjugasi ( ion CH 3 COO- ) akan berkurang dan asam lemah CH 3 COOH akan bertambah. Penambahan asam ke dalam akan menurunkan konsentrasi basa konjugasi dan meningkatkan konsentrasi asam. Perubahan ini tidak menyebabkan perubahan ph yang besar Dasar SMAN 13 Bandung SMAN 4 Cimahi SMAN 3 Tasikmaya SMAN 1 Jika ke dalam campuran tersebut ditambahkan sedikit basa, misal NaOH akan terjadi reaksi sebagai berikut : - CH3COOH (aq) + NaOH (aq) CH3COO- (aq) + Na+ (aq) + H2O (l) Berdasarkan reaksi ini, berarti jumlah asam lemah CH3COOH akan berkurang dan basa konjugasi ( ion CH3COO- ) akan bertambah.
6 Seperti pada penambahan sedikit asam, perubahan ini pun tidak menyebabkan perubahan ph yang besar. Berapapun tingkat pengenceran larutan, secara teoritis tidak akan mengubah harga ph. Akan tetapi pada praktiknya, jika dilakukan pengenceran yang terlalu besar, misalnya 1 L larutan diencerkan dengan 1 drum air ( kira-kira 200 L air ) tentu ph akan berubah Dasar SMAN 13 Bandung SMAN 4 Cimahi SMAN 3 Tasikmaya SMAN 1 Dalam tubuh manusia, sistem larutan terdapat dalam sel, cairan antarsel, dan dalam darah. Seluruhnya memiliki fungsi yang berbeda dalam mempertahankan ph.
7 Contoh larutan dalam : a. Sel adalah campuran asam lemah dihidrogen fosfat (H2PO4-) dan basa konjugasinya, yaitu monohidrogen fosfat (HPO42-) b. Cairan antarsel adalah campuran asam karbonat (H2CO3) dan basa konjugasinya, yaitu ion bikarbonat (HCO3-) c. Darah adalah campuran asam karbonat (H2CO3) dan basa konjugasinya ( ion bikarbonat HCO3- ), serta campuran asam hemoglobin (HHb) dan basa konjugasinya (hemoglobin/ Hb). ph darah normal ( 7,35 7,45 ), jika ph darah kurang dari 7,35 disebut Asidosis dan jika ph darah lebih Dasar SMAN 13 Bandung SMAN 4 Cimahi SMAN 3 Tasikmaya SMAN 1 Dalam tubuh manusia, sistem larutan terdapat dalam sel, cairan
8 antarsel, dan dalam darah. Seluruhnya memiliki fungsi yang berbeda dalam mempertahankan ph. Contoh larutan dalam : a. Sel adalah campuran asam lemah dihidrogen fosfat (H2PO4-) dan basa konjugasinya, yaitu monohidrogen fosfat (HPO42-) b. Cairan antarsel adalah campuran asam karbonat (H2CO3) dan basa konjugasinya, yaitu ion bikarbonat (HCO3-) c. Darah adalah campuran asam karbonat (H2CO3) dan basa konjugasinya ( ion bikarbonat HCO3- ), serta campuran asam hemoglobin (HHb) dan basa konjugasinya (hemoglobin/ Hb). ph darah normal ( 7,35 7,45 ), jika ph darah kurang dari 7,35 disebut Asidosis dan jika ph darah lebih Dasar SMAN 13 Bandung SMAN 4 Cimahi SMAN 3 Tasikmaya SMAN 1 lebih dari 7,45 disebut
9 Alkalosi. Kematian dapat terjadi jika ph darah kurang dari 7,0 atau lebih besar dari 7,8 VI. Analisis Langkah Pembelajaran Dasar SMAN 13 Bandung SMAN 4 Cimahi SMAN 3 Tasikmaya SMAN 1 9. Memahami sifat-sifat larutan asambasa, metode pengukuran, dan terapannya 4.10 Mendeskripsikan dan dalam tubuh mahluk hidup. Pertemuan 1 Pendahuluan A. Kegiatan Awal Guru menyampaikan tujuan pembelajaran dan motivasi kepada peserta didik : Kegiatan awal Tujuan : Menganalisis larutan dan bukan melalui percobaan Motivasi : Menanyakan kepada peserta didik tentang asam lemah dan basa lemah serta garam yang dibentuk dari asam dan basa Menanyakan pada siswa tentang bagian penting di dalam tubuh kita yang mengandung larutan yaitu darah. Mengapa darah 1. Pertemuan Pertama : «Kegiatan Awal : - Tanya jawab tentang pengertian larutan. - Tanya jawab tentang ph larutan asam dan basa. Tanya jawab tentang prinsip kesetimbangan «Kegiatan Inti : Mengkaji tugas atau masalah yang diberikan guru tentang ph larutan. Mendiskusikan penurunan rumus untuk menghitung ph atau poh larutan dengan menggunakan prinsip kesetimbangan. Mendiskusikan penggunaan rumus untuk menghitung Pendahuluan Siswa menjawab salam dan dicek kehadirannya Apersepsi Siswa menjawab pertanyaan-pertanyaan mengenai teori asam basa dan reaksi dalam asam basa. Motivasi Siswa termotivasi melalui tanya jawab mengenai teori asam basa. Berdasarkan teori asam basa, maka siswa dapat memahami konsep ph. Kegiatan inti Eksplorasi - Siswa dibagi lembar kerja siswa (LKS) yang harus diisi per individu. - Siswa dikenalkan alat dan bahan yang digunakan untuk 1. Kegiatan awal Pendahuluan Siswa menjawab salam dan dicek kehadirannya Apersepsi Siswa menjawab pertanyaanpertanyaan mengenai teori asam basa dan reaksi dalam asam basa. Motivasi Siswa termotivasi melalui tanya jawab mengenai teori asam basa PERTEMUAN-1 Pembukaan Apersepsi: Siswa mendapat pertanyaan dari guru Jika air murni ditambahkan larutan asam atau basa,apakah ph-na akan berubah? Siswa kembali mendapat Adakah larutan yang jika ditambah sedikit asam atau sedikit basa ph-nya tidak berubah? tersebut disebut reaksi Kegiatan Inti Siswa mengamati video demonstrasi. Siswa menjawab Dari video demonstrasi yang telah kalian lihat,
10 mengandung larutan ph atau poh larutan demonstrasi. Dasar SMAN 13 Bandung SMAN 4 Cimahi SMAN 3 Tasikmaya SMAN 1? menggunakan prinsip kesetimbangan. B. Kegiatan Inti Peserta didik diberikan penjelasan tentang definisi Peserta didik merancang alat dan melakukan percobaan untuk menganalisis dan bukan melalui kerja kelompok di laboratorium Pertemuan 2 Diskusi tentang hasil percobaan C. Penutup Menyimpulkan : Sifat larutan dan bukan Latihan soal-soal Mendiskusikan penggunaan rumus untuk menghitung ph atau poh larutan dengan menggunakan prinsip kesetimbangan dalam contoh soal. Menyamakan persepsi. Menyimpulkan penggunaan rumus untuk menghitung ph atau poh larutan dengan menggunakan prinsip kesetimbangan. Latihan soal tentang ph atau poh larutan. Elaborasi - Siswa mengamati kegiatan demonstrasi yang dilakukan oleh guru di depan kelas. - Siswa dilibatkan dalam pengukuran ph menggunakan kertas indikator universal dan mencatat hasilnya dalam tabel pengamatan kelas. - Siswa lainnya mencatat hasil pengamatan pada LKS masing-masing. - Siswa menjawab pertanyaan yang ada pada LKS. Konfirmasi - Siswa membuat kesimpulan tentang berdasarkan hasil percobaan. - Siswa mendengarkan penjelasan guru tentang asam. 2. Kegiatan inti Eksplorasi - Siswa dibagi lembar kerja siswa (LKS) yang harus diisi per individu. Siswa dikenalkan alat dan bahan yang digunakan untuk demonstrasi. Elaborasi - Siswa mengamati kegiatan demonstrasi yang dilakukan oleh guru di depan kelas. - Siswa dilibatkan dalam pengukuran ph menggunakan kertas indikator universal dan mencatat hasilnya dalam tabel Bagaimana ph setelah ditambahkan sedikit asam? Siswa menjawab pertanyaan guru Bagaimanakah ph larutan setelah ditambahkan sedikit basa? Siswa menjawab pertanyaan guru Bagaimanakah ph larutan setelah diencerkan? Siswa menyimpulkan pengertian dan sifat melalui hasil pengamatan dari video demonstrasi. Siswa mendapat penguatan dari guru mengenai pengertian dan. Siswa mendapat beberapa soal reaksi asam dan basa dengan diketahui volume dan konsentrasinya.
11 pengamatan kelas. Dasar SMAN 13 Bandung SMAN 4 Cimahi SMAN 3 Tasikmaya SMAN 1 Kegiatan Akhir : Tes uji kompetensi. 2. Pertemuan Kedua : «Kegiatan Awal : - Tanya jawab tentang kekuatan asam/basa (kuat dan lemah) - Tanya jawab tentang contoh-contoh larutan yang bersifat asam kuat, asam lemah, basa kuat dan basa lemah. - Tanya jawab tentang ph larutan asam/basa baik yang kuat maupun yang lemah. «Kegiatan Inti : Mengkaji lembar kerja eksperimen tentang larutan dan bukan baik setelah ditambah sedikit asam, basa maupun Kegiatan penutup - Siswa menyimpulkan kembali tentang perbedaan sifat dan larutan bukan. - Siswa menyimpulkan asam. - Siswa diberi penguatan oleh guru mengenai larutan Siswa diberikan tugas untuk mengetahui ketercapaian indikator pembelajaran. - Siswa lainnya mencatat hasil pengamatan pada LKS masingmasing. - Siswa menjawab pertanyaan yang ada pada LKS. Konfirmasi - Siswa membuat kesimpulan tentang sifat larutan berdasarkan hasil percobaan. - Siswa mendengarka n penjelasan guru tentang asam. Siswa menentukan zat yang habis bereaksi dan zat sisa. Siswa menentukan reaksi yang menghasilkan. Siswa menyimpulkan komponenkomponen pembentuk larutan. Siswa mendapat penjelasan mengenai rumus perhitungan ph larutan. Siswa mengerjakan beberapa contoh soal dalam menghitung ph larutan Penutup - Siswa menjawab mengenai pengertian
12 pengenceran. Melakukan eksperimen tentang dan bukan baik setelah ditambah sedikit asam, basa maupun pengenceran.. - Siswa menjawab mengenai sifat. - Siswa menjawab mengenai cara menenentukan ph. Dasar SMAN 13 Bandung SMAN 4 Cimahi SMAN 3 Tasikmaya SMAN 1 Mencatat hasil pengamatan. Mendiskusikan hasil pengamatan. Menyamakan persepsi tentang pengertian larutan dari data hasil eksperimen. Menyimpulkan pengertian larutan dari data hasil eksperimen. Membuat laporan. «Kegiatan Akhir : Tes uji kompetensi. 3. Kegiatan penutup - Siswa menyimpulka n kembali tentang perbedaan dan larutan bukan. - Siswa menyimpulka n asam. - Siswa diberi penguatan oleh guru mengenai larutan Penutup - Siswa menjawab mengenai pengertian. - Siswa menjawab mengenai sifat. - Siswa menjawab mengenai cara menenentukan ph. PERTEMUAN-2 Pembukaan Apersepsi Siswa mendapat pertanyaan dari guru Bagaimana cara menentukan ph
13 Siswa diberikan tugas untuk mengetahui ketercapaian indikator pembelajaran.? Siswa mendapat pertanyaan dari guru Bagaimana cara menentukan ph setelah adanya penambahan sedikit asam,sedikit basa, dan pengenceran? Apakah caranya sama dengan penentuan ph sebelum ditambahkan sedikit asam, sedikit basa, dan pengenceran Dasar SMAN 13 Bandung SMAN 4 Cimahi SMAN 3 Tasikmaya SMAN 1 Kegiatan inti Siswa mendapat pertanyaan dari guru Berapa menentukan ph dari campuran 25mLCH 3 COOH 0,1 M dengan 25 ml CH 3 COONa 0,1 M? Siswa mendapat pertanyaan dari guru Siswa mendapatpertanyaan dari guru Berapa ph larutan tersebut
14 jika ditambahkan lima tetes HCl? Bagaimanacara menghitungnya? Siswa mendapat penjelasan mengenai rumus perhitungan ph larutan setelah adanya penambahan sedikit asam, sedikit basa, dan pengenceran serta level mikroskopik dari penyanga tersebut. Siswa mengerjakan soal Dasar SMAN 13 Bandung SMAN 4 Cimahi SMAN 3 Tasikmaya SMAN 1 yang sebelumnya ditanyakan. Penutup Siswa menjawab mengenai cara menentukan ph. Siswa menjawab mengenai cara menentukan ph
15 setelah adanya penambahan sedikit asam, sedikit basa, dan pengenceran. PERTEMUAN-3 Kegiatan Awal Siswa mendapat pertanyaan dari guru, Darah mempunyai ph sekitar 7,4,fungsi darah akan terganggu jika ph berubah hingga di bawah 7 atau 7,8. Bagaimanakah tubuh kita mempertahankan rentang ph darah yang sempit itu? Kegiatan Inti Siswa membentuk kelompok untuk berdiskusi tentang fungsi larutan Dasar SMAN 13 Bandung SMAN 4 Cimahi SMAN 3 Tasikmaya SMAN 1 yang sebelumnya ditanyakan. Penutup Siswa menjawab mengenai cara
16 menentukan ph. Siswa menjawab mengenai cara menentukan ph setelah adanya penambahan sedikit asam, sedikit basa, dan pengenceran. PERTEMUAN-3 Kegiatan Awal Siswa mendapat pertanyaan dari guru, Darah mempunyai ph sekitar 7,4,fungsi darah akan terganggu jika ph berubah hingga di bawah 7 atau 7,8. Bagaimanakah tubuh kita mempertahankan rentang ph darah yang sempit itu? Dasar SMAN 13 Bandung SMAN 4 Cimahi SMAN 3 Tasikmaya SMAN 1 Kegiatan Inti
17 Siswa membentuk kelompok untuk berdiskusi tentang fungsi larutan dalam darah. Siswa juga mendiskusikan dalam tubuh makhluk hidup selain dalam darah. Siswa dari tiap kelompok mempresentasikan hasil diskusinya. Siswa mendapat penguatan tentang dalam tubuh makhluk hidup. Penutup Siswa mendapat pertanyaan tentang dalam tubuh makhluk hidup.
LARUTAN PENYANGGA Bahan Ajar Kelas XI IPA Semester Gasal 2012/2013
 LARUTAN PENYANGGA [Yea r] LARUTAN PENYANGGA Bahan Ajar Kelas XI IPA Semester Gasal 2012/2013 MARI BELAJAR Indikator Produk Menjelaskan komponen pembentuk larutan penyangga dengan berpikir kritis. Menjelaskan
LARUTAN PENYANGGA [Yea r] LARUTAN PENYANGGA Bahan Ajar Kelas XI IPA Semester Gasal 2012/2013 MARI BELAJAR Indikator Produk Menjelaskan komponen pembentuk larutan penyangga dengan berpikir kritis. Menjelaskan
LARUTAN PENYANGGA (BUFFER)
 LARUTAN PENYANGGA (BUFFER) Larutan penyangga Larutan penyangga atau larutan buffer adalah larutan yang ph-nya praktis tidak berubah walaupun kepadanya ditambahkan sedikit asam, sedikit basa, atau bila
LARUTAN PENYANGGA (BUFFER) Larutan penyangga Larutan penyangga atau larutan buffer adalah larutan yang ph-nya praktis tidak berubah walaupun kepadanya ditambahkan sedikit asam, sedikit basa, atau bila
LARUTAN PENYANGGA (BUFFER)
 LARUTAN PENYANGGA (BUFFER) Larutan penyangga Larutan penyangga atau larutan buffer adalah larutan yang ph-nya praktis tidak berubah walaupun kepadanya ditambahkan sedikit asam, sedikit basa, atau bila
LARUTAN PENYANGGA (BUFFER) Larutan penyangga Larutan penyangga atau larutan buffer adalah larutan yang ph-nya praktis tidak berubah walaupun kepadanya ditambahkan sedikit asam, sedikit basa, atau bila
Larutan Penyangga XI MIA
 Larutan Penyangga XI MIA Komponen Larutan Penyangga Larutan Penyangga Asam Terdiri dari Asam lemah dan basa konjugasinya (Contoh : CH 3 COOH dan CH 3 COO -, HF dan F - ) Cara membuatnya : 1. Mencampurkan
Larutan Penyangga XI MIA Komponen Larutan Penyangga Larutan Penyangga Asam Terdiri dari Asam lemah dan basa konjugasinya (Contoh : CH 3 COOH dan CH 3 COO -, HF dan F - ) Cara membuatnya : 1. Mencampurkan
Larutan penyangga dapat terbentuk dari campuran asam lemah dan basa
 Larutan penyangga dapat terbentuk dari campuran asam lemah dan basa konjugasinya atau campuran basa lemah dan asam konjugasinya. Larutan penyangga disebut juga larutan penahan atau larutan dapar atau buffer.
Larutan penyangga dapat terbentuk dari campuran asam lemah dan basa konjugasinya atau campuran basa lemah dan asam konjugasinya. Larutan penyangga disebut juga larutan penahan atau larutan dapar atau buffer.
LARUTAN ASAM-BASA DAN LARUTAN PENYANGGA
 LARUTAN ASAM-BASA DAN LARUTAN PENYANGGA A. Pengertian Larutan Penyangga Larutan penyangga biasa disebut juga dengan larutan Buffer atau larutan Dapar. Dimana larutan penyangga merupakan larutan yang mampu
LARUTAN ASAM-BASA DAN LARUTAN PENYANGGA A. Pengertian Larutan Penyangga Larutan penyangga biasa disebut juga dengan larutan Buffer atau larutan Dapar. Dimana larutan penyangga merupakan larutan yang mampu
PETA KONSEP. Larutan Penyangga. Larutan Penyangga Basa. Larutan Penyangga Asam. Asam konjugasi. Basa lemah. Asam lemah. Basa konjugasi.
 PETA KONSEP Larutan Penyangga mempertahankan berupa ph Larutan Penyangga Asam mengandung Larutan Penyangga Basa mengandung Asam lemah Basa konjugasi Asam konjugasi Basa lemah contoh contoh contoh contoh
PETA KONSEP Larutan Penyangga mempertahankan berupa ph Larutan Penyangga Asam mengandung Larutan Penyangga Basa mengandung Asam lemah Basa konjugasi Asam konjugasi Basa lemah contoh contoh contoh contoh
LARUTAN PENYANGGA (BUFFER)
 LARUTAN PENYANGGA (BUFFER) Larutan penyangga Larutan penyangga atau larutan buffer adalah larutan yang ph-nya praktis tidak berubah walaupun kepadanya ditambahkan sedikit asam, sedikit basa, atau bila
LARUTAN PENYANGGA (BUFFER) Larutan penyangga Larutan penyangga atau larutan buffer adalah larutan yang ph-nya praktis tidak berubah walaupun kepadanya ditambahkan sedikit asam, sedikit basa, atau bila
BAB 6. Jika ke dalam air murni ditambahkan asam atau basa meskipun dalam jumlah. Larutan Penyangga. Kata Kunci. Pengantar
 Kimia XI SMA 179 BAB 6 Larutan Penyangga Tujuan Pembelajaran: Setelah mempelajari bab ini, Anda diharapkan mampu: 1. Menjelaskan pengertian larutan penyangga dan komponen penyusunnya. 2. Merumuskan persamaan
Kimia XI SMA 179 BAB 6 Larutan Penyangga Tujuan Pembelajaran: Setelah mempelajari bab ini, Anda diharapkan mampu: 1. Menjelaskan pengertian larutan penyangga dan komponen penyusunnya. 2. Merumuskan persamaan
Larutan penyangga adalah larutan yang dapat mempertahankan harga ph terhadap pengaruh penambahan sedikit asam atau basa, atau terhadap pengenceran.
 Standar Kompetensi Kompetensi Dasar Memahami sifatsifat larutan asambasa, metode pengukuran, dan terapannya. Mendeskripsikan sifat larutan penyangga dan peranan larutan penyangga dalam tubuh makhluk hidup.
Standar Kompetensi Kompetensi Dasar Memahami sifatsifat larutan asambasa, metode pengukuran, dan terapannya. Mendeskripsikan sifat larutan penyangga dan peranan larutan penyangga dalam tubuh makhluk hidup.
LARUTAN PENYANGGA (BUFFER) Disusun Oleh: Diah Tria Agustina ( ) JURUSAN KIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
 HANDOUT klik di sini LARUTAN PENYANGGA (BUFFER) Disusun Oleh: Diah Tria Agustina (4301414032) JURUSAN KIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS NEGERI SEMARANG 2016 PENGERTIAN LARUTAN
HANDOUT klik di sini LARUTAN PENYANGGA (BUFFER) Disusun Oleh: Diah Tria Agustina (4301414032) JURUSAN KIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS NEGERI SEMARANG 2016 PENGERTIAN LARUTAN
kimia ASAM-BASA III Tujuan Pembelajaran
 KTSP K-13 kimia K e l a s XI ASAM-BASA III Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami mekanisme reaksi asam-basa. 2. Memahami stoikiometri
KTSP K-13 kimia K e l a s XI ASAM-BASA III Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami mekanisme reaksi asam-basa. 2. Memahami stoikiometri
LARUTAN PENYANGGA DAN HIDROLISIS
 6 LARUTAN PENYANGGA DAN HIDROLISIS A. LARUTAN PENYANGGA B. HIDROLISIS Pada bab sebelumnya, kita sudah mempelajari tentang reaksi asam-basa dan titrasi. Jika asam direaksikan dengan basa akan menghasilkan
6 LARUTAN PENYANGGA DAN HIDROLISIS A. LARUTAN PENYANGGA B. HIDROLISIS Pada bab sebelumnya, kita sudah mempelajari tentang reaksi asam-basa dan titrasi. Jika asam direaksikan dengan basa akan menghasilkan
LEMBARAN SOAL 4. Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA )
 LEMBARAN SOAL 4 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah
LEMBARAN SOAL 4 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah
BAB LARUTAN PENYANGGA. Click to edit Master subtitle style 4/8/12
 BAB 8 7 LARUTAN Click to edit Master subtitle style PENYANGGA Oleh : Ariel Evansyah Herianto Arika Budi Yarti Arina Dyah Yuliarti Permata Rahmatul Hijjah Risma Eva Rizki Imansari Rizki Mamluatuz Zahro
BAB 8 7 LARUTAN Click to edit Master subtitle style PENYANGGA Oleh : Ariel Evansyah Herianto Arika Budi Yarti Arina Dyah Yuliarti Permata Rahmatul Hijjah Risma Eva Rizki Imansari Rizki Mamluatuz Zahro
M 0,4 0,1 0,2 B 0,1 0,1 0,1 0,1 S 0,3-0,3 0,1 POH = -
 1. Campuran di bawah ini yang dapat membentuk larutan penyangga adalah.... A. Asam nitrat dengan natrium asetat B. Asam fosfat dengan natrium asetat C. Asam nitrat dengan kalium nitrat D.Asam asetat dengan
1. Campuran di bawah ini yang dapat membentuk larutan penyangga adalah.... A. Asam nitrat dengan natrium asetat B. Asam fosfat dengan natrium asetat C. Asam nitrat dengan kalium nitrat D.Asam asetat dengan
I. LARUTAN BUFFER. 1. Membuat Larutan Buffer 2. Mempelajari Daya Sanggah Larutan Buffer TINJAUAN PUSTAKA
 I. LARUTAN BUFFER II. TUJUAN 1. Membuat Larutan Buffer 2. Mempelajari Daya Sanggah Larutan Buffer III. TINJAUAN PUSTAKA Larutan penyangga atau larutan buffer atau larutan dapar merupakan suatu larutan
I. LARUTAN BUFFER II. TUJUAN 1. Membuat Larutan Buffer 2. Mempelajari Daya Sanggah Larutan Buffer III. TINJAUAN PUSTAKA Larutan penyangga atau larutan buffer atau larutan dapar merupakan suatu larutan
SOAL LARUTAN PENYANGGA MAN 2 KAB. BOGOR
 SOAL LARUTAN PENYANGGA MAN 2 KAB. BOGOR NAMA : KHOERUL ANAM KELAS : XI MIA 2 21. Dicampurkan dua larutan yaitu 50 ml NaOH 0,1 M dan 50 ml CH3COOH 0,2 M. Tentukan apakah campuran tersebut membentuk larutan
SOAL LARUTAN PENYANGGA MAN 2 KAB. BOGOR NAMA : KHOERUL ANAM KELAS : XI MIA 2 21. Dicampurkan dua larutan yaitu 50 ml NaOH 0,1 M dan 50 ml CH3COOH 0,2 M. Tentukan apakah campuran tersebut membentuk larutan
Bab IV Hasil dan Pembahasan
 Bab IV Hasil dan Pembahasan IV.1 Pembuatan Larutan Buffer Semua zat yang digunakan untuk membuat larutan buffer dapat larut dengan sempurna. Larutan yang diperoleh jernih, homogen, dan tidak berbau. Data
Bab IV Hasil dan Pembahasan IV.1 Pembuatan Larutan Buffer Semua zat yang digunakan untuk membuat larutan buffer dapat larut dengan sempurna. Larutan yang diperoleh jernih, homogen, dan tidak berbau. Data
CH 3 COONa 0,1 M K a CH 3 COOH = 10 5
 Soal No. 1 Dari beberapa larutan berikut ini yang tidak mengalami hidrolisis adalah... A. NH 4 Cl C. K 2 SO 4 D. CH 3 COONa E. CH 3 COOK Yang tidak mengalami peristiwa hidrolisis adalah garam yang berasal
Soal No. 1 Dari beberapa larutan berikut ini yang tidak mengalami hidrolisis adalah... A. NH 4 Cl C. K 2 SO 4 D. CH 3 COONa E. CH 3 COOK Yang tidak mengalami peristiwa hidrolisis adalah garam yang berasal
LAPORAN PRAKTIKUM 3 ph METER, BUFFER, dan PENGENCERAN DISUSUN OLEH : MARIA LESTARI DAN YULIA FITRI GHAZALI Kamis 04 Oktober s/d 16.
 LAPORAN PRAKTIKUM 3 ph METER, BUFFER, dan PENGENCERAN DISUSUN OLEH : MARIA LESTARI DAN YULIA FITRI GHAZALI Kamis 04 Oktober 2012 14.00 s/d 16.00 wib TUJUAN : 1. Agar mahasiswa dapat memahami prinsip-prinsip
LAPORAN PRAKTIKUM 3 ph METER, BUFFER, dan PENGENCERAN DISUSUN OLEH : MARIA LESTARI DAN YULIA FITRI GHAZALI Kamis 04 Oktober 2012 14.00 s/d 16.00 wib TUJUAN : 1. Agar mahasiswa dapat memahami prinsip-prinsip
Kimia Study Center - Contoh soal dan pembahasan tentang hidrolisis larutan garam dan menentukan ph atau poh larutan garam, kimia SMA kelas 11 IPA.
 Kimia Study Center - Contoh soal dan pembahasan tentang hidrolisis larutan garam dan menentukan ph atau poh larutan garam, kimia SMA kelas 11 IPA. Soal No. 1 Dari beberapa larutan berikut ini yang tidak
Kimia Study Center - Contoh soal dan pembahasan tentang hidrolisis larutan garam dan menentukan ph atau poh larutan garam, kimia SMA kelas 11 IPA. Soal No. 1 Dari beberapa larutan berikut ini yang tidak
4. Memahami sifat-sifat larutan asam-basa, metode pengukuran, dan terapannya.
 RENCANA PELAKSANAAN PEMBELAJARAN (RPP) LARUTAN PENYANGGA/ BUFFER SEKOLAH : SMAN 16 SURABAYA MATA PELAJARAN : KIMIA KELAS / SEMESTER : XI / 2 (dua) ALOKASI WAKTU : 2 Jam Pelajaran I. STANDAR KOMPETENSI
RENCANA PELAKSANAAN PEMBELAJARAN (RPP) LARUTAN PENYANGGA/ BUFFER SEKOLAH : SMAN 16 SURABAYA MATA PELAJARAN : KIMIA KELAS / SEMESTER : XI / 2 (dua) ALOKASI WAKTU : 2 Jam Pelajaran I. STANDAR KOMPETENSI
BAB V PENUTUP. 5.1 Kesimpulan. Berdasarkan hasil analisis data dan pembahasan secara deskriptif dan statistik. dapat disimpulkan sebagai berikut :
 BAB V PENUTUP 5.1 Kesimpulan Berdasarkan hasil analisis data dan pembahasan secara deskriptif dan statistik dapat disimpulkan sebagai berikut : 1. Penerapan pendekatan saintifik efektif pada materi pokok
BAB V PENUTUP 5.1 Kesimpulan Berdasarkan hasil analisis data dan pembahasan secara deskriptif dan statistik dapat disimpulkan sebagai berikut : 1. Penerapan pendekatan saintifik efektif pada materi pokok
LAPORAN PRAKTIKUM KIMIA DASAR LARUTAN BUFFER
 LAPORAN PRAKTIKUM KIMIA DASAR LARUTAN BUFFER Nama : Fathul Muin NIM : 12/334686/PA/14919 LABORATORIUM KIMIA DASAR JURUSAN KIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS GADJAH MADA DASAR
LAPORAN PRAKTIKUM KIMIA DASAR LARUTAN BUFFER Nama : Fathul Muin NIM : 12/334686/PA/14919 LABORATORIUM KIMIA DASAR JURUSAN KIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS GADJAH MADA DASAR
LEMBAR SOAL. Mata pelajaran : Kimia. Kelas/Program : XI/IPA Hari, tanggal : Selasa, 8 April 2008 Alokasi waktu : 90 Menit
 DEPARTEMEN PENDIDIKAN NASIONAL UNIVERSITAS NEGERI SEMARANG FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM JURUSAN KIMIA Gedung D6. Kampus Sekaran Gunungpati Semarang 50229 Telp. 8508035 LEMBAR SOAL Mata
DEPARTEMEN PENDIDIKAN NASIONAL UNIVERSITAS NEGERI SEMARANG FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM JURUSAN KIMIA Gedung D6. Kampus Sekaran Gunungpati Semarang 50229 Telp. 8508035 LEMBAR SOAL Mata
YAYASAN WIDYA BHAKTI SEKOLAH MENENGAH ATAS SANTA ANGELA TERAKREDITASI A
 YAYASAN WIDYA BHAKTI SEKOLAH MENENGAH ATAS SANTA ANGELA TERAKREDITASI A Jl. Merdeka No. 24 Bandung 022. 4214714 Fax.022. 4222587 http//: www.smasantaangela.sch.id, e-mail : smaangela@yahoo.co.id 043 URS
YAYASAN WIDYA BHAKTI SEKOLAH MENENGAH ATAS SANTA ANGELA TERAKREDITASI A Jl. Merdeka No. 24 Bandung 022. 4214714 Fax.022. 4222587 http//: www.smasantaangela.sch.id, e-mail : smaangela@yahoo.co.id 043 URS
wanibesak.wordpress.com 1
 Ringkasan, contoh soal dan pembahasan mengenai asam, basa dan larutan penyangga atau larutan buffer Persamaan ionisasi air H 2O H + + OH Dari reaksi di atas sesuai hukum kesetimbangan, tetapan kesetimbangan
Ringkasan, contoh soal dan pembahasan mengenai asam, basa dan larutan penyangga atau larutan buffer Persamaan ionisasi air H 2O H + + OH Dari reaksi di atas sesuai hukum kesetimbangan, tetapan kesetimbangan
BAB IV TEMUAN DAN PEMBAHASAN. Untuk mengembangkan strategi pembelajaran pada materi titrasi asam basa
 BAB IV TEMUAN DAN PEMBAHASAN Untuk mengembangkan strategi pembelajaran pada materi titrasi asam basa dilakukan tiga tahap yaitu tahap pertama melakukan analisis standar kompetensi dan kompetensi dasar
BAB IV TEMUAN DAN PEMBAHASAN Untuk mengembangkan strategi pembelajaran pada materi titrasi asam basa dilakukan tiga tahap yaitu tahap pertama melakukan analisis standar kompetensi dan kompetensi dasar
MATERI HIDROLISIS GARAM KIMIA KELAS XI SEMESTER GENAP
 MATERI HIDROLISIS GARAM KIMIA KELAS XI SEMESTER GENAP PENDAHULUAN Kalian pasti mendengar penyedap makanan. Penyedap makanan yang sering digunakan adalah vitsin. Penyedap ini mengandung monosodium glutamat
MATERI HIDROLISIS GARAM KIMIA KELAS XI SEMESTER GENAP PENDAHULUAN Kalian pasti mendengar penyedap makanan. Penyedap makanan yang sering digunakan adalah vitsin. Penyedap ini mengandung monosodium glutamat
Nova Nurfauziawati Kelompok 11A V. PEMBAHASAN
 V. PEMBAHASAN Praktikum yang dilaksanakan tanggal 3 Oktober 2011 mengenai pembuatan larutan buffer dan pengujian kestabilannya. Larutan buffer adalah campuran asam/basa lemah dan basa/asam konjugasinya
V. PEMBAHASAN Praktikum yang dilaksanakan tanggal 3 Oktober 2011 mengenai pembuatan larutan buffer dan pengujian kestabilannya. Larutan buffer adalah campuran asam/basa lemah dan basa/asam konjugasinya
Tentukan ph dari suatu larutan yang memiliki konsentrasi ion H + sebesar 10 4 M dengan tanpa bantuan alat hitung kalkulator!
 Kimia Study Center - Contoh soal dan pembahasan tentang cara menghitung ph dan poh larutan asam basa berdasarkan konsentrasi ion [H + ] dan [OH ] SMA kelas 11 IPA. Berikut contoh-contoh soal yang bisa
Kimia Study Center - Contoh soal dan pembahasan tentang cara menghitung ph dan poh larutan asam basa berdasarkan konsentrasi ion [H + ] dan [OH ] SMA kelas 11 IPA. Berikut contoh-contoh soal yang bisa
BAB 7. ASAM DAN BASA
 BAB 7. ASAM DAN BASA 7. 1 TEORI ASAM BASA 7. 2 TETAPAN KESETIMBANGAN PENGIONAN ASAM DAN BASA 7. 3 KONSENTRASI ION H + DAN ph 7. 4 INDIKATOR ASAM-BASA (INDIKATOR ph) 7. 5 CAMPURAN PENAHAN 7. 6 APLIKASI
BAB 7. ASAM DAN BASA 7. 1 TEORI ASAM BASA 7. 2 TETAPAN KESETIMBANGAN PENGIONAN ASAM DAN BASA 7. 3 KONSENTRASI ION H + DAN ph 7. 4 INDIKATOR ASAM-BASA (INDIKATOR ph) 7. 5 CAMPURAN PENAHAN 7. 6 APLIKASI
Artikel Kimia tentang Peranan Larutan Penyangga
 Artikel Kimia tentang Peranan Larutan Penyangga A. PENGERTIAN Larutan penyangga atau dikenal juga dengan nama larutan buffer adalah larutan yang dapat mempertahankan nilai ph apabila larutan tersebut ditambahkan
Artikel Kimia tentang Peranan Larutan Penyangga A. PENGERTIAN Larutan penyangga atau dikenal juga dengan nama larutan buffer adalah larutan yang dapat mempertahankan nilai ph apabila larutan tersebut ditambahkan
GALAT TITRASI. Ilma Nugrahani
 GALAT TITRASI Ilma Nugrahani Galat Titrasi Adalah galat yang terjadi karena indikator berubah warna sebelum atau sesudah titik setara ditunjukkan dari kurva titrasi titik akhir titik ekivalen. Dapat disebabkan
GALAT TITRASI Ilma Nugrahani Galat Titrasi Adalah galat yang terjadi karena indikator berubah warna sebelum atau sesudah titik setara ditunjukkan dari kurva titrasi titik akhir titik ekivalen. Dapat disebabkan
TUGAS KIMIA SMA NEGERI 1 BAJAWA TITRASI ASAM BASA. Nama : Kelas. Disusun oleh:
 TUGAS KIMIA TITRASI ASAM BASA Disusun oleh: Nama : Kelas : SMA NEGERI 1 BAJAWA 2015 TITRASI ASAM BASA 1. Prinsip Dasar Titrasi netralisasi adalah titrasi yang didasarkan pada reaksi antara suatu asam dengan
TUGAS KIMIA TITRASI ASAM BASA Disusun oleh: Nama : Kelas : SMA NEGERI 1 BAJAWA 2015 TITRASI ASAM BASA 1. Prinsip Dasar Titrasi netralisasi adalah titrasi yang didasarkan pada reaksi antara suatu asam dengan
Lampiran Sumber Belajar : Purba, Michael Kimia SMA. Erlangga. Jakarta
 Lampiran 3 95 INTRUKSI 1. Setiap siswa harus membaca penuntun praktikum ini dengan seksama. 2. Setelah alat dan bahan siap tersedia, laksanakanlah percobaan menurut prosedur percobaan. 3. Setelah melakukan
Lampiran 3 95 INTRUKSI 1. Setiap siswa harus membaca penuntun praktikum ini dengan seksama. 2. Setelah alat dan bahan siap tersedia, laksanakanlah percobaan menurut prosedur percobaan. 3. Setelah melakukan
RENCANA PELAKSANAAN PEMBELAJARAN I. Standar Kompetensi 1. Memahami sifat-sifat larutan asam basa, metode pengukuran, dan terapannya
 Lampiran 2 63 RENCANA PELAKSANAAN PEMBELAJARAN I Mata Pelajaran Kelas/Semester Sub Materi Pokok Alokasi Waktu Pertemuan ke : Kimia : XI IPA 4/ 2 (dua) : Teori Asam Basa Arrhenius : 2 x 45 menit : I Standar
Lampiran 2 63 RENCANA PELAKSANAAN PEMBELAJARAN I Mata Pelajaran Kelas/Semester Sub Materi Pokok Alokasi Waktu Pertemuan ke : Kimia : XI IPA 4/ 2 (dua) : Teori Asam Basa Arrhenius : 2 x 45 menit : I Standar
Metodologi Penelitian
 Bab III Metodologi Penelitian Pembuatan larutan buffer menggunakan metode pencampuran antara asam lemah dengan basa konjugasinya. Selanjutnya larutan buffer yang sudah dibuat diuji kemampuannya dalam mempertahankan
Bab III Metodologi Penelitian Pembuatan larutan buffer menggunakan metode pencampuran antara asam lemah dengan basa konjugasinya. Selanjutnya larutan buffer yang sudah dibuat diuji kemampuannya dalam mempertahankan
SMA Negeri 6 Denpasar Alamat Jalan Raya Sanur Tlp : 0361(247843) Denpasar
 RENCANA PELAKSANAAN PEMBELAJARAN ( RPP ) Mata Pelajaran : Kimia Materi : Reaksi Asam Basa dan Perhitungannya Kelas / Smt : XI / 2 Oleh : I Wayan Subaga SMA Negeri 6 Denpasar Alamat Jalan Raya Sanur Tlp
RENCANA PELAKSANAAN PEMBELAJARAN ( RPP ) Mata Pelajaran : Kimia Materi : Reaksi Asam Basa dan Perhitungannya Kelas / Smt : XI / 2 Oleh : I Wayan Subaga SMA Negeri 6 Denpasar Alamat Jalan Raya Sanur Tlp
KONTROL KEASAMAN LARUTAN PENYANGGA (BUFFER)
 KONTROL KEASAMAN LARUTAN PENYANGGA (BUFFER) TUJUAN: 1. Memahami manfaat mengontrol ph, terutama dalam sistem fisiologi. 2. Mempelajari tehnik mempertahankan nilai ph larutan dalam berbagai aplikasi. 3.
KONTROL KEASAMAN LARUTAN PENYANGGA (BUFFER) TUJUAN: 1. Memahami manfaat mengontrol ph, terutama dalam sistem fisiologi. 2. Mempelajari tehnik mempertahankan nilai ph larutan dalam berbagai aplikasi. 3.
PERCOBAAN IV PEMBUATAN BUFFER Tujuan Menghitung dan pembuat larutan buffer atau dapar untuk aplikasi dalam bidang farmasi.
 A B PERCOBAAN IV PEMBUATAN BUFFER Tujuan Menghitung dan pembuat larutan buffer atau dapar untuk aplikasi dalam bidang farmasi. Dasar Teori Larutan penyangga atau larutan buffer atau larutan dapar merupakan
A B PERCOBAAN IV PEMBUATAN BUFFER Tujuan Menghitung dan pembuat larutan buffer atau dapar untuk aplikasi dalam bidang farmasi. Dasar Teori Larutan penyangga atau larutan buffer atau larutan dapar merupakan
Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi. Bab17. Kesetimbangan Asam-Basa dan Kesetimbangan Kelarutan
 Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi Bab17 Kesetimbangan Asam-Basa dan Kesetimbangan Kelarutan Larutan buffer adalah larutan yg terdiri dari: 1. asam lemah/basa
Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi Bab17 Kesetimbangan Asam-Basa dan Kesetimbangan Kelarutan Larutan buffer adalah larutan yg terdiri dari: 1. asam lemah/basa
RENCANA PELAKSANAAN PEMBELAJARAN
 RENCANA PELAKSANAAN PEMBELAJARAN Nama Sekolah Mata Pelajaran Pokok Bahasan Kelas/semester : Madrasah Darul Ihksan Samarinda : Kimia : Larutan Penyangga : XI /Genap Tahun Ajaran : 2012/2013 Alokasi waktu
RENCANA PELAKSANAAN PEMBELAJARAN Nama Sekolah Mata Pelajaran Pokok Bahasan Kelas/semester : Madrasah Darul Ihksan Samarinda : Kimia : Larutan Penyangga : XI /Genap Tahun Ajaran : 2012/2013 Alokasi waktu
TEORI ASAM BASA Secara Umum :
 TEORI ASAM BASA Secara Umum : Asam Basa : : Cairan berasa asam dan dapat memerahkan kertas lakmus biru Cairan berasa pahit dan dapat membirukan kertas lakmus merah Garam : Cairan yang berasa asin TEORI
TEORI ASAM BASA Secara Umum : Asam Basa : : Cairan berasa asam dan dapat memerahkan kertas lakmus biru Cairan berasa pahit dan dapat membirukan kertas lakmus merah Garam : Cairan yang berasa asin TEORI
Penambahan oleh sedikit asam-kuat (H + ) menyebabkan kesetimbangan. CH 3 COOH(aq) CH 3 COO - (aq) + H + (aq) (9.1) asam lemah
 Larutan bufer* merupakan sistem larutan yang dapat mempertahankan lingkungannya dari pengaruh seperti oleh penambahan sedikit asam/basa kuat, atau oleh pengenceran. Sistem bufer terdiri atas dua komponen,
Larutan bufer* merupakan sistem larutan yang dapat mempertahankan lingkungannya dari pengaruh seperti oleh penambahan sedikit asam/basa kuat, atau oleh pengenceran. Sistem bufer terdiri atas dua komponen,
Dikenal : - Asidimetri : zat baku asam - Alkalimetri : zat baku basa DASAR : Reaksi penetralan Asam + Basa - hidrolisis - buffer - hal lain ttg lart
 Dikenal : - Asidimetri : zat baku asam - Alkalimetri : zat baku basa DASAR : Reaksi penetralan Asam + Basa - hidrolisis - buffer - hal lain ttg lart a. AK + BK ph = 7 B. AK + BL ph < 7 C. AL + BK ph >
Dikenal : - Asidimetri : zat baku asam - Alkalimetri : zat baku basa DASAR : Reaksi penetralan Asam + Basa - hidrolisis - buffer - hal lain ttg lart a. AK + BK ph = 7 B. AK + BL ph < 7 C. AL + BK ph >
Teori Asam-Basa Arrhenius
 Standar Kompetensi emahami terapannya. sifatsifat larutan asambasa, metode pengukuran, dan Kompetensi Dasar enjelaskan teori asam basa menurut Arrhenius mengklasifikasi berbagai larutan asam, netral, dan
Standar Kompetensi emahami terapannya. sifatsifat larutan asambasa, metode pengukuran, dan Kompetensi Dasar enjelaskan teori asam basa menurut Arrhenius mengklasifikasi berbagai larutan asam, netral, dan
Bab II Tinjauan Pustaka. Asam basa Konjugasi Menurut Bronsted Lowry
 Bab II Tinjauan Pustaka II.1 Asam basa Konjugasi Menurut Bronsted Lowry Untuk memahami konsep larutan buffer perlu diketahui konsep asam basa. Konsep asam basa ada tiga yaitu menurut Arrhenius, Bronsted
Bab II Tinjauan Pustaka II.1 Asam basa Konjugasi Menurut Bronsted Lowry Untuk memahami konsep larutan buffer perlu diketahui konsep asam basa. Konsep asam basa ada tiga yaitu menurut Arrhenius, Bronsted
SMA NEGERI 6 SURABAYA LARUTAN ASAM & BASA. K a = 2.M a. 2. H 2 SO 4 (asam kuat) α = 1 H 2 SO 4 2H + 2
 SMA NEGERI 6 SURABAYA LARUTAN ASAM & BASA K I M I A 1). TEORI ARCHENIUS Asam adalah zat yang jika di dalam air melepaskan ion H +, dengan kata lain pembawa sifat asam adalah ion H +. jumlah ion H+ yang
SMA NEGERI 6 SURABAYA LARUTAN ASAM & BASA K I M I A 1). TEORI ARCHENIUS Asam adalah zat yang jika di dalam air melepaskan ion H +, dengan kata lain pembawa sifat asam adalah ion H +. jumlah ion H+ yang
Derajat Keasaman dan kebasaan (ph dan poh)
 Derajat Keasaman dan kebasaan (ph dan poh) Berdasarkan teori asam basa Arhenius, suatu larutan dapat bersifat asam, basa atau netral tergantung pada konsentrasi ion H+ atau ion OH dalam larutan tersebut.
Derajat Keasaman dan kebasaan (ph dan poh) Berdasarkan teori asam basa Arhenius, suatu larutan dapat bersifat asam, basa atau netral tergantung pada konsentrasi ion H+ atau ion OH dalam larutan tersebut.
Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi. Bab 16. Asam dan Basa
 Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi Bab 16 Asam dan Basa Asam Memiliki rasa masam; misalnya cuka mempunyai rasa dari asam asetat, dan lemon serta buah-buahan sitrun
Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi Bab 16 Asam dan Basa Asam Memiliki rasa masam; misalnya cuka mempunyai rasa dari asam asetat, dan lemon serta buah-buahan sitrun
2/14/2012 LOGO Asam Basa Apa yang terjadi? Koma Tulang keropos Sesak napas dll
 LOGO Bab 08 Asam Basa Apa yang terjadi? - Koma - Tulang keropos - Sesak napas - dll 1 Ikhtisar Teori Asam Basa Sifat Asam-Basa dari Air ph-suatu ukuran keasaman Kesetimbangan Asam-Basa Lemah dan Garam
LOGO Bab 08 Asam Basa Apa yang terjadi? - Koma - Tulang keropos - Sesak napas - dll 1 Ikhtisar Teori Asam Basa Sifat Asam-Basa dari Air ph-suatu ukuran keasaman Kesetimbangan Asam-Basa Lemah dan Garam
Titrasi asam kuat-basa kuat
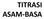 TITRASI ASAM-BASA KURVA TITRASI plot atau kurva antara ph atau poh terhadap volume titran untuk menguji apakah suatu reaksi dapat digunakan untuk analisa titrimetri ataukah tidak memilih indikator Titrasi
TITRASI ASAM-BASA KURVA TITRASI plot atau kurva antara ph atau poh terhadap volume titran untuk menguji apakah suatu reaksi dapat digunakan untuk analisa titrimetri ataukah tidak memilih indikator Titrasi
BAB IV DESKRIPSI DAN ANALISIS DATA
 BAB IV DESKRIPSI DAN ANALISIS DATA A. Deskripsi Data Data yang didapatkan dari penelitian ini yaitu hasil pretest dan posttest. Hasil pretest digunakan sebagai data pendukung untuk mengetahui kemampuan
BAB IV DESKRIPSI DAN ANALISIS DATA A. Deskripsi Data Data yang didapatkan dari penelitian ini yaitu hasil pretest dan posttest. Hasil pretest digunakan sebagai data pendukung untuk mengetahui kemampuan
BAB I PRAKTIKUM ASIDI AL-KALIMETRI
 BAB I PRAKTIKUM ASIDI AL-KALIMETRI I. TUJUAN a. Mahasiswa dapat menjelaskan proses titrasi asidi alkalimetri. b. Mahasiswa mampu menghitung konsentrasi sampel dengan metode asidi alkalimetri. II. DASAR
BAB I PRAKTIKUM ASIDI AL-KALIMETRI I. TUJUAN a. Mahasiswa dapat menjelaskan proses titrasi asidi alkalimetri. b. Mahasiswa mampu menghitung konsentrasi sampel dengan metode asidi alkalimetri. II. DASAR
PRESENTASI POWERPOINT PENGAJAR OLEH PENERBIT ERLANGGA DIVISI PERGURUAN TINGGI. BAB 16. ASAM DAN BASA
 PRESENTASI POWERPOINT PENGAJAR OLEH PENERBIT ERLANGGA DIVISI PERGURUAN TINGGI. BAB 16. ASAM DAN BASA Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi Bab 16 Asam dan Basa Asam
PRESENTASI POWERPOINT PENGAJAR OLEH PENERBIT ERLANGGA DIVISI PERGURUAN TINGGI. BAB 16. ASAM DAN BASA Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi Bab 16 Asam dan Basa Asam
Soal dan Pembahasan Asam Basa, Larutan Penyangga, Hidrolisis Garam, dan K SP
 Soal dan Pembahasan Asam Basa, Larutan Penyangga, Hidrolisis Garam, dan K SP Θ Asam Basa 1. Jelaskan Pengertian Asam Basa menurut arrhenius! Asam Zat yang dalam air melepaskan ion H + Basa Senyawa yang
Soal dan Pembahasan Asam Basa, Larutan Penyangga, Hidrolisis Garam, dan K SP Θ Asam Basa 1. Jelaskan Pengertian Asam Basa menurut arrhenius! Asam Zat yang dalam air melepaskan ion H + Basa Senyawa yang
1. Dari pengujian larutan dengan kertas lakmus diperoleh data berikut:
 SOAL-SOAL BAB 5 LARUTAN ASAM BASA/ Kimia Erlangga 2B 1. Dari pengujian larutan dengan kertas lakmus diperoleh data berikut: No Larutan yang diuji Warna lakmus Merah Biru 1 X Merah Biru 2 Y Merah Merah
SOAL-SOAL BAB 5 LARUTAN ASAM BASA/ Kimia Erlangga 2B 1. Dari pengujian larutan dengan kertas lakmus diperoleh data berikut: No Larutan yang diuji Warna lakmus Merah Biru 1 X Merah Biru 2 Y Merah Merah
H + + OH - > H 2 O. Jumlah mol asam (proton) sama dengan jumlah mol basa (ion hidroksida). Stoikiometri netralisasi
 Netralisasi a. Netralisasi Neutralisasi dapat didefinisikan sebagai reaksi antara proton (atau ion hidronium) dan ion hidroksida membentuk air. Dalam bab ini kita hanya mendiskusikan netralisasi di larutan
Netralisasi a. Netralisasi Neutralisasi dapat didefinisikan sebagai reaksi antara proton (atau ion hidronium) dan ion hidroksida membentuk air. Dalam bab ini kita hanya mendiskusikan netralisasi di larutan
OAL TES SEMESTER II. I. Pilihlah jawaban yang paling tepat!
 KIMIA XI SMA 217 S OAL TES SEMESTER II I. Pilihlah jawaban yang paling tepat! 1. Basa menurut Arhenius adalah senyawa yang bila dilarutkan dalam air akan menghasilkan a. proton d. ion H b. elektron e.
KIMIA XI SMA 217 S OAL TES SEMESTER II I. Pilihlah jawaban yang paling tepat! 1. Basa menurut Arhenius adalah senyawa yang bila dilarutkan dalam air akan menghasilkan a. proton d. ion H b. elektron e.
BAB IV HASIL PENELITIAN DAN PEMBAHASAN
 62 BAB IV HASIL PENELITIAN DAN PEMBAHASAN Pada bab ini akan dibahas mengenai hasil penelitian dan pembahasannya. Hasil penelitian ini merupakan deskripsi tentang tahap-tahap proses pembuatan video pembelajaran
62 BAB IV HASIL PENELITIAN DAN PEMBAHASAN Pada bab ini akan dibahas mengenai hasil penelitian dan pembahasannya. Hasil penelitian ini merupakan deskripsi tentang tahap-tahap proses pembuatan video pembelajaran
Larutan Dapar Dapar adalah senyawa-senyawa atau campuran senyawa yang dapat meniadakan perubahan ph terhadap penambahan sedikit asam atau basa.
 Larutan Dapar Dapar adalah senyawa-senyawa atau campuran senyawa yang dapat meniadakan perubahan ph terhadap penambahan sedikit asam atau basa. Peniadaan perubahan ph tersebut dikenal sebagai aksi dapar.
Larutan Dapar Dapar adalah senyawa-senyawa atau campuran senyawa yang dapat meniadakan perubahan ph terhadap penambahan sedikit asam atau basa. Peniadaan perubahan ph tersebut dikenal sebagai aksi dapar.
PERCOBAAN 3 REAKSI ASAM BASA
 PERCOBAAN 3 REAKSI ASAM BASA I. Teori Dasar Kita sering menjumpai asam dan basa dalam kehidupan sehari-hari. Buah-buahan, seperti jeruk, apel, dll., mengandung asam. Amonia rumah tangga, bahan pembersih,
PERCOBAAN 3 REAKSI ASAM BASA I. Teori Dasar Kita sering menjumpai asam dan basa dalam kehidupan sehari-hari. Buah-buahan, seperti jeruk, apel, dll., mengandung asam. Amonia rumah tangga, bahan pembersih,
Hidrolisis Garam. Model Problem Based Learning (PBL)
 E-BOOK KIMIA Hidrolisis Garam Special video included Model Problem Based Learning (PBL) Penulis Barista Kristyaningsih Pembimbing Prof. Sulistyo Saputro, M.Si, Ph.D Prof. Sentot Budi R., Ph.D Untuk Kelas
E-BOOK KIMIA Hidrolisis Garam Special video included Model Problem Based Learning (PBL) Penulis Barista Kristyaningsih Pembimbing Prof. Sulistyo Saputro, M.Si, Ph.D Prof. Sentot Budi R., Ph.D Untuk Kelas
LAPORAN PRAKTIKUM KIMIA MENENTUKAN KONSENTRASI LARUTAN H 2 SO 4 DAN KONSENTRASI LARUTAN CH 3 COOH DENGAN TITRASI ASAM BASA (ASIDI-ALKALIMETRI)
 LAPORAN PRAKTIKUM KIMIA MENENTUKAN KONSENTRASI LARUTAN H 2 SO 4 DAN KONSENTRASI LARUTAN CH 3 COOH DENGAN TITRASI ASAM BASA (ASIDI-ALKALIMETRI) Disusun Oleh : 1. Ela Bintang Bahari (XI IPA 4 / 03) 2. Alfian
LAPORAN PRAKTIKUM KIMIA MENENTUKAN KONSENTRASI LARUTAN H 2 SO 4 DAN KONSENTRASI LARUTAN CH 3 COOH DENGAN TITRASI ASAM BASA (ASIDI-ALKALIMETRI) Disusun Oleh : 1. Ela Bintang Bahari (XI IPA 4 / 03) 2. Alfian
BAB III LARUTAN PENYANGGA (BUFFER)
 BAB III LARUTAN PENYANGGA (BUFFER) BAB 1. PRE-LAB 1. Apakah yang dimaksud dengan larutan penyangga? Larutan buffer atau larutan penyangga adalah semua larutan yang ph-nya dapat dikatakan tetap, walaupun
BAB III LARUTAN PENYANGGA (BUFFER) BAB 1. PRE-LAB 1. Apakah yang dimaksud dengan larutan penyangga? Larutan buffer atau larutan penyangga adalah semua larutan yang ph-nya dapat dikatakan tetap, walaupun
Asam-Basa. Kimia. Kelas XI. B usiness Name. Indikator: A. Teori Asam-Basa
 Asam-Basa Kimia Kelas XI B usiness Name Indikator: 3.1.1 Menjelaskan teori asam basa berdasarkan konsep Arrhenius, Brosnted Lowry dan Lewis 3.1.2 Menjelaskan pengertian indikator asam-basa 3.1.3 Menyebutkan
Asam-Basa Kimia Kelas XI B usiness Name Indikator: 3.1.1 Menjelaskan teori asam basa berdasarkan konsep Arrhenius, Brosnted Lowry dan Lewis 3.1.2 Menjelaskan pengertian indikator asam-basa 3.1.3 Menyebutkan
Silabus dan Rencana Pelaksanaan Pembelajaran (RPP)
 Endang Susilowati MODEL Silabus dan Rencana Pelaksanaan Pembelajaran (RPP) SAINS KIMIA Prinsip dan Terapannya untuk Kelas XI SMA dan MA Semester 2 Program Ilmu Pengetahuan Alam 2B Berdasarkan Permendiknas
Endang Susilowati MODEL Silabus dan Rencana Pelaksanaan Pembelajaran (RPP) SAINS KIMIA Prinsip dan Terapannya untuk Kelas XI SMA dan MA Semester 2 Program Ilmu Pengetahuan Alam 2B Berdasarkan Permendiknas
BAB II KAJIAN TEORITIS. sebagai hasil pengalamannya sendiri dalam interaksi dengan
 9 BAB II KAJIAN TEORITIS A. Konsep Teoritis 1. Belajar dan hasil belajar Belajar adalah suatu proses usaha yang dilakukan seseorang untuk memperoleh suatu perubahan tingkah laku yang baru secara keseluruhan,
9 BAB II KAJIAN TEORITIS A. Konsep Teoritis 1. Belajar dan hasil belajar Belajar adalah suatu proses usaha yang dilakukan seseorang untuk memperoleh suatu perubahan tingkah laku yang baru secara keseluruhan,
BAB III METODOLOGI PENELITIAN
 BAB III METODOLOGI PENELITIAN A. Lokasi dan Subjek Penelitian Penelitian ini dilakukan di salah satu SMA Negeri di Kota Bandung. Subjek penelitian ini adalah enam orang siswa SMA kelas XI IPA yang sudah
BAB III METODOLOGI PENELITIAN A. Lokasi dan Subjek Penelitian Penelitian ini dilakukan di salah satu SMA Negeri di Kota Bandung. Subjek penelitian ini adalah enam orang siswa SMA kelas XI IPA yang sudah
Mahasiswa Program Studi Pendidikan Kimia, FKIP, UNS, Surakarta, Indonesia 2. Dosen Program Studi Pendidikan Kimia, FKIP, UNS, Surakarta, Indonesia
 Jurnal Pendidikan Kimia (JPK), Vol. 2 No. 3 Tahun 2013 Program Studi Pendidikan Kimia Universitas Sebelas Maret ISSN 2337-9995 jpk.pkimiauns@ymail.com PEMBELAJARAN DIRECT INSTRUCTION DISERTAI HIERARKI
Jurnal Pendidikan Kimia (JPK), Vol. 2 No. 3 Tahun 2013 Program Studi Pendidikan Kimia Universitas Sebelas Maret ISSN 2337-9995 jpk.pkimiauns@ymail.com PEMBELAJARAN DIRECT INSTRUCTION DISERTAI HIERARKI
kimia Kelas X LARUTAN ELEKTROLIT DAN NONELEKTROLIT K-13 A. Pengertian Larutan dan Daya Hantar Listrik
 K-13 Kelas X kimia LARUTAN ELEKTROLIT DAN NONELEKTROLIT Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami perbedaan antara larutan elektrolit dan
K-13 Kelas X kimia LARUTAN ELEKTROLIT DAN NONELEKTROLIT Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami perbedaan antara larutan elektrolit dan
Aplikasi Larutan Buffer dalam Kehidupan Sehari-hari
 Aplikasi Larutan Buffer dalam Kehidupan Sehari-hari Buat apa sih belajar tapi gak dipake? Pertanyaan ini tuh selalu muncul di otak gue tiap ngadepin pelajaran yang bikin gue mabok 3 x 24 jam. Dan mungkin
Aplikasi Larutan Buffer dalam Kehidupan Sehari-hari Buat apa sih belajar tapi gak dipake? Pertanyaan ini tuh selalu muncul di otak gue tiap ngadepin pelajaran yang bikin gue mabok 3 x 24 jam. Dan mungkin
LAPORAN PRATIKUM II PRATIKUM PH METER DAN PERSIAPAN LARUTAN PENYANGGA
 LAPORAN PRATIKUM II PRATIKUM PH METER DAN PERSIAPAN LARUTAN PENYANGGA NAMA : ASTRID SISKA PRATIWI (147008007) IKA WARAZTUTY (147008019) PRODI : MAGISTER ILMU BIOMEDIK TGL PRATIKUM : 10 MARET 2015 TUJUAN
LAPORAN PRATIKUM II PRATIKUM PH METER DAN PERSIAPAN LARUTAN PENYANGGA NAMA : ASTRID SISKA PRATIWI (147008007) IKA WARAZTUTY (147008019) PRODI : MAGISTER ILMU BIOMEDIK TGL PRATIKUM : 10 MARET 2015 TUJUAN
Sumber: Silberberg, Chemistry: The Molecular Nature of Matter and Change
 Bab VII ph Larutan Asam-Basa Sumber: Silberberg, Chemistry: The Molecular Nature of Matter and Change Indikator universal dan kertas lakmus digunakan untuk mengindentifikasi ph larutan asam-basa. TUJUAN
Bab VII ph Larutan Asam-Basa Sumber: Silberberg, Chemistry: The Molecular Nature of Matter and Change Indikator universal dan kertas lakmus digunakan untuk mengindentifikasi ph larutan asam-basa. TUJUAN
FAKULTAS TEKNIK UNIVERSITAS NEGERI YOGYAKARTA BAHAN AJAR KIMIA DASAR
 No. BAK/TBB/SBG201 Revisi : 00 Tgl. 01 Mei 2008 Hal 1 dari 11 BAB VIII LARUTAN ASAM DAN BASA Asam dan basa sudah dikenal sejak dahulu. Istilah asam (acid) berasal dari bahasa Latin acetum yang berarti
No. BAK/TBB/SBG201 Revisi : 00 Tgl. 01 Mei 2008 Hal 1 dari 11 BAB VIII LARUTAN ASAM DAN BASA Asam dan basa sudah dikenal sejak dahulu. Istilah asam (acid) berasal dari bahasa Latin acetum yang berarti
Titrasi Asam Basa. Sophi Damayanti
 Titrasi Asam Basa Sophi Damayanti 1 Highlight Kuliah Lalu KUALITATIF KUANTITATIF Berkaitan dengan identifikasi Berkaitan dengan kadar Menjawab pertanyaan Apa Menjawab pertanyaan Berapa What chemicals are
Titrasi Asam Basa Sophi Damayanti 1 Highlight Kuliah Lalu KUALITATIF KUANTITATIF Berkaitan dengan identifikasi Berkaitan dengan kadar Menjawab pertanyaan Apa Menjawab pertanyaan Berapa What chemicals are
Bab IV Hasil dan Diskusi
 Bab IV Hasil dan Diskusi IV.1 Hasil Eksperimen Eksperimen dikerjakan di laboratorium penelitian Kimia Analitik. Suhu ruang saat bekerja berkisar 24-25 C. Data yang diperoleh mencakup data hasil kalibrasi
Bab IV Hasil dan Diskusi IV.1 Hasil Eksperimen Eksperimen dikerjakan di laboratorium penelitian Kimia Analitik. Suhu ruang saat bekerja berkisar 24-25 C. Data yang diperoleh mencakup data hasil kalibrasi
LOGO TEORI ASAM BASA
 LOGO TEORI ASAM BASA TIM DOSEN KIMIA DASAR FTP 2012 Beberapa ilmuan telah memberikan definisi tentang konsep asam basa Meskipun beberapa definisi terlihat kurang jelas dan berbeda satu sama lain, tetapi
LOGO TEORI ASAM BASA TIM DOSEN KIMIA DASAR FTP 2012 Beberapa ilmuan telah memberikan definisi tentang konsep asam basa Meskipun beberapa definisi terlihat kurang jelas dan berbeda satu sama lain, tetapi
PEMERINTAH KOTA SURABAYA DINAS PENDIDIKAN SMA NEGERI 16 SURABAYA JL. RAYA PRAPEN TELP FAX KODE POS 60299
 PEMERINTAH KOTA SURABAYA DINAS PENDIDIKAN SMA NEGERI 16 SURABAYA JL. RAYA PRAPEN TELP. 031-8415492 FAX 031-8430673 KODE POS 60299 ULANGAN AKHIR SEMESTER 2 (DUA) TAHUN PELAJARAN 2011 2012 Hari/Tanggal :
PEMERINTAH KOTA SURABAYA DINAS PENDIDIKAN SMA NEGERI 16 SURABAYA JL. RAYA PRAPEN TELP. 031-8415492 FAX 031-8430673 KODE POS 60299 ULANGAN AKHIR SEMESTER 2 (DUA) TAHUN PELAJARAN 2011 2012 Hari/Tanggal :
TEORI ASAM BASA SECARA UMUM :
 TEORI ASAM BASA SECARA UMUM : TEORI ASAM BASA Secara Umum : Cairan berasa asam dan dapat Asam : memerahkan kertas lakmus biru Basa : Garam : Cairan berasa pahit dan dapat membirukan kertas lakmus merah
TEORI ASAM BASA SECARA UMUM : TEORI ASAM BASA Secara Umum : Cairan berasa asam dan dapat Asam : memerahkan kertas lakmus biru Basa : Garam : Cairan berasa pahit dan dapat membirukan kertas lakmus merah
Laporan Praktikum Kimia ~Titrasi asam basa~
 Laporan Praktikum Kimia ~Titrasi asam basa~ -Menentukan konsentrasi NaOH dengan HCl 0,1 M- Latifa Dinna Prayudipta XI IPA 1 SMAN 3 TANGERANG SELATAN TAHUN AJARAN 2009/2010 Laporan praktikum kimia -titrasi
Laporan Praktikum Kimia ~Titrasi asam basa~ -Menentukan konsentrasi NaOH dengan HCl 0,1 M- Latifa Dinna Prayudipta XI IPA 1 SMAN 3 TANGERANG SELATAN TAHUN AJARAN 2009/2010 Laporan praktikum kimia -titrasi
SILABUS MATA PELAJARAN KIMIA SEMESTER GENAP (Peminatan Bidang MIPA)
 SILABUS MATA PELAJARAN KIMIA SEMESTER GENAP (Peminatan Bidang MIPA) Satuan Pendidikan : SMAN 7 Kupang Kelas : XI IPA Kompetensi Inti KI 1 : Menghayati dan mengamalkan ajaran agama yang dianutnya KI 2 :
SILABUS MATA PELAJARAN KIMIA SEMESTER GENAP (Peminatan Bidang MIPA) Satuan Pendidikan : SMAN 7 Kupang Kelas : XI IPA Kompetensi Inti KI 1 : Menghayati dan mengamalkan ajaran agama yang dianutnya KI 2 :
KLASIFIKASI ZAT. 1. Identifikasi Sifat Asam, Basa, dan Garam
 KLASIFIKASI ZAT Pola konsep 1. Identifikasi Sifat Asam, Basa, dan Garam Di antara berbagai zat yang ada di alam semesta ini, asam,basa, dan garam merupakan zat yang paling penting yang diamati oleh para
KLASIFIKASI ZAT Pola konsep 1. Identifikasi Sifat Asam, Basa, dan Garam Di antara berbagai zat yang ada di alam semesta ini, asam,basa, dan garam merupakan zat yang paling penting yang diamati oleh para
SOAL KIMIA 1 KELAS : XI IPA
 SOAL KIIA 1 KELAS : XI IPA PETUNJUK UU 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah soal dengan teliti sebelum Anda bekerja 3. Kerjakanlah soal anda pada lembar
SOAL KIIA 1 KELAS : XI IPA PETUNJUK UU 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah soal dengan teliti sebelum Anda bekerja 3. Kerjakanlah soal anda pada lembar
DERAJAT KEASAMAN (ph)
 LAPORAN PRAKTIKUM KIMIA DASAR DERAJAT KEASAMAN (ph) DISUSUN OLEH FAISAL ARSYAD (13513128) NURUL FIKRI (13513136) JURUSAN TEKNIK LINGKUNGAN FAKULTAS TEKNIK SIPIL DAN PERENCANAAN UNIVERSITAS ISLAM INDONESIA
LAPORAN PRAKTIKUM KIMIA DASAR DERAJAT KEASAMAN (ph) DISUSUN OLEH FAISAL ARSYAD (13513128) NURUL FIKRI (13513136) JURUSAN TEKNIK LINGKUNGAN FAKULTAS TEKNIK SIPIL DAN PERENCANAAN UNIVERSITAS ISLAM INDONESIA
Soal-Soal. Bab 7. Latihan Larutan Penyangga, Hidrolisis Garam, serta Kelarutan dan Hasil Kali Kelarutan. Larutan Penyangga
 Bab 7 Soal-Soal Latihan Larutan Penyangga, Hidrolisis Garam, serta Kelarutan dan Hasil Kali Kelarutan Larutan Penyangga 1. Berikut ini yang merupakan pasangan asam basa terkonjugasi (A) H 3 O + dan OH
Bab 7 Soal-Soal Latihan Larutan Penyangga, Hidrolisis Garam, serta Kelarutan dan Hasil Kali Kelarutan Larutan Penyangga 1. Berikut ini yang merupakan pasangan asam basa terkonjugasi (A) H 3 O + dan OH
Kelas : XI IPA Guru : Tim Guru HSPG Tanggal : Senin, 23 Mei 2016 Mata pelajaran : Kimia Waktu : WIB
 Kelas : XI IPA Guru : Tim Guru HSPG Tanggal : Senin, 23 Mei 2016 Mata pelajaran : Kimia Waktu : 10.15 11.45 WIB Petunjuk Pengerjaan Soal Berdoa terlebih dahulu sebelum mengerjakan! Isikan identitas Anda
Kelas : XI IPA Guru : Tim Guru HSPG Tanggal : Senin, 23 Mei 2016 Mata pelajaran : Kimia Waktu : 10.15 11.45 WIB Petunjuk Pengerjaan Soal Berdoa terlebih dahulu sebelum mengerjakan! Isikan identitas Anda
LEMBARAN SOAL 11. Sat. Pendidikan
 LEMBARAN SOAL 11 Mata Pelajaran Sat. Pendidikan Kelas / Program : KIMIA : SMA : XI IPA PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah soal dengan
LEMBARAN SOAL 11 Mata Pelajaran Sat. Pendidikan Kelas / Program : KIMIA : SMA : XI IPA PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah soal dengan
BAB IV TEMUAN PENELITIAN DAN PEMBAHASAN Pengkategorian Penggunaan Level Mikroskopik dalam Buku Teks. Kimia SMA pada Materi Larutan Penyangga
 BAB IV TEMUAN PENELITIAN DAN PEMBAHASAN 4.1 Temuan 4.1.1 Pengkategorian Penggunaan Level Mikroskopik dalam Buku Teks Kimia SMA pada Materi Larutan Penyangga Penggunaan level mikroskopik dalam buku teks
BAB IV TEMUAN PENELITIAN DAN PEMBAHASAN 4.1 Temuan 4.1.1 Pengkategorian Penggunaan Level Mikroskopik dalam Buku Teks Kimia SMA pada Materi Larutan Penyangga Penggunaan level mikroskopik dalam buku teks
SKL- 3: LARUTAN. Ringkasan Materi. 1. Konsep Asam basa menurut Arrhenius. 2. Konsep Asam-Basa Bronsted dan Lowry
 SKL- 3: LARUTAN 3 Menjelaskan sifat-sifat larutan, metode pengukuran dan terapannya. o Menganalisis data daya hantar listrik beberapa larutan o Mendeskripsikan konsep ph larutan o Menghitung konsentrasi
SKL- 3: LARUTAN 3 Menjelaskan sifat-sifat larutan, metode pengukuran dan terapannya. o Menganalisis data daya hantar listrik beberapa larutan o Mendeskripsikan konsep ph larutan o Menghitung konsentrasi
LAPORAN PRAKTIKUM 2. : Magister Ilmu Biolmedik : ph meter, persiapan larutan penyangga Tanggal pelaksanaan : 10 Maret 2015
 LAPORAN PRAKTIKUM NAMA PRAKTIKAN : Nini Chairani (14700801) Zakirullah Syafei (1470080) PRODI : Magister Ilmu Biolmedik JUDUL : ph meter, persiapan larutan penyangga Tanggal pelaksanaan : 10 Maret 015
LAPORAN PRAKTIKUM NAMA PRAKTIKAN : Nini Chairani (14700801) Zakirullah Syafei (1470080) PRODI : Magister Ilmu Biolmedik JUDUL : ph meter, persiapan larutan penyangga Tanggal pelaksanaan : 10 Maret 015
RENCANA PELAKSANAAN PEMBELAJARAN ( RPP )
 RENCANA PELAKSANAAN PEMBELAJARAN ( RPP ) Satuan Pendidikan : Mata Pelajaran : KIMIA Kelas/ Semester : XI / 2 Pertemuan : 1-3 Alokasi Waktu : 2 x 45 menit Pertemuan : 1 Standar Kompetensi :Memahami sifat-sifat
RENCANA PELAKSANAAN PEMBELAJARAN ( RPP ) Satuan Pendidikan : Mata Pelajaran : KIMIA Kelas/ Semester : XI / 2 Pertemuan : 1-3 Alokasi Waktu : 2 x 45 menit Pertemuan : 1 Standar Kompetensi :Memahami sifat-sifat
Bab VIII Reaksi Penetralan dan Titrasi Asam-Basa
 Bab VIII Reaksi Penetralan dan Titrasi Asam-Basa Sumber: James Mapple, Chemistry an Enquiry-Based Approach Pengukuran ph selama titrasi akan lebih akurat dengan menggunakan alat ph-meter. TUJUAN PEMBELAJARAN
Bab VIII Reaksi Penetralan dan Titrasi Asam-Basa Sumber: James Mapple, Chemistry an Enquiry-Based Approach Pengukuran ph selama titrasi akan lebih akurat dengan menggunakan alat ph-meter. TUJUAN PEMBELAJARAN
KIMIa ASAM-BASA II. K e l a s. A. Kesetimbangan Air. Kurikulum 2006/2013
 Kurikulum 2006/2013 KIMIa K e l a s XI ASAM-BASA II Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami kesetimbangan air. 2. Memahami pengaruh asam
Kurikulum 2006/2013 KIMIa K e l a s XI ASAM-BASA II Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami kesetimbangan air. 2. Memahami pengaruh asam
BAB IV HASIL DAN PEMBAHASAN
 BAB IV HASIL DAN PEMBAHASAN Penelitian ini merupakan Penelitian Tindakan Kelas (Classroom Action Research). Penelitian Tindakan Kelas ini dilaksanakan di SMAN 1 Kota Bengkulu pada kelas XI IPA 4 untuk
BAB IV HASIL DAN PEMBAHASAN Penelitian ini merupakan Penelitian Tindakan Kelas (Classroom Action Research). Penelitian Tindakan Kelas ini dilaksanakan di SMAN 1 Kota Bengkulu pada kelas XI IPA 4 untuk
KESEIMBANGAN ASAM BASA
 LAPORAN PRAKTIKUM PRAKTIKUM PH METER, PERSIAPAN LARUTAN PENYANGGA NAMA PRAKTIKAN : Fani Nuryana Manihuruk (NIM 147008013) Mesrida Simarmata (NIM 147008011) HARI/TGL. PRAKTIKUM : Selasa, 10 Maret 2015 TUJUAN
LAPORAN PRAKTIKUM PRAKTIKUM PH METER, PERSIAPAN LARUTAN PENYANGGA NAMA PRAKTIKAN : Fani Nuryana Manihuruk (NIM 147008013) Mesrida Simarmata (NIM 147008011) HARI/TGL. PRAKTIKUM : Selasa, 10 Maret 2015 TUJUAN
KIMIA (2-1)
 03035307 KIMIA (2-1) Dr.oec.troph.Ir.Krishna Purnawan Candra, M.S. Kuliah ke-9 Teori Asam Basa Bahan kuliah ini disarikan dari Chemistry 4th ed. McMurray and Fay Faperta UNMUL 2011 Pengertian Asam dan
03035307 KIMIA (2-1) Dr.oec.troph.Ir.Krishna Purnawan Candra, M.S. Kuliah ke-9 Teori Asam Basa Bahan kuliah ini disarikan dari Chemistry 4th ed. McMurray and Fay Faperta UNMUL 2011 Pengertian Asam dan
