1. Perhatikan struktur senyawa berikut!
|
|
|
- Yenny Tanudjaja
- 6 tahun lalu
- Tontonan:
Transkripsi
1 . Perhatikan struktur senyawa berikut! CH CH CH CH CH CH CH Jumlah atom C primer, atom C sekunder, dan atom C tersier dari senyawa di atas adalah...,, dan D.,, dan,, dan E.,, dan,, dan. Di bawah ini merupakan sifat alkana, kecuali... banyak terdapat pada minyak bumi seluruh ikatannya jenuh dapat mengalami substitusi D. larut baik dalam air E. mempunyai rumus molekul C nh n+. Kekhasan atom karbon yang menyebabkan unsur karbon mempunyai banyak ragam senyawa adalah... dapat membentuk rantai karbon dengan berbagai bentuk mempunyai elektron valensi yang dapat berikatan kovalen merupakan zat padat yang sangat stabil pada suhu kamar D. bentuk ruang ikatan padat atom karbon adalah tetrahedral E. mempunyai konfigurasi elektron yang belum stabil seperti gas mulia. Di antara senyawa-senyawa berikut yang mempunyai titik didih paling rendah adalah... n-pentana D. isobutana n-butana E. isopentana n-heksana 5. Hidrokarbon berikut yang merupakan hidrokarbon tak jenuh adalah... C H 8 D. C 5H C H 6 E. C H 8 C H 0 6. Senyawa etilpentana berisomer dengan... metilheptana D. n heksana,, trimetilbutana E. isopentana tetra metilmetana 7. Jumlah isomer dari C 5H adalah... D. 6 E Terdapat dua persamaan reaksi senyawa hidrokarbon berikut!. CH CH=CH + Cl CH CHCl CH Cl. CH CHOH CH CH H SO o CH 70 C CH=CH CH + H O Kedua jenis reaksi tersebut berturut-turut disebut reaksi... adisi dan eliminasi substitusi dan eliminasi adisi dan substitusi D. eliminasi dan adisi E. eliminasi dan substitusi 9. Jika butena diadisi dengan HCl maka senyawa yang terbentuk adalah... klorobutana klorobutana klorobutana D. metilbutana E. kloropropana 0. Produk utama dari reaksi kimia antara metil propena dengan Br adalah..., dibromo metilpropana, dibromo metilpropana, dibromo metilpropana D., dibromo metilpropana E., dibromo metilpropana. Cara yang digunakan untuk memisahkan fraksifraksi dalam minyak bumi dari minyak mentah pengeboran pemanasan direaksikan dengan asam D. direaksikan dengan basa E. penyulingan bertingkat. Bahan bakar untuk pesawat terbang solar D. petroleum eter avtur E. LPG kerosin. Bensin jenis premium memiliki bilangan oktan sebesar. 8 D E Bensin dengan nilai oktan 95% artinya mempunyai komposisi. 95% isooktana dan 5% n-heptana 95 n-heptana dan 5% isooktana 95% n-oktana dan 5% n-heptana D. 95% n-oktana dan 5% isooktana E. 95% isooktana dan 5% n-oktana 5. Fraksi minyak bumi berdasarkan kenaikan titik didihnya bensin minyak tanah solar minyak tanah solar - bensin solar bensin minyak tanah D. minyak tanah bensin solar E. solar minyak tanah bensin 6. Zat yang ditambahkan ke dalam bensin untuk menaikan nilai oktannya partamax dan pertamax plus LPG dan TEL TEL dan dibromoetana D. MTBE dan LNG E. TEL dan MTBE 7. Zat berbahaya bagi kesehatan yang dihasilkan dari asap kendaraan bermotor CO dan jelaga D. CO dan O CO dan uap air E. CO dan CO CO dan timbal 8. Sebuah kristal KNO dimasukkan ke dalam tabung reaksi, kemudian ditetesi dengan air. Pada dasar tabung terasa dingin. Reaksi ini digolongkan...
2 eksoterm, berpindah dari sistem ke lingkungan eksoterm, berpindah dari lingkungan ke sistem endoterm, berpindah dari sistem ke lingkungan D. endoterm, berpindah dari lingkungan ke sistem E. endoterm, tidak berpindah 9. Perhatikan gambar berikut. Yang merupakan reaksi eksoterm dan D. dan 5 dan E. dan 5 dan 0. Persamaan reaksi yang perubahan entalpinya dapat disebut sebagai entalpi pembentukan ialah. N (g) + H (g) NH (g) H = -9, kj CH (g) +O (g) CO (g) + H O(g) H=-890 kj C(s) + H (g) + O (g) C H O (l) H = -87 kj D. SO (g) + H O(l) H SO (l) H = -00 kj E. Ca(s) + Cl(g) CaCl (s) H = kj. Untuk menguraikan mol CaCO menjadi CaO dan CO diperlukan 78 kj. Diagram tingkat yang sesuai dengan data tersebut D. CaCO CaO + CO CaO + CO CaCO CaO + CO CaCO CaCO CaO + CO H = -78 H = +78 H = +78 H = +78kJ E. CaO + CO CaCO H = -78 kj. Perhatikan data hasil pembakaran 00 gram beberapa bahan bakar dengan jumlah jelaga yang dihasilkan: Nama Bahan Bakar Jelaga yang Dihasilkan P 5 0 gram Q 0 0, gram R 0 0 gram S 0 0 gram T 0 gram Bahan bakar yang memiliki angka oktan yang paling tinggi adalah... P D. S Q E. T R. Pada diagram siklus berikut: S(s) + O(g) SO(g) H = 9 kj SO(g) + O(g) H = 7 kj ΔH pembentukan SO adalah... (UAN 0) 0 kj D. 790 kj 0 kj E. 80 kj 675 kj. Diketahui: H f H O (g) = kj/mol H f CO (g) = 9 kj/mol H f C H (g) = 5 kj/mol Sebanyak gram C H dibakar secara sempurna akan dihasilkan kalor sebesar. (Ar C = H = ) 80 kj D. 978 kj 60 kj E. 987 kj 89 kj 5. Diketahui ikatan rata-rata: Cl Cl = kj/mol H Cl = kj/mol O H = 6 kj/mol O = O = 98 kj/mol Preubahan entalpi untuk reaksi: Cl (g) + H O(g) HCl(g) + O (g) adalah... kj D. +8 kj kj E. + kj 8 kj 6. Pada reaksi: NH (g) N (g) + H (g) H = +9 Energi ikatan rata-rata N N dan H H berturutturut 96 kj dan 6 kj, maka ikatan ratarata N H adalah....7,0 kj D. 95,5 kj 586,5 kj E. 59,5 kj 9,0 kj
3 7. Jika 00 ml larutan NaOH M direaksikan dengan 00 ml larutan HCl M dalam sebuah bejana, ternyata suhu larutan naik dari 9 o C menjadi 9 o Larutan dianggap sama dengan air, kalor jenis air =, J/g cm. Maka H netralisasi 8, kjmol - D. 8 kjmol - + 8, kjmol - E. +80 kjmol kjmol - 8. Untuk membuat 500 ml larutan NaOH 0, M diperlukan kristal NaOH murni sebanyak... (Ar Na =, O=6, H = ) 0 gram D. gram 0 gram E.,5 gram 0 gram 9. Untuk mengubah 00 ml larutan H SO 0,5 M menjadi 0, M diperlukan air sebanyak ml D. 00 ml 50 ml E. 500 ml 50 ml 0. Sebanyak 00 ml NaOH 0, M dicampur dengan 00 ml Ca(OH) 0, M. Kemolaran larutan yang didapat adalah... 0,05 D. 0,5 0,0 E.,50 0,5. Laju reaksi: NH (g) + 5 O (g) NO(g) + 6 H O(g) dapat dinyatakan sebagai... laju bertambahnya konsentrasi NH dalam satu satuan waktu laju berkurangnya konsentrasi H O dalam satu satuan waktu laju bertambahnya konsentrasi O dalam satu satuan waktu D. laju berkurangnya tekanan sistem dalam satu satuan waktu E. laju bertambahnya konsentrasi NO dalam satu satuan waktu. Data percobaan reaksi antara kalsium karbonat dengan larutan asam klorida: No CaCO (s) HCl(aq) Suhu ( o C) gram serbuk M 5 gram kepingan M 0 gram serbuk M 5 gram serbuk M 0 5 gram serbuk M 0 Reaksi paling cepat terjadi pada percobaan nomor. D. E. 5. Data percobaan reaksi gram kalsium karbonat dengan asam klorida berlebih: Percob Bentuk Suhu Waktu HCl zat Serbuk Serbuk Serbuk butiran M M M M 0 o C 0 o C 8 o C 0 o C 0 detik 0 detik 5 detik 5 detik Dari percobaan dan diperoleh kesimpulan. reaksi dalam bentuk serbuk lebih cepat dibanding butiran makin tinggi suhu, laju reaksi makin bertambah katalis mempercepat laju reaksi D. laju reaksi dalam bentuk butiran lebih cepat dibanding kepingan E. semakin besar konsentrasi pereaksi, makin cepat laju reaksinya. Berikut ini beberapa gambar proses pelarutan gula dengan massa yang sama. Gambar yang laju reaksinya hanya dipengaruhi oleh suhu adalah... menjadi D. menjadi menjadi E. menjadi 5 menjadi 5. Data hasil eksperimen dari reaksi: Percobaan [F ] M [ClO ] M Laju awal 0, 0,0, 0-0, 0,0,8 0-0, 0,0, 0 - Laju reaksi yang terjadi jika konsentrasi F dan ClO masing-masing 0, M dan 0, M k (0,) (0,) D. k (0,) k (0,) (0,) E. k (0,) k (0,) (0,) 6. Pada reaksi P + Q R, diperoleh data: No [P] [Q] Waktu(detik) 0,0 0,06 6 0,0 0,06 8 0,0 0, Bila harga k = 0-5, maka persamaan laju reaksi yang sesuai dengan data tersebut adalah... v =,0 0-5 [P] [Q] v =,0 0-5 [P] [Q] v =,0 0-5 [P] [Q] D. v =,0 0-5 [P] [Q] E. v =,0 0-5 [Q] 7. Laju reaksi (r) antara A dan B mengikuti persamaan laju: r = k [A] [B] dengan k adalah konstanta laju reaksi, konsentrasi A pada suatu percobaan dijadikan setengah kali semula. Untuk membuat laju reaksi menjadi empat kali semula, maka konsentrasi B harus... dinaikan kali semula diturunkan ¼ kali semula dinaikan kali semula D. diturunkan ½ kali semula E. dibuat tetap (konstan)
4 8. Percobaan penentuan laju reaksi: H (g) + NO(g) H O(g) + N (g) No [H ] [N ] Laju awal (M/s) 0,0 0,0 0,0 0,0 6 0,0 0,0 56 Harga tetapan laju reaksi (mol - L S - ) dari reaksi tersebut adalah... 0 D E Pada suhu 7 o C, gas brom dapat bereaksi dengan gas nitrogen monoksida menurut persamaan reaksi. Percobaan Konsentrasi Awal (M) NO Br 0, 0,05 6 0, 0,0 Laju Reaksi Awal (Ms - ) 0, 0,0 Laju reaksi bila konsentrasi gas NO = 0,0 M dan gas Br = 0,0 M adalah... 0,0 D.,800 0,8 E.,00,00 0. Perhatikan data pada tabel percobaan dari reaksi berikut! No Suhu ( o C) Volume H (ml) Waktu (detik) Laju reaks pembentukan gas H adalah... 0,0 ml.det - D. 0,5 ml.det - 0,05 ml.det - E. 0,50 ml.det - 0,0 ml.det -. Tiap kenaikan 0 o C laju reaksi suatu zat akan naik dua kali semula. Jika pada suhu 0 o C reaksi tersebut berlangsung selama menit, maka pada suhu 70 o C reaksi tersebut akan berlangsung selama... ¼ menit D. menit ½ menit E. menit menit. Suatu reaksi berlangsung pada suhu 0 Bila pada setiap kenaikan 0 C tetapan kecepatan reaksinya meningkat kali, maka kecepatan reaksi pada suhu 60 C dibandingkan pada suhu 0 C akan meningkat... kali D. kali 8 kali E. 6 kali 6 kali. Reaksi keseimbangan di bawah ini yang menghasilkan lebih banyak pereaksi reaksi jika volumenya diperbesar adalah... NO(g) + O (g) NO (g) C(s) + O (g) CO (g) CaCO (s) CaO(s) + CO (g) D. N O (g) NO (g) E. HI(g) H (g) + I (g). Pada reaksi: N (g) + H (g) NH (g) H = kkal, Untuk memperoleh hasil yang banyak, maka yang harus dilakukan adalah. digunakan katalis tekanan diperkecil ditambah gas NH D. volume diperbesar E. suhu diturunkan 5. Larutan FeCl bereaksi dengan larutan KSCN membentuk ion FeSCN + yang berwarna merah menurut persamaan : Fe + (aq) + SCN - (aq) Fe(SCN) + (aq) Apabila pada suhu tetap pada sistem itu ditambah air maka. seimbang akan bergeser ke kanan, warna makin merah dan harga K bertambah seimbang bergeser ke kiri, warna makin merah, dan harga K berkurang seimbang bergeser ke kiri, warna luntur, dan harga K berkurang D. seimbang bergeser ke kiri, warna luntur tetapi harga K tetap E. seimbang tidak bergeser 6. Pada reaksi keseimbangan: H (g) + I (g) HI(g) H = x kj Jika suhu dinaikan, maka hasil keseimbangan... bergeser ke kanan, harga K tetap bergeser ke kanan, harga K bertambah bergeser ke kanan, harga K berkurang D. bergeser ke kiri, harga K berkurang E. bergeser ke kiri, harga K bertambah 7. Tetapan keseimbangan reaksi: Sn(s) + Cl (g) SnCl (g) diberikan oleh... [Sn][Cl] [Cl] K c = D. K c = K c = E. K c = [Sn][Cl] [Cl] K c = [Cl] 8. Pada reaksi keseimbangan: CO(g) + H (g) CH (g) + H O(g) Dalam wadah 0 liter diperoleh data sebagai berikut: CO H CH H O Mula mol mol - - Reaksi 0,5 mol,5 mol 0,5 mol 0,5 mol Sisa,5 mol,5 mol 0,5 mol 0,5 mol Harga Kc dari reaksi tersebut [0,5][0,5] [0,05][0,05] Kc = Kc = D. [,5][,5] [0,5][0,5] Kc = E. [,5],5] [0,05][0,05] Kc = [0,5]0,5] [0,5]0,5] [0,5][0,5] Kc = [0,05]0,05] 9. Dalam volume L dipanaskan mol HI terjadi reaksi: HI(g) H (g) + I (g) Jika I yang terbentuk = 0, mol, maka harga tetapan keseimbangan tersebut adalah...
5 D. E Dalam ruang 5 liter berlangsung reaksi keseimbangan: SO (g) SO (g) + O (g) Pada pemanasan mol gas SO diperoleh 0,5 mol gas O, maka tetapan keseimbangan adalah. 0,0 D.,00 0,05 E.,00 0,5 5. Pada reaksi keseimbangan dari CO (g) + H O (g) CO (g) + H (g) harga K = 0,80. Untuk menghasilkan mol H per liter dari 6 mol H O per liter, jumlah gas CO yang ditambahkan adalah mol/l D. 0 E Sebanyak,5 mol NOCl ditempatkan dalam wadah tertutup bervolume L pada 800 o Setelah keseimbangan tercapai (60% NOCl) terurai menurut reaksi: NOCl(g) NO(g) + Cl (g) Harga Kc untuk reaksi keseimbangan tersebut D. E Pada reaksi: PCl 5(g) PCl (g) + Cl (g) Mempunyai nilai Kp =,5 pada suhu 50 o Pada suhu tersebut tekanan parsial gas PCl 5 dan gas PCl saat keseimbangan adalah 0,90 atm dan 0,75 atm, maka tekanan parsial gas Cl (dalam atm) 0,5 D.,50 0,75 E.,65 0,90 5. Dalam volume L dipanaskan mol gas N O terjadi reaksi: N O (g) NO (g). Jika N O yang terurai sebesar 50% dan tekanan total gas pada keseimbangan 6 atm maka harga Kp,0 D. 8,0,0 E. 0,0 6,0 55. Dalam suatu wadah tertutup, amonium klorida dipanaskan pada suhu 00 o C dan terjadi reaksi: NH Cl(s) NH (g) + HCl(g) Jika pada suhu tersebut K p = a (tekanan dalam atm), maka tekanan total dalam wadah (dalam atm) adalah... a D. a a E. a a 56. Jika natrium bikarbonat dipanaskan menurut reaksi : NaHCO (s) Na CO (s) + H O(g) + CO (g) Ternyata tekanan total pada keseimbangan adalah 5 atm. Harga K p untuk reaksi tersebut 5 D.,5 6,5 E Pada reaksi keseimbangan : PCl 5(g) PCl (g) + Cl (g). Harga K c pada suhu 9 o C =,6 0 - M, maka harga K p pada suhu tersebut atm D.,8 atm, atm E.,5 atm atm 58. Diketahui reaksi keseimbangan: NH (g) N (g) + H (g) Jika 0,5 mol gas NH dimasukkan ke dalam wadah sebesar liter dan dipanaskan pada suhu 00 o C terbentuk 0,6 mol gas H. Pada keadaan seimbang derajat disosiasinya 0, D. 0,8 0, E.,0 0,6 59. SO (Mr = 80) sebanyak 60 gram dipanaskan dalam wadah bervolume L dan terjadi reaksi: SO (g) SO (g) + O (g). Pada saat seimbang perbandingan mol SO : O = :, maka derajat disosiasi SO D. E. 60. Diketahui reaksi keseimbangan: H + Cl HCl K = 0 N + H NH K = 5 0 N + H + Cl NH Cl K = 0 8 Harga K untuk reaksi NH + HCl NH Cl adalah.,0 0 D.,0 0,0 0 E.,0 0 8,6 0
6 C B D B A A D C 5 E 5 A 6 B 6 C 7 A 7 D 8 A 8 D 9 A 9 D 0 D 0 D E E B D B E A B 5 A 5 C 6 E 6 C 7 C 7 A 8 D 8 D 9 A 9 B 0 C 0 E A C A E 5 D 6 D 7 C 8 C 9 B 50 B 5 D 5 A 5 D 5 D 55 E 56 B 57 C 58 D 59 E 60 A
KESETIMBANGAN KIMIA SOAL DAN PEMBAHASAN
 KESETIMBANGAN KIMIA SOAL DAN PEMBAHASAN 1. Suatu reaksi dikatakan mencapai kesetimbangan apabila. A. laju reaksi ke kiri sama dengan ke kanan B. jumlah koefisien reaksi ruas kiri sama dengan ruas kanan
KESETIMBANGAN KIMIA SOAL DAN PEMBAHASAN 1. Suatu reaksi dikatakan mencapai kesetimbangan apabila. A. laju reaksi ke kiri sama dengan ke kanan B. jumlah koefisien reaksi ruas kiri sama dengan ruas kanan
2. Konfigurasi elektron dua buah unsur tidak sebenarnya:
 . Atom X memiliki elektron valensi dengan bilangan kuantum: n =, l =, m = 0, dan s =. Periode dan golongan yang mungkin untuk atom X adalah A. dan IIIB B. dan VA C. 4 dan III B D. 4 dan V B E. 5 dan III
. Atom X memiliki elektron valensi dengan bilangan kuantum: n =, l =, m = 0, dan s =. Periode dan golongan yang mungkin untuk atom X adalah A. dan IIIB B. dan VA C. 4 dan III B D. 4 dan V B E. 5 dan III
K13 Revisi Antiremed Kelas 11 Kimia
 K13 Revisi Antiremed Kelas 11 Kimia Persiapan UTS Semester Ganjil Doc. Name: RK13AR11KIM01UTS Doc. Version: 2016-10 halaman 1 01. Sebenarnya kimia organik dan anorganik tidaklah perlu dipisah-pisahkan,
K13 Revisi Antiremed Kelas 11 Kimia Persiapan UTS Semester Ganjil Doc. Name: RK13AR11KIM01UTS Doc. Version: 2016-10 halaman 1 01. Sebenarnya kimia organik dan anorganik tidaklah perlu dipisah-pisahkan,
SOAL KIMIA 2 KELAS : XI IPA
 SOAL KIMIA KELAS : XI IPA PETUNJUK UMUM. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan. Periksa dan bacalah soal dengan teliti sebelum Anda bekerja. Kerjakanlah soal anda pada lembar jawaban
SOAL KIMIA KELAS : XI IPA PETUNJUK UMUM. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan. Periksa dan bacalah soal dengan teliti sebelum Anda bekerja. Kerjakanlah soal anda pada lembar jawaban
LEMBAR AKTIVITAS SISWA ( LAS )_ 1
 LEMBAR AKTIVITAS SISWA ( LAS )_ 1 1. Perhatikan reaksi berikut: CaCO 2 (s) CaO (s) + CO 2 (g) H = 178 KJ/mol. Jelaskan! a. Arah kesetimbangan ditambahkan CaCO 2 (s) b. Tiga kemungkinan yang dapat dilakukan
LEMBAR AKTIVITAS SISWA ( LAS )_ 1 1. Perhatikan reaksi berikut: CaCO 2 (s) CaO (s) + CO 2 (g) H = 178 KJ/mol. Jelaskan! a. Arah kesetimbangan ditambahkan CaCO 2 (s) b. Tiga kemungkinan yang dapat dilakukan
Contoh Soal & Pembahasan Reaksi Kesetimbangan
 Soal No.1 Contoh Soal & Pembahasan Reaksi Kesetimbangan Reaksi kimia ada yang berlangsung searah (berkesudahan) dan ada yang dapat balik (bolak-balik). Jelaskan perbedaanya disertai dengan contoh-contohnya.
Soal No.1 Contoh Soal & Pembahasan Reaksi Kesetimbangan Reaksi kimia ada yang berlangsung searah (berkesudahan) dan ada yang dapat balik (bolak-balik). Jelaskan perbedaanya disertai dengan contoh-contohnya.
SOAL UJIAN AKHIR SEMESTER 2 KIMIA KELAS X (SEPULUH) TP. 2008/2009
 SOAL UJIAN AKHIR SEMESTER 2 KIMIA KELAS X (SEPULUH) TP. 2008/2009 1. Dari suatu percobaan daya hantar listrik suatu larutan diperoleh data sebagai berikut: Percobaan Larutan Lampu Gelembung gas 1 2 3 4
SOAL UJIAN AKHIR SEMESTER 2 KIMIA KELAS X (SEPULUH) TP. 2008/2009 1. Dari suatu percobaan daya hantar listrik suatu larutan diperoleh data sebagai berikut: Percobaan Larutan Lampu Gelembung gas 1 2 3 4
OAL TES SEMESTER I. I. Pilihlah jawaban yang paling tepat! a. 2d d. 3p b. 2p e. 3s c. 3d 6. Unsur X dengan nomor atom
 KIMIA XI SMA 3 S OAL TES SEMESTER I I. Pilihlah jawaban yang paling tepat!. Elektron dengan bilangan kuantum yang tidak diizinkan n = 3, l = 0, m = 0, s = - / n = 3, l =, m =, s = / c. n = 3, l =, m =
KIMIA XI SMA 3 S OAL TES SEMESTER I I. Pilihlah jawaban yang paling tepat!. Elektron dengan bilangan kuantum yang tidak diizinkan n = 3, l = 0, m = 0, s = - / n = 3, l =, m =, s = / c. n = 3, l =, m =
LATIHAN ULANGAN KIMIA : HIDROKARBON KELAS X
 LATIHAN ULANGAN KIMIA : HIDROKARBON KELAS X Pilihlah salah satu jawaban yang paling tepat! 1. Alkana yang tidak mengandung lima atom karbon yaitu.... a. n-pentena b. 2-metil-butana c. isopentana d. 2-metil-pentana
LATIHAN ULANGAN KIMIA : HIDROKARBON KELAS X Pilihlah salah satu jawaban yang paling tepat! 1. Alkana yang tidak mengandung lima atom karbon yaitu.... a. n-pentena b. 2-metil-butana c. isopentana d. 2-metil-pentana
Soal Pilihan Ganda Berilah tanda silang pada huruf A, B, C, D atau E di depan jawaban yang benar!
 Soal Pilihan Ganda Berilah tanda silang pada huruf A, B, C, D atau E di depan jawaban yang benar!. Berikut ini adalah ciri-ciri terjadinya reaksi kesetimbangan, kecuali. reaksi reversibel B. terjadi dalam
Soal Pilihan Ganda Berilah tanda silang pada huruf A, B, C, D atau E di depan jawaban yang benar!. Berikut ini adalah ciri-ciri terjadinya reaksi kesetimbangan, kecuali. reaksi reversibel B. terjadi dalam
LEMBARAN SOAL 7. Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA )
 LEMBARAN SOAL 7 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA ) PETUNJUK UMUM. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan. Periksa dan bacalah soal
LEMBARAN SOAL 7 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA ) PETUNJUK UMUM. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan. Periksa dan bacalah soal
SOAL-SOAL KESETIMBANGAN KIMIA
 H=+380 kj/mol SOAL-SOAL KESETIMBANGAN KIMIA 1. Ebtanas 99 Suatu reaksi berada dalam keadaan setimbang apabila A. Reaksi ke kanan dan kiri telah berhenti B. Mol pereaksi selalu sama dengan mol hasil reaksi
H=+380 kj/mol SOAL-SOAL KESETIMBANGAN KIMIA 1. Ebtanas 99 Suatu reaksi berada dalam keadaan setimbang apabila A. Reaksi ke kanan dan kiri telah berhenti B. Mol pereaksi selalu sama dengan mol hasil reaksi
BAB 1 1. Atom karbon mempunyai ke khasan. Pernyataan yang tepat mengenai kekhasan atom karbon
 SOAL DAN PEMBAHASAN KIMIA KELAS XI SEMESTER 1 BAB 1 1. Atom karbon mempunyai ke khasan. Pernyataan yang tepat mengenai kekhasan atom karbon adalah A. Karbon mempunyai 4 elektron valensi yang mampu membentuk
SOAL DAN PEMBAHASAN KIMIA KELAS XI SEMESTER 1 BAB 1 1. Atom karbon mempunyai ke khasan. Pernyataan yang tepat mengenai kekhasan atom karbon adalah A. Karbon mempunyai 4 elektron valensi yang mampu membentuk
LEMBARAN SOAL 5. Pilih satu jawaban yang benar!
 LEMBARAN SOAL 5 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah
LEMBARAN SOAL 5 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah
MODUL KIMIA SMA IPA Kelas 11
 SMA IPA Kelas Di sekitar kita banyak dijumpai peristiwa reaksi kimia, misalnya reaksi pembakaran kayu, pembakaran bensin, fotosintesis, perkaratan besi dan lain sebagainya. Dalam reaksi kimia, ada reaksi
SMA IPA Kelas Di sekitar kita banyak dijumpai peristiwa reaksi kimia, misalnya reaksi pembakaran kayu, pembakaran bensin, fotosintesis, perkaratan besi dan lain sebagainya. Dalam reaksi kimia, ada reaksi
KIMIA 2 KELAS X. D. molekul-molekul kovalen yang bereaksi dengan air E. molekul-molekul kovalen yang bergerak bebas di dalam air
 KIMIA 2 KELAS X PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah soal dengan teliti sebelum Anda bekerja 3. Kerjakanlah soal anda pada lembar jawaban
KIMIA 2 KELAS X PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah soal dengan teliti sebelum Anda bekerja 3. Kerjakanlah soal anda pada lembar jawaban
H = H hasil reaksi H pereaksi. Larutan HCl
 Standar Kompetensi Kompetensi Dasar Memahami perubahan energi dalam kimia, cara pengukuran dan sifat ketidakteraturan dalam alam semesta. Menjelaskan pengertian tentang entalpi suatu zat dan perubahannya.
Standar Kompetensi Kompetensi Dasar Memahami perubahan energi dalam kimia, cara pengukuran dan sifat ketidakteraturan dalam alam semesta. Menjelaskan pengertian tentang entalpi suatu zat dan perubahannya.
1. Isilah Biodata anda dengan lengkap (di lembar Jawaban) Tulis dengan huruf cetak dan jangan disingkat!
 Petunjuk : 1. Isilah Biodata anda dengan lengkap (di lembar Jawaban) Tulis dengan huruf cetak dan jangan disingkat! 2. Soal Teori ini terdiri dari dua bagian: A. 30 soal pilihan Ganda : 60 poin B. 5 Nomor
Petunjuk : 1. Isilah Biodata anda dengan lengkap (di lembar Jawaban) Tulis dengan huruf cetak dan jangan disingkat! 2. Soal Teori ini terdiri dari dua bagian: A. 30 soal pilihan Ganda : 60 poin B. 5 Nomor
BAB VI KINETIKA REAKSI KIMIA
 BANK SOAL SELEKSI MASUK PERGURUAN TINGGI BIDANG KIMIA 1 BAB VI 1. Padatan NH 4 NO 3 diaduk hingga larut selama 77 detik dalam akuades 100 ml sesuai persamaan reaksi berikut: NH 4 NO 2 (s) + H 2 O (l) NH
BANK SOAL SELEKSI MASUK PERGURUAN TINGGI BIDANG KIMIA 1 BAB VI 1. Padatan NH 4 NO 3 diaduk hingga larut selama 77 detik dalam akuades 100 ml sesuai persamaan reaksi berikut: NH 4 NO 2 (s) + H 2 O (l) NH
LEMBARAN SOAL 10. Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH) Pilihlah jawaban yang paling tepat.
 LEMBARAN SOAL 10 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan. Periksa dan bacalah soal dengan
LEMBARAN SOAL 10 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan. Periksa dan bacalah soal dengan
a. Ion c. Molekul senyawa e. Campuran b. Molekul unsur d. Unsur a. Air c. Kuningan e. Perunggu b. Gula d. Besi
 A. PILIHAN GANDA 1. Molekul oksigen atau O2 merupakan lambang dari partikel a. Ion c. Molekul senyawa e. Campuran b. Molekul unsur d. Unsur 2. Di antara zat berikut yang merupakan unsur ialah... a. Air
A. PILIHAN GANDA 1. Molekul oksigen atau O2 merupakan lambang dari partikel a. Ion c. Molekul senyawa e. Campuran b. Molekul unsur d. Unsur 2. Di antara zat berikut yang merupakan unsur ialah... a. Air
 TRY OUT SELEKSI OLIMPIADE TINGKAT KABUPATEN/KOTA 2010 TIM OLIMPIADE KIMIA INDONESIA 2011 Waktu: 150 Menit PUSAT KLINIK PENDIDIKAN INDONESIA (PKPI) bekerjasama dengan LEMBAGA BIMBINGAN BELAJAR SSCIntersolusi
TRY OUT SELEKSI OLIMPIADE TINGKAT KABUPATEN/KOTA 2010 TIM OLIMPIADE KIMIA INDONESIA 2011 Waktu: 150 Menit PUSAT KLINIK PENDIDIKAN INDONESIA (PKPI) bekerjasama dengan LEMBAGA BIMBINGAN BELAJAR SSCIntersolusi
Sebutkan data pada kalor yang diserap atau dikeluarkan pada sistem reaksi!
 contoh soal termokimia dan pembahasannya 1. Apa yang dimaksud dengan energi kinetik dan energi potensial? Jawab : Energi kinetik adalah energi yang terkandung di dalam materi yang bergerak, sedangkan energi
contoh soal termokimia dan pembahasannya 1. Apa yang dimaksud dengan energi kinetik dan energi potensial? Jawab : Energi kinetik adalah energi yang terkandung di dalam materi yang bergerak, sedangkan energi
1. Salah satu faktor yang menyebabkan senyawa karbon banyak jumlahnya adalah...
 1. Salah satu faktor yang menyebabkan senyawa karbon banyak jumlahnya adalah... A. Karbon melimpah di kulit bumi B. Karbon memiliki 4 elektron valensi C. Dapat membentuk rantai atom karbon D. Titik didih
1. Salah satu faktor yang menyebabkan senyawa karbon banyak jumlahnya adalah... A. Karbon melimpah di kulit bumi B. Karbon memiliki 4 elektron valensi C. Dapat membentuk rantai atom karbon D. Titik didih
kecuali . kecuali . kecuali
 1. Berikut ini adalah ciri-ciri terjadinya reaksi kesetimbangan, kecuali. A. reaksi reversibel B. terjadi dalam ruang tertutup C. laju reaksi ke kiri sama dengan laju reaksi ke kanan D. reaksinya tidak
1. Berikut ini adalah ciri-ciri terjadinya reaksi kesetimbangan, kecuali. A. reaksi reversibel B. terjadi dalam ruang tertutup C. laju reaksi ke kiri sama dengan laju reaksi ke kanan D. reaksinya tidak
MODUL KESETIMBANGAN. Perhatikan reaksi berikut
 MODUL KESETIMBANGAN Perhatikan reaksi berikut a.n 2 (g) + 3H 2 (g) 2NH 3 (g), di sebut juga reaksi... b. N 2 (g) + 3H 2 (g) 2NH 3 (g), di sebut juga reaksi... Perhatikan reaksi: Maka persamaan laju reaksi
MODUL KESETIMBANGAN Perhatikan reaksi berikut a.n 2 (g) + 3H 2 (g) 2NH 3 (g), di sebut juga reaksi... b. N 2 (g) + 3H 2 (g) 2NH 3 (g), di sebut juga reaksi... Perhatikan reaksi: Maka persamaan laju reaksi
TERMOKIMIA. Hukum Hess Perubahan entalpi reaksi tetap sama, baik berlangsung dalam satu tahap maupun beberapa tahap.
 TERMOKIMIA (Teori) Entalpi adalah jumlah total energi kalor yang terkandung dalam suatu materi Reaksi Eksoterm Menghasilkan kalor Melepas energi Perubahan entalpi negatif Reaksi Endoterm Menyerap kalor
TERMOKIMIA (Teori) Entalpi adalah jumlah total energi kalor yang terkandung dalam suatu materi Reaksi Eksoterm Menghasilkan kalor Melepas energi Perubahan entalpi negatif Reaksi Endoterm Menyerap kalor
MODUL 1 TERMOKIMIA. A. Hukum Pertama Termodinamika. B. Kalor Reaksi
 MODUL 1 TERMOKIMIA Termokimia adalah ilmu yang mempelajari hubungan antara energi panas dan energi kimia. Sebagai prasyarat untuk mempelajari termokimia, kita harus mengetahui tentang perbedaan kalor (Q)
MODUL 1 TERMOKIMIA Termokimia adalah ilmu yang mempelajari hubungan antara energi panas dan energi kimia. Sebagai prasyarat untuk mempelajari termokimia, kita harus mengetahui tentang perbedaan kalor (Q)
KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI
 KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI 1. Untuk membuat 500 ml larutan H 2 SO 4 0.05 M dibutuhkan larutan H 2 SO 4 5 M sebanyak ml a. 5 ml b. 10 ml c. 2.5 ml d. 15 ml e. 5.5 ml 2. Konsentrasi larutan yang
KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI 1. Untuk membuat 500 ml larutan H 2 SO 4 0.05 M dibutuhkan larutan H 2 SO 4 5 M sebanyak ml a. 5 ml b. 10 ml c. 2.5 ml d. 15 ml e. 5.5 ml 2. Konsentrasi larutan yang
LEMBARAN SOAL 6. Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH )
 LEMBARAN SOAL 6 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah soal dengan
LEMBARAN SOAL 6 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah soal dengan
SOAL SELEKSI OLIMPIADE SAINS TINGKAT KABUPATEN/KOTA 2004 CALON TIM OLIMPIADE KIMIA INDONESIA
 SOAL SELEKSI OLIMPIADE SAINS TINGKAT KABUPATEN/KOTA 2004 CALON TIM OLIMPIADE KIMIA INDONESIA 2005 Bidang Kimia KEMENTERIAN PENDIDIKAN DAN KEBUDAYAAN DIREKTORAT JENDERAL PENDIDIKAN MENENGAH DIREKTORAT PEMBINAAN
SOAL SELEKSI OLIMPIADE SAINS TINGKAT KABUPATEN/KOTA 2004 CALON TIM OLIMPIADE KIMIA INDONESIA 2005 Bidang Kimia KEMENTERIAN PENDIDIKAN DAN KEBUDAYAAN DIREKTORAT JENDERAL PENDIDIKAN MENENGAH DIREKTORAT PEMBINAAN
PAKET UJIAN NASIONAL 17 Pelajaran : KIMIA Waktu : 120 Menit
 PAKET UJIAN NASIONAL 17 Pelajaran : KIMIA Waktu : 120 Menit Pilihlah salah satu jawaban yang tepat! Jangan lupa Berdoa dan memulai dari yang mudah. 01. Diketahui ion X 3+ mempunyai 10 elektron dan 14 neutron.
PAKET UJIAN NASIONAL 17 Pelajaran : KIMIA Waktu : 120 Menit Pilihlah salah satu jawaban yang tepat! Jangan lupa Berdoa dan memulai dari yang mudah. 01. Diketahui ion X 3+ mempunyai 10 elektron dan 14 neutron.
Siswa diingatkan tentang struktur atom, bilangan kuantum, bentuk-bentuk orbital, dan konfigurasi elektron
 RENCANA PELAKSANAAN PEMBELAJARAN NO: 1 Mata Pelajaran : Kimia Kelas/Semester : XI/1 Materi Pokok : Stuktur atom dan sistem periodik unsur Pertemuan Ke- : 1 dan 2 Alokasi Waktu : 2 x pertemuan (4 x 45 menit)
RENCANA PELAKSANAAN PEMBELAJARAN NO: 1 Mata Pelajaran : Kimia Kelas/Semester : XI/1 Materi Pokok : Stuktur atom dan sistem periodik unsur Pertemuan Ke- : 1 dan 2 Alokasi Waktu : 2 x pertemuan (4 x 45 menit)
BAB 9 HIDROKARBON. Gambar 9.1 Asam askorbat Sumber: Kimia Dasar Konsep-konsep Inti
 BAB 9 HIDROKARBON Gambar 9.1 Asam askorbat Sumber: Kimia Dasar Konsep-konsep Inti Pada pelajaran bab kesembilan ini akan dipelajari tentang kekhasan atom karbon, identitifikasi senyawa karbon, alkana,
BAB 9 HIDROKARBON Gambar 9.1 Asam askorbat Sumber: Kimia Dasar Konsep-konsep Inti Pada pelajaran bab kesembilan ini akan dipelajari tentang kekhasan atom karbon, identitifikasi senyawa karbon, alkana,
Wardaya College. Tes Simulasi Ujian Nasional SMA Berbasis Komputer. Mata Pelajaran Kimia Tahun Ajaran 2017/2018. Departemen Kimia - Wardaya College
 Tes Simulasi Ujian Nasional SMA Berbasis Komputer Mata Pelajaran Kimia Tahun Ajaran 2017/2018-1. Sebuah unsur X memiliki no massa 52 dan jumlah neutron sebesar 28. Kongurasi elektron dari ion X + adalah...
Tes Simulasi Ujian Nasional SMA Berbasis Komputer Mata Pelajaran Kimia Tahun Ajaran 2017/2018-1. Sebuah unsur X memiliki no massa 52 dan jumlah neutron sebesar 28. Kongurasi elektron dari ion X + adalah...
KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI
 KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI 1. Untuk membuat 500 ml larutan H2SO4 0.05 M dibutuhkan larutan H2SO4 5 M sebanyak ml a. 5 ml b. 10 ml c. 2.5 ml d. 15 ml e. 5.5
KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI 1. Untuk membuat 500 ml larutan H2SO4 0.05 M dibutuhkan larutan H2SO4 5 M sebanyak ml a. 5 ml b. 10 ml c. 2.5 ml d. 15 ml e. 5.5
Kesetimbangan Kimia. Bab 4
 Kesetimbangan Kimia Bab 4 Standar Kompetensi 3. Memahami kinetika reaksi, kesetimbangan kimia, dan faktor-faktor yang memengaruhinya, serta penerapannya dalam kehidupan sehari-hari dan industri Kompetensi
Kesetimbangan Kimia Bab 4 Standar Kompetensi 3. Memahami kinetika reaksi, kesetimbangan kimia, dan faktor-faktor yang memengaruhinya, serta penerapannya dalam kehidupan sehari-hari dan industri Kompetensi
UJIAN NASIONAL TAHUN PELAJARAN 2007/2008
 UJIAN NASIONAL TAHUN PELAJARAN 2007/2008 PANDUAN MATERI SMA DAN MA K I M I A PROGRAM STUDI IPA PUSAT PENILAIAN PENDIDIKAN BALITBANG DEPDIKNAS KATA PENGANTAR Dalam rangka sosialisasi kebijakan dan persiapan
UJIAN NASIONAL TAHUN PELAJARAN 2007/2008 PANDUAN MATERI SMA DAN MA K I M I A PROGRAM STUDI IPA PUSAT PENILAIAN PENDIDIKAN BALITBANG DEPDIKNAS KATA PENGANTAR Dalam rangka sosialisasi kebijakan dan persiapan
PEMERINTAH KOTA SURABAYA DINAS PENDIDIKAN SMA NEGERI 16 SURABAYA JL. RAYA PRAPEN TELP FAX KODE POS 60299
 PEMERINTAH KOTA SURABAYA DINAS PENDIDIKAN SMA NEGERI 16 SURABAYA JL. RAYA PRAPEN TELP. 031-8415492 FAX 031-8430673 KODE POS 60299 ULANGAN AKHIR SEMESTER 2 (DUA) TAHUN PELAJARAN 2011 2012 Hari/Tanggal :
PEMERINTAH KOTA SURABAYA DINAS PENDIDIKAN SMA NEGERI 16 SURABAYA JL. RAYA PRAPEN TELP. 031-8415492 FAX 031-8430673 KODE POS 60299 ULANGAN AKHIR SEMESTER 2 (DUA) TAHUN PELAJARAN 2011 2012 Hari/Tanggal :
Kesetimbangan Kimia. Tim Dosen Kimia Dasar FTP
 Kesetimbangan Kimia Tim Dosen Kimia Dasar FTP Pengertian kesetimbangan kimia Suatu sistem dikatakan setimbang jika dua proses yang berlawanan terjadi dengan laju yang sama atau dengan kata lain tidak terjadi
Kesetimbangan Kimia Tim Dosen Kimia Dasar FTP Pengertian kesetimbangan kimia Suatu sistem dikatakan setimbang jika dua proses yang berlawanan terjadi dengan laju yang sama atau dengan kata lain tidak terjadi
OAL TES SEMESTER II. I. Pilihlah jawaban yang paling tepat!
 176 KIMIA X SMA S AL TES SEMESTER II I. Pilihlah jawaban yang paling tepat! 1. Suatu zat padat dilarutkan dalam air, ternyata larutannya dapat menghantarkan arus listrik. Pernyataan yang benar tentang
176 KIMIA X SMA S AL TES SEMESTER II I. Pilihlah jawaban yang paling tepat! 1. Suatu zat padat dilarutkan dalam air, ternyata larutannya dapat menghantarkan arus listrik. Pernyataan yang benar tentang
Faktor-Faktor yang Mempengaruhi Pergeseran Kesetimbangan
 Standar Kometensi Kometensi Dasar Menjelaskan kinetika dan kesetimbangan reaksi kimia serta faktor-faktor yang memengaruhinya. Menjelaskan engertian reaksi kesetimbangan. Menyelidiki faktor-faktor yang
Standar Kometensi Kometensi Dasar Menjelaskan kinetika dan kesetimbangan reaksi kimia serta faktor-faktor yang memengaruhinya. Menjelaskan engertian reaksi kesetimbangan. Menyelidiki faktor-faktor yang
Kekekalan Energi energi tidak dapat diciptakan maupun dimusnahkan
 Termokimia XI IPA CO 2, mineral, panas, cahaya Kekekalan Energi energi tidak dapat diciptakan maupun dimusnahkan Manusia Fotosintesis Sayuran dan Buah Entalpi energi / kalor yang terdapat dalam suatu materi.
Termokimia XI IPA CO 2, mineral, panas, cahaya Kekekalan Energi energi tidak dapat diciptakan maupun dimusnahkan Manusia Fotosintesis Sayuran dan Buah Entalpi energi / kalor yang terdapat dalam suatu materi.
SKL 2 RINGKASAN MATERI. 1. Konsep mol dan Bagan Stoikiometri ( kelas X )
 SKL 2 Menerapkan hukum-hukum dasar kimia untuk memecahkan masalah dalam perhitungan kimia. o Menganalisis persamaan reaksi kimia o Menyelesaikan perhitungan kimia yang berkaitan dengan hukum dasar kimia
SKL 2 Menerapkan hukum-hukum dasar kimia untuk memecahkan masalah dalam perhitungan kimia. o Menganalisis persamaan reaksi kimia o Menyelesaikan perhitungan kimia yang berkaitan dengan hukum dasar kimia
Antiremed Kelas 11 Kimia
 Antiremed Kelas 11 Kimia Persiapan UAS 1 Kimia Doc. Name: AR11KIM01UAS Version: 016-08 halaman 1 01. Salah satu teori yang menjadi dasar sehingga tercipta model atom modern (A) Rutherford, Niels Bohr,
Antiremed Kelas 11 Kimia Persiapan UAS 1 Kimia Doc. Name: AR11KIM01UAS Version: 016-08 halaman 1 01. Salah satu teori yang menjadi dasar sehingga tercipta model atom modern (A) Rutherford, Niels Bohr,
TERMOKIMIA. Sistem terbagi atas: 1. Sistem tersekat: Antara sistem dan lingkungan tidak dapat terjadi pertukaran energi maupun materi
 TERMOKIMIA almair amrulloh 12:04:00 AM 11 IPAKimia 11 IPA Asas kekekalan energi menyatakan bahwa energi tidak dapat diciptakan atau dimusnahkan, tetapi energi dapat diubah dari satu bentuk kebentuk lain
TERMOKIMIA almair amrulloh 12:04:00 AM 11 IPAKimia 11 IPA Asas kekekalan energi menyatakan bahwa energi tidak dapat diciptakan atau dimusnahkan, tetapi energi dapat diubah dari satu bentuk kebentuk lain
SOAL LAJU REAKSI. Mol CaCO 3 = = 0.25 mol = 25. m Mr
 SOAL LAJU REAKSI 1. Untuk membuat 500 ml larutan H 2 SO 4 0.05 M dibutuhkan larutan H 2 SO 4 5 M sebanyak ml A. 5 ml B. 10 ml C. 2.5 ml D. 15 ml E. 5.5 ml : A Mencari volume yang dibutuhkan pada proses
SOAL LAJU REAKSI 1. Untuk membuat 500 ml larutan H 2 SO 4 0.05 M dibutuhkan larutan H 2 SO 4 5 M sebanyak ml A. 5 ml B. 10 ml C. 2.5 ml D. 15 ml E. 5.5 ml : A Mencari volume yang dibutuhkan pada proses
Pelatihan Online I OSN Bidang Kimia Page 1 PETUNJUK PENGERJAAN SOAL
 PETUNJUK PENGERJAAN SOAL 1. Periksalah terlebih dahulu soal yang Anda terima, apakah dalam keadaan baik, terbaca, lengkap, dan jelas, sebelum Anda mengerjakan. 2. Jawaban dikerjakan pada lembar jawaban
PETUNJUK PENGERJAAN SOAL 1. Periksalah terlebih dahulu soal yang Anda terima, apakah dalam keadaan baik, terbaca, lengkap, dan jelas, sebelum Anda mengerjakan. 2. Jawaban dikerjakan pada lembar jawaban
PAKET UJIAN NASIONAL 11 Pelajaran : KIMIA Waktu : 120 Menit
 PAKET UJIAN NASIONAL 11 Pelajaran : KIMIA Waktu : 120 Menit Pilihlah salah satu jawaban yang tepat! Jangan lupa Berdoa dan memulai dari yang mudah. 1. Unsur dengan nomor massa 45 dan mempunyai jumlah netron
PAKET UJIAN NASIONAL 11 Pelajaran : KIMIA Waktu : 120 Menit Pilihlah salah satu jawaban yang tepat! Jangan lupa Berdoa dan memulai dari yang mudah. 1. Unsur dengan nomor massa 45 dan mempunyai jumlah netron
Bab III Termokimia TUJUAN PEMBELAJARAN. Termokimia 47. Ketika batang korek api dinyalakan terjadi reaksi kimia dan pelepasan energi.
 Bab III Termokimia Sumber: Silberberg, Chemistry: The Molecular Nature of Matter and Change Ketika batang korek api dinyalakan terjadi reaksi kimia dan pelepasan energi. TUJUAN PEMBELAJARAN Setelah mengikuti
Bab III Termokimia Sumber: Silberberg, Chemistry: The Molecular Nature of Matter and Change Ketika batang korek api dinyalakan terjadi reaksi kimia dan pelepasan energi. TUJUAN PEMBELAJARAN Setelah mengikuti
TERMOKIMIA. STANDART KOMPETENSI; 2. Memahami perubahan energi dalam kimia dan cara pengukuran. ENTALPI DAN PERUBAHANNYA
 TERMOKIMIA STANDART KOMPETENSI; 2. Memahami perubahan energi dalam kimia dan cara pengukuran. ENTALPI DAN PERUBAHANNYA KOMPETENSI DASAR; 2.1. Mendeskripsikan perubahan entalpi suatu reaksi, reaksi eksoterm
TERMOKIMIA STANDART KOMPETENSI; 2. Memahami perubahan energi dalam kimia dan cara pengukuran. ENTALPI DAN PERUBAHANNYA KOMPETENSI DASAR; 2.1. Mendeskripsikan perubahan entalpi suatu reaksi, reaksi eksoterm
BAB II KESETIMBANGAN KIMIA
 BAB II KESETIMBANGAN KIMIA TIU : 1. Memahami definisi kimia dan mengidentifikasi keadaan kimia. Memahami faktor-faktor yang mempengaruhi kimia: Prinsip Le Chatelier. Memahami aplikasi kimia dalam perolehan
BAB II KESETIMBANGAN KIMIA TIU : 1. Memahami definisi kimia dan mengidentifikasi keadaan kimia. Memahami faktor-faktor yang mempengaruhi kimia: Prinsip Le Chatelier. Memahami aplikasi kimia dalam perolehan
SIMULASI UJIAN NASIONAL 1
 SIMULASI UJIAN NASIONAL 1 1. Bilangan-bilangan kuantum yang mungkin dimiliki oleh suatu elektron (A) n = 2, l = 2, m = 0, s = - 1 2 (B) n = 3, l = 0, m = +1, s = + 1 2 (C) n = 4, l = 2, m = - 3, s = -
SIMULASI UJIAN NASIONAL 1 1. Bilangan-bilangan kuantum yang mungkin dimiliki oleh suatu elektron (A) n = 2, l = 2, m = 0, s = - 1 2 (B) n = 3, l = 0, m = +1, s = + 1 2 (C) n = 4, l = 2, m = - 3, s = -
H 2 O (l) H 2 O (g) Kesetimbangan kimia. N 2 O 4 (g) 2NO 2 (g)
 Purwanti Widhy H Kesetimbangan adalah suatu keadaan di mana tidak ada perubahan yang terlihat seiring berjalannya waktu. Kesetimbangan kimia tercapai jika: Laju reaksi maju dan laju reaksi balik sama besar
Purwanti Widhy H Kesetimbangan adalah suatu keadaan di mana tidak ada perubahan yang terlihat seiring berjalannya waktu. Kesetimbangan kimia tercapai jika: Laju reaksi maju dan laju reaksi balik sama besar
Soal Soal Kesetimbangan Kimia. Proses Haber-Bosch merupakan proses pembentukan atau produksi ammonia berdasarkan reaksi:
 Nama : Fitria Puspita NIM : 1201760 Kelas : Pendidikan Kimia A Soal Soal Kesetimbangan Kimia SBMPTN 2014 Untuk soal no 1-3, bacalah narasi berikut. Proses Haber-Bosch merupakan proses pembentukan atau
Nama : Fitria Puspita NIM : 1201760 Kelas : Pendidikan Kimia A Soal Soal Kesetimbangan Kimia SBMPTN 2014 Untuk soal no 1-3, bacalah narasi berikut. Proses Haber-Bosch merupakan proses pembentukan atau
BAB IV TERMOKIMIA A. PENGERTIAN KALOR REAKSI
 BAB IV TERMOKIMIA A. Standar Kompetensi: Memahami tentang ilmu kimia dan dasar-dasarnya serta mampu menerapkannya dalam kehidupan se-hari-hari terutama yang berhubungan langsung dengan kehidupan. B. Kompetensi
BAB IV TERMOKIMIA A. Standar Kompetensi: Memahami tentang ilmu kimia dan dasar-dasarnya serta mampu menerapkannya dalam kehidupan se-hari-hari terutama yang berhubungan langsung dengan kehidupan. B. Kompetensi
PAKET UJIAN NASIONAL 16 Pelajaran : KIMIA Waktu : 120 Menit
 PAKET UJIAN NASIONAL 16 Pelajaran : KIMIA Waktu : 120 Menit Pilihlah salah satu jawaban yang tepat! Jangan lupa Berdoa dan memulai dari yang mudah. 01. 27 Isotop 13 Al terdiri dari... A. 13 proton,14 elektron
PAKET UJIAN NASIONAL 16 Pelajaran : KIMIA Waktu : 120 Menit Pilihlah salah satu jawaban yang tepat! Jangan lupa Berdoa dan memulai dari yang mudah. 01. 27 Isotop 13 Al terdiri dari... A. 13 proton,14 elektron
TERMOKIMIA. Kalor reaksi pada pembakaran 1 mol metanol menurut reaksi adalah... CH 3 OH + O 2 CO H 2 O. Penyelesaian : H
 1. Diketahui energi ikatan rata-rata : H - O : 111 kkal.mol -1 C - H : 99 kkal.mol -1 C - O : 85 kkal.mol -1 C = O : 173 kkal.mol -1 O = O : 119 Kkal.mol -1 TERMOKIMIA Kalor reaksi pada pembakaran 1 mol
1. Diketahui energi ikatan rata-rata : H - O : 111 kkal.mol -1 C - H : 99 kkal.mol -1 C - O : 85 kkal.mol -1 C = O : 173 kkal.mol -1 O = O : 119 Kkal.mol -1 TERMOKIMIA Kalor reaksi pada pembakaran 1 mol
Kesetimbangan dinamis adalah keadaan dimana dua proses yang berlawanan terjadi dengan laju yang sama, akibatnya tidak terjadi perubahan bersih dalam
 Kesetimbangan dinamis adalah keadaan dimana dua proses yang berlawanan terjadi dengan laju yang sama, akibatnya tidak terjadi perubahan bersih dalam sistem pada kesetimbangan Uap mengembun dengan laju
Kesetimbangan dinamis adalah keadaan dimana dua proses yang berlawanan terjadi dengan laju yang sama, akibatnya tidak terjadi perubahan bersih dalam sistem pada kesetimbangan Uap mengembun dengan laju
PAKET UJIAN NASIONAL 14 Pelajaran : KIMIA Waktu : 120 Menit
 PAKET UJIAN NASINAL 14 Pelajaran : KIMIA Waktu : 120 Menit Pilihlah salah satu jawaban yang tepat! Jangan lupa Berdoa dan memulai dari yang mudah. 1. Diketahui ion X 3+ mempunyai 10 elektron dan 14 neutron.
PAKET UJIAN NASINAL 14 Pelajaran : KIMIA Waktu : 120 Menit Pilihlah salah satu jawaban yang tepat! Jangan lupa Berdoa dan memulai dari yang mudah. 1. Diketahui ion X 3+ mempunyai 10 elektron dan 14 neutron.
H 2 O (L) H 2 O (G) KESETIMBANGAN KIMIA. N 2 O 4 (G) 2NO 2 (G)
 H 2 O (L) H 2 O (G) KESETIMBANGAN KIMIA. N 2 O 4 (G) 2NO 2 (G) Purwanti Widhy H Kesetimbangan adalah suatu keadaan di mana tidak ada perubahan yang terlihat seiring berjalannya waktu. Kesetimbangan kimia
H 2 O (L) H 2 O (G) KESETIMBANGAN KIMIA. N 2 O 4 (G) 2NO 2 (G) Purwanti Widhy H Kesetimbangan adalah suatu keadaan di mana tidak ada perubahan yang terlihat seiring berjalannya waktu. Kesetimbangan kimia
D. beta dan alfa E. alfa dan beta
 1. Pada peluruhan menjadi kemudian meluruh menjadi, partikel-partikel yang dipancarkan berturut-turut adalah... A. foton dan beta B. foton dan alfa C. beta dan foton Reaksi peluruhan : D. beta dan alfa
1. Pada peluruhan menjadi kemudian meluruh menjadi, partikel-partikel yang dipancarkan berturut-turut adalah... A. foton dan beta B. foton dan alfa C. beta dan foton Reaksi peluruhan : D. beta dan alfa
SIMULASI UJIAN NASIONAL 2
 SIMULASI UJIAN NASIONAL 2. Diketahui nomor atom dan nomor massa dari atom X adalah 29 dan 63. Jumlah proton, elektron, dan neutron dalam ion X 2+ (A) 29, 27, dan 63 (B) 29, 29, dan 34 (C) 29, 27, dan 34
SIMULASI UJIAN NASIONAL 2. Diketahui nomor atom dan nomor massa dari atom X adalah 29 dan 63. Jumlah proton, elektron, dan neutron dalam ion X 2+ (A) 29, 27, dan 63 (B) 29, 29, dan 34 (C) 29, 27, dan 34
K13 Revisi Antiremed Kelas 11 Kimia
 K1 Revisi Antiremed Kelas 11 Kimia Hidrokarbon - Soal Doc Name: RK1AR11KIM0101 Version: 016-10 halaman 1 01 Untuk mengenali adanya senyawa karbon dalam suatu bahan dapat dilakukan dengan cara membakar
K1 Revisi Antiremed Kelas 11 Kimia Hidrokarbon - Soal Doc Name: RK1AR11KIM0101 Version: 016-10 halaman 1 01 Untuk mengenali adanya senyawa karbon dalam suatu bahan dapat dilakukan dengan cara membakar
D. H 2 S 2 O E. H 2 S 2 O 7
 1. Jika gas belerang dioksida dialirkan ke dalam larutan hidrogen sulfida, maka zat terakhir ini akan teroksidasi menjadi... A. S B. H 2 SO 3 C. H 2 SO 4 D. H 2 S 2 O E. H 2 S 2 O 7 Reaksi yang terjadi
1. Jika gas belerang dioksida dialirkan ke dalam larutan hidrogen sulfida, maka zat terakhir ini akan teroksidasi menjadi... A. S B. H 2 SO 3 C. H 2 SO 4 D. H 2 S 2 O E. H 2 S 2 O 7 Reaksi yang terjadi
PREDIKSI 2. Ikatan kovalen koordinat dan ikatan kovalen berturut-turut adalah... A. 1 dan 2 B. 1 dan 3 C. 2 dan 3 D. 3 dan 4 E.
 PREDIKSI 2 Pilihlah jawaban yang paling tepat! 1. Perhatikan gambar struktur Lewis senyawa NH 4 Cl sebagai berikut; Ikatan kovalen koordinat dan ikatan kovalen berturut-turut adalah... A. 1 dan 2 B. 1
PREDIKSI 2 Pilihlah jawaban yang paling tepat! 1. Perhatikan gambar struktur Lewis senyawa NH 4 Cl sebagai berikut; Ikatan kovalen koordinat dan ikatan kovalen berturut-turut adalah... A. 1 dan 2 B. 1
HAND OUT KIMIA XI IPA BAB IV KESETIMBANGAN KIMIA
 HAND OUT KIMIA XI IPA BAB IV KESETIMBANGAN KIMIA 1 BAB IV KESETIMBANGAN KIMIA I. Standar Kompetensi 3. Memahami kinetika reaksi, kesetimbangan kimia, dan faktor-faktor yang mempengaruhinya, serta penerapannya
HAND OUT KIMIA XI IPA BAB IV KESETIMBANGAN KIMIA 1 BAB IV KESETIMBANGAN KIMIA I. Standar Kompetensi 3. Memahami kinetika reaksi, kesetimbangan kimia, dan faktor-faktor yang mempengaruhinya, serta penerapannya
Berdasarkan data di atas yang merupakan larutan non elektrolit adalah nomor A. 1 B. 2 C. 3 D. 4 E. 5
 PREDIKSI UN 2010 ( semoga soal soal ini ada manfaatnya) 1. Jika diketahui nuklida 11 Na 23, maka jumlah elektron, proton dan neutron adalah A. 23 proton, 12 elektron dan 11 neutron B. 11 proton, 12 elektron
PREDIKSI UN 2010 ( semoga soal soal ini ada manfaatnya) 1. Jika diketahui nuklida 11 Na 23, maka jumlah elektron, proton dan neutron adalah A. 23 proton, 12 elektron dan 11 neutron B. 11 proton, 12 elektron
UN SMA IPA Kimia. Kode Soal 305
 UN SMA IPA Kimia Kode Soal 305 Doc.name : UNSMAIPAKIM305 Version : 2012-12 halaman 1 1. Di antara hal-hal di bawah ini : 1. besi berpilar 2. pagar di cat 3. belerang meleleh 4. nasi jadi basi 5. bel berdering
UN SMA IPA Kimia Kode Soal 305 Doc.name : UNSMAIPAKIM305 Version : 2012-12 halaman 1 1. Di antara hal-hal di bawah ini : 1. besi berpilar 2. pagar di cat 3. belerang meleleh 4. nasi jadi basi 5. bel berdering
Oleh. Dewi Candrawati
 126 Lampiran 4 Oleh Dewi Candrawati 2014 127 Petunjuk Pengerjaan: 1. Tes diagnostik ini terdiri dari delapan soal pilihan ganda dua tingkat. 2. Setiap soal memiliki 4 pilihan jawaban dan 5 pilihan alasan.
126 Lampiran 4 Oleh Dewi Candrawati 2014 127 Petunjuk Pengerjaan: 1. Tes diagnostik ini terdiri dari delapan soal pilihan ganda dua tingkat. 2. Setiap soal memiliki 4 pilihan jawaban dan 5 pilihan alasan.
PREDIKSI UJIAN NASIONAL 2011 KIMIA
 Soal PREDIKSI Latihan UJIAN NASIONAL 2011 2013 KIMIA 1 LATIHAN UJIAN AKHIR NASIONAL TAHUN AJARAN 2012/2013 KIMIA 1. Jika unsur 19 X berikatan dengan unsur 35 Z maka, rumus senyawa dan jenis ikatan yang
Soal PREDIKSI Latihan UJIAN NASIONAL 2011 2013 KIMIA 1 LATIHAN UJIAN AKHIR NASIONAL TAHUN AJARAN 2012/2013 KIMIA 1. Jika unsur 19 X berikatan dengan unsur 35 Z maka, rumus senyawa dan jenis ikatan yang
PEMBAHASAN SOAL KIMIA KSM PROVINSI 2016 Oleh Urip Rukim (www.urip.info) JENJANG MADRASAH ALIYAH SELEKSI TINGKAT PROVINSI KOMPETISI SAINS MADRASAH
 PEMBAHASAN SOAL KIMIA KSM PROVINSI 2016 Oleh Urip Rukim (www.urip.info) JENJANG MADRASAH ALIYAH SELEKSI TINGKAT PROVINSI KOMPETISI SAINS MADRASAH TAHUN 2016 Soal diketik ulang oleh urip rukim (www.urip.info)
PEMBAHASAN SOAL KIMIA KSM PROVINSI 2016 Oleh Urip Rukim (www.urip.info) JENJANG MADRASAH ALIYAH SELEKSI TINGKAT PROVINSI KOMPETISI SAINS MADRASAH TAHUN 2016 Soal diketik ulang oleh urip rukim (www.urip.info)
KONSEP MOL DAN STOIKIOMETRI
 BAB V KONSEP MOL DAN STOIKIOMETRI Dalam ilmu fisika, dikenal satuan mol untuk besaran jumlah zat. Dalam bab ini, akan dibahas mengenai konsep mol yang mendasari perhitungan kimia (stoikiometri). A. KONSEP
BAB V KONSEP MOL DAN STOIKIOMETRI Dalam ilmu fisika, dikenal satuan mol untuk besaran jumlah zat. Dalam bab ini, akan dibahas mengenai konsep mol yang mendasari perhitungan kimia (stoikiometri). A. KONSEP
LATIHAN ULANGAN TENGAH SEMESTER 2
 Pilihlah jawaban yang paling benar LATIHAN ULANGAN TENGAH SEMESTER 2 TATANAMA 1. Nama senyawa berikut ini sesuai dengan rumus kimianya, kecuali. A. NO = nitrogen oksida B. CO 2 = karbon dioksida C. PCl
Pilihlah jawaban yang paling benar LATIHAN ULANGAN TENGAH SEMESTER 2 TATANAMA 1. Nama senyawa berikut ini sesuai dengan rumus kimianya, kecuali. A. NO = nitrogen oksida B. CO 2 = karbon dioksida C. PCl
1s 2 2s 2 2p 6 3s 2 2p 6 3d 4s 1 4p 4d 4f 5s 5p 5d 5f
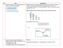 NO SOAL PEMBAHASAN 1 Konfigurasi elekttron ion X - yang memiliki nomor massa 39 dan 21 neutron adalah.. A. 1s2 2s2 2p6 3s2 3p6 4s2 3d1 B. 1s2 2s2 2p6 3s2 3p6 4s1 C. 1s2 2s2 2p6 3s2 3p6 3d1 D. 1s2 2s2 2p6
NO SOAL PEMBAHASAN 1 Konfigurasi elekttron ion X - yang memiliki nomor massa 39 dan 21 neutron adalah.. A. 1s2 2s2 2p6 3s2 3p6 4s2 3d1 B. 1s2 2s2 2p6 3s2 3p6 4s1 C. 1s2 2s2 2p6 3s2 3p6 3d1 D. 1s2 2s2 2p6
TUGAS LIBURAN. Dijawab dalam sebuah folio/kertas putih. Beri penjelasan secukupnya untuk materi hafalan
 TUGAS LIBURAN Dijawab dalam sebuah folio/kertas putih. Beri penjelasan secukupnya untuk materi hafalan LATIHAN UAN KIMIA KELAS 3 IPA By : Rachmad Junaedi Diketahui dua buah unsur yaitu : dan 1. Diagram
TUGAS LIBURAN Dijawab dalam sebuah folio/kertas putih. Beri penjelasan secukupnya untuk materi hafalan LATIHAN UAN KIMIA KELAS 3 IPA By : Rachmad Junaedi Diketahui dua buah unsur yaitu : dan 1. Diagram
BAB 6. (lihat diktat kuliah KIMIA : Bab 6 dan 7)
 BAB 6 (lihat diktat kuliah KIMIA : Bab 6 dan 7) KONSEP KESETIMBANGAN KIMIA 1. HUKUM KEKEKALAN ENERGI 2. PENGERTIAN KERJA DAN KALOR 3. PENGERTIAN SISTEM, LINGKUNGAN, DAN FUNGSI KEADAAN 4. HUKUM PERTAMA
BAB 6 (lihat diktat kuliah KIMIA : Bab 6 dan 7) KONSEP KESETIMBANGAN KIMIA 1. HUKUM KEKEKALAN ENERGI 2. PENGERTIAN KERJA DAN KALOR 3. PENGERTIAN SISTEM, LINGKUNGAN, DAN FUNGSI KEADAAN 4. HUKUM PERTAMA
BANK SOAL SELEKSI MASUK PERGURUAN TINGGI BIDANG KIMIA
 BANK SOAL SELEKSI MASUK PERGURUAN TINGGI BIDANG KIMIA 1 BAB V 1. Polipropena merupakan senyawa polimer yang digunakan untuk membuat botol minuman dan berbagai jenis karung. Senyawa ini dibuat dari monomer
BANK SOAL SELEKSI MASUK PERGURUAN TINGGI BIDANG KIMIA 1 BAB V 1. Polipropena merupakan senyawa polimer yang digunakan untuk membuat botol minuman dan berbagai jenis karung. Senyawa ini dibuat dari monomer
Kesetimbangan Kimia. Chapter 9 P N2 O 4. Kesetimbangan akan. Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi
 Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi Kesetimbangan adalah suatu keadaan di mana tidak ada perubahan yang terlihat seiring berjalannya waktu. Kesetimbangan kimia
Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi Kesetimbangan adalah suatu keadaan di mana tidak ada perubahan yang terlihat seiring berjalannya waktu. Kesetimbangan kimia
Sumber: Silberberg, Chemistry: The Molecular Nature of Matter and Change
 Bab V Kesetimbangan Kimia Sumber: Silberberg, Chemistry: The Molecular Nature of Matter and Change Amonia cair digunakan sebagai pupuk. Pembuatan gas amonia menggunakan prinsip-prinsip reaksi kesetimbangan,
Bab V Kesetimbangan Kimia Sumber: Silberberg, Chemistry: The Molecular Nature of Matter and Change Amonia cair digunakan sebagai pupuk. Pembuatan gas amonia menggunakan prinsip-prinsip reaksi kesetimbangan,
D. 8 mol S E. 4 mol Fe(OH) 3 C. 6 mol S Kunci : B Penyelesaian : Reaksi :
 1. Perhatikan reaksi, 2 Fe 2 S 3 + 3O 2 + 6 H 2 O 4 Fe(OH) 3 + 6S Jika 2 mol Fe 2 S 3, 2 mol O 2 dan 3 mol H 2 O bereaksi dengan sempurna, akan dihasilkan : A. 3 mol Fe(OH) 3 B. 2 mol Fe(OH) 3 D. 8 mol
1. Perhatikan reaksi, 2 Fe 2 S 3 + 3O 2 + 6 H 2 O 4 Fe(OH) 3 + 6S Jika 2 mol Fe 2 S 3, 2 mol O 2 dan 3 mol H 2 O bereaksi dengan sempurna, akan dihasilkan : A. 3 mol Fe(OH) 3 B. 2 mol Fe(OH) 3 D. 8 mol
BAB III KESETIMBANGAN KIMIA. AH = 92 kj
 BAB III KESETIMBANGAN KIMIA Amonia (NH 3 ) merupakan salah satu zat kimia yang paling banyak diproduksi. Amonia digunakan terutama untuk membuat pupuk, yaitu urea dan ZA. Penggunaan amonia yang lain, yaitu
BAB III KESETIMBANGAN KIMIA Amonia (NH 3 ) merupakan salah satu zat kimia yang paling banyak diproduksi. Amonia digunakan terutama untuk membuat pupuk, yaitu urea dan ZA. Penggunaan amonia yang lain, yaitu
LEMBARAN SOAL Larutan senyawa di bawah ini dalam air bersifat elektrolit kuat, kecuali... a. NaOH c. HCl e. Ba(OH) 2 b. H 2 SO 4 e.
 LEMBARAN SOAL 13 Mata Pelajaran : KMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah soal dengan
LEMBARAN SOAL 13 Mata Pelajaran : KMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah soal dengan
KESETIMBANGAN. titik setimbang
 KESETIMBANGAN STANDART KOMPETENSI;. Memahami kinetika reaksi, kesetimbangan kimia, dan faktor-faktor yang berpengaruh, serta penerapannya dalam kehidupan sehari-hari. KOMPETENSI DASAR;.. Menjelaskan kestimbangan
KESETIMBANGAN STANDART KOMPETENSI;. Memahami kinetika reaksi, kesetimbangan kimia, dan faktor-faktor yang berpengaruh, serta penerapannya dalam kehidupan sehari-hari. KOMPETENSI DASAR;.. Menjelaskan kestimbangan
No Indikator Soal Valid
 107 Lampiran 3 Rekapitulasi asi Instrumen TDM-TWO-TIER No Indikator Soal 1 Memahami kesetimbangan Reaksi kesetimbangan antara N 2 O 4 dengan NO 2 mengikuti persamaan kimia berikut ini : ator 1 :- dinamis
107 Lampiran 3 Rekapitulasi asi Instrumen TDM-TWO-TIER No Indikator Soal 1 Memahami kesetimbangan Reaksi kesetimbangan antara N 2 O 4 dengan NO 2 mengikuti persamaan kimia berikut ini : ator 1 :- dinamis
D. 4,50 x 10-8 E. 1,35 x 10-8
 1. Pada suatu suhu tertentu, kelarutan PbI 2 dalam air adalah 1,5 x 10-3 mol/liter. Berdasarkan itu maka Kp PbI 2 adalah... A. 4,50 x 10-9 B. 3,37 x 10-9 C. 6,75 x 10-8 S : PbI 2 = 1,5. 10-3 mol/liter
1. Pada suatu suhu tertentu, kelarutan PbI 2 dalam air adalah 1,5 x 10-3 mol/liter. Berdasarkan itu maka Kp PbI 2 adalah... A. 4,50 x 10-9 B. 3,37 x 10-9 C. 6,75 x 10-8 S : PbI 2 = 1,5. 10-3 mol/liter
D kj/mol E kj/mol
 1. Dari data : 2H 2 (g) + O 2 (g) 2H 2 O (l) H = -571 kj 2Ca (s) + O 2 (g) 2CaO(s) H = -1269 kj CaO (s) + H 2 O (l) Ca(OH)2(s) H = -64 kj Dapat dihitung entalpi pembentukan Ca(OH) 2 (s) sebesar... A. -984
1. Dari data : 2H 2 (g) + O 2 (g) 2H 2 O (l) H = -571 kj 2Ca (s) + O 2 (g) 2CaO(s) H = -1269 kj CaO (s) + H 2 O (l) Ca(OH)2(s) H = -64 kj Dapat dihitung entalpi pembentukan Ca(OH) 2 (s) sebesar... A. -984
PAKET UJIAN NASIONAL 8 Pelajaran : KIMIA Waktu : 120 Menit
 PAKET UJIAN NASIONAL 8 Pelajaran : KIMIA Waktu : 120 Menit Pilihlah salah satu jawaban yang tepat! Jangan lupa Berdoa dan memulai dari yang mudah. 1. Di antara unsur-unsur 12 P, 16 Q, 19 R, 34 S dan 53
PAKET UJIAN NASIONAL 8 Pelajaran : KIMIA Waktu : 120 Menit Pilihlah salah satu jawaban yang tepat! Jangan lupa Berdoa dan memulai dari yang mudah. 1. Di antara unsur-unsur 12 P, 16 Q, 19 R, 34 S dan 53
PEMERINTAH KABUPATEN BANYUMAS DINAS PENDIDIKAN SMA NEGERI PATIKRAJA Jalan Adipura 3 Patikraja Telp (0281) Banyumas 53171
 PEMERINTAH KABUPATEN BANYUMAS DINAS PENDIDIKAN SMA NEGERI PATIKRAJA Jalan Adipura 3 Patikraja Telp (0281) 6844576 Banyumas 53171 ULANGAN KENAIKAN KELAS TAHUN PELAJARAN 2010/ 2011 Mata Pelajaran : Kimia
PEMERINTAH KABUPATEN BANYUMAS DINAS PENDIDIKAN SMA NEGERI PATIKRAJA Jalan Adipura 3 Patikraja Telp (0281) 6844576 Banyumas 53171 ULANGAN KENAIKAN KELAS TAHUN PELAJARAN 2010/ 2011 Mata Pelajaran : Kimia
UN SMA 2012 IPA Kimia
 UN SMA 2012 IPA Kimia Kode Soal Doc. Name: UNSMAIPA2011KIM999 Doc. Version : 2012-12 halaman 1 01. Tahap awal pembuatan asam nitrat dalam industri melibatkan reaksi oksidasi ammonia yang menghasilkan nitrogen
UN SMA 2012 IPA Kimia Kode Soal Doc. Name: UNSMAIPA2011KIM999 Doc. Version : 2012-12 halaman 1 01. Tahap awal pembuatan asam nitrat dalam industri melibatkan reaksi oksidasi ammonia yang menghasilkan nitrogen
A. KESEIMBANGAN DINAMIS
 1 Tugas Kimia IV Prakerin KESEIMBANGAN KIMIA Coba kamu perhatikan proses pendidihan air dengan panci tertutup. Pada waktu air menguap, uap air akan tertahan dalam tutup panci. Selanjutnya, uap air akan
1 Tugas Kimia IV Prakerin KESEIMBANGAN KIMIA Coba kamu perhatikan proses pendidihan air dengan panci tertutup. Pada waktu air menguap, uap air akan tertahan dalam tutup panci. Selanjutnya, uap air akan
Kesetimbangan Kimia KIM 2 A. PENDAHULUAN B. REAKSI KESETIMBANGAN. α = KESETIMBANGAN KIMIA. materi78.co.nr. setimbang
 konsentrasi laju reaksi materi78.co.nr Kesetimbangan Kimia A. PENDAHULUAN Reaksi satu arah (irreversible) atau reaksi tidak dapat balik adalah reaksi yang terjadi pada satu arah, dan produknya tidak dapat
konsentrasi laju reaksi materi78.co.nr Kesetimbangan Kimia A. PENDAHULUAN Reaksi satu arah (irreversible) atau reaksi tidak dapat balik adalah reaksi yang terjadi pada satu arah, dan produknya tidak dapat
OLIMPIADE SAINS NASIONAL 2012 SELEKSI KABUPATEN / KOTA SOAL. UjianTeori. Waktu: 100 menit
 OLIMPIADE SAINS NASIONAL 2012 SELEKSI KABUPATEN / KOTA SOAL UjianTeori Waktu: 100 menit Kementerian Pendidikan dan Kebudayaan Direktorat Jenderal Pendidikan Menengah Direktorat Pembinaan Sekolah Menengah
OLIMPIADE SAINS NASIONAL 2012 SELEKSI KABUPATEN / KOTA SOAL UjianTeori Waktu: 100 menit Kementerian Pendidikan dan Kebudayaan Direktorat Jenderal Pendidikan Menengah Direktorat Pembinaan Sekolah Menengah
UN SMA 2015 PRE Kimia
 UN SMA 2015 PRE Kimia Kode Soal Doc. UNSMAIPA2015KIM999 Doc. Version : 2015-11 halaman 1 01. Suatu unsur Z mempunyai konfigurasi elektron [Ar]4s 2 3d 7. Jika neutron unsur tersebut 32, letak unsur Z dalam
UN SMA 2015 PRE Kimia Kode Soal Doc. UNSMAIPA2015KIM999 Doc. Version : 2015-11 halaman 1 01. Suatu unsur Z mempunyai konfigurasi elektron [Ar]4s 2 3d 7. Jika neutron unsur tersebut 32, letak unsur Z dalam
MODUL KIMIA SMA IPA Kelas 11
 SMA IPA Kelas 11 A. Senyawa Karbon Hidrokarbon termasuk senyawa organik yang hanya terdiri atas unsur karbon (C) dan hidrogen (H). Contohnya adalah metana (CH 4), etena (C 2H 4), dan asetilena (C 2H 2).
SMA IPA Kelas 11 A. Senyawa Karbon Hidrokarbon termasuk senyawa organik yang hanya terdiri atas unsur karbon (C) dan hidrogen (H). Contohnya adalah metana (CH 4), etena (C 2H 4), dan asetilena (C 2H 2).
Kunci jawaban dan pembahasan soal laju reaksi
 Kunci jawaban dan pembahasan soal laju reaksi Soal nomor 1 Mencari volume yang dibutuhkan pada proses pengenceran. Rumus pengenceran V 1. M 1 = V 2. M 2 Misal volume yang dibutuhkan sebanyak x ml, maka
Kunci jawaban dan pembahasan soal laju reaksi Soal nomor 1 Mencari volume yang dibutuhkan pada proses pengenceran. Rumus pengenceran V 1. M 1 = V 2. M 2 Misal volume yang dibutuhkan sebanyak x ml, maka
A. ARTI KESETIMBANGAN B. FAKTOR-FAKTOR YANG MEMPENGARUHI PERGESERAN KESETIMBANGAN C. TETAPAN KESETIMBANGAN D. KESETIMBANGAN KIMIA DALAM INDUSTRI
 4 KESETIMBANGAN KIMIA A. ARTI KESETIMBANGAN B. FAKTOR-FAKTOR YANG MEMPENGARUHI PERGESERAN KESETIMBANGAN C. TETAPAN KESETIMBANGAN D. KESETIMBANGAN KIMIA DALAM INDUSTRI Dalam kehidupan sehari-hari, sering
4 KESETIMBANGAN KIMIA A. ARTI KESETIMBANGAN B. FAKTOR-FAKTOR YANG MEMPENGARUHI PERGESERAN KESETIMBANGAN C. TETAPAN KESETIMBANGAN D. KESETIMBANGAN KIMIA DALAM INDUSTRI Dalam kehidupan sehari-hari, sering
Addres: Fb: Khayasar ALKANA. Rumus umum alkana: C n H 2n + 2. R (alkil) = C n H 2n + 1
 ALKANA Rumus umum alkana: C n H 2n + 2 R (alkil) = C n H 2n + 1 Alkana Adalah rantai karbon yang memiliki ikatan tunggal (jenuh) A. Alkana 1. Alkana disebut juga senyawa hidrokarbon jenuh (senyawa parafin).
ALKANA Rumus umum alkana: C n H 2n + 2 R (alkil) = C n H 2n + 1 Alkana Adalah rantai karbon yang memiliki ikatan tunggal (jenuh) A. Alkana 1. Alkana disebut juga senyawa hidrokarbon jenuh (senyawa parafin).
Materi Pokok Bahasan :
 STOIKIOMETRI Kompetensi : Memiliki kemampuan untuk menginterpretasikan serta menerapkan dalam perhitungan kimia. Memiliki kemampuan untuk mengaplikasikan pengetahuan yang dimilikinya dan terbiasa menggunakan
STOIKIOMETRI Kompetensi : Memiliki kemampuan untuk menginterpretasikan serta menerapkan dalam perhitungan kimia. Memiliki kemampuan untuk mengaplikasikan pengetahuan yang dimilikinya dan terbiasa menggunakan
TRY OUT UJIAN NASIONAL TAHUN AJARAN 2008 / 2009
 TRY UT UJIAN NASINAL TAHUN AJARAN 2008 / 2009 LEMBAR SAL B Bidang Studi : KIMIA Kelas/Program : XII (Dua Belas)/IPA PETUNJUK UMUM 1. Berdo alah sebelum mengerjakan soal 2. Tulislah dahulu nama dan kelas
TRY UT UJIAN NASINAL TAHUN AJARAN 2008 / 2009 LEMBAR SAL B Bidang Studi : KIMIA Kelas/Program : XII (Dua Belas)/IPA PETUNJUK UMUM 1. Berdo alah sebelum mengerjakan soal 2. Tulislah dahulu nama dan kelas
