HASIL DAN PEMBAHASAN
|
|
|
- Bambang Atmadja
- 6 tahun lalu
- Tontonan:
Transkripsi
1 14 HASIL DAN PEMBAHASAN Gejala Penyakit oleh B. theobromae Penyakit yang disebabkan oleh B. theobromae pada lima tanaman inang menunjukkan gejala yang beragam dan bagian yang terinfeksi berbeda-beda (Gambar 1). Gejala pada tanaman jeruk adalah kulit batang dan cabang mengelupas dan kering, pengelupasan kulit batang dan cabang terus meluas hingga ke seluruh permukaan sehingga terbentuk luka yang terbuka (Wiratno & Nurbanah 1997). Pada tingkat serangan yang berat batang tanaman jeruk membusuk dan kemudian mati (1A). Tanaman kakao yang terserang B. theobromae mengalami penyakit pod rot. Pada buah yang terserang terdapat bercak cokelat dan menjadi keriput (1B). Menurut CABI (2007) bercak pada buah kakao yang disebabkan B. theobromae pada awalnya merupakan klorosis yang kemudian menjadi bercak cokelat yang meluas. A B C D E Gambar 1 Gejala penyakit yang disebabkan oleh cendawan B. theobromae pada lima tanaman inang. Jeruk (A); kakao (B); karet (C); manggis (D); pisang (E). Sumber foto: (A,C,D,E) Suryo Wiyono; (B) TNAU 2008
2 15 Permukaan batang tanaman karet muda yang terserang B. theobromae menjadi berwarna cokelat dan teksturnya menjadi kasar (1C). Menurut Pha et al. (2009) pada kelembaban yang cukup miselia berwarna putih akan muncul pada permukaan batang yang retak serta kulit batang dan ranting terkelupas. kulit batang karet yang terserang menjadi busuk disertai keluarnya lateks atau getah pada tanaman muda berumur 1-2 tahun. Pada serangan yang berat dapat menyebabkan retak dan gummosis. Tanaman manggis yang terserang B. theobromae mengalami mati ujung, ranting menjadi kering dan berwarna hitam, selain itu kulit terkelupas dan menjadi luka (1D). Buah pisang yang terserang B. theobromae mengalami busuk buah. Pada kulit buah terdapat bercak-bercak hitam kecokelatan tidak beraturan yang dapat meluas (1E). Menurut Raut & Ranade (2004) pada awalnya bercak berwarna cokelat muda, lama kelamaan bercak berubah warna menjadi cokelat tua hingga hitam. Bercak meluas dimulai dari bagian ujung atas buah yang kemudian menyebar hingga ke seluruh bagian buah sehingga daging buah menjadi berwarna cokelat tua hingga hitam, lembek dan berair. Dalam keadaan yang lembab miselium dan piknidia berwarna hitam juga dapat terlihat pada jaringan tanaman yang bergejala. Karakter Morfologi B. theobromae Karakter morfologi cendawan B. theobromae berasal dari lima inang menunjukkan bahwa cendawan-cendawan tersebut memiliki perbedaan dalam warna koloni (Gambar 2). Koloni pada usia 11 hari (tua) isolat asal jeruk berwarna abu-abu muda, kakao berwarna cokelat, karet berwarna cokelat tua, manggis berwarna hitam keabuan, dan pisang berwarna hitam pekat. Perubahan warna koloni pada karet, kakao, pisang, dan jeruk secara merata di seluruh miselium pada cawan petri pada awalnya berwarna putih terus bertambah gelap dengan bertambahnya umur koloni. Sedangkan pada manggis perubahan warna dimulai dari tengah koloni yang mulai berwarna gelap dan terus menyebar hingga ke bagian pinggir koloni pada cawan petri.
3 16 3 HST 11 HST A B C D E Gambar 2 Koloni isolat cendawan B. theobromae dari lima tanaman inang pada media PDA berumur 3 dan 11 hari setelah tanam (HST). Jeruk (A), kakao (B), karet (C), manggis (D), pisang (E). Koloni mengalami perubahan warna dengan bertambahnya umur koloni. Pada isolat asal manggis miselium berwarna putih hingga 3 hari setelah tanam (HST) dan terus bertambah gelap seiring waktu hingga 7 HST. Isolat asal pisang dan karet berwarna putih hingga 6 HST dan terus bertambah gelap seiring waktu hingga 8 HST, sedangkan isolat asal kakao dan jeruk miselium masih berwarna putih hingga 10 HST dan terus bertambah gelap seiring waktu hingga 15 HST. Diameter koloni (cm) Umur biakan (Jam) Jeruk Kakao Karet Manggis Pisang Gambar 3 Pertumbuhan ukuran koloni cendawan B. theobromae pada media PDA selama 96 jam
4 Tabel 2 Pertumbuhan diameter koloni cendawan B. theobromae B. theobromae Kecepatan pertumbuhan koloni isolat asal (cm)/12 Jam ± SD Jeruk 1,48 a ± 0,24 Kakao 1,20 ab ± 0,17 Karet 1,45 a ± 0,13 Manggis 0,68 b ± 0,59 Pisang 1,68 a ± 0,15 Keterangan: Huruf berbeda menunjukkan perbedaan nyata dengan uji selang ganda Duncan (α = 0,05), SD = standar deviasi Pertumbuhan koloni B. theobromae pada lima tanaman inang menunjukkan kecepatan yang berbeda-beda. Koloni isolat asal pisang memiliki kecepatan tumbuh paling cepat yaitu 1,68 cm per 12 jam, sedangkan isolat asal manggis menunjukkan kecepatan pertumbuhan paling lambat yaitu 0,68 cm per 12 jam (Tabel 2). Kecepatan pertumbuhan isolat asal jeruk, karet dan pisang tidak berbeda nyata, isolat asal kakao tidak berbeda nyata dengan semua isolat lain. Ukuran maksimum koloni cendawan B. theobromae pada media PDA di dalam cawan petri dalam penelitian ini adalah 9 cm. Pada umumnya pertumbuhan miselium mencapai 9 cm pada jam setelah tanam (JST). Pada Gambar 3 ditunjukkan bahwa pertumbuhan paling cepat adalah pada isolat B. theobromae asal pisang yaitu mencapai 9 cm pada 36 JST, miselium isolat asal jeruk dan karet memiliki kecepatan pertumbuhan yang hampir sama mencapai 9 cm pada 48 HST. Pada isolat asal kakao pertumbuhan miselium mencapai 9 cm pada 72 JST, sedangkan pertumbuhan miselium asal manggis adalah yang paling lambat yaitu mencapai 9 cm pada 84 JST. Gambar 4 menunjukkan piknidia B. theobromae asal tanaman jeruk, kakao, karet, manggis dan pisang dengan perbesaran 4 X 10. Piknidia merupakan tubuh buah yang berbentuk seperti labu yang didalamnya terdapat konidiofor dan memproduksi konidia (Agrios 2005). Pada umumnya piknidia berwarna cokelat hingga hitam dan diselimuti oleh miselia. Piknidia terbentuk secara berpencar atau tidak berkelompok. Pada Gambar 4 A, B, C, dan D piknidia tampak dari atas, sebagian tubuh piknidia muncul di permukaan, sehingga jika tampak dari atas piknidia berbentuk bulat dan timbul serta diselimuti oleh miselium cendawan 17
5 18 putih. Piknidia asal tanaman jeruk, kakao dan manggis berwarna hitam, sedangkan piknidia asal tanaman karet dan pisang berwarna cokelat tua hingga cokelat kehitaman. A B C D E Gambar 4 Piknidia cendawan B. theobromae dari lima tanaman inang dengan perbesaran 40x. Jeruk (A); kakao (B); karet (C); manggis (D); pisang (E). Piknidia B. theobromae yang berasal dari tanaman pisang (Gambar 4 E), tampak dari samping berbentuk jorong atau tabung, berwarna cokelat, dan piknidia terbentuk diantara miselium cendawan. Tampak samping terlihat bahwa sebagian tubuh piknidia muncul di atas permukaan koloni cendawan, sedangkan sebagian lainnya berada di dalam miselium. Gambar 5 Piknidia B. theobromae yang pecah mengeluarkan konidia
6 19 Piknidia berwarna hitam yang pecah dan mengeluarkan konidia muda (Gambar 5). Dengan pewarnaan menggunakan lactophenol blue konidia muda tampak berwarna biru, konidia keluar dari dalam piknidia yang dipecahkan. Menurut Masilamani & Muthumar (1996) pada kondisi alami piknidia matang akan menghasilkan konidia matang yang kemudian konidia matang akan keluar melalui lubang ostiol pada piknidia dan kemudian menyebar. Gambar 6 menunjukkan konidia muda dan konidia matang B. theobromae yang berasal dari empat tanaman inang dengan perbesaran 10 X 100 dan pewarnaan dengan lactophenol blue. Konidia muda tidak memiliki sekat (bersel satu), dinding konidia relatif tebal, dan berwarna hialin sehingga jika diwarnai dengan lactophenol blue maka konidia akan terlihat berwarna biru. Morfologi konidia matang memiliki perbedaan dengan konidia muda, yaitu konidia matang berwarna cokelat tua, memiliki sekat, terdiri dari dua sel dan dinding konidia yang tidak nampak ketebalannya. Menurut Watanabe (2002) konidia B. theobromae berpencar secara tunggal, hialin, berbentuk jorong atau silinder, dan pada umumnya konidia matang terdiri dari dua sel (bersekat satu). Pada Tabel 3 ditunjukkan bahwa semua isolat B. theobromae asal lima tanaman inang membentuk piknidia pada media WA+jerami, sedangkan pada media PDA hanya tiga isolat saja (asal jeruk, karet dan pisang). Konidia muda dan konidia matang dibentuk oleh isolat asal empat tanaman inang pada media WA+jerami sedangkan pada media PDA hanya tiga isolat. Pada media PDA, B. theobromae asal kakao tidak terbentuk piknidia, konidia muda, dan konidia matang, hal ini karena media PDA termasuk media yang kaya hara seperti glukosa dan karbohidrat. Menurut Shivas & Beasley (2005), lingkungan yang tidak alami, seperti media agar-agar yang kaya hara, dapat saja merupakan kondisi yang kurang cocok untuk sporulasi cendawan patogen tanaman. Sporulasi B. theobromae dapat ditingkatkan dengan penambahan material asal tanaman yang telah disterilkan, misalnya jerami.
7 20 Konidia muda A B C D Konidia matang A B C Gambar 6 D Konidia muda maupun matang cendawan B. theobromae dari empat tanaman inang. Jeruk (A); kakao (B); karet (C); pisang (D).
8 21 Tabel 3 Pembentukan piknidia, konidia muda, dan konidia matang B. theobromae lima tanaman inang pada media WA dan PDA Tanaman Inang WA +jerami Waktu (hari) untuk pembentukan Piknidia Konidia Muda Konidia Matang PDA WA +jerami PDA WA +jerami PDA Jeruk Kakao Karet Manggis Pisang Keterangan: WA = water agar, PDA = potato dextrose agar, (-): tidak terbentuk Pembentukan piknidia, konidia muda, dan konidia matang pada media WA+jerami cenderung lebih cepat dibanding pada media PDA. B. theobromae memproduksi piknidia yang menghasilkan konidia pada kondisi lingkungan yang kurang menguntungkan yaitu kurangnya hara dan media WA+jerami merupakan media yang miskin hara sehingga piknidia dan konidia terbentuk lebih cepat pada media tersebut. Piknidia isolat B. theobromae pada media PDA terbentuk antara HST. Pada isolat asal jeruk dan pisang piknidia terbentuk paling cepat yaitu pada 17 HST, sedangkan pembentukan piknidia pada isolat asal karet paling lambat yaitu terbentuk setelah 32 HST. Pada isolat asal jeruk konidia muda terbentuk paling cepat diantara isolat lain yaitu pada 17 HST, sedangkan isolat asal kakao terbentuk paling lambat yaitu setelah 39 HST. Konidia matang pada media PDA terbentuk antara HST. Pada isolat asal jeruk dan pisang konidia matang terbentuk paling cepat yaitu pada 22 HST, isolat asal karet pembentukan konidia matang paling lambat yaitu terbentuk setelah 48 HST. Menurut Shah et al. (2010) waktu yang dibutuhkan B. theobromae untuk menghasilkan piknidia pada media buatan adalah antara hari setelah tanam. Isolat B. theobromae asal manggis hanya membentuk piknidia pada media WA+jerami saja, tetapi tidak pada PDA. Konidia muda, dan konidia matang tidak terbentuk baik pada media WA+jerami maupun media PDA. Sandra (2011) menyatakan bahwa piknidia dan konidia B. theobromae asal manggis hanya dapat terbentuk pada media dengan bahan induksi berupa kulit manggis, hal ini
9 22 menunjukkan bahwa dalam pembentukan piknidia dan konidia diperlukan nutrisi tertentu agar dapat merangsang pembentukannya. Konidia muda pada isolat B. theobromae asal jeruk berukuran µm X µm, konidia muda asal kakao berukuran µm X 9-11 µm, konidia muda asal karet berukuran µm X 9-12 µm, sedangkan konidia asal pisang berukuran µm X 8-12 µm (Tabel 4). Menurut Watanabe (2002) piknidia cendawan B. theobromae berukuran 210 µm X 150 µm, dan konidia berukuran 7,5-17,5 µm X 2,2-4,5 µm. Tabel 4 Ukuran panjang, lebar, dan tebal dinding konidia muda B. theobromae asal empat tanaman inang pada media water agar + jerami Tanaman Inang Panjang (µm) ± SD Ukuran konidia muda Lebar (µm) ± SD Rasio panjang/lebar ± SD Tebal dinding (µm) ± SD Jeruk 22,91 a ± 2,38 12,68 a ± 0,73 1,82 a ± 0,27 1,72 a ± 0,23 Kakao 16,96 b ± 1,64 9,54 c ± 0,52 1,78 a ± 0,19 1,54 ab ± 0,49 Karet 17,44 b ± 1,25 10,56 b ± 1,19 1,67 a ± 0,23 1,86 a ± 0,29 Pisang 17,42 b ± 1,38 10,09 bc ± 1,07 1,75 a ± 0,30 1,32 b ± 0,25 Keterangan: Huruf berbeda menunjukkan perbedaan nyata dengan uji selang ganda Duncan (α = 0,05) SD = standar deviasi Ukuran panjang, lebar, dan tebal dinding konidia muda B. theobromae berbeda nyata (Tabel 4). Konidia muda B. theobromae asal jeruk memiliki ukuran paling besar yaitu rata-rata panjang konidia 22,91 µm dan lebar 12,68 µm, sedangkan konidia muda isolat asal kakao memiliki ukuran paling kecil, yaitu rata-rata panjang konidia 16,96 µm dan lebar 9,54 µm. Tebal dinding isolat asal karet memiliki ukuran yang paling besar yaitu 1,86 µm, sedangkan isolat asal pisang memiliki tebal dinding yang paling kecil yaitu 1,32 µm. Rasio panjang/lebar konidia muda B. theobromae asal jeruk, kakao, karet, dan pisang tidak berbeda nyata (Tabel 5). Konidia muda isolat asal jeruk memiliki rasio panjang/lebar tertinggi yaitu 1,82 sedangkan konidia isolat asal karet memiliki rasio panjang/lebar terendah yaitu 1,67. Rasio panjang/lebar konidia muda dari keempat isolat >1 sehingga konidia berbentuk jorong. Bentuk konidia akan semakin bulat jika rasio panjang/lebar mendekati 1.
10 23 Panjang dan lebar konidia matang isolat B. theobromae asal empat tanaman inang memiliki ukuran panjang dan lebar konidia matang yang berbeda nyata (Tabel 5). Konidia matang pada isolat B. theobromae asal jeruk berukuran µm X µm, konidia matang asal kakao berukuran µm X 9-12 µm, konidia matang asal karet berukuran µm X 9-13 µm, sedangkan konidia matang asal pisang berukuran µm X µm. Berdasarkan pengukuran, ukuran konidia matang cenderung lebih besar dibandingkan konidia muda, namun tebal dinding konidia matang tidak dapat diukur karena tebal dinding terlalu kecil. Tabel 5 Ukuran panjang dan lebar konidia matang cendawa B. theobromae asal empat tanaman inang pada media water agar + jerami Ukuran konidia matang Tanaman Panjang (µm) Rasio panjang/lebar Inang Lebar (µm) ± SD ± SD ± SD Jeruk 23,63 a ± 2,26 12,83 a ± 1,10 1,86 a ± 0,31 Kakao 15,40 c ± 1,96 10,67 b ± 1,00 1,44 b ± 0,12 Karet 21,08 b ± 3,19 11,39 b ± 1,45 1,89 a ± 0,46 Pisang 19,32 b ± 1,98 11,59 b ± 1,01 1,68 ab ± 0,21 Keterangan: Huruf berbeda menunjukkan perbedaan nyata dengan uji selang ganda Duncan (α = 0,05) SD = standar deviasi Panjang dan lebar konidia matang isolat B. theobromae asal empat tanaman inang memiliki ukuran panjang dan lebar konidia matang yang berbeda nyata (Tabel 5). Konidia matang B. theobromae asal jeruk memiliki ukuran paling besar yaitu rata-rata panjang konidia 23,63 µm dan lebar 12,83 µm, sedangkan konidia matang isolat asal kakao memiliki ukuran paling kecil, yaitu rata-rata panjang konidia 15,40 µm dan lebar 10,67 µm. Perbedaan ukuran konidia matang dan muda B. theobromae menunjukkan bahwa ada keragaman ukuran konidia antar isolat yang berasal dari tanaman inang yang berbeda. Rasio panjang/lebar konidia muda B. theobromae asal jeruk, kakao, karet, dan pisang berbeda nyata (Tabel 4). Rasio panjang/lebar konidia matang dari keempat isolat >1 sehingga konidia berbentuk jorong (Tabel 5). Bentuk konidia akan semakin bulat jika rasio panjang/lebar mendekati 1. Konidia muda isolat asal karet memiliki rasio panjang/lebar tertinggi yaitu 1,89 sedangkan konidia isolat asal kakao memiliki rasio panjang/lebar terendah yaitu 1,44. Rasio panjang/lebar
11 24 konidia muda lebih rendah dibanding konidia matang kecuali pada isolat asal kakao, sehingga bentuk konidia matang lebih jorong dibanding konidia muda. Karakter Molekuler Cendawan B. theobromae Analisis molekuler terhadap DNA cendawan B. theobromae dilakukan dengan teknik RAPD-PCR menggunakan primer OPD 06 (Gambar 7, Tabel 6) dan OPN 07 (Gambar 8, Tabel 7). Gambar 7 menunjukkan pola RAPD-PCR menggunakan primer OPD 06 dan Gambar 8 menggunakan primer OPN 07 dan marker GeneRuler TM DNA Ladder. Gambar tersebut menunjukkan bahwa primer OPD 06 dan OPN 07 dapat mengamplifikasi DNA cendawan B. theobromae asal berbagai tanaman inang di beberapa lokasi pada genom cendawan tersebut dengan ukuran amplikon yang berbeda-beda. Gambar 7 Profil DNA lima isolat cendawan B. theobromae yang diamplifikasi dengan RAPD-PCR menggunakan primer OPD 06 Tabel 6 Ukuran fragmen DNA cendawan B. theobromae asal berbagai tanaman inang dengan RAPD menggunakan primer OPD 06 Pita DNA ke- Ukuran (bp) pita DNA isolat B. theobromae asal Jeruk Kakao Karet Manggis Pisang <500 < Keterangan: bp= base pair (pasangan basa)
12 25 Tabel 6 menunjukkan ukuran fragmen DNA cendawan B. theobromae asal lima tanaman inang hasil RAPD menggunakan primer OPD 06. Profil DNA kelima cendawan B. theobromae memiliki perbedaan jumlah dan ukuran pita DNA yang dihasilkan. Pada isolat B. theobromae asal kakao, karet, dan manggis DNA teramplifikasi pada satu lokasi, DNA isolat asal jeruk dan pisang teramplifikasi pada dua lokasi, selain itu ukuran pita DNA yang teramplifikasi pada kelima isolat berbeda-beda. Hal ini menunjukkan bahwa kelima isolat tersebut memiliki perbedaan genetik. Gambar 8 Profil DNA lima isolat cendawan B. theobromae yang diamplifikasi dengan RAPD-PCR menggunakan primer OPN 07. Tabel 7 Ukuran fragmen DNA cendawan B. theobromae asal berbagai tanaman inang dengan RAPD menggunakan primer OPN 07 Pita DNA ke- Ukuran (bp) pita DNA isolat B. theobromae asal Jeruk Kakao Karet Manggis Pisang Keterangan: bp= base pair (pasangan basa)
13 26 Tabel 7 menunjukkan ukuran fragmen DNA isolat B. theobromae asal lima tanaman inang hasil RAPD menggunakan primer OPN 07. Profil DNA kelima isolat B. theobromae menunjukkan perbedaan jumlah dan ukuran pita DNA yang lebih beragam dibandingkan dengan pola RAPD dengan primer OPD 06. Pada isolat B. theobromae asal manggis DNA teramplifikasi pada satu lokasi, DNA isolat asal jeruk dan kakao teramplifikasi pada tiga lokasi, sedangkan DNA isolat asal karet teramplifikasi pada enam lokasi. Selain itu ukuran pita DNA yang teramplifikasi pada kelima isolat berbeda-beda (Gambar 8), hal ini menunjukkan bahwa keempat isolat tersebut memiliki perbedaan genetik yang cukup nyata. RAPD menggunakan primer tunggal pendek dengan urutan nukleotida acak, dilakukan dengan suhu annealing rendah dan menghasilkan beberapa produk PCR yang menghasilkan pola pita setelah dilakukan pemisahan oleh elektroforesis (Edel 1998). Menurut Edel (1998), analisis DNA menggunakan RAPD umumnya dilakukan dengan primer non-spesifik sehingga kondisi reaksi dan thermocycle RAPD lebih sensitif dibandingkan tes PCR konvensional. Dengan demikian konsentrasi dari semua campuran bahan dalam reaksi harus akurat. Selain itu kualitas dari template DNA dan Taq polymerase merupakan faktor yang juga dapat mempengaruhi hasil RAPD. Gejala Penyakit oleh Cendawan R. solani Penyakit yang disebabkan oleh R. solani pada tiga tanaman inang menunjukan gejala yang beragam (Gambar 9). Gejala yang disebabkan oleh R. solani pada tanaman jagung (Gambar 9A) yaitu terdapat bercak tidak teratur berwarna putih kotor atau cokelat muda dan pada bagian pinggir bercak berwarna cokelat tua. Bercak terus meluas dari mulai bagian pelepah hingga ke seluruh jaringan tanaman. Pada bagian tanaman yang terserang cukup parah, seluruh bagian tanaman menjadi berwarna cokelat dan kering, kemudian tanaman mati. Pada bagian tanaman yang sudah mati terdapat sklerotia berwarna cokelat.
14 27 A B C Gambar 9 Gejala penyakit yang disebabkan oleh cendawan R. solani pada tiga tanaman inang. Jagung (A); Padi (B); Sorghum (C). Pelepah tanaman padi yang terserang cendawan R. solani (9B) terdapat bercak tidak beraturan berwarna cokelat hingga hitam dengan pusat bercak berwarna putih, abu-abu atau cokelat muda, biasanya cendawan tersebut menyerang pada bagian bawah pelepah kemudian akan terus menyebar ke bagian atas. Pelepah bagian atas yang terserang menjadi kering, sedangkan pelepah bagian bawah menjadi lembek dan mudah hancur atau patah karena pada bagian bawah pelepah memiliki kelembaban yang lebih tinggi. Tanaman Sorghum (9C) yang terserang R. solani menunjukkan gejala yang khas, yaitu terdapat bercak meluas yang bersudut pada bagian bawah bercak dengan pusat bercak berwarna putih, putih kotor atau cokelat muda. Pada bagian pinggir bercak berwarna cokelat tua. Bagian yang terserang parah akan menjadi kering dan kemudian tanaman mati. Pada bagian tanaman yang mati terdapat sklerotia berwarna cokelat. Karakter Morfologi R. solani Hasil pengamatan karakter morfologi terhadap cendawan R. solani yang berasal dari lima inang yaitu: jagung, nanas, padi, sorghum, dan ubi jalar (Gambar 10), menunjukkan bahwa koloni kelima isolat R. solani memiliki warna yang berbeda. Pada isolat asal jagung miselium berwarna kuning cerah, isolat asal nanas berwarna cokelat, isolat asal padi berwarna cokelat kemerahan, isolat asal sorghum berwarna cokelat muda, sedangkan isolat asal ubi jalar miselium berwarna hitam pada bagian tengah koloni dan berwarna cokelat tua pada pinggiran koloni. Pada isolat asal jagung, nanas dan sorghum perubahan warna merata pada seluruh miselium seiring waktu, sedangkan pada isolat asal padi dan
15 ubi jalar perubahan warna dimulai dari tengah koloni dan terus bertambah gelap hingga bagian pinggir koloni HST 18 HST A B C D E Gambar 10 Koloni isolat cendawan R. solani dari lima tanaman inang pada umur 4 dan 18 HST pada media PDA. jagung (A); nanas (B); padi (C); sorghum (D); ubi jalar (E). Koloni mengalami perubahan warna dengan bertambahnya umur koloni. Pada isolat asal jagung miselium berwarna putih hingga 2 HST kemudian berubah menjadi berwarna kuning hingga 5 HST dan menjadi kuning cerah hingga 18 HST. Sedangkan pada isolat nanas, padi dan sorghum miselium berwarna putih hingga 3 HST kemudian menjadi berwarna kuning muda hingga 4 HST dan terus bertambah gelap hingga 15 HST. Isolat asal ubi menunjukkan perubahan warna paling cepat diantara isolat lain yaitu berwarna putih hingga 1 HST kemudian terus bertambah gelap hingga 5 HST. Kecepatan pertumbuhan koloni R. solani pada lima tanaman inang berbeda nyata (Tabel 8). Koloni isolat asal jagung memiliki kecepatan tumbuh paling cepat yaitu rata-rata pertumbuhan 4,20 cm per 12 jam, sedangkan isolat asal ubi jalar menunjukkan kecepatan pertumbuhan paling lambat yaitu rata-rata 1,60 cm per 12 jam. Pertumbuhan maksimum koloni R. solani pada media PDA di dalam cawan petri adalah 9 cm. Umumnya pertumbuhan koloni cendawan R. solani mencapai maksimum pada jam setelah tanam (JST).
16 Diameter Koloni (cm) Jagung Nanas Padi Sorghum Ubi Jalar Umur Biakan (Jam) Gambar 11 Grafik pertumbuhan koloni cendawan R. solani pada media PDA. Tabel 8 Pertumbuhan diameter koloni cendawan R. solani Tanaman Inang Kecepatan pertumbuhan koloni isolat asal (cm)/12 jam ± SD Jagung 4,20 a ± 0.36 Nanas 2,37 b ± 0.58 Padi 1,87 bc ± 0.15 Sorghum 1,80 bc ± 0.17 Ubi Jalar 1,60 c ± 0.17 Keterangan: Huruf berbeda menunjukkan perbedaan nyata dengan uji selang ganda Duncan (α = 0,05) SD = standar deviasi Pada Gambar 11 ditunjukkan bahwa pertumbuhan miselium paling cepat adalah isolat asal jagung, yaitu pada 48 JST dan yang paling lambat adalah isolat asal ubi jalar yaitu pada 120 JST. Terdapat perbedaan kecepatan pertumbuhan pada kelima isolat tersebut. Gambar 12 merupakan hifa R. solani yang berasal dari lima tanaman inang, dengan pewarnaan lactophenol blue. Hifa R. solani memiliki percabangan yang tegak lurus, berwarna hialin dan memiliki sekat. Menurut Schumann & D Arcy (2006) R. solani dapat diidentifikasi dari karakter hifa yang khas, yaitu sudut percabangan yang tegak lurus yang membedakan dengan cendawan lainnya.
17 30 A B C D E Gambar 12 Hifa cendawan R. solani asal lima tanaman inang dengan perbesaran 10 X 100 dan pewarnaan lactophenol blue. Jagung (A); nanas (B); padi (C); sorghum (D); ubi jalar (E). Tabel 9 Ukuran panjang ruas dan lebar hifa cendawan R. solani pada lima tanaman inang Ukuran hifa (µm) Tanaman Inang Panjang ruas ± SD Lebar ± SD Jagung 29,32 c ± 7,36 2,78 c ± 0,46 Nanas 45,57 b ± 13,21 3,98 b ± 0,52 Padi 56,99 a ± 18,54 4,59 a ± 1,13 Sorghum 60,15 a ± 23,16 5,01 a ± 0,83 Ubi Jalar 39,57 b ± 11,03 3,78 b ± 0,67 Keterangan: Huruf berbeda menunjukkan perbedaan nyata dengan uji selang ganda Duncan (α = 0,05) SD = standar deviasi Panjang ruas dan lebar hifa R. solani asal padi dengan asal sorghum tidak berbeda nyata dan isolat asal nanas dengan asal ubi jalar tidak berbeda nyata, sedangkan isolat asal jagung berbeda nyata terhadap keempat isolat lainnya. R. solani asal sorghum memiliki panjang ruas dan lebar yang paling besar diantara isolat lainnya yaitu panjang ruas µm dan lebar 4-7 µm, sedangkan jagung memiliki panjang ruas dan lebar yang paling kecil diantara isolat lainnya yaitu panjang ruas µm dan lebar 2-4 µm (Tabel 9).
18 31 Hifa R. solani pada lima tanaman inang yaitu, jagung, nanas, padi, sorghum dan ubi jalar memiliki rata-rata sudut percabangan yang berbeda-beda namun tidak berbeda nyata. Sudut percabangan cendawan tersebut pada kelima tanaman inang hampir tegak lurus mendekati 90º. Hifa isolat asal ubi jalar memiliki sudut tumpul yang paling besar yaitu dengan rata-rata 108,95º, kemudian isolat asal sorghum dengan sudut tumpul 106,1º, isolat asal padi 105,75º, isolat asal jagung 105,3º, sedangkan isolat asal nanas cenderung lebih tegak lurus dibandingkan isolat lainnya karena memiliki sudut tumpul yang paling kecil yaitu 103º. A B Gambar 13 Sklerotia cendawan R. solani. Sklerotia muda (A); sklerotia tua (B). Sklerotia merupakan sekumpulan hifa yang mengalami pemadatan, berwarna gelap dan mampu betahan dalam kondisi lingkungan yang tidak menguntungkan (Agrios 2005). Sklerotia merupakan struktur bertahan pada cendawan R. solani (Gambar 13), terbentuk ketika cendawan dalam kondisi kekurangan nutrisi namun kelembaban cukup. Sklerotia R. solani memiliki permukaan kasar dengan bentuk yang tidak beraturan serta memiliki struktur yang keras. Pada hari pertama terbentuk sklerotia berwarna putih yang merupakan sklerotia muda, kemudian hari kedua hingga hari keempat sklerotia akan berubah menjadi warna cokelat. Karakter Molekuler Cendawan R. solani Analisis molekuler terhadap DNA R. solani dilakukan dengan teknik RAPD-PCR menggunakan primer OPD 06 dan OPN 07. Gambar 14 menunjukkan pola RAPD-PCR dengan primer OPD 06, sedangkan Gambar 15 merupakan pola RAPD-PCR menggunakan primer OPN 07 dan marker GeneRuler TM DNA
19 32 Ladder. Dari kedua gambar tersebut dapat dilihat bahwa kedua primer dapat mengamplifikasi DNA cendawan R. solani dari lima tanaman inang di berbagai lokasi pada genom cendawan tersebut. Gambar 14 Profil DNA empat isolat cendawan R. solani yang diamplifikasi dengan RAPD-PCR menggunakan primer OPD 06. Tabel 10 Ukuran fragmen DNA cendawan R. solani asal berbagai tanaman inang dengan RAPD menggunakan primer OPD 06 Pita DNA ke- Ukuran (bp) pita DNA isolat R. solani asal Jagung Nanas Padi Sorghum Ubi Jalar Keterangan: bp= base pair (pasangan basa) Tabel 10 menunjukkan ukuran fragmen DNA cendawan R. solani asal berbagai tanaman inang hasil RAPD dengan primer OPD 06. Profil DNA keempat cendawan R. solani menunjukkan perbedaan jumlah dan ukuran pita DNA yang dihasilkan. Pada isolat R. solani asal jagung DNA teramplifikasi pada satu lokasi,
20 33 isolat asal sorghum teramplifikasi pada dua lokasi, isolat asal nanas dan ubi jalar teramplifikasi pada tiga lokasi, sedangkan isolat asal padi teramplifikasi pada empat lokasi. Ukuran pita DNA dan jumlah DNA yang teramplifikasi pada kelima isolat berbeda-beda, hal ini menunjukkan bahwa kelima isolat tersebut menunjukkan perbedaan genetik yang cukup nyata. Gambar 15 Profil DNA empat isolat cendawan R. solani yang diamplifikasi dengan RAPD-PCR menggunakan primer OPN 07. Tabel 11 Ukuran fragmen DNA cendawan R. solani asal berbagai tanaman inang dengan RAPD menggunakan primer OPN 07 Pita DNA ke- Ukuran (bp) pita DNA isolat R. solani asal Jagung Nanas Padi Sorghum Ubi Jalar Keterangan: bp= base pair (pasangan basa)
21 34 Tabel 11 menunjukkan ukuran fragmen DNA cendawan R. solani asal berbagai tanaman inang hasil RAPD menggunakan primer OPN 07. Profil DNA keempat cendawan R. solani menunjukkan perbedaan jumlah dan ukuran pita DNA yang dihasilkan dan lebih beragam dibandingkan pola RAPD dengan primer OPD 06. Pada isolat R. solani asal nanas DNA teramplifikasi pada dua lokasi, DNA isolat asal padi dan sorghum teramplifikasi pada enam lokasi, sedangkan DNA isolat asal ubi jalar teramplifikasi pada tujuh lokasi. Selain itu ukuran pita DNA yang teramplifikasi pada keempat isolat juga berbeda-beda, hal ini menunjukkan bahwa keempat isolat tersebut menunjukkan perbedaan genetik yang cukup nyata.
KARAKTERISASI CENDAWAN Botryodiplodia theobromae DAN Rhizoctonia solani DARI BERBAGAI TANAMAN INANG BERDASARKAN MORFOLOGI DAN POLA RAPD-PCR
 KARAKTERISASI CENDAWAN Botryodiplodia theobromae DAN Rhizoctonia solani DARI BERBAGAI TANAMAN INANG BERDASARKAN MORFOLOGI DAN POLA RAPD-PCR YAYU SITI NURHASANAH DEPARTEMEN PROTEKSI TANAMAN FAKULTAS PERTANIAN
KARAKTERISASI CENDAWAN Botryodiplodia theobromae DAN Rhizoctonia solani DARI BERBAGAI TANAMAN INANG BERDASARKAN MORFOLOGI DAN POLA RAPD-PCR YAYU SITI NURHASANAH DEPARTEMEN PROTEKSI TANAMAN FAKULTAS PERTANIAN
TINJAUAN PUSTAKA Cendawan Botryodiplodia theobromae Taksonomi Cendawan Bioekologi dan Nilai Ekonomi
 3 TINJAUAN PUSTAKA Cendawan Botryodiplodia theobromae Taksonomi Cendawan Klasifikasi cendawan Botryodiplodia theobromae (Alexopoulos et al. 1996) adalah sebagai berikut: Domain : Eukaryota Kingdom : Fungi
3 TINJAUAN PUSTAKA Cendawan Botryodiplodia theobromae Taksonomi Cendawan Klasifikasi cendawan Botryodiplodia theobromae (Alexopoulos et al. 1996) adalah sebagai berikut: Domain : Eukaryota Kingdom : Fungi
TINJAUAN PUSTAKA. Adapun klasifikasi Colletotrichum gloeosporioides Penz. Sacc. menurut. : Colletotrichum gloeosporioides Penz. Sacc.
 TINJAUAN PUSTAKA Biologi Penyakit Adapun klasifikasi Colletotrichum gloeosporioides Penz. Sacc. menurut Dwidjoseputro (1978) sebagai berikut : Divisio Subdivisio Kelas Ordo Family Genus Spesies : Mycota
TINJAUAN PUSTAKA Biologi Penyakit Adapun klasifikasi Colletotrichum gloeosporioides Penz. Sacc. menurut Dwidjoseputro (1978) sebagai berikut : Divisio Subdivisio Kelas Ordo Family Genus Spesies : Mycota
TINJAUAN PUSTAKA Nilai Ekonomi Cendawan Botryodiplodia theobromae
 TINJAUAN PUSTAKA Nilai Ekonomi Cendawan Botryodiplodia theobromae B. theobromae dilaporkan telah menyebabkan berbagai penyakit diantaranya mati ujung, busuk akar, busuk buah, bercak daun, dan sapu setan
TINJAUAN PUSTAKA Nilai Ekonomi Cendawan Botryodiplodia theobromae B. theobromae dilaporkan telah menyebabkan berbagai penyakit diantaranya mati ujung, busuk akar, busuk buah, bercak daun, dan sapu setan
TINJAUAN PUSTAKA. Menurut Alexopoulus dan Mims (1979), jamur Ceratocystis fimbriata
 4 TINJAUAN PUSTAKA Biologi Ceratocystis fimbriata. Menurut Alexopoulus dan Mims (1979), jamur Ceratocystis fimbriata dapat diklasifikasikan sebagai berikut, Kingdom : Myceteae, Divisi : Amastigomycota,
4 TINJAUAN PUSTAKA Biologi Ceratocystis fimbriata. Menurut Alexopoulus dan Mims (1979), jamur Ceratocystis fimbriata dapat diklasifikasikan sebagai berikut, Kingdom : Myceteae, Divisi : Amastigomycota,
HASIL DAN PEMBAHASAN
 HASIL DAN PEMBAHASAN Eksplorasi Cendawan Rhizosfer Hasil eksplorasi cendawan yang dilakukan pada tanah rhizosfer yang berasal dari areal tanaman karet di PT Perkebunan Nusantara VIII, Jalupang, Subang,
HASIL DAN PEMBAHASAN Eksplorasi Cendawan Rhizosfer Hasil eksplorasi cendawan yang dilakukan pada tanah rhizosfer yang berasal dari areal tanaman karet di PT Perkebunan Nusantara VIII, Jalupang, Subang,
TINJAUAN PUSTAKA. Menurut Alexopoulus dan Mims (1979), klasifikasi jamur C. cassiicola. : Corynespora cassiicola (Berk. & Curt.) Wei.
 19 TINJAUAN PUSTAKA Biologi Penyakit Menurut Alexopoulus dan Mims (1979), klasifikasi jamur C. cassiicola adalah sebagai berikut : Divisio Sub Divisio Kelas Ordo Famili Genus Spesies : Eumycophyta : Eumycotina
19 TINJAUAN PUSTAKA Biologi Penyakit Menurut Alexopoulus dan Mims (1979), klasifikasi jamur C. cassiicola adalah sebagai berikut : Divisio Sub Divisio Kelas Ordo Famili Genus Spesies : Eumycophyta : Eumycotina
HASIL DAN PEMBAHASAN Deteksi Fi F top lasma p ada Tanaman Sumb m er e I r nokulum
 HASIL DAN PEMBAHASAN Deteksi Fitoplasma pada Tanaman Sumber Inokulum Sumber inokulum yang digunakan dalam uji penularan adalah tanaman kacang tanah yang menunjukkan gejala penyakit sapu yang berasal dari
HASIL DAN PEMBAHASAN Deteksi Fitoplasma pada Tanaman Sumber Inokulum Sumber inokulum yang digunakan dalam uji penularan adalah tanaman kacang tanah yang menunjukkan gejala penyakit sapu yang berasal dari
BAHAN DAN METODE. Tabel 1 Kombinasi perlakuan yang dilakukan di lapangan
 13 BAHAN DAN METODE Tempat dan waktu Penelitian ini dilaksanakan di Desa Ciburuy, Kecamatan Cigombong, Kabupaten Bogor serta di Laboratorium Bakteriologi, Departemen Proteksi Tanaman, Fakultas Pertanian,
13 BAHAN DAN METODE Tempat dan waktu Penelitian ini dilaksanakan di Desa Ciburuy, Kecamatan Cigombong, Kabupaten Bogor serta di Laboratorium Bakteriologi, Departemen Proteksi Tanaman, Fakultas Pertanian,
HASIL DAN PEMBAHASAN Identifikasi Penyebab Berdasarkan Karakter Morfologi
 19 HASIL DAN PEMBAHASAN Identifikasi Penyebab Berdasarkan Karakter Morfologi Dalam pengembangan jeruk di lahan basah, penyakit Busuk Pangkal Batang yang disebabkan oleh organisme mirip cendawan (fungal
19 HASIL DAN PEMBAHASAN Identifikasi Penyebab Berdasarkan Karakter Morfologi Dalam pengembangan jeruk di lahan basah, penyakit Busuk Pangkal Batang yang disebabkan oleh organisme mirip cendawan (fungal
II. TELAAH PUSTAKA. bio.unsoed.ac.id
 II. TELAAH PUSTAKA Koloni Trichoderma spp. pada medium Malt Extract Agar (MEA) berwarna putih, kuning, hijau muda, dan hijau tua. Trichoderma spp. merupakan kapang Deutromycetes yang tersusun atas banyak
II. TELAAH PUSTAKA Koloni Trichoderma spp. pada medium Malt Extract Agar (MEA) berwarna putih, kuning, hijau muda, dan hijau tua. Trichoderma spp. merupakan kapang Deutromycetes yang tersusun atas banyak
TINJAUAN PUSTAKA. enam instar dan berlangsung selama hari (Prayogo et al., 2005). Gambar 1 : telur Spodoptera litura
 S. litura (Lepidoptera: Noctuidae) Biologi TINJAUAN PUSTAKA Telur berbentuk hampir bulat dengan bagian datar melekat pada daun (kadangkadang tersusun 2 lapis), berwarna coklat kekuning-kuningan diletakkan
S. litura (Lepidoptera: Noctuidae) Biologi TINJAUAN PUSTAKA Telur berbentuk hampir bulat dengan bagian datar melekat pada daun (kadangkadang tersusun 2 lapis), berwarna coklat kekuning-kuningan diletakkan
BAHAN DAN METODE Waktu dan Tempat Bahan Metode Isolasi C. gloeosporioides dari Buah Avokad
 15 BAHAN DAN METODE Waktu dan Tempat Penelitian dilaksanakan di Laboratorium Balai Besar Karantina Pertanian (BBKP) Tanjung Priok Wilayah Kerja Bogor, mulai bulan Oktober 2011 sampai Februari 2012. Bahan
15 BAHAN DAN METODE Waktu dan Tempat Penelitian dilaksanakan di Laboratorium Balai Besar Karantina Pertanian (BBKP) Tanjung Priok Wilayah Kerja Bogor, mulai bulan Oktober 2011 sampai Februari 2012. Bahan
III. METODE PENELITIAN. Penelitian dilaksanakan pada Oktober 2011 sampai Maret 2012 di Rumah Kaca
 III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian dilaksanakan pada Oktober 2011 sampai Maret 2012 di Rumah Kaca dan di Laboratorium Penyakit Tumbuhan Jurusan Proteksi Tanaman Fakultas Pertanian Universitas
III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian dilaksanakan pada Oktober 2011 sampai Maret 2012 di Rumah Kaca dan di Laboratorium Penyakit Tumbuhan Jurusan Proteksi Tanaman Fakultas Pertanian Universitas
KERAGAMAN CENDAWAN Botryodiplodia theobromae DARI BERBAGAI TANAMAN INANG BERDASARKAN MORFOLOGI DAN POLA RAPD FITRI KEMALA SANDRA A
 KERAGAMAN CENDAWAN Botryodiplodia theobromae DARI BERBAGAI TANAMAN INANG BERDASARKAN MORFOLOGI DAN POLA RAPD FITRI KEMALA SANDRA A34063054 DEPARTEMEN PROTEKSI TANAMAN FAKULTAS PERTANIAN INSTITUT PERTANIAN
KERAGAMAN CENDAWAN Botryodiplodia theobromae DARI BERBAGAI TANAMAN INANG BERDASARKAN MORFOLOGI DAN POLA RAPD FITRI KEMALA SANDRA A34063054 DEPARTEMEN PROTEKSI TANAMAN FAKULTAS PERTANIAN INSTITUT PERTANIAN
TINJAUAN LITERATUR. Klasifikasi penyakit C. gloeosporioides (Penz.) Sacc menurut
 TINJAUAN LITERATUR Biologi penyakit Klasifikasi penyakit C. gloeosporioides (Penz.) Sacc menurut Dwidjoseputro (1978) sebagai berikut: Divisio Sub divisi Kelas Ordo Family Genus Species : Mycota : Eumycotyna
TINJAUAN LITERATUR Biologi penyakit Klasifikasi penyakit C. gloeosporioides (Penz.) Sacc menurut Dwidjoseputro (1978) sebagai berikut: Divisio Sub divisi Kelas Ordo Family Genus Species : Mycota : Eumycotyna
TINJAUAN PUSTAKA. Menurut Agrios (1996) taksonomi penyakit busuk pangkal batang
 TINJAUAN PUSTAKA Biologi Jamur Busuk Pangkal Batang Menurut Agrios (1996) taksonomi penyakit busuk pangkal batang (Ganoderma spp.) adalah sebagai berikut: Kingdom Phylum Class Subclass Order Family Genus
TINJAUAN PUSTAKA Biologi Jamur Busuk Pangkal Batang Menurut Agrios (1996) taksonomi penyakit busuk pangkal batang (Ganoderma spp.) adalah sebagai berikut: Kingdom Phylum Class Subclass Order Family Genus
II. MATERI DAN METODE PENELITIAN
 8 II. MATERI DAN METODE PENELITIAN 1. Materi, Lokasi, dan Waktu Penelitian 1.1 Materi Penelitian 1.1.1 Bahan Bahan yang digunakan dalam penelitian ini adalah jamur yang bertubuh buah, serasah daun, batang/ranting
8 II. MATERI DAN METODE PENELITIAN 1. Materi, Lokasi, dan Waktu Penelitian 1.1 Materi Penelitian 1.1.1 Bahan Bahan yang digunakan dalam penelitian ini adalah jamur yang bertubuh buah, serasah daun, batang/ranting
II. TINJAUAN PUSTAKA. A. Klasifikasi dan Deskripsi Tanaman Cabai Merah (Capsicum annuum L.)
 II. TINJAUAN PUSTAKA A. Klasifikasi dan Deskripsi Tanaman Cabai Merah (Capsicum annuum L.) Tanaman cabai merah (Capsicum annuum L.) merupakan tanaman sayuran yang tergolong tanaman tahunan berbentuk perdu.
II. TINJAUAN PUSTAKA A. Klasifikasi dan Deskripsi Tanaman Cabai Merah (Capsicum annuum L.) Tanaman cabai merah (Capsicum annuum L.) merupakan tanaman sayuran yang tergolong tanaman tahunan berbentuk perdu.
TINJAUAN PUSTAKA. Biologi Hama Boleng (Cylas formicarius (Fabr.))
 TINJAUAN PUSTAKA Biologi Hama Boleng (Cylas formicarius (Fabr.)) C. formicarius merupakan kendala utama dalam peningkatan mutu ubi jalar (CIP 1991) dan tersebar di seluruh dunia seperti Amerika, Kenya,
TINJAUAN PUSTAKA Biologi Hama Boleng (Cylas formicarius (Fabr.)) C. formicarius merupakan kendala utama dalam peningkatan mutu ubi jalar (CIP 1991) dan tersebar di seluruh dunia seperti Amerika, Kenya,
III. METODE PENELITIAN
 III. METODE PENELITIAN A. Materi, Lokasi dan Waktu Penelitian 1. Materi Penelitian a. Bahan Bahan yang digunakan dalam penelitian ini adalah jamur yang memiliki tubuh buah, serasah daun, ranting, kayu
III. METODE PENELITIAN A. Materi, Lokasi dan Waktu Penelitian 1. Materi Penelitian a. Bahan Bahan yang digunakan dalam penelitian ini adalah jamur yang memiliki tubuh buah, serasah daun, ranting, kayu
HASIL DAN PEMBAHASAN
 6 HASIL DAN PEMBAHASAN Pembiakan Streptomyces katrae pada Formulasi Media Beras, Jagung dan Limbah Baglog Jamur S. katrae merupakan aktinomiset dari golongan Streptomyces yang pertama diisolasi dari tanah
6 HASIL DAN PEMBAHASAN Pembiakan Streptomyces katrae pada Formulasi Media Beras, Jagung dan Limbah Baglog Jamur S. katrae merupakan aktinomiset dari golongan Streptomyces yang pertama diisolasi dari tanah
BAHAN DAN METODE Waktu dan Tempat Bahan dan Alat
 BAHAN DAN METODE Waktu dan Tempat Perbanyakan P. citrophthora dan B. theobromae dilaksanakan di Laboratorium Mikologi Tumbuhan Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor,
BAHAN DAN METODE Waktu dan Tempat Perbanyakan P. citrophthora dan B. theobromae dilaksanakan di Laboratorium Mikologi Tumbuhan Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor,
TINJAUAN PUSTAKA. Gambar 1 : Pengamatan mikroskopis S. rolfsii Sumber :
 4 TINJAUAN PUSTAKA Biologi Penyebab Penyakit Jamur penyebab penyakit rebah semai ini dapat diklasifikasikan sebagai berikut : Kingdom Divisi Kelas Ordo Famili Genus Spesies : Fungi : Basidiomycota : Basidiomycetes
4 TINJAUAN PUSTAKA Biologi Penyebab Penyakit Jamur penyebab penyakit rebah semai ini dapat diklasifikasikan sebagai berikut : Kingdom Divisi Kelas Ordo Famili Genus Spesies : Fungi : Basidiomycota : Basidiomycetes
Analisis Sidik Ragam Jumlah Sklerotium S. rolfsii Pada Perlakuan Jenis Ekstrak Pupuk Kandang dan Lama Perendaman umur 1, 2, 3 dan 4 hsi
 Lampiran 1. Analisis Sidik Ragam Jumlah Sklerotium S. rolfsii Pada Perlakuan Jenis Ekstrak Pupuk Kandang dan Lama Perendaman umur 1, 2, 3 dan 4 hsi SK db F hit 1 hsi 2 hsi 3 hsi 4 hsi Efek K 2 8.60** 19.30**
Lampiran 1. Analisis Sidik Ragam Jumlah Sklerotium S. rolfsii Pada Perlakuan Jenis Ekstrak Pupuk Kandang dan Lama Perendaman umur 1, 2, 3 dan 4 hsi SK db F hit 1 hsi 2 hsi 3 hsi 4 hsi Efek K 2 8.60** 19.30**
BAHAN DAN METODE. Penelitian dilaksanakan di Laboratorium Penyakit Tumbuhan Jurusan Proteksi
 11 III. BAHAN DAN METODE 3.1 Tempat Penelitian dan Waktu Penelitian dilaksanakan di Laboratorium Penyakit Tumbuhan Jurusan Proteksi Tanaman Fakultas Pertanian Universitas Lampung. Pelaksanaan penelitian
11 III. BAHAN DAN METODE 3.1 Tempat Penelitian dan Waktu Penelitian dilaksanakan di Laboratorium Penyakit Tumbuhan Jurusan Proteksi Tanaman Fakultas Pertanian Universitas Lampung. Pelaksanaan penelitian
BAHAN DAN METODE. Pembiakan P. fluorescens dari Kultur Penyimpanan
 BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilaksanakan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor mulai bulan Februari
BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilaksanakan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor mulai bulan Februari
LAMPIRAN. Ciri makroskopis : mula-mula koloni berupa jelaga-jelaga hitam yang halus, hari fungi mulai menutupi permukaan cawan petri.
 LAMPIRAN Lampiran 1. Ciri makroskopis dan mikroskopis fungi yang ditemukan pada serasah A. marina yang mengalami proses dekomposisi pada berbagai tingkat salinitas 1. Aspergillus sp.1 Ciri makroskopis
LAMPIRAN Lampiran 1. Ciri makroskopis dan mikroskopis fungi yang ditemukan pada serasah A. marina yang mengalami proses dekomposisi pada berbagai tingkat salinitas 1. Aspergillus sp.1 Ciri makroskopis
TINJAUAN PUSTAKA Botani dan Morfologi Cabai
 3 TINJAUAN PUSTAKA Botani dan Morfologi Cabai Cabai (Capsicum annuum L.) termasuk dalam genus Capsicum yang spesiesnya telah dibudidayakan, keempat spesies lainnya yaitu Capsicum baccatum, Capsicum pubescens,
3 TINJAUAN PUSTAKA Botani dan Morfologi Cabai Cabai (Capsicum annuum L.) termasuk dalam genus Capsicum yang spesiesnya telah dibudidayakan, keempat spesies lainnya yaitu Capsicum baccatum, Capsicum pubescens,
HASIL DAN PEMBAHASAN
 18 HASIL DAN PEMBAHASAN Hasil Pengujian Inokulasi Virus Tungro pada Varietas Hibrida dan Beberapa Galur Padi di Rumah Kaca Pengaruh Infeksi Virus Tungro terhadap Tipe Gejala Gambar 2 menunjukkan variasi
18 HASIL DAN PEMBAHASAN Hasil Pengujian Inokulasi Virus Tungro pada Varietas Hibrida dan Beberapa Galur Padi di Rumah Kaca Pengaruh Infeksi Virus Tungro terhadap Tipe Gejala Gambar 2 menunjukkan variasi
HASIL DAN PEMBAHASAN
 HSIL DN PEMBHSN R. pickettii sebagai gen Hayati R. solani Isolat yang digunakan adalah R. pickettii yang memiliki ciri-ciri koloni berwarna kuning dengan bentuk bundar dengan tepian licin dan elevasi seperti
HSIL DN PEMBHSN R. pickettii sebagai gen Hayati R. solani Isolat yang digunakan adalah R. pickettii yang memiliki ciri-ciri koloni berwarna kuning dengan bentuk bundar dengan tepian licin dan elevasi seperti
4. HASIL DAN PEMBAHASAN
 29 4. HASIL DAN PEMBAHASAN 4.1 Karakteristik isolat bakteri dari ikan tuna dan cakalang 4.1.1 Morfologi isolat bakteri Secara alamiah, mikroba terdapat dalam bentuk campuran dari berbagai jenis. Untuk
29 4. HASIL DAN PEMBAHASAN 4.1 Karakteristik isolat bakteri dari ikan tuna dan cakalang 4.1.1 Morfologi isolat bakteri Secara alamiah, mikroba terdapat dalam bentuk campuran dari berbagai jenis. Untuk
BAB 2 TINJAUAN PUSTAKA
 BAB 2 TINJAUAN PUSTAKA 2.1 Kitin dan Bakteri Kitinolitik Kitin adalah polimer kedua terbanyak di alam setelah selulosa. Kitin merupakan komponen penyusun tubuh serangga, udang, kepiting, cumi-cumi, dan
BAB 2 TINJAUAN PUSTAKA 2.1 Kitin dan Bakteri Kitinolitik Kitin adalah polimer kedua terbanyak di alam setelah selulosa. Kitin merupakan komponen penyusun tubuh serangga, udang, kepiting, cumi-cumi, dan
HASIL. Pengaruh Seduhan Kompos terhadap Pertumbuhan Koloni S. rolfsii secara In Vitro A B C
 HASIL Pengaruh Seduhan Kompos terhadap Pertumbuhan Koloni S. rolfsii secara In Vitro Pertumbuhan Koloni S. rolfsii dengan Inokulum Sklerotia Pada 5 HSI diameter koloni cendawan pada semua perlakuan seduhan
HASIL Pengaruh Seduhan Kompos terhadap Pertumbuhan Koloni S. rolfsii secara In Vitro Pertumbuhan Koloni S. rolfsii dengan Inokulum Sklerotia Pada 5 HSI diameter koloni cendawan pada semua perlakuan seduhan
I. PENDAHULUAN. tanaman jagung di Indonesia mencapai lebih dari 3,8 juta hektar, sementara produksi
 I. PENDAHULUAN 1.1 Latar Belakang Jagung merupakan salah satu komoditas pertanian yang sangat penting. Lahan tanaman jagung di Indonesia mencapai lebih dari 3,8 juta hektar, sementara produksi jagung tahun
I. PENDAHULUAN 1.1 Latar Belakang Jagung merupakan salah satu komoditas pertanian yang sangat penting. Lahan tanaman jagung di Indonesia mencapai lebih dari 3,8 juta hektar, sementara produksi jagung tahun
BAHAN DAN METODE Tempat dan Waktu Bahan Peremajaan Aktinomiset dari Kultur Penyimpanan Perbanyakan Sclerotium rolfsii dari Kultur Penyimpanan
 BAHAN DAN METODE Tempat dan Waktu Penelitian dilaksanakan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor (IPB) mulai Maret 2011 sampai
BAHAN DAN METODE Tempat dan Waktu Penelitian dilaksanakan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor (IPB) mulai Maret 2011 sampai
III. BAHAN DAN METODE. Penelitian dilakukan di Laboratorium Penyakit Tanaman, Fakultas Pertanian,
 16 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian dilakukan di Laboratorium Penyakit Tanaman, Fakultas Pertanian, Universitas Lampung dan penelitian ini dilaksanakan pada bulan Juni 2014
16 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian dilakukan di Laboratorium Penyakit Tanaman, Fakultas Pertanian, Universitas Lampung dan penelitian ini dilaksanakan pada bulan Juni 2014
II. TINJAUAN PUSTAKA. Benih adalah ovule atau bakal biji yang masak yang mengandung suatu
 II. TINJAUAN PUSTAKA 2.1. Kuaiitas dan Kesehatan Benih Cabai Benih adalah ovule atau bakal biji yang masak yang mengandung suatu tanaman mini atau embrio yang biasanya terbentuk dari bersatunya sel-sel
II. TINJAUAN PUSTAKA 2.1. Kuaiitas dan Kesehatan Benih Cabai Benih adalah ovule atau bakal biji yang masak yang mengandung suatu tanaman mini atau embrio yang biasanya terbentuk dari bersatunya sel-sel
PEMERINTAH KABUPATEN PROBOLINGGO
 PEMERINTAH KABUPATEN PROBOLINGGO Jalan Raya Dringu Nomor 81 Telp. (0335) 420517 Fax. (4238210) PROBOLINGGO 67271 POTENSI JAMUR ANTAGONIS Trichoderma spp PENGENDALI HAYATI PENYAKIT LANAS DI PEMBIBITAN TEMBAKAU
PEMERINTAH KABUPATEN PROBOLINGGO Jalan Raya Dringu Nomor 81 Telp. (0335) 420517 Fax. (4238210) PROBOLINGGO 67271 POTENSI JAMUR ANTAGONIS Trichoderma spp PENGENDALI HAYATI PENYAKIT LANAS DI PEMBIBITAN TEMBAKAU
TINJAUAN PUSTAKA. Klasifikasi jamur Corynespora cassiicola menurut Alexopolus dan Mims. : Corynespora cassiicola (Berk. & Curt.
 TINJAUAN PUSTAKA Biologi Penyakit Klasifikasi jamur Corynespora cassiicola menurut Alexopolus dan Mims (1979) adalah sebagai berikut : Divisi Sub Divisi Kelas Ordo Famili Genus Spesies : Eumycophyta :
TINJAUAN PUSTAKA Biologi Penyakit Klasifikasi jamur Corynespora cassiicola menurut Alexopolus dan Mims (1979) adalah sebagai berikut : Divisi Sub Divisi Kelas Ordo Famili Genus Spesies : Eumycophyta :
BAB I PENDAHULUAN. A. Latar Belakang
 A. Latar Belakang BAB I PENDAHULUAN Biakan murni merupakan tahapan awal di dalam pembuatan bibit jamur. Pembuatan biakan murni diperlukan ketelitian, kebersihan, dan keterampilan. Pertumbuhan miselium
A. Latar Belakang BAB I PENDAHULUAN Biakan murni merupakan tahapan awal di dalam pembuatan bibit jamur. Pembuatan biakan murni diperlukan ketelitian, kebersihan, dan keterampilan. Pertumbuhan miselium
TINJAUAN PUSTAKA. Menurut Agrios (1996), penyakit bercak coklat sempit diklasifikasikan
 TINJAUAN PUSTAKA Patogen C. oryzae Miyake Biologi Menurut Agrios (1996), penyakit bercak coklat sempit diklasifikasikan sebagai berikut: Kingdom Divisio Sub divisi Kelas Ordo Famili Genus Spesies : Myceteae
TINJAUAN PUSTAKA Patogen C. oryzae Miyake Biologi Menurut Agrios (1996), penyakit bercak coklat sempit diklasifikasikan sebagai berikut: Kingdom Divisio Sub divisi Kelas Ordo Famili Genus Spesies : Myceteae
HASIL DAN PEMBAHASAN A B C
 18 HASIL DAN PEMBAHASAN Tahap I: Seleksi Limbah Organik sebagai Media Tumbuh A. niger mampu tumbuh pada semua media. Pertumbuhan spora dan propagul ditandai dengan terbentunya koloni setelah ditumbuhkan
18 HASIL DAN PEMBAHASAN Tahap I: Seleksi Limbah Organik sebagai Media Tumbuh A. niger mampu tumbuh pada semua media. Pertumbuhan spora dan propagul ditandai dengan terbentunya koloni setelah ditumbuhkan
HASIL DAN PEMBAHASAN
 HASIL DAN PEMBAHASAN Pengaruh L. lecanii Terhadap Telur Inang yang Terparasit Cendawan L. lecanii dengan kerapatan konidia 9 /ml mampu menginfeksi telur inang C. cephalonica yang telah terparasit T. bactrae
HASIL DAN PEMBAHASAN Pengaruh L. lecanii Terhadap Telur Inang yang Terparasit Cendawan L. lecanii dengan kerapatan konidia 9 /ml mampu menginfeksi telur inang C. cephalonica yang telah terparasit T. bactrae
BAHAN DAN METODE. Pertanian Universitas Sumatera Utara, Medan dengan ketinggian tempat + 25
 BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Penyakit Tumbuhan Fakultas Pertanian, Medan dengan ketinggian tempat + 25 meter di atas permukaan laut pada bulan
BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Penyakit Tumbuhan Fakultas Pertanian, Medan dengan ketinggian tempat + 25 meter di atas permukaan laut pada bulan
BAB 2 TINJAUAN PUSTAKA. 2.1 Taksonomi Tanaman Karet Sistem klasifikasi, kedudukan tanaman karet sebagai berikut :
 BAB 2 TINJAUAN PUSTAKA 2.1 Taksonomi Tanaman Karet Sistem klasifikasi, kedudukan tanaman karet sebagai berikut : Kingdom Divisi Sub divisi Kelas Ordo Family Genus Spesies : Plantae (tumbuh-tumbuhan) :
BAB 2 TINJAUAN PUSTAKA 2.1 Taksonomi Tanaman Karet Sistem klasifikasi, kedudukan tanaman karet sebagai berikut : Kingdom Divisi Sub divisi Kelas Ordo Family Genus Spesies : Plantae (tumbuh-tumbuhan) :
METODE PENELITIAN. Kehutanan dan di Laboratorium Hama dan Penyakit Tanaman Program Studi
 23 METODE PENELITIAN Tempat dan Waktu Penelitian Penelitian dilakukan di Laboratorium Bioteknologi Program Studi Kehutanan dan di Laboratorium Hama dan Penyakit Tanaman Program Studi Agroekoteknologi,
23 METODE PENELITIAN Tempat dan Waktu Penelitian Penelitian dilakukan di Laboratorium Bioteknologi Program Studi Kehutanan dan di Laboratorium Hama dan Penyakit Tanaman Program Studi Agroekoteknologi,
HASIL DAN PEMBAHASAN. Pola Pita DNA Monomorfis Beberapa Tanaman dari Klon yang Sama
 121 HASIL DAN PEMBAHASAN Pola Pita DNA Monomorfis Beberapa Tanaman dari Klon yang Sama Tiga tanaman yang digunakan dari klon MK 152 menunjukkan morfologi organ bunga abnormal dengan adanya struktur seperti
121 HASIL DAN PEMBAHASAN Pola Pita DNA Monomorfis Beberapa Tanaman dari Klon yang Sama Tiga tanaman yang digunakan dari klon MK 152 menunjukkan morfologi organ bunga abnormal dengan adanya struktur seperti
II. TINJAUAN PUSTAKA A.
 6 4 II. TINJAUAN PUSTAKA A. Antraknosa Cabai Antraknosa pada cabai disebabkan oleh tiga spesies cendawan Colletotrichum yaitu C. acutatum, C. gloeosporioides, dan C. capsici. Siklus penyakit antraknosa
6 4 II. TINJAUAN PUSTAKA A. Antraknosa Cabai Antraknosa pada cabai disebabkan oleh tiga spesies cendawan Colletotrichum yaitu C. acutatum, C. gloeosporioides, dan C. capsici. Siklus penyakit antraknosa
HASIL DAN PEMBAHASAN
 HASIL DAN PEMBAHASAN 1. Kondisi Umum Tanaman Phalaenopsis pada setiap botol tidak digunakan seluruhnya, hanya 3-7 tanaman (disesuaikan dengan keadaan tanaman). Hal ini disebabkan oleh pertumbuhan tanaman
HASIL DAN PEMBAHASAN 1. Kondisi Umum Tanaman Phalaenopsis pada setiap botol tidak digunakan seluruhnya, hanya 3-7 tanaman (disesuaikan dengan keadaan tanaman). Hal ini disebabkan oleh pertumbuhan tanaman
BAHAN DAN METODE Waktu dan Tempat Penelitian Bahan Penelitian Metode Penelitian Isolasi dan Identifikasi Cendawan Patogen
 14 BAHAN DAN METODE Waktu dan Tempat Penelitian Percobaan dilaksanakan dari bulan Maret sampai bulan Juli 2012 di Laboratorium Mikologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut
14 BAHAN DAN METODE Waktu dan Tempat Penelitian Percobaan dilaksanakan dari bulan Maret sampai bulan Juli 2012 di Laboratorium Mikologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut
HASIL DAN PEMBAHASAN
 HASIL DAN PEMBAHASAN Identitas Kutukebul Pengkoloni Pertanaman Tomat Kutukebul yang dikumpulkan dari pertanaman tomat di daerah Cisarua, Bogor diperbanyak di tanaman tomat dalam kurungan kedap serangga
HASIL DAN PEMBAHASAN Identitas Kutukebul Pengkoloni Pertanaman Tomat Kutukebul yang dikumpulkan dari pertanaman tomat di daerah Cisarua, Bogor diperbanyak di tanaman tomat dalam kurungan kedap serangga
UJI PERTUMBUHAN IN VITRO
 UJI PERTUMBUHAN IN VITRO PATOGEN LODOH Rhizoctonia solani PADA BERBAGAI TINGKATAN ph DAN JENIS MEDIA TUMBUH 1) Oleh : Nanang Herdiana 2) ABSTRAK Lodoh (damping-off) merupakan kendala yang dapat menurunkan
UJI PERTUMBUHAN IN VITRO PATOGEN LODOH Rhizoctonia solani PADA BERBAGAI TINGKATAN ph DAN JENIS MEDIA TUMBUH 1) Oleh : Nanang Herdiana 2) ABSTRAK Lodoh (damping-off) merupakan kendala yang dapat menurunkan
IV. HASIL DAN PEMBAHASAN
 IV. HASIL DAN PEMBAHASAN 4.1 Hasil Penelitian 4.1.1 Jumlah Spora Sebelum Trapping Hasil pengamatan jumlah spora pada kedua jenis lahan sayur dan semak sebelum trapping disajikan pada Tabel 3. Lahan sayuran
IV. HASIL DAN PEMBAHASAN 4.1 Hasil Penelitian 4.1.1 Jumlah Spora Sebelum Trapping Hasil pengamatan jumlah spora pada kedua jenis lahan sayur dan semak sebelum trapping disajikan pada Tabel 3. Lahan sayuran
Pengendalian Penyakit pada Tanaman Jagung Oleh : Ratnawati
 Pengendalian Penyakit pada Tanaman Jagung Oleh : Ratnawati Tanaman jagung disamping sebagai bahan baku industri pakan dan pangan pada daerah tertentu di Indonesia dapat juga sebagai makanan pokok. Karena
Pengendalian Penyakit pada Tanaman Jagung Oleh : Ratnawati Tanaman jagung disamping sebagai bahan baku industri pakan dan pangan pada daerah tertentu di Indonesia dapat juga sebagai makanan pokok. Karena
HASIL DAN PEMBAHASAN
 17 HASIL DAN PEMBAHASAN Kondisi Umum Penelitian ini berlangsung di kebun manggis daerah Cicantayan Kabupaten Sukabumi dengan ketinggian 500 700 meter di atas permukaan laut (m dpl). Area penanaman manggis
17 HASIL DAN PEMBAHASAN Kondisi Umum Penelitian ini berlangsung di kebun manggis daerah Cicantayan Kabupaten Sukabumi dengan ketinggian 500 700 meter di atas permukaan laut (m dpl). Area penanaman manggis
HASIL DAN PEMBAHASAN
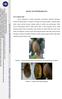 10 HASIL DAN PEMBAHASAN Survei Buah Sakit Survei dilakukan di kebun percobaan Leuwikopo, Fakultas Pertanian, Institut Pertanian Bogor, di lahan ini terdapat 69 tanaman pepaya. Kondisi lahan tidak terawat
10 HASIL DAN PEMBAHASAN Survei Buah Sakit Survei dilakukan di kebun percobaan Leuwikopo, Fakultas Pertanian, Institut Pertanian Bogor, di lahan ini terdapat 69 tanaman pepaya. Kondisi lahan tidak terawat
Pengenalan Penyakit yang Menyerang Pada Tanaman Kentang
 1 Pengenalan Penyakit yang Menyerang Pada Tanaman Kentang Kelompok penyakit tanaman adalah organisme pengganggu tumbuhan yang penyebabnya tidak dapat dilihat dengan mata telanjang seperti : cendawan, bakteri,
1 Pengenalan Penyakit yang Menyerang Pada Tanaman Kentang Kelompok penyakit tanaman adalah organisme pengganggu tumbuhan yang penyebabnya tidak dapat dilihat dengan mata telanjang seperti : cendawan, bakteri,
Fusarium sp. ENDOFIT NON PATOGENIK
 INDUKSI KETAHANAN KULTUR JARINGAN PISANG TERHADAP LAYU FUSARIUM MENGGUNAKAN Fusarium sp. ENDOFIT NON PATOGENIK Arif Wibowo, Aisyah Irmiyatiningsih, Suryanti, dan J. Widada Fakultas Pertanian, Universitas
INDUKSI KETAHANAN KULTUR JARINGAN PISANG TERHADAP LAYU FUSARIUM MENGGUNAKAN Fusarium sp. ENDOFIT NON PATOGENIK Arif Wibowo, Aisyah Irmiyatiningsih, Suryanti, dan J. Widada Fakultas Pertanian, Universitas
BAHAN DAN METODE Waktu dan Tempat Bahan dan Alat Metode Penelitian Penyediaan Isolat Fusarium sp. dan Bakteri Aktivator
 BAHAN DAN METODE Waktu dan Tempat Penelitian ini dilakukan di Laboratorium Mikologi, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor, dan Laboratorium Mikrobiologi dan Kesehatan
BAHAN DAN METODE Waktu dan Tempat Penelitian ini dilakukan di Laboratorium Mikologi, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor, dan Laboratorium Mikrobiologi dan Kesehatan
TINJAUAN PUSTAKA. Penyakit Eucalyptus spp. Ada beberapa penyakit penting yang sering menyerang tanaman. Eucalyptus spp.
 TINJAUAN PUSTAKA Penyakit Eucalyptus spp Ada beberapa penyakit penting yang sering menyerang tanaman Eucalyptus spp. antara lain: 1. Penyakit pada akar a. Busuk akar Phytophthora Penyakit ini disebabkan
TINJAUAN PUSTAKA Penyakit Eucalyptus spp Ada beberapa penyakit penting yang sering menyerang tanaman Eucalyptus spp. antara lain: 1. Penyakit pada akar a. Busuk akar Phytophthora Penyakit ini disebabkan
III. METODE PENELITIAN. dan Ilmu Pengetahuan Alam, Universitas Lampung dari bulan Januari sampai
 23 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Mikrobiologi Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Lampung dari bulan Januari sampai
23 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Mikrobiologi Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Lampung dari bulan Januari sampai
HASIL DAN PEMBAHASAN Kondisi Umum
 16 HASIL DAN PEMBAHASAN Kondisi Umum Keadaan tanaman cabai selama di persemaian secara umum tergolong cukup baik. Serangan hama dan penyakit pada tanaman di semaian tidak terlalu banyak. Hanya ada beberapa
16 HASIL DAN PEMBAHASAN Kondisi Umum Keadaan tanaman cabai selama di persemaian secara umum tergolong cukup baik. Serangan hama dan penyakit pada tanaman di semaian tidak terlalu banyak. Hanya ada beberapa
III. BAHAN DAN METODE. Penelitian dilaksanakan di Laboratorium Ilmu Penyakit Tumbuhan, Bidang
 8 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian dilaksanakan di Laboratorium Ilmu Penyakit Tumbuhan, Bidang Proteksi Tanaman, Jurusan Agroteknologi, Fakultas Pertanian Universitas Lampung
8 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian dilaksanakan di Laboratorium Ilmu Penyakit Tumbuhan, Bidang Proteksi Tanaman, Jurusan Agroteknologi, Fakultas Pertanian Universitas Lampung
HASIL DAN PEMBAHASAN Uji Penapisan
 11 HASIL DAN PEMBAHASAN Uji Penapisan Pada pengujian ini diperolah 3 isolat yang menyebabkan munculnya gejala busuk pangkal batang dan mengakibatkan pertumbuhan tanaman lebih rendah daripada tanpa perlakuan
11 HASIL DAN PEMBAHASAN Uji Penapisan Pada pengujian ini diperolah 3 isolat yang menyebabkan munculnya gejala busuk pangkal batang dan mengakibatkan pertumbuhan tanaman lebih rendah daripada tanpa perlakuan
HASIL ANALISIS DAN PEMBAHASAN. cendawan MVA, sterilisasi tanah, penanaman tanaman kedelai varietas Detam-1.
 IV. HASIL ANALISIS DAN PEMBAHASAN Penelitian ini dilakukan melalui tiga tahapan, yakni perbanyakan inokulum cendawan MVA, sterilisasi tanah, penanaman tanaman kedelai varietas Detam-1. Perbanyakan inokulum
IV. HASIL ANALISIS DAN PEMBAHASAN Penelitian ini dilakukan melalui tiga tahapan, yakni perbanyakan inokulum cendawan MVA, sterilisasi tanah, penanaman tanaman kedelai varietas Detam-1. Perbanyakan inokulum
`BAB IV HASIL DAN PEMBAHASAN. isolatnya ditunjukkan dalam table 4.1 di bawah ini;
 4.1 Hasil Isolasi Bakteri Endofit `BAB IV HASIL DAN PEMBAHASAN Berdasarkan penelitian yang telah dilakukan terhadap 6 isolat dari tanaman umbi kentang, hasil isolasi serta bentuk morfologi koloni bakteri
4.1 Hasil Isolasi Bakteri Endofit `BAB IV HASIL DAN PEMBAHASAN Berdasarkan penelitian yang telah dilakukan terhadap 6 isolat dari tanaman umbi kentang, hasil isolasi serta bentuk morfologi koloni bakteri
IV. HASIL DAN PEMBAHASAN
 IV. HASIL DAN PEMBAHASAN 4.1. Uk'ntiflkasi.lamur Ri/o.sfir Tanaman Ncna» Bcrdasarkan hasil identifikasi di laboratorium, ditemukan beberapa mikroorganisme rizosfir dari tanaman nenas di lahan petani nenas
IV. HASIL DAN PEMBAHASAN 4.1. Uk'ntiflkasi.lamur Ri/o.sfir Tanaman Ncna» Bcrdasarkan hasil identifikasi di laboratorium, ditemukan beberapa mikroorganisme rizosfir dari tanaman nenas di lahan petani nenas
6. Panjang helaian daun. Daun diukur mulai dari pangkal hingga ujung daun. Notasi : 3. Pendek 5.Sedang 7. Panjang 7. Bentuk daun
 LAMPIRAN Lampiran 1. Skoring sifat dan karakter tanaman cabai 1. Tinggi tanaman : Tinggi tanaman diukur mulai dari atas permukaan tanah hingga ujung tanaman yang paling tinggi dan dinyatakan dengan cm.
LAMPIRAN Lampiran 1. Skoring sifat dan karakter tanaman cabai 1. Tinggi tanaman : Tinggi tanaman diukur mulai dari atas permukaan tanah hingga ujung tanaman yang paling tinggi dan dinyatakan dengan cm.
III. BAHAN DAN METODE. Penelitian ini dilaksanakan pada bulan Juli sampai dengan Desember 2014.
 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan pada bulan Juli sampai dengan Desember 2014. Isolasi dan karakterisasi penyebab penyakit dilakukan di Laboratorium Penyakit
III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan pada bulan Juli sampai dengan Desember 2014. Isolasi dan karakterisasi penyebab penyakit dilakukan di Laboratorium Penyakit
PELAKSANAAN PENELITIAN
 PELAKSANAAN PENELITIAN Persiapan Lahan Disiapkan lahan dengan panjang 21 m dan lebar 12 m yang kemudian dibersihkan dari gulma. Dalam persiapan lahan dilakukan pembuatan plot dengan 4 baris petakan dan
PELAKSANAAN PENELITIAN Persiapan Lahan Disiapkan lahan dengan panjang 21 m dan lebar 12 m yang kemudian dibersihkan dari gulma. Dalam persiapan lahan dilakukan pembuatan plot dengan 4 baris petakan dan
BAHAN DAN METODE. Bahan
 9 BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilaksanakan di Laboratorium Patologi Serangga, dan Laboratorium Fisiologi dan Toksikologi Serangga, Departemen Proteksi Tanaman, Fakultas Pertanian,
9 BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilaksanakan di Laboratorium Patologi Serangga, dan Laboratorium Fisiologi dan Toksikologi Serangga, Departemen Proteksi Tanaman, Fakultas Pertanian,
HASIL DAN PEMBAHASAN
 HASIL DAN PEMBAHASAN Hasil Pengamatan Pengaruh Aplikasi Getah Pepaya Betina Secara in-vitro Aplikasi getah pepaya betina pada media tumbuh PDA dengan berbagai konsentrasi mempengaruhi secara signifikan
HASIL DAN PEMBAHASAN Hasil Pengamatan Pengaruh Aplikasi Getah Pepaya Betina Secara in-vitro Aplikasi getah pepaya betina pada media tumbuh PDA dengan berbagai konsentrasi mempengaruhi secara signifikan
III. METODE PENELITIAN. Penelitian ini dilaksanakan di Laboratorium Botani, Jurusan Biologi, Fakultas
 17 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Botani, Jurusan Biologi, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Lampung, pada bulan
17 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Botani, Jurusan Biologi, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Lampung, pada bulan
WASPADA PENYAKIT Rhizoctonia!!
 WASPADA PENYAKIT Rhizoctonia!! I. Latar Belakang Luas areal kebun kopi di Indonesia sekarang, lebih kurang 1,3 juta ha, sedangkan produksi kopi Indonesia sekarang, lebih kurang 740.000 ton dengan produksi
WASPADA PENYAKIT Rhizoctonia!! I. Latar Belakang Luas areal kebun kopi di Indonesia sekarang, lebih kurang 1,3 juta ha, sedangkan produksi kopi Indonesia sekarang, lebih kurang 740.000 ton dengan produksi
III. METODE PENELITIAN. Penelitian dilaksanakan di Laboratorium Biocontrol, Divisi Research and
 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian dilaksanakan di Laboratorium Biocontrol, Divisi Research and Development, PT Gunung Madu Plantations (PT GMP), Kabupaten Lampung Tengah.
III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian dilaksanakan di Laboratorium Biocontrol, Divisi Research and Development, PT Gunung Madu Plantations (PT GMP), Kabupaten Lampung Tengah.
HASIL DAN PEMBAHASAN
 HASIL DAN PEMBAHASAN Kondisi Umum Benih Indigofera yang digunakan dalam penelitian ini cenderung berjamur ketika dikecambahkan. Hal ini disebabkan karena tanaman indukan sudah diserang cendawan sehingga
HASIL DAN PEMBAHASAN Kondisi Umum Benih Indigofera yang digunakan dalam penelitian ini cenderung berjamur ketika dikecambahkan. Hal ini disebabkan karena tanaman indukan sudah diserang cendawan sehingga
melakukan inokulasi langsung pada buah pepaya selanjutnya mengamati karakter yang berhubungan dengan ketahanan, diantaranya masa inkubasi, diameter
 PEMBAHASAN UMUM Pengembangan konsep pemuliaan pepaya tahan antraknosa adalah suatu kegiatam dalam upaya mendapatkan genotipe tahan. Salah satu metode pengendalian yang aman, murah dan ramah lingkungan
PEMBAHASAN UMUM Pengembangan konsep pemuliaan pepaya tahan antraknosa adalah suatu kegiatam dalam upaya mendapatkan genotipe tahan. Salah satu metode pengendalian yang aman, murah dan ramah lingkungan
V. PEMBAHASAN Penyakit gugur buah kelapa dan busuk buah kakao merupakan penyakit penting secara ekonomi dan dipandang sebagai ancaman utama pada
 V. PEMBAHASAN Penyakit gugur buah kelapa dan busuk buah kakao merupakan penyakit penting secara ekonomi dan dipandang sebagai ancaman utama pada perusahaan perkebunan dan petani kelapa dan kakao di Indonesia.
V. PEMBAHASAN Penyakit gugur buah kelapa dan busuk buah kakao merupakan penyakit penting secara ekonomi dan dipandang sebagai ancaman utama pada perusahaan perkebunan dan petani kelapa dan kakao di Indonesia.
Diagnosa Penyakit Akibat Jamur pada Tanaman Padi (Oryza sativa) di Sawah Penduduk Kecamatan Sungai Kakap, Kabupaten Kubu Raya, Kalimantan Barat
 Diagnosa Penyakit Akibat Jamur pada Tanaman Padi (Oryza sativa) di Sawah Penduduk Kecamatan Sungai Kakap, Kabupaten Kubu Raya, Kalimantan Barat Rahmawati 1)*, Achmad Jailanis 2), Nurul Huda 1) 1) Program
Diagnosa Penyakit Akibat Jamur pada Tanaman Padi (Oryza sativa) di Sawah Penduduk Kecamatan Sungai Kakap, Kabupaten Kubu Raya, Kalimantan Barat Rahmawati 1)*, Achmad Jailanis 2), Nurul Huda 1) 1) Program
II. TINJAUAN PUSTAKA. Penyakit antraknosa pada tanaman cabai disebabkan oleh tiga spesies cendawan
 5 II. TINJAUAN PUSTAKA 2.1 Penyakit Antraknosa Cabai Penyakit antraknosa pada tanaman cabai disebabkan oleh tiga spesies cendawan Colletotrichum yaitu C. acutatum, C. gloeosporioides, dan C. capsici (Direktorat
5 II. TINJAUAN PUSTAKA 2.1 Penyakit Antraknosa Cabai Penyakit antraknosa pada tanaman cabai disebabkan oleh tiga spesies cendawan Colletotrichum yaitu C. acutatum, C. gloeosporioides, dan C. capsici (Direktorat
BAB V HASIL DAN PEMBAHASAN
 11 BAB V HASIL DAN PEMBAHASAN 5.1 Hasil Hasil penelitian menunjukkan bahwa dari 2 lokasi penelitian yang digunakan yaitu Harapan dan Inalahi yang terbagi menjadi 4 plot pengamatan terdapat 4 jenis tanaman
11 BAB V HASIL DAN PEMBAHASAN 5.1 Hasil Hasil penelitian menunjukkan bahwa dari 2 lokasi penelitian yang digunakan yaitu Harapan dan Inalahi yang terbagi menjadi 4 plot pengamatan terdapat 4 jenis tanaman
III. BAHAN DAN METODE. Penelitian ini dilaksanakan di kebun PT NTF (Nusantara Tropical Farm) Way
 31 III. BAHAN DAN METODE A. Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di kebun PT NTF (Nusantara Tropical Farm) Way Jepara, Lampung Timur dan Laboratorium Penyakit Tumbuhan, Bidang Proteksi
31 III. BAHAN DAN METODE A. Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di kebun PT NTF (Nusantara Tropical Farm) Way Jepara, Lampung Timur dan Laboratorium Penyakit Tumbuhan, Bidang Proteksi
TINJAUAN PUSTAKA Botani Kentang
 4 TINJAUAN PUSTAKA Botani Kentang Tanaman kentang (Solanum tuberosum L.) dikenal sebagai The King of Vegetable dan produksinya menempati urutan keempat dunia setelah beras, gandum dan jagung (The International
4 TINJAUAN PUSTAKA Botani Kentang Tanaman kentang (Solanum tuberosum L.) dikenal sebagai The King of Vegetable dan produksinya menempati urutan keempat dunia setelah beras, gandum dan jagung (The International
HASIL DAN PEMBAHASAN
 HASIL DAN PEMBAHASAN Isolasi Bakteri Endofit Asal Bogor, Cipanas, dan Lembang Bakteri endofit yang digunakan dalam penelitian ini berasal dari tiga tempat yang berbeda dalam satu propinsi Jawa Barat. Bogor,
HASIL DAN PEMBAHASAN Isolasi Bakteri Endofit Asal Bogor, Cipanas, dan Lembang Bakteri endofit yang digunakan dalam penelitian ini berasal dari tiga tempat yang berbeda dalam satu propinsi Jawa Barat. Bogor,
TINJAUAN PUSTAKA. menjadi tegas, kering, berwarna terang segar bertepung. Lembab-berdaging jenis
 16 TINJAUAN PUSTAKA Botani Tanaman Ada 2 tipe akar ubi jalar yaitu akar penyerap hara di dalam tanah dan akar lumbung atau umbi. Menurut Sonhaji (2007) akar penyerap hara berfungsi untuk menyerap unsur-unsur
16 TINJAUAN PUSTAKA Botani Tanaman Ada 2 tipe akar ubi jalar yaitu akar penyerap hara di dalam tanah dan akar lumbung atau umbi. Menurut Sonhaji (2007) akar penyerap hara berfungsi untuk menyerap unsur-unsur
III. BAHAN DAN METODE. Tanaman, serta Laboratorium Lapang Terpadu, Fakultas Pertanian, Universitas
 13 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Hama dan Penyakit Bidang Proteksi Tanaman, serta Laboratorium Lapang Terpadu, Fakultas Pertanian, Universitas
13 III. BAHAN DAN METODE 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Hama dan Penyakit Bidang Proteksi Tanaman, serta Laboratorium Lapang Terpadu, Fakultas Pertanian, Universitas
BAB 4 HASIL PERCOBAAN DAN PEMBAHASAN
 BAB 4 HASIL PERCOBAAN DAN PEMBAHASAN Sebelum melakukan PCR, terlebih dahulu dilakukan perancangan primer menggunakan program DNA Star. Pemilihan primer dilakukan dengan mempertimbangkan parameter spesifisitas,
BAB 4 HASIL PERCOBAAN DAN PEMBAHASAN Sebelum melakukan PCR, terlebih dahulu dilakukan perancangan primer menggunakan program DNA Star. Pemilihan primer dilakukan dengan mempertimbangkan parameter spesifisitas,
BAHAN. bulan Juli diremajakan. pertumbuhan. Gambar 4
 14 BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilakukan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian serta di Rumah Kaca University Farm, Institut
14 BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian dilakukan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian serta di Rumah Kaca University Farm, Institut
a. Karakteristik makroskopis dan mikroskopis Rsalani. penyebab penyakit busuk pelepah
 4T Lampiran 1. Karakteristik makroskopis dan mikroskopis R solani penyeba penyakit busuk pelepah dan P. oryzae penyebab penyakit blas a. Karakteristik makroskopis dan mikroskopis Rsalani. penyebab penyakit
4T Lampiran 1. Karakteristik makroskopis dan mikroskopis R solani penyeba penyakit busuk pelepah dan P. oryzae penyebab penyakit blas a. Karakteristik makroskopis dan mikroskopis Rsalani. penyebab penyakit
III. BAHAN DAN METODE. Jurusan Agroteknologi, Universitas Lampung. Penelitian ini dilaksanakan mulai
 14 III. BAHAN DAN METODE 3.1 Tempat dan waktu penelitian Penelitian ini dilakukan di Laboratorium Penyakit Tumbuhan, Fakultas Pertanian, Jurusan Agroteknologi, Universitas Lampung. Penelitian ini dilaksanakan
14 III. BAHAN DAN METODE 3.1 Tempat dan waktu penelitian Penelitian ini dilakukan di Laboratorium Penyakit Tumbuhan, Fakultas Pertanian, Jurusan Agroteknologi, Universitas Lampung. Penelitian ini dilaksanakan
Pembinaan Terhadap Terpidana Lanjut Usia di Lembaga Pemasyarakatan Klas II A Jambi
 IDENTIFIKASI JAMUR PATOGEN PENYEBAB PENYAKIT PADA TANAMAN PADI (Oryza sativa) DI LUBUK RUSO KECAMATAN PEMAYUNG KABUPATENBATANGHARI JAMBI Yuza Defitri 1 Abstract The research about identification of pathogenic
IDENTIFIKASI JAMUR PATOGEN PENYEBAB PENYAKIT PADA TANAMAN PADI (Oryza sativa) DI LUBUK RUSO KECAMATAN PEMAYUNG KABUPATENBATANGHARI JAMBI Yuza Defitri 1 Abstract The research about identification of pathogenic
BAB I PENDAHULUAN. tuberosum dari family Solanaceae. Kentang juga termasuk salah satu pangan. pengembangannya di Indonesia (Suwarno, 2008).
 1 BAB I PENDAHULUAN 1.1 Latar Balakang Kentang merupakan bahan pangan dari umbi tanaman perennial Solanum tuberosum dari family Solanaceae. Kentang juga termasuk salah satu pangan utama dunia setelah padi,
1 BAB I PENDAHULUAN 1.1 Latar Balakang Kentang merupakan bahan pangan dari umbi tanaman perennial Solanum tuberosum dari family Solanaceae. Kentang juga termasuk salah satu pangan utama dunia setelah padi,
HASIL DAN PEMBAHASAN Keadaan Umum Lokasi Isolasi Cendawan Rizosfer
 10 HASIL DAN PEMBAHASAN Keadaan Umum Lokasi Lokasi pengambilan sampel berada di dua tempat yang berbeda : lokasi pertama, Kabupaten Bogor. Kabupaten Bogor memiliki ketinggian + 400 m dpl (diatas permukaan
10 HASIL DAN PEMBAHASAN Keadaan Umum Lokasi Lokasi pengambilan sampel berada di dua tempat yang berbeda : lokasi pertama, Kabupaten Bogor. Kabupaten Bogor memiliki ketinggian + 400 m dpl (diatas permukaan
TINJAUAN PUSTAKA Botani Manggis
 4 TINJAUAN PUSTAKA Botani Manggis Tanaman manggis (Garcinia mangostana L.) termasuk famili Clusiaceae yang diperkirakan berasal dari Asia Tenggara khususnya di semenanjung Malaya, Myanmar, Thailand, Kamboja,
4 TINJAUAN PUSTAKA Botani Manggis Tanaman manggis (Garcinia mangostana L.) termasuk famili Clusiaceae yang diperkirakan berasal dari Asia Tenggara khususnya di semenanjung Malaya, Myanmar, Thailand, Kamboja,
III. METODE PENELITIAN. Penelitian dilaksanakan di Laboratorium Penyakit Tumbuhan Jurusan
 14 III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian dilaksanakan di Laboratorium Penyakit Tumbuhan Jurusan Agroteknologi Fakultas Pertanian Universitas Lampung. Pelaksanaan penelitian
14 III. METODE PENELITIAN 3.1 Waktu dan Tempat Penelitian Penelitian dilaksanakan di Laboratorium Penyakit Tumbuhan Jurusan Agroteknologi Fakultas Pertanian Universitas Lampung. Pelaksanaan penelitian
TINJAUAN PUSTAKA. Botani Tanaman. akar-akar cabang banyak terdapat bintil akar berisi bakteri Rhizobium japonicum
 TINJAUAN PUSTAKA Botani Tanaman Susunan akar kedelai pada umumnya sangat baik, pertumbuhan akar tunggang lurus masuk kedalam tanah dan mempunyai banyak akar cabang. Pada akar-akar cabang banyak terdapat
TINJAUAN PUSTAKA Botani Tanaman Susunan akar kedelai pada umumnya sangat baik, pertumbuhan akar tunggang lurus masuk kedalam tanah dan mempunyai banyak akar cabang. Pada akar-akar cabang banyak terdapat
TINJAUAN LITERATUR. Klasifikasi jamur Corynespora cassiicola menurut Alexopolus dan Mims. : Corynespora cassiicola (Berk. & Curt.
 TINJAUAN LITERATUR Biologi Penyakit Klasifikasi jamur Corynespora cassiicola menurut Alexopolus dan Mims (1979) adalah sebagai berikut : Divisi Sub Divisi Kelas Ordo Famili Genus Spesies : Eumicophyta
TINJAUAN LITERATUR Biologi Penyakit Klasifikasi jamur Corynespora cassiicola menurut Alexopolus dan Mims (1979) adalah sebagai berikut : Divisi Sub Divisi Kelas Ordo Famili Genus Spesies : Eumicophyta
BAB II TINJAUAN PUSTAKA
 BAB II TINJAUAN PUSTAKA 2.1 Jamur Trichoderma sp. Jamur tanah merupakan salah satu golongan yang penting dari golongangolongan populasi tanah yang tersebar secara luas. Bentuk-bentuk tertentu merupakan
BAB II TINJAUAN PUSTAKA 2.1 Jamur Trichoderma sp. Jamur tanah merupakan salah satu golongan yang penting dari golongangolongan populasi tanah yang tersebar secara luas. Bentuk-bentuk tertentu merupakan
TATA CARA PENELITIAN. A. Tempat dan Waktu Penelitian. Yogyakarta, GreenHouse di Fakultas Pertanian Universitas Muhammadiyah
 III. TATA CARA PENELITIAN A. Tempat dan Waktu Penelitian Penelitian dilaksanakan di lahan kering, Desa Gading PlayenGunungkidul Yogyakarta, GreenHouse di Fakultas Pertanian Universitas Muhammadiyah Yogyakarta,
III. TATA CARA PENELITIAN A. Tempat dan Waktu Penelitian Penelitian dilaksanakan di lahan kering, Desa Gading PlayenGunungkidul Yogyakarta, GreenHouse di Fakultas Pertanian Universitas Muhammadiyah Yogyakarta,
