BAB II KAJIAN TEORI 1.1 Kemampuan siswa
|
|
|
- Leony Santoso
- 7 tahun lalu
- Tontonan:
Transkripsi
1 BAB II KAJIAN TEORI 1.1 Kemampuan siswa Kemampuan siswa dalam belajar adalah kecakapan seorang peserta didik, yang dimiliki dari hasil apa yang telah dipelajari yang dapat ditunjukkan atau dilihat melalui hasil belajarnya (Syah, 2004). Ada tiga ranah (aspek) yang terkait dengan kemampuan siswa dalam belajar, yaitu ranah kognitif, ranah afektif, dan ranah psikomotorik. Contoh ranah kognitif adalah kemampuan siswa dalam menganalisis suatu masalah berdasarkan pemahaman yang dimilikinya. Contoh ranah afektif adalah siswa mampu menentukan sikap untuk menerima atau menolak suatu objek. Contoh ranah psikomotorik adalah siswa mampu berekspresi dengan baik. Setiap siswa dikatakan berhasil dalam belajar apabila memiliki kemampuan dalam belajar sebagaimana dikemukakan di atas. Akan tetapi yang menjadi masalah adalah tidak semua siswa memiliki kemampuan yang sama. Banyak faktor yang mempengaruhi kemampuan siswa dalam belajar, antara lain faktor internal, faktor eksternal, dan faktor pendekatan belajar. Contoh faktor internal yang mempengaruhi kemampuan siswa dalam belajar adalah kesehatan siswa dan intelegensinya. Siswa yang sehat dan mempunyai intelegensi yang baik akan mempunyai kesiapan yang lebih baik dalam belajar sehingga kemampuan belajarnya dapat optimal. Sebaliknya siswa yang kurang sehat (sedang sakit) akan sulit menerima pelajaran sehingga kurang optimal kemampuan belajarnya. Contoh faktor eksternal yang mempengaruhi kemampuan siswa dalam belajar adalah lingkungan keluarga. Lingkungan keluarga yang mendukung akan membuat siswa mudah untuk menerima pelajaran, sebaliknya lingkungan keluarga yang tidak mendukung, akan membuat siswa tidak tenang dalam belajar sehingga kemampuan siswamenjadi tidak optimal. Faktor pendekatan belajar yang berbeda juga akan memberikan kemampuan belajar yang berbeda. Siswa yang belajar secara mendalam akan memiliki kemampuan belajar yang lebih baik daripada siswa yang hanya belajar sambil dipelajari begitu saja (tidak mendalam). 1
2 Salah satu faktor yang dapat mempengaruhi kemampuan siswa dalam belajar adalah kemampuan siswa dalam mempersepsi materi pelajaran yang diterimanya disekolah. Persepsi merupakan aktivitas mengindera, mengorganisasi, dan menginterpretasikan serta menilai stimulus yang ada dalam lingkungan. Dalam hal ini stimulus yang sama belum tentu membuat seseorang mempunyai persepsi yang sama terhadap suatu hal. Berdasarkan pengertian persepsi di atas dapat diketahui bahwa persepsi terkait erat dengan panca indera karena persepsi terjadi setelah objek yang bersangkutan melihat, mendengar atau merasakan sesuatu dan kemudian mengorganisasi serta menginterpretasikannya sehingga timbullah persepsi. Proses yang sama juga terjadi pada persepsi siswa terhadap sistem pembelajaran. Siswa akan membuat persepsi mengenai sistem pembelajaran dari apa yang ditangkap oleh inderanya, kemudian dari hasil persepsinya itu siswa akan bereaksi. Reaksi yang muncul dapat berupa tindakan-tindakan yang menunjang ke arah tercapainya kemampuan dalam belajar, seperti menghafal, menghitung, menulis, membaca, dan lain-lain. Oleh karena itulah persepsi siswa dalam belajar mempunyai hubungan dengan kemampuan siswa dalam belajar. Karena persepsi berbeda-beda untuk setiap individu, maka kemampuan siswa dalam belajar sangat tergantung kepada persepsinya, sehingga dapat dikatakan ada hubungan yang sangat kuat antara persepsi siswa terhadap sistem pembelajaran dengan kemampuan siswa dalam belajar. 1.2 Pengertian dan Pentingnya Pemahaman Konsep Kimia Konsep-konsep kimia umumnya merupakan konsep-konsep berjenjang yang berkembang dari yang sederhana ke yang kompleks. Suatu konsep kompleks hanya dapat dikuasai dengan baik dan benar bila konsep-konsep yang mendasari telah dikuasai dengan baik dan benar pula. Itulah sebabnya terjadinya kesalahan konsep harus dicegah. Salah satu caranya adalah melalui penerapan metode pembelajaran yang tepat dan sesuai dengan hakikat ilmu kimia itu sendiri. Ilmu kimia di SMA disajikan sebagai mata pelajaran umum bagi siswa kelas X dan XI, dan merupakan program khusus bagi kelas XII. Pengajaran ilmu 2
3 kimia di SMA menawarkan salah satu dari tantangan besar pengajarannya, karena sejumlah besar materi pelajaran yang luas bersifat abstrak harus diberikan secara benar dan tepat. Mata pelajaran ilmu kimia sebagai salah satu dari ilmu pengetahuan Alam (IPA) yang pengajarannya memerlukan penanganan khusus, karena pelajaran kimia mempunyai karakteristik tersendiri, terutama berkaitan dengan tingkat keabstrakan konsep-konsep dalam kimia. Konsep-konsep dalam ilmu kimia sebagian besar merupakan konsepkonsep abstrak (Wiseman 1981:484). Selain sarat dengan konsep abstrak konsepkonsep kimia umumnya merupakan konsep-konsep berjenjang yang berkembang dari yang sederhana ke yang kompleks. Suatu konsep kompleks hanya dapat dikuasai dengan baik dan benar bila konsep-konsep yang mendasari telah dikuasai dengan baik dan benar pula. Pengetahuan kimia terdiri antara lain dari konsep-konsep. Konsep-konsep dalam ilmu kimia ada yang berupa konsep-konsep konkret yaitu konsep yang dibangun dari objek yang teramati, dan konsep-konsep abstrak yaitu konsepkonsep yang dibangun berdasarkan logika, imaginasi (Scerri. 2003) dan teori-teori berdasarkan hal-hal yang teramati (Eddy. 2000, Nakleh. 1993, Bunce. 2001). Untuk menentukan apakah suatu konsep adalah konsep konkret atau abstrak, konsep terlebih dahulu harus didefinisikan (Carin, 1993). Pernyataan ini memberi makna bahwa suatu konsep kimia dapat berupa konsep konkret dan atau konsep abstrak, tergantung pada definisi dari konsep tersebut. Oleh sebab itu sebelum membelajarkan konsep-konsep kimia, konsep-konsep terlebih dahulu harus didefinisikan. Hal ini akan membantu guru memilih strategi dan perangkat pembelajaran yang akan digunakan dalam proses membelajarkan siswa. Pada dasarnya setiap konsep dalam ilmu kimia tidak berdiri sendiri melainkan suatu konsep saling berkaitan dengan konsep lain. Misalnya konsep tentang hukum-hukum dasar kimia yang melibatkan kansep tentang hukum kekekalan massa, hukum perbandingan tetap, hukum perbandingan berganda, hukum perbandingan volume. Hal ini diperkuat oleh pendapat Sastrawijaya (1988:197) yang mengemukakan bahwa suatu konsep yang kompleks dalam ilmu kimia hanya dapat dikuasai jika konsep-konsep dasarnya yang ikut dalam 3
4 pembentukan konsep baru telah benar-benar dipahami oleh siswa. Mencermati pendapat tersebut dan kaitannya dengan tujuan pembelajaran kimia yang menekankan pada penguasaan konsep-konsep dan keterkaitannya, maka siswa dituntut untuk menguasai sejumlah konsep-konsep dalam ilmu kimia dengan benar diharapkan akan terjadi pemahaman terhadap fakta-fakta, prinsip-prinsip, teori-teori dan hukum-hukum secara benar oleh karena itu penekanan pembelajaran kimia di SMA atau yang sederajat pada pemahaman konsep merupakan salah satu tujuan yang tepat. Suatu proses belajar dapat dikatakan bermakna apabila: (1) siswa telah memiliki dan memahami dengan benar konsep-konsep dasar yang berhubungan dengan materi yang akan disajikan, (2) dapat mengaitkan (menggunakan) konsepkonsep dasar tersebut dengan informasi atau konsep baru yang diterimanya dengan cara mengorganisasi ke dalam bagian-bagian tertentu. Berkaitan dengan pemerolehan konsep ini, Bruner berpandangan bahwa pemerolehan konsep merupakan suatu proses interaktif yang berarti bahwa konstruksi pengetahuan terjadi karena adanya interaksi dengan lingkungan sehingga terjadi perubahan dalam diri anak. Kontruksi pengetahuan tersebut menurut Bruner harus dikaitkan dengan informasi yang telah diperoleh sebelumnya (Dahar, 1989:120). Penekanan Bruner yakni pada bagaimana anak dapat belajar sesuatu dengan cara penemuan empiris. Belajar penemuan ini merupakan suatu proses pencarian pengetahuan secara aktif oleh anak. Osborne dan Witrock (1985:64) memandang bahwa anak sebelum diajar telah mengembangkan pemahaman tentang peristiwa-peristiwa, istilah-istilah, dan strategi-strategi tertentu untuk memahami fenomena alam yang ada. Dengan demikian anak sewaktu memasuki kelas bukan dengan kepala kosong yang siap diisi dengan pengetahuan-pengetahuan atas asumsi guru. Pemerolehan konsep merupakan hasil belajar generatif yang ciri utamanya adalah orang cenderung membentuk persepsi dan arti yang konsisten dengan hasil belajar awalnya. Pengetahuan adalah bentukan (konstruksi) kita sendiri yang sedang menekuninya (Glasersfeld dalam Suparno, 1997). Bila yang sedang menekuni adalah siswa, maka pengetahuan itu adalah bentukan siswa sendiri. Maka 4
5 pengetahuan bukanlah sesuatu yang sudah jadi, yang ada di luar kita, tetapi sesuatu yang harus kita bentuk sendiri dalam pikiran kita. Proses pembentukan ini berjalan terus menerus dengan setiap kali terjadi reorganisasi karena adanya suatu pemahaman yang baru. Berdasarkan teori perkembangan intelek Piaget, pemerolehan konsep berkaitan dengan proses pembentukan skema atau skemata. Skema merupakan struktur mental atau struktur kognitif yang dengannya seseorang secara intelektual beradaptasi dan mengkoordinasi lingkungan sekitarnya (Wadsworth dalam Suparno, 1997). Proses pembentukan skema melibatkan dua aktivitas, yaitu asimilasi dan akomodasi. Asimilasi adalah proses kognitif yang dengannya seseorang mengintegrasikan persepsi, konsep, atau pengalaman baru ke dalam skema atau pola yang sudah ada dalam pikirannya (Suparno, 1997:31). Asimilasi terjadi bila ciri-ciri perangsang atau informasi baru bersesuaian dengan ciri-ciri skema yang telah dimilikinya. Apabila ciri-ciri perangsang tersebut tidak cocok dengan ciri-ciri skema yang telah ada maka perangsang tersebut tidak diasimilasikan. Dalam hal ini seseorang dapat melakukan dua hal, yaitu: (1) menciptakan skema baru yang dapat cocok dengan rangsangan yang baru, atau (2) memodifikasi skema yang ada sehingga cocok dengan rangsangan itu (Suparno, 1997:32). Dua alternatif ini merupakan bentuk-bentuk dari akomodasi. Dalam perkembangan intelek seseorang diperlukan keseimbangan antara asimilasi dan akomodasi. Hal ini disebut dengan ekuilibrasi ( equilibration atau self regulation), yaitu pengaturan diri secara mekanis untuk mengatur kesetimbangan antara asimilasi dan akomodasi. Seseorang yang selalu mengadakan asimilasi akan tetapi jarang melakukan akomodasi cenderung memiliki skema yang luas. Sebaliknya, seseorang yang hanya melakukan akomodasi dan tidak pernah melakukan asimilasi cenderung memiliki skema yang banyak jumlahnya akan tetapi skemata itu cenderung memiliki tingkat keumuman yang kecil (Sund & Trowbridge, 1973:42). 5
6 Berkaitan dengan perolehan konsep, asimilasi terjadi bila ciri-ciri konsep baru dapat cocok dengan ciri-ciri skema yang telah ada. Misalnya, seorang siswa yang baru belajar konsep tentang ion, yaitu atom atau molekul yang bermuatan, di dalam pikirannya akan dimiliki skema tentang ion. Kalau dalam proses belajar selanjutnya ia bertemu dengan konsep tentang ion positif (kation) dan ion negatif (anion) maka ia akan memiliki skema yang sama tentang ion. Bedanya adalah skemanya tentang ion diperluas dan diperinci lebih lengkap. Akomodasi terjadi bila ciri-ciri konsep baru tidak cocok dengan ciri-ciri skema yang telah ada. Jika Piaget memandang pemerolehan konsep terjadi bila konsep baru tersebut dapat dikaitkan dengan skemata yang telah ada, maka pandangan Ausubel menekankan pada bagaimana anak dapat belajar secara bermakna. Proses belajar bermakna menurut Ausubel merupakan suatu proses mengaitkan informasi baru dengan konsep-konsep yang telah ada dalam struktur kognitif. Konsep-konsep yang telah ada dalam struktur kognitif tersebut menurut Ausubel (1963:85) dapat berfungsi sebagai pengatur awal (advance organizer) untuk menghubungkan dan membantu memahami konsep baru yang diterimanya. Struktur kognitif yang dimiliki siswa dapat berupa bangunan konsep yang saling berkaitan satu sama lainnya dan dapat pula berupa sekumpulan konsep yang saling berdiri sendiri. Jenis struktur kognitif ini berhubungan dengan ciri ilmu yang dipelajari serta sumber proses belajar yang diterapkan dalam mempelajari suatu ilmu. Proses pembentukan struktur kognitif yang diharapkan adalah menghasilkan prinsip belajar bermakna. 1.3 Persamaan Reaksi Kimia Persamaan reaksi merupakan salah satu konsep materi kimia yang sangat penting dikuasai oleh siswa dalam mempelajari materi kimia secara keseluruhan, sebab konsep ini merupakan salah satu dasar dalam mempelajari ilmu kimia. Hampir seluruh konsep kimia selalu berhubungan dengan persamaan reaksi. Oleh karena itu, para siswa diharapkan dapat mempelajari dan menguasai konsep persamaan reaksi ini dengan baik. 6
7 Materi persamaan reaksi kimia dipelajari oleh siswa kelas X SMA pada semester pertama. Persamaan reaksi kimia merupakan bahasa ilmu kimia.persamaan reaksi menjelaskan secara kualitatif peristiwa-peristiwa yang terjadi jika dua pereaksi atau lebih bergabung dan secara kuantatif menyatakan jumlah zat yang bereaksi serta produk reaksi. Kita sudah mengetahui perubahan materi secara kimia disebut reaksi kimia. Biasanya suatu reaksi kimia disertai adanya perubahan warna, perubahan suhu, pembentukan endapan, atau timbulnya gas, reaksi kimia dituliskan dalam bentuk persamaan reaksi. Persamaan reaksi menggambarkan zat-zat yang bereaksi (pereaksi = reaktan) dan hasil reaksi (produk), wujud reaktan dan hasil reaksi, perbandingan jumlah partikel reaktan dan hasil reaksi (dinyatakan oleh koefisien), serta arah reaksi (tanda anak panah). Dalam persamaan reaksi, reaktan dituliskan di ruas kiri (sebelah kiri tanda panah) sedangkan hasil rea ksi di ruas kanan (sebelah kanan tanda panah) Reaktan Produk Koefisien Reaksi 2Fe (s) + 6HCl (ag) 2FeCl 3(ag) + 3H 2(ag) Wujud zat Wujud zat yang bereaksi biasanya dituliskan dalam bentuk singkatan (s), (I), (g), dan (aq). Dalam memahami konsep persamaan reaksi kimia beberapa hal mendasar yang harus diperhatikan, yakni: Penulisan Persamaan Reaksi Penulisan persamaan reaksi dapat dilakukan dengan dua langkah sebagai berikut 1. Tuliskan persamaan reaksi dengan menggunakan lambang-lambang, yaitu rumus-rumus kimia zat dan wujud reaksi. 7
8 Contoh: NO (g) + O 2(g) NO 2(g) 2. Memberi koefisien yang sesuai, sehingga jumlah atom ruas kiri sama dengan jumlah atom ruas sehingga diperoleh persamaan reaksi setara yaitu 2NO (g) + O2 (g) 2NO 2(g) Penyetaraan Persamaan Reaksi Penyetaraan persamaan reaksi sesuai dengan hukum kekekalan massa Lavoisier dan teori atom Dalton. Menurut hukum Lavoisier pada reaksi kimia tidak terjadi perubahan massa. Artinya, jumlah dan jenis atom di ruas kiri (reaktan) sama dengan jumlah dan jenis atom di ruas kanan (hasil reaksi). Sesuai dengan teori atom Dalton, dalam reaksi tidak ada atom yang hilang atau tercipta, yang terjadi hanyalah penataan ulang atom-atom reaktan membentuk susunan baru, yaitu hasil reaksi. Agar jenis dan jumlah atom di ruas kiri sama dengan di ruas kanan, persamaan reaksi disetarakan (diseimbangkan) dengan cara mengatur angka di depan reaktan dan hasil reaksi yang disebut koefisien. Angka atau sebagai koefisien tidak dituliskan. Sebagai contoh, perhatikan persamaan reaksi pembakaran gas metana (CH 4 ) menghasilkan karbon dioksida dan uap air, langkah-langkah yang harus dijalankan adalah sebagai berikut. 1. Zat-zat pereaksi ditulis disebelah kiri tanda panah, sedangkan zat hasil reaksi ditulis disebelah kanan tanda panah. CH 4(g) + O 2(g) CO 2(g) + H 2 O (g) 2. menetapkan koefisien salah satu zat, biasanya zat yang rumus kimianya paling kompleks, sama dengan 1, sedangkan zat lain diberikan koefisien sementara dengan huruf 1CH 4(g) + ao 2(g) bco 2(g) + ch 2 O (g) 3. menyetarakan terlebih dahulu unsur yang terkait langsung dengan zat yang diberi koefisien 1 itu. Penyetaraan atom C di ruas kiri = 1 dan di ruas kanan = b, berarti b = 1. Penyetaraan atom H di ruas kiri = 4 dan di ruas kanan = 2c, berarti 2c = 4, atau c = 2. Dengan b = 1 dan c = 2, persamaan reaksinya menjadi : 8
9 1CH 4(g) + ao 2(g) 1CO 2(g) + 2H 2 O (g) 4. menyetarakan unsur lainnya, biasanya akan membantu jika atom O disetarakan paling akhir. Penetaraan atom O di ruas kiri = 2a dan di ruas kanan = = 4 berarti 2a = 4 atau a = 2. Dengan demikian persamaan setaranya adalah 1CH 4 + 2O 2 1CO 2 + 2H 2 O 5. Terakhir, mencantumkan simbol keadaan fasa, seperti I (liqiud), s (solid), g (gas), aq (aqueous). 1CH 4(g) + 2O 2(g) 1CO 2(g) + 2H 2 O (l) Penyetaraan reaksi merupakan penerapan hukum kekekalakan massa. Hukum kekekalan massa menyatakan bahwa sebelum dan sesudah reaksi menyatakan bahwa sebelum dan sesudah reaksi adalah sama. Contoh reaksi di atas merupakan reaksi yang mudah disetarakan sehingga dapat disetarakan secara langsung atau dengan cara pemeriksaan. Namun tidak semua reaksi dapat disetarakan secara langsung atau dengan cara pemeriksaan. Reaksi yang tidak dapat disetarakan secara langsung atau dengan cara pemeriksaan. Merupakan reaksi yang rumit.reaksi rumit dapat diselesaikan dengan menggunakan persamaan subtitusi dan eliminasi. Misalnya untuk reaksi berikut: Sn + HNO 3 SnO 2 + NO 2 + H 2 O Untuk reaksi tersebut bisa kita selesaikan dengan membuat simbol huruf untuk mewakili koefisien masing masing zat: asn + bhno 3 csno 2 + dno 2 + eh 2 O Jumlah atom Sn : a = c..(1) H : b = 2c.... (2) N : b = d (3) O : 3b = 2c + 2d + e.(4) Misalkan b : 1 Dari persamaan (3) diperoleh d 9
10 d = 1 Dari persamaan (2) diperoleh e c = ½ Dari persamaan (4) diperoleh c 3(1) = 2c + 2 (1) + ½ c = ¼ Dari persamaan (1) diperoleh a a : ¼ Reaksinya menjadi ½ Sn +HNO 3 ¼ SnO 3 + NO 2 + ½ H 2 O karena untuk koefisien harus bilangan bulat yang sederhana maka seluruh koefisien dikalikan 4 sehingga reaksinya menjadi : Sn + 4HNO 3 SnO 2 + 4NO 2 + 2H 2 O Macam-macam Reaksi Kimia Reaksi kimia dapat digolongkang menjadi 4 macam: a. Reaksi Penguraian Reaksi penguraian adalah suatu reaksi senyawa tunggal terurai menjadi dua atau lebih zat yang baru. Contoh: Jika amonium klorida dipanaskan maka akan terurai menjadi amonium dan asam klorida. Persamaan reaksinya: NH 4 Cl NH 3 + HCl b. Reaksi Penggabungan Reaksi Penggabungan adalah reaksi dimana dua zat atau lebih bergabung membentuk satu jenis zat yang baru Contoh: Gas nitrogen dan gas hidrogen dapat bereaksi membentuk amonia. Persamaan reaksinya: N 2 + 3H 2 2NH 3 c. Reaksi Pendesakan 10
11 Reaksi pendesakan adalah dimana suatu unsur menggantikan posisi unsur lain dalam suatu senyawa. Contoh: Jika logam seng dicelupkan ke dalam larutan tembaga(ii) sulfat akan menggantikan posisi tembaga. Persamaan reaksinya: Zn (s) + CuSO 4(aq) Cu (s) + ZnSO 4(aq) d. Reaksi Metatitis Reaksi matatetis adalah reaksi kimia yang melibatkan pertukaran antar ion-ion dalam senyawa yang bereaksi. Contoh: Larutan natrium sulfat bereaksi dengan barium nitrat membentuk endapan putih dari barium sulfat. Persamaan reaksinya: NaSO 4(ag) + Ba(NO 3 ) 2(ag) 2NaNO 3(ag) + BaSO 4(s) (Anonim. 2008) 11
12 12
BAB 1V HASIL DAN PEMBAHASAN
 4.1.1 HASIL PENELITIAN BAB 1V HASIL DAN PEMBAHASAN Berdasarkan data hasil penelitian, persentase kemampuan siswa kelas dalam menyelesaikan soal-soal persamaan reaksi kimia dapat dilihat pada tabel dibawah
4.1.1 HASIL PENELITIAN BAB 1V HASIL DAN PEMBAHASAN Berdasarkan data hasil penelitian, persentase kemampuan siswa kelas dalam menyelesaikan soal-soal persamaan reaksi kimia dapat dilihat pada tabel dibawah
BAB III TATA NAMA SENYAWA DAN PERSAMAAN REAKSI
 BAB III TATA NAMA SENYAWA DAN PERSAMAAN REAKSI A. STANDAR KOMPETENSI Mendiskripsikan hukumhukum dasar kimia dan penerapannya dalam perhitungan kimia. B. Kompetensi Dasar : Menuliskan nama senyawa anorganik
BAB III TATA NAMA SENYAWA DAN PERSAMAAN REAKSI A. STANDAR KOMPETENSI Mendiskripsikan hukumhukum dasar kimia dan penerapannya dalam perhitungan kimia. B. Kompetensi Dasar : Menuliskan nama senyawa anorganik
1. Hukum Lavoisier 2. Hukum Proust 3. Hukum Dalton 4. Hukum Gay Lussac & Hipotesis Avogadro
 - - 1. Hukum Lavoisier 2. Hukum Proust 3. Hukum Dalton 4. Hukum Gay Lussac & Hipotesis Avogadro 1. Hukum Lavoisier (Hukum Kekekalan Massa) : Dalam sistem tertutup, massa zat sebelum dan sesudah reaksi
- - 1. Hukum Lavoisier 2. Hukum Proust 3. Hukum Dalton 4. Hukum Gay Lussac & Hipotesis Avogadro 1. Hukum Lavoisier (Hukum Kekekalan Massa) : Dalam sistem tertutup, massa zat sebelum dan sesudah reaksi
IDENTIFIKASI KEMAMPUAN SISWA KELAS X SMA PRASETYA GORONTALO DALAM MENYELESAIKAN SOAL-SOAL PERSAMAAN REAKSI KIMIA. Jurnal
 IDENTIFIKASI KEMAMPUAN SISWA KELAS X SMA PRASETYA GORONTALO DALAM MENYELESAIKAN SOAL-SOAL PERSAMAAN REAKSI KIMIA Jurnal Diajukan Untuk Memenuhi Persyaratan Guna Menempuh Ujian Sarjana Pendidikan Pada Fakultas
IDENTIFIKASI KEMAMPUAN SISWA KELAS X SMA PRASETYA GORONTALO DALAM MENYELESAIKAN SOAL-SOAL PERSAMAAN REAKSI KIMIA Jurnal Diajukan Untuk Memenuhi Persyaratan Guna Menempuh Ujian Sarjana Pendidikan Pada Fakultas
Stoikiometri. OLEH Lie Miah
 Stoikiometri OLEH Lie Miah 1 STANDAR KOMPETENSI KOMPETENSI DASAR INDIKATOR KARAKTERISTIK MATERI KESULITAN BELAJAR SISWA STANDAR KOMPETENSI Memahami hukum-hukum dasar Kimia dan penerapannya dalam perhitungan
Stoikiometri OLEH Lie Miah 1 STANDAR KOMPETENSI KOMPETENSI DASAR INDIKATOR KARAKTERISTIK MATERI KESULITAN BELAJAR SISWA STANDAR KOMPETENSI Memahami hukum-hukum dasar Kimia dan penerapannya dalam perhitungan
MODUL KIMIA SMA IPA Kelas 10
 SMA IPA Kelas 0 A. Massa Atom. Massa Atom Relatif (Ar) Massa atom relatif (Ar) merupakan perbandingan massa atom dengan massa satu atom yang tetap. Secara matematis dapat dirumuskan sebagai berikut. sma
SMA IPA Kelas 0 A. Massa Atom. Massa Atom Relatif (Ar) Massa atom relatif (Ar) merupakan perbandingan massa atom dengan massa satu atom yang tetap. Secara matematis dapat dirumuskan sebagai berikut. sma
STOKIOMETRI. Kimia Kelas X
 STOKIOMETRI Kimia Kelas X SEKOLAH MENENGAH ATAS NEGERI 12 SURABAYA 2015 STOKIOMETRI STOKIOMETRI Pada materi stokiometri, kita akan mempelajari beberapa hal seperti persamaan reaksi, hukum-hukum dasar kimia,
STOKIOMETRI Kimia Kelas X SEKOLAH MENENGAH ATAS NEGERI 12 SURABAYA 2015 STOKIOMETRI STOKIOMETRI Pada materi stokiometri, kita akan mempelajari beberapa hal seperti persamaan reaksi, hukum-hukum dasar kimia,
Materi Pokok Bahasan :
 STOIKIOMETRI Kompetensi : Memiliki kemampuan untuk menginterpretasikan serta menerapkan dalam perhitungan kimia. Memiliki kemampuan untuk mengaplikasikan pengetahuan yang dimilikinya dan terbiasa menggunakan
STOIKIOMETRI Kompetensi : Memiliki kemampuan untuk menginterpretasikan serta menerapkan dalam perhitungan kimia. Memiliki kemampuan untuk mengaplikasikan pengetahuan yang dimilikinya dan terbiasa menggunakan
LOGO STOIKIOMETRI. Marselinus Laga Nur
 LOGO STOIKIOMETRI Marselinus Laga Nur Materi Pokok Bahasan : A. Konsep Mol B. Penentuan Rumus Kimia C. Koefisien Reaksi D. Hukum-hukum Gas A. Konsep Mol Pengertian konsep mol Hubungan mol dengan jumlah
LOGO STOIKIOMETRI Marselinus Laga Nur Materi Pokok Bahasan : A. Konsep Mol B. Penentuan Rumus Kimia C. Koefisien Reaksi D. Hukum-hukum Gas A. Konsep Mol Pengertian konsep mol Hubungan mol dengan jumlah
Hukum Dasar Kimia Dan Konsep Mol
 A. PENDAHULUAN Hukum Dasar Kimia Dan Konsep Mol Hukum dasar kimia merupakan hukum dasar yang digunakan dalam stoikiometri (perhitungan kimia), antara lain: 1) Hukum Lavoisier atau hukum kekekalan massa.
A. PENDAHULUAN Hukum Dasar Kimia Dan Konsep Mol Hukum dasar kimia merupakan hukum dasar yang digunakan dalam stoikiometri (perhitungan kimia), antara lain: 1) Hukum Lavoisier atau hukum kekekalan massa.
LATIHAN ULANGAN TENGAH SEMESTER 2
 Pilihlah jawaban yang paling benar LATIHAN ULANGAN TENGAH SEMESTER 2 TATANAMA 1. Nama senyawa berikut ini sesuai dengan rumus kimianya, kecuali. A. NO = nitrogen oksida B. CO 2 = karbon dioksida C. PCl
Pilihlah jawaban yang paling benar LATIHAN ULANGAN TENGAH SEMESTER 2 TATANAMA 1. Nama senyawa berikut ini sesuai dengan rumus kimianya, kecuali. A. NO = nitrogen oksida B. CO 2 = karbon dioksida C. PCl
Reaksi kimia. Lambang-lambang yang digunakan dalam persamaan reaksi, antara lain:
 Reaksi kimia Reaksi kimia A Persamaan Reaksi Persamaan reaksi menggambarkan reaksi kimia yang terdiri atas rumus kimia pereaksi dan hasil reaksi disertai koefisien masing-masing. Pada reaksi kimia, satu
Reaksi kimia Reaksi kimia A Persamaan Reaksi Persamaan reaksi menggambarkan reaksi kimia yang terdiri atas rumus kimia pereaksi dan hasil reaksi disertai koefisien masing-masing. Pada reaksi kimia, satu
Sulistyani, M.Si.
 Sulistyani, M.Si. sulistyani@uny.ac.id Reaksi oksidasi: perubahan kimia suatu spesies (atom, unsur, molekul) melepaskan elektron. Cu Cu 2+ + 2e Reaksi reduksi: perubahan kimia suatu spesies (atom, unsur,
Sulistyani, M.Si. sulistyani@uny.ac.id Reaksi oksidasi: perubahan kimia suatu spesies (atom, unsur, molekul) melepaskan elektron. Cu Cu 2+ + 2e Reaksi reduksi: perubahan kimia suatu spesies (atom, unsur,
Bab IV Hukum Dasar Kimia
 Bab IV Hukum Dasar Kimia Sumber: Silberberg, Chemistry :The Molecular Nature of Matter and Change Kalsium karbonat ditemukan pada beberapa bentuk seperti pualam, batu koral, dan kapur. Persen massa unsur-unsur
Bab IV Hukum Dasar Kimia Sumber: Silberberg, Chemistry :The Molecular Nature of Matter and Change Kalsium karbonat ditemukan pada beberapa bentuk seperti pualam, batu koral, dan kapur. Persen massa unsur-unsur
KONSEP MOL DAN STOIKIOMETRI
 BAB V KONSEP MOL DAN STOIKIOMETRI Dalam ilmu fisika, dikenal satuan mol untuk besaran jumlah zat. Dalam bab ini, akan dibahas mengenai konsep mol yang mendasari perhitungan kimia (stoikiometri). A. KONSEP
BAB V KONSEP MOL DAN STOIKIOMETRI Dalam ilmu fisika, dikenal satuan mol untuk besaran jumlah zat. Dalam bab ini, akan dibahas mengenai konsep mol yang mendasari perhitungan kimia (stoikiometri). A. KONSEP
KIMIA TERAPAN STOIKIOMETRI DAN HUKUM-HUKUM KIMIA Haris Puspito Buwono
 KIMIA TERAPAN STOIKIOMETRI DAN HUKUM-HUKUM KIMIA Haris Puspito Buwono Semester Gasal 2012/2013 STOIKIOMETRI 2 STOIKIOMETRI adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif dari komposisi
KIMIA TERAPAN STOIKIOMETRI DAN HUKUM-HUKUM KIMIA Haris Puspito Buwono Semester Gasal 2012/2013 STOIKIOMETRI 2 STOIKIOMETRI adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif dari komposisi
Ujian Akhir Semester Mata Pelajaran Kimia Kelas X Wacana berikut digunakan untuk menjawab soal no 1 dan 2. Ditentukan 5 unsur dengan konfigurasi
 Ujian Akhir Semester Mata Pelajaran Kimia Kelas X Wacana berikut digunakan untuk menjawab soal no 1 dan 2. Ditentukan 5 unsur dengan konfigurasi elektron sebagai berikut: P : 2 8 7 S : 2 8 8 Q : 2 8 8
Ujian Akhir Semester Mata Pelajaran Kimia Kelas X Wacana berikut digunakan untuk menjawab soal no 1 dan 2. Ditentukan 5 unsur dengan konfigurasi elektron sebagai berikut: P : 2 8 7 S : 2 8 8 Q : 2 8 8
HUKUM DASAR KIMIA. 2CUO. 28GRAM NITROGEN 52 GRAM MAGNESIUM NITRIDA 3 MG + N 2 MG 3 N 2
 HUKUM DASAR KIMIA. 2CUO. 28GRAM NITROGEN 52 GRAM MAGNESIUM NITRIDA 3 MG + N 2 MG 3 N 2 HUKUM DASAR KIMIA 1) Hukum Kekekalan Massa ( Hukum Lavoisier ). Yaitu : Dalam sistem tertutup, massa zat sebelum
HUKUM DASAR KIMIA. 2CUO. 28GRAM NITROGEN 52 GRAM MAGNESIUM NITRIDA 3 MG + N 2 MG 3 N 2 HUKUM DASAR KIMIA 1) Hukum Kekekalan Massa ( Hukum Lavoisier ). Yaitu : Dalam sistem tertutup, massa zat sebelum
STOIKIOMETRI. STOIKIOMETRI adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif dari komposisi zat-zat kimia dan reaksi-reaksinya.
 STOIKIOMETRI STOIKIOMETRI adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif dari komposisi zat-zat kimia dan reaksi-reaksinya. 1.HUKUM KEKEKALAN MASSA = HUKUM LAVOISIER "Massa zat-zat sebelum
STOIKIOMETRI STOIKIOMETRI adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif dari komposisi zat-zat kimia dan reaksi-reaksinya. 1.HUKUM KEKEKALAN MASSA = HUKUM LAVOISIER "Massa zat-zat sebelum
LOGO. Stoikiometri. Tim Dosen Pengampu MK. Kimia Dasar
 LOGO Stoikiometri Tim Dosen Pengampu MK. Kimia Dasar Konsep Mol Satuan jumlah zat dalam ilmu kimia disebut mol. 1 mol zat mengandung jumlah partikel yang sama dengan jumlah partikel dalam 12 gram C 12,
LOGO Stoikiometri Tim Dosen Pengampu MK. Kimia Dasar Konsep Mol Satuan jumlah zat dalam ilmu kimia disebut mol. 1 mol zat mengandung jumlah partikel yang sama dengan jumlah partikel dalam 12 gram C 12,
STOKIOMETRI BAB. B. Konsep Mol 1. Hubungan Mol dengan Jumlah Partikel. Contoh: Jika Ar Ca = 40, Ar O = 16, Ar H = 1, tentukan Mr Ca(OH) 2!
 BAB 7 STOKIOMETRI A. Massa Molekul Relatif Massa Molekul Relatif (Mr) biasanya dihitung menggunakan data Ar masing-masing atom yang ada dalam molekul tersebut. Mr senyawa = (indeks atom x Ar atom) Contoh:
BAB 7 STOKIOMETRI A. Massa Molekul Relatif Massa Molekul Relatif (Mr) biasanya dihitung menggunakan data Ar masing-masing atom yang ada dalam molekul tersebut. Mr senyawa = (indeks atom x Ar atom) Contoh:
STOIKIOMETRI. Oleh. Sitti Rahmawati S.Pd.
 STOIKIOMETRI Oleh Sitti Rahmawati S.Pd Copyright oke.or.id Artikel ini boleh dicopy,diubah, dikutip, di cetak dalam media kertas atau yang lain, dipublikasikan kembali dalam berbagai bentuk dengan tetap
STOIKIOMETRI Oleh Sitti Rahmawati S.Pd Copyright oke.or.id Artikel ini boleh dicopy,diubah, dikutip, di cetak dalam media kertas atau yang lain, dipublikasikan kembali dalam berbagai bentuk dengan tetap
30 Soal Pilihan Berganda Olimpiade Kimia Tingkat Kabupaten/Kota 2011 Alternatif jawaban berwarna merah adalah kunci jawabannya.
 30 Soal Pilihan Berganda Olimpiade Kimia Tingkat Kabupaten/Kota 2011 Alternatif jawaban berwarna merah adalah kunci jawabannya. 1. Semua pernyataan berikut benar, kecuali: A. Energi kimia ialah energi
30 Soal Pilihan Berganda Olimpiade Kimia Tingkat Kabupaten/Kota 2011 Alternatif jawaban berwarna merah adalah kunci jawabannya. 1. Semua pernyataan berikut benar, kecuali: A. Energi kimia ialah energi
Hubungan koefisien dalam persamaan reaksi dengan hitungan
 STOIKIOMETRI Pengertian Stoikiometri adalah ilmu yang mempelajari dan menghitung hubungan kuantitatif dari reaktan dan produk dalam reaksi kimia (persamaan kimia) Stoikiometri adalah hitungan kimia Hubungan
STOIKIOMETRI Pengertian Stoikiometri adalah ilmu yang mempelajari dan menghitung hubungan kuantitatif dari reaktan dan produk dalam reaksi kimia (persamaan kimia) Stoikiometri adalah hitungan kimia Hubungan
STOIKIOMETRI Konsep mol
 STOIKIOMETRI Konsep mol Dalam hukum-hukum dasar materi ditegaskan bahwa senyawa terbentuk dari unsur bukan dengan perbandingan sembarang tetapi dalam jumlah yang spesifik, demikian juga reaksi kimia antara
STOIKIOMETRI Konsep mol Dalam hukum-hukum dasar materi ditegaskan bahwa senyawa terbentuk dari unsur bukan dengan perbandingan sembarang tetapi dalam jumlah yang spesifik, demikian juga reaksi kimia antara
FAKULTAS TEKNIK UNIVERSITAS NEGERI YOGYAKARTA BAHAN AJAR KIMIA DASAR BAB II RUMUS KIMIA DAN TATANAMA
 No. BAK/TBB/SBG201 Revisi : 00 Tgl. 01 Mei 2008 Hal 1 dari 6 BAB II RUMUS KIMIA DAN TATANAMA A. Rumus Kimia Rumus kimia merupakan kumpulan lambang atom dengan komposisi tertentu. Rumus kimia terdiri dari
No. BAK/TBB/SBG201 Revisi : 00 Tgl. 01 Mei 2008 Hal 1 dari 6 BAB II RUMUS KIMIA DAN TATANAMA A. Rumus Kimia Rumus kimia merupakan kumpulan lambang atom dengan komposisi tertentu. Rumus kimia terdiri dari
WEEK 3, 4 & 5 Bag 3:STOIKIOMETRI. Joko Sedyono Benyamin
 WEEK 3, 4 & 5 Bag 3:STOIKIOMETRI Joko Sedyono Benyamin 1 Diskripsi Stoikiometri adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif/jumlah zat yang terlibat dalam reaksi kimia. Kata ini berasal
WEEK 3, 4 & 5 Bag 3:STOIKIOMETRI Joko Sedyono Benyamin 1 Diskripsi Stoikiometri adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif/jumlah zat yang terlibat dalam reaksi kimia. Kata ini berasal
BAB I STOIKHIOMETRI I - 1
 BAB I STOIKHIOMETRI 1.1 PENDAHULUAN Setiap zat, unsur, senyawa dalam kimia mempunyai nama dan rumus uniknya sendiri. Cara tersingkat untuk memerikan suatu reaksi kimia adalah dengan menuliskan rumus untuk
BAB I STOIKHIOMETRI 1.1 PENDAHULUAN Setiap zat, unsur, senyawa dalam kimia mempunyai nama dan rumus uniknya sendiri. Cara tersingkat untuk memerikan suatu reaksi kimia adalah dengan menuliskan rumus untuk
kimia ASAM-BASA III Tujuan Pembelajaran
 KTSP K-13 kimia K e l a s XI ASAM-BASA III Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami mekanisme reaksi asam-basa. 2. Memahami stoikiometri
KTSP K-13 kimia K e l a s XI ASAM-BASA III Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami mekanisme reaksi asam-basa. 2. Memahami stoikiometri
Menuliskan nama senyawa kimia
 81 Bab 6. Stoikiometri Standar Kompetensi Memahami terjadinya ikatan kimia Memahami konsep mol Kompetensi Dasar Menuliskan nama senyawa kimia Menjelaskan konsep mol Menerapkan hukum Gay Lussac dan hukum
81 Bab 6. Stoikiometri Standar Kompetensi Memahami terjadinya ikatan kimia Memahami konsep mol Kompetensi Dasar Menuliskan nama senyawa kimia Menjelaskan konsep mol Menerapkan hukum Gay Lussac dan hukum
Tujuh4reaksi - - REAKSI KIMIA - - 2H 2 (g) + O 2(g) 2H 2 O ( l ) Reaksi Kimia 7206 Kimia. Reaksi Kimia
 - - REAKSI KIMIA - - Modul ini singkron dengan Aplikasi Android, Download melalui Play Store di HP Kamu, ketik di pencarian Tujuh4reaksi Jika Kamu kesulitan, Tanyakan ke tentor bagaimana cara downloadnya.
- - REAKSI KIMIA - - Modul ini singkron dengan Aplikasi Android, Download melalui Play Store di HP Kamu, ketik di pencarian Tujuh4reaksi Jika Kamu kesulitan, Tanyakan ke tentor bagaimana cara downloadnya.
OAL TES SEMESTER I. I. Pilihlah jawaban yang paling tepat!
 KIMIA X SMA 103 S AL TES SEMESTER I I. Pilihlah jawaban yang paling tepat! 1. Partikel penyusun inti atom terdiri dari... a. proton dan elektron b. proton dan netron c. elektron dan netron d. elektron
KIMIA X SMA 103 S AL TES SEMESTER I I. Pilihlah jawaban yang paling tepat! 1. Partikel penyusun inti atom terdiri dari... a. proton dan elektron b. proton dan netron c. elektron dan netron d. elektron
No. BAK/TBB/SBG201 Revisi : 00 Tgl. 01 Mei 2008 Hal 1 dari 8 Semester I BAB I Prodi PT Boga BAB I MATERI
 No. BAK/TBB/SBG201 Revisi : 00 Tgl. 01 Mei 2008 Hal 1 dari 8 BAB I MATERI Materi adalah sesuatu yang menempati ruang dan mempunyai massa. Materi dapat berupa benda padat, cair, maupun gas. A. Penggolongan
No. BAK/TBB/SBG201 Revisi : 00 Tgl. 01 Mei 2008 Hal 1 dari 8 BAB I MATERI Materi adalah sesuatu yang menempati ruang dan mempunyai massa. Materi dapat berupa benda padat, cair, maupun gas. A. Penggolongan
A. HUKUM PERBANDINGAN VOLUM DAN HIPOTESIS AVOGADRO*
 Di muka kita telah membahas tentang jenis perubahan materi. Bagian dari Kimia yang membahas hubungan kuantitatif (jumlah) antara zat-zat yang terlibat dalam suatu perubahan kimia atau reaksi kimia dikenal
Di muka kita telah membahas tentang jenis perubahan materi. Bagian dari Kimia yang membahas hubungan kuantitatif (jumlah) antara zat-zat yang terlibat dalam suatu perubahan kimia atau reaksi kimia dikenal
Ikatan kimia. 1. Peranan Elektron dalam Pembentukan Ikatan Kimia. Ikatan kimia
 Ikatan kimia 1. Peranan Elektron dalam Pembentukan Ikatan Kimia Ikatan kimia Gaya tarik menarik antara atom sehingga atom tersebut tetap berada bersama-sama dan terkombinasi dalam senyawaan. gol 8 A sangat
Ikatan kimia 1. Peranan Elektron dalam Pembentukan Ikatan Kimia Ikatan kimia Gaya tarik menarik antara atom sehingga atom tersebut tetap berada bersama-sama dan terkombinasi dalam senyawaan. gol 8 A sangat
REDOKS dan ELEKTROKIMIA
 REDOKS dan ELEKTROKIMIA Overview Konsep termodinamika tidak hanya berhubungan dengan mesin uap, atau transfer energi berupa kalor dan kerja Dalam konteks kehidupan sehari-hari aplikasinya sangat luas mulai
REDOKS dan ELEKTROKIMIA Overview Konsep termodinamika tidak hanya berhubungan dengan mesin uap, atau transfer energi berupa kalor dan kerja Dalam konteks kehidupan sehari-hari aplikasinya sangat luas mulai
MODUL STOIKIOMETRI 1
 MODUL STOIKIOMETRI 1 1. Pengertian Mol Mol merupakan suatu satuan jumlah, yang berasal dari kata moles yang artinya sejumlah massa / sejumlah kecil massa, hampir sama dengan lusin. 1 mol = 6,02 X 10 23
MODUL STOIKIOMETRI 1 1. Pengertian Mol Mol merupakan suatu satuan jumlah, yang berasal dari kata moles yang artinya sejumlah massa / sejumlah kecil massa, hampir sama dengan lusin. 1 mol = 6,02 X 10 23
Redoks dan Elektrokimia Tim Kimia FTP
 Redoks dan Elektrokimia Tim Kimia FTP KONSEP ELEKTROKIMIA Dalam arti yang sempit elektrokimia adalah ilmu pengetahuan yang mempelajari peristiwa-peristiwa yang terjadi di dalam sel elektrokimia. Sel jenis
Redoks dan Elektrokimia Tim Kimia FTP KONSEP ELEKTROKIMIA Dalam arti yang sempit elektrokimia adalah ilmu pengetahuan yang mempelajari peristiwa-peristiwa yang terjadi di dalam sel elektrokimia. Sel jenis
LARUTAN ELEKTROLIT DAN KONSEP REDOKS
 LARUTAN ELEKTROLIT DAN KONSEP REDOKS LARUTAN ELEKTROLIT DAN KONSEP REDOKS \usepackage{chemmacros} \ch{n2 \gas{} + 3 H2 \gas{} ->2 NH3 \gas{} } Stoikimiometri Membahas tentang hubungan massa antar unsur
LARUTAN ELEKTROLIT DAN KONSEP REDOKS LARUTAN ELEKTROLIT DAN KONSEP REDOKS \usepackage{chemmacros} \ch{n2 \gas{} + 3 H2 \gas{} ->2 NH3 \gas{} } Stoikimiometri Membahas tentang hubungan massa antar unsur
REAKSI REDOKS dan ELEKTROKIMIA
 REAKSI REDOKS dan ELEKTROKIMIA 1. Konsep Reduksi Oksidasi (Redoks) No Reaksi Oksidasi Reaksi Reduksi 1 reaksi penambahan oksigen reaksi pengurangan oksigen 2 peristiwa pelepasan elektron Contoh : Cu Cu
REAKSI REDOKS dan ELEKTROKIMIA 1. Konsep Reduksi Oksidasi (Redoks) No Reaksi Oksidasi Reaksi Reduksi 1 reaksi penambahan oksigen reaksi pengurangan oksigen 2 peristiwa pelepasan elektron Contoh : Cu Cu
TATA NAMA SENYAWA DAN PER- SAMAAN REAKSI
 TATA NAMA SENYAWA DAN PER- SAMAAN REAKSI A. RUMUS KIMIA B. TATA NAMA SENYAWA ANRGANIK C. PERSAMAAN REAKSI Materi tersusun oleh atom-atom, misalnya tembaga, jika tembaga kita potong menjadi dua bagian masing-masing
TATA NAMA SENYAWA DAN PER- SAMAAN REAKSI A. RUMUS KIMIA B. TATA NAMA SENYAWA ANRGANIK C. PERSAMAAN REAKSI Materi tersusun oleh atom-atom, misalnya tembaga, jika tembaga kita potong menjadi dua bagian masing-masing
III. REAKSI KIMIA. Jenis kelima adalah reaksi penetralan, merupakan reaksi asam dengan basa membentuk garam dan air.
 III. REAKSI KIMIA Tujuan 1. Mengamati bukti terjadinya suatu reaksi kimia. 2. Menuliskan persamaan reaksi kimia. 3. Mempelajari secara sistematis lima jenis reaksi utama. 4. Membuat logam tembaga dari
III. REAKSI KIMIA Tujuan 1. Mengamati bukti terjadinya suatu reaksi kimia. 2. Menuliskan persamaan reaksi kimia. 3. Mempelajari secara sistematis lima jenis reaksi utama. 4. Membuat logam tembaga dari
HUKUM DASAR KIMIA DAN STOIKIOMETRI
 HUKUM DASAR KIMIA DAN STOIKIOMETRI Bagaimana cara untuk mengukur jumlah suatu senyawa yang terkandung dalam suatu material? Ini merupakan pertanyaan dasar yang telah dijawab oleh para kimiawan terdahulu.
HUKUM DASAR KIMIA DAN STOIKIOMETRI Bagaimana cara untuk mengukur jumlah suatu senyawa yang terkandung dalam suatu material? Ini merupakan pertanyaan dasar yang telah dijawab oleh para kimiawan terdahulu.
Elektrokimia. Tim Kimia FTP
 Elektrokimia Tim Kimia FTP KONSEP ELEKTROKIMIA Dalam arti yang sempit elektrokimia adalah ilmu pengetahuan yang mempelajari peristiwa-peristiwa yang terjadi di dalam sel elektrokimia. Sel jenis ini merupakan
Elektrokimia Tim Kimia FTP KONSEP ELEKTROKIMIA Dalam arti yang sempit elektrokimia adalah ilmu pengetahuan yang mempelajari peristiwa-peristiwa yang terjadi di dalam sel elektrokimia. Sel jenis ini merupakan
Stoikiometri. Bab 3. Massa atom merupakan massa dari atom dalam satuan massa atom (sma). Secara Mikro atom & molekul.
 Bab 3 Stoikiometri Secara Mikro atom & molekul Secara Makro gram Massa atom merupakan massa dari atom dalam satuan massa atom (sma). Perjanjian internasional: 1 atom 12 C beratnya 12 sma Jika ditimbang
Bab 3 Stoikiometri Secara Mikro atom & molekul Secara Makro gram Massa atom merupakan massa dari atom dalam satuan massa atom (sma). Perjanjian internasional: 1 atom 12 C beratnya 12 sma Jika ditimbang
K13 Revisi Antiremed Kelas 11 Kimia
 K13 Revisi Antiremed Kelas 11 Kimia Stoikiometri Larutan - Soal Doc. Name: RK13AR11KIM0601 Doc. Version : 2016-12 01. Zat-zat berikut ini dapat bereaksi dengan larutan asam sulfat, kecuali... (A) kalsium
K13 Revisi Antiremed Kelas 11 Kimia Stoikiometri Larutan - Soal Doc. Name: RK13AR11KIM0601 Doc. Version : 2016-12 01. Zat-zat berikut ini dapat bereaksi dengan larutan asam sulfat, kecuali... (A) kalsium
AMALDO FIRJARAHADI TANE
 DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN UTUL UGM KIMIA 2013 Page 1 1. 2. MATERI: HUKUM-HUKUM DASAR KIMIA Di soal diketahui dan ditanya: m (NH 2 ) 2 CO = 12.000 ton/tahun (pabrik) m N 2 = ton/tahun?
DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN UTUL UGM KIMIA 2013 Page 1 1. 2. MATERI: HUKUM-HUKUM DASAR KIMIA Di soal diketahui dan ditanya: m (NH 2 ) 2 CO = 12.000 ton/tahun (pabrik) m N 2 = ton/tahun?
AMALDO FIRJARAHADI TANE
 DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN UTUL UGM KIMIA 2013 Page 1 1. 2. MATERI: TERMOKIMIA Pada soal diketahui dan ditanya: ΔH c C 2 H 5 OH = -1380 kj/mol ΔH d C 6 H 12 O 6 = -60 kj/mol ΔH c C
DISUSUN OLEH AMALDO FIRJARAHADI TANE PEMBAHASAN UTUL UGM KIMIA 2013 Page 1 1. 2. MATERI: TERMOKIMIA Pada soal diketahui dan ditanya: ΔH c C 2 H 5 OH = -1380 kj/mol ΔH d C 6 H 12 O 6 = -60 kj/mol ΔH c C
kimia Kelas X KONSEP MOL I K-13 A. Persamaan Reaksi
 K-13 Kelas X kimia KNSEP ML I Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami persamaan reaksi kimia dan komponen-komponennya. 2. Memahami cara
K-13 Kelas X kimia KNSEP ML I Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami persamaan reaksi kimia dan komponen-komponennya. 2. Memahami cara
BAB 5 HUKUM DASAR KIMIA
 BAB 5 HUKUM DASAR KIMIA Dalam ilmu kimia perlu dipelajari massa dan volume zat-zat yang bereaksi dan zat yang dihasilkan dalam suatu reaksi kimia. Studi tentang hubungan-hubungan kuantitatif dalam suatu
BAB 5 HUKUM DASAR KIMIA Dalam ilmu kimia perlu dipelajari massa dan volume zat-zat yang bereaksi dan zat yang dihasilkan dalam suatu reaksi kimia. Studi tentang hubungan-hubungan kuantitatif dalam suatu
KONSEP MOL DAN STOIKIOMETRI
 KONSEP MOL DAN STOIKIOMETRI HUKUM-HUKUM DASAR KIMIA 1. Asas Lavoiser atau kekekalan massa jumlah sebelum dan setelah reaksi kimia adalah tetap 2. Hukum Gas Ideal P V = nrt Dengan P adalah tekanan (atm),
KONSEP MOL DAN STOIKIOMETRI HUKUM-HUKUM DASAR KIMIA 1. Asas Lavoiser atau kekekalan massa jumlah sebelum dan setelah reaksi kimia adalah tetap 2. Hukum Gas Ideal P V = nrt Dengan P adalah tekanan (atm),
BAB II KAJIAN PUSTAKA. dikemukakan oleh Ehrenberg (dalam Pakaya, 2008: 3) bahwa konsep merupakan
 6 BAB II KAJIAN PUSTAKA 2. 1 Konsep dan Pemahaman Konsep Kimia Banyak definisi konsep yang dikemukakan oleh para ahli, seperti yang dikemukakan oleh Ehrenberg (dalam Pakaya, 2008: 3) bahwa konsep merupakan
6 BAB II KAJIAN PUSTAKA 2. 1 Konsep dan Pemahaman Konsep Kimia Banyak definisi konsep yang dikemukakan oleh para ahli, seperti yang dikemukakan oleh Ehrenberg (dalam Pakaya, 2008: 3) bahwa konsep merupakan
Hukum Dasar Ilmu Kimia Sumber :
 A Hukum Kekekalan Massa (Hukum Lavoisier) Hukum Dasar Ilmu Kimia Sumber : wwwe-dukasinet Pernahkah Anda memperhatikan sepotong besi yang dibiarkan di udara terbuka, dan pada suatu waktu kita akan menemukan,
A Hukum Kekekalan Massa (Hukum Lavoisier) Hukum Dasar Ilmu Kimia Sumber : wwwe-dukasinet Pernahkah Anda memperhatikan sepotong besi yang dibiarkan di udara terbuka, dan pada suatu waktu kita akan menemukan,
1. Tragedi Minamata di Jepang disebabkan pencemaran logam berat... A. Hg B. Ag C. Pb Kunci : A. D. Cu E. Zn
 1. Tragedi Minamata di Jepang disebabkan pencemaran logam berat... A. Hg B. Ag C. Pb Kunci : A D. Cu E. Zn 2. Nomor atom belerang adalah 16. Dalam anion sulfida, S 2-, konfigurasi elektronnya adalah...
1. Tragedi Minamata di Jepang disebabkan pencemaran logam berat... A. Hg B. Ag C. Pb Kunci : A D. Cu E. Zn 2. Nomor atom belerang adalah 16. Dalam anion sulfida, S 2-, konfigurasi elektronnya adalah...
Sumber: Silberberg, Chemistry: The Molecular Nature of Matter and Change
 Bab V Perhitungan Kimia Sumber: Silberberg, Chemistry: The Molecular Nature of Matter and Change Jumlah permen dalam stoples dapat diketahui jika berat dari satu permen dan seluruh permen diketahui. Cara
Bab V Perhitungan Kimia Sumber: Silberberg, Chemistry: The Molecular Nature of Matter and Change Jumlah permen dalam stoples dapat diketahui jika berat dari satu permen dan seluruh permen diketahui. Cara
STOIKIOMETRI STOIKIOMETRI
 BAB V STOIKIOMETRI Standar Kompetensi Memahami hukum-hukum dasar kimia dan penerapannya dalam perhitungan kimia (stoikiometri) Kompetensi Dasar Mendeskripsikan tata nama senyawa anorganik dan organik sederhana
BAB V STOIKIOMETRI Standar Kompetensi Memahami hukum-hukum dasar kimia dan penerapannya dalam perhitungan kimia (stoikiometri) Kompetensi Dasar Mendeskripsikan tata nama senyawa anorganik dan organik sederhana
Stoikhiometri : dan metron = mengukur. Membahas tentang : senyawa) senyawa (stoikhiometri. (stoikhiometri. reaksi)
 STOIKHIOMETRI Stoikhiometri : Dari kata Stoicheion = unsur dan metron = mengukur Membahas tentang : hub massa antar unsur dalam suatu senyawa (stoikhiometri senyawa) dan antar zat dalam suatu reaksi (stoikhiometri
STOIKHIOMETRI Stoikhiometri : Dari kata Stoicheion = unsur dan metron = mengukur Membahas tentang : hub massa antar unsur dalam suatu senyawa (stoikhiometri senyawa) dan antar zat dalam suatu reaksi (stoikhiometri
BAB IV HUKUM DASAR KIMIA
 BAB IV HUKUM DASAR KIMIA KOMPETENSI DASAR : 2.1 Membuktikan dan mengkomunikasikan berlakunya hukum-hukum dasar kimia melalui percobaan Indikator : 1. Membuktikan berdasarkan percobaan bahwa massa zat sebelum
BAB IV HUKUM DASAR KIMIA KOMPETENSI DASAR : 2.1 Membuktikan dan mengkomunikasikan berlakunya hukum-hukum dasar kimia melalui percobaan Indikator : 1. Membuktikan berdasarkan percobaan bahwa massa zat sebelum
Rangkuman Materi Larutan Elektrolit dan Non elektrolit
 Rangkuman Materi Larutan Elektrolit dan Non elektrolit LARUTAN ELEKTROLIT DAN LARUTAN NON ELEKTROLIT LARUTAN ELEKTROLIT 1. Pengertian Larutan Elektrolit Larutan elektrolit adalah larutan yang dapat menghantarkan
Rangkuman Materi Larutan Elektrolit dan Non elektrolit LARUTAN ELEKTROLIT DAN LARUTAN NON ELEKTROLIT LARUTAN ELEKTROLIT 1. Pengertian Larutan Elektrolit Larutan elektrolit adalah larutan yang dapat menghantarkan
Massa atom merupakan massa dari atom dalam satuan massa atom (sma).
 Bab 3 Stoikiometri Secara Mikro atom & molekul Secara Makro gram Massa atom merupakan massa dari atom dalam satuan massa atom (sma). Perjanjian internasional: 1 atom 12 C beratnya 12 sma Jika ditimbang
Bab 3 Stoikiometri Secara Mikro atom & molekul Secara Makro gram Massa atom merupakan massa dari atom dalam satuan massa atom (sma). Perjanjian internasional: 1 atom 12 C beratnya 12 sma Jika ditimbang
Chapter 7 Larutan tirtawi (aqueous solution)
 Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi modif oleh Dr I Kartini Chapter 7 Larutan tirtawi (aqueous solution) Larutan adalah campuran yang homogen dari dua atau lebih
Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi modif oleh Dr I Kartini Chapter 7 Larutan tirtawi (aqueous solution) Larutan adalah campuran yang homogen dari dua atau lebih
1. Ciri-Ciri Reaksi Kimia
 Apakah yang dimaksud dengan reaksi kimia? Reaksi kimia adalah peristiwa perubahan kimia dari zat-zat yang bereaksi (reaktan) menjadi zat-zat hasil reaksi (produk). Pada reaksi kimia selalu dihasilkan zat-zat
Apakah yang dimaksud dengan reaksi kimia? Reaksi kimia adalah peristiwa perubahan kimia dari zat-zat yang bereaksi (reaktan) menjadi zat-zat hasil reaksi (produk). Pada reaksi kimia selalu dihasilkan zat-zat
TES PRESTASI BELAJAR
 TES PRESTASI BELAJAR Hari/tanggal : selasa/8 Mei 2012 Mata Pelajaran: Kimia Waktu : 90 menit Petunjuk : 1. Berdoalah sebelum mengerjakan soal 2. Bacalah petunjuk soal terlebih dahulu 3. Pilih salah satu
TES PRESTASI BELAJAR Hari/tanggal : selasa/8 Mei 2012 Mata Pelajaran: Kimia Waktu : 90 menit Petunjuk : 1. Berdoalah sebelum mengerjakan soal 2. Bacalah petunjuk soal terlebih dahulu 3. Pilih salah satu
Reaksi Oksidasi-Reduksi
 Reaksi ksidasireduksi Reaksi yang melibatkan transfer Elektron disebut ksidasireduksi atau Reaksi Redoks ksidasi adalah hilangnya Elektron suatu reaktan Reduksi adalah penangkapan Elektron oleh reaktan
Reaksi ksidasireduksi Reaksi yang melibatkan transfer Elektron disebut ksidasireduksi atau Reaksi Redoks ksidasi adalah hilangnya Elektron suatu reaktan Reduksi adalah penangkapan Elektron oleh reaktan
Soal 2.1. unsurnya dan menghasilkan. Penyelesaian. Perbandingan unsur-unsur Zn : O : P 25,40 : 16,58 : 8,02 65,
 Soal. Seng fosfat digunakan sebagai semen gigi. Sebanyak 50,00 mg sampel dihancurkan menjadi unsur-unsurnya unsurnya dan menghasilkan 6,58 mg oksigen,, 8,0 mg fosforus, dan 5,40 mg seng. Tentukan rumus
Soal. Seng fosfat digunakan sebagai semen gigi. Sebanyak 50,00 mg sampel dihancurkan menjadi unsur-unsurnya unsurnya dan menghasilkan 6,58 mg oksigen,, 8,0 mg fosforus, dan 5,40 mg seng. Tentukan rumus
Reaksi dan Stoikiometri Larutan
 Reaksi dan Stoikiometri Larutan A. PERSAMAAN REAKSI ION Persamaan reaksi ion adalah persamaan reaksi yang menjelaskan bagaimana reaksi antar-ion terjadi pada larutan elektrolit. Persamaan reaksi ion terdiri
Reaksi dan Stoikiometri Larutan A. PERSAMAAN REAKSI ION Persamaan reaksi ion adalah persamaan reaksi yang menjelaskan bagaimana reaksi antar-ion terjadi pada larutan elektrolit. Persamaan reaksi ion terdiri
Asam + Oksida Basa Garam + air
 MODUL JENIS - JENIS REAKSI dalam LARUTAN Jenis-Jenis reaksi antara lain : Reaksi Asam dan Basa Reaksi pendesakan logam Reaksi Metatesis ( Dekomposisi ) A. PENGGARAMAN Jenis-jenis Reaksi penggaraman : 1.
MODUL JENIS - JENIS REAKSI dalam LARUTAN Jenis-Jenis reaksi antara lain : Reaksi Asam dan Basa Reaksi pendesakan logam Reaksi Metatesis ( Dekomposisi ) A. PENGGARAMAN Jenis-jenis Reaksi penggaraman : 1.
Laporan Praktikum Analisis Kualitatif Anion
 Laporan Praktikum Analisis Kualitatif Anion I. Tujuan Tujuan dari praktikum ini adalah untuk memahami prinsip-prinsip dasar yang melatarbelakangi prosedur pemisahan anion serta mengidentifikasi jenis anion
Laporan Praktikum Analisis Kualitatif Anion I. Tujuan Tujuan dari praktikum ini adalah untuk memahami prinsip-prinsip dasar yang melatarbelakangi prosedur pemisahan anion serta mengidentifikasi jenis anion
Antiremed Kelas 11 Kimia
 Antiremed Kelas 11 Kimia Stoikiometri Larutan - Latihan Soal Doc. Name: AR11KIM0699 Doc. Version : 2012-07 01. Zat-zat berikut ini dapat bereaksi dengan larutan asam sulfat, kecuali... (A) kalsium oksida
Antiremed Kelas 11 Kimia Stoikiometri Larutan - Latihan Soal Doc. Name: AR11KIM0699 Doc. Version : 2012-07 01. Zat-zat berikut ini dapat bereaksi dengan larutan asam sulfat, kecuali... (A) kalsium oksida
K13 Revisi Antiremed Kelas 10 Kimia
 K1 Revisi Antiremed Kelas 10 Kimia Stoikiometri - Soal Doc. Name:RK1AR10KIM0901 Version : 2016-10 halaman 1 1. Jika diketahui massa atom C-12= p gram dan massa 1 atom unsur X adalah a gram. Massa atom
K1 Revisi Antiremed Kelas 10 Kimia Stoikiometri - Soal Doc. Name:RK1AR10KIM0901 Version : 2016-10 halaman 1 1. Jika diketahui massa atom C-12= p gram dan massa 1 atom unsur X adalah a gram. Massa atom
K13 Revisi Antiremed Kelas 10 Kimia
 K13 Revisi Antiremed Kelas 10 Kimia Hukum Dasar Perhitungan Kimia - Latihan Soal Doc. Name: RK13AR10KIM0801 Version : 2016-11 halaman 1 01. Pernyataan yang paling sesuai tentang hukum Lavoisier (A) Jumlah
K13 Revisi Antiremed Kelas 10 Kimia Hukum Dasar Perhitungan Kimia - Latihan Soal Doc. Name: RK13AR10KIM0801 Version : 2016-11 halaman 1 01. Pernyataan yang paling sesuai tentang hukum Lavoisier (A) Jumlah
D. 4,50 x 10-8 E. 1,35 x 10-8
 1. Pada suatu suhu tertentu, kelarutan PbI 2 dalam air adalah 1,5 x 10-3 mol/liter. Berdasarkan itu maka Kp PbI 2 adalah... A. 4,50 x 10-9 B. 3,37 x 10-9 C. 6,75 x 10-8 S : PbI 2 = 1,5. 10-3 mol/liter
1. Pada suatu suhu tertentu, kelarutan PbI 2 dalam air adalah 1,5 x 10-3 mol/liter. Berdasarkan itu maka Kp PbI 2 adalah... A. 4,50 x 10-9 B. 3,37 x 10-9 C. 6,75 x 10-8 S : PbI 2 = 1,5. 10-3 mol/liter
BAB III METODOLOGI PENELITIAN
 BAB III METODOLOGI PENELITIAN A. Lokasi dan Subjek Penelitian Penelitian ini dilaksanakan di SMA Negeri 2 Bandung. Subyek penelitian dalam penelitian ini adalah siswa SMA kelas X dan XI yang telah mempelajari
BAB III METODOLOGI PENELITIAN A. Lokasi dan Subjek Penelitian Penelitian ini dilaksanakan di SMA Negeri 2 Bandung. Subyek penelitian dalam penelitian ini adalah siswa SMA kelas X dan XI yang telah mempelajari
Antiremed Kelas 10 KIMIA
 Antiremed Kelas 10 KIMIA Persiapan UAS 1 Kimia Doc Name: AR10KIM01UAS Version : 2016-07 halaman 1 01. Partikel berikut yang muatannya sebesar 19 1,6 10 C dan bermassa 1 sma (A) elektron (B) proton (C)
Antiremed Kelas 10 KIMIA Persiapan UAS 1 Kimia Doc Name: AR10KIM01UAS Version : 2016-07 halaman 1 01. Partikel berikut yang muatannya sebesar 19 1,6 10 C dan bermassa 1 sma (A) elektron (B) proton (C)
Partikel Materi. Partikel Materi
 Bab 4 Partikel Materi Tujuan Pembelajaran Setelah mempelajari bab ini, kamu diharapkan mampu: menjelaskan konsep atom, ion, dan molekul; menghubungkan konsep atom, ion, dan molekul dengan produk kimia
Bab 4 Partikel Materi Tujuan Pembelajaran Setelah mempelajari bab ini, kamu diharapkan mampu: menjelaskan konsep atom, ion, dan molekul; menghubungkan konsep atom, ion, dan molekul dengan produk kimia
Soal 5 Jumlah mol dari 29,8 gram amonium fosfat ((NH4)3PO4) (Ar N = 14, H = 1, dan P = 31) adalah. A. 0,05 mol
 Bank Soal Stoikiometri Kimia Bagian 2 Soal 1 Satu liter campuran gas terdiri dari 60% volume metana (CH4) dan sisanya gas etana (C2H6) dibakar sempurna sesuai reaksi: CH4 + 3 O2 2 CO2 + 2 H2O 2 C2H6 +
Bank Soal Stoikiometri Kimia Bagian 2 Soal 1 Satu liter campuran gas terdiri dari 60% volume metana (CH4) dan sisanya gas etana (C2H6) dibakar sempurna sesuai reaksi: CH4 + 3 O2 2 CO2 + 2 H2O 2 C2H6 +
LEMBARAN SOAL 11. Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH )
 LEMBARAN SOAL 11 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan. Periksa dan bacalah soal dengan
LEMBARAN SOAL 11 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan. Periksa dan bacalah soal dengan
MATERI adalah segala sesuatu yang mempunyai massa dan menempati ruang ( punya volume )
 MATERI adalah segala sesuatu yang mempunyai massa dan menempati ruang ( punya volume ) Perubahan materi 1. perubahan fisis a) perubahan yang tidak menghasilkan zat baru b) perubahan bentuk dan wujud tanpa
MATERI adalah segala sesuatu yang mempunyai massa dan menempati ruang ( punya volume ) Perubahan materi 1. perubahan fisis a) perubahan yang tidak menghasilkan zat baru b) perubahan bentuk dan wujud tanpa
BAB V PERHITUNGAN KIMIA
 BAB V PERHITUNGAN KIMIA KOMPETENSI DASAR 2.3 : Menerapkan hukum Gay Lussac dan hukum Avogadro serta konsep mol dalam menyelesaikan perhitungan kimia (stoikiometri ) Indikator : 1. Siswa dapat menghitung
BAB V PERHITUNGAN KIMIA KOMPETENSI DASAR 2.3 : Menerapkan hukum Gay Lussac dan hukum Avogadro serta konsep mol dalam menyelesaikan perhitungan kimia (stoikiometri ) Indikator : 1. Siswa dapat menghitung
Reaksi Dan Stoikiometri Larutan
 A. PERSAMAAN REAKSI ION Reaksi Dan Stoikiometri Larutan Persamaan reaksi ion adalah persamaan reaksi yang menjelaskan bagaimana reaksi antar-ion terjadi pada elektrolit. Persamaan reaksi ion terdiri dari:
A. PERSAMAAN REAKSI ION Reaksi Dan Stoikiometri Larutan Persamaan reaksi ion adalah persamaan reaksi yang menjelaskan bagaimana reaksi antar-ion terjadi pada elektrolit. Persamaan reaksi ion terdiri dari:
TES PRESTASI BELAJAR. Hari/tanggal : Senin/7 Mei 2012 Mata Pelajaran: Kimia Waktu : 90 menit
 TES PRESTASI BELAJAR Hari/tanggal : Senin/7 Mei 2012 Mata Pelajaran: Kimia Waktu : 90 menit Petunjuk : 1. Berdoalah sebelum mengerjakan soal 2. Bacalah petunjuk soal terlebih dahulu 3. Pilih salah satu
TES PRESTASI BELAJAR Hari/tanggal : Senin/7 Mei 2012 Mata Pelajaran: Kimia Waktu : 90 menit Petunjuk : 1. Berdoalah sebelum mengerjakan soal 2. Bacalah petunjuk soal terlebih dahulu 3. Pilih salah satu
Penyetaraan Persamaan Reaksi Kimia dengan Metode Eliminasi Gauss
 Penyetaraan Persamaan Reaksi Kimia dengan Metode Eliminasi Gauss Jonathan Marcel T (13507072) 1 Program Studi Teknik Informatika Sekolah Teknik Elektro dan Informatika Institut Teknologi Bandung, Jl. Ganesha
Penyetaraan Persamaan Reaksi Kimia dengan Metode Eliminasi Gauss Jonathan Marcel T (13507072) 1 Program Studi Teknik Informatika Sekolah Teknik Elektro dan Informatika Institut Teknologi Bandung, Jl. Ganesha
Bab V Ikatan Kimia. B. Struktur Lewis Antar unsur saling berinteraksi dengan menerima dan melepaskan elektron di kulit terluarnya. Gambaran terjadinya
 Bab V Ikatan Kimia Sebagian besar unsur yang ada di alam mempunyai kecenderungan untuk berinteraksi (berikatan) dengan unsur lain. Hal itu dilakukan karena unsur tersebut ingin mencapai kestabilan. Cara
Bab V Ikatan Kimia Sebagian besar unsur yang ada di alam mempunyai kecenderungan untuk berinteraksi (berikatan) dengan unsur lain. Hal itu dilakukan karena unsur tersebut ingin mencapai kestabilan. Cara
Reaksi kimia. Di susun oleh ; 1.Ario kristian KELOMPOK 3. 3.M zaenal arifin M. ARIF RAMDHONI 4.Lutfi hilman f
 Reaksi kimia Di susun oleh ; 1.Ario kristian 2.Arif rahmat KELOMPOK 3 DI PRESENTASIKAN OLEH : 3.M zaenal arifin M. ARIF RAMDHONI 4.Lutfi hilman f 111910101083 Apa sih reaksi kimia itu?? Reaksi kimia adalah
Reaksi kimia Di susun oleh ; 1.Ario kristian 2.Arif rahmat KELOMPOK 3 DI PRESENTASIKAN OLEH : 3.M zaenal arifin M. ARIF RAMDHONI 4.Lutfi hilman f 111910101083 Apa sih reaksi kimia itu?? Reaksi kimia adalah
SATUAN ACARA PERKULIAHAN (SAP)
 Mata Kuliah : Kimia Teknik Kode Mata Kuliah : MKT 1105 SKS : 2(2-0) Waktu Pertemuan : 100 Menit SATUAN ACARA PERKULIAHAN (SAP) A. Tujuan Pembelajaran 1. Tujuan pembelajaran umum mata kuliah Setelah menyelesaikan
Mata Kuliah : Kimia Teknik Kode Mata Kuliah : MKT 1105 SKS : 2(2-0) Waktu Pertemuan : 100 Menit SATUAN ACARA PERKULIAHAN (SAP) A. Tujuan Pembelajaran 1. Tujuan pembelajaran umum mata kuliah Setelah menyelesaikan
C. Reaksi oksidasi reduksi berdasarkan peningkatan dan penurunan bilangan oksidasi. Bilangan Oksidasi (biloks)
 97 Nama : Kelompok : Mata Pelajaran : Kimia Kelas/Semester : X 5 /2 Alokasi Waktu : 2 x 45 menit. Materi pokok : Konsep Redoks Standar Kompetensi : 3. Memahami sifat-sifat larutan elektrolit dan non elektrolit
97 Nama : Kelompok : Mata Pelajaran : Kimia Kelas/Semester : X 5 /2 Alokasi Waktu : 2 x 45 menit. Materi pokok : Konsep Redoks Standar Kompetensi : 3. Memahami sifat-sifat larutan elektrolit dan non elektrolit
PRAKTIKUM KIMIA DASAR I
 PRAKTIKUM KIMIA DASAR I REAKSI KIMIA PADA SIKLUS LOGAM TEMBAGA Oleh : Luh Putu Arisanti 1308105006 JURUSAN KIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS UDAYANA BADUNG TAHUN 2013/2014
PRAKTIKUM KIMIA DASAR I REAKSI KIMIA PADA SIKLUS LOGAM TEMBAGA Oleh : Luh Putu Arisanti 1308105006 JURUSAN KIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS UDAYANA BADUNG TAHUN 2013/2014
Oksidasi dan Reduksi
 Oksidasi dan Reduksi Reaksi kimia dapat diklasifikasikan dengan beberapa cara antara lain reduksi-oksidasi (redoks) Reaksi : selalu terjadi bersama-sama. Zat yang teroksidasi = reduktor Zat yang tereduksi
Oksidasi dan Reduksi Reaksi kimia dapat diklasifikasikan dengan beberapa cara antara lain reduksi-oksidasi (redoks) Reaksi : selalu terjadi bersama-sama. Zat yang teroksidasi = reduktor Zat yang tereduksi
6.1 HUKUM-HUKUM DASAR KIMIA
 6.1 HUKUM-HUKUM DASAR KIMIA 1. Hukum kekekalan massa oleh Antoine Laurent Lavoiser (1789). Lavoiser mengemukakan pernyataan yang disebut hukum kekekalan massa, yang berbunyi : Pada reaksi kimia, massa
6.1 HUKUM-HUKUM DASAR KIMIA 1. Hukum kekekalan massa oleh Antoine Laurent Lavoiser (1789). Lavoiser mengemukakan pernyataan yang disebut hukum kekekalan massa, yang berbunyi : Pada reaksi kimia, massa
BAB IV TEMUAN DAN PEMBAHASAN. Dalam pengembangan strategi pembelajaran intertekstual pada materi
 BAB IV TEMUAN DAN PEMBAHASAN Dalam pengembangan strategi pembelajaran intertekstual pada materi pokok kesetimbangan kimia secara garis besar penelitian terbagi dalam beberapa tahapan yaitu: Tahap pertama
BAB IV TEMUAN DAN PEMBAHASAN Dalam pengembangan strategi pembelajaran intertekstual pada materi pokok kesetimbangan kimia secara garis besar penelitian terbagi dalam beberapa tahapan yaitu: Tahap pertama
PEMBAHASAN SOAL KIMIA KSM PROVINSI 2016 Oleh Urip Rukim (www.urip.info) JENJANG MADRASAH ALIYAH SELEKSI TINGKAT PROVINSI KOMPETISI SAINS MADRASAH
 PEMBAHASAN SOAL KIMIA KSM PROVINSI 2016 Oleh Urip Rukim (www.urip.info) JENJANG MADRASAH ALIYAH SELEKSI TINGKAT PROVINSI KOMPETISI SAINS MADRASAH TAHUN 2016 Soal diketik ulang oleh urip rukim (www.urip.info)
PEMBAHASAN SOAL KIMIA KSM PROVINSI 2016 Oleh Urip Rukim (www.urip.info) JENJANG MADRASAH ALIYAH SELEKSI TINGKAT PROVINSI KOMPETISI SAINS MADRASAH TAHUN 2016 Soal diketik ulang oleh urip rukim (www.urip.info)
Abdul Wahid Surhim 2014
 Abdul Wahid Surhim 2014 Kerangka Pembelajaran Persamaan Kimia Pola Reaktivitas Kimia Berat Atom dan Molekul Mol Rumus Empirik dari Analisis Informasi Kuantitatif dari Persamaan yang Disetarakan Membatasi
Abdul Wahid Surhim 2014 Kerangka Pembelajaran Persamaan Kimia Pola Reaktivitas Kimia Berat Atom dan Molekul Mol Rumus Empirik dari Analisis Informasi Kuantitatif dari Persamaan yang Disetarakan Membatasi
Reaksi kimia yang terjadi ketika memasak nasi?
 Reaksi kimia adalah suatu reaksi antar senyawa kimia atau unsur kimia yang melibatkan perubahan struktur dari molekul, yang umumnya berkaitan dengan pembentukan dan pemutusan ikatan kimia. Dalam suatu
Reaksi kimia adalah suatu reaksi antar senyawa kimia atau unsur kimia yang melibatkan perubahan struktur dari molekul, yang umumnya berkaitan dengan pembentukan dan pemutusan ikatan kimia. Dalam suatu
BAB IV HASIL PENELITIAN DAN PEMBAHASAN
 BAB IV HASIL PENELITIAN DAN PEMBAHASAN 4.1.Hasil Penelitian Pada dasarnya tujuan utama penelitian ini adalah untuk mengetahui kesulitan belajar siswa pada materi persamaan reaksi di Kelas X dan XI IPA
BAB IV HASIL PENELITIAN DAN PEMBAHASAN 4.1.Hasil Penelitian Pada dasarnya tujuan utama penelitian ini adalah untuk mengetahui kesulitan belajar siswa pada materi persamaan reaksi di Kelas X dan XI IPA
HUKUM DASAR KIMIA DAN PERHITUNGAN KIMIA
 HUKUM DASAR KIMIA DAN PERHITUNGAN KIMIA Mata Pelajaran : Kimia Kelas : X (Sepuluh) Nomor Modul : Kim.X.06 Penulis : Dorthy Hariandja, S.Pd. Penyunting Materi : Drs. Darsef, M.Si Penyunting Media : Drs.
HUKUM DASAR KIMIA DAN PERHITUNGAN KIMIA Mata Pelajaran : Kimia Kelas : X (Sepuluh) Nomor Modul : Kim.X.06 Penulis : Dorthy Hariandja, S.Pd. Penyunting Materi : Drs. Darsef, M.Si Penyunting Media : Drs.
Rumus Kimia. Mol unsur =
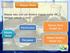 Rumus Kimia Menentukan Rumus Kimia Zat Rumus kimia zat dapat dibedakan menjadi rumus empiris dan rumus molekul. Rumus empiris dapat ditentukan dengan menghitung mol komponen penyusun zat dengan menggunakan
Rumus Kimia Menentukan Rumus Kimia Zat Rumus kimia zat dapat dibedakan menjadi rumus empiris dan rumus molekul. Rumus empiris dapat ditentukan dengan menghitung mol komponen penyusun zat dengan menggunakan
FAKULTAS TEKNIK UNIVERSITAS NEGERI YOGYAKARTA BAHAN AJAR KIMIA DASAR BAB IV STOIKIOMETRI
 No. BAK/TBB/SBG201 Revisi : 00 Tgl. 01 Mei 2008 Hal 1 dari 6 BAB IV STOIKIOMETRI A. HUKUM GAY LUSSAC Bila diukur pada suhu dan tekanan yang sama, volum gas yang bereaksi dan volum gas hasil reaksi berbanding
No. BAK/TBB/SBG201 Revisi : 00 Tgl. 01 Mei 2008 Hal 1 dari 6 BAB IV STOIKIOMETRI A. HUKUM GAY LUSSAC Bila diukur pada suhu dan tekanan yang sama, volum gas yang bereaksi dan volum gas hasil reaksi berbanding
 UJIAN MASUK BERSAMA (UMB) Mata Pelajaran : Kimia Tanggal : 07 Juni 009 Kode Soal : 9. Penamaan yang tepat untuk : CH CH CH CH CH CH OH CH CH adalah A. -etil-5-metil-6-heksanol B.,5-dimetil-1-heptanol C.
UJIAN MASUK BERSAMA (UMB) Mata Pelajaran : Kimia Tanggal : 07 Juni 009 Kode Soal : 9. Penamaan yang tepat untuk : CH CH CH CH CH CH OH CH CH adalah A. -etil-5-metil-6-heksanol B.,5-dimetil-1-heptanol C.
II. TINJAUAN PUSTAKA. Teori konstruktivistik dikembangkan oleh Piaget pada pertengahan abad 20.
 8 II. TINJAUAN PUSTAKA A. Pembelajaran Konstruktivisme Teori konstruktivistik dikembangkan oleh Piaget pada pertengahan abad 20. Piaget berpendapat bahwa pada dasarnya setiap individu sejak kecil sudah
8 II. TINJAUAN PUSTAKA A. Pembelajaran Konstruktivisme Teori konstruktivistik dikembangkan oleh Piaget pada pertengahan abad 20. Piaget berpendapat bahwa pada dasarnya setiap individu sejak kecil sudah
BAB III STOIKIOMETRI
 BAB III STOIKIOMETRI A. Standar Kompetensi: Memahami tentang ilmu kimia dan dasar-dasarnya serta mampu menerapkannya dalam kehidupan se-hari-hari terutama yang berhubungan langsung dengan kehidupan. B.
BAB III STOIKIOMETRI A. Standar Kompetensi: Memahami tentang ilmu kimia dan dasar-dasarnya serta mampu menerapkannya dalam kehidupan se-hari-hari terutama yang berhubungan langsung dengan kehidupan. B.
