WRAP UP SKENARIO 3 DIARE
|
|
|
- Benny Lesmana
- 7 tahun lalu
- Tontonan:
Transkripsi
1 WRAP UP SKENARIO 3 DIARE Disusun oleh: KELOMPOK A-1 KETUA : ANISA NURJANAH SEKRETARIS: ANGGIE ELKA PRATIWI ANGGOTA ( ) ( ) : ABDUL RAHMAN ( ) ABI RAFDI ZHAFARI ( ) ABIYYA FARAH PUTRI ( ) ADELIA PUTRI SABRINA ( ) ADELINA ANNISA PERMATA ( ) ANDINI ZULMAETA ( ) ANDREW ROZAAN F ( ) AURYN ZHAFIRI ( ) FAKULTAS KEDOKTERAN UNIVERSITAS YARSI 2013/2014 0
2 Skenario : DIARE Seorang mahasiswa, 35 tahun, dibawa ke Puskesmas karena mengalami mencret lebih dari 12 kali dalam sehari sejak 2 hari yang lalu. Keluhan ini timbul setelah makan di warung nasi dekat kampusnya. Pemeriksaan fisik : kesadaran komposmentis lemah, urine sedikit. Di Puskesmas penderita dipasang infuse dan diberikan pertolongan pertama lalu dirujuk ke RS terdekat. Dokter meminta untuk diperiksa Analisa Gas Darah. Kesannya : terdapat gangguan keseimbangan asam basa berupa asidosis metabolic, dengan anion gap yang normal. 1
3 A. Brainstroming / Activation Prior Knowledge : 1. Mengapa dokter meminta untuk melakukan analisis gas darah? 2. Kenapa pada penderita diare denyut nadi naik, pernapasan naik dan tekanan darah menurun? 3. Apa hubungan asidosis metabolic dengan diare? 4. Berapakah kadar normal anion gap? 5. Mengapa anion gap menjadi indicator dalam pemeriksaan? 6. Apa saja gangguan keseimbangan asam basa? 7. Kenapa urine yang keluar sedikit? 8. Bagaimana terjadinya diare? A. Jawaban: 1. untuk mengukur keasaman ph, kadar oksigen dan CO2 dalam darah dan untuk mengetahui keseimbangan asam basa dalam tubuh. 2. tekanan darah = karena volume cairan tubuh berkurang sehingga tekanan darah menurun akibat pengeluaran cairan berlebihan Nadi = karena kekurangan cairan tubuh jantung dan paru memompa lebih cepat untuk menyeimbangkan tubuh sehingga nadi dan pernapasan meningkat. 3. karena bikarbonat keluar lebih banyak sehingga H+ tidak bias berikatan dengan HCO3 menyebabkan ph darah menurun dan H+ meningkat mmol/l 5. karena untuk mengetahui perbedaan antara jumlah muatan ion positif pada Na+ dan jumlah muatan ion negative pada Cl- dan HCO36. - asidosis metabolik - alkalosis metabolik - asidosis respiratorik - alkalosis respiratorik 7. karena sekresi ADH meningkat sehingga urine yang keluar sedikit untuk menyeimbangkan kesetimbangan cairan 8. karena makanan yang mengandung bakteri sehingga usus tidak melakukan absorbsi air melainkan sekresi air untuk mengencerkan kadar toksin yang ada dalam usus besar A. Hipotesa Makanan yang mengandung bakteri, virus dll dapat menyebabkan absorbsi air di usus sehingga terjadi diare karena pengeluaran HCO3 yang berlebihan menyebabkan gangguan keseimbangan asam basa yaitu asidosis metabolik. 2
4 B. Learning Objective / Sasaran belajar : 1. Memahami dan Menjelaskan Keseimbangan Asam Basa 1.1 Definisi 1.2 Klasifikasi 1.3 Fungsi 1.4 Mekanisme 1.5 Indikator 1.6 Fisiologis 2. Memahami dan Menjelaskan ukuran keasaman ph 2.1 Definisi 2.2 Cara Menentukan ph 2.3 Penyebab Perubahan ph 3. Memahami dan Menjelaskan Asidosis Metabolik 3.1 Definisi 3.2 Etiologi 3.3 Mekanisme 3.4 Gejala 3.5 Pemeriksaan Analisa Gas Darah 3.6 Diagnosis 3.7 Penatalaksanaan 3.8 Kompensasi 4. Memahami dan menjelaskan Alkalosis Metabolik 4.1 Definisi 4.2 Etiologi 4.3 Manifestasi 4.4 Kompensasi LI 1. Memahami dan Menjelaskan tentang Keseimbangan Asam Basa LO 1.1 Definisi Menurut Arrhenius 3
5 - Asam adalah zat yang terdisosiasi dalam air membentuk H+ Basa adalah zat yang tedisosisasi dalam air membentuk OH- Menurut Bronsted dan lowry - Asam adalah zat yang dapat memberikan ion H ke zat lain (disebut sebagai donor proton). - Basa adalah zat yang dapat menerima ion H dari zat yang lain (disebut sebagai akseptor proton). Menurut konsep dari G.N Lewis - Asam adalah suatu zat yang menerima sebuah pasangan elektron. - Basa adalah suatu zat yang memberikan sepasang electron. LO 1.2 Klasifikasi Berdasarkan kemampuan melepas H+ 1. Asam lemah Adalah asam yang hanya terdisosiasi sebagian dalam air (berdisodiasi tidak sempurna). 2. Asam kuat Adalah asam yang berdisosiasi sempurna dalam air. 3. Basa lemah Adalah basa yang hanya terdisosiasi sebagian dalam air/suatu persenyawaan yang bergabung tidak sempurna dengan ion hidrogen dalam larutan air. 4. Basa kuat Adalah persenyawaan yang berdisosiasi secara sempurna dalam larutan air. Berdasarkan bentuk ion 1. Asam anion Asam yang mempunyai muatan negatif. Misalnya : H2SO4 dan SO3 2. Asam kation Asam yang mempunyai muatan positif. Misalnya : NH4 dan H3O 3. Basa anion Basa yang mempunyai muatan negative. Misalnya : CL dan CN 4. Basa kation Basa yang mempunyai muatan positif. LO 1.3 Fungsi Mempengaruhi aktifitas reaksi enzimatik Mempengaruhi permeabilitas sel Mempengaruhi struktur sel 4
6 Memepengaruhi sifat-sifat dan fungsi dari sistem biologis LO 1.4 Mekanisme Mekanisme untuk mengendalikan keseimbangan asam basa darah : 1.Kelebihan asam dibuang oleh ginjal, sebagian besar dalam bentuk ammonia. Ginjal memiliki kemampuan untuk merubah jumlah asam atau basa yang dibuang, yang biasanya berlangsung beberapa hari. 2.Tubuh menggunakan penyangga ph (buffer) dalam darah sebagai pelindung terhadap perubahan yang terjadi secara tiba-tiba dalam ph darah. Penyangga ph yang paling penting dalam darah menggunakan bikarbonat. Bikarbonat ( suatu komponen basa ) berada dalam kesetimbangan dengan karbondioksida ( suatu komponen asam ). Jika lebih banyak asam yang masuk ke dalam aliran darah, maka akan dihasilkan lebih banyak bikarbonat dan lebih sedikit karbondioksida. Jika lebih banyak basa yang masuk kedalam aliran darah, maka akan dihasilkan lebih banyak karbondioksida dan lebih sedikit bikarbonat. 3.Pembuangan karbondioksidajika pernafasan meningkat, kadar karbondioksida darah menurun dan darah menjadi lebih basa. Jika pernafasan menurun, kadar karbondioksida darah menigkat dan darah menjadi lebih asam. LO 1.5 Indikator larutan indikator adalah zat-zat yang mempunyai warna berbeda dalam larutan yang bersifat asam, basa, dan netral, sehingga dapat digunakan untuik membedakan larutan yang bersifat asam, basa, dan netral. Larutan indikator akan berubah warna jika PH (derajat keasaman) berubah. Pada suhu 25 derajat celcius maka ph + poh = 14, untuk larutan netral ph = poh = 7, sedangkan untuk larutan asam ph lebih kecil 7 dan larutan basa lebih besar 7. Jadi, ph merupakan ukuran konsentrasi ion hidrogen atau ukuran keasaman larutan. Ada dua macam indikator, yaitu: Indikator penunjuk asam adalah indikator yang akan berubah warnanya, jika konsentrasi asam berubah sedikit saja. Daerah perubahan warna untuk indikator ini kurang dari 7. Indikator penunjuk basa adalah indikator yang akan berubah warnanya, jika konsentrasi basa (OH) berubah sedikit saja. Daerah perubahan warnanya lebih dari 7. Di laboratorium, indikator yang sering digunakan adalah larutan fenolftalein (PP), metil merah, dan metil orange. 5
7 Table beberapa indicator Asam-Basa yang lazim Warna Indikator Dalam Asam Dalam Basa Kisaran ph Timol biru merah Kuning 1,2-2,8 Bromofenol biru Kuning Ungu kebiruan 3,0-4,6 Metil jingga Jingga Kuning 3,1-4,4 Metil merah Merah Kuning 4,2-6,3 Klorofenol biru Kuning Merah 4,8-6,4 Bromotimol biru Kuning Biru 6,0-7,6 Kresol merah Kuning Merah 7,2-8,8 fenolftalein Tidak berwarna Pink kemerahan 8,3-10,0 *kisaran ph didefinisikan sebagai kisaran di mana indicator berubah dari warna asam ke warna basa LO 1.6 Fisiologis Keseimbangan asam basa adalah keseimbangan ion hidrogen, keseimbangan antara ion [ ] bebas dan [HC ion [ ] dalam cairan tubuh sehingga keseimbangan tubuh yang harus dijaga kadar ] bebas dalam batas normal maupun pembentukan asam maupun basa terus berlangsung dalam kehidupan. ph darah normal adalah asam adalah ph dibawah 7.3 dan basa adalah ph di atas 7.5.pH harus tetap dipertahankan,walaupun banyak senyawa-senyawa metabolit atau nutrien yang bersifat mengganggu nilai tersebut.gangguan ke arah keasaman (asidosis) ph kurang dari 7.3 atau ke arah kebasaan (alkalosis) ph diatas 7.5.Gangguan dapat dipulihkan ke keadaan semula oleh alat kompensasi tubuh. Karena ion [H+] berpengaruh besar dalam keseimbangan asam-basa, maka faktor yang mempengaruhi [H+] juga mempengaruhi keseimbangan asam basa, yaitu : A. Lebihnya kadar [H+] yang ada dalam cairan tubuh, berasal dari Pembentukan yang sebagian berdisosiasi menjadi H+ dan 6
8 Katabolisme zat organik Disosiasi asam organik pada metabolisme intermedik, contoh pada metabolik lemak terbentuk asam lemak dan laktat yaitu melepaskan [H+] B. Keseimbangan intake dan output ion [H+] tubuh Bervariasi tergantung dari: Diet ( makanan ), H+ naik, jika kebanyakan makan asam (asidosis), sedangkan dengan mengkonsumsi sayur dan buah bersifat basa banyak menghasilkan. Aktivitas yaitu lari cepat membuat tubuh kita asam karena menghasilkan banyak CO2 sehingga ph turun. Proses anaerob yaitu lebih banyak penumpukan asam laktat seperti olahraga berat sehingga menimbulkan reaksi asam dan membuat ph turun. LI 2. Memahami dan menjelaskan ukuran keasaman ph LO 2.1 Definisi Simbol yang berhubungan dengan konsentrasi hidrogen ] atau aktivitas larutan dibandingkan larutan standar yang diberikan. Secara numeric, ph kira-kira sama dengan logaritma negative konsentrasi yang dinyatakan dalma molaritas, ph 7 merupakan keadaan netral; di atas 7 terjadi peningkatan alkalinitas sedangkan dibawah 7 dan peningkatan keasaman (asiditas). LO 2.2 Cara menentukan ph PH adalah konsentrasi ion hidrogen (hydronium) yang dapat dinyatakan dengan ph = log 1 = -log[h+] [H+] = -log [HCO3-] Selain itu menurut persamaan Henderson-Hasselbach PH dihitung dengan rumus : ph = pka + log [garam]/[asam] atau ph = pk + log [HCO3-]/[H2CO3] dimana : Pk = konstanta disosiasi asam karbonat =6,1 [HCO3] = kadar bikarbonat plasma 7
9 [H2CO3] = kadar asam karbonat plasma PH = pk + log [HCO3]/S X PCO2 S = konstan kelarutan CO2 dengan nilai sebesar 0.03 LO 2.3 Penyebab perubahan ph Beban makanan dan beban metabolic Ion hydrogen di tambahkan atau di kurangi sebagai akibat makan-makanan tertentu atau akibat perubahan metabolic Beban respirasi Peningkatan laju pernafasan yang tidak di sertai peningkatan aliran CO2 ke paruparu akan mengurangi tekanan Co2 dalam alveoli. begitu juga pada darah yang kembali menuju ke jaringan perifer sehingga terjadi akibat respiratorik à H+ menurun PH meningkat LI 3. Memahami dan Menjelaskan Asidosis Metabolik LO 3.1 Definisi Asidosis Metabolik Asidosis Metabolik adalah penurunan kadar ion HCO3- diikuti dengan penurunan tekanan parsial CO2 didalam arteri (Gangguan Keseimbangan Asam basa, FKUI) Asidosis Metabolik adalah gangguan sistemik yang ditandai dengan penurunan primer kadar bikarbonat plasma sehingga menyebabkan terjadinya penurunan ph yaitu peningkatan [H+] (Price. Wilson.2006.Patofisiologi) Asidosis Metabolik yang disebut juga Asidosis Non-Respiratori adalah keadaan asidosis yang status asam basa tubuhnya bergeser ke sisi asam akibat kehilangan basa atau retensi asam selain asam karbonat. (Kamus Dorland) LO 3.2 Etiologi asidosis metabolik Penyebab asidosis metabolik dapat dibagi dalam tiga kelompok yaitu : 1. Pembentukan asam yang berlebhan di dalam tubuh. Ion hidrogen dibebaskan oleh sistem buffer asam karbonat-bikarbonat, sehingga terjadi penurunan ph. Dalam klinik ditemukan keadaan ini seperti pada: - Asidosis laktat. Timbul karena hipoksia jaringan berkepanjangan, mengakibatkan jaringan mengalami proses metabolisme anaerob. - Ketoasidosis. Timbul karena produksi badan keton dalam jumlah sangat tinggi pada metabolisme fase pasca absortif. Ketoasidosis merupakan akibat dari starvasi dan 8
10 komplikasi diabetes mellitus yang tidak terkendali, jaringan tidak dapat memanfaatkan glukosa dari sirkulasi, sehingga mengandalkan metabolisme lipid dan keton - Intoksikasi salisat - Intoksikasi etanol 2. Berkurangnya kadar ion-hco3 didalam tubuh Sistem buffer asam karbonat-bikarbonat yang mengatur keseimbangan ion hidrogen dan mempengaruhi keseimbangan ph. Penurunan konsentrasi HCO3 di cairan ekstraseluler menyebabkan penurunan efektifitas sistem buffer dan asidosis timbul. Penyebab penurunan konsentrasi HCO3 anatara lain adalah diare, renal tubular acidosis (RTA ), pemakaian obat inhibitor enzime anhidrase karbonat atau pada penyakit ginjal kronik stadium III-IV 3. Adanya rentesi ion-h dalam tubuh Jaringan tidak mampu ekskresi ion hidrogen melalui ginjal. Ini terjadi pada penyakit ginjal kronik stadium IV-V, RTA-1 atau RTA-4 LO 3.3 Mekanisme Asidosis Metabolik Asidosis Metabolik (juga dikenal sebagai asidosis non respiratorik ) mencakup semua jenis asidosis selain yang disebabkan oleh kelebihan dicairan tubuh. Pada keadaan tak terkompensasi (gambar 15-12), asidosis metabolik selalu ditandai oleh penurunan (dalam contoh kita menjadi separuhnya), sementara [ plasma ] normal sehingga terbentuk rasio asidotik 10/1. Masalah dapt timbul karena pengeluaran cairan kaya tubuh/karena akumulasi asam nonkarbonat. Pada kasus yang terakhir, yang berlebihan dari plasma. 9
11 Asidosis Metabolik adalah keasaman darah yang berlebihan, yang ditandai dengan rendahnya kadar bikarbonat dalam darah. Asidosis dapat terjadi jika diare. Bila peningkatan keasaman melampaui system penyangga ph, darah akan menjadi asam. Seiring dengan menurunnya ph darah, eprnapasan menjadi lebih salam dan lebih cepat sebagai usaha tubuh untuj menurunkan kelebihan asam dalam darah dengan cara menurunkan jumlah CO2. Jika kita makan, saluran pencernaan seperti lambung, usus dsb akan menghasilkan HCO 3. Nanti HCO3 akan diserap oleh plasma yang akan dieksresi bersama urin. Tetapi jika terjadi diare, HCO3 akan banyak keluar bersama feses. Karena diare tidak terjadi absorbsi pada usus. Diare dapat disebabkan oleh infeksi, alergi, virus serta bakteri. Sehingga HCO 3 dalam plasma akan 10
12 terjadi penurunan besar-besaran karena keluar bersama feses. Sedangkan jika HCO3 berkurang, H+ tidak dapat diikat. Karena HCO3 berperan sebagi buffer bagi H+ agar tidak kelebihan asam dalam tubuh. Karena penurunan HCO3 akan menyebabkan kenaikan H+ dalam tubuh lalu ph akan turun, HCO3 turun, tetapi H+ naik sehingga tubuh menjadi asam. Maka terjadilah Asidosis Metabolik. LO 3.4 Gejala Asidosis Metabolik Mual Muntah Kelelahan Pernapasan menjadi lebih dalam atau sedikit lebih cepat (pernafasan kussmaul s); Rasa mengantuk Mengalami kebingungan Tekanan darah menurun, menyebabkan syok, koma dan kematian LO 3.5 Pemeriksaan (AGD) Pemeriksaan Diagnostik 1. Nilai-nilai AGD: menentukan ph (biasanya, 7,35) dan derajat kompensasi respiratori seperti dilihatkan oleh PaC, yang biasanya adalah < 35 mmhg. 2. Bikarbonat serum: menentukan adanya asidosis metabolik ( < 22 meq/l). 3. Elektrolit serum: mungkin terjadi peningkatan kalium Karena pertukaran kalium intrasellular dari ion-ion hydrogen dalam usaha tubuh untuk menormalkan lingkungan asam-basa. Anion Gap: dalam usaha untuk mengidentifikasi penyebab asidosis metabolik, penganalisaan elektrolit serum untuk mendeteksi anion gap mungkin sangat membantu. Anion gap mencerminkan adanya anion yang tak terukur dalam plasma dan dihitung dengan mengurangi penjumlahan klorida dan natrium bikarbonat dengan jumlah konsentrasi natrium plasma. Anion Gap = minus ( + 4. EKG: mendeteksi distrima yang disebabkan oleh hyperkalemia. Perubahan yang tampak pada hyperkalemia termasuk memuncaknya gelombang T, penurunan segmen ST, penurunan ukuran gelombang R, menurun atau tidak terdapatnya gelombang P, dan pelebaran kompleks QRS, asidosis dapat menyebabkan perubahan ECG yang tidak spesifik. LO 3.6 Diagnosis Asidosis metabolic akut dapat menyebabkan : 1. depresi miokardial disertai reduksi cardiac output (curah jantung) 11
13 penurunan tekanan darah, penurunan aliran ke sirkulasi hepatic dan renal menyebabkan aritmia dan fibrillasi ventricular metabolism otak menurun secara progresif pada ph yang lebih dari 7,1 akan menyebabkan fatigue (rasa lelah), sesak napas, nyeri perut, nyeri tulang, dan mual/muntah 7. pada ph kurang atau sama dengan 7,1 akan menyebabkan inotropic negative, aritmia, konstriksi vena perifer, dilatasi arteri perifer, penurunan tekanan darah, penurunan aliran darah ke hati, kontriksi pembuluh darah paru (pertukaran oksigen terganggu) Diagnosis asidosis metabolic ditegakkan berdasarkan gambaran klinis dan dipastikan oleh hasil pemeriksaan laboratorium yaitu ph, PaCO2, dan HCO3 dengan menggunakan pendekatan sistematik. Hasil pemeriksaan menunjukkan : ph : <7,35 HCO3 : <22 meq/l PaCO2 : <40 mmhg LO 3.7 Penatalaksanaan Tujuan penanganan asidosis metabolic adalah untuk meningkatkan ph sistemik sampai ke batas aman, dan mengobati penyebab asidosis yang mendasari. Langkah koreksi asidosis metabolic : 1. Langkah pertama, tetapkan berat ringannya gangguan asidosis. Gangguan disebut letal bila ph darah kurang dari 7 atau kadar ion H lebih dari 100 nmol/l. gangguan yang perlu mendapat perhatian bila ph darah 7,1-7,3 atau kadar ion H antara nmol/l. 2. Langkah kedua, tetapkan anion gap atau bila perlu anion gap urin untuk mengetahui dugaan etiologi asidosis metabolic. Dengan bantuan gejala klinis lain dapat dengan mudah ditetapkan etiologinya. 3. Langkah ketiga, bila dicurigai kemungkinan asidosis laktat, hitung rasio delta anion gap dengan delta HCO3 (delta anion gap : anion gap pada saat pasien diperiksa dikurangi dengan median anion gap normal, delta HCO3: kadar HCO3 normal dikurangi dengan kadar HCO3 pada saat pasien diperiksa). Bila rasio lebih dari 1, asidosis disebabkan oleh asidosis laktat. Langkah ini menetapkan sampai sejauh mana koreksi dapat dilakukan. LO 3.8 Kompensasi Asidosis Metabolik 12
14 Kecuali pada asidosis uremik, asidosis metabolic dikompensasi oleh mekanisme pernapasan dan ginjal serta dapar kimiawi. Penyangga menyerap kelebihan H+ Paru mengeluarkan lebih banyak CO2 penghasil H+ Ginjal mengeksresikan H+ lebih banyak dan menahan HCO3- lebih banyak. Dalam mengompensasi asidosis metabolik, paru secara sengaja menggeser CO 2 dari normal dalam upaya memulihkan H+ kearah normal. Sementara pada gangguan asam basa yang disebabkan oleh faktor pernapasan kelainan CO2 adalah penyebab ketidakseimbangan H+, pada gangguan asam basa metabolic CO2 secara sengaja digeser dari normal sebagai kompensasi penting untuk ketidakseimbangan H+. LI 4. Memahami dan menjelaskan Alkalosis Metabolik LO 4.1 Definisi Alkalosis metabolik (kelebihan HCO3-) adalah suatu gangguan sistemik yang dicirikan dengan adanya peningkatan primer kadar HCO3- plasma, sehingga menyebabkan peningkatan ph (penurunan [H+]. [HCO3-] ECF lebih besar dari 26 meq/l dan ph lebih besar dari Alkalosis metabolik sering disertai dengan berkurangnya volume ECF dan hipokalemia. LO 4.2 Etiologi - Kekurangan H+ dari ECF (Muntah,penyedotan nasogastrik, diare dengan kehilangan klorida, diuretik, hipokalemia) - Retensi HCO3- (Pemberian natrium bikarbonat berlebihan, sindrom susu alkali) LO 4.3 Manifestasi Tidak terdapat gejala dan tanda alkalosis metabolik yang spesifik. Adanya gangguan ini harus dicurigai pada pasien yang memiliki riwayat muntah, penyedotan, nasogastrik, pengobatan diuretik atau pasien yang baru sembuh dari gagal nafas (Hiperkapnia) LO 4.4 Kompensasi Alkalosis Metabolik Kompensasi utamanya adalah penurunan ventilasi, yang meningkatkan PaCO2 dan peningkatan ekskresi HCO3 oleh ginjal, yang membantu mengkompensasi peningkatan awal konsentrasi HCO3 cairan ekstrasel. DAFTAR PUSTAKA (zenius.net) (Madjid.2008 Gangguan keseimbangan cairan elektrolit asam basa FKUI) 13
15 (Horne, Mima M Keseimbangan Cairan, Elektrolit, dan Asam-basa. Jakarta:EGC) (Kee, Joyce LeFever. Pemeriksaan Laboratorium & Diagnostik. Jakarta: EGC) (Danis, Difa. Kamus Istilah Kedokteran.Gitamedia press) (Guyton, 1996) (Price. Wilson.2006.Patofisiologi) (Chang, Raymond. Kimia Dasar. Erlangga) (Fay, McMurry Chemistry. New Jersey) (Sherwood, Lauralee. Fisiologi Manusia Dari sel ke Sistem. EGC) ( Corwin, Elizabeth J Buku Saku Patofisiologi. Jakarta:EGC) 14
Reaksi keseluruhannya :
 LI 1. Memahami dan Mengetahui Tentang Asam-Basa LO 1.1 Definisi Asam-Basa Definisi asam-basa menurut Arrhenius Menurut Arrhenius pada tahun 1903, asam adalah zat yang dalam air dapat menghasilkan ion hidrogen
LI 1. Memahami dan Mengetahui Tentang Asam-Basa LO 1.1 Definisi Asam-Basa Definisi asam-basa menurut Arrhenius Menurut Arrhenius pada tahun 1903, asam adalah zat yang dalam air dapat menghasilkan ion hidrogen
Kesetimbangan asam basa tubuh
 Kesetimbangan asam basa tubuh dr. Syazili Mustofa, M.Biomed Departemen Biokimia, Biologi Molekuler dan Fisiologi Fakultas Kedokteran Universitas Lampung ph normal darah Dipertahankan oleh sistem pernafasan
Kesetimbangan asam basa tubuh dr. Syazili Mustofa, M.Biomed Departemen Biokimia, Biologi Molekuler dan Fisiologi Fakultas Kedokteran Universitas Lampung ph normal darah Dipertahankan oleh sistem pernafasan
SEKOLAH TINGGI ILMU KESEHATAN NASIONAL TAHUN
 ASIDOSIS METABOLIK Disusun oleh: Desi (A101.19.006) Dewi Sekar (A101.19.007) Dina Fitri Astuti (A101.19.008) Ela Kusumawati (A101.19.009) Fatoni Aditya O (A101.19.010) Febriana Ramadhani (A101.19.011)
ASIDOSIS METABOLIK Disusun oleh: Desi (A101.19.006) Dewi Sekar (A101.19.007) Dina Fitri Astuti (A101.19.008) Ela Kusumawati (A101.19.009) Fatoni Aditya O (A101.19.010) Febriana Ramadhani (A101.19.011)
KESEIMBANGAN ASAM- BASA. dr.sudarno
 KESEIMBANGAN ASAM- BASA dr.sudarno KESEIMBANGAN ASAM BASA Afinitas Hb terhadap O 2 terutama dikendalikan oleh ph darah ph darah (arterial) : 7,4 (7,35-7,45) Sistem yang berperan mempertahankan ph darah:
KESEIMBANGAN ASAM- BASA dr.sudarno KESEIMBANGAN ASAM BASA Afinitas Hb terhadap O 2 terutama dikendalikan oleh ph darah ph darah (arterial) : 7,4 (7,35-7,45) Sistem yang berperan mempertahankan ph darah:
2
 Keseimbangan Asam Basa Dr. OK.M. Syahputra, M.Kes Dr. Almaycano Ginting, M.Kes Departemen Biokimia FK USU KESEIMBANGAN ASAM BASA Pengertian ph Defanisi ph -log (H + ) Untuk menghitung ph larutan : 1.Hitung
Keseimbangan Asam Basa Dr. OK.M. Syahputra, M.Kes Dr. Almaycano Ginting, M.Kes Departemen Biokimia FK USU KESEIMBANGAN ASAM BASA Pengertian ph Defanisi ph -log (H + ) Untuk menghitung ph larutan : 1.Hitung
BAB 2 TINJAUAN PUSTAKA. Pemberian cairan diperlukan karena gangguan dalam keseimbangan cairan dan
 BAB 2 TINJAUAN PUSTAKA 2.1. Terapi cairan Pemberian cairan bertujuan untuk memulihkan volume sirkulasi darah. 6,13 Pemberian cairan diperlukan karena gangguan dalam keseimbangan cairan dan elektrolit merupakan
BAB 2 TINJAUAN PUSTAKA 2.1. Terapi cairan Pemberian cairan bertujuan untuk memulihkan volume sirkulasi darah. 6,13 Pemberian cairan diperlukan karena gangguan dalam keseimbangan cairan dan elektrolit merupakan
Interpretasi Hasil Analisa Gas Darah dan Peranannya Dalam Penilaian Pasien- Pasien Kritis
 Interpretasi Hasil Analisa Gas Darah dan Peranannya Dalam Penilaian Pasien- Pasien Kritis Analisa gas darah merupakan salah satu alat diagnosis dan penatalaksanaan penting bagi pasien untuk mengetahui
Interpretasi Hasil Analisa Gas Darah dan Peranannya Dalam Penilaian Pasien- Pasien Kritis Analisa gas darah merupakan salah satu alat diagnosis dan penatalaksanaan penting bagi pasien untuk mengetahui
KESEIMBANGAN ASAM BASA Pengertian ph Definisi ph -log (H + ) Untuk menghitung ph larutan : 1.Hitung konsentrasi ion Hidrogen (H + ) 2.Hitung logaritma
 Keseimbangan Asam Basa Dr. OK.M. Syahputra, M.kes Dr. Almaycano Ginting Departemen Biokimia FK USU KESEIMBANGAN ASAM BASA Pengertian ph Definisi ph -log (H + ) Untuk menghitung ph larutan : 1.Hitung konsentrasi
Keseimbangan Asam Basa Dr. OK.M. Syahputra, M.kes Dr. Almaycano Ginting Departemen Biokimia FK USU KESEIMBANGAN ASAM BASA Pengertian ph Definisi ph -log (H + ) Untuk menghitung ph larutan : 1.Hitung konsentrasi
respiratorik adalah alkalosis metabolic, sedangkan kompensasi dari alkalosis respiratorik adalah asidosis metabolic dan demikian juga sebaliknya.
 BAB I PENDAHULUAN Keseimbangan asam basa adalah homeostasis dari kadar ion hydrogen ([H + ]). Pada cairan tubuh asam terus menerus diproduksi dalam metabolisme yang normal. Meskipun terbentuk banyak asam
BAB I PENDAHULUAN Keseimbangan asam basa adalah homeostasis dari kadar ion hydrogen ([H + ]). Pada cairan tubuh asam terus menerus diproduksi dalam metabolisme yang normal. Meskipun terbentuk banyak asam
FUNGSI SISTEM GINJAL DALAM HOMEOSTASIS ph
 FUNGSI SISTEM GINJAL DALAM HOMEOSTASIS ph Dr. MUTIARA INDAH SARI NIP: 132 296 973 2007 DAFTAR ISI I. PENDAHULUAN.......... 1 II. ASAM BASA DEFINISI dan ARTINYA............ 2 III. PENGATURAN KESEIMBANGAN
FUNGSI SISTEM GINJAL DALAM HOMEOSTASIS ph Dr. MUTIARA INDAH SARI NIP: 132 296 973 2007 DAFTAR ISI I. PENDAHULUAN.......... 1 II. ASAM BASA DEFINISI dan ARTINYA............ 2 III. PENGATURAN KESEIMBANGAN
LARUTAN PENYANGGA (BUFFER) Disusun Oleh: Diah Tria Agustina ( ) JURUSAN KIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
 HANDOUT klik di sini LARUTAN PENYANGGA (BUFFER) Disusun Oleh: Diah Tria Agustina (4301414032) JURUSAN KIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS NEGERI SEMARANG 2016 PENGERTIAN LARUTAN
HANDOUT klik di sini LARUTAN PENYANGGA (BUFFER) Disusun Oleh: Diah Tria Agustina (4301414032) JURUSAN KIMIA FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS NEGERI SEMARANG 2016 PENGERTIAN LARUTAN
LARUTAN ASAM-BASA DAN LARUTAN PENYANGGA
 LARUTAN ASAM-BASA DAN LARUTAN PENYANGGA A. Pengertian Larutan Penyangga Larutan penyangga biasa disebut juga dengan larutan Buffer atau larutan Dapar. Dimana larutan penyangga merupakan larutan yang mampu
LARUTAN ASAM-BASA DAN LARUTAN PENYANGGA A. Pengertian Larutan Penyangga Larutan penyangga biasa disebut juga dengan larutan Buffer atau larutan Dapar. Dimana larutan penyangga merupakan larutan yang mampu
LARUTAN PENYANGGA (BUFFER)
 LARUTAN PENYANGGA (BUFFER) Larutan penyangga Larutan penyangga atau larutan buffer adalah larutan yang ph-nya praktis tidak berubah walaupun kepadanya ditambahkan sedikit asam, sedikit basa, atau bila
LARUTAN PENYANGGA (BUFFER) Larutan penyangga Larutan penyangga atau larutan buffer adalah larutan yang ph-nya praktis tidak berubah walaupun kepadanya ditambahkan sedikit asam, sedikit basa, atau bila
VII. KESEIMBANGAN ASAM BASA
 VII. KESEIMBANGAN ASAM BASA Mohammad Hanafi, MBBS (Syd)., dr., MS. 1.Pendahuluan Untuk mempelajari keseimbangan asam basa, diperlukan pengertian tentang air, asam, basa dan mekanisme kompensasi tubuh untuk
VII. KESEIMBANGAN ASAM BASA Mohammad Hanafi, MBBS (Syd)., dr., MS. 1.Pendahuluan Untuk mempelajari keseimbangan asam basa, diperlukan pengertian tentang air, asam, basa dan mekanisme kompensasi tubuh untuk
PETA KONSEP. Larutan Penyangga. Larutan Penyangga Basa. Larutan Penyangga Asam. Asam konjugasi. Basa lemah. Asam lemah. Basa konjugasi.
 PETA KONSEP Larutan Penyangga mempertahankan berupa ph Larutan Penyangga Asam mengandung Larutan Penyangga Basa mengandung Asam lemah Basa konjugasi Asam konjugasi Basa lemah contoh contoh contoh contoh
PETA KONSEP Larutan Penyangga mempertahankan berupa ph Larutan Penyangga Asam mengandung Larutan Penyangga Basa mengandung Asam lemah Basa konjugasi Asam konjugasi Basa lemah contoh contoh contoh contoh
SOP TINDAKAN ANALISA GAS DARAH (AGD)
 SOP TINDAKAN ANALISA GAS DARAH (AGD) 1. Analisa Gas Darah Gas darah arteri memungkinkan utnuk pengukuran ph (dan juga keseimbangan asam basa), oksigenasi, kadar karbondioksida, kadar bikarbonat, saturasi
SOP TINDAKAN ANALISA GAS DARAH (AGD) 1. Analisa Gas Darah Gas darah arteri memungkinkan utnuk pengukuran ph (dan juga keseimbangan asam basa), oksigenasi, kadar karbondioksida, kadar bikarbonat, saturasi
PELATIHAN NEFROLOGI MEET THE PROFESSOR OF PEDIATRICS. TOPIK: Tata laksana Acute Kidney Injury (AKI)
 PELATIHAN NEFROLOGI MEET THE PROFESSOR OF PEDIATRICS TOPIK: Tata laksana Acute Kidney Injury (AKI) Pembicara/ Fasilitator: DR. Dr. Dedi Rachmadi, SpA(K), M.Kes Tanggal 15-16 JUNI 2013 Continuing Professional
PELATIHAN NEFROLOGI MEET THE PROFESSOR OF PEDIATRICS TOPIK: Tata laksana Acute Kidney Injury (AKI) Pembicara/ Fasilitator: DR. Dr. Dedi Rachmadi, SpA(K), M.Kes Tanggal 15-16 JUNI 2013 Continuing Professional
Hubungan Hipertensi dan Diabetes Melitus terhadap Gagal Ginjal Kronik
 Hubungan Hipertensi dan Diabetes Melitus terhadap Gagal Ginjal Kronik Latar Belakang Masalah Gagal ginjal kronik merupakan keadaan klinis kerusakan ginjal yang progresif dan irreversibel yang berasal dari
Hubungan Hipertensi dan Diabetes Melitus terhadap Gagal Ginjal Kronik Latar Belakang Masalah Gagal ginjal kronik merupakan keadaan klinis kerusakan ginjal yang progresif dan irreversibel yang berasal dari
KESEIMBANGAN ASAM BASA
 KESEIMBANGAN ASAM BASA Oleh: Putu Aksa Viswanatha dr. Kadek Agus Heryana Putra,SpAn BAGIAN/SMF ILMU ANESTESIA DAN TERAPI INTESIF FK UNUD/RSUP SANGLAH 2017 DAFTAR ISI Halaman HALAMAN JUDUL... KATA PENGANTAR...
KESEIMBANGAN ASAM BASA Oleh: Putu Aksa Viswanatha dr. Kadek Agus Heryana Putra,SpAn BAGIAN/SMF ILMU ANESTESIA DAN TERAPI INTESIF FK UNUD/RSUP SANGLAH 2017 DAFTAR ISI Halaman HALAMAN JUDUL... KATA PENGANTAR...
ASIDOSIS RESPIRATORIK
 ASIDOSIS RESPIRATORIK A. PENGERTIAN. Asidosis Respiratorik (Kelebihan Asam Karbonat). 1. Asidosis Respiratorik adalah gangguan klinis dimana PH kurang dari 7,35 dan tekanan parsial karbondioksida arteri
ASIDOSIS RESPIRATORIK A. PENGERTIAN. Asidosis Respiratorik (Kelebihan Asam Karbonat). 1. Asidosis Respiratorik adalah gangguan klinis dimana PH kurang dari 7,35 dan tekanan parsial karbondioksida arteri
Larutan penyangga dapat terbentuk dari campuran asam lemah dan basa
 Larutan penyangga dapat terbentuk dari campuran asam lemah dan basa konjugasinya atau campuran basa lemah dan asam konjugasinya. Larutan penyangga disebut juga larutan penahan atau larutan dapar atau buffer.
Larutan penyangga dapat terbentuk dari campuran asam lemah dan basa konjugasinya atau campuran basa lemah dan asam konjugasinya. Larutan penyangga disebut juga larutan penahan atau larutan dapar atau buffer.
Pertukaran cairan tubuh sehari-hari (antar kompartemen) Keseimbangan cairan dan elektrolit:
 Keseimbangan cairan dan elektrolit: Pengertian cairan tubuh total (total body water / TBW) Pembagian ruangan cairan tubuh dan volume dalam masing-masing ruangan Perbedaan komposisi elektrolit di intraseluler
Keseimbangan cairan dan elektrolit: Pengertian cairan tubuh total (total body water / TBW) Pembagian ruangan cairan tubuh dan volume dalam masing-masing ruangan Perbedaan komposisi elektrolit di intraseluler
BAB I PENDAHULUAN. keterbatasan aliran udara yang menetap pada saluran napas dan bersifat progresif.
 BAB I PENDAHULUAN 1.1 Latar Belakang Penyakit Paru Obstruktif Kronik (PPOK) adalah suatu keadaan terdapatnya keterbatasan aliran udara yang menetap pada saluran napas dan bersifat progresif. Penyakit ini
BAB I PENDAHULUAN 1.1 Latar Belakang Penyakit Paru Obstruktif Kronik (PPOK) adalah suatu keadaan terdapatnya keterbatasan aliran udara yang menetap pada saluran napas dan bersifat progresif. Penyakit ini
BAB I PENDAHULUAN. lain. Elektrolit terdiri dari kation dan anion. Kation ekstraseluler utama adalah natrium (Na + ), sedangkan kation
 BAB I PENDAHULUAN 1.1. Latar Belakang Masalah Cairan tubuh adalah cairan suspense sel di dalam tubuh yang memiliki fungsi fisiologis tertentu.cairan tubuh merupakan komponen penting bagi cairan ekstraseluler,
BAB I PENDAHULUAN 1.1. Latar Belakang Masalah Cairan tubuh adalah cairan suspense sel di dalam tubuh yang memiliki fungsi fisiologis tertentu.cairan tubuh merupakan komponen penting bagi cairan ekstraseluler,
PRESENTASI POWERPOINT PENGAJAR OLEH PENERBIT ERLANGGA DIVISI PERGURUAN TINGGI. BAB 16. ASAM DAN BASA
 PRESENTASI POWERPOINT PENGAJAR OLEH PENERBIT ERLANGGA DIVISI PERGURUAN TINGGI. BAB 16. ASAM DAN BASA Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi Bab 16 Asam dan Basa Asam
PRESENTASI POWERPOINT PENGAJAR OLEH PENERBIT ERLANGGA DIVISI PERGURUAN TINGGI. BAB 16. ASAM DAN BASA Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi Bab 16 Asam dan Basa Asam
G R A C I A C I N T I A M A S S I E P E M B I M B I N G : D R. A G U S K O O S H A RT O R O, S P. P D
 HIPOKALEMIA GRACIA CINTIA MASSIE PEMBIMBING : DR. AGUS KOOSHARTORO, SP.PD DEFINISI Hipokalemia adalah suatu keadaan dimana konsentrasi kalium dalam darah dibawah 3.5 meq/l yang disebabkan oleh berkurangnya
HIPOKALEMIA GRACIA CINTIA MASSIE PEMBIMBING : DR. AGUS KOOSHARTORO, SP.PD DEFINISI Hipokalemia adalah suatu keadaan dimana konsentrasi kalium dalam darah dibawah 3.5 meq/l yang disebabkan oleh berkurangnya
LOGO TEORI ASAM BASA
 LOGO TEORI ASAM BASA TIM DOSEN KIMIA DASAR FTP 2012 Beberapa ilmuan telah memberikan definisi tentang konsep asam basa Meskipun beberapa definisi terlihat kurang jelas dan berbeda satu sama lain, tetapi
LOGO TEORI ASAM BASA TIM DOSEN KIMIA DASAR FTP 2012 Beberapa ilmuan telah memberikan definisi tentang konsep asam basa Meskipun beberapa definisi terlihat kurang jelas dan berbeda satu sama lain, tetapi
Artikel Kimia tentang Peranan Larutan Penyangga
 Artikel Kimia tentang Peranan Larutan Penyangga A. PENGERTIAN Larutan penyangga atau dikenal juga dengan nama larutan buffer adalah larutan yang dapat mempertahankan nilai ph apabila larutan tersebut ditambahkan
Artikel Kimia tentang Peranan Larutan Penyangga A. PENGERTIAN Larutan penyangga atau dikenal juga dengan nama larutan buffer adalah larutan yang dapat mempertahankan nilai ph apabila larutan tersebut ditambahkan
Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi. Bab 16. Asam dan Basa
 Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi Bab 16 Asam dan Basa Asam Memiliki rasa masam; misalnya cuka mempunyai rasa dari asam asetat, dan lemon serta buah-buahan sitrun
Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi Bab 16 Asam dan Basa Asam Memiliki rasa masam; misalnya cuka mempunyai rasa dari asam asetat, dan lemon serta buah-buahan sitrun
MATERI KIMIA KELAS XI SEMESTER 2 Tinggalkan Balasan
 MATERI KIMIA KELAS XI SEMESTER 2 Tinggalkan Balasan A. Pengertian Asam Basa Asam dan basa sudah dikenal sejak zaman dulu. Istilah asam (acid) berasal dari bahasa Latin acetum yang berarti cuka. Istilah
MATERI KIMIA KELAS XI SEMESTER 2 Tinggalkan Balasan A. Pengertian Asam Basa Asam dan basa sudah dikenal sejak zaman dulu. Istilah asam (acid) berasal dari bahasa Latin acetum yang berarti cuka. Istilah
2/14/2012 LOGO Asam Basa Apa yang terjadi? Koma Tulang keropos Sesak napas dll
 LOGO Bab 08 Asam Basa Apa yang terjadi? - Koma - Tulang keropos - Sesak napas - dll 1 Ikhtisar Teori Asam Basa Sifat Asam-Basa dari Air ph-suatu ukuran keasaman Kesetimbangan Asam-Basa Lemah dan Garam
LOGO Bab 08 Asam Basa Apa yang terjadi? - Koma - Tulang keropos - Sesak napas - dll 1 Ikhtisar Teori Asam Basa Sifat Asam-Basa dari Air ph-suatu ukuran keasaman Kesetimbangan Asam-Basa Lemah dan Garam
ASUHAN KEPERAWATAN PADA KLIEN ASIDOSIS RESPIRATORI
 ASUHAN KEPERAWATAN PADA KLIEN ASIDOSIS RESPIRATORI A. PENGAKAJIAN. 1. Teliti Riwayat Klinis Dari Perjalanan Penyakit Yang Dapat Mengakibatkan Asidosis Respiratorik. 2. Teliti Tanda Dan Gejala Klinis Yang
ASUHAN KEPERAWATAN PADA KLIEN ASIDOSIS RESPIRATORI A. PENGAKAJIAN. 1. Teliti Riwayat Klinis Dari Perjalanan Penyakit Yang Dapat Mengakibatkan Asidosis Respiratorik. 2. Teliti Tanda Dan Gejala Klinis Yang
TEORI ASAM BASA Secara Umum :
 TEORI ASAM BASA Secara Umum : Asam Basa : : Cairan berasa asam dan dapat memerahkan kertas lakmus biru Cairan berasa pahit dan dapat membirukan kertas lakmus merah Garam : Cairan yang berasa asin TEORI
TEORI ASAM BASA Secara Umum : Asam Basa : : Cairan berasa asam dan dapat memerahkan kertas lakmus biru Cairan berasa pahit dan dapat membirukan kertas lakmus merah Garam : Cairan yang berasa asin TEORI
MAKALAH ASIDOSIS METABOLIK
 MAKALAH ASIDOSIS METABOLIK Definisi Asidosis metabolic adalah keasaman darah yang berlebihan,yang di tandai dengan rendahnya kadar bikarbonat dalam darah. Bila peningkatan keasaman melampaui system penyangga
MAKALAH ASIDOSIS METABOLIK Definisi Asidosis metabolic adalah keasaman darah yang berlebihan,yang di tandai dengan rendahnya kadar bikarbonat dalam darah. Bila peningkatan keasaman melampaui system penyangga
BAB 7. ASAM DAN BASA
 BAB 7. ASAM DAN BASA 7. 1 TEORI ASAM BASA 7. 2 TETAPAN KESETIMBANGAN PENGIONAN ASAM DAN BASA 7. 3 KONSENTRASI ION H + DAN ph 7. 4 INDIKATOR ASAM-BASA (INDIKATOR ph) 7. 5 CAMPURAN PENAHAN 7. 6 APLIKASI
BAB 7. ASAM DAN BASA 7. 1 TEORI ASAM BASA 7. 2 TETAPAN KESETIMBANGAN PENGIONAN ASAM DAN BASA 7. 3 KONSENTRASI ION H + DAN ph 7. 4 INDIKATOR ASAM-BASA (INDIKATOR ph) 7. 5 CAMPURAN PENAHAN 7. 6 APLIKASI
BAB I PENDAHULUAN. 1.1 Latar Belakang
 BAB I PENDAHULUAN 1.1 Latar Belakang Kegiatan olahraga sudah menjadi bagian dari aktivitas sehari-hari. Olahraga banyak diminati oleh masyarakat karena dikenal memiliki berbagai manfaat untuk menjaga kesehatan
BAB I PENDAHULUAN 1.1 Latar Belakang Kegiatan olahraga sudah menjadi bagian dari aktivitas sehari-hari. Olahraga banyak diminati oleh masyarakat karena dikenal memiliki berbagai manfaat untuk menjaga kesehatan
BAB 6. Jika ke dalam air murni ditambahkan asam atau basa meskipun dalam jumlah. Larutan Penyangga. Kata Kunci. Pengantar
 Kimia XI SMA 179 BAB 6 Larutan Penyangga Tujuan Pembelajaran: Setelah mempelajari bab ini, Anda diharapkan mampu: 1. Menjelaskan pengertian larutan penyangga dan komponen penyusunnya. 2. Merumuskan persamaan
Kimia XI SMA 179 BAB 6 Larutan Penyangga Tujuan Pembelajaran: Setelah mempelajari bab ini, Anda diharapkan mampu: 1. Menjelaskan pengertian larutan penyangga dan komponen penyusunnya. 2. Merumuskan persamaan
MAKALAH KOMA HIPERGLIKEMI
 MAKALAH KOMA HIPERGLIKEMI OLEH: Vita Wahyuningtias 07.70.0279 Daftar Isi Bab 1 Pendahuluan...1 Bab 2 Tujuan...2 Bab 3 Pembahasan...3 1. Pengertian...3 2. Etiologi...4 3. Patofisiologi...4 4. Gejala dan
MAKALAH KOMA HIPERGLIKEMI OLEH: Vita Wahyuningtias 07.70.0279 Daftar Isi Bab 1 Pendahuluan...1 Bab 2 Tujuan...2 Bab 3 Pembahasan...3 1. Pengertian...3 2. Etiologi...4 3. Patofisiologi...4 4. Gejala dan
Gejala Diabetes pada Anak yang Harus Diwaspadai
 Gejala Diabetes pada Anak yang Harus Diwaspadai Gejala diabetes sering kali tidak terlihat secara jelas di awalnya. Kadang kita baru sadar atau terindikasi diabetes ketika sudah mengalami komplikasi diabetes.
Gejala Diabetes pada Anak yang Harus Diwaspadai Gejala diabetes sering kali tidak terlihat secara jelas di awalnya. Kadang kita baru sadar atau terindikasi diabetes ketika sudah mengalami komplikasi diabetes.
mekanisme penyebab hipoksemia dan hiperkapnia akan dibicarakan lebih lanjut.
 B. HIPERKAPNIA Hiperkapnia adalah berlebihnya karbon dioksida dalam jaringan. Mekanisme penting yang mendasari terjadinya hiperkapnia adalah ventilasi alveolar yang inadekuat untuk jumlah CO 2 yang diproduksi
B. HIPERKAPNIA Hiperkapnia adalah berlebihnya karbon dioksida dalam jaringan. Mekanisme penting yang mendasari terjadinya hiperkapnia adalah ventilasi alveolar yang inadekuat untuk jumlah CO 2 yang diproduksi
LARUTAN PENYANGGA (BUFFER)
 LARUTAN PENYANGGA (BUFFER) Larutan penyangga Larutan penyangga atau larutan buffer adalah larutan yang ph-nya praktis tidak berubah walaupun kepadanya ditambahkan sedikit asam, sedikit basa, atau bila
LARUTAN PENYANGGA (BUFFER) Larutan penyangga Larutan penyangga atau larutan buffer adalah larutan yang ph-nya praktis tidak berubah walaupun kepadanya ditambahkan sedikit asam, sedikit basa, atau bila
BAB I PENDAHULUAN. dikonsumsi, tetapi juga dari aktivitas atau latihan fisik yang dilakukan. Efek akut
 BAB I PENDAHULUAN 1.1 Latar Belakang Kesehatan tubuh manusia tidak hanya tergantung dari jenis makanan yang dikonsumsi, tetapi juga dari aktivitas atau latihan fisik yang dilakukan. Efek akut aktivitas
BAB I PENDAHULUAN 1.1 Latar Belakang Kesehatan tubuh manusia tidak hanya tergantung dari jenis makanan yang dikonsumsi, tetapi juga dari aktivitas atau latihan fisik yang dilakukan. Efek akut aktivitas
BAB I PENDAHULUAN. 1.1 Latar Belakang
 BAB I PENDAHULUAN 1.1 Latar Belakang Pada tubuh manusia, mineral berperan dalam proses fisiologis. Dalam sistem fisiologis manusia, mineral tersebut dibagi menjadi dua bagian yaitu makroelemen antara lain
BAB I PENDAHULUAN 1.1 Latar Belakang Pada tubuh manusia, mineral berperan dalam proses fisiologis. Dalam sistem fisiologis manusia, mineral tersebut dibagi menjadi dua bagian yaitu makroelemen antara lain
kimia ASAM-BASA I Tujuan Pembelajaran
 KTSP & K-13 kimia K e l a s XI ASAM-BASA I Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami definisi dan sifat asam serta basa. 2. Memahami teori
KTSP & K-13 kimia K e l a s XI ASAM-BASA I Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami definisi dan sifat asam serta basa. 2. Memahami teori
BAB 1 PENDAHULUAN. sistem kardiovaskular dalam keadaan optimal yaitu dapat menghasilkan aliran
 BAB 1 PENDAHULUAN 1.1. LATAR BELAKANG Tujuan dari terapi cairan perioperatif adalah menyediakan jumlah cairan yang cukup untuk mempertahankan volume intravaskular yang adekuat agar sistem kardiovaskular
BAB 1 PENDAHULUAN 1.1. LATAR BELAKANG Tujuan dari terapi cairan perioperatif adalah menyediakan jumlah cairan yang cukup untuk mempertahankan volume intravaskular yang adekuat agar sistem kardiovaskular
JENIS GANGGUAN ELEKTROLIT
 A.HIPERKALEMIA a. pengertian JENIS GANGGUAN ELEKTROLIT Hiperkalemia (kadar kalium darah yang tinggi b. penyebab 1.pemakaian obat tertentu yang menghalangi pembuangan kalium oleh ginjal misalnya spironolakton
A.HIPERKALEMIA a. pengertian JENIS GANGGUAN ELEKTROLIT Hiperkalemia (kadar kalium darah yang tinggi b. penyebab 1.pemakaian obat tertentu yang menghalangi pembuangan kalium oleh ginjal misalnya spironolakton
glukosa darah melebihi 500 mg/dl, disertai : (b) Banyak kencing waktu 2 4 minggu)
 14 (polidipsia), banyak kencing (poliuria). Atau di singkat 3P dalam fase ini biasanya penderita menujukan berat badan yang terus naik, bertambah gemuk karena pada fase ini jumlah insulin masih mencukupi.
14 (polidipsia), banyak kencing (poliuria). Atau di singkat 3P dalam fase ini biasanya penderita menujukan berat badan yang terus naik, bertambah gemuk karena pada fase ini jumlah insulin masih mencukupi.
LARUTAN PENYANGGA DAN HIDROLISIS
 6 LARUTAN PENYANGGA DAN HIDROLISIS A. LARUTAN PENYANGGA B. HIDROLISIS Pada bab sebelumnya, kita sudah mempelajari tentang reaksi asam-basa dan titrasi. Jika asam direaksikan dengan basa akan menghasilkan
6 LARUTAN PENYANGGA DAN HIDROLISIS A. LARUTAN PENYANGGA B. HIDROLISIS Pada bab sebelumnya, kita sudah mempelajari tentang reaksi asam-basa dan titrasi. Jika asam direaksikan dengan basa akan menghasilkan
Gagal Ginjal Akut pada bayi dan anak
 Gagal Ginjal Akut pada bayi dan anak Haryson Tondy Winoto, dr,msi.med. Sp.A Bag. IKA UWK ANATOMI & FISIOLOGI GINJAL pada bayi dan anak Nefrogenesis : s/d 35 mg fetal stop Nefron : unit fungsional terkecil
Gagal Ginjal Akut pada bayi dan anak Haryson Tondy Winoto, dr,msi.med. Sp.A Bag. IKA UWK ANATOMI & FISIOLOGI GINJAL pada bayi dan anak Nefrogenesis : s/d 35 mg fetal stop Nefron : unit fungsional terkecil
1. Dari pengujian larutan dengan kertas lakmus diperoleh data berikut:
 SOAL-SOAL BAB 5 LARUTAN ASAM BASA/ Kimia Erlangga 2B 1. Dari pengujian larutan dengan kertas lakmus diperoleh data berikut: No Larutan yang diuji Warna lakmus Merah Biru 1 X Merah Biru 2 Y Merah Merah
SOAL-SOAL BAB 5 LARUTAN ASAM BASA/ Kimia Erlangga 2B 1. Dari pengujian larutan dengan kertas lakmus diperoleh data berikut: No Larutan yang diuji Warna lakmus Merah Biru 1 X Merah Biru 2 Y Merah Merah
ph = log = - log [H + ] ph = - log [0, ] ph = 7,4
![ph = log = - log [H + ] ph = - log [0, ] ph = 7,4 ph = log = - log [H + ] ph = - log [0, ] ph = 7,4](/thumbs/75/71505323.jpg) KESEIMBANGAN ASAM BASA Ion hidrogen adalah proton tunggal bebas yang dilepaskan dari atom hidrogen. Molekul yang mengandung atom-atom hidrogen yang dapat melepaskan ion ion hidrogen dalam larutan dikenal
KESEIMBANGAN ASAM BASA Ion hidrogen adalah proton tunggal bebas yang dilepaskan dari atom hidrogen. Molekul yang mengandung atom-atom hidrogen yang dapat melepaskan ion ion hidrogen dalam larutan dikenal
LARUTAN PENYANGGA (BUFFER)
 LARUTAN PENYANGGA (BUFFER) Larutan penyangga Larutan penyangga atau larutan buffer adalah larutan yang ph-nya praktis tidak berubah walaupun kepadanya ditambahkan sedikit asam, sedikit basa, atau bila
LARUTAN PENYANGGA (BUFFER) Larutan penyangga Larutan penyangga atau larutan buffer adalah larutan yang ph-nya praktis tidak berubah walaupun kepadanya ditambahkan sedikit asam, sedikit basa, atau bila
HIPONATREMIA. Banyak kemungkinan kondisi dan faktor gaya hidup dapat menyebabkan hiponatremia, termasuk:
 HIPONATREMIA 1. PENGERTIAN Hiponatremia adalah suatu kondisi yang terjadi ketika kadar natrium dalam darah adalah rendah abnormal. Natrium merupakan elektrolit yang membantu mengatur jumlah air di dalam
HIPONATREMIA 1. PENGERTIAN Hiponatremia adalah suatu kondisi yang terjadi ketika kadar natrium dalam darah adalah rendah abnormal. Natrium merupakan elektrolit yang membantu mengatur jumlah air di dalam
PEMERIKSAAN ASTRUP/ANALISA GAS DARAH * * * * * * * * * * EFY AFIFAH, M.Kes DKKD FIK UI
 PEMERIKSAAN ASTRUP/ANALISA GAS DARAH EFY AFIFAH, M.Kes DKKD FIK UI Pendahuluan Pengukuran gas darah arteri sangat penting dalam menilai pertukaran gas di dalam paru. Pengukuran ini untuk mengukur keasaman
PEMERIKSAAN ASTRUP/ANALISA GAS DARAH EFY AFIFAH, M.Kes DKKD FIK UI Pendahuluan Pengukuran gas darah arteri sangat penting dalam menilai pertukaran gas di dalam paru. Pengukuran ini untuk mengukur keasaman
BAB 1 PENDAHULUAN 1.1. Latar Belakang
 BAB 1 PENDAHULUAN 1.1. Latar Belakang Penyakit ginjal adalah salah satu penyebab paling penting dari kematian dan cacat tubuh di banyak negara di seluruh dunia (Guyton & Hall, 1997). Sedangkan menurut
BAB 1 PENDAHULUAN 1.1. Latar Belakang Penyakit ginjal adalah salah satu penyebab paling penting dari kematian dan cacat tubuh di banyak negara di seluruh dunia (Guyton & Hall, 1997). Sedangkan menurut
Pokok Bahasan. Teori tentang asam, basa dan garam Kesetimbangan asam-basa Skala ph Sörensen (Sörensen ph scale) Konstanta keasaman
 Kesetimbangan Ionik Pokok Bahasan Teori tentang asam, basa dan garam Kesetimbangan asam-basa Skala ph Sörensen (Sörensen ph scale) Konstanta keasaman Teori tentang asam dan basa Arrhenius: Asam: zat yg
Kesetimbangan Ionik Pokok Bahasan Teori tentang asam, basa dan garam Kesetimbangan asam-basa Skala ph Sörensen (Sörensen ph scale) Konstanta keasaman Teori tentang asam dan basa Arrhenius: Asam: zat yg
BAB II TINJAUAN PUSTAKA
 BAB II TINJAUAN PUSTAKA A. Ginjal Ginjal merupakan organ ekskresi utama pada manusia. Ginjal mempunyai peran penting dalam mempertahankan kestabilan tubuh. Ginjal memiliki fungsi yaitu mempertahankan keseimbangan
BAB II TINJAUAN PUSTAKA A. Ginjal Ginjal merupakan organ ekskresi utama pada manusia. Ginjal mempunyai peran penting dalam mempertahankan kestabilan tubuh. Ginjal memiliki fungsi yaitu mempertahankan keseimbangan
BAB II TINJAUAN PUSTAKA. positif dan anion bermuatan negatif. Keseimbangan keduanya disebut sebagai
 BAB II TINJAUAN PUSTAKA 2.1 Elektrolit Elektrolit adalah senyawa di dalam larutan yang di sebut kation bermuatan positif dan anion bermuatan negatif. Keseimbangan keduanya disebut sebagai elektronetralitas.
BAB II TINJAUAN PUSTAKA 2.1 Elektrolit Elektrolit adalah senyawa di dalam larutan yang di sebut kation bermuatan positif dan anion bermuatan negatif. Keseimbangan keduanya disebut sebagai elektronetralitas.
Dikenal : - Asidimetri : zat baku asam - Alkalimetri : zat baku basa DASAR : Reaksi penetralan Asam + Basa - hidrolisis - buffer - hal lain ttg lart
 Dikenal : - Asidimetri : zat baku asam - Alkalimetri : zat baku basa DASAR : Reaksi penetralan Asam + Basa - hidrolisis - buffer - hal lain ttg lart a. AK + BK ph = 7 B. AK + BL ph < 7 C. AL + BK ph >
Dikenal : - Asidimetri : zat baku asam - Alkalimetri : zat baku basa DASAR : Reaksi penetralan Asam + Basa - hidrolisis - buffer - hal lain ttg lart a. AK + BK ph = 7 B. AK + BL ph < 7 C. AL + BK ph >
I. PENDAHULUAN. mempertahankan homeostasis tubuh. Ginjal menjalankan fungsi yang vital
 I. PENDAHULUAN A. Latar Belakang Ginjal merupakan salah satu organ penting dalam tubuh yang berperan dalam mempertahankan homeostasis tubuh. Ginjal menjalankan fungsi yang vital sebagai pengatur volume
I. PENDAHULUAN A. Latar Belakang Ginjal merupakan salah satu organ penting dalam tubuh yang berperan dalam mempertahankan homeostasis tubuh. Ginjal menjalankan fungsi yang vital sebagai pengatur volume
PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA
 PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA 1 Tujuan Percobaan Tujuan dari percobaan ini adalah menentukan kadar natrium karbonat dan natrium hidrogen karbonat dengan titrasi
PENENTUAN KADAR KARBONAT DAN HIDROGEN KARBONAT MELALUI TITRASI ASAM BASA 1 Tujuan Percobaan Tujuan dari percobaan ini adalah menentukan kadar natrium karbonat dan natrium hidrogen karbonat dengan titrasi
DIABETES MELLITUS I. DEFINISI DIABETES MELLITUS Diabetes mellitus merupakan gangguan metabolisme yang secara genetis dan klinis termasuk heterogen
 DIABETES MELLITUS I. DEFINISI DIABETES MELLITUS Diabetes mellitus merupakan gangguan metabolisme yang secara genetis dan klinis termasuk heterogen dengan manifestasi berupa hilangnya toleransi karbohidrat.
DIABETES MELLITUS I. DEFINISI DIABETES MELLITUS Diabetes mellitus merupakan gangguan metabolisme yang secara genetis dan klinis termasuk heterogen dengan manifestasi berupa hilangnya toleransi karbohidrat.
TERAPI CAIRAN MAINTENANCE. RSUD ABDUL AZIS 21 April Partner in Health and Hope
 TERAPI CAIRAN MAINTENANCE RSUD ABDUL AZIS 21 April 2015 TERAPI CAIRAN TERAPI CAIRAN RESUSITASI RUMATAN Kristaloid Koloid Elektrolit Nutrisi Mengganti Kehilangan Akut Koreksi 1. Kebutuhan normal 2. Dukungan
TERAPI CAIRAN MAINTENANCE RSUD ABDUL AZIS 21 April 2015 TERAPI CAIRAN TERAPI CAIRAN RESUSITASI RUMATAN Kristaloid Koloid Elektrolit Nutrisi Mengganti Kehilangan Akut Koreksi 1. Kebutuhan normal 2. Dukungan
LEMBARAN SOAL 4. Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA )
 LEMBARAN SOAL 4 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah
LEMBARAN SOAL 4 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah
LAPORAN PRAKTIKUM. ph METER DAN PERSIAPAN LARUTAN PENYANGGA
 LAPORAN PRAKTIKUM ph METER DAN PERSIAPAN LARUTAN PENYANGGA Hari/Tanggal Praktikum : Kamis/ 17 Oktober 2013 Nama Mahasiswa : 1. Nita Andriani Lubis 2. Ade Sinaga Tujuan Praktikum : Teori 1. Mengetahui pembuatan
LAPORAN PRAKTIKUM ph METER DAN PERSIAPAN LARUTAN PENYANGGA Hari/Tanggal Praktikum : Kamis/ 17 Oktober 2013 Nama Mahasiswa : 1. Nita Andriani Lubis 2. Ade Sinaga Tujuan Praktikum : Teori 1. Mengetahui pembuatan
BAB 1 PENDAHULUAN. Ginjal merupakan salah satu organ yang memiliki fungsi penting dalam
 BAB 1 PENDAHULUAN 1.1 Latar Belakang Ginjal merupakan salah satu organ yang memiliki fungsi penting dalam tubuh manusia. Fungsi tersebut diantaranya mengatur konsentrasi garam dalam darah, dan mengatur
BAB 1 PENDAHULUAN 1.1 Latar Belakang Ginjal merupakan salah satu organ yang memiliki fungsi penting dalam tubuh manusia. Fungsi tersebut diantaranya mengatur konsentrasi garam dalam darah, dan mengatur
Easy Way to Interpret
 Easy Way to Interpret (Arterial) Blood Gases Eddy Rahardjo Dept Anestesiologi & Reanimasi Fak. Kedokteran Univ. Airlangga Surabaya 1 Tujuan presentasi: memahami hasil pemeriksaan gas darah untuk membantu
Easy Way to Interpret (Arterial) Blood Gases Eddy Rahardjo Dept Anestesiologi & Reanimasi Fak. Kedokteran Univ. Airlangga Surabaya 1 Tujuan presentasi: memahami hasil pemeriksaan gas darah untuk membantu
PERCOBAAN 3 REAKSI ASAM BASA
 PERCOBAAN 3 REAKSI ASAM BASA I. Teori Dasar Kita sering menjumpai asam dan basa dalam kehidupan sehari-hari. Buah-buahan, seperti jeruk, apel, dll., mengandung asam. Amonia rumah tangga, bahan pembersih,
PERCOBAAN 3 REAKSI ASAM BASA I. Teori Dasar Kita sering menjumpai asam dan basa dalam kehidupan sehari-hari. Buah-buahan, seperti jeruk, apel, dll., mengandung asam. Amonia rumah tangga, bahan pembersih,
LAPORAN PENDAHULUAN ASKEP PADA KLIEN DENGAN PERDARAHAN SALURAN CERNA
 1 LAPORAN PENDAHULUAN ASKEP PADA KLIEN DENGAN PERDARAHAN SALURAN CERNA I Deskripsi Perdarahan pada saluran cerna terutama disebabkan oleh tukak lambung atau gastritis. Perdarahan saluran cerna dibagi menjadi
1 LAPORAN PENDAHULUAN ASKEP PADA KLIEN DENGAN PERDARAHAN SALURAN CERNA I Deskripsi Perdarahan pada saluran cerna terutama disebabkan oleh tukak lambung atau gastritis. Perdarahan saluran cerna dibagi menjadi
KIMIa ASAM-BASA II. K e l a s. A. Kesetimbangan Air. Kurikulum 2006/2013
 Kurikulum 2006/2013 KIMIa K e l a s XI ASAM-BASA II Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami kesetimbangan air. 2. Memahami pengaruh asam
Kurikulum 2006/2013 KIMIa K e l a s XI ASAM-BASA II Tujuan Pembelajaran Setelah mempelajari materi ini, kamu diharapkan memiliki kemampuan berikut. 1. Memahami kesetimbangan air. 2. Memahami pengaruh asam
LARUTAN PENYANGGA Bahan Ajar Kelas XI IPA Semester Gasal 2012/2013
 LARUTAN PENYANGGA [Yea r] LARUTAN PENYANGGA Bahan Ajar Kelas XI IPA Semester Gasal 2012/2013 MARI BELAJAR Indikator Produk Menjelaskan komponen pembentuk larutan penyangga dengan berpikir kritis. Menjelaskan
LARUTAN PENYANGGA [Yea r] LARUTAN PENYANGGA Bahan Ajar Kelas XI IPA Semester Gasal 2012/2013 MARI BELAJAR Indikator Produk Menjelaskan komponen pembentuk larutan penyangga dengan berpikir kritis. Menjelaskan
ETIOLOGI : 1. Ada 5 kategori virus yang menjadi agen penyebab: Virus Hepatitis A (HAV) Virus Hepatitis B (VHB) Virus Hepatitis C (CV) / Non A Non B
 HEPATITIS REJO PENGERTIAN: Hepatitis adalah inflamasi yang menyebar pada hepar (hepatitis) dapat disebabkan oleh infeksi virus dan reaksi toksik terhadap obat-obatan dan bahan kimia ETIOLOGI : 1. Ada 5
HEPATITIS REJO PENGERTIAN: Hepatitis adalah inflamasi yang menyebar pada hepar (hepatitis) dapat disebabkan oleh infeksi virus dan reaksi toksik terhadap obat-obatan dan bahan kimia ETIOLOGI : 1. Ada 5
LAPORAN PENDAHULUAN GANGGUAN PEMENUHAN KEBUTUHAN NUTRISI DI RS ROEMANI RUANG AYUB 3 : ANDHIKA ARIYANTO :G3A014095
 LAPORAN PENDAHULUAN GANGGUAN PEMENUHAN KEBUTUHAN NUTRISI DI RS ROEMANI RUANG AYUB 3 NAMA NIM : ANDHIKA ARIYANTO :G3A014095 PROGRAM S1 KEPERAWATAN FIKKES UNIVERSITAS MUHAMMADIAH SEMARANG 2014-2015 1 LAPORAN
LAPORAN PENDAHULUAN GANGGUAN PEMENUHAN KEBUTUHAN NUTRISI DI RS ROEMANI RUANG AYUB 3 NAMA NIM : ANDHIKA ARIYANTO :G3A014095 PROGRAM S1 KEPERAWATAN FIKKES UNIVERSITAS MUHAMMADIAH SEMARANG 2014-2015 1 LAPORAN
MAKALAH LARUTAN ASAM DAN BASA
 MAKALAH LARUTAN ASAM DAN BASA OLEH: IRMA MULYANI (1313031073) MARIA VERONIKA (1613031041) NI MADE DWI RIANTI AGUSTINI (1613031024) NI NENGAH PRATIWI CAHYANI (1613031015) RINDA HENDRIKA UTAMI MAHMUDA (1613031028)
MAKALAH LARUTAN ASAM DAN BASA OLEH: IRMA MULYANI (1313031073) MARIA VERONIKA (1613031041) NI MADE DWI RIANTI AGUSTINI (1613031024) NI NENGAH PRATIWI CAHYANI (1613031015) RINDA HENDRIKA UTAMI MAHMUDA (1613031028)
NETRALISASI ASAM BASA SEDERHANA
 NETRALISASI ASAM BASA SEDERHANA Dosen Pembimbing : Zora Olivia, S. Farm., M.Farm, Apt GOLONGAN/KELOMPOK : A / 3 Anindiya Tazkiyah Aji Gesang Jati Abrar Rivanio Putra Siti Sofiya Miranda Faradilla Rozziqa
NETRALISASI ASAM BASA SEDERHANA Dosen Pembimbing : Zora Olivia, S. Farm., M.Farm, Apt GOLONGAN/KELOMPOK : A / 3 Anindiya Tazkiyah Aji Gesang Jati Abrar Rivanio Putra Siti Sofiya Miranda Faradilla Rozziqa
BAB 2 TINJAUAN PUSTAKA
 5 BAB 2 TINJAUAN PUSTAKA 2.1. Olahraga 2.1.1. Definisi Olahraga Olahraga ialah tindakan fisik untuk meningkatkan kesehatan atau memperbaiki deformitas fisik (Dorland s 2004). Sedangkan menurut Gale Encyclopedia
5 BAB 2 TINJAUAN PUSTAKA 2.1. Olahraga 2.1.1. Definisi Olahraga Olahraga ialah tindakan fisik untuk meningkatkan kesehatan atau memperbaiki deformitas fisik (Dorland s 2004). Sedangkan menurut Gale Encyclopedia
M.Nuralamsyah,S.Kep.Ns
 M.Nuralamsyah,S.Kep.Ns Pendahuluan Ginjal mempertahankan komposisi dan volume cairan supaya tetap konstan Ginjal terletak retroperitoneal Bentuknya menyerupai kacang dengan sisi cekungnya menghadap ke
M.Nuralamsyah,S.Kep.Ns Pendahuluan Ginjal mempertahankan komposisi dan volume cairan supaya tetap konstan Ginjal terletak retroperitoneal Bentuknya menyerupai kacang dengan sisi cekungnya menghadap ke
KIMIA (2-1)
 03035307 KIMIA (2-1) Dr.oec.troph.Ir.Krishna Purnawan Candra, M.S. Kuliah ke-9 Teori Asam Basa Bahan kuliah ini disarikan dari Chemistry 4th ed. McMurray and Fay Faperta UNMUL 2011 Pengertian Asam dan
03035307 KIMIA (2-1) Dr.oec.troph.Ir.Krishna Purnawan Candra, M.S. Kuliah ke-9 Teori Asam Basa Bahan kuliah ini disarikan dari Chemistry 4th ed. McMurray and Fay Faperta UNMUL 2011 Pengertian Asam dan
Anatomi & Fisiologi Sistem Respirasi II Pertemuan 7 Trisia Lusiana Amir, S. Pd., M. Biomed PRODI MIK FAKULTAS ILMU-ILMU KESEHATAN
 Anatomi & Fisiologi Sistem Respirasi II Pertemuan 7 Trisia Lusiana Amir, S. Pd., M. Biomed PRODI MIK FAKULTAS ILMU-ILMU KESEHATAN KEMAMPUAN AKHIR YANG DIHARAPKAN Mahasiswa mampu menjelaskan anatomi dan
Anatomi & Fisiologi Sistem Respirasi II Pertemuan 7 Trisia Lusiana Amir, S. Pd., M. Biomed PRODI MIK FAKULTAS ILMU-ILMU KESEHATAN KEMAMPUAN AKHIR YANG DIHARAPKAN Mahasiswa mampu menjelaskan anatomi dan
Bab II Tinjauan Pustaka. Asam basa Konjugasi Menurut Bronsted Lowry
 Bab II Tinjauan Pustaka II.1 Asam basa Konjugasi Menurut Bronsted Lowry Untuk memahami konsep larutan buffer perlu diketahui konsep asam basa. Konsep asam basa ada tiga yaitu menurut Arrhenius, Bronsted
Bab II Tinjauan Pustaka II.1 Asam basa Konjugasi Menurut Bronsted Lowry Untuk memahami konsep larutan buffer perlu diketahui konsep asam basa. Konsep asam basa ada tiga yaitu menurut Arrhenius, Bronsted
BAB II TINJAUAN PUSTAKA. yang terkandung di dalam urine serta adanya kelainan-kelainan pada urine.
 BAB II TINJAUAN PUSTAKA A. Urinalisis Urinalisis merupakan suatu metode analisa untuk mengetahui zat-zat yang terkandung di dalam urine serta adanya kelainan-kelainan pada urine. Urinalisis berasal dari
BAB II TINJAUAN PUSTAKA A. Urinalisis Urinalisis merupakan suatu metode analisa untuk mengetahui zat-zat yang terkandung di dalam urine serta adanya kelainan-kelainan pada urine. Urinalisis berasal dari
BAB I PENDAHULUAN. sama lain. Elektrolit terdiri dari kation dan anion. Muatan positif merupakan hasil pembentukan dari kation dalam larutan.
 BAB I PENDAHULUAN 1.1. Latar Belakang Masalah Air adalah kebutuhan utama pada makhluk hidup, terutama manusia.tidak ada makhluk hidup bisa hidup tanpa adanya air yang di konsumsi. Karena pada proses metabolisme,
BAB I PENDAHULUAN 1.1. Latar Belakang Masalah Air adalah kebutuhan utama pada makhluk hidup, terutama manusia.tidak ada makhluk hidup bisa hidup tanpa adanya air yang di konsumsi. Karena pada proses metabolisme,
Titrasi asam kuat-basa kuat
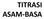 TITRASI ASAM-BASA KURVA TITRASI plot atau kurva antara ph atau poh terhadap volume titran untuk menguji apakah suatu reaksi dapat digunakan untuk analisa titrimetri ataukah tidak memilih indikator Titrasi
TITRASI ASAM-BASA KURVA TITRASI plot atau kurva antara ph atau poh terhadap volume titran untuk menguji apakah suatu reaksi dapat digunakan untuk analisa titrimetri ataukah tidak memilih indikator Titrasi
BAB I PENDAHULUAN. yang progresif dan irreversibel akibat berbagai penyakit yang merusak nefron
 BAB I PENDAHULUAN 1.1 Latar Belakang Penyakit ginjal kronik merupakan suatu keadaan klinis kerusakan ginjal yang progresif dan irreversibel akibat berbagai penyakit yang merusak nefron ginjal, mengakibatkan
BAB I PENDAHULUAN 1.1 Latar Belakang Penyakit ginjal kronik merupakan suatu keadaan klinis kerusakan ginjal yang progresif dan irreversibel akibat berbagai penyakit yang merusak nefron ginjal, mengakibatkan
Aplikasi Larutan Buffer dalam Kehidupan Sehari-hari
 Aplikasi Larutan Buffer dalam Kehidupan Sehari-hari Buat apa sih belajar tapi gak dipake? Pertanyaan ini tuh selalu muncul di otak gue tiap ngadepin pelajaran yang bikin gue mabok 3 x 24 jam. Dan mungkin
Aplikasi Larutan Buffer dalam Kehidupan Sehari-hari Buat apa sih belajar tapi gak dipake? Pertanyaan ini tuh selalu muncul di otak gue tiap ngadepin pelajaran yang bikin gue mabok 3 x 24 jam. Dan mungkin
Titrasi Asam Basa. Sophi Damayanti
 Titrasi Asam Basa Sophi Damayanti 1 Highlight Kuliah Lalu KUALITATIF KUANTITATIF Berkaitan dengan identifikasi Berkaitan dengan kadar Menjawab pertanyaan Apa Menjawab pertanyaan Berapa What chemicals are
Titrasi Asam Basa Sophi Damayanti 1 Highlight Kuliah Lalu KUALITATIF KUANTITATIF Berkaitan dengan identifikasi Berkaitan dengan kadar Menjawab pertanyaan Apa Menjawab pertanyaan Berapa What chemicals are
Disusun Oleh: Anastasia Latif ( XI IPA 1 ) Christine ( XI IPA 1 ) Josephine Putri ( XI IPA 2 ) Kelvin Ricky (XI IPA 2 ) Patty Regina (XI IPA 1 )
 LAPORAN PRAKTIKUM KIMIA Asam dan Basa Disusun Oleh: Anastasia Latif ( XI IPA 1 ) Christine ( XI IPA 1 ) Josephine Putri ( XI IPA 2 ) Kelvin Ricky (XI IPA 2 ) Patty Regina (XI IPA 1 ) Windy Saputra ( XI
LAPORAN PRAKTIKUM KIMIA Asam dan Basa Disusun Oleh: Anastasia Latif ( XI IPA 1 ) Christine ( XI IPA 1 ) Josephine Putri ( XI IPA 2 ) Kelvin Ricky (XI IPA 2 ) Patty Regina (XI IPA 1 ) Windy Saputra ( XI
BAB II TINJAUAN PUSTAKA. pakan. Biaya untuk memenuhi pakan mencapai 60-70% dari total biaya produksi
 4 BAB II TINJAUAN PUSTAKA 2. 1. Pakan Sapi Perah Faktor utama dalam keberhasilan usaha peternakan yaitu ketersediaan pakan. Biaya untuk memenuhi pakan mencapai 60-70% dari total biaya produksi (Firman,
4 BAB II TINJAUAN PUSTAKA 2. 1. Pakan Sapi Perah Faktor utama dalam keberhasilan usaha peternakan yaitu ketersediaan pakan. Biaya untuk memenuhi pakan mencapai 60-70% dari total biaya produksi (Firman,
RENCANA PELAKSANAAN PEMBELAJARAN I. Standar Kompetensi 1. Memahami sifat-sifat larutan asam basa, metode pengukuran, dan terapannya
 Lampiran 2 63 RENCANA PELAKSANAAN PEMBELAJARAN I Mata Pelajaran Kelas/Semester Sub Materi Pokok Alokasi Waktu Pertemuan ke : Kimia : XI IPA 4/ 2 (dua) : Teori Asam Basa Arrhenius : 2 x 45 menit : I Standar
Lampiran 2 63 RENCANA PELAKSANAAN PEMBELAJARAN I Mata Pelajaran Kelas/Semester Sub Materi Pokok Alokasi Waktu Pertemuan ke : Kimia : XI IPA 4/ 2 (dua) : Teori Asam Basa Arrhenius : 2 x 45 menit : I Standar
TEORI ASAM BASA SECARA UMUM :
 TEORI ASAM BASA SECARA UMUM : TEORI ASAM BASA Secara Umum : Cairan berasa asam dan dapat Asam : memerahkan kertas lakmus biru Basa : Garam : Cairan berasa pahit dan dapat membirukan kertas lakmus merah
TEORI ASAM BASA SECARA UMUM : TEORI ASAM BASA Secara Umum : Cairan berasa asam dan dapat Asam : memerahkan kertas lakmus biru Basa : Garam : Cairan berasa pahit dan dapat membirukan kertas lakmus merah
GANGGUAN KESEIMBANGAN CAIRAN DAN ELEKTROLIT
 GANGGUAN KESEIMBANGAN CAIRAN DAN ELEKTROLIT Dr. Suparyanto, M.Kes GANGGUAN KESEIMBANGAN CAIRAN DAN ELEKTROLIT CAIRAN TUBUH Cairan tubuh adalah larutan isotonik yang tersusun atas air dan zat terlarut (mineral)
GANGGUAN KESEIMBANGAN CAIRAN DAN ELEKTROLIT Dr. Suparyanto, M.Kes GANGGUAN KESEIMBANGAN CAIRAN DAN ELEKTROLIT CAIRAN TUBUH Cairan tubuh adalah larutan isotonik yang tersusun atas air dan zat terlarut (mineral)
Pokok Bahasan: GASTROENTEROLOGI dan HEPATOLOGI Sakit perut berulang M. Juffrie
 Pokok Bahasan: GASTROENTEROLOGI dan HEPATOLOGI Sakit perut berulang M. Juffrie Definisi Sakit perut yang terjadi paling sedikit 3 kali, cukup berat sampai tidak bisa melakukan kegiatan sehari hari dalam
Pokok Bahasan: GASTROENTEROLOGI dan HEPATOLOGI Sakit perut berulang M. Juffrie Definisi Sakit perut yang terjadi paling sedikit 3 kali, cukup berat sampai tidak bisa melakukan kegiatan sehari hari dalam
Gangguan Keseimbangan Asam dan Basa
 Gangguan Keseimbangan Asam dan Basa KASUS 1 Seorang anak perempuan berusia 12 tahun, dibawa ke ruang gawat darurat karena tubuhnya semakin lemas dan lemah. Selama empat hari ini, ia mengalami diare dan
Gangguan Keseimbangan Asam dan Basa KASUS 1 Seorang anak perempuan berusia 12 tahun, dibawa ke ruang gawat darurat karena tubuhnya semakin lemas dan lemah. Selama empat hari ini, ia mengalami diare dan
BAB IV HASIL DAN PEMBAHASAN. A. Gambaran Umum Rumah Sakit RSUD dr. Moewardi. 1. Rumah Sakit Umum Daerah dr. Moewardi
 BAB IV HASIL DAN PEMBAHASAN A. Gambaran Umum Rumah Sakit RSUD dr. Moewardi 1. Rumah Sakit Umum Daerah dr. Moewardi RSUD dr. Moewardi adalah rumah sakit umum milik pemerintah Propinsi Jawa Tengah. Berdasarkan
BAB IV HASIL DAN PEMBAHASAN A. Gambaran Umum Rumah Sakit RSUD dr. Moewardi 1. Rumah Sakit Umum Daerah dr. Moewardi RSUD dr. Moewardi adalah rumah sakit umum milik pemerintah Propinsi Jawa Tengah. Berdasarkan
BAB 2. TINJAUAN PUSTAKA. Sakit perut berulang menurut kriteria Apley adalah sindroma sakit perut
 BAB 2. TINJAUAN PUSTAKA 2.1.Sakit Perut Berulang Sakit perut berulang menurut kriteria Apley adalah sindroma sakit perut berulang pada remaja terjadi paling sedikit tiga kali dengan jarak paling sedikit
BAB 2. TINJAUAN PUSTAKA 2.1.Sakit Perut Berulang Sakit perut berulang menurut kriteria Apley adalah sindroma sakit perut berulang pada remaja terjadi paling sedikit tiga kali dengan jarak paling sedikit
Asam-Basa. Kimia. Kelas XI. B usiness Name. Indikator: A. Teori Asam-Basa
 Asam-Basa Kimia Kelas XI B usiness Name Indikator: 3.1.1 Menjelaskan teori asam basa berdasarkan konsep Arrhenius, Brosnted Lowry dan Lewis 3.1.2 Menjelaskan pengertian indikator asam-basa 3.1.3 Menyebutkan
Asam-Basa Kimia Kelas XI B usiness Name Indikator: 3.1.1 Menjelaskan teori asam basa berdasarkan konsep Arrhenius, Brosnted Lowry dan Lewis 3.1.2 Menjelaskan pengertian indikator asam-basa 3.1.3 Menyebutkan
a. Cedera akibat terbakar dan benturan b. Reaksi transfusi yang parah c. Agen nefrotoksik d. Antibiotik aminoglikosida
 A. Pengertian Gagal Ginjal Akut (GGA) adalah penurunan fungsi ginjal mendadak dengan akibat hilangnya kemampuan ginjal untuk mempertahankan homeostasis tubuh. Akibat penurunan fungsi ginjal terjadi peningkatan
A. Pengertian Gagal Ginjal Akut (GGA) adalah penurunan fungsi ginjal mendadak dengan akibat hilangnya kemampuan ginjal untuk mempertahankan homeostasis tubuh. Akibat penurunan fungsi ginjal terjadi peningkatan
Efek Diabetes Pada Sistem Ekskresi (Pembuangan)
 Efek Diabetes Pada Sistem Ekskresi (Pembuangan) Diabetes merupakan penyakit yang mempengaruhi kemampuan tubuh anda untuk memproduksi atau menggunakan insulin. Yaitu, hormon yang bekerja untuk mengubah
Efek Diabetes Pada Sistem Ekskresi (Pembuangan) Diabetes merupakan penyakit yang mempengaruhi kemampuan tubuh anda untuk memproduksi atau menggunakan insulin. Yaitu, hormon yang bekerja untuk mengubah
TITRASI DENGAN INDIKATOR GABUNGAN DAN DUA INDIKATOR
 TITRASI DENGAN INDIKATOR GABUNGAN DAN DUA INDIKATOR I. TUJUAN 1. Memahami prinsip kerja dari percobaan. 2. Menentukan konsentrasi dari NaOH dan Na 2 CO 3. 3. Mengetahui kegunaan dari titrasi dengan indikator
TITRASI DENGAN INDIKATOR GABUNGAN DAN DUA INDIKATOR I. TUJUAN 1. Memahami prinsip kerja dari percobaan. 2. Menentukan konsentrasi dari NaOH dan Na 2 CO 3. 3. Mengetahui kegunaan dari titrasi dengan indikator
BALANCE CAIRAN. IWL (insensible water loss(iwl) : jumlah cairan keluarnya tidak disadari dan sulit diitung, yaitu jumlah keringat, uap hawa nafa.
 SARI CHAERUNISAH 04091401070 BALANCE CAIRAN Balance cairan atau keseimbangan cairan adalah keseimbangan antara pemasukan cairan (intake) dan pengeluaran cairan (output). Masukan cairan orang dewasa normalnya
SARI CHAERUNISAH 04091401070 BALANCE CAIRAN Balance cairan atau keseimbangan cairan adalah keseimbangan antara pemasukan cairan (intake) dan pengeluaran cairan (output). Masukan cairan orang dewasa normalnya
