KINETIKA AKTIVITAS REDUKSI NITRAT BAKTERI NITRAT AMONIFIKASI DISIMILATIF DARI MUARA SUNGAI PADA KONSENTRASI OKSIGEN (O 2 ) YANG BERBEDA TETI MARDIATI
|
|
|
- Hendri Sumadi
- 7 tahun lalu
- Tontonan:
Transkripsi
1 KINETIKA AKTIVITAS REDUKSI NITRAT BAKTERI NITRAT AMONIFIKASI DISIMILATIF DARI MUARA SUNGAI PADA KONSENTRASI OKSIGEN (O 2 ) YANG BERBEDA TETI MARDIATI SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR BOGOR 2009
2 PERNYATAAN MENGENAI TESIS DAN SUMBER INFORMASI Dengan ini saya menyatakan bahwa tesis Kinetika Aktivitas Reduksi Nitrat Bakteri Nitrat Amonifikasi Disimilatif dari Muara Sungai pada Konsentrasi Oksigen (O2) yang Berbeda adalah benar hasil karya saya sendiri dengan arahan komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulisan lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini Bogor, Juni 2009 Teti Mardiati NRP G
3 ABSTRACT TETI MARDIATI, Nitrate Reduction Activity Kinetics of Dissimilative Nitrate Ammonification Bacteria Isolated from Estuary under Different Concentration of Oxygen. Under direction of IMAN RUSMANA and TRI WIDIYANTO. Dissimilative Nitrate ammonification bacteria have ability to remove nitrate in aquatic environments. These groups are consist of fermentative bacteria which reduce nitrate to ammonium with nitrous oxide (N 2 O) as by product. Four selected isolates from tropical estuary were tested the growth and nitrate reduction activities under different concentration of oxygen (O 2 ). The results showed that Cell density was increased by increasing of oxygen concentration. In contrast, the activities of nitrate reduction was decreased by increasing of oxygen concentration. HF7 and LF6 isolates had the highest nitrate reducing activity. The maximum specific growth of HF7 isolate with asetate as carbon source, and mm nitrate after 96 h incubation under air saturated of 1%, 10%, 100% was CFUh -1, CFUh -1, and CFUh -1 respectively. While LF6 isolate was CFU h -1, CFU h -1, and CFU h -1. Nitrate removal rate of HF7 isolate with asetate as carbon source, and mm nitrate after 96 h incubation under air saturated of 1%, 10%, 100% was 6.3 x mmh -1, 5.1 x mmh -1, and 3.3 x mmh -1 respectively. While LF6 isolate was 2.0 x mmh -1, 2,1 x mmh -1 and 1,0 x mmh -1 respectively. Keywords: nitrate reduction, dissimilative nitrate ammonification bacteria, oxygen concentration.
4 RINGKASAN TETI MARDIATI. Kinetika Aktivitas Reduksi Nitrat Bakteri Nitrat Amonifikasi Disimilatif dari Muara Sungai pada Konsentrasi Oksigen yang Berbeda. Dibimbing oleh IMAN RUSMANA dan TRI WIDIYANTO. Bakteri nitrat amonifikasi disimilatif atau Dissimilatory Nitrate Reduction to Ammonium (DNRA) termasuk kedalam kelompok bakteri pereduksi nitrat. Bakteri DNRA bersifat fermentatif, dapat mendegradasi senyawa organik dalam lingkungan oksigen terbatas atau anaerob. Penggunaan nitrat sebagai akseptor elektron oleh kelompok bakteri ini, dapat mengurangi kadar nitrat di perairan. Pada sisi lain bakteri DNRA menghasilkan produk samping N 2 O (nitrous oksida), gas yang berpotensi meningkatkan pemanasan global. Meskipun bakteri DNRA umumnya mereduksi nitrat menjadi amonium pada kondisi anoksik, tetapi pada beberapa bakteri ditemukan reduksi nitrat berlangsung secara aerob. Sensitivitas sistem reduktase bakteri DNRA daerah tropik terhadap oksigen belum banyak diketahui. Bertolak dari hal tersebut perlu dilakukan penelitian pengaruh oksigen terhadap kinetika aktivitas reduksi nitrat bakteri DNRA yang berasal dari muara sungai di daerah tropik. Empat isolat terseleksi dari muara sungai daerah tropik, telah diuji pertumbuhan dan aktivitas reduksi nitratnya pada konsentrasi oksigen yang berbeda. Keempat isolat tersebut adalah isolat HF7, LF6 (berasal dari muara Sungai Cisadane) dan isolat FR1, FR2 (berasal dari muara Sungai Cimandiri). Tingkat pencemaran muara Sungai Cisadane lebih tinggi dari pada muara Sungai Cimandiri. Metoda penelitian dilakukan melalui 3 tahap, yaitu konfirmasi kemurnian isolat dan peremajaan, seleksi aktivitas konsentrasi oksigen berbeda, dan kinetika aktivitas reduksi nitrat isolat terpilih pada konsentrasi oksigen berbeda. Pengkondisian konsentrasi oksigen dilakukan dengan mengatur volume saturasi udara pada head space botol sampel dengan penggunaan gas nitrogen murni. Aktivitas reduksi nitrat dan senyawa-senyawa yang dihasilkan diukur dengan analisis nitrat metoda Greenberg, analisis nitrit metode Sulfanilamid dan analisis amonium metoda Phenate. Hasil penelitian tahap seleksi menunjukkan kerapatan sel cenderung meningkat sejalan dengan penambahan konsentrasi oksigen. Aktivitas reduksi nitrat cenderung menurun sejalan dengan penambahan konsentrasi oksigen. Isolat HF7 dan LF6 memiliki kemampuan mereduksi nitrat paling tinggi, dengan perkiraan gas N 2 O yang dihasilkan lebih sedikit dibandingkan isolat FR1 dan FR2. Kedua isolat dijadikan isolat terpilih untuk diamati laju pertumbuhan dan kinetika aktivitas reduksi nitratnya. Hasil pengamatan laju pertumbuhan isolat HF7 dan LF6 menunjukkan konsentrasi oksigen mempengaruhi laju pertumbuhan kedua isolat. Laju pertumbuhan spesifik maksimum (µ maks ) dari isolat HF7 pada konsentrasi saturasi udara 1%, 10% dan 100% dengan sumber karbon asetat dan nitrat media 49,41mM secara berurut adalah 0,034 CFU/jam, 0,040 CFU/jam, dan 0,070 CFU/jam. Laju pertumbuhan spesifik dari isolat LF6 pada kondisi yang sama secara berurut adalah 0,035 CFU /jam, 0,045 CFU /jam, dan 0,057 CFU /jam.
5 Kecepatan rata-rata mengurangi nitrat medium oleh setiap sel isolat HF7 dengan sumber karbon asetat, nitrat medium 49,41 mm, masa inkubasi 96 jam pada konsentrasi udara saturasi 1%, 10%, 100% secara berurut adalah 6,3 x mmj -1, 5,1 x mmj -1, dan 3,3 x mmj -1. Sedangkan rata-rata kecepatan reduksi setiap sel isolat LF6 pada kondisi yang sama secara berurut adalah 2,0 x mmj -1, 2,1 x mmj -1 dan 1,0 x mmj -1. Dari hasil penelitian keseluruhan menunjukkan bahwa oksigen berpengaruh terhadap kinetika aktivitas reduksi nitrat bakteri DNRA yang berasal dari muara sungai daerah tropik. Besarnya pengaruh oksigen terhadap kinetika aktivitas reduksi nitrat tergantung pada sensitivitas sistem nitrat reduktase yang dimiliki oleh isolat bakteri. Konsentrasi oksigen berbeda lebih besar pengaruhnya pada isolat HF7 dibandingkan terhadap isolat LF6. Perkiraan konsentrasi gas N 2 O tertinggi yang dihasilkan pada isolat HF7 dengan nitrat medium 49,41 mm dan sumber karbon asetat terdapat pada konsentrasi saturasi udara 100%. Sedangkan pada isolat LF6 diperkirakan menghasilkan gas N 2 O terbesar pada konsentrasi saturasi udara 10%. Kata kunci : Reduksi nitrat, bakteri nitrat amonifikasi disimilatif, konsentrasi oksigen.
6 Hak Cipta milik IPB, tahun 2009 Hak Cipta dilindungi Undang-Undang Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumber. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB. Dilarang mengumumkan dan memperbanyak sebagian atau seluruh karya tulis dalam bentuk apa pun tanpa izin IPB.
7 KINETIKA AKTIVITAS REDUKSI NITRAT BAKTERI NITRAT AMONIFIKASI DISIMILATIF DARI MUARA SUNGAI PADA KONSENTRASI OKSIGEN (O 2 ) YANG BERBEDA TETI MARDIATI Tesis Sebagai salah satu syarat untukmemperoleh gelar Magister Sains pada Mayor Mikrobiologi SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR BOGOR 2009
8 Judul Tesis Nama NRP : Kinetika Aktivitas Reduksi Nitrat Bakteri Nitrat Amonifikasi Disimilatif dari Muara Sungai pada Konsentrasi Oksigen (O 2 ) yang Berbeda : Teti Mardiati : G Disetujui Komisi Pembimbing Dr. Ir. Iman Rusmana, M. Si. Ketua Dr. Tri Widiyanto, M. Si Anggota Diketahui Ketua Mayor Mikrobiologi Dekan Sekolah Pascasarjana Dr. Ir. Gayuh Rahayu Prof. Dr. Ir. Khairil Anwar Notodiputro, M.S. Tanggal Ujian: 18 Juni 2009 Tanggal Lulus:
9 Penguji Luar Komisi pada Ujian Tesis: Dr. Ir. Munti Yuhana, M.Si.
10 PRAKATA Puji dan syukur penulis panjatkan kepada Allah SWT atas limpahan rahmat, karunia dan ridho-nyalah tesis yang berjudul Kinetika Aktivitas Reduksi Nitrat Bakteri Nitrat Amonifikasi Disimilatif dari Muara Sungai pada Konsentrasi Oksigen (O 2 ) yang Berbeda dapat diselesaikan. Pelaksanaan penelitian dan penulisan tesis ini tidak terlepas dari bantuan dan bimbingan berbagai pihak. Pada kesempatan ini penulis menyampaikan terima kasih yang sebesar-besarnya kepada: 1. Bapak Dr. Ir. Iman Rusmana, M.Si dan Bapak Dr. Tri Widiyanto, M.Si selaku komisi pembimbing atas bantuan, bimbingan dan pengarahan yang telah diberikan selama penelitian dan penulisan tesis ini sehingga penulis dapat menyelesaikan dengan baik. 2. Departemen Agama RI yang telah memberikan beasiswa pendidikan. 3. Ketua Program Studi Biologi, Ketua Mayor Mikrobiologi, Ketua dan Staf Laboratorium Mikrobiologi Departemen Biologi, Fakultas Ilmu Pengetahuan Alam, Institut Pertanian Bogor yang telah membantu dalam menyediakan fasilitas hingga terlaksananya penelitian ini. 4. Suami, Ibunda, dan anak-anak tercinta, seluruh keluarga serta rekan-rekan di MAN Batumandi yang telah banyak memberikan dukungan, hingga penulis mampu menyelesaikan studi ini dengan baik. 5. Rekan-rekan angkatan 2007 Program studi Biologi, rekan-rekan lab mikrobiologi, Mbak Ratna, Irul dan Ria atas segala bantuan dan kerjasamanya. Akhirnya semoga tesis ini bermanfaat bagi semuanya. Amin. Bogor, juni 2009 Teti Mardiati
11 RIWAYAT HIDUP Penulis dilahirkan di Bandung pada tanggal 19 Agustus 1967 dari ayah Ahmad Hidayat dan ibu Siti Rokilah. Penulis merupakan anak pertama dari enam bersaudara. Penulis menyelesaikan program sarjana (SI) Jurusan Biologi Fakultas Pendidikan Matematika dan Ilmu Pengetahuan Alam IKIP Bandung pada tahun Penulis bertugas sebagai staf Pengajar Biologi pada Madrasah Aliyah Negeri (MAN) Batumandi Kabupaten Agam Sumatera Barat sejak tahun 1992 sampai sekarang. Pada bulan Juli 2007 penulis melanjutkan kuliah ke Sekolah Pascasarjana Institut Pertanian Bogor Program Studi Biologi Mayor Mikrobiologi melalui beasiswa pendidikan Departemen Agama RI. Bogor, juni 2009 Penulis
12 DAFTAR ISI Halaman. DAFTAR TABEL... xiii DAFTAR GAMBAR... DAFTAR LAMPIRAN... xiv xv PENDAHULUAN... 1 Latar Belakang... 1 Tujuan... 3 TINJAUAN PUSTAKA... 4 Muara sungai... 4 Muara Sungai Cimandiri dan Cisadane... 6 Bakteri Pereduksi Nitrat... 7 Enzim-Enzim yang Berperan Dalam Reduksi Nitrat... 8 Bakteri Nitrat Amonifikasi Disimilatif (DNRA)... 9 METODE PENELITIAN Waktu dan Tempat penelitian Bahan Penelitian Konfirmasi dan Peremajaan Isolat Seleksi Aktivitas Reduksi Nitrat pada Konsentrasi Oksigen (O 2 ) yang Berbeda Analisis nitrit Analisis nitrat Analisis amonium Perhitungan Pembentukan Gas Kinetika Aktivitas Reduksi Nitrat Isolat Terpilih HASIL Karakteristik, Morfologi dan Fisiologi Bakteri Amonifikasi Disimilatif Densitas Sel isolat Bakteri DNRA Pada Konsentrasi O 2
13 yang Berbeda Aktivitas Reduksi Nitrat Bakteri DNRA pada Konsentrasi Oksigen yang Berbeda Pertumbuhan Isolat Terpilih Kinetika Aktivitas Reduksi Nitrat PEMBAHASAN SIMPULAN DAN SARAN Simpulan Saran DAFTAR PUSTAKA LAMPIRAN... 46
14 DAFTAR TABEL Halaman 1. Karakterisasi morfologi dan fisiologi isolat LF6, HF7, FR2,dan FR Aktivitas reduksi nitrat dan senyawa yang dihasilkan isolat HF7 pada konsentrasi saturasi udara 1%, 10% dan 100% setelah inkubasi 96 jam suhu ruang (29-31) o C Aktivitas reduksi nitrat dan senyawa yang dihasilkan isolat LF6 pada konsentrasi saturasi udara 1%, 10% dan 100%, setelah inkubasi 96 jam suhu ruang (29-31) o C... 31
15 DAFTAR GAMBAR Halaman 1. Daur biogeokimia nitrogen di perairan Lintasan reduksi nitrat oleh aktivitas bakteri (1) Denitrifikasi, (2).Reduksi nitrat amonifikasi disimilatif (3) Oksidasi amonia secara anaerob Bagan pembentukan N 2 O pada reduksi nitrat oleh bakteri DNRA Enzim pereduksi nitrat bakteri nitrat amonifikasi disimilatif Morfologi koloni dari isolat LF6, HF7, FR2 dan FR1 pada medium denitrifikasi Hasil uji fermentatif pada isolat FR1, FR2, HF7 dan LF6, setelah inkubasi 48 jam Densitas sel Isolat LF6, HF7, FR2, dan FR1 pada konsentrasi saturasi udara yang berbeda, setelah diinkubasi selama 96 jam pada suhu ruang (29-31) 0 C Jumlah nitrat tereduksi oleh isolat LF6, HF7, FR2, dan FR1 pada konsentrasi saturasi udara yang berbeda, setelah diinkubasi selama 96 jam pada suhu ruang ( 29-31) 0 C Jumlah nitrit terakumulasi dari isolat LF6, HF7, FR2, dan FR1 pada konsentrasi saturasi udara yang berbeda, setelah diinkubasi selama 96 jam pada suhu ruang (29-31) 0 C Jumlah amonium yang dihasilkan dari isolat LF6, HF7, FR2, dan FR1 pada konsentrasi saturasi udara yang berbeda, setelah diinkubasi selama 96 jam pada suhu ruang ( 29-31) 0 C Pola pertumbuhan isolat HF7 dan LF6 pada konsentrasi saturasi udara Berbeda Laju pertumbuhan maksimum isolat HF7 dan LF6 pada konsentrasi saturasi udara berbeda Aktivitas reduksi nitrat, pembentukan nitrit dan amonium dari isolat HF7 dan LF6 pada konsentrasi saturasi udara 1%, 10% dan 100% Perbandingan pertumbuhan sel isolat HF7 dan LF6 dengan penurunan konsentrasi nitrat pada konsentrasi saturasi udara 1%, 10% dan 100%... 29
16 DAFTAR LAMPIRAN Halaman 1. Pembentukan warna pada uji kadar nitrat (A), nitrit (B) dan amonium (C) Kurva standar konsentrasi amonium (A) dan kurva standar konsentrasi nitrit (B) Jumlah CFU Isolat HF7 dan LF6 pada pengenceran Kurva standar pertumbuhan isolat HF7 dan LF6 pada kondisi nitrat medium 49,41 mm Presentase nitrat tereduksi dan senyawa yang dihasilkan isolat LF6,HF7 dan FR2 pada kadar saturasi udara berbeda dengan inkubasi selama 4 hari suhu ruang (29-31) o C Presentase nitrat tereduksi dan senyawa yang dihasilkan isolat FR1 pada kadar saturasi udara berbeda dengan inkubasi selama 4 hari suhu ruang (29-31) o C Perbandingan konsentrasi nitrat tereduksi, nitrit, nitrat, amonium dan estimasi gas yang dihasilkan isolat LF6 dan HF Perbandingan konsentrasi nitrat tereduksi, nitrit, nitrat, amonium dan estimasi gas yang dihasilkan isolat FR1 dan FR
17 PENDAHULUAN Latar Belakang Bakteri nitrat amonifikasi disimilatif atau Dissimilatory Nitrate Reduction to Ammonium (DNRA) termasuk ke dalam kelompok bakteri pereduksi nitrat. Kelompok bakteri pereduksi nitrat menggunakan nitrat sebagai akseptor elektron dalam respirasi anaerob (Purwoko 2007). Di alam bakteri pereduksi nitrat berperan dalam degradasi senyawa organik pada lingkungan oksigen terbatas atau anaerob. Bakteri pereduksi nitrat juga merupakan bagian dari mikroorganisma yang terlibat dalam siklus biogeokimia nitrogen global. Kelompok bakteri ini dapat mengurangi kadar nitrogen tanah pertanian (kelompok denitrifikasi), bermanfaat dalam pengolahan air limbah, perbaikan kualitas perairan seperti tambak (Madigan et al. 2006; Maier et al. 2000; Widiyanto 2006). Pada sisi lain kelompok bakteri ini dapat menghasilkan produk samping atau produk antara gas nitrous oksida (N 2 O). Gas N 2 O merupakan salah satu gas rumah kaca yang dapat meningkatkan pemanasan global seperti gas CO 2 dan CH 4. Penambahan gas N 2 O setiap tahunnya 0,2-0,3% (Conrad 1995) dengan kalor jenis N 2 O lebih besar dan waktu tinggal (residence time) di atmosfer lebih lama, maka jumlah kalor yang diserap oleh N 2 O tinggi. Gas N 2 O memiliki potensi penyerapan panas 150 kali lebih besar dari pada gas CO 2. Pada stratosfer N 2 O dapat terfotolisis menjadi NO atau N 2 yang menyebabkan terjadinya pengkisan lapisan ozon (Rusmana 2003c). Proses Fotolisis N 2 O menjadi NO atau N 2 dapat mengubah senyawa ozon (O 3 ) menjadi gas oksigen (O 2 ). Hal tersebut memperbesar radiasi cahaya matahari terhadap bumi. N 2 O diperkirakan sebanyak 90% berasal dari proses biotik (Rusmana 2003c). Penambahan pupuk nitrogen, limbah senyawa nitrogen dari industri, dan pembakaran bahan bakar fosil memperbesar emisi senyawa N 2 O. Terdapat hubungan linier antara penambahan pupuk nitrogen pada areal pertanian dengan peningkatan emisi N 2 O (Li 2004). Pencemaran nitrogen dari daratan terakumulasi di muara sungai. Mikroorganisma pereduksi nitrat menjadi dominan pada muara sungai yang tercemar senyawa nitrogen termasuk bakteri DNRA yang bersifat fermentatif (Rusmana dan Nedwell 2004).
18 Proses pembentukan N 2 O pada bakteri DNRA bukan sebagai senyawa antara seperti yang dihasilkan oleh bakteri denitrifikasi, tetapi merupakan produk samping melalui reaksi kimia dalam menghasilkan amonium (Rusmana 2003a). Kelompok bakteri ini memanfatkan senyawa nitrat sebagai penerima elektron alternatif untuk mendapatkan energi dibawah kondisi oksigen terbatas (Ricardson et al. 2001). Purwoko (2007) menyatakan bahwa fermentasi sebenarnya merupakan proses yang tidak memerlukan oksigen tetapi organisma fermentatif terkadang memerlukan oksigen untuk proses metabolisma lainnya maupun pertumbuhannya. Walaupun nitrat amonifikasi disimilatif dan denitrifikasi termasuk proses anoksik tetapi reduksi nitrat dapat terjadi pada kondisi aerob. Jenis bakteri yang dapat melakukan reduksi nitrat pada kondisi aerob diantaranya Escherichia coli, Thiosphaera pantotropha, dan Pseudomonas aeroginosa (Carter et al. 1995). Kemampuan bakteri tersebut mereduksi nitrat pada kondisi aerob dan anaerob berkaitan dengan enzim yang dimilikinya. Enzim nitrat reduktase pada membran sel (Nar) aktivitasnya dapat dipengaruhi oleh konsentrasi oksigen, dimana oksigen menghambat sistem transpor nitrat ke membran. Enzim Nap yang mereduksi nitrat dalam periplasma tidak sensitif terhadap oksigen. Ekspresi gen nar dipengaruhi oleh ketersediaan oksigen dan nitrit sedangkan gen nap tidak (Moreno - Vivian et al. 1999). Menurut Holt et al. (1994) sebagian besar bakteri fermentatif memiliki dua jalur metabolisma, yaitu respirasi dan fermentatif. Secara umum bakteri fermentatif pereduksi nitrat bersifat anaerob fakultatif, Desulfovibrio desulfuricans adalah salah satu bakteri yang dapat memanfaatkan nitrat atau sulfat sebagai akseptor elektron yang bersifat anaerob obligat. Keberadaan oksigen berpengaruh pada aktivitas reduksi nitrat bakteri fermentatif. Terdapat hubungan antara ketersediaan oksigen dengan pembentukan amonium hasil aktivitas bakteri fermentatif. Hasil penelitian pada sedimen perairan estuari Colne di Inggris menunjukkan konsentrasi amonium bertambah dengan bertambahnya kedalaman (Rusmana 2003a). Hasil penelitian yang dilakukan Bonin et al. (1989) menunjukkan bahwa pembentukan nitrat, nitrit dan N 2 O oleh Pseudomonas nautica pada konsentrasi
19 oksigen lebih besar dari 4,05 mg/l; 2,15 mg/l; 0,25 mg/l sepenuhnya dihambat. Demikian juga pada percobaan Kester et al. (1997) menunjukkan bahwa pada kultur Alcaligenes eutropus, Nitrosomonas europia dan Pseudomonas stutzeri dengan aerasi berbeda didapatkan jumlah produk yang berbeda. Pada udara saturasi 80 % produksi NO dan N 2 O adalah 0,87% dan 0,17%, sedangkan pada udara saturasi 1% berubah menjadi 2,32% dan 0,78%. Kemampuan mereduksi nitrat Pseudomonas stutzeri pada udara saturasi 90% setelah diinkubasi 92 jam, dengan sumber karbon suksinat adalah 99,24%. Sementara itu pada Thiosphaera pantotropha ATCC pada kondisi udara saturasi, suhu dan sumber karbon yang sama adalah 27,29% (Su et.al 2000). Berdasarkan beberapa penelitian tersebut yang banyak dilakukan pada kelompok bakteri denitrifikasi dan bakteri yang berasal dari daerah beriklim sedang, maka perlu dilakukan pengujian pengaruh konsentrasi oksigen terhadap kinetika aktivitas bakteri DNRA muara sungai di daerah tropik. Pengaruh oksigen sebagai sesama akseptor elektron terhadap efektivitas reduksi nitrat menjadi amonium perlu diamati, termasuk prediksi senyawa N 2 O yang dihasilkan. Hasil penelitian ini diharapkan dapat melengkapi pengetahuan fisiologi respirasi bakteri pereduksi nitrat. Langkah selanjutnya adalah kemungkinan kelompok bakteri ini dapat dimanfaatkan dalam strategi penanggulangan masalah lingkungan seperti pengolahan limbah dan perairan tercemar, konservasi kesuburan tanah dan menjaga kualitas perairan seperti tambak, danau tanpa menimbulkan emisi Nitrous Oksida (N 2 O). Tujuan Penelitian ini bertujuan untuk mengetahui pengaruh konsentrasi oksigen terhadap kinetika aktivitas reduksi nitrat oleh bakteri nitrat amonifikasi disimilatif yang berasal dari muara Sungai Cimandiri Sukabumi Jawa Barat dan muara Sungai Cisadane Tanggerang Banten.
20 TINJAUAN PUSTAKA Muara sungai Muara sungai termasuk ke dalam ekosistem estuari, dimana air tawar dan air laut bercampur. Bahan-bahan organik dan anorganik yang terdapat di muara sungai sebagian diendapkan, terlarut dan terbawa oleh arus ke laut. Salah satu proses yang mempengaruhi konsentrasi bahan-bahan organik dan anorganik pada muara sungai adalah proses biologi (Chester 1990). Menurut Dahuri et al. (1996) kualitas air suatu perairan pesisir seperti muara dicirikan oleh karakteristik kimianya yang mudah dipengaruhi oleh masukan air yang berasal dari daratan (melalui sungai) dan lautan sekitarnya. Proses pembuangan limbah dari daratan melalui aliran sungai atau dari lautan yang berlangsung secara terus menerus akan mengakibatkan turunnya kualitas air muara sungai. Pencemaran muara sungai oleh senyawa nitrogen lebih dominan berasal dari daratan. Pada muara sungai terjadi daur biogeokimia nitrogen, yaitu terjadinya perubahan-perubahan senyawa atau unsur nitrogen dalam medium dan peristiwa yang berbeda. Beberapa proses transformasi senyawa nitrogen melibatkan berbagai jenis bakteri yaitu bakteri yang berperan dalam amonifikasi, asimilasi, fiksasi, nitrifikasi dan reduksi nitrat disimilatif. Amonifikasi adalah proses pembentukan amonia dari materi organik dilakukan oleh bakteri dan cendawan safrofit. Asimilasi adalah proses pemanfaatan senyawa nitrogen anorganik untuk pembentukan asam amino dalam protoplasma. Fiksasi nitrogen yaitu peristiwa pengikatan gas nitrogen (N 2 ) umumnya terjadi di daratan, simbiosis alga di perairan dan percampuran nitrogen dari atmosfer. Nitrifikasi merupakan reaksi oksidasi pembentukan nitrat yang berasal dari amonia. Reduksi nitrat disimilatif merupakan reaksi reduksi terhadap nitrat dimana nitrat direduksi melalui tahap-tahap tertentu dengan hasil akhir amonium atau gas nitrogen. Reduksi nitrat disimilatif yang dominan terjadi di atas sedimen muara sungai adalah denitrifikasi (Dong et al. 2002). Denitrifikasi yaitu reaksi reduksi yang mengubah nitrat menjadi nitrit, nitrit oksida, nitrous oksida dan terakhir gas nitrogen. Reduksi nitrat disimilatif yang dominan pada
21 bagian sedimen muara sungai adalah nitrat amonifikasi disimilatif (Rusmana 2003a). Madigan et al. (2006) menyatakan proses penghilangan senyawa nitrogen di tanah dan perairan melalui proses denitrifikasi dan anaerob ammonia oxidation (anammox). Kedua proses tersebut menghasilkan gas nitrogen dan nitrous oksida (denitrifikasi) sebagai produk akhir. Proses ini jika terjadi di areal pertanian dapat menurunkan produktivitas hasil pertanian. Senyawa-senyawa nitrogen yang terdapat di muara sungai secara umum terlibat dalam daur biogeokimia seperti yang dijelaskan oleh Kennish (1994) seperti terlihat pada Gambar 1. Gambar 1 Daur biogeokimia nitrogen di perairan
22 Muara Sungai Cimandiri dan Cisadane Muara Sungai Cimandiri kabupaten Sukabumi Jawa Barat, merupakan muara sungai yang telah tercemar. Berbagai sampah rumah tangga / pemukiman, limbah areal pertanian (sawah, perkebunan) dan bahan-bahan lain sepanjang Daerah Aliran Sungai (DAS) Sungai Cimandiri terakumulasi di muara. Kualitas air pada muara sungai Cimandiri sudah mengalami penurunan (Marnis 2008). Selain limbah yang masuk ke perairan sungai, aktivitas penambangan pasir sepanjang DAS menyebabkan warna perairan di sekitar muara menjadi coklat sampai jarak yang cukup jauh dari pantai (Marnis 2008). Pada kondisi kimia dan fisik perairan seperti itu akan memicu pertumbuhan mikroorganismamikroorganisma aerob fakultatif dan anaerob disamping bakteri aerob, termasuk mikroorganisme yang memanfaatkan senyawa nitrogen baik organik (protein, asam amino) atau senyawa anorganik (nitrat, nitrit, dan amonium). Muara Sungai Cisadane merupakan muara sungai yang tingkat pencemarannya lebih tinggi dari muara Sungai Cimandiri. Sungai Cisadane selain sebagai sumber air yang dimanfaatkan penduduk untuk keperluan sehari-hari, juga merupakan sumber perairan pertanian. Disamping itu berfungsi sebagai tempat penampungan limbah yang berasal dari limbah rumah tangga, industri, pertanian dan perternakan (Brahmana & Suriati 2001). Beberapa parameter kualitas air yang menunjukkan muara Sungai Cisadane tercemar adalah rendahnya kandungan oksigen terlarut, tingginya konsentrasi nitrit dan amonia serta suhu perairan yang tinggi. Kandungan oksigen terlarut berkisar antara 0,39-2,33 mg/l, dan suhu 32,0-32,6 0 C. Kandungan senyawa nitrit 0,03-0,14 mg/l dan amonia 0,09-1,19 mg/l (Syahputra 2007). Tingkat pencemaran muara Sungai Cisadane pada musim hujan akan lebih rendah karena faktor pengenceran oleh air hujan, termasuk air hujan dari hulu melalui aliran sungai. Muara sungai yang banyak mengandung limbah organik dan anorganik yang mengandung senyawa nitrogen diduga menghasilkan emisi Nitrous Oksida (N 2 O) yang lebih besar. Emisi N 2 O dari perairan dan muara kurang lebih 66%, produksi gas ini berkorelasi positif dengan konsentrasi nitrat atau nitrit perairan (Seitzinger & Kroezen 1998; Rusmana 2003c).
23 Pada kedua muara sungai diatas senyawa nitrogen umumnya berasal dari limbah organik rumah tangga sepanjang daerah aliran sungai yang mengalami dekomposisi, limbah pupuk nitrogen anorganik areal pertanian dan senyawa nitrogen anorganik tanah yang mengalami erosi tepi sungai. Sumber senyawa nitrogen lain berasal dari proses nitrifikasi, proses dekomposisi mikroorganisma dan eksresi organisma di habitat muara sungai serta gas oksida nitrogen dari udara yang terlarut melalui air hujan. Limbah industri merupakan faktor utama pencemaran yang meningkatkan senyawa nitrogen pada muara Sungai Cisadane disamping faktor-faktor di atas. Bakteri Pereduksi Nitrat Kelompok bakteri pereduksi nitrat merupakan mikroorganisma yang terlibat dalam daur nitrogen di alam. Kelompok bakteri ini berperanan dalam pengubahan senyawa nitrat menjadi produk akhir gas nitrogen atau senyawa amonium. Rusmana (2003b) menyatakan bahwa terdapat tiga proses reduksi nitrat disimilatif pada bakteri yaitu denitrifikasi, reduksi nitrat menjadi amonium disimilatif dan oksidasi amonium disimilatif (anaerob ammonia oxidation, anammox). Denitrifikasi adalah proses reduksi nitrat menjadi N 2 O atau N 2. Pada proses ini bakteri menggunakan nitrat sebagai penerima elektron terakhir untuk memperoleh energi pada kondisi O 2 terbatas atau anaerob (Zumft 1997; Ricardson 2000; Ricardson et al. 2001). Reduksi nitrat menjadi amonium disimilatif adalah proses untuk menghilangkan kelebihan tenaga pereduksi dan menunjang pertumbuhan bakteri pada kondisi anaerob (Cole 1996). Anamoks adalah oksidasi amonia secara anaerobik dimana terjadi pengubahan amonium dan nitrat atau nitrit menjadi gas nitrogen. Pada metabolisma ini membentuk senyawa antara hidroksil amin dan hidrazin (Jetten et al. 2001). Tiga lintasan proses reduksi nitrat oleh aktivitas bakteri dapat digambarkan sebagai berikut (Rusmana 2003b).
24 NO 3 - NO 2 - NO NO N 2 O N 2 O N 2 O N 2 O NH 4 N 2 N 2 (1) (1) (2) (3) - NO 3 - NO 2 NH 2 OH NH 4 N 2 H 2 N 2 (2) (3) NH 2 OH NH 3 N 2 H 2 N 2 (3) NH 3 Gambar 2 Lintasan reduksi nitrat oleh aktivitas bakteri (1) Denitrifikasi, (2).Reduksi nitrat amonifikasi disimilatif (3) Oksidasi amonia secara anaerob. Enzim-Enzim yang Berperan pada Reduksi Nitrat Kelompok bakteri pereduksi nitrat baik denitrifikasi, bakteri DNRA maupun anamoks memiliki enzim-enzim tertentu untuk mengkatalisasi reaksi-reaksi reduksi nitrat. Enzim pada bakteri denitrifikasi adalah nitrat reduktase (Nar dan Nap), Nitrit reduktase (Nir), Nitrit oksid reduktase (Nor), Nitrous oksid reduktase (Nos) (Moreno - Vivian et al. 1999; Zumft 1997; Ricardson et al. 2001). Bakteri DNRA memiliki enzim nitrat reduktase (Nap dan Nar) yang mereduksi nitrat menjadi nitrit dan dua enzim yang mereduksi nitrat menjadi amonium yaitu Nir B (Harbone et al. 1992) dan enzim formate dependent nitrite reduction to amonium atau Nrf (Cole 1996). Pada spesies tertentu seperti Wollinella succinogens dan Campylobacter fetus memiliki enzim nitrous oksida reduktase (Nos). Enzim ini mereduksi gas N 2 O menjadi gas Nitrogen (Zumft 1997). Enzim yang terdapat pada bakteri anamoks adalah nitrit reducing enzyme (NR) yaitu enzim yang mereduksi nitrit menjadi hidroksil amin (NH 2 OH). Hidrazin Hidrolase (HH) enzim yang mereduksi hidroksilamin menjadi hidrazin (N 2 H 4 ) dan Hydrazine oxidising enzyme (HZO), enzim yang mengoksidasi hidrazin menjadi gas nitrogen (Jetten et al. 2001).
25 Bakteri Nitrat Amonifikasi Disimilatif (DNRA) Pada kondisi yang sesuai beberapa genus dapat mereduksi nitrit menjadi amonia melalui proses reduksi nitrat disimilasif. Prosesnya berlangsung pada saat kandungan senyawa nitrit tinggi (Kelso et al. 1997). Kelompok bakteri ini bersifat fermentatif (Rusmana & Nedwell 2004), dapat memanfaatkan senyawa organik untuk pembentukan energi melalui transfer elektron di sitoplasma (Purwoko 2007). Purwoko (2007) mengemukakan bahwa sebagian besar prokariota fermentatif menghasilkan semua ATP melalui fosforilasi tingkat subtrat, kemudian ATP dihidrolisis oleh ATP sintetase, sehingga dapat menghasilkan perbedaan potensial yang digunakan untuk aktivitas membran. Organisma fermentatif memerlukan akseptor elektron untuk menerima elektron dari NADH. Kelompok bakteri pereduksi nitrat dapat memanfaatkan senyawa nitrat sebagai penerima elektron alternatif untuk mendapatkan energi dibawah kondisi oksigen terbatas (Ricardson et al. 2001). Kelompok bakteri DNRA mereduksi senyawa nitrat sejalan dengan penambahan senyawa nitrit, ketika konsentrasi nitrat rendah terjadi penambahan senyawa amonium (Kelso et al. 1997). Pada beberapa pengamatan di lapangan menunjukkan bahwa proses nitrat amonifikasi disimilatif banyak terjadi pada suhu tinggi (Herbert & Nedwell 1990). Bakteri DNRA lebih dominan pada lingkungan yang rasio C/N nya tinggi (Nedwell 1982). Bakteri DNRA lebih kompetitif dari pada bakteri denitrifikasi pada konsentrasi bahan organik tinggi. Bakteri-bakteri nitrat amonifikasi disimilatif diantaranya adalah Bacillus pyocyanes, Clostridium pasteurianum, Desulfovibrio desulfuricans (Moat et al. 2002). Bacillus licheniformis, Wollinella succinogenes, Citrobacter freundii, Klebsiella oxytoca, K. Pneumonia, Escherichia coli (Rusmana 2003a). Rusmana (2003a) telah mengisolasi dan mengkarakterisasi Klebsiella pneumonia yang mereduksi nitrat menjadi amonium dan menghasilkan N 2 O sebagai produk sampingnya. Syahputra (2007) telah mengisolasi dan menyeleksi bakteri nitrat amonifikasi disimilatif dari muara sungai Cisadane. Isolat terpilih dikarakterisasi mempunyai kemiripan dengan Escherichia sp 21 CR dengan
26 tingkat kemiripan 97%. Sebagian besar famili Enterobacteriaceae mereduksi nitrat dan bersifat fermentatif (Holt et al. 1994). Proses pembentukan N 2 O pada kelompok bakteri nitrat amonifikasi disimilatif bukan sebagai senyawa antara seperti pada kelompok bakteri denitrifikasi, tetapi merupakan produk samping melalui reaksi kimia dalam menghasilkan amonium (Rusmana 2003a). Bagan proses reaksi kimia reduksi nitrat ke amonium dapat ditunjukkan pada Gambar 3. N 2 O NO 3 - NO 2 - NO N 2 O 2 H 2 NOH NH 2 OH NH 4 + Gambar 3 Bagan pembentukan N 2 O pada reduksi nitrat oleh bakteri DNRA (Darjamurni 2003) Pada kelompok bakteri DNRA terjadi dua tahap reaksi enzimatik yaitu tahap pertama oleh enzim Nap dan Nar seperti pada bakteri dinitrifikasi. Patereu et al. (1994) menyatakan bahwa ada dua tipe enzim yang mereduksi nitrat menjadi nitrit yaitu nitrat reduktase yang terdapat pada membran (Nar) dan nitrat reduktase yang terdapat pada periplasmik (Nap). Enzim Nar aktivitasnya berhubungan langsung dengan proses respirasi pembentukan ATP yang dapat dipengaruhi oleh konsentrasi oksigen dimana oksigen menghambat sistem transpor nitrat. Enzim Nap yang mereduksi nitrat dalam periplasma tidak sensitif terhadap oksigen. Enzim Nar yang terdapat di membran plasma mempunyai transmembran proton motive force (PMF) tempat terjadinya sintesis ATP (Moreno- Vivian et.al 1999). Demikian pula menurut Carter et al. (1995) reduksi nitrat dalam periplasma tidak sensitif terhadap hambatan oksigen. Oleh karena itu, nitrat reduktase periplasmik berhubungan dengan kemampuan untuk respirasi nitrat dalam ketersediaan oksigen pada spesies laboratorium. Oksidasi quinol oleh nitrat reduktase periplasmik tidak terpusat untuk menghasilkan gradien proton elektrokimia, tetapi cukup bertindak sebagai katup untuk membantu keseimbangan regulasi reaksi redoks dan mempertahankan jalannya rantai respirasi aerobik.
27 Enzim Nap merupakan komplek dari dua sub unit protein. Sub unit Nap A mengikat kofaktor Molibdenum (Mo) sebagai sisi aktif dari enzim. Sub unit Nap B mempunyai dua situs ikatan heme C yang memiliki perbedaan potensial. Nap C merupakan sitokrom tipe tetraheme C, berperan dalam transfer elektron antara Quinol dan Nap AB (Richardson 2000). Reaksi enzimatik tahap kedua yaitu perubahan nitrit menjadi amonium oleh enzim Nir B yang aktivitasnya bergantung pada NADH sitoplasma sebagai donor elektron (Harbone et al. 1992) dan enzim Nrf yang aktivitasnya bergantung pada format sebagai donor elektron (Cole 1996). Dalam Richardson (2000) kinerja enzim pereduksi nitrat menjadi amonium disimilatif digambarkan sebagai berikut (Gambar 4). Periplasma NapB NapA NO 2 - NO 3 - NH 4 + NO 2 - NrfA NO 3 - NO 2 - NrfB NrfB NapC NrfC NrfC NarI Membran plasma NrfD NO 3 - NO 2 - NarH NarG NirD Sitoplasma NO 3 - NO 2 - NirB Gambar 4 Enzim pereduksi nitrat bakteri nitrat amonifikasi disimilatif Ketersediaan oksigen di lingkungan pada bakteri nitrat amonifikasi disimilatif diantaranya berkaitan erat dengan sistem sensor regulator sebagai mikroorganisme anaerob fakultatif. Kelompok bakteri DNRA memiliki kemampuan adaptasi dari aerob ke anaerob atau sebaliknya. Oksigen merepresi sintesis reduktase anaerob, sebaliknya pada kondisi oksigen terbatas akan merepresi sintesis ketoglutarat dehidrogenase. Hal ini mengakibatkan perubahan NO 2 - NH 4 +
28 kondisi jalur asam sitrat dari siklus TCA oksidatif menjadi non siklus/ reduktif (White 1995). Pada White (1995) dijelaskan bahwa pergantian respirasi oksidatif dan reduktif Escherichia coli sebagai salah satu bakteri DNRA diatur oleh tiga sistem, yaitu sistem Arc (Aerobic respiration control), sistem Nar (Nitrat anaerobic respiration) dan sistem Fnr. Sistem Arc merupakan sistem dua komponen. Sistem ini merepresi gen-gen aerob berupa enzim-enzim siklus asam sitrat, piruvat dehidrogenase, asam lemak oksidase, dan sitokrom oksidase. Selain itu sistem Arc menginduksi gen-gen mikroaerob (sitokrom d oksidase dan sintesis kobal alamin). Sistem Nar terdiri dari 3 protein yaitu Nar X, Nar L dan Nar Q. Sistem ini juga merupakan sistem dua komponen, Nar X berperan sebagai histidin kinase, sedangkan Nar L sebagai protein regulator respons. Sistem ini menginduksi sintesis transkripsi gen nitrat reduktase dan menghambat gen fumarat reduktase serta gen aerobik lainnya. Penelitian selanjutnya diketahui bahwa Nar Q juga berperan sebagai penerima sensor (White 1995 ; Purwoko 2007). Sistem Fnr merupakan sistem tunggal yang berperanan pada kondisi anaerob. Protein Fnr berperan sebagai regulator positif untuk transkripsi gen-gen dalam pertumbuhan anaerob dan regulator negatif untuk transkripsi gen-gen pertumbuhan aerob (White 1995 ; Purwoko 2007). METODE PENELITIAN Waktu dan Tempat penelitian Penelitian ini dilaksanakan pada bulan Oktober 2008 sampai Maret Tempat penelitian di Laboratorium Mikrobiologi Departemen Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor. Bahan Penelitian Isolat yang digunakan dalam penelitian ini adalah bakteri nitrat amonifikasi disimilatif (DNRA) koleksi Laboratorium Mikrobiologi Departemen Biologi, FMIPA IPB Bogor. Isolat merupakan bakteri terpilih dari penelitian sebelumnya hasil isolasi dari muara Sungai Cimandiri Pelabuhan Ratu Sukabumi Jawa Barat
29 dan muara Sungai Cisadane Tangerang Banten. Kode isolat dari muara Sungai Cimandiri adalah FR1 dan FR2 (Marnis 2008). Kode isolat dari muara Sungai Cisadane HF7 dan LF6 (Syahputra 2007). Konfirmasi dan Peremajaan Isolat. Peremajaan isolat murni dimulai dengan konfirmasi kemurnian isolat menggunakan media padat, dilanjutkan dengan peremajaan isolat murni pada media cair. Komposisi media cair adalah: 10 g Natrium asetat, 4,2 g NaNO 3, 3,0 g yeast ekstrak, 0,5 g (NH 4 ) 2 SO 4, 0,9 g K 2 HPO 4. 3 H 2 O, 0,5 g MgSO 4. 7H 2 O, 0,2 g KH 2 PO 4, 0,1 g CaCl 2.2H 2 O dengan salinitas 2% dan ph 7 (Rodina 1972). Media padat dibuat sama dengan media cair ditambah agar bacto 20 g per liter. Media disterilisasi pada suhu C tekanan udara 1 atmosfer selama 15 menit. Konfirmasi kemurnian isolat dilakukan dengan cara diinokulasikan masingmasing isolat murni bakteri nitrat amonifikasi disimilatif dengan metoda cawan gores pada medium agar, kemudian diinkubasikan selama 7 hari. Karakterisasi dan morfologi sel tiap isolat dilakukan dengan teknik pewarnaan gram (Hadioetomo 1993). Konfirmasi kemurnian isolat secara fisiologi dilakukan dengan uji fermentatif. Keempat isolat ditumbuhkan pada medium glukosa dengan indikator brom cressol purple. Isolat diletakkan pada tabung bertutup untuk membatasi masukan oksigen. Uji ini dilakukan untuk melihat kemampuan fermentasi dari tiap isolat. Perubahan warna ungu menjadi kuning menunjukkan isolat tersebut melakukan fermentasi, jika tidak terjadi perubahan warna bukan kelompok bakteri fermentatif. Peremajaan bakteri pada medium cair dilakukan dengan cara diinokulasikan 1 lup tiap isolat pada medium cair masing-masing sebanyak 20 ml kedalam botol yang berukuran 100 ml. Inkubasi dilakukan selama 24 jam Tahap selanjutnya masing-masing isolat diambil 1 ml dimasukkan ke medium 50 ml untuk perbanyakan inokulan dan diinkubasikan selama 24 jam.
30 Seleksi Aktivitas Reduksi Nitrat pada Konsentrasi Oksigen (O 2 ) yang Berbeda Pengukuran aktivitas reduksi nitrat pada konsentrasi oksigen berbeda dilakukan pada botol serum steril 75 ml yang ditutup dengan butyl rubber septum. Pengkondisian konsentrasi oksigen dengan pengaturan volume saturasi udara pada head space botol serum. Botol serum steril volume 75 ml diisi dengan 23 ml medium cair. Botol dibuat kondisi an aerobik dengan cara menghilangkan oksigen yang terdapat di dalam botol. Gas nitrogen bebas oksigen dialirkan ke dalam botol reaksi dengan menggunakan jarum/syringe steril selama 15 menit. Sebelum gas dimasukkan, gas terlebih dahulu disaring dengan filter steril diameter 47 mm dengan ukuran 0,45 mikro meter. Langkah berikutnya, saturasi udara pada masing-masing botol dikondisikan menjadi 0%, 1%, 10%, 30%, 50%, 80%, dan 100%. Saturasi udara dimasukkan pada masing-masing botol serum yang telah diberi perlakuan pembebasan oksigen sebanyak 0,5 ml, 5 ml, 15 ml, 25 ml, dan 40 ml. Pada waktu proses pemasukan saturasi udara, gas nitrogen akan terdorong keluar melalui jarum yang dipasang pada tutup botol disamping syringe, sehingga volume saturasi udara pada masingmasing botol menjadi 1%, 10%, 30%, 50%, 80%. Pengkondisian saturasi udara 100% dilakukan dengan tanpa memasukkan gas nitrogen murni pada botol serum. Kondisi saturasi udara 0% dengan pengisian gas nitrogen murni tanpa memasukkan saturasi udara. Seluruh botol serum yang telah dikondisikan saturasi udaranya dikocok untuk melarutkan gas perlakuan. Masing-masing botol serum diinokulasi dengan 1 ml isolat. Isolat diletakan pada inkubator berpenggoyang pada kecepatan 80 rpm suhu ruang (28-31) o C selama 96 jam (Su et al. 2001). Setelah diinkubasi pada kadar oksigen yang berbeda, dilakukan pengukuran densitas sel dengan spektrofotometer pada panjang gelombang 620 nm. Kultur biakan bakteri diambil sebanyak 1ml pada tabung efendorf dan disentrifugasi dengan kecepatan 4000 rpm selama 15 menit untuk mendapatkan supernatan. Supernatan dari kultur biakan dianalisis kandungan nitrit, nitrat dan amonium.
31 Analisis nitrit. Analisis Nitrit menggunakan metode Sulfanilamide (Cleseri et al 1989). Nitrit dengan amina aromatik pada sulfalinamide akan membentuk diazonium. Senyawa tersebut dengan NED (N-I-Naphtyl Ethylene Diamine Dyhidrochloride) membentuk gugus kromofor yang berwarna merah muda (Lampiran 1) dan dapat diukur dengan spektrofotometer pada panjang gelombang 540 nm. Kadar nitrit ditentukan dengan cara memasukkan 5 ml sampel yang telah diencerkan kedalam tabung reaksi, ditambahkan 0,1 sulfanilamid (C 6 H 8 N 2 O 2 S) dan 0,1 NED. Kemudian diukur absorbansinya dengan spektrofotometer pada panjang gelombang 540 nm. Kurva standar natrium nitrit (NaNO 2 ) dengan konsentrasi sebesar : 0 ; 0,2; 0,4; 0,6; 0,8, dan 1,0 mg/l kemudian dikonversi ke mm digunakan untuk menentukan kadar nitrit pada sampel (Lampiran 2). Analisis nitrat Analisis senyawa nitrat dengan menggunakan metode Greenberg et al (1992). Kadar nitrat ditentukan dengan cara memasukkan 20 ml sampel yang telah diencerkan ke dalam kolom reduksi yang berisi cadmium. Pada saat sampel melewati kolom reduksi, cadmium akan mereduksi nitrat menjadi nitrit. Sampel sebanyak 5 ml direaksikan dengan reagen pada analisis nitrit. Sampel akan menunjukkan perubahan warna merah muda (Lampiran 1), diukur pada panjang gelombang 540 nm. Kurva standar natrium nitrit (NaNO 2 ) dengan konsentrasi sebesar : 0 ; 0,2; 0,4; 0,6; 0,8; dan 1,0 mg/l, kemudian dikonversi ke mm digunakan untuk menentukan kadar nitrit pada sampel. Nilai konsentrasi nitrat adalah hasil pengurangan antara konsentrasi nitrit yang dilewatkan pada kolom reduksi dengan konsentrasi nitrit yang tidak dilewatkan. Analisis amonium Pengukuran konsentrasi amonium menggunakan metode phenate (Cleseri et al. 1989). Kadar amonium ditentukan dengan cara 5 ml sampel yang diencerkan, dimasukkan kedalam tabung reaksi, ditambahkan 0,2 ml larutan fenol alkohol (C 6 H 5 OH) lalu dihomogenkan, diamkan selama 1 menit lalu tambahkan 0,2 ml Na-Dihidro Nitroprusid (Na 2 [Fe(CN)NO] 2. H 2 O), kemudian ditambahkan 0,5 ml larutan oksidan yang terdiri dari Natrium Sitrat (C 6 H 5 Na 3 O 7.2H 2 O) dan Natrium
32 hipoklorit (NaOCl 2 ) dan dibiarkan selama satu jam pada suhu ruang (28-31) o C. Sampel yang telah diberi larutan indikator menunjukkan perubahan warna hijau sampai biru (Lampiran 1), diukur dengan spektrofotometer pada panjang gelombang 640 nm. Kurva standar amonium klorida (NH 4 Cl) sebesar: 0 ; 0,2; 0,4; 0,6; 0,8 ; 1,0; 2,0; 4,0; dan 8,0 mg/l kemudian dikonversi ke mm digunakan untuk menghitung konsentrasi amonia pada sampel (Lampiran 2). Perhitungan Pembentukan Gas. Setelah konsentrasi nitrat (NO - 3 ), nitrit (NO - 2 ), dan amonium (NH + 4 ) diketahui dari masing-masing sampel, dihitung jumlah nitrat yang tereduksi dengan rumus : [NO - 3 ] tereduksi = [NO - 3 ] kontrol [NO - 3 ] inokulasi % [NO - 3 ] tereduksi = [NO - 3 ] red x 100 [NO - 3 ] kontrol Jumlah senyawa nitrit yang terbentuk dihitung dengan rumus sebagai berikut: [NO - 2 ] terbentuk = [NO - 2 ] perlakuan [NO - 2 ] kontrol %[NO - 2 ] terbentuk = [NO - 2 ] perlakuan [NO - 2 ] kontrol x 100 [NO - 3 ] tereduksi Jumlah senyawa amonium yang terbentuk dihitung dengan rumus sebagai berikut: [NH + 4 ] terbentuk = [NH + 4 ] perlakuan [NH + 4 ] kontrol % [NH + 4 ] terbentuk = [NH + 4 ] perlakuan [NH + 4 ] kontrol x 100 [NO - 3 ] tereduksi Estimasi produk akhir gas yang terbentuk dihitung dengan rumus [Gas ] = [NO - 3 ] reduksi [NO - 2 ] terbentuk [NH + 4 ] terbentuk % [ Gas] = [Gas] X 100% [NO - 3 ] tereduksi Keterangan : Konsentrasi nitrat kontrol didapatkan dari sediaan medium steril tanpa bakteri.
33 Kinetika Aktivitas Reduksi Nitrat Isolat Terpilih Dua isolat terbaik dalam mereduksi nitrat dan responsif terhadap oksigen dipilih untuk diamati kinetikanya. Botol serum steril volume 125 ml diisi dengan 50 ml medium cair. Sebanyak 1 ml isolat diinokulasikan pada tiap botol yang telah dikondisikan saturasi udaranya secara berurutan masing-masing 1 %, 10%, 100%. Kultur biakan diinkubasikan pada suhu ruang (28-31) o C selama 96 jam (Su et al 2001). Kultur biakan diamati pola pertumbuhannya dan dianalisis konsentrasi nitrat, nitrat, dan amonium dengan metoda yang telah diuraikan sebelumnya. Analisis dilakukan setiap selang waktu 12 jam selama 96 jam (4 hari). Hasil pertumbuhan digambarkan pada suatu grafik pertumbuhan pada kondisi oksigen berbeda. Korelasi antara konsentrasi sel dengan kerapatan optis (OD) isolat, dilakukan metoda hitungan cawan (Lampiran 3) pada konsentrasi pengenceran 10-6, 10-7, 10-8, dan Kultur biakan yang sama diencerkan dan OD dari beberapa pengenceran diukur. Kurva standar pertumbuhan dibuat dari nilai-nilai OD pengenceran dan konsentrasi sel sehingga didapatkan nilai regresi dan persamaan garis (Lampiran 4) untuk menentukan jumlah sel. Laju pertumbuhan spesifik maksimum didapatkan dengan mencari nilai regresi dan persamaan garis dari korelasi waktu inkubasi dengan nilai ln jumlah sel. Laju pertumbuhan maksimum merupakan koefisien variabel x pada persamaan garis Y= ax + c (Maier et al. 2000). Hasil uji kimia digambarkan dalam suatu grafik yang menunjukkan hubungan lama inkubasi dengan nitrat tereduksi, nitrit, dan amonium serta estimasi gas N 2 O yang terbentuk pada setiap konsentrasi oksigen yang berbeda. Kecepatan reduksi setiap sel masing-masing isolat dihitung pada kondisi saturasi udara 1 %, 10% dan 100%.
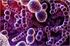
34 HASIL Karakteristik, Morfologi dan Fisiologi Bakteri Nitrat Amonifikasi Disimilatif Hasil konfirmasi kemurnian dari keempat isolat dengan metoda cawan gores, morfologi koloninya berbentuk bulat, elevasi tombol dan cembung, tepian licin. Faktor pembeda keempat isolat adalah warna koloni (Gambar 5). Gambar 5 Morfologi koloni dari isolat LF6, HF7, FR2 dan FR1 pada medium denitrifikasi Secara mikroskopis sel isolat LF6, HF7, FR2 dan FR1 berupa bakteri Gram negatif dan berbentuk batang (Tabel 1).
35 Tabel 1 Karakterisasi morfologi dan fisiologi isolat LF6, HF7,FR2, dan FR1 No Isolat Bentuk Sel Pewarnaan Morfologi Koloni Gram Bentuk Warna 1 LF6 Batang negatif Bulat, elevasi cembung, tepian licin 2 HF7 Batang negatif Bulat, elevasi cembung, tepian licin 3 FR2 Batang negatif Bulat, elevasi tombol, tepian licin 4 FR1 Batang negatif Bulat, elevasi tombol, tepian licin Putih susu Krem kuning Kuning oranye Kuning pucat Hasil uji fermentatif dengan menggunakan glukosa dan indikator brom cressol purple menunjukkan keempat isolat merupakan kelompok bakteri fermentatif (Gambar 6). Hal ini ditunjukkan dengan adanya perubahan warna medium dari ungu menjadi kuning. Kecepatan untuk merubah warna medium dari keempat isolat berbeda. Isolat LF6 dan HF7 (asal muara Sungai Cisadane) merubah warna medium glukosa dan indikator brom cressol purple dari ungu menjadi berwarna kuning dalam waktu 24 jam. Perubahan warna medium oleh isolat FR1 dan FR2 (asal muara Sungai Cimandiri) memerlukan waktu 36 jam dan 48 jam. Selain perubahan warna akibat asam organik hasil fermentasi yang meningkatkan derajat keasaman (menurunkan ph) medium, pembentukan gas karbon dioksida (CO 2 ) sebagai hasil fermentasi juga dapat diamati pada tabung durham.
36 Gambar 6 Hasil uji fermentatif pada isolat FR1, FR2, HF7 dan LF6, setelah inkubasi 48 jam Densitas Sel Isolat Bakteri DNRA pada Konsentrasi O 2 yang Berbeda Empat isolat bakteri DNRA yang ditumbuhkan pada konsentrasi oksigen berbeda, sumber karbon asetat, masa inkubasi 96 jam menunjukkan kerapatan (densitas) sel yang berbeda (Gambar 7). Secara umum densitas sel keempat isolat lebih rendah pada konsentrasi oksigen (saturasi udara) 0%, yaitu antara OD 0,06 sampai 0,28 (620 nm). Densitas sel tertinggi pada konsentrasi saturasi udara 0 % adalah isolat FR1 yaitu dengan OD sebesar 0,28. Pada konsentrasi saturasi udara 1-10% densitas sel cenderung lebih tinggi dari konsentrasi saturasi udara 0%. Pada konsentrasi saturasi udara 30%, 50% dan 80% kecenderungan densitas keempat isolat tidak seluruhnya lebih tinggi dari konsentrasi saturasi udara sebelumnya. Densitas tertinggi dari keempat isolat terdapat pada konsentrasi saturasi udara 100% yaitu dengan OD antara 0,27 sampai 0,42 (620 nm). Kecenderungan peningkatan densitas sel isolat FR1 sejalan dengan penambahan konsentrasi saturasi udara lebih nyata dari isolat lainnya. Densitas sel isolat FR1 lebih tinggi dari pada tiga isolat lainnya pada saturasi udara 0%, 30%, 50%, 80% dan 100%. Densitas sel terendah pada konsentrasi saturasi udara 100 % adalah isolat LF6 dengan OD 0,27.
37 OD (620nm) % 1% 10% 30% 50% 80% 100% Konsentrasi Saturasi udara (%) Gambar 7 Densitas sel isolat LF6, HF7, FR2, dan FR1 pada konsentrasi saturasi udara yang berbeda, setelah diinkubasi selama 96 jam pada suhu ruang (29-31) 0 C. LF6 HF7 FR2 FR1 Aktivitas Reduksi Nitrat Bakteri DNRA pada Konsentrasi Oksigen yang Berbeda Berdasarkan hasil uji nitrat (NO 3 - ) terhadap isolat FR1, FR2, HF7, dan LF6 menunjukkan kemampuan yang berbeda dalam mereduksi nitrat. Konsentrasi nitrat tereduksi oleh keempat isolat dengan nitrat awal sebanyak 49,41 mm, sumber karbon asetat setelah diinkubasi 4 hari adalah diatas 45 mm (Gambar 8). Jumlah nitrat tereduksi (mm % 1% 10% 30% 50% 80% 100% Konsentrasi Saturasi udara (%) Gambar 8 Jumlah nitrat tereduksi oleh isolat LF6, HF7, FR2, dan FR1 pada konsentrasi saturasi udara yang berbeda, setelah diinkubasi selama 96 jam pada suhu ruang (29-31) 0 C LF6 HF7 FR2 FR1
38 Secara umum kecenderungan konsentrasi nitrat tereduksi lebih besar pada konsentrasi saturasi udara lebih kecil. Reduksi nitrat terbesar terjadi pada konsentrasi saturasi udara 0%. Konsentrasi nitrat tereduksi cenderung menurun seiring dengan peningkatan konsentrasi saturasi udara. Dari hasil uji nitrit (NO - 2 ), isolat FR1 mengakumulasi nitrit paling tinggi dibandingkan isolat lainnya. Akumulasi nitrit tertinggi terjadi pada konsentrasi saturasi udara 100% (Gambar 9), yaitu 4,95 mm. Isolat LF6, HF7 dan FR2 pada akhir masa inkubasi masih mengakumulasi nitrit. Konsentrasi nitrit tertinggi pada isolat LF6 adalah 0,05 mm. Isolat HF7 dan FR2 mengakumulasi nitrit paling tinggi pada akhir masa inkubasi dengan konsentrasi yang sama yaitu 0,03 mm (Lampiran 5 dan 6) Akumulasi nitrit (mm % 1% 10% 30% 50% 80% 100% Konsentrasi Saturasi udara (%) Gambar 9 Jumlah nitrit terakumulasi dari isolat LF6, HF7, FR2, dan FR1 pada konsentrasi saturasi udara yang berbeda, setelah diinkubasi selama 96 jam pada suhu ruang (29-31) 0 C LF6 HF7 FR2 FR1 Pada uji amonium (NH + 4 ), isolat LF6 dan HF7 menghasilkan amonium lebih tinggi dari isolat lainnya (Gambar 10), sehingga diperkirakan gas yang terbentuk pada kedua isolat bakteri tersebut lebih kecil dibandingkan isolat FR1 dan FR2. Konsentrasi amonium tertinggi yang dihasilkan isolat LF6 adalah sebesar 15,02 mm (30,95%) pada konsentrasi saturasi udara 0%. Isolat HF7 menghasilkan amonium sebesar 14,77 mm (30,29%) pada konsentrasi saturasi udara 0% (Lampiran 5).
KINETIKA AKTIVITAS REDUKSI NITRAT BAKTERI NITRAT AMONIFIKASI DISIMILATIF DARI MUARA SUNGAI PADA KONSENTRASI OKSIGEN (O 2 ) YANG BERBEDA TETI MARDIATI
 KINETIKA AKTIVITAS REDUKSI NITRAT BAKTERI NITRAT AMONIFIKASI DISIMILATIF DARI MUARA SUNGAI PADA KONSENTRASI OKSIGEN (O 2 ) YANG BERBEDA TETI MARDIATI SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR BOGOR
KINETIKA AKTIVITAS REDUKSI NITRAT BAKTERI NITRAT AMONIFIKASI DISIMILATIF DARI MUARA SUNGAI PADA KONSENTRASI OKSIGEN (O 2 ) YANG BERBEDA TETI MARDIATI SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR BOGOR
AKTIVITAS REDUKSI NITRAT BAKTERI AMONIFIKASI DISIMILATIF PADA SUMBER KARBON BERBEDA AHADIYANTO SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR BOGOR
 AKTIVITAS REDUKSI NITRAT BAKTERI AMONIFIKASI DISIMILATIF PADA SUMBER KARBON BERBEDA AHADIYANTO SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR BOGOR 2009 PERNYATAAN MENGENAI TESIS DAN SUMBER INFORMASI Dengan
AKTIVITAS REDUKSI NITRAT BAKTERI AMONIFIKASI DISIMILATIF PADA SUMBER KARBON BERBEDA AHADIYANTO SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR BOGOR 2009 PERNYATAAN MENGENAI TESIS DAN SUMBER INFORMASI Dengan
TINJAUAN PUSTAKA Muara sungai
 TINJAUAN PUSTAKA Muara sungai Muara sungai termasuk ke dalam ekosistem estuari, dimana air tawar dan air laut bercampur. Bahanbahan organik dan anorganik yang terdapat di muara sungai sebagian diendapkan,
TINJAUAN PUSTAKA Muara sungai Muara sungai termasuk ke dalam ekosistem estuari, dimana air tawar dan air laut bercampur. Bahanbahan organik dan anorganik yang terdapat di muara sungai sebagian diendapkan,
TINJAUAN PUSTAKA Muara Sungai
 TINJAUAN PUSTAKA Muara Sungai Sungai Cimandiri merupakan bagian dari kawasan Daerah Aliran Sungai (DAS) yang terletak di bagian timur Teluk Pelabuhan Ratu. Posisi geografis kawasan Teluk Pelabuhan Ratu
TINJAUAN PUSTAKA Muara Sungai Sungai Cimandiri merupakan bagian dari kawasan Daerah Aliran Sungai (DAS) yang terletak di bagian timur Teluk Pelabuhan Ratu. Posisi geografis kawasan Teluk Pelabuhan Ratu
HASIL. Karakteristik, Morfologi dan Fisiologi Bakteri Nitrat Amonifikasi Disimilatif
 HASIL Karakteristik, Morfologi dan Fisiologi Bakteri Nitrat Amonifikasi Disimilatif Hasil konfirmasi kemurnian dari keempat isolat dengan metoda cawan gores, morfologi koloninya berbentuk bulat, elevasi
HASIL Karakteristik, Morfologi dan Fisiologi Bakteri Nitrat Amonifikasi Disimilatif Hasil konfirmasi kemurnian dari keempat isolat dengan metoda cawan gores, morfologi koloninya berbentuk bulat, elevasi
akseptor elektron pada saat medium aerob. Disisi lain keberadaan akseptor elektron nitrat dapat menimbulkan interaksi dan berpengaruh terhadap jalur
 PEMBAHASAN Isolat FR1, FR2, HF7 dan LF6 adalah kelompok bakteri fermentatif, tumbuh pada medium denitrifikasi yang mengandung nitrat baik secara anaerob maupun aerob. Rusmana dan Nedwell (2004), melaporkan
PEMBAHASAN Isolat FR1, FR2, HF7 dan LF6 adalah kelompok bakteri fermentatif, tumbuh pada medium denitrifikasi yang mengandung nitrat baik secara anaerob maupun aerob. Rusmana dan Nedwell (2004), melaporkan
TINJAUAN PUSTAKA Muara Sungai
 TINJAUAN PUSTAKA Muara Sungai Menurut Dahuri et al. (1996) ekosistem muara sungai adalah merupakan bagian dari wilayah pesisir. Muara adalah bentuk pantai yang tertutup, dimana air tawar dan air laut bertemu
TINJAUAN PUSTAKA Muara Sungai Menurut Dahuri et al. (1996) ekosistem muara sungai adalah merupakan bagian dari wilayah pesisir. Muara adalah bentuk pantai yang tertutup, dimana air tawar dan air laut bertemu
NFR4, berarti isolat ini paling mampu beradaptasi dengan faktor lingkungan yang ada walaupun kurang responsif terhadap perubahan konsentrasi udara
 PEMBAHASAN Pangamatan morfologi sel menunjukkan bentuk sel batang, dan ada yang bulat. Sementara koloni bervariasi dari bentuk, tepian, elevasi dan warna. Hasil pewarnaan gram menunjukan bahwa ada isolat
PEMBAHASAN Pangamatan morfologi sel menunjukkan bentuk sel batang, dan ada yang bulat. Sementara koloni bervariasi dari bentuk, tepian, elevasi dan warna. Hasil pewarnaan gram menunjukan bahwa ada isolat
Pengaruh oksigen terhadap pertumbuhan isolat lebih jelas terlihat pada grafik pertumbuhan isolat terpilih HF7 dan LF6 yang diukur setiap selang waktu
 PEMBAHASAN Isolat FR1, FR2, HF7 dan LF6 bersifat fermentatif, tumbuh pada medium denitrifikasi yang mengandung nitrat dan tumbuh pada kondisi saturasi udara dari variasi 0-100%. Hal ini menunjukkan keempat
PEMBAHASAN Isolat FR1, FR2, HF7 dan LF6 bersifat fermentatif, tumbuh pada medium denitrifikasi yang mengandung nitrat dan tumbuh pada kondisi saturasi udara dari variasi 0-100%. Hal ini menunjukkan keempat
Analisis Nitrit Analisis Chemical Oxygen Demand (COD) HASIL DAN PEMBAHASAN Isolasi dan Identifikasi Bakteri
 11 didinginkan. absorbansi diukur pada panjang gelombang 410 nm. Setelah kalibrasi sampel disaring dengan milipore dan ditambahkan 1 ml natrium arsenit. Selanjutnya 5 ml sampel dipipet ke dalam tabung
11 didinginkan. absorbansi diukur pada panjang gelombang 410 nm. Setelah kalibrasi sampel disaring dengan milipore dan ditambahkan 1 ml natrium arsenit. Selanjutnya 5 ml sampel dipipet ke dalam tabung
PERANAN MIKROORGANISME DALAM SIKLUS UNSUR DI LINGKUNGAN AKUATIK
 PERANAN MIKROORGANISME DALAM SIKLUS UNSUR DI LINGKUNGAN AKUATIK 1. Siklus Nitrogen Nitrogen merupakan limiting factor yang harus diperhatikan dalam suatu ekosistem perairan. Nitrgen di perairan terdapat
PERANAN MIKROORGANISME DALAM SIKLUS UNSUR DI LINGKUNGAN AKUATIK 1. Siklus Nitrogen Nitrogen merupakan limiting factor yang harus diperhatikan dalam suatu ekosistem perairan. Nitrgen di perairan terdapat
1 Asimilasi nitrogen dan sulfur
 BAB I PENDAHULUAN 1.1 Latar Belakang Tumbuhan tingkat tinggi merupakan organisme autotrof dapat mensintesa komponen molekular organik yang dibutuhkannya, selain juga membutuhkan hara dalam bentuk anorganik
BAB I PENDAHULUAN 1.1 Latar Belakang Tumbuhan tingkat tinggi merupakan organisme autotrof dapat mensintesa komponen molekular organik yang dibutuhkannya, selain juga membutuhkan hara dalam bentuk anorganik
BAB II TINJAUAN PUSTAKA
 BAB II TINJAUAN PUSTAKA A. Landasan Teori Keberadaan amonium di alam dapat berasal dari dekomposisi senyawa-senyawa protein. Senyawa ini perlu didegradasi menjadi gas nitrogen (N2) karena amonium menyebabkan
BAB II TINJAUAN PUSTAKA A. Landasan Teori Keberadaan amonium di alam dapat berasal dari dekomposisi senyawa-senyawa protein. Senyawa ini perlu didegradasi menjadi gas nitrogen (N2) karena amonium menyebabkan
III. METODOLOGI PENELITIAN. Penelitian ini dilakukan pada bulan Juli 2012 sampai bulan Desember 2012 di
 23 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan Juli 2012 sampai bulan Desember 2012 di Laboratorium Biokimia Jurusan Kimia Fakultas Matematika dan Ilmu
23 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan Juli 2012 sampai bulan Desember 2012 di Laboratorium Biokimia Jurusan Kimia Fakultas Matematika dan Ilmu
TINJAUAN PUSTAKA Karakteristik dan Klasifikasi Bakteri Metanotrof Metanotrof sebagai Bakteri Pengoksidasi Metan
 TINJAUAN PUSTAKA Karakteristik dan Klasifikasi Bakteri Metanotrof Bakteri metanotrof adalah bakteri Gram negatif, bersifat aerob dan menggunakan metan sebagai sumber karbon dan energi (Auman 2001). Karakteristik
TINJAUAN PUSTAKA Karakteristik dan Klasifikasi Bakteri Metanotrof Bakteri metanotrof adalah bakteri Gram negatif, bersifat aerob dan menggunakan metan sebagai sumber karbon dan energi (Auman 2001). Karakteristik
BAB 4 SIKLUS BIOGEOKIMIA
 Siklus Biogeokimia 33 BAB 4 SIKLUS BIOGEOKIMIA Kompetensi Dasar: Menjelaskan siklus karbon, nitrogen, oksigen, belerang dan fosfor A. Definisi Siklus Biogeokimia Siklus biogeokimia atau yang biasa disebut
Siklus Biogeokimia 33 BAB 4 SIKLUS BIOGEOKIMIA Kompetensi Dasar: Menjelaskan siklus karbon, nitrogen, oksigen, belerang dan fosfor A. Definisi Siklus Biogeokimia Siklus biogeokimia atau yang biasa disebut
BAB III METODE PENELITIAN
 BAB III METODE PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian dilakukan pada 4 April 2016 sampai 16 Agustus 2016. Penelitian ini dilaksanakan di Laboratorium Riset Kimia Material dan Hayati Departemen
BAB III METODE PENELITIAN 3.1 Waktu dan Lokasi Penelitian Penelitian dilakukan pada 4 April 2016 sampai 16 Agustus 2016. Penelitian ini dilaksanakan di Laboratorium Riset Kimia Material dan Hayati Departemen
BAB I PENDAHULUAN. Latar Belakang. dibicarakan karena mengancam masa depan dari kehidupan di bumi
 BAB I PENDAHULUAN Latar Belakang Perubahan iklim dewasa ini menjadi isu yang paling hangat dibicarakan karena mengancam masa depan dari kehidupan di bumi termasuk manusia. Pelepasan gas-gas yang disebabkan
BAB I PENDAHULUAN Latar Belakang Perubahan iklim dewasa ini menjadi isu yang paling hangat dibicarakan karena mengancam masa depan dari kehidupan di bumi termasuk manusia. Pelepasan gas-gas yang disebabkan
BAB VIII PROSES FOTOSINTESIS, RESPIRASI DAN FIKSASI NITROGEN OLEH TANAMAN
 BAB VIII PROSES FOTOSINTESIS, RESPIRASI DAN FIKSASI NITROGEN OLEH TANAMAN 8.1. Fotosintesis Fotosintesis atau fotosintesa merupakan proses pembuatan makanan yang terjadi pada tumbuhan hijau dengan bantuan
BAB VIII PROSES FOTOSINTESIS, RESPIRASI DAN FIKSASI NITROGEN OLEH TANAMAN 8.1. Fotosintesis Fotosintesis atau fotosintesa merupakan proses pembuatan makanan yang terjadi pada tumbuhan hijau dengan bantuan
HASIL DAN PEMBAHASAN 4.1 PENELITIAN PENDAHULUAN
 IV. HASIL DAN PEMBAHASAN.1 PENELITIAN PENDAHULUAN Penelitian pendahuluan dilakukan untuk menentukan titik kritis pengenceran limbah dan kondisi mulai mampu beradaptasi hidup pada limbah cair tahu. Limbah
IV. HASIL DAN PEMBAHASAN.1 PENELITIAN PENDAHULUAN Penelitian pendahuluan dilakukan untuk menentukan titik kritis pengenceran limbah dan kondisi mulai mampu beradaptasi hidup pada limbah cair tahu. Limbah
BAB III METODE PENELITIAN. Biologi dan Laboratorium Biokimia, Departemen Kimia Fakultas Sains dan
 BAB III METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Mikrobiologi, Departemen Biologi dan Laboratorium Biokimia, Departemen Kimia Fakultas Sains dan Teknologi,
BAB III METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Mikrobiologi, Departemen Biologi dan Laboratorium Biokimia, Departemen Kimia Fakultas Sains dan Teknologi,
4. HASIL DAN PEMBAHASAN
 4. HASIL DAN PEMBAHASAN 4.1. Pertumbuhan Mikroalga Laut Scenedesmus sp. Hasil pengamatan pengaruh kelimpahan sel Scenedesmus sp. terhadap limbah industri dengan dua pelakuan yang berbeda yaitu menggunakan
4. HASIL DAN PEMBAHASAN 4.1. Pertumbuhan Mikroalga Laut Scenedesmus sp. Hasil pengamatan pengaruh kelimpahan sel Scenedesmus sp. terhadap limbah industri dengan dua pelakuan yang berbeda yaitu menggunakan
BAB IV HASIL DAN PEMBAHASAN
 BAB IV HASIL DAN PEMBAHASAN Dalam penelitian ini, aktivitas pengurangan amonium oleh bakteri nitrifikasi dan anamox diamati pada dua jenis sampel, yaitu air limbah industri dan lindi. A. Pengurangan amonium
BAB IV HASIL DAN PEMBAHASAN Dalam penelitian ini, aktivitas pengurangan amonium oleh bakteri nitrifikasi dan anamox diamati pada dua jenis sampel, yaitu air limbah industri dan lindi. A. Pengurangan amonium
IV. HASIL DAN PEMBAHASAN
 20 IV. HASIL DAN PEMBAHASAN 4.1. Isolasi Bakteri Penitrifikasi Sumber isolat yang digunakan dalam penelitian ini berupa sampel tanah yang berada di sekitar kandang ternak dengan jenis ternak berupa sapi,
20 IV. HASIL DAN PEMBAHASAN 4.1. Isolasi Bakteri Penitrifikasi Sumber isolat yang digunakan dalam penelitian ini berupa sampel tanah yang berada di sekitar kandang ternak dengan jenis ternak berupa sapi,
BAHAN DAN METODE Tempat dan Waktu Bahan Pertumbuhan dan Peremajaan Isolat Pengamatan Morfologi Isolat B. thuringiensis
 13 BAHAN DAN METODE Tempat dan Waktu Penelitian ini dilaksanakan di Laboratorium Mikrobiologi, Departemen Biologi, IPB, dari bulan Oktober 2011 Mei 2012. Bahan Isolasi untuk memperoleh isolat B. thuringiensis
13 BAHAN DAN METODE Tempat dan Waktu Penelitian ini dilaksanakan di Laboratorium Mikrobiologi, Departemen Biologi, IPB, dari bulan Oktober 2011 Mei 2012. Bahan Isolasi untuk memperoleh isolat B. thuringiensis
BAB IV DESKRIPSI DAN ANALISIS DATA
 BAB IV DESKRIPSI DAN ANALISIS DATA A. Deskripsi Data 1. Kondisi saluran sekunder sungai Sawojajar Saluran sekunder sungai Sawojajar merupakan aliran sungai yang mengalir ke induk sungai Sawojajar. Letak
BAB IV DESKRIPSI DAN ANALISIS DATA A. Deskripsi Data 1. Kondisi saluran sekunder sungai Sawojajar Saluran sekunder sungai Sawojajar merupakan aliran sungai yang mengalir ke induk sungai Sawojajar. Letak
METODOLOGI PENELITIAN. Penelitian ini dilakukan pada bulan April 2012 sampai dengan bulan Juni 2012 di
 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan April 2012 sampai dengan bulan Juni 2012 di Laboratorium Biokimia Jurusan Kimia Fakultas Matematika dan Ilmu
III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan April 2012 sampai dengan bulan Juni 2012 di Laboratorium Biokimia Jurusan Kimia Fakultas Matematika dan Ilmu
Potensi Desikator untuk Inkubator Anaerob
 Potensi Desikator untuk Inkubator Anaerob DISUSUN OLEH: Siti Humaidah NRP. 1506 100 030 DOSEN PEMBIMBING: Dr. rer.nat. Maya Shovitri, M.Si Nengah Dwianita Kuswytasari, S.Si., M.Si PROGRAM STUDI BIOLOGI
Potensi Desikator untuk Inkubator Anaerob DISUSUN OLEH: Siti Humaidah NRP. 1506 100 030 DOSEN PEMBIMBING: Dr. rer.nat. Maya Shovitri, M.Si Nengah Dwianita Kuswytasari, S.Si., M.Si PROGRAM STUDI BIOLOGI
Dr. Dwi Suryanto Prof. Dr. Erman Munir Nunuk Priyani, M.Sc.
 BIO210 Mikrobiologi Dr. Dwi Suryanto Prof. Dr. Erman Munir Nunuk Priyani, M.Sc. Kuliah 4-5. METABOLISME Ada 2 reaksi penting yang berlangsung dalam sel: Anabolisme reaksi kimia yang menggabungkan bahan
BIO210 Mikrobiologi Dr. Dwi Suryanto Prof. Dr. Erman Munir Nunuk Priyani, M.Sc. Kuliah 4-5. METABOLISME Ada 2 reaksi penting yang berlangsung dalam sel: Anabolisme reaksi kimia yang menggabungkan bahan
Sampel air panas. Pengenceran 10-1
 Lampiran 1. Metode kerja Sampel air panas Diambil 10 ml Dicampur dengan media selektif 90ml Di inkubasi 24 jam, suhu 50 C Pengenceran 10-1 Di encerkan sampai 10-10 Tiap pengenceran di tanam di cawan petri
Lampiran 1. Metode kerja Sampel air panas Diambil 10 ml Dicampur dengan media selektif 90ml Di inkubasi 24 jam, suhu 50 C Pengenceran 10-1 Di encerkan sampai 10-10 Tiap pengenceran di tanam di cawan petri
LAMPIRAN Lampiran 1: Komposisi dan Penyiapan Media Skim Milk Agar, Komposisi Media Feather Meal Agar, Komposisi Media Garam Cair.
 LAMPIRAN Lampiran 1: Komposisi dan Penyiapan Media Skim Milk Agar, Komposisi Media Feather Meal Agar, Komposisi Media Garam Cair. a. Komposisi media skim milk agar (Widhyastuti & Dewi, 2001) yang telah
LAMPIRAN Lampiran 1: Komposisi dan Penyiapan Media Skim Milk Agar, Komposisi Media Feather Meal Agar, Komposisi Media Garam Cair. a. Komposisi media skim milk agar (Widhyastuti & Dewi, 2001) yang telah
HASIL. Tekstur dan komposisi tanah Hasil analisis tekstur dan komposisi bahan organik pada tabel 1 menunjukkan bahwa
 Analisa Reduksi Asetilen (ARA : Acetylene Reduction Assay). Sebanyak,5 ml inokulum bakteri pertama pertama dan,5 ml inokulum bakteri kedua diinokulasikan kedalam campuran 2 ml NMS cair bebas nitrogen yang
Analisa Reduksi Asetilen (ARA : Acetylene Reduction Assay). Sebanyak,5 ml inokulum bakteri pertama pertama dan,5 ml inokulum bakteri kedua diinokulasikan kedalam campuran 2 ml NMS cair bebas nitrogen yang
BAB I PENDAHULUAN. A. Latar Belakang Masalah. Mikroorganisme banyak ditemukan di lingkungan perairan, di antaranya di
 BAB I PENDAHULUAN A. Latar Belakang Masalah Mikroorganisme banyak ditemukan di lingkungan perairan, di antaranya di ekosistem perairan rawa. Perairan rawa merupakan perairan tawar yang menggenang (lentik)
BAB I PENDAHULUAN A. Latar Belakang Masalah Mikroorganisme banyak ditemukan di lingkungan perairan, di antaranya di ekosistem perairan rawa. Perairan rawa merupakan perairan tawar yang menggenang (lentik)
BAB IV METABOLISME. Proses pembentukan atau penguraian zat di dalam sel yang disertai dengan adanya perubahan energi.
 BAB IV METABOLISME Proses pembentukan atau penguraian zat di dalam sel yang disertai dengan adanya perubahan energi METABOLISME ANABOLISME Proses Pembentukan Contoh: Fotosintesis, Kemosintesis Sintesis
BAB IV METABOLISME Proses pembentukan atau penguraian zat di dalam sel yang disertai dengan adanya perubahan energi METABOLISME ANABOLISME Proses Pembentukan Contoh: Fotosintesis, Kemosintesis Sintesis
VIII. AKTIVITAS BAKTERI NITROGEN
 VIII. AKTIVITAS BAKTERI NITROGEN TUJUAN 1. Mendemonstrasikan peran mikroba dalam proses pengubahan senyawa nitrogen organik menjadi ammonia (amonifikasi). 2. Mendemonstrasikan peran mikroba dalam biokonversi
VIII. AKTIVITAS BAKTERI NITROGEN TUJUAN 1. Mendemonstrasikan peran mikroba dalam proses pengubahan senyawa nitrogen organik menjadi ammonia (amonifikasi). 2. Mendemonstrasikan peran mikroba dalam biokonversi
METODE PENELITIAN. Penelitian ini telah dilakukan pada bulan Januari-Mei 2015 di Laboratorium
 15 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian ini telah dilakukan pada bulan Januari-Mei 2015 di Laboratorium Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas
15 III. METODE PENELITIAN A. Waktu dan Tempat Penelitian ini telah dilakukan pada bulan Januari-Mei 2015 di Laboratorium Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas
Biogeokimia adalah pertukaran atau perubahan yang terus menerus, antara komponen biosfer yang hidup dengan tak hidup.
 SIKLUS BIOGEOKIMIA Biogeokimia adalah pertukaran atau perubahan yang terus menerus, antara komponen biosfer yang hidup dengan tak hidup. Dalam suatu ekosistem, materi pada setiap tingkat trofik tidak hilang.
SIKLUS BIOGEOKIMIA Biogeokimia adalah pertukaran atau perubahan yang terus menerus, antara komponen biosfer yang hidup dengan tak hidup. Dalam suatu ekosistem, materi pada setiap tingkat trofik tidak hilang.
III. METODE PENELITIAN. Penelitian dilaksanakan pada Desember 2014 Mei 2015 di. Laboratorium Mikrobiologi FMIPA Universitas Lampung.
 19 III. METODE PENELITIAN 3.1. Waktu dan Tempat Penelitian Penelitian dilaksanakan pada Desember 2014 Mei 2015 di Laboratorium Mikrobiologi FMIPA Universitas Lampung. 3.2. Alat dan Bahan Alat yang digunakan
19 III. METODE PENELITIAN 3.1. Waktu dan Tempat Penelitian Penelitian dilaksanakan pada Desember 2014 Mei 2015 di Laboratorium Mikrobiologi FMIPA Universitas Lampung. 3.2. Alat dan Bahan Alat yang digunakan
I. METODOLOGI PENELITIAN. Penelitian ini dilaksanakan pada bulan April - Juli 2012 di Laboratorium. Ilmu Pengetahuan Alam Universitas Lampung.
 1 I. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan April - Juli 2012 di Laboratorium Biokimia, Laboratorium Instrumentasi Jurusan Kimia Fakultas Matematika
1 I. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan April - Juli 2012 di Laboratorium Biokimia, Laboratorium Instrumentasi Jurusan Kimia Fakultas Matematika
Gambar 1 Tanaman uji hasil meriklon (A) anggrek Phalaenopsis, (B) bunga Phalaenopsis yang berwarna putih
 BAHAN DAN METODE Tempat dan Waktu Penelitian Isolasi dan perbanyakan sumber inokulum E. carotovora dilakukan di Laboratorium Bakteriologi Departemen Proteksi Tanaman Fakultas Pertanian, Institut Pertanian
BAHAN DAN METODE Tempat dan Waktu Penelitian Isolasi dan perbanyakan sumber inokulum E. carotovora dilakukan di Laboratorium Bakteriologi Departemen Proteksi Tanaman Fakultas Pertanian, Institut Pertanian
organel yang tersebar dalam sitosol organisme
 STRUKTUR DAN FUNGSI MITOKONDRIA Mitokondria Mitokondria merupakan organel yang tersebar dalam sitosol organisme eukariot. STRUKTUR MITOKONDRIA Ukuran : diameter 0.2 1.0 μm panjang 1-4 μm mitokondria dalam
STRUKTUR DAN FUNGSI MITOKONDRIA Mitokondria Mitokondria merupakan organel yang tersebar dalam sitosol organisme eukariot. STRUKTUR MITOKONDRIA Ukuran : diameter 0.2 1.0 μm panjang 1-4 μm mitokondria dalam
Respirasi Anaerob (Fermentasi Alkohol)
 Respirasi Anaerob (Fermentasi Alkohol) I. TUJUAN Mengamati hasil dari peristiwa fermentasi alkohol II. LANDASAN TEORI Respirasi anaerob merupakan salah satu proses katabolisme yang tidak menggunakan oksigen
Respirasi Anaerob (Fermentasi Alkohol) I. TUJUAN Mengamati hasil dari peristiwa fermentasi alkohol II. LANDASAN TEORI Respirasi anaerob merupakan salah satu proses katabolisme yang tidak menggunakan oksigen
SMA XII (DUA BELAS) BIOLOGI METABOLISME
 JENJANG KELAS MATA PELAJARAN TOPIK BAHASAN SMA XII (DUA BELAS) BIOLOGI METABOLISME Metabolisme adalah seluruh reaksi kimia yang dilakukan oleh organisme. Metabolisme juga dapat dikatakan sebagai proses
JENJANG KELAS MATA PELAJARAN TOPIK BAHASAN SMA XII (DUA BELAS) BIOLOGI METABOLISME Metabolisme adalah seluruh reaksi kimia yang dilakukan oleh organisme. Metabolisme juga dapat dikatakan sebagai proses
Bab V Hasil dan Pembahasan. Gambar V.10 Konsentrasi Nitrat Pada Setiap Kedalaman
 Gambar V.10 Konsentrasi Nitrat Pada Setiap Kedalaman Dekomposisi material organik akan menyerap oksigen sehingga proses nitrifikasi akan berlangsung lambat atau bahkan terhenti. Hal ini ditunjukkan dari
Gambar V.10 Konsentrasi Nitrat Pada Setiap Kedalaman Dekomposisi material organik akan menyerap oksigen sehingga proses nitrifikasi akan berlangsung lambat atau bahkan terhenti. Hal ini ditunjukkan dari
BAHAN DAN METODE Tempat dan Waktu Bahan Peremajaan Aktinomiset dari Kultur Penyimpanan Perbanyakan Sclerotium rolfsii dari Kultur Penyimpanan
 BAHAN DAN METODE Tempat dan Waktu Penelitian dilaksanakan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor (IPB) mulai Maret 2011 sampai
BAHAN DAN METODE Tempat dan Waktu Penelitian dilaksanakan di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas Pertanian, Institut Pertanian Bogor (IPB) mulai Maret 2011 sampai
HASIL DAN PEMBAHASAN
 HASIL DAN PEMBAHASAN Keadaan Umum Penelitian Penelitian pembuatan pupuk organik cair ini dilaksanakan di Laboratorium Pengolahan Limbah Peternakan, Fakultas Peternakan, Institut Pertanian Bogor. Secara
HASIL DAN PEMBAHASAN Keadaan Umum Penelitian Penelitian pembuatan pupuk organik cair ini dilaksanakan di Laboratorium Pengolahan Limbah Peternakan, Fakultas Peternakan, Institut Pertanian Bogor. Secara
IV. HASIL DAN PEMBAHASAN
 IV. HASIL DAN PEMBAHASAN 4.1. Populasi Bakteri Penambat N 2 Populasi Azotobacter pada perakaran tebu transgenik IPB 1 menunjukkan jumlah populasi tertinggi pada perakaran IPB1-51 sebesar 87,8 x 10 4 CFU/gram
IV. HASIL DAN PEMBAHASAN 4.1. Populasi Bakteri Penambat N 2 Populasi Azotobacter pada perakaran tebu transgenik IPB 1 menunjukkan jumlah populasi tertinggi pada perakaran IPB1-51 sebesar 87,8 x 10 4 CFU/gram
PEMANFAATAN LIMBAH CAIR TAPIOKA UNTUK PENGHASIL BIOGAS SKALA LABORATORIUM. Mhd F Cholis Kurniawan
 PEMANFAATAN LIMBAH CAIR TAPIOKA UNTUK PENGHASIL BIOGAS SKALA LABORATORIUM Mhd F Cholis Kurniawan SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR BOGOR 2009 PERNYATAAN TESIS DAN MENGENAI SUMBER INFORMASI
PEMANFAATAN LIMBAH CAIR TAPIOKA UNTUK PENGHASIL BIOGAS SKALA LABORATORIUM Mhd F Cholis Kurniawan SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR BOGOR 2009 PERNYATAAN TESIS DAN MENGENAI SUMBER INFORMASI
1. ENERGI DALAM EKOSISTEM 2. KONSEP PRODUKTIVITAS 3. RANTAI PANGAN 4. STRUKTUR TROFIK DAN PIRAMIDA EKOLOGI
 PRINSIP DAN KONSEP ENERGI DALAM SISTEM EKOLOGI 1. ENERGI DALAM EKOSISTEM 2. KONSEP PRODUKTIVITAS 3. RANTAI PANGAN 4. STRUKTUR TROFIK DAN PIRAMIDA EKOLOGI ENERGI DALAM EKOSISTEM Hukum thermodinamika I energi
PRINSIP DAN KONSEP ENERGI DALAM SISTEM EKOLOGI 1. ENERGI DALAM EKOSISTEM 2. KONSEP PRODUKTIVITAS 3. RANTAI PANGAN 4. STRUKTUR TROFIK DAN PIRAMIDA EKOLOGI ENERGI DALAM EKOSISTEM Hukum thermodinamika I energi
DAUR BIOGEOKIMIA 1. DAUR/SIKLUS KARBON (C)
 DAUR BIOGEOKIMIA 1. DAUR/SIKLUS KARBON (C) Berkaitan dengan siklus oksigen Siklus karbon berkaitan erat dengan peristiwa fotosintesis yang berlangsung pada organisme autotrof dan peristiwa respirasi yang
DAUR BIOGEOKIMIA 1. DAUR/SIKLUS KARBON (C) Berkaitan dengan siklus oksigen Siklus karbon berkaitan erat dengan peristiwa fotosintesis yang berlangsung pada organisme autotrof dan peristiwa respirasi yang
III BAHAN DAN METODE
 meliputi daerah Jawa, Kalimantan dan Sumatera. Tanaman Kilemo di daerah Jawa banyak ditemui pada daerah dengan ketinggian 230 700 meter di atas permukaan laut (mdpl). Tanaman ini terutama banyak ditemui
meliputi daerah Jawa, Kalimantan dan Sumatera. Tanaman Kilemo di daerah Jawa banyak ditemui pada daerah dengan ketinggian 230 700 meter di atas permukaan laut (mdpl). Tanaman ini terutama banyak ditemui
II. TINJAUAN PUSTAKA 2.1 Pencemaran Perairan
 8 II. TINJAUAN PUSTAKA 2.1 Pencemaran Perairan Menurut Odum (1971), pencemaran adalah perubahan sifat fisik, kimia dan biologi yang tidak dikehendaki pada udara, tanah dan air. Sedangkan menurut Saeni
8 II. TINJAUAN PUSTAKA 2.1 Pencemaran Perairan Menurut Odum (1971), pencemaran adalah perubahan sifat fisik, kimia dan biologi yang tidak dikehendaki pada udara, tanah dan air. Sedangkan menurut Saeni
Proses Nitrifikasi Dan Denitrifikasi Dalam Pengolahan Limbah
 Proses Nitrifikasi Dan Denitrifikasi Dalam Pengolahan Limbah Salmah Fakultas Teknik Program Studi Teknik Kimia Universitas Sumatera Utara BAB I 1.1 Nitrifikasi yang Menggunakan Proses Lumpur Aktif Dua
Proses Nitrifikasi Dan Denitrifikasi Dalam Pengolahan Limbah Salmah Fakultas Teknik Program Studi Teknik Kimia Universitas Sumatera Utara BAB I 1.1 Nitrifikasi yang Menggunakan Proses Lumpur Aktif Dua
KARAKTERISASI MOLEKULAR DAN UJI AKTIVITAS BAKTERI PEREDUKSI NITRAT DARI MUARA CIMANDIRI PELABUHAN RATU SUKABUMI JAWA BARAT HURIA MARNIS
 KARAKTERISASI MOLEKULAR DAN UJI AKTIVITAS BAKTERI PEREDUKSI NITRAT DARI MUARA CIMANDIRI PELABUHAN RATU SUKABUMI JAWA BARAT HURIA MARNIS SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR BOGOR 2008 PERNYATAAN
KARAKTERISASI MOLEKULAR DAN UJI AKTIVITAS BAKTERI PEREDUKSI NITRAT DARI MUARA CIMANDIRI PELABUHAN RATU SUKABUMI JAWA BARAT HURIA MARNIS SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR BOGOR 2008 PERNYATAAN
BAB III METODE PENELITIAN. terdiri atas 5 perlakuan dengan 3 ulangan yang terdiri dari:
 BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian ini menggunakan rancangan acak lengkap (RAL) yang terdiri atas 5 perlakuan dengan 3 ulangan yang terdiri dari: 1. 0 ppm: perbandingan media
BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian ini menggunakan rancangan acak lengkap (RAL) yang terdiri atas 5 perlakuan dengan 3 ulangan yang terdiri dari: 1. 0 ppm: perbandingan media
BAB I PENDAHULUAN. tetapi limbah cair memiliki tingkat pencemaran lebih besar dari pada limbah
 BAB I PENDAHULUAN 1.1 Latar Belakang Industri tahu merupakan salah satu industri yang menghasilkan limbah organik. Limbah industri tahu yang dihasilkan dapat berupa limbah padat dan cair, tetapi limbah
BAB I PENDAHULUAN 1.1 Latar Belakang Industri tahu merupakan salah satu industri yang menghasilkan limbah organik. Limbah industri tahu yang dihasilkan dapat berupa limbah padat dan cair, tetapi limbah
DESAIN DAN SINTESIS AMINA SEKUNDER RANTAI KARBON GENAP DARI ASAM KARBOKSILAT RANTAI PANJANG RAHMAD FAJAR SIDIK
 DESAIN DAN SINTESIS AMINA SEKUNDER RANTAI KARBON GENAP DARI ASAM KARBOKSILAT RANTAI PANJANG RAHMAD FAJAR SIDIK SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR BOGOR 2007 PERNYATAAN TENTANG TESIS DAN SUMBER
DESAIN DAN SINTESIS AMINA SEKUNDER RANTAI KARBON GENAP DARI ASAM KARBOKSILAT RANTAI PANJANG RAHMAD FAJAR SIDIK SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR BOGOR 2007 PERNYATAAN TENTANG TESIS DAN SUMBER
BAHAN DAN METODE. Hrp -, IAA +, BPF Hrp -, IAA + + , BPF Hrp. , BPF Hrp -, IAA +, BPF + Hrp. , BPF Hrp. , BPF Hrp. Penambat Nitrogen Penambat Nitrogen
 BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Mikrobiologi, Departemen Biologi, FMIPA, IPB dan lahan pertanian Kampung Bongkor, Desa Situgede, Karang Pawitan-Wanaraja,
BAHAN DAN METODE Tempat dan Waktu Penelitian Penelitian ini dilaksanakan di Laboratorium Mikrobiologi, Departemen Biologi, FMIPA, IPB dan lahan pertanian Kampung Bongkor, Desa Situgede, Karang Pawitan-Wanaraja,
III. METODE PENELITIAN. Penelitian ini dilakukan di Laboratorium Mikrobiologi Jurusan Biologi
 17 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung pada Januari
17 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilakukan di Laboratorium Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung pada Januari
III. HASIL DAN PEMBAHASAN
 III. HASIL DAN PEMBAHASAN 3.1 Hasil 3.1.1 Kadar Oksigen Terlarut Hasil pengukuran konsentrasi oksigen terlarut pada kolam pemeliharaan ikan nila Oreochromis sp dapat dilihat pada Gambar 2. Dari gambar
III. HASIL DAN PEMBAHASAN 3.1 Hasil 3.1.1 Kadar Oksigen Terlarut Hasil pengukuran konsentrasi oksigen terlarut pada kolam pemeliharaan ikan nila Oreochromis sp dapat dilihat pada Gambar 2. Dari gambar
III. NUTRISI DAN MEDIUM KULTUR MIKROBA
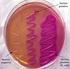 III. NUTRISI DAN MEDIUM KULTUR MIKROBA Medium pertumbuhan (disingkat medium) adalah tempat untuk menumbuhkan mikroba. Mikroba memerlukan nutrisi untuk memenuhi kebutuhan energi dan untuk bahan pembangun
III. NUTRISI DAN MEDIUM KULTUR MIKROBA Medium pertumbuhan (disingkat medium) adalah tempat untuk menumbuhkan mikroba. Mikroba memerlukan nutrisi untuk memenuhi kebutuhan energi dan untuk bahan pembangun
ISOLASI, SELEKSI DAN OPTIMASI PERTUMBUHAN GANGGANG MIKRO YANG POTENSIAL SEBAGAI PENGHASIL BAHAN BAKAR NABATI
 ISOLASI, SELEKSI DAN OPTIMASI PERTUMBUHAN GANGGANGG MIKRO YANG POTENSIAL SEBAGAI PENGHASIL BAHAN BAKAR NABATI YOLANDA FITRIA SYAHRI SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR BOGOR 2009 PERNYATAAN MENGENAI
ISOLASI, SELEKSI DAN OPTIMASI PERTUMBUHAN GANGGANGG MIKRO YANG POTENSIAL SEBAGAI PENGHASIL BAHAN BAKAR NABATI YOLANDA FITRIA SYAHRI SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR BOGOR 2009 PERNYATAAN MENGENAI
Air Panas. Isolat Murni Bakteri. Isolat Bakteri Selulolitik. Isolat Terpilih Bakteri Selulolitik. Kuantitatif
 75 Lampiran 1. Metode Kerja L.1.1 Bagan kerja Air Panas - Isolasi dan Seleksi Bakteri Pemurnian Bakteri Isolat Murni Bakteri Uji Bakteri Penghasil Selulase Secara Kualitatif Isolat Bakteri Selulolitik
75 Lampiran 1. Metode Kerja L.1.1 Bagan kerja Air Panas - Isolasi dan Seleksi Bakteri Pemurnian Bakteri Isolat Murni Bakteri Uji Bakteri Penghasil Selulase Secara Kualitatif Isolat Bakteri Selulolitik
Aliran elektron pembawa elektron berupa satu seri protein pembawa elektron dan lipid (quinone)
 Aliran elektron pembawa elektron berupa satu seri protein pembawa elektron dan lipid (quinone) Setiap pembawa elektron mempunyai potensial elektroda yang berbeda serta mentransfer elektron ke pembawa dengan
Aliran elektron pembawa elektron berupa satu seri protein pembawa elektron dan lipid (quinone) Setiap pembawa elektron mempunyai potensial elektroda yang berbeda serta mentransfer elektron ke pembawa dengan
IV. HASIL DAN PEMBAHASAN
 IV. HASIL DAN PEMBAHASAN A. Isolat Actinomycetes Amilolitik Terpilih 1. Isolat Actinomycetes Terpilih Peremajaan isolat actinomycetes dilakukan dengan tujuan sebagai pemeliharaan isolat actinomycetes agar
IV. HASIL DAN PEMBAHASAN A. Isolat Actinomycetes Amilolitik Terpilih 1. Isolat Actinomycetes Terpilih Peremajaan isolat actinomycetes dilakukan dengan tujuan sebagai pemeliharaan isolat actinomycetes agar
RESPIRASI BAKTERI LAPORAN PRAKTIKUM. Disusun untuk memenuhi tugas mata kuliah Mikrobiologi. Yang dibina oleh Sitoresmi Prabaningtyas, S.Si, M.
 RESPIRASI BAKTERI LAPORAN PRAKTIKUM Disusun untuk memenuhi tugas mata kuliah Mikrobiologi Yang dibina oleh Sitoresmi Prabaningtyas, S.Si, M.Si Oleh : Kelompok 2 / Kelas H Lely Hermawati (140342600679)
RESPIRASI BAKTERI LAPORAN PRAKTIKUM Disusun untuk memenuhi tugas mata kuliah Mikrobiologi Yang dibina oleh Sitoresmi Prabaningtyas, S.Si, M.Si Oleh : Kelompok 2 / Kelas H Lely Hermawati (140342600679)
BAB 5. HASIL DAN PEMBAHASAN. Percobaan 1 : Isolasi dan identifikasi bakteri penambat nitrogen nonsimbiotik
 Tahap I BAB 5. HASIL DAN PEMBAHASAN Percobaan 1 : Isolasi dan identifikasi bakteri penambat nitrogen nonsimbiotik Hasil pengukuran sampel tanah yang digunakan pada percobaan 1 meliputi ph tanah, kadar
Tahap I BAB 5. HASIL DAN PEMBAHASAN Percobaan 1 : Isolasi dan identifikasi bakteri penambat nitrogen nonsimbiotik Hasil pengukuran sampel tanah yang digunakan pada percobaan 1 meliputi ph tanah, kadar
Lampiran 1 Komposisi media pertumbuhan bakteri
 LAMPIRAN 13 14 Lampiran 1 Komposisi media pertumbuhan bakteri No Media Komposisi 1 Media gelatin Sebanyak 150 g gelatin dilarutkan dengan akuades hingga 1000 ml, cek ph 6.7±7.0, lalu disterilisasi dengan
LAMPIRAN 13 14 Lampiran 1 Komposisi media pertumbuhan bakteri No Media Komposisi 1 Media gelatin Sebanyak 150 g gelatin dilarutkan dengan akuades hingga 1000 ml, cek ph 6.7±7.0, lalu disterilisasi dengan
III. METODOLOGI PENELITIAN. Penelitian ini akan dilakukan pada bulan Juli sampai September 2012,
 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini akan dilakukan pada bulan Juli sampai September 2012, bertempat di Laboratorium Biokimia Jurusan Kimia Fakultas MIPA Universitas
III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini akan dilakukan pada bulan Juli sampai September 2012, bertempat di Laboratorium Biokimia Jurusan Kimia Fakultas MIPA Universitas
III. METODE PENELITIAN. Penelitian ini dilaksanakan pada bulan Januari - Februari 2015 di Balai Besar
 III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilaksanakan pada bulan Januari - Februari 2015 di Balai Besar Pengembangan Budidaya Laut Lampung dan Laboratorium Pengelolaan Limbah
III. METODE PENELITIAN A. Tempat dan Waktu Penelitian Penelitian ini dilaksanakan pada bulan Januari - Februari 2015 di Balai Besar Pengembangan Budidaya Laut Lampung dan Laboratorium Pengelolaan Limbah
A.1 Reduksi Nitrat dan Nitrit Reduksi nitrat terjadi di dalam sitoplasma, sedangkan reduksi nitrit terjadi di kloroplas.
 Pertemuan : Minggu ke 8 Estimasi waktu : 150 menit Pokok Bahasan : Asimilasi N - S - P pada tumbuhan Sub pokok bahasan : 1. Asimilasi nitrogen (sintesis protein) 2. Asimilasi sulfur 3. Asimilasi fosfat
Pertemuan : Minggu ke 8 Estimasi waktu : 150 menit Pokok Bahasan : Asimilasi N - S - P pada tumbuhan Sub pokok bahasan : 1. Asimilasi nitrogen (sintesis protein) 2. Asimilasi sulfur 3. Asimilasi fosfat
Reaksi BIOKIMIA PADA UJI BAKTERIOLOGI. No UJI BIOKIMIA KETERENGAN. 1. Uji fermentasi karbohidrat
 Reaksi BIKIMIA PADA UJI BAKTERILGI o UJI BIKIMIA KETEREGA 1. Uji fermentasi karbohidrat Uji positif ditandai dengan perubahan warna indikator BTB (brom timol biru) pada media biakan dari biru menjadi kuning.
Reaksi BIKIMIA PADA UJI BAKTERILGI o UJI BIKIMIA KETEREGA 1. Uji fermentasi karbohidrat Uji positif ditandai dengan perubahan warna indikator BTB (brom timol biru) pada media biakan dari biru menjadi kuning.
BAB IV HASIL DAN PEMBAHASAN A. AKTIVITAS KUALITATIF ENZIM KITINOLITIK (INDEKS KITINOLITIK)
 BAB IV HASIL DAN PEMBAHASAN A. AKTIVITAS KUALITATIF ENZIM KITINOLITIK (INDEKS KITINOLITIK) Peremajaan dan purifikasi terhadap kedelapan kultur koleksi isolat bakteri dilakukan terlebih dahulu sebelum pengujian
BAB IV HASIL DAN PEMBAHASAN A. AKTIVITAS KUALITATIF ENZIM KITINOLITIK (INDEKS KITINOLITIK) Peremajaan dan purifikasi terhadap kedelapan kultur koleksi isolat bakteri dilakukan terlebih dahulu sebelum pengujian
BAB III METODE PENELITIAN. dengan mengadakan manipulasi terhadap objek penelitian serta adanya kontrol
 24 BAB III METODE PENELITIAN A. Jenis Penelitian Penelitian yang dilakukan termasuk penelitian dasar dengan metode penelitian eksperimen. Penelitian eksperimen adalah penelitian yang dilakukan dengan mengadakan
24 BAB III METODE PENELITIAN A. Jenis Penelitian Penelitian yang dilakukan termasuk penelitian dasar dengan metode penelitian eksperimen. Penelitian eksperimen adalah penelitian yang dilakukan dengan mengadakan
PERTEMUAN XIV: EKOSISTEM DAN BIOLOGI KONSERVASI. Program Tingkat Persiapan Bersama IPB 2011
 PERTEMUAN XIV: EKOSISTEM DAN BIOLOGI KONSERVASI Program Tingkat Persiapan Bersama IPB 2011 1 EKOSISTEM Topik Bahasan: Aliran energi dan siklus materi Struktur trofik (trophic level) Rantai makanan dan
PERTEMUAN XIV: EKOSISTEM DAN BIOLOGI KONSERVASI Program Tingkat Persiapan Bersama IPB 2011 1 EKOSISTEM Topik Bahasan: Aliran energi dan siklus materi Struktur trofik (trophic level) Rantai makanan dan
BAB I PENDAHULUAN UKDW. kosmetik, pembuatan karet sintetis, hingga industri bahan bakar.
 1 BAB I PENDAHULUAN A. Latar Belakang Etanol banyak digunakan dalam dunia industri obat obatan, kosmetik, pembuatan karet sintetis, hingga industri bahan bakar. Penggunaan etanol pada industri bahan bakar
1 BAB I PENDAHULUAN A. Latar Belakang Etanol banyak digunakan dalam dunia industri obat obatan, kosmetik, pembuatan karet sintetis, hingga industri bahan bakar. Penggunaan etanol pada industri bahan bakar
BAHAN DAN METODE. Tempat dan Waktu
 15 BAHAN DAN METODE Tempat dan Waktu Penelitian dilaksanakan di laboratorium dan rumah kaca Hama dan Penyakit dan rumah kaca Balai penelitian Tanaman Obat dan Aromatik (BALITTRO), Bogor; pada bulan Oktober
15 BAHAN DAN METODE Tempat dan Waktu Penelitian dilaksanakan di laboratorium dan rumah kaca Hama dan Penyakit dan rumah kaca Balai penelitian Tanaman Obat dan Aromatik (BALITTRO), Bogor; pada bulan Oktober
Wardaya College IKATAN KIMIA STOIKIOMETRI TERMOKIMIA CHEMISTRY. Part III. Summer Olympiad Camp Kimia SMA
 Part I IKATAN KIMIA CHEMISTRY Summer Olympiad Camp 2017 - Kimia SMA 1. Untuk menggambarkan ikatan yang terjadi dalam suatu molekul kita menggunakan struktur Lewis atau 'dot and cross' (a) Tuliskan formula
Part I IKATAN KIMIA CHEMISTRY Summer Olympiad Camp 2017 - Kimia SMA 1. Untuk menggambarkan ikatan yang terjadi dalam suatu molekul kita menggunakan struktur Lewis atau 'dot and cross' (a) Tuliskan formula
Media Kultur. Pendahuluan. Komposisi Media 3/9/2016. Materi Kuliah Mikrobiologi Industri Minggu ke 3 Nur Hidayat
 Media Kultur Materi Kuliah Mikrobiologi Industri Minggu ke 3 Nur Hidayat Pendahuluan Medium untuk pertumbuhan skala laboratorium umumnya mahal sehingga dibutuhkan perubahan agar dapat dipakai medium yang
Media Kultur Materi Kuliah Mikrobiologi Industri Minggu ke 3 Nur Hidayat Pendahuluan Medium untuk pertumbuhan skala laboratorium umumnya mahal sehingga dibutuhkan perubahan agar dapat dipakai medium yang
Effect of ammonium concentration on alcoholic fermentation kinetics by wine yeasts for high sugar content
 NAMA : FATMALIKA FIKRIA H KELAS : THP-B NIM : 121710101049 Effect of ammonium concentration on alcoholic fermentation kinetics by wine yeasts for high sugar content 1. Jenis dan sifat Mikroba Dalam fermentasi
NAMA : FATMALIKA FIKRIA H KELAS : THP-B NIM : 121710101049 Effect of ammonium concentration on alcoholic fermentation kinetics by wine yeasts for high sugar content 1. Jenis dan sifat Mikroba Dalam fermentasi
LAMPIRAN. Lampiran 1. Foto Lokasi Pengambilan Sampel Air Panas Pacet Mojokerto
 LAMPIRAN Lampiran 1. Foto Lokasi Pengambilan Sampel Air Panas Pacet Mojokerto Lampiran 2. Pembuatan Media dan Reagen 2.1 Pembuatan Media Skim Milk Agar (SMA) dalam 1000 ml (Amelia, 2005) a. 20 gram susu
LAMPIRAN Lampiran 1. Foto Lokasi Pengambilan Sampel Air Panas Pacet Mojokerto Lampiran 2. Pembuatan Media dan Reagen 2.1 Pembuatan Media Skim Milk Agar (SMA) dalam 1000 ml (Amelia, 2005) a. 20 gram susu
BAB III METODE PENELITIAN. konsentrasi limbah cair tapioka (10%, 20%, 30%, 40%, 50% dan 0% atau kontrol)
 34 BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian disusun menggunakan metoda statistika rancangan acak lengkap (RAL) satu faktor, dimana faktor yang diujikan adalah pengaruh konsentrasi
34 BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian disusun menggunakan metoda statistika rancangan acak lengkap (RAL) satu faktor, dimana faktor yang diujikan adalah pengaruh konsentrasi
Metabolisme Energi. Pertemuan ke-4 Mikrobiologi Dasar. Prof. Ir. H. Usman Pato, MSc. PhD. Fakultas Pertanian Universitas Riau
 Metabolisme Energi Pertemuan ke-4 Mikrobiologi Dasar Prof. Ir. H. Usman Pato, MSc. PhD. Fakultas Pertanian Universitas Riau Sumber Energi Mikroba Setiap makhluk hidup butuh energi untuk kelangsungan hidupnya
Metabolisme Energi Pertemuan ke-4 Mikrobiologi Dasar Prof. Ir. H. Usman Pato, MSc. PhD. Fakultas Pertanian Universitas Riau Sumber Energi Mikroba Setiap makhluk hidup butuh energi untuk kelangsungan hidupnya
III. METODE PERCOBAAN. Penelitian ini dilaksanakan pada bulan Februari sampai April 2014 di
 18 III. METODE PERCOBAAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan Februari sampai April 2014 di Laboratorium Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan
18 III. METODE PERCOBAAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan pada bulan Februari sampai April 2014 di Laboratorium Mikrobiologi Jurusan Biologi Fakultas Matematika dan Ilmu Pengetahuan
III. METODOLOGI PENELITIAN. Penelitian ini dilaksanakan dari bulan Maret sampai bulan Agustus 2013 di
 25 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan dari bulan Maret sampai bulan Agustus 2013 di Laboratorium Instrumentasi dan Laboratorium Biokimia Jurusan Kimia
25 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilaksanakan dari bulan Maret sampai bulan Agustus 2013 di Laboratorium Instrumentasi dan Laboratorium Biokimia Jurusan Kimia
III. METODOLOGI PENELITIAN. Penelitian ini dilakukan pada bulan Juni-November Penelitian ini
 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan Juni-November 2013. Penelitian ini dilakukan di Laboratorium Biokimia dan Laboratorium Biomassa Jurusan Kimia
III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan Juni-November 2013. Penelitian ini dilakukan di Laboratorium Biokimia dan Laboratorium Biomassa Jurusan Kimia
BAB 1 PENDAHULUAN. 1.1 Latar Belakang
 BAB 1 PENDAHULUAN 1.1 Latar Belakang Proses hidrolisis minyak/lemak menjadi asam lemak dan gliserol secara komersial yang sampai kini digunakan, beroperasi pada suhu 240-250 o C dan tekanan 45-50 bar.
BAB 1 PENDAHULUAN 1.1 Latar Belakang Proses hidrolisis minyak/lemak menjadi asam lemak dan gliserol secara komersial yang sampai kini digunakan, beroperasi pada suhu 240-250 o C dan tekanan 45-50 bar.
TINJAUAN PUSTAKA. memiliki empat buah flagella. Flagella ini bergerak secara aktif seperti hewan. Inti
 II. TINJAUAN PUSTAKA A. Klasifikasi dan Biologi Tetraselmis sp. Tetraselmis sp. merupakan alga bersel tunggal, berbentuk oval elips dan memiliki empat buah flagella. Flagella ini bergerak secara aktif
II. TINJAUAN PUSTAKA A. Klasifikasi dan Biologi Tetraselmis sp. Tetraselmis sp. merupakan alga bersel tunggal, berbentuk oval elips dan memiliki empat buah flagella. Flagella ini bergerak secara aktif
Bab IV Data dan Hasil Pembahasan
 Bab IV Data dan Hasil Pembahasan IV.1. Seeding dan Aklimatisasi Pada tahap awal penelitian, dilakukan seeding mikroorganisme mix culture dengan tujuan untuk memperbanyak jumlahnya dan mengadaptasikan mikroorganisme
Bab IV Data dan Hasil Pembahasan IV.1. Seeding dan Aklimatisasi Pada tahap awal penelitian, dilakukan seeding mikroorganisme mix culture dengan tujuan untuk memperbanyak jumlahnya dan mengadaptasikan mikroorganisme
III. BAHAN DAN METODE
 15 III. BAHAN DAN METODE 3.1. Waktu dan Tempat Penelitian dilaksanakan dari bulan April hingga bulan September 2010 di Laboratorium Bioteknologi Tanah serta Laboratorium Kimia dan Kesuburan Tanah, Departemen
15 III. BAHAN DAN METODE 3.1. Waktu dan Tempat Penelitian dilaksanakan dari bulan April hingga bulan September 2010 di Laboratorium Bioteknologi Tanah serta Laboratorium Kimia dan Kesuburan Tanah, Departemen
INTERAKSI ANTAR KOMPONEN EKOSISTEM
 INTERAKSI ANTAR KOMPONEN EKOSISTEM 1. Interaksi antar Organisme Komponen Biotik Untuk memenuhi kebutuhannya akan makanan, setiap organisme melakukan interaksi tertentu dengan organisme lain. Pola-pola
INTERAKSI ANTAR KOMPONEN EKOSISTEM 1. Interaksi antar Organisme Komponen Biotik Untuk memenuhi kebutuhannya akan makanan, setiap organisme melakukan interaksi tertentu dengan organisme lain. Pola-pola
BAB III METODE PENELITIAN. menggunakan campuran bakteri (Pseudomonas aeruginosa dan Pseudomonas
 BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian bioremediasi logam berat timbal (Pb) dalam lumpur Lapindo menggunakan campuran bakteri (Pseudomonas aeruginosa dan Pseudomonas pseudomallei)
BAB III METODE PENELITIAN 3.1 Rancangan Penelitian Penelitian bioremediasi logam berat timbal (Pb) dalam lumpur Lapindo menggunakan campuran bakteri (Pseudomonas aeruginosa dan Pseudomonas pseudomallei)
I. PENDAHULUAN. 1.1 Latar Belakang. biologis. Biohidrogen berpotensi sebagai bahan bakar alternatif karena kandungan
 I. PENDAHULUAN 1.1 Latar Belakang Biohidrogen merupakan gas hidrogen yang dihasilkan melalui proses biologis. Biohidrogen berpotensi sebagai bahan bakar alternatif karena kandungan energi yang tinggi,
I. PENDAHULUAN 1.1 Latar Belakang Biohidrogen merupakan gas hidrogen yang dihasilkan melalui proses biologis. Biohidrogen berpotensi sebagai bahan bakar alternatif karena kandungan energi yang tinggi,
TINJAUAN PUSTAKA Pemanasan Global dan Pertanian Sawah
 TINJAUAN PUSTAKA Pemanasan Global dan Pertanian Sawah Pemanasan global berkaitan dengan peningkatan gas rumah kaca (GRK) di atmosfer dan perubahan iklim. Metan (CH 4 ) dan dinitrogen oksida (N 2 O) merupakan
TINJAUAN PUSTAKA Pemanasan Global dan Pertanian Sawah Pemanasan global berkaitan dengan peningkatan gas rumah kaca (GRK) di atmosfer dan perubahan iklim. Metan (CH 4 ) dan dinitrogen oksida (N 2 O) merupakan
I. PENDAHULUAN 1.1. Latar Belakang
 I. PENDAHULUAN 1.1. Latar Belakang Tanaman yang banyak mengonsumsi pupuk, terutama pupuk nitrogen (N) adalah tanaman padi sawah, yaitu sebanyak 72 % dan 13 % untuk palawija (Agency for Agricultural Research
I. PENDAHULUAN 1.1. Latar Belakang Tanaman yang banyak mengonsumsi pupuk, terutama pupuk nitrogen (N) adalah tanaman padi sawah, yaitu sebanyak 72 % dan 13 % untuk palawija (Agency for Agricultural Research
TINJAUAN PUSTAKA. Fitoplankton adalah alga yang berfungsi sebagai produsen primer, selama
 7 II. TINJAUAN PUSTAKA 2.1. Biologi Nannochloropsis sp. Fitoplankton adalah alga yang berfungsi sebagai produsen primer, selama hidupnya tetap dalam bentuk plankton dan merupakan makanan langsung bagi
7 II. TINJAUAN PUSTAKA 2.1. Biologi Nannochloropsis sp. Fitoplankton adalah alga yang berfungsi sebagai produsen primer, selama hidupnya tetap dalam bentuk plankton dan merupakan makanan langsung bagi
2. TINJAUAN PUSTAKA. berflagel. Selnya berbentuk bola berukuran kecil dengan diameter 4-6 µm.
 3 2. TINJAUAN PUSTAKA 2.1 Biologi Nannochloropsis sp Mikroalga adalah tumbuhan tingkat rendah yang memiliki klorofil, yang dapat digunakan untuk melakukan proses fotosintesis. Mikroalga tidak memiliki
3 2. TINJAUAN PUSTAKA 2.1 Biologi Nannochloropsis sp Mikroalga adalah tumbuhan tingkat rendah yang memiliki klorofil, yang dapat digunakan untuk melakukan proses fotosintesis. Mikroalga tidak memiliki
BAB III METODE PENELITIAN. A. Waktu dan Tempat Penelitian. Penelitian dilaksanakan pada bulan Maret-November 2012 di
 digilib.uns.ac.id BAB III METODE PENELITIAN A. Waktu dan Tempat Penelitian Penelitian dilaksanakan pada bulan Maret-November 2012 di Laboratorium Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas
digilib.uns.ac.id BAB III METODE PENELITIAN A. Waktu dan Tempat Penelitian Penelitian dilaksanakan pada bulan Maret-November 2012 di Laboratorium Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas
II. TINJAUAN PUSTAKA. A. Mineralisasi N dari Bahan Organik yang Dikomposkan
 II. TINJAUAN PUSTAKA A. Mineralisasi N dari Bahan Organik yang Dikomposkan Bahan organik adalah bagian dari tanah yang merupakan suatu sistem kompleks dan dinamis, yang bersumber dari bahan-bahan yang
II. TINJAUAN PUSTAKA A. Mineralisasi N dari Bahan Organik yang Dikomposkan Bahan organik adalah bagian dari tanah yang merupakan suatu sistem kompleks dan dinamis, yang bersumber dari bahan-bahan yang
III. METODOLOGI PENELITIAN. Penelitian ini dilakukan pada bulan Agustus-Desember 2015 di Laboratorium
 23 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan Agustus-Desember 2015 di Laboratorium Biokimia Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam
23 III. METODOLOGI PENELITIAN A. Waktu dan Tempat Penelitian Penelitian ini dilakukan pada bulan Agustus-Desember 2015 di Laboratorium Biokimia Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam
