BAB 3 FORMULA DAN PERSAMAAN KIMIA
|
|
|
- Bambang Pranata
- 5 tahun lalu
- Tontonan:
Transkripsi
1 BAB 3 FORMULA DAN PERSAMAAN KIMIA 3.1 KONSEP MOL [A] Bilangan Mol dan bilangan zarah 1) 1 mol bahan mengandungi 6.02 x zarah (atom / molekul / ion ) 1 mol = 6.02 x zarah (atom / molekul / ion ) 2) 6.02 x disebut sebagai pemalar Avogadro. 1) Berapa banyak atom yang terdapat dalam 1 mol atom natrium? 2) Berapa banyak ion yang terdapat dalam 0.5 mol ion kalsium, Ca 2+? 3) Hitung bilangan molekul dalam 1.2 mol karbon dioksida, CO 2. 4) Cari bilangan mol atom dalam 3.01 x aluminium atom. 5) Berapakah mol gas oksigen, O 2 yang mengandungi x molekul gas oksigen? [B] Bilangan Mol dan jisim bahan [B.1] Jisim atom relatif dan Jisim molekul relatif 1) Karbon-12 dipilih sebagai atom piawai 2) Jisim atom relatif = jisim purata satu atom unsur itu 1/12 x jisim satu atom karbon-12 Jisim molekul relatif= jisim purata satu molekul bahan itu 1/12 x jisim satu atom karbon-12 3) Jisim formula relatif digunakan untuk sebatian ion. 1) Kira jisim molekul relatif bagi bahan berikut (Jisim atom relatif: F = 19; O = 16; C = 12; H = 1; N = 14) a) F 2 b) O 3 c) CO 2 d) H 2 O e) C 2 H 5 OH f) NH 3 1
2 2) Kira jisim formula relatif bagi bahan berikut: (Jisim atom relatif: Na = 23; N = 14; O = 16; H = 1; S = 32; Mg = 24; Ca = 40; C = 12; Pb = 207; Cu = 64) a) CaCO 3 b) PbSO 4 c) Mg(NO 3 ) 2 d) Na 2 CO 3 e) Ca(OH) 2 f) CuSO 4.5H 2 O 3) Formula kimia bagi ammonium sulfat adalah (NH 4 ) 2 SO 4. Apakah jisim formula relatif bagi ammonium sulfat? [Jisim atom relatif: H = 1; N = 14;S = 32; O = 16] 4) Jisim formula relatif bagi XNO 2 ialah 100. Apakah jisim atom relatif bagi unsur X? [Jisim atom relatif: N = 14; O = 16] [B.2] Bilangan Mol dan jisim bahan 1. Jisim molar sesuatu bahan ialah jisim 1 mol bahan tersebut. ( g mol -1 ) 2. Mesti menggunakan formula (unsur atau sebatian) semasa membuat kiraan (Jisim atom relatif: Ca=40, C=12, O=16, Fe=56, Cl=35.5, H=1) 1) Berapakah jisim 1 mol karbon dioksida, CO 2? 2) Hitung jisim bagi 0.5 mol CaCO 3 kalsium karbonat. 3) Hitung jisim bagi 0.1 mol atom hidrogen. 4) Berapakah mol yang terdapat di dalam 73 g HCl. 5) Berapakah mol kalsium hidroksida yang terdapat dalam 2.22 g kalsium hidroksida, Ca(OH) 2 2
3 Bilangan Mol dan Isi padu gas 1. Isi padu molar sesuatu gas ialah isi padu yang ditempati oleh satu mol gas. 2. Satu mol gas menempati = 22.4 dm 3 = cm 3 pada STP. = 24 dm 3 = cm 3 pada keadaan bilik. 1) Hitung isi padu gas dalam 1 mol bromin, Br 2 pada STP. 2) Berapakah isi padu bagi 1.4 mol gas klorin, Cl 2 pada keadaan bilik? 3) Hitung bilangan mol gas oksigen dalam 8.96 dm 3 gas oksigen pada STP 4) Berapakah mol bagi 720 cm 3 oksigen, O 2 pada keadaan bilik. Hubung kait antara bilangan mol, bilangan zarah, jisim dan isi padu gas 1) Berapakah molekul yang terdapat dalam 16 g gas sulfur dioksida, SO 2? [Jisim atom relatif: O = 16, S = 32, Pemalar Avogadro = 6.02 x mol -1 ] 2) Hitung jisim bagi 2.4 x molekul etana (C 2 H 6 )? [Jisim atom relatif: H = 1, C = 12, Pemalar Avogadro = 6.02 x mol -1 ] 3) Berapakah molekul yang terdapat dalam 150 cm 3 oksigen pada keadaan bilik. [Pemalar Avogadro = 6.02 x mol -1, Isi padu molar gas = 24 dm 3 mol -1 pada keadaan bilik] 3
4 3.2 Formula Kimia [A] Formula Empirik 1. Dua jenis formula kimia: a) formula empirik b) formula Molekul 2. Formula empirik adalah formula kimia yang menunjukkan nisbah teringkas bilangan atom setiap jenis unsur dalam sesuatu sebatian. 1) oksida logam M mengandungi 60.0% logam M. Tentukan formula empiriknya. [Jisim atom relatif: M = 48; O = 16] 2) Satu sampel aluminium oksida mengandungi 1.08 g aluminium dan 0.96 g oksigen. Apakah formula empirik sebatian ini? [Jisim atom relatif: Al = 27, O = 16;] 3) X g unsur M menggabungkan dengan 21.3 g klorin untuk menghasilkan sebatian yang mempunyai formula MCl 2. Cari nilai X. [Jisim atom relatif: M = 59; Cl = 35.5] Dua kaedah untuk menentukan formula empirik: a) Membakar Logam reaktif di dalam udara (gas oksigen) Logam reaktif + oksigen oksida logam (Untuk logam reaktif: Mg, Al, Zn yang lebih reaktif daripada hidrogen) b) Menurunkan oksida logam dalam gas hidrogen oksida logam + gas hidrogen logam + air (untuk logam kurang reaktif: Cu, Pb, Sn) H 2 4
5 [B] Formula Molekul 1. Formula molekul adalah formula kimia yang menunjukkan bilangan sebenar atom-atom setiap jenis unsur di dalam satu molekul sesuatu sebatian. C 2 H 4 = formula molekul CH 2 = formula empirik 2. Formula molekul boleh didapati jika maklumat berikut diketahui: a) formula empirik b) jisim molekul relatif 1) formula empirik Y adalah CH 2 O. Jisim relatif molekul adalah 180. Cari formula molekul Y. [Jisim atom relatif: C = 12, H = 1, O = 16] 2) Rajah menunjukkan maklumat daripada hidrokarbon X. Kandungan: Karbon: 82,76% Hidrogen: 17.24% Jisim molekul relatif = 58 Berdasarkan maklumat diatas, tentukan: a) formula empirik hidrokarbon X. [Jisim atom relatif: H = 1; C = 12] b) formula molekul hidrokarbon X. 3) Rajah menunjukkan formula struktur alkana. a) Tentukan formula molekul bagi sebatian ini. b) Tentukan formula empirik bagi sebatian ini. c) Kira jisim molekul relatif bagi sebatian ini. [Jisim atom relatif: H = 1; C = 12] 5
6 [C] Formula Kimia 1. Sebatian ion terdiri daripada ion positif (kation) dan ion negatif(anion) 2. Kation datang pertama, diikuti dengan nama anion. 3. Kation formula Ion hidrogen H + Ion litium Li + Ion kalium K + Ion natrium Na + Ion kuprum(i) Cu + Ion argentum Ag + Ion ammonium + NH 4 Ion magnesium Mg 2+ Ion kalsium Ca 2+ Ion zink Zn 2+ Ion kuprum(ii) Cu 2+ Ion plumbum(ii) Pb 2+ Ion ferum(ii) Fe 2+ Ion ferum(iii) Fe 3+ Ion aluminium Al 3+ Anion formula Ion klorida Cl - Ion bromide Br - Ion iodida I - Ion hidroksida OH - Ion nitrat - NO 3 Ion oksida O 2- Ion sulfat 2- SO 4 Ion karbonat 2- CO 3 Ion fosfat 3- PO 4 Nama Formula kimia Nama Formula kimia Gas oksigen O 2 Asid hidroklorik HCl Gas nitrogen N 2 Asid sulfurik H 2 SO 4 Gas Hidrogen H 2 Asid nitrik HNO 3 Karbon dioksida CO 2 Larutan ammonia NH 3 1) Tuliskan formula kimia: a) natrium klorida e) Magnesium oksida b) Magnesium klorida f) Zink nitrat c) Kuprum(I) oksida g) Ferum(III) hidroksida d) Natrium sulfat h) Aluminium oksida 6
7 3.3 Persamaan Kimia [A] Persamaan Kimia 1) Persamaan Kimia adalah perwakilan tindak balas kimia dalam perkataan atau menggunakan formula kimia 2) persamaan kimia menunjukkan: a) bahan tindak balas b) hasil tindak balas c) keadaan fizikal bahan kimia yang digunakan. [pepejal (p), cecair (c), gas (g), Larutan akueus (ak)] d) bilangan mol bahan dan hasil tindak balas yang terlibat. 2) 2H 2 O 2 (c) O 2 (g) + 2H 2 O (c) Bahan tindak balas: hidrogen peroksida, H 2 O 2 Hasil tindak balas: oksigen dan air 2 mol hidrogen peroksida menghasilkan 1 mol gas oksigen dan 2 mol air. 3. Persamaan kimia mesti seimbang Contoh 1) Mengimbangkan persamaan yang diberikan di bawah: a) Na + Cl 2 NaCl b) K + O 2 K 2 O c) Li + H 2 0 LiOH + H 2 d) Cl 2 + NaOH NaCl + NaOCl + H 2 O e) Br 2 + Fe FeBr 3 f) Mg + O 2 MgO g) Zn + HCl ZnCl 2 + H 2 h) Zn + Pb(NO 3 ) 2 Zn(NO 3 ) 2 + Pb i) NaOH + H 2 SO 4 Na 2 SO 4 + H 2 O j) H 2 O 2 O 2 + H 2 O 2) Maklumat menunjukkan tindak balas kimia bagi logam kalium. Apabila sekeping kalium diletakkan di dalam air, ia boleh terbakar dengan nyalaan ungu dan menghasilkan bunyi 'pop' untuk menghasilkan gas hidrogen dan larutan kalium hidroksida. a) Nyatakan bahan tindak balas dan hasil tindak balas. b) Tuliskan formula kalium hidroksida. c) Tuliskan persamaan kimia bagi tindak balas yang berlaku. d) Jelaskan persamaan kimia dalam c). 7
8 [B] Masalah yang melibatkan persamaan kimia 1. Pekali dalam persamaan seimbang memberitahu kita nisbah mol bahan tindak balas dan hasil tindak balas. 2H 2 + O 2 2H 2 O 2 mol 1 mol 2 mol 1) Berapa gram Ag 2 O yang digunakan untuk menghasilkan 50.0 g logam Argentum? [Jisim atom relatif: Ag, 108; O, 16; H, 1] Persamaan kimia: Ag 2 O + H 2 Ag + H 2 O 2) Berapakah isi padu gas (pada STP) Cl 2 akan bertindak balas jika 5.50g PCl 5 dihasilkan? [Jisim atom relatif: P, 31; Cl, 35.5; Isi padu molar: 22.4 dm 3 mol -1 pada STP] Persamaan kimia: P + Cl 2 PCl 5 3) Persamaan kimia berikut menunjukkan tindak balas antara besi dan bromin 2Fe + 3Br 2 2FeBr g besi terbakar sepenuhnya dalam bromin. Apakah jisim hasil tindak balas? [Jisim atom relatif: Br = 80, Fe = 56] 4) Aluminium boleh diekstrak daripada aluminium oksida mengikut persamaan kimia di bawah: 5) Pemanasan XCO 3 mengikut persamaan di bawah: Berapakah jisim maksimum aluminium yang boleh diekstrak daripada 102 g aluminium oksida? [Jisim atom relatif: O = 16; Al = 27] Berapakah mol XCO 3 yang diperlukan untuk menghasilkan 4.0 g oksida X? [Jisim atom relatif: C = 12; O = 16; X = 64] 8
Kaedah Penyediaan Garam Tak Terlarutkan
 Kaedah Penyediaan Garam Tak Terlarutkan Dalam tindak balas penguraian ganda dua, larutan berlainan bahan tindak balas akan saling bertukar pasangan nya supaya membentuk sebatian baru sebagai garam tak
Kaedah Penyediaan Garam Tak Terlarutkan Dalam tindak balas penguraian ganda dua, larutan berlainan bahan tindak balas akan saling bertukar pasangan nya supaya membentuk sebatian baru sebagai garam tak
3.2 Penambahan dan kehilangan oksigen, hidrogen and elektron dalam tindak balas redoks
 BAB 3 PENGOKSIDAAN DAN PENURUNAN 3.1 Tindak balas Redoks 1. Tindak balas redoks adalah tindak balas yang melibatkan pengoksidaan dan penurunan yang berlaku secara serentak. 2. Pengoksidaan Penurunan Penambahan
BAB 3 PENGOKSIDAAN DAN PENURUNAN 3.1 Tindak balas Redoks 1. Tindak balas redoks adalah tindak balas yang melibatkan pengoksidaan dan penurunan yang berlaku secara serentak. 2. Pengoksidaan Penurunan Penambahan
LATIHAN ULANGAN TENGAH SEMESTER 2
 Pilihlah jawaban yang paling benar LATIHAN ULANGAN TENGAH SEMESTER 2 TATANAMA 1. Nama senyawa berikut ini sesuai dengan rumus kimianya, kecuali. A. NO = nitrogen oksida B. CO 2 = karbon dioksida C. PCl
Pilihlah jawaban yang paling benar LATIHAN ULANGAN TENGAH SEMESTER 2 TATANAMA 1. Nama senyawa berikut ini sesuai dengan rumus kimianya, kecuali. A. NO = nitrogen oksida B. CO 2 = karbon dioksida C. PCl
SKEMA KIMIA KERTAS 2 SET 3
 SKEMA KIMIA KERTAS 2 SET 3 No (a)(i) Mark Scheme Penambahan// pembrominan// penghalogenan Sub Mark Total Mark Warna perang dinyahwarna (iii) Alkena (iv) C n H 2n (v). Formula molekul: C 4 H 8 2. Formula
SKEMA KIMIA KERTAS 2 SET 3 No (a)(i) Mark Scheme Penambahan// pembrominan// penghalogenan Sub Mark Total Mark Warna perang dinyahwarna (iii) Alkena (iv) C n H 2n (v). Formula molekul: C 4 H 8 2. Formula
Tahap Kefahaman Masalah Stoikiometri dalam Perwakilan Makroskopik, Mikroskopik Dan Simbol
 Tahap Kefahaman Masalah Stoikiometri dalam Perwakilan Makroskopik, Mikroskopik Dan Simbol Bahagian ini akan menjelaskan dengan lebih mendalam bagi menjawab soalan kajian ketiga. Apakah tahap kefahaman
Tahap Kefahaman Masalah Stoikiometri dalam Perwakilan Makroskopik, Mikroskopik Dan Simbol Bahagian ini akan menjelaskan dengan lebih mendalam bagi menjawab soalan kajian ketiga. Apakah tahap kefahaman
Bahagian A [60 markah] Jawab semua soalan dalam bahagian ini.
![Bahagian A [60 markah] Jawab semua soalan dalam bahagian ini. Bahagian A [60 markah] Jawab semua soalan dalam bahagian ini.](/thumbs/71/64653310.jpg) 1 Bahagian A [60 markah] Jawab semua soalan dalam bahagian ini. 1. Rajah 1 menunjukkan unsur-unsur dalam Kala 3 Jadual Berkala unsur. https://cikguadura.wordpress.com/ Rajah 1 (a) Mengapakah unsur-unsur
1 Bahagian A [60 markah] Jawab semua soalan dalam bahagian ini. 1. Rajah 1 menunjukkan unsur-unsur dalam Kala 3 Jadual Berkala unsur. https://cikguadura.wordpress.com/ Rajah 1 (a) Mengapakah unsur-unsur
K13 Revisi Antiremed Kelas 11 Kimia
 K13 Revisi Antiremed Kelas 11 Kimia Stoikiometri Larutan - Soal Doc. Name: RK13AR11KIM0601 Doc. Version : 2016-12 01. Zat-zat berikut ini dapat bereaksi dengan larutan asam sulfat, kecuali... (A) kalsium
K13 Revisi Antiremed Kelas 11 Kimia Stoikiometri Larutan - Soal Doc. Name: RK13AR11KIM0601 Doc. Version : 2016-12 01. Zat-zat berikut ini dapat bereaksi dengan larutan asam sulfat, kecuali... (A) kalsium
kajian ini adalah Janna-S, Sida-S dan Nabila-S. Dapatan hasil analisis transkrip
 Murid Berpencapaian Sederhana Murid berpencapaian sederhana yang terlibat dengan pengumpulan data dalam kajian ini adalah Janna-S, Sida-S dan Nabila-S. Dapatan hasil analisis transkrip berfikir secara
Murid Berpencapaian Sederhana Murid berpencapaian sederhana yang terlibat dengan pengumpulan data dalam kajian ini adalah Janna-S, Sida-S dan Nabila-S. Dapatan hasil analisis transkrip berfikir secara
1 P a g e Kimia SPM Ulangkaji Pantas T4. Milik abadi :.. Tingkatan 4. : Frequently Asked Questions
 1 P a g e Kimia SPM Ulangkaji Pantas T4 Milik abadi :.. Tingkatan 4 2 P a g e Kimia SPM Ulangkaji Pantas T4 1) Apakah itu takat lebur sesuatu bahan? adalah suhu di mana bahan berkeadaan pepejal berubah
1 P a g e Kimia SPM Ulangkaji Pantas T4 Milik abadi :.. Tingkatan 4 2 P a g e Kimia SPM Ulangkaji Pantas T4 1) Apakah itu takat lebur sesuatu bahan? adalah suhu di mana bahan berkeadaan pepejal berubah
Antiremed Kelas 11 Kimia
 Antiremed Kelas 11 Kimia Stoikiometri Larutan - Latihan Soal Doc. Name: AR11KIM0699 Doc. Version : 2012-07 01. Zat-zat berikut ini dapat bereaksi dengan larutan asam sulfat, kecuali... (A) kalsium oksida
Antiremed Kelas 11 Kimia Stoikiometri Larutan - Latihan Soal Doc. Name: AR11KIM0699 Doc. Version : 2012-07 01. Zat-zat berikut ini dapat bereaksi dengan larutan asam sulfat, kecuali... (A) kalsium oksida
EzLearn2U.my. TINGKATAN 4 KIMIA BAB 3 FORMULA & PERSAMAAN KIMIA Soalan Objektif. 1 Persamaan berikut mewakili satu tindak balas.
 TINGKTN 4 KIMI 3 FORMUL & PERSMN KIMI Soalan Objektif Persamaan berikut mewakili satu tindak balas. 3H2 (g) + N2 (g) 2NH3 (g) pakah jisim molekul relative bagi hasil tersebut? [Jisim atom relatif : H=
TINGKTN 4 KIMI 3 FORMUL & PERSMN KIMI Soalan Objektif Persamaan berikut mewakili satu tindak balas. 3H2 (g) + N2 (g) 2NH3 (g) pakah jisim molekul relative bagi hasil tersebut? [Jisim atom relatif : H=
FAKULTAS TEKNIK UNIVERSITAS NEGERI YOGYAKARTA BAHAN AJAR KIMIA DASAR BAB IV STOIKIOMETRI
 No. BAK/TBB/SBG201 Revisi : 00 Tgl. 01 Mei 2008 Hal 1 dari 6 BAB IV STOIKIOMETRI A. HUKUM GAY LUSSAC Bila diukur pada suhu dan tekanan yang sama, volum gas yang bereaksi dan volum gas hasil reaksi berbanding
No. BAK/TBB/SBG201 Revisi : 00 Tgl. 01 Mei 2008 Hal 1 dari 6 BAB IV STOIKIOMETRI A. HUKUM GAY LUSSAC Bila diukur pada suhu dan tekanan yang sama, volum gas yang bereaksi dan volum gas hasil reaksi berbanding
LOGO. Stoikiometri. Tim Dosen Pengampu MK. Kimia Dasar
 LOGO Stoikiometri Tim Dosen Pengampu MK. Kimia Dasar Konsep Mol Satuan jumlah zat dalam ilmu kimia disebut mol. 1 mol zat mengandung jumlah partikel yang sama dengan jumlah partikel dalam 12 gram C 12,
LOGO Stoikiometri Tim Dosen Pengampu MK. Kimia Dasar Konsep Mol Satuan jumlah zat dalam ilmu kimia disebut mol. 1 mol zat mengandung jumlah partikel yang sama dengan jumlah partikel dalam 12 gram C 12,
FAKULTAS TEKNIK UNIVERSITAS NEGERI YOGYAKARTA BAHAN AJAR KIMIA DASAR BAB II RUMUS KIMIA DAN TATANAMA
 No. BAK/TBB/SBG201 Revisi : 00 Tgl. 01 Mei 2008 Hal 1 dari 6 BAB II RUMUS KIMIA DAN TATANAMA A. Rumus Kimia Rumus kimia merupakan kumpulan lambang atom dengan komposisi tertentu. Rumus kimia terdiri dari
No. BAK/TBB/SBG201 Revisi : 00 Tgl. 01 Mei 2008 Hal 1 dari 6 BAB II RUMUS KIMIA DAN TATANAMA A. Rumus Kimia Rumus kimia merupakan kumpulan lambang atom dengan komposisi tertentu. Rumus kimia terdiri dari
STOKIOMETRI BAB. B. Konsep Mol 1. Hubungan Mol dengan Jumlah Partikel. Contoh: Jika Ar Ca = 40, Ar O = 16, Ar H = 1, tentukan Mr Ca(OH) 2!
 BAB 7 STOKIOMETRI A. Massa Molekul Relatif Massa Molekul Relatif (Mr) biasanya dihitung menggunakan data Ar masing-masing atom yang ada dalam molekul tersebut. Mr senyawa = (indeks atom x Ar atom) Contoh:
BAB 7 STOKIOMETRI A. Massa Molekul Relatif Massa Molekul Relatif (Mr) biasanya dihitung menggunakan data Ar masing-masing atom yang ada dalam molekul tersebut. Mr senyawa = (indeks atom x Ar atom) Contoh:
BAB IV BILANGAN OKSIDASI DAN TATA NAMA SENYAWA
 BAB IV BILANGAN OKSIDASI DAN TATA NAMA SENYAWA 1. BILANGAN OKSIDASI Bilangan oksidasi suatu unsur menggambarkan kemampuan unsur tersebut berikatan dengan unsur lain dan menunjukkan bagaimana peranan elektron
BAB IV BILANGAN OKSIDASI DAN TATA NAMA SENYAWA 1. BILANGAN OKSIDASI Bilangan oksidasi suatu unsur menggambarkan kemampuan unsur tersebut berikatan dengan unsur lain dan menunjukkan bagaimana peranan elektron
Ujian Akhir Semester Mata Pelajaran Kimia Kelas X Wacana berikut digunakan untuk menjawab soal no 1 dan 2. Ditentukan 5 unsur dengan konfigurasi
 Ujian Akhir Semester Mata Pelajaran Kimia Kelas X Wacana berikut digunakan untuk menjawab soal no 1 dan 2. Ditentukan 5 unsur dengan konfigurasi elektron sebagai berikut: P : 2 8 7 S : 2 8 8 Q : 2 8 8
Ujian Akhir Semester Mata Pelajaran Kimia Kelas X Wacana berikut digunakan untuk menjawab soal no 1 dan 2. Ditentukan 5 unsur dengan konfigurasi elektron sebagai berikut: P : 2 8 7 S : 2 8 8 Q : 2 8 8
Reaksi Dan Stoikiometri Larutan
 A. PERSAMAAN REAKSI ION Reaksi Dan Stoikiometri Larutan Persamaan reaksi ion adalah persamaan reaksi yang menjelaskan bagaimana reaksi antar-ion terjadi pada elektrolit. Persamaan reaksi ion terdiri dari:
A. PERSAMAAN REAKSI ION Reaksi Dan Stoikiometri Larutan Persamaan reaksi ion adalah persamaan reaksi yang menjelaskan bagaimana reaksi antar-ion terjadi pada elektrolit. Persamaan reaksi ion terdiri dari:
Reaksi dan Stoikiometri Larutan
 Reaksi dan Stoikiometri Larutan A. PERSAMAAN REAKSI ION Persamaan reaksi ion adalah persamaan reaksi yang menjelaskan bagaimana reaksi antar-ion terjadi pada larutan elektrolit. Persamaan reaksi ion terdiri
Reaksi dan Stoikiometri Larutan A. PERSAMAAN REAKSI ION Persamaan reaksi ion adalah persamaan reaksi yang menjelaskan bagaimana reaksi antar-ion terjadi pada larutan elektrolit. Persamaan reaksi ion terdiri
MODUL KIMIA SMA IPA Kelas 10
 SMA IPA Kelas 0 A. Massa Atom. Massa Atom Relatif (Ar) Massa atom relatif (Ar) merupakan perbandingan massa atom dengan massa satu atom yang tetap. Secara matematis dapat dirumuskan sebagai berikut. sma
SMA IPA Kelas 0 A. Massa Atom. Massa Atom Relatif (Ar) Massa atom relatif (Ar) merupakan perbandingan massa atom dengan massa satu atom yang tetap. Secara matematis dapat dirumuskan sebagai berikut. sma
Hubungan koefisien dalam persamaan reaksi dengan hitungan
 STOIKIOMETRI Pengertian Stoikiometri adalah ilmu yang mempelajari dan menghitung hubungan kuantitatif dari reaktan dan produk dalam reaksi kimia (persamaan kimia) Stoikiometri adalah hitungan kimia Hubungan
STOIKIOMETRI Pengertian Stoikiometri adalah ilmu yang mempelajari dan menghitung hubungan kuantitatif dari reaktan dan produk dalam reaksi kimia (persamaan kimia) Stoikiometri adalah hitungan kimia Hubungan
Asid dalam keadaan kering (tanpa kehadiran air) tidak menunjukkan sifat keasidannya kerana ion-ion hidrogen tidak hadir.
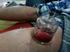 7.2 PERANAN AIR DALAM MENUNJUKKAN SIFAT ASID DAN ALKALI Asid dalam keadaan kering (tanpa kehadiran air) tidak menunjukkan sifat keasidannya kerana ion-ion hidrogen tidak hadir. H Cl H Cl + Air Cl - H +
7.2 PERANAN AIR DALAM MENUNJUKKAN SIFAT ASID DAN ALKALI Asid dalam keadaan kering (tanpa kehadiran air) tidak menunjukkan sifat keasidannya kerana ion-ion hidrogen tidak hadir. H Cl H Cl + Air Cl - H +
Asam + Oksida Basa Garam + air
 MODUL JENIS - JENIS REAKSI dalam LARUTAN Jenis-Jenis reaksi antara lain : Reaksi Asam dan Basa Reaksi pendesakan logam Reaksi Metatesis ( Dekomposisi ) A. PENGGARAMAN Jenis-jenis Reaksi penggaraman : 1.
MODUL JENIS - JENIS REAKSI dalam LARUTAN Jenis-Jenis reaksi antara lain : Reaksi Asam dan Basa Reaksi pendesakan logam Reaksi Metatesis ( Dekomposisi ) A. PENGGARAMAN Jenis-jenis Reaksi penggaraman : 1.
KONSEP MOL DAN STOIKIOMETRI
 BAB V KONSEP MOL DAN STOIKIOMETRI Dalam ilmu fisika, dikenal satuan mol untuk besaran jumlah zat. Dalam bab ini, akan dibahas mengenai konsep mol yang mendasari perhitungan kimia (stoikiometri). A. KONSEP
BAB V KONSEP MOL DAN STOIKIOMETRI Dalam ilmu fisika, dikenal satuan mol untuk besaran jumlah zat. Dalam bab ini, akan dibahas mengenai konsep mol yang mendasari perhitungan kimia (stoikiometri). A. KONSEP
LEMBAR AKTIVITAS SISWA ( LAS )
 LEMBAR AKTIVITAS SISWA ( LAS ) 1. Sebanyak 2 gram suatu logam alkali tanah dilarutkan dalam asam klorida menghasilan 1,25 liter gas hidrogen ( T,P ).Pada ( T,P ) yang sama 5,6 gram N 2 mempunyai volume
LEMBAR AKTIVITAS SISWA ( LAS ) 1. Sebanyak 2 gram suatu logam alkali tanah dilarutkan dalam asam klorida menghasilan 1,25 liter gas hidrogen ( T,P ).Pada ( T,P ) yang sama 5,6 gram N 2 mempunyai volume
Stoikiometri. OLEH Lie Miah
 Stoikiometri OLEH Lie Miah 1 STANDAR KOMPETENSI KOMPETENSI DASAR INDIKATOR KARAKTERISTIK MATERI KESULITAN BELAJAR SISWA STANDAR KOMPETENSI Memahami hukum-hukum dasar Kimia dan penerapannya dalam perhitungan
Stoikiometri OLEH Lie Miah 1 STANDAR KOMPETENSI KOMPETENSI DASAR INDIKATOR KARAKTERISTIK MATERI KESULITAN BELAJAR SISWA STANDAR KOMPETENSI Memahami hukum-hukum dasar Kimia dan penerapannya dalam perhitungan
STOIKIOMETRI. Oleh. Sitti Rahmawati S.Pd.
 STOIKIOMETRI Oleh Sitti Rahmawati S.Pd Copyright oke.or.id Artikel ini boleh dicopy,diubah, dikutip, di cetak dalam media kertas atau yang lain, dipublikasikan kembali dalam berbagai bentuk dengan tetap
STOIKIOMETRI Oleh Sitti Rahmawati S.Pd Copyright oke.or.id Artikel ini boleh dicopy,diubah, dikutip, di cetak dalam media kertas atau yang lain, dipublikasikan kembali dalam berbagai bentuk dengan tetap
BAB III TATA NAMA SENYAWA DAN PERSAMAAN REAKSI
 BAB III TATA NAMA SENYAWA DAN PERSAMAAN REAKSI A. STANDAR KOMPETENSI Mendiskripsikan hukumhukum dasar kimia dan penerapannya dalam perhitungan kimia. B. Kompetensi Dasar : Menuliskan nama senyawa anorganik
BAB III TATA NAMA SENYAWA DAN PERSAMAAN REAKSI A. STANDAR KOMPETENSI Mendiskripsikan hukumhukum dasar kimia dan penerapannya dalam perhitungan kimia. B. Kompetensi Dasar : Menuliskan nama senyawa anorganik
30 Soal Pilihan Berganda Olimpiade Kimia Tingkat Kabupaten/Kota 2011 Alternatif jawaban berwarna merah adalah kunci jawabannya.
 30 Soal Pilihan Berganda Olimpiade Kimia Tingkat Kabupaten/Kota 2011 Alternatif jawaban berwarna merah adalah kunci jawabannya. 1. Semua pernyataan berikut benar, kecuali: A. Energi kimia ialah energi
30 Soal Pilihan Berganda Olimpiade Kimia Tingkat Kabupaten/Kota 2011 Alternatif jawaban berwarna merah adalah kunci jawabannya. 1. Semua pernyataan berikut benar, kecuali: A. Energi kimia ialah energi
STOIKIOMETRI. STOIKIOMETRI adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif dari komposisi zat-zat kimia dan reaksi-reaksinya.
 STOIKIOMETRI STOIKIOMETRI adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif dari komposisi zat-zat kimia dan reaksi-reaksinya. 1.HUKUM KEKEKALAN MASSA = HUKUM LAVOISIER "Massa zat-zat sebelum
STOIKIOMETRI STOIKIOMETRI adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif dari komposisi zat-zat kimia dan reaksi-reaksinya. 1.HUKUM KEKEKALAN MASSA = HUKUM LAVOISIER "Massa zat-zat sebelum
LEMBARAN SOAL 4. Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA )
 LEMBARAN SOAL 4 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah
LEMBARAN SOAL 4 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : XI IPA ( SEBELAS IPA ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah
Chapter 7 Larutan tirtawi (aqueous solution)
 Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi modif oleh Dr I Kartini Chapter 7 Larutan tirtawi (aqueous solution) Larutan adalah campuran yang homogen dari dua atau lebih
Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi modif oleh Dr I Kartini Chapter 7 Larutan tirtawi (aqueous solution) Larutan adalah campuran yang homogen dari dua atau lebih
Tata Nama Senyawa Kimia
 ~CO2 = KARBONDIOKSIDA ~NaCl = NATRIUM KLORIDA ~CH3COOH = CUKA / ASAM ASETAT ~H2SO4 = ASAM SULFAT ~Na2CO3 = NATRIUM KARBONAT ~MgCO3 = MAGNESIUM KARBONAT ~NaOH = NATRIUM KARBONAT ~(NH4)2SO4 = AMONIUM SULFAT
~CO2 = KARBONDIOKSIDA ~NaCl = NATRIUM KLORIDA ~CH3COOH = CUKA / ASAM ASETAT ~H2SO4 = ASAM SULFAT ~Na2CO3 = NATRIUM KARBONAT ~MgCO3 = MAGNESIUM KARBONAT ~NaOH = NATRIUM KARBONAT ~(NH4)2SO4 = AMONIUM SULFAT
KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI
 KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI 1. Untuk membuat 500 ml larutan H 2 SO 4 0.05 M dibutuhkan larutan H 2 SO 4 5 M sebanyak ml a. 5 ml b. 10 ml c. 2.5 ml d. 15 ml e. 5.5 ml 2. Konsentrasi larutan yang
KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI 1. Untuk membuat 500 ml larutan H 2 SO 4 0.05 M dibutuhkan larutan H 2 SO 4 5 M sebanyak ml a. 5 ml b. 10 ml c. 2.5 ml d. 15 ml e. 5.5 ml 2. Konsentrasi larutan yang
TENAGA DAN PERUBAHAN KIMIA
 1 BAB 6 TENAGA DAN PERUBAHAN KIMIA 6.1: Perubahan Kimia dan Perubahan Fizik Perubahan Fizik 1. Maksud: Perubahan yang tidak menghasilkan bahan baru. Hanya sifat fizik bahan berubah 2. Perubahan fizik Contoh
1 BAB 6 TENAGA DAN PERUBAHAN KIMIA 6.1: Perubahan Kimia dan Perubahan Fizik Perubahan Fizik 1. Maksud: Perubahan yang tidak menghasilkan bahan baru. Hanya sifat fizik bahan berubah 2. Perubahan fizik Contoh
LEMBARAN SOAL 11. Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH )
 LEMBARAN SOAL 11 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan. Periksa dan bacalah soal dengan
LEMBARAN SOAL 11 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan. Periksa dan bacalah soal dengan
MODUL STOIKIOMETRI 1
 MODUL STOIKIOMETRI 1 1. Pengertian Mol Mol merupakan suatu satuan jumlah, yang berasal dari kata moles yang artinya sejumlah massa / sejumlah kecil massa, hampir sama dengan lusin. 1 mol = 6,02 X 10 23
MODUL STOIKIOMETRI 1 1. Pengertian Mol Mol merupakan suatu satuan jumlah, yang berasal dari kata moles yang artinya sejumlah massa / sejumlah kecil massa, hampir sama dengan lusin. 1 mol = 6,02 X 10 23
Soal 5 Jumlah mol dari 29,8 gram amonium fosfat ((NH4)3PO4) (Ar N = 14, H = 1, dan P = 31) adalah. A. 0,05 mol
 Bank Soal Stoikiometri Kimia Bagian 2 Soal 1 Satu liter campuran gas terdiri dari 60% volume metana (CH4) dan sisanya gas etana (C2H6) dibakar sempurna sesuai reaksi: CH4 + 3 O2 2 CO2 + 2 H2O 2 C2H6 +
Bank Soal Stoikiometri Kimia Bagian 2 Soal 1 Satu liter campuran gas terdiri dari 60% volume metana (CH4) dan sisanya gas etana (C2H6) dibakar sempurna sesuai reaksi: CH4 + 3 O2 2 CO2 + 2 H2O 2 C2H6 +
Materi Pokok Bahasan :
 STOIKIOMETRI Kompetensi : Memiliki kemampuan untuk menginterpretasikan serta menerapkan dalam perhitungan kimia. Memiliki kemampuan untuk mengaplikasikan pengetahuan yang dimilikinya dan terbiasa menggunakan
STOIKIOMETRI Kompetensi : Memiliki kemampuan untuk menginterpretasikan serta menerapkan dalam perhitungan kimia. Memiliki kemampuan untuk mengaplikasikan pengetahuan yang dimilikinya dan terbiasa menggunakan
EzLearn2U.my. TINGKATAN 4 KIMIA BAB 2 STRUKTUR ATOM Soalan Objektif. Apakah keadaan fizikal bahan W, X, Y dan
 TINGKATAN 4 KIMIA BAB 2 STRUKTUR ATOM Soalan Objektif Siapakah yang mencadangkan model di atas? A B C D Proton Ernest Rutherford James Chadwick J.J Thomson Neils Bohr 2 Apakah keadaan fizikal jirim di
TINGKATAN 4 KIMIA BAB 2 STRUKTUR ATOM Soalan Objektif Siapakah yang mencadangkan model di atas? A B C D Proton Ernest Rutherford James Chadwick J.J Thomson Neils Bohr 2 Apakah keadaan fizikal jirim di
SKEMA PEPERIKSAAN PERCUBAAN KIMIA 2017 KERTAS 1 https://cikguadura.wordpress.com/
 SKEMA PEPERIKSAAN PERCUBAAN KIMIA 07 KERTAS https://cikguadura.wordpress.com/ NO NO JAWAPAN SOALAN SOALAN JAWAPAN D 6 D A 7 C D 8 C 4 B 9 B 5 C 0 D 6 D A 7 D D 8 B A 9 C 4 A 0 C 5 A D 6 C B 7 D B 8 B 4
SKEMA PEPERIKSAAN PERCUBAAN KIMIA 07 KERTAS https://cikguadura.wordpress.com/ NO NO JAWAPAN SOALAN SOALAN JAWAPAN D 6 D A 7 C D 8 C 4 B 9 B 5 C 0 D 6 D A 7 D D 8 B A 9 C 4 A 0 C 5 A D 6 C B 7 D B 8 B 4
KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI
 KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI 1. Untuk membuat 500 ml larutan H2SO4 0.05 M dibutuhkan larutan H2SO4 5 M sebanyak ml a. 5 ml b. 10 ml c. 2.5 ml d. 15 ml e. 5.5
KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI KUMPULAN SOAL-SOAL KIMIA LAJU REAKSI 1. Untuk membuat 500 ml larutan H2SO4 0.05 M dibutuhkan larutan H2SO4 5 M sebanyak ml a. 5 ml b. 10 ml c. 2.5 ml d. 15 ml e. 5.5
soal stoikiometri larutan I. KEGIATAN: 1. Logam aluminium sebanyak 2,7 gram direaksikan dengan larutan asam sulfat. Hitunglah: (a) Volume gas yang
 soal stoikiometri larutan I. KEGIATAN: 1. Logam aluminium sebanyak 2,7 gram direaksikan dengan larutan asam sulfat. Hitunglah: (a) Volume gas yang dihasilkan pada t,p tertentu bila 8 gram gas oksigen volumenya
soal stoikiometri larutan I. KEGIATAN: 1. Logam aluminium sebanyak 2,7 gram direaksikan dengan larutan asam sulfat. Hitunglah: (a) Volume gas yang dihasilkan pada t,p tertentu bila 8 gram gas oksigen volumenya
Oksidasi dan Reduksi
 Oksidasi dan Reduksi Reaksi kimia dapat diklasifikasikan dengan beberapa cara antara lain reduksi-oksidasi (redoks) Reaksi : selalu terjadi bersama-sama. Zat yang teroksidasi = reduktor Zat yang tereduksi
Oksidasi dan Reduksi Reaksi kimia dapat diklasifikasikan dengan beberapa cara antara lain reduksi-oksidasi (redoks) Reaksi : selalu terjadi bersama-sama. Zat yang teroksidasi = reduktor Zat yang tereduksi
SOAL LAJU REAKSI. Mol CaCO 3 = = 0.25 mol = 25. m Mr
 SOAL LAJU REAKSI 1. Untuk membuat 500 ml larutan H 2 SO 4 0.05 M dibutuhkan larutan H 2 SO 4 5 M sebanyak ml A. 5 ml B. 10 ml C. 2.5 ml D. 15 ml E. 5.5 ml : A Mencari volume yang dibutuhkan pada proses
SOAL LAJU REAKSI 1. Untuk membuat 500 ml larutan H 2 SO 4 0.05 M dibutuhkan larutan H 2 SO 4 5 M sebanyak ml A. 5 ml B. 10 ml C. 2.5 ml D. 15 ml E. 5.5 ml : A Mencari volume yang dibutuhkan pada proses
Review II. 1. Pada elektrolisis larutan NaCl dengan elektroda karbon, reaksi yang terjadi pada katoda adalah... A. 2H 2
 KIMIA KELAS XII IPA - KURIKULUM GABUNGAN 14 Sesi NGAN Review II A. ELEKTROLISIS 1. Pada elektrolisis larutan NaCl dengan elektroda karbon, reaksi yang terjadi pada katoda adalah... A. 2H 2 O 4H + + O 2
KIMIA KELAS XII IPA - KURIKULUM GABUNGAN 14 Sesi NGAN Review II A. ELEKTROLISIS 1. Pada elektrolisis larutan NaCl dengan elektroda karbon, reaksi yang terjadi pada katoda adalah... A. 2H 2 O 4H + + O 2
EzLearn2U.my. TINGKATAN 4 KIMIA BAB 6 ELEKTROLISIS Soalan Objektif. Antara yang berikut, yang manakah
 TINGKTN 4 KIMI 6 ELEKTROLISIS Soalan Objektif 1 ntara yang berikut, yang manakah merupakan elektrolit? Larutan kuprum (II) sulfat Leburan naftalena Larutan glukosa Logam zink 2 alam rajah di bawah, bahan
TINGKTN 4 KIMI 6 ELEKTROLISIS Soalan Objektif 1 ntara yang berikut, yang manakah merupakan elektrolit? Larutan kuprum (II) sulfat Leburan naftalena Larutan glukosa Logam zink 2 alam rajah di bawah, bahan
Stoikiometri. Bab 3. Massa atom merupakan massa dari atom dalam satuan massa atom (sma). Secara Mikro atom & molekul.
 Bab 3 Stoikiometri Secara Mikro atom & molekul Secara Makro gram Massa atom merupakan massa dari atom dalam satuan massa atom (sma). Perjanjian internasional: 1 atom 12 C beratnya 12 sma Jika ditimbang
Bab 3 Stoikiometri Secara Mikro atom & molekul Secara Makro gram Massa atom merupakan massa dari atom dalam satuan massa atom (sma). Perjanjian internasional: 1 atom 12 C beratnya 12 sma Jika ditimbang
Sumber: Silberberg, Chemistry: The Molecular Nature of Matter and Change
 Bab V Perhitungan Kimia Sumber: Silberberg, Chemistry: The Molecular Nature of Matter and Change Jumlah permen dalam stoples dapat diketahui jika berat dari satu permen dan seluruh permen diketahui. Cara
Bab V Perhitungan Kimia Sumber: Silberberg, Chemistry: The Molecular Nature of Matter and Change Jumlah permen dalam stoples dapat diketahui jika berat dari satu permen dan seluruh permen diketahui. Cara
Soal-soal Redoks dan elektrokimia
 1. Reaksi redoks : MnO 4 (aq) + C 2 O 4 2- (aq) Mn 2+ (aq) + CO 2 (g), berlangsung dalam suasana asam. Setiap mol MnO 4 memerlukan H + sebanyak A. 4 mol B. 6 mol D. 10 mol C. 8 mol E. 12 mol 2. Reaksi
1. Reaksi redoks : MnO 4 (aq) + C 2 O 4 2- (aq) Mn 2+ (aq) + CO 2 (g), berlangsung dalam suasana asam. Setiap mol MnO 4 memerlukan H + sebanyak A. 4 mol B. 6 mol D. 10 mol C. 8 mol E. 12 mol 2. Reaksi
Hukum Dasar Kimia Dan Konsep Mol
 A. PENDAHULUAN Hukum Dasar Kimia Dan Konsep Mol Hukum dasar kimia merupakan hukum dasar yang digunakan dalam stoikiometri (perhitungan kimia), antara lain: 1) Hukum Lavoisier atau hukum kekekalan massa.
A. PENDAHULUAN Hukum Dasar Kimia Dan Konsep Mol Hukum dasar kimia merupakan hukum dasar yang digunakan dalam stoikiometri (perhitungan kimia), antara lain: 1) Hukum Lavoisier atau hukum kekekalan massa.
BAB V PERHITUNGAN KIMIA
 BAB V PERHITUNGAN KIMIA KOMPETENSI DASAR 2.3 : Menerapkan hukum Gay Lussac dan hukum Avogadro serta konsep mol dalam menyelesaikan perhitungan kimia (stoikiometri ) Indikator : 1. Siswa dapat menghitung
BAB V PERHITUNGAN KIMIA KOMPETENSI DASAR 2.3 : Menerapkan hukum Gay Lussac dan hukum Avogadro serta konsep mol dalam menyelesaikan perhitungan kimia (stoikiometri ) Indikator : 1. Siswa dapat menghitung
Ikatan kimia. 1. Peranan Elektron dalam Pembentukan Ikatan Kimia. Ikatan kimia
 Ikatan kimia 1. Peranan Elektron dalam Pembentukan Ikatan Kimia Ikatan kimia Gaya tarik menarik antara atom sehingga atom tersebut tetap berada bersama-sama dan terkombinasi dalam senyawaan. gol 8 A sangat
Ikatan kimia 1. Peranan Elektron dalam Pembentukan Ikatan Kimia Ikatan kimia Gaya tarik menarik antara atom sehingga atom tersebut tetap berada bersama-sama dan terkombinasi dalam senyawaan. gol 8 A sangat
III. REAKSI KIMIA. Jenis kelima adalah reaksi penetralan, merupakan reaksi asam dengan basa membentuk garam dan air.
 III. REAKSI KIMIA Tujuan 1. Mengamati bukti terjadinya suatu reaksi kimia. 2. Menuliskan persamaan reaksi kimia. 3. Mempelajari secara sistematis lima jenis reaksi utama. 4. Membuat logam tembaga dari
III. REAKSI KIMIA Tujuan 1. Mengamati bukti terjadinya suatu reaksi kimia. 2. Menuliskan persamaan reaksi kimia. 3. Mempelajari secara sistematis lima jenis reaksi utama. 4. Membuat logam tembaga dari
Tabel Periodik. Bab 3a. Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi 2010 dimodifikasi oleh Dr.
 Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi 2010 dimodifikasi oleh Dr. Indriana Kartini Bab 3a Tabel Periodik Kapan unsur-unsur ditemukan? 8.1 1 ns 1 Konfigurasi elektron
Presentasi Powerpoint Pengajar oleh Penerbit ERLANGGA Divisi Perguruan Tinggi 2010 dimodifikasi oleh Dr. Indriana Kartini Bab 3a Tabel Periodik Kapan unsur-unsur ditemukan? 8.1 1 ns 1 Konfigurasi elektron
BAB 1V HASIL DAN PEMBAHASAN
 4.1.1 HASIL PENELITIAN BAB 1V HASIL DAN PEMBAHASAN Berdasarkan data hasil penelitian, persentase kemampuan siswa kelas dalam menyelesaikan soal-soal persamaan reaksi kimia dapat dilihat pada tabel dibawah
4.1.1 HASIL PENELITIAN BAB 1V HASIL DAN PEMBAHASAN Berdasarkan data hasil penelitian, persentase kemampuan siswa kelas dalam menyelesaikan soal-soal persamaan reaksi kimia dapat dilihat pada tabel dibawah
= 125 = em' (unit betul)
 SULT 4541/2 BAHAGAN A 1. a. (i) Proses pergerakan zarah daripada kawasantumpat kepada kawasan kurang tumpat proses pergerakanzarah daripada kawasan berkepekatan tinggi kepada kawasan berkepekatanrendah.
SULT 4541/2 BAHAGAN A 1. a. (i) Proses pergerakan zarah daripada kawasantumpat kepada kawasan kurang tumpat proses pergerakanzarah daripada kawasan berkepekatan tinggi kepada kawasan berkepekatanrendah.
LOGO STOIKIOMETRI. Marselinus Laga Nur
 LOGO STOIKIOMETRI Marselinus Laga Nur Materi Pokok Bahasan : A. Konsep Mol B. Penentuan Rumus Kimia C. Koefisien Reaksi D. Hukum-hukum Gas A. Konsep Mol Pengertian konsep mol Hubungan mol dengan jumlah
LOGO STOIKIOMETRI Marselinus Laga Nur Materi Pokok Bahasan : A. Konsep Mol B. Penentuan Rumus Kimia C. Koefisien Reaksi D. Hukum-hukum Gas A. Konsep Mol Pengertian konsep mol Hubungan mol dengan jumlah
No. BAK/TBB/SBG201 Revisi : 00 Tgl. 01 Mei 2008 Hal 1 dari 8 Semester I BAB I Prodi PT Boga BAB I MATERI
 No. BAK/TBB/SBG201 Revisi : 00 Tgl. 01 Mei 2008 Hal 1 dari 8 BAB I MATERI Materi adalah sesuatu yang menempati ruang dan mempunyai massa. Materi dapat berupa benda padat, cair, maupun gas. A. Penggolongan
No. BAK/TBB/SBG201 Revisi : 00 Tgl. 01 Mei 2008 Hal 1 dari 8 BAB I MATERI Materi adalah sesuatu yang menempati ruang dan mempunyai massa. Materi dapat berupa benda padat, cair, maupun gas. A. Penggolongan
Emas yang terbentuk sebanyak 20 gram, jika ArAu = 198, maka tentukan Ar M!
 1. Suatu senyawa mengandung kadar unsur (% berat) sebagai berikut : S = 35,97%; O = 62,9%; dan H = 1,13%. Rumus molekul senyawa tersebut adalah. 2. Gas hidrogen dapat dibuat dari reaksi antara logam magnesium
1. Suatu senyawa mengandung kadar unsur (% berat) sebagai berikut : S = 35,97%; O = 62,9%; dan H = 1,13%. Rumus molekul senyawa tersebut adalah. 2. Gas hidrogen dapat dibuat dari reaksi antara logam magnesium
Massa atom merupakan massa dari atom dalam satuan massa atom (sma).
 Bab 3 Stoikiometri Secara Mikro atom & molekul Secara Makro gram Massa atom merupakan massa dari atom dalam satuan massa atom (sma). Perjanjian internasional: 1 atom 12 C beratnya 12 sma Jika ditimbang
Bab 3 Stoikiometri Secara Mikro atom & molekul Secara Makro gram Massa atom merupakan massa dari atom dalam satuan massa atom (sma). Perjanjian internasional: 1 atom 12 C beratnya 12 sma Jika ditimbang
TES AWAL II KIMIA DASAR II (KI-112)
 TES AWAL II KIMIA DASAR II (KI112) NAMA : Tanda Tangan N I M : JURUSAN :... BERBAGAI DATA. Tetapan gas R = 0,082 L atm mol 1 K 1 = 1,987 kal mol 1 K 1 = 8,314 J mol 1 K 1 Tetapan Avogadro = 6,023 x 10
TES AWAL II KIMIA DASAR II (KI112) NAMA : Tanda Tangan N I M : JURUSAN :... BERBAGAI DATA. Tetapan gas R = 0,082 L atm mol 1 K 1 = 1,987 kal mol 1 K 1 = 8,314 J mol 1 K 1 Tetapan Avogadro = 6,023 x 10
SMA NEGERI 6 SURABAYA LARUTAN ASAM & BASA. K a = 2.M a. 2. H 2 SO 4 (asam kuat) α = 1 H 2 SO 4 2H + 2
 SMA NEGERI 6 SURABAYA LARUTAN ASAM & BASA K I M I A 1). TEORI ARCHENIUS Asam adalah zat yang jika di dalam air melepaskan ion H +, dengan kata lain pembawa sifat asam adalah ion H +. jumlah ion H+ yang
SMA NEGERI 6 SURABAYA LARUTAN ASAM & BASA K I M I A 1). TEORI ARCHENIUS Asam adalah zat yang jika di dalam air melepaskan ion H +, dengan kata lain pembawa sifat asam adalah ion H +. jumlah ion H+ yang
PEPERIKSAAN PERCUBAAN SPM SELARAS ANTARA SBP
 Kimia Kertas 1 Ogos 2003 1 ¼ jam SEKOLH-SEKOLH ERSRM PENUH KEMENTERN PENKN MLYS PEPERKSN PERUN SPM SELRS NTR SP http://cikguadura.wordpress.com/ KM Kertas 1 Satu jam lima belas minit JNGN UK KERTS SOLN
Kimia Kertas 1 Ogos 2003 1 ¼ jam SEKOLH-SEKOLH ERSRM PENUH KEMENTERN PENKN MLYS PEPERKSN PERUN SPM SELRS NTR SP http://cikguadura.wordpress.com/ KM Kertas 1 Satu jam lima belas minit JNGN UK KERTS SOLN
 UJIAN MASUK BERSAMA (UMB) Mata Pelajaran : Kimia Tanggal : 07 Juni 009 Kode Soal : 9. Penamaan yang tepat untuk : CH CH CH CH CH CH OH CH CH adalah A. -etil-5-metil-6-heksanol B.,5-dimetil-1-heptanol C.
UJIAN MASUK BERSAMA (UMB) Mata Pelajaran : Kimia Tanggal : 07 Juni 009 Kode Soal : 9. Penamaan yang tepat untuk : CH CH CH CH CH CH OH CH CH adalah A. -etil-5-metil-6-heksanol B.,5-dimetil-1-heptanol C.
TES PRESTASI BELAJAR. Hari/tanggal : Senin/7 Mei 2012 Mata Pelajaran: Kimia Waktu : 90 menit
 TES PRESTASI BELAJAR Hari/tanggal : Senin/7 Mei 2012 Mata Pelajaran: Kimia Waktu : 90 menit Petunjuk : 1. Berdoalah sebelum mengerjakan soal 2. Bacalah petunjuk soal terlebih dahulu 3. Pilih salah satu
TES PRESTASI BELAJAR Hari/tanggal : Senin/7 Mei 2012 Mata Pelajaran: Kimia Waktu : 90 menit Petunjuk : 1. Berdoalah sebelum mengerjakan soal 2. Bacalah petunjuk soal terlebih dahulu 3. Pilih salah satu
STOIKIOMETRI STOIKIOMETRI
 BAB V STOIKIOMETRI Standar Kompetensi Memahami hukum-hukum dasar kimia dan penerapannya dalam perhitungan kimia (stoikiometri) Kompetensi Dasar Mendeskripsikan tata nama senyawa anorganik dan organik sederhana
BAB V STOIKIOMETRI Standar Kompetensi Memahami hukum-hukum dasar kimia dan penerapannya dalam perhitungan kimia (stoikiometri) Kompetensi Dasar Mendeskripsikan tata nama senyawa anorganik dan organik sederhana
SOAL KIMIA 2 KELAS : XI IPA
 SOAL KIMIA KELAS : XI IPA PETUNJUK UMUM. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan. Periksa dan bacalah soal dengan teliti sebelum Anda bekerja. Kerjakanlah soal anda pada lembar jawaban
SOAL KIMIA KELAS : XI IPA PETUNJUK UMUM. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan. Periksa dan bacalah soal dengan teliti sebelum Anda bekerja. Kerjakanlah soal anda pada lembar jawaban
TERMOKIMIA. Hukum Hess Perubahan entalpi reaksi tetap sama, baik berlangsung dalam satu tahap maupun beberapa tahap.
 TERMOKIMIA (Teori) Entalpi adalah jumlah total energi kalor yang terkandung dalam suatu materi Reaksi Eksoterm Menghasilkan kalor Melepas energi Perubahan entalpi negatif Reaksi Endoterm Menyerap kalor
TERMOKIMIA (Teori) Entalpi adalah jumlah total energi kalor yang terkandung dalam suatu materi Reaksi Eksoterm Menghasilkan kalor Melepas energi Perubahan entalpi negatif Reaksi Endoterm Menyerap kalor
SKL 2 RINGKASAN MATERI. 1. Konsep mol dan Bagan Stoikiometri ( kelas X )
 SKL 2 Menerapkan hukum-hukum dasar kimia untuk memecahkan masalah dalam perhitungan kimia. o Menganalisis persamaan reaksi kimia o Menyelesaikan perhitungan kimia yang berkaitan dengan hukum dasar kimia
SKL 2 Menerapkan hukum-hukum dasar kimia untuk memecahkan masalah dalam perhitungan kimia. o Menganalisis persamaan reaksi kimia o Menyelesaikan perhitungan kimia yang berkaitan dengan hukum dasar kimia
PEPERIKSAAN SPM 2016 TIPS DAN RAMALAN - KIMIA
 PEPERIKSAAN SPM 2016 TIPS DAN RAMALAN - KIMIA Tingkatan 4 Bab 2 & 3 (Struktur Atom & Formula & Persamaan Kimia) Spot dalam Struktur / Esei!! [SPM 2015 Bab 2 (Struktur K2): Tindak balas antara gas HCl dan
PEPERIKSAAN SPM 2016 TIPS DAN RAMALAN - KIMIA Tingkatan 4 Bab 2 & 3 (Struktur Atom & Formula & Persamaan Kimia) Spot dalam Struktur / Esei!! [SPM 2015 Bab 2 (Struktur K2): Tindak balas antara gas HCl dan
JIK 001- Kimia I UNIVERSITI SAINS MALAYSIA. Peperiksaan Semester Kedua Sidang Akademik 2002/2003. Februari/Mac 2003
 UNIVERSITI SAINS MALAYSIA Peperiksaan Semester Kedua Sidang Akademik 2002/2003 Februari/Mac 2003 JIK 001- Kimia I Masa : 3 jam Sila pastikan bahawa kertas peperiksaan ini mengandungi ENAM muka surat yang
UNIVERSITI SAINS MALAYSIA Peperiksaan Semester Kedua Sidang Akademik 2002/2003 Februari/Mac 2003 JIK 001- Kimia I Masa : 3 jam Sila pastikan bahawa kertas peperiksaan ini mengandungi ENAM muka surat yang
UH : ELEKTROLISIS & KOROSI KODE SOAL : A
 UH : ELEKTROLISIS & KOROSI KODE SOAL : A Selesaikan dengan cara!!! 1. Reduksi 1 mol ion SO 4 2- menjadi H 2S, memerlukan muatan listrik sebanyak A. 4 F D. 6 F B. 8F E. 16 F C. 20 F 2. Proses elektrolisis
UH : ELEKTROLISIS & KOROSI KODE SOAL : A Selesaikan dengan cara!!! 1. Reduksi 1 mol ion SO 4 2- menjadi H 2S, memerlukan muatan listrik sebanyak A. 4 F D. 6 F B. 8F E. 16 F C. 20 F 2. Proses elektrolisis
BAB 5 HUKUM DASAR KIMIA
 BAB 5 HUKUM DASAR KIMIA Dalam ilmu kimia perlu dipelajari massa dan volume zat-zat yang bereaksi dan zat yang dihasilkan dalam suatu reaksi kimia. Studi tentang hubungan-hubungan kuantitatif dalam suatu
BAB 5 HUKUM DASAR KIMIA Dalam ilmu kimia perlu dipelajari massa dan volume zat-zat yang bereaksi dan zat yang dihasilkan dalam suatu reaksi kimia. Studi tentang hubungan-hubungan kuantitatif dalam suatu
KERTAS 2 Masa : jam Bahagian A Jawab semua soalan dalam bahagian ini. ( 60 markah )
 KERTAS 2 Masa : 2 1 2 jam Bahagian A Jawab semua soalan dalam bahagian ini. ( 60 markah ) 1. Atom Bilangan proton Bilangan neutron Bilangan electron J 8 8 8 K 8 9 8 L 11 12 11 M 15 16 15 N 16 16 16 Q 19
KERTAS 2 Masa : 2 1 2 jam Bahagian A Jawab semua soalan dalam bahagian ini. ( 60 markah ) 1. Atom Bilangan proton Bilangan neutron Bilangan electron J 8 8 8 K 8 9 8 L 11 12 11 M 15 16 15 N 16 16 16 Q 19
L A R U T A N _KIMIA INDUSTRI_ DEWI HARDININGTYAS, ST, MT, MBA WIDHA KUSUMA NINGDYAH, ST, MT AGUSTINA EUNIKE, ST, MT, MBA
 L A R U T A N _KIMIA INDUSTRI_ DEWI HARDININGTYAS, ST, MT, MBA WIDHA KUSUMA NINGDYAH, ST, MT AGUSTINA EUNIKE, ST, MT, MBA 1. Larutan Elektrolit 2. Persamaan Ionik 3. Reaksi Asam Basa 4. Perlakuan Larutan
L A R U T A N _KIMIA INDUSTRI_ DEWI HARDININGTYAS, ST, MT, MBA WIDHA KUSUMA NINGDYAH, ST, MT AGUSTINA EUNIKE, ST, MT, MBA 1. Larutan Elektrolit 2. Persamaan Ionik 3. Reaksi Asam Basa 4. Perlakuan Larutan
Bab 4. Reaksi dalam Larutan Berair
 Bab 4 Reaksi dalam Larutan Berair Larutan adalah campuran yang homogen dari dua atau lebih zat. Zat yang jumlahnya lebih sedikit disebut zat terlarut. Zat yang jumlahnya lebih banyak disebut zat pelarut.
Bab 4 Reaksi dalam Larutan Berair Larutan adalah campuran yang homogen dari dua atau lebih zat. Zat yang jumlahnya lebih sedikit disebut zat terlarut. Zat yang jumlahnya lebih banyak disebut zat pelarut.
BAB 2. PERSAMAAN KIMIA DAN HASIL REAKSI
 BAB 2. PERSAMAAN KIMIA DAN HASIL REAKSI 1. RUMUS KIMIA 2. MENULISKAN PERSAMAAN KIMIA YANG BALANS 3. HUBUNGAN MASSA DALAM REAKSI KIMIA 4. REAKTAN PEMBATAS 5. HASIL PERSENTASE Reaktan (Pereaksi) Produk (Hasil
BAB 2. PERSAMAAN KIMIA DAN HASIL REAKSI 1. RUMUS KIMIA 2. MENULISKAN PERSAMAAN KIMIA YANG BALANS 3. HUBUNGAN MASSA DALAM REAKSI KIMIA 4. REAKTAN PEMBATAS 5. HASIL PERSENTASE Reaktan (Pereaksi) Produk (Hasil
D. Ag 2 S, Ksp = 1,6 x E. Ag 2 CrO 4, Ksp = 3,2 x 10-11
 1. Garam dengan kelarutan paling besar adalah... A. AgCl, Ksp = 10-10 B. AgI, Ksp = 10-16 C. Ag 2 CrO 4, Ksp = 3,2 x 10-12 D. Ag 2 S, Ksp = 1,6 x 10-49 E. Ag 2 CrO 4, Ksp = 3,2 x 10-11 Jadi garam dengan
1. Garam dengan kelarutan paling besar adalah... A. AgCl, Ksp = 10-10 B. AgI, Ksp = 10-16 C. Ag 2 CrO 4, Ksp = 3,2 x 10-12 D. Ag 2 S, Ksp = 1,6 x 10-49 E. Ag 2 CrO 4, Ksp = 3,2 x 10-11 Jadi garam dengan
KERTAS 2 Masa : jam Bahagian A Jawab semua soalan dalam bahagian ini. ( 60 markah )
 KERTAS 2 Masa : 2 1 2 jam Bahagian A Jawab semua soalan dalam bahagian ini. ( 60 markah ) 1. Cecair A ialah satu sebatian tak tepu. Cecair A mempunyai formula molekul C 7 H 14. Cecair B mempunyai formula
KERTAS 2 Masa : 2 1 2 jam Bahagian A Jawab semua soalan dalam bahagian ini. ( 60 markah ) 1. Cecair A ialah satu sebatian tak tepu. Cecair A mempunyai formula molekul C 7 H 14. Cecair B mempunyai formula
OLIMPIADE SAINS NASIONAL 2012 SELEKSI KABUPATEN / KOTA SOAL. UjianTeori. Waktu: 100 menit
 OLIMPIADE SAINS NASIONAL 2012 SELEKSI KABUPATEN / KOTA SOAL UjianTeori Waktu: 100 menit Kementerian Pendidikan dan Kebudayaan Direktorat Jenderal Pendidikan Menengah Direktorat Pembinaan Sekolah Menengah
OLIMPIADE SAINS NASIONAL 2012 SELEKSI KABUPATEN / KOTA SOAL UjianTeori Waktu: 100 menit Kementerian Pendidikan dan Kebudayaan Direktorat Jenderal Pendidikan Menengah Direktorat Pembinaan Sekolah Menengah
Reaksi dalam larutan berair
 Reaksi dalam larutan berair Drs. Iqmal Tahir, M.Si. iqmal@gadjahmada.edu Larutan - Suatu campuran homogen dua atau lebih senyawa. Pelarut (solven) - komponen dalam larutan yang membuat penuh larutan (ditandai
Reaksi dalam larutan berair Drs. Iqmal Tahir, M.Si. iqmal@gadjahmada.edu Larutan - Suatu campuran homogen dua atau lebih senyawa. Pelarut (solven) - komponen dalam larutan yang membuat penuh larutan (ditandai
PAKET UJIAN NASIONAL 9 Pelajaran : KIMIA Waktu : 120 Menit
 PAKET UJIAN NASIONAL 9 Pelajaran : KIMIA Waktu : 120 Menit Pilihlah salah satu jawaban yang tepat! Jangan lupa Berdoa dan memulai dari yang mudah. 1. Isotop terdiri dari A. 13 proton, 14 elektron dan 27
PAKET UJIAN NASIONAL 9 Pelajaran : KIMIA Waktu : 120 Menit Pilihlah salah satu jawaban yang tepat! Jangan lupa Berdoa dan memulai dari yang mudah. 1. Isotop terdiri dari A. 13 proton, 14 elektron dan 27
KIMIA 2 KELAS X. D. molekul-molekul kovalen yang bereaksi dengan air E. molekul-molekul kovalen yang bergerak bebas di dalam air
 KIMIA 2 KELAS X PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah soal dengan teliti sebelum Anda bekerja 3. Kerjakanlah soal anda pada lembar jawaban
KIMIA 2 KELAS X PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan 2. Periksa dan bacalah soal dengan teliti sebelum Anda bekerja 3. Kerjakanlah soal anda pada lembar jawaban
D. 2 dan 3 E. 2 dan 5
 1. Pada suhu dan tekanan sama, 40 ml P 2 tepat habis bereaksi dengan 100 ml, Q 2 menghasilkan 40 ml gas PxOy. Harga x dan y adalah... A. 1 dan 2 B. 1 dan 3 C. 1 dan 5 Kunci : E D. 2 dan 3 E. 2 dan 5 Persamaan
1. Pada suhu dan tekanan sama, 40 ml P 2 tepat habis bereaksi dengan 100 ml, Q 2 menghasilkan 40 ml gas PxOy. Harga x dan y adalah... A. 1 dan 2 B. 1 dan 3 C. 1 dan 5 Kunci : E D. 2 dan 3 E. 2 dan 5 Persamaan
Antiremed Kelas 10 KIMIA
 Antiremed Kelas 10 KIMIA Persiapan UAS 1 Kimia Doc Name: AR10KIM01UAS Version : 2016-07 halaman 1 01. Partikel berikut yang muatannya sebesar 19 1,6 10 C dan bermassa 1 sma (A) elektron (B) proton (C)
Antiremed Kelas 10 KIMIA Persiapan UAS 1 Kimia Doc Name: AR10KIM01UAS Version : 2016-07 halaman 1 01. Partikel berikut yang muatannya sebesar 19 1,6 10 C dan bermassa 1 sma (A) elektron (B) proton (C)
STOKIOMETRI. Kimia Kelas X
 STOKIOMETRI Kimia Kelas X SEKOLAH MENENGAH ATAS NEGERI 12 SURABAYA 2015 STOKIOMETRI STOKIOMETRI Pada materi stokiometri, kita akan mempelajari beberapa hal seperti persamaan reaksi, hukum-hukum dasar kimia,
STOKIOMETRI Kimia Kelas X SEKOLAH MENENGAH ATAS NEGERI 12 SURABAYA 2015 STOKIOMETRI STOKIOMETRI Pada materi stokiometri, kita akan mempelajari beberapa hal seperti persamaan reaksi, hukum-hukum dasar kimia,
D. golongan IIIA perioda 4 E. golongan VIA perioda 5
 1. Isotop terdiri dari... A. 13 proton, 14 elektron dan 27 neutron B. 13 proton, 13 elektron dan 27 neutron C. 13 proton, 13 elektron dan 14 neutron D. 14 proton, 14 elektron dan 13 neutron E. 27 proton,
1. Isotop terdiri dari... A. 13 proton, 14 elektron dan 27 neutron B. 13 proton, 13 elektron dan 27 neutron C. 13 proton, 13 elektron dan 14 neutron D. 14 proton, 14 elektron dan 13 neutron E. 27 proton,
TATA NAMA SENYAWA, PERSAMAAN REAKSI SEDERHANA, & HUKUM-HUKUM DASAR KIMIA
 Bidang: KIMIA DASAR Materi ini dapat diunduh di https://arisarianto.wordpress.com Materi tambahan lainnya, kunjungi portal https://school.quipper.com/id/index.html buka kelas khusus SMAN MODEL TERPADU
Bidang: KIMIA DASAR Materi ini dapat diunduh di https://arisarianto.wordpress.com Materi tambahan lainnya, kunjungi portal https://school.quipper.com/id/index.html buka kelas khusus SMAN MODEL TERPADU
D. 4,50 x 10-8 E. 1,35 x 10-8
 1. Pada suatu suhu tertentu, kelarutan PbI 2 dalam air adalah 1,5 x 10-3 mol/liter. Berdasarkan itu maka Kp PbI 2 adalah... A. 4,50 x 10-9 B. 3,37 x 10-9 C. 6,75 x 10-8 S : PbI 2 = 1,5. 10-3 mol/liter
1. Pada suatu suhu tertentu, kelarutan PbI 2 dalam air adalah 1,5 x 10-3 mol/liter. Berdasarkan itu maka Kp PbI 2 adalah... A. 4,50 x 10-9 B. 3,37 x 10-9 C. 6,75 x 10-8 S : PbI 2 = 1,5. 10-3 mol/liter
C. Reaksi oksidasi reduksi berdasarkan peningkatan dan penurunan bilangan oksidasi. Bilangan Oksidasi (biloks)
 97 Nama : Kelompok : Mata Pelajaran : Kimia Kelas/Semester : X 5 /2 Alokasi Waktu : 2 x 45 menit. Materi pokok : Konsep Redoks Standar Kompetensi : 3. Memahami sifat-sifat larutan elektrolit dan non elektrolit
97 Nama : Kelompok : Mata Pelajaran : Kimia Kelas/Semester : X 5 /2 Alokasi Waktu : 2 x 45 menit. Materi pokok : Konsep Redoks Standar Kompetensi : 3. Memahami sifat-sifat larutan elektrolit dan non elektrolit
REAKSI REDOKS dan ELEKTROKIMIA
 REAKSI REDOKS dan ELEKTROKIMIA 1. Konsep Reduksi Oksidasi (Redoks) No Reaksi Oksidasi Reaksi Reduksi 1 reaksi penambahan oksigen reaksi pengurangan oksigen 2 peristiwa pelepasan elektron Contoh : Cu Cu
REAKSI REDOKS dan ELEKTROKIMIA 1. Konsep Reduksi Oksidasi (Redoks) No Reaksi Oksidasi Reaksi Reduksi 1 reaksi penambahan oksigen reaksi pengurangan oksigen 2 peristiwa pelepasan elektron Contoh : Cu Cu
UNIVERSITI SAINS MALAYSIA. Peperiksaan Semester Kedua Sidang Akademik 2004/2005. Mac Masa : 3 jam
 UNIVERSITI SAINS MALAYSIA Peperiksaan Semester Kedua Sidang Akademik 2004/2005 Mac 2005 JIK 101 - KIMIA AM I Masa : 3 jam Sila pastikan bahawa kertas peperiksaan ini mengandungi ENAM muka swat yang bercetak
UNIVERSITI SAINS MALAYSIA Peperiksaan Semester Kedua Sidang Akademik 2004/2005 Mac 2005 JIK 101 - KIMIA AM I Masa : 3 jam Sila pastikan bahawa kertas peperiksaan ini mengandungi ENAM muka swat yang bercetak
TES PRESTASI BELAJAR
 TES PRESTASI BELAJAR Hari/tanggal : selasa/8 Mei 2012 Mata Pelajaran: Kimia Waktu : 90 menit Petunjuk : 1. Berdoalah sebelum mengerjakan soal 2. Bacalah petunjuk soal terlebih dahulu 3. Pilih salah satu
TES PRESTASI BELAJAR Hari/tanggal : selasa/8 Mei 2012 Mata Pelajaran: Kimia Waktu : 90 menit Petunjuk : 1. Berdoalah sebelum mengerjakan soal 2. Bacalah petunjuk soal terlebih dahulu 3. Pilih salah satu
TATA NAMA SENYAWA DAN PERSAMAAN REAKSI. A. Kompetensi Inti KI 1 : Menghayati dan mengamalkan ajaran agama yang dianutnya
 BAB 4 TATA NAMA SENYAWA DAN PERSAMAAN REAKSI A. Kompetensi Inti KI 1 : Menghayati dan mengamalkan ajaran agama yang dianutnya KI 2 : Menghayati dan mengamalkan perilaku jujur, disiplin, tanggungjawab,
BAB 4 TATA NAMA SENYAWA DAN PERSAMAAN REAKSI A. Kompetensi Inti KI 1 : Menghayati dan mengamalkan ajaran agama yang dianutnya KI 2 : Menghayati dan mengamalkan perilaku jujur, disiplin, tanggungjawab,
Tabel Hasil Analisis Kebenaran Konsep pada Objek Penelitian
 202 Lampiran B Label Pengertian stoikiometri Pengertian massa atom Perhitungan massa atom Tabel Hasil Analisis pada Objek Penelitian Penjelasan pada Stoikiometri berasal dari bahasa Yunani (stoicheion,
202 Lampiran B Label Pengertian stoikiometri Pengertian massa atom Perhitungan massa atom Tabel Hasil Analisis pada Objek Penelitian Penjelasan pada Stoikiometri berasal dari bahasa Yunani (stoicheion,
LEMBARAN SOAL 9. Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH )
 LEMBARAN SOAL 9 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan. Periksa dan bacalah soal dengan
LEMBARAN SOAL 9 Mata Pelajaran : KIMIA Sat. Pendidikan : SMA Kelas / Program : X ( SEPULUH ) PETUNJUK UMUM 1. Tulis nomor dan nama Anda pada lembar jawaban yang disediakan. Periksa dan bacalah soal dengan
PEMBAHASAN UJIAN NASIONAL KIMIA TAHUN 2006
 UJIAN NASIONAL KIMIA TAHUN 2006 HTTP://GUDANGSOALPRO.BLOGSPOT.COM 1 1. Di antara unsur-unsur 12 P, 16 Q, 19 R, 34 S dan 53 T yang terletak pada golongan yang sama dalam sistem periodik unsur adalah...
UJIAN NASIONAL KIMIA TAHUN 2006 HTTP://GUDANGSOALPRO.BLOGSPOT.COM 1 1. Di antara unsur-unsur 12 P, 16 Q, 19 R, 34 S dan 53 T yang terletak pada golongan yang sama dalam sistem periodik unsur adalah...
KIMIA TERAPAN STOIKIOMETRI DAN HUKUM-HUKUM KIMIA Haris Puspito Buwono
 KIMIA TERAPAN STOIKIOMETRI DAN HUKUM-HUKUM KIMIA Haris Puspito Buwono Semester Gasal 2012/2013 STOIKIOMETRI 2 STOIKIOMETRI adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif dari komposisi
KIMIA TERAPAN STOIKIOMETRI DAN HUKUM-HUKUM KIMIA Haris Puspito Buwono Semester Gasal 2012/2013 STOIKIOMETRI 2 STOIKIOMETRI adalah cabang ilmu kimia yang mempelajari hubungan kuantitatif dari komposisi
OLIMPIADE SAINS NASIONAL 2012 SELEKSI KABUPATEN / KOTA JAWABAN (DOKUMEN NEGARA) UjianTeori. Waktu: 100 menit
 OLIMPIADE SAINS NASIONAL 2012 SELEKSI KABUPATEN / KOTA JAWABAN (DOKUMEN NEGARA) UjianTeori Waktu: 100 menit Kementerian Pendidikan Nasional Dan Kebudayaan Direktorat Jenderal Managemen Pendidikan Dasar
OLIMPIADE SAINS NASIONAL 2012 SELEKSI KABUPATEN / KOTA JAWABAN (DOKUMEN NEGARA) UjianTeori Waktu: 100 menit Kementerian Pendidikan Nasional Dan Kebudayaan Direktorat Jenderal Managemen Pendidikan Dasar
